Bedeutung in Forschung und Medizin
|
|
|
- Jobst Richter
- vor 6 Jahren
- Abrufe
Transkript
1 E. coli Bedeutung in Forschung und Medizin 3., überarbeitete Auflage M. Schiemann, U. Sonnenborn, J. Schulze, H. Müller
2 M. Schiemann, U. Sonnenborn, J. Schulze, H. Müller E. coli Bedeutung in Forschung und Medizin 3., überarbeitete Auflage
3 Fotohinweis zum Titelblatt (von oben nach unten): Wachstum von E. coli auf McConkey-Agar (Aufnahme T. Grela, U. Sonnenborn, Herdecke) Adhäsion von E. coli Stamm Nissle 1917 an das Darmepithel (Aufnahme J. Schulze, A. Lorenz, Potsdam-Rehbrücke) Rasterelektronenmikroskopische Aufnahme von E. coli Stamm Nissle 1917 (Aufnahme H. J. Jacob, Bochum) Autoren: Dipl.-Biol. Martina Schiemann Dr. rer. nat. Ulrich Sonnenborn Priv.-Doz. Dr. rer. nat. habil. Jürgen Schulze Dr. med. Hilke Müller Herausgeber: Alfred-Nissle-Gesellschaft Internationale Vereinigung zur Förderung der mikroökologischen Forschung und mikrobiologischen Therapie e. V. Vorsitzender: Prof. Dr. med. dent. Dr. med. Dieter Loew An der Residenz Sörgenloch office@a-nissle-ges.de Im Fokus dieser Broschüre steht der weltweit am besten untersuchte Mikroorganismus, das Bakterium Escherichia coli (E. coli), mit seiner Bedeutung für Gesundheit und Krankheit sowie für die medizinische, mikrobiologische, biochemische und molekularbiologische Forschung des 20sten und 21sten Jahrhunderts. 3., überarbeitete Auflage Alle Rechte, insbesondere das Recht der Vervielfältigung und Verbreitung sowie der Übersetzung in fremde Sprachen vorbehalten. Kein Teil des Werkes darf in irgendeiner Form (Fotokopie, Mikrofilm oder ein anderes Verfahren) ohne schriftliche Genehmigung reproduziert werden Alfred-Nissle-Gesellschaft e. V. Deutschland ISBN
4 Inhaltsverzeichnis Seite Theodor Escherich Erstbeschreiber des Bacterium coli commune 7 Mikrobiologische Kurzcharakteristik von E. coli 11 E. coli K-12: Das beliebteste Versuchstier der Molekulargenetiker 13 E. coli in der Biotechnologie 15 E. coli is the first to come, and the last to go 17 Intra- und extraintestinal pathogene E. coli -Varianten 19 Alfred Nissles Entdeckung des Coli-Antagonismus und sein neues Heilprinzip 25 Das Auf und Ab der Therapie mit lebenden Mikroorganismen 29 E. coli Stamm Nissle 1917: der weltweit am besten untersuchte probiotische E. coli -Stamm 32 Wirkungen und Wirkmechanismen von E. coli Stamm Nissle Mikrobielle Kommunikation und Interaktionen ( Cross Talk ) im Gastrointestinaltrakt 34 Bildung von Biofilmen und Mikrokolonien im Darm 35 Die Stärkung der intestinalen Barrierefunktion Der Anti-Invasionseffekt am Darmepithel Der Induktionseffekt auf die Synthese antimikrobieller Peptide des Darmepithels Die Stärkung des Zusammenhalts des epithelialen Zellverbands 47 Immunmodulierende Wirkungen 55 Antimutagenität 64 Indikationsspektrum für E. coli Stamm Nissle 1917 (Mutaflor ) und konfirmatorische klinische Studien 67 Ausblick 78 Literatur 81 Sachverzeichnis
5 Theodor Escherich Erstbeschreiber des Bacterium coli commune Am 14. Juli des Jahres 1885 hielt der damals 27-jährige Theodor Escherich* vor der Gesellschaft für Morphologie und Physiologie in München einen Vortrag mit dem Titel Die Darmbacterien des Neugeborenen und Säuglings (Escherich, 1885) [Abb. 1]. Escherich, zu der Zeit Assistent am Dr. von Hauner schen Kinderspital, berichtete über seine Forschungs ergebnisse und trug dem Auditorium vor, dass das Mekonium des Neugeborenen steril sei, aber innerhalb der ersten Lebensstunden von Mikroorganismen besiedelt werde. Weil er fest davon überzeugt war, dass es für die Pathologie und Therapie der myco tischen Darmerkrankungen unentbehrlich sei, versuchte er, die scheinbar ganz regellose und von tausend Zufällig keiten abhängige Menge der im normalen Stuhl- und Darmkanal vorkommenden Bacterien zu entwirren. Dazu entwickelte er spezielle Kultivierungsmethoden mit flüssigen und festen Nährmedien, die im Prinzip noch heute zum klassischen Handwerkszeug eines mikrobiologischen Labors gehören. Prof. Dr. med. Theodor Escherich ( ) Nach eineinhalbjähriger intensiver Forschung präsentierte er diese und weitere Ergebnisse in seiner umfangreichen Habilitationsschrift Die Darmbakterien des Säuglings und ihre Beziehungen zur Physiologie der Verdauung, die 1886 im Verlag von Ferdinand Enke, Stuttgart, abgedruckt wurde (Escherich, 1886). Hier teilte er u. a. minutiös seine Erkenntnisse zum Vorkommen, zur Gestalt und zu den Eigenschaften der von ihm beobachteten Bakterien mit, die er je nach Häufigkeit und Menge in obligate und fakultative Darmbakterien einteilte. Im Säuglingsstuhl fielen ihm hauptsächlich zwei Bakterientypen auf, die er als obligate Milchkotharten bezeichnete. Eine davon war wie bereits in seinem 1885 publizierten Vortrag dargestellt besonders häufig in den unteren Darmabschnitten anzutreffen, weshalb Theodor Escherich sie als typische Colonbacterien bezeichnete und ihnen den Artnamen Bacterium coli commune, das allgemeine Dickdarmbakte rium, gab [Abb. 2]. Dasselbe findet sich so- * Weiteres über Leben und Arbeit von Theodor Escherich kann der Monographie von B.A. Oberbauer Theodor Escherich Leben und Werk, Paul-Ehrlich-Gesellschaft für Chemotherapie (Hrsg.), Futuramed Verlag München, 1992, entnommen werden. 6 7
6 Abb. 2 Die erste Abbildung vom Bacterium coli commune. Dauerpräparat von Th. Escherich, 1886: angefärbt mit Gentiana violett in wässrigem Anilin. In: Die Darmbakterien des Säuglings und ihre Beziehungen zur Physiologie der Verdauung. Verlag von Ferdinand Enke, Stuttgart. wohl im Mekoniumkothe als bei Milch-, Fleischdiät und gemischter Kost und kann insofern als ein diesen verschiedenen Kotharten gemeinsamer Spalt pilz bezeichnet werden, während die Bakterienvegetation der selben im Übrigen große Verschiedenheiten darbietet.... Später fand er das Bacterium coli commune auch als obligates Darmbakterium in den Fäzes Erwachsener. Neben der Erstbeschreibung weiterer Darmbakterien (z. B. Klebsiella, Campylobacter) ist es ein weiteres großes Verdienst Escherichs, auch auf mikroökologische Zusammenhänge im Darm hingewiesen zu haben (der Begriff Mikroökologie wurde allerdings erst 1960 von Helmut Haenel eingeführt). Im Stuhl von gestillten Kindern stellte er eine auf fällige Verminderung oder sogar das Fehlen von gelatineverflüssigenden Keimen, von Eiweißspalt produkten und von fäkalem Geruch 1885 Erstbeschreibung (Th. Escherich): Bacterium coli commune (später: Bacterium coli) 1919 Systematisierung (A. Castellani, A. J. Chalmers): Vorschlag zur Umbenennung in 1930 Internationaler Mikrobiologenkongress, Paris: offizielle Umbenennung in 1953 Internationaler Mikrobiologenkongress, Rom: Streichung der Bezeichnung zugunsten von 1958 Judicial Commission: Conservation of the Enterobacteriacea,... verbindliche Veröffentlichung zur Bezeichnung Escherichia coli Escherichia coli Bacterium coli Escherichia coli Escherichia coli Abb. 1 Titelseite der Arbeit, in der Escherich erstmals das Bacterium coli commune beschrieb. Abb. 3 Von der Erstbeschreibung als Bacterium coli commune zur heute gültigen Bezeichnung Escherichia coli. 8 9
7 fest, was später als antiputrider Effekt der Muttermilch beschrieben wurde. Nach seinen Befunden bezeichnete Escherich die Besiedlung der oberen Darmabschnitte als monoton und spärlich, und stellte fest, dass die Zahl der Bakterien jenseits der Ileozäkalklappe im Dickdarm sprunghaft ansteigt. Er vermutete, dass die Vermehrung der Bakterien unabhängig von der Nahrungs zufuhr sei und dass die Bakterien ihren Nah rungs bedarf aus der Verstoffwechselung von Darmsekreten decken würden. Mikrobiologische Kurzcharakteristik von E. coli Die Art Escherichia coli (E. coli) gehört zur Familie der Enterobacteriaceae und steht in enger verwandt schaftlicher Nachbarschaft zur Gattung Shigella und in naher Verwandtschaft zu den Gattungen Citrobacter und Salmonella. Ent ferntere Verwandte sind die Gattungen Enterobacter und Klebsiella [Abb. 4]. Trotz aller Weitsicht konnte Theodor Escherich nicht ahnen, dass das von ihm entdeckte Bacterium coli und die später nach ihm benannte Spezies Escherichia coli [Abb. 3] zum weltberühmten Modellobjekt der naturwissenschaftlichen und medizinischen Mikrobiologen, Mikroökologen sowie der Biochemiker und Molekulargenetiker aufsteigen sollte. Abb. 4 Stammbaum und Verwandtschaftsbeziehungen der Familie Enterobacteriaceae (nach Brenner, 1984). Das E. coli-bakterium ist ein gramnegatives Stäbchen von etwa 1,1 1,5 µm x 2,0 6,0 µm Größe. Es wächst unter aeroben und anaeroben Bedingungen (fakultativ anaerob), weil es zwei verschiedene Redoxsysteme besitzt (Mena chinon und Ubichinon), die eine Energiegewinnung aus dem katabolen Stoffwechsel sowohl unter aeroben als auch unter anaeroben Bedingungen ermöglichen. Unter optimalen Wachstumsbedingungen ist die Zellteilungsgeschwindigkeit der Coli-Bakterien rasant: Alle 20 Minuten kann sich die Zahl der Bakterienzellen verdoppeln. Allerdings werden diese für die Populationsdynamik idealen Zustände nur unter Laborbedingungen, nicht aber im natürlichen Umfeld der Bakterien erreicht. Midtvedt (1998) berichtete von einer Verdoppelung der E. coli-zellen im Zäkum der Ratte nach etwa 100 Minuten, im menschlichen Darm kann es 30 Stunden 10 11
8 dauern und in wässrigen Biotopen im Freien bis zu mehreren Tagen (Hecker, 1998). Bereits Escherich beobachtete die morphologische Vielfalt der Kolonie formen dieser Bakterien bei Wachs tum auf festen Nährböden. Noch zahlreicher sind die serologischen Varianten. In der medizinischen Mikrobiologie dient die Serologie seit langem zur Keim differen zierung. Die serologische Einteilung der unterschied lichen E. coli-stämme wird durch die Sero typisierung ihrer O-, K- und H-Antigene möglich. O-Antigene stellen dabei hitzestabile Bestandteile des Lipo poly saccha rid- Komplexes (LPS) der äußeren Zellmembran, K-Antigene Poly saccha ride der Kapsel und H-Antigene Geißel- oder Flagellenantigene dar [Abb. 5]. Abb. 5 Schematischer Längsschnitt und Zellwandaufbau einer gramnegativen E. coli-zelle. Serologisch werden E. coli-stämme anhand ihrer unterschiedlichen O-, K- und H-Antigene differenziert, z. B. E. coli Nissle 1917 = Serotyp O6 : K5 : H1. In der Natur können rund unterschiedliche Serovare von E. coli vorkommen, die sich aus der Kombination verschiedener Antigenstrukturen ergeben (Hacker & Kruis, 1998). Bisher sind 200 Oberflächen-(O-), 80 Kapsel-(K-) und 60 Geißel-(H-)Antigene bei E. coli bekannt. Zudem gibt es noch mehr als 100 serologisch unterscheidbare Fimbrien-Varianten, die als Adhäsine verschiedene Rezeptoren erkennen. E. coli K-12: Das beliebteste Versuchstier der Molekulargenetiker (Arber, 1982) Es war reiner Zufall, dass 1922 aus dem Stuhl eines an Diphtherie erkrankten Patienten eine E. coli-variante isoliert wurde, die wegen ihrer völligen Harmlosigkeit auffiel und mit der Laborbezeichnung K-12 einen Platz in der bakteriologischen Stammsammlung der Medical School der Stanford- University in Kalifornien fand. Bereits im zweiten Drittel des vergangenen Jahr hunderts suchten Genforscher nach geeigneten Studien objekten, um die Frage zu beantworten: Wie funktionieren Gene und wie kontrollieren sie spezifische Merkmale?. Diese Versuchsobjekte sollten leicht, schnell und in unbegrenzter Menge zu züchten, und zudem in der Lage sein, genetische Veränderungen anhand phäno typischer Ausprägungen offenzulegen. So fand die K-12- Variante von E. coli das besondere Interesse eines amerikanischen Forscherteams um J. Lederberg und E.L. Tatum (1946). Als dann bei diesem E. coli K-12 para sexuelle Vorgänge d. h. die Fähigkeit des Austauschs genetischen Materials zwischen zwei Bakterienzellen entdeckt wurden, war die Basis für die Durchführbarkeit der gezielten Übertragung von Genen gegeben, und E. coli K-12 avancierte zum Standardobjekt der Genetiker und Moleku lar biologen. Ähnlich wie die klassischen Tier- und Pflanzenzüchter suchten auch die Mikrobiologen bei ihrem Haustier E. coli nach neuen Stämmen. Mit Hilfe von Röntgen- und UV-Strahlen führten sie verschiedene Mutationen in den K-12- Wildstamm ein. Sehr bald wurde mit dem Ausgangsstamm und den daraus hergestellten Varianten in vielen Laboratorien weltweit gearbeitet. Die Varianten von E. coli K-12 weisen Veränderungen in den verschiedensten Genen auf, sie tragen z. B. Merkmale für Auxotrophien (Stämme mit zusätzlichen Nährstoffbedürfnissen), Resistenzen und andere Mutationen. Als Sicherheitsmaßnahme wurden diese Mutantenstämme so verändert, dass sie keine Adhäsionsorganellen (Fimbrien) haben, um den Darm zu besiedeln, fremde Plasmide ohne die Möglichkeit der Weitergabe an artfremde Zellen zuverlässig aufnehmen können, in der freien Natur nicht überleben können, UV- und Chemikalien-empfindlich sind
9 Unterdessen sind weit mehr als 3000 verschiedene Mutanten von E. coli K-12 bekannt, mit deren Hilfe grundlegende Erkenntnisse zur Biochemie und Zellphysiologie, zur Genregulation und zum Gentransfer gewonnen wurden. Einer der ersten Bakterienstämme, dessen Genom vollständig sequenziert wurde, war folgerichtig ein E. coli K-12-Stamm (MG 1655) (Blattner et al., 1997). Die erste genetische Karte des E. coli K-12-Genoms wurde bereits im Jahr 1964 u. a. mit Hilfe von Restriktionsenzymen, die Stränge der DNA an spezifischen Basensequenzen schneiden, erstellt (Taylor & Thomann, 1964). Während auf ihr 99 Gene vermerkt waren, wies die Genkarte aus dem Jahr 1990 schon 1403 Gene auf (Bachmann, 1990). Die 1997 ver öffentlichte vollständige Genomsequenz des E. coli K-12-Stamms ergab etwa 4300 Gene (Blattner et al., 1997) [Abb. 6]. Mit einer Größe von 4,7 x 10 6 Basenpaaren ist das Genom von E. coli K-12 um den Faktor 1000 kleiner als das mensch liche Genom, das infolge des Human Genome Projects ebenfalls voll ständig sequenziert ist. Ein Forschungsschwerpunkt der modernen Molekulargenetik ist die Analyse der Genome ganzer Mikrobengemeinschaften wie z. B. der mensch lichen Darmmikrobiota. Seit einiger Zeit wird die Gesamtheit aller Mikroorganismen im Magen-Darm-Trakt als intestinale Mikrobiota bzw. Darmmikrobiota bezeichnet. Intestinale Mikrobiota oder Darmmikrobiota ersetzen in der heutigen Fachliteratur den klassischen Begriff Darmflora. Die Gesamtheit aller Genome der Darmmikrobiota wird als Mikro biom bezeichnet. Abb. 6 Genom von E. coli K-12 (MG1655), Größe 4,7 x 10 6 Basenpaare (Blum-Oehler, 2001). Die Bedeutung von Escherichia coli für den internationalen Wissenschaftsfortschritt wird auch dadurch unter strichen, dass in den letzten Jahrzehnten eine Reihe von Nobelpreisen für Arbeiten an und mit E. coli vergeben wurden. E. coli in der Biotechnologie Im Laufe der immer genaueren Charakterisierung des Genoms von E. coli erschlossen sich mit gentechnisch veränderten E. coli-bakterien vielfältige Anwendungsgebiete. Bereits 1973 wurde gezeigt, wie man menschliches Insulin mit Hilfe eines gentechnisch veränderten E. coli-stammes herstellen kann (Cohen et al., 1973). Mit Hilfe der modernen Gen- und Biotechnologie gelang es nun, rekombinante Arzneimittel herzustellen. Dabei wird das Gen für ein menschliches Protein in das Erbgut der Bakterien eingeschleust, die anschließend dieses Eiweiß herstellen [Abb. 7]. Abb. 7 Aus einer menschlichen Zelle wird die DNA isoliert. Mit Restriktions enzymen ( molekulare Scheren ) wird ein DNA-Fragment mit dem gesuchten Gen ausgeschnitten und mit Hilfe von Ligasen in einen ebenfalls aufgeschnittenen DNA-Plasmidring von E. coli eingeführt. Nach Einschleusung dieses Konstrukts in die E. coli-zelle enthält das Bakteriengenom nun z. B. die genetische Information für das menschliche Hormon Insulin. Artfremde Proteine, die in Bakterien exprimiert werden, nennt man rekombinante Proteine
10 Als erstes rekombinantes Medikament wurde 1982 das Hormon Humaninsulin in den Markt eingeführt. Danach wurden Gene für weitere Proteine menschlicher, tierischer, pflanzlicher und bakterieller Herkunft erfolgreich in das E. coli-genom integriert [Abb. 8]. Von E. coli exprimierte Pharmaproteine: Humaninsulin Wachstumshormone (Somatostatin, Somatotropin) Immunmodulatoren (Interferone, Interleukine, TNFα) Wachstumsfaktoren (G-CSF, EGF) Blutfaktoren, Gerinnungshemmer (t-pa, Staphylokinase) Enzyme E. coli is the first to come, and the last to go (Midtvedt, 1998) Bis zur Geburt entwickelt sich der Fötus im Mutterleib unter keimfreien Bedingungen. Die Beobachtung Escherichs, dass sich bereits wenige Stunden nach der Geburt Colonbacterien im Mekonium nachweisen lassen, hat auch heute noch Bestand. Die sich ansiedelnden Keime stammen aus der Mikrobiota der Mutter oder aus der Umgebung und werden während der Geburt bzw. der ersten Lebensstunden erworben (Sonnenborn et al., 1990). Fakultativ anaerobe Keime, allen voran E. coli, sind die klassischen Erstbesiedler des menschlichen Gastro intestinaltrakts (Hoogkamp-Korstanje et al., 1979) [Abb. 9]. Abb. 8 Beispiele für von gentechnisch veränderten E. coli produzierte, pharmazeutisch verwendete Proteine und Peptide. 10 Keimzahl (log/g Fäzes) Stunden Tage Aerobier: E. coli Lactobacillus Enterococcus Anaerobier: Bacteroides Bifidobacterium Abb. 9 Sequenzielle mikrobielle Besiedlung des Neugeborenendarms durch aerobe und anaerobe Bakterien (nach Hoogkamp-Korstanje et al., 1979). Sie betreiben im zunächst noch sauerstoffhaltigen Dickdarm einen regen Stoffwechsel und senken dadurch den O 2 -Gehalt und das Redox potential im Darmlumen so weit herab, dass sich nachfolgend anaerobe Darmbakterien wie Bacteroides-Keime, Bifidobakterien u. a. ansiedeln können (Schulze et al., 2008). Den Verbrauch von Sauerstoff durch die Colonbakterien hatte bereits Escherich beobachtet. Da über die Nahrung durch Abschlucken, aber auch über die Darmwand ständig neuer Sauerstoff in das Darmlumen eingebracht wird, bleibt diese Aufgabe der Milieubereitung für E. coli während des gesamten Lebens des Wirtsorganismus erhalten
11 Die mikrobielle Besiedlungsdichte des Magen-Darmtrakts nimmt von proximal nach distal zu [Abb. 10]. Die durch schnitt liche Keimkonzentration von E. coli im Dickdarm unterliegt interindi viduell aber auch intraindividuell großen Schwankungen und beträgt beim gesunden Erwachsenen zwischen 10 5 und 10 9 Kolonie-bildende Einheiten pro Gramm Fäzes (KBE/g). Da der über die Dickdarmwand ins Darmlumen diffundierende Sauerstoff für die Coli- Bakterien als chemotaktischer Reiz wirkt, sind diese auch an der Mucosa, genauer gesagt an der aufliegenden Schleimschicht in großer Zahl zu finden. Durch diese Anreicherung von E. coli an der Darmschleimhaut erhöht sich der Gehalt der sog. wandständigen Mikrobiota an aeroben Keimen. Magen und Duodenum ( KBE*/ml) Jejunum und Ileum ( KBE*/ml) Colon ( KBE*/g) *KBE = Kolonie-bildende Einheiten (syn. für Lebendkeime) Bacteroides-Arten Bifidobakterien Peptostreptokokken Eubakterien Fusobakterien Clostridien Veillonellen Laktobazillen Streptokokken Hefen (Candida albicans) Helicobacter pylori Laktobazillen E. coli u.a. Enterobakterien Strepto- und Enterokokken Bacteroides-Arten Bifidobakterien Fusobakterien E. coli u.a. Enterobakterien (Enterobacter, Proteus, etc.) Enterokokken Laktobazillen Staphylokokken Pseudomonaden Hefen (Candida albicans) Protozoen (z.b. Entamoeba) Intra- und extraintestinal pathogene E. coli-varianten Escherich war anfangs überzeugt, dass es sich bei dem Bacterium coli commune um einen harmlosen Schmarotzer handelt. Sicher hatte er damit recht, weil die meisten der oben erwähnten rund Serovare zu den kommensalen Darmkeimen zu zählen sind. Allerdings berichtete Escherich bereits 1894 in einem publizierten Vortrag über Cystitis bei Kindern hervorgerufen durch das Bacterium coli commune (Escherich, 1894). Er vermutete, dass die Darmbakterien als Quelle für Harnwegsinfektionen (Blasen- und Niereninfektionen) in Frage kämen. Diese frühe Hypothese, dass u. U. harnwegspathogene E. coli im Darm symptomlos persistieren und aus verschiedenen Gründen in die harnableitenden Organe gelangen und dort Ent zündungen verursachen könnten, ist unterdessen mit modernen bio chemischen und molekularbiologischen Methoden bestätigt worden (Blum et al., 1995; Hacker et al., 1983; Plos et al., 1995). Über die wirtsspezifische pathogene Potenz verschiedener E. coli- Varianten [Abb. 11] gibt es mittlerweile eine enorm umfangreiche Sammlung von Publikationen. Darminfektionen Harnwegsinfektionen Sepsis Meningitis Diarrhö Sepsis Mastitis Abb. 10 Unterschiede in Keimgehalt und Keimspektrum in verschiedenen Abschnitten des Gastrointestinaltrakts (nach Sonnenborn & Greinwald, 1991). Obwohl sich in den letzten Jahren Laborbefunde mehren, dass Neugeborene in den hoch industrialisierten Ländern immer später mit E. coli besiedelt werden, und dass die Keimzahlen von E. coli in Stuhlproben von Patienten (vornehmlich von Allergikern) reduziert sind, bzw. sich manchmal sogar keine Coli-Bakterien nachweisen lassen (Adlerberth et al., 2006; Nowrouzian et al., 2003; Sepp et al., 2000), gilt auch heute noch die Aussage von Escherich: Die Keime der Colonbacterien, die eine sehr große Verbreitung zu besitzen scheinen, finden sich regelmäßig schon im Mekonium und bleiben von da bis zum Tode des Wirthes und darüber hinaus ständige Bewohner des Darmkanals. Diarrhö Ödemkrankheiten Harnwegsinfektionen Diarrhö Sepsis Sepsis Abb. 11 Wirtsspektrum und Krankheitsbilder intestinaler und extraintestinaler pathogener E. coli
12 In Abhängigkeit von der Schädigungsstrategie werden pathogene E. coli in sog. Pathotypen eingeteilt (Hacker & Heesemann, 2000) [Abb. 12]. Pathogene E. coli-varianten sind durch das Vorkommen von diversen Virulenzfaktoren, wie z. B. verschiedenen Toxinen, besonderen Fimbrien- Adhäsinen, Invasinen oder Sekretionssystemen, gekennzeichnet [Abb. 13]. Sie können sowohl plasmid- oder phagen- als auch chromosomal codiert im Bakteriengenom vorliegen. Darmpathogene E. coli werden aufgrund ihrer in den letzten Jahren aufgedeckten Virulenzfaktoren in derzeit 6 Klassen unterteilt, die Durchfallerkrankungen mit unterschiedlichen klinischen Erscheinungsformen verursachen (Kaper et al., 2004). Dabei werden die klinische Symptomatik sowie die von den Stämmen gebildeten Virulenzmerkmale, die Adhäsionsfaktoren und Toxine, als Einteilungskriterien verwendet. Die in früheren Jahren vor allem angewandte Serotypisierung zur Identifizierung und Klassifizierung klinischer Isolate wird heute immer mehr durch den molekulargenetischen Nachweis der jetzt bekannten bakteriellen Virulenz- und Pathogenitätsgene ersetzt, unterstützt durch den Nachweis spezifischer pathogener Merkmale. EPEC EIEC EHEC Toxinbildung Toxinbildung Toxinbildung Enteropathogene E. coli (EPEC) wurden erstmals in den 40er Jahren des vergangenen Jahrhunderts als Erreger der Säuglingsenteritis während eines massiven Ausbruchs in Großbritannien isoliert. Enteropathogene E. coli nutzen zum Andocken an die Darmschleimhaut spezifische ETEC Toxinbildung EAggEC UPEC SEPEC MENEC Abb. 12 Pathotypen und Pathogenitätsmechanismen humanpathogener E. coli (nach Hacker & Heesemann, 2000). Virulenzmerkmale Adhäsine (CFA I/II-, P-, M-, S-Fimbrien) Toxine (CNF, Hämolysin, hitzestabile und hitzelabile Toxine, Shiga-Toxine) Invasine Typ-III-Sekretionsapparat (biologische Injektionsspritze ) Abb. 13 Beispiele für Virulenzfaktoren pathogener E. coli-stämme. Fimbrien-Adhäsine (bundle-forming pili) und injizieren über ein Typ-III- Sekretionssystem bakterielle Signalproteine in die Epithelzelle, was zu Veränderungen des Aktingerüsts führt und letztlich zu einer Destruktion der Mikrovilli. Sie gelten heute vor allem in Entwicklungsländern als Verursacher von wässrigen Durchfall erkrankungen mit Fieber und Erbrechen bei Säuglingen und Kleinkindern unter 2 Jahren (Cravioto et al., 1991; Levine & Edelmann, 1984). EPEC sind auch für Tiere pathogen und verursachen z. B. beim Kaninchen große Verluste in der Jungtieraufzucht. Infektionen durch enterohämorrhagische E. coli (EHEC) traten erstmals 1982 in den USA auf. Sie sind im Gegensatz zu anderen darmpathogenen E. coli-stämmen, die sich nur beim Menschen finden und deren Übertragung durch fäkal kontaminiertes Gemüse oder durch Schmierinfektionen erfolgt, eher als Zoonoseerreger einzustufen (Baljer & Wieler, 1999; Karch 2011). Sie repräsentieren eine Untergruppe der auch als Shiga-Toxin-produzierende (STEC) bzw. Vero-Toxin-produzierende (VTEC) bezeichneten E. coli und kommen in der Natur relativ häufig vor. E. coli dieses Typs sind Auslöser meist blutiger Diarrhöen (MacDonald et al., 1988). Bei % der Erkrankten entwickelt sich als schwere Verlaufsform eine hämorrhagische Colitis. Enterohämorrhagische E. coli schleusen nach der Anheftung Enterohämolysin und weitere Toxine in die Mucosazelle ein, was zu blutigen Läsionen im Darm führen kann. Da die Toxine auch in andere Organe gelangen können, kommt es u.u. zu irrever siblen Schäden im Nierengewebe (Hämolytisch-urämisches Syndrom, HUS) sowie zur Thrombotisch-Thrombozytopenischen Purpura (TTP) (Karch 2011; Karmali, 1989; MacDonald et al., 1988). Nach heutiger Kenntnis sind landwirtschaft liche Nutztiere in Massentierhaltung, vor allem Rinder, die wichtigsten Erreger reservoire für Infektionen des Menschen (Beutin et al., 1995). Durch enterotoxische E. coli (ETEC) bedingte Infektionen sind eine weit verbreitete Ursache von Darmerkrankungen bei Kleinkindern sowie bei Reisen den in tropischen und subtropischen Ländern (Reisediarrhö). ETEC besitzen typische Adhäsine und schädigen die Enterozyten über zwei Toxine 20 21
13 (hitzelabiles und/oder hitzestabiles Enterotoxin). ETEC- Infektionen äußern sich in einem Cholera-ähnlichen Krankheitsbild. Es kommt zu wässrigen Durchfällen, abdominalen Krämpfen, Fieber und Erbrechen (Levine, 1987). Beim Tier sind vor allem neugeborene Lämmer, Kälber und Ferkel betroffen (Kennan & Monckton, 1990; Tzipori et al., 1981). Enteroaggregative E. coli (EAggEC) wurden bisher vor allem bei Kindern als Infektionserreger nachgewiesen und verursachen wässrige, oft persistierende Durchfälle. EAggEC haften an den Enterozyten des Dünndarms und lagern sich in typischer Weise zu Aggregaten zusammen, die an gestapelte Ziegelsteine erinnern (Nataro & Kaper, 1998). Sie schädigen die Epithelzellen durch Bildung eines besonderen Toxins (EAST I), das dem hitzestabilen Enterotoxin der ETEC ähnelt. Enteroinvasive E. coli (EIEC) besitzen die Fähigkeit, in die Darmwand einzudringen. Sie sind bezüglich ihrer pathogenen Eigenschaften den Ruhr bakterien (Shigellen) vergleichbar und verursachen beim Menschen Ruhr -ähnliche Symptome, wie anhaltende Bauchkrämpfe (Tenesmen) und breiige, blutige und blutig-schleimige Diarrhöen (Formal, 1983). Es kommt zu lokalen Entzündungen mit Bildung von Geschwüren durch Einwandern der Erreger in die Dickdarmwand. Eine Tierpathogenität ist nicht bekannt. Diffus adhärente E. coli (DAEC) wurden als Infektionsauslöser vor allem bei Kindern mit wässrigen Durchfällen nachgewiesen (Nataro & Kaper, 1998). Über ihre Pathogenitätsmechanismen ist noch wenig bekannt. Nekrotoxische E. coli (NTEC) zeichnen sich durch die Bildung spezieller Toxine, die sog. Cytonekrose-Faktoren (CNF) aus (De Rycke et al., 1990). CNF1- bildende NTEC sind vor allem beim Menschen mit extra intestinalen Coli-Infektionen nachgewiesen worden, während CNF2-bildende NTEC bei Kälbern sowohl mit Durchfall als auch mit Septikämien in Verbindung gebracht werden (Caprioli et al., 1987). Extraintestinale Infektionen entstehen durch das Vordringen von Coli-Bakterien, die sich z. T. aus der eigenen Darmmikrobiota rekrutieren, in ansonsten sterile oder spärlich besiedelte Bereiche des Organismus, in denen eine Vermehrung begünstigt wird. Bei extraintestinalen Infektionen spielt E. coli vor allem als Erreger von Harnwegsinfekten (UPEC = uropathogene E. coli) eine wich tige Rolle (Johnson & Stamm, 1989). Uropathogene E. coli heften sich mit spezifischen Adhäsinen (z. B. P-Fimbrien, S-Fimbrien) an uroepi theliale Zellen und setzen zur Schädigung des Epithels ein zytolytisch wirkendes Toxin (α-hämolysin) ein. Gleichzeitig entziehen sie sich den Attacken der Immunabwehr durch Kapselbildung. UPEC können die Harnwege von Menschen, Affen und Hunden infizieren. Ein wesentlich selteneres Krankheitsbild ist die Sepsis oder Meningitis bei Neugeborenen, die durch Sepsis/Meningitis-assoziierte E. coli (SEPEC, MENEC) hervorgerufen werden kann (Dawson et al., 1999). Sepsisauslösende E. coli nutzen ähnliche Pathogenitätsfaktoren wie die UPEC. Durch E. coli ausgelöste Sepsis kommt bei Mensch, Rind, Schaf, Schwein und Geflügel vor. SEPEC schützen sich vor der Attacke durch das Komplementsystem durch den Besitz bestimmter Kapseltypen und langkettiger Lipopolysaccharide. Dies ermöglicht ihnen, längerfristig im Blutserum zu überleben. SEPEC werden daher als serumresistent bezeichnet. Meningitis-assoziierte E. coli (MENEC) sind E. coli-varianten, die auch Harnwegsinfektionen verursachen können. Sie werden beim Menschen während der Geburt von der Mutter auf das Neugeborene übertragen, bei dem sie eine Meningitis auslösen können. MENEC schützen sich ebenfalls durch Bildung einer Kapsel (oft vom K1-Serotyp). Sie docken mit pathogenen S-Fimbrien-Adhäsinen an Epithel- und Endothelzellen an und können diese Gewebsbarrieren durchdringen. Nach der vollständigen Genom-Sequenzierung des E. coli K-12-Stammes MG 1655 (Blattner et al., 1997) folgte die Entschlüsselung weiterer Genome von apathogenen wie auch pathogenen Varianten der Spezies Escherichia coli. Durch Vergleiche der jeweiligen DNA-Sequenzen konnten Unterschiede in der genetischen Organisation aufgezeigt und Hinweise auf die phylogenetische Entwicklung von Bakterienstämmen gegeben werden (Dobrindt et al., 2010). Die Analyse der Sequenzdaten hat zu der Erkenntnis geführt, dass bakterielle Genome aus einem Kern genom bestehen, aber daneben zusätzliche Gene vorhanden sind, die für stammtypische Eigenschaften codieren und möglicherweise über horizontalen Gentransfer in das Genom integriert wurden [Abb. 14]. Kerngenom Phagen Plasmide Genom-Inseln Pathogenität Resistenz Sekretion Metabolismus Degradation Symbiose Abb. 14 Genomstruktur von Bakterien (nach Hacker et al., 2001)
14 Hierbei trägt die Integration von Fremd-DNA über mobile genetische Elemente (z. B. Plasmide, Bakteriophagen, Transposons), Mutationen und intragenomische Umlagerungen wesentlich zur Ausbildung eines flexiblen Genpools bei (Dobrindt et al., 2004; Hacker & Kaper, 2000). Bei der Ent stehung von pathogenen Varianten durch horizontalen Gentransfer [Abb. 15] spielen auch die sog. Pathogenitätsinseln (große chromosomale DNA-Regionen mit DNA-Sequenzen, die sich in ihrer Zusammensetzung stark vom Kern-Genom unterscheiden), eine besondere Rolle (Hacker et al., 1997). Hier sind gehäuft Gene für die Expression von bestimmten Virulenz- bzw. Fitnessfaktoren lokalisiert. Patho gene und apathogene E. coli-stämme unterscheiden sich durch das Vorhandensein oder Fehlen solcher Virulenzgene (Dobrindt, 2005; Grozdanov et al., 2004). Bakterien tauschen ihre DNA aus Die der Pathogenität zu Grunde liegenden Virulenzgene befinden sich häufig auf übertragbaren DNA-Elementen. Es wird vermutet, dass die Entstehung der EHEC-Stämme durch horizontalen Gentransfer via Plasmide und Bakteriophagen erfolgte. Während z. B. die evolutionäre Trennung der Spezies E. coli und Salmonella ssp. auf die Zeit vor ca. 160 Millionen Jahren datiert wird, liegt die Entstehung von EHEC O157 : H7 nur wenige Jahrzehnte zurück (Armstrong et al., 1996). Wahrscheinlich wurden u. a. durch Phagen die Toxin-Determinanten von Shigella dysenteriae auf E. coli O55 übertragen, der dadurch zu einem neuen Stamm E. coli EHEC O157 : H7 mutierte, dem Auslöser der enterohämorrhagischen Colitis (Lathem et al., 2003). Transposon Pathogenitätsinsel Bakteriophage Plasmid Bakterienruhr (EIEC) Diarrhöen (EPEC, EHEC, ETEC, EAggEC, DAEC) Kommensale E. coli Hämolytisch-Urämisches Syndrom (EHEC) Meningitis (MENEC) Harnwegsinfekte (UPEC) Abb. 15 Mobile genetische Elemente in der Evolution pathogener E. coli. Enteropathogene (EPEC), enterohämorrhagische (EHEC), enteroinvasive (EIEC), enteroaggregative (EAggEC), diffus adhärente (DAEC), uropathogene (UPEC), Meningitis-assoziierte (MENEC) E. coli (nach Kaper et al., 2004). Alfred Nissles Entdeckung des Coli-Antagonismus und sein neues Heilprinzip Gegen Ende des 19. Jahrhunderts erlebte die mikrobiologische Forschung, insbesondere die Medizinische Mikrobiologie, einen enormen Aufschwung, vor allem durch die bahnbrechenden Entdeckungen von Louis Pasteur, Robert Koch, Theodor Escherich, Paul Ehrlich, Ilja Metchnikoff u.v.a. Indes blieb die Frage, ob die Darmmikrobiota als Ganzes oder aber bestimmte Darmkeime einen eher positiven oder mehr negativen Einfluss auf den Wirt haben, ebenso unbeantwortet wie die Frage nach den regulierenden Mechanismen im Zusammenleben der Bakterien im Gastrointestinaltrakt untereinander. Verschiedene Forschergruppen versuchten bereits damals, diesen Geheimnissen auf die Spur zu kommen. So war es nicht verwunderlich, dass sich der Freiburger Hygieniker und Bakteriologe Alfred Nissle auf Grund seiner Untersuchungen an Darmkeimen im Routine-Labor weitere Fragen stellte, nämlich: Warum und wie beeinflussen sich Bakterien in einer Mischkultur, wie im Darm vorhanden, gegenseitig in ihrem Wachstum? oder Warum bleiben bei epidemie artigen Durchfallerkrankungen einige wenige Menschen darmgesund? Nachdem sich Nissle etwa 4 Jahre mit diesen Fragen experimentell auseinandergesetzt hatte, präsentierte er 1916 vor der Freiburger Medizinischen Gesellschaft seine Ergebnisse in einem Vortrag mit dem Titel Über die Grundlagen einer neuen ursächlichen Bekämpfung der pathologischen Prof. Dr. med. Alfred Nissle ( ) Darmflora (Nissle, 1916) [Abb. 16]. Die metho dische Grundlage bildete ein von Nissle entwickelter und im Prinzip noch heute verwendeter Testansatz zur In-vitro-Bestimmung bakterieller Interferenz ( Antagonismus-Test ) [Abb. 17]. Dabei werden Reinkulturen eines Infektions erregers mit Reinkulturen eines Bakterienstamms aus der physiologischen Darmmikrobiota (potenzieller Antagonist) gemeinsam in Flüssigkultur gezüchtet. Nach bestimmter Zeit, meist nach Übernacht-Kultur, werden Proben entnom men und auf geeigneten Festnährböden die Keimzahlen der co-kultivierten Bakterien bestimmt. Kann der physiologische Darmkeim das Hochwachsen des Infektionserregers behindern oder unterbinden, so gibt das Ausmaß der Wachstums hemmung die Stärke der antagonistischen Aktivität wieder
15 Nissle hatte für die Kennzeichnung solcher Darmkeime einen Antagonistischen Index entwickelt und fand unter den von ihm isolierten Coli-Stämmen aus dem menschlichen Intestinaltrakt solche mit starker oder schwacher antagonistischer Wirkung. Er nutzte diese Methode auch für die Bestimmung der wechselseitigen antagonistischen Aktivität zwischen verschiedenen Coli-Stämmen. E. coli mit besonders starker Hemmwirkung fand er während des Ersten Weltkrieges bei zwei Patienten im Freiburger Verwundeten-Lazarett, die niemals Neigung zu Darmerkrankungen gezeigt hatten und speziell auch dann nicht an infektiösen Darmprozessen erkrankt waren, als ein größerer Teil ihrer Umgebung daran erkrankte und sie infolge des engen Zusammen lebens mit bereits Erkrankten der Gelegenheit zur Infektion in reichlichstem Maße ausgesetzt waren (Nissle, 1916). Diese Stämme, die auch unter Labor bedingungen ihre antagonistische Wirksamkeit behielten, wurden von Nissle zuerst im Selbstversuch und an gesunden Personen getestet, um ihre Unschädlichkeit beim Menschen nach oraler Verabreichung festzustellen. Anschließend therapierte er versuchsweise Patienten, zuerst solche mit infektiösen Diarrhöen, Paratyphus B, Shigellen-Ruhr und Salmonellen-Dauerausscheider und später Patienten mit post-dysenterischen Darmfunktionsstörungen ( Colon irritabile, heute Reizdarm-Syndrom ) oder chronischer habitueller Obstipation (Nissle, 1916, 1918). Obwohl es sich hierbei um Einzel fall beobachtungen handelte, war Nissle von der klinischen Wirksamkeit seiner Coli-Kulturen überzeugt und dehnte die Untersuchungen auch auf weitere Darmerkrankungen, wie z. B. Colitis ulcerosa und dyspep tische Beschwerden, aus (Nissle, 1918, 1925). Abb. 16 Titelseite der Arbeit, in der Nissle erstmals über den E. coli-antagonismus berichtete. Ein weiteres E. coli-isolat von besonderer antagonistischer Stärke gewann Nissle 1917 aus den Fäzes eines Soldaten, der während des Balkanfeldzugs im Ersten Weltkrieg in der Region Dobrudscha stationiert war und der im Gegensatz zur großen Mehrzahl seiner Kameraden weder an Ruhr noch anderen Darmkrankheiten gelitten hat (Nissle, 1925). Nissle züchtete, von der asservierten Stammkultur ausgehend, die Keime auf Festagar platten und füllte die frisch abgeernteten Bakterienkulturen in Hartgela tinekapseln. Damit schuf er die Grundlage für ein Arzneimittel, das als Wirkstoff lebende Coli-Bakterien enthält. Nissle meldete für dieses Arzneimittel den Namen MUTAFLOR beim Reichspatentamt an, der am 1. März 1917 als Waren zeichen geschützt wurde. Später erhielt der im Mutaflor enthaltene E. coli-stamm, im Gedenken an Alfred Nissle, die Stammbezeichnung E. coli Nissle 1917, abgekürzt EcN. Der gegen verschiedene pathogene E. coli-stämme sowie gegen Salmonellen, Shigellen, 26 27
16 Cholera-Vibrionen, Proteus und Candida in vitro gefundene Antago nismus von E. coli Nissle 1917 [Abb. 17] wurde später auch in vivo bei gnotobiotischen Ferkeln [Abb. 18] und Ratten nachgewiesen. Selbst bei Neu geborenen ist der antimikrobielle Effekt nachweisbar, worauf nachfolgend noch eingegangen wird. Relative Keimzahl (%) EcN Testorganismen Antagonismus von EcN, Co-Kultivierung mit: 1 Salmonella enteritidis 2 Shigella dysenteriae 3 E. coli O112 ab (EPEC) 4 E. coli O6 : K15 : H31 (UPEC) 5 Proteus vulgaris 6 Candida albicans Abb. 17 Antagonismus von E. coli Nissle 1917 (EcN) gegen verschiedene Mikro organismen. EcN hemmt in vitro signifikant das Wachstum pathogener Bakterien und Pilze (nach Sonnenborn & Greinwald, 1991). Abb. 18 Beispiel für die antagonistische Wirkung von E. coli Nissle 1917 (EcN) im gnotobiotischen Ferkel. Die orale Gabe von EcN bekämpft Infektionen mit enteropathogenen E. coli (nach Schulze et al., 1992). Nissle selbst, aber auch andere Autoren, veröffentlichten in den Folgejahren zahlreiche Kasuistiken und Fallsammlungen, die wichtige Hinweise für die therapeutische Anwendbarkeit des antagonistisch aktiven E. coli-stamms Nissle 1917 lieferten. Das Auf und Ab der Therapie mit lebenden Mikroorganismen Nissle war zu seiner Zeit nicht der alleinige Protagonist einer Therapie mit lebenden Mikroorganismen. Die zunehmende Kenntnis über Infektionen des Darms und die damit im Zusammenhang stehenden Erkrankungen sowie die Erfahrungen über die Möglichkeit, Immunitäten dagegen zu entwickeln, ließen auch bei anderen Forschern die Idee reifen, zur Bekämpfung von Infektions erregern harmlose Bakterien aus der körpereigenen Mikrobiota zu nutzen. Bereits um das Jahr 1900 und später wurden vor allem Laktobazillen kulturen gezielt zur Therapie eingesetzt (Brudzinski, 1900; Distaso & Schiller, 1914; Rettger & Cheplin, 1921; u. a.), nicht zuletzt auch ausgelöst durch Metchnikoffs Bestseller The prolongation of life ( Metchnikoff, 1907). Nissle war aber jahrzehntelang der Einzige, der durch den Einsatz des von ihm isolierten lebenden E. coli-stamms in Form des Präparats Mutaflor therapeu tische Erfolge erzielte. Dennoch ebbte das allgemeine Interesse an dieser Therapiestrategie gegen Mitte des vergangenen Jahrhunderts ab. Hauptgrund war der Beginn des Antibiotika-Zeitalters hatte Alexander Fleming aus dem Schimmelpilz Penicillium notatum eine antibakteriell wirkende Substanz isoliert, die ab 1940 zur therapeutischen Anwendung kam (Penicillin). In der Folge zeit wurde eine Fülle weiterer Antibiotika entwickelt, mit dem Ergebnis einer äußerst erfolgreichen Eliminierung von Infektionskeimen aus Entzündungsherden. Das Ziel, alle Infektionskrankheiten mit diesen antimikrobiellen Substanzen zu beherrschen, schien erreichbar zu sein (Muniesa et al., 2012). Je näher man sich aber dem Ziel glaubte, umso häufiger wurden therapeutische Misserfolge dokumentiert und umso intensiver wurde entweder nach neuen wirksamen Antibiotika oder nach solchen mit einem noch breiteren Wirkungs spektrum gesucht. Schätzungsweise sind es heute Tonnen an Antibiotika, die weltweit jährlich von Mensch und Tier aufgenommen und z. T. unverändert in die Umwelt wieder ausgeschieden werden. Ohne diese Antibiotika wäre in den zivilisierten Ländern der heutige Gesundheits- und Lebensstandard nur schwer vorstellbar. Allerdings können Antibiotika auch krank machen: Übelkeit, Durchfälle, Erschöpfung, Psychosen, Leber- und Nieren schä den, Allergien, anaphylaktischer Schock sind nur einige der vielfach dokumen tierten Nebenwirkungen. Hinzu kommt, dass Mikroorganismen in der Lage sind, sich schnell und effektiv an veränderte Umweltbedingungen anzupassen. So können sie auf verschiedenen Wegen Resistenzen ausbilden und sich so der Wirkung 28 29
17 der Anti biotika entziehen. In Biotopen mit hoher Antibiotikakonzentration z. B. ist der Gastrointestinaltrakt eines Patienten im Krankenhaus solch ein Biotop ist die residente Mikrobiota einem zunehmenden Selektionsdruck durch anti mikrobiell wirkende Substanzen ausgesetzt. Das Ergebnis ist eine Häufung multiresistenter Keime im Hospitalmilieu und ein Anstieg von nosokomialen Infektionen mit multiresistenten Erregern weltweit. Diese Entwicklung und das langsam zunehmende Bewusstsein bei Therapeuten und Patienten, mit der Anwendung von Antibiotika kritischer umzugehen sowie zusätzlich oder alternativ bewährte und positiv evaluierte Methoden einzusetzen, haben in den letzten Jahren zu einer Renaissance der Therapie mit lebenden Mikro organismen geführt. Übereinstimmend mit der internationalen Literatur bezeichnet man diese Therapie heute auch als probiotische Therapie und die dabei eingesetzten Mikroorganismen als Probiotika. Probiotika sind definitionsgemäß apatho gene lebende Mikroorganismen, die, wenn sie in genügend hoher Zahl lebensfähig in den Gastrointestinaltrakt gelangen, einen positiven Effekt auf die Gesundheit des Wirtsorganismus ausüben (FAO/ WHO, 2001). Ein Probiotikum, das als Arzneimittel zugelassen werden soll, muss hohe Anforderungen erfüllen [Abb. 19]. Im Gegensatz zu Nahrungsergänzungsmitteln müssen hier der Nachweis der klinischen Wirksamkeit bei definierten medizinischen Indikationen und Belege zu Wirkungen und Wirkmechanismen erbracht werden. Außerdem muss die Einhaltung spezieller Kriterien zur Produktqualität und Unbedenklichkeit (u. a. mikrobiologische Reinheit und definierter Lebendkeimgehalt sowie Apathogenität und genetische Stabilität des therapeutisch eingesetzten Mikroorganismus) garantiert sein [Abb. 19]. Wirksamkeit Durch kontrollierte klinische Studien nachgewiesene Wirksamkeit bei definierten Indikationen Produktqualität Mikrobiologische Reinheit Definierter Lebendkeimgehalt Exakte Identifizierung und Abgrenzung von nahe verwandten Mikroorganismen Lebensfähigkeit im GI-Trakt Unbedenklichkeit Apathogenität Genetische Stabilität Wirkmechanismen Unterdrückung von Wachstum und Kolonisation unerwünschter Mikroorganismen Beitrag zur Optimierung des intestinalen Milieus und zum luminalen Stoffwechsel Kommunikation mit Darmepithel und Immunsystem Kolonisationsfähigkeit Abb. 19 Anforderungen an probiotische Arzneimittel: Nachweis der Wirksamkeit und Unbedenklichkeit, Erkenntnisse zu den Wirkmecha nismen, nachgewiesene und reproduzierbare Produktqualität. Der Nachweis der Apathogenität oder Avirulenz ist bei der Überprüfung von E. coli-stämmen, die als Probiotika therapeutisch eingesetzt werden sollen, von besonderer Bedeutung, da wie bereits beschrieben die Spezies Escherichia coli eine Reihe von pathogenen Varianten beinhaltet. Aus diesem Grunde wurde die Verwendung von Präparaten mit lebenden E. coli-bakterien von einigen Autoren noch bis Mitte der 90er Jahre des letzten Jahrhunderts pauschal abgelehnt (Expert s Opinion Poll Marget et al., 1995). Diese pauschale Ablehnung ist mittlerweile einer differenzierteren Betrachtungs weise gewichen, was nicht zuletzt der Weiterentwicklung molekular genetischer Differenzierungs- und Identifizierungsmethoden zu verdanken ist. Mit Hilfe dieser Techniken ist es möglich, pathogene E. coli-varianten eindeutig von apathogenen Stämmen zu unterscheiden. Darüber hinaus zeigen apathogene Stämme, wie E. coli Nissle 1917, im Gegensatz zu virulenten E. coli- Varianten in toxikologischen Untersuchungen sowohl an konventionell als auch an keimfrei gehaltenen Tieren keinerlei schädliche Wirkungen
18 E. coli Stamm Nissle 1917: der weltweit am besten untersuchte probiotische E. coli-stamm Alle in Abb. 19 aufgelisteten Anforderungen an ein probiotisches Arznei mittel werden von E. coli Nissle 1917 (EcN), der Wirksubstanz von Mutaflor, vollständig erfüllt (Sonnenborn & Schulze, 2009). Die Aufklärung der Genomstruktur (Grozdanov et al., 2004; Hancock, Vejborg et al., 2010; Sun et al., 2005) wie auch die vollständige Genom-Sequenzierung (Cress et al., 2013; Reister et al., 2014) hat gezeigt, dass das Fehlen von Pathogenitätsfaktoren (z. B. von Enterotoxinen, Hämolysinen, Zytotoxinen, Invasinen, pathogenspezifischen Fimbrien) [Abb. 20], kombiniert mit dem Vorhandensein von sog. Fitness- Faktoren (z. B. Mikrocinen, multiplen Eisenaufnahmesystemen, typischen Adhäsinen, Flagellen) [Abb. 21], die das Überleben und die Kolonisierung im Darm ermöglichen, zu den probiotischen Eigenschaften von EcN beitragen (Blum-Oehler et al., 2001; Deriu et al., 2013; Dobrindt, 2005; Grosse et al., 2006; Jacobi & Malfertheiner, 2011; Lasaro et al., 2009; Patzer et al., 2003; Schlee et al., 2007; Valdebenito et al., 2006, Vassiliadis et al., 2010). Apathogener E. coli-stamm (Serotyp O6 : K5 : H1) Genetische Stabilität Keine Enterotoxin-Produktion Zytotoxin-Produktion Hämolysin-Produktion Pathogenen Adhäsionsfaktoren Invasivität Immuntoxizität Serumresistenz (keine Sepsisgefahr) Uropathogenität Toxizität in keimfreien und konventionell gehaltenen Tieren Stamm zwar immunmodulatorisch wirksam, zeigt aber keine immuntoxi schen Wirkungen (Grozdanov et al., 2002). Serologisch-diagnostisch ist das EcN-Lipopolysaccharid als Oberflächenantigen (O-Antigen) vom Typ O6 anzusprechen. Ein zweites Set von Strukturelementen mit signalvermittelnder Wirkung sind die drei verschiedenen, in ihrer Kombination EcN- typischen Fimbrien (F1A-, F1C- und Curli - Fimbrien). Diese sind zum einen wichtig für die Biofilmbildung, zu der EcN im Gegensatz zu anderen Coli-Bakterien auch bei der physiologischen Körpertemperatur von 37 C in der Lage ist (Lasaro et al., 2009). Zum anderen können die Fimbrien aufgrund ihrer Adhäsions eigenschaften auch den Kontakt zur Epithelzelle bzw. zum Darmschleim vermitteln. Ein drittes Strukturelement mit signalvermittelnden Eigenschaften sind die Geißeln (Flagellen), die den EcN-Stamm primär in die Lage versetzen, sich im zähflüssigen Darmschleim aktiv fortzubewegen. Daneben sind die Flagellen von EcN verantwortlich für die Induktion der Synthese anti mikrobieller Peptide (Defensine u. a.) im Darm epithel, eine Fähigkeit, die unter anderem für die therapeutische Effektivität des Keims bei Colitis ulcerosa von Bedeutung ist (Schlee et al., 2007). Auch die Kapsel vom Serotyp K5 ist wichtig bei der Interaktion zwischen EcN und den Darmepithelzellen (Hafez et al., 2009, 2010). Gencluster des Chromosoms, die für die phäno typischen Merkmale von E. coli Nissle 1917 codieren 7 verschiedene Eisen - auf nahme- Systeme als wichtige Fitness faktoren 2 antagonistisch aktive Mikrocine Chromosom keine Pathogenitätsfaktoren Fimbrien 3 verschiedene Typen von Fimbrien ermöglichen Adhärenz und Biofilm bildung Flagellen (H1-Serotyp) sorgen für aktive Fortbewegung Abb. 20 Sicherheitsaspekte von E. coli Nissle Neben den Syntheseleistungen (Produktion von löslichen Signalstoffen), die das Vorhandensein der lebenden Bakterienzelle voraussetzen, sind auch bakterielle Strukturelemente, die für das Wirtsgewebe Signalfunktion haben, für die Interaktionen zwischen E. coli Nissle 1917 (EcN) und dem Darmepithel von Bedeutung (Behnsen et al., 2013). Zu diesen Struktur elementen zählt das besondere stammtypische Lipopolysaccharid (LPS), das aufgrund der stark ver kürzten Oligosaccharid-Seitenkette dafür verantwortlich ist, dass EcN nicht in der Lage ist, eine Sepsis zu verursachen. So ist der EcN- 2 stammtypische Plasmide ohne Antibiotika- Resistenz-Gene, nicht übertragbar Spezielle immunmodulatorische LPS-Variante vom Serotyp O6, bisher bei keinem anderen Stamm nachgewiesen Kapsel (K5) Serotyp O6 : K5 : H1 Abb. 21 Phänotypische Charakteristika von E. coli Nissle 1917 (EcN) und ihre Genloci auf dem Bakterien chromosom. Die wichtigsten Strukturkomponenten von E. coli Nissle 1917 mit signalvermittelnden Eigenschaften sind rot umkreist: O6-Antigen, adhäsive Fimbrien (F1A-, F1Cund Curli -Fimbrien), Kapsel-Komponenten und Flagellen (H1-Antigen)
19 Wirkungen und Wirkmechanismen von E. coli Stamm Nissle 1917 Mikrobielle Kommunikation und Interaktionen ( Cross Talk ) im Gastrointestinaltrakt Mikroorganismen im Gastrointestinaltrakt kommunizieren über lösliche oder strukturgebundene Signalmoleküle mit der Darmschleimhaut des Wirtes. Diese Interaktion nennt man Cross Talk [Abb. 22] (Köhler et al., 2003; Lebeer et al., 2010; Sekirov et al., 2010). Darmkeime Pathogene Kommensale Probiotische Mikroorganismen Signalmoleküle Darmlumen Tight Junctions, Adherence Junctions und Desmosomen die vielfältige anti mikrobielle Wirkungen haben, halten bestimmte Darmbakterien Infektionskeime fern eine Eigenschaft, die auch für uns als Wirtsorganismen von Nutzen ist (Gillor et al., 2008; Kirkup, 2006) [Abb. 22]. So produziert z. B. E. coli Nissle 1917 (EcN) zwei verschiedene antibakteriell wirkende Substanzen, Mikrocin M (M von Mutaflor ) und Mikrocin H47 (Patzer et al., 2003). Die Mikrocine bilden eine Untergruppe der Bakteriocine und wirken hauptsächlich auf nahe verwandte Keime des Produ zentenstamms, bei EcN vor allem auf andere gramnegative Entero bakterien. Bildung von Biofilmen und Mikrokolonien im Darm Als strukturgebundene Signalmoleküle sind insbesondere die von E. coli Nissle 1917 (EcN) gebildeten Fimbrien und Geißeln (Flagellen) von Bedeutung, die die interbakterielle Vernetzung und die Biofilmbildung des Keims an der Darmschleimhaut, genauer gesagt an der dem Darmepithel lumenseitig aufliegenden Mucinschicht, vermitteln (Troge et al., 2012). Die schematische Darstellung der Entste hung eines Biofilms ist in Abb. 23 gezeigt (Jenkinson & Lappin-Scott, 2001). Wie Untersuchungen mit keimfreien Ratten gezeigt haben, deren Intestinaltrakt nach oraler Verabreichung (Monoassoziation) mit EcN besiedelt wurde, haben die probiotischen Coli-Bakterien eine starke Affinität zum Darmschleim, wo sie Mikrokolonien oder Mucinschicht Darmepithelzellen Basalmembran Abb. 22 Mikrobielle Kommunikation und Interaktion im Gastrointestinaltrakt. Kommensale Darmkeime (blau) und probiotische Mikroorganismen (grün) produzieren verschiedene, sich gegenseitig beeinflussende und auch auf die Darmepithelzellen einwirkende Signalmoleküle (blaue und grüne Kügelchen). Durch die Produktion von Bakteriocinen (rote Blitze) hemmen bestimmte Darmbakterien, wie E. coli Nissle 1917, pathogene Mikroorganismen und hindern diese an der Kolonisierung des Intestinaltrakts. Oberflächenenergie des Substrats Räumliche Nähe propinquity Strömungsrichtung Phänotypische Veränderungen Physiko-chemische Faktoren Nährstoffangebot Kommemsalismus Mutualismus Hydrodynamische Scherkräfte Auch untereinander tauschen Darmbakterien Informationen aus, was zumeist durch lösliche Signalstoffe vermittelt wird. Zu diesen Signalstoffen gehören die N-Acylhomoserinlaktone (AHSL) gramnegativer Bakterien und die modi fizier ten Peptidmoleküle grampositiver Bakterien, die beim sog. Quorum Sensing von Bedeutung sind (Kaper & Sperandio, 2005; Shiner et al., 2005). Darunter versteht man die Fähigkeit der Darmbakterien, die Zelldichte ihrer Populationen zu messen und entsprechend zu agieren. Mit anderen löslichen Faktoren, den chemisch heterogenen Bakteriocinen, Adhäsion Kolonisation Akkumulation Verbandsbildung Ablösung climax community Abb. 23 Schematische Darstellung der Ausbildung eines Biofilms an der Darmschleimhaut (nach Jenkinson & Lappin-Scott, 2001)
20 Bio filme ausbilden [Abb. 24]. Für den Menschen als Patient bedeutet die Fähigkeit von EcN zur Biofilmbildung, dass eine im Verhältnis zur gesamten Darm mikrobiota (ca Keime) relativ geringe Menge an probiotischen Bakterien (ca lebende Zellen/Einzeldosis) sich nach der Freisetzung aus der magensaftresistenten Mutaflor -Kapsel nicht nur im Dickdarm lokal verteilt, sondern auch nach Assoziation an den Darmschleim dreidimensional vernetzen kann. Dies hat zur Folge, dass die Verweilzeit der verabreichten Keime am Ziel ort, dem Colon, verlängert wird. (Joeres-Nguyen-Xuan et al., 2010). Die Fähigkeit von EcN zur Biofilmbildung zeigte sich in dieser Studie dadurch, dass eine Elimination des Keims aus dem Darm nach Absetzen der Medikation stark verzögert verlief. So war EcN nach 2 Wochen noch bei knapp 50 % der Probanden nachweisbar, nach 12 Wochen noch bei ca. 25 %. [Abb. 25]. Die Lebens fähigkeit der EcN- Bakterien im Darm wurde durch die antibakterielle Wirkung von Mesalazin nicht signifikant beeinflusst. Die Feststellung, dass Mesalazin keine negativen Auswirkungen auf die Vitalität von EcN hat, eröffnet die Möglichkeit einer Co-Medikation bei chronisch entzündlichen Darmerkrankungen. Die bei E. coli Nissle 1917 (EcN) besonders stark ausgeprägte Fähigkeit zur Adhäsion verhindert, dass die oral verabfolgten EcN-Bakterien nach der Magen-Darm- Passage schnell wieder ausgeschieden werden und verlängert ihre Persistenz im Intestinaltrakt. Probanden [%] mit positivem Nachweis von E. coli Nissle 1917 im Stuhl 100 E. coli Nissle Mesalazin E. coli Nissle Placebo Abb. 24 Besiedlung des Darmschleims durch E. coli Nissle 1917 nach oraler Verabreichung an keimfreie Ratten. Die Pfeile zeigen auf schleimumhüllte Bakterienzellen (rasterelektronenmikroskopische Aufnahme: A. Lorenz, J. Schulze, Potsdam-Rehbrücke). Eine experimentelle Untersuchung zur Entstehung von Biofilmen zeigte für E. coli Nissle 1917 (EcN) eine im Vergleich zu entero pathogenen (EPEC), entero toxischen (ETEC) und entero hämorrhagischen E. coli-stämmen (EHEC) deutlich bessere Fähigkeit zur Biofilmbildung. Auch scheint EcN in der Lage zu sein, die pathogenen E. coli-stämme während der Biofilmbildung zu verdrängen (Hancock, Dahl et al., 2010). Die Biofilmbildung beruht u. a. darauf, dass EcN Cellulose produzieren kann, die in Biofilmen als extrazelluläre Matrix dient (Monteiro et al., 2009). Für die Ausbildung von Biofilmen sind die F1C- Fimbrien von EcN von besonderer Bedeutung (Lasaro et al., 2009). In einer placebokontrollierten, randomisierten doppelblinden Studie erhielten 48 gesunde Probanden 2 x täglich 2,5 25 x 10 9 E. coli Nissle 1917 (EcN)/Kapsel mg Mesalazin oder 2,5 25 x 10 9 EcN-Bakterien/Kapsel + Placebo Wochen Abb. 25 Nach oraler Verabreichung an Probanden persistiert E. coli Nissle 1917 noch über Wochen im Darm einiger Testpersonen. Die Überlebensfähigkeit von E. coli Nissle 1917 im Darm wird durch Mesalazin nicht signifikant beeinflusst (nach Joeres-Nguyen-Xuan et al., 2010). Als Konsequenz für die klinische Praxis kann festgestellt werden, dass die Biofilmbildung von E. coli Nissle 1917 die Kolonisationsfähigkeit des Probiotikums verbessert und die Persistenz der Keime im Intestinaltrakt verlängert
21 Die Stärkung der intestinalen Barrierefunktion Präklinische In-vitro- und In-vivo-Untersuchungen haben zu der Erkenntnis geführt, dass die klinische Wirksamkeit von bestimmten Probiotika, darunter auch von E. coli Nissle 1917 (EcN), zumindest teilweise, wenn nicht sogar über wiegend, auf eine intensive Kommunikation ( Cross Talk ) der verabreichten nützlichen Mikroorganismen mit dem Darmepithel zurückzuführen ist. Dabei resultiert diese Kommunikation zwischen Probiotikum und Wirtsorganismus in einer generellen Stärkung der Barrierefunktion der Darmschleimhaut. Für EcN wurden bisher drei grundlegende Wirkmechanismen entdeckt, die in ihrer Gesamtheit eine Verbesserung der intestinalen Barrierefunktion zur Folge haben: 1. ein Anti-Invasionseffekt (Hemmung der Invasion von pathogenen entero invasiven Mikroorganismen in die Darmepithelzellen), 2. ein Induktionseffekt auf die Synthese von antimikrobiell wirkenden körpereigenen Peptiden (Defensinen u. a. Wirkstoffen) durch die Darmepithelzellen, 3. eine Stärkung des Zusammenhalts des epithelialen Zellverbands durch die Beeinflussung bestimmter Zell-Kitt-Proteine (Zonula-occludens-Proteine) der sog. Tight Junctions. 1. Der Anti-Invasionseffekt am Darmepithel: Bestimmte pathogene Durchfallerreger sind in der Lage, in die Epithelzellen der Darmschleimhaut einzudringen. Man spricht hier von sog. enteroinvasiven Mikroorganismen. Zu diesen gehören beispielsweise die Ruhr-Bazillen (Shigellen), Salmonellen, Yersinien u. a. Die invasive Aktivität dieser Mikroorganismen kann man im mikrobio logischen Labor durch spezielle Invasionstests mit menschlichen epithelialen Zellkulturen nachweisen [Abb. 26]. Die Infektion des Darmepithels mit entero invasiven pathogenen Keimen initiiert profuse Diarrhöen, die bei stärkerem Befall der Schleimhaut auch zum Absetzen blutiger oder blutig-schleimiger Stühle führen können. Dies beruht darauf, dass die enteroinvasiven Keime letztendlich die Darmepithelzellen zerstören und z. T. großflächige Ulzerationen bewirken können. Die gegen solche Infektionserreger gerichtete Aktivität von Probiotika kann prinzipiell durch drei Wirkmechanismen zustande kommen: a) ein direkter antagonistischer Effekt gegen die patho genen Erreger (Hemmung der Zellvermehrung bzw. Abtötung der Durchfallkeime), b) eine Besetzung von Rezeptoren an der Zellmembran der Darmepithelzelle oder in der aufliegenden Mucinschicht, so dass die pathogenen Keime keine Andock stellen finden, und/oder c) eine stabilisierende Wirkung auf die Darmepithelzelle, so dass diese dem Angriff der invasiven Erreger besser standhalten kann. A HeLa-Kontrolle (ohne Mikroorganismen) D B HeLa- + EIEC Abb. 26 In-vitro-Invasionstests von enteroinvasiven und apathogenen Enterobakterien mit HeLa-Zellen in der Zellkultur. EIEC: Enteroinvasive Escherichia coli-bakterien, S. typhimurium: Salmonella typhimurium. Nach gemeinsamer Inkubation von enteroinva siven Keimen und Epithelzellen sind Erstere bald im Inneren der Epithelzelle zu finden, wo sie sich rasch vermehren können (B, C, D). Demgegenüber ist der nicht-invasive E. coli Stamm Nissle 1917 nach Co-Inkubation mit den Epithelzellen nicht im Inneren der Epithelzelle zu finden, sondern adhäriert außen an der Zellmembran (E). (Fluoreszenzmikroskopische Darstellung; Aufnahmen: A. Fahsbender, U. Sonnenborn, Herdecke). Ein direkter antagonistischer Effekt von E. coli Nissle 1917 (EcN) gegen pathogene Erreger ist seit langem bekannt und wurde durch aktuelle Untersuchungen bestätigt [Abb. 27] (Kandasamy et al., 2014; Kleta et al., 2014; Leatham et al., 2009; Schinner et al., 2015; Schroeder et al., 2006; Sonnenborn & Schulze, 2009; Storm et al., 2011). Es hat sich herausgestellt, dass EcN auch in der Lage ist, die Toxinproduktion pathogener Keime zu unterbinden. So reduziert EcN in Co-Kultivierung mit Shiga-Toxin produzierenden E. coli- Stämmen (EHEC) signifikant deren Wachstum, die stx-genexpression und die Shiga-Toxin-Produktion (Mohsin et al., 2015; Reissbrodt et al., 2009; Rund et al., 2013). Während ein kürzlich von einer Forschergruppe des Robert-Koch-Instituts isolierter kommensaler E. coli-stamm ähnliche Wirkun gen auf EHEC-Stämme wie EcN aufweist, zeigen andere kommensale E. coli-stämme und probiotische Bakterienstämme keine oder nur geringe Hemmwirkung [Abb. 28]. Eine Verdrängung von pathogenen Keimen am Darm epithel beruht u. a. auf der Fähigkeit von EcN, Biofilme zu bilden (Hancock, Dahl et al., 2010, s. oben Bildung von Biofilmen ). Die Biofilmbildung geht einher mit einer Stimulierung der intestinalen Mucinsynthese (Hafez et al., 2012). EcN reduziert auch die Salmonellenadhäsion an Darmepithelzellen bei Schweinen (Schierack et al., 2011). E C HeLa + S. typhimurium HeLa + S. typhimurium HeLa + E. coli Nissle
22 log KBE/g Fäzes EHEC (E. coli EDL933) E. coli MG Zeit (d) log KBE/g Fäzes EHEC (E. coli EDL933) E. coli Nissle Zeit (d) Abb. 27 Mit Streptomycin behandelte CD-1 Mäuse wurden prophylaktisch mit kommensalen E. coli- Stämmen (E. coli MG1655, E. coli Nissle 1917) besiedelt. Nur E. coli Nissle 1917 hemmt die An siedlung des nach 10 Tagen verabreichten enterohämorrhagischen E. coli (EHEC EDL933) im Mäusedarm. KBE = Kolonie-bildende Einheiten (nach Leatham et al., 2009). Abb. 28 Stamm-spezifische Wirkung von probiotischen Bakterien auf die Konzentration von Shiga- Toxinen nach Co-Kultivierung mit Shiga-Toxin produzierenden E. coli (EHEC-Stämme). E. coli Nissle 1917 reduziert signifikant die Shiga-Toxin-Konzentration (nach Reissbrodt et al., 2009). Untersuchungen am Institut für Mikrobiologie der Tschechischen Akademie der Wissenschaften in Novy Hradek haben darüber hinaus gezeigt, dass eine Besiedlung keimfreier Schweinchen mit E. coli Nissle 1917 die Translokation nachfolgend verabreichter Salmonella Thyphimurium- Bakterien über die Darmschleimhaut in die mesenterialen Lymphknoten und die weitere Streuung über den Blutkreislauf verhinderte (Splichalova et al., 2011). Demgegenüber konnte für Bifidobacterium choerinum, einen schweinespezifischen Darmkeim, kein prophylaktischer Effekt gezeigt werden. Untersuchungen am Institut für Molekulare Infektionsbiologie der Universität Würzburg mit der intestinalen Zelllinie INT407 haben ergeben, dass der anti-invasive Wirkmechanismus von E. coli Nissle 1917 (EcN) durch eine direkte Einwirkung des pro biotischen Coli-Bakteriums auf die Darmepithelzelle zustande kommt (Altenhoefer et al., 2004; Oelschlaeger et al., 2001). Bei Co- Kulti vierungen von INT407-Zellen mit EcN oder dem apathogenen Kontrollstamm E. coli K-12 wurden keine Bakterien in den Epithelzellen gefunden, d. h. beide Escherichia coli-stämme haben keine invasiven Fähigkeiten. Im Gegensatz dazu kommt es bei Co-Kultivierung der Epithelzellen mit den Salmonella typhimurium-stämmen C17 bzw. LT2 zum Eindringen der invasiven Bakterien in die Darmzellen. Nach Co-Inkubation kann man mehr als 40 % des verabreichten Inokulums des virulenteren Salmonellenstamms (C17) in den Epithelzellen wiederfinden. Bei dem schwächer virulenten Salmonellenstamm (LT2) beträgt die Invasionsrate gut 10 %. Führt man nun eine dreifache Co-Kultivierung mit Epithelzellen, Salmonellen und E. coli-bakterien durch, so wird die Invasivität der Salmonellen nur im Falle der Co-Kultivierung mit E. coli Nissle 1917 deutlich reduziert. Im Vergleich dazu zeigt der Kontrollstamm E. coli K-12 keinen anti-invasiven Effekt. Zur Klärung der Frage, wie der anti-invasive Effekt von E. coli Nissle 1917 (EcN) zustande kommt, wurden verschiedene Versuchsansätze in der Zellkultur durchgeführt. Bei Inkubationen der Epithelzellen mit S. typhimurium C17 und EcN ließ sich der Anti-Invasionseffekt von EcN gegenüber S. typhimurium C17 gut reproduzieren. Dabei kam es zu keiner Abnahme der Salmonellen-Zellzahlen in den Versuchs ansätzen, was vermuten lässt, dass der durch EcN bewirkte Anti-Invasions effekt nicht durch die Ausschüttung der antimikrobiell wirkenden Mikrocine zustande kommt. Auch mit einer Mikrocin-negativen Mutante von EcN (Stamm H5445) war der anti-invasive Effekt noch in vollem Umfang vorhanden. Das beweist, dass dieser Wirkmechanismus des EcN-Stamms nicht mit seiner Fähigkeit verknüpft ist, antimikrobielle Substanzen zu produzieren. Ebenso kommt eine Besetzung von Haftstellen für die invasiven Salmonellen an der Zellmembran der Epithelzellen durch EcN nicht als Wirkmechanismus 40 41
23 in Frage. Diese Möglichkeit konnte man ausschließen durch eine Versuchsanordnung, bei der die probiotischen EcN-Bakterien durch Einbringen in einen Filtereinsatz von den pathogenen Salmonellen wie auch von den Epithelzellen getrennt wurden. Bei diesem sog. Transwell-System handelt es sich um einen Filtereinsatz, dessen Bodenfläche mit einer semipermeablen Membran bestückt ist, die zwar durchlässig ist für Moleküle, nicht aber für ganze Bakterienzellen. Trotz der räumlichen Trennung von EcN und den anderen Testkomponenten blieb der Anti-Invasionseffekt von EcN erhalten. Dieser Befund spricht in Zusammenhang mit den anderen Ergebnissen dafür, dass der anti-invasive Effekt von EcN auf der Synthese diffusibler Signal moleküle beruht, die auf die Epithelzellen in einer Art und Weise einwirken, dass diese unempfindlicher werden gegenüber den Invasions mechanismen des virulenten Salmonellenstamms. Welche Signalsubstanzen von EcN diesen Effekt bewirken und welche Gene dafür verantwortlich sind, ist zur Zeit Gegenstand intensiver Forschung. Neuere Untersuchungen auf zellbiologischer Ebene haben ergeben, dass E. coli Nissle 1917 die Aktivität des Invasionsapparats von Salmonellen reduziert (Schierack et al., 2011). Dies führt dazu, dass die ersten Invasions schritte der pathogenen Erreger, wie die Epithelzelladhäsion, unterdrückt werden. Invasionseffizienz [%] Salmonella enterica Serovar Typhimurium Stamm C17 Stamm SL 1344 Monoinkubation Co-Inkubation mit E. coli K-12 DH5α Co-Inkubation mit E. coli Nissle 1917 Yersinia enterocolitica Stamm WA-C Stamm WA314 Shigella flexneri Stamm M90T Abb. 29 Nachweis der Anti-Invasionswirkung von E. coli Nissle 1917 gegen die Salmonella Typhimurium- Stämme C17 und SL1344, die Yersinia enterocolitica-stämme WA-C und WA314 und den Shigella flexneri-stamm M90T in vitro. Für den Nachweis wurden Co-Inkubationen von E. coli Nissle 1917 mit den o. g. pathogenen Bakterienstämmen in Zellkulturversuchen mit INT407- Zellen durchgeführt (nach Altenhoefer et al., 2004). Erfreulicherweise funktioniert die Anti-Invasionswirkung von E. coli Nissle 1917 (EcN) nicht nur mit Salmonellen, sondern auch mit verschiedenen anderen invasiven Infek tions erregern (Altenhoefer et al., 2004; Huebner et al., 2011). So konnten Altenhoefer et al. (2004) in Zellkulturver suchen mit der INT407-Zelllinie auch die Hemm wirkung von EcN auf das Invasionsvermögen von Yersinia enterocolitica und Shigella flexneri [Abb. 29] sowie von Listeria monocytogenes und Legionella pneumophila nachweisen. Dies ist um so interessanter, da die verschiedenen invasiven Keime über völlig unterschied liche Invasionsmechanismen verfügen, ein weiterer Hinweis darauf, dass die Anti-Invasionswirkung von EcN auf einer direkten Beeinflussung grundlegender Signalvorgänge in der Epithelzelle selbst beruht. Desweiteren konnten die Infektionsbiologen bestätigen, dass die beobachtete Hemmung der Zellinvasion der darmpathogenen Erreger durch EcN nicht auf der Mikrocin-Produktion beruht, keines direkten Kontakts zwischen EcN und den invasiven Bakterien bzw. zwischen EcN und den Epithelzellen bedarf und auch nicht vom Vorhandensein der F1A- bzw. F1C-Fimbrien abhängig ist. Eine mögliche Bedeutung von plasmidcodierten Genprodukten für den Anti-Invasionseffekt konnte ebenfalls nicht gefunden werden, da ein plasmidfreies EcN-Derivat dieselbe Anti- In vasionswirkung zeigte wie der Originalstamm. Dies bedeutet, dass auch die EcN-typischen kleinen Plasmide pmut1 und pmut2 [s. Abb. 21] für den invasions hemmenden Effekt von EcN nicht erforderlich sind, die Erb information für die Anti-Invasionswirkung also chromosomal codiert sein muss. Welche Gene auf dem EcN-Chromosom den anti-invasiven Effekt bewirken, ist Thema aktueller molekulargenetischer Untersuchungen. Zusammenfassend bleibt festzustellen, dass E. coli Nissle 1917 (EcN) bisher noch unbekannte Signalmoleküle sezerniert, die direkt auf die Darmepithelzellen einwirken, wodurch deren Funktion als Infektionsbarriere gegen entero invasive Keime deutlich verbessert wird. Diese anti-invasive Aktivität repräsentiert einen Aspekt des Cross Talk von EcN mit dem Darmepithel, der für die klinische Wirksamkeit bei bestimmten gastroenterologischen Indikationen von Bedeutung sein dürfte. Als Konsequenz für die klinische Praxis kann festgehalten werden, dass der anti-invasive Effekt von E. coli Nissle 1917 nicht nur wichtig ist bei Durchfallerkrankungen als Folge einer Infektion mit enteroin vasiven Er regern, sondern auch bei der Behandlung von Patienten mit Colitis ulcerosa, bei denen bekanntlich eine Infektion mit enteropathogenen Keimen einen akuten Entzündungsschub auslösen kann
24 2. Der Induktionseffekt auf die Synthese antimikrobieller Peptide des Darmepithels: Die Barrierefunktion der Darmschleimhaut gegenüber den im Darmlumen vorhandenen kommensalen Mikroorganismen wie auch gegenüber Infektionskeimen ist gekennzeichnet durch die Fähigkeit der Enterozyten, auf einen mikrobiellen Reiz hin besondere Peptidmoleküle und Proteine zu synthetisieren und auszuschütten, die sich durch breite anti mikro bielle Wirkungen auszeichnen. Zu den in den letzten Jahren intensiv untersuchten körper eigenen Schutzsubstanzen gehören die humanen α- und β-defensine und die Cathelicidine als niedermolekulare antimikrobielle Peptide, wie auch das vergleichsweise höhermolekulare Calprotectin und funktionell verwandte Proteine. Diese evolutionsbiologisch sehr alten Schutzsubstanzen der Epithelien sind Komponenten der sog. natürlichen oder angeborenen Immunität und werden nicht durch das spezifische adaptive Immunsystem reguliert. Bei bestimmten Darmerkrankungen, z. B. Colitis ulcerosa und Morbus Crohn, ist die Synthese dieser Schutzstoffe vermindert (Wehkamp et al., 2005). Als Folge findet man bei den betroffenen Patienten im Gegensatz zu gesunden Personen eine dichte Besiedlung der Mucinschicht und der Darmepithelzellschicht mit kommensalen, z. T. auch mit pathogenen Darmkeimen (Swidsinski et al., 2002). Eine mögliche Stimulierung der krankheitsbedingt brach liegen den Produktion dieser körpereigenen antimikrobiellen Schutzstoffe durch Probiotika wäre daher eine neue Wirkqualität dieser Lebendkeimpräparate. Die ersten experi mentellen Untersuchungen zur Wirkung verschiedener physio logischer wie auch pathogener Darmkeime, darunter auch E. coli Nissle 1917 (EcN), auf die intestinale Defensin-Produktion wurden von Jan Wehkamp und Kollegen am Robert-Bosch-Krankenhaus in Stuttgart vorgenommen (Wehkamp et al., 2002, 2004). Hierbei zeigte sich in In-vitro-Untersuchungen mit Zell kulturen von Dickdarmepithelzellen (Caco-2-Zellen), dass der EcN-Stamm im Vergleich zu mehr als 40 anderen getesteten E. coli-stämmen eine außer gewöhnlich starke Stimulierung der Genexpression des induzierbaren Schutzfaktors humanes β-defensin-2 (HBD-2) bewirkte [Abb. 30]. Weiterfüh rende Untersuchungen zeigten, dass nicht nur die Genexpression von HBD-2 durch EcN dosis- und zeitabhängig stimuliert wurde, sondern dass die erhöhte Genexpression auch mit einer vermehrten Synthese des HBD-2-Peptids einherging (Wehkamp et al., 2004). Damit war ein neues Wirkprinzip von EcN entdeckt, das vermutlich für die klinische Wirksamkeit bei Patienten mit Colitis ulcerosa von großer Bedeutung ist. Weitere Unter suchungen zur Aufklärung des molekularen Wirkprinzips führten zu der Erkenntnis, dass die HBD-2-stimulierende Aktivität auf dem Vorhandensein von zwei Komponenten des EcN-Stamms beruht, und zwar dem EcN-eigenen Flagellenapparat (Schlee et al., 2007) sowie dem Modulatorprotein tcpc (Menz et al., 2011). Experimente mit Abb. 30 Wirkung veschiedener pathogener und apathogener E. coli-stämme auf die Induktion der antimikrobiellen Peptide HBD-1, HBD-2, HD-5 und HD-6 : E. coli Nissle 1917 (EcN) zeigt die stärkste Induktion von HBD-2 in humanen CaCo-2 Epithelzellen (Wehkamp et al., 2002, 2004). Abb. 31 Aufbau des Geißel(Flagellen)apparates von E. coli. Als ein Induktor der HBD-2-Synthese in Colonepithelzellen durch E. coli Nissle 1917 wurde das Strukturprotein Flagellin identifiziert, aus dem sich das Geißelfilament zusammensetzt
25 verschiedenen Defektmutanten von EcN ergaben, dass nur EcN-Keime, die ein intaktes Flagellum synthetisieren konnten, in der Lage waren, die HBD-2-Produktion in den Colonepithelzellen zu stimulieren. Als wirksame Komponente wurde das Geißel-Strukturprotein Flagellin iden tifiziert, aus dem die eigentliche Geißel, das sog. Flagellenfilament, aufgebaut ist [Abb. 31]. Weitere Untersuchungen auf molekularer Ebene sollen zeigen, welches die Besonderheiten des EcN-Flagellins sind, die den ungewöhnlich starken HBD-2-induzierenden Effekt bewirken. EcN induziert nicht nur die Expression von humanem β-defensin-2 (HBD-2) und von Cathelicidin LL37 in humanen Colonepithelzellen in vitro [Abb. 30] (Wehkamp et al., 2004), sondern auch die Synthese von Calprotectin im Darm gnotobiotischer Ferkel in vivo (Splichal et al., 2005). Als Konsequenz für die klinische Praxis bedeutet die Induktion von körpereigenen Abwehrstoffen der angeborenen Immunität durch E. coli Nissle 1917 eine generelle Stärkung der antimikrobiellen Abwehrkraft der Darmschleimhaut. Dies ist von besonderer Bedeutung für bestimmte gastroenterologische Erkrankungen, wie die chronisch entzündlichen Darmerkrankungen, bei denen die Synthese antimikrobieller Peptide durch die Mucosa krankheitsbedingt darniederliegt. 3. Die Stärkung des Zusammenhalts des epithelialen Zellverbands: Im gesunden Zustand ist die Translokationsrate (Übertrittfrequenz) von großmolekularen antigenen Nahrungsbestandteilen oder korpuskulären Teilchen, wie Bakterien, Viren und Pilzen, vom Darm ins Körperinnere sehr niedrig und strikt reguliert (Arrieta et al., 2006; Turner, 2009). Dabei wird nur soviel an Translokation erlaubt, wie benötigt wird, um eine gewisse Basisaktivierung ( Hab-acht-Stellung ) des Immunsystems zu gewährleisten. Beim gesunden Menschen gibt es kein überschießendes Wachstum der luminalen Darmmikrobiota, die Permeabilität des Darmepithels für größere Partikel ist stark reduziert und das darmassoziierte Immunsystem verfügt über genügend Makrophagen, regulatorische T-Zellen, IgA-produzierende Plasmazellen und andere Lymphozyten, um einzelne, über das Darmepithel translozierte Mikro organismen abzufangen. Unter bestimmten pathophysiologischen Bedingungen erfolgt jedoch ein erhöhter Transfer luminaler Antigene ins Körper innere. Dies kann verschiedene Ursachen haben [Abb. 32]: eine überschießende Vermehrung von Darmkeimen oder von pathogenen Erregern im Darm bzw. eine reduzierte intraluminale Abtötung/Verdauung von Mikroorganismen und Nahrungsbestandteilen, eine beschädigte Darmschleimhaut mit erhöhter Permeabilität für großmolekulare Antigene und ganze Mikrobenzellen ( Leaky Gut ), eine reduzierte Abwehrleistung des darmassoziierten Immunsystems, z. B. durch einen Mangel an Antikörper-produzierenden Plasmazellen (IgA, IgM) in der Lamina propria. In der Praxis ist das Vorkommen eines Leaky Gut mit erhöhter Permeabilität der Darmschleimhaut wesentlich häufiger anzutreffen als etwa eine überschießende Vermehrung von Darmmikrobiota-Komponenten oder eine drastische Reduzierung der Aktivität des darmassoziierten Immunsystems. Der Leaky Gut ist durch eine pathologisch veränderte epitheliale Barriere mit erhöhter Durchlässigkeit für antigenes Material aus dem Gastrointestinaltrakt gekennzeichnet. Dieser Zustand beruht in vielen Fällen auf einer Reduzierung der Zahl der Zell-Kitt-Proteine in den sog. Tight Junctions (auf deutsch feste Verbindungen ), und damit einer Lockerung des intestinalen Zellverbands. Der Leaky Gut kann nach Schädigung des Darmepithels durch pathogene Erreger und deren Toxine, durch bestimmte Arzneimittel und andere das Epithel schädigende Substanzen sowie durch Bestrahlungen entstehen. Eine erhöhte Permeabilität des Darmepithels kann aber auch Begleiterscheinung bestimmter intestinaler Erkrankungen sein und lässt sich beispielsweise bei Colitis ulcerosa und Morbus Crohn nachweisen
26 IgM IgA IgA Lumen Mucosa Submucosa normal IgM IgA Lymphsystem Lumen Mucosa Submucosa pathologisch Die erhöhte Durchlässigkeit der Darmschleimhaut ( Leaky Gut ), die Zunahme der bakte riellen Trans lokation und in der Folge erhöhte Endotoxinspiegel im Blut werden auch für die progrediente Leberschädigung bei der Alkohol-induzierten Leberzirrhose verantwortlich gemacht. E. coli Nissle 1917 (EcN) kann durch Modulation der gestörten Darmmikrobiota, durch Stärkung der Darmbarriere und Senkung der Infektanfälligkeit, die klinischen Symptome bei Zirrhose-Patienten ( Child Pugh Score ) deutlich bessern. Die dafür ursächlichen molekularen Wirkmechanismen sind noch zu entschlüsseln, um das Infektions risiko bei Zirrhose-Patienten gezielt zu senken und die protektive Wirkung von EcN optimal zu nutzen (Lata et al., 2007). Die zuvor angesprochenen Tight Junctions, die auf der apikalen Seite der Darmepithelzelle die sog. Zonula occludens des Interzellularraums bilden, repräsentieren einen Typ von speziellen Verbindungen zwischen den Epithelzellen. Zu den Interzellularverbindungen gehören verschiedene membran stän dige Multiprotein-Komplexe, die eine Bindung zwischen den Zellmembranen benachbarter Epithelzellen der Darmschleimhaut vermitteln. Die interzellu lären Verbindungen sorgen dafür, dass die Epithelzellen IgM IgA Lymphsystem ➊ reduzierte intraluminale Verdauung / überschießende mikrobielle Vermehrung ➋ beschädigte Schleimhaut-Barriere, erhöhte Permeabilität ( Leaky Gut ) ➌ Abnahme der IgA- und IgM-produzierenden Plasmazellen in der Lamina propria Abb. 32 Regulierte und restriktive Aufnahme von großmolekularen Antigenen und Mikroorganismen aus dem Darmlumen ins Körperinnere (Translokation) unter physiologischen Bedingungen (linkes Bild) und erhöhter Transfer unter pathologischen Bedingungen verschiedener Ursache (rechtes Bild). ➊ ➋ ➌ dicht aneinander liegen und dass das Darmgewebe zusammengehalten wird. Weitere Verbindungen mit Haltefunktion sind die Desmosomen, wobei man zyto logisch zwischen Belt-Desmosomen (Zonula adhaerens) und Spot-Desmosomen (Macula adhaerens) unterscheidet. Sogenannte Adherence Junctions folgen auf die apikal lokalisierten Tight Junctions und stellen einen besonderen Typ an Desmosomen dar, der die Epithelzellen bandartig umgibt. Funktionell dienen alle Arten von Desmosomen in erster Linie der mechanischen Festigkeit des epithelialen Zellverbands. Besondere Interzellularverbindungen sind die Gap Junctions (Nexus), die direkte plasmatische Verbindungen zwischen den Epithelzellen darstellen und daher vor allem kommunikative Aufgaben haben. Der kompliziert aufgebaute Tight Junctional Complex (TJC) gehört zu den Interzellularverbindungen, die räumlich gesehen dem Darmlumen am nächsten sind, da sie sich auf der apikalen Seite der Epithelzellschicht befinden. Der TJC enthält mehrere Klammer - oder Kitt -Proteine, die als Zonula occludens-proteine bezeichnet werden (abgekürzt ZO-1, ZO-2 und ZO-3) [Abb. 33]. Diese Kitt -Proteine sorgen für den festen Zusammenhalt des Zellverbands und die Dichtigkeit der Interzellularspalten zwischen den Epithelzellen, daher die lateinische Bezeichnung Zonula occludens. Die Zahl der Kitt -Proteine vor Ort bestimmt die Dichtigkeit des Interzellularspalts und damit die Un durch lässigkeit des epithelialen Zellverbands. Apikale Membran F- Aktin Basalmembran Matrix Tight Junction Adherence Junction Desmosom Adherence Junction Occludin Claudin JAM ZO-3 Protein X Nectin Afadin E-Cadherin ZO-1 ZO-2 Protein Y β-catenin α-catenin Abb. 33 Bild links: Schematische Darstellung der Interzellularverbindungen von Darmepithelzellen (Tight Junctions, Adherence Junctions, Desmosomen). Bild rechts: Aufbau des Tight Junctional Complex (TJC) auf der apikalen Seite der Darmepithelzellen. Die wichtigsten Kitt -Proteine, die den Interzellularspalt aktiv öffnen oder schließen können, sind dargestellt (nach Miyoshi & Takai, 2005)
27 Tight Junction Zonula adhaerens Macula adhaerens Abb. 34 Elektronenmikroskopische Aufnahme: Benachbarte Darmepithelzellen mit Interzellular spalt, Tight Junction und Desmosomen. Ihre Verteilung innerhalb der Epithelzelle (zytoplasmatische oder mem branständige Lokalisierung wird durch ein Netzwerk komplexer Signalkaskaden reguliert, wobei Sub typen der Proteinkinase C (PKC) von besonderer Be deutung sind (Hering et al., 2014; Zyrek et al., 2007). Im Gegensatz zu den Ad herence Junctions bzw. Des mosomen haben die Tight Junctions dynamische Funktionen zu erfüllen [Abb. 34]. Ihre Tightness reguliert den Einstrom von Elektrolyten und korpuskulären Partikeln, wie Bakte rien, Viren oder Pilze, ins Körperinnere. Im gesunden Zustand sind die Tight Junctions völlig dicht und es findet so gut wie kein Austausch von Substanzen oder Organismen über den Interzellularspalt statt. Bestimmte Durchfallerreger, wie enteropathogene E. coli-stämme (EPEC), sind in der Lage, durch die Ausschüttung von Toxinen oder Signalstoffen die Festigkeit der Tight Junctions zu lockern und sich so eine Zugangspforte in den menschlichen Körper zu öffnen. Interessanterweise ist E. coli Nissle 1917 (EcN) in der Lage, die durch den Angriff enteropathogener Erreger gelockerten Tight Junction-Verbindungen wieder zu festigen und damit die Integrität des Darmepithels wieder herzustellen (Trebichavsky et al., 2010). Wie M. Alexander Schmidt und Mitarbeiter am Institut für Infektiologie des Universitätsklinikums Münster unter Verwendung der sog. DNA-Microarray-Technik zeigen konnten (Cichon et al., 2004; Zyrek et al., 2007), bewirkt eine Co-Inkubation von Darmepithelzellen (T84-Zellen) mit EcN eine zeitabhängige Induktion der Genexpression für Proteine, die an Aufbau und Zusammenhalt von Tight Junctions bzw. Desmosomen beteiligt sind. Insgesamt führt der Kontakt der Epithelzellen mit EcN zu einer Veränderung der Expression von über 300 Genen, wobei sowohl Herauf- als auch Herunter regu lierungen der Gen aktivität verschiedener epithelialer Erbfaktoren fest gestellt wurden. In den verwendeten T84-Zellen wurde eine erhöhte Genexpression für die Tight Junction- bzw. Desmosomen-Proteine ZO-2 und Pinin nach gewiesen, die nach 120 Minuten Inkubationszeit ein Maximum erreichte (Cichon et al., 2004). Weiterführende Untersuchungen derselben Arbeitsgruppe (Zyrek et al., 2007), die sich mit der molekularen Regulation der ZO-2-Expression in den Epithelzellen befassten, konnten mit hochauflösenden mikroskopischen Techniken unter Verwendung von spezifischen Fluoreszenz-markierten Antikörpern [Abb. 35] und proteinchemischen Analysen nachweisen, dass EcN eine durch die Infektion mit enteropathogenen E. coli (EPEC) geschädigte epitheliale Barriere wieder restaurieren kann. Dabei kommt es zu einer Umverteilung des ZO- 2-Proteins vom Zytoplasma an die Zellmembran der Epithelzelle. Dieser stabilisierende Effekt von EcN konnte in verschiedenen Zellkulturversuchen sowohl für eine prophylaktische als auch für eine therapeutische Gabe gezeigt werden. In T84 Epithelzellen kann die durch E. coli Nissle 1917 bewirkte Ver besserung einer gestörten Barrierefunktion auch durch die Transfektion der Zellen mit bestimmten regulatorischen micrornas (mirnas) induziert werden (Veltman et al., 2012). Abb. 35 Darstellung der Induktion der ZO-2-Genexpression in T84-Epithelzellen und der Einlagerung des ZO-2-Proteins in die Tight Junctions. Die Anfärbung mit ZO-2-spezifischen fluoreszie ren - den Antikörpern zeigt (Kontrolle ohne Bakterien), dass das ZO-2-Protein sich überwiegend in den Membranen der Epithelzellen befindet. Dies wird sichtbar durch die starke hellrote Färbung der Zellumrisse. Eine 120-minütige Inkubation mit EcN (E. coli Nissle 1917) führte zu keiner Veränderung der Distribution des ZO-2-Proteins. Eine 120-minütige Inkubation mit enteropathogenen E. coli (EPEC) führte demgegenüber zu einer Umverteilung von ZO-2 und einer Reduzierung der Dichtigkeit der Tight Junctions. Bei gleichzeitiger Inkubation von EPEC und EcN konnten die EPEC-Bakterien ihre schädliche Wirkung nicht entfalten (nach Zyrek et al., 2007)
Bedeutung von EPEC, ETEC und EHEC. 5. Hygienetag Köln Sabine Messler
 Bedeutung von EPEC, ETEC und EHEC 5. Hygienetag Köln Sabine Messler 22.10.2014 PathogenitätsfaktorendarmpathogenerE.coli E.coli Pathovar Krankheitsbild Pathogenitätsfaktor (codierendes Gen) Enterohämorrhagische
Bedeutung von EPEC, ETEC und EHEC 5. Hygienetag Köln Sabine Messler 22.10.2014 PathogenitätsfaktorendarmpathogenerE.coli E.coli Pathovar Krankheitsbild Pathogenitätsfaktor (codierendes Gen) Enterohämorrhagische
Landesamt für Gesundheit und Soziales
 Landesamt für Gesundheit und Soziales 2 A K T U E L L Epidemiologische Informationen Deutschland für das Land Berlin herausgegeben am 9.12.211 In dieser Ausgabe: E. coli-enteritiden Aktuelle Entwicklungen
Landesamt für Gesundheit und Soziales 2 A K T U E L L Epidemiologische Informationen Deutschland für das Land Berlin herausgegeben am 9.12.211 In dieser Ausgabe: E. coli-enteritiden Aktuelle Entwicklungen
Escherichia coli (E. coli)
 Escherichia coli (E. coli) 1885 als Bacterium coli commune beschrieben Theodor Escherich, 1857-1911 1 1 Escherichia coli (E. coli) Enterobakterium, normaler Bestandteil der Darmflora von Mensch und Tier
Escherichia coli (E. coli) 1885 als Bacterium coli commune beschrieben Theodor Escherich, 1857-1911 1 1 Escherichia coli (E. coli) Enterobakterium, normaler Bestandteil der Darmflora von Mensch und Tier
1. Einleitung Stand der Forschung Enteropathogene E. coli. 1. Einleitung
 1. Einleitung Escherichia coli (E. coli) ist der häufigste Erreger bakterieller Infektionen beim Menschen. Fakultativ pathogene Stämme von E. coli sind Bestandteil der physiologischen Darmflora. Sie können
1. Einleitung Escherichia coli (E. coli) ist der häufigste Erreger bakterieller Infektionen beim Menschen. Fakultativ pathogene Stämme von E. coli sind Bestandteil der physiologischen Darmflora. Sie können
Klebsiella oxytoca als Ursache der hämorrhagischen
 Klebsiella oxytoca als Ursache der hämorrhagischen Antibiotikacolitis a.o. Univ. Prof. Dr. Christoph Högenauer, Abteilung für Gastroenterologie und Hepatologie, Universitätsklinik für Innere Medizin Graz.
Klebsiella oxytoca als Ursache der hämorrhagischen Antibiotikacolitis a.o. Univ. Prof. Dr. Christoph Högenauer, Abteilung für Gastroenterologie und Hepatologie, Universitätsklinik für Innere Medizin Graz.
Auswertung der Surveillance von darmpathogener Escherichia coli Hélène Englund
 Auswertung der Surveillance von darmpathogener Escherichia coli Hélène Englund helene.englund@smi.se Hintergrund Escherichia coli Teil der normalen humanen Darmflora Stämme mit Virulenzfaktoren können
Auswertung der Surveillance von darmpathogener Escherichia coli Hélène Englund helene.englund@smi.se Hintergrund Escherichia coli Teil der normalen humanen Darmflora Stämme mit Virulenzfaktoren können
Treffen Hygiene Netzwerk Bern 07. Mai Agenda. Hygienisch relevante Erreger. 07. Mai 2014 von 13:30 16:30 Uhr.
 10. Treffen Hygiene Netzwerk Bern 07. Mai 2014 Agenda 07. Mai 2014 von 13:30 16:30 Uhr Traktandenliste Begrüssung und Programm Informationen zum Netzwerk Organisatorisches Fachlicher Input: Hygienisch
10. Treffen Hygiene Netzwerk Bern 07. Mai 2014 Agenda 07. Mai 2014 von 13:30 16:30 Uhr Traktandenliste Begrüssung und Programm Informationen zum Netzwerk Organisatorisches Fachlicher Input: Hygienisch
Übersicht. Yersiniose Shigellose
 Übersicht Yersiniose Shigellose Statistik-Erkrankungsfälle in Deutschland Erkrankung 2013 2014 2015 Yersiniose 2.590 2.485 2.747 Shigellose 578 552 571 Quelle: RKI, Epid. Bulletin Nr.3; Datenstand: 25.01.2016
Übersicht Yersiniose Shigellose Statistik-Erkrankungsfälle in Deutschland Erkrankung 2013 2014 2015 Yersiniose 2.590 2.485 2.747 Shigellose 578 552 571 Quelle: RKI, Epid. Bulletin Nr.3; Datenstand: 25.01.2016
Kolonisation oder Infektion?
 Kolonisation oder Infektion? Die physiologische bakterielle Besiedlung des Menschen Nase: Staphylococcus aureus Staphylococcus epidermidis Mund/Rachen: Streptococcus mutans Streptococcus pneumoniae Neisseria
Kolonisation oder Infektion? Die physiologische bakterielle Besiedlung des Menschen Nase: Staphylococcus aureus Staphylococcus epidermidis Mund/Rachen: Streptococcus mutans Streptococcus pneumoniae Neisseria
Geschichte der Probiotischen Medizin
 Geschichte der Probiotischen Medizin Mag. Anita Frauwallner CEO Institut Allergosan Präsidentin der ÖPROM Österreichische Gesellschaft für Probiotische Medizin ÖPROM Österreichische Gesellschaft für probiotische
Geschichte der Probiotischen Medizin Mag. Anita Frauwallner CEO Institut Allergosan Präsidentin der ÖPROM Österreichische Gesellschaft für Probiotische Medizin ÖPROM Österreichische Gesellschaft für probiotische
EHEC droht eine neue Gefahr oder schon wieder vergessen? Quelle: Akif Ciftci & Karsten Peters
 EHEC droht eine neue Gefahr oder schon wieder vergessen? Quelle: Akif Ciftci & Karsten Peters Inhalt: Verlauf der HUS-Epidemie 2011 Hämolytisch-urämisches Syndrom (HUS) Problematik der Therapie Escherichia
EHEC droht eine neue Gefahr oder schon wieder vergessen? Quelle: Akif Ciftci & Karsten Peters Inhalt: Verlauf der HUS-Epidemie 2011 Hämolytisch-urämisches Syndrom (HUS) Problematik der Therapie Escherichia
Shigatoxin-bildende Escherichia coli (STEC)
 Institut für Lebensmittelsicherheit und -hygiene Shigatoxin-bildende Escherichia coli (STEC) Roger Stephan, Claudio Zweifel Institut für Lebensmittelsicherheit und hygiene Nationales Referenzlabor für
Institut für Lebensmittelsicherheit und -hygiene Shigatoxin-bildende Escherichia coli (STEC) Roger Stephan, Claudio Zweifel Institut für Lebensmittelsicherheit und hygiene Nationales Referenzlabor für
ANGABEN ZUM EMPFÄNGERORGANISMUS 1
 ANGABEN ZUM EMPFÄNGERORGANISMUS 1 I. CHARAKTERISIERUNG DES EMPFÄNGERORGANISMUS 1. Vollständiger Name, taxonomischer Name bei Mikroorganismen sowie Zellkulturen (i.s. von 3 Nr. 1 und 1a GenTSV) Ursprung
ANGABEN ZUM EMPFÄNGERORGANISMUS 1 I. CHARAKTERISIERUNG DES EMPFÄNGERORGANISMUS 1. Vollständiger Name, taxonomischer Name bei Mikroorganismen sowie Zellkulturen (i.s. von 3 Nr. 1 und 1a GenTSV) Ursprung
Enterohämorrhagische Escherichia coli (EHEC)
 Enterohämorrhagische Escherichia coli (EHEC) Worterklärung enteron = Darm (i.s. Dünndarm) häm = Blut rhagie = fließend, strömend Escherichia coli = Bakterium (s.u.) Bei EHEC handelt es sich um eine Gastroenteritis,
Enterohämorrhagische Escherichia coli (EHEC) Worterklärung enteron = Darm (i.s. Dünndarm) häm = Blut rhagie = fließend, strömend Escherichia coli = Bakterium (s.u.) Bei EHEC handelt es sich um eine Gastroenteritis,
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS MUTAFLOR Suspension 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Suspension enthält als Wirkstoff: Bakterienkultur
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS MUTAFLOR Suspension 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Suspension enthält als Wirkstoff: Bakterienkultur
Stammspezifische Eigenschaften und Wirkprinzipien von Escherichia coli Stamm Nissle 1917
 Hintergrundinformation Stammspezifische Eigenschaften und Wirkprinzipien von Escherichia coli Stamm Nissle 1917 Das natürliche Darmbakterium Escherichia coli Stamm Nissle 1917 (EcN) wurde umfangreich erforscht
Hintergrundinformation Stammspezifische Eigenschaften und Wirkprinzipien von Escherichia coli Stamm Nissle 1917 Das natürliche Darmbakterium Escherichia coli Stamm Nissle 1917 (EcN) wurde umfangreich erforscht
Prophylaxe und Therapie der Reisediarrhoe H. Pichler
 Aus der Universitätsklinik für Chemotherapie Vorstand: Prof. Dr. K. H. Spitzy Prophylaxe und Therapie der Reisediarrhoe H. Pichler Bevor man auf Prophylaxe und Therapie der Reisediarrhoe eingeht, muß zuerst
Aus der Universitätsklinik für Chemotherapie Vorstand: Prof. Dr. K. H. Spitzy Prophylaxe und Therapie der Reisediarrhoe H. Pichler Bevor man auf Prophylaxe und Therapie der Reisediarrhoe eingeht, muß zuerst
Infektiöse Gastroenteritis
 Infektiöse Gastroenteritis Epidemiologie der Gastroenteritis Eine der häufigsten Ursachen für Morbidität und Mortalität der Weltbevölkerung 5 Mio. Kinder versterben jährlich an Diarrhoe 1997 in Deutschland
Infektiöse Gastroenteritis Epidemiologie der Gastroenteritis Eine der häufigsten Ursachen für Morbidität und Mortalität der Weltbevölkerung 5 Mio. Kinder versterben jährlich an Diarrhoe 1997 in Deutschland
DIE ZEIT IST REIF- IMPFEN GEGEN DIE ÖDEMKRANKHEIT
 DIE ZEIT IST REIF- IMPFEN GEGEN DIE ÖDEMKRANKHEIT Schweinetag Sachsen-Anhalt Iden 28.10.2014 Dr. Kathrin Lillie-Jaschniski IDT Biologika GmbH Gliederung Diagnose Prophylaxe/Therapie Feldstudien Zusammenfassung
DIE ZEIT IST REIF- IMPFEN GEGEN DIE ÖDEMKRANKHEIT Schweinetag Sachsen-Anhalt Iden 28.10.2014 Dr. Kathrin Lillie-Jaschniski IDT Biologika GmbH Gliederung Diagnose Prophylaxe/Therapie Feldstudien Zusammenfassung
Beim Neugeborenen ist die Darmoberfläche steril. Wie es kommt, dass es bei dem anschließenden Bakterienwachstum im Darm nicht zu Abwehr- und
 Beim Neugeborenen ist die Darmoberfläche steril. Wie es kommt, dass es bei dem anschließenden Bakterienwachstum im Darm nicht zu Abwehr- und Entzündungsreaktionen durch das Darmimmunsystem kommt, war bislang
Beim Neugeborenen ist die Darmoberfläche steril. Wie es kommt, dass es bei dem anschließenden Bakterienwachstum im Darm nicht zu Abwehr- und Entzündungsreaktionen durch das Darmimmunsystem kommt, war bislang
zur Unterstützung des Magen-Darm-Traktes
 zur Unterstützung des Magen-Darm-Traktes Die Wirkstoffe Prebiotika bzw. Ballaststoffe aus Apfelfasern, Chicorée-Wurzel und Maltodextrin Probiotika von Lactobacillus Rhamnosus Lactobacillus Acidophilus
zur Unterstützung des Magen-Darm-Traktes Die Wirkstoffe Prebiotika bzw. Ballaststoffe aus Apfelfasern, Chicorée-Wurzel und Maltodextrin Probiotika von Lactobacillus Rhamnosus Lactobacillus Acidophilus
Geliehene Gene. Vielfalt und Evolution darmpathogener Escherichia coli und Herausforderungen an deren Nachweis in Lebensmitteln
 e.coli Geliehene Gene Vielfalt und Evolution darmpathogener Escherichia coli und Herausforderungen an deren Nachweis in Lebensmitteln PD Dr. Lothar Beutin Bundesinstitut für Risikobewertung, Nationales
e.coli Geliehene Gene Vielfalt und Evolution darmpathogener Escherichia coli und Herausforderungen an deren Nachweis in Lebensmitteln PD Dr. Lothar Beutin Bundesinstitut für Risikobewertung, Nationales
HÄMOLYTISCH-URÄMISCHES SYNDROM (HUS)
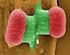 HÄMOLYTISCH-URÄMISCHES SYNDROM (HUS) DEFINITION eine Erkrankung der kleinen Blutgefäße, der Blutzellen und der Nieren seltene Krankheit, die vorwiegend bei Säuglingen, Kleinkindern (zwischen einem und
HÄMOLYTISCH-URÄMISCHES SYNDROM (HUS) DEFINITION eine Erkrankung der kleinen Blutgefäße, der Blutzellen und der Nieren seltene Krankheit, die vorwiegend bei Säuglingen, Kleinkindern (zwischen einem und
Labortests für Ihre Gesundheit. Warum und wann Antibiotika? 07
 Labortests für Ihre Gesundheit Warum und wann Antibiotika? 07 01IPF Labortests für Ihre Gesundheit Warum und wann Antibiotika? Infektionskrankheiten und ihre Behandlung heute und morgen Heutzutage ist
Labortests für Ihre Gesundheit Warum und wann Antibiotika? 07 01IPF Labortests für Ihre Gesundheit Warum und wann Antibiotika? Infektionskrankheiten und ihre Behandlung heute und morgen Heutzutage ist
Grundlagen der Physiologie
 Grundlagen der Physiologie Humanpathogene Mikroben und Viren www.icbm.de/pmbio Keimzahlen der menschlichen Bakterienflora Körperteil Anzahl Bemerkung Haut 10 2-10 4 cm -2 Speichel 10 9 ml -1 Zahn-Plaque
Grundlagen der Physiologie Humanpathogene Mikroben und Viren www.icbm.de/pmbio Keimzahlen der menschlichen Bakterienflora Körperteil Anzahl Bemerkung Haut 10 2-10 4 cm -2 Speichel 10 9 ml -1 Zahn-Plaque
ESBL ESBL. Dies bedeutet eine Resistenz gegenüber Antibiotika! Übersicht. Übersicht. Was genau? Besiedlung / Infektion. Ursachen. Infektion.
 Besiedlung / Extended Spectrum Beta Lactamasen Zu deutsch: Diese Darmbakterien bilden von sich aus ein: extended spectrum = ein erweitertes Spektrum, einen erweiterten Bereich von Beta Lactamasen aus.
Besiedlung / Extended Spectrum Beta Lactamasen Zu deutsch: Diese Darmbakterien bilden von sich aus ein: extended spectrum = ein erweitertes Spektrum, einen erweiterten Bereich von Beta Lactamasen aus.
Ich möchte Ihnen zeigen, wie Sie einen Mittelweg finden.
 Liebe Leserin, lieber Leser, ich freue mich, dass Sie sich für eine Darmsanierung interessieren und möchte Sie gerne dabei unterstützen, Ihre Gesundheit zu verbessern und Ihr Wohlbefinden zu steigern.
Liebe Leserin, lieber Leser, ich freue mich, dass Sie sich für eine Darmsanierung interessieren und möchte Sie gerne dabei unterstützen, Ihre Gesundheit zu verbessern und Ihr Wohlbefinden zu steigern.
ESBL PEG Rheinland 2014
 ESBL PEG Rheinland 2014 ESBL = Extended-Spectrum Beta- Laktamase Keime aus der Familie der Enterobakterien (z.b. E. coli, Salmonella, Klebsiella, Enterobacter, Proteus, Shigella, Yersinia u.a.) erzeugen
ESBL PEG Rheinland 2014 ESBL = Extended-Spectrum Beta- Laktamase Keime aus der Familie der Enterobakterien (z.b. E. coli, Salmonella, Klebsiella, Enterobacter, Proteus, Shigella, Yersinia u.a.) erzeugen
B a k t e r i e n & V i r e n M a t e r i a l 1
 B a k t e r i e n & V i r e n M a t e r i a l 1 Ziele Wir wollen Bakterien & Viren kennen lernen. Uns interessiert zudem die Frage, wo sich Bakterien finden lassen. Damit wir Bakterien besser sehen können,
B a k t e r i e n & V i r e n M a t e r i a l 1 Ziele Wir wollen Bakterien & Viren kennen lernen. Uns interessiert zudem die Frage, wo sich Bakterien finden lassen. Damit wir Bakterien besser sehen können,
BfR stuft den massiven Einsatz von Antibiotika in der Tierproduktion als bedenklich ein
 Antibiotikaresistente Keime auf Hähnchenfleisch-Proben sind nichts Neues BfR stuft den massiven Einsatz von Antibiotika in der Tierproduktion als bedenklich ein Berlin (10. Januar 2012) - Eine Stichprobe
Antibiotikaresistente Keime auf Hähnchenfleisch-Proben sind nichts Neues BfR stuft den massiven Einsatz von Antibiotika in der Tierproduktion als bedenklich ein Berlin (10. Januar 2012) - Eine Stichprobe
Aufgabe 1 Viren und Bakterien können Infektionskrankheiten verursachen. Was unterscheidet Viren von
 10 Mikrobiologie/Stuhlanalysen Aufgabe 1 Viren und Bakterien können Infektionskrankheiten verursachen. Was unterscheidet Viren von Bakterien? Aufgabe 2 Erreger und Infektionskrankheiten: Ergänzen Sie die
10 Mikrobiologie/Stuhlanalysen Aufgabe 1 Viren und Bakterien können Infektionskrankheiten verursachen. Was unterscheidet Viren von Bakterien? Aufgabe 2 Erreger und Infektionskrankheiten: Ergänzen Sie die
Zusätzliche Informationen
 MILCHSÄUREKULTUREN MINERALSTOFFE 6 Milchsäure Anleitung LP Die Lernenden wissen, dass im Körper und in Nahrungsmitteln verschiedene Bakterien vorkommen und dass Nahrungsmittel damit angereichert werden.
MILCHSÄUREKULTUREN MINERALSTOFFE 6 Milchsäure Anleitung LP Die Lernenden wissen, dass im Körper und in Nahrungsmitteln verschiedene Bakterien vorkommen und dass Nahrungsmittel damit angereichert werden.
Entwicklung einer Multiplex-PCR zum Nachweis Enteropathogener Escherichia coli
 Charité-Universitätsmedizin Berlin Campus Benjamin Franklin Aus dem Institut für Infektionsmedizin Geschäftsführender Direktor Prof. Dr. med. Dr. h.c. Helmut Hahn Abteilung: Medizinische Mikrobiologie
Charité-Universitätsmedizin Berlin Campus Benjamin Franklin Aus dem Institut für Infektionsmedizin Geschäftsführender Direktor Prof. Dr. med. Dr. h.c. Helmut Hahn Abteilung: Medizinische Mikrobiologie
Genetik der Bakteriophagen
 Phagen Genetik der Bakteriophagen Bakteriophagen: Viren der Bakterien Virus: Giftstoff Manche der wichtigsten und grundlegenden genetischen Informationen resultierten aus Studien mit den E. coli Phagen
Phagen Genetik der Bakteriophagen Bakteriophagen: Viren der Bakterien Virus: Giftstoff Manche der wichtigsten und grundlegenden genetischen Informationen resultierten aus Studien mit den E. coli Phagen
INTEST.pro. Die erste umfassende Darmflora-Analyse mit individuellen Empfehlungen zur Steigerung der Lebensqualität
 INTEST.pro Die erste umfassende Darmflora-Analyse mit individuellen Empfehlungen zur Steigerung der Lebensqualität Kein Organ ist so wichtig für das Wohlbefinden wie der Darm. Übergewicht, Darmbeschwerden,
INTEST.pro Die erste umfassende Darmflora-Analyse mit individuellen Empfehlungen zur Steigerung der Lebensqualität Kein Organ ist so wichtig für das Wohlbefinden wie der Darm. Übergewicht, Darmbeschwerden,
Stellungnahme der ZKBS zu gentechnischen Arbeiten mit enterohämorrhagischen Escherichia coli Stämmen (EHEC)
 Az. 6790-10-57 Geänderte Fassung von September 2017 Stellungnahme der ZKBS zu gentechnischen Arbeiten mit enterohämorrhagischen Escherichia coli Stämmen (EHEC) 1. Einführung Escherichia coli (E. coli)
Az. 6790-10-57 Geänderte Fassung von September 2017 Stellungnahme der ZKBS zu gentechnischen Arbeiten mit enterohämorrhagischen Escherichia coli Stämmen (EHEC) 1. Einführung Escherichia coli (E. coli)
Empfehlungen zur Verhütung und Bekämpfung von bakteriellen Darminfektionen beim Menschen im Freistaat Sachsen Stand: September 2017.
 Empfehlungen zur Verhütung und Bekämpfung von bakteriellen Darminfektionen beim Menschen im Freistaat Sachsen Stand: September 2017 Erreger Salmonella enterica mit ca. 2.500 Serovaren, Sonderregelungen
Empfehlungen zur Verhütung und Bekämpfung von bakteriellen Darminfektionen beim Menschen im Freistaat Sachsen Stand: September 2017 Erreger Salmonella enterica mit ca. 2.500 Serovaren, Sonderregelungen
AntibiotikaResistenzmechanismen
 AntibiotikaResistenzmechanismen 20. Oktober 2011 Patricia Kahl Charlotte Schäfer Definition: Antimikrobielle Medikamentenresistenz Erworbene Fähigkeit eines Mikroorganismus, der Wirkung einer chemotherapeutisch
AntibiotikaResistenzmechanismen 20. Oktober 2011 Patricia Kahl Charlotte Schäfer Definition: Antimikrobielle Medikamentenresistenz Erworbene Fähigkeit eines Mikroorganismus, der Wirkung einer chemotherapeutisch
Vorlesungsthemen Mikrobiologie
 Vorlesungsthemen Mikrobiologie 1. Einführung in die Mikrobiologie B. Bukau 2. Zellaufbau von Prokaryoten B. Bukau 3. Bakterielles Wachstum und Differenzierung B. Bukau 4. Bakterielle Genetik und Evolution
Vorlesungsthemen Mikrobiologie 1. Einführung in die Mikrobiologie B. Bukau 2. Zellaufbau von Prokaryoten B. Bukau 3. Bakterielles Wachstum und Differenzierung B. Bukau 4. Bakterielle Genetik und Evolution
49. Fortbildungsveranstaltung für Hals-Nasen- Ohrenärzte
 Multiresistente Keime: Mikrobiologie, Hygiene Autor: Prof. Dr. med. Wolfgang Pfister, Universitätsklinikum Jena, Institut für Medizinische Mikrobiologie, Erlanger Allee 101, 07747 Jena, E-Mail: Wolfgang.Pfister@med.uni-jena.de
Multiresistente Keime: Mikrobiologie, Hygiene Autor: Prof. Dr. med. Wolfgang Pfister, Universitätsklinikum Jena, Institut für Medizinische Mikrobiologie, Erlanger Allee 101, 07747 Jena, E-Mail: Wolfgang.Pfister@med.uni-jena.de
Das intestinale Mikrobiomein Einstieg ins Thema
 Steiermärkische Krankenanstaltengesellschaft m.b.h. Institut für Krankenhaushygiene und Mikrobiologie Hygiene Bakteriologie Serologie Molekularbiologie Tbc-Diagnostik Mykologie Parasitologie Ärztlicher
Steiermärkische Krankenanstaltengesellschaft m.b.h. Institut für Krankenhaushygiene und Mikrobiologie Hygiene Bakteriologie Serologie Molekularbiologie Tbc-Diagnostik Mykologie Parasitologie Ärztlicher
KyberMetabolic. Neue Wege um Übergewicht und Diabetes zu bekämpfen
 KyberMetabolic Neue Wege um Übergewicht und Diabetes zu bekämpfen Leiden Leiden Sie an Übergewicht, Fettstoffwechselstörungen, Bluthochdruck, Typ-2-Diabetes? Sie an Diabetes vom Typ 2 und /oder lästigem
KyberMetabolic Neue Wege um Übergewicht und Diabetes zu bekämpfen Leiden Leiden Sie an Übergewicht, Fettstoffwechselstörungen, Bluthochdruck, Typ-2-Diabetes? Sie an Diabetes vom Typ 2 und /oder lästigem
Phagen. Extra Anforderung
 Phagen Extra Anforderung Genetik der Bakteriophagen Bakteriophagen: Viren der Bakterien Virus: Giftstoff Manche der wichtigsten und grundlegenden genetischen Informationen resultierten aus Studien mit
Phagen Extra Anforderung Genetik der Bakteriophagen Bakteriophagen: Viren der Bakterien Virus: Giftstoff Manche der wichtigsten und grundlegenden genetischen Informationen resultierten aus Studien mit
Antibiotika schützen Ihre Gesundheit. Schützen Sie Ihren Darm!
 Antibiotika schützen Ihre Gesundheit. Schützen Sie Ihren Darm! Manchmal sind Antibiotika unvermeidlich Bakterien sind überall. Viele sind gut für uns; so zum Beispiel diejenigen, die unseren Darm besiedeln
Antibiotika schützen Ihre Gesundheit. Schützen Sie Ihren Darm! Manchmal sind Antibiotika unvermeidlich Bakterien sind überall. Viele sind gut für uns; so zum Beispiel diejenigen, die unseren Darm besiedeln
- I - INHALTSVERZEICHNIS. Inhaltsverzeichnis Verzeichnis der Abkürzungen 1. EINLEITUNG UND PROBLEMSTELLUNG 1
 - I - INHALTSVERZEICHNIS Seite Inhaltsverzeichnis Verzeichnis der Abkürzungen I - V VI - VII 1. EINLEITUNG UND PROBLEMSTELLUNG 1 2. SCHRIFTTUM 2 2.1 Direktvermarktung 2 2.1.1 Bedeutung 2 2.1.2 Gesetzliche
- I - INHALTSVERZEICHNIS Seite Inhaltsverzeichnis Verzeichnis der Abkürzungen I - V VI - VII 1. EINLEITUNG UND PROBLEMSTELLUNG 1 2. SCHRIFTTUM 2 2.1 Direktvermarktung 2 2.1.1 Bedeutung 2 2.1.2 Gesetzliche
Epidemiologisches Bulletin
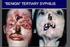 Epidemiologisches Bulletin 25. August 2 /Nr. 34 aktuelle daten und informationen zu infektionskrankheiten und public health Wichtige Infektionskrankheiten in Deutschland zur Situation im Jahr 1999 Teil
Epidemiologisches Bulletin 25. August 2 /Nr. 34 aktuelle daten und informationen zu infektionskrankheiten und public health Wichtige Infektionskrankheiten in Deutschland zur Situation im Jahr 1999 Teil
Vorlesungsthemen Mikrobiologie
 Vorlesungsthemen Mikrobiologie 1. Einführung in die Mikrobiologie B. Bukau 2. Zellaufbau von Prokaryoten B. Bukau 3. Bakterielles Wachstum und Differenzierung B. Bukau 4. Bakterielle Genetik und Evolution
Vorlesungsthemen Mikrobiologie 1. Einführung in die Mikrobiologie B. Bukau 2. Zellaufbau von Prokaryoten B. Bukau 3. Bakterielles Wachstum und Differenzierung B. Bukau 4. Bakterielle Genetik und Evolution
Gentechnologie für Einsteiger
 T. A. Brown Gentechnologie für Einsteiger 3. Auflage Aus dem Englischen übersetzt von Sebastian Vogel Spektrum Akademischer Verlag Heidelberg Berlin Vorwort Vorwort zur dritten englischen Auflage Vorwort
T. A. Brown Gentechnologie für Einsteiger 3. Auflage Aus dem Englischen übersetzt von Sebastian Vogel Spektrum Akademischer Verlag Heidelberg Berlin Vorwort Vorwort zur dritten englischen Auflage Vorwort
Gastroenteritis Gastrointestinale Infektionen
 Infektiöse Gastroenteritis Gastrointestinale Infektionen OA Dr. M. Kutilek Zentralklinikum St. Pölten Laut WHO Schätzungen leiden jährlich 900 Mio.Menschen an infektiösen Durchfallserkrankungen 8 15 Mio
Infektiöse Gastroenteritis Gastrointestinale Infektionen OA Dr. M. Kutilek Zentralklinikum St. Pölten Laut WHO Schätzungen leiden jährlich 900 Mio.Menschen an infektiösen Durchfallserkrankungen 8 15 Mio
Entyvio (Vedolizumab) Der darmselektiv wirkende Integrin-Hemmer bei Colitis ulcerosa und Morbus Crohn 1 4
 Entyvio (Vedolizumab) Der darmselektiv wirkende Integrin-Hemmer bei Colitis ulcerosa und Morbus Crohn 1 4 INTERAKTIVES PDF Gelangen Sie per Klick auf die gewünschte Seite. NUR FÜR ACROBAT Chronisch-entzündliche
Entyvio (Vedolizumab) Der darmselektiv wirkende Integrin-Hemmer bei Colitis ulcerosa und Morbus Crohn 1 4 INTERAKTIVES PDF Gelangen Sie per Klick auf die gewünschte Seite. NUR FÜR ACROBAT Chronisch-entzündliche
Rheinisch-Westfälische Akademie der Wissenschaften
 Rheinisch-Westfälische Akademie der Wissenschaften VORTRÄGE N328 PETER STARLING ER Transposition: Ein neuer Mechanismus zur Evolution KLAUS RAJEWSKY Antikörperdiversität und Netzwerkregulation im Immunsystem
Rheinisch-Westfälische Akademie der Wissenschaften VORTRÄGE N328 PETER STARLING ER Transposition: Ein neuer Mechanismus zur Evolution KLAUS RAJEWSKY Antikörperdiversität und Netzwerkregulation im Immunsystem
ZEOFLORIN. Für Ihre Darmflora
 ZEOFLORIN Für Ihre Darmflora Zeoflorin Stimulierung der Eigenheilkräfte, da 80 % des Immunsystems des Menschen im Darm angeregt werden. Bildung der wertvollen Milchsäure damit Verhinderung von anaeroben
ZEOFLORIN Für Ihre Darmflora Zeoflorin Stimulierung der Eigenheilkräfte, da 80 % des Immunsystems des Menschen im Darm angeregt werden. Bildung der wertvollen Milchsäure damit Verhinderung von anaeroben
Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben?
 Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben? 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung
Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben? 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung
Salmonellen. Campylobacter
 Textvorschläge des Robert Koch-Instituts zur Verwendung bei öffentlichen Warnungen und Informationen zu Lebensmitteln, von denen eine Gesundheitsgefährdung von Verbraucherinnen und Verbrauchern durch mikrobielle
Textvorschläge des Robert Koch-Instituts zur Verwendung bei öffentlichen Warnungen und Informationen zu Lebensmitteln, von denen eine Gesundheitsgefährdung von Verbraucherinnen und Verbrauchern durch mikrobielle
Traditionelle und innovative Impfstoffentwicklung
 Traditionelle und innovative Impfstoffentwicklung Reingard.grabherr@boku.ac.at Traditionelle Impfstoffentwicklung Traditionelle Impfstoffentwicklung Louis Pasteur in his laboratory, painting by A. Edelfeldt
Traditionelle und innovative Impfstoffentwicklung Reingard.grabherr@boku.ac.at Traditionelle Impfstoffentwicklung Traditionelle Impfstoffentwicklung Louis Pasteur in his laboratory, painting by A. Edelfeldt
Infektionsübertragung in der Endoskopie. Priv.-Doz. Dr. med. Florian Daxböck FA für Hygiene und Mikrobiologie
 Infektionsübertragung in der Endoskopie Priv.-Doz. Dr. med. Florian Daxböck FA für Hygiene und Mikrobiologie Infektionsquellen Anderer Patient (mangelhafte Reinigung, Desinfektion) Letztes Spülwasser der
Infektionsübertragung in der Endoskopie Priv.-Doz. Dr. med. Florian Daxböck FA für Hygiene und Mikrobiologie Infektionsquellen Anderer Patient (mangelhafte Reinigung, Desinfektion) Letztes Spülwasser der
BactiGuard Infektionsschutz Katheter. ein gewaltiger Schritt in Richtung Infektionskontrolle
 BactiGuard Infektionsschutz Katheter ein gewaltiger Schritt in Richtung Infektionskontrolle Innovationen Exklusivvertrieb bei Menke-Med DIE HERAUSFORDERUNG Infektionen im Krankenhausbereich die vierthäufigste
BactiGuard Infektionsschutz Katheter ein gewaltiger Schritt in Richtung Infektionskontrolle Innovationen Exklusivvertrieb bei Menke-Med DIE HERAUSFORDERUNG Infektionen im Krankenhausbereich die vierthäufigste
Defensine: Können wir sie in der Therapie einsetzen?
 Defensine: Können wir sie in der Therapie einsetzen? Dr. Jan Wehkamp, Dr. Julia Beisner und Prof. Dr. Eduard F. Stange Defensine sind körpereigene Antibiotika des angeborenen Immunsystems, die die Darmschleimhaut
Defensine: Können wir sie in der Therapie einsetzen? Dr. Jan Wehkamp, Dr. Julia Beisner und Prof. Dr. Eduard F. Stange Defensine sind körpereigene Antibiotika des angeborenen Immunsystems, die die Darmschleimhaut
Reemers Publishing Services GmbH o:/wiley/ehec_und_mrsa/3d/c01.3d from :18:59 3B ; Page size: mm x 165.
 o:/wiley/ehec_und_mrsa/3d/c01.3d from 02.12.2011 16:18:59 1 EHEC o:/wiley/ehec_und_mrsa/3d/c01.3d from 02.12.2011 16:18:59 EHEC-Zellen auf Fibroblasten. Aufnahme: Manfred Rohde, Helmholtz-Zentrum für Infektionsforschung,
o:/wiley/ehec_und_mrsa/3d/c01.3d from 02.12.2011 16:18:59 1 EHEC o:/wiley/ehec_und_mrsa/3d/c01.3d from 02.12.2011 16:18:59 EHEC-Zellen auf Fibroblasten. Aufnahme: Manfred Rohde, Helmholtz-Zentrum für Infektionsforschung,
Rheinische Friedrich-Wilhelms-Universität Institut für Medizinische Mikrobiologie Immunologie und Parasitologie
 Inhaltsverzeichnis Rheinische Friedrich-Wilhelms-Universität Institut für Medizinische Mikrobiologie Immunologie und Parasitologie Direktor: Prof. Dr. A. HÖRAUF 1 Direkte Erregernachweise 1 1.1 Mikroskopie..............
Inhaltsverzeichnis Rheinische Friedrich-Wilhelms-Universität Institut für Medizinische Mikrobiologie Immunologie und Parasitologie Direktor: Prof. Dr. A. HÖRAUF 1 Direkte Erregernachweise 1 1.1 Mikroskopie..............
Aspekte der Eisenresorption. PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse Binningen
 Aspekte der Eisenresorption PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse 19 4102 Binningen Chemische Eigenschaften Fe-II wird leichter aufgenommen als Fe-III wegen der besseren
Aspekte der Eisenresorption PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse 19 4102 Binningen Chemische Eigenschaften Fe-II wird leichter aufgenommen als Fe-III wegen der besseren
Antibiotikaresistenz: Carbapenemase-bildende Keime in Nutztierbeständen
 Antibiotikaresistenz: Carbapenemase-bildende Keime in Nutztierbeständen Aktualisierte Mitteilung Nr. 036/2016 des BfR vom 23.12.2016* Carbapeneme sind Antibiotika, die für die Behandlung von Menschen zugelassen
Antibiotikaresistenz: Carbapenemase-bildende Keime in Nutztierbeständen Aktualisierte Mitteilung Nr. 036/2016 des BfR vom 23.12.2016* Carbapeneme sind Antibiotika, die für die Behandlung von Menschen zugelassen
Einsatz nur bei bestimmten Erkrankungen sinnvoll individuelle Therapie und Dosierung notwendig
 Probiotika: Wundermittel oder Monster? Einsatz nur bei bestimmten Erkrankungen sinnvoll individuelle Therapie und Dosierung notwendig Irsee (5. November 2009) - Die Bedeutung der Darmflora bei bestimmten
Probiotika: Wundermittel oder Monster? Einsatz nur bei bestimmten Erkrankungen sinnvoll individuelle Therapie und Dosierung notwendig Irsee (5. November 2009) - Die Bedeutung der Darmflora bei bestimmten
27 Funktionelle Genomanalysen Sachverzeichnis
 Inhaltsverzeichnis 27 Funktionelle Genomanalysen... 543 27.1 Einleitung... 543 27.2 RNA-Interferenz: sirna/shrna-screens 543 Gunter Meister 27.3 Knock-out-Technologie: homologe Rekombination im Genom der
Inhaltsverzeichnis 27 Funktionelle Genomanalysen... 543 27.1 Einleitung... 543 27.2 RNA-Interferenz: sirna/shrna-screens 543 Gunter Meister 27.3 Knock-out-Technologie: homologe Rekombination im Genom der
PHYTO-EXTRAKT. Aktuelles für Sie und Ihre Patienten
 Liebe Leserin, lieber Leser, PHYTO-EXTRAKT Aktuelles für Sie und Ihre Patienten das Schwabe Premium Service Team und ich danken Ihnen für das in diesem Jahr entgegengebrachte Interesse am Phyto-Extrakt.
Liebe Leserin, lieber Leser, PHYTO-EXTRAKT Aktuelles für Sie und Ihre Patienten das Schwabe Premium Service Team und ich danken Ihnen für das in diesem Jahr entgegengebrachte Interesse am Phyto-Extrakt.
Rekombinante Antikorperfragmente fur die. Zoonosediagnostik
 Rekombinante Antikorperfragmente fur die Zoonosediagnostik Von der Fakultat fur Lebenswissenschaften der Technischen Universitat Carolo-Wilhelmina zu Braunschweig zur Erlangung des Grades eines Doktors
Rekombinante Antikorperfragmente fur die Zoonosediagnostik Von der Fakultat fur Lebenswissenschaften der Technischen Universitat Carolo-Wilhelmina zu Braunschweig zur Erlangung des Grades eines Doktors
Nosokomiale Infektionen
 Definitionen Nosokomiale Infektion Infektion, die bei Aufnahme ins Krankenhaus weder vorhanden noch in Inkubation war Healthcare-associated Infektionen werden nicht nur im Krankenhaus, sondern auch außerhalb
Definitionen Nosokomiale Infektion Infektion, die bei Aufnahme ins Krankenhaus weder vorhanden noch in Inkubation war Healthcare-associated Infektionen werden nicht nur im Krankenhaus, sondern auch außerhalb
Repetitorium: Di D arr r h r oe
 Repetitorium: Diarrhoe Durchfall ist ein Symptom und keine Krankheit Es gibt viele Erkrankungen welche Durchfall als Symptom aufweisen : Infektionskrankheiten Nahrungsmittelintolleranzen Vergiftungen Tumoren
Repetitorium: Diarrhoe Durchfall ist ein Symptom und keine Krankheit Es gibt viele Erkrankungen welche Durchfall als Symptom aufweisen : Infektionskrankheiten Nahrungsmittelintolleranzen Vergiftungen Tumoren
Humanpathogene und antibiotikaresistente Bakterien in Frischgemüse und Potential von Bakteriophagen zu deren Kontrolle
 Humanpathogene und antibiotikaresistente Bakterien in Frischgemüse und Potential von Bakteriophagen zu deren Kontrolle Charles M.A.P. Franz Max Rubner-Institut Bundesforschungsinstitut für Ernährung und
Humanpathogene und antibiotikaresistente Bakterien in Frischgemüse und Potential von Bakteriophagen zu deren Kontrolle Charles M.A.P. Franz Max Rubner-Institut Bundesforschungsinstitut für Ernährung und
Kurstag 5. -Infektionen mit gramnegativen Erregern. -Therapie. -Auswertung der letzten Stunde. -Differenzierung gramnegativer Erreger
 Kurstag 5 -Infektionen mit gramnegativen Erregern -Therapie -Auswertung der letzten Stunde -Differenzierung gramnegativer Erreger Antibiotika-Seminar Freitag: Vorbesprechung Praktischer Teil Dienstag:
Kurstag 5 -Infektionen mit gramnegativen Erregern -Therapie -Auswertung der letzten Stunde -Differenzierung gramnegativer Erreger Antibiotika-Seminar Freitag: Vorbesprechung Praktischer Teil Dienstag:
FBI-Zoo. Food-Borne Zoonotic Infections of Humans. Koordinator: Prof. Dr. L. Wieler, Berlin
 FBI-Zoo Food-Borne Zoonotic Infections of Humans Koordinator: Prof. Dr. L. Wieler, Berlin Dr. Alexander Mellmann Institut für Hygiene, Universitätsklinikum Münster Food-Borne Zoonotic Infections of Humans
FBI-Zoo Food-Borne Zoonotic Infections of Humans Koordinator: Prof. Dr. L. Wieler, Berlin Dr. Alexander Mellmann Institut für Hygiene, Universitätsklinikum Münster Food-Borne Zoonotic Infections of Humans
Tätigkeiten mit biologischen Arbeitsstoffen - Gesetze, Definitionen und mehr...
 Tätigkeiten mit biologischen Arbeitsstoffen - Gesetze, Definitionen und mehr... Was ist ein biologischer Arbeitsstoff? Biologische Arbeitsstoffe?!? 2 BioStoffV: Biologische Arbeitsstoffe sind Mikroorganismen
Tätigkeiten mit biologischen Arbeitsstoffen - Gesetze, Definitionen und mehr... Was ist ein biologischer Arbeitsstoff? Biologische Arbeitsstoffe?!? 2 BioStoffV: Biologische Arbeitsstoffe sind Mikroorganismen
Klausur Mikrobiologie, Hygiene und Virologie SS (Humanmedizin, Universität zu Köln) Gedächtnisprotokoll Revision: v1.0 /
 Klausur Mikrobiologie, Hygiene und Virologie SS 2007 (Humanmedizin, Universität zu Köln) Gedächtnisprotokoll Revision: v1.0 / 13.07.2007 IK Studiengang: Anzahl: Format: Zeit: RSG und MSG 54 short-answer-
Klausur Mikrobiologie, Hygiene und Virologie SS 2007 (Humanmedizin, Universität zu Köln) Gedächtnisprotokoll Revision: v1.0 / 13.07.2007 IK Studiengang: Anzahl: Format: Zeit: RSG und MSG 54 short-answer-
Johannes Hübner erforscht Darmbakterien und ihre süß-saure Hülle
 Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/johannes-huebner-erforschtdarmbakterien-und-ihre-suess-saure-huelle/ Johannes Hübner erforscht Darmbakterien und
Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/johannes-huebner-erforschtdarmbakterien-und-ihre-suess-saure-huelle/ Johannes Hübner erforscht Darmbakterien und
Gliederung. 1) Was ist ein Toxin? 2) Klassifizierung bakterieller Toxine - Wirkmechanismen - Populäre Vertreter 3) Fazit
 Bakterielle Toxine Maximilian Benedikt Rossol Johannes-Gutenberg-Universität Mainz Insitut für Mikrobiologie und Weinforschung Johann-Joachim-Becherweg 15, 55128 Mainz Gliederung 1) Was ist ein Toxin?
Bakterielle Toxine Maximilian Benedikt Rossol Johannes-Gutenberg-Universität Mainz Insitut für Mikrobiologie und Weinforschung Johann-Joachim-Becherweg 15, 55128 Mainz Gliederung 1) Was ist ein Toxin?
1 Modellorganismen. 1.1 Escherichia coli
 1 Modellorganismen Wesentliche biologische Erkenntnisse der letzten Jahrzehnte wurden an Modellorganismen gewonnen. Sie sind dadurch gekennzeichnet, dass sie für die Laborarbeit genetisch angepasst wurden
1 Modellorganismen Wesentliche biologische Erkenntnisse der letzten Jahrzehnte wurden an Modellorganismen gewonnen. Sie sind dadurch gekennzeichnet, dass sie für die Laborarbeit genetisch angepasst wurden
Unterdrückung der bakteriellen Kommunikation Einsatzmöglichkeiten in der Lebensmittelhygiene
 Unterdrückung der bakteriellen Kommunikation Einsatzmöglichkeiten in der Lebensmittelhygiene Thomas Alter, Greta Gölz Institut für Lebensmittelsicherheit und -hygiene, FU Berlin Übersicht Bakterielle Kommunikation
Unterdrückung der bakteriellen Kommunikation Einsatzmöglichkeiten in der Lebensmittelhygiene Thomas Alter, Greta Gölz Institut für Lebensmittelsicherheit und -hygiene, FU Berlin Übersicht Bakterielle Kommunikation
Grundideen der Gentechnik
 Grundideen der Gentechnik Die Gentechnik kombiniert Biotechnik und Züchtung. Wie in der Züchtung wird die Erbinformation eines Lebewesen verändert. Dabei nutzte man in den Anfängen der Gentechnik vor allem
Grundideen der Gentechnik Die Gentechnik kombiniert Biotechnik und Züchtung. Wie in der Züchtung wird die Erbinformation eines Lebewesen verändert. Dabei nutzte man in den Anfängen der Gentechnik vor allem
Gesunder Darm gesunder Mensch Wie hilft uns die Stuhldiagnostik weiter?
 7 DARMGESUNDHEIT Gesunder Darm gesunder Mensch Wie hilft uns die Stuhldiagnostik weiter? Wunderwerk Darm Der Darm ist unser flächenmäßig größtes Organ. Seine Oberfläche wird durch Falten, Zotten, Mikrovilli
7 DARMGESUNDHEIT Gesunder Darm gesunder Mensch Wie hilft uns die Stuhldiagnostik weiter? Wunderwerk Darm Der Darm ist unser flächenmäßig größtes Organ. Seine Oberfläche wird durch Falten, Zotten, Mikrovilli
Die Mikroimmuntherapie
 M E D I Z I N I S C H E MeGeMIT G E S E L L S C H A F T Die Mikroimmuntherapie Unterstützung und Regulierung des Immunsystems Die Mikroimmuntherapie: Das Immunsystem im Gleichgewicht Das Immunsystem ist
M E D I Z I N I S C H E MeGeMIT G E S E L L S C H A F T Die Mikroimmuntherapie Unterstützung und Regulierung des Immunsystems Die Mikroimmuntherapie: Das Immunsystem im Gleichgewicht Das Immunsystem ist
Wie bezeichnet man den Vorgang der Integration des Lambda-Phagen in das Bakteriengenom?
 2004: Wie bezeichnet man den Vorgang der Integration des Lambda-Phagen in das Bakteriengenom? Wie nennt man den Zustand des Bakteriums und des Lambda-Phagen nach erfolgreicher Integration des Phagen? (1,5)
2004: Wie bezeichnet man den Vorgang der Integration des Lambda-Phagen in das Bakteriengenom? Wie nennt man den Zustand des Bakteriums und des Lambda-Phagen nach erfolgreicher Integration des Phagen? (1,5)
Lactobact. HLH BioPharma. Patientenbroschüre. Ein Leitfaden für die Wahl des richtigen Probiotikums. Patienteninformation
 Lactobact Patientenbroschüre Ein Leitfaden für die Wahl des richtigen Probiotikums Patienteninformation HLH BioPharma Inhaltsübersicht Probiotika gesundheitsbewusst leben 3 Probiotische Lebensmittel ausreichend
Lactobact Patientenbroschüre Ein Leitfaden für die Wahl des richtigen Probiotikums Patienteninformation HLH BioPharma Inhaltsübersicht Probiotika gesundheitsbewusst leben 3 Probiotische Lebensmittel ausreichend
Gesundheit aus der Balance
 Rath international 04-2016 Probiotika Gesundheit aus der Balance Der Mensch ist Lebensraum für Billionen mikroskopisch kleiner Lebewesen (Mikroorganismen). Zusammen bilden sie ein hoch komplexes dynamisches
Rath international 04-2016 Probiotika Gesundheit aus der Balance Der Mensch ist Lebensraum für Billionen mikroskopisch kleiner Lebewesen (Mikroorganismen). Zusammen bilden sie ein hoch komplexes dynamisches
MRSA Typisierungen
 EUREGIO Gronau/Enschede MRSA Typisierungen 2012-2013 Ansprechpartner Dr. med. R. Köck Institut für Hygiene Universitätsklinikum Münster robin.koeck@ukmuenster.de Tel. 0251-83-55348 0 Inhaltsverzeichnis
EUREGIO Gronau/Enschede MRSA Typisierungen 2012-2013 Ansprechpartner Dr. med. R. Köck Institut für Hygiene Universitätsklinikum Münster robin.koeck@ukmuenster.de Tel. 0251-83-55348 0 Inhaltsverzeichnis
MRE AK Krankenhäuser Punktprävalenz-Untersuchung MRE Netzwerk Metropolregion Rhein-Neckar
 MRE AK Krankenhäuser Punktprävalenz-Untersuchung MRE Netzwerk Metropolregion Rhein-Neckar Warum sind wir hier? Wir möchten Ihnen eine Untersuchung vorstellen, die zeigt dass die Zahl der von multiresistenten
MRE AK Krankenhäuser Punktprävalenz-Untersuchung MRE Netzwerk Metropolregion Rhein-Neckar Warum sind wir hier? Wir möchten Ihnen eine Untersuchung vorstellen, die zeigt dass die Zahl der von multiresistenten
312/AB XXIII. GP. Dieser Text wurde elektronisch übermittelt. Abweichungen vom Original sind möglich.
 312/AB XXIII. GP - Anfragebeantwortung 1 von 5 312/AB XXIII. GP Eingelangt am 04.04.2007 BM für Gesundheit, Familie und Jugend Anfragebeantwortung Frau Präsidentin des Nationalrates Mag a. Barbara Prammer
312/AB XXIII. GP - Anfragebeantwortung 1 von 5 312/AB XXIII. GP Eingelangt am 04.04.2007 BM für Gesundheit, Familie und Jugend Anfragebeantwortung Frau Präsidentin des Nationalrates Mag a. Barbara Prammer
Strahlenbiologische Grundlagen
 Strahlenbiologische Grundlagen Wolfgang-Ulrich MüllerM Häufigkeit von Tumoren im Kindesalter (auf der Basis der Jahre 1997-2006) (Quelle: Robert-Koch-Institut basierend auf den Daten des Deutschen Kinderkrebsregisters,
Strahlenbiologische Grundlagen Wolfgang-Ulrich MüllerM Häufigkeit von Tumoren im Kindesalter (auf der Basis der Jahre 1997-2006) (Quelle: Robert-Koch-Institut basierend auf den Daten des Deutschen Kinderkrebsregisters,
Grundlagen und Facts zur Lebensmittelsicherheit
 Grundlagen und Facts zur Lebensmittelsicherheit von Geflügelfleisch Roger Stephan Vetsuisse-Fakultät Universität Zürich, Schweiz www.ils.uzh.ch Ziele Ich möchte die aus lebensmittelhygienischer Sicht relevanten
Grundlagen und Facts zur Lebensmittelsicherheit von Geflügelfleisch Roger Stephan Vetsuisse-Fakultät Universität Zürich, Schweiz www.ils.uzh.ch Ziele Ich möchte die aus lebensmittelhygienischer Sicht relevanten
Vorlesungsthemen Mikrobiologie
 Vorlesungsthemen Mikrobiologie 1. Einführung in die Mikrobiologie B. Bukau 2. Zellaufbau von Prokaryoten B. Bukau 3. Bakterielles Wachstum und Differenzierung B. Bukau 4. Bakterielle Genetik und Evolution
Vorlesungsthemen Mikrobiologie 1. Einführung in die Mikrobiologie B. Bukau 2. Zellaufbau von Prokaryoten B. Bukau 3. Bakterielles Wachstum und Differenzierung B. Bukau 4. Bakterielle Genetik und Evolution
KULTIVIERUNG VON MIKROORGANISMEN
 KULTIVIERUNG VON MIKROORGANISMEN KULTIVIERUNG VON MIKROORGANISMEN Verfahren, das Bakterien außerhalb des natürlichen Standortes zur Vermehrung bringt (unbelebte Substrate oder Zellkulturen) 1 Voraussetzungen
KULTIVIERUNG VON MIKROORGANISMEN KULTIVIERUNG VON MIKROORGANISMEN Verfahren, das Bakterien außerhalb des natürlichen Standortes zur Vermehrung bringt (unbelebte Substrate oder Zellkulturen) 1 Voraussetzungen
Alexander Titz: Molekül-Design gegen antibiotikaresistente Bakterien
 Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/alexander-titz-molekueldesign-gegen-antibiotikaresistente-bakterien/ Alexander Titz: Molekül-Design gegen antibiotikaresistente
Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/alexander-titz-molekueldesign-gegen-antibiotikaresistente-bakterien/ Alexander Titz: Molekül-Design gegen antibiotikaresistente
Cystistat natürliche Hilfe für gesunde Harnwege
 Cystistat natürliche Hilfe für gesunde Harnwege Liebe Patientin, lieber Patient, Sie leiden unter Schmerzen in der Blasenregion, haben starken Harndrang und müssen sehr häufig auf die Toilette gehen? Diese
Cystistat natürliche Hilfe für gesunde Harnwege Liebe Patientin, lieber Patient, Sie leiden unter Schmerzen in der Blasenregion, haben starken Harndrang und müssen sehr häufig auf die Toilette gehen? Diese
 1 Gesundheit beginnt im Darm Wolfgang Schafzahl Gliederung Mikrobiota ein neues Organsystem Antibiotika Resistenzen, Nutzen, Risiken, Aussichten Fütterungsbedingte Krankheiten gesunder Darm gesundes Ferkel
1 Gesundheit beginnt im Darm Wolfgang Schafzahl Gliederung Mikrobiota ein neues Organsystem Antibiotika Resistenzen, Nutzen, Risiken, Aussichten Fütterungsbedingte Krankheiten gesunder Darm gesundes Ferkel
GENTECHNIK BEI PFLANZEN
 - 1 - GENTECHNIK BEI PFLANZEN 1. Grüne Gentechnik - was ist das? "Grüne Gentechnik" ist laut Gentechnik-Wörterbuch eine "umgangssprachliche Bezeichnung für gentechnische Forschung mit Pflanzen, während
- 1 - GENTECHNIK BEI PFLANZEN 1. Grüne Gentechnik - was ist das? "Grüne Gentechnik" ist laut Gentechnik-Wörterbuch eine "umgangssprachliche Bezeichnung für gentechnische Forschung mit Pflanzen, während
Sicherer Schutz für alle Babys
 Sicherer Schutz für alle Babys Pneumokokken - was ist das? Bakterien Fachname: Pneumokokken oder Streptococcus pneumoniae Das Besondere: dicke Kapsel aus Zuckermolekülen (Polysachariden), schützt den Erreger
Sicherer Schutz für alle Babys Pneumokokken - was ist das? Bakterien Fachname: Pneumokokken oder Streptococcus pneumoniae Das Besondere: dicke Kapsel aus Zuckermolekülen (Polysachariden), schützt den Erreger
ahus: Entstehung, Symptome und Diagnostik
 ahus: Entstehung, Symptome und Diagnostik Prof. Dr. med. Thorsten Feldkamp 3. ahus-patienten- und Angehörigentag Universitätsklinikum Mainz 20. Juni 2015 Atypisches hämolytisches urämisches Syndrom Einführung
ahus: Entstehung, Symptome und Diagnostik Prof. Dr. med. Thorsten Feldkamp 3. ahus-patienten- und Angehörigentag Universitätsklinikum Mainz 20. Juni 2015 Atypisches hämolytisches urämisches Syndrom Einführung
Prüfungsfragenkatalog für für Grundlagen der Gentechnik und Biotechnologie (Prof. Prof. Rudolf Bauer und Prof. Karin Ardjomand-Wölkart)
 Prüfungsfragenkatalog für für Grundlagen der Gentechnik und Biotechnologie (Prof. Prof. Rudolf Bauer und Prof. Karin Ardjomand-Wölkart) Stand: September 2014 Termin: 29.09.2014 1. Was ist Western Blot?
Prüfungsfragenkatalog für für Grundlagen der Gentechnik und Biotechnologie (Prof. Prof. Rudolf Bauer und Prof. Karin Ardjomand-Wölkart) Stand: September 2014 Termin: 29.09.2014 1. Was ist Western Blot?
