Fragen und Antworten. zu Gesetzen, Vorgaben, Verordnungen sowie der Reinigung, Desinfektion und Sterilisation von Instrumenten
|
|
|
- Guido Kurzmann
- vor 6 Jahren
- Abrufe
Transkript
1 Fragen und Antworten zu Gesetzen, Vorgaben, Verordnungen sowie der Reinigung, Desinfektion und Sterilisation von Instrumenten Dokumentation der Instrumentenaufbereitung
2 Rechtsanwältin steht sie ihrem Mann Heinrich Reinstädler, der eine Zahnarztpraxis in Paderborn betreibt, in rechtlichen Fragen zur Seite. Im Zuge anstehender Modernisierungsmaßnahmen soll der Instrumentenaufbereitungsbereich neu gestaltet werden. 2 3 Interview: Gesetzliche Vorgaben Auch Ihnen wollen wir die Antworten nicht vorenthalten In dem Interview mit der ZWP Zahnarzt Wirtschaft und Praxis antwortete die Anwältin für Medizinrecht Heike Reinstädler auf die Frage, wie die Dokumentation der Instrumentenaufbereitung rechtlich abgesichert werden kann. Gleich im Anschluss beantwortet der Experte Manfred Korn Fragen zu Gesetzen, Vorgaben, Verordnungen sowie der Reinigung, Desinfektion und Sterilisation von Instrumenten. Dokumentation der Instrumentenaufbereitung aus rechtlicher Sicht Heike Reinstädler ist seit 1992 Anwältin für Medizinrecht. Neben ihrer Tätigkeit als
3 Frau Reinstädler, welche gesetzlichen Vorgaben haben Sie für die Dokumentation der Instrumentenaufbereitung herangezogen Die gesetzlichen Vorgaben sind genau geregelt. Hier sind die Medizinprodukte-Richtlinie 93/42/EWG, das Medizinproduktegesetz (MPG), die Medizin produkte- Betreiberverordnung (MPBetreibV), das Infektionsschutzgesetz (IfSG), das Patientenrechtegesetz (BGB), das Arbeitsschutzgesetz (ArbSchG) und die Richtlinien des Robert Koch-Instituts zu nennen. Bei der Frage nach der rechtlichen Absicherung der Dokumentation der Instrumentenaufbereitung haben sich bestimmt einige Hauptaspekte herauskristallisiert, oder Ja. Uns war von Anfang an klar, dass wir eine effiziente digitale Dokumentation der Instrumentenaufbereitung haben wollen. Dabei ist es zwingend notwendig, dass die anzuwendende Software absolute Rechtssicherheit gewährleistet, damit im Falle eines Rechtsstreits die Hygienedokumentation als Beweismittel vor Gericht verwertbar ist. Der ganze Aufzeichnungsprozess muss von A bis Z lückenlos nachvollziehbar und vor allem fälschungssicher sein. Was macht eine Dokumentationssoftware eigentlich Eine Dokumentationssoft ware sammelt, verwaltet und archiviert automatisch die Prozess daten vom Thermodesinfektor und/oder Sterilisator.
4 4 5 Interview: Rechtssichere Dokumentation Sie sprachen von einem fälschungssicheren Aufzeichnungsprozess, wie meinen Sie das Nach der Festlegung durch das Robert Koch-Institut bezüglich der Aufbereitungsdokumentation darf weder der ursprüngliche Inhalt einer Eintragung unkenntlich gemacht werden, noch dürfen Änderungen vorgenommen werden, die nicht erkennen lassen, ob sie während oder nach der ursprünglichen Eintragung vorgenommen worden sind. Somit besitzt eine manipulierbare Dokumentation keinerlei rechtliche Verwertbarkeit. Allein schon der Vorwurf der Manipulierbarkeit kann erhebliche Konsequenzen nach sich ziehen. quittieren. Hier wird eine fortgeschrittene elektronische Signatur im Sinne des deutschen Signaturgesetzes benötigt. Eine fortgeschrittene elektronische Signatur Ja, durch den Gesetzgeber wird mit dieser Signatur das Ziel verfolgt, eine öffentlich überprüfbare und sichere Signierungsmethode zu entwickeln, mit der eine Person auf elektronischem Wege Daten unterzeichnen kann. Diese Signatur gilt im Sinne des deutschen Signaturgesetzes ( 2 Nr. 2 SigG) als elektronischer Echtheitsnachweis. Und wie kann dieser Vorwurf der Manipulierbarkeit ausgeräumt werden Indem die Software einen elektronischen Echtheitsnachweis liefert. Anders als auf dem Papier kann die zuständige Person, die die Instrumentenaufbereitung durchführt, nicht mit Ihrer Unterschrift die Freigabe der aufbereiteten Instrumente
5 Haben Sie eine Dokumentationssoftware gefunden, die mit einer fortgeschrittenen elektronischen Signatur arbeitet Ja, die SegoSoft von der Firma Comcotec. Neben der rechtlichen Absicherung sind für Sie bestimmt noch andere Entscheidungskriterien wichtig, oder Bedienerfreundlichkeit und Zeitersparnis. Die ganze Instrumentenaufbereitung nimmt schon sehr viel Zeit in Anspruch. Und da ist es hilfreich für das Personal nur den Sterilisator oder den Thermodesinfektor bestücken zu müssen und das Aufbereitungsprogramm zu starten. Die SegoSoft erkennt selbstständig den Beginn und das Ende eines solchen Programms. Am Ende des Aufbereitungsprogramms erscheint auf dem Bildschirm automatisch ein Freigabedialog. Und was bezweckt dieser Freigabedialog Es ist wichtig alle Entscheidungskriterien für die Freigabe der aufbereiteten Instrumente seinen Anforderungen entsprechend festzuhalten. In diesem Dialog werden z. B. Informationen zur Beladung und das Chargenkontrollergebnis des Prozessindikators festgehalten. Das Personal füllt den Freigabedialog zeitnah aus und so ist gewährleistet, dass alle wichtigen Angaben festgehalten werden. Sehr praktisch finde ich die Möglichkeit in der SegoSoft aus dem Freigabedialog heraus direkt Etiketten für verpackte Güter ausdrucken zu können.
6 6 7 Interview: Rechtssichere Dokumentation Was passiert mit den Angaben aus dem Freigabedialog Nun, die Angaben werden mit den aufgezeichneten Prozessdaten, die der Sterilisator oder der Thermodesinfektor an die SegoSoft übermittelt, verknüpft und manipulationsgeschützt gespeichert. Diese werden dann mit der fortgeschrittenen elektronischen Signatur der freigebenden Person versehen und automatisch in das für die Langzeitarchivierung geeignete PDF/A-1-Format umgewandelt. Was meinen Sie mit dem in das für die Langzeitarchivierung geeignete PDF/A-1-Format Nach der aktualisierten Empfehlung der KRINKO und des BfArM beträgt die Aufbewahrungsfrist der Dokumentation der Instrumentenaufbereitung 5 Jahre. Innerhalb dieser Zeit muss eine problemlose Wiedergabe der Aufbereitungsdokumentation gewährleistet sein. Durch die automatische Umwandlung der angefallenen Daten in das PDF/A-1-Format können wir ohne Rücksicht auf verwendete Software-Versionen die Aufzeichnungen jederzeit öffnen und vorweisen.
7 Ihr Mann ist gerade dabei sich einen neuen Sterilisator anzuschaffen. Hat er von der Firma Comcotec Vorgaben bezüglich der passenden Hersteller bekommen Nein. Meines Wissens wirbt die Firma Comcotec damit, dass über SegoSoft ca. 300 verschiedene Aufbereitungsgeräte von verschiedenen Herstellern in einem System über eine einheitliche Oberfläche bedient werden können. Sie unterstützt alle gängigen Hersteller und Systeme und ist kompatibel zu allen gängigen Praxismanagement- und Patientenverwaltungssystemen. Frau Reinstädler, abschließend noch eine Frage zum Qualitätsmanagement-System. Gehört die Dokumentation der Instrumentenaufbereitung für Sie dazu Die Dokumentation der Instrumentenaufbereitung gehört auf jeden Fall zu einem gut gelebten Qualitätsmanagement-System. Wie heißt es so schön: Was nicht dokumentiert ist, wurde nicht gemacht.
8 8 9 Vorschriften, Aufbereitungspersonal, Indikatoren Fragen und Antworten zu Gesetzen, Vorgaben, Verordnungen sowie der Reinigung, Desinfektion und Sterilisation von Instrumenten Manfred Korn ist über 30 Jahre in der Sterilisationsbranche tätig und seit 15 Jahren Geschäftsführer des Unternehmens Comcotec Messtechnik GmbH. Das Unternehmen entwickelt und vermarktet Lösungen zur Steuerung, Dokumentation und Validierung der Prozesse von Sterilisatoren, Thermodesinfektoren, Siegelgeräten und Brutschränken. Herr Korn, welche hygienerechtlichen Vorschriften gibt es und welche Behörden sind zuständig für die Überwachung der Hygiene in einer Zahnarztpraxis Hygienerechtliche Vorschriften finden sich in verschiedenen Gesetzen wie z. B. dem Infektionsschutzgesetz, dem Medizinproduktegesetz, dem Patientenrechtegesetz, dem Arbeitsschutzgesetz, länderspezifischen Gesetzen über den öffentlichen Gesundheitsdienst oder auch in berufsgenossenschaftlichen Vorschriften. Zuständig für die behördliche Überwachung der Hygiene in einer Praxis sind insbesondere die Gesundheitsämter. Für die Umsetzung der anzuwendenden Normen, insbesondere des Medizinproduktegesetzes und des Infektionsschutzgesetzes, sind je nach Bundesland unterschiedliche Behörden zuständig. Das ausführende Organ in Bayern ist das Gewerbeaufsichts amt.
9 Welche Personen dürfen die Instrumentenaufbereitung durchführen Welche Indikatoren sollten verwendet werden Mit der Instandhaltung (Wartung, Inspektion, Instandsetzung und Aufbereitung) von Medizinprodukten, so steht es in den Empfehlungen des RKI (Infektionsprävention in der Zahnheilkunde), dürfen nur Personen beauftragt werden, die aufgrund ihrer Ausbildung und praktischen Tätigkeit über die erforderlichen speziellen Sachkenntnisse verfügen. Veränderte Arbeitsbedingungen oder die Einführung neuer Verfahren oder neuer Medizinprodukte erfordern eine Anpassung der Kenntnisse durch entsprechende Unterweisung. Es sollte eine Benennung einer berechtigten Person zur Freigabe der aufbereiteten Medizinprodukte unter Berücksichtigung der individuellen Qualifikation der einzelnen Mitarbeiter erfolgen. Diese sollte auch schriftlich im Organigramm mit der entsprechenden Arbeitsplatzbeschreibung festgehalten werden. Hier sollte als Prozessindikator mindestens ein Chemoindikator Klasse 5 (DIN EN ISO ), bei Kritisch A Produkten ohne PCD (Process Challenge Device) und bei Kritisch B Produkten mit PCD, z. B. Helix-Test (DIN 867-5) verwendet werden. Ebenfalls sollte der Einsatz von Behandlungsindikatoren (Klasse 1; DIN EN ISO ) erfolgen. Diese müssen auf jedem sterilisierten Gegenstand angebracht werden, um einen sterilisierten von einem unsterilisierten Artikel unterscheiden zu können.
10 10 11 Testverfahren, MP-Aufbereitungsende, MP-Wiederverwendung Helix-Test Was ist der Unterschied zwischen dem Bowie & Dick-Test und dem Beide Testverfahren überprüfen die Dampfdurchdringung. Der Bowie & Dick-Test prüft die Dampfdurchdringung eines Wäschepaketes von 7 kg Textilien (DIN EN 867-3), dies entspricht einem Einheitssterilisationscontainer, der in Krankenhäusern Verwendung findet. Um für den Test nicht immer ein Wäschepaket mit einem Indikatorstreifen packen zu müssen, gibt es auf dem Markt diverse Bowie & Dick-Test-Einmaltestpakete. Der Helix-Test ist ein Standardtest bei dem Betrieb eines Klasse B Autoklaven und wird in der DIN EN beschrieben. Er besteht aus einem 1,50 cm langen Schlauch, mit einem Durchmesser von 2 mm. Der Schlauch wird an einem Ende durch eine kleine Kapsel verschlossen, in der sich ein Indikatorstreifen befindet. Bei dem Durchdringungstest muss der heiße Dampf erst durch den Schlauch gelangen, um einen Farbumschlag des Indikators bewirken zu können. Hierbei muss durch das Vakuumziehen des Autoklaven erst die Luft aus dem Schlauch entfernt werden. Dazu ist ein Autoklav mit einem fraktioniertem Vorvakuum nötig. Dieser Test wird eingesetzt um die Wirkung des Sterilisationsprozesses in Hohlkörpern mit engen Lumina zu kontrollieren. Die kleinste Menge an Restluft in dem Schlauch führt zu einer nicht ordnungsgemäßen Verfärbung des Indikatorstreifens und dementsprechend zu einem nicht bestandenen Durchdringungstest. Das Bestehen dieser Härtetests bietet Garantie für die zuverlässige Sterilisation von Übertragungsinstrumenten. Wann ist die Aufbereitung von Medizinprodukten beendet Die Aufbereitung von Medizinprodukten endet mit der Freigabe zur Anwendung. Diese erfolgt auf der Basis der Übereinstimmung der bei der Aufbereitung jeweils ermittelten Prozessparameter mit denen der Validierungsprotokolle und schließt die Durchführung und Dokumentation der
11 täglichen Routineprüfungen, die Überprüfung und Dokumentation des vollständigen und korrekten Prozessverlaufs (chargenbezogene Routineprüfung und Chargendokumentation), die Überprüfung der Verpackung auf Unversehrtheit und Trockenheit und die Überprüfung der Kennzeichnung mit ein. Welche Voraussetzungen für die Wiederverwendung von Medizinprodukten müssen gegeben sein Generell muss von dem Hygieneverantwortlichen der Zahnarztpraxis für jede Gruppe von Medizinprodukten festgelegt werden, ob, wie oft und mit welchem validierten Verfahren es aufbereitet werden soll. Hierzu müssen die Hersteller von Medizinprodukten Angaben zur Aufbereitung einschließlich Reinigung/Desinfektion, Spülung, Trocknung, Sterilisation, Transport, sowie zur sachgerechten Lagerung der von ihnen vertriebenen Produkte dem Käufer zur Verfügung stellen (DIN EN ISO 17664). Liegen diese Informationen nicht vor, muss der Hygieneverantwortliche entscheiden, ob er aufgrund vorhandener Kenntnisse über das betreffende oder ein ähnliches Medizinprodukt ein validiertes Aufbereitungsverfahren festlegen kann. Trifft dieses nicht zu, dürfen kritische Medizinprodukte nicht aufbereitet werden. Manche Hersteller von Medizinprodukten setzen eine begrenzte Anzahl von Aufbereitungszyklen fest. Mit einer geeigneten Kennzeichnung des aufzubereitenden Instrumentes kann mit einem Blick die Anzahl der noch möglichen Aufbereitungen sichtbar gemacht werden. Ebenfalls müssen diese Medizinprodukte durch die Risikobewertung vor der Aufbereitung als unkritisch, semikritisch oder kritisch eingestuft werden. Die Festlegung eines validierten Verfahrens und die Einstufung des aufzubereitenden Medizinproduktes muss in ihren Einzelschritten unter Angabe der jeweilig notwendigen Prüfungen detailliert in einer Standardarbeits- und Betriebsanweisung festgelegt werden, egal ob die Aufbereitung maschinell oder händisch erfolgt. Ein manuelles Verfahren ist jedoch nur standardisierbar und nicht validierbar.
12 12 13 Validierung Was sind validierte Verfahren Gemäß der MPBetreiberverordnung sind die Reinigung, Desinfektion und Sterilisation von Medizinprodukten mit geeigneten, validierten Verfahren so durchzuführen, dass der Erfolg dieser Verfahren nachvollziehbar ist. Das bedeutet, dass für alle Schritte der Aufbereitung dokumentierbare und zu dokumentierende Verfahren anzuwenden sind, die das Erreichen der vorgegebenen Ziele, wie Sauberkeit, Keimarmut und Abwesenheit pathogener Erreger mit jedem ausgeführten Prozess zuverlässig und reproduzierbar erreicht werden. Mit der Validierung der Aufbereitungsprozesse werden auch die Parameter definiert, die erforderlich sind zu beweisen, dass der jeweilige Prozess (Einzelschritt der Aufbereitung) in einer Form durchlaufen wurde, die die Erzielung der jeweils vorgegebenen Spezifikationen reproduzierbar garantiert. Was ist unter einer Prozessvalidierung zu verstehen Die Prozessvalidierung ist ein essentielles und kritisches Element für die Sicherheit und Funktionsfähigkeit von Medizinprodukten und Laboruntersuchungen. Sie wird explizit in QM-Systemen (DIN EN ISO 9001:2008, DIN EN ISO 13485:2003, GMP, DIN EN ISO 15189:2007), in der Richtlinie der Bundesärztekammer (RiliBÄK:2008) und in der Medizinprodukte Betreiberverordnung (MPBetreibV:2002) gefordert. Die Prozessvalidierung umfasst die Ausarbeitung eines dokumentierten Nachweises, dass ein Prozess dauernd ein Ergebnis oder Produkt erzeugt, welches vorgegebene Anforderungen erfüllt. Sie wird unterteilt in folgende Bereiche: Designerqualifikation (DQ), Installationsqualifikation (IQ), Funktionsqualifikation (OQ), Leistungsqualifikation (PQ) und Instandhaltungs-, Wartungs-, Instandsetzungsqualifikation (MQ).
13 Was bedeuten die einzelnen Qualifikationen genau Designerqualifikation/Design Qualifikation (DQ): Beinhaltet den dokumentierten Nachweis, dass das Produkt (Gerät) entsprechend den geplanten Anforderungen/Spezifikationen für den beabsichtigten Verwendungszweck geeignet ist. Installationsqualifikation/Installation Qualification (IQ): Beinhaltet den dokumentierten Nachweis, dass das Produkt (Gerät) in Auftrag gegebenen und installierten Ausführung der vorgesehenen Bestimmung und den Herstellerangaben entspricht. Funktionsqualifikation/Operational Qualification (OQ): Beinhaltet den dokumentierten Nachweis, dass das Produkt (Gerät) in der installierten Ausführung seiner Spezifikationen entsprechend funktioniert. Leistungsqualifikation/Performance Qualification (PQ): Beinhaltet den dokumentierten Nachweis, dass das Produkt (Gerät) in Betrieb unter realen (Routine-) Bedin gungen vorschriftsmäßig und den An forderungen (Spezifikationen) entsprechend funktioniert. Instandhaltungs-, Wartungs-, Instandsetzungsqualifikation/Maintenance Qualification (MQ): Beinhaltet den dokumentierten Nachweis einer regelmäßigen Wartung. Beschreibung aller zur Reinigung, Wartung und Instandsetzung erforderlichen Maßnahmen.
14 14 15 Sterilisationsmethode, Aufbereitungsdokumentation, Kennzeichnung angewandt Welche Sterilisationsmethode wird am häufigsten in der Zahnmedizin In der Zahnmedizin ist die Sterilisation mit Heißdampf bei 121 C oder 134 C die häufigste Methode. Dafür werden Dampf-Kleinsterilisatoren (Autoklaven) benutzt. Das Robert Koch-Institut empfiehlt, die Heißdampfsterilisation der Heißluftsterilisation vorzuziehen. Diese Autoklaven besitzen ein Kammervolumen das kleiner ist als eine Sterilisiereinheit (1 STE = 30 x 30 x 60 cm). Für diese Dampf-Kleinsterilisatoren gelten die Anforderungen der DIN EN ISO Hier werden drei verschiedene Klassen unterschieden. Die Klasse N ist nur für unverpackte, massive Produkte vorgesehen, die Klasse B für alle verpackten oder unverpackten massiven Produkte, Hohlkörper (z. B. Hand- und Winkelstücke) sowie poröse Produkte (Textilien). Das ist das Verfahren, bei dem mit fraktioniertem Vakuum alle Instrumente in allen Verpackungsvarianten sterilisiert werden können. Die Klasse S hingegen ist nur für Produkte, die vom Hersteller des Sterilisationsgerätes angegeben werden. Für die Zahnarztpraxis sind insbesondere Geräte der Klasse B und S geeignet. werden Welche Daten der Instrumentenaufbereitung müssen dokumentiert Gemäß den Empfehlungen des Robert Koch-Instituts sind die im Rahmen der Aufbereitung erfassten Messwerte der Prozessparameter und die Freigabeentscheidung mit Bezug auf die freigebende Person und die Charge zu dokumentieren. Sie müssen belegen, dass der angewendete Aufbereitungsprozess gemäß den Standardarbeitsanweisungen unter Einhaltung der im Validierungsprotokoll niedergelegten Parameter erfolgt ist. Es darf weder der ursprüngliche Inhalt einer Eintragung unkenntlich gemacht werden, noch dürfen Änderungen vorgenommen werden, die nicht erkennen lassen, ob sie während oder nach der ursprünglichen Eintragung vorgenommen worden sind. Die Aufzeichnungen können auch auf Bild- oder Datenträgern aufbewahrt werden. Es muss sichergestellt sein, dass sie während der Aufbewahrungsfrist verfügbar und leserlich sind.
15 Welche Informationen müssen bei der Kennzeichnung von verpackten, aufbereiteten Medizinprodukten berücksichtigt werden Gemäß der aktualisierten Empfehlung Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten (Oktober 2012) der KRINKO und des BfArM müssen für den Anwender jederzeit die Bezeichnung des Medizinproduktes, die eine nutzungsrelevante Identifizierung erlaubt (z. B. Modell, Größe), sofern nicht unmittelbar ersichtlich, erkennbar sein. Ebenfalls müssen Angaben zur Kennzeichnung freigegebener Medizinprodukte wie die Freigabeentscheidung und gegebenenfalls Prozessindikatoren sowie Angaben, die die Entscheidung über zeitabhängige Aspekte der gefahrlosen Anwendung des Medizinproduktes erlauben, wie z. B. den Zeitpunkt und Art des verwendeten Steri lisationsverfahrens (Chargenkennzeichnung der erfolgten Sterilisation, Sterilisierdatum) gemacht werden. Genauso wichtig ist die Angabe des Verfalldatums im Sinne des vom Hersteller angegebenen Datums, bis zu dem eine gefahrlose Anwendung nachweislich möglich ist und die Sterilgutlagerfrist, sofern diese kürzer ist als das Verfalldatum. Falls notwendig müssen z. B. bei Medizinprodukten der Gruppe kritisch C Hinweise zur technisch-funktionellen Prüfung und Sicherheit, Sicherheits- und Warnhinweise, sowie andere, aus schließlich auf der Originalverpackung vorhandene, für die sichere Anwendung und Rückverfolgbarkeit relevante Informationen, wie der Name des Herstellers und die Chargen- oder Seriennummer aufgeführt werden.
16 16 17 Chargendokumentation, digitale Dokumentation Welche Vor- und Nachteile hat die Dokumentation der Instrumentenaufbereitung über einen integrierten Chargendrucker oder externen Drucker Die Vorteile der Dokumentation über einen integrierten Chargendrucker oder einen externen Drucker besteht in dem automatischen Prozessdatenausdruck, der eine Vielzahl von Informationen fälschungssicher wiedergibt. Die meisten Ausdrucke besitzen auch ein Unterschriftenfeld, indem die Freigabeentscheidung mit der Unterschrift der freigebenden Person festgehalten werden kann. Die Nachteile dieser Art von Dokumentation ist der Unsicherheitsfaktor Mensch. Die vollständige Dokumentation und zeitnahe Freigabe und Archivierung der Prozessdaten durch Mitarbeiter sind nicht immer gewährleistet. Zumal hier auch ein großer Zeit- und Kostenaufwand entsteht. Ganz zu schweigen von der Platzproblematik. Die ganzen Papierausdrucke müssen ja nachvollziehbar archiviert werden und auf Verlangen der zuständigen Behörde vorzuweisen sein. Ebenso als Nachteil ist die Abhängigkeit von Verbrauchsmaterial (Farbband, Toner, Papier) anzusehen. Die aufgeführten Nachteile können am Besten durch Automatisierung umgangen werden. Die Daten können mit einer entsprechenden Dokumentationssoftware (z. B. der SegoSoft) automatisch und vor allem papierlos kontrolliert, dokumentiert und archiviert werden.
17 Welche Vorteile hat die Dokumentation der Instrumentenaufbereitung über die serielle Schnittstelle (RS 232) in Verbindung mit der Dokumentationssoftware SegoSoft Die Prozessdatenübertragung erfolgt automatisch, da die Software den Programmstart und das -ende des Aufbereitungsprogrammes erkennt. Am Ende angelangt, erscheint automatisch ein Freigabedialog auf dem Bildschirm, mit dessen Hilfe eine zeitnahe Freigabe der aufbereiteten Instrumente von der verantwortlichen Person durchgeführt werden kann. Die Freigabe zu vergessen ist praktisch unmöglich. Sämtliche Prozessdaten werden aufgezeichnet und in Form einer PDF/A-1-Datei für die Archivierung nach dem deutschen Signaturgesetz 2 Nr. 2 SigG manipulationsgeschützt gesichert. Durch diese Automatisierung kann viel Zeit und somit auch Kosten gespart werden. Die aufgezeichneten Prozessdaten können direkt an gängige Praxismanagement- und Patientenverwaltungssysteme angebunden werden, sodass problemlos eine Behandlungsdokumentation durchgeführt werden kann. Ein wesentlicher Vorteil der SegoSoft ist ebenfalls die einfache Anbindung von über 300 verschiedenen Aufbereitungsgeräten über die bereits vorhandene EDV und der Ausdruck von Barcode-Etiketten für das Anbringen wichtiger Informationen wie z. B. Chargennummer, Mindesthaltbarkeit, etc. auf die Sterilverpackungen. Beim Verwenden der Instrumente am Patienten können mit Hilfe eines Scanners und der Erweiterung SegoAssign die Informationen in die digitale Patientenkarte aufgenommen werden.
18 18 19 Behandlungsdokumentation, PC-Anbindung Wie funktioniert der patientenbezogene Nachweis der Instrumentenaufbereitung mit der SegoSoft Mit der Erweiterung SegoAssign werden die rechtssicheren Hygienedokumente der Sterilisationschargen direkt dem Patienten zugeordnet. SegoAssign integriert sich direkt in die digitale Patientenakte des in der Praxis verwendeten Praxismanagement- und Patientenverwaltungssystems. Die Zuweisung zum Patienten erfolgt schnell und einfach von jedem beliebigen Arbeitsplatz aus. Allein über das Öffnen der Eingabemaske in der Behandlungsakte werden automatisch die Patientenund Behandlungsdaten übernommen. Für die Zuordnung der Sterilisationschargen zum jeweiligen Patienten werden mithilfe eines Scanners die vorhandenen Barcode- Etiketten eingelesen. Alternativ besteht natürlich auch die Möglichkeit einer manuellen Eingabe von Chargennummern, Bemerkungen und anderen relevanten Daten. Durch die direkte Verfügbarkeit von SegoAssign innerhalb der digitalen Patienten- und Behandlungsakte können jederzeit die am betreffenden Patienten eingesetzten Sterilisationschargen nachvollzogen werden. Welche technischen Lösungen gibt es zur Anbindung eines Medizingerätes mit dem PC Es gibt die Direktanbindung des Medizingerätes über die serielle Schnittstelle am PC. Die maximale Länge dieser Verbindung beträgt jedoch nur ca. 13 Meter und die maximale Anzahl der anschließbaren Geräte ist durch die Anzahl der seriellen Schnittstellen des eingesetzten PCs begrenzt. Dann gibt es noch die Möglichkeit das Medizingerät mithilfe des SegoConnect Moduls an den PC anzuschließen. Einmal über die Direktanbindung, dann beträgt die maximale Länge der Standard-Ethernet- Implementation ca. 100 Meter oder über die Netzwerkanbindung. Hier ist die maximale Länge der Verbindung netzwerkspezifisch und die maximale Anzahl der anschließbaren Geräte unbegrenzt.
19
20 Video Comcotec Messtechnik GmbH Gutenbergstraße 3 D Unterschleißheim info@segosoft.info Phone Fax: info@comcotec.info Comcotec, the Comcotec logo, SegoSoft, the SegoSoft logo are registered trademarks of Comcotec Messtechnik GmbH. All other product names are trademarks of their respective companies All rights reserved. Art.-Nr
Dokumentation der Instrumentenaufbereitung
 Dokumentation der Instrumentenaufbereitung Fragen und Antworten zu Gesetzen, Vorgaben, Verordnungen sowie der Reinigung, Desinfektion und Sterilisation von Instrumenten Heike Reinstädler ist seit 1992
Dokumentation der Instrumentenaufbereitung Fragen und Antworten zu Gesetzen, Vorgaben, Verordnungen sowie der Reinigung, Desinfektion und Sterilisation von Instrumenten Heike Reinstädler ist seit 1992
IMC Systems GmbH. Instrumentenaufbereitung CHECKLISTE. Rechtsgrundlagen. Zahnarztpraxis. Infektionsschutz - Gesetz. Medizinprodukte Gesetz.
 IMC Systems GmbH CHECKLISTE zur Sicherung und Weiterentwicklung von Qualität und Leistung in der Zahnheilkunde gemäß der aktuellen Gesetzte, Verordnungen, Normen, Richtlinien und Empfehlungen Rechtsgrundlagen
IMC Systems GmbH CHECKLISTE zur Sicherung und Weiterentwicklung von Qualität und Leistung in der Zahnheilkunde gemäß der aktuellen Gesetzte, Verordnungen, Normen, Richtlinien und Empfehlungen Rechtsgrundlagen
Aufbereitung v. Medizinprodukten
 1. ULTRASCHALL (optional) 2. REINIGUNG 2. REINIGUNG 3. DESINFEKTION 3. DESINFEKTION & SPÜLUNG 4. KONTROLLE 5. SIEGELGERÄT 6. STERILISATOR Die Rechtsgrundlagen Die Aufbereitung ist definiert durch folgende
1. ULTRASCHALL (optional) 2. REINIGUNG 2. REINIGUNG 3. DESINFEKTION 3. DESINFEKTION & SPÜLUNG 4. KONTROLLE 5. SIEGELGERÄT 6. STERILISATOR Die Rechtsgrundlagen Die Aufbereitung ist definiert durch folgende
Podiumsdiskussion. Dr. Früh Control GmbH DGSV-Kongress
 Podiumsdiskussion Dr. Früh Control GmbH DGSV-Kongress 10-09 1 Generelle Vorgaben für Medizinprodukte Medizinprodukte-Gesetz 14: Medizinprodukte dürfen nicht betrieben und angewendet werden, wenn sie Mängel
Podiumsdiskussion Dr. Früh Control GmbH DGSV-Kongress 10-09 1 Generelle Vorgaben für Medizinprodukte Medizinprodukte-Gesetz 14: Medizinprodukte dürfen nicht betrieben und angewendet werden, wenn sie Mängel
Instrumentenaufbereitung sicher dokumentiert
 Instrumentenaufbereitung sicher dokumentiert Vorteile & Service Recht & Sicherheit Funktion SegoSoft das ideale Werkzeug zur Dokumentation Die anwenderfreundliche SegoSoft-Software ist einfach zu installieren
Instrumentenaufbereitung sicher dokumentiert Vorteile & Service Recht & Sicherheit Funktion SegoSoft das ideale Werkzeug zur Dokumentation Die anwenderfreundliche SegoSoft-Software ist einfach zu installieren
Dokumentation in der MP- Aufbereitung mit dem Schwerpunkt Endoskopie Vortrag beim AMAH
 Dokumentation in der MP- Aufbereitung mit dem Schwerpunkt Endoskopie Vortrag beim AMAH Olympus Deutschland Medical Systems Jesco Danylow, Produktmanagement Hannover, 11. Juni 2016 Inhalt 1. Einführung
Dokumentation in der MP- Aufbereitung mit dem Schwerpunkt Endoskopie Vortrag beim AMAH Olympus Deutschland Medical Systems Jesco Danylow, Produktmanagement Hannover, 11. Juni 2016 Inhalt 1. Einführung
Aufbereitung von Instrumenten und Medizinprodukten
 Dritter Hygienetag der Kassenärztlichen Vereinigung Bayerns Nürnberg, 10.Mai 2014 Aufbereitung von Instrumenten und Medizinprodukten Vortrag: Validierung der Instrumentenaufbereitung in der Arztpraxis;
Dritter Hygienetag der Kassenärztlichen Vereinigung Bayerns Nürnberg, 10.Mai 2014 Aufbereitung von Instrumenten und Medizinprodukten Vortrag: Validierung der Instrumentenaufbereitung in der Arztpraxis;
Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis
 Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis Ute Wurmstich gilborn zahnärzte Kaltenweider Str. 11 D-30900 Wedemark Fachkunde I-III DGSV/SGSV 1 Grundsätzliche
Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis Ute Wurmstich gilborn zahnärzte Kaltenweider Str. 11 D-30900 Wedemark Fachkunde I-III DGSV/SGSV 1 Grundsätzliche
Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung
 Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung Dipl.-Kfm. Matthias Klar, IfB Hagenow Tel. 0160 96420022 1 4 Absatz 1 MP BetreibV
Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung Dipl.-Kfm. Matthias Klar, IfB Hagenow Tel. 0160 96420022 1 4 Absatz 1 MP BetreibV
ZSVA: Zertifizierung + Barcode Klinikum Heidenheim
 ZSVA: Zertifizierung + Barcode Klinikum Heidenheim Jürgen Bierlein Ltg. ZSVA Wir stellen uns Vor 11.1 VZ-Stellen auf 12 Mitarbeiter Ca. 45.000 StE im Jahr Betriebszeit von 6.00-21.00h Rufbereitschaft am
ZSVA: Zertifizierung + Barcode Klinikum Heidenheim Jürgen Bierlein Ltg. ZSVA Wir stellen uns Vor 11.1 VZ-Stellen auf 12 Mitarbeiter Ca. 45.000 StE im Jahr Betriebszeit von 6.00-21.00h Rufbereitschaft am
Dokumentation und Freigabe
 MELAG informiert Dokumentation und Freigabe Stichworte: Dokumentation, FreIgabe, Bowie&Dick-Test, Helix- Test, Kennzeichnung von Sterilgut, Vakuumtest, Leerkammer- Sterilisation Sehr geehrte Frau Doktor,
MELAG informiert Dokumentation und Freigabe Stichworte: Dokumentation, FreIgabe, Bowie&Dick-Test, Helix- Test, Kennzeichnung von Sterilgut, Vakuumtest, Leerkammer- Sterilisation Sehr geehrte Frau Doktor,
Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und Aufbereitungsverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen
 Seite 1 von 8 Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und sverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen Inhalt: Unterscheidung aufgrund von Verwendungszweck und sverfahren Risikobewertung
Seite 1 von 8 Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und sverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen Inhalt: Unterscheidung aufgrund von Verwendungszweck und sverfahren Risikobewertung
8. Hygieneforum Osthessen "Hygiene in der Zahnarztpraxis"
 8. Hygieneforum Osthessen "Hygiene in der Zahnarztpraxis" Aufbereitung von Medizinprodukten in der Zahnarztpraxis Überwachung durch das Regierungspräsidiums Kassel Dipl. -Ing. (FH) Ilker Büyükok, MHBA
8. Hygieneforum Osthessen "Hygiene in der Zahnarztpraxis" Aufbereitung von Medizinprodukten in der Zahnarztpraxis Überwachung durch das Regierungspräsidiums Kassel Dipl. -Ing. (FH) Ilker Büyükok, MHBA
W&H Schweiz. Geschäftsführung W&H Schweiz. Instrumentenaufbereitung Hygieneschulung. Seite 1
 W&H Schweiz Dany Badstuber Geschäftsführung W&H Schweiz Instrumentenaufbereitung Hygieneschulung > Sterilisation gemäß Referenznorm EN13060: Zyklus/Ladungstypen > Erste und wiederkehrende Validierung von
W&H Schweiz Dany Badstuber Geschäftsführung W&H Schweiz Instrumentenaufbereitung Hygieneschulung > Sterilisation gemäß Referenznorm EN13060: Zyklus/Ladungstypen > Erste und wiederkehrende Validierung von
Neue gesetzliche Anforderungen für Reinigungs- und Desinfektionsgeräte und deren Bedeutung für den Betreiber
 Neue gesetzliche Anforderungen für Reinigungs- und Desinfektionsgeräte und deren Bedeutung für den Betreiber (am Beispiel des Steckbeckenspülers) Referent: Frank Hoffmann Leiter Vertrieb Deutschland Reinigungs-
Neue gesetzliche Anforderungen für Reinigungs- und Desinfektionsgeräte und deren Bedeutung für den Betreiber (am Beispiel des Steckbeckenspülers) Referent: Frank Hoffmann Leiter Vertrieb Deutschland Reinigungs-
ÜBERWACHUNG DER AUFBEREITUNG VON MEDIZINPRODUKTEN. im Bereich der Zahnheilkunde. Gliederung
 ÜBERWACHUNG DER AUFBEREITUNG VON MEDIZINPRODUKTEN im Bereich der Zahnheilkunde Referat 25 Ärztliche und pharmazeutische Angelegenheiten 26. März 2014 Gliederung Rechtliche Grundlagen für Betreiber und
ÜBERWACHUNG DER AUFBEREITUNG VON MEDIZINPRODUKTEN im Bereich der Zahnheilkunde Referat 25 Ärztliche und pharmazeutische Angelegenheiten 26. März 2014 Gliederung Rechtliche Grundlagen für Betreiber und
Anforderungen an die Aufbereitung von Medizinprodukten Gesundheitssystem Pflichten Reinigung Desinfektion Sterilisation Haftung
 Positionspapier Anforderungen an die Aufbereitung von Medizinprodukten Pflichten der Hersteller und Pflichten der GesundheitssystemAufbereitun Pflichten Reinigung Desinfektion Sterilisation Haftung Hygiene
Positionspapier Anforderungen an die Aufbereitung von Medizinprodukten Pflichten der Hersteller und Pflichten der GesundheitssystemAufbereitun Pflichten Reinigung Desinfektion Sterilisation Haftung Hygiene
Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels
 Professionelle Aufbereitung von Medizinprodukten Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels Grundaussagen zur Validierung (1)
Professionelle Aufbereitung von Medizinprodukten Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels Grundaussagen zur Validierung (1)
Zahl der Units.. Zahl der Behandler.. in Stellenprozenten.. % davon Zahnärzte.. in Stellenprozenten.. % davon DH / PA.. in Stellenprozenten.. % ...
 Kommission für Praxishygiene und Umweltschutz Stabsstelle Postgasse 19, Postfach, 3000 Bern 8 Telefon 031 310 20 80 Fax 031 310 20 82 E-Mail info@sso.ch www.sso.ch Schweizerische Zahnärzte-Gesellschaft
Kommission für Praxishygiene und Umweltschutz Stabsstelle Postgasse 19, Postfach, 3000 Bern 8 Telefon 031 310 20 80 Fax 031 310 20 82 E-Mail info@sso.ch www.sso.ch Schweizerische Zahnärzte-Gesellschaft
Die Sicht des Gesetzgebers
 Essen, 23. Februar 2005 Aufbereitung von Medizinprodukten die Verantwortung des Herstellers und des Anwenders Die Sicht des Gesetzgebers Bundesministerium für Gesundheit und Soziale Sicherung 1 Gliederung
Essen, 23. Februar 2005 Aufbereitung von Medizinprodukten die Verantwortung des Herstellers und des Anwenders Die Sicht des Gesetzgebers Bundesministerium für Gesundheit und Soziale Sicherung 1 Gliederung
Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen. Referent: Dipl.-Ing. Burkhard Schulze
 Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen Referent: Dipl.-Ing. Burkhard Schulze Definition: Aufbereitung Reinigung, Desinfektion und Sterilisation von bestimmungsgemäß
Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen Referent: Dipl.-Ing. Burkhard Schulze Definition: Aufbereitung Reinigung, Desinfektion und Sterilisation von bestimmungsgemäß
Praktische Umsetzung in der Handhabung von Medizinprodukten
 Praktische Umsetzung in der Handhabung von Medizinprodukten Andreas Clarin Hygieneakademie Ruhr, Essen Definition Medizinprodukte ( 3 MPG) Medizinprodukte sind alle Instrumente, Apparate, Vorrichtungen,
Praktische Umsetzung in der Handhabung von Medizinprodukten Andreas Clarin Hygieneakademie Ruhr, Essen Definition Medizinprodukte ( 3 MPG) Medizinprodukte sind alle Instrumente, Apparate, Vorrichtungen,
Erfahrungen aus der Zertifizierung
 DGSV-Kongress 2010 08.10.2010, Fulda Erfahrungen aus der Zertifizierung von Qualitätsmanagement-Systemen nach DIN EN ISO 13485 für die Aufbereitung von Medizinprodukten Dr. Thomas Kießling Sachverständiger
DGSV-Kongress 2010 08.10.2010, Fulda Erfahrungen aus der Zertifizierung von Qualitätsmanagement-Systemen nach DIN EN ISO 13485 für die Aufbereitung von Medizinprodukten Dr. Thomas Kießling Sachverständiger
Bernd Vogler Fachauditor für hygienische Aufbereitung
 Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
AMAH Aufbereitung in der Endoskopie
 AMAH Aufbereitung in der Endoskopie Risikobewertung von flexiblen Endoskopen und Folgerungen für die Aufbereitung Christian Roth Olympus Deutschland GmbH OLYMPUS Deutschland GmbH, Medical Systems Hannover,
AMAH Aufbereitung in der Endoskopie Risikobewertung von flexiblen Endoskopen und Folgerungen für die Aufbereitung Christian Roth Olympus Deutschland GmbH OLYMPUS Deutschland GmbH, Medical Systems Hannover,
Medizinproduktebuch. Blatt 1. Geräte-Stammdaten Funktionsprüfung Geräteeinweisung... 4
 Medizinproduktebuch Nach 7 MPBetreibV für Medizinprodukte 1 Für das Gerät Inhalt Blatt 1. Geräte-Stammdaten... 2 2. Funktionsprüfung... 3 3. Geräteeinweisung... 4 3.1 Einweisung der vom Betreiber beauftragten
Medizinproduktebuch Nach 7 MPBetreibV für Medizinprodukte 1 Für das Gerät Inhalt Blatt 1. Geräte-Stammdaten... 2 2. Funktionsprüfung... 3 3. Geräteeinweisung... 4 3.1 Einweisung der vom Betreiber beauftragten
Bernd Vogler Fachauditor für hygienische Aufbereitung
 Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
MELA quick 12+ Kompakt. Schnell. Stark.
 MELA quick 12+ Kompakt. Schnell. Stark. Die Anforderung. Die Anforderungen an die Aufbereitung zahnärztlicher Instrumente werden vom Robert-Koch-Institut (RKI) definiert. Übertragungsinstrumente für den»semikritischen«einsatz
MELA quick 12+ Kompakt. Schnell. Stark. Die Anforderung. Die Anforderungen an die Aufbereitung zahnärztlicher Instrumente werden vom Robert-Koch-Institut (RKI) definiert. Übertragungsinstrumente für den»semikritischen«einsatz
Aufbereitung von Medizinprodukten- Inspektionsergebnisse im Freistaat Sachsen
 Aufbereitung von Medizinprodukten- Inspektionsergebnisse im Freistaat Sachsen Andreas Modes Landesdirektion Dresden Arbeitsschutz- Außenstelle Chemnitz Lothar Streit Straße 24 08056 Zwickau Tel.: 0375/
Aufbereitung von Medizinprodukten- Inspektionsergebnisse im Freistaat Sachsen Andreas Modes Landesdirektion Dresden Arbeitsschutz- Außenstelle Chemnitz Lothar Streit Straße 24 08056 Zwickau Tel.: 0375/
Verfahrensanweisung: Hygienische Aufbereitung von Medizinprodukten
 Seite 1 von 5 1 Zweck... 1 2 Geltungsbereich... 1 3 Abkürzungen... 2 4 Definitionen... 2 5 Beschreibung... 4 5.1 Allgemeines... 4 5.2 Zuständigkeiten und Verantwortlichkeiten... 4 5.3 Ablauf einer Überwachung
Seite 1 von 5 1 Zweck... 1 2 Geltungsbereich... 1 3 Abkürzungen... 2 4 Definitionen... 2 5 Beschreibung... 4 5.1 Allgemeines... 4 5.2 Zuständigkeiten und Verantwortlichkeiten... 4 5.3 Ablauf einer Überwachung
Validierung, validiertes Verfahren
 MELAG informiert Validierung, validiertes Verfahren Validierung von Sterilisationsprozessen von Praxis-Autoklaven, EN 17665, Erst-Validierung, Re-Validierung Sehr geehrte Frau Doktor, Sehr geehrter Herr
MELAG informiert Validierung, validiertes Verfahren Validierung von Sterilisationsprozessen von Praxis-Autoklaven, EN 17665, Erst-Validierung, Re-Validierung Sehr geehrte Frau Doktor, Sehr geehrter Herr
Unser Fortbildungsprogramm für die zahnärztliche und ärztliche Praxis
 EINLADUNG Hygienefortbildung Unser Fortbildungsprogramm für die zahnärztliche und ärztliche Praxis Sachkunde in der zahnärztlichen und ärztlichen Praxis (inkl. Hygienebeauftragte) Hygiene und Aufbereitung
EINLADUNG Hygienefortbildung Unser Fortbildungsprogramm für die zahnärztliche und ärztliche Praxis Sachkunde in der zahnärztlichen und ärztlichen Praxis (inkl. Hygienebeauftragte) Hygiene und Aufbereitung
ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN
 Zentrale Sterilgut-Versorgung, Geschäftsbereich Bau, Technik und Medizintechnik C 5 ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN Toni Zanette Leiter Zentrale Sterilgutversorgung C 5 Rechtliche Anforderungen
Zentrale Sterilgut-Versorgung, Geschäftsbereich Bau, Technik und Medizintechnik C 5 ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN Toni Zanette Leiter Zentrale Sterilgutversorgung C 5 Rechtliche Anforderungen
Dokumentation und Freigabe
 MELAG informiert Dokumentation und Freigabe Stichworte: Dokumentation, Bowie&Dick-Test, Helix-Test, Kennzeichnung von Sterilgut, Vakuumtest, Leerkammer-Sterilisation Sehr geehrte Frau Doktor, Sehr geehrter
MELAG informiert Dokumentation und Freigabe Stichworte: Dokumentation, Bowie&Dick-Test, Helix-Test, Kennzeichnung von Sterilgut, Vakuumtest, Leerkammer-Sterilisation Sehr geehrte Frau Doktor, Sehr geehrter
Umsetzung des Medizinprodukterechts
 Landesamt für Gesundheit und Soziales Abteilung Arbeitsschutz und technische Sicherheit Stofflicher Gefahrenschutz, Strahlenschutz, Verbraucherschutz in der Medizin Umsetzung des Medizinprodukterechts
Landesamt für Gesundheit und Soziales Abteilung Arbeitsschutz und technische Sicherheit Stofflicher Gefahrenschutz, Strahlenschutz, Verbraucherschutz in der Medizin Umsetzung des Medizinprodukterechts
Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie
 Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie Rechtliche Abgrenzung zwischen Podologie und Fußpflege Ziele des Medizinprodukterechtes: für die Gesundheit und den erforderlichen
Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie Rechtliche Abgrenzung zwischen Podologie und Fußpflege Ziele des Medizinprodukterechtes: für die Gesundheit und den erforderlichen
DECKBLATT. Selbstauskunft von Einrichtungen für ambulantes Operieren
 DECKBLATT (diese Seite bitte nicht an HLPUG senden!) Selbstauskunft von Einrichtungen für ambulantes Operieren für die Erhebung der Qualität des Hygienemanagements auf Grundlage des Infektionsschutzgesetzes
DECKBLATT (diese Seite bitte nicht an HLPUG senden!) Selbstauskunft von Einrichtungen für ambulantes Operieren für die Erhebung der Qualität des Hygienemanagements auf Grundlage des Infektionsschutzgesetzes
Intensivschulung Endoskope von KARL STORZ für ZSVA-Leiter. KARL STORZ Tuttlingen Schulungszentrum Oktober 2012.
 Intensivschulung Endoskope von KARL STORZ für ZSVA-Leiter KARL STORZ Tuttlingen Schulungszentrum 8. 12. Oktober 2012 MIC-Instrumente Aufgaben und Ziel Grundlagen Reinigung, Desinfektion, Trocknung Sterilisation
Intensivschulung Endoskope von KARL STORZ für ZSVA-Leiter KARL STORZ Tuttlingen Schulungszentrum 8. 12. Oktober 2012 MIC-Instrumente Aufgaben und Ziel Grundlagen Reinigung, Desinfektion, Trocknung Sterilisation
Dokumentieren Intelligente Dokumentations-Software für jederzeit nachvollziehbare Prozessabläufe.
 Reinigen/Desinfizieren Innovative Reinigungs- und Desinfektionsautomaten mit individuellen Einsätzen, abgestimmter Prozess-Chemie und effizienter Wasseraufbereitung. Dokumentieren Intelligente Dokumentations-Software
Reinigen/Desinfizieren Innovative Reinigungs- und Desinfektionsautomaten mit individuellen Einsätzen, abgestimmter Prozess-Chemie und effizienter Wasseraufbereitung. Dokumentieren Intelligente Dokumentations-Software
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ)
 Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
9.5 Medizinprodukte-Betreiberverordnung - MPBetreibV
 9.5 -Betreiberverordnung - MPBetreibV Die -Betreiberverordnung (MPBetreibV) regelt das Errichten, Betreiben und Anwenden von n und von Zubehör für. Zubehör sind Gegenstände, Stoffe, Zubereitungen aus Stoffen
9.5 -Betreiberverordnung - MPBetreibV Die -Betreiberverordnung (MPBetreibV) regelt das Errichten, Betreiben und Anwenden von n und von Zubehör für. Zubehör sind Gegenstände, Stoffe, Zubereitungen aus Stoffen
Umgang mit unsteril angelieferten Implantaten
 Kreiskrankenhaus Erding mit Klinik Dorfen Akademisches Lehrkrankenhaus Technische Universität München Umgang mit unsteril angelieferten Implantaten Birgit Wagener 03. März 2011 Gliederung 1. Vorstellung
Kreiskrankenhaus Erding mit Klinik Dorfen Akademisches Lehrkrankenhaus Technische Universität München Umgang mit unsteril angelieferten Implantaten Birgit Wagener 03. März 2011 Gliederung 1. Vorstellung
Hygienemanagement und Praxisbegehungen
 Hygienemanagement und Praxisbegehungen Sind Sie vorbereitet? 1 Hygiene und MPG in 45 Minuten? Dr. Kai Voss, Kirchbarkau Vizepräsident Vorstand Qualitätsmanagement Mitglied im Ausschuss Hygiene Mitglied
Hygienemanagement und Praxisbegehungen Sind Sie vorbereitet? 1 Hygiene und MPG in 45 Minuten? Dr. Kai Voss, Kirchbarkau Vizepräsident Vorstand Qualitätsmanagement Mitglied im Ausschuss Hygiene Mitglied
Überwachung und Begehung durch die Gewerbeaufsicht Niedersachsen
 Behörde für betrieblichen Arbeits-, Umwelt- und Verbraucherschutz Überwachung und Begehung durch die Gewerbeaufsicht Niedersachsen AMAH 27.06.2015 Fragen, die der Vortrag beantworten soll Warum dürfen
Behörde für betrieblichen Arbeits-, Umwelt- und Verbraucherschutz Überwachung und Begehung durch die Gewerbeaufsicht Niedersachsen AMAH 27.06.2015 Fragen, die der Vortrag beantworten soll Warum dürfen
Anforderungen an die hygienische Aufbereitung von Medizinprodukten in NRW
 Anforderungen an die hygienische Aufbereitung von Medizinprodukten in NRW Dr. med. univ. Sebastian Werner 1,2 1 HygCen Germany GmbH, Schwerin / Bochum 2 Abteilung für Hygiene, Sozial- und Umweltmedizin,
Anforderungen an die hygienische Aufbereitung von Medizinprodukten in NRW Dr. med. univ. Sebastian Werner 1,2 1 HygCen Germany GmbH, Schwerin / Bochum 2 Abteilung für Hygiene, Sozial- und Umweltmedizin,
Aufbereitung von MIC- und Hohlkörper-Instrumenten
 Arbeitskreis Medizinprodukte Aufbereitung Hannover 14. Juni 2014 Aufbereitung von MIC- und Hohlkörper-Instrumenten Jörn Krämer Vertrieb Webeco GmbH An der Trave 14 23923 Selmsdorf Tel.: 0451-2807212 Mobil
Arbeitskreis Medizinprodukte Aufbereitung Hannover 14. Juni 2014 Aufbereitung von MIC- und Hohlkörper-Instrumenten Jörn Krämer Vertrieb Webeco GmbH An der Trave 14 23923 Selmsdorf Tel.: 0451-2807212 Mobil
Die Prüfung der Ausgangsstoffe. Eine Hilfe zur Umsetzung
 Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung Gesetzliche Vorgaben Apothekenbetriebsordnung (ApBetrO) Arzneimittel, die in der Apotheke hergestellt werden, müssen die nach der pharmazeutischen
Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung Gesetzliche Vorgaben Apothekenbetriebsordnung (ApBetrO) Arzneimittel, die in der Apotheke hergestellt werden, müssen die nach der pharmazeutischen
Verantwortung und Haftung der ärztlichen Leitung in Praxis und MVZ. Verteilung der Beweislast bei Hygienemängeln in der Arztpraxis
 Verantwortung und Haftung der ärztlichen Leitung in Praxis und MVZ Verteilung der Beweislast bei Hygienemängeln in der Arztpraxis Dritter Hygienetag der KVB 10. Mai 2014 in Nürnberg Petra Geistberger Rechtsanwältin
Verantwortung und Haftung der ärztlichen Leitung in Praxis und MVZ Verteilung der Beweislast bei Hygienemängeln in der Arztpraxis Dritter Hygienetag der KVB 10. Mai 2014 in Nürnberg Petra Geistberger Rechtsanwältin
Aufzeichnungen nach 9a Tierschutzgesetz
 Aufzeichnungen nach 9a Tierschutzgesetz Gertrud Klumpp 10. Mai 2012 5. Fortbildungsveranstaltung der GV-SOLAS für Tierschutzbeauftragte und Behördenmitglieder Tierschutzgesetz 9 a Aufzeichnungen Über die
Aufzeichnungen nach 9a Tierschutzgesetz Gertrud Klumpp 10. Mai 2012 5. Fortbildungsveranstaltung der GV-SOLAS für Tierschutzbeauftragte und Behördenmitglieder Tierschutzgesetz 9 a Aufzeichnungen Über die
Bedienungsanweisung für MELAdoc-Etikettendrucker
 Bedienungsanweisung für MELAdoc-Etikettendrucker Sehr geehrte Frau Doktor, sehr geehrter Herr Doktor, mit MELAdoc haben Sie ein Gerät erworben, das noch vor wenigen Jahren in der Arzt- oder Zahnarztpraxis
Bedienungsanweisung für MELAdoc-Etikettendrucker Sehr geehrte Frau Doktor, sehr geehrter Herr Doktor, mit MELAdoc haben Sie ein Gerät erworben, das noch vor wenigen Jahren in der Arzt- oder Zahnarztpraxis
Ausstattung Praxis 1 : Bohrerbad, Tauchdesinfektion (= chem. Desinfektion), Autoklav mit Gravitationsverfahren
 Anlage 23 Beispiele für die Aufbereitung von Medizinprodukten Nachdem der Praxisinhaber den prinzipiellen Ablauf der Aufbereitung vorbereitet hat, muss er nun unter seinen individuellen Praxisbedingungen
Anlage 23 Beispiele für die Aufbereitung von Medizinprodukten Nachdem der Praxisinhaber den prinzipiellen Ablauf der Aufbereitung vorbereitet hat, muss er nun unter seinen individuellen Praxisbedingungen
Internistische Thorakoskopie - Anmerkungen aus der Sicht der Krankenhaushygiene
 Internistische Thorakoskopie - Anmerkungen aus der Sicht der Krankenhaushygiene Dr. Silvia Fanghänel 17.10.2013 Grundsätzliche Hygieneanforderungen Richtlinien, Empfehlungen, DIN Management von Patienten
Internistische Thorakoskopie - Anmerkungen aus der Sicht der Krankenhaushygiene Dr. Silvia Fanghänel 17.10.2013 Grundsätzliche Hygieneanforderungen Richtlinien, Empfehlungen, DIN Management von Patienten
Clinic-Master / Vital-Master B C R. Medizinproduktebuch. Walitschek Medizintechnik GmbH 2013 Rev. 1
 B C R Medizinproduktebuch B C R R 1 Hersteller/manufacturer: Walitschek Medizintechnik GmbH Fuldablick 3 D-34355 Staufenberg Tel: 05543 4558 Email: info@clinic-master.com B C R 0044 2 Inhalt Medizinproduktebuch
B C R Medizinproduktebuch B C R R 1 Hersteller/manufacturer: Walitschek Medizintechnik GmbH Fuldablick 3 D-34355 Staufenberg Tel: 05543 4558 Email: info@clinic-master.com B C R 0044 2 Inhalt Medizinproduktebuch
Skalpell, Spritze oder Koloskop. Mehrfach verwenden eine sichere Sache?!
 Infektionen im Krankenhaus Pro Jahr erleiden in Deutschland ca. 600.000 800.000 Patienten Infektionen, die sie sich im Krankenhaus zuziehen. Nosokomiale Infektionen Ca. 50.000 Patienten sterben an diesen
Infektionen im Krankenhaus Pro Jahr erleiden in Deutschland ca. 600.000 800.000 Patienten Infektionen, die sie sich im Krankenhaus zuziehen. Nosokomiale Infektionen Ca. 50.000 Patienten sterben an diesen
Die Aufbereitung zahnärztlicher Instrumente
 Die Aufbereitung zahnärztlicher Instrumente Autor: Dr. Gerd Leidig, QM-Berater und Auditor, Mailadresse: gerd.leidig@online.de Rechtliche Grundlagen Die Aufbereitung... ist unter Berücksichtigung der Angaben
Die Aufbereitung zahnärztlicher Instrumente Autor: Dr. Gerd Leidig, QM-Berater und Auditor, Mailadresse: gerd.leidig@online.de Rechtliche Grundlagen Die Aufbereitung... ist unter Berücksichtigung der Angaben
Die Kombination von Medizinprodukten. SystemCheck
 Die Kombination von Medizinprodukten SystemCheck Fachtagung der FKT 12.06.2008 Untertitel Die Prüfung und Bewertung von medizinischen elektrischen Systemen mit rechtssicherer Dokumentation zum Schutz von
Die Kombination von Medizinprodukten SystemCheck Fachtagung der FKT 12.06.2008 Untertitel Die Prüfung und Bewertung von medizinischen elektrischen Systemen mit rechtssicherer Dokumentation zum Schutz von
Einsatzort: Name LehrgangsteilnehmerIn: Name der Leitung Aufbereitungseinheit: Name MentorIn:
 Tätigkeitskatalog "Aufbereitung von Medizinprodukten" im Fachkundelehrgang I Nachweis der praktischen Tätigkeiten nach Zulassungsvoraussetzungen der DGSV e.v./sgsv (gültig ab 01.01.2013) Der Lehrgangsteilnehmer
Tätigkeitskatalog "Aufbereitung von Medizinprodukten" im Fachkundelehrgang I Nachweis der praktischen Tätigkeiten nach Zulassungsvoraussetzungen der DGSV e.v./sgsv (gültig ab 01.01.2013) Der Lehrgangsteilnehmer
Medizinproduktbuch 1
 1 Vertrieb: EyeNovation GmbH Heidsieker Heide 90 33739 Bielefeld Tel: 05206/6031-0 Fax: 05206/6031-11 Hersteller: CenterVue SpA v. Tommaseo 77 35131 Padova - Italy Tel: +39 049 781 1828 Fax: +39 049 781
1 Vertrieb: EyeNovation GmbH Heidsieker Heide 90 33739 Bielefeld Tel: 05206/6031-0 Fax: 05206/6031-11 Hersteller: CenterVue SpA v. Tommaseo 77 35131 Padova - Italy Tel: +39 049 781 1828 Fax: +39 049 781
Reinigungs- und Desinfektionsgeräte (RDG)/ Sterilisatoren 8
 Die Aufbereitung von bestimmungsgemäß keimarm oder steril zur Anwendung kommenden Medizinprodukten ist unter Berücksichtigung der Angaben des Herstellers mit geeigneten validierten Verfahren so durchzuführen,
Die Aufbereitung von bestimmungsgemäß keimarm oder steril zur Anwendung kommenden Medizinprodukten ist unter Berücksichtigung der Angaben des Herstellers mit geeigneten validierten Verfahren so durchzuführen,
Lagerungsschränke mit geregelten Umgebungsbedingungen für aufbereitete, thermolabile Endoskope (Trockenschrank) - Validierung und Typprüfung
 Lagerungsschränke mit geregelten Umgebungsbedingungen für aufbereitete, thermolabile Endoskope (Trockenschrank) - Validierung und Typprüfung M. Feltgen, S. Werner HygCen Germany GmbH, Schwerin / Bochum
Lagerungsschränke mit geregelten Umgebungsbedingungen für aufbereitete, thermolabile Endoskope (Trockenschrank) - Validierung und Typprüfung M. Feltgen, S. Werner HygCen Germany GmbH, Schwerin / Bochum
Übersicht über ISO 9001:2000
 Übersicht über die ISO 9001:2000 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe Übersicht über die ISO 9001:2000 4 Qualitätsmanagementsystem 5 Verantwortung der Leitung 6 Management
Übersicht über die ISO 9001:2000 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe Übersicht über die ISO 9001:2000 4 Qualitätsmanagementsystem 5 Verantwortung der Leitung 6 Management
Aus der Praxis - für die Praxis
 MELAG informiert - Humanmedizin - Aus der Praxis - für die Praxis Stichworte: Chargenkontrolle, Bio-/ Chemoindikatoren; Lagerdauer von Sterilgut; Sterilraum-Anordnung; Wasser-Aufbereitung; Sehr geehrte
MELAG informiert - Humanmedizin - Aus der Praxis - für die Praxis Stichworte: Chargenkontrolle, Bio-/ Chemoindikatoren; Lagerdauer von Sterilgut; Sterilraum-Anordnung; Wasser-Aufbereitung; Sehr geehrte
Medizinproduktegesetz
 Medizinproduktegesetz Anforderungen an maschinelle Reinigung und Desinfektion A. Prozesse Die Prozesse der Reinigung und Desinfektion von Medizinprodukten sind grundsätzlich zu validieren. Dazu sind qualifizierte
Medizinproduktegesetz Anforderungen an maschinelle Reinigung und Desinfektion A. Prozesse Die Prozesse der Reinigung und Desinfektion von Medizinprodukten sind grundsätzlich zu validieren. Dazu sind qualifizierte
Überprüfung der Aufbereitung von Medizinprodukten in Krankenanstalten im Rahmen der sanitären Aufsicht
 Überprüfung der Aufbereitung von Medizinprodukten in Krankenanstalten im Rahmen der sanitären Aufsicht Prof. Dr. Elisabeth Presterl MBA Medizinische Universität Wien Klin. Inst. f. Krankenhaushygiene Indirekte
Überprüfung der Aufbereitung von Medizinprodukten in Krankenanstalten im Rahmen der sanitären Aufsicht Prof. Dr. Elisabeth Presterl MBA Medizinische Universität Wien Klin. Inst. f. Krankenhaushygiene Indirekte
NACHWEISBARE UND QUALITÄTSSICHERE AUFBEREITUNG VON MEDIZINPRODUKTEN
 NACHWEISBARE UND QUALITÄTSSICHERE AUFBEREITUNG VON MEDIZINPRODUKTEN Anke Carter, Münchener Medizin Mechanik GmbH, Planegg, Deutschland Anke.Carter@mmmgroup.com Zusammenfassung Der nachweisbaren und qualitätssicheren
NACHWEISBARE UND QUALITÄTSSICHERE AUFBEREITUNG VON MEDIZINPRODUKTEN Anke Carter, Münchener Medizin Mechanik GmbH, Planegg, Deutschland Anke.Carter@mmmgroup.com Zusammenfassung Der nachweisbaren und qualitätssicheren
Medizintechnologie.de. Hygiene von Medizinprodukten. Hygiene, Anforderungen und Umsetzungen
 Medizintechnologie.de Hygiene von Medizinprodukten Jährlich infizieren sich circa 600.000 Patienten im Krankenhaus mit einer Nosokomialinfektion. 15.000 davon sterben. Ein hohes Lebensalter, eine vorhandene
Medizintechnologie.de Hygiene von Medizinprodukten Jährlich infizieren sich circa 600.000 Patienten im Krankenhaus mit einer Nosokomialinfektion. 15.000 davon sterben. Ein hohes Lebensalter, eine vorhandene
RoMed Klinikum Rosenheim: Bad Aibling, Prien am Chiemsee, Wasserburg am Inn und Rosenheim
 RoMed Klinikum Rosenheim: Bad Aibling, Prien am Chiemsee, Wasserburg am Inn und Rosenheim Irmgard Weise RoMed Klinikum Rosenheim OP-Fachschwester Fachkunde I III Lehrerin für Pflegeberufe Schwerpunkt Aus
RoMed Klinikum Rosenheim: Bad Aibling, Prien am Chiemsee, Wasserburg am Inn und Rosenheim Irmgard Weise RoMed Klinikum Rosenheim OP-Fachschwester Fachkunde I III Lehrerin für Pflegeberufe Schwerpunkt Aus
Formblatt MPBetreibV: Betrieb Medizinprodukte Nicht geprüfte Punkte sind zu streichen oder als nicht geprüft zu kennzeichnen.
 Dienststelle: Sachbearbeiter(-in): Datum der Überwachung: Formblatt MPBetreibV: Betrieb Medizinprodukte Nicht geprüfte Punkte sind zu streichen oder als nicht geprüft zu kennzeichnen. 1. Name und Anschrift
Dienststelle: Sachbearbeiter(-in): Datum der Überwachung: Formblatt MPBetreibV: Betrieb Medizinprodukte Nicht geprüfte Punkte sind zu streichen oder als nicht geprüft zu kennzeichnen. 1. Name und Anschrift
Sterilgutversorgung Qualität durch Kompetenz
 Sterilgutversorgung Qualität durch Kompetenz Eine Dienstleistung der Immanuel Diakonie 7. Kommissionierung und Bereitstellung Nach definierten Fahrplänen werden die Sterilgüter von bewährten externen Transportdienstleistern,
Sterilgutversorgung Qualität durch Kompetenz Eine Dienstleistung der Immanuel Diakonie 7. Kommissionierung und Bereitstellung Nach definierten Fahrplänen werden die Sterilgüter von bewährten externen Transportdienstleistern,
Aktueller Leitfaden zur Sterilgutaufbereitung in der Praxis mit Produktübersicht
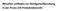 Aktueller Leitfaden zur Sterilgutaufbereitung in der Praxis mit Produktübersicht Annahme von benutztem Sterilgut Geschlossene Lagerung/ Anwendung 9 Sortierung nach - Aufbereitungsart - Einsatzzweck 1 unrein
Aktueller Leitfaden zur Sterilgutaufbereitung in der Praxis mit Produktübersicht Annahme von benutztem Sterilgut Geschlossene Lagerung/ Anwendung 9 Sortierung nach - Aufbereitungsart - Einsatzzweck 1 unrein
Sterilisation von Medizinprodukten
 Autoklaven MDA-Serie1-12 STE Sterilisation von Medizinprodukten...schnell, sicher und effizient Ihr kompetenter Hersteller von Autoklaven und Gefriertrocknungsanlagen für Labor, Medizin, Pharma und Industrie...mehr
Autoklaven MDA-Serie1-12 STE Sterilisation von Medizinprodukten...schnell, sicher und effizient Ihr kompetenter Hersteller von Autoklaven und Gefriertrocknungsanlagen für Labor, Medizin, Pharma und Industrie...mehr
Gerätequalifizierung IQ/OQ/PQ
 Gerätequalifizierung IQ/OQ/PQ Gerätequalifizierung im Rahmen von Qualitätsmanagement oder Validierung ist bei einer Vielzahl von Unternehmen unabdingbare Voraussetzung für eine Lieferantenentscheidung.
Gerätequalifizierung IQ/OQ/PQ Gerätequalifizierung im Rahmen von Qualitätsmanagement oder Validierung ist bei einer Vielzahl von Unternehmen unabdingbare Voraussetzung für eine Lieferantenentscheidung.
Änderungen der MPBetreibV 2014
 Änderungen der MPBetreibV 2014 3 Instandhaltung von Medizinprodukten (1) Die Instandhaltung von Medizinprodukten umfasst insbesondere Instandhaltungsmaßnahmen und die Instandsetzung. Instandhaltungsmaßnahmen
Änderungen der MPBetreibV 2014 3 Instandhaltung von Medizinprodukten (1) Die Instandhaltung von Medizinprodukten umfasst insbesondere Instandhaltungsmaßnahmen und die Instandsetzung. Instandhaltungsmaßnahmen
aseptica Aufbereitung von Medizinprodukten in Arzt- und Zahnarztpraxen
 aseptica 2 11 Sonderdruck aseptica Aufbereitung von Medizinprodukten in Arzt- und Zahnarztpraxen I. Wälter-Bergob Sonderdruck Juli 2011 www.aseptica.com Instrumentenkreislauf Praxishygiene und Qualitätsmanagement
aseptica 2 11 Sonderdruck aseptica Aufbereitung von Medizinprodukten in Arzt- und Zahnarztpraxen I. Wälter-Bergob Sonderdruck Juli 2011 www.aseptica.com Instrumentenkreislauf Praxishygiene und Qualitätsmanagement
Wichtige Punkte der Qualitätssicherung in einer ärztlichen Privatapotheke
 Gesundheitsdirektion Wichtige Punkte der Qualitätssicherung in einer ärztlichen Privatapotheke Symposium Vereinigung Zürcher Internisten Universität Irchel 28. Januar 2016 Janine Arvedson, Heilmittelinspektorin
Gesundheitsdirektion Wichtige Punkte der Qualitätssicherung in einer ärztlichen Privatapotheke Symposium Vereinigung Zürcher Internisten Universität Irchel 28. Januar 2016 Janine Arvedson, Heilmittelinspektorin
Sterilisationsprozesse mit Wasserstoffperoxid
 Sterilisationsprozesse mit Wasserstoffperoxid Grundlagen der Prozessführung und Validierung im Vergleich zur Dampfsterilisation Kernfrage zur Validierung von H 2 O 2 -Sterilisationsprozessen Warum wird
Sterilisationsprozesse mit Wasserstoffperoxid Grundlagen der Prozessführung und Validierung im Vergleich zur Dampfsterilisation Kernfrage zur Validierung von H 2 O 2 -Sterilisationsprozessen Warum wird
Erfahrungen der. DQS GmbH. bei der Zertifizierung von Medizinprodukteherstellern
 Erfahrungen der DQS GmbH bei der Zertifizierung von Medizinprodukteherstellern 2004-11-24, Seite 1 Normensituation Medizinprodukte DIN EN ISO 9001:94 DIN EN ISO 9001:2000 DIN EN 46001/2:1996 DIN EN ISO
Erfahrungen der DQS GmbH bei der Zertifizierung von Medizinprodukteherstellern 2004-11-24, Seite 1 Normensituation Medizinprodukte DIN EN ISO 9001:94 DIN EN ISO 9001:2000 DIN EN 46001/2:1996 DIN EN ISO
Herstellerinformation zur Aufbereitung von resterilisierbaren
 Medizinprodukten gemäß EN ISO 17664 1 von 5 WARNHINWEISE: Bei Einhaltung der Gebrauchsanweisung der zur Anwendung kommenden Geräte sowie der zur Anwendung kommenden Desinfektions- und Reinigungslösungen
Medizinprodukten gemäß EN ISO 17664 1 von 5 WARNHINWEISE: Bei Einhaltung der Gebrauchsanweisung der zur Anwendung kommenden Geräte sowie der zur Anwendung kommenden Desinfektions- und Reinigungslösungen
Einsatzort: Name Lehrgangsteilnehmer/in: Name der Leitung Aufbereitungseinheit: Name Mentor/in:
 Tätigkeitskatalog "Aufbereitung von Medizinprodukten" im Fachkundelehrgang I Nachweis der praktischen Tätigkeiten nach Zulassungsvoraussetzungen der DGSV e.v./sgsv (vorliegende Version 03 ist gültig ab
Tätigkeitskatalog "Aufbereitung von Medizinprodukten" im Fachkundelehrgang I Nachweis der praktischen Tätigkeiten nach Zulassungsvoraussetzungen der DGSV e.v./sgsv (vorliegende Version 03 ist gültig ab
Sachkenntnis-Lehrgang Hygienemanagement/Aufbereitung von Medizinprodukten
 Die erfolgreiche Teilnahme am Sachkenntnis-Lehrgang Hygienemanagement/Aufbereitung von Medizinprodukten gibt den Teilnehmern die notwendige Sicherheit, als Hygienebeauftragter und/oder Beauftragter für
Die erfolgreiche Teilnahme am Sachkenntnis-Lehrgang Hygienemanagement/Aufbereitung von Medizinprodukten gibt den Teilnehmern die notwendige Sicherheit, als Hygienebeauftragter und/oder Beauftragter für
A smart, hygienic decision. Instrumentenaufbereitung sicher dokumentiert
 A smart, hygienic decision Instrumentenaufbereitung sicher dokumentiert Zertifikat Nummer: BSI-DSZ-CC-0930-2014 Vorwort Hygiene ist einer der Grundpfeiler ärztlichen Handelns. Sie ist die wichtigste vorbeugende
A smart, hygienic decision Instrumentenaufbereitung sicher dokumentiert Zertifikat Nummer: BSI-DSZ-CC-0930-2014 Vorwort Hygiene ist einer der Grundpfeiler ärztlichen Handelns. Sie ist die wichtigste vorbeugende
Chargendokumentation: High-End für die chirurgische Praxis
 Neue Materialien und Methoden 39 M. Keweloh Chargendokumentation: High-End für die chirurgische Praxis Einleitung: Abbildung 1 Startmaske. (Fotos: M. Keweloh) Nachweisbare Qualitätssicherung in chirurgischen
Neue Materialien und Methoden 39 M. Keweloh Chargendokumentation: High-End für die chirurgische Praxis Einleitung: Abbildung 1 Startmaske. (Fotos: M. Keweloh) Nachweisbare Qualitätssicherung in chirurgischen
Aufbereitung von Medizinprodukten
 R K I - R I C H T L I N I E N Aufbereitung von Medizinprodukten Erläuterungen zu der Übersicht Nachfolgend veröffentlichen wir eine Übersicht zur Aufbereitung von Medizinprodukten der Gruppen semikritisch
R K I - R I C H T L I N I E N Aufbereitung von Medizinprodukten Erläuterungen zu der Übersicht Nachfolgend veröffentlichen wir eine Übersicht zur Aufbereitung von Medizinprodukten der Gruppen semikritisch
SERVICE. Checkliste. Für Hygiene-Begehungen von Zahnarztpraxen und Praxen für Mund-, Kiefer- und Gesichtschirurgie
 PRAXIS SERVICE Checkliste Für Hygiene-Begehungen von Zahnarztpraxen und Praxen für Mund-, Kiefer- und Gesichtschirurgie PRAXIS Kundennummer (falls vorhanden) Datum der Begehung: Uhrzeit der Begehung: Praxisstempel
PRAXIS SERVICE Checkliste Für Hygiene-Begehungen von Zahnarztpraxen und Praxen für Mund-, Kiefer- und Gesichtschirurgie PRAXIS Kundennummer (falls vorhanden) Datum der Begehung: Uhrzeit der Begehung: Praxisstempel
ÖGSV Fachtagung 2013 Thea Enko
 ÖGSV Fachtagung 2013 Thea Enko Leitlinie zur Auswahl von aufbereitbaren Medizinprodukten Ziel: Beschaffung optimieren Fehlkäufe vermeiden Hilfestellung bei der Beschaffung von aufbereitbaren Medizinprodukten
ÖGSV Fachtagung 2013 Thea Enko Leitlinie zur Auswahl von aufbereitbaren Medizinprodukten Ziel: Beschaffung optimieren Fehlkäufe vermeiden Hilfestellung bei der Beschaffung von aufbereitbaren Medizinprodukten
Medizinproduktegesetz
 Medizinproduktegesetz IB. 006_V.1 Anforderungen an das Betreiben von Dampfsterilisatoren A. Dampfsterilisationsverfahren sind grundsätzlich nach den allgemein anerkannten Regeln der Technik (z.b. einschlägige
Medizinproduktegesetz IB. 006_V.1 Anforderungen an das Betreiben von Dampfsterilisatoren A. Dampfsterilisationsverfahren sind grundsätzlich nach den allgemein anerkannten Regeln der Technik (z.b. einschlägige
Validierung der Software Anwendung für das Instrumentenmanagement und die Prozessdokumentation
 Validierung der Software Anwendung für das Instrumentenmanagement und die Prozessdokumentation Präsentation von Markus Geissmann anlässlich der 7èmes Journées Nationales Suissessursur la Stérilisation
Validierung der Software Anwendung für das Instrumentenmanagement und die Prozessdokumentation Präsentation von Markus Geissmann anlässlich der 7èmes Journées Nationales Suissessursur la Stérilisation
Landesamt für f r soziale Dienste - Abt. Gesundheitsschutz - Schleswig-Holstein. Erfahrungsbericht
 RiliBÄK 2008 Erfahrungsbericht Zuständige Behörde in Ministerium für Soziales, Gesundheit, Familie, Jugend und Senioren Landesamt für soziale Dienste Schleswig- Holstein - Abteilung Gesundheitsschutz -
RiliBÄK 2008 Erfahrungsbericht Zuständige Behörde in Ministerium für Soziales, Gesundheit, Familie, Jugend und Senioren Landesamt für soziale Dienste Schleswig- Holstein - Abteilung Gesundheitsschutz -
Medizinprodukte-Überwachung im Land Bremen
 Medizinprodukte-Überwachung im Land Bremen Wiederaufbereitung in HNO- und urologischen Arztpraxen durch die Senatorin für Arbeit, Frauen, Gesundheit, Jugend und Soziales, Referat 34, als zuständige Behörde
Medizinprodukte-Überwachung im Land Bremen Wiederaufbereitung in HNO- und urologischen Arztpraxen durch die Senatorin für Arbeit, Frauen, Gesundheit, Jugend und Soziales, Referat 34, als zuständige Behörde
Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit?
 Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit? S. Werner, F. v. Rheinbaben HygCen Germany GmbH, Schwerin / Bochum 13.04.2016 DGKH Kongress Berlin
Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit? S. Werner, F. v. Rheinbaben HygCen Germany GmbH, Schwerin / Bochum 13.04.2016 DGKH Kongress Berlin
Verantwortung t bei der Aufbereitung von Medizinprodukten
 5. Schweizerische Fachtage über die Sterilisation, 3. 4. Juni 2009 Verantwortung t bei der Aufbereitung von Medizinprodukten aus Sicht der Behörde Markus Weiss Inspektor Swissmedic, Abteilung Medizinprodukte
5. Schweizerische Fachtage über die Sterilisation, 3. 4. Juni 2009 Verantwortung t bei der Aufbereitung von Medizinprodukten aus Sicht der Behörde Markus Weiss Inspektor Swissmedic, Abteilung Medizinprodukte
1/2/3 das elektronische Abfallnachweisverfahren. Einfach, sicher, effizient. im Unternehmensverbund der Entsorgung Dortmund GmbH
 1/2/3 das elektronische Abfallnachweisverfahren mit der DOGA Einfach, sicher, effizient. im Unternehmensverbund der Entsorgung Dortmund GmbH Ist-Zustand 1. April 2010: elektronische Nachweisund Registerführung
1/2/3 das elektronische Abfallnachweisverfahren mit der DOGA Einfach, sicher, effizient. im Unternehmensverbund der Entsorgung Dortmund GmbH Ist-Zustand 1. April 2010: elektronische Nachweisund Registerführung
6 Instrumentenhygiene/Aufbereitung von Medizinprodukten
 6 Instrumentenhygiene/Aufbereitung von Medizinprodukten Komplexe Instrumententechnik Gesetzliche Regelungen MPG 140 Die moderne Medizin ist ohne ihre technische Ausrüstung nicht mehr denkbar. Letztere
6 Instrumentenhygiene/Aufbereitung von Medizinprodukten Komplexe Instrumententechnik Gesetzliche Regelungen MPG 140 Die moderne Medizin ist ohne ihre technische Ausrüstung nicht mehr denkbar. Letztere
Hygienestraße. Die neue Qualität bei der Reinigung von Hilfsmitteln und Medizinprodukten
 Hygienestraße Die neue Qualität bei der Reinigung von Hilfsmitteln und Medizinprodukten Herausforderung Krankenhausinfektion Reinigung von Hilfsmitteln und Medizinprodukten Krankenhausinfektionen bedeuten
Hygienestraße Die neue Qualität bei der Reinigung von Hilfsmitteln und Medizinprodukten Herausforderung Krankenhausinfektion Reinigung von Hilfsmitteln und Medizinprodukten Krankenhausinfektionen bedeuten
DOKUMENTATION Protokollieren Auswerten Sortieren Freigeben
 DOKUMENTATION Protokollieren Auswerten Sortieren Freigeben MELAflash MELAnet Box MELAview MELAsoft MELAdoc MELAprint MELAcontrol MELAcontrol PRO competence in hygiene MELAflash CF-Card-Printer MELAnet
DOKUMENTATION Protokollieren Auswerten Sortieren Freigeben MELAflash MELAnet Box MELAview MELAsoft MELAdoc MELAprint MELAcontrol MELAcontrol PRO competence in hygiene MELAflash CF-Card-Printer MELAnet
Errichten. Sterilisation+Desinfektion+Reinigung von MP
 Medizinproduktegesetz (MPG) 1.1.1997 Klinische Bewertung + Prüfung Herstellung Funktionstüchtigkeit Inbetriebnahme Instandhaltung Errichten Betrieb Inverkehrbringen Leistungsfähigkeit Überwachung Sicherheit
Medizinproduktegesetz (MPG) 1.1.1997 Klinische Bewertung + Prüfung Herstellung Funktionstüchtigkeit Inbetriebnahme Instandhaltung Errichten Betrieb Inverkehrbringen Leistungsfähigkeit Überwachung Sicherheit
Medizinprodukte - Aufbereitung in Deutschland - im 17. Jahr nach der Einführung des
 Medizinprodukte - Aufbereitung in Deutschland - im 17. Jahr nach der Einführung des MPG Beantwortete und offene Fragen Prof. Dr. M. Mielke, RKI Patientenschutz bei Medizinprodukten Verpflichtung der Migliedstaaten
Medizinprodukte - Aufbereitung in Deutschland - im 17. Jahr nach der Einführung des MPG Beantwortete und offene Fragen Prof. Dr. M. Mielke, RKI Patientenschutz bei Medizinprodukten Verpflichtung der Migliedstaaten
Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Aufbereitung von Medizinprodukten
 Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Aufbereitung von Medizinprodukten Geltungsbereich: Die vorliegenden Speziellen Regeln legen Anforderungen fest an Zertifizierungsstellen
Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Aufbereitung von Medizinprodukten Geltungsbereich: Die vorliegenden Speziellen Regeln legen Anforderungen fest an Zertifizierungsstellen
Validierung von Heißsiegelprozessen nach DIN EN ISO 11607-2
 Validierung von Heißsiegelprozessen nach DIN EN ISO 11607-2 Ralph Ebersbach Vortrag auf dem 3. Berlin/Brandenburger Steritreff am 15. September 2012 in Berlin Mehr wissen. Weiter denken. Über HYBETA HYBETA
Validierung von Heißsiegelprozessen nach DIN EN ISO 11607-2 Ralph Ebersbach Vortrag auf dem 3. Berlin/Brandenburger Steritreff am 15. September 2012 in Berlin Mehr wissen. Weiter denken. Über HYBETA HYBETA
