Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P )
|
|
|
- Maike Baumgartner
- vor 5 Jahren
- Abrufe
Transkript
1 Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P ) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Salze Experiment: Saure, neutrale und alkalische Reaktionen von Salzlösungen Schwierigkeitsgrad Vorbereitungszeit Durchführungszeit empfohlene Gruppengröße Leicht 10 Minuten 10 Minuten 1 Schüler/Student Zusätzlich wird benötigt: Versuchsvarianten: ph-wert- Bestimmung mit ph-papier Schlagwörter: Salzlösungen, ph-wert Lehrerinformationen Einführung Prinzip Im Allgemeinen lässt sich aus der Stärke bzw. Schwäche der Säuren und Basen, aus welchen die Salze hergestellt wurden, der ph-wert ableiten. Salze aus gleich starken Säuren und Basen (z.b. NaCl) reagieren in wässriger Lösung neutral. Wohingegen Salze aus einer schwachen Säure/Base sowie starken Base/Säure entweder alkalisch oder sauer reagieren (z.b. reagiert Natriumacetat aus schwacher Essigsäure und starker Natronlauge alkalisch). Diese lässt sich dadurch erkläen, dass Salze in Wasser gelöst, dabei in der Lösung vollständig oder teilweise dissoziiert werden. Die Anionen und Kationen der gelösten Salze können unabhängig voneinander mit Wasser in Wechselwirkung treten und so eine saure, neutrale oder alkalische Reaktion hervorrufen. In diesem Versuch werden mit Hilfe eines geeigneten Indikators (Lackmuss-Lösung) der ph-wert der hergestellten Salzlösungen bestimmt. Dabei werden die ph-werte von Salzen untersucht, was zu einem besseren Verständnis über die Eigenschaften von Salzen in wässriger Lösung bei Schülerinnen und Schülern führt. Versuchsaufbau
2 Lernziele Die Schüler sollen durch dieses Experiment herausfinden, welche Salze neutral, sauer oder alkalisch reagieren. Vorwissen Die Schüler sollten mit den Reaktionsmechanismen von Säuren und Basen vertraut sein. Die Funktionsweise volumetrischer Messinstrumente (Messpipette, Bürette, Pipettierball) sollte den Schülern bekannt sein. Hinweise zu Aufbau und Durchführung Die Salzlösungen müssen nicht einheitlich konzentriert sein, es sollte aber auf Zugabe der angegebenen Wassermenge geachtet werden. Die als Musterlösung in den Ergebnissen angeführten ph-werte sind konzentrationsabhängig. Entsorgung Die verwendeten Lösungen können im Sammelbehälter für Säure- und Basen-Abfälle entsorgt werden. Ergebnisübersicht Musterergebnis
3 Material Position Material Bestellnr. Menge 1 Kaliumhydrogensulfat 250 g Eisen-III-chlorid-6-Hydrat 500 g Natriumdisulfit, reinst 250 g Reagenzglasgestell mit 6 Bohrungen, d = 31 mm, Holz Natriumsulfat Decahydrat 500 g Ammoniumsulfat, reinst 250 g Lackmuslösung, 100 ml Pasteurpipetten, l = 145 mm, 250 Stück Ammoniumchlorid, reinst 250 g Kaliumcarbonat,reinst 250 g Natriumnitrat, reinst 250 g Wasser, destilliert 5 l Kaliumdihydrogenphosphat 100 g Natriumacetat Trihydrat 250 g Natriumcarbonat, wasserfrei, 250g Natriumchlorid, reinst 500 g Gummihütchen, 10 Stück Löffelspatel, Stahl, l = 150 mm Reagenzglas, d=30 mm, l=200 mm, DURAN,1 Stück Spritzflasche, 500 ml, Kunststoff Glasrührstab, Boro 3.3, l = 300 mm, d = 7 mm
4 Sicherheitshinweise H- und P-Sätze Gefahren Säuren und Laugen wirken ätzend! Die verwendeten Salze sind teilweise gesundheitsschädlich. Nicht verschlucken! Nach dem Versuch sorgfältig die Hände waschen Unbedingt Schutzbrille tragen!
5 Einführung Anwendung und Aufgabe Saure, alkalische und neutrale Salze Anwendung Bei einer Neutralisationsreaktion (Umsetzung einer Säure mit einer Lauge) entstehen Wasser und das entsprechende Salz als Produkt. Reagiert eine starke Säure (z.b. Salzsäure) mit einer starken Base (z.b. Natronlauge), so bildet sich Natriumchlorid und Wasser. Der ph-wert dieser Lösung ist hierbei neutral. Es gibt jedoch Salze, die in wässrigen Lösungen saure oder alkalische ph-werte haben. Auch im Alltag begegnet man den Eigenschaften von Salzen. Als Hobbygärtner weiß man, wenn Pflanzen im Garten nicht ausreichend wachsen, muss man das alkalische Salz Calciumcarbonat zur Gartenerde hinzufügen, um sie zu entsäuern. Aufgabe Versuchsaufbau In diesem Versuch werden unterschiedlliche Salzlösungen hergestellt und mit einem geeigneten Indikator (Lackmus-Lösung) die ph-werte der Salzlösungen bestimmt und somit den Salzlösungen zugeordnet, ob sie in Wasser saure, neutrale oder alkaische Reaktionen zeigen.
6 Material Position Material Bestellnr. Menge 1 Kaliumhydrogensulfat 250 g Eisen-III-chlorid-6-Hydrat 500 g Natriumdisulfit, reinst 250 g Reagenzglasgestell mit 6 Bohrungen, d = 31 mm, Holz Natriumsulfat Decahydrat 500 g Ammoniumsulfat, reinst 250 g Lackmuslösung, 100 ml Pasteurpipetten, l = 145 mm, 250 Stück Ammoniumchlorid, reinst 250 g Kaliumcarbonat,reinst 250 g Natriumnitrat, reinst 250 g Wasser, destilliert 5 l Kaliumdihydrogenphosphat 100 g Natriumacetat Trihydrat 250 g Natriumcarbonat, wasserfrei, 250g Natriumchlorid, reinst 500 g Gummihütchen, 10 Stück Löffelspatel, Stahl, l = 150 mm Reagenzglas, d=30 mm, l=200 mm, DURAN,1 Stück Spritzflasche, 500 ml, Kunststoff Glasrührstab, Boro 3.3, l = 300 mm, d = 7 mm
7 Aufbau und Durchführung Aufbau Gefahren Säuren und Laugen wirken ätzend! Die verwendeten Salze sind teilweise gesundheitsschädlich. Nicht verschlucken! Nach dem Versuch sorgfältig die Hände waschen Unbedingt Schutzbrille tragen! Aufbau Nummeriere die Reagenzgläser von 1 bis 6 (Abb. 1) und stelle die Reagenzgläser nebeneinander in das Reagenzglasgestell (Abb. 2). Abb. 1 Abb. 2 Durchführung 1. Saure Reaktion von Salzlösungen Durchführung Im ersten Schritt werden die benötigen Salzlösungen hergestellt. Durch Zugabe von je einer Spatelspitze Substanz in mit Wasser gefüllte Reagenzgläser werden die entsprechenden Salzlösungen hergestellt. Dazu wird in die nummerierten Reagenzgläser jeweils eine Spatelspitze (Abb. 3) der aufgeführten Salze gegeben. Anschließend werden die Reagenzgläser zu einem Drittel mit destilliertem Wasser (Abb. 4) gefüllt. 1. Ammoniumsulfat 2. Ammoniumchlorid 3. Eisen(III)chlorid 4. Kaliumhydrogenphosphat 5. Kaliumhydrogensulfat 6. Natriumdisulfit
8 Abb. 3 Abb. 4 Für eine optimale Versuchsdurchführung sollen die Salze in Wasser gelöst sein (eventuell durch kräftiges Schütteln). Zur Bestimmung des ph-wertes werden die Salzlösungen in den Reagenzgläser mit einigen Tropfen Lackmuslösung versetzt (Abb. 5). Abb. 5 Anhand der Frärbung der Lösung (durch den Indikator) kann nun der ph-wert der jeweiligen Salzlösungen bestimmt werden. Gegebenfalls kann ph-papier verwendet werden, um den genauen ph-wert zu bestimmen. 2. Neutrale Reaktion von Salzlösungen Durchführung Im ersten Schritt werden die benötigen Salzlösungen hergestellt. Durch Zugabe von je einer Spatelspitze Substanz in mit Wasser gefüllte Reagenzgläser werden die entsprechenden Salzlösungen hergestellt. Dazu wird in die nummerierten Reagenzgläser jeweils eine Spatelspitze (Abb. 3) der aufgeführten Salze gegeben. Anschließend werden die Reagenzgläser zu einem Drittel mit destilliertem Wasser (Abb. 4) gefüllt. 1. Natriumchlorid 2. Natriumnitrat 3. Natriumsulfat 3. Alkalische (Basische) Reaktion von Salzlösungen Durchführung Im ersten Schritt werden die benötigen Salzlösungen hergestellt. Durch Zugabe von je einer Spatelspitze Substanz in mit Wasser gefüllte Reagenzgläser werden die entsprechenden Salzlösungen hergestellt. Dazu wird in die nummerierten Reagenzgläser jeweils eine Spatelspitze (Abb. 3) der aufgeführten Salze gegeben. Anschließend werden die Reagenzgläser zu einem Drittel mit destilliertem Wasser (Abb. 4) gefüllt.
9 1. Natriumacetat 2. Natriumcarbonat 3. Kaliumcarbonat
10 Beobachtung und Auswertung Beobachtung 1. Saure Reaktionen von Salzlösungen Durch Zugabe von Lackmusslösung zu den Salzlösungen (Lösungen von Ammoniumsulfat, Ammoniumchlorid, Eisenchlorid, Kaliumhydrogenphosphat und Natriumdisulfit) färben sich die Lösungen rot. Das bedeutet, dass die entsprechenden Salzlösungen sauer reagieren. Dies lässt sich auch mit einem ph-papier bestätigen. 2. Neutrale Reaktion von Salzlösungen Durch Zugabe von Lackmusslösung zu den Salzlösungen (Lösungen von Natriumchlorid, Natriumnitrat und Natriumsulfat) färben sich die Lösungen violett. Das bedeutet, dass die entsprechenden Salzlösungen neutral reagieren. Dies lässt sich auch mit einem ph-papier bestätigen. 3. Alkalische (basische) Reaktion von Salzlösungen Durch Zugabe von Lackmusslösung zu den Salzlösungen (Lösungen von Natriumacetat, Natriumcarbonat und Kaliumcarbonat) färben sich die Lösungen blau. Das bedeutet, dass die entsprechenden Salzlösungen alkalisch reagieren. Dies lässt sich auch mit einem ph-papier bestätigen. Auswertung Die Salze werden in Wasser gelöst, dabei sind die Salze anschließend in der Lösung vollständig dissoziiert. Die Anionen und Kationen der gelösten Salze können unabhängig voneinander mit Wasser in Wechselwirkung treten und so eine saure, neutrale oder alkalische Reaktion hervorrufen. Neutrale Reaktion von Salzlösungen Die Ionen (bzw. Anionen) starker Säuren wie Cl-, SO42-, NO3- und Ionen (bzw. Kationen) starker Basen wie Na+ und K+ bleiben vollständig in Wasser dissoziiert und beeinflussen den ph-wert nicht. Daher zeigen Salzlösungen von Natriumchlorid, Natriumnitrat und Natriumsulfat in wärssigen Lösungen einen neutralen Charakter. Allgemein gilt, dass die Salze, die aus starken Säuren und starken Basen entstanden sind, in wässriger Lösung Ionen bilden, die nicht protolysiert werden können (bzw. selbst keine Protonen abgegen). Die Lösung solcher Salze reagiert damit neutral. Saure Reaktion von Salzlösungen Ionen schwacher Säuren oder schwacher Laugen liegen im Gegensatz zu starken Säuren/Laugen im Gleichgewicht zu einem bestimmten Anteil undissoziiert vor. Um das Gleichgewicht zu erreichen, müssen sie also Protonen an das Wasser abgeben oder dem Wasser entziehen und verändern dadurch den ph-wert der wässrigen Salzlösung. So bildet beispielsweise Ammoniumchlorid bei der Dissoziation das stabile Chloridion Cl- (Anion einer starken Säure) und die Kationensäure NH4+. Diese Kationensäure kann gem. nachfolgender Gleichung Protonen an das Wasser abgeben. Eisen(III)ionen neigen in wässriger Lösung stark dazu, aquotisierte Komplexe zu bilden. Dabei findet auch eine Hydrolyse des Komplexes statt, der durch folgende Gleichung beschrieben werden kann: Diesem (Hydrolyse-) Schritt können weitere folgen, so dass eine wässrige Lösung von Eisen(III)chlorid stark sauer reagiert (ph- Wert einer 0,1 M Lösung beträgt ca. 2). Dihydrogenphosphat- oder Hydrogensulfationen sind Anionensäuren, die in wässriger Lösung noch Protonen abspalten können. Daher reagieren wässriger Kaliumdihydrogenphosphat- bzw. Kaliumhydrogensulfat-Lösungen sauer Alkalische (basische) Reaktion von Salzlösungen Salze, die durch die Umsetzung schwacher Säuren mit starken Basen dargestellt wurden, bilden in wässriger Lösung teils die undissoziierte Säure zurück und reagieren daher alkalisch (aufgrund der Hydroxid-Ionen in Lösung)
3.5 Hydrolyse von Salzen. Aufgabe. Reagieren wässrige Salzlösungen neutral? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
Anionen-Nachweis durch Fällungsreaktionen
 Lehrer-/Dozentenblatt Anionen-Nachweis durch Fällungsreaktionen (Artikelnr.: P7511300) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Allgemeine Chemie- Einführung
Lehrer-/Dozentenblatt Anionen-Nachweis durch Fällungsreaktionen (Artikelnr.: P7511300) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Allgemeine Chemie- Einführung
Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren (Artikelnr.: P )
 Lehrer-/Dozentenblatt Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren (Artikelnr.: P7510200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Lehrer-/Dozentenblatt Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren (Artikelnr.: P7510200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Wirkung von Säuren auf Metalle (Artikelnr.: P )
 Lehrer-/Dozentenblatt Wirkung von Säuren auf Metalle (Artikelnr.: P7157500) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Säuren
Lehrer-/Dozentenblatt Wirkung von Säuren auf Metalle (Artikelnr.: P7157500) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Säuren
Lösungen, Kolloide, Suspensionen (Artikelnr.: P )
 Lehrer-/Dozentenblatt Lösungen, Kolloide, Suspensionen (Artikelnr.: P7154800) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Wasser
Lehrer-/Dozentenblatt Lösungen, Kolloide, Suspensionen (Artikelnr.: P7154800) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Wasser
Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) (Artikelnr.: P )
 Lehrer-/Dozentenblatt Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) (Artikelnr.: P7158900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Lehrer-/Dozentenblatt Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) (Artikelnr.: P7158900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Säurestärke (Artikelnr.: P )
 Lehrer-/Dozentenblatt Säurestärke (Artikelnr.: P7157600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Säuren und Basen, Protonenübergänge
Lehrer-/Dozentenblatt Säurestärke (Artikelnr.: P7157600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Säuren und Basen, Protonenübergänge
Allgemeine Vorsichtsmaßnahmen beim Umgang mit Säuren (Artikelnr.: P )
 Lehrer-/Dozentenblatt Allgemeine Vorsichtsmaßnahmen beim Umgang mit Säuren (Artikelnr.: P757000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie
Lehrer-/Dozentenblatt Allgemeine Vorsichtsmaßnahmen beim Umgang mit Säuren (Artikelnr.: P757000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie
Salzbildung durch Reaktion von Säuren mit Laugen
 Lehrer-/Dozentenblatt Salzbildung durch Reaktion von Säuren mit Laugen (Artikelnr.: P7159400) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie
Lehrer-/Dozentenblatt Salzbildung durch Reaktion von Säuren mit Laugen (Artikelnr.: P7159400) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie
Herstellung und Eigenschaften von Natronlauge
 Lehrer-/Dozentenblatt Herstellung und Eigenschaften von Natronlauge (Artikelnr.: P759000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie Unterthema:
Lehrer-/Dozentenblatt Herstellung und Eigenschaften von Natronlauge (Artikelnr.: P759000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie Unterthema:
Leicht verdauliches und schwer verdauliches Eiweiß
 Lehrer-/Dozentenblatt Leicht verdauliches und schwer verdauliches Eiweiß (Artikelnr.: P8012900) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und
Lehrer-/Dozentenblatt Leicht verdauliches und schwer verdauliches Eiweiß (Artikelnr.: P8012900) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und
Bestimmung des pks-wertes einer schwachen Säure durch Halbtitration (Artikelnr.: P )
 Lehrer-/Dozentenblatt Bestimmung des pks-wertes einer schwachen Säure durch Halbtitration (Artikelnr.: P7511100) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Lehrer-/Dozentenblatt Bestimmung des pks-wertes einer schwachen Säure durch Halbtitration (Artikelnr.: P7511100) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Eiweißhaltige Nahrungsmittel (Artikelnr.: P )
 Lehrer-/Dozentenblatt Eiweißhaltige Nahrungsmittel (Artikelnr.: P8012600) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und Verdauung Unterthema:
Lehrer-/Dozentenblatt Eiweißhaltige Nahrungsmittel (Artikelnr.: P8012600) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und Verdauung Unterthema:
Die Verdauung im Magen (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die Verdauung im Magen (Artikelnr.: P8012800) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und Verdauung Unterthema: Verdauung
Lehrer-/Dozentenblatt Die Verdauung im Magen (Artikelnr.: P8012800) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und Verdauung Unterthema: Verdauung
Titration einer starken Säure mit einer starken Base unter Verwendung verschiedener Indikatoren
 Lehrer-/Dozentenblatt Titration einer starken Säure mit einer starken Base unter Verwendung verschiedener Indikatoren (Artikelnr.: P7510600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe:
Lehrer-/Dozentenblatt Titration einer starken Säure mit einer starken Base unter Verwendung verschiedener Indikatoren (Artikelnr.: P7510600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe:
Aufbau von Konzentrationsketten aus Kaliumchloridlösungen und Silber/Silberchloridelektroden (Artikelnr.: P )
 Aufbau von Konzentrationsketten aus Kaliumchloridlösungen und Silber/Silberchloridelektroden (Artikelnr.: P7401400) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema:
Aufbau von Konzentrationsketten aus Kaliumchloridlösungen und Silber/Silberchloridelektroden (Artikelnr.: P7401400) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema:
Rosa Geheimschrift. Durchführung
 Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Die Funktion der Keimblätter (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die Funktion der Keimblätter (Artikelnr.: P8011200) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Pflanzen Unterthema: Keimung und Wachstum
Lehrer-/Dozentenblatt Die Funktion der Keimblätter (Artikelnr.: P8011200) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Pflanzen Unterthema: Keimung und Wachstum
Zerlegung von Wasser durch Reduktionsmittel
 Lehrer-/Dozentenblatt Zerlegung von Wasser durch Reduktionsmittel (Artikelnr.: P7155500) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Lehrer-/Dozentenblatt Zerlegung von Wasser durch Reduktionsmittel (Artikelnr.: P7155500) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Vorsichtsmaßnahmen beim Umgang mit Laugen
 Lehrer-/Dozentenblatt Vorsichtsmaßnahmen beim Umgang mit Laugen (Artikelnr.: P7158600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Lehrer-/Dozentenblatt Vorsichtsmaßnahmen beim Umgang mit Laugen (Artikelnr.: P7158600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Untersuche die Wirkung verschiedener Säuren und Laugen auf natürliche und industriell hergestellte Indikatoren.
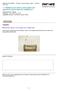 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157400) 1.5 Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:37:56
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157400) 1.5 Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:37:56
Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration (Landolt-Reaktion) (Artikelnr.: P )
 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration (Landolt-Reaktion) (Artikelnr.: P1149300) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische
Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration (Landolt-Reaktion) (Artikelnr.: P1149300) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische
Titration einer Pufferlösung gegen eine starke Säure mit Cobra4 (Artikelnr.: P )
 Lehrer-/Dozentenblatt Titration einer Pufferlösung gegen eine starke Säure mit Cobra4 (Artikelnr.: P7511562) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische
Lehrer-/Dozentenblatt Titration einer Pufferlösung gegen eine starke Säure mit Cobra4 (Artikelnr.: P7511562) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische
Stelle Salzlösungen her und überprüfe die Vorgänge beim Mischen der Lösungen.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P7159700) 3.4 Salzbildung durch Fällungsreaktion Experiment von: Phywe Gedruckt: 15.10.2013 12:20:35 intertess (Version 13.06 B200, Export
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P7159700) 3.4 Salzbildung durch Fällungsreaktion Experiment von: Phywe Gedruckt: 15.10.2013 12:20:35 intertess (Version 13.06 B200, Export
Gipsverarbeitung (Artikelnr.: P )
 Lehrer-/Dozentenblatt Gipsverarbeitung (Artikelnr.: P7155800) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Anorganische Chemie Unterthema: Spezialtehmen: Brandbekämpfung,
Lehrer-/Dozentenblatt Gipsverarbeitung (Artikelnr.: P7155800) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Anorganische Chemie Unterthema: Spezialtehmen: Brandbekämpfung,
8.1 Ammonium in Lakritz. Aufgabe. Warum schmecken Lakritze scharf? Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P )
 Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788200) 8. Ammonium in Lakritz Experiment von: Anouch Gedruckt: 28.02.204 :5:33 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788200) 8. Ammonium in Lakritz Experiment von: Anouch Gedruckt: 28.02.204 :5:33 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Einführung in die Elektronenübertragungsreaktion
 Lehrer-/Dozentenblatt Einführung in die Elektronenübertragungsreaktion (Artikelnr.: P1033000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie
Lehrer-/Dozentenblatt Einführung in die Elektronenübertragungsreaktion (Artikelnr.: P1033000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie
Die Verdauung im Mund (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die Verdauung im Mund (Artikelnr.: P8012700) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und Verdauung Unterthema: Verdauung
Lehrer-/Dozentenblatt Die Verdauung im Mund (Artikelnr.: P8012700) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und Verdauung Unterthema: Verdauung
Untersuche die Wirkung von verschiedenen Säuren auf Gemüse- und Blütenfarbstoffe.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157300) 1.4 Die Wirkung von Säuren auf Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:36:51 intertess (Version 13.06 B200, Export
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157300) 1.4 Die Wirkung von Säuren auf Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:36:51 intertess (Version 13.06 B200, Export
Reibung (Artikelnr.: P )
 Lehrer-/Dozentenblatt Reibung (Artikelnr.: P1000300) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Mechanik Unterthema: Kräfte, einfache Maschinen Experiment:
Lehrer-/Dozentenblatt Reibung (Artikelnr.: P1000300) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Mechanik Unterthema: Kräfte, einfache Maschinen Experiment:
Der Kalkgehalt des Bodens (Artikelnr.: P )
 Lehrer-/Dozentenblatt Der Kalkgehalt des Bodens (Artikelnr.: P8121) Curriculare Themenzuordnung Fachgebiet:.iologie Bildungsstufe: Klasse 7-1 Lehrplanthema: Ökosysteme Unterthema: Land-Ökosysteme,.odenuntersuchung
Lehrer-/Dozentenblatt Der Kalkgehalt des Bodens (Artikelnr.: P8121) Curriculare Themenzuordnung Fachgebiet:.iologie Bildungsstufe: Klasse 7-1 Lehrplanthema: Ökosysteme Unterthema: Land-Ökosysteme,.odenuntersuchung
Welche Eigenschaften besitzen Calcium- und Magnesiumlaugen?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P758900) 2.5 Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) Experiment von: Phywe Gedruckt: 5.0.203 2:3:05 intertess
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P758900) 2.5 Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) Experiment von: Phywe Gedruckt: 5.0.203 2:3:05 intertess
Die Kerzenflamme (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die Kerzenflamme (Artikelnr.: P7154200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Luft und Verbrennungen
Lehrer-/Dozentenblatt Die Kerzenflamme (Artikelnr.: P7154200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Luft und Verbrennungen
Stoffe oder Teilchen, die Protonen abgeben kånnen, werden als SÄuren bezeichnet (Protonendonatoren).
 5 10 15 20 25 30 35 40 45 O C 50 Chemie Technische BerufsmaturitÄt BMS AGS Basel Kapitel 6 SÄuren und Basen Baars, Kap. 12.1; 12.2; 13 Versuch 1 Ein Becherglas mit Thermometer enthält violette FarbstofflÅsung
5 10 15 20 25 30 35 40 45 O C 50 Chemie Technische BerufsmaturitÄt BMS AGS Basel Kapitel 6 SÄuren und Basen Baars, Kap. 12.1; 12.2; 13 Versuch 1 Ein Becherglas mit Thermometer enthält violette FarbstofflÅsung
Alkoholische Gärung (Artikelnr.: P )
 Lehrer-/Dozentenblatt Alkoholische Gärung (Artikelnr.: P7171600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Organische Chemie Unterthema: Sauerstoffhaltige
Lehrer-/Dozentenblatt Alkoholische Gärung (Artikelnr.: P7171600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Organische Chemie Unterthema: Sauerstoffhaltige
Keimung und Sauerstoff (Artikelnr.: P )
 Lehrer-/Dozentenblatt Keimung und Sauerstoff (Artikelnr.: P8010800) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Pflanzen Unterthema: Keimung und Wachstum
Lehrer-/Dozentenblatt Keimung und Sauerstoff (Artikelnr.: P8010800) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Pflanzen Unterthema: Keimung und Wachstum
Untersuche das Verhalten von Zitronensäure gegenüber verschiedene Stoffen in Wasser und in Aceton.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P758500).6 Brönstedt Säuren - Aciditätvergleich einer wässrigen und einer acetonischen Citronensäurel Experiment von: Phywe Gedruckt: 5.0.203
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P758500).6 Brönstedt Säuren - Aciditätvergleich einer wässrigen und einer acetonischen Citronensäurel Experiment von: Phywe Gedruckt: 5.0.203
Voraussetzungen für Keimung (Artikelnr.: P )
 Lehrer-/Dozentenblatt Voraussetzungen für Keimung (Artikelnr.: P8010600) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Pflanzen Unterthema: Keimung und Wachstum
Lehrer-/Dozentenblatt Voraussetzungen für Keimung (Artikelnr.: P8010600) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Pflanzen Unterthema: Keimung und Wachstum
Entwicklung einer Pflanze (Artikelnr.: P )
 Lehrer-/Dozentenblatt Entwicklung einer Pflanze (Artikelnr.: P8010500) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Pflanzen Unterthema: Keimung und Wachstum
Lehrer-/Dozentenblatt Entwicklung einer Pflanze (Artikelnr.: P8010500) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Pflanzen Unterthema: Keimung und Wachstum
2.1 Eigenschaften von Stoffgemischen. Aufgabe. Welche Eigenschaften haben Stoffgemische?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750600) 2. Eigenschaften von Stoffgemischen Experiment von: Phywe Gedruckt:.0.203 2:49:48 intertess (Version 3.06 B200, Export 2000)
Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750600) 2. Eigenschaften von Stoffgemischen Experiment von: Phywe Gedruckt:.0.203 2:49:48 intertess (Version 3.06 B200, Export 2000)
Säuren- und Basendefinition nach Arrhenius
 Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren- und Basendefinition nach Arrhenius
 Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Säuren und Basen - Definitionen - Ionenprodukt des Wassers - ph-wert - Säure- und Basenstärke / ph-wert Bestimmungen - Neutralisationen - Puffersysteme Säuren- und Basendefinition nach Arrhenius Säure:
Wie kann eine Bräunung von zerkleinertem Obst und Gemüse verhindert werden?
 Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788500) 8.4 Enzymatische Bräunung Experiment von: Anouch Gedruckt: 28.02.204 :7:37 intertess (Version 3.2 B24, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788500) 8.4 Enzymatische Bräunung Experiment von: Anouch Gedruckt: 28.02.204 :7:37 intertess (Version 3.2 B24, Export 2000) Aufgabe
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Essigsäure färbt ph-papier rot. Natronlauge färbt ph-papier blau
 5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
Wasseraufbereitung in Kläranlagen (Artikelnr.: P )
 Lehrer-/Dozentenblatt Wasseraufbereitung in Kläranlagen (Artikelnr.: P7155100) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Allgemeine Chemie- Einführung Unterthema:
Lehrer-/Dozentenblatt Wasseraufbereitung in Kläranlagen (Artikelnr.: P7155100) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Allgemeine Chemie- Einführung Unterthema:
Von Arrhenius zu Brönsted
 Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Dichtebestimmung flüssiger Körper (Artikelnr.: P )
 Lehrer-/Dozentenblatt Gedruckt: 22.08.207 :6:57 P0998600 Dichtebestimmung flüssiger Körper (Artikelnr.: P0998600) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema:
Lehrer-/Dozentenblatt Gedruckt: 22.08.207 :6:57 P0998600 Dichtebestimmung flüssiger Körper (Artikelnr.: P0998600) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema:
Welche Vorsichtsmaßnahmen sind beim Umgang mit Laugen zu beachten?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P7158600) 2.1 Vorsichtsmaßnahmen beim Umgang mit Laugen Experiment von: Phywe Gedruckt: 15.10.2013 11:54:37 intertess (Version 13.06 B200,
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P7158600) 2.1 Vorsichtsmaßnahmen beim Umgang mit Laugen Experiment von: Phywe Gedruckt: 15.10.2013 11:54:37 intertess (Version 13.06 B200,
Welcher Unterschied besteht zwischen schwefliger Säure und Schwefelsäure?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P75800).2 Oxidation von schwefliger Säure Experiment von: PHYWE Gedruckt: 0.0.205 3:05:3 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P75800).2 Oxidation von schwefliger Säure Experiment von: PHYWE Gedruckt: 0.0.205 3:05:3 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Untersuche, warum zu Ammoniakdüngern häufig gebrannter Kalk gegeben wird.
 Naturwissenschaften - Chemie - Anorganische Chemie - 5 Düngemittel (P756300) 5.4 Gebrannter Kalk als Düngemittel Experiment von: Seb Gedruckt: 24.03.204 :57:28 intertess (Version 3.2 B24, Export 2000)
Naturwissenschaften - Chemie - Anorganische Chemie - 5 Düngemittel (P756300) 5.4 Gebrannter Kalk als Düngemittel Experiment von: Seb Gedruckt: 24.03.204 :57:28 intertess (Version 3.2 B24, Export 2000)
Kohlenstoffdioxyd, Darstellung und Eigenschaften
 Lehrer-/Dozentenblatt Kohlenstoffdioxyd, Darstellung und Eigenschaften (Artikelnr.: P753900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie
Lehrer-/Dozentenblatt Kohlenstoffdioxyd, Darstellung und Eigenschaften (Artikelnr.: P753900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7
 AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
3.7 Osmose - Chemischer Garten. Aufgabe. Wie lösen sich Salze in Wasserglas? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P760000) 3.7 Osmose - Chemischer Garten Experiment von: Phywe Gedruckt: 5.0.203 2:25:55 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P760000) 3.7 Osmose - Chemischer Garten Experiment von: Phywe Gedruckt: 5.0.203 2:25:55 intertess (Version 3.06 B200, Export 2000) Aufgabe
Erhitze verschiedene Kohlenhydrate und prüfe welche Stoffe dabei gebildet werden.
 Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P786600) 5. Begriff Kohlenhydrate Experiment von: Anouch Gedruckt: 28.02.204 :00:8 intertess (Version 3.2 B24, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P786600) 5. Begriff Kohlenhydrate Experiment von: Anouch Gedruckt: 28.02.204 :00:8 intertess (Version 3.2 B24, Export 2000) Aufgabe
Destillation (Artikelnr.: P )
 Lehrer-/Dozentenblatt Destillation (Artikelnr.: P1045000) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Wärmelehre Unterthema: Schmelzen, Sieden, Verdampfen (Aggregatzustände)
Lehrer-/Dozentenblatt Destillation (Artikelnr.: P1045000) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Wärmelehre Unterthema: Schmelzen, Sieden, Verdampfen (Aggregatzustände)
Dissoziation, ph-wert und Puffer
 Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
3.6 Thermische Zersetzung von Salzen. Aufgabe. Wie verhalten sich Salze beim Erhitzen? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759900) 3.6 Thermische Zersetzung von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:22:38 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759900) 3.6 Thermische Zersetzung von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:22:38 intertess (Version 3.06 B200, Export 2000) Aufgabe
Der spezifische Widerstand von Drähten (Artikelnr.: P )
 Lehrer-/Dozentenblatt Der spezifische Widerstand von Drähten (Artikelnr.: P1372700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema:
Lehrer-/Dozentenblatt Der spezifische Widerstand von Drähten (Artikelnr.: P1372700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema:
1 Basenrest Säurerest Lewisformel Anion - O
 AC2 ÜB6 Säuren und Basen LÖSUNGEN Seite 1 von 6 1 Basenrest Säurerest Lewisformel Anion Na 2 S 4 (s) > 2 Na (aq) S 2 4 (aq) 2 S H KHS 4 (s) > K (aq) HS 2 4 (aq) S CaBr 2 (s) > Ca 2 (aq) 2 Br (aq) Br Pb(N
AC2 ÜB6 Säuren und Basen LÖSUNGEN Seite 1 von 6 1 Basenrest Säurerest Lewisformel Anion Na 2 S 4 (s) > 2 Na (aq) S 2 4 (aq) 2 S H KHS 4 (s) > K (aq) HS 2 4 (aq) S CaBr 2 (s) > Ca 2 (aq) 2 Br (aq) Br Pb(N
Aufbau und Zusammensetzung von Eiweißstoffen
 Lehrer-/Dozentenblatt Aufbau und Zusammensetzung von Eiweißstoffen (Artikelnr.: P7185000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Organische Chemie Unterthema:
Lehrer-/Dozentenblatt Aufbau und Zusammensetzung von Eiweißstoffen (Artikelnr.: P7185000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Organische Chemie Unterthema:
Salzgehalt von Böden und Pflanzsubstraten
 Lehrer-/Dozentenblatt Salzgehalt von Böden und Pflanzsubstraten (Artikelnr.: P1521162) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 10-13 Lehrplanthema: Ökologie Unterthema: Biotop
Lehrer-/Dozentenblatt Salzgehalt von Böden und Pflanzsubstraten (Artikelnr.: P1521162) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 10-13 Lehrplanthema: Ökologie Unterthema: Biotop
Eigenschaften der homologen Reihe (Artikelnr.: P )
 Lehrer-/Dozentenblatt Eigenschaften der homologen Reihe (Artikelnr.: P7172100) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Organische Chemie Unterthema: Sauerstoffhaltige
Lehrer-/Dozentenblatt Eigenschaften der homologen Reihe (Artikelnr.: P7172100) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Organische Chemie Unterthema: Sauerstoffhaltige
Säuren und Basen. Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17.
 Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
Keimhemmung in Früchten (Artikelnr.: P )
 Lehrer-/Dozentenblatt Keimhemmung in Früchten (Artikelnr.: P8011100) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Pflanzen Unterthema: Keimung und Wachstum
Lehrer-/Dozentenblatt Keimhemmung in Früchten (Artikelnr.: P8011100) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Pflanzen Unterthema: Keimung und Wachstum
Lösungswärme (Artikelnr.: P )
 Lehrer-/Dozentenblatt Gedruckt: 30.03.207 4:46:24 P045200 Lösungswärme (Artikelnr.: P045200) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema:
Lehrer-/Dozentenblatt Gedruckt: 30.03.207 4:46:24 P045200 Lösungswärme (Artikelnr.: P045200) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema:
Galvanische Zellen aus Nichtmetallen (Artikelnr.: P )
 Lehrer-/Dozentenblatt Galvanische Zellen aus Nichtmetallen (Artikelnr.: P7400900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische Chemie Unterthema:
Lehrer-/Dozentenblatt Galvanische Zellen aus Nichtmetallen (Artikelnr.: P7400900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische Chemie Unterthema:
A B - AB K D. Elektrolytische Dissoziation. AB(aq) Stoffe, die in Lösung Ionen bilden, heißen Elektrolyte. Es gilt das Massenwirkungsgesetz
 Elektrolytische Dissoziation AB(aq) A + (aq) + B - (aq) Stoffe, die in Lösung Ionen bilden, heißen Elektrolyte. Es gilt das Massenwirkungsgesetz K D A B - AB K D : Dissoziationskonstante Dissoziation ist
Elektrolytische Dissoziation AB(aq) A + (aq) + B - (aq) Stoffe, die in Lösung Ionen bilden, heißen Elektrolyte. Es gilt das Massenwirkungsgesetz K D A B - AB K D : Dissoziationskonstante Dissoziation ist
Schweflige Säure - Umweltgefährdung durch Verbrennung fossiler Brennstoffe (Artikelnr.: P )
 Lehrer-/Dozentenblatt Schweflige Säure - Umweltgefährdung durch Verbrennung fossiler Brennstoffe (Artikelnr.: P7158000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Lehrer-/Dozentenblatt Schweflige Säure - Umweltgefährdung durch Verbrennung fossiler Brennstoffe (Artikelnr.: P7158000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Aufbau und Funktion eines Bunsenbrenners
 Lehrer-/Dozentenblatt Aufbau und Funktion eines Bunsenbrenners (Artikelnr.: P7154100) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Lehrer-/Dozentenblatt Aufbau und Funktion eines Bunsenbrenners (Artikelnr.: P7154100) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Praktikumsprotokoll. Grundlagen der Chemie Teil II SS Praktikum vom
 Grundlagen der Chemie Teil II SS 2002 Praktikumsprotokoll Praktikum vom 02.05.2002 Versuch 11: Herstellung einer Pufferlösung von definiertem ph Versuch 12: Sauer und alkalisch reagierende Salzlösungen
Grundlagen der Chemie Teil II SS 2002 Praktikumsprotokoll Praktikum vom 02.05.2002 Versuch 11: Herstellung einer Pufferlösung von definiertem ph Versuch 12: Sauer und alkalisch reagierende Salzlösungen
V 1 Herstellung von Natriumchlorid
 1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
Säure/Base - Reaktionen. 6) Titration starker und schwacher Säuren/Basen. Elektrolytische Dissoziation. AB(aq)
 Säure/Base - Reaktionen 1) Elektrolytische Dissoziation ) Definitionen Säuren Basen ) Autoprotolyse 4) p- und po-wert 5) Stärke von Säure/Basen 6) Titration starker und schwacher Säuren/Basen 7) Puffersysteme
Säure/Base - Reaktionen 1) Elektrolytische Dissoziation ) Definitionen Säuren Basen ) Autoprotolyse 4) p- und po-wert 5) Stärke von Säure/Basen 6) Titration starker und schwacher Säuren/Basen 7) Puffersysteme
Das ohmsche Gesetz (Artikelnr.: P )
 Das ohmsche Gesetz (Artikelnr.: P1381000) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Der elektrische Widerstand Experiment:
Das ohmsche Gesetz (Artikelnr.: P1381000) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Der elektrische Widerstand Experiment:
Schwierigkeitsgrad Vorbereitungszeit Durchführungszeit Empfohlene Gruppengröße. {time:2} 20 Minuten. Versuchsvarianten:
 Lehrer-/Dozentenblatt Gedruckt: 2.8.27 6::24 P753 Siedetemperatur Lehrerinformationen Einführung Schwierigkeitsgrad Vorbereitungszeit Durchführungszeit Empfohlene Gruppengröße {complexity:3} mittel {time:}
Lehrer-/Dozentenblatt Gedruckt: 2.8.27 6::24 P753 Siedetemperatur Lehrerinformationen Einführung Schwierigkeitsgrad Vorbereitungszeit Durchführungszeit Empfohlene Gruppengröße {complexity:3} mittel {time:}
Stromstärke und Widerstand bei der Parallelschaltung (Artikelnr.: P )
 Stromstärke und Widerstand bei der Parallelschaltung (Artikelnr.: P1381400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Der elektrische
Stromstärke und Widerstand bei der Parallelschaltung (Artikelnr.: P1381400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Der elektrische
Das Verhalten von Algen zu Licht (Artikelnr.: P )
 Lehrer-/Dozentenblatt Das Verhalten von Algen zu Licht (Artikelnr.: P8013900) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Sinnesorgane Unterthema: Lichtsinn
Lehrer-/Dozentenblatt Das Verhalten von Algen zu Licht (Artikelnr.: P8013900) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Sinnesorgane Unterthema: Lichtsinn
Wärmeleitung in Flüssigkeiten (Artikelnr.: P )
 Lehrer-/Dozentenblatt Wärmeleitung in Flüssigkeiten (Artikelnr.: P1043400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Wärmelehre Unterthema: Wärmetransport
Lehrer-/Dozentenblatt Wärmeleitung in Flüssigkeiten (Artikelnr.: P1043400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Wärmelehre Unterthema: Wärmetransport
Versuch: Fünf Farben in einer Lösung
 Name: Datum: Versuch: Materialien: 5 x 100 ml Bechergläser (nummeriert von 1-5), Tropfpipetten, Messzylinder (50 ml), Spritzflasche mit destilliertem Wasser Chemikalien: Lösung Nr. 1: Lösung Nr. 2: Lösung
Name: Datum: Versuch: Materialien: 5 x 100 ml Bechergläser (nummeriert von 1-5), Tropfpipetten, Messzylinder (50 ml), Spritzflasche mit destilliertem Wasser Chemikalien: Lösung Nr. 1: Lösung Nr. 2: Lösung
Iodoformprobe (Artikelnr.: P )
 Lehrer-/Dozentenblatt Gedruckt: 30.03.207 7:40:37 P772000 Iodoformprobe (Artikelnr.: P772000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Organische Chemie Unterthema:
Lehrer-/Dozentenblatt Gedruckt: 30.03.207 7:40:37 P772000 Iodoformprobe (Artikelnr.: P772000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Organische Chemie Unterthema:
1.9 Darstellung und Eigenschaften von schwefliger Säure. Aufgabe. Welche Eigenschaften besitzt schweflige Säure?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P757800).9 Darstellung und Eigenschaften von schwefliger Säure Experiment von: Phywe Gedruckt: 5.0.203 :43:57 intertess (Version 3.06 B200,
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P757800).9 Darstellung und Eigenschaften von schwefliger Säure Experiment von: Phywe Gedruckt: 5.0.203 :43:57 intertess (Version 3.06 B200,
Die elektrische Klingel (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die elektrische Klingel (Artikelnr.: P1375700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Elektromagnetismus
Lehrer-/Dozentenblatt Die elektrische Klingel (Artikelnr.: P1375700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Elektromagnetismus
Der Permanentmagnet-Gleichstrommotor (Artikelnr.: P )
 Lehrer-/Dozentenblatt Der Permanentmagnet-Gleichstrommotor (Artikelnr.: P1376200) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema:
Lehrer-/Dozentenblatt Der Permanentmagnet-Gleichstrommotor (Artikelnr.: P1376200) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema:
1.7 Säurestärke. Aufgabe. Gibt es verschieden starke Säuren? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157600) 1.7 Säurestärke Experiment von: Phywe Gedruckt: 15.10.2013 11:41:12 intertess (Version 13.06 B200, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157600) 1.7 Säurestärke Experiment von: Phywe Gedruckt: 15.10.2013 11:41:12 intertess (Version 13.06 B200, Export 2000) Aufgabe Aufgabe
(Atommassen: Ca = 40, O = 16, H = 1;
 1.) Welche Molarität hat eine 14,8%ige Ca(OH) 2 - Lösung? (Atommassen: Ca = 40, O = 16, H = 1; M: mol/l)! 1! 2! 2,5! 3! 4 M 2.) Wieviel (Gewichts)%ig ist eine 2-molare Salpetersäure der Dichte 1,100 g/cm
1.) Welche Molarität hat eine 14,8%ige Ca(OH) 2 - Lösung? (Atommassen: Ca = 40, O = 16, H = 1; M: mol/l)! 1! 2! 2,5! 3! 4 M 2.) Wieviel (Gewichts)%ig ist eine 2-molare Salpetersäure der Dichte 1,100 g/cm
7. Chemische Reaktionen
 7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte Grundlagen Lösung: homogene Phase aus Lösungsmittel und gelösten Stoff Lösungsmittel liegt im Überschuss vor
7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte Grundlagen Lösung: homogene Phase aus Lösungsmittel und gelösten Stoff Lösungsmittel liegt im Überschuss vor
Schulversuchspraktikum. Jans Manjali. Sommersemester Klassenstufen 9 & 10. Titration. Kurzprotokoll
 Schulversuchspraktikum Jans Manjali Sommersemester 2015 Klassenstufen 9 & 10 Titration Kurzprotokoll Auf einen Blick: Die hier vorgestellte Argentometrie ist eine Fällungstitration, bei der Silberionen
Schulversuchspraktikum Jans Manjali Sommersemester 2015 Klassenstufen 9 & 10 Titration Kurzprotokoll Auf einen Blick: Die hier vorgestellte Argentometrie ist eine Fällungstitration, bei der Silberionen
Titration einer schwachen Säure gegen eine starke Base mit Cobra4 (Artikelnr.: P )
 Lehrer-/Dozentenblatt Gedruckt: 7.08.207 0:04:43 P750762 Titration einer schwachen Säure gegen eine starke Base mit Cobra4 (Artikelnr.: P750762) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe:
Lehrer-/Dozentenblatt Gedruckt: 7.08.207 0:04:43 P750762 Titration einer schwachen Säure gegen eine starke Base mit Cobra4 (Artikelnr.: P750762) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe:
2.6 Herstellung und Eigenschaften von Natronlauge. Aufgabe. Welche Eigenschaften besitzt Natronlauge?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P759000) 2.6 Herstellung und Eigenschaften von Natronlauge Experiment von: Phywe Gedruckt: 5.0.203 2:4:04 intertess (Version 3.06 B200, Export
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P759000) 2.6 Herstellung und Eigenschaften von Natronlauge Experiment von: Phywe Gedruckt: 5.0.203 2:4:04 intertess (Version 3.06 B200, Export
Brennbarkeit von wunststoffen (Artikelnr.: P )
 Lehrer-/Dozentenblatt Gedruckt: 30.03.207 7:43:46 P780600 Brennbarkeit von wunststoffen (Artikelnr.: P780600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 0-3 Lehrplanthema: Organische
Lehrer-/Dozentenblatt Gedruckt: 30.03.207 7:43:46 P780600 Brennbarkeit von wunststoffen (Artikelnr.: P780600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 0-3 Lehrplanthema: Organische
Die Schmelzsicherung (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die Schmelzsicherung (Artikelnr.: P1372200) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Der elektrische
Lehrer-/Dozentenblatt Die Schmelzsicherung (Artikelnr.: P1372200) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Der elektrische
Wie verändern sich die Eigenschaften der Alkohole bei Zunahme der Kohlenstoffzahl?
 Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
5.3 Glucosenachweis mit Fehlingscher Lösung. Aufgabe. Wie kann Traubenzucker nachgewiesen werden?
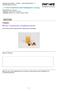 Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P786800) 5.3 Glucosenachweis mit Fehlingscher Lösung Experiment von: Anouch Gedruckt: 28.02.204 :0:4 intertess (Version 3.2 B24, Export
Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P786800) 5.3 Glucosenachweis mit Fehlingscher Lösung Experiment von: Anouch Gedruckt: 28.02.204 :0:4 intertess (Version 3.2 B24, Export
Lasse Pflanzen in mineraldüngerhaltigem Wasser und in Trinkwasser wachsen.
 Naturwissenschaften - Chemie - Anorganische Chemie - 5 Düngemittel (P75600) 5.2 Mineralstoffaufnahme der Pflanzen Experiment von: Seb Gedruckt: 24.03.204 :54:0 intertess (Version 3.2 B24, Export 2000)
Naturwissenschaften - Chemie - Anorganische Chemie - 5 Düngemittel (P75600) 5.2 Mineralstoffaufnahme der Pflanzen Experiment von: Seb Gedruckt: 24.03.204 :54:0 intertess (Version 3.2 B24, Export 2000)
Lerne Nachweismöglichkeiten für Eiweiße kennen und untersuche verschiedene Lebensmittel auf Eiweiße.
 Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802600) 4.5 Eiweißhaltige Nahrungsmittel Experiment von: Phywe Gedruckt: 07.0.203 5:40:59 intertess (Version
Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802600) 4.5 Eiweißhaltige Nahrungsmittel Experiment von: Phywe Gedruckt: 07.0.203 5:40:59 intertess (Version
Stelle Stoffgemische aus Flüssigkeiten her und untersuche ihre Eigenschaften.
 Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750700) 2.2 Flüssigkeitsgemische Experiment von: Phywe Gedruckt:.0.203 2:50:52 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufbau
Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750700) 2.2 Flüssigkeitsgemische Experiment von: Phywe Gedruckt:.0.203 2:50:52 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufbau
