Lernen an Stationen zum Thema Carbonate
|
|
|
- Susanne Erika Frei
- vor 7 Jahren
- Abrufe
Transkript
1 - CO 2 in der Ausatemluft - Führt das folgende durch und wertet es mithilfe des folgenden Textes umfassend aus. Geräte/Chemikalien: Reagenzglas, Glasrohr, Bariumhydroxidlösung 1. Füllt das Reagenzglas zu 1/4 mit Bariumhydroxid-Lösung. 2. Puste deine Ausatemluft vorsichtig durch das eingetauchte Glasrohr in die Bariumhydroxidlösung. Begründet eure Beobachtung mit Hilfe von Wort und Reaktionsgleichungen. Infotext Hinterlasst die Station bitte so, wie ihr sie vorfinden möchtet! Aus dem Biologieunterricht dürfte dir bekannt sein, dass unser menschlicher Körper Energie benötigt, z. B. um seine Temperatur auf den normalen 36,5 C zu halten oder um unsere Muskeln arbeiten zu lassen. Doch woher kommt diese Energie? Der Körper gewinnt diese Energie aus Nährstoffen, die wir in Form von Brot, Kartoffeln, Kavier, Champagner, Äpfeln usw. zu uns nehmen. Der Energiegehalt der Nahrungsmittel wird durch die Angabe des Brennwertes in kj oder kcal gekennzeichnet (siehe Abbildung). Die Energie wird durch Verdauung von Zucker und Stärke, Fetten und Eiweißen, unseren Hauptnährstoffen, gewonnen. Alle diese Stoffe bestehen aus sehr großen und kompliziert gebauten Molekülen, die zu einem großen Teil aus Kohlenstoff bestehen. Während des Verdauungsprozesses, der im Mund beginnt, und in Magen und Darm fortgesetzt wird, werden diese Moleküle zerkleinert und dann Abb. 1: Durchschnittlicher Nährwert eines Müslis in das Blutsystem übernommen, von wo aus sie zu allen Zellen des Körpers gelangen. Über das Blut wird auch Sauerstoff von der Lunge zu den einzelnen Körperzellen transportiert. In den Körperzellen werden dann die aus den Nährstoffen entstandenen kleineren Moleküle verbrannt. Dabei entstehen im wesentlichen Kohlenstoffdioxid und Wasser. Beides wird über die Lunge wieder abgegeben. In der Einatemluft befinden sich 0,035% CO 2 gegenüber ca. 5% in der Ausatemluft. Während für die Verbrennung von Kohlenstoff an der Luft eine Brennerflamme nötig ist, also eine extrem hohe Temperatur, läuft die Verbrennung der Nährstoffe im Körper bereits bei 36,5 C ab. Man spricht deshalb auch von sanfter Oxidation. Diese sanfte Oxidation wird durch Enzyme ermöglicht. Für Fette z. B. gilt: Enzyme Fett + Sauerstoff Kohlenstoffdioxid + Wasser Diese einfache Wortgleichung fasst die Vorgänge im Körper bei der Fettverdauung stark vereinfacht zusammen, gibt aber keine Auskunft über die komplizierten Vorgänge, die dabei ablaufen.
2 - Erhitzen von n - Führt das folgende durch und entnehmt dem folgenden Text wesentliche Informationen über Soda. Geräte/Chemikalien: Reagenzgläser mit Ableitungsrohr, Reagenzglashalter, Reagenzgläser, Schlauchverbindungen, Glasrohre, Brenner, Bariumhydroxid-Lösung oder Calciumhydroxid- Lösung, Soda, Pottasche, Magnesiumcarbonat, Natron 1. Füllt die Reagenzgläser mit Ableitungsrohr mit je einem der. 2. Leitet eventuell entstehende Gase über ein Glasrohr in die Barium- bzw. Calciumhydroxid-Lösung. Nennt die direkte Ursache für eure Beobachtung. Gebt alle zur Erklärung notwendigen Reaktionsgleichungen an. Infotext 1 Soda: Natriumcarbonat Na 2 CO 3 - auch Soda genannt - ist das Natriumsalz der Kohlensäure. Natriumcarbonat ist ein gut in Wasser lösliches Salz, dessen wässrige Lösung stark alkalisch reagiert. Natriumcarbonat wurde schon von den alten Ägyptern als waschaktive Substanz erkannt und zur Reinigung von Kleidung verwendet. Ebenfalls eine lange Geschichte hat der Einsatz von Soda bei der Glasherstellung. Große Mengen Natriumcarbonat findet man (in Mischung mit Natriumhydrogencarbonat) in Salzseen Ägyptens oder Nord- und Südamerikas. Bis zum 19. Jahrhundert gewann man Soda aus kochsalzreichen Meeres- oder Strandpflanzen. Diese wurde verbrannt und hinterließen eine sodareiche Asche. Heute wird Soda mit Hilfe des sogenannten Solvay-Verfahrens großtechnisch und in großen Mengen hergestellt, denn Soda ist das wichtigste Zwischenprodukt für die Herstellung von Natrium-Verbindungen. Es wird zum Beispiel zur Herstellung von Natriumhydroxid, Natriumhydrogencarbonat oder Ultramarinblau eingesetzt, dient bei der Produktion von Glas als Flussmittel und wird zur Herstellung von Seifen und Waschmitteln (siehe Bild 2 ) sowie in der Zellstoff- und Papierindustrie und zum Enthärten von Wasser verwendet. 1 Vgl.: (10. Mai 2005), (10. Mai 2005) 2 (10. Mai 2005)
3 - Löslichkeit von n - Führt das folgende durch und entnehmt dem folgenden Text wesentliche Informationen über Pottasche. Geräte/Chemikalien: Reagenzgläser, Wasser, Spatel, Unitest-Lösung, Soda, Pottasche, Magnesiumcarbonat, Calciumcarbonat, Natron 1. Füllt die Reagenzgläser zu ¼ mit Wasser. 2. Fügt eine Spatelspitze des jeweiligen Carbonats hinzu, schüttelt kräftig. 3. Fügt einige Tropfen Unitest-Lösung hinzu. Nennt die direkte Ursache für eure Beobachtung. Gebt alle zur Erklärung notwendigen Reaktionsgleichungen an. (Tipp: Aufgabe von Station 4 benutzen!) Infotext 1 Pottasche ist chemisch gesehen Kaliumcarbonat. Kaliumcarbonat wirkt stark hygroskopisch und zeigt im Übrigen alle typischen Eigenschaften der. Pottasche wurde früher aus Holzasche gewonnen. Man laugte die Holzasche in Holzbottichen mit Siebböden aus, bis die Lösung etwa 25% Salze enthielt. Diese Lauge wurde in Töpfen (Pötten) eingedampft, daher die Bezeichnung Pottasche. Verwendet wurde die Pottasche zur Herstellung von Seifen und Gläsern. Seifen wurden schon von den Galliern aus Fett und Pottasche gewonnen. Heute wird Kaliumcarbonat zur Synthese anderer Kaliumverbindungen und zur Herstellung von Glas, keramischen Erzeugnissen und Pigmenten verwendet und auch im Labor findet es als Trockenmittel Verwendung. Im Haushalt findet Pottasche als Backpulver Anwendung (siehe Bild 2 ). Pottasche wird meistens für Leb- und Honigkuchen, d.h. für Kleingebäck, das relativ lange gelagert wird, eingesetzt. Sie wird durch die im Mehl vorhandenen und aus der Luft hinzutretenden Mikroorganismen, die eine leichte Säuerung verursachen, zersetzt. Es tritt eine alkalische Reaktion ein, die die Elastizität des Teiges verbessert und ihm einen typischen Geschmack gibt. Außerdem wird der Teig gelockert. Pottasche unterscheidet sich von anderen Backpulvern, durch das Fehlen saurer Bestandteile. 1 Vgl. (10. Mai 2005), (10. Mai 2005) 2 (10. Mai 2005)
4 - Reaktion mit Säuren - Führt das folgende durch und löst die unten stehende Aufgabe. Geräte/Chemikalien: Urgläschen, Glasstab, Spatel, Barium- oder Calciumhydroxid-Lösung, Magnesiumcarbonat, Natriumcarbonat, Natriumcarbonat, Salzsäure, 1. Platziert mit Hilfe des Spatels ein kleines Häufchen des jeweiligen Carbonats auf je ein Urgläschen. 2. Taucht einen sauberen Glasstab in die Barium- bzw. Calciumhydroxid- Lösung. 3. Tropft Salzsäure auf das jeweilige Carbonat. 4. Haltet das Glasstäbchen über die Mischung, ohne diese zu berühren. Nennt die direkte Ursache für eure Beobachtung. Gebt alle zur Erklärung notwendigen Reaktionsgleichungen an. Aufgabe Gib in deinen eigenen Worten die Aussage der folgenden Reaktionsgleichungen wider und überlege, ob sich ein verwertbarer Bezug zu Station 3 herstellen lässt. (1) Na 2 CO 3 2 Na CO 3 (2) CO H 2 O HCO OH - (3) HCO H 2 O CO OH -
5 - Reaktion der Hydrogencarbonate mit Säuren - : Führt das folgende durch und löst die unten gestellte Aufgabe. Geräte/Chemikalien: pneumatische Wanne, Teelicht, Streichhölzer, Backpulver, Salzsäure, Pipette 1. Füllt den Boden der pneumatischen Wanne mit Backpulver und stellt ein brennendes Teelicht hinein. 2. Tropft die Säure auf das Backpulver in der Umgebung der Kerze. Nennt die direkte Ursache für eure Beobachtung. Erklärt die Beobachtung unter Benutzung notwendiger Reaktionsgleichungen. Hinterlasst die Station bitte so, wie ihr sie vorfinden möchtet! Aufgabe Erläutert die Funktionsweise von Brausepulver und Backpulver. (Tipp: Benutzt dazu auch ein Ergebnis von Station 2.)
6 - Kalk brennen - Führt das durch und entnehmt dem folgenden Text wesentliche Informationen über Calciumcarbonat. Geräte/Chemikalien: Tiegelzange, 2 Bechergläser, Marmor, Phenolphthalein-Lösung, Wasser 1. Füllt ein Becherglas etwa fingerbreit mit Wasser und setzt einige Tropfen Phenolphthalein-Lösung zu. 2. Haltet mit einer Tiegelzange ein Stück Marmor etwa 1 bis 2 Minuten in die entleuchtete Brennerflamme. 3. Gebt das erhitzte Marmorstück in das vorbereitete Becherglas. Nenne die direkte Ursache für deine Beobachtung. Erkläre das Vorhandensein dieser Ursache mit Hilfe deiner Ergebnisse von den Stationen 2 und 3. Gib alle zur Erklärung notwendigen Reaktionsgleichungen an. Infotext 5 Hinterlasst die Station bitte so, wie ihr sie vorfinden möchtet! Calciumcarbonat, ein vielseitiger Stoff: Wenn der Chemiker von Calciumcarbonat spricht, meint er ein weißes Pulver, das sich in einer Chemikalienflasche befindet. Doch der "Stoff Calciumcarbonat" begegnet uns in der Natur in vielen Variationen. a) Kalkstein ist durch sedimentäre Ablagerung im Meer gebildetes Calciumcarbonat. Oft sind Kalksteine reich an Versteinerungen. Kalkstein war schon im Altertum ein wichtiges Baumaterial, z.b. für den Bau der Cheops- Pyramide. b) Calcit ist die chemisch stabilste Form des Calciumcarbonats und bildet farblose oder durch Fremdeinschlüsse gefärbte Kristalle. Die meisten Kalksteine oder Marmore enthalten kleinste Kristalle von Calcit. Sie bilden sich in Hohlräumen oder Spalten, die von hartem Wasser durchflossen werden. c) Aragonit ist im chemischen Aufbau dem Calcit sehr ähnlich aber nicht so beständig und kommt darum in der Natur nicht als Gestein vor. Er bildet in reiner Form farblose bis weiße Kristalle, die sich nicht gut spalten und unterscheidet sich dadurch vom Calcit. d) Dolomit bildet wasserklare oder durchscheinende Kristalle, die gut spaltbar sind. Das Mineral ist ein Calcium- Magnesiumcarbonat. Das mit verdünnter Salzsäure zunächst kein Kohlenstoffdioxid entwickelt, erst beim Erwärmen lässt sich das typische Sprudeln beobachten. e) Kreide heißen die in der Kreidezeit aus den Schalen von Kleinstlebewesen gebildeten weißen Kalke, die im Gegensatz zum Kalkstein stark abfärben und daher als Pigmente verwendet werden. Kreidevorkommen finden sich z. B auf Rügen. Kreide wird zur Herstellung von Tafelkreide und als weißes Pigment verwendet. f) Kalksinter entsteht, wenn hartes Wasser aus dem Untergrund zutage tritt. Das gelöste Calciumhydrogencarbonat wandelt sich zu Kohlenstoffdioxid und zu Kalk um, der dann treppenstufig angeordnete Terrassen und tropfsteinartige Gebilde um die Quelle herum bildet. g) Marmorgesteine bilden sich metamorph. D. h. sie entstehen, wenn sedimentär entstandener Kalkstein unter hohem Druck wieder in die Erdkruste hineingeschoben und dort bei hohen Temperaturen umgewandelt wird ("Metamorphose"). Der Kalkstein wird dabei grobkörniger und dichter. Dies ermöglicht die Polierfähigkeit der Marmore, welcher schon den Römern als Baumaterial diente. 5 Vgl. Seilnacht, T.: Calciumcarbonat, ein vielseitiger Stoff. (10. Mai 2005)
7 - Kalk löschen - Führt das durch und löst die unten stehende Aufgabe. Geräte/Chemikalien: Petrischale, Thermometer, Calciumoxid wasserfrei, Universalindikatorpapier, Thermometer 1. Gebt in die Petrischale einige Stücken Calciumoxid. 2. Haltet ein feuchtes Stück ph-papier an eines der Stücke. 3. Gebt soviel Wasser hinzu (einige Tropen), dass sich die Stücke damit vollsaugen können und miss während dessen die Temperatur. Anmerkung: Die Reaktion kann mit einiger Verzögerung einsetzen, dann aber um so intensiver ablaufen. Sicherheitshinweis: Achtung Spritzgefahr! Unbedingt Schutzbrille tragen! Nenne die direkten Ursachen deiner Beobachtungen. Erkläre das Vorhandensein dieser Ursache. Gib alle zur Erklärung notwendigen Reaktionsgleichungen an. Hinterlasst die Station bitte so, wie ihr sie vorfinden möchtet! Aufgabe Berechne, wie viel Salzsäure notwendig ist, um die beim Löschen von 100g Kalk entstehende basische Lösung zu neutralisieren.
8 - - Beobachtung: Auswertung: Stoff: Beobachtungen: Auswertung: Natriumcarbonat Kaliumcarbonat Magnesiumcarbonat Natron Stoff: Beobachtungen: Auswertung: Natriumcarbonat Kaliumcarbonat Magnesiumcarbonat Calciumcarbonat Natron
9 Stoff: Beobachtungen: Auswertung: Natriumcarbonat Kaliumcarbonat Magnesiumcarbonat Auswertung: Beobachtung: Auswertung: Beobachtung: Auswertung: Beobachtung: Viel Spaß!
Verbrennung einer Kerze
 Verbrennung einer Kerze Schauen wir uns zunächst die Kerze genauer an. Aus welchen Bestandteilen besteht sie? Und wozu dienen diese? Bestandteil Stoff Funktion Der Stoff ist das Material, woraus ein Körper
Verbrennung einer Kerze Schauen wir uns zunächst die Kerze genauer an. Aus welchen Bestandteilen besteht sie? Und wozu dienen diese? Bestandteil Stoff Funktion Der Stoff ist das Material, woraus ein Körper
Kohlensäure ohne sie wäre unser Alltag
 1 von 26 Von Soda-Streamern, Backpulver und Kalk Kohlensäure und ihre Salze Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von Dr. Wolfgang Zettlmeier, Barbing Foto: Thinkstock/Stockbyte
1 von 26 Von Soda-Streamern, Backpulver und Kalk Kohlensäure und ihre Salze Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von Dr. Wolfgang Zettlmeier, Barbing Foto: Thinkstock/Stockbyte
Verbrennung einer Kerze
 Verbrennung einer Kerze Zünde eine Kerze an und notiere deine Beobachtungen: Was passiert eigentlich genau bei der Verbrennung einer Kerze? Diese Frage versuchen wir in diesem Kapitel zu beantworten. Schauen
Verbrennung einer Kerze Zünde eine Kerze an und notiere deine Beobachtungen: Was passiert eigentlich genau bei der Verbrennung einer Kerze? Diese Frage versuchen wir in diesem Kapitel zu beantworten. Schauen
Gemische. Zeitangabe: 8 min SCHUTZBRILLE NICHT VERGESSEN! VERSUCH 1 VERSUCH 2
 Gemische Zeitangabe: 8 min SCHUTZBRILLE NICHT VERGESSEN! Materialien: Becherglas, Spatel Chemikalien: Wasser, Tinte VERSUCH 1 Gebt in das Becherglas ca. 2 cm hoch Wasser und gebt dann fünf Tropfen Tinte
Gemische Zeitangabe: 8 min SCHUTZBRILLE NICHT VERGESSEN! Materialien: Becherglas, Spatel Chemikalien: Wasser, Tinte VERSUCH 1 Gebt in das Becherglas ca. 2 cm hoch Wasser und gebt dann fünf Tropfen Tinte
Neutralisation Die Wirkung von Antazida im Körper
 Neutralisation Die Wirkung von Antazida im Körper Stand: 01.08.2018 Jahrgangsstufen 11 Fach/Fächer Chemie Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material 45 Minuten Antazida, demineralisiertes
Neutralisation Die Wirkung von Antazida im Körper Stand: 01.08.2018 Jahrgangsstufen 11 Fach/Fächer Chemie Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material 45 Minuten Antazida, demineralisiertes
fest, nicht gelöst: Na + Cl -
 Salzsäure + Natriumlauge Natriumchlorid + Wasser / exotherm HCl + NaOH NaCl + H 2 O / exotherm H + (aq) + Cl (aq) + Na + (aq) + OH (aq) Na + (aq) + Cl (aq) + H 2 O / exotherm fest, nicht gelöst: Na + Cl
Salzsäure + Natriumlauge Natriumchlorid + Wasser / exotherm HCl + NaOH NaCl + H 2 O / exotherm H + (aq) + Cl (aq) + Na + (aq) + OH (aq) Na + (aq) + Cl (aq) + H 2 O / exotherm fest, nicht gelöst: Na + Cl
Junior-Laborführerschein für die Orientierungsstufe
 Junior-Laborführerschein für die Orientierungsstufe Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in
Junior-Laborführerschein für die Orientierungsstufe Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in
Untersuche an einigen Beispielen, welche Grundstoffe am Aufbau unserer Nahrung beteiligt sind.
 Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802200) 4. Nahrungsmittel und Nährstoffe Experiment von: Phywe Gedruckt: 07.0.203 5:36:8 intertess (Version
Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802200) 4. Nahrungsmittel und Nährstoffe Experiment von: Phywe Gedruckt: 07.0.203 5:36:8 intertess (Version
Rein oder nicht rein?
 Station 1: Rein oder nicht rein? Versuche: 1 Bestimmen Sie experimentell die Löslichkeit von Kochsalz. [Hinweis: Unter der Löslichkeit versteht man die Masse eines Stoffes in Gramm, die sich gerade noch
Station 1: Rein oder nicht rein? Versuche: 1 Bestimmen Sie experimentell die Löslichkeit von Kochsalz. [Hinweis: Unter der Löslichkeit versteht man die Masse eines Stoffes in Gramm, die sich gerade noch
Gruppe I : Darstellung und Nachweis von Säuren
 Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
10. Kohlensäure und ihre Salze (Kl. 9/10) Von Soda-Streamern, Backpulver und Kalk Kohlensäure und ihre Salze
 VI Säuren und Basen 10. Kohlensäure und ihre Salze (Kl. 9/10) 1 von 26 Von Soda-Streamern, Backpulver und Kalk Kohlensäure und ihre Salze Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von
VI Säuren und Basen 10. Kohlensäure und ihre Salze (Kl. 9/10) 1 von 26 Von Soda-Streamern, Backpulver und Kalk Kohlensäure und ihre Salze Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von
Entscheide bei jeder Aussage, ob es eine reine Beobachtung ist oder nicht, und kreuze an!
 Kerze Eine brennende Kerze wandelt Energie und Stoffe um. N_9d_44 Über eine brennende Rechaudkerze (Teelicht) wird ein «leeres» Glas gestülpt. Schülerinnen und Schüler notieren Aussagen zum Versuch. Entscheide
Kerze Eine brennende Kerze wandelt Energie und Stoffe um. N_9d_44 Über eine brennende Rechaudkerze (Teelicht) wird ein «leeres» Glas gestülpt. Schülerinnen und Schüler notieren Aussagen zum Versuch. Entscheide
Echt ätzend! - Was ist und wie wirkt Abflussreiniger?
 Echt ätzend! - Was ist und wie wirkt Abflussreiniger? Versuch 1: Zusammensetzung von festem Abflussreiniger (Analyse nach Prof. Pick ): fester Abflussreiniger (z.b. Drano Rohrfrei) Petrischale, Holzstab
Echt ätzend! - Was ist und wie wirkt Abflussreiniger? Versuch 1: Zusammensetzung von festem Abflussreiniger (Analyse nach Prof. Pick ): fester Abflussreiniger (z.b. Drano Rohrfrei) Petrischale, Holzstab
Rosa Geheimschrift. Durchführung
 Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Laborführerschein. Dieses Skript gehört:
 Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Veranstaltung 5: Zaubereien gibt es nicht!
 Veranstaltung 5: Zaubereien gibt es nicht! Station 1: Kerzenversuche E1 Steigendes Wasser E2 Löschen von Kerzenflammen durch Geisterhand Station 2: Farbenzauber E3 Zauberschriften E4 Zauberhafte Umwandlung
Veranstaltung 5: Zaubereien gibt es nicht! Station 1: Kerzenversuche E1 Steigendes Wasser E2 Löschen von Kerzenflammen durch Geisterhand Station 2: Farbenzauber E3 Zauberschriften E4 Zauberhafte Umwandlung
Merkmale Chemischer Reaktionen (qualitativ)
 Schulversuchspraktikum Carolin Schilling Sommersemester 2016 Klassenstufen 7&8 Merkmale Chemischer Reaktionen (qualitativ) Kurzprotokoll Auf einen Blick: Die beiden Schülerexperimente dieses Kurzprotokolls
Schulversuchspraktikum Carolin Schilling Sommersemester 2016 Klassenstufen 7&8 Merkmale Chemischer Reaktionen (qualitativ) Kurzprotokoll Auf einen Blick: Die beiden Schülerexperimente dieses Kurzprotokolls
Säuren und Basen im Haushalt
 Schulversuchspraktikum Lars Lichtenberg Sommersemester 2015 Klassenstufen 9 & 10 Säuren und Basen im Haushalt Kurzprotokoll Auf einen Blick: Die Unterrichtseinheit,,Säuren und Basen im Haushalt für die
Schulversuchspraktikum Lars Lichtenberg Sommersemester 2015 Klassenstufen 9 & 10 Säuren und Basen im Haushalt Kurzprotokoll Auf einen Blick: Die Unterrichtseinheit,,Säuren und Basen im Haushalt für die
Unser Magen produziert täglich bis
 VI Säuren und Basen 12. Neutralisation im Magen (Kl. 9/10) 1 von 20 Neutralisation im Magen Medikamente gegen Sodbrennen Ein Beitrag von Marie Emmerich-Barten, Nieder-Olm Mit Illustrationen von Katja Rau,
VI Säuren und Basen 12. Neutralisation im Magen (Kl. 9/10) 1 von 20 Neutralisation im Magen Medikamente gegen Sodbrennen Ein Beitrag von Marie Emmerich-Barten, Nieder-Olm Mit Illustrationen von Katja Rau,
Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) (Artikelnr.: P )
 Lehrer-/Dozentenblatt Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) (Artikelnr.: P7158900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Lehrer-/Dozentenblatt Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) (Artikelnr.: P7158900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Welche Eigenschaften besitzen Calcium- und Magnesiumlaugen?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P758900) 2.5 Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) Experiment von: Phywe Gedruckt: 5.0.203 2:3:05 intertess
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P758900) 2.5 Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) Experiment von: Phywe Gedruckt: 5.0.203 2:3:05 intertess
Betriebsanweisung nach 20 Gefahrstoffverordnung. Verwendete Chemikalien /37/ Kupfer (Pulver) - -
 Versuche 85-91 3 Problemfeld Stoffkreisläufe Betriebsanweisung nach 20 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeits merkmale Ammoniumdiammintetrathiocyanatochromat(III)
Versuche 85-91 3 Problemfeld Stoffkreisläufe Betriebsanweisung nach 20 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeits merkmale Ammoniumdiammintetrathiocyanatochromat(III)
In der Natur verschwindet nichts - Lösen und Auskristallisieren von Kochsalz
 Name: Datum: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Kochsalz Geräte Becherglas, Spatel, Alu-Teelichtschale, Heizplatte, Pipette, Tiegelzange, Glasstab, Lupe Materialien Kochsalz
Name: Datum: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Kochsalz Geräte Becherglas, Spatel, Alu-Teelichtschale, Heizplatte, Pipette, Tiegelzange, Glasstab, Lupe Materialien Kochsalz
Untersuche, warum zu Ammoniakdüngern häufig gebrannter Kalk gegeben wird.
 Naturwissenschaften - Chemie - Anorganische Chemie - 5 Düngemittel (P756300) 5.4 Gebrannter Kalk als Düngemittel Experiment von: Seb Gedruckt: 24.03.204 :57:28 intertess (Version 3.2 B24, Export 2000)
Naturwissenschaften - Chemie - Anorganische Chemie - 5 Düngemittel (P756300) 5.4 Gebrannter Kalk als Düngemittel Experiment von: Seb Gedruckt: 24.03.204 :57:28 intertess (Version 3.2 B24, Export 2000)
4.6 Die Verdauung im Mund. Aufgabe. Beginnt die Verdauung der Nahrungsmittel schon im Mund?
 Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802700) 4.6 Die Verdauung im Mund Experiment von: Phywe Gedruckt: 07.0.203 5:5:27 intertess (Version
Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802700) 4.6 Die Verdauung im Mund Experiment von: Phywe Gedruckt: 07.0.203 5:5:27 intertess (Version
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Kohlensäure und ihre Salze - Von Soda-Streamern, Backpulver und Kalk
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Kohlensäure und ihre Salze - Von Soda-Streamern, Backpulver und Kalk Das komplette Material finden Sie hier: School-Scout.de VI Säuren
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Kohlensäure und ihre Salze - Von Soda-Streamern, Backpulver und Kalk Das komplette Material finden Sie hier: School-Scout.de VI Säuren
Fortbildung am Schülerlabor in Rechtenthal für die Grundschule. Ideen zu weiterführenden Versuchen in der Klasse:
 Fortbildung am 16.11.2012 Schülerlabor in Rechtenthal für die Grundschule Ideen zu weiterführenden Versuchen in der Klasse: Lernziele: -Die Kinder erkennen chemische, physikalische Veränderungen (auch
Fortbildung am 16.11.2012 Schülerlabor in Rechtenthal für die Grundschule Ideen zu weiterführenden Versuchen in der Klasse: Lernziele: -Die Kinder erkennen chemische, physikalische Veränderungen (auch
Teil der Erdkruste die Erdalkalimetalle. Ein Beitrag von Günther Lohmer, Leverkusen Mit Illustrationen von Katja Rau, Berglen VORANSICHT
 1 von 26 Teil der Erdkruste die Erdalkalimetalle Ein Beitrag von Günther Lohmer, Leverkusen Mit Illustrationen von Katja Rau, Berglen Ob im Blitzlicht, im Feuerwerk, als Kreide oder als Mörtel Erdalkalimetalle
1 von 26 Teil der Erdkruste die Erdalkalimetalle Ein Beitrag von Günther Lohmer, Leverkusen Mit Illustrationen von Katja Rau, Berglen Ob im Blitzlicht, im Feuerwerk, als Kreide oder als Mörtel Erdalkalimetalle
»Kistenlernen«im Chemieunterricht. Online-Ergänzung HEIKE NICKEL. MNU 66/3 ( ) Seiten 1 7, ISSN , Verlag Klaus Seeberger, Neuss
 »Kistenlernen«im Chemieunterricht HEIKE NICKEL Online-Ergänzung MNU 66/3 (15.4.2013) Seiten 1 7, ISSN 0025-5866, Verlag Klaus Seeberger, Neuss 1 Material 1: Kisteninhalt»KISTENLERNEN«IM CHEMIEUNTERRICHT
»Kistenlernen«im Chemieunterricht HEIKE NICKEL Online-Ergänzung MNU 66/3 (15.4.2013) Seiten 1 7, ISSN 0025-5866, Verlag Klaus Seeberger, Neuss 1 Material 1: Kisteninhalt»KISTENLERNEN«IM CHEMIEUNTERRICHT
Junior-Laborführerschein
 Dieses Skript gehört: Junior-Laborführerschein für die Orientierungsstufe Station 1: Laborgeräte, ein Muss für jede Chemikerin und jeden Chemiker Suche an deinem Laborplatz die echten Gegenstände und überlege,
Dieses Skript gehört: Junior-Laborführerschein für die Orientierungsstufe Station 1: Laborgeräte, ein Muss für jede Chemikerin und jeden Chemiker Suche an deinem Laborplatz die echten Gegenstände und überlege,
Redoxreaktion oder Säure-Base-Reaktion?
 Redoxreaktion oder SäureBaseReaktion? Stand: 09.12.2018 Jahrgangsstufen 12 Fach Zeitrahmen Benötigtes Material Chemie 45 Minuten Zitrone, Natron, Soda, Spitzer mit Magnesiumgehäuse, Teelöffel (TL), 3 Bechergläser
Redoxreaktion oder SäureBaseReaktion? Stand: 09.12.2018 Jahrgangsstufen 12 Fach Zeitrahmen Benötigtes Material Chemie 45 Minuten Zitrone, Natron, Soda, Spitzer mit Magnesiumgehäuse, Teelöffel (TL), 3 Bechergläser
DOWNLOAD. Lineare Texte verstehen: Die Verdauung. Ulrike Neumann-Riedel. Downloadauszug aus dem Originaltitel: Sachtexte verstehen kein Problem!
 DOWNLOAD Ulrike Neumann-Riedel Lineare Texte verstehen: Die Verdauung Sachtexte verstehen kein Problem! Klasse 3 4 auszug aus dem Originaltitel: Vielseitig abwechslungsreich differenziert Was geschieht
DOWNLOAD Ulrike Neumann-Riedel Lineare Texte verstehen: Die Verdauung Sachtexte verstehen kein Problem! Klasse 3 4 auszug aus dem Originaltitel: Vielseitig abwechslungsreich differenziert Was geschieht
GEFÄHRDUNGSBEURT BADEN - WÜRTTEMBERG. Chemie. Gesamtband _2CBBH_ U1+U4_SI 1
 GEFÄHRDUNGSBEURT EILUNGEN BADEN - WÜRTTEMBERG Chemie Gesamtband _2CBBH_9783060156900 U1+U4_SI 1 06.02.17 12:37 Eine Welt aus en In ruhigem Wasser Wirf mit der Pinzette einen einzigen Kristall Kaliumpermanganat
GEFÄHRDUNGSBEURT EILUNGEN BADEN - WÜRTTEMBERG Chemie Gesamtband _2CBBH_9783060156900 U1+U4_SI 1 06.02.17 12:37 Eine Welt aus en In ruhigem Wasser Wirf mit der Pinzette einen einzigen Kristall Kaliumpermanganat
8.5 Backpulver. Aufgabe. Wieviel Backtriebmittel enthält Backpulver? Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P )
 Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P7188600) 8.5 Backpulver Experiment von: Seb Gedruckt: 08.04.2014 09:30:31 intertess (Version 13.12 B214, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P7188600) 8.5 Backpulver Experiment von: Seb Gedruckt: 08.04.2014 09:30:31 intertess (Version 13.12 B214, Export 2000) Aufgabe Aufgabe
Luft. Dieses Skript gehört: Wie setzt sich die Erdatmosphäre heute zusammen? 0,03% % 21% ca.1% 78% Stickstoff Sauerstoff Kohlendioxid Edelgase
 Luft Wie setzt sich die Erdatmosphäre heute zusammen? 0,03% % 21% ca.1% 78% Stickstoff Sauerstoff Kohlendioxid Edelgase Dieses Skript gehört: Versuch 1: Der Taucher findet einen Schatz Luft Seite 2 Schüssel
Luft Wie setzt sich die Erdatmosphäre heute zusammen? 0,03% % 21% ca.1% 78% Stickstoff Sauerstoff Kohlendioxid Edelgase Dieses Skript gehört: Versuch 1: Der Taucher findet einen Schatz Luft Seite 2 Schüssel
Name, Vorname: Klasse: Schule: Seite 1 von 7
 Name, Vorname: Klasse: Schule: Seite 1 von 7 Aufgabe 1: Roheisenherstellung im Hochofen Für die Herstellung von Roheisen im Hochofen werden die Ausgangsstoffe Eisenerz (Fe 2 O 3 ), Kohle (Kohlenstoff)
Name, Vorname: Klasse: Schule: Seite 1 von 7 Aufgabe 1: Roheisenherstellung im Hochofen Für die Herstellung von Roheisen im Hochofen werden die Ausgangsstoffe Eisenerz (Fe 2 O 3 ), Kohle (Kohlenstoff)
Sicher experimentieren
 Sicher experimentieren A1 Das Experimentieren im Labor kann gefährlich sein. Deswegen muss man sich an Regeln im Labor halten. Lies dir die 6 wichtigsten Regeln im Labor durch. 1. Kein Essen und Trinken
Sicher experimentieren A1 Das Experimentieren im Labor kann gefährlich sein. Deswegen muss man sich an Regeln im Labor halten. Lies dir die 6 wichtigsten Regeln im Labor durch. 1. Kein Essen und Trinken
Schüler und Schülerinnen im Labor in Rechtenthal. 4 weiße Stoffe
 Schüler und Schülerinnen im Labor in Rechtenthal 4 weiße Stoffe Chemische Laborgeräte (www.seilnacht.com) Chemische Stoffe unterscheiden sich durch ihre Eigenschaften 4 weiße Stoffe: Von außen sind sie
Schüler und Schülerinnen im Labor in Rechtenthal 4 weiße Stoffe Chemische Laborgeräte (www.seilnacht.com) Chemische Stoffe unterscheiden sich durch ihre Eigenschaften 4 weiße Stoffe: Von außen sind sie
Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker
 Name: Datum: Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter Materialien Lebensmittel: Glucose,
Name: Datum: Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter Materialien Lebensmittel: Glucose,
HTBL-PINKAFELD Arbeitsblatt A3/1 1.Station: KOHLENMONOXID. VORSICHT: Ameisensäure und konz. Schwefelsäure sind gefährliche Chemikalien!!
 HTBL-PINKAFELD Arbeitsblatt A3/1 1.Station: KOHLENMONOXID ÜBUNG: KOHLENMONOXID Für diese Versuche brauchst du: Proberöhren Proberöhrenständer Proberöhrenhalter Laborbrenner Ameisensäure konz. Schwefelsäure
HTBL-PINKAFELD Arbeitsblatt A3/1 1.Station: KOHLENMONOXID ÜBUNG: KOHLENMONOXID Für diese Versuche brauchst du: Proberöhren Proberöhrenständer Proberöhrenhalter Laborbrenner Ameisensäure konz. Schwefelsäure
Experimente Arbeitsblatt
 Lehrerinformation 1/6 Arbeitsauftrag Die SuS führen nacheinander verschiedene Versuche durch und protokollieren ihre Beobachtungen. Ziel Die SuS verstehen die chemischen Prozesse und die naturwissenschaftlichen
Lehrerinformation 1/6 Arbeitsauftrag Die SuS führen nacheinander verschiedene Versuche durch und protokollieren ihre Beobachtungen. Ziel Die SuS verstehen die chemischen Prozesse und die naturwissenschaftlichen
Die Verdauung im Mund (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die Verdauung im Mund (Artikelnr.: P8012700) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und Verdauung Unterthema: Verdauung
Lehrer-/Dozentenblatt Die Verdauung im Mund (Artikelnr.: P8012700) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und Verdauung Unterthema: Verdauung
Was macht ein Chemiker
 Was macht ein Chemiker Ein Chemiker befasst sich mit den unterschiedlichsten Stoffen und en. Er versucht herauszufinden, aus was sie bestehen, wie sie sich verhalten, wenn man sie zum Beispiel heiß oder
Was macht ein Chemiker Ein Chemiker befasst sich mit den unterschiedlichsten Stoffen und en. Er versucht herauszufinden, aus was sie bestehen, wie sie sich verhalten, wenn man sie zum Beispiel heiß oder
Name, Vorname: Klasse: Schule: Seite 1 von 7
 Name, Vorname: Klasse: Schule: Seite 1 von 7 Aufgabe 1: Chemische Reaktionen zur Metallherstellung Für die Herstellung von Roheisen im Hochofen werden die Ausgangsstoffe Eisenerz (Fe 2 O 3 ), Kohle (Kohlenstoff)
Name, Vorname: Klasse: Schule: Seite 1 von 7 Aufgabe 1: Chemische Reaktionen zur Metallherstellung Für die Herstellung von Roheisen im Hochofen werden die Ausgangsstoffe Eisenerz (Fe 2 O 3 ), Kohle (Kohlenstoff)
Institut für Anorganische Chemie (Materialchemie)
 1. Gib auf das Blatt Papier 2 Teelöffel Sand, 2 Teelöffel Kochsalz und einige kleine Nägel. 2. Vermische die drei Stoffe gut miteinander. Du hast jetzt ein so genanntes Gemenge hergestellt. 3. Zur Abtrennung
1. Gib auf das Blatt Papier 2 Teelöffel Sand, 2 Teelöffel Kochsalz und einige kleine Nägel. 2. Vermische die drei Stoffe gut miteinander. Du hast jetzt ein so genanntes Gemenge hergestellt. 3. Zur Abtrennung
DARUM GEHT S IN DIESER LernBOX. Mit dieser LernBOX kannst du folgendes lernen: A1 -wie man Kohlenstoffdioxid von Sprudel abtrennt. erledigt?
 Kohlenstoffdioxid (Teil1) Im Sprudel und in vielen Erfrischungsgetränken sorgen kleine Gasbläschen für ein angenehmes Kribbeln auf der Zunge. Sie bestehen aus Kohlenstoffdioxid, ein Gas, das nicht nur
Kohlenstoffdioxid (Teil1) Im Sprudel und in vielen Erfrischungsgetränken sorgen kleine Gasbläschen für ein angenehmes Kribbeln auf der Zunge. Sie bestehen aus Kohlenstoffdioxid, ein Gas, das nicht nur
Herstellung und Eigenschaften von Natronlauge
 Lehrer-/Dozentenblatt Herstellung und Eigenschaften von Natronlauge (Artikelnr.: P759000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie Unterthema:
Lehrer-/Dozentenblatt Herstellung und Eigenschaften von Natronlauge (Artikelnr.: P759000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie Unterthema:
Experimente mit Brausetabletten
 Experimente mit Brausetabletten Beim Auflösen von Brausetabletten reagiert Natriumhydrogencarbonat NaHCO 3 mit der ebenfalls in der Tablette enthaltener Säure (meist Wein- oder Citronensäure; allgemein
Experimente mit Brausetabletten Beim Auflösen von Brausetabletten reagiert Natriumhydrogencarbonat NaHCO 3 mit der ebenfalls in der Tablette enthaltener Säure (meist Wein- oder Citronensäure; allgemein
Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Rezepte: 1. Brause herstellen
 1D Rezepte: 1. Brause herstellen zutaten ½ TL Natron 2 TL Zucker 1 TL Zitronensäure 200 ml Wasser zubereitung Natron, Zucker und Zitronensäure in das Glas geben. Das Wasser hinzufügen. aufgaben Vergleiche
1D Rezepte: 1. Brause herstellen zutaten ½ TL Natron 2 TL Zucker 1 TL Zitronensäure 200 ml Wasser zubereitung Natron, Zucker und Zitronensäure in das Glas geben. Das Wasser hinzufügen. aufgaben Vergleiche
Von Arrhenius zu Brönsted
 Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Versuch 2: Darstellung von Natriumthiosulfat Na 2 S 2 O 3 * 5 H 2 O. Verwendete Geräte:
 Versuch 2: Darstellung von Natriumthiosulfat Na 2 S 2 O 3 * 5 H 2 O Verwendete Geräte: 250ml Kolben Heizpliz Kühler Magnetrührplatte Brenner Ceranplatte Filter Kristallisierschale Hot-Hand Messzylinder
Versuch 2: Darstellung von Natriumthiosulfat Na 2 S 2 O 3 * 5 H 2 O Verwendete Geräte: 250ml Kolben Heizpliz Kühler Magnetrührplatte Brenner Ceranplatte Filter Kristallisierschale Hot-Hand Messzylinder
Untersuche, ob Wasser gelöste Gase enthält und wovon die Löslichkeit der Gase abhängt.
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754700) 3.3 Löslichkeit von Gasen in Wasser Experiment von: Seb Gedruckt: 24.03.204 :24:34 intertess
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754700) 3.3 Löslichkeit von Gasen in Wasser Experiment von: Seb Gedruckt: 24.03.204 :24:34 intertess
Welcher Unterschied besteht zwischen schwefliger Säure und Schwefelsäure?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P75800).2 Oxidation von schwefliger Säure Experiment von: PHYWE Gedruckt: 0.0.205 3:05:3 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P75800).2 Oxidation von schwefliger Säure Experiment von: PHYWE Gedruckt: 0.0.205 3:05:3 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Den Advent mit allen Sinnen erleben
 Den Advent mit allen Sinnen erleben Ein Unterrichtsmodul für den naturwissenschaftlichen Anfangsunterricht E. MUSTROPH T. BECKMANNSHAGEN Online-Ergänzung MNU 63/7 (15.10.2010) Seiten 1 11, ISSN 0025-5866,
Den Advent mit allen Sinnen erleben Ein Unterrichtsmodul für den naturwissenschaftlichen Anfangsunterricht E. MUSTROPH T. BECKMANNSHAGEN Online-Ergänzung MNU 63/7 (15.10.2010) Seiten 1 11, ISSN 0025-5866,
Dieses Skript gehört:
 1 Dieses Skript gehört: 1 Quelle: http://www.hyperkommunikation.ch/lexikon/photosynthese.htm Versuch 1: Wie kann man Luft sichtbar machen? Vor euch auf dem Tisch steht eine Flasche. Beschreibt den Inhalt
1 Dieses Skript gehört: 1 Quelle: http://www.hyperkommunikation.ch/lexikon/photosynthese.htm Versuch 1: Wie kann man Luft sichtbar machen? Vor euch auf dem Tisch steht eine Flasche. Beschreibt den Inhalt
Zerlegung von Wasser durch Reduktionsmittel
 Lehrer-/Dozentenblatt Zerlegung von Wasser durch Reduktionsmittel (Artikelnr.: P7155500) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Lehrer-/Dozentenblatt Zerlegung von Wasser durch Reduktionsmittel (Artikelnr.: P7155500) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann.
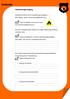 Verbrennungsvorgang Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann. Trage die Begriffe in die leeren Felder des Verbrennungsdreiecks ein. Die drei Voraussetzungen
Verbrennungsvorgang Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann. Trage die Begriffe in die leeren Felder des Verbrennungsdreiecks ein. Die drei Voraussetzungen
Verbrennung von Eisenwolle und Holz
 Name: Datum: Versuch: Verbrennung von Eisenwolle und Holz Geräte: 1 Stativ 2 Muffen 2 Klemmen 1 Laborboy (hier Holzklotz) 1 Porzellanschale 1 Analysetrichter 1 Gaswaschflasche 1 Wasserstrahlpumpe 1 Gummischlauch
Name: Datum: Versuch: Verbrennung von Eisenwolle und Holz Geräte: 1 Stativ 2 Muffen 2 Klemmen 1 Laborboy (hier Holzklotz) 1 Porzellanschale 1 Analysetrichter 1 Gaswaschflasche 1 Wasserstrahlpumpe 1 Gummischlauch
Die Verdauung im Magen (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die Verdauung im Magen (Artikelnr.: P8012800) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und Verdauung Unterthema: Verdauung
Lehrer-/Dozentenblatt Die Verdauung im Magen (Artikelnr.: P8012800) Curriculare Themenzuordnung Fachgebiet: Biologie Bildungsstufe: Klasse 7-10 Lehrplanthema: Ernährung und Verdauung Unterthema: Verdauung
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 2005/2006 Geltungsbereich: für Klassenstufe 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 2005/2006 Geltungsbereich: für Klassenstufe 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz
 Name: Datum: Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz Material: Kochsalz (NaCl), Leitungswasser, Mineralwasser, Becherglas, Spatel, destilliertes Wasser, Alu-Teelichtschalen,
Name: Datum: Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz Material: Kochsalz (NaCl), Leitungswasser, Mineralwasser, Becherglas, Spatel, destilliertes Wasser, Alu-Teelichtschalen,
Die Kerzenflamme (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die Kerzenflamme (Artikelnr.: P7154200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Luft und Verbrennungen
Lehrer-/Dozentenblatt Die Kerzenflamme (Artikelnr.: P7154200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Luft und Verbrennungen
SÄUR E. BASE oder LAU GE SAUE R BASI SCH
 SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
Gasentwickler Best.- Nr. MT00476
 Gasentwickler Best.- Nr. MT00476 I. Beschreibung Dieser Aufbau kann im Schullabor als Gasentwickler für die Erzeugung von geringen Gasmengen eingesetzt werden - Herstellung von Gasen aus Feststoffen (Granulat)
Gasentwickler Best.- Nr. MT00476 I. Beschreibung Dieser Aufbau kann im Schullabor als Gasentwickler für die Erzeugung von geringen Gasmengen eingesetzt werden - Herstellung von Gasen aus Feststoffen (Granulat)
Stoffeigenschaften auf der Spur
 Stoffeigenschaften auf der Spur Station 1 Welche Stoffe sind magnetisch? Sicherheit Entsorgung:/ Prüfe, welche Stoffe vom Magneten angezogen werden! Trage deine Beobachtungen in die Tabelle in deinem Forscherbuch
Stoffeigenschaften auf der Spur Station 1 Welche Stoffe sind magnetisch? Sicherheit Entsorgung:/ Prüfe, welche Stoffe vom Magneten angezogen werden! Trage deine Beobachtungen in die Tabelle in deinem Forscherbuch
Kohlenhydrate in Lebensmitteln - Nachweis von Zucker
 Name: Datum: Kohlenhydrate in Lebensmitteln - Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter, schwarzer Stift Materialien Glucose,
Name: Datum: Kohlenhydrate in Lebensmitteln - Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter, schwarzer Stift Materialien Glucose,
Untersuche die Kerzenflamme sowie die Vorgänge, die beim Verbrennen des Kerzenwachses ablaufen.
 Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P7154200) 2.10 Die Kerzenflamme Experiment von: Seb Gedruckt: 24.03.2014 11:14:37 intertess (Version 13.12 B214, Export 2000)
Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P7154200) 2.10 Die Kerzenflamme Experiment von: Seb Gedruckt: 24.03.2014 11:14:37 intertess (Version 13.12 B214, Export 2000)
4.7 Die Verdauung im Magen. Aufgabe. Wie funktioniert der Abbau der Eiweiße im Magen?
 Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802800) 4.7 Die Verdauung im Magen Experiment von: Phywe Gedruckt: 07.0.203 5:52:39 intertess (Version
Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802800) 4.7 Die Verdauung im Magen Experiment von: Phywe Gedruckt: 07.0.203 5:52:39 intertess (Version
Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser"
 Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser" a) Identifizierung des entstehenden Gases: Chemikalien: Geräte: Lithium [C] [F], Natrium [C] [F] (jeweils in Benzin mit Siedebereich 90-110
Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser" a) Identifizierung des entstehenden Gases: Chemikalien: Geräte: Lithium [C] [F], Natrium [C] [F] (jeweils in Benzin mit Siedebereich 90-110
Die SuS erklären die Entstehung saurer Lösungen mit dem Konzept von Arrhenius als Dissoziation von Chlorwasserstoff zu Hydoniumionen und
 1 Arbeitsblatt Das Arbeitsblatt dient der Protokollierung und der Auswertung des Lehrerversuches V1. Während die Versuchsdurchführung und Versuchbeobachtung wenig strukturiert sind, da die SuS über diese
1 Arbeitsblatt Das Arbeitsblatt dient der Protokollierung und der Auswertung des Lehrerversuches V1. Während die Versuchsdurchführung und Versuchbeobachtung wenig strukturiert sind, da die SuS über diese
3 150 ml-bechergläser als Wasserbäder Thermometer 2 ml-plastikpipetten Parafilm
 Nachweis der Enzymaktivität und Enzymhemmung Chemikalien: Harnstofflösung (10% w/v) Phenolphtalein-Lösung Urease rohe Kartoffel Wasserstoffperoxid-Lösung (30 % w/v) Bäckerhefe verdünnte Lösung von Methylenblau
Nachweis der Enzymaktivität und Enzymhemmung Chemikalien: Harnstofflösung (10% w/v) Phenolphtalein-Lösung Urease rohe Kartoffel Wasserstoffperoxid-Lösung (30 % w/v) Bäckerhefe verdünnte Lösung von Methylenblau
Stoffkreislauf: - Atmung und Kohlenstoffdioxid - Inhalt
 : - Atmung und Kohlenstoffdioxid - Inhalt Versuch 1 Kohlenstoffdioxidnachweis mit Kalkwasser 2 Versuch 2.1 Kohlenstoffdioxid in der Atemluft 3 Versuch 2.2 Kohlenstoffdioxid als Produkt der Verbrennung
: - Atmung und Kohlenstoffdioxid - Inhalt Versuch 1 Kohlenstoffdioxidnachweis mit Kalkwasser 2 Versuch 2.1 Kohlenstoffdioxid in der Atemluft 3 Versuch 2.2 Kohlenstoffdioxid als Produkt der Verbrennung
UNTERSUCHUNG VON KNALLERBSEN
 VERSUCHSANLEITUNGEN UNTERSUCHUNG VON KNALLERBSEN Knallerbsen 1 Reagenzglas 10/80 mm 1 Wäscheklammer 600 ml Der Inhalt einer noch nicht zur Reaktion gebrachten Knallerbse wird vorsichtig vom umhüllenden
VERSUCHSANLEITUNGEN UNTERSUCHUNG VON KNALLERBSEN Knallerbsen 1 Reagenzglas 10/80 mm 1 Wäscheklammer 600 ml Der Inhalt einer noch nicht zur Reaktion gebrachten Knallerbse wird vorsichtig vom umhüllenden
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen
 ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
Experimente zu den Themen Energie und Klimawandel
 Experimente zu den Themen Energie und Klimawandel Station 6: Kohlenstoffdioxid Schulfach: Biologie/Naturwissenschaften Sekundarstufe 1 Dieses Material ist im Rahmen des Projekts Bildung für einen nachhaltige
Experimente zu den Themen Energie und Klimawandel Station 6: Kohlenstoffdioxid Schulfach: Biologie/Naturwissenschaften Sekundarstufe 1 Dieses Material ist im Rahmen des Projekts Bildung für einen nachhaltige
Nachweis von Eisen-Ionen mit Kaliumthiocyanat
 Name: Datum: Nachweis von Eisen- mit Kaliumthiocyanat Geräte 3 Bechergläser (100 ml), 4 Reagenzgläser, Reagenzglasständer, kleiner Trichter, Faltenfilter, Spatel Materialien Eisennagel, Muscheln (braun
Name: Datum: Nachweis von Eisen- mit Kaliumthiocyanat Geräte 3 Bechergläser (100 ml), 4 Reagenzgläser, Reagenzglasständer, kleiner Trichter, Faltenfilter, Spatel Materialien Eisennagel, Muscheln (braun
Kopiervorlage 1: Eisen und Aluminium
 Kopiervorlage 1: Eisen und Aluminium 1. Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus: Eisen Aluminium Dichte Härte Schmelzpunkt Magnetisierbarkeit 2. a) Berechne die Eisenmenge
Kopiervorlage 1: Eisen und Aluminium 1. Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus: Eisen Aluminium Dichte Härte Schmelzpunkt Magnetisierbarkeit 2. a) Berechne die Eisenmenge
Essigsäure färbt ph-papier rot. Natronlauge färbt ph-papier blau
 5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
Anhand welcher Eigenschaften lässt sich Sauerstoff identifizieren?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75400) 5. Nachweis von Sauerstoff Experiment von: Phywe Gedruckt:.0.203 3:00:4 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75400) 5. Nachweis von Sauerstoff Experiment von: Phywe Gedruckt:.0.203 3:00:4 intertess (Version 3.06 B200, Export 2000) Aufgabe
Brenner Streichhölzer Eis
 Versuch 1: Wir erhitzen Eis! Reagenzglas Reagenzglasklammer Reagenzglasständer Brenner Streichhölzer Eis Fülle soviel Eis in das Reagenzglas, dass es zu einem Drittel gefüllt ist. Damit Du Dir beim Erhitzen
Versuch 1: Wir erhitzen Eis! Reagenzglas Reagenzglasklammer Reagenzglasständer Brenner Streichhölzer Eis Fülle soviel Eis in das Reagenzglas, dass es zu einem Drittel gefüllt ist. Damit Du Dir beim Erhitzen
Kohlenstoffdioxid (Teil1): LÖSUNGEN. DARUM GEHT S IN DIESER LernBOX. Mit dieser LernBOX kannst du folgendes lernen:
 Kohlenstoffdioxid (Teil1): LÖSUNGEN Im Sprudel und in vielen Erfrischungsgetränken sorgen kleine Gasbläschen für ein angenehmes Kribbeln auf der Zunge. Sie bestehen aus Kohlenstoffdioxid, ein Gas, das
Kohlenstoffdioxid (Teil1): LÖSUNGEN Im Sprudel und in vielen Erfrischungsgetränken sorgen kleine Gasbläschen für ein angenehmes Kribbeln auf der Zunge. Sie bestehen aus Kohlenstoffdioxid, ein Gas, das
7.3 Kohlendioxid. Aufgabe. Wie kann Kohlendioxid nachgewiesen werden? Naturwissenschaften - Chemie - Lebensmittelchemie - 7 Wasser
 Naturwissenschaften - Chemie - Lebensmittelchemie - 7 Wasser (P78800) 7.3 Kohlendioxid Experiment von: Anouch Gedruckt: 28.02.204 :4:54 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe Wie kann
Naturwissenschaften - Chemie - Lebensmittelchemie - 7 Wasser (P78800) 7.3 Kohlendioxid Experiment von: Anouch Gedruckt: 28.02.204 :4:54 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe Wie kann
Anhand welcher Eigenschaften lässt sich Wasserstoff identifizieren?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75500) 5.2 Nachweis von Wasserstoff Experiment von: Phywe Gedruckt:.0.203 3:02:34 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75500) 5.2 Nachweis von Wasserstoff Experiment von: Phywe Gedruckt:.0.203 3:02:34 intertess (Version 3.06 B200, Export 2000) Aufgabe
Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P )
 Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P1145600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P1145600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Schülercode Erste zwei Buchstaben Letzte zwei Buchstaben des Vornamens deiner Geburtstag (TT) deines Vornamens Mutter Kontext Experiment Aufgabe
 Schülercode Letzte zwei Buchstaben deines Vornamens Erste zwei Buchstaben des Vornamens deiner Mutter Geburtstag (TT) Kontext Experiment Aufgabe Erklärung Box 1 Kontext Kohlensäure im Mineralwasser Heute
Schülercode Letzte zwei Buchstaben deines Vornamens Erste zwei Buchstaben des Vornamens deiner Mutter Geburtstag (TT) Kontext Experiment Aufgabe Erklärung Box 1 Kontext Kohlensäure im Mineralwasser Heute
Lerne eine Nachweismöglichkeit für Zucker kennen und untersuche verschiedene Nahrungsmittel auf Zucker.
 Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802400) 4.3 Zuckerhaltige Nahrungsmittel Experiment von: Phywe Gedruckt: 07.0.203 5:38:40 intertess (Version
Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802400) 4.3 Zuckerhaltige Nahrungsmittel Experiment von: Phywe Gedruckt: 07.0.203 5:38:40 intertess (Version
M 4a 1: Fragen stellen
 M 4a 1: Fragen stellen Wozu? (Sinn, Zweck) Wo? (Ort) Bei Bewegung entsteht mehr Kohlenstoffdioxid. Wodurch? (Ursache) Wie viel? (Menge) Wie? (Art und Weise) M 4a 2: Je mehr man sich bewegt, desto mehr
M 4a 1: Fragen stellen Wozu? (Sinn, Zweck) Wo? (Ort) Bei Bewegung entsteht mehr Kohlenstoffdioxid. Wodurch? (Ursache) Wie viel? (Menge) Wie? (Art und Weise) M 4a 2: Je mehr man sich bewegt, desto mehr
2. Lebensmittel und Nährstoffe 2.2 Die Zusammensetzung von Lebensmitteln aus verschiedenen Nährstoffen Die Nährstoffe
 2. Lebensmittel und Nährstoffe 2.2 Die Zusammensetzung von Lebensmitteln aus verschiedenen Nährstoffen 2.2.1 Die Nährstoffe DIE ZUSAMMENSETZUNG DER LEBENSMITTEL Die meisten Lebensmittel bestehen aus zahlreichen
2. Lebensmittel und Nährstoffe 2.2 Die Zusammensetzung von Lebensmitteln aus verschiedenen Nährstoffen 2.2.1 Die Nährstoffe DIE ZUSAMMENSETZUNG DER LEBENSMITTEL Die meisten Lebensmittel bestehen aus zahlreichen
Endotherm und Exotherm
 Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 7 & 8 Endotherm und Exotherm Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 7 und 8 einen Lehrerversuch und einen
Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 7 & 8 Endotherm und Exotherm Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 7 und 8 einen Lehrerversuch und einen
2.6 Herstellung und Eigenschaften von Natronlauge. Aufgabe. Welche Eigenschaften besitzt Natronlauge?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P759000) 2.6 Herstellung und Eigenschaften von Natronlauge Experiment von: Phywe Gedruckt: 5.0.203 2:4:04 intertess (Version 3.06 B200, Export
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P759000) 2.6 Herstellung und Eigenschaften von Natronlauge Experiment von: Phywe Gedruckt: 5.0.203 2:4:04 intertess (Version 3.06 B200, Export
Zellen brauchen Sauerstoff Information
 Zellen brauchen Sauerstoff Information Tauchregel: Suche mit deiner schweren Tauchausrüstung einen direkten Weg zum Einstieg ins Wasser. Tauchen ist wie jede andere Sportart geprägt von körperlicher Anstrengung.
Zellen brauchen Sauerstoff Information Tauchregel: Suche mit deiner schweren Tauchausrüstung einen direkten Weg zum Einstieg ins Wasser. Tauchen ist wie jede andere Sportart geprägt von körperlicher Anstrengung.
Untersuche, wie rasch die Verdauung bei verschiedenen Eiweißarten erfolgt.
 Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802900) 4.8 Leicht verdauliches und schwer verdauliches Eiweiß Experiment von: Phywe Gedruckt: 07.0.203
Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802900) 4.8 Leicht verdauliches und schwer verdauliches Eiweiß Experiment von: Phywe Gedruckt: 07.0.203
8.1 Ammonium in Lakritz. Aufgabe. Warum schmecken Lakritze scharf? Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P )
 Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788200) 8. Ammonium in Lakritz Experiment von: Anouch Gedruckt: 28.02.204 :5:33 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788200) 8. Ammonium in Lakritz Experiment von: Anouch Gedruckt: 28.02.204 :5:33 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Anionen-Nachweis durch Fällungsreaktionen
 Lehrer-/Dozentenblatt Anionen-Nachweis durch Fällungsreaktionen (Artikelnr.: P7511300) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Allgemeine Chemie- Einführung
Lehrer-/Dozentenblatt Anionen-Nachweis durch Fällungsreaktionen (Artikelnr.: P7511300) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Allgemeine Chemie- Einführung
Veranstaltung 2: Wasser ist nicht nur zum Waschen da!
 Veranstaltung 2: Wasser ist nicht nur zum Waschen da! Station 1: Wann ist Wasser wirklich rein? E1 Wasser ist nicht gleich Wasser! E2 Können Stoffe in Wasser verschwinden? E3 Was sprudelt im Mineralwasser?
Veranstaltung 2: Wasser ist nicht nur zum Waschen da! Station 1: Wann ist Wasser wirklich rein? E1 Wasser ist nicht gleich Wasser! E2 Können Stoffe in Wasser verschwinden? E3 Was sprudelt im Mineralwasser?
