Destillation von Rohöl. + Rohbenzine + Petroleum
|
|
|
- Lennart Junge
- vor 7 Jahren
- Abrufe
Transkript
1 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/ Schulversuche Assistentin: Beate Abé Versuchsprotokoll Destillation von Rohöl Gruppe 1, Typ: Pflichtversuch 1. Reaktionsgleichung Erdöl C n + C C n + Rohbenzine + Petroleum + (...) z.b. Methan, Ethan..., langkettige (verzweigte) Kohlenwasserstoffe z.b. Ethen, Propen..., langkettige (verzweigte) Kohlenwasserstoffe n = 1,2, Zeitbedarf Vorbereitung Durchführung Nachbearbeitung Teil 1 Teil 2 15 min 1 min 10 min 5 min 10 min 1 min 3. Chemikalien Name Summenformel Gefahrensymbol R-Sätze S-Sätze Einsatz in der Schule Rohöl? F, T 45 53, 45 erlaubt Glaswolle Gefahrensymbole 4. Materialien/Geräte wärmeresistentes Reagenzglas mit Seitenansatz, nichtbrennbarer Stopfen mit Loch, Thermometer (bis 220 C), 4 Reagenzgläser, 4 Stopfen, 2 x Stativ und Stativklemme, gebogenes Glasrohr, Papier zum Kühlen, Porzellanschale 1
2 5. Versuchsaufbau Abb. 1: schematischer Versuchsaufbau für die Destillation von Rohöl [1] Abb. 2 Versuchsaufbau für die Destillation von Rohöl 6. Versuchsdurchführung In das wärmeresistente Reagenzglas mit Seitenansatz wird 2 ml Rohöl und ein kleines Bäuschen Glaswolle gegeben. Anschließend wird die Mischung mit dem Bunsenbrenner bis 90 C vorsichtig erhitzt. Das übergehende Destillat wird ein einem Reagenzglas aufgefangen und mit einem Stopfen verschlossen. Nun wird das Gemisch weiter bis 140 C und 220 C erhitzt und das Destillat jeweils wieder in einem Reagenzglas aufgefangen und mit einem Stopfen verschlossen. Die einzelnen Fraktionen werden dann nacheinander in eine Porzellanschale gegeben und angezündet. 2
3 7. Beobachtung Schon nach wenigen Sekunden des Erhitzens mit dem Bunsenbrenner siedet das Rohöl. Anschließend steigen weiße Nebelschwaden auf. Die Temperatur auf Höhe des Seitenansatzes steigt enorm schnell an. Bei 90 C geht das erste Destillat über. Dieses ist orange, leicht trüb und leicht viskos. Beim weiteren Erhitzen schnellt die Temperatur hoch bis auf 140 C. Das Destillat ist gelb, klar und viskoser als das erste. Erst beim dritten Destillationsversuch bewirkte weiteres Erhitzen des Rückstandes einen weiteren Temperaturanstieg auf 220 C. Dieses Destillat war orange, klar und ebenfalls viskos. Das erste Destillat verbrennt bei kleiner gelber Flamme. Beim zweiten ist die Flamme um einiges größer (Abb. 3), sie brennt länger und unter mehr Rußentwicklung. Die dritte Flamme erlischt sehr schnell, ist ebenfalls gelb, aber etwas kleiner als die Zweite (Abb. 4). Auch hier entwickelt sich Ruß. Abb. 3: Flamme der zweiten Fraktion Abb. 4: Flamme der dritten Fraktion 8. Entsorgung Der Rückstand im wärmeresistenten Reagenzglas kann am besten entfernt werden, indem mit Petrolether und Eis kräftig ausgeschüttelt wird. Die Lösung wird neutral im Behälter für organische Lösungsmittel entsorgt. Die Glaswolle wird getrocknet und im Behälter für Feststoffe entsorgt. 9. Fachliche Analyse Das direkt aus der Erde stammende unbehandelte Erdöl wird auch als Rohöl bezeichnet. Dabei handelt es sich um einen fossilen Rohstoff, der vorwiegend durch bakterielle Zersetzung organischer Substanzen entsteht. Es befindet sich als lipophiles Stoffgemisch in der Erdkruste. Die Hauptbestandteile sind gesättigte und ungesättigte Kohlenwasserstoffe, sowie Aromaten Phenole, Harze, Aldehyde und organische Schwefelverbindungen. Je nach Mischung dieser Bestandteile reicht die Farbe des Erdöls von hellgelb bis schwarz. Die Tatsache, dass fast überall auf der Erde Erdöl gefördert wird macht deutlich, dass kein Öl einem anderen gleicht. Je nach der Herkunft ist die Zusammensetzung der Erdöle sehr verschieden. Heute wird Erdöl hauptsächlich als Kraftstoffe aller Verkehrsmittel und zur Erzeugung von Elektrizität, also als Energiequelle, genutzt. Durch chemische Behandlung und Destillation von Erdöl erhält man Benzin, Kerosin, Heizöl, Dieselkraftstoff, Schmieröl, Paraffine und andere Verbindungen. Für die Autokraftstoffe ist die Octanzahl von großer Bedeutung. Sie gibt an, wie gleichmäßig die 3
4 Zündtemperatur ist, beschreibt also die Klopffestigkeit. Ist die Zündtemperatur ungleichmäßig bzw. die Klopffestigkeit nur mäßig, so stottert der Motor. Dazu wird das jeweilige Benzin mit dem sehr klopffesten 2,2,4-Trimethylpentan (Isooctan), das die Octanzahl 100, und dem wenig klopffesten Heptan, das die Octanzahl 0 erhielt verglichen. Verhält sich dieser Kraftstoffe beispielsweise wie ein Gemisch aus 90 % Isooctan und 10 % Heptan, so enthält dieser die Octanzahl 90. In Deutschland werden 39 % des Energiebedarfs durch Erdöl gedeckt. Der Verbrauch lag 2001 bei Tonnen, von denen Tonnen aus anderen Ländern importiert wurden. Wissenschaftler weltweit versuchen aufgrund der Abhängigkeit von Erdöl alternative Energiequellen zu finden. Vor allem für Länder wie Deutschland, die selber keine großen Erdöl vorkommen haben, würden sie andere Energiequellen positiv auf die Ökonomie auswirken. Die bisher vorgestellten Ideen zu alternativen Energiequellen sind z.b. Kernenergie, Wasserkraft Solarenergie, Windkraft, die Energie von Meereswellen und auch die Herstellung von Brennstoff aus organischen Substanzen. Das Erdöl wird entweder in der Nähe des Herkunftsortes aufgearbeitet, oder aber durch Pipelines zu so genannten Ölraffinerien transportiert. Dort werden die Kohlenwasserstoffgemische entsprechend ihrer Siedetemperatur durch Destillation in verschiedene Fraktionen getrennt. Abb. 5: Destillation von Rohöl in einer Raffinerie [7] Dabei wird in einem Röhrenofen das Öl auf mehr als 360 C erhitzt. Da die Temperatur über der Siedetemperatur des Öls liegt verdampfen die Bestandteile und gelangen in den Destillationsturm, der durch zahlreiche Glockenböden unterteilt wird. Da die Temperatur darin von unten nach oben abnimmt, kondensieren die einzelnen Bestandteile auf unterschiedlichen Glockenböden. Dort werden die Fraktionen seitlich abgeleitet. Der Rückstand wird schließlich einer Vakuumdestillation zugeführt. Durch die Siedepunkterniedrigung verdampfen auch diese Bestandteile bei ca C und können auf Höhe der jeweiligen Glocke abgeleitet werden. Hier ist die Vakuumdestillation enorm wichtig, da die meisten Kohlenwasserstoff bei Temperaturen über 400 C zerfallen würden, dies aber durch die Siedepunkterniedrigung vermieden werden kann. Durch dieses Verfahren folgende Fraktionen enthalten: 4
5 Gase (Methan, Ethan) und Flüssiggase(Propan, Butan): Sdp. bis 35 C Sie durchströmen die Kolonne und werden am Kopf dieser abgezogen. Durch Flüssiggastrennanlagen werden sie getrennt. Rohbenzin: Sdp C ( C Leichtbenzine; C Schwerbenzine) Sie werden im oberen Teil der Kolonne abgezogen. Petroleum/Kerosin: Sdp C leichte Gasöle: Sdp C schwere Gasöle: Sdp C atmosphärischer Rückstand In diesem Versuch wurde eine vereinfachte Destillation von Rohöl durchgeführt. Die einzelnen Fraktionen sind nicht rein, sondern enthalten mehrere Stoffe, die alle eine ähnliche Siedetemperatur haben. Wie in der Reaktionsgleichung zu sehen ist, reichen die Produkte von kurzkettigen Kohlenwasserstoffen wie Methan oder Ethan bis zu sehr langkettigen Kohlenstoffverbidnungen.Die unterschiedlichen Farben der Destillate resultieren aus der Zusammensetzung der verschiedenen Kohlenwasserstoffen in einer Fraktion. Die Destillate gehen jedoch nicht wie in der Vorschrift bei 70 C, 120 C, 140 C und 220 C über, sondern erst bei 90 C bzw. 140 C und 220 C. Dies liegt wahrscheinlich daran, dass in diesem Versuch nicht das gleiche Erdöl wie in der Versuchsvorschrift verwendet wurde. Wie oben beschrieben gleicht kein Erdöl dem anderen. Dadurch enthält man für jedes Öl verschiedene Siedetemperaturen, die von der Zusammensetzung der Bestandteile abhängig ist. Durch die ungenaue Temperatureinstellung mit dem Bunsenbrenner ist es des Weiteren wahrscheinlich dazu gekommen, dass in einem der Destillate gleich zwei Fraktionen zusammen überdestilliert wurden. Die Beobachtung der steigenden Viskosität und vermehrten Rußentwicklung bei der Verbrennung mit den Fraktionen mit steigender Siedetemperatur spiegelt die Gesetzmäßigkeiten der homologen Reihe wider. Mit zunehmender Kettenlänge steigen sowohl die Siedetemperatur und die Schmelztemperatur, als auch die Van-der-Waals-Kräfte aufgrund der zunehmenden Anzahl der Elektronen der Moleküle. Bei sehr langen Alkanen können die Van-der-Waals-Kräfte sogar stärker werden als eine Elektronenbindung zwischen zwei Kohlenstoffatomen. Bei starkem Erwärmen kommt es dann nicht zur Trennung von Molekülen, sondern zur Spaltung der Atombindung im Molekül. Dieser Vorgang ist in einer Destillation jedoch unerwünscht, deshalb wird der Rückstand in einer Ölraffinerie wie oben beschrieben einer Vakuumdestillation zugeführt. Die Van-der-Waals-Kräfte beeinflussen jedoch nicht nur den Siedepunkt, sondern auch die Viskosität einer Flüssigkeit. Durch größer werdende Van-der- Waals-Kräfte fließen die Moleküle einer Flüssigkeit immer langsamer aneinander vorbei. Innerhalb der homologen Reihe nimmt ebenfalls die Intensität der Flamme und der Rußbildung zu. Das Leuchten der Flamme liegt am Glühen einzelner Kohlenstoffteilchen, die im Saum der Flamme mit Luftsauerstoff zu Kohlenstoffdioxid reagieren. Bei gleich bleibendem Sauerstoffangebot (Verbrennung an der Luft) verbrennen die Fraktionen immer unvollständiger, da der Anteil der Kohlenstoffatome mit jeder Fraktion zunimmt. Diese Kohlenstoffteilchen gelangen in kältere Bereiche der Flamme und werden dort als Ruß sichtbar, da sie aufgrund der fehlenden Wärme nicht mehr mit dem Sauerstoff reagieren. 5
6 Das erste Destillat enthielt also kurzkettigen Kohlenwasserstoffe, während die die Destillate der höheren Temperatur langkettigere Kohlenwasserstoffe enthalten. Das Problem, dass erst im dritten Versuch Destillat bei 220 C überging, könnte entweder daran gelegen haben, dass zu wenig Rückstand im Reagenzglas übrig geblieben ist, also einfach zu wenig Substanz verwendet worden ist, oder aber auch daran, dass die Temperatur des Erdöls im unteren Teil des Reagenzglases zu hoch war und es dadurch zu der oben beschriebenen Spaltung der Atombindung im Molekül gekommen ist. Diese Eigenschaft wird sich jedoch beim Crack-Verfahren zu Nutze gemacht. Bei der fraktionierten Destillation entstehen zu viele langkettige Kohlenwasserstoffe, die kaum Verwendung finden. Deshalb werden diese Moleküle unter erhöhtem Druck und starker Hitze (thermisches Cracken) in Schwingung gebracht, um sie zu spalten. Diese kurzkettigen Kohlenwasserstoffe können anschließend erneut einer fraktionierten Destillation zugeführt werden, um Benzine zu erhalten. 10. Didaktische Analyse Dieser Versuch kann nach dem Lehrplan für G 9 gut ans Ende der 10. Klasse gesetzt werden, denn dann lautet das Thema Brennstoffe: Erdöl und Erdgas. Vor allem für den Einstieg ist dieses Experiment zu empfehlen, da sich die Frage aufwirft, welche Bestandteile in welchen Fraktionen wieder zu finden sind und woraus Erdöl überhaupt besteht. Daran schließt sich die fraktionierte Destillation im Industriemaßstab und das Cracken von Erdöl an. Im weiteren Verlauf kann über die Entstehung und die Vorkommen des Erdöls, die Erdölförderung und den Transport gesprochen werden. Vielleicht bietet sich hier eine Gelegenheit zusammen mit dem Fach Erdkunde fächerübergreifend zu unterrichten. Gerade heute schließt sich daran ein wichtiges weltpolitisches bzw. -wirtschaftliches Problem an: die immer kleiner werdenden Erdölreserven und alternative Energiequellen, wie z.b. Rapsöl. In diesem Zusammenhang muss die gesellschaftliche Frage, ob Energiequellen anstelle von anderen Lebensmitteln angebaut werden dürfen, diskutiert werden. Auch auf das große Thema Klimawandel kann in diesem Atemzug Bezug genommen werden. Bei den Schülerinnen und Schüler sollte das Thema auf breites Interesse stoßen, da hier der Alltagsbezug im Fach Chemie sofort gesehen wird. Es kann jedoch auch als Einleitung für die Themen Viskosität von Flüssigkeiten oder Van-der-Waals-Kräfte dienen. Ebenso könnte dieser Versuch als Einführung in die organische Chemie genutzt werden. Anschließend könnte allgemein auf organische Verbindungen und die Nomenklatur der Kohlenwasserstoffe eingegangen werden. Die Vorbereitung dieses Versuchs nimmt nicht sehr viel Zeit in Anspruch. Es müssen lediglich die Stative aufgestellt werden, solange das gebogene Glasrohr schon vorhanden ist. Der Versuch sollte von der Lehrperson jedoch schon einmal im Vorfeld durchgeführt worden sein, um zu wissen bei welchen Temperaturen die Destillate übergehen. Wie oben beschrieben, variieren diese von Erdöl zu Erdöl. Beim Wechsel der Reagenzgläser sollte nicht viel Zeit verstreichen und der Bunsenbrenner mit etwas Abstand unter dem wärmeresistenten Reagenzglas stehen bleiben, damit die Temperatur nicht wieder absinkt. Die Destillate in der Porzellanschale werden am einfachsten mit dem Bunsenbrenner angezündet. Da die Schüler selbst mit dem Erdöl experimentieren dürfen, vielen Schulen jedoch die entsprechende Menge an Apparaturen fehlt, sollte dieser Versuch vom Lehrer durchgeführt werden. Die Zündung in der Porzellanschale kann jedoch von den Schülern übernommen werden. Auch wenn 6
7 die einzelnen Fraktionen nicht rein sind, so stellt diese Destillation von Rohöl einen sinnvollen und nicht allzu zeitintensiven Versuch dar, der für die Schule auf jeden Fall lohnenswert ist. Trotz der Verunreinigungen kann das Prinzip der Destillation verständlich vermittelt werden und die fraktionierte Destillation des Erdöls veranschaulicht werden. Bei dieser Destillation ist vor allem sehr gut beobachtbar, dass im Rückstand die spät siedenden Substanzen zurückbleiben, da dieser noch schwarz ist, die früh siedenden Substanzen jedoch als Destillat übergegangen sind. Die Unterschiede in der Zusammensetzung der Destillate sind aufgrund der Farbunterschiede ersichtlich. 11. Literatur Versuchsquelle: [1] CONATEX-DIDACTIC Lehrmittel GmBH, Chemie: Erdöl und Cracken, (letzter Zugriff: , 17:48 Uhr) Fachquellen: [2] BGIA (Berufsgenossenschaftliches Institut für Arbeitsschutz), Gefahrstoffinformationssystem der gewerblichen Berufsgenossenschaften, [3] Elemente Chemie II, Organische Chemie, 1. Auflage, Ernst-Klett-Verlag, Stuttgart, 2005 [4] Landesinstitut für Schule Nordrhein-Westfalen, Liste zur Einstufung von Gefahrstoffen (Soester- Liste), 10. Auflage, Stand: , Version 2.7 [5] Fachinformationszentrum Chemie, (letzter Zugriff: , 15:09 Uhr) [6] Hessisches Kultusministerium, Lehrplan Chemie für die Jahrgansstufen G7 bis G12, (letzter Zugriff: , 16:28 Uhr) [7] Seilnacht, T., Erdöl und Erölverarbeitung, (letzter Zugriff: , 22:26 Uhr) [8] Vollhardt, K. Peter C., Schore, Neil E., Organische Chemie, Vierte Auflage, Wiley-VCH, Weinheim, 2005 [9] Wikimedia Foundation Inc., (letzter Zugriff: , 15:09 Uhr) 7
Versuch: Thermisches Cracken von Paraffinöl
 Philipps-Universität Marburg 21.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2, Alkane Versuch: Thermisches Cracken von Paraffinöl
Philipps-Universität Marburg 21.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2, Alkane Versuch: Thermisches Cracken von Paraffinöl
Versuch: Destillation von Rohöl
 Philipps-Universität Marburg 26.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Destillation von Rohöl
Philipps-Universität Marburg 26.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Destillation von Rohöl
Versuchsprotokoll. Züchtung von Kandiszucker-Kristallen
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Züchtung von Kandiszucker-Kristallen
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Züchtung von Kandiszucker-Kristallen
Organisch-chemisches Praktikum für Studierende des Lehramts WS 2010/11
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 00/ Praktikumsleitung: Dr. Reiß Assistent(in): Sarah Henkel Name: Johannes Hergt Datum: 6..00 Gruppe : Alkane Versuch (Assi): Umgießen von
Organisch-chemisches Praktikum für Studierende des Lehramts WS 00/ Praktikumsleitung: Dr. Reiß Assistent(in): Sarah Henkel Name: Johannes Hergt Datum: 6..00 Gruppe : Alkane Versuch (Assi): Umgießen von
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 25.11.2008 Zeitbedarf Vorbereitung: 5 Minuten Durchführung:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 25.11.2008 Zeitbedarf Vorbereitung: 5 Minuten Durchführung:
Versuchsprotokoll. Mischbarkeit von Alkoholen
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
Versuchsprotokoll. Reaktivität von Alkylbromiden. Gruppe 5, Typ: Pflichtversuch. AgBr + HNO 3 + H 3 C C C C. AgBr + HNO 3 +
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Reaktivität von Alkylbromiden Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Reaktivität von Alkylbromiden Gruppe
Fossile Rohstoffe. Erdöl
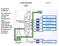 Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
Versuchsprotokoll. Nitrierung von Phenol. Gruppe 4, Typ: Pflichtversuch O O - N
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Versuchsprotokoll. Nachweis von Kohlenstoff und Wasserstoff in Spagetti
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 12.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Nachweis von Kohlenstoff und Wasserstoff
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 12.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Nachweis von Kohlenstoff und Wasserstoff
+ 30,5 O 2 (g) 20 CO 2 (g) + 21 H 2 O
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 1: Einführung der OC Versuch: Nachweis
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 1: Einführung der OC Versuch: Nachweis
Erdöl. "... ist eine nutzlose Absonderung der Erde eine klebrige Flüssigkeit, die stinkt und in. keiner Weise verwendet werden kann.
 Erdöl "... ist eine nutzlose Absonderung der Erde eine klebrige Flüssigkeit, die stinkt und in keiner Weise verwendet werden kann." ('Akademie der Wissenschaften' in St. Petersburg 1806) Erdöl, schwarzes
Erdöl "... ist eine nutzlose Absonderung der Erde eine klebrige Flüssigkeit, die stinkt und in keiner Weise verwendet werden kann." ('Akademie der Wissenschaften' in St. Petersburg 1806) Erdöl, schwarzes
Versuch: Bromierung von n-hexan. Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Bemerkung
 Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
Gruppe 02: Chemischer Flammenwerfer
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 02: Chemischer Flammenwerfer Reaktion: Chemikalien: Eingesetzte Stoffe
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 02: Chemischer Flammenwerfer Reaktion: Chemikalien: Eingesetzte Stoffe
Versuchsprotokoll. Maillard-Reaktion
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.08 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Maillard-Reaktion Gruppe 10,
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.08 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Maillard-Reaktion Gruppe 10,
Versuchsprotokoll. Kernbromierung und Seitenkettenbromierung von Xylol. Gruppe 4, Typ: Assiversuch KKK SSS
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Kernbromierung und Seitenkettenbromierung
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Kernbromierung und Seitenkettenbromierung
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lehrerhandreichungen zum Unterrichtsfilm: "Erdöl - Ein Rohstoff wird verarbeitet und veredelt" Das komplette Material finden Sie hier:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lehrerhandreichungen zum Unterrichtsfilm: "Erdöl - Ein Rohstoff wird verarbeitet und veredelt" Das komplette Material finden Sie hier:
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Alkane - eine vielseitige Stoffgruppe. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Alkane - eine vielseitige Stoffgruppe Das komplette Material finden Sie hier: School-Scout.de RAAbits Hauptschule 7 9 Naturwissenschaften
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Alkane - eine vielseitige Stoffgruppe Das komplette Material finden Sie hier: School-Scout.de RAAbits Hauptschule 7 9 Naturwissenschaften
Versuchsprotokoll. Synthese von Aromastoffen. Gruppe 7, Typ: Pflichtversuch O OH H 3 C C C C C CH 3 H H 3 C C C C C O C C OH
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 26.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Synthese von Aromastoffen Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 26.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Synthese von Aromastoffen Gruppe
Versuchsprotokoll. Alkoholische Gärung von Traubensaft
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 27.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Alkoholische Gärung von Traubensaft
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 27.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Alkoholische Gärung von Traubensaft
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
Lernzirkel Erdöl. Name:
 Lernzirkel Erdöl Name: Namen der weiteren Gruppenmitglieder: 1 2 3 Inhalt des Lernzirkels: Station Name Inhalt 1 Cracken Experimental Durchführung des Crackens 2 Oktanzahl Internet Recherche Definition
Lernzirkel Erdöl Name: Namen der weiteren Gruppenmitglieder: 1 2 3 Inhalt des Lernzirkels: Station Name Inhalt 1 Cracken Experimental Durchführung des Crackens 2 Oktanzahl Internet Recherche Definition
Untersuche die Kerzenflamme sowie die Vorgänge, die beim Verbrennen des Kerzenwachses ablaufen.
 Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P7154200) 2.10 Die Kerzenflamme Experiment von: Seb Gedruckt: 24.03.2014 11:14:37 intertess (Version 13.12 B214, Export 2000)
Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P7154200) 2.10 Die Kerzenflamme Experiment von: Seb Gedruckt: 24.03.2014 11:14:37 intertess (Version 13.12 B214, Export 2000)
Fossile Rohstoffe. Kohlenwasserstoffe als Energieträger
 Kohlenwasserstoffe als Energieträger, Kohle, Erdgas und Torf sind im Laufe von Millionen von Jahren aus Kleinlebwesen und Pflanzen entstanden und werden deswegen als fossile Energieträger bezeichnet. Da
Kohlenwasserstoffe als Energieträger, Kohle, Erdgas und Torf sind im Laufe von Millionen von Jahren aus Kleinlebwesen und Pflanzen entstanden und werden deswegen als fossile Energieträger bezeichnet. Da
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch: Reaktivität
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch: Reaktivität
Versuch: Qualitativer Nachweis von Kohlenstoff und Wasserstoff
 Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Sublimation & Resublimation
 Reaktionsgleichung I 2 (s) I2 (g) I 2 (s) Zeitbedarf Vorbereitung: 15 min. Durchführung: 7 Std. Nachbereitung: 20 min. Chemikalienliste Edukte Chemikalien Summenformel R-Sätze S-Sätze Gefahrensymbole Schuleinsatz
Reaktionsgleichung I 2 (s) I2 (g) I 2 (s) Zeitbedarf Vorbereitung: 15 min. Durchführung: 7 Std. Nachbereitung: 20 min. Chemikalienliste Edukte Chemikalien Summenformel R-Sätze S-Sätze Gefahrensymbole Schuleinsatz
Bromierung von Hexan G2 Pflichtversuch Bromierung von Cyclohexan und Cyclohexen G3 Pflichtversuch
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.11.08 Schulversuche Assistentin: Beate Abé omierung von exan G2 Pflichtversuch omierung von
Anna-Lena Eicke Philipps-Universität Marburg Organisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.11.08 Schulversuche Assistentin: Beate Abé omierung von exan G2 Pflichtversuch omierung von
Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Eigenschaften, Vorkommen und Anwendungen einiger C 5 -C 10 -Alkane
 Eigenschaften, Vorkommen und Anwendungen einiger C 5 -C 10 -Alkane C 5 H 12 : Pentane (3 Konstitutions-Isomere) n-pentan: SdT 36 C SmT - 130 C Dichte 0,63g/cm 3 (20 C) F +, X n, N R 12-65-66-51/53 S (2)-9-16-29-33-61-62
Eigenschaften, Vorkommen und Anwendungen einiger C 5 -C 10 -Alkane C 5 H 12 : Pentane (3 Konstitutions-Isomere) n-pentan: SdT 36 C SmT - 130 C Dichte 0,63g/cm 3 (20 C) F +, X n, N R 12-65-66-51/53 S (2)-9-16-29-33-61-62
FWU Schule und Unterricht. FWU-Klassiker Erdöl Ein Rohstoff wird veredelt. FWU das Medieninstitut der Länder
 FWU Schule und Unterricht DVD 46 02480 14 min, Farbe FWU-Klassiker Erdöl Ein Rohstoff wird veredelt FWU das Medieninstitut der Länder 00 Lernziele nach Lehrplänen und Schulbüchern Erkenntnis, dass Erdöl
FWU Schule und Unterricht DVD 46 02480 14 min, Farbe FWU-Klassiker Erdöl Ein Rohstoff wird veredelt FWU das Medieninstitut der Länder 00 Lernziele nach Lehrplänen und Schulbüchern Erkenntnis, dass Erdöl
Schulversuch-Protokoll Jan gr. Austing
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von Nitroglycerin
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von Nitroglycerin
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 1: Einführung der OC Versuch: Modellversuch
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 1: Einführung der OC Versuch: Modellversuch
Untersuche die ausgegebenen Stoffe auf Brennbarkeit und Schmelztemperatur.
 Naturwissenschaften - Chemie - Allgemeine Chemie - Stoffeigenschaften (P750200).2 Stoffeigenschaften - Brennbarkeit, Schmelztemperatur Experiment von: Phywe Gedruckt: 07.2.205 :7:33 intertess (Version
Naturwissenschaften - Chemie - Allgemeine Chemie - Stoffeigenschaften (P750200).2 Stoffeigenschaften - Brennbarkeit, Schmelztemperatur Experiment von: Phywe Gedruckt: 07.2.205 :7:33 intertess (Version
Gruppe 6 Pflichtversuch. Abnahme der Wasserlöslichkeit der Alkanole mit zunehmender Molekülgröße
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 02.06.09 SS 09 Gruppe 6 Pflichtversuch Abnahme der Wasserlöslichkeit
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 02.06.09 SS 09 Gruppe 6 Pflichtversuch Abnahme der Wasserlöslichkeit
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Alkoholtest):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Alkoholtest):
Kapitel 02: Erdgas und Erdöl
 Kapitel 02: Erdgas und Erdöl 1 Kapitel 02: Erdgas und Erdöl Kapitel 02: Erdgas und Erdöl 2 Inhalt Kapitel 02: Erdgas und Erdöl...1 Inhalt... 2 Einige Produkte aus Erdöl...3 Erdöl ist nicht gleich Erdöl...3
Kapitel 02: Erdgas und Erdöl 1 Kapitel 02: Erdgas und Erdöl Kapitel 02: Erdgas und Erdöl 2 Inhalt Kapitel 02: Erdgas und Erdöl...1 Inhalt... 2 Einige Produkte aus Erdöl...3 Erdöl ist nicht gleich Erdöl...3
Versuch: Fäden spinnen Polymer aus Citronensäure und Glycerin
 Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Versuchsprotokoll. Gummibärchen-Indikator
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Gummibärchen-Indikator Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Gummibärchen-Indikator Gruppe
Gruppe 2 eigener Versuch. Veränderung einer Kerzenflamme in Feuerzeuggas
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 20.05.09 SS 09 Gruppe 2 eigener Versuch Veränderung einer Kerzenflamme
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 20.05.09 SS 09 Gruppe 2 eigener Versuch Veränderung einer Kerzenflamme
Gruppe 1 Pflichtversuch. Qualitative Analyse: Nachweis von Kohlenstoff als Kohlendioxid
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 19.05.09 SS 09 Gruppe 1 Pflichtversuch Qualitative Analyse: Nachweis
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 19.05.09 SS 09 Gruppe 1 Pflichtversuch Qualitative Analyse: Nachweis
Schulcurriculum für die Einführungsphase Chemie Jahrgang 11
 Helene-Lange-Schule Hannover Schulcurriculum für die Einführungsphase Chemie Jahrgang 11 ganzjähriger Unterricht: ca. 64 Unterrichtsstd. Hinweis: Folgende grundlegende Kompetenzen aus dem Bereich Kommunikation
Helene-Lange-Schule Hannover Schulcurriculum für die Einführungsphase Chemie Jahrgang 11 ganzjähriger Unterricht: ca. 64 Unterrichtsstd. Hinweis: Folgende grundlegende Kompetenzen aus dem Bereich Kommunikation
Versuch: Isolierung von Citronensäure aus Zitronen
 Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 11, Naturstoffe und Lebensmittel Versuch: Isolierung
Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 11, Naturstoffe und Lebensmittel Versuch: Isolierung
Untersuche die ausgegebenen Stoffe auf Brennbarkeit und Schmelztemperatur.
 Naturwissenschaften - Chemie - Allgemeine Chemie - Stoffeigenschaften (P750200).2 Stoffeigenschaften - Brennbarkeit, Schmelztemperatur Experiment von: Phywe Gedruckt:.0.203 2:44:57 intertess (Version 3.06
Naturwissenschaften - Chemie - Allgemeine Chemie - Stoffeigenschaften (P750200).2 Stoffeigenschaften - Brennbarkeit, Schmelztemperatur Experiment von: Phywe Gedruckt:.0.203 2:44:57 intertess (Version 3.06
+ 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose
![+ 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose + 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose](/thumbs/54/33374656.jpg) Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Tollensprobe mit Glucose
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Tollensprobe mit Glucose
Versuch: Molischprobe mit Gelatine H 2 SO 4. O - 2 H e H 2. Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
 Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Molischprobe
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Molischprobe
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 2: Alkane Versuch: Gewinnung von Methan
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 2: Alkane Versuch: Gewinnung von Methan
Endersch, Jonas 09./
 Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Organische Chemie II. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Wie ist der räumliche Bau von Methan? Wie kann dies als zweidimensionale Formel dargestellte werden?
 Wie ist der räumliche Bau von Methan? Wie kann dies als zweidimensionale Formel dargestellte werden? Formeln von Methan Methan hat die ermittelte Summenformel CH 4. Dies ist eine Molekülformel. Die vier
Wie ist der räumliche Bau von Methan? Wie kann dies als zweidimensionale Formel dargestellte werden? Formeln von Methan Methan hat die ermittelte Summenformel CH 4. Dies ist eine Molekülformel. Die vier
Merkmale chemischer Reaktionen
 Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 7 & 8 Merkmale chemischer Reaktionen Kurzprotokoll Auf einen Blick: Im Folgenden werden weitere Versuche zum Thema Merkmale einer
Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 7 & 8 Merkmale chemischer Reaktionen Kurzprotokoll Auf einen Blick: Im Folgenden werden weitere Versuche zum Thema Merkmale einer
Struktur-Eigenschafts-Beziehungen von unverzweigten Alkanen
 Struktur-Eigenschafts-Beziehungen von unverzweigten Alkanen Martin Trockel, Dorsten; Petra Wlotzka, Dortmund Niveau: Dauer: Sek. I/II 3 Unterrichtsstunden Kompetenzen: Die Schülerinnen und Schüler 1 können
Struktur-Eigenschafts-Beziehungen von unverzweigten Alkanen Martin Trockel, Dorsten; Petra Wlotzka, Dortmund Niveau: Dauer: Sek. I/II 3 Unterrichtsstunden Kompetenzen: Die Schülerinnen und Schüler 1 können
Schuleinsatz Calciumfluorid CaF 2 (s) 22-24/ S1 Schwefelsäure, (konz., w = 96 %)
 Reaktionsgleichungen F + (aq ) + H (aq ) HF (g) 4 HF (g) + SiO 2 (s) SiF 4 g + 2 H 2 O (l) Zeitbedarf Vorbereitung: 5min. Durchführung: 5 min. Nachbereitung: 5 min. Chemikalienliste Edukte Chemikalien
Reaktionsgleichungen F + (aq ) + H (aq ) HF (g) 4 HF (g) + SiO 2 (s) SiF 4 g + 2 H 2 O (l) Zeitbedarf Vorbereitung: 5min. Durchführung: 5 min. Nachbereitung: 5 min. Chemikalienliste Edukte Chemikalien
Alles was uns umgibt!
 Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Endersch, Jonas Praktikum Allgemeine Chemie 2, Saal G1, Platz 53
 Endersch, Jonas 03.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 1.1: Einführung in die Laboratoriumstechnik Einleitung Um die in diesem Praktikum verwendeten Glasgeräte
Endersch, Jonas 03.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 1.1: Einführung in die Laboratoriumstechnik Einleitung Um die in diesem Praktikum verwendeten Glasgeräte
Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 2010/11
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in):Beate Abé Name: Johannes Hergt Datum: 16.11.2010 Gruppe 1: Einführung in die organische
Organisch-chemisches Praktikum für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in):Beate Abé Name: Johannes Hergt Datum: 16.11.2010 Gruppe 1: Einführung in die organische
Organisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß. Schulversuch-Protokoll Jan gr.
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von β-aphtholorange
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von β-aphtholorange
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 2: Alkane Versuch: alogenierung von Alkanen
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 2: Alkane Versuch: alogenierung von Alkanen
Schulversuchspraktikum. Julia Müller. Eigenschaften gesättigter Kohlenwasserstoffe
 Schulversuchspraktikum Name: Julia Müller Semester: SoSe 2012 Klassenstufen: 9 und 10 Eigenschaften gesättigter Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum Name: Julia Müller Semester: SoSe 2012 Klassenstufen: 9 und 10 Eigenschaften gesättigter Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Wie verändern sich die Eigenschaften der Alkohole bei Zunahme der Kohlenstoffzahl?
 Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
Gruppe 6 eigener Versuch. Reaktion von Methanol mit Calciumchlorid
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 02.06.09 SS 09 Gruppe 6 eigener Versuch Reaktion von Methanol mit
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 02.06.09 SS 09 Gruppe 6 eigener Versuch Reaktion von Methanol mit
Die Kerzenflamme (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die Kerzenflamme (Artikelnr.: P7154200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Luft und Verbrennungen
Lehrer-/Dozentenblatt Die Kerzenflamme (Artikelnr.: P7154200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Luft und Verbrennungen
Gruppe 03: Pyrolyse von LDPE und Nachreifung von Bananen mit dem PE- Pyrolysegas
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 03: Pyrolyse von LDPE und Nachreifung von Bananen mit dem PE- Pyrolysegas
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 03: Pyrolyse von LDPE und Nachreifung von Bananen mit dem PE- Pyrolysegas
1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat
 1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat Geräte/Chemikalien: Mörser mit Pistill, feuerfeste Unterlage, Zucker, Kaliumnitrat, Zünder: Kaliumpermanganat
1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat Geräte/Chemikalien: Mörser mit Pistill, feuerfeste Unterlage, Zucker, Kaliumnitrat, Zünder: Kaliumpermanganat
Versuch: Blitze unter Wasser
 Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Blitze unter Wasser
Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Blitze unter Wasser
Isomere. 3. Bsp. C5H12
 Fachdidaktik Chemie ET Grundlagenfach: Moleküle S. 7 Isomere Input: 1. Bsp C26 Inszenierung: Schülerinnen zeichnen in einer Aufgabe verschiedene Lewisformeln von C26. Sie gehen durch die Klasse, schauen
Fachdidaktik Chemie ET Grundlagenfach: Moleküle S. 7 Isomere Input: 1. Bsp C26 Inszenierung: Schülerinnen zeichnen in einer Aufgabe verschiedene Lewisformeln von C26. Sie gehen durch die Klasse, schauen
Trennung eines Flüssigkeitsgemisches durch Destillation (Artikelnr.: P )
 Trennung eines Flüssigkeitsgemisches durch Destillation (Artikelnr.: P1132500) Lehrerinformation Einleitung Viele Stoffe liegen in der Natur als Stoffgemisch und nicht als Reinstoff vor. Da viele Stoffe
Trennung eines Flüssigkeitsgemisches durch Destillation (Artikelnr.: P1132500) Lehrerinformation Einleitung Viele Stoffe liegen in der Natur als Stoffgemisch und nicht als Reinstoff vor. Da viele Stoffe
Fossile Rohstoffe. Kohlenwasserstoffe als Energieträger
 nwasserstoffe als Energieträger Erdöl,, Erdgas und Torf sind im Laufe von Millionen von Jahren aus Kleinlebwesen und Pflanzen entstanden und werden deswegen als fossile Energieträger bezeichnet. Da sie
nwasserstoffe als Energieträger Erdöl,, Erdgas und Torf sind im Laufe von Millionen von Jahren aus Kleinlebwesen und Pflanzen entstanden und werden deswegen als fossile Energieträger bezeichnet. Da sie
Alkane als Kraftstoffe
 Alkane als Kraftstoffe Du hast bereits gelernt, dass bei der fraktionierten Destillation Alkane erhalten werden können, die geeignet sind als Kraftstoffe eingesetzt zu werden. Unterschiedliche Motoren
Alkane als Kraftstoffe Du hast bereits gelernt, dass bei der fraktionierten Destillation Alkane erhalten werden können, die geeignet sind als Kraftstoffe eingesetzt zu werden. Unterschiedliche Motoren
Untersuche, ob Wasser gelöste Gase enthält und wovon die Löslichkeit der Gase abhängt.
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754700) 3.3 Löslichkeit von Gasen in Wasser Experiment von: Seb Gedruckt: 24.03.204 :24:34 intertess
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754700) 3.3 Löslichkeit von Gasen in Wasser Experiment von: Seb Gedruckt: 24.03.204 :24:34 intertess
Temperaturabhängigkeit, Schmelzund Siedetemperatur
 Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit, Schmelzund Siedetemperatur Kurzprotokoll Auf einen Blick: Im Folgenden
Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit, Schmelzund Siedetemperatur Kurzprotokoll Auf einen Blick: Im Folgenden
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Kopiervorlagen Organische Chemie. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Kopiervorlagen Organische Chemie Das komplette Material finden Sie hier: Download bei School-Scout.de Inhaltsverzeichnis Organische
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Kopiervorlagen Organische Chemie Das komplette Material finden Sie hier: Download bei School-Scout.de Inhaltsverzeichnis Organische
+ H 2 O. Versuch: Zersetzung von Milchsäure
 Philipps-Universität Marburg 25.12.2007 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 7, Aldehyde und Carbonsäuren Versuch: Zersetzung von Milchsäure
Philipps-Universität Marburg 25.12.2007 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 7, Aldehyde und Carbonsäuren Versuch: Zersetzung von Milchsäure
,Prinzip: Versuchsaufbau - Variante I: Materialliste:
 Computer im Chemieunterricht Gaschromatographische Identifizierung Chromatogr.,Prinzip: Einige Kohlenwasserstoffe werden aus Carbiden im Minigasentwickler hergestellt. Weitere Kohlenwasserstoffe lassen
Computer im Chemieunterricht Gaschromatographische Identifizierung Chromatogr.,Prinzip: Einige Kohlenwasserstoffe werden aus Carbiden im Minigasentwickler hergestellt. Weitere Kohlenwasserstoffe lassen
Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen. Kurzprotokoll. Schulversuchspraktikum.
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Versuch: Hydrolyse von Stärke mit Speichel
 Philipps-Universität Marburg 27.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Hydrolyse von Stärke mit
Philipps-Universität Marburg 27.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Hydrolyse von Stärke mit
Versuchsprotokoll. Luminol Kaltes Feuerwerk
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 28.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Luminol Kaltes Feuerwerk Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 28.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Luminol Kaltes Feuerwerk Gruppe
Gruppe 05: Alkylchloride gegenüber AgNO 3
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Alkylchloride gegenüber AgNO 3 Reaktion: am Beispiel des sekundären
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Alkylchloride gegenüber AgNO 3 Reaktion: am Beispiel des sekundären
Schulversuchspraktikum. Isabelle Faltiska. Sommersemester Klassenstufen 11 & 12. Quantitative Analyse von. Kohlenwasserstoffen
 Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 11 & 12 Quantitative Analyse von Kohlenwasserstoffen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Im Folgenden
Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 11 & 12 Quantitative Analyse von Kohlenwasserstoffen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Im Folgenden
Flüssigkeitsthermometer Bimetallthermometer Gasthermometer Celsius Fahrenheit
 Wärme Ob etwas warm oder kalt ist können wir fühlen. Wenn etwas wärmer ist, so hat es eine höhere Temperatur. Temperaturen können wir im Bereich von etwa 15 Grad Celsius bis etwa 45 Grad Celsius recht
Wärme Ob etwas warm oder kalt ist können wir fühlen. Wenn etwas wärmer ist, so hat es eine höhere Temperatur. Temperaturen können wir im Bereich von etwa 15 Grad Celsius bis etwa 45 Grad Celsius recht
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 17.12.2010 Gruppe 9: Kohlenhydrate Versuch (Nachweis):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 17.12.2010 Gruppe 9: Kohlenhydrate Versuch (Nachweis):
Versuchsprotokoll: Zuckerwürfel in Kaliumchlorat
 Versuchsprotokoll: Zuckerwürfel in Kaliumchlorat Zeitaufwand: Aufbau: 5 Minuten Durchführung: 10 Minuten Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
Versuchsprotokoll: Zuckerwürfel in Kaliumchlorat Zeitaufwand: Aufbau: 5 Minuten Durchführung: 10 Minuten Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
4.1 Vergleich von physikalischem Vorgang und chemischer Reaktion. Aufgabe. Woran lassen sich chemische Reaktionen erkennen? (1)
 Naturwissenschaften - Chemie - Allgemeine Chemie - 4 Chemische Reaktionen (P75200) 4. Vergleich von physikalischem Vorgang und chemischer Reaktion Experiment von: Phywe Gedruckt:.0.203 2:58:37 intertess
Naturwissenschaften - Chemie - Allgemeine Chemie - 4 Chemische Reaktionen (P75200) 4. Vergleich von physikalischem Vorgang und chemischer Reaktion Experiment von: Phywe Gedruckt:.0.203 2:58:37 intertess
Versuch: Elektrophile Addition von Brom an Ethen
 Philipps-Universität Marburg 03.12.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 3, Alkene / Alkine Versuch: Elektrophile Addition von
Philipps-Universität Marburg 03.12.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 3, Alkene / Alkine Versuch: Elektrophile Addition von
Versuchsprotokoll: Fehling- Spaltung von Saccharose
 Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll. Pyrolyse von LDPE Einfache Versuche mit Ethen
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 18.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Pyrolyse von LDPE Einfache Versuche
Anna-Lena Eicke Philipps-Universität Marburg Organisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 18.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Pyrolyse von LDPE Einfache Versuche
Kerzen - Lichter der Gemütlichkeit oder offene Zündquelle
 Brennende Kerzen dienen in der heutigen Zeit kaum noch als eigentliche Lichtquelle, sondern sind ein Symbol von Gemütlich- oder Feierlichkeit. Wenn wir eine Kerze anzünden, geschieht das frei von Furcht
Brennende Kerzen dienen in der heutigen Zeit kaum noch als eigentliche Lichtquelle, sondern sind ein Symbol von Gemütlich- oder Feierlichkeit. Wenn wir eine Kerze anzünden, geschieht das frei von Furcht
Summenformel Elektronenstrichformel Name Siedepunkt
 Die homologe Reihe der Alkene Summenformel Elektronenstrichformel Name Siedepunkt C 2 H 4 Ethen -104 C C 3 H 6 Propen -47 C C 4 H 8 1-Buten -6 C C 5 H 10 (...) 1-Penten 30 C C 6 H 12 (...) 1-Hexen 63 C
Die homologe Reihe der Alkene Summenformel Elektronenstrichformel Name Siedepunkt C 2 H 4 Ethen -104 C C 3 H 6 Propen -47 C C 4 H 8 1-Buten -6 C C 5 H 10 (...) 1-Penten 30 C C 6 H 12 (...) 1-Hexen 63 C
Schulversuch-Protokoll Jan gr. Austing
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: xidation von Milchsäure ) Reaktionsgleichung:
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: xidation von Milchsäure ) Reaktionsgleichung:
 Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Versuchsprotokoll. Nachweis von Tensiden in Kernseife, Spülmittel und Waschmittel
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 5.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Nachweis von Tensiden in
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 5.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Nachweis von Tensiden in
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 5: alogenalkane Versuch: Reaktivität von
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 5: alogenalkane Versuch: Reaktivität von
Versuch: Maillardreaktion
 Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Maillardreaktion
Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Maillardreaktion
Fraktionierte Destillation eines Gemisches
 Fraktionierte Destillation eines Gemisches Die Destillation ist eine physikalische Trennmethode, bei welcher die unterschiedlichen Siedepunkte der Bestandteile (Komponenten) eines Gemisches zur Trennung
Fraktionierte Destillation eines Gemisches Die Destillation ist eine physikalische Trennmethode, bei welcher die unterschiedlichen Siedepunkte der Bestandteile (Komponenten) eines Gemisches zur Trennung
Destillation von Rotwein
 Destillation von Rotwein Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Zerlegung der Verbindung Wasser Titration Herstellung von Natronlauge Öltröpfchen versuch
Destillation von Rotwein Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Zerlegung der Verbindung Wasser Titration Herstellung von Natronlauge Öltröpfchen versuch
Versuchsprotokoll: Ampel-Bottle - Experiment
 Versuchsprotokoll: Ampel-Bottle - Experiment Zeitaufwand: Aufbau: 5 Minuten Durchführung: 1 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
Versuchsprotokoll: Ampel-Bottle - Experiment Zeitaufwand: Aufbau: 5 Minuten Durchführung: 1 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
Versuchsprotokoll. Nachweis von Stickstoff in Eiweißen. Gruppe 1, Typ: Eigenversuch. Na + O -
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. eiß WS 08/09 13.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Nachweis von Stickstoff in Eiweißen
Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. eiß WS 08/09 13.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Nachweis von Stickstoff in Eiweißen
Destillation und Alkohol
 Destillation und Alkohol Destillation Veronikas Vater hat die Genehmigung Schnaps zu brennen. Dazu braucht er eine Destillationsanlage: Abb. 1: Destillationsanlage Bei der Destillation wird eine Flüssigkeit
Destillation und Alkohol Destillation Veronikas Vater hat die Genehmigung Schnaps zu brennen. Dazu braucht er eine Destillationsanlage: Abb. 1: Destillationsanlage Bei der Destillation wird eine Flüssigkeit
Aggregatzustände und deren Temperaturabhängigkeit
 Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
