Tierversuche Medikamentenentwicklung
|
|
|
- Hajo Küchler
- vor 5 Jahren
- Abrufe
Transkript
1 Tierversuche Medikamentenentwicklung Methodisch-didaktischer Kommentar Die Frage Sollen wir denn etwa am Menschen testen? kommt in der Diskussion über Tierversuche nur allzu oft auf. Die Tatsache, dass gerade Tierversuche durch ihre mangelnde Validität und Übertragbarkeit jedoch ein erhöhtes Risiko für den Menschen darstellen, wird allerdings außer Acht gelassen. Denn die wenigsten Menschen sind sich über den Prozess der Medikamentenentwicklung, in deren Rahmen Versuche an Testpersonen gesetzlich vorgeschrieben sind, bewusst. Es handelt sich also keineswegs um eine philosophische Fragestellung, vielmehr ist eine Betrachtung der Sinnhaftigkeit von Tierversuchen im Ganzen notwendig. In diesem Arbeitsmaterial wird der Ablauf der Entwicklung eines Medikaments veranschaulicht. Es wird deutlich, dass in der Medikamentenentwicklung Menschenversuche Gang und Gäbe und durch vorherige Testungen an Tieren besonders gefährlich sind. Auf Basis der Kenntnis des Prozesses der Medikamentenentwicklung sind die Schülerinnen und Schüler dazu angehalten, sich tiefer mit der Frage Sollen wir etwa am Menschen testen? auseinanderzusetzen. Weiterhin bietet sich eine anschließende Erarbeitung der der Thematik von Risikomedikamenten an, welche mithilfe einer Textarbeit des angehängten Vertiefungsmaterials erfolgen kann. Ebenfalls kann das Arbeitsmaterial zu Risiken und Misserfolgen von Tierversuchen angeschlossen werden. Online abrufbar ist eine Übersicht über bekannte Risikomedikamente, in welcher sich Antworten auf die Fragen in den Arbeitsaufträgen finden. Die Liste ist keineswegs vollständig, gibt aber Aufschluss darüber, dass Tierversuche keine definitiven Aussagen über die Medikamentensicherheit beim Menschen erlauben. Hinweis: Die Tabelle zeigt eine knappe Darstellung eines komplexen Sachverhaltes. Alle aufgeführten Wirkstoffe sind kritisch zu beurteilen, jedoch bedeutet die Nennung eines Stoffes in dieser Liste nicht unbedingt, dass von der Verabreichung abzuraten ist. Bei den noch auf dem Markt befindlichen Medikamenten mag in Einzelfällen eine Verwendung indiziert sein. Ziel dieser Übersicht ist es lediglich, aufzuzeigen, dass Tierversuche nicht vor den genannten unerwünschten Wirkungen schützen konnten. 1
2 Tierversuche Medikamentenentwicklung Ablauf klinischer Studien Ja sollen wir denn dann etwa am Menschen testen?! - dies hört man häufig als Rechtfertigung von Tierversuchen. Die Frage, ob statt an Tieren an Menschen getestet werden soll, ist allerdings hinfällig, denn kein Medikament kommt auf den Markt, ohne zuvor in klinischen Studien (also in Studien an Versuchspersonen) welche auf den Tierversuch folgen, getestet worden zu sein. Diese schematische Darstellung veranschaulicht den Prozess der Medikamentenentwicklung. Abbildung 1: Prozess der Medikamentenentwicklung Die Entwicklung eines neuen Medikaments, die über 1 Mrd. kostet, verläuft über zahlreiche Stationen. Bis zur ersten Zulassung dauert es durchschnittlich 13 Jahre und weitere Jahre 2
3 vergehen bis es allen Altersgruppen zur Verfügung steht. Von ursprünglich Wirkstoffen schafft es letztendlich einer in die Apotheke. In der Anfangsphase werden Computermodelle und Simulationsprogramme eingesetzt. Allerdings wird bereits in dieser Phase häufig unter falschen Bedingungen und Annahmen geforscht, da die Ideen aus der Grundlagenforschung an Tieren stammen (vgl. hierzu Arbeitsmaterial zur Übertragbarkeit). Innerhalb der nächsten 2 Jahre setzen sich ca. 250 interessante, d.h. potenziell wirksame und nutzbare, Substanzen durch. Nun beginnen die Tierversuche. Hier bleiben etwa 5 Substanzen, die im Tierexperiment positive Resultate erbrachten haben, übrig, d.h. sie erwiesen sich im Tierversuch als wirksam gegen bestimmte künstlich beigebrachte Symptome und waren nicht schädlich. Aussagen über die Wirksamkeit am Menschen können noch nicht getroffen werden. In der Phase der sog. präklinischen Testung werden die meisten Tierversuche durchgeführt. Zunächst wird an Bakterien, Zell- und Gewebekulturen und isolierten Organen getestet, zuletzt am Gesamtorganismus Tier (mindestens 2-3 Tierarten) vor der ersten Anwendung am Menschen. Tierversuche verhindern die Probandenstudien nicht, sondern erfordern diese zwangsläufig. Die Klinische Phase I bis III ist durch den Gesetzgeber vorgeschrieben. Phase I: Erprobung an wenigen gesunden Probanden, ca , meist männlich Phase II: Test an ca Erkrankten Phase III: Testung an größerer Patientenanzahl ( ), weiterhin Überprüfung von Sicherheit und Wirksamkeit des Präparates Ein Medikament kommt nur ins Zulassungsverfahren, wenn es alle drei klinischen Phasen ohne Probleme durchlaufen hat. In der Phase IV erfolgen weitere Studien nach der Zulassung. Aufgrund schwerwiegender Nebenwirkungen oder Wirkungslosigkeit während der klinischen Phase erhalten 95 % der potentiellen Arzneimittel, die im Tierversuch als sicher und wirksam galten, keine Marktzulassung. Das bedeutet, nur 5 % der im Tierversuch erfolgreichen Medikamente überstehen die klinische Phase. Seit 2013 werden in allen EU-Mitgliedsstaaten neu zugelassene Medikamente und jene mit unzureichenden Daten zur Langzeitanwendung mit einem schwarzen Dreieck in der 3
4 Packungsbeilage als Arzneimittel unter zusätzlicher Überwachung gekennzeichnet. Die Patienten werden aufgefordert, eventuelle Nebenwirkungen zu melden. Auch dies ist ein großangelegter Menschenversuch, bei dem mögliche Nebenwirkungen erst noch herausgefunden werden sollen. Arbeitsaufträge: 1. Wieso ist davon auszugehen, dass die Entwicklung von Medikamenten wie sie gesetzlich vorgeschrieben ist, nicht effektiv ist? Belege am Text. 2. Welche Erklärung könnte es dafür geben, dass die Testpersonen in der Klinischen Phase I überwiegend männlich sind? Beziehe auch deine Überlegungen aus Aufgabe 2 mit ein. 3. Was ist ein Arzneimittel unter zusätzlicher Überwachung? Welche Rückschlüsse lassen sich daraus für die Validität von Tierversuchen in der Medikamentenentwicklung ziehen? 4. Die Frage Sollen wir denn etwa am Menschen testen? zeigt, dass Bürger besorgt um die Gesundheit ihrer Mitmenschen sind. a) Was kannst du nun auf diese Frage antworten? Wende dein Wissen aus den Aufgaben 1-3 an. b) Überlege nun, wie der gesamte Prozess der Medikamentenentwicklung so optimiert werden könnte, dass er für Menschen weniger risikoreich ist. 4
5 Vertiefendes Material Medikamentensicherheit und Tierversuche Alle Medikamente werden vor der Zulassung bzw. Anwendung am kranken Menschen in der so genannten präklinischen Phase exzessiv an Tieren geprüft. Damit soll die Sicherheit eines neuen Medikamentes gewährleistet werden. So sehen es die entsprechenden Vorschriften und Gesetze seit vielen Jahrzehnten vor. Konkret bedeutet dies, dass unzählige Tiere (meist Ratten und Mäuse, aber auch Hunde und weitere Tierarten) in qualvollen Versuchen die neue Substanz per Schlundsonde oder Injektion verabreicht bekommen und unter Umständen mehr oder weniger schnell vergiftet werden. Am Ende der Versuche, die Tage, Wochen, aber auch viele Monate dauern können, werden die Tiere getötet und ihre Organe seziert. Diese Experimente sollen dazu dienen, die Risiken eines neuen Medikaments bezüglich der Anwendung beim Menschen abzuschätzen. Doch diese qualvollen Versuche, die vor der Vermarktung einer Substanz durchgeführt werden, machen Arzneimittel nicht sicher. Es gibt eine lange Reihe von Medikamenten, welche von den zuständigen Behörden für den Verkauf in der Apotheke zugelassen wurden und dann auf Grund von Problemen, welche tierexperimentell nicht vorausgesehen wurden, wieder aus dem Verkehr gezogen oder zumindest im Gebrauch erheblich eingeschränkt werden mussten. So sind einer vom Institut für Klinische Pharmakologie, Bremen, veröffentlichten Studie zufolge jährlich Krankenhauseinweisungen auf Arzneimittelnebenwirkungen zurückzuführen. Davon sind lebensbedrohlich, verlaufen tödlich. Eine Studie der Medizinischen Hochschule Hannover geht sogar von tödlichen unerwünschten Arzneimittelwirkungen pro Jahr in Deutschland aus. Das Problem besteht immer wieder in der fraglichen Übertragbarkeit von tierexperimentellen Ergebnissen auf den kranken Menschen. Eine Substanz, welche bei der Maus keine Schäden hervorruft, kann bei der Ratte zum Tode führen. Eine andere Substanz, welche für die Maus tödlich ist, kann von der Ratte ohne Probleme vertragen werden. Die Giftigkeit kann sogar innerhalb einer Tierart, je nach Stamm und genetischen Eigenschaften variieren. Also werden für die Sicherheitsabschätzung mehrere unterschiedliche Tierarten und Tierstämme verwendet. Jedoch kann niemand vorhersagen, ob eine neue Substanz, die bei Maus, Ratte, Hund und Affen keine Schäden hervorruft, sicher für den Menschen ist. Auf zwei besonders bekannte Beispiele soll hier kurz hingewiesen werden. Thalidomid (Contergan ), das bei Föten (Embryonen) von Frauen, welche in der Schwangerschaft das damals als sicher angepriesene Schlafmittel eingenommen hatten, schwerste Missbildungen 5
6 hervorrief. Mit Thalidomid waren tatsächlich vor der Zulassung Tierversuche durchgeführt worden. Allerdings mit den falschen Tieren, nämlich mit Mäusen und Ratten, bei denen bei üblicher Dosierung keine so genannten teratogenen (d.h. missbildenden) Schäden auftreten. In der Folge wurden weitere Tierversuche gemacht, bis einige Tierarten gefunden wurden, bei denen ähnliche teratogene Schäden wie beim Menschen auftreten: dem Neuseeland- Kaninchen und eine bestimmte Affenart. Diese Tierarten zeigen zwar die missbildenden Eigenschaften des Thalidomids im Nachhinein, aber nicht die anderer teratogener Substanzen. Zum Glück gibt es nur wenige wirklich teratogene Substanzen in der Pharmakologie. Der Tierversuch könnte uns letztlich nicht vor einer neuen Katastrophe dieser Art schützen. Entsprechend dürfen nach heutigem Standard neue Medikamente prinzipiell in der Schwangerschaft nicht eingesetzt werden. Das hat man aus der Contergankatastrophe für die Zukunft gelernt. Aber nicht aus dem Tierversuch! Es bleibt nicht bei diesem einen Beispiel. Das zweite Beispiel ist der Blutfettsenker Cerivastatin (Lipobay ), der zu Muskelzerfall und zum Tode führen kann. Hunderte von Fällen sind klinisch dokumentiert. Auch bei diesem Medikament wurden vorher exzessiv Tierversuche mit verschiedensten Tierarten gemacht. Die Schwierigkeit besteht darin, dass es bei der Anwendung am Menschen Nebenwirkungen gibt, die tödlich sein können, aber nur relativ selten auftreten. Ein Problem, das bei einer Substanz mit einem tödlichen Risiko von 1: behaftet ist, wird bei der Anwendung an einer Gruppe von Kranken unter Umständen gar nicht auffallen. Wird das Medikament aber bei einer Million Menschen eingesetzt, gibt es unter Umständen 100 Todesfälle und die Katastrophe ist da. Dieses Problem ist mit keinem Tierversuch vorauszusehen oder zu verhindern! Warum setzt man dann neue Medikamente nicht zuerst bei kleineren Gruppen von Kranken über viele Jahre ein, um Erfahrungen zu gewinnen? Weil die Pharmaindustrie für die Entwicklung einer neuen Substanz ca. eine Milliarde Euro investiert und das Patent nur eine begrenzte Zeit geschützt ist, bevor Nachahmer-Firmen die Substanz billig selbst produzieren können. Das Dilemma ist also: Aus kommerziellen Gründen muss ein neues Medikament in kurzer Zeit bei einer möglichst großen Zahl von Menschen eingesetzt werden, sonst sind die hohen Investitionen verloren. Vor diesem Problem schützt kein noch so ausgefeilter Tierversuch. Aber es existieren noch zahlreiche weitere Beispiele für Medikamente, die wegen unvorhersehbarer schwerer Nebenwirkungen vom Markt genommen werden mussten, in ihrer Anwendung eingeschränkt wurden oder erhebliche Kritik erfahren haben. Keines der genannten Probleme konnte aufgrund von tierexperimentellen Studien vorausgesehen werden. Alle aufgeführten schwerwiegenden Nebenwirkungen bis hin zu Todesfällen traten erst bei der Anwendung am Menschen auf. 6
7 (Gekürzt und bearbeitet nach: Abbildung 2: Übersicht über einige Medikamentenskandale, Quelle: Arbeitsaufträge 1. Recherchiere weitere aktuelle Arzneimittelskandale im Internet. Berücksichtige hierbei nicht nur bereits im Handel erhältliche Medikamente, sondern auch jene, welche sich noch in der klinischen Testung befanden. 2. Wie viele sogenannte Risikomedikamente gibt es? Recherchiere einen Richtwert. a) Lässt sich eine eindeutige Aussage über die Anzahl der Risikomedikamente geben? b) Setze diese Zahl in Relation zu der Gesamtzahl der auf dem Markt erhältlichen Medikamente und beurteile, ob der Anteil hoch oder niedrig ist. c) Beziehe die Tatsache, dass jedes Risikomedikament für den Anwender schlimmstenfalls Todesfolge haben kann, mit in deine Überlegungen ein. Hinweis: Nutze für deine Recherchen z.b. die Homepage von Ärzte gegen Tierversuche oder Tierschutz in der Schule 7
Ein Wirkstoff ist ein Stoff der Krankheiten heilen oder lindern kann. Er kann natürlicher oder künstlicher Herkunft sein.
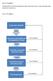 Buch S. 83 Aufgabe 1 Ein Wirkstoff ist ein Stoff der Krankheiten heilen oder lindern kann. Er kann natürlicher oder künstlicher Herkunft sein. Buch S. 83 Aufgabe 2 Suche nach Wirkstoff Testen der Wirksamkeit
Buch S. 83 Aufgabe 1 Ein Wirkstoff ist ein Stoff der Krankheiten heilen oder lindern kann. Er kann natürlicher oder künstlicher Herkunft sein. Buch S. 83 Aufgabe 2 Suche nach Wirkstoff Testen der Wirksamkeit
UNSERE VERANTWORTUNG FÜR DIE PATIENTENSICHERHEIT
 UNSERE VERANTWORTUNG FÜR DIE PATIENTENSICHERHEIT Im Gleichgewicht bleiben Ein gesunder Körper ist im Gleichgewicht. Wenn wir krank sind, bemüht sich der Körper, diese Balance wiederherzustellen. Doch manchmal
UNSERE VERANTWORTUNG FÜR DIE PATIENTENSICHERHEIT Im Gleichgewicht bleiben Ein gesunder Körper ist im Gleichgewicht. Wenn wir krank sind, bemüht sich der Körper, diese Balance wiederherzustellen. Doch manchmal
WAS SIE BEKOMMEN? Gefälschte Medikamente können töten. Gehen Sie auf Nummer sicher. Nutzen Sie das Logo.
 MedikamentE im INternet KAUFEN? WISSEN SIE wirklich, WAS SIE BEKOMMEN? Gefälschte Medikamente können töten. Gehen Sie auf Nummer sicher. Nutzen Sie das Logo. Erkennen Sie die Gefahr Illegale Arzneimittel,
MedikamentE im INternet KAUFEN? WISSEN SIE wirklich, WAS SIE BEKOMMEN? Gefälschte Medikamente können töten. Gehen Sie auf Nummer sicher. Nutzen Sie das Logo. Erkennen Sie die Gefahr Illegale Arzneimittel,
Informationsbroschüre für Patienten
 Haben Sie Gedächtnisprobleme? Schwierigkeiten, klar zu denken? Wenn das auf Sie oder auf jemanden in Ihrem Bekanntenkreis zutrifft, dann ziehen Sie bitte eine Teilnahme an der EMERGE- Studie in Betracht
Haben Sie Gedächtnisprobleme? Schwierigkeiten, klar zu denken? Wenn das auf Sie oder auf jemanden in Ihrem Bekanntenkreis zutrifft, dann ziehen Sie bitte eine Teilnahme an der EMERGE- Studie in Betracht
Tierversuche. Medizinische Notwendigkeit oder grausames Relikt? Dr. med. vet.. Corina Gericke Ärzte gegen Tierversuche e.v.
 Tierversuche Medizinische Notwendigkeit oder grausames Relikt? Dr. med. vet.. Corina Gericke 2,5 Mio. Tiere 2006 Ausbildung 1,7 % Toxikologie 6,4 % Qualitätskontrolle 13,8 % Arzneimittelforschung 19,3
Tierversuche Medizinische Notwendigkeit oder grausames Relikt? Dr. med. vet.. Corina Gericke 2,5 Mio. Tiere 2006 Ausbildung 1,7 % Toxikologie 6,4 % Qualitätskontrolle 13,8 % Arzneimittelforschung 19,3
Ein langer Weg: Von der Idee zum Medikament
 Ein langer Weg: Von der Idee zum Medikament 7 Die Entwicklung von Medikamenten ist ein langwieriger und aufwendiger Prozess, der mit enormen Kosten für den Hersteller verbunden ist. Nur ein funktionierender
Ein langer Weg: Von der Idee zum Medikament 7 Die Entwicklung von Medikamenten ist ein langwieriger und aufwendiger Prozess, der mit enormen Kosten für den Hersteller verbunden ist. Nur ein funktionierender
Antrag auf Entlassung aus der Verschreibungspflicht. -Diclazuril-
 Antrag auf Entlassung aus der Verschreibungspflicht Antrag der Firma: Erweiterung des Eintrags in der AMVV von derzeit Diclazuril in Diclazuril ausgenommen zur Anwendung bei Bartagame und Leopardgecko
Antrag auf Entlassung aus der Verschreibungspflicht Antrag der Firma: Erweiterung des Eintrags in der AMVV von derzeit Diclazuril in Diclazuril ausgenommen zur Anwendung bei Bartagame und Leopardgecko
Von der Idee zum Medikament Arbeitsblatt
 Lehrerinformation 1/7 Arbeitsauftrag Ziel Material Illegal hergestellte Medikamente entsprechen nicht den geforderten Qualitätskriterien. Die Unternehmen, welche legal Medikamente entwickeln und produzieren,
Lehrerinformation 1/7 Arbeitsauftrag Ziel Material Illegal hergestellte Medikamente entsprechen nicht den geforderten Qualitätskriterien. Die Unternehmen, welche legal Medikamente entwickeln und produzieren,
Anhang III. Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage
 Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
Diagnose MS. Leitfaden zur Therapieauswahl
 Diagnose MS Leitfaden zur Therapieauswahl Vorbereitung ist alles Vor einer Entscheidung für eine Behandlung stehen viele Fragen. Zum einzelnen Wirkstoff. Zum Behandlungsplan. Zur Krankheit generell. Alles
Diagnose MS Leitfaden zur Therapieauswahl Vorbereitung ist alles Vor einer Entscheidung für eine Behandlung stehen viele Fragen. Zum einzelnen Wirkstoff. Zum Behandlungsplan. Zur Krankheit generell. Alles
Auswertung der STS-Botox-Umfrage an Anwender
 Auswertung der STS-Botox-Umfrage an Anwender im April/Mai 2012 Der Schweizer Tierschutz STS hat im April 2012, nachdem die Swissmedic das alternative Testverfahren der Firma Allergan zugelassen hat, 560
Auswertung der STS-Botox-Umfrage an Anwender im April/Mai 2012 Der Schweizer Tierschutz STS hat im April 2012, nachdem die Swissmedic das alternative Testverfahren der Firma Allergan zugelassen hat, 560
Zulassung von Arzneimitteln. Klinische Untersuchungen. Katalin Müllner
 Zulassung von Arzneimitteln. Klinische Untersuchungen Katalin Müllner Arzneimittel In gesetzlicher Definition sind Arzneimittel Stoffe oder Zubereitungen aus Stoffen, die vom Hersteller, der sie in den
Zulassung von Arzneimitteln. Klinische Untersuchungen Katalin Müllner Arzneimittel In gesetzlicher Definition sind Arzneimittel Stoffe oder Zubereitungen aus Stoffen, die vom Hersteller, der sie in den
STUDIEN PRO UND CONTRA
 V) WEITERE THEMEN STUDIEN PRO UND CONTRA Die Erfahrung hat gezeigt, dass Behandlungsergebnisse an mehr oder weniger kleinen Patientenzahlen von Autor zu Autor auch bei Einsatz gleicher Zytostatika zu unterschiedlichen,
V) WEITERE THEMEN STUDIEN PRO UND CONTRA Die Erfahrung hat gezeigt, dass Behandlungsergebnisse an mehr oder weniger kleinen Patientenzahlen von Autor zu Autor auch bei Einsatz gleicher Zytostatika zu unterschiedlichen,
RoACTEMRA (Tocilizumab) Patientenpass
 RoACTEMRA (Tocilizumab) Patientenpass Dieser Patientenpass ist eine Auflage im Rahmen der Zulassung von RoACTEMRA und enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/gesetzliche
RoACTEMRA (Tocilizumab) Patientenpass Dieser Patientenpass ist eine Auflage im Rahmen der Zulassung von RoACTEMRA und enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/gesetzliche
Tierversuche Fakten und Zahlen
 Tierversuche Fakten und Zahlen Methodisch-didaktischer Kommentar: Der verwendete Text bietet sich als eine Diskussionsgrundlage an, mit welcher in die Thematik der Tierversuche eingeführt werden kann.
Tierversuche Fakten und Zahlen Methodisch-didaktischer Kommentar: Der verwendete Text bietet sich als eine Diskussionsgrundlage an, mit welcher in die Thematik der Tierversuche eingeführt werden kann.
Tierversuche für Botox
 Tierversuche für Botox Methodisch-didaktischer Kommentar Botox, ein Handelsname für Botulinumtoxin-Präparate, ist als Mittel zur Faltenglättung weltweit in Mode. Doch dass mit jeder Botox-Spitze grausame
Tierversuche für Botox Methodisch-didaktischer Kommentar Botox, ein Handelsname für Botulinumtoxin-Präparate, ist als Mittel zur Faltenglättung weltweit in Mode. Doch dass mit jeder Botox-Spitze grausame
Pharmakologische Grundlagen
 Pharmakologische Grundlagen Die Pharmakologie ist die Wissenschaft von den Wechselwirkungen zwischen Stoffen und Lebewesen (Zitat: Wikipedia) Wertung der Stoffe: Arzneistoffe (Pharmakologie) Giftstoffe
Pharmakologische Grundlagen Die Pharmakologie ist die Wissenschaft von den Wechselwirkungen zwischen Stoffen und Lebewesen (Zitat: Wikipedia) Wertung der Stoffe: Arzneistoffe (Pharmakologie) Giftstoffe
Antrag auf Entlassung aus der Verschreibungspflicht. -Doramectin-
 Antrag auf Entlassung aus der Verschreibungspflicht Antrag auf Entlassung von Doramectin aus der Verschreibungspflicht für die topische Anwendung bei Königspython, Abgottschlange und Bartagame bei einem
Antrag auf Entlassung aus der Verschreibungspflicht Antrag auf Entlassung von Doramectin aus der Verschreibungspflicht für die topische Anwendung bei Königspython, Abgottschlange und Bartagame bei einem
Wie wird die Entwicklung eines Medikaments dokumentiert?
 Wie wird die Entwicklung eines Medikaments dokumentiert? TAUSEND FRAGEN EINE STADT Prof. Dr. Wolfgang Schulz 1 Ein kleines Quiz zu Anfang Wie viele Krankheiten kennen wir heute? 1 1.000 2 5.000 3 10.000
Wie wird die Entwicklung eines Medikaments dokumentiert? TAUSEND FRAGEN EINE STADT Prof. Dr. Wolfgang Schulz 1 Ein kleines Quiz zu Anfang Wie viele Krankheiten kennen wir heute? 1 1.000 2 5.000 3 10.000
KLINISCHE PRÜFUNG EINE EINFÜHRUNG. ATA Conference 2003 - Elke Vogt-Arendt
 KLINISCHE PRÜFUNG EINE EINFÜHRUNG ATA Conference 2003 - Elke Vogt-Arendt Was ist eine klinische Prüfung? Überprüfung von Wirkung, Nebenwirkung, Dosierung usw. eines neuen Arzneimittels vor Markteinführung.
KLINISCHE PRÜFUNG EINE EINFÜHRUNG ATA Conference 2003 - Elke Vogt-Arendt Was ist eine klinische Prüfung? Überprüfung von Wirkung, Nebenwirkung, Dosierung usw. eines neuen Arzneimittels vor Markteinführung.
Erivedge Schwangerschaftsverhütungs-Programm:
 Erivedge Schwangerschaftsverhütungs-Programm: Wichtige Informationen zu Empfängnisverhütung und Verhütungsmethoden für männliche und weibliche Patienten, die Erivedge einnehmen. Erivedge kann schwere Geburtsfehler
Erivedge Schwangerschaftsverhütungs-Programm: Wichtige Informationen zu Empfängnisverhütung und Verhütungsmethoden für männliche und weibliche Patienten, die Erivedge einnehmen. Erivedge kann schwere Geburtsfehler
Anhang III. Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des
Anhang III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des
Ausbildungsinhalte zum Sonderfach Pharmakologie und Toxikologie. Sonderfach Grundausbildung (36 Monate)
 Ausbildungsinhalte zum Sonderfach Pharmakologie und Toxikologie Anlage 24 Sonderfach Grundausbildung (36 Monate) 1. Standardisierungsmethoden und biologische Tests 2. Biometrische Methoden 3. Medikamente,
Ausbildungsinhalte zum Sonderfach Pharmakologie und Toxikologie Anlage 24 Sonderfach Grundausbildung (36 Monate) 1. Standardisierungsmethoden und biologische Tests 2. Biometrische Methoden 3. Medikamente,
Was Sie über MabThera wissen sollten
 Die Gesundheitsbehörden der Europäischen Union haben die Markteinführung des Medikaments MabThera an bestimmte Bedingungen gebunden. Der vorgeschriebene Plan zur Risikominimierung in Belgien und im Großherzogtum
Die Gesundheitsbehörden der Europäischen Union haben die Markteinführung des Medikaments MabThera an bestimmte Bedingungen gebunden. Der vorgeschriebene Plan zur Risikominimierung in Belgien und im Großherzogtum
Anhang III. Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale
Anhang III Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale
AMGEVITA (Adalimumab)
 AMGEVITA (Adalimumab) Patientenpass für Ihr Kind behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an der medizinischen Versorgung
AMGEVITA (Adalimumab) Patientenpass für Ihr Kind behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an der medizinischen Versorgung
AMGEVITA (Adalimumab)
 AMGEVITA (Adalimumab) Patientenpass behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an Ihrer medizinischen Versorgung beteiligt sind,
AMGEVITA (Adalimumab) Patientenpass behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an Ihrer medizinischen Versorgung beteiligt sind,
Ausbildungsinhalte zum Sonderfach Pharmakologie und Toxikologie. Sonderfach Grundausbildung (36 Monate)
 Ausbildungsinhalte zum Sonderfach Pharmakologie und Toxikologie Anlage 24 Sonderfach Grundausbildung (36 Monate) A) Kenntnisse absolviert 1. Standardisierungsmethoden und biologische Tests 2. Biometrische
Ausbildungsinhalte zum Sonderfach Pharmakologie und Toxikologie Anlage 24 Sonderfach Grundausbildung (36 Monate) A) Kenntnisse absolviert 1. Standardisierungsmethoden und biologische Tests 2. Biometrische
Die Rolle des Tierversuchs als Erkenntnismethode in der Humanmedizin
 Tierethik Vorlesungsreihe Universität Heidelberg / IAT / 20. Mai 2014 Die Rolle des Tierversuchs als Erkenntnismethode in der Humanmedizin - Aspekte grausamer Forschung - Dr. Rolf Simon M.A. 20. Mai 2014
Tierethik Vorlesungsreihe Universität Heidelberg / IAT / 20. Mai 2014 Die Rolle des Tierversuchs als Erkenntnismethode in der Humanmedizin - Aspekte grausamer Forschung - Dr. Rolf Simon M.A. 20. Mai 2014
Risikoüberwachung von Arzneimitteln - Aktuelle Situation
 Risikoüberwachung von Arzneimitteln - Aktuelle Situation U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte Abteilung Pharmakovigilanz Fortbildung für den Öffentlichen Dienst Berlin, 2. April
Risikoüberwachung von Arzneimitteln - Aktuelle Situation U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte Abteilung Pharmakovigilanz Fortbildung für den Öffentlichen Dienst Berlin, 2. April
Tierversuche Rechtliche Grundlagen
 Tierversuche Rechtliche Grundlagen Methodisch-didaktischer Kommentar Das vorliegende Unterrichtsmaterial zu den rechtlichen Grundlagen von Tierversuchen dient der vertiefenden Erarbeitung des breiten Themenfeldes
Tierversuche Rechtliche Grundlagen Methodisch-didaktischer Kommentar Das vorliegende Unterrichtsmaterial zu den rechtlichen Grundlagen von Tierversuchen dient der vertiefenden Erarbeitung des breiten Themenfeldes
Was sind klinische Prüfungen Eine Einführung. Dr. Thorsten Ruppert Senior Referent Grundsatzfragen Forschung/Entwicklung/Innovation, vfa
 Was sind klinische Prüfungen Eine Einführung Dr. Thorsten Ruppert Senior Referent Grundsatzfragen Forschung/Entwicklung/Innovation, vfa Berlin, 28. Januar 2016 Klinische Studie vs. Klinische Prüfung Wie
Was sind klinische Prüfungen Eine Einführung Dr. Thorsten Ruppert Senior Referent Grundsatzfragen Forschung/Entwicklung/Innovation, vfa Berlin, 28. Januar 2016 Klinische Studie vs. Klinische Prüfung Wie
ANHANG III. Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 ANHANG III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Die zuständigen Behörden der Mitgliedstaaten müssen die Zusammenfassung der
ANHANG III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Die zuständigen Behörden der Mitgliedstaaten müssen die Zusammenfassung der
Wie ein neues Medikament entsteht
 Wie ein neues Medikament entsteht Bis ein neues Medikament entwickelt ist und auf den Markt kommt, braucht es eine zündende Idee der Forscher und viel Ausdauer. Zehn und mehr Jahre vergehen bis das Medikament
Wie ein neues Medikament entsteht Bis ein neues Medikament entwickelt ist und auf den Markt kommt, braucht es eine zündende Idee der Forscher und viel Ausdauer. Zehn und mehr Jahre vergehen bis das Medikament
MYCOPHENOLAT-MOFETIL (MMF)-/ MYCOPHENOLSÄURE (MPA)-HALTIGE ARZNEIMITTEL LEITFADEN FÜR PATIENTEN. Information über die Risiken für das ungeborene Baby
 MYCOPHENOLAT-MOFETIL (MMF)-/ MYCOPHENOLSÄURE (MPA)-HALTIGE ARZNEIMITTEL LEITFADEN FÜR PATIENTEN Information über die Risiken für das ungeborene Baby Dieser Leitfaden zur Anwendung von Mycophenolat-haltigen
MYCOPHENOLAT-MOFETIL (MMF)-/ MYCOPHENOLSÄURE (MPA)-HALTIGE ARZNEIMITTEL LEITFADEN FÜR PATIENTEN Information über die Risiken für das ungeborene Baby Dieser Leitfaden zur Anwendung von Mycophenolat-haltigen
Was ist ein Arzneimittel? Lehrerinformation
 Lehrerinformation 1/8 Arbeitsauftrag Ziel Material Sozialform Sch lesen Text, notieren eine Definition mit eigenen Worten LP fragt die Definition ab Sch beantworten die Fragen des Kurztests Sch erstellen
Lehrerinformation 1/8 Arbeitsauftrag Ziel Material Sozialform Sch lesen Text, notieren eine Definition mit eigenen Worten LP fragt die Definition ab Sch beantworten die Fragen des Kurztests Sch erstellen
Einleitung und Leseanweisung
 VII Einleitung und Leseanweisung Für wen ist dieses Buch? Der Pocket Guide ist für alle klinisch tätigen Psychiater geschrieben, denen das Kompendium der Psychiatrischen Pharmakotherapie für die Kitteltasche
VII Einleitung und Leseanweisung Für wen ist dieses Buch? Der Pocket Guide ist für alle klinisch tätigen Psychiater geschrieben, denen das Kompendium der Psychiatrischen Pharmakotherapie für die Kitteltasche
Sachstand zu den Antihistaminika Dimenhydrinat, Diphenhydramin und Doxylamin
 Sachstand zu den Antihistaminika Dimenhydrinat, Diphenhydramin und Doxylamin Sachverständigen-Ausschuss für Verschreibungspflicht 3. Juli 2018 Sachverständigen-Ausschuss für Verschreibungspflicht 3. Juli
Sachstand zu den Antihistaminika Dimenhydrinat, Diphenhydramin und Doxylamin Sachverständigen-Ausschuss für Verschreibungspflicht 3. Juli 2018 Sachverständigen-Ausschuss für Verschreibungspflicht 3. Juli
Pharmakologie 1 Allgemeine Prinzipien Spezielle Arzneistoffgruppen 78
 Pharmakologie 1 Allgemeine Prinzipien 20 2 Spezielle Arzneistoffgruppen 78 I Allgemeine Prinzipien 1 Allgemeine Prinzipien 1.1 Arzneimittelherkunft Am Anfang der Entwicklung steht die Synthese neuer chemischer
Pharmakologie 1 Allgemeine Prinzipien 20 2 Spezielle Arzneistoffgruppen 78 I Allgemeine Prinzipien 1 Allgemeine Prinzipien 1.1 Arzneimittelherkunft Am Anfang der Entwicklung steht die Synthese neuer chemischer
'Y Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
 'Y Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie können dabei helfen, indem Sie jede auftretende
'Y Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie können dabei helfen, indem Sie jede auftretende
Parenteralia. Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017
 Parenteralia Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Hintergrund Diskussion auf der 76. Sitzung
Parenteralia Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Hintergrund Diskussion auf der 76. Sitzung
GEBRAUCHSINFORMATION Purevax RCP Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension
 GEBRAUCHSINFORMATION Purevax RCP Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR
GEBRAUCHSINFORMATION Purevax RCP Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR
LEITFADEN FÜR PATIENTINNEN
 LEITFADEN FÜR PATIENTINNEN Valproathaltige Arzneimittel Empfängnisverhütung und Schwangerschaft: Was Sie unbedingt wissen sollten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies er
LEITFADEN FÜR PATIENTINNEN Valproathaltige Arzneimittel Empfängnisverhütung und Schwangerschaft: Was Sie unbedingt wissen sollten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies er
Arbeitsauftrag für die Gruppenarbeiten:
 Zentrum für Ersatz- und Ergänzungsmethoden zu Tierversuchen Institut für Pädagogik und Psychologie Thema: Erprobung von Unterrichtsmaterialien für ein Buchprojekt zu Alternativen zu Tierversuchen Arbeitsauftrag
Zentrum für Ersatz- und Ergänzungsmethoden zu Tierversuchen Institut für Pädagogik und Psychologie Thema: Erprobung von Unterrichtsmaterialien für ein Buchprojekt zu Alternativen zu Tierversuchen Arbeitsauftrag
Tierversuche Kosmetik
 Tierversuche Kosmetik Methodisch-didaktischer Kommentar Die erste Assoziation mit dem Begriff Tierversuche ist häufig jene mit Tierversuchen in der Kosmetik. So glauben viele Menschen, dass diese den Großteil
Tierversuche Kosmetik Methodisch-didaktischer Kommentar Die erste Assoziation mit dem Begriff Tierversuche ist häufig jene mit Tierversuchen in der Kosmetik. So glauben viele Menschen, dass diese den Großteil
Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome
 Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome Basisinformation FACHINFORMATION Lang wirksame Beta-Mimetika - Long Acting Beta Agonists
Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome Basisinformation FACHINFORMATION Lang wirksame Beta-Mimetika - Long Acting Beta Agonists
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
 Gebrauchsinformation: Information für den Anwender Mallebrin Konzentrat zum Gurgeln 2,2 g/10 ml Lösung Wirkstoff: Aluminiumchlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält
Gebrauchsinformation: Information für den Anwender Mallebrin Konzentrat zum Gurgeln 2,2 g/10 ml Lösung Wirkstoff: Aluminiumchlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält
Tierversuche. medizinische Notwendigkeit oder sinnlose Quälerei? Dipl.-Biol. Silke Bitz Ärzte gegen Tierversuche e.v. Bund gegen Missbrauch der Tiere
 Tierversuche medizinische Notwendigkeit oder sinnlose Quälerei? Dipl.-Biol. Silke Bitz Bund gegen Missbrauch der Tiere Themenauswahl Tierschutzgesetz / Tierzahlen Ethik Beispiele für f r Tierversuche /
Tierversuche medizinische Notwendigkeit oder sinnlose Quälerei? Dipl.-Biol. Silke Bitz Bund gegen Missbrauch der Tiere Themenauswahl Tierschutzgesetz / Tierzahlen Ethik Beispiele für f r Tierversuche /
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION
 ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION Diese Änderungen von SPC und Packungsbeilage treten zum Zeitpunkt der Kommissionsentscheidung in Kraft.
ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION Diese Änderungen von SPC und Packungsbeilage treten zum Zeitpunkt der Kommissionsentscheidung in Kraft.
Inhalt: Themenkomplex III:
 26.1.2018 Inhalt: Themenkomplex I: Themenkomplex II: Themenkomplex III: Definitionen FSCA Trendmeldungen I Themenkomplex: Definitionen 1 Frage: Wie ist eine schwerwiegende Verschlechterung des Gesundheitszustandes
26.1.2018 Inhalt: Themenkomplex I: Themenkomplex II: Themenkomplex III: Definitionen FSCA Trendmeldungen I Themenkomplex: Definitionen 1 Frage: Wie ist eine schwerwiegende Verschlechterung des Gesundheitszustandes
Antrag bei der Krankenkasse Zur Übernahme der Behandlungskosten - Off Label Therapie bei Uveitis - Patient:, geb. Datum:
 Antrag bei der Krankenkasse Zur Übernahme der Behandlungskosten - Off Label Therapie bei Uveitis - Patient:, geb. Datum: Augen-Diagnosen (bitte alle auflisten): Uveitis bekannt seit: Symptome durch die
Antrag bei der Krankenkasse Zur Übernahme der Behandlungskosten - Off Label Therapie bei Uveitis - Patient:, geb. Datum: Augen-Diagnosen (bitte alle auflisten): Uveitis bekannt seit: Symptome durch die
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien
 Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Dimebon Enttäuschend bei Alzheimer, könnte aber bei Huntington funktionieren
 Neuigkeiten aus der Huntington-Forschung. In einfacher Sprache. Von Wissenschaftlern geschrieben Für die Huntington-Gemeinschaft weltweit. Ein neuer Artikel mit aktualisierten Informationen zu diesem Thema
Neuigkeiten aus der Huntington-Forschung. In einfacher Sprache. Von Wissenschaftlern geschrieben Für die Huntington-Gemeinschaft weltweit. Ein neuer Artikel mit aktualisierten Informationen zu diesem Thema
RoACTEMRA (Tocilizumab) i.v. und s.c. Patientenpass
 RoACTEMRA (Tocilizumab) i.v. und s.c. Patientenpass Dieser Patientenpass enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/ Erziehungsberechtigte Bescheid wissen müssen, bevor,
RoACTEMRA (Tocilizumab) i.v. und s.c. Patientenpass Dieser Patientenpass enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/ Erziehungsberechtigte Bescheid wissen müssen, bevor,
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Erivedge Schwangerschaftsverhütungs-Programm
 behördlich genehmigtes Schulungsmaterial Erivedge Schwangerschaftsverhütungs-Programm Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
behördlich genehmigtes Schulungsmaterial Erivedge Schwangerschaftsverhütungs-Programm Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
Gebrauchsinformation Zintona
 Gebrauchsinformation Bitte aufmerksam lesen Sehr geehrte Patientin, sehr geehrter Patient, bitte lesen Sie folgende Gebrauchsinformation aufmerksam, weil sie wichtige Informationen darüber enthält, was
Gebrauchsinformation Bitte aufmerksam lesen Sehr geehrte Patientin, sehr geehrter Patient, bitte lesen Sie folgende Gebrauchsinformation aufmerksam, weil sie wichtige Informationen darüber enthält, was
: Schulungsmaterial (Educational Material) für medizinisches Fachpersonal
 Kadcyla : Schulungsmaterial (Educational Material) für medizinisches Fachpersonal EU Information für medizinisches Fachpersonal Januar 2017 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung.
Kadcyla : Schulungsmaterial (Educational Material) für medizinisches Fachpersonal EU Information für medizinisches Fachpersonal Januar 2017 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung.
Transparenz in der Zusammenarbeit mit Ärzten
 Transparenz in der Zusammenarbeit mit Ärzten Offenlegung von Zahlungen an Ärzte und andere Heilberufe Die Pharmaindustrie und Angehörige medizinischer Fachkreise arbeiten in vielen Bereichen zusammen:
Transparenz in der Zusammenarbeit mit Ärzten Offenlegung von Zahlungen an Ärzte und andere Heilberufe Die Pharmaindustrie und Angehörige medizinischer Fachkreise arbeiten in vielen Bereichen zusammen:
Biosimilars- Die Sicht der Patienten
 Ähnlich, aber eben doch nicht gleich - Biopharmazeutika: Der Unterschied liegt im Detail Biosimilars- Die Sicht der Patienten 27. November 2012 Ludwigshafen Renate Haidinger Medozinjournalistin 1.Vorsitzende
Ähnlich, aber eben doch nicht gleich - Biopharmazeutika: Der Unterschied liegt im Detail Biosimilars- Die Sicht der Patienten 27. November 2012 Ludwigshafen Renate Haidinger Medozinjournalistin 1.Vorsitzende
Therapie mit Acitretin-haltigen Arzneimitteln: Was Sie wissen müssen
 Therapie mit Acitretin-haltigen Arzneimitteln: Was Sie wissen müssen Informationsbroschüre für männliche Patienten und Patientinnen, die nicht im gebärfähigen Alter sind Diese Informationsbroschüre wurde
Therapie mit Acitretin-haltigen Arzneimitteln: Was Sie wissen müssen Informationsbroschüre für männliche Patienten und Patientinnen, die nicht im gebärfähigen Alter sind Diese Informationsbroschüre wurde
Gebrauchsinformation: Information für Anwender
 Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für Anwender AKNICHTHOL 1% Emulsion zur Anwendung auf der Haut (Lotio) Wirkstoff: Natriumbituminosulfonat (ICHTHYOL
Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für Anwender AKNICHTHOL 1% Emulsion zur Anwendung auf der Haut (Lotio) Wirkstoff: Natriumbituminosulfonat (ICHTHYOL
behördlich genehmigtes Schulungsmaterial (Adalimumab) Patientenpass für Erwachsene
 behördlich genehmigtes Schulungsmaterial HUMIRA (Adalimumab) Patientenpass für Erwachsene Juli 2017 Liebe Patienten, lieber Patient, Ihr behandelnder Arzt hat Ihnen HUMIRA verordnet. Dieser Patientenpass
behördlich genehmigtes Schulungsmaterial HUMIRA (Adalimumab) Patientenpass für Erwachsene Juli 2017 Liebe Patienten, lieber Patient, Ihr behandelnder Arzt hat Ihnen HUMIRA verordnet. Dieser Patientenpass
Leitfaden für Patienten zur Anwendung von KYMRIAH (Tisagenlecleucel)
 Leitfaden für Patienten zur Anwendung von KYMRIAH (Tisagenlecleucel) Wichtige Sicherheitsinformationen zur Minimierung des Risikos von KYMRIAH Der Wirkstoff von KYMRIAH heißt Tisagenlecleucel. Diese Bezeichnung
Leitfaden für Patienten zur Anwendung von KYMRIAH (Tisagenlecleucel) Wichtige Sicherheitsinformationen zur Minimierung des Risikos von KYMRIAH Der Wirkstoff von KYMRIAH heißt Tisagenlecleucel. Diese Bezeichnung
Als Krebspatient an einer Studie teilnehmen was sollte man wissen?
 Als Krebspatient an einer Studie teilnehmen was sollte man wissen? Krebsinformationsdienst, Heidelberg Dr. Susanne Weg-Remers Seite 2 Grundlage für evidenzbasiertes medizinisches Wissen sind klinische
Als Krebspatient an einer Studie teilnehmen was sollte man wissen? Krebsinformationsdienst, Heidelberg Dr. Susanne Weg-Remers Seite 2 Grundlage für evidenzbasiertes medizinisches Wissen sind klinische
Quelle Salzburg Tourismus
 Quelle Salzburg Tourismus Möglichkeiten für Patientenpartizipation In akademischer Forschung Florian B Lagler Institut für Angeborene Stoffwechselerkrankungen & UK für Kinder- und Jugendheilkunde Paracelsus
Quelle Salzburg Tourismus Möglichkeiten für Patientenpartizipation In akademischer Forschung Florian B Lagler Institut für Angeborene Stoffwechselerkrankungen & UK für Kinder- und Jugendheilkunde Paracelsus
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Nr. 19 Aknetropfen Mag. Doskar Kalium iodatum D3, Juglans regia D2, Berberis vulgaris D3
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 19 Aknetropfen Mag. Doskar Kalium iodatum D3, Juglans regia D2, Berberis vulgaris D3 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 19 Aknetropfen Mag. Doskar Kalium iodatum D3, Juglans regia D2, Berberis vulgaris D3 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Neurobion 100 mg 100 mg 1 mg / 3 ml Injektionslösung Vitamine B 1 + B 6 + B 12
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Neurobion 100 mg 100 mg 1 mg / 3 ml Injektionslösung Vitamine B 1 + B 6 + B 12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch bevor Sie mit der Anwendung
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Neurobion 100 mg 100 mg 1 mg / 3 ml Injektionslösung Vitamine B 1 + B 6 + B 12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch bevor Sie mit der Anwendung
Anlage 1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 Anlage 1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER (Name/Phantasiebezeichnung des Arzneimittels Stärke Darreichungsform) 1 (Wirkstoff(e)) 1 Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Anlage 1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER (Name/Phantasiebezeichnung des Arzneimittels Stärke Darreichungsform) 1 (Wirkstoff(e)) 1 Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
COMMUNICATIONS TO SUCCESS. Marketing in der pharmazeutischen Industrie. Akademie
 Marketing in der pharmazeutischen Industrie Akademie 6.1. 2005 1 Ausgaben der GKV 2003 (in Millrd. Euro) 8,6 Krankenhauskosten 31,3 9,3 24,2 24,3 46,8 ärztliche Leistung Arzneimiitel Heil- und Hilfsmittel
Marketing in der pharmazeutischen Industrie Akademie 6.1. 2005 1 Ausgaben der GKV 2003 (in Millrd. Euro) 8,6 Krankenhauskosten 31,3 9,3 24,2 24,3 46,8 ärztliche Leistung Arzneimiitel Heil- und Hilfsmittel
KRANKEN- UND PFLEGEVERSICHERUNG. Die elektronische Behandlungsinformation. Mit Sicherheit für Sie.
 KRANKEN- UND PFLEGEVERSICHERUNG Die elektronische Behandlungsinformation Mit Sicherheit für Sie. Ein neuer und für Sie kostenloser Service der Knappschaft: ebi. elektronische Behandlungsinformation 3 Liebe
KRANKEN- UND PFLEGEVERSICHERUNG Die elektronische Behandlungsinformation Mit Sicherheit für Sie. Ein neuer und für Sie kostenloser Service der Knappschaft: ebi. elektronische Behandlungsinformation 3 Liebe
Studien im Darmzentrum Oberhavel
 Studien im Darmzentrum Oberhavel? 1564484 medizinische-ausrüstung-wi.de/123rfcom Studien im Darmzentrum Oberhavel Ziel dieses Vortrages: - Sinn und Zweck von Studien zu verstehen - Aufgabenbereiche kennen
Studien im Darmzentrum Oberhavel? 1564484 medizinische-ausrüstung-wi.de/123rfcom Studien im Darmzentrum Oberhavel Ziel dieses Vortrages: - Sinn und Zweck von Studien zu verstehen - Aufgabenbereiche kennen
Antrag auf Freistellung aus der Verschreibungspflicht für Omeprazol 20 mg
 Antrag auf Freistellung aus der Verschreibungspflicht für Omeprazol 20 mg Sachverständigen-Ausschuss für Verschreibungspflicht 13. Januar 2009 Rationale des Antrags Omeprazol ist eine der effektivsten
Antrag auf Freistellung aus der Verschreibungspflicht für Omeprazol 20 mg Sachverständigen-Ausschuss für Verschreibungspflicht 13. Januar 2009 Rationale des Antrags Omeprazol ist eine der effektivsten
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Nux vomica-homaccord -Tropfen
 1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Nux vomica-homaccord -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Nux vomica-homaccord -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
octenisept Wund-Desinfektion ist ein Antiseptikum zur wiederholten, zeitlich begrenzten unterstützenden antiseptischen Wundbehandlung.
 Gebrauchsinformation: Information für den Anwender OCTENISEPT WUND-DESINFEKTION Antiseptikum zur unterstützenden Wundbehandlung Lösung zum Aufsprühen auf die Wunde Wirkstoffe: 0.1 g Octenidinhydrochlorid
Gebrauchsinformation: Information für den Anwender OCTENISEPT WUND-DESINFEKTION Antiseptikum zur unterstützenden Wundbehandlung Lösung zum Aufsprühen auf die Wunde Wirkstoffe: 0.1 g Octenidinhydrochlorid
Arzneimittelentwicklung
 Arzneimittelentwicklung Vom Molekül zum Medikament /////////// Dr. med. Konstanze Diefenbach (Leitern Medizin Bayer Vital GmbH) Mai 2018 Vom Molekül zum Medikament: Der lange Weg der Arzneimittelentwicklung
Arzneimittelentwicklung Vom Molekül zum Medikament /////////// Dr. med. Konstanze Diefenbach (Leitern Medizin Bayer Vital GmbH) Mai 2018 Vom Molekül zum Medikament: Der lange Weg der Arzneimittelentwicklung
Sind Studien notwendig? Studien sind notwendig! Auch wenn dies so manchen Zweifel auslösen mag, müssen wir doch erkennen, dass die wissenschaftliche
 Sind Studien notwendig? Studien sind notwendig! Auch wenn dies so manchen Zweifel auslösen mag, müssen wir doch erkennen, dass die wissenschaftliche Forschung den Zweck hat, neue oder bessere Therapien
Sind Studien notwendig? Studien sind notwendig! Auch wenn dies so manchen Zweifel auslösen mag, müssen wir doch erkennen, dass die wissenschaftliche Forschung den Zweck hat, neue oder bessere Therapien
Natriumchlorid 10 % und 20 %, Konzentrat zur Herstellung einer Infusionslösung Natriumchlorid
 Seite 1/5 Gebrauchsinformation für den Benutzer Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
Seite 1/5 Gebrauchsinformation für den Benutzer Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
MAVENCLAD. Informationsmaterial für Patienten. Version 1.0, [Stand Juli 2017]
![MAVENCLAD. Informationsmaterial für Patienten. Version 1.0, [Stand Juli 2017] MAVENCLAD. Informationsmaterial für Patienten. Version 1.0, [Stand Juli 2017]](/thumbs/78/78512222.jpg) MAVENCLAD Informationsmaterial für Patienten Version 1.0, [Stand Juli 2017] Wichtige Informationen für Patienten, die eine Therapie mit Mavenclad beginnen Inhalt Einführung Wie erfolgt die Behandlung mit
MAVENCLAD Informationsmaterial für Patienten Version 1.0, [Stand Juli 2017] Wichtige Informationen für Patienten, die eine Therapie mit Mavenclad beginnen Inhalt Einführung Wie erfolgt die Behandlung mit
Biologika trotz Nebenwirkungen sicher anwendbar
 Zielgenaue Medikamente gegen Rheuma Biologika trotz Nebenwirkungen sicher anwendbar Köln (23. September 2009) Biotechnologische Medikamente gegen Rheuma sogenannte Biologika lindern nicht nur die Krankheit
Zielgenaue Medikamente gegen Rheuma Biologika trotz Nebenwirkungen sicher anwendbar Köln (23. September 2009) Biotechnologische Medikamente gegen Rheuma sogenannte Biologika lindern nicht nur die Krankheit
Tierethik. Angelika Pfannenschmid Elke Sedlak Kommentar: Jenny Klein
 Tierethik Angelika Pfannenschmid Elke Sedlak Kommentar: Jenny Klein Peter Singer Alle Tiere sind gleich Vorurteile: Unterdrücker vs. Unterdrückte Bewusstwerden der Vorurteile ist die erste Stufe auf dem
Tierethik Angelika Pfannenschmid Elke Sedlak Kommentar: Jenny Klein Peter Singer Alle Tiere sind gleich Vorurteile: Unterdrücker vs. Unterdrückte Bewusstwerden der Vorurteile ist die erste Stufe auf dem
Wieso Patente in der Pharmaindustrie sinnvoll sind
 Wieso Patente in der Pharmaindustrie sinnvoll sind Bericht von Franziska Madlo- Thiess (Initiative Humanismus), Titelbild von Magnus Manske, CC BY 1.0 Ich hatte das Programm der Initiative Humanismus in
Wieso Patente in der Pharmaindustrie sinnvoll sind Bericht von Franziska Madlo- Thiess (Initiative Humanismus), Titelbild von Magnus Manske, CC BY 1.0 Ich hatte das Programm der Initiative Humanismus in
PATIENTEN- INFORMATIONSKARTE
 PATIENTEN- INFORMATIONSKARTE Diese Patienteninformationskarte ist ein verpflichtender Teil der Zulassung, um sicherzustellen, dass Angehörige der Heilberufe, sowie Patienten die besonderen Sicherheitsanforder
PATIENTEN- INFORMATIONSKARTE Diese Patienteninformationskarte ist ein verpflichtender Teil der Zulassung, um sicherzustellen, dass Angehörige der Heilberufe, sowie Patienten die besonderen Sicherheitsanforder
Gebrauchsinformation: Information für Patienten. Schlaf- und Entspannungstropfen Similasan Avena sativa D1, Passiflora incarnata D1
 1/5 Gebrauchsinformation: Information für Patienten Schlaf- und Entspannungstropfen Similasan Avena sativa D1, Passiflora incarnata D1 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
1/5 Gebrauchsinformation: Information für Patienten Schlaf- und Entspannungstropfen Similasan Avena sativa D1, Passiflora incarnata D1 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
VPRIV (Velaglucerase alfa)
 VPRIV (Velaglucerase alfa) Schulungsmaterial für Ärzte Die hier aufgeführten Dokumente wurden von Shire im Rahmen der Verpflichtung zu Risikominimierungsmaβnahmen für VPRIV erstellt und dienen als Leitlinie
VPRIV (Velaglucerase alfa) Schulungsmaterial für Ärzte Die hier aufgeführten Dokumente wurden von Shire im Rahmen der Verpflichtung zu Risikominimierungsmaβnahmen für VPRIV erstellt und dienen als Leitlinie
PATENT DE B4
 P A T E N T M E R K M A L E PATENT DE10 2007 048 094 B4 VERFAHREN UND PATENTGRUNDLAGE M.O.M HELENAA Das patentierte Verfahren M.O.M Helenaa beschreibt eine Technologie z.b. über Apps, als integrierte Lösung
P A T E N T M E R K M A L E PATENT DE10 2007 048 094 B4 VERFAHREN UND PATENTGRUNDLAGE M.O.M HELENAA Das patentierte Verfahren M.O.M Helenaa beschreibt eine Technologie z.b. über Apps, als integrierte Lösung
Medizinischer Dienst der Krankenversicherung im Saarland. Bewertung der Nebenwirkungen. Diskussionsforum SEG 6
 Bewertung der Nebenwirkungen von Diskussionsforum SEG 6 Dortmund, 14.09.2010 Dr. med. Horst Rixecker Berührungspunkte Off-label-Begutachtung Behandlungsfehler Dr. med. Horst Rixecker Fallbeispiel Operation
Bewertung der Nebenwirkungen von Diskussionsforum SEG 6 Dortmund, 14.09.2010 Dr. med. Horst Rixecker Berührungspunkte Off-label-Begutachtung Behandlungsfehler Dr. med. Horst Rixecker Fallbeispiel Operation
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang III Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Es kann notwendig sein, dass die Änderungen in der Zusammenfassung
Anhang III Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Es kann notwendig sein, dass die Änderungen in der Zusammenfassung
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER AFLUBIN chronisch- Hustentropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER AFLUBIN chronisch- Hustentropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn sie
Gebrauchsinformation: Information für den Anwender
 Gebrauchsinformation: Information für den Anwender OPTOVIT forte 1 Weichkapsel enthält 134,2 mg RRR--Tocopherol (Vitamin E) Liebe Patientin, lieber Patient, bitte lesen Sie die gesamte Gebrauchsinformation
Gebrauchsinformation: Information für den Anwender OPTOVIT forte 1 Weichkapsel enthält 134,2 mg RRR--Tocopherol (Vitamin E) Liebe Patientin, lieber Patient, bitte lesen Sie die gesamte Gebrauchsinformation
WAS SIE ÜBER RIXATHON (RITUXIMAB) WISSEN SOLLTEN
 WAS SIE ÜBER RIXATHON (RITUXIMAB) WISSEN SOLLTEN WICHTIGE SICHERHEITSINFORMATIONEN FÜR PATIENTEN, DIE MIT RIXATHON BEHANDELT WERDEN Dieses Informationsmaterial zur Anwendung von Rixathon (Rituximab) wurde
WAS SIE ÜBER RIXATHON (RITUXIMAB) WISSEN SOLLTEN WICHTIGE SICHERHEITSINFORMATIONEN FÜR PATIENTEN, DIE MIT RIXATHON BEHANDELT WERDEN Dieses Informationsmaterial zur Anwendung von Rixathon (Rituximab) wurde
MYCOPHENOLATMOFETIL (MMF)-/ MYCOPHENOLSÄURE (MPA)-HALTIGE ARZNEIMITTEL: Teratogenes Risiko LEITFADEN FÜR ANGEHÖRIGE DER GESUNDHEITSBERUFE
 MYCOPHENOLATMOFETIL (MMF)-/ MYCOPHENOLSÄURE (MPA)-HALTIGE ARZNEIMITTEL: Teratogenes Risiko LEITFADEN FÜR ANGEHÖRIGE DER GESUNDHEITSBERUFE Dieser Leitfaden zur Anwendung von Mycophenolat-haltigen Arzneimitteln
MYCOPHENOLATMOFETIL (MMF)-/ MYCOPHENOLSÄURE (MPA)-HALTIGE ARZNEIMITTEL: Teratogenes Risiko LEITFADEN FÜR ANGEHÖRIGE DER GESUNDHEITSBERUFE Dieser Leitfaden zur Anwendung von Mycophenolat-haltigen Arzneimitteln
Gebrauchsinformation: Information für Anwender
 Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für Anwender AKNICHTHOL SOFT 1% Emulsion zur Anwendung auf der Haut (Lotio) Wirkstoff: Natriumbituminosulfonat
Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für Anwender AKNICHTHOL SOFT 1% Emulsion zur Anwendung auf der Haut (Lotio) Wirkstoff: Natriumbituminosulfonat
