Risikoüberwachung von Arzneimitteln - Aktuelle Situation
|
|
|
- Paula Kranz
- vor 6 Jahren
- Abrufe
Transkript
1 Risikoüberwachung von Arzneimitteln - Aktuelle Situation U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte Abteilung Pharmakovigilanz Fortbildung für den Öffentlichen Dienst Berlin, 2. April 2008 Besuchen Sie unsere Webseite:
2 Was ist Pharmakovigilanz? Die WHO definiert Pharmakovigilanz als Wissenschaft und alle Aktivitäten, die sich mit der Aufdeckung, Bewertung, dem Verstehen und der Prävention von Nebenwirkungen oder von anderen Arzneimittel-bezogenen Problemen befassen. U. Hagemann, ÖGD, Berlin, 2. April
3 Das ist Pharmakovigilanz! Ich glaube, dass wir Beweise dafür haben, dass es einen Unterschied gibt zwischen dem, was wir wussten, und dem, was wir gefunden haben. Condoleeza Rice zu CBS am 30. Januar 2004 U. Hagemann, ÖGD, Berlin, 2. April
4 Erkenntnisse über neue Arzneimittel sind begrenzt Unbekannte (in Studien nicht beobachtete) Nebenwirkungen oder Wechselwirkungen Seltene Nebenwirkungen oder Wechselwirkungen und ihre tatsächliche Häufigkeit Einfluss von Risikofaktoren (Krankheiten, Alter, Schwangerschaft etc.) Spätwirkungen U. Hagemann, ÖGD, Berlin, 2. April
5 Einige Gründe für das Wissensdefizit Klinische Prüfungen: Kleine Anzahl behandelter Patienten Ausgewählte Patienten, keine Alltagsbedingungen Häufig nicht (völlig) bekannte Wirkungsweisen (Mechanismus) Deshalb: regelmäßige und wiederholte Nutzen-Schaden-Bewertung von Arzneimitteln nötig U. Hagemann, ÖGD, Berlin, 2. April
6 Informationsquellen über Arzneimittelrisiken Bundesinstitut für Arzneimittel Toxikologische Untersuchungen Spontanberichte = UAW-Berichte Untersuchungen zur Qualität Klinische Studien Ereignisfeld Epidemiologische Studien Beobachtungsstudien Neuer Erkenntnisstand U. Hagemann, ÖGD, Berlin, 2. April
7 Anzahl der UAW-Berichte (Inland) Zeitraum: 1995 bis Oktober 2007, Gesamtzahl: ~ Bundesinstitut für Arzneimittel Todesfälle andere U. Hagemann, ÖGD, Berlin, 2. April
8 Verteilung der Spontanberichte nach ATC-Code (2005) Bundesinstitut für Arzneimittel U. Hagemann, ÖGD, Berlin, 2. April
9 Anlass für regulatorische Maßnahmen Bei begründetem Verdacht auf unvertretbare Risiken Und wann ist das der Fall? Es gibt keine allgemein gültige Messlatte dafür. Gesonderte Nutzen-Schaden- Bewertung in jedem Einzelfall U. Hagemann, ÖGD, Berlin, 2. April
10 Was ist in einer Nutzen-Schaden- Bewertung zu berücksichtigen? Art und Häufigkeit der Nebenwirkung Schweregrad der Nebenwirkung Ursächlicher Zusammenhang Nutzen und Schaden von Behandlungsalternativen Qualität der Belege dafür U. Hagemann, ÖGD, Berlin, 2. April
11 Risikobewertungsverfahren So genannte Signalverfahren Wenige Arzneimittel, kleine Anzahl von beteiligten Firmen, kein schwerwiegendes Problem Stufenplanverfahren In allen anderen Fällen EU Verfahren Artikel 30, 36 oder 107 der RL 2001/83/EG Artikel 20 der VO 726/2004 U. Hagemann, ÖGD, Berlin, 2. April
12 Was kann das BfArM/PEI veranlassen? Weitere Studien anordnen Produktinformation verbessern Gegenanzeigen anordnen Anwendungsgebiete einschränken Verschreibungs- oder Apothekenpflicht empfehlen Arzneimittel verbieten U. Hagemann, ÖGD, Berlin, 2. April
13 Das Konzept der Risk Management-Pläne Bundesinstitut für Arzneimittel Wann ist ein RMP zu erstellen? Neue Wirkstoffe bzw. prinzipien Signifikante Änderungen bei bekannten Wirkstoffen Neue Patientenpopulationen oder neue Indikationen Neue Sicherheitsbedenken U. Hagemann, ÖGD, Berlin, 2. April
14 Risiko- Spezifikation: die weißen Flecken benennen Bundesinstitut für Arzneimittel Nicht geklärte präklinische Befunde z.b. Reproduktionstoxizität, Interaktionen, genetische Polymorphismen Nicht abschließend untersuchte klinische Sicherheit und mögliche Risiken weitere Populationen, identifizierte Risiken Epidemiologie der Erkrankung z.b. Inzidenz, Prävalenz, Mortalität Klasseneffekte U. Hagemann, ÖGD, Berlin, 2. April
15 Der Pharmakovigilanz-Plan Routine-Aktivitäten in der Pharmakovigilanz, aber darüber hinaus gehend Orientiert sich an Risiko-Spezifikation mit Fragen nach Häufigkeit von UAW relativen Risiken und Risikounterschieden Risikomodulation Risikofaktoren zu den identifizierten Risiken Beobachtungsinstrumente: Beobachtungsstudien, klinische Studien U. Hagemann, ÖGD, Berlin, 2. April
16 Planung zur Risikominderung ( Risk minimisation ) Instrumente reichen von Warnhinweisen bis zu ausgefeilten Monitoring Programmen Spektrum möglicher Medikationsfehler diskutieren zugeschnitten auf das Problem Bundesinstitut für Arzneimittel U. Hagemann, ÖGD, Berlin, 2. April
17 Riskokommunikation: Transparenz und Offenheit Rolle der Behörden: Bindeglied zwischen Industrie, Ärzten, Patienten und Politikern Dem Verbraucherschutz verpflichtet Unabhängig und unbeeinflusst Offen für abweichende Meinungen Kein closed shop Hauptzweck: Empfehlungen geben, die Wahrheit sagen, richtige Aussagen machen U. Hagemann, ÖGD, Berlin, 2. April
18 Riskokommunikation: Transparenz und Offenheit Bundesinstitut für Arzneimittel Die Medienumwelt Massenmedien, Internet, Gesundheitsbücher, Werbung Wann kommunizieren? In Krisen, in Bewertungsverfahren, Richtigstellung falscher Informationen etc. Was kommunizieren? Seltene und bedeutende Risiken, wichtige negative Befunde etc. Zusammengefasst und ausgewogen Keine Spekulationen und Annahmen U. Hagemann, ÖGD, Berlin, 2. April
19 Frühe Darstellung eines Behörden- Pharmakovigilanzlers Japan, 16. Jhdt. U. Hagemann, ÖGD, Berlin, 2. April
Risikomanagement bei neuartigen Arzneimitteln
 Risikomanagement bei neuartigen Arzneimitteln IQWiG Herbst - Symposion Köln, 28. November Ulrich Hagemann Abteilung Pharmakovigilanz im BfArM, Bonn Besuchen Sie unsere Webseite: www.bfarm.de/pharmakovigilanz
Risikomanagement bei neuartigen Arzneimitteln IQWiG Herbst - Symposion Köln, 28. November Ulrich Hagemann Abteilung Pharmakovigilanz im BfArM, Bonn Besuchen Sie unsere Webseite: www.bfarm.de/pharmakovigilanz
Nutzen-Schaden-Bewertung von Arzneimitteln nach der Zulassung
 Nutzen-Schaden-Bewertung von Arzneimitteln nach der Zulassung U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Abteilung Pharmakovigilanz IQWiG im Dialog Köln, 19. Besuchen Sie unsere
Nutzen-Schaden-Bewertung von Arzneimitteln nach der Zulassung U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Abteilung Pharmakovigilanz IQWiG im Dialog Köln, 19. Besuchen Sie unsere
Beteiligung von Patienten an der Bewertung von Arzneimitteln bei der Zulassung und der Nutzen-Schaden- Bewertung
 Beteiligung von Patienten an der Bewertung von Arzneimitteln bei der Zulassung und der Nutzen-Schaden- Bewertung U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte, Bonn Gesundheit e.v. 10.
Beteiligung von Patienten an der Bewertung von Arzneimitteln bei der Zulassung und der Nutzen-Schaden- Bewertung U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte, Bonn Gesundheit e.v. 10.
Zydelig (Idelalisib) :
 Zydelig (Idelalisib) : Erhöhte Anzahl infektionsbedingter Todesfälle Vorläufige Maßnahmen im Verfahren nach Art. 20 der VO (EG) 726/2004 78. Routinesitzung, 26. April 2016 Routinesitzung 78. Sitzung 26.04.2016
Zydelig (Idelalisib) : Erhöhte Anzahl infektionsbedingter Todesfälle Vorläufige Maßnahmen im Verfahren nach Art. 20 der VO (EG) 726/2004 78. Routinesitzung, 26. April 2016 Routinesitzung 78. Sitzung 26.04.2016
Einleitung und Leseanweisung
 VII Einleitung und Leseanweisung Für wen ist dieses Buch? Der Pocket Guide ist für alle klinisch tätigen Psychiater geschrieben, denen das Kompendium der Psychiatrischen Pharmakotherapie für die Kitteltasche
VII Einleitung und Leseanweisung Für wen ist dieses Buch? Der Pocket Guide ist für alle klinisch tätigen Psychiater geschrieben, denen das Kompendium der Psychiatrischen Pharmakotherapie für die Kitteltasche
i:fox WEB Arzneimittel-Therapie- Sicherheit und aktuellste Daten für Online-Apotheken
 Mit Sicherheit mehr Visits & Umsatz durch Online-Checks für Medikamente i:fox WEB Arzneimittel-Therapie- Sicherheit und aktuellste Daten für Online-Apotheken Mehr Information = mehr Visits = mehr Umsatz
Mit Sicherheit mehr Visits & Umsatz durch Online-Checks für Medikamente i:fox WEB Arzneimittel-Therapie- Sicherheit und aktuellste Daten für Online-Apotheken Mehr Information = mehr Visits = mehr Umsatz
Bundesinstitut für Arzneimittel und Medizinprodukte Langwirksame Beta-Mimetika (LABA) Salmeterol/ Formoterol
 Langwirksame Beta-Mimetika (LABA) Salmeterol/ Formoterol Risikobewertung Änderung der Produktinformationen Anstoß der Diskussion Salmeterol-Studien: SMART-Studie (Salmeterol Multicenter Asthma Research
Langwirksame Beta-Mimetika (LABA) Salmeterol/ Formoterol Risikobewertung Änderung der Produktinformationen Anstoß der Diskussion Salmeterol-Studien: SMART-Studie (Salmeterol Multicenter Asthma Research
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Täuschung und Manipulation mit Zahlen Teil 1
 Täuschung und Manipulation mit Zahlen Teil 1 Kleines Statistikseminar zum kritischen Umgang mit Zahlen 23.3.2011 Dr. med. H.-J. Koubenec Mammasprechstunde im Immanuel Krankenhaus Berlin Folien: Mammographie-Screening.de
Täuschung und Manipulation mit Zahlen Teil 1 Kleines Statistikseminar zum kritischen Umgang mit Zahlen 23.3.2011 Dr. med. H.-J. Koubenec Mammasprechstunde im Immanuel Krankenhaus Berlin Folien: Mammographie-Screening.de
Anhang III. Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage
 Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
Täuschung und Manipulation mit Zahlen
 58. Ärztekongress Berlin/Charité 4.11.2010 Täuschung und Manipulation mit Zahlen Kleines Statistikseminar zum kritischen Umgang mit Zahlen Dr. med. H.-J. Koubenec Mammasprechstunde im Immanuel Krankenhaus
58. Ärztekongress Berlin/Charité 4.11.2010 Täuschung und Manipulation mit Zahlen Kleines Statistikseminar zum kritischen Umgang mit Zahlen Dr. med. H.-J. Koubenec Mammasprechstunde im Immanuel Krankenhaus
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic )
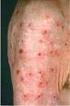 Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 23.11.2016 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 23.11.2016 Inhaltsverzeichnis
Anhang III. Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilagen
 Anhang III Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilagen Anmerkung: Diese Änderungen der entsprechenden Abschnitte der Zusammenfassung
Anhang III Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilagen Anmerkung: Diese Änderungen der entsprechenden Abschnitte der Zusammenfassung
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Die frühe Nutzenbewertung und ihre rechtlichen Herausforderungen
 und ihre rechtlichen Herausforderungen Rechtssymposium Die frühe Nutzenbewertung von Arzneimitteln nach AMNOG G-BA, Berlin Referent: Dr. jur. Rainer Hess, G-BA Seite 1 16. November 2010 Rechtssymposium
und ihre rechtlichen Herausforderungen Rechtssymposium Die frühe Nutzenbewertung von Arzneimitteln nach AMNOG G-BA, Berlin Referent: Dr. jur. Rainer Hess, G-BA Seite 1 16. November 2010 Rechtssymposium
Wortlaut der für die Packungsbeilage vorgesehenen Angaben
 Zulassungsnummer: 6312395.00.00 Seite 1 von 5 Apothekenpflichtig TUSSISANA Mischung 20 und 50 ml Stoff Darreichungsform Menge Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation:
Zulassungsnummer: 6312395.00.00 Seite 1 von 5 Apothekenpflichtig TUSSISANA Mischung 20 und 50 ml Stoff Darreichungsform Menge Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation:
UNERWÜNSCHTE ARZNEIMITTELWIRKUNGEN? So schützen Sie sich!
 /medikationsplan Die Versandapotheke Die Versandapotheke Die Versandapotheke Sicherheit durch PATHOS UNERWÜNSCHTE ARZNEIMITTELWIRKUNGEN? So schützen Sie sich! SANICARE Die Versandapotheke Grüner Weg 1
/medikationsplan Die Versandapotheke Die Versandapotheke Die Versandapotheke Sicherheit durch PATHOS UNERWÜNSCHTE ARZNEIMITTELWIRKUNGEN? So schützen Sie sich! SANICARE Die Versandapotheke Grüner Weg 1
1. Interaktionen erkennen und bewerten 2. ANSG
 1. Interaktionen erkennen und bewerten 2. ANSG Referentin: Bettina Hansen Mai 2014 Inhalt 1. Was ist Interaktion? 1.1. Maßnahmenklassifikation 1.2. Interaktionsmonografie 1.3. Beispiele 2. ANSG 3. Fragen
1. Interaktionen erkennen und bewerten 2. ANSG Referentin: Bettina Hansen Mai 2014 Inhalt 1. Was ist Interaktion? 1.1. Maßnahmenklassifikation 1.2. Interaktionsmonografie 1.3. Beispiele 2. ANSG 3. Fragen
GVP Module V Risk Management Systems
 GVP Module V Risk Management Systems Dr. Susanne Wolf Institut für Pharmakovigilanz AGES Gespräche Wien, 26.04.2012 Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Guideline on good
GVP Module V Risk Management Systems Dr. Susanne Wolf Institut für Pharmakovigilanz AGES Gespräche Wien, 26.04.2012 Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Guideline on good
Querschnittsbereich Nr. 1: Epidemiologie, Medizinische Biometrie und Medizinische Informatik. Behandelt werden 4 Themenblöcke
 Querschnittsbereich Nr. 1: Epidemiologie, Medizinische Biometrie und Medizinische Informatik Behandelt werden 4 Themenblöcke Ätiologie und Risiko Diagnose und Prognose Intervention Medizinische Informatik
Querschnittsbereich Nr. 1: Epidemiologie, Medizinische Biometrie und Medizinische Informatik Behandelt werden 4 Themenblöcke Ätiologie und Risiko Diagnose und Prognose Intervention Medizinische Informatik
Als Krebspatient an einer Studie teilnehmen was sollte man wissen?
 Als Krebspatient an einer Studie teilnehmen was sollte man wissen? Krebsinformationsdienst, Heidelberg Dr. Susanne Weg-Remers Seite 2 Grundlage für evidenzbasiertes medizinisches Wissen sind klinische
Als Krebspatient an einer Studie teilnehmen was sollte man wissen? Krebsinformationsdienst, Heidelberg Dr. Susanne Weg-Remers Seite 2 Grundlage für evidenzbasiertes medizinisches Wissen sind klinische
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Zovirax 3%-Augensalbe Wirkstoff: Aciclovir
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Zovirax 3%-Augensalbe Wirkstoff: Aciclovir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Zovirax 3%-Augensalbe Wirkstoff: Aciclovir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
nachrichtlich: Stufenplanbeteiligte, Zul mit DE= CMS
 - 2 - Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn pharmazeutische Unternehmer mit DE=RMS, nat. Zul, Parallelimp nachrichtlich: Stufenplanbeteiligte,
- 2 - Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn pharmazeutische Unternehmer mit DE=RMS, nat. Zul, Parallelimp nachrichtlich: Stufenplanbeteiligte,
Service-Angebote des BPI
 Pharmakovigilanz Service-Angebote des BPI BPI-Pharmakovigilanz Knowledge Base Mit dem EU-Pharmapackage und dem Zweiten Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften vom 19. Oktober
Pharmakovigilanz Service-Angebote des BPI BPI-Pharmakovigilanz Knowledge Base Mit dem EU-Pharmapackage und dem Zweiten Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften vom 19. Oktober
IQWiG Herbstsymposium / Unterschied zwischen Risiko-Nutzenabwägung (nach AMG) und Nutzen-Schadenabwägung (nach SGB V)
 IQWiG Herbstsymposium 19.11./20.11.2010 Unterschied zwischen Risiko-Nutzenabwägung (nach AMG) und Nutzen-Schadenabwägung (nach SGB V) Referent: Maximilian Grüne, Justiziar Gemeinsamer Bundesausschuss Seite
IQWiG Herbstsymposium 19.11./20.11.2010 Unterschied zwischen Risiko-Nutzenabwägung (nach AMG) und Nutzen-Schadenabwägung (nach SGB V) Referent: Maximilian Grüne, Justiziar Gemeinsamer Bundesausschuss Seite
/ November 2008
 - 2 - Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn Zweites Deutsches Fernsehen Redaktion Frontal 21 Unter den Linden 36-38 10117 Berlin Postanschrift:
- 2 - Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn Zweites Deutsches Fernsehen Redaktion Frontal 21 Unter den Linden 36-38 10117 Berlin Postanschrift:
Die Aufgaben des Pharmacovigilance Risk Assessment Committee (PRAC)
 Die Aufgaben des Pharmacovigilance Risk Assessment Committee (PRAC) November 2012 Hintergrund Verordnung (EU) Nr. 1235/2010 des Europäischen Parlaments und des Rates vom 15. Dezember 2010 (8) Um sicherzustellen,
Die Aufgaben des Pharmacovigilance Risk Assessment Committee (PRAC) November 2012 Hintergrund Verordnung (EU) Nr. 1235/2010 des Europäischen Parlaments und des Rates vom 15. Dezember 2010 (8) Um sicherzustellen,
Anhang III. Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale des Arzneimittels, der Etikettierung und
Anhang III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale des Arzneimittels, der Etikettierung und
Der Leitfaden zur Beratung. Informations- und Beratungshinweise in öffentlichen Apotheken
 Informations- und shinweise in öffentlichen Apotheken Dieser Leitfaden dient zur Eigen- und Fremdbeurteilung der und Information bei der Abgabe von Arzneimitteln auf ärztliche Verordnung sowie im Rahmen
Informations- und shinweise in öffentlichen Apotheken Dieser Leitfaden dient zur Eigen- und Fremdbeurteilung der und Information bei der Abgabe von Arzneimitteln auf ärztliche Verordnung sowie im Rahmen
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Ell-Cranell 250 Mikrogramm / ml Lösung zur Anwendung auf der Kopfhaut Zur Anwendung bei Erwachsenen Wirkstoff: Alfatradiol Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Ell-Cranell 250 Mikrogramm / ml Lösung zur Anwendung auf der Kopfhaut Zur Anwendung bei Erwachsenen Wirkstoff: Alfatradiol Lesen Sie die gesamte Packungsbeilage
octenisept Wund-Desinfektion ist ein Antiseptikum zur wiederholten, zeitlich begrenzten unterstützenden antiseptischen Wundbehandlung.
 Gebrauchsinformation: Information für den Anwender OCTENISEPT WUND-DESINFEKTION Antiseptikum zur unterstützenden Wundbehandlung Lösung zum Aufsprühen auf die Wunde Wirkstoffe: 0.1 g Octenidinhydrochlorid
Gebrauchsinformation: Information für den Anwender OCTENISEPT WUND-DESINFEKTION Antiseptikum zur unterstützenden Wundbehandlung Lösung zum Aufsprühen auf die Wunde Wirkstoffe: 0.1 g Octenidinhydrochlorid
Wissen, worauf es ankommt
 Wissen, worauf es ankommt www.tuev-sued.de/akademie GmbH Westendstraße 160 80339 München Telefon: 089 5791 2389 E-Mail: akademie@tuev-sued.de Bleiben wir in Kontakt! AC46-Pharma-fly-210x297-w-15-07-03
Wissen, worauf es ankommt www.tuev-sued.de/akademie GmbH Westendstraße 160 80339 München Telefon: 089 5791 2389 E-Mail: akademie@tuev-sued.de Bleiben wir in Kontakt! AC46-Pharma-fly-210x297-w-15-07-03
Biosimilars ähnlich, aber nicht identisch!
 Biosimilars ähnlich, aber nicht identisch! München, 23. April 2007 Dr. Frank Mathias Geschäftsführer, AMGEN GmbH Deutschland Die Frage...... identisch - oder nur ähnlich? 2 Biotechnologisch hergestellte
Biosimilars ähnlich, aber nicht identisch! München, 23. April 2007 Dr. Frank Mathias Geschäftsführer, AMGEN GmbH Deutschland Die Frage...... identisch - oder nur ähnlich? 2 Biotechnologisch hergestellte
Datum: Kontakt: Abteilung: Tel. / Fax: Unser Zeichen: Ihr Zeichen:
 BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 25.06.2015 Mag. pharm. Dr. Ulrike Rehberger REGA +43 (0) 505 55 36258 pv-implementation@ages.at
BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 25.06.2015 Mag. pharm. Dr. Ulrike Rehberger REGA +43 (0) 505 55 36258 pv-implementation@ages.at
Epidemiologische Grundbegriffe und Verfahren
 Epidemiologische Grundbegriffe und Verfahren Tumorzentrum Erlangen-Nürnberg 26.01.2004 Anja Daugs Epidemiologie Untersuchung der Verteilung und der Determinanten von Krankheitshäufigkeiten in umschriebenen
Epidemiologische Grundbegriffe und Verfahren Tumorzentrum Erlangen-Nürnberg 26.01.2004 Anja Daugs Epidemiologie Untersuchung der Verteilung und der Determinanten von Krankheitshäufigkeiten in umschriebenen
Gebrauchsinformation: Information für Patienten. Osanit Blähungskügelchen Wirkstoff: Matricaria recutita (Chamomilla) D12
 Seite 1 von 5 Gebrauchsinformation: Information für Patienten Osanit Blähungskügelchen Wirkstoff: Matricaria recutita (Chamomilla) D12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
Seite 1 von 5 Gebrauchsinformation: Information für Patienten Osanit Blähungskügelchen Wirkstoff: Matricaria recutita (Chamomilla) D12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
Paul-Ehrlich-Institut Bundesamt für Sera und Impfstoffe
 Bundesinstitut für Arzneimittel und Medizinprodukte Bundesamt für Sera und Impfstoffe Gemeinsame Empfehlungen des Bundesinstituts für Arzneimittel und Medizinprodukte und des s zur Planung, Durchführung
Bundesinstitut für Arzneimittel und Medizinprodukte Bundesamt für Sera und Impfstoffe Gemeinsame Empfehlungen des Bundesinstituts für Arzneimittel und Medizinprodukte und des s zur Planung, Durchführung
Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 13.11.2013 Inhaltsübersicht
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 13.11.2013 Inhaltsübersicht
Wechselwirkungen zwischen Arzneimitteln DR. KATALIN MÜLLNER
 Wechselwirkungen zwischen Arzneimitteln DR. KATALIN MÜLLNER Wechselwirkungen zwischen Arzneimitteln - Definition Auch als Arzneimittelinteraktionen Viele Patienten erhalten gleichzeitig mehrere Medikamente
Wechselwirkungen zwischen Arzneimitteln DR. KATALIN MÜLLNER Wechselwirkungen zwischen Arzneimitteln - Definition Auch als Arzneimittelinteraktionen Viele Patienten erhalten gleichzeitig mehrere Medikamente
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen
 Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Verein Demokratischer Pharmazeutinnen und Pharmazeuten
 Verein Demokratischer Pharmazeutinnen und Pharmazeuten Geschäftsstelle Neptun-Apotheke Bramfelder Chaussee 291 22177 Hamburg Tel.: 040 / 6391 7720 Fax.: 040 / 6391 7724 E-Mail: info@vdpp.de Internet: www.vdpp.de
Verein Demokratischer Pharmazeutinnen und Pharmazeuten Geschäftsstelle Neptun-Apotheke Bramfelder Chaussee 291 22177 Hamburg Tel.: 040 / 6391 7720 Fax.: 040 / 6391 7724 E-Mail: info@vdpp.de Internet: www.vdpp.de
Querschnittsbereich Nr. 1: Epidemiologie, Med. Biometrie und Med. Informatik
 Prävalenz Die Prävalenz ist eine Maßzahl für die Häufigkeit eines Zustandes zu einem bestimmten Zeitpunkt, z. B. der Anteil der Bevölkerung, der zu einem bestimmten Zeitpunkt übergewichtig ist oder der
Prävalenz Die Prävalenz ist eine Maßzahl für die Häufigkeit eines Zustandes zu einem bestimmten Zeitpunkt, z. B. der Anteil der Bevölkerung, der zu einem bestimmten Zeitpunkt übergewichtig ist oder der
Zur Anwendung bei Erwachsenen und Heranwachsenden ab 12 Jahren
 Gebrauchsinformation: Information für Patienten Aspecton Eukaps 100 mg magensaftresistente Weichkapseln Wirkstoff: Eukalyptusöl Zur Anwendung bei Erwachsenen und Heranwachsenden ab 12 Jahren Lesen Sie
Gebrauchsinformation: Information für Patienten Aspecton Eukaps 100 mg magensaftresistente Weichkapseln Wirkstoff: Eukalyptusöl Zur Anwendung bei Erwachsenen und Heranwachsenden ab 12 Jahren Lesen Sie
Pressemitteilung der EMEA vom in deutscher Übersetzung:
 Pressemitteilung der EMEA vom 9. 12. 2004 in deutscher Übersetzung: Außerordentliche Sitzung des CHMP zu Paroxetin und anderen selektiven Serotonin-Wiederaufnahmehemmern Der Ausschuss für Humanarzneimittel
Pressemitteilung der EMEA vom 9. 12. 2004 in deutscher Übersetzung: Außerordentliche Sitzung des CHMP zu Paroxetin und anderen selektiven Serotonin-Wiederaufnahmehemmern Der Ausschuss für Humanarzneimittel
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. Bezeichnung des Arzneimittels 2. Qualitative und quantitative Zusammensetzung Wirkstoffe: Natriumchlorid Wirkstoffe: Natriumchlorid Wirkstoffe: Natriumchlorid
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. Bezeichnung des Arzneimittels 2. Qualitative und quantitative Zusammensetzung Wirkstoffe: Natriumchlorid Wirkstoffe: Natriumchlorid Wirkstoffe: Natriumchlorid
Pflanzenschutzmittel Fakten statt Hysterie Gefahr, Risiko oder Sicherheit
 Pflanzenschutzmittel Fakten statt Hysterie Gefahr, Risiko oder Sicherheit Dr. Albert Bergmann Institut für Pflanzenschutzmittel Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Zusammenfassung
Pflanzenschutzmittel Fakten statt Hysterie Gefahr, Risiko oder Sicherheit Dr. Albert Bergmann Institut für Pflanzenschutzmittel Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Zusammenfassung
Erfahrungen zum Darmkrebs-Screening im Saarland Christa Stegmaier Krebsregister Saarland
 Erfahrungen zum Darmkrebs-Screening im Saarland Christa Stegmaier Krebsregister Saarland Inhalt Eckdaten zu Darmkrebs im Saarland Kampagne Saarland gegen Darmkrebs Studien und Projekte zum Darmkrebsscreening
Erfahrungen zum Darmkrebs-Screening im Saarland Christa Stegmaier Krebsregister Saarland Inhalt Eckdaten zu Darmkrebs im Saarland Kampagne Saarland gegen Darmkrebs Studien und Projekte zum Darmkrebsscreening
Mammographie-Screening in der Diskussion um Nutzen und Schaden: Was glauben wir und was wissen wir über den Nutzen?
 Urania Berlin 13.10. 2008 Mammographie-Screening in der Diskussion um Nutzen und Schaden: Was glauben wir und was wissen wir über den Nutzen? Dr. med. H.-J. Koubenec Mammasprechstunde im Immanuel Krankenhaus
Urania Berlin 13.10. 2008 Mammographie-Screening in der Diskussion um Nutzen und Schaden: Was glauben wir und was wissen wir über den Nutzen? Dr. med. H.-J. Koubenec Mammasprechstunde im Immanuel Krankenhaus
Bekanntmachung über die Registrierung und Zulassung von Arzneimitteln
 Bekanntmachung über die Registrierung und Zulassung von Arzneimitteln vom 6. Dezember 2010 Abwehr von Gefahren durch Arzneimittel, Stufe II 1. SSRI und TCA: Risiko von Knochenbrüchen 2. SSRI, Venlafaxin
Bekanntmachung über die Registrierung und Zulassung von Arzneimitteln vom 6. Dezember 2010 Abwehr von Gefahren durch Arzneimittel, Stufe II 1. SSRI und TCA: Risiko von Knochenbrüchen 2. SSRI, Venlafaxin
Nutzenbewertung und unabhängige Arzneimittelinformationen
 Gemeinsame Fortbildungs- und Informationsveranstaltung der AkdÄ und der AMK Berlin, 11. Juli 2015 Nutzenbewertung und unabhängige Arzneimittelinformationen Dr. med. Katrin Bräutigam Geschäftsführerin der
Gemeinsame Fortbildungs- und Informationsveranstaltung der AkdÄ und der AMK Berlin, 11. Juli 2015 Nutzenbewertung und unabhängige Arzneimittelinformationen Dr. med. Katrin Bräutigam Geschäftsführerin der
Abgrenzung klinischer Prüfungen Phase III und IV gegenüber nichtinterventionellen
 Abgrenzung klinischer Prüfungen Phase III und IV gegenüber nichtinterventionellen Studien Studien PHIII und IV versus Nichtinterventionelle Studien 1 Welche Aussagen sind richtig?? -1- Klinische Studien
Abgrenzung klinischer Prüfungen Phase III und IV gegenüber nichtinterventionellen Studien Studien PHIII und IV versus Nichtinterventionelle Studien 1 Welche Aussagen sind richtig?? -1- Klinische Studien
Wenn Sie sich nach 7 Tagen nicht besser oder gar schlechter fühlen, wenden Sie sich an Ihren
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Sidroga Kamillenblütentee Wirkstoff: Kamillenblüten Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Sidroga Kamillenblütentee Wirkstoff: Kamillenblüten Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Dossierbewertung A14-28 Version 1.0 Apixaban (neues Anwendungsgebiet) Nutzenbewertung gemäß 35a SGB V
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Apixaban (neues Anwendungsgebiet) gemäß 35a SGB V beauftragt. Die Bewertung
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Apixaban (neues Anwendungsgebiet) gemäß 35a SGB V beauftragt. Die Bewertung
Screening-Untersuchungen. Zu Risiken und Nebenwirkungen fragen Sie Ihren Statistiker. Fazit. XX. Februar 2015
 XX. Februar 2015 Bruxelles Airport 2011 Screening-Untersuchungen Zu Risiken und Nebenwirkungen fragen Sie Ihren Statistiker Gerhard Rogler, Klinik für Gastroenterologie und Hepatologie, UniversitätsSpital
XX. Februar 2015 Bruxelles Airport 2011 Screening-Untersuchungen Zu Risiken und Nebenwirkungen fragen Sie Ihren Statistiker Gerhard Rogler, Klinik für Gastroenterologie und Hepatologie, UniversitätsSpital
Frühe Nutzenbewertungen nach AMNOG: Einblicke in die aktuellen Verfahren und mögliche Auswirkungen für Ärzte und Patienten
 Frühe Nutzenbewertungen nach AMNOG: Einblicke in die aktuellen Verfahren und mögliche Auswirkungen für Ärzte und Patienten Arzneimittelmarktneuordnungsgesetz (AMNOG) 35a Bewertung des Nutzens von Arzneimitteln
Frühe Nutzenbewertungen nach AMNOG: Einblicke in die aktuellen Verfahren und mögliche Auswirkungen für Ärzte und Patienten Arzneimittelmarktneuordnungsgesetz (AMNOG) 35a Bewertung des Nutzens von Arzneimitteln
Anhang II. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen für die Genehmigungen für das Inverkehrbringen
 Anhang II Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen für die Genehmigungen für das Inverkehrbringen 12 Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung
Anhang II Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen für die Genehmigungen für das Inverkehrbringen 12 Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung
Epidemiologie der spezifischen Phobien
 Geisteswissenschaft Marcel Maier Epidemiologie der spezifischen Phobien Studienarbeit - Review Artikel - (benotete Seminararbeit) Epidemiologie der Spezifischen Phobien erstellt von Marcel Maier (SS 2005)
Geisteswissenschaft Marcel Maier Epidemiologie der spezifischen Phobien Studienarbeit - Review Artikel - (benotete Seminararbeit) Epidemiologie der Spezifischen Phobien erstellt von Marcel Maier (SS 2005)
Gebrauchsinformation: Information für Anwender. Euphrasia D3 Augentropfen Weleda
 1/5 Gebrauchsinformation: Information für Anwender Euphrasia D3 Augentropfen Weleda Wirkstoff: Euphrasia officinalis D3 Dilution Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
1/5 Gebrauchsinformation: Information für Anwender Euphrasia D3 Augentropfen Weleda Wirkstoff: Euphrasia officinalis D3 Dilution Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Verordnung über das Inverkehrbringen von Arzneimitteln ohne Genehmigung oder ohne Zulassung in Härtefällen (Arzneimittel- Härtefall-Verordnung - AMHV)
 Verordnung über das Inverkehrbringen von Arzneimitteln ohne Genehmigung oder ohne Zulassung in Härtefällen (Arzneimittel- Härtefall-Verordnung - AMHV) AMHV Ausfertigungsdatum: 14.07.2010 Vollzitat: "Arzneimittel-Härtefall-Verordnung
Verordnung über das Inverkehrbringen von Arzneimitteln ohne Genehmigung oder ohne Zulassung in Härtefällen (Arzneimittel- Härtefall-Verordnung - AMHV) AMHV Ausfertigungsdatum: 14.07.2010 Vollzitat: "Arzneimittel-Härtefall-Verordnung
Gebrauchsinformation: Information für Patienten. Aspecton Hustentropfen Flüssigkeit zum Einnehmen Thymiankraut-Dickextrakt
 Gebrauchsinformation: Information für Patienten Aspecton Hustentropfen Flüssigkeit zum Einnehmen Thymiankraut-Dickextrakt Für Erwachsene und Kinder ab 2 Jahren Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Patienten Aspecton Hustentropfen Flüssigkeit zum Einnehmen Thymiankraut-Dickextrakt Für Erwachsene und Kinder ab 2 Jahren Lesen Sie die gesamte Packungsbeilage sorgfältig
Die Regelung wurde eingeführt durch das GKV- Gesundheitsreformgesetz v mit Wirkung vom
 Exkurs Positivliste Der Gesetzgeber hatte in 33 a SGB V bestimmt, dass das BMGS ermächtigt wird, durch Rechtsverordnung eine Liste der verordnungsfähigen Arzneimittel zu erlassen. Die Regelung wurde eingeführt
Exkurs Positivliste Der Gesetzgeber hatte in 33 a SGB V bestimmt, dass das BMGS ermächtigt wird, durch Rechtsverordnung eine Liste der verordnungsfähigen Arzneimittel zu erlassen. Die Regelung wurde eingeführt
Dr. Johannes Knollmeyer Direktor Gesundheitspolitik Sanofi-Aventis Deutschland GmbH
 Versorgungsforschungskongress 2015 Versorgungforschung und klinische Forschung: Synergien und Alleinstellungsmerkmale Perspektive der pharmazeutischen Industrie Dr. Johannes Knollmeyer Direktor Gesundheitspolitik
Versorgungsforschungskongress 2015 Versorgungforschung und klinische Forschung: Synergien und Alleinstellungsmerkmale Perspektive der pharmazeutischen Industrie Dr. Johannes Knollmeyer Direktor Gesundheitspolitik
Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission
 Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission ass. iur. Jan Paus, LL.M. Rechtsreferent Ethik-Kommission der Ärztekammer Westfalen-Lippe und der Medizinischen Fakultät der WWU Münster
Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission ass. iur. Jan Paus, LL.M. Rechtsreferent Ethik-Kommission der Ärztekammer Westfalen-Lippe und der Medizinischen Fakultät der WWU Münster
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER VENODRIL Tropfen Wirkstoffe: Aesculus hippocastanum Dil. D6, Hamamelis virginiana Dil. D4, Melilotus officinalis Dil. D6, Silybum marianum Dil. D4 Lesen Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER VENODRIL Tropfen Wirkstoffe: Aesculus hippocastanum Dil. D6, Hamamelis virginiana Dil. D4, Melilotus officinalis Dil. D6, Silybum marianum Dil. D4 Lesen Sie
Educational Material und paralleler Vertrieb von Infobroschüren durch pu 73. Routinesitzung, Bonn, 28.11.2013
 Educational Material und paralleler Vertrieb von Infobroschüren durch pu 73. Routinesitzung, Bonn, 28.11.2013 Hintergrund zu Educational Material (EM) Möglicher Bestandteil der 2005 eingeführten Risikomanagement
Educational Material und paralleler Vertrieb von Infobroschüren durch pu 73. Routinesitzung, Bonn, 28.11.2013 Hintergrund zu Educational Material (EM) Möglicher Bestandteil der 2005 eingeführten Risikomanagement
Klinische Bewertung für Medizinprodukte inklusive Software
 Klinische Bewertung für Medizinprodukte inklusive Software 13. Linzer Forum Medizintechnik 5.10.2016 Bundesministerium für Gesundheit und Frauen, Wien Klinische Bewertung Aufgaben des Herstellers Teil
Klinische Bewertung für Medizinprodukte inklusive Software 13. Linzer Forum Medizintechnik 5.10.2016 Bundesministerium für Gesundheit und Frauen, Wien Klinische Bewertung Aufgaben des Herstellers Teil
Was ist anders bei Studien mit Medizinprodukten?
 Was ist anders bei Studien mit Medizinprodukten? CHRISTIAN WOLFLEHNER DR. ROBERT HEINZ & PARTNER GMBH CW RESEARCH & MANAGEMENT GMBH DACH SYMPOSIUM FREIBURG 07-MAR-2016 AMG versus MPG 2 Sehr viel Deckungsgleichheit
Was ist anders bei Studien mit Medizinprodukten? CHRISTIAN WOLFLEHNER DR. ROBERT HEINZ & PARTNER GMBH CW RESEARCH & MANAGEMENT GMBH DACH SYMPOSIUM FREIBURG 07-MAR-2016 AMG versus MPG 2 Sehr viel Deckungsgleichheit
Medikamente im Alter - Hilfe oder Problem?
 Medikamente im Alter - Hilfe oder Problem? Vortragsreihe Altersgerechte Zukunft Verein Graue Panther Bern Dr. med. Jon Lory, Chefarzt, Geriatrische Universitätsklinik Publikumsvortrag Medikamente 2014
Medikamente im Alter - Hilfe oder Problem? Vortragsreihe Altersgerechte Zukunft Verein Graue Panther Bern Dr. med. Jon Lory, Chefarzt, Geriatrische Universitätsklinik Publikumsvortrag Medikamente 2014
EMPFEHLUNG DES PAUL-EHRLICH-INSITUTES ZUR VORLAGE VON PERIODISCHEN SICHERHEITSBERICHTEN (Periodic Safety Update Report - PSUR)
 EMPFEHLUNG DES PAUL-EHRLICH-INSITUTES ZUR VORLAGE VON PERIODISCHEN SICHERHEITSBERICHTEN (Periodic Safety Update Report - PSUR) IM ZUSAMMENHANG MIT BLUTKOMPONENTEN nach 63i Abs. 4 AMG Allgemeines: Durch
EMPFEHLUNG DES PAUL-EHRLICH-INSITUTES ZUR VORLAGE VON PERIODISCHEN SICHERHEITSBERICHTEN (Periodic Safety Update Report - PSUR) IM ZUSAMMENHANG MIT BLUTKOMPONENTEN nach 63i Abs. 4 AMG Allgemeines: Durch
Kombinationsprodukte im Kontext der Revision der RL 93/42/EWG. Tamara Bauer
 Kombinationsprodukte im Kontext der Revision der RL 93/42/EWG Tamara Bauer Inhalt Definitionen Richtlinien Kombinationsprodukte 2 Fallbeispiele: Medizinprodukt/Arzneimittel Medizinprodukt/Arzneimittel
Kombinationsprodukte im Kontext der Revision der RL 93/42/EWG Tamara Bauer Inhalt Definitionen Richtlinien Kombinationsprodukte 2 Fallbeispiele: Medizinprodukt/Arzneimittel Medizinprodukt/Arzneimittel
Anhang III. Ergänzungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Ergänzungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage 20 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS [Der unten genannte Wortlaut
Anhang III Ergänzungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage 20 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS [Der unten genannte Wortlaut
Anforderungen an eine patientenorientierte Arzneimittelanwendungsforschung
 Anforderungen an eine patientenorientierte Arzneimittelanwendungsforschung Prof. Dr. Marion Schaefer Institut für Klinische Pharmakologie / Charité Universitätsmedizin Berlin 3. Eisensymposium / Basel
Anforderungen an eine patientenorientierte Arzneimittelanwendungsforschung Prof. Dr. Marion Schaefer Institut für Klinische Pharmakologie / Charité Universitätsmedizin Berlin 3. Eisensymposium / Basel
Pascorbin Das Power-Vitamin
 Pascorbin Das Power-Vitamin Vitamin des Lebens Vitamin C ist an vielen Vorgängen im menschlichen Körper beteiligt und erfüllt wichtige Aufgaben z. B. in folgenden Organen: Gehirn Augenlinse Herz Nieren
Pascorbin Das Power-Vitamin Vitamin des Lebens Vitamin C ist an vielen Vorgängen im menschlichen Körper beteiligt und erfüllt wichtige Aufgaben z. B. in folgenden Organen: Gehirn Augenlinse Herz Nieren
FACHINFORMATION. Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Ciclopirox WinthropNagellack 8 % 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 g wirkstoffhaltiger Nagellack enthält 80 mg Ciclopirox. Vollständige
FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Ciclopirox WinthropNagellack 8 % 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 g wirkstoffhaltiger Nagellack enthält 80 mg Ciclopirox. Vollständige
Epidemiologie des Iodmangels. Gruppe 1: Epidemiologie
 Gruppe 1: Epidemiologie 1. Beschreiben Sie mündlich die Aussagen der unten dargestellten Abbildung. Die Definition der Epidemiologie Die Beschreibung einer epidemiologischen Untersuchung Das Ziel einer
Gruppe 1: Epidemiologie 1. Beschreiben Sie mündlich die Aussagen der unten dargestellten Abbildung. Die Definition der Epidemiologie Die Beschreibung einer epidemiologischen Untersuchung Das Ziel einer
zur Verfügung gestellt von Gebrauchs.info
 Liebe Patientin! Lieber Patient! Bitte lesen Sie die folgende Gebrauchsinformation aufmerksam, weil sie wichtige Informationen darüber enthält, was Sie bei der Anwendung dieses Arzneimittels beachten sollen.
Liebe Patientin! Lieber Patient! Bitte lesen Sie die folgende Gebrauchsinformation aufmerksam, weil sie wichtige Informationen darüber enthält, was Sie bei der Anwendung dieses Arzneimittels beachten sollen.
FÜR RISIKOBEWERTUNG REACH. Verbessert das neue europäische Chemikalienrecht den gesundheitlichen Verbraucherschutz? BUNDESINSTITUT. Dr.
 BUNDESINSTITUT FÜR RISIKOBEWERTUNG REACH Verbessert das neue europäische Chemikalienrecht den gesundheitlichen Verbraucherschutz? Dr. Was ist REACH? Verordnung (EG) Nr. 1907/2006 des Europäischen Parlaments
BUNDESINSTITUT FÜR RISIKOBEWERTUNG REACH Verbessert das neue europäische Chemikalienrecht den gesundheitlichen Verbraucherschutz? Dr. Was ist REACH? Verordnung (EG) Nr. 1907/2006 des Europäischen Parlaments
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CORASAN Tropfen Wirkstoffe: Crataegus D1, Selenicereus grandiflorus (Cactus) D2, Digitalis purpurea D6, Strophanthus gratus D6. Lesen Sie die
Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CORASAN Tropfen Wirkstoffe: Crataegus D1, Selenicereus grandiflorus (Cactus) D2, Digitalis purpurea D6, Strophanthus gratus D6. Lesen Sie die
imedication Identifizierung und Überwachung von unerwünschten Arzneimittelwirkungen
 imedication Identifizierung und Überwachung von unerwünschten Arzneimittelwirkungen DI Manuela Plößnig, MSc Salzburg Research 21. November 2012 Heilen ist eine Frage der Zeit, mitunter aber auch eine Frage
imedication Identifizierung und Überwachung von unerwünschten Arzneimittelwirkungen DI Manuela Plößnig, MSc Salzburg Research 21. November 2012 Heilen ist eine Frage der Zeit, mitunter aber auch eine Frage
Wortlaut der für die Packungsbeilage vorgesehenen Angaben
 Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für den Anwender Presselin FE Mischung Homöopathisches Arzneimittel Zur Anwendung bei Kindern über 12 Jahren
Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für den Anwender Presselin FE Mischung Homöopathisches Arzneimittel Zur Anwendung bei Kindern über 12 Jahren
Baldrian-Dispert 45 mg überzogene Tabletten Wirkstoff: Baldrianwurzel-Trockenextrakt Zur Anwendung bei Heranwachsenden über 12 Jahren und Erwachsenen
 Gebrauchsinformation: Information für den Anwender Baldrian-Dispert 45 mg überzogene Tabletten Wirkstoff: Baldrianwurzel-Trockenextrakt Zur Anwendung bei Heranwachsenden über 12 Jahren und Erwachsenen
Gebrauchsinformation: Information für den Anwender Baldrian-Dispert 45 mg überzogene Tabletten Wirkstoff: Baldrianwurzel-Trockenextrakt Zur Anwendung bei Heranwachsenden über 12 Jahren und Erwachsenen
Anhang III. Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale
Anhang III Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale
Leitlinien des Berufsverbandes der Fachzahnärzte und Spezialisten (DGP) für Parodontologie e.v. für die Betreuung parodontal erkrankter Patienten
 Leitlinien des Berufsverbandes der Fachzahnärzte und Spezialisten (DGP) für Parodontologie e.v. für die Betreuung parodontal erkrankter Patienten Trotz aller Fortschritte in der Parodontologie bleibt die
Leitlinien des Berufsverbandes der Fachzahnärzte und Spezialisten (DGP) für Parodontologie e.v. für die Betreuung parodontal erkrankter Patienten Trotz aller Fortschritte in der Parodontologie bleibt die
Erivedge (Vismodegib): Wichtige Informationen für die sichere Anwendung, einschließlich Informationen zum Schwangerschaftsverhütungs-Programm
 Erivedge (Vismodegib): Wichtige Informationen für die sichere Anwendung, einschließlich Informationen zum Schwangerschaftsverhütungs-Programm Sehr geehrte Frau Doktor, sehr geehrter Herr Doktor, Dieses
Erivedge (Vismodegib): Wichtige Informationen für die sichere Anwendung, einschließlich Informationen zum Schwangerschaftsverhütungs-Programm Sehr geehrte Frau Doktor, sehr geehrter Herr Doktor, Dieses
PARENTERAL VE Infusionslösung
 Gebrauchsinformation und Fachinformation SERAG-WIESSNER GmbH & Co. KG Zum Kugelfang 8-12 95119 Naila PARENTERAL VE Infusionslösung Diese Packungsbeilage beinhaltet: 1. Was ist PARENTERAL VE und wofür wird
Gebrauchsinformation und Fachinformation SERAG-WIESSNER GmbH & Co. KG Zum Kugelfang 8-12 95119 Naila PARENTERAL VE Infusionslösung Diese Packungsbeilage beinhaltet: 1. Was ist PARENTERAL VE und wofür wird
KOMMENTAR ZUR LEITLINIE. Information und Beratung des Patienten bei der Abgabe von Arzneimitteln. Selbstmedikation
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung KOMMENTAR ZUR LEITLINIE Information und Beratung des Patienten bei der Abgabe von Arzneimitteln Selbstmedikation Stand der Revision: 06.05.2008
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung KOMMENTAR ZUR LEITLINIE Information und Beratung des Patienten bei der Abgabe von Arzneimitteln Selbstmedikation Stand der Revision: 06.05.2008
Anhang III. Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage
 Anhang III Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage Hinweis: Änderungen an der Fachinformation und der Packungsbeilage müssen unter Umständen im Anschluss durch
Anhang III Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage Hinweis: Änderungen an der Fachinformation und der Packungsbeilage müssen unter Umständen im Anschluss durch
Patientenratgeber. Disease-Management-Programme (DMP) Asthma bronchiale und COPD. Immer gut betreut. Was Sie über AOK-Curaplan wissen sollten
 Patientenratgeber Disease-Management-Programme (DMP) Asthma bronchiale und COPD Immer gut betreut Was Sie über AOK-Curaplan wissen sollten 2 Programme speziell für chronisch Kranke AOK-Curaplan ist ein
Patientenratgeber Disease-Management-Programme (DMP) Asthma bronchiale und COPD Immer gut betreut Was Sie über AOK-Curaplan wissen sollten 2 Programme speziell für chronisch Kranke AOK-Curaplan ist ein
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Daflon 500 mg Filmtabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Filmtablette enthält 500 mg gereinigte, mikronisierte
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Daflon 500 mg Filmtabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Filmtablette enthält 500 mg gereinigte, mikronisierte
Mirfulan. Salbe. täglich auftragen. Vitaminreiche Wund- und Heilsalbe
 1 Mirfulan Salbe Dosierung: Je nach Bedarf mehrmals täglich auftragen. Patienteninformation Bitte aufmerksam lesen! Vitaminreiche Wund- und Heilsalbe 2 Liebe Patientin, lieber Patient! Bitte lesen Sie
1 Mirfulan Salbe Dosierung: Je nach Bedarf mehrmals täglich auftragen. Patienteninformation Bitte aufmerksam lesen! Vitaminreiche Wund- und Heilsalbe 2 Liebe Patientin, lieber Patient! Bitte lesen Sie
Zusammenfassung der Merkmale des Arzneimittels. Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Virupos 30 mg/g Augensalbe 2. Qualitative und quantitative Zusammensetzung Wirkstoff: 1 g Salbe enthält Aciclovir 30 mg Die
Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Virupos 30 mg/g Augensalbe 2. Qualitative und quantitative Zusammensetzung Wirkstoff: 1 g Salbe enthält Aciclovir 30 mg Die
Wenn Sie sich nach 7 Tagen nicht besser oder gar schlechter fühlen, wenden Sie sich an Ihren
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Bronchoverde Hustenlöser 25 mg Granulat Granulat zur Herstellung einer Lösung zum Einnehmen Wirkstoff: Efeublätter-Trockenextrakt Pflanzliches Arzneimittel
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Bronchoverde Hustenlöser 25 mg Granulat Granulat zur Herstellung einer Lösung zum Einnehmen Wirkstoff: Efeublätter-Trockenextrakt Pflanzliches Arzneimittel
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels)
 FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Condrosulf 800 mg-tabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Tablette enthält 800 mg Natriumchondroitinsulfat
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Condrosulf 800 mg-tabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Tablette enthält 800 mg Natriumchondroitinsulfat
kontrolliert wurden. Es erfolgte zudem kein Ausschluss einer sekundären Genese der Eisenüberladung. Erhöhte Ferritinkonzentrationen wurden in dieser S
 5.8 Zusammenfassung Auf der Grundlage der dargestellten Ergebnisse dieser Studie erscheint die laborchemische Bestimmung der Transferrinsättigung zur Abklärung einer unklaren Lebererkrankung und Verdacht
5.8 Zusammenfassung Auf der Grundlage der dargestellten Ergebnisse dieser Studie erscheint die laborchemische Bestimmung der Transferrinsättigung zur Abklärung einer unklaren Lebererkrankung und Verdacht
Qualitätsprüfungen der Indikationsstellung in der vertragsärztlichen Versorgung
 Qualitätsprüfungen der Indikationsstellung in der vertragsärztlichen Versorgung Per Zufall oder nach Auffälligkeiten? 8. Qualitätssicherungskonferenz des G-BA 28. September 2016 Dr. Horst Schuster, GKV-SV
Qualitätsprüfungen der Indikationsstellung in der vertragsärztlichen Versorgung Per Zufall oder nach Auffälligkeiten? 8. Qualitätssicherungskonferenz des G-BA 28. September 2016 Dr. Horst Schuster, GKV-SV
