2. Materialien Prüfsubstanzen
|
|
|
- Jasmin Schwarz
- vor 6 Jahren
- Abrufe
Transkript
1 6 2. Materialien 2.1. Prüfsubstanzen Bei allen Prüfsubstanzen handelt es sich um polyanionische Verbindungen, welchen keine totale Molekularstruktur zugeordnet werden kann. Die untersuchten Makromoleküle sind Stoffe, die in Lösung einer Strukturwandlung bis hin zu Fragmentierungen unterliegen können. Dies ist ein Vorgang, der v.a. stark von Milieuänderungen abhängig ist und eine Erklärung für die relativ schwierige Molekulargewichtsbestimmung darstellt. Trotz ihres polydispersen Charakters besitzen alle Substanzen typische physikalische, chemische und z.t. biologische Eigenschaften. Für die chemische Reaktivität sind hauptsächlich sauerstoffhaltige Gruppen wie Carboxyl- und Phenolgruppen, schwefelhaltige Gruppen wie Sulfatgruppen und stickstoffhaltige Gruppen wie Aminogruppen verantwortlich. Eine genaue Charakterisierung im Sinne einer umfassenden physikalisch-chemischen Stoffkenntnis ist aufgrund dieser polydispersen Struktur kaum möglich, ebenso wie die Angabe eines Molekulargewichtes bei einzelnen Substanzen. Der Schlüssel zum Verständnis der Reaktionen solcher Substanzen liegt deshalb eher in den physikalischen, chemischen und biologischen Funktionalitäten, die den einzelnen Strukturbereichen zukommen, als in der genauen Kenntnis der Molekularstruktur (Frimmel et al., 1990; Hayes et al., 1989) Natürlich vorkommende Huminsäuren Natrium-Humat (NaHS, Ch.B.: I-IV/80, MG Da) ist das Salz einer natürlich vorkommenden Huminsäure aus dem Küstenhochmoor (Dierhagen, Mecklenburg-Vorpommern). Sie wurde nach einer von Klöcking et al. (1977) beschriebenen Methode am Institut für Medizinische Mikrobiologie der Medizinischen Akademie Erfurt isoliert. Es handelt sich um ein braunes, wasserlösliches Pulver. Humussäure-Natriumsalz (Aldrich HS, Lot: ) ist eine dunkelbraun gefärbte und wasserlösliche Huminsäure, die von Sigma Aldrich Chemie GmbH, D Steinheim, bezogen wurde. Die Isolierung dieser HS erfolgte aus Braunkohle.
2 Synthetische Huminsäure-ähnliche Polymere Kaffesäureoxidationsprodukt (NaKOP, Ch.B.: 409/85, MG 6500 Da) wurde hergestellt durch Lösen von Kaffeesäure in verdünnter NaOH, umsetzen mit Periodat bei ph 9,0, erwärmen auf 80 C und abkühlen über Nacht. Durch fällen mit einem Eisessig/Ethylacetat-Gemisch (1:5), filtrieren des Niederschlages und anschließendem Trocknen wurde ein sehr gut wasserlösliches Produkt erhalten. Die Synthese der Substanz fand am Institut für Medizinische Mikrobiologie der Medizinischen Akademie Erfurt statt (Klöcking et al., 1983; Hänninen et al., 1987). Melanoidine Melanoidine sind synthetisch hergestellte polyanionische Verbindungen mit huminsäureähnlichen Eigenschaften. Zur Synthese bedient man sich der Melanoidinreaktion, die nach ihrem Erfinder auch Maillard-Reaktion genannt wird und als eine Möglichkeit für die natürliche Bildungsweise von Huminsäuren angesehen wird (Pompe et al., 1996). Beide Substanzen wurden am Institut für Radiochemie des Forschungszentrums Rossendorf e.v. synthetisiert (Tab.1). Tabelle 1: Synthese- und Analysendaten der Melanoidine Typ M1 und Typ M42 Typ M1 M42 Synthesecharge M100A 81 Zucker Xylose Xylose Aminosäure Glycin + Phenylalanin Glutaminsäure Analysendaten Elementaranalyse: C/H/N (%) 64,69/ 5,28/ 5,1 58,4/ 4,9/ 4,5 COOH-Gruppen (meq/g) 1,37 4,1 phenolische OH-Gruppen (meq/g) 2,45 2,3 ROS-Modellsubstanzen Die durchgeführten Synthesen beruhen auf der Oxidation von Phenolen (Eller et al., 1920) wie Hydrochinon mit Aminosäuren im alkalischen Medium bei Raumtemperatur. Als Oxidationsmittel wurde bevorzugt Luftsauerstoff in Na 2 CO 3 -Lösung verwendet (Herdering, 1998). Genannte Methode ahmt die Bildungsbedingungen von natürlichen
3 8 Huminsäuren nach und vermeidet die Einführung unerwünschten Stickstoffs aus anderen Bereichen. Die untersuchten Substanzen wurden vom Institut für Anorganische und Angewandte Chemie der Universität Hamburg bereitgestellt (Tab.2). Tabelle 2: Synthese- und Analysendaten der ROS-Substanzen HS 5, HS 130 und HS 136 Typ HS 5 HS 130 HS 136 Aminosäure Glycin L-Glutaminsäure L Lysin Phenolderivat Hydrochinon Hydrochinon Hydrochinon Elementaranalyse C/H/N (%) O (%) Cl (%) 54,9/ 3,26/ 3,67 36, ,18/3,5/2,54 37,65 0 Gesamtsäure (meq/g) 9,6 10,0 8,5 COOH-Gruppen (meq/g) 4,3 5,2 5,1 50,99/4,68/6,55 29,5 7, Sulfatierte Hyaluronsäurederivate In die Versuche mit einbezogen wurden weiterhin zwei hochsulfatierte Hyaluronsäurederivate (HYA DS 48 und HYA PS 10A) welche am Hans-Knöll Institut in Jena synthetisiert wurden (Tab.3). Beide Substanzen wurden nach einem Verfahren hergestellt, dass es gestattet, vollständig homogene Sulfatierungsreaktionen durchzuführen. Die Prozessführung wurde durch die Wahl eines geeigneten Sulfatierungsreagenzes, dessen eingesetzter Konzentration, einer günstigen Reaktionstemperatur und der Reaktionszeit so gesteuert, dass der Sulfatierungsgrad wahlweise eingestellt werden konnte (Möller et al., 1998; Tan et al., 1990; Wada et al., 1994). Ziel dabei war es, einen Sulfatierungsgrad höher 3,5 pro Disaccharideinheit des Hyaluronsäuremoleküles zu erreichen. Der Schwefelgehalt wurde mittels elementaranalytischer und NMR-spektroskopischer Untersuchungen bestimmt.
4 9 Tabelle 3: Synthese- und Analysendaten der sulfatierten Hyaluronsäurederivate HYA PS 10A und HYA DS 48 HYA DS 48 HYA PS 10A Molekulargewicht Da Da Ammoniumhyaluronat-Herstellung aus Tributylamin Tributylamin Sulfatierungsreagenz SO 3 /DMF SO 3 /Pyridin Reaktionstemperatur 4h: 45min bei 0 C dann 3,15h bei RT Reaktionszeit 4,15h 4h Schwefelgehalt (%) 9,68 12,24 Eisbad (3-4 C) Vergleichssubstanzen Als Vergleichssubstanzen wurde zum einen unfraktioniertes Heparin und zum anderen Pentosanpolysulfat als sog. Heparinoid verwendet. Bei beiden Substanzen handelt es sich um Stoffe mit einem hohen Gehalt an negativ geladenen funktionellen Gruppen, die klinisch geprüft sind und therapeutisch zum Einsatz kommen. Die Versuche wurden mit den reinen Wirkstoffen durchgeführt. Heparin-Natrium Lot. 1652/47, Aktivität: 134E/m ex-lung Pentapharm AG, CH-4002 Basel Pentosanpolysulfat (SP 54 ) bene-arzneimittel GmbH, als reiner Wirkstoff D München, CH.B.: B Physiologische Enzyme, Substrate und Inhibitoren Thrombin 240 NIH-U/Fl, Ch.B.: , MG Da, gefriergetrocknet vom Rind Feinchemie GmbH, D Sebnitz Prothrombin 51,1 U/mg gefriergetrockneter Feststoff (= 137 U/mg Eiweiß), MG Da, human ICN Biomedical, Ohio Faktor Xa human, 71nkat/Fl, Lot-Ch.B.:991256, MG Da GmbH,
5 10 Protein C human, MG Da, 0,10 mg/fl. lyophilisiertes Pulver, Lot: HPC 1590AL, Lot: HPC 1740PAL Haemochrom Diagnostica GmbH, Aktiviertes Protein C human, 0,10 mg/fl. lyophilisiertes Pulver, Lot: APC 1630PAL GmbH, STACLOT VII-rTF - Reagenz 1: konzentrierter Puffer (R1) - Reagenz 2: gefriergetrocknetes Humanplasma, Faktor VII- frei (R2) - Reagenz 3: rekombinanter löslicher tissue Faktor (rstf) und Phospholipide, gefriergetrocknet (R3) - Reagenz 4: rekombinanter humaner Faktor VIIa, gefriergetrocknet (R4) Roche Diagnostics GmbH, Mannheim Fibrinogen human, Ch.B.: , MG Da, 1g Lyophilisat = 380mg Protein (davon 325 mg Fibrinogen) Impfstoffwerk Dessau- Tornau Anti- thrombin III 10 IU/Fl. Ch.B.: X2860, MG Da, gefriergetrocknet GmbH, Poolplasma aus Humancitratblut Plasmapool von 6-9 Spendern, DRK Blutspendedienst Thüringen, Institut für Transfusionsmedizin, D Erfurt Protein C Mangelplasma Ch.B.: 723/011, PC-Spiegel<1%, gefriergetrocknet Haemochrom Diagnostica GmbH,
6 Nichtphysiologische Inhibitoren und Aktivatoren Hirudin rekombinant, ATU/mL (ATU= Antithrombin-Unit) Sigma Aldrich Chemie GmbH, D Taufkirchen Aprotinin Trasylol, Ch.B.: TN 371, MG 6200 Da, 1 Ampulle= KIE/5mL (KIE= Kallikrein-Inhibierungs- Einheit) Bayer AG/ Leverkusen Protaminsulfat Ch.B.: Merck, Darmstadt Pefabloc FG Fibrin-Polymerisationsinhibitor, Lot.: , MG 485,5 Da, chemische H-Gly-Pro-Arg-Pro-OH. AcOH LOXO GmbH, D Dossenheim Protac MG Da, 1,2 U/Fl., Ch.B.: , 3 U/Fl., Lot.: / GmbH, Loxo GmbH, D Dossenheim Echis Carinatus Schlangengift Lot: 65H0657 Sigma Aldrich Chemie GmbH, D Steinheim Streptokinase MG Da, Ch.B.: , IE/Ampulle Arzneimittelwerk Dresden 2.4. Chromogene Peptidsubstrate S-2238 (thrombinselektiv) MG 625,6 Da, Lot.: N , chemische H-D-Phe-Pip-Arg-pNA. 2HCl Haemochrom Diagnostica GmbH,
7 12 Th-1 (thrombinselektiv) S-2765 (FXa-selektiv) MG 624,7 Da, Lot.: TH03, chemische 2AcOH. H-D-CHG-Ala-Arg-pNA MG 714,6 Da, Lot.:N , chemische N-α-D-Arg-Gly-Arg-pNA. 2HCl Immuno GmbH, D-6900 Heidelberg GmbH, D Essen FXa-1 (FXa-selektiv) MG 622,7 Da, Lot.:FX02, chemische AcOH. CH 3 OCO-D-CHA-Gly-Arg-pNA Firma Immuno GmbH, D-6900 Heidelberg S-2366 (APC-selektiv) MG 539 Da, Lot.:N , chemische Glu-Pro-Arg-pNA. HCl GmbH, D Essen PK-1 (kallikreinselektiv) MG 652,8 Da, Lot.:PK01, chemische 2 AcOH. H-D-But-CHA-Arg-pNA Firma Immuno GmbH, D-6900 Heidelberg 2.5. Chemikalien und weitere Reagenzien Bovines Serum Albumin (BSA) Feinbiochemica GmbH, Heidelberg Cephalinsuspension aus einem Testkit zur Bestimmung der aptt Roche Diagnostics GmbH, Mannheim Essigsäure (CH 3 COOH) Laborchemie, Apolda Imidazol Feinbiochemica GmbH, Heidelberg Natriumazid (NaN 3 ) Sprengstoffwerk, Schönebeck Natriumchlorid (NaCl) Carl Roth GmbH, Karlsruhe Natriumhydroxid (NaOH) Klinikumsapotheke, Erfurt
8 13 Polyethylenglykol 6000 (PEG 6000) Sigma Aldrich Chemie GmbH, Steinheim Salzsäure (HCl) Carl Roth GmbH, Karlsruhe Puffer 1 (Tris-Imidazol-Puffer ph 7,4) Tris 0,03 mol/l, Imidazol 0,03 mol/l, NaCl 0,022 mol/l Puffer 2 (Tris-NaCl-BSA-Puffer ph 7,4) Tris 50mmol/L, NaCl 0,15 mol/l, 0,2% BSA, 0,5% PEG 6000 Puffer 3 Puffer 2, Ca 2+ 9 mmol/l Tris-(hydroxymethyl)-aminomethan (Tris) Fluka Chemie AG, Buchs/ Schweiz 2.6. Geräte und Hilfsmittel Analysenwaage AC 210S-OD1 Sartorius, Göttingen Auslaufpipetten 1, 5 und 10 ml einzeln Nunc, Wiesbaden Easy Reader EAR 340 AT SLT Labinstruments, Crailsheim Einmalkanülen Sterican 1,20x40mm B. Braun Melsungen AG Koagulometer CL 4, Behuk Elektronik Bender & Hobein, München Küvettenriegel und Kugeln Immuno GmbH, Heidelberg Megafuge 1,0R Heraeus, Hanau Mikrotiterplatten: Nunclon 96, steril,flachboden 86x127mm Nunc GmbH, Wiesbaden
9 14 ph- Meter CG840 Schott-Geräte GmbH, Jena Pipettenspitzen 100µL, 1000µL Eppendorf GmbH, Hamburg Pipettierhilfe Sarpette Saarstedt, Nürnberg Reinraumwerkbank Elektromat Dresden, Dresden Zentrifugenröhrchen aus Polystyren 17x100mm, 14mL Becton-Dickinson, Heidelberg
D i s s e r t a t i o n
 Einfluss von sulfatierten Hyaluronsäuren, natürlichen Huminsäuren und synthetischen Huminsäure-ähnlichen Polymeren auf das Gerinnungssystem in vitro D i s s e r t a t i o n zur Erlangung des akademischen
Einfluss von sulfatierten Hyaluronsäuren, natürlichen Huminsäuren und synthetischen Huminsäure-ähnlichen Polymeren auf das Gerinnungssystem in vitro D i s s e r t a t i o n zur Erlangung des akademischen
D i s s e r t a t i o n
 Einfluss von sulfatierten Hyaluronsäuren, natürlichen Huminsäuren und synthetischen Huminsäure-ähnlichen Polymeren auf das Gerinnungssystem in vitro D i s s e r t a t i o n zur Erlangung des akademischen
Einfluss von sulfatierten Hyaluronsäuren, natürlichen Huminsäuren und synthetischen Huminsäure-ähnlichen Polymeren auf das Gerinnungssystem in vitro D i s s e r t a t i o n zur Erlangung des akademischen
2 Materialien. 2.1 Testsubstanzen
 2 Materialien 2.1 Testsubstanzen 2.1.1 Sulfatierte Hyaluronsäuren Die in den Versuchen verwendeten sulfatierten Hyaluronsäuren (Abb. 4) werden folgendermaßen synthetisiert: Durch Überführung der Hyaluronsäure
2 Materialien 2.1 Testsubstanzen 2.1.1 Sulfatierte Hyaluronsäuren Die in den Versuchen verwendeten sulfatierten Hyaluronsäuren (Abb. 4) werden folgendermaßen synthetisiert: Durch Überführung der Hyaluronsäure
6. Zusammenfassung Hyaluronsäuren Huminsäuren HS-ähnliche Polymere
 143 6. Zusammenfassung Thrombo-embolische Erkrankungen gehören in den westlichen Industrienationen bis heute zu den häufigsten Todesursachen. Für die Prophylaxe dieser Erkrankungen stehen neben Thrombozytenaggregationshemmstoffen
143 6. Zusammenfassung Thrombo-embolische Erkrankungen gehören in den westlichen Industrienationen bis heute zu den häufigsten Todesursachen. Für die Prophylaxe dieser Erkrankungen stehen neben Thrombozytenaggregationshemmstoffen
8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung
 8. Anhang 8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung 1.) Spüllösung (modifizierte PBS-Lösung) modifizierte PBS-Lösung 500
8. Anhang 8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung 1.) Spüllösung (modifizierte PBS-Lösung) modifizierte PBS-Lösung 500
Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6
 Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6 Säure-Base-Gleichgewichte E 1. Sie möchten 200 ml einer Pufferlösung mit ph = 5.00 mit dem Säure-Base-Paar Essigsäure
Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6 Säure-Base-Gleichgewichte E 1. Sie möchten 200 ml einer Pufferlösung mit ph = 5.00 mit dem Säure-Base-Paar Essigsäure
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7
 AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
Campherchinon (teuer)
 chiral pool alle chiralen, nicht racemischen Verbindungen aturstoffe - müssen enantiomerenrein verfügbar sein - müssen leicht und rein isolierbar sein dann sind diese billig im andel verfügbar alle Verbindungen,
chiral pool alle chiralen, nicht racemischen Verbindungen aturstoffe - müssen enantiomerenrein verfügbar sein - müssen leicht und rein isolierbar sein dann sind diese billig im andel verfügbar alle Verbindungen,
HA + B A - + HB + Säuren und Basen. Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor!
 Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
15. Aminosäuren, Peptide und Proteine
 15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
3. Methoden Gerinnungsanalysen mit dem Koagulometer CL 4
 15 3. Methoden 3.1. Gerinnungsanalysen mit dem Koagulometer CL 4 Allgemeines Meßprinzip für Gerinnungs- und Lyseuntersuchungen Untersuchungen mit dem Koagulometer CL 4 erlauben eine halbautomatisierte
15 3. Methoden 3.1. Gerinnungsanalysen mit dem Koagulometer CL 4 Allgemeines Meßprinzip für Gerinnungs- und Lyseuntersuchungen Untersuchungen mit dem Koagulometer CL 4 erlauben eine halbautomatisierte
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
DOAKs Direkte orale Antikoagulantien
 DOAKs Direkte orale Antikoagulantien Reagenzien, Kalibratoren und Kontrollen zur Bestimmung von Heparin, heparinähnlichen Antikoagulantien, Xa Inhibitoren und direkten Thrombin Inhibitoren DOAKs Direkte
DOAKs Direkte orale Antikoagulantien Reagenzien, Kalibratoren und Kontrollen zur Bestimmung von Heparin, heparinähnlichen Antikoagulantien, Xa Inhibitoren und direkten Thrombin Inhibitoren DOAKs Direkte
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
Die Substratspezifität der Enzyme Trypsin und Chymotrypsin
 Die Substratspezifität der Enzyme Trypsin und Chymotrypsin Einleitung Die Proteine Trypsin und Chymotrypsin sind Enzyme, die im Magen von Säugetieren vorkommen und die Hydrolyse von Peptidbindungen katalysieren.
Die Substratspezifität der Enzyme Trypsin und Chymotrypsin Einleitung Die Proteine Trypsin und Chymotrypsin sind Enzyme, die im Magen von Säugetieren vorkommen und die Hydrolyse von Peptidbindungen katalysieren.
Endersch, Jonas Praktikum Allgemeine Chemie 2, Saal G1, Platz 53
 Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
RESOLUTION OIV-OENO gestützt auf die Arbeiten der Expertengruppen Spezifikationen önologischer Erzeugnisse und Mikrobiologie
 RESOLUTION OIV-OENO 496-2013 MONOGRAPHIE ÜBER HEFEAUTOLYSATE DIE GENERALVERSAMMLUNG, gestützt auf Artikel 2 Absatz iv des Übereinkommens vom 3. April 2001 zur Gründung der Internationalen Organisation
RESOLUTION OIV-OENO 496-2013 MONOGRAPHIE ÜBER HEFEAUTOLYSATE DIE GENERALVERSAMMLUNG, gestützt auf Artikel 2 Absatz iv des Übereinkommens vom 3. April 2001 zur Gründung der Internationalen Organisation
Selbsteinschätzungstest zum Vorkurs Anorganische Chemie
 WS 15/16 1/7 Selbsteinschätzungstest zum Vorkurs Anorganische Chemie Liebe Studierende! Der Vorkurs frischt Ihr Schulwissen auf, vermittelt aber NICHT die späteren Studieninhalte. Die Inhalte des Vorkurses
WS 15/16 1/7 Selbsteinschätzungstest zum Vorkurs Anorganische Chemie Liebe Studierende! Der Vorkurs frischt Ihr Schulwissen auf, vermittelt aber NICHT die späteren Studieninhalte. Die Inhalte des Vorkurses
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden?
 41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden? A) Ca B) C C) F D) Na 42. Steinsalz löst sich in Wasser, A) weil beide Ionen Hydrathüllen bilden können B) es eine Säure
41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden? A) Ca B) C C) F D) Na 42. Steinsalz löst sich in Wasser, A) weil beide Ionen Hydrathüllen bilden können B) es eine Säure
Analytische Chemie. B. Sc. Chemieingenieurwesen. 14. März Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
7 Anhang. Tabelle I: Zusammensetzung der Restriktionsansätze.
 7 Anhang Tabelle I: Zusammensetzung der Restriktionsansätze. Reagenz Konzentration Volumen je Endkonzentration der Stammlösung Reaktionansatz Reaktionspuffer 10x NEB-Puffer 2 1.50 µl 1x MseI 4 U/µl 0.30
7 Anhang Tabelle I: Zusammensetzung der Restriktionsansätze. Reagenz Konzentration Volumen je Endkonzentration der Stammlösung Reaktionansatz Reaktionspuffer 10x NEB-Puffer 2 1.50 µl 1x MseI 4 U/µl 0.30
Aufgabe 1: Geben Sie die korrespondierenden Basen zu folgenden Verbindungen an: a) H 3 PO 4 b) H 2 PO 4
 Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Martin Raiber Chemie Protokoll Nr Gruppe 2 (Schrankseite) Untersuchung von Glycin
 Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
2 Materialien und Methodik
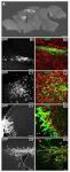
 2 Materialien und Methodik 2.1 Geräte Adhäsivobjektträger; MERCK, Darmstadt Brutschrank INCO 2; MEMMERT, Schwabach Cydok Bildanalysesystem; FIRMA C. H. HILGES, Königswinter Deckglas; TECHNISCHES GLAS ILMENAU
2 Materialien und Methodik 2.1 Geräte Adhäsivobjektträger; MERCK, Darmstadt Brutschrank INCO 2; MEMMERT, Schwabach Cydok Bildanalysesystem; FIRMA C. H. HILGES, Königswinter Deckglas; TECHNISCHES GLAS ILMENAU
Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum WS 2002/
 Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum WS 2002/2003 22.04.2003 Name: Vorname: Matrikelnummer: Fachsemester: Punkte: Note: Frage 1 Welche Flammenfärbung zeigen folgende
Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum WS 2002/2003 22.04.2003 Name: Vorname: Matrikelnummer: Fachsemester: Punkte: Note: Frage 1 Welche Flammenfärbung zeigen folgende
Vorlesung Hämostaseologie WS 2015/16
 Universitätsklinikum Düsseldorf Vorlesung Hämostaseologie WS 2015/16 Teil 2 (Thrombophilie) Dr. med. Derik Hermsen, OA Zentrallabor, Hämostaseologe Geschätztes relatives venöses Thromboserisiko Normalbevölkerung
Universitätsklinikum Düsseldorf Vorlesung Hämostaseologie WS 2015/16 Teil 2 (Thrombophilie) Dr. med. Derik Hermsen, OA Zentrallabor, Hämostaseologe Geschätztes relatives venöses Thromboserisiko Normalbevölkerung
GEBRAUCHSANLEITUNG. Lowry Assay Kit. Kit für die Proteinkonzentrationsbestimmung. (Kat.-Nr )
 GEBRAUCHSANLEITUNG Lowry Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39236) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG Lowry Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39236) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
CHEMISCHE CHARAKTERISIERUNG VON LIGNINEN AUS DEM ACETOSOLV-VERFAHREN UND DEREN UMSETZUNG ZU PHENOL-FORMALDEHYD-HARZEN DISSERTATION
 4S2*?-- CHEMISCHE CHARAKTERISIERUNG VON LIGNINEN AUS DEM ACETOSOLV-VERFAHREN UND DEREN UMSETZUNG ZU PHENOL-FORMALDEHYD-HARZEN DISSERTATION zur Erlangung des Doktorgrades an der Universität Hamburg Fachbereich
4S2*?-- CHEMISCHE CHARAKTERISIERUNG VON LIGNINEN AUS DEM ACETOSOLV-VERFAHREN UND DEREN UMSETZUNG ZU PHENOL-FORMALDEHYD-HARZEN DISSERTATION zur Erlangung des Doktorgrades an der Universität Hamburg Fachbereich
CHEMIE KAPITEL 4 SÄURE-BASE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner Samstag, Uhr Allgemeine Chemie
 Seite 1 von 6 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner 25.02. 04.03.2017 Samstag, 25.02.17 15.00 17.00 Uhr Allgemeine Chemie Mittwoch,
Seite 1 von 6 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner 25.02. 04.03.2017 Samstag, 25.02.17 15.00 17.00 Uhr Allgemeine Chemie Mittwoch,
Lösungen, Salze, Ionen und Elektrolyte
 Lösungen, Salze, Ionen und Elektrolyte Lösungen Eine Lösung ist in der Chemie ein homogenes Gemisch, das aus zwei oder mehr chemisch reinen Stoffen besteht. Sie enthält einen oder mehrere gelöste Stoffe
Lösungen, Salze, Ionen und Elektrolyte Lösungen Eine Lösung ist in der Chemie ein homogenes Gemisch, das aus zwei oder mehr chemisch reinen Stoffen besteht. Sie enthält einen oder mehrere gelöste Stoffe
Name: Punktzahl: von 57 Note:
 Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Nachklausur zum Praktikum Allgemeine und Anorganische Chemie für Naturwissenschaftler Sommersemester 2007
 Nachklausur zum Praktikum Allgemeine und Anorganische Chemie für Naturwissenschaftler Sommersemester 2007 Name: Matr. Nr.: Studiengang (Bachelor/Diplom): Ergebnis: Punkte/Note: Aufg 1 2 3 4 5 6 7 8 9 10
Nachklausur zum Praktikum Allgemeine und Anorganische Chemie für Naturwissenschaftler Sommersemester 2007 Name: Matr. Nr.: Studiengang (Bachelor/Diplom): Ergebnis: Punkte/Note: Aufg 1 2 3 4 5 6 7 8 9 10
5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp)
 8 Anhang 8.1 Chemikalien und Reagenzien Bromphenolblau Bromma, Schweden 5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp) Invitrogen TM, Karlsruhe Ethanol (RNase-frei)
8 Anhang 8.1 Chemikalien und Reagenzien Bromphenolblau Bromma, Schweden 5,6- Carboxy- Rhodamin (Rox) TIB MolBiol, Berlin Desoxynukleosidtriphosphat (dntp) Invitrogen TM, Karlsruhe Ethanol (RNase-frei)
3,58 g 0,136 g. ad 100 ml
 9 Anhang 9.1 Rezepturen der Puffer und Lösungen 9.1.1 Vorbereitung der Proben zur Extraktion Coon s-puffer (0,1 M, ph 7,2-7,6) Na 2 HPO 4 x 12 H 2 O KH 2 PO 4 Aqua dest. 3,58 g 0,136 g 8,77 g 9.1.2 Aufbereitung
9 Anhang 9.1 Rezepturen der Puffer und Lösungen 9.1.1 Vorbereitung der Proben zur Extraktion Coon s-puffer (0,1 M, ph 7,2-7,6) Na 2 HPO 4 x 12 H 2 O KH 2 PO 4 Aqua dest. 3,58 g 0,136 g 8,77 g 9.1.2 Aufbereitung
SÄUREN, BASEN, ph-wert
 8. Einheit: SÄUREN, BASEN, ph-wert Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 23 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Säuren, Basen, ph-wert.. können Sie die Begriffe Säure und Base in
8. Einheit: SÄUREN, BASEN, ph-wert Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 23 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Säuren, Basen, ph-wert.. können Sie die Begriffe Säure und Base in
Das Arzneimittel Blut
 Das Arzneimittel Blut Prof. Dr. med. H. Eichler Institut für Klinische Hämostaseologie und Transfusionsmedizin Medizinische Fakultät der Universität des Saarlandes Serologische Ära der Transfusionsmedizin
Das Arzneimittel Blut Prof. Dr. med. H. Eichler Institut für Klinische Hämostaseologie und Transfusionsmedizin Medizinische Fakultät der Universität des Saarlandes Serologische Ära der Transfusionsmedizin
Chloro(triphenylphosphin)gold(I)
 raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
Analytische Chemie. B. Sc. Chemieingenieurwesen. 22. September 2017, 13 bis 16 Uhr. Dr. Stephanie Möller & Prof. Dr. Thomas Jüstel.
 Analytische Chemie B. Sc. Chemieingenieurwesen 22. September 2017, 13 bis 16 Uhr Dr. Stephanie Möller & Prof. Dr. Thomas Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des
Analytische Chemie B. Sc. Chemieingenieurwesen 22. September 2017, 13 bis 16 Uhr Dr. Stephanie Möller & Prof. Dr. Thomas Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des
Säuren und Basen. Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17.
 Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
Analytische Chemie. B. Sc. Chemieingenieurwesen. 19. März Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 19. März 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
Analytische Chemie B. Sc. Chemieingenieurwesen 19. März 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
DIREKTE ORALE ANTIKOAGULANZIEN UND DEREN EINFLUSS AUF GERINNUNGSANALYSEN
 DIREKTE ORALE ANTIKOAGULANZIEN UND DEREN EINFLUSS AUF GERINNUNGSANALYSEN // EINFLUSS DIREKTER ORALER ANTIKOAGULANZIEN AUF GERINNUNGSANALYSEN DARUM GEHT S Direkte ( neue ) orale Antikoagulanzien können
DIREKTE ORALE ANTIKOAGULANZIEN UND DEREN EINFLUSS AUF GERINNUNGSANALYSEN // EINFLUSS DIREKTER ORALER ANTIKOAGULANZIEN AUF GERINNUNGSANALYSEN DARUM GEHT S Direkte ( neue ) orale Antikoagulanzien können
SICHERHEITSDATENBLATT
 SICHERHEITSDATENBLATT 1. PRODUKTBEZEICHNUNG: Name: ZYMUPHEN MP-AKTIVITÄT Artikelnummer: 521096 Kitkomponenten: Hersteller: - 1 ELISA Mikrotiterplatte im verschlossenen Aluminiumbeutel - 2 Flaschen mit
SICHERHEITSDATENBLATT 1. PRODUKTBEZEICHNUNG: Name: ZYMUPHEN MP-AKTIVITÄT Artikelnummer: 521096 Kitkomponenten: Hersteller: - 1 ELISA Mikrotiterplatte im verschlossenen Aluminiumbeutel - 2 Flaschen mit
Lösung Sauerstoff: 1s 2 2s 2 2p 4, Bor: 1s 2 2s 2 2p 1, Chlor: 1s 2 2s 2 2p 6 3s 2 3p 5 Neon: 1s 2 2s 2 2p 6
 1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
Analytische Chemie. B. Sc. Chemieingenieurwesen. 6. Juli 2016, Uhr. Prof. Dr. T. Jüstel & Stephanie Möller M.Sc.
 Analytische Chemie B. Sc. Chemieingenieurwesen 6. Juli 2016, 10.30 13.30 Uhr Prof. Dr. T. Jüstel & Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Analytische Chemie B. Sc. Chemieingenieurwesen 6. Juli 2016, 10.30 13.30 Uhr Prof. Dr. T. Jüstel & Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Analytische Chemie. B. Sc. Chemieingenieurwesen. 13. September 2016, Uhr. Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc.
 Analytische Chemie B. Sc. Chemieingenieurwesen 13. September 2016, 8.00 11.00 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Analytische Chemie B. Sc. Chemieingenieurwesen 13. September 2016, 8.00 11.00 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Text Anlage. Heparin-Calcium
 Kurztitel 27. Nachtrag zum Arzneibuch Kundmachungsorgan BGBl. II Nr. 307/2008 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 03.09.2008 Text Anlage Heparin-Calcium Definition Heparinum calcicum Heparin-Calcium
Kurztitel 27. Nachtrag zum Arzneibuch Kundmachungsorgan BGBl. II Nr. 307/2008 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 03.09.2008 Text Anlage Heparin-Calcium Definition Heparinum calcicum Heparin-Calcium
Aufgabengruppe BMS Chemie
 Aufgabengruppe BMS Chemie Zeitvorgabe: Bitte lösen Sie die folgenden 24 Aufgaben innerhalb von 18 Minuten! 1) Welche Aussagen treffen auf Proteine zu? I. Die Primärstruktur gibt die Aminosäurenabfolge
Aufgabengruppe BMS Chemie Zeitvorgabe: Bitte lösen Sie die folgenden 24 Aufgaben innerhalb von 18 Minuten! 1) Welche Aussagen treffen auf Proteine zu? I. Die Primärstruktur gibt die Aminosäurenabfolge
Stoffe oder Teilchen, die Protonen abgeben kånnen, werden als SÄuren bezeichnet (Protonendonatoren).
 5 10 15 20 25 30 35 40 45 O C 50 Chemie Technische BerufsmaturitÄt BMS AGS Basel Kapitel 6 SÄuren und Basen Baars, Kap. 12.1; 12.2; 13 Versuch 1 Ein Becherglas mit Thermometer enthält violette FarbstofflÅsung
5 10 15 20 25 30 35 40 45 O C 50 Chemie Technische BerufsmaturitÄt BMS AGS Basel Kapitel 6 SÄuren und Basen Baars, Kap. 12.1; 12.2; 13 Versuch 1 Ein Becherglas mit Thermometer enthält violette FarbstofflÅsung
Experimentelle Durchführung u. Eingabe der Ergebnisse Gruppen-Nr C2
 7-Eisen_Komplex_pH-08.xls Fe_Phe_pH 2.08.2007 ph-abhängige Bildung eines gefärbten Eisen-Chelat-Komplexes. Photometrische Bestimmung der Gesamt-Komplexbildungskonstanten. Datum 01.05.2006 Experimentelle
7-Eisen_Komplex_pH-08.xls Fe_Phe_pH 2.08.2007 ph-abhängige Bildung eines gefärbten Eisen-Chelat-Komplexes. Photometrische Bestimmung der Gesamt-Komplexbildungskonstanten. Datum 01.05.2006 Experimentelle
Übung zu den Vorlesungen Organische und Anorganische Chemie
 Übung zu den Vorlesungen Organische und Anorganische Chemie für Biologen und Humanbiologen 07.11.08 - Lösungen - 1. Vervollständigen Sie die Reaktionsgleichungen und benennen Sie alle Verbindungen und
Übung zu den Vorlesungen Organische und Anorganische Chemie für Biologen und Humanbiologen 07.11.08 - Lösungen - 1. Vervollständigen Sie die Reaktionsgleichungen und benennen Sie alle Verbindungen und
Die Maillard-Reaktion in der Synthesemikrowelle
 Die Maillard-Reaktion in der Synthesemikrowelle Eine Arbeit von Laurence Heins und Henry Eckelmann für Jugend forscht Inhalt Jugend forscht am Gymnasium Altona (S. 3) Kurzfassung (S. 4) Einleitung (S.
Die Maillard-Reaktion in der Synthesemikrowelle Eine Arbeit von Laurence Heins und Henry Eckelmann für Jugend forscht Inhalt Jugend forscht am Gymnasium Altona (S. 3) Kurzfassung (S. 4) Einleitung (S.
Anleitung zum Auflösen von AppliChem Pulvermedien zur Herstellung steriler Flüssigmedien für die Zellkultur
 Anleitung zum Auflösen von AppliChem Pulvermedien zur Herstellung steriler Flüssigmedien für die Zellkultur Allgemeine Information zum Ansetzen von Flüssigmedien aus Pulver Pulvermedien und Salzgemische
Anleitung zum Auflösen von AppliChem Pulvermedien zur Herstellung steriler Flüssigmedien für die Zellkultur Allgemeine Information zum Ansetzen von Flüssigmedien aus Pulver Pulvermedien und Salzgemische
TZ (Fibrinogen) 0,5 ± 0,1 2,2 ± 0,6 * 1,4 ± 0,2 382,9 ± 40,4 *** 356,3 ± 87,4 *** THS-A2 410,3 ± 6,6 ***
 5 Diskussion Einfluss der Testsubstanzen auf das Gerinnungssystem Auf eine antikoagulierende Wirkung werden sulfatierte Hyaluronsäuren, carboxymethylierte sulfatierte Hyaluronsäuren und die natürlichen
5 Diskussion Einfluss der Testsubstanzen auf das Gerinnungssystem Auf eine antikoagulierende Wirkung werden sulfatierte Hyaluronsäuren, carboxymethylierte sulfatierte Hyaluronsäuren und die natürlichen
Linearität und Nachweisgrenzen
 ASA-Doku 2015-2 Linearität und Nachweisgrenzen Linearität und Nachweisgrenzen im Hydrolysatprogramm k.jansen@sykam.de Version 1.3 /6.8.2015 SYKAM Chromatographie Vertriebs GmbH Carl-von-Linde-Straße 2
ASA-Doku 2015-2 Linearität und Nachweisgrenzen Linearität und Nachweisgrenzen im Hydrolysatprogramm k.jansen@sykam.de Version 1.3 /6.8.2015 SYKAM Chromatographie Vertriebs GmbH Carl-von-Linde-Straße 2
Chemie-Tutorien zur Vorbereitung auf das Praktikum
 Seite 1 von 7 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie-Tutorien zur Vorbereitung auf das Praktikum 07.03.-18.03.2017 Dienstag, 07.03.2017 18.00-20.00 Uhr Grundlagen der Chemie I Donnerstag, 09.03.2017
Seite 1 von 7 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie-Tutorien zur Vorbereitung auf das Praktikum 07.03.-18.03.2017 Dienstag, 07.03.2017 18.00-20.00 Uhr Grundlagen der Chemie I Donnerstag, 09.03.2017
Lösungen zu den Übungen zur Experimentalvorlesung AC
 Lösungen zu den Übungen zur Experimentalvorlesung AC 1. Stöchiometrisches Rechnen 1.1. n (S = mol n (S 8 = 0,5 mol 1.. n (P = 8 mol n (P = mol 1.3. m (P =,8 g m (P =,8 g m (P = 1, g 1.. m (1/3 As 3+ =
Lösungen zu den Übungen zur Experimentalvorlesung AC 1. Stöchiometrisches Rechnen 1.1. n (S = mol n (S 8 = 0,5 mol 1.. n (P = 8 mol n (P = mol 1.3. m (P =,8 g m (P =,8 g m (P = 1, g 1.. m (1/3 As 3+ =
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
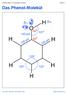 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Einteilung der Maßanalyse
 Einteilung der Maßanalyse Neutralisation (Säure-Base-Titration Acidimetrie Alkalimetrie Fällungstitration Redoxtitration Iodometrie Dichromatometrie Manganometrie etc. Komplexometrie Säure/Basen Theorien
Einteilung der Maßanalyse Neutralisation (Säure-Base-Titration Acidimetrie Alkalimetrie Fällungstitration Redoxtitration Iodometrie Dichromatometrie Manganometrie etc. Komplexometrie Säure/Basen Theorien
A. Wieviel molar ist eine 30 % Wasserstoffperoxidlösung (d = 1.11, M = 34)
 Grundlagen der Biochemie 29. 2. 2008 Einfache Rechenfragen: A. Wieviel molar ist eine 30 % Wasserstoffperoxidlösung (d = 1.11, M = 34) B. Welche Stoffmenge enthalten 2 µl einer 5 µm Lösung? Richtige Einheit
Grundlagen der Biochemie 29. 2. 2008 Einfache Rechenfragen: A. Wieviel molar ist eine 30 % Wasserstoffperoxidlösung (d = 1.11, M = 34) B. Welche Stoffmenge enthalten 2 µl einer 5 µm Lösung? Richtige Einheit
Analytische Chemie. B. Sc. Chemieingenieurwesen. 17. März Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 17. März 2010 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 17. März 2010 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
15. Aminosäuren, Peptide und Proteine
 Inhalt Index 15. Aminosäuren, Peptide und Proteine Proteine (Polypeptide) erfüllen in biologischen Systemen die unterschiedlichsten Funktionen. So wirken sie z.b. bei vielen chemischen Reaktionen in der
Inhalt Index 15. Aminosäuren, Peptide und Proteine Proteine (Polypeptide) erfüllen in biologischen Systemen die unterschiedlichsten Funktionen. So wirken sie z.b. bei vielen chemischen Reaktionen in der
pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
 Aminosäuren mit sauren Seitengruppen Asparaginsäure (Asp,D) pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
Aminosäuren mit sauren Seitengruppen Asparaginsäure (Asp,D) pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
Analytische Chemie. B. Sc. Chemieingenieurwesen. 11. Februar Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 11. Februar 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
Analytische Chemie B. Sc. Chemieingenieurwesen 11. Februar 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
Seite 1 von Standortbestimmung / Äquivalenzprüfung. Chemie. Freitag, 23. Mai 2014, Uhr
 Seite 1 von 8 2. Standortbestimmung / Äquivalenzprüfung Chemie Freitag, 23. Mai 2014, 16.45-18.45 Uhr Dauer der Prüfung: 120 Minuten Erlaubte Hilfsmittel: Eine vom Dozenten visierte Formelsammlung, Ein
Seite 1 von 8 2. Standortbestimmung / Äquivalenzprüfung Chemie Freitag, 23. Mai 2014, 16.45-18.45 Uhr Dauer der Prüfung: 120 Minuten Erlaubte Hilfsmittel: Eine vom Dozenten visierte Formelsammlung, Ein
Für enzymkinetische Untersuchungen legen Sie 0.2 ml einer 5 mm Substratlösung vor. Der fertige Inkubationsansatz hat ein Volumen von 2 ml.
 Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Der Test wird im Anschluss an die Prüfung aus Grundlagen der Biochemie angeboten, welche 90 min dauert (also bei der Türe
Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Der Test wird im Anschluss an die Prüfung aus Grundlagen der Biochemie angeboten, welche 90 min dauert (also bei der Türe
Peptidkupplung zum Einbau fluorierter Aminosäuren mittels mikrowellenunterstützter Synthesemethoden
 Freie Universität Berlin Institut für Chemie rganische Chemie Peptidkupplung zum Einbau fluorierter Aminosäuren mittels mikrowellenunterstützter Synthesemethoden Funda Mario Matthias Christian René Kevin
Freie Universität Berlin Institut für Chemie rganische Chemie Peptidkupplung zum Einbau fluorierter Aminosäuren mittels mikrowellenunterstützter Synthesemethoden Funda Mario Matthias Christian René Kevin
Chemie Klausur SS Aminosäuren (11.5 Punkte) a) Benennen Sie die unten stehenden Aminosäuren:
 Chemie Klausur SS14 1. Aminosäuren (11.5 Punkte) a) Benennen Sie die unten stehenden Aminosäuren: b) Bestimmen Sie den isoelektrischen Punkt der Aminosäure Lysin (unterer Graph)! pks1 = 2,0 pks2 = 9,1
Chemie Klausur SS14 1. Aminosäuren (11.5 Punkte) a) Benennen Sie die unten stehenden Aminosäuren: b) Bestimmen Sie den isoelektrischen Punkt der Aminosäure Lysin (unterer Graph)! pks1 = 2,0 pks2 = 9,1
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Chemische Gleichgewichte, Säuren und
 Wiederholung der letzten Vorlesungsstunde: Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Thema heute: Chemische Gleichgewichte, Säuren
Wiederholung der letzten Vorlesungsstunde: Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Thema heute: Chemische Gleichgewichte, Säuren
Laborprotokoll Qualitative Analyse Ralph Koitz, Einzelsalz
 1. Einzelsalz Aufgabenstellung: Nasschemische qualitative Analyse eines anorganischen Einzelsalzes. o Farblose, grobkörnige Kristalle o Flammenfärbung: leicht orange, nicht charakteristisch da vermutlich
1. Einzelsalz Aufgabenstellung: Nasschemische qualitative Analyse eines anorganischen Einzelsalzes. o Farblose, grobkörnige Kristalle o Flammenfärbung: leicht orange, nicht charakteristisch da vermutlich
Protokoll Tag 3. C. Kationennachweise. C.1. Nachweis von Na +, Mg 2+, Ca 2+, Sr 2+, BA 2+ sowie NH + 4
 Protokoll Tag 3 C. Kationennachweise C.1. Nachweis von Na +, Mg 2+, Ca 2+, Sr 2+, BA 2+ sowie NH + 4 V16 Nachweis von Na +, K +, Ca 2+, Sr 2+ und Ba 2+ durch Flammenfärbung Bei der Flammenprobe geht es
Protokoll Tag 3 C. Kationennachweise C.1. Nachweis von Na +, Mg 2+, Ca 2+, Sr 2+, BA 2+ sowie NH + 4 V16 Nachweis von Na +, K +, Ca 2+, Sr 2+ und Ba 2+ durch Flammenfärbung Bei der Flammenprobe geht es
NEUE ORALE ANTIKOAGULANZIEN UND DEREN EINFLUSS AUF GERINNUNGSANALYSEN
 NEUE ORALE ANTIKOAGULANZIEN UND DEREN EINFLUSS AUF GERINNUNGSANALYSEN // EINFLUSS NEUER ORALER ANTIKOAGULANZIEN AUF GERINNUNGSANALYSEN DARUM GEHT S Direkte ( neue ) orale Antikoagulanzien können zu signifikanten
NEUE ORALE ANTIKOAGULANZIEN UND DEREN EINFLUSS AUF GERINNUNGSANALYSEN // EINFLUSS NEUER ORALER ANTIKOAGULANZIEN AUF GERINNUNGSANALYSEN DARUM GEHT S Direkte ( neue ) orale Antikoagulanzien können zu signifikanten
Seminar zum Grundpraktikum Anorganische Chemie
 Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2012 Christoph Wölper Universität Duisburg-Essen Analyse 2 (NH 4 ) 2 CO 3 -Gruppe Ba 2+ Sr 2+ Ca 2+ Lösliche Gruppe Na + Mg 2+ NH 4+ Eigenschaften
Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2012 Christoph Wölper Universität Duisburg-Essen Analyse 2 (NH 4 ) 2 CO 3 -Gruppe Ba 2+ Sr 2+ Ca 2+ Lösliche Gruppe Na + Mg 2+ NH 4+ Eigenschaften
Vorpraktikum Grundoperationen im chemischen Laboratorium
 Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 09. April 2018 Inhalt: Volumetrische Messgeräte Analysenwaagen Fest-Flüssig-Trennverfahren Flüssig-Flüssig-Trennverfahren Wasserlöslichkeit
Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 09. April 2018 Inhalt: Volumetrische Messgeräte Analysenwaagen Fest-Flüssig-Trennverfahren Flüssig-Flüssig-Trennverfahren Wasserlöslichkeit
2. Materialien Zellen U937-Zellen. 2. Materialien
 2. Materialien 2.1. Zellen 2.1.1. U937-Zellen Für den AART und die Zytotoxizitätsbestimmungen wurden U937-Zellen verwendet, die vom Institut für Physiologische Chemie der Universität Mainz, Abteilung angewandte
2. Materialien 2.1. Zellen 2.1.1. U937-Zellen Für den AART und die Zytotoxizitätsbestimmungen wurden U937-Zellen verwendet, die vom Institut für Physiologische Chemie der Universität Mainz, Abteilung angewandte
7. Chemische Reaktionen
 7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte Grundlagen Lösung: homogene Phase aus Lösungsmittel und gelösten Stoff Lösungsmittel liegt im Überschuss vor
7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte Grundlagen Lösung: homogene Phase aus Lösungsmittel und gelösten Stoff Lösungsmittel liegt im Überschuss vor
ph-wert Berechnung starke Säuren z.b. HCl, HNO 3, H 2 SO 4 vollständige Dissoziation c(h 3 O + ) = c(säure)
 ph-wert Berehnung starke Säuren z.b. HCl, HNO 3, H 2 SO 4 vollständige Dissoziation (H 3 O + ) = (Säure) ph lg H 3 O Beispiel H 2 SO 4 (H 2 SO 4 ) = 0,1 mol/l (H 3 O + ) = 0,2 mol/l ph = -lg 0,2 = -(-0,699)
ph-wert Berehnung starke Säuren z.b. HCl, HNO 3, H 2 SO 4 vollständige Dissoziation (H 3 O + ) = (Säure) ph lg H 3 O Beispiel H 2 SO 4 (H 2 SO 4 ) = 0,1 mol/l (H 3 O + ) = 0,2 mol/l ph = -lg 0,2 = -(-0,699)
Neue Therapieoptionen der oralen Antikoagulation. Inselspital Bern
 Neue Therapieoptionen der oralen Antikoagulation Ilk Rü W lt Ilka Rüsges-Wolter Inselspital Bern Neue Therapieoptionen p der oralen Antikoagulation Exkurs Hämostase Wirkungsweise bisheriger Antikoagulantien
Neue Therapieoptionen der oralen Antikoagulation Ilk Rü W lt Ilka Rüsges-Wolter Inselspital Bern Neue Therapieoptionen p der oralen Antikoagulation Exkurs Hämostase Wirkungsweise bisheriger Antikoagulantien
Qualitative Analyse. - Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch,
 - Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch, Löslichkeit - charakteristische Nachweisreaktionen für Einzelionen: - Fällungsreaktionen
- Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch, Löslichkeit - charakteristische Nachweisreaktionen für Einzelionen: - Fällungsreaktionen
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler
 Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Analytische Chemie. B. Sc. Chemieingenieurwesen. 15. März 2017, Uhr. Prof. Dr. Thomas Jüstel, Dr. Stephanie Möller.
 Analytische Chemie B. Sc. Chemieingenieurwesen 15. März 2017, 12.30 15.30 Uhr Prof. Dr. Thomas Jüstel, Dr. Stephanie Möller Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Analytische Chemie B. Sc. Chemieingenieurwesen 15. März 2017, 12.30 15.30 Uhr Prof. Dr. Thomas Jüstel, Dr. Stephanie Möller Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
SÄUREN, BASE, SALZE GRUNDLAGEN CHEMIE
 SÄUREN, BASE, SALZE GRUNDLAGEN CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE Wikipedia: Die organische Chemie (kurz: OC), häufig auch kurz Organik, ist ein Teilgebiet der
SÄUREN, BASE, SALZE GRUNDLAGEN CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE Wikipedia: Die organische Chemie (kurz: OC), häufig auch kurz Organik, ist ein Teilgebiet der
Aminosäuren - Proteine
 Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
6 Anhang Verzeichnis häufig gebrauchter Lösungen und Puffer
 6 Anhang 85 6 Anhang 6.1 Verzeichnis häufig gebrauchter Lösungen und Puffer Alkoholreihe (30%, 70%, 90%, 100% Ethanol) Zur Vereinfachung wurde das käufliche 98,8%- Ethanol als 100%-ig gesetzt. Die entsprechenden
6 Anhang 85 6 Anhang 6.1 Verzeichnis häufig gebrauchter Lösungen und Puffer Alkoholreihe (30%, 70%, 90%, 100% Ethanol) Zur Vereinfachung wurde das käufliche 98,8%- Ethanol als 100%-ig gesetzt. Die entsprechenden
Studienbegleitende Prüfung Anorganisch-Chemisches Grundpraktikum WS 2004/
 Klausur zum Anorganisch-Chemischen Grundpraktikum vom 08.04.05 Seite 1 von 10 Punkte: von 84 Studienbegleitende Prüfung Anorganisch-Chemisches Grundpraktikum WS 2004/2005 08.04.2005 Matrikelnummer: Name:
Klausur zum Anorganisch-Chemischen Grundpraktikum vom 08.04.05 Seite 1 von 10 Punkte: von 84 Studienbegleitende Prüfung Anorganisch-Chemisches Grundpraktikum WS 2004/2005 08.04.2005 Matrikelnummer: Name:
Teil 2. Puffersysteme. Puffersysteme. Puffersysteme. MTA-Schule
 Puffersysteme Säure-Basen-Haushalt Teil 2 MTA-Schule Lösungen, die die Fähigkeit besitzen, ihren -Wert trotz Zugabe von H + oder OH Ionen weitgehend konstant zu halten, nennt man Pufferlösungen. Puffersysteme:
Puffersysteme Säure-Basen-Haushalt Teil 2 MTA-Schule Lösungen, die die Fähigkeit besitzen, ihren -Wert trotz Zugabe von H + oder OH Ionen weitgehend konstant zu halten, nennt man Pufferlösungen. Puffersysteme:
3.2. Aufgaben zu Säure-Base-Gleichgewichten
 .. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
.. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Chemisches Rechnen. Diese Lerneinheit befasst sich mit verschiedenen chemisch relevanten Größen Konzentrationsangaben mit den folgenden Lehrzielen:
 Chemisches Rechnen Diese Lerneinheit befasst sich mit verschiedenen chemisch relevanten Größen Konzentrationsangaben mit den folgenden Lehrzielen: Verständnis der unterschiedlichen Größen Sichere Anwendung
Chemisches Rechnen Diese Lerneinheit befasst sich mit verschiedenen chemisch relevanten Größen Konzentrationsangaben mit den folgenden Lehrzielen: Verständnis der unterschiedlichen Größen Sichere Anwendung
