Spektroskopiemodul II. H-NMR und 13 C-NMR
|
|
|
- Clara Scholz
- vor 6 Jahren
- Abrufe
Transkript
1 Spektroskopiemodul II 1 H-NMR und 13 C-NMR 1
2 1. Was gehört zu einer vollständigen Spektreninterpretation zur Strukturaufklärung? H-NMR-Spektren Man muss die chemische Verschiebung jedes einzelnen Protons oder jeder Gruppe von äquivalenten Protonen kennen. Man muss wissen, wie viele Protonen zu einer Gruppe von äquivalenten Protonen gehören. Man muss das Aufspaltungsmuster jedes einzelnen Protons kennen, sofern es sich um Teilspektren 1. Ordnung handelt. Man muss alle Kopplungskonstanten jedes einzelnen Protons mit seinen Nachbarn kennen, sofern es sich um Teilspektren 1. Ordnung handelt. Kurz gesagt: Man muss jedes Proton im Molekül persönlich kennen. 2
3 Zahl der chemisch äquivalenten Protonen in einer Gruppe, charakteristische Strukturelemente CH 3, tbu, Ph, Integration Chemische Verschiebung Aufspaltungsmuster Elektronendichte des betrachteten H-Atoms, Hybridisierung des C-Atoms, an dem sich das beobachtete H befindet, elektronenschiebende oder elektronenziehende Gruppen in der Nachbarschaft, Konjugation, Funktionelle Gruppen, Anisotropieeffekte, Heteroatome 1 H s, d, tr, quart, quint, sext, sept, dd, dt, trtr, ddd, ddt, ddquart, ddquint, dddd Nachbarschaft eines betrachteten Kerns, Chiralität, chemische und magnetische Äquivalenz 3
4 C-NMR-Spektren Man muss die chemische Verschiebung jedes einzelnen Kohlenstoffatoms kennen. Man muss die Multiplizität jedes einzelnen Kohlenstoffatoms im Molekül kennen. Kurz gesagt: Man muss jedes Kohlenstoffatom im Molekül persönlich kennen. Chemische Verschiebung Hybridisierung Strukturelemente Funktionelle Gruppen 13 C Multiplizität CH 3? CH 2? CH? C? 13 C BB-entkoppelt DEPT90, DEPT135, APT 4
5 2. Chemische Verschiebung 2.1. Chemische Verschiebung von Protonen Die chemische Verschiebung δ eines Protons wird bestimmt durch die Hybridisierung des C-Atoms, an das das Proton gebunden ist. Die chemische Verschiebung eines Protons wird durch die Elektronendichte der Elektronenhülle des Protons bestimmt. Diese Elektronendichte hängt von der Nachbarschaft des Protons ab. Elektronenschiebende Substituenten (+I, +M) am Kohlenstoff des betrachteten Protons erhöhen die Elektronendichte und verkleinern die chemische Verschiebung. Elektronenziehende Substituenten ( I, M) am Kohlenstoff des betrachteten Protons verkleinern die Elektronendichte und vergrößern die chemische Verschiebung. Funktionelle Gruppen zeigen charakteristische chemische Verschiebungen, an denen man sie erkennen kann (z.b. Aldehyde, Doppelbindungen, Aromaten, Alkohole, Amine usw.) 5
6 Einen Aldehyden erkennt man an δ 9,5 ppm. Es ist nicht sinnvoll, ein Aldehyd-Proton bei 5 ppm zu suchen! Eine Methylgruppe am Ende einer Alkylkette erscheint im Spektrum immer bei 0,7 1,0 ppm. Es ist nicht sinnvoll, eine Methylgruppe bei 7 ppm zu suchen! Grobe Übersicht: N-H O-H Aldehyde Aromaten Alkene CH CH 2 δ CH Der Methylbereich reicht hier von 0,5 ppm bis 4,5 ppm. Dies berücksichtigt auch Methylgruppen, die direkt mit Heteroatomen verknüpft sind. In MeOH findet man die Methylgruppe bei 3,39 ppm. Dies gilt entsprechend für die anderen Strukturelemente. 6
7 Elektronische Effekte, die die chemische Verschiebung eines Protons beeinflussen, sind additiv. Das ist die Grundlage von Inkrementrechungen zur Abschätzung von chemischen Verschiebungen! Inkremente für zahlreiche Strukturelemente sind tabelliert, z.b. in Hesse, Maier, Zeh, Spektroskopische Methoden in der Organischen Chemie, Thieme-Verlag, oder in Pretsch, Clerc, Seibl, Simon, Tabellen zur Strukturaufklärung organischer Verbindungen, Springer- Verlag. Auch Berechnungen von chemischen Verschiebungen mit Hilfe von Computerprogrammen basieren auf Inkrementrechungen. Vgl. z.b. Spektrenvorhersage von ChemDraw oder von nmrdb.org. Diese Berechungen sind ähnlich genau, wie Inkrementrechungen von Hand mit tabellierten Inkrementen. Besser: man orientiert sich an Spektren von ähnlichen Verbindungen aus der Literatur! Chemische Verschiebungen von Protonen hängen ab von Anisotropieeffekten, die durch unsymmetrische Ladungsverteilung in Bindungen zustande kommen. Typisches Beispiel für einen Anisotropieeffekt sind Moleküle mit aromatischem π-elektronensextett ( Ringstromeffekt ). Aber auch Ketogruppen, C=C-Doppelbindungen, 7 C C-Dreifachbindungen, Nitril-Gruppen u.a. zeigen Anisotropieeffekte.
8 B 0 B 0 H H H H H H 8
9 Wichtig: die chemische Verschiebung eines Protons hängt vom Lösungsmittel ab. In Aceton-d 6, in DMSO-d 6, in Methanol-d 4, in Acetonitril-d 3 beobachtet man oft geringfügig (bis zu ± 0,2 ppm) andere chemische Verschiebungen als in CDCl 3. In Benzol-d 6 und in Pyridin-d 5 beobachtet man dagegen komplett andere Werte (bis zu ± 1 ppm) Werte als in CDCl 3. Nützlich für die Praxis: wenn in CDCl 3 zwei oder mehrere Signale überlagern, dann kann man durch Zugabe von einigen Tropfen C 6 D 6 eine Aufhebung der Überlagerung bewirken. Das kann so weit führen, dass aus einem Teilspektrum 2. Ordnung ein Teilspektrum 1. Ordnung wird (vgl. Bsp. von Eugenol). 9
10 2.2. Chemische Verschiebung von 13 C Nur 13 C ist NMR-aktiv, 12 C kann man NMR-spektroskopisch nicht messen. 13 C tritt nur mit ca. 1% natürlicher Häufigkeit auf geringe Empfindlichkeit bei der Messung Chemische Verschiebung von 13 C-Kernen hängt von der Hybridisierung und von der Elektronendichte um den 13 C-Kern ab. Die chemische Verschiebung von 13 C-Kernen von den üblichen organischen Verbindungen erstreckt sich von 0 ppm bis ca. 220 ppm. Grobe Regel: Unterhalb von 100 ppm findet man nur sp 3 -hybridisierte C-Atome, oberhalb von 100 ppm findet man nur sp 2 -hybridisierte C- Atome. sp-hybridisierte C-Atome von Alkinen liegen etwa bei ppm, sp-hybridisierte C-Atome von Nitrilen liegen zwischen 110 und 120 ppm. Wichtiger Unterschied zur 1 H-NMR: Alkene und Aromaten liegen im selben δ-bereich, d.h. auf C-Atome wirken sich Anisotropieeffekte nicht aus. 10
11 Auch die Verschiebung von 13 C-Kernen kann über Inkrementrechung abgeschätzt werden (vgl. Hesse, Maier, Zeh oder Pretsch, Clerk, Seibl, Simon). Man kann auch 13 C-Spektren mit Computerprogrammen vorhersagen, z.b. mit ChemDraw oder NMRDB.ORG. Diese Vorhersagen sind aber genauso fehlerbehaftet, wie Inkrementrechungen von Hand. Besser, als sich auf die berechneten chemischen Verschiebungen zu verlassen, ist die Verwendung von Daten ähnlicher Verbindungen aus der Literatur. 13 NMR-Spektren sind nur geringfügig lösunsmittelabhängig, allerdings findet man auch hier in Benzol-d 6 und Pyridin-d 5 größere Abweichungen von den entsprechenden Werten in CDCl 3, Aceton-d 6, DMSO-d 6 oder Methanol-d 4. Die Bestimmung der Multiplizität von 13 C-Signalen (= Aufspaltung durch Kopplung mit direkt gebundenen H-Atomen) erfolgt mit DEPT- Spektren. DEPT90 zeigt nur CH, DEPT135 zeigt CH 2 -Gruppen als negative Signale, CH- und CH 3 -Gruppen als positive Signale. Alle Signale, die man im BB-entkoppelten 13 C-Spektrum zusätzlich zu den DEPT135-Signalen findet, stammen von quartären C-Atomen. 11
12 3. Spin-Spin-Kopplung 3.1. Kopplung zwischen zwei Hs Es gibt zwei Arten von Kopplungen zwischen Protonen: die direkte Kopplung durch den Raum (diploare Kopplung), und die indirekte Kopplung über Bindungen (skalare Kopplung). Obwohl die dipolare Kopplung viel stärker ist als die skalare Kopplung, sieht man in verdünnten Lösungen von organischen Molekülen nur die skalare Kopplung. In Festkörpern und hochviskosen Flüssigkeiten überdeckt die dipolare Kopplung i.d.r. die skalare Kopplung. Hier: nur skalare Kopplung über Bindungen. Die Stärke der Kopplung wird durch die Kopplungskonstante J beschrieben. Die Kopplungskonstante ist unabhängig von der Magnetfeldstärke des NMR-Spektrometers und wird ausschließlich in Hz angegeben (nicht in ppm!!!). Üblicherweise stellt man die Zahl der Bindungen, die an der Kopplung zweier Kerne beteiligt ist, als Hochzahl vorne an. Es gibt zwischen Protonen in organischen Molekülen also generell 2 J, 3 J, 4 J usw. 12
13 Kopplungen über mehr als 3 Bindungen werden als sogenannte Long- Rage-Kopplungen bezeichnet und sind in der Regel so klein, dass man sie im Spektrum nicht erkennen kann. Ausnahmen: W-Kopplung, Allylische Kopplung und Propargylische Kopplung. Kopplungskonstanten sind vorzeichenbehaftet. 2 J sind üblicherweise negativ, 3 J sind immer positiv, 4 J wieder negativ usw. In Spektren 1. Ordnung kann man das Vorzeichen jedoch nicht erkennen und es spielt dort auch keine Rolle. In Spektren 2. Ordnung wirkt sich das Vorzeichen der Kopplungskonstante dramatisch aus. Spektren 1. Ordnung: durch Spin-Spin-Kopplung ergeben sich charakteristische Aufspaltungsmuster für die Signale, die Aussagen über die Nachbarschaft zulassen. Dublett: 1 Kopplungspartner Triplett: 2 chemisch und magnetisch äquivalente Kopplungspartner Quartett: 3 chemisch und magnetisch äquivalente Kopplungspartner Dublett von Dubletts: 2 chemisch und magnetisch nicht äquivalente Kopplungspartner 13
14 Dublett von Dublett von Dubletts: drei chemisch und magnetisch nicht äquivalente Kopplungspartner Für Kerne mit I = ½ gilt: bei n chemisch und magnetisch äquivalenten Kopplungspartnern erhält man ein Signal mit n+1 Linien. Für Kerne mit I = ½ gilt: bei n chemisch und magnetisch nicht äquivalenten Kernen erhält man ein Signal mit 2 n Linien. Wichtige Kopplungskonstanten: (aus 14
15 15
16 16
17 17
18 18
19 19
20 20
21 21
22 Protonen können auch mit anderen Atomen mit I = ½ koppeln. Wichtigste Kerne sind 19 F und 31 P (beide mit 100% Häufigkeit). 22
23 23
24 24
25 Protonen können auch mit Kernen mit I > ½ koppeln. Kerne mit I > ½ haben ein sogenanntes Quadrupolmoment. Das bedeutet, dass die Ladungsverteilung im Kern nicht mehr kugelsymmetrisch ist, sondern ellipsoid (analog dem Trägheitsellipsoid eines starren Rotators). Je größer das Quadrupolmoment, um so unsymmetrischer ist die Ladungsverteilung im Kern. Wenn sich ein Kern mit großem Quadrupolmoment in stark unsymmetrischer Ladungsverteilung (Elektronen um den Kern herum) befindet, dann tritt eine effiziente, schnelle Relaxation des Kernspins I > ½ auf, was zu extrem breiten Signalen führt (die oft im Rauschen untergehen). Nur wenn um den Kern herum eine symmetrische Ladungsverteilung existiert, vergrößert sich die Relaxationszeit der Kerne mit I > ½ und man kann Spektroskopie von Molekülen mit solchen Kernen betreiben (NMR in AC). 25
26 Nur wenn die Quadrupolmomente von Kernen mit I > ½ klein sind, relaxieren deren Spins in organischen Molekülen langsam und können dann mit Kernen mit I = ½ koppeln. Kerne mit großem Quadrupolmoment zeigen keine Kopplung mit Protonen, auch wenn es auf Grund von I > ½ zur Aufspaltung kommen müsste. Die Werte in der Tabelle sind bei einem 400 MHz-Gerät (B 0 = 9,4 T) gemessen. Deshalb sieht man in 1H-Spektren und 13 C-Spektren oft Kopplungen mit Deuterium. 26
27 2 H (I = 1) besitzt ein sehr kleines Quadrupolmoment und zeigt daher eine entsprechende Kopplung im 1 H-NMR-Spektrum (deuterierte Lösungsmittel). 14 N (I = 1) besitzt ein großes Quadrupolmoment und führt zu sehr breiten Linien im 1 H-Spektrum der gebundenen Protonen. 35 Cl und 37 Cl (beide I = 3/2) besitzen ein großes Quadrupolmoment, man sieht aber keine Kopplung mit C oder H in chlorierten Verbindungen (CHCl 3 ergibt ein Singulett im 1 H-NMR- Spektrum, ebenso im 13 C-NMR-Spektrum, obwohl die 3 Cl-Kerne mit 1 H und 13 C koppeln müssten). Lösungsmittelsignal DMSO-d 6 Wie kommt das Aufspaltungsmuster zustande? Wie groß ist die Kopplungskonstante (400 MHz-Gerät)? 27
28 3.2. Kopplung zwischen 13 C und 1 H Protonen können auch mit C-Atomen mit I = ½ koppeln. Auf Grund der geringen Häufigkeit von 13 C beobachtet man im 1H-NMR-Spektrum nur kleine 13 C-Satelliten. Der Abstand der beiden 13 C-Satelliten ist die Kopplungskonstante zwischen 1 H und 13 C. C-H-Kopplungen über eine Bindung sind üblicherweise sehr groß und hängen von der Hybridisierung des C-Atoms ab. Um durch diese Kopplung 13 C-Spektren nicht zu kompliziert zu machen, werden 13 C-Spektren üblicherweise mit 1 H-Breitbandentkopplung aufgenommen. 28
29 29
30 30
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4.1 Allgemeines Spektroskopische Methode zur Untersuchung von Atomen: elektronische Umgebung Wechselwirkung
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4.1 Allgemeines Spektroskopische Methode zur Untersuchung von Atomen: elektronische Umgebung Wechselwirkung
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
NMR-Lösungsmittel. 1 H-NMR. Bei der Verwendung der normalen, nichtdeuterierten Lösungsmittel. Spektroskopie in der Organischen Chemie
 NMR-Lösungsmittel In der werden i.a. deuterierte Lösungsmittel verwendet. ie Substitution der leichten durch die schweren Wasserstoffatome hat zwei Vorteile: - euterium als Spin-1-Kern hat ebenfalls ein
NMR-Lösungsmittel In der werden i.a. deuterierte Lösungsmittel verwendet. ie Substitution der leichten durch die schweren Wasserstoffatome hat zwei Vorteile: - euterium als Spin-1-Kern hat ebenfalls ein
Übungen zur Spektroskopie 2
 Übungen zur Spektroskopie 2 C. Dubler und Dr. D. S. Stephenson Department Chemie, Universität München Sie finden diese Übungen und alte Klausuren (mit Lösung) auf unserer Homepage: http://cicum200.cup.unimuenchen.de/intranet/depch/analytik/nmr_f/index.php
Übungen zur Spektroskopie 2 C. Dubler und Dr. D. S. Stephenson Department Chemie, Universität München Sie finden diese Übungen und alte Klausuren (mit Lösung) auf unserer Homepage: http://cicum200.cup.unimuenchen.de/intranet/depch/analytik/nmr_f/index.php
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Chemische Verschiebung Chemische Umgebung Funktionelle Gruppen Signalintensitäten
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Chemische Verschiebung Chemische Umgebung Funktionelle Gruppen Signalintensitäten
Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden
 Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden Grundlagen Die meisten Atomkerne führen eine Drehbewegung um die eigene Achse aus ("Spin"). Da sie geladene Teilchen (Protonen) enthalten,
Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden Grundlagen Die meisten Atomkerne führen eine Drehbewegung um die eigene Achse aus ("Spin"). Da sie geladene Teilchen (Protonen) enthalten,
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
13 C, 1 H-Kopplungskonstanten. 13 C, 1 H-Kopplungen hier leichter erkannt werden können. Spektroskopie in der Organischen Chemie
 Spektroskopie in der Organischen hemie 13, 1 -Kopplungskonstanten NMR-Signalaufspaltungen aufgrund von skalaren Kopplungen treten grundsätzlich bei beiden Kopplungspartnern auf. Entsprechend kann man 13,
Spektroskopie in der Organischen hemie 13, 1 -Kopplungskonstanten NMR-Signalaufspaltungen aufgrund von skalaren Kopplungen treten grundsätzlich bei beiden Kopplungspartnern auf. Entsprechend kann man 13,
Übungsaufgaben zur NMR-Spektrometrie
 Übungsaufgaben NMR 33 Übungsaufgaben zur NMR-Spektrometrie Aufgabe 1 a) Wieviele unterschiedliche Orientierungen des Kernmomentes relativ zu einem externen Magnetfeld sind beim 14 N-Kern (I = 1, γ = 1.932
Übungsaufgaben NMR 33 Übungsaufgaben zur NMR-Spektrometrie Aufgabe 1 a) Wieviele unterschiedliche Orientierungen des Kernmomentes relativ zu einem externen Magnetfeld sind beim 14 N-Kern (I = 1, γ = 1.932
Spektroskopie-Seminar SS NMR-Spektroskopie. C-NMR-Spektroskopie und 2D-Spektroskopie
 13 C-NMR-Spektroskopie und 2D-Spektroskopie 6.1 Allgemeines Kernresonanz: Wechselwirkungen zwischen dem magnetischen Moment von Atomkernen mit einem magnetischen Wechselfeld Nur solche Isotope können untersucht
13 C-NMR-Spektroskopie und 2D-Spektroskopie 6.1 Allgemeines Kernresonanz: Wechselwirkungen zwischen dem magnetischen Moment von Atomkernen mit einem magnetischen Wechselfeld Nur solche Isotope können untersucht
Analytische Methoden in Org. Chemie und optische Eigenschaften von chiralen Molekülen
 Analytische Methoden in Org. Chemie und optische Eigenschaften von chiralen Molekülen Seminar 5. 0. 200 Teil : NMR Spektroskopie. Einführung und Physikalische Grundlagen.2 H NMR Parameter: a) Chemische
Analytische Methoden in Org. Chemie und optische Eigenschaften von chiralen Molekülen Seminar 5. 0. 200 Teil : NMR Spektroskopie. Einführung und Physikalische Grundlagen.2 H NMR Parameter: a) Chemische
Spektroskopie-Seminar WS 17/18 5 NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 WS 17/18 1 -NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 1 5.1 1 -NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung δ(in
WS 17/18 1 -NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 1 5.1 1 -NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung δ(in
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Übungsaufgaben NMR-Spektroskopie (1)
 Übungsaufgaben NMR-Spektroskopie (1) 1. Kerne haben drei wichtige Eigenschaften: Masse m, Ladung Q und Eigendrehimpuls p. Kernsorte Spin natürliche Häufigkeit Gyromagnet. Verhältnis γ [Tsec] 1 1 H 1/2
Übungsaufgaben NMR-Spektroskopie (1) 1. Kerne haben drei wichtige Eigenschaften: Masse m, Ladung Q und Eigendrehimpuls p. Kernsorte Spin natürliche Häufigkeit Gyromagnet. Verhältnis γ [Tsec] 1 1 H 1/2
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
Einführung in die NMR-Spektroskopie. NMR-Spektroskopie. Teil 1: Einführung und Grundlagen der 1 H NMR. Das NMR Spektrometer
 NMR-Spektroskopie Einführung in die NMR-Spektroskopie m I = - /2 (β) Teil : Einführung und Grundlagen der NMR E E. Physikalische und apparative Grundlagen m I = + /2 (α).2 Das D NMR Experiment.3 Die chemische
NMR-Spektroskopie Einführung in die NMR-Spektroskopie m I = - /2 (β) Teil : Einführung und Grundlagen der NMR E E. Physikalische und apparative Grundlagen m I = + /2 (α).2 Das D NMR Experiment.3 Die chemische
NMR-Spektroskopie Teil 2
 BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
Der Kern-Overhauser-Effekt (Nuclear Overhauser Effect, NOE)
 Der Kern-verhauser-Effekt (Nuclear verhauser Effect, NE) Die Intensität eines 1 H-Signals kann durch ein Entkopplungsexperiment verändert werden. Wird der Übergang eines ausgewählten 1 H-Kerns S für eine
Der Kern-verhauser-Effekt (Nuclear verhauser Effect, NE) Die Intensität eines 1 H-Signals kann durch ein Entkopplungsexperiment verändert werden. Wird der Übergang eines ausgewählten 1 H-Kerns S für eine
1 1 H-NMR-Spektroskopie in metallorganischen Komplexen. 1.1 Allgemeines. 1.2 Chiralität in Metallkomplexen 1.3 Dynamische Prozesse
 1 1 H-NMR-Spektroskopie in metallorganischen Komplexen 1.1 Allgemeines Chemische Verschiebungen Beispiele für einfache Komplexe 1.2 Chiralität in Metallkomplexen 1.3 Dynamische Prozesse 1.4 Heteronukleare
1 1 H-NMR-Spektroskopie in metallorganischen Komplexen 1.1 Allgemeines Chemische Verschiebungen Beispiele für einfache Komplexe 1.2 Chiralität in Metallkomplexen 1.3 Dynamische Prozesse 1.4 Heteronukleare
NMR Spektroskopie (Nuclear Magnetic Resonance Kern-Magnetische Resonanz)
 NMR Spektroskopie (Nuclear Magnetic Resonance Kern-Magnetische Resonanz) Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p = ħ I, der ganz - oder halbzahlige Werte von ħ betragen
NMR Spektroskopie (Nuclear Magnetic Resonance Kern-Magnetische Resonanz) Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p = ħ I, der ganz - oder halbzahlige Werte von ħ betragen
Spektroskopische Methoden in der Organischen Chemie (OC IV) C NMR Spektroskopie
 6. 3 C NMR Spektroskopie Die Empfindlichkeit des NMR Experiments hängt von folgenden physikalischen Parametern (optimale Abstimmung des Spektrometers vorausgesetzt) ab: Feldstärke B o, Temperatur T, gyromagnetisches
6. 3 C NMR Spektroskopie Die Empfindlichkeit des NMR Experiments hängt von folgenden physikalischen Parametern (optimale Abstimmung des Spektrometers vorausgesetzt) ab: Feldstärke B o, Temperatur T, gyromagnetisches
7 Kernresonanz-Spektroskopische Untersuchungen
 7 Kernresonanz-Spektroskopische Untersuchungen 79 7 Kernresonanz-Spektroskopische Untersuchungen 7.1 1 H-MR-Signale Die 1 H-MR-Spektroskopie liefert aufgrund der charakteristischen chemischen Verschiebung
7 Kernresonanz-Spektroskopische Untersuchungen 79 7 Kernresonanz-Spektroskopische Untersuchungen 7.1 1 H-MR-Signale Die 1 H-MR-Spektroskopie liefert aufgrund der charakteristischen chemischen Verschiebung
Bestimmung der Struktur einer (un)bekannten Verbindung
 Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektrometrie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie H 3 C H 3
Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektrometrie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie H 3 C H 3
NMR - Seite 1. NMR (Kernresonanzspektroskopie) Allgemeines zur Theorie
 NMR - Seite 1 NMR (Kernresonanzspektroskopie) Allgemeines zur Theorie Protonen besitzen ebenso wie Elektronen einen eigenen Spin (Drehung um die eigene Achse).Allerdings gibt es mehrere Möglichkeiten als
NMR - Seite 1 NMR (Kernresonanzspektroskopie) Allgemeines zur Theorie Protonen besitzen ebenso wie Elektronen einen eigenen Spin (Drehung um die eigene Achse).Allerdings gibt es mehrere Möglichkeiten als
Chemische und Magnetische Äquivalenz
 Chemische und Magnetische Äquivalenz Das Aussehen von NMR-Signalen in Mehr-Spinsystemen wird ganz wesentlich davon beeinflusst, ob es äquivalente Kerne gibt oder nicht. ierbei sind zwei wichtige Arten
Chemische und Magnetische Äquivalenz Das Aussehen von NMR-Signalen in Mehr-Spinsystemen wird ganz wesentlich davon beeinflusst, ob es äquivalente Kerne gibt oder nicht. ierbei sind zwei wichtige Arten
NMR Spektroskopie I = 0 : C, 16 O (sogenannte gg-kerne haben immer I=0!) I = 1/2: 1 H, 13 C, 15 N, 19 F, 31 P,... I = 1: 2. H=D, 6 Li, 14 N I = 3/2: 7
 NMR Spektroskopie folie00 Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
NMR Spektroskopie folie00 Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
gleicher Magnetfeldstärke die Resonanzfrequenz entsprechend kleiner; z.b: 400 MHz 1 H, aber MHz 13 C.
 Der 13 C-Kern ist in seinen wichtigsten Kerneigenschaften dem 1 H ähnlich. Er ist ebenso ein Spin-½-Kern, weist also im äußeren Magnetfeld B 0 nur zwei praktisch gleich populierte Energiezustande auf.
Der 13 C-Kern ist in seinen wichtigsten Kerneigenschaften dem 1 H ähnlich. Er ist ebenso ein Spin-½-Kern, weist also im äußeren Magnetfeld B 0 nur zwei praktisch gleich populierte Energiezustande auf.
Spektroskopische Methoden in der Organischen Chemie (OC IV)
 H 3 C 10 O G F D E 8 5 I H GF E D CB A 10 8 5 3 2 1 125 MHz 13 C NMR Spektrum 500 MHz 1 H NMR Spektrum NMR -_1 32 1 H 3 C 10 8 5 10 O G F D E 8 5 Dieder-Winkel: H 10 -H : 5, H -H : 80 H H 8 : 2, H -H :
H 3 C 10 O G F D E 8 5 I H GF E D CB A 10 8 5 3 2 1 125 MHz 13 C NMR Spektrum 500 MHz 1 H NMR Spektrum NMR -_1 32 1 H 3 C 10 8 5 10 O G F D E 8 5 Dieder-Winkel: H 10 -H : 5, H -H : 80 H H 8 : 2, H -H :
Chemisches Grundpraktikum II (270002) Kernresonanzspektroskopie. NMR-Spektroskopie
 hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
Teil 2: Spin-Spin Kopplung
 NMR-Spektroskopie Teil 2: Spin-Spin Kopplung 1. Die skalare Spin-Spin Kopplung 2. Multiplizitaet und Intensitaetsverteilung 3. Geminale, vicinale und allylische Kopplungskonstanten 4. Anschauliche Beschreibung
NMR-Spektroskopie Teil 2: Spin-Spin Kopplung 1. Die skalare Spin-Spin Kopplung 2. Multiplizitaet und Intensitaetsverteilung 3. Geminale, vicinale und allylische Kopplungskonstanten 4. Anschauliche Beschreibung
Spinsysteme. AX 3 -Spinsystem
 Spinsysteme Eine Gruppe aus zwei oder mehreren Kernspins, die miteinander eine magnetische Wechselwirkung eingehen, bezeichnet man als ein Spinsystem. Die Struktur eines hochaufgelösten NMR-Spektrums und
Spinsysteme Eine Gruppe aus zwei oder mehreren Kernspins, die miteinander eine magnetische Wechselwirkung eingehen, bezeichnet man als ein Spinsystem. Die Struktur eines hochaufgelösten NMR-Spektrums und
NMR Spektroskopie. 1nm Frequenz X-ray UV/VIS Infrared Microwave Radio
 NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
Die Strukturabhängigkeit der chemischen Verschiebung
 Die Strukturabhängigkeit der chemischen Verschiebung. Abschirmung in einem Atom (wie bisher geschildert) Die Elektronenverteilung in einem Wasserstoffatom ist sphärisch. B 0 0 0000000 000000000 000000000
Die Strukturabhängigkeit der chemischen Verschiebung. Abschirmung in einem Atom (wie bisher geschildert) Die Elektronenverteilung in einem Wasserstoffatom ist sphärisch. B 0 0 0000000 000000000 000000000
Teil 3 2D-NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 3 2D-NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Protonen-Protonen-Korrelation durch J-Kopplung Pulssequenz für ein klassisches 1D- 1 H-NMR
Teil 3 2D-NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Protonen-Protonen-Korrelation durch J-Kopplung Pulssequenz für ein klassisches 1D- 1 H-NMR
Kurs "Spektroskopische Methoden in der Anorganischen und Organischen Chemie" Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt 1)
 Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt ) Zum Lösungsmittel: Das Kohlenstoffspektrum zeigt bei 77 ppm drei gleich große äquidistante Signale. Diese stammen von CDC 3. Chemische Verschiebungen
Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt ) Zum Lösungsmittel: Das Kohlenstoffspektrum zeigt bei 77 ppm drei gleich große äquidistante Signale. Diese stammen von CDC 3. Chemische Verschiebungen
Strukturaufklärung in der Organischen Chemie I
 Strukturaufklärung in der Organischen Chemie I 1 Empfohlene Literatur 1. Spektroskopische Methoden in der organischen Chemie M. Hesse, H. Meier, B. Zeeh, Thieme-Verlag, 9. Auflage, 2016, 90 Gute Einführung
Strukturaufklärung in der Organischen Chemie I 1 Empfohlene Literatur 1. Spektroskopische Methoden in der organischen Chemie M. Hesse, H. Meier, B. Zeeh, Thieme-Verlag, 9. Auflage, 2016, 90 Gute Einführung
Z 12 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN
 ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie
 Fragenkatalog AC III NMR Teil 3 (Fröhlich) Die Boltzmann-Verteilung lautet: 1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie bezeichnet die Anzahl der Teilchen
Fragenkatalog AC III NMR Teil 3 (Fröhlich) Die Boltzmann-Verteilung lautet: 1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie bezeichnet die Anzahl der Teilchen
NMR-Spektroskopie. Magnet. Steuerung. Probenrohr Spinner. Shimspulen. B -Spulen. Gradient 2. Vorverstärker
 NMR-Spektroskopie Magnet Steuerung He He CPU Frequenz Pulsform Pulsleistung Zeitkontrolle Temperierung Gradienten Shim/Lock/Gas Vorverstärker N N Probenrohr Spinner Shimspulen B -Spulen Gradient 2 H K
NMR-Spektroskopie Magnet Steuerung He He CPU Frequenz Pulsform Pulsleistung Zeitkontrolle Temperierung Gradienten Shim/Lock/Gas Vorverstärker N N Probenrohr Spinner Shimspulen B -Spulen Gradient 2 H K
Kernmagnetismus und Magnetfelder
 Kernmagnetismus und Magnetfelder. Kernspin Die meisten Kerne besitzen einen Eigendrehimpuls oder P ist gequantelt P = h I(I + ) h = h und h: das Plancksche Wirkungsquantum. π I: Kernspinquantenzahl (kurz:
Kernmagnetismus und Magnetfelder. Kernspin Die meisten Kerne besitzen einen Eigendrehimpuls oder P ist gequantelt P = h I(I + ) h = h und h: das Plancksche Wirkungsquantum. π I: Kernspinquantenzahl (kurz:
18. Strukturaufklärung in der Organischen Chemie
 Inhalt Index 18. Strukturaufklärung in der Organischen Chemie Die Kenntnis der zahlreichen organischen Reaktionen und funktionellen Gruppen, die in den vorangegangenen Kapiteln vorgestellt wurden, sollten
Inhalt Index 18. Strukturaufklärung in der Organischen Chemie Die Kenntnis der zahlreichen organischen Reaktionen und funktionellen Gruppen, die in den vorangegangenen Kapiteln vorgestellt wurden, sollten
Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006
 Prüfungen Analytische Chemie Mittwoch, 27. September 2006 Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Prüfungen Analytische Chemie Mittwoch, 27. September 2006 Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Seminar WiSe 2015/2016. PD Dr. Markus Nett. Leibniz Institut für Naturstoff Forschung und Infektionsbiologie E mail: jena.
 Kernresonanzspektroskopie Seminar WiSe 2015/2016 PD Dr. Markus Nett Nachwuchsgruppenleiter Leibniz Institut für Naturstoff Forschung und Infektionsbiologie E mail: markus.nett@hki jena.de NMR = nuclear
Kernresonanzspektroskopie Seminar WiSe 2015/2016 PD Dr. Markus Nett Nachwuchsgruppenleiter Leibniz Institut für Naturstoff Forschung und Infektionsbiologie E mail: markus.nett@hki jena.de NMR = nuclear
Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL. Musterlösung. für den Teil Spektroskopie
 Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Musterlösung für den Teil Spektroskopie Vorname:... Name:... Jede Aufgabe wird separat bewertet.
Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Musterlösung für den Teil Spektroskopie Vorname:... Name:... Jede Aufgabe wird separat bewertet.
Spektroskopie-Seminar SS Infrarot-Spektroskopie. Infrarot-Spektroskopie
 Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Studiengang Chemie Gruppen Nr. : 2 OCP II Übung Nr. : 2. Jael Bürki. NMR-Kurs OCP II Beginn: Ende: Abgabe:
 Studiengang Chemie Gruppen Nr. : 2 OCP II Übung Nr. : 2 Verfasser: Dozent: Michael Ott Jael Bürki Dr. Stefan Höck NMR-Kurs OCP II Beginn: 23.02.13 Ende: 09.04.13 Abgabe: 09.04.13 Inhaltsverzeichnis 1 Aufgabenstellung...
Studiengang Chemie Gruppen Nr. : 2 OCP II Übung Nr. : 2 Verfasser: Dozent: Michael Ott Jael Bürki Dr. Stefan Höck NMR-Kurs OCP II Beginn: 23.02.13 Ende: 09.04.13 Abgabe: 09.04.13 Inhaltsverzeichnis 1 Aufgabenstellung...
Aufgabe 1: (18 Punkte)
 Aufgabe 1: (18 Punkte) In der Arbeitsgruppe Hilt wurde folgende Reaktionssequenz durchgeführt: A H 10 H B O O O 1 1 2 2 + 10 3 3 4 4 Δ DA- Produkt 6-9 5 5 6-9 2 Ph Ph Co(dppe) 2 3 3 4 4 Im ersten Reaktionsschritt
Aufgabe 1: (18 Punkte) In der Arbeitsgruppe Hilt wurde folgende Reaktionssequenz durchgeführt: A H 10 H B O O O 1 1 2 2 + 10 3 3 4 4 Δ DA- Produkt 6-9 5 5 6-9 2 Ph Ph Co(dppe) 2 3 3 4 4 Im ersten Reaktionsschritt
III. Strukturbestimmung organischer Moleküle
 III. Strukturbestimmung organischer Moleküle Röntgenstrukturbestimmung g Spektroskopie UV-VIS IR NMR Massenspektrometrie (MS) Röntgenstruktur eines bakteriellen Kohlenhydrats O O O O O O O C3 Röntgenstruktur
III. Strukturbestimmung organischer Moleküle Röntgenstrukturbestimmung g Spektroskopie UV-VIS IR NMR Massenspektrometrie (MS) Röntgenstruktur eines bakteriellen Kohlenhydrats O O O O O O O C3 Röntgenstruktur
Spektroskopie-Seminar WS 17/18 3 Infrarot-Spektroskopie. Infrarot-Spektroskopie
 WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
Die Anwendung der Kernmagnetischen Resonanz (NMR) Spektroskopie zur Strukturaufklärung
 Die Anwendung der Kernmagnetischen Resonanz (NMR) Spektroskopie zur Strukturaufklärung - eine kurze Einführung im Rahmen des C Grundpraktikums - Prof. Dr. Reinhard Meusinger Leiter der NMR Abteilung am
Die Anwendung der Kernmagnetischen Resonanz (NMR) Spektroskopie zur Strukturaufklärung - eine kurze Einführung im Rahmen des C Grundpraktikums - Prof. Dr. Reinhard Meusinger Leiter der NMR Abteilung am
Spektroskopische Methoden in der Organischen Chemie (OC IV) NMR Spektroskopie 1. Physikalische Grundlagen
 NMR Spektroskopie 1. Physikalische Grundlagen Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
NMR Spektroskopie 1. Physikalische Grundlagen Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
Kombinierte Übungen zur Spektroskopie Beispiele für die Bearbeitung
 Im folgenden soll gezeigt werden, daß es großen Spaß macht, spektroskopische Probleme zu lösen. Es gibt kein automatisches Lösungsschema, sondern höchstens Strategien, wie beim "Puzzle Lösen"; häufig hilft
Im folgenden soll gezeigt werden, daß es großen Spaß macht, spektroskopische Probleme zu lösen. Es gibt kein automatisches Lösungsschema, sondern höchstens Strategien, wie beim "Puzzle Lösen"; häufig hilft
P105. Konstitution. Massenspektrum 100 % m/z
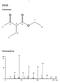 1 P105 Konstitution 7 1 2 6 8 4 5 Massenspektrum 100 % 4 116 50 7 101 29 55 88 15 61 10 14 158 0 0 50 100 150 m/z 2 Direkte Fragmentierungen: 4 115 11 45 129 29 85 7 Damit lassen sich die prominenten Signale
1 P105 Konstitution 7 1 2 6 8 4 5 Massenspektrum 100 % 4 116 50 7 101 29 55 88 15 61 10 14 158 0 0 50 100 150 m/z 2 Direkte Fragmentierungen: 4 115 11 45 129 29 85 7 Damit lassen sich die prominenten Signale
INADEQUATE 13 C, 13 C-COSY
 INADEQUATE 13 C, 13 C-COSY Die bisher diskutierten Korrelationsmethoden beruhen auf Protonen. Da das eigentliche Skelett eines organischen Moleküls das Kohlenstoffgerüst ist, wäre es in einigen Fällen
INADEQUATE 13 C, 13 C-COSY Die bisher diskutierten Korrelationsmethoden beruhen auf Protonen. Da das eigentliche Skelett eines organischen Moleküls das Kohlenstoffgerüst ist, wäre es in einigen Fällen
NMR-Spektroskopie Teil 2
 BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
Methodische Ansätze zur Strukturaufklärung: Rnt. - Kernmagnetische Resonanzspektroskopie (NMR)
 ? Methodische Ansäte ur Strukturaufklärung: - Rastersondenmikroskopie (AFM, SPM) SPM - Röntgenbeugung Rnt. - Elektronenspektroskopie (UV-vis) UV-vis - Schwingungsspektroskopie (IR) IR - Massenspektroskopie
? Methodische Ansäte ur Strukturaufklärung: - Rastersondenmikroskopie (AFM, SPM) SPM - Röntgenbeugung Rnt. - Elektronenspektroskopie (UV-vis) UV-vis - Schwingungsspektroskopie (IR) IR - Massenspektroskopie
IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC
 IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC Peter.Bellstedt@uni-jena.de Terminübersicht (14 täg.) Gruppe 1 Gruppe 2 1. Seminar
IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC Peter.Bellstedt@uni-jena.de Terminübersicht (14 täg.) Gruppe 1 Gruppe 2 1. Seminar
Spektroskopie in der Organischen Chemie. Spin-Entkopplung
 Spin-Entkopplung Spin-Spin-Kopplung zwischen nichtäquivalenten Kernen führt zur Aufspaltung der Signale der Kopplungspartner: im Falle größerer Spinsysteme können komplexe Multiplettsignale entstehen.
Spin-Entkopplung Spin-Spin-Kopplung zwischen nichtäquivalenten Kernen führt zur Aufspaltung der Signale der Kopplungspartner: im Falle größerer Spinsysteme können komplexe Multiplettsignale entstehen.
Spektroskopische Methoden in der Organischen Chemie (OC IV)
 2 3 4 O 1 2 3 1 N 5 6 O 5 4 6 Probleme bei der Interpretation von NMR Spektren großer Moleküle Zuordnung der Resonanzen Bestimmung der geometrischen Beziehungen (Bindungen, Abstände, Winkel) zwischen den
2 3 4 O 1 2 3 1 N 5 6 O 5 4 6 Probleme bei der Interpretation von NMR Spektren großer Moleküle Zuordnung der Resonanzen Bestimmung der geometrischen Beziehungen (Bindungen, Abstände, Winkel) zwischen den
Infrarot-Spektroskopie
 SoSe 19 Infrarot-Spektroskopie E = h v = h c ሚθ E = Energie; h = Planck sches Wirkungsquantum; v = Frequenz; c = Lichtgeschwindigkeit, ሚθ = Wellenzahl 1 3.1 Schwingungsmodi T / % Moleküle werden mit Licht
SoSe 19 Infrarot-Spektroskopie E = h v = h c ሚθ E = Energie; h = Planck sches Wirkungsquantum; v = Frequenz; c = Lichtgeschwindigkeit, ሚθ = Wellenzahl 1 3.1 Schwingungsmodi T / % Moleküle werden mit Licht
Grundlagen der NMR-Spektroskopie
 Westfälische Wilhelms-Universität Münster Institut für Pharmazeutische und Medizinische Chemie 8. Semester Übersicht: Einleitung Physikalische Grundlagen Magnetische Kerne Resonanz Spektrometer 1 Chem.
Westfälische Wilhelms-Universität Münster Institut für Pharmazeutische und Medizinische Chemie 8. Semester Übersicht: Einleitung Physikalische Grundlagen Magnetische Kerne Resonanz Spektrometer 1 Chem.
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
4 Synthesen antiprionen-aktiver Verbindungen
 4 Synthesen antiprionen-aktiver Verbindungen Quinacrinanaloga (Grundstruktur C) 77 4 Synthesen antiprionen-aktiver Verbindungen 4.1 Synthesen der Quinacrinanaloga (Grundstruktur C) Die Synthesen der Quinacrinanaloga
4 Synthesen antiprionen-aktiver Verbindungen Quinacrinanaloga (Grundstruktur C) 77 4 Synthesen antiprionen-aktiver Verbindungen 4.1 Synthesen der Quinacrinanaloga (Grundstruktur C) Die Synthesen der Quinacrinanaloga
Polarisationstransfer
 Polarisationstransfer Schon früh in der Geschichte der NMR-Spektroskopie hat man Experimente durchgeführt, bei denen auf einzelne Signale, d.h. bestimmte Spinübergänge, selektiv mit einer B 2 -Frequenz
Polarisationstransfer Schon früh in der Geschichte der NMR-Spektroskopie hat man Experimente durchgeführt, bei denen auf einzelne Signale, d.h. bestimmte Spinübergänge, selektiv mit einer B 2 -Frequenz
Vorlesung Einführung in die NMR- und IR-Spektroskopie
 c) b) a) x 8 50 45 40 35 30 25 20 15 ppm Abb. 22: 75,5 MHz 13 C-NMR-Spektren von Cholesterylacetat in CDCl 3. a) ohne 1 H- Entkopplung; b) mit invers gepulster 1 H-Entkopplung; c) mit 1 H-Breitband- Entkopplung.
c) b) a) x 8 50 45 40 35 30 25 20 15 ppm Abb. 22: 75,5 MHz 13 C-NMR-Spektren von Cholesterylacetat in CDCl 3. a) ohne 1 H- Entkopplung; b) mit invers gepulster 1 H-Entkopplung; c) mit 1 H-Breitband- Entkopplung.
Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIOL. Musterlösung. für den Teil Spektroskopie
 Prüfungen Analytische Chemie Samstag, 9. Februar 2008 Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIL Musterlösung für den Teil Spektroskopie Vorname:... Name:... Jede Aufgabe wird separat bewertet.
Prüfungen Analytische Chemie Samstag, 9. Februar 2008 Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIL Musterlösung für den Teil Spektroskopie Vorname:... Name:... Jede Aufgabe wird separat bewertet.
Dynamische Prozesse Chemischer Austausch
 Dynamische Prozesse Chemischer Austausch Weil die Messfrequenz der Kernresonanz (100 bis 900 MHz, also ca. 10 8 bis 10 9 s -1 ) in einem Frequenzbereich liegt, in dem auch viele Molekülbewegungen (Moleküldynamik)
Dynamische Prozesse Chemischer Austausch Weil die Messfrequenz der Kernresonanz (100 bis 900 MHz, also ca. 10 8 bis 10 9 s -1 ) in einem Frequenzbereich liegt, in dem auch viele Molekülbewegungen (Moleküldynamik)
Zentralabstand b, Spaltbreite a. Dreifachspalt Zentralabstand b, Spaltbreite a. Beugungsgitter (N Spalte, N<10 4, Abstand a)
 Doppelspalt (ideal) Doppelspalt (real) Zentralabstand b, Spaltbreite a Dreifachspalt Zentralabstand b, Spaltbreite a Beugungsgitter (N Spalte, N
Doppelspalt (ideal) Doppelspalt (real) Zentralabstand b, Spaltbreite a Dreifachspalt Zentralabstand b, Spaltbreite a Beugungsgitter (N Spalte, N
NMR Spektroskopie. Aufgaben
 hemische Verschiebung 1. Zeichnen Sie zu den nachfolgend aufgeführten Stoffen die Strukturformeln! Unterscheiden Sie dann zwischen chemisch äquvalenten und nichtäquivalenten Kernen. Bezeichnen Sie die
hemische Verschiebung 1. Zeichnen Sie zu den nachfolgend aufgeführten Stoffen die Strukturformeln! Unterscheiden Sie dann zwischen chemisch äquvalenten und nichtäquivalenten Kernen. Bezeichnen Sie die
Spektroskopie in der Organischen Chemie. 1 H, 1 H-Kopplungskonstanten. Geminale Kopplungen
 Spektroskopie in der rganischen hemie Geminale Kopplungen 1, 1 -Kopplungskonstanten Wenn sich die beiden Kopplungspartner (wie Zwillinge; lat.: gemini) am gleichen Kohlenstoffatom befinden, also nur zwei
Spektroskopie in der rganischen hemie Geminale Kopplungen 1, 1 -Kopplungskonstanten Wenn sich die beiden Kopplungspartner (wie Zwillinge; lat.: gemini) am gleichen Kohlenstoffatom befinden, also nur zwei
Organische Chemie I Molekül der Woche - Azulen
 I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
1 Grundbegriffe, Meßgrößen, Meßverfahren in Kürze
 Grundbegriffe, Meßgrößen, Meßverfahren in Kürze. hemische Verschiebung Als chemische Verschiebung bezeichnet man die Abängigkeit der Larmorfrequenz eines Kernspins von seiner chemischen Umgebung. Der Kernspin
Grundbegriffe, Meßgrößen, Meßverfahren in Kürze. hemische Verschiebung Als chemische Verschiebung bezeichnet man die Abängigkeit der Larmorfrequenz eines Kernspins von seiner chemischen Umgebung. Der Kernspin
Kernresonanzspektroskopie
 Gleich geht s los! Kernresonanzspektroskopie 1. Geschichtliche Entwicklung 2. Physikalische Grundlagen 3. Das NMR-Spektrometer 4. Anwendung der 1 H-NMR-Spektren zur Analyse der Konstitution von Molekülen
Gleich geht s los! Kernresonanzspektroskopie 1. Geschichtliche Entwicklung 2. Physikalische Grundlagen 3. Das NMR-Spektrometer 4. Anwendung der 1 H-NMR-Spektren zur Analyse der Konstitution von Molekülen
Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil III. Peter Schmieder AG NMR
 Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil III Programm 2/92 Was haben wir uns letztes Mal angeschaut: Wie beschreibt man Experimente mit Produktoperatoren Wie funktioniert
Vorlesung Moderne Methoden der Strukturaufklärung - NMR-Spektroskopie Teil III Programm 2/92 Was haben wir uns letztes Mal angeschaut: Wie beschreibt man Experimente mit Produktoperatoren Wie funktioniert
Homonukleare Korrelationsspektroskopie (COSY)
 Homonukleare Korrelationsspektroskopie (COSY) Hier wird ähnlich wie bei HETCOR in beiden Dimensionen die chemische Verschiebung abgebildet. Im homonuklearen Fall ( 1 H, 1 H COSY) jedoch, ist es in beiden
Homonukleare Korrelationsspektroskopie (COSY) Hier wird ähnlich wie bei HETCOR in beiden Dimensionen die chemische Verschiebung abgebildet. Im homonuklearen Fall ( 1 H, 1 H COSY) jedoch, ist es in beiden
Einführung in die NMR-Spektroskopie im Rahmen des Praktikums OC-II
 Einführung in die NMR-Spektroskopie im Rahmen des Praktikums O-II Till Opatz Kerne im statischen Magnetfeld Zeeman-Aufspaltung -1-3/2 Energie -1/2 +1/2 0 +1-1/2 +1/2-3/2 I = 1/2 I = 1 I = 3/2 Insgesamt
Einführung in die NMR-Spektroskopie im Rahmen des Praktikums O-II Till Opatz Kerne im statischen Magnetfeld Zeeman-Aufspaltung -1-3/2 Energie -1/2 +1/2 0 +1-1/2 +1/2-3/2 I = 1/2 I = 1 I = 3/2 Insgesamt
Schriftliche Prüfung BSc Frühling 2006 D CHAB/BIOL. Musterlösung. für den Teil Spektroskopie
 Prüfungen Analytische Chemie Mittwoch, 8. März 2006 Schriftliche Prüfung BSc Frühling 2006 D CAB/BIL Musterlösung für den Teil Spektroskopie Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die
Prüfungen Analytische Chemie Mittwoch, 8. März 2006 Schriftliche Prüfung BSc Frühling 2006 D CAB/BIL Musterlösung für den Teil Spektroskopie Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Kernmagnetische Resonanzspektroskopie. N Nuclear M Magnetic R Resonance Beobachtung magnetisch aktiver Kerne in einem äußeren Magnetfeld
 NMR- SPEKTROSKOPIE Prüfungsfrage Radiospektroskopische Methode: NMR. Das Spin und magnetische Moment, die Bedingung der Resonanz, Spektralspaltung, chemische Verschiebung. Kernmagnetische Resonanzspektroskopie
NMR- SPEKTROSKOPIE Prüfungsfrage Radiospektroskopische Methode: NMR. Das Spin und magnetische Moment, die Bedingung der Resonanz, Spektralspaltung, chemische Verschiebung. Kernmagnetische Resonanzspektroskopie
Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013
 Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013 Universität Leipzig Fakultät für Chemie und Mineralogie Wasserdampfdestillation von Anisöl aus Anissamen Anton Werwein, Richard Cybik
Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013 Universität Leipzig Fakultät für Chemie und Mineralogie Wasserdampfdestillation von Anisöl aus Anissamen Anton Werwein, Richard Cybik
Präparat Organische Analyse. Synthesepraktikum Assoc. Prof. Michael Schnürch
 Präparat Organische Analyse Synthesepraktikum 163.145 Assoc. Prof. Michael Schnürch Aufgabenstellung Trennung eines 3 Komponentengemisches 2 Neutralstoffe und 1 Verbindung mit sauren/basischen Eigenschaften
Präparat Organische Analyse Synthesepraktikum 163.145 Assoc. Prof. Michael Schnürch Aufgabenstellung Trennung eines 3 Komponentengemisches 2 Neutralstoffe und 1 Verbindung mit sauren/basischen Eigenschaften
NOESY und ROESY. Wir hatten gesehen (NMR-8), dass die Intensität eines 1 B
 NOESY und ROESY Wir hatten gesehen (NMR-8), dass die Intensität eines 1 B -Signals kann durch ein Entkopplungsexperiment verändert werden kann. Wird der Über- 2 A C gang eines ausgewählten 1 -Kerns S für
NOESY und ROESY Wir hatten gesehen (NMR-8), dass die Intensität eines 1 B -Signals kann durch ein Entkopplungsexperiment verändert werden kann. Wird der Über- 2 A C gang eines ausgewählten 1 -Kerns S für
Schriftliche Prüfung BSc Herbst 2007
 Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
