Instructions for use. Fast Track 2-CAT RIA. Please use only the valid version of the Instructions for Use provided with the kit BA R-6500
|
|
|
- Inge Becke
- vor 5 Jahren
- Abrufe
Transkript
1 Instructions for use 2-CAT RIA Fast Track BA R-6500
2 2-CAT RIA Fast Track 1. Introduction English 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative determination of Adrenaline (Epinephrine) and Noradrenaline (Norepinephrine) in plasma and urine. Adrenaline (epinephrine) and noradrenaline (norepinephrine) are extracted by using a cis-diol- specific affinity gel, acylated and then converted enzymatically. The assay procedure follows the basic principle of radioimmunoassay, involving competition between a radioactive and a non-radioactive antigen for a fixed number of antibody binding sites. The amount of 125 I- labelled antigen bound to the antibody is inversely proportional to the analyte concentration of the sample. When the system is in equilibrium, the antibody bound radioactivity is precipitated with a second antibody in the presence of polyethylene glycol. The precipitate is counted in a gamma counter. Quantification of unknown samples is achieved by comparing their activity with a reference curve prepared with known standards. 1.2 Clinical application In humans the catecholamines adrenaline (epinephrine), noradrenaline (norepinephrine) and dopamine are neurotransmitters of the sympathetic nervous system and are involved in many physiological processes. The sympathetic nervous system sets the body to a heightened state of alert, also called as the body s fight-orflight response. In the human body the catecholamines and their metabolites indicate the adaption of the body to acute and chronic stress. Next to the metanephrine/normetanephrine the catecholamines are important for the diagnosis and the follow-up of tumors of the sympathoadrenal system like the pheochromocytoma. The quantitative determination of catecholamines in urine is preferred for the diagnosis of these tumors, whereas the determination of catecholamines in plasma is medically sensible for the localization of the tumor and for function testing. Values above the cut-off can provide an indication for neuroendocrine tumors. However, in literature various diseases like hypertension, cardiovascular diseases, schizophrenia and manic depression are described with different levels of catecholamines. Therapeutic consequences should never be based on laboratory results alone even if all test results are in agreement with the items as under point Procedural cautions, guidelines and warnings. Any laboratory result is only a part of the total clinical picture of the patient. Only in cases where the laboratory results are in an acceptable agreement with the overall clinical picture of the patient it can be used for therapeutic consequences. The test result itself should never be the sole determinant for deriving any therapeutic consequences. 2. Procedural cautions, guidelines, warnings and limitations 2.1 Precautions, guidelines and warnings (1) This kit is intended for professional use only. Users should have a thorough understanding of this protocol for the successful use of this kit. Only the test instruction provided with the kit is valid and has to be used to run the assay. Reliable performance will only be attained by strict and careful adherence to the instructions provided. (2) This assay was validated for a certain type of sample as indicated in Intended Use (please refer to Chapter 1). Any off-label use of this kit is in the responsibility of the user and the manufacturer cannot be held liable. (3) The principles of Good Laboratory Practice (GLP) have to be followed. (4) In order to reduce exposure to potentially harmful substances, wear lab coats, disposable protective gloves and protective glasses where necessary. (5) All kit reagents - with the exception of Precipitating Reagent and specimens should be brought to room temperature and mixed gently but thoroughly before use. Avoid repeated freezing and thawing of reagents and specimens. (6) For the dilution or reconstitution purposes use deionized, distilled, or ultra-pure water. (7) The radioactive material ( 125 Iodine, half life 60 days, emitting ionizing X-radiation with 28 kev and G- radiation with 35.5 kev) may be received, acquired, possessed and used only by physicians, laboratories or hospitals. Products are dispatched on the basis of the nuclear and radiation protection regulations. (8) Duplicate determination of sample is highly recommended to be able to identify potential pipetting errors. (9) Once the test has been started, all steps should be completed without interruption. Make sure that the required reagents, materials and devices are prepared ready at the appropriate time. (10) Incubation times do influence the results. All tubes should be handled in the same order and time intervals. (11) To avoid cross-contamination of reagents, use new disposable pipette tips for dispensing each reagent, sample, standard and control. (12) A standard curve must be established for each run. Version: 15.0 Effective: /17
3 (13) The controls should be included in each run and fall within established confidence limits. The confidence limits are listed in the QC-Report provided with the kit. (14) Do not mix kit components with different lot numbers within a test and do not use reagents beyond expiry date as shown on the kit labels. (15) For information on hazardous substances included in the kit please refer to Safety Data Sheet (SDS). The Safety Data Sheet for this product is available directly on the website of the manufacturer or upon request. (16) The expected reference values reported in this test instruction are only indicative. It is recommended that each laboratory establishes its own reference intervals. (17) The results obtained with this test kit should not be taken as the sole reason for any therapeutic consequence (e.g. medication before a scheduled surgery) but have to be correlated to other diagnostic tests and clinical observations. (18) Kit reagents must be regarded as hazardous waste and disposed of according to national regulations. 2.2 Limitations Any inappropriate handling of samples or modification of this test might influence the results Interfering substances Plasma Samples containing precipitates or fibrin strands or which are haemolytic or lipemic might cause inaccurate results. 24-hour urine Please note the sample preparation! If the percentage of the final concentration of acid is too high, this will lead to incorrect results for the urine samples Drug interferences There are no known substances (drugs) which ingestion interferes with the measurement of catecholamine level in the sample High-Dose-Hook effect No hook effect was observed in this test. 3. Storage and stability Store the unopened reagents at 2-8 C until expiration date. Do not use components beyond the expiry date indicated on the kit labels. Once opened the reagents are stable for 1 month when stored at 2 8 C. 4. Materials 4.1 Content of the kit BA D-0090 BA R-0025 Adhesive Foil - Ready to use Adhesive Foils in a resealable pouch 1 x 4 foils Precipitating Reagent - Ready to use Goat anti-rabbit serum in PEG phosphate buffer 2 x 55 ml/vial, white cap BA R-6618 BA R-0050 BA R-0120 Hazards identification: Extraction Plate - Ready to use 2 x 48 well plates coated with boronate affinity gel in a resealable pouch Adjustment Buffer - Ready to use TRIS buffer 1 x 4 ml/vial, green cap 125 I Adrenaline - Ready to use 125 I labeled Adrenaline, red coloured 1 x 5.5 ml/vial, blue cap Radioactive, activity < 200 kbq Version: 15.0 Effective: /17
4 BA R-0220 Hazards identification: BA R-6110 BA R I Noradrenaline - Ready to use 125 I labeled Noradrenaline, red coloured 1 x 5.5 ml/vial, yellow cap Radioactive, activity < 200 kbq Adrenaline Antiserum - Ready to use Rabbit anti- Adrenaline antibody, blue coloured 1 x 5.25 ml/vial, blue cap Noradrenaline Antiserum - Ready to use Rabbit anti- Noradrenaline antibody, yellow coloured 1 x 5.25 ml/vial, yellow cap Standards and Controls - Ready to use Cat. no. Component Colour/ Cap Concentration ng/ml Concentration nmol/l Volume/ Vial BA R-6601 white ml BA R-6602 light yellow ml BA R-6603 orange ml BA R-6604 dark blue ml BA R-6605 light grey ml BA R-6606 black ml BA R-6651 light green Refer to QC-Report for expected value and 4 ml BA R-6652 dark red acceptable range! 4 ml Conversion: Adrenaline (ng/ml) x 5.46 = Adrenaline (nmol/l) Noradrenaline (ng/ml) x 5.91 = Noradrenaline (nmol/l) Acidic buffer with non-mercury stabilizer, spiked with defined quantity of adrenaline and noradrenaline BA R-6611 BA R-6613 BA R-6612 Hazards identification: Buffer with light alkaline ph 1 x 20 ml/vial, white cap Acylation Buffer - Ready to use Assay Buffer - Ready to use 1M hydrochloric acid and a non-mercury preservative 1 x 6 ml/vial, light grey cap Acylation Reagent - Ready to use Acylation reagent in DMF and DMSO 1 x 3 ml/vial, light red cap H226 Flammable liquid and vapour. H360D May damage the unborn child. H312 + H332 Harmful in contact with skin or if inhaled. H319 Causes serious eye irritation. BA R-6614 BA R-6615 Coenzyme - Ready to use S-adenosyl-L-methionine 1 x 4 ml/vial, purple cap Enzyme - Lyophilized Catechol-O-methyltransferase 4 vials, pink cap Version: 15.0 Effective: /17
5 BA R-6617 BA R-6619 Extraction Buffer - Ready to use Buffer containing carbonate 1 x 6 ml/vial, brown cap Hydrochloric Acid - Ready to use M Hydrochloric Acid, yellow coloured 1 x 20 ml/vial, dark green cap 4.2 Additional materials and equipment required but not provided in the kit - Calibrated precision pipettes to dispense volumes between µl - Polystyrene tubes and suitable rack - Temperature controlled water bath, heating block or incubator (37 C) - Centrifuge capable of at least 3,000 x g - Suitable device for aspirating or decanting - Shaker (shaking amplitude 3 mm; approx. 600 rpm) - Gamma counter - Vortex mixer - Absorbent material (paper towel) - Water (deionized, distilled or ultra-pure) 5. Sample collection and storage Plasma Whole blood should be collected by venipuncture into centrifuge tubes containing EDTA as anti-coagulant (e.g. Monovette TM or Vacuette TM for plasma) and centrifuged according to manufacturer s instructions at room temperature immediately after collection. Haemolytic and especially lipemic samples should not be used for the assay. Storage: up to 6 hours at 2-8 C, for longer period (up to 6 month) at -20 C. Repeated freezing and thawing should be avoided. Urine Spontaneous urine or 24-hour urine, collected in a bottle containing ml of 6 M HCl, can be used. If 24-hour urine is used please record the total volume of the collected urine. Storage: up to 48 hours at 2-8 C, up to 24 hours at room temperature, for longer periods (up to 6 month) at -20 C. Repeated freezing and thawing should be avoided. Avoid exposure to direct sunlight. 6. Test procedure Allow all reagents with the exception of Precipitating Reagent - to reach room temperature and mix thoroughly by gentle inversion before use. Number the assay tubes accordingly. Duplicates are recommended. Pipetted liquids should not adhere to the wall of the RIA tubes. If necessary please centrifuge the tubes for 1 minute at 500 x g to spin down adhering liquids. 6.1 Preparation of reagents Enzyme Solution Reconstitute the content of the vial labelled Enzyme with 1 ml water (deionized, distilled or ultra-pure) and mix thoroughly. Add 0.3 ml of Coenzyme followed by 0.7 ml of Adjustment Buffer. The total volume of the Enzyme Solution is 2.0 ml. The Enzyme Solution has to be prepared freshly prior to the assay (not longer than minutes in advance). Discard after use! Version: 15.0 Effective: /17
6 6.2 Sample preparation, extraction and acylation 1. Pipette 10 µl of standards and controls, 10 µl of urine samples and 300 µl of plasma samples into the respective wells of the Extraction Plate. 2. Add 250 µl of water (deionized, distilled, or ultra-pure) to the wells with standards, controls and urine samples. 3. Pipette 50 µl of Assay Buffer into all wells. 4. Pipette 50 µl of Extraction Buffer into all wells. 5. Cover the plate with adhesive foil. Incubate for 30 min at RT (20-25 C) on a shaker (approx. 600 rpm). 6. Remove the foil and empty the plate. Blot dry by tapping the inverted plate on absorbent material. 7. Pipette 1 ml water (deionized, distilled or ultra-pure) into all wells. Incubate the plate for 5 min at RT (20-25 C) on a shaker (approx. 600 rpm). Empty plate and blot dry by tapping the inverted plate on absorbent material. 8. Pipette 150 µl of Acylation Buffer into all wells. 9. Pipette 25 µl of Acylation Reagent into all wells. 10. Incubate 15 min at RT (20-25 C) on a shaker (approx. 600 rpm). 11. Empty the plate. Blot dry by tapping the inverted plate on absorbent material. 12. Pipette 1 ml water (deionized, distilled, or ultra-pure) into all wells. Incubate the plate for 5 min at RT (20-25 C) on a shaker (approx. 600 rpm). Empty plate and blot dry by tapping the inverted plate on absorbent material. 13. Pipette 150 µl of Hydrochloric Acid into all wells. 14. Cover plate with adhesive foil. Incubate 10 min at RT (20-25 C) on a shaker (approx. 600 rpm). Remove the foil. Do not decant the supernatant thereafter! The following volumes of the supernatant are needed for the subsequent RIA: Adrenaline 100 µl Noradrenaline 20 µl 6.3 Adrenaline RIA 1. Pipette 100 µl of Hydrochloric Acid into the tubes for the NSB. 2. Pipette 100 µl of the extracted standards, controls and samples into the respective tubes. 3. Pipette 25 µl of Enzyme Solution (refer to 6.1) into all tubes (except totals). 4. Mix thoroughly and incubate for 30 min at 37 C. 5. Pipette 50 µl of the 125 I Adrenaline into all tubes. 6. Pipette 50 µl of Adrenaline Antiserum into all tubes (except totals and NSB); mix thoroughly. 7. Cover tubes. Incubate for h (overnight) at 2-8 C. Alternatively incubate for 2 h at RT (20-25 C) on a shaker (approx. 600 rpm). 8. Mix the chilled (2-8 C) Precipitating Reagent thoroughly, pipette each 500 µl into all tubes (except totals), and mix on a vortex. 9. Incubate for 15 min at 2-8 C. 10. Centrifuge for 15 min at 3,000 x g, if possible in a refrigerated centrifuge. 11. Decant or aspirate the supernatant carefully (except totals). Blot the tubes dry and leave them upside down for 2 minutes. 12. Count all tubes for 1 min in a gamma counter. Version: 15.0 Effective: /17
7 6.4 Noradrenaline RIA 1. Pipette 20 µl of Hydrochloric Acid into the tubes for the NSB. 2. Pipette 20 µl of the extracted standards, controls and samples into the respective tubes. 3. Pipette 25 µl of Enzyme Solution (refer to 6.1) into all tubes (except totals). 4. Mix thoroughly and incubate for 30 min at 37 C. 5. Pipette 50 µl of the 125 I Noradrenaline into all tubes. 6. Pipette 50 µl of Noradrenaline Antiserum into all tubes (except totals and NSB); mix thoroughly. 7. Cover tubes. Incubate for h (overnight) at 2-8 C. Alternatively incubate for 2 h at RT (20-25 C) on a shaker (approx. 600 rpm). 8. Mix the chilled (2-8 C) Precipitating Reagent thoroughly, pipette each 500 µl into all tubes (except totals), and mix on a vortex. 9. Incubate for 15 min at 2-8 C. 10. Centrifuge for 15 min at 3,000 x g, if possible in a refrigerated centrifuge. 11. Decant or aspirate the supernatant carefully (except totals). Blot the tubes dry and leave them upside down for 2 minutes. 12. Count all tubes for 1 min in a gamma counter. 7. Calculation of results Measuring range Adrenaline Noradrenaline Urine ng/ml ng/ml Plasma pg/ml pg/ml Subtract the mean cpm of the non-specific binding NSB from the mean cpm of standards, controls and samples. The standard curve from which the concentrations in the samples can be read off, is obtained by plotting the percentage of (B-NSB)/ (B 0 -NSB) measured for the standards (linear, y-axis) against the corresponding standard concentrations (logarithmic, x-axis). Use a non-linear regression for curve fitting (e.g. spline, 4- parameter, akima). This assay is a competitive assay. This means: the counts are decreasing with increasing concentrations of the analyte. Counts found below the standard curve correspond to high concentrations of the analyte in the sample and have to be reported as being positive. Urine samples and controls The concentrations of the urine samples and the Controls 1 & 2 can be read directly from the standard curve. Calculate the 24 h excretion for each urine sample: µg/24h = µg/l x l/24h Plasma samples The read concentrations of the plasma samples have to be divided by 30. Conversion Adrenaline (ng/ml) x 5.46 = Adrenaline (nmol/l) Noradrenaline (ng/ml) x 5.91 = Noradrenaline (nmol/l) Expected reference values It is strongly recommended that each laboratory should determine its own reference values. Adrenaline Noradrenaline 24-hour urine < 20 µg/day (110 nmol/day) < 90 µg/day (535 nmol/day) Plasma < 100 pg/ml < 600 pg/ml 7.1 Quality control It is recommended to use control samples according to national regulations. Use controls at both normal and pathological levels. The kit controls or other commercial controls should fall within established confidence limits. The confidence limits of the kit controls are printed on the QC-Report. Version: 15.0 Effective: /17
8 7.2 Typical standard curves Examples, do not use for calculation! Adrenaline Noradrenaline B/B 0 (%) ng/ml 8. Assay characteristics Analytical Sensitivity (Limit of Detection) Analytical Specificity (Cross Reactivity) Precision ng/ml Adrenaline Noradrenaline Urine 0.2 ng/ml 1.1 ng/ml Plasma 4.1 pg/ml 42 pg/ml Substance Cross Reactivity (%) Adrenaline Noradrenaline Derivatized Adrenaline Derivatized Noradrenaline Derivatized Dopamine Metanephrine 0.7 < 0.01 Normetanephrine < Methoxytyramine < 0.01 < Methoxy-4-hydroxyphenylglycol < 0.01 < 0.01 Tyramine < 0.01 < 0.01 Phenylalanine, Caffenic acid, L-Dopa, Homovanillic acid, Tyrosine, 3-Methoxy-4-hydroxymandelic acid < 0.01 < 0.01 Intra-Assay Urine (n = 40) Intra-Assay Plasma (n = 40) Adrenaline Noradrenaline Sample Range (ng/ml) CV (%) Sample Range (pg/ml) CV (%) ± ± ± Adrenaline ± ± ± ± ± ± Noradrenaline ± ± ± Version: 15.0 Effective: /17
9 Inter-Assay Urine (n = 13) Inter-Assay Plasma (n = 14) Adrenaline Noradrenaline Sample Range (ng/ml) CV (%) Sample Range (pg/ml) CV (%) ± ± ± Adrenaline ± ± ± ± ± ± Noradrenaline ± ± ± Linearity Adrenaline Noradrenaline Serial dilution up to Range (%) Mean (%) Urine 1: Plasma 1: Urine 1: Plasma 1: Recovery Method Comparison versus HPLC* Adrenaline Noradrenaline Noradrenaline Concentration range Range (%) Mean (%) Urine ng/ml Plasma pg/ml Urine ng/ml Plasma pg/ml Urine HPLC = 1.23 RIA 0.12 r = 0.99; n = 21 Plasma HPLC = 1.27 RIA 0.14 r = 0.99; n = 20 *The concentrations were assessed using both the RIA and the HPLC method (external QC samples from UK NEQAS). The correlation between RIA and HPLC is excellent. This means, that the RIA measure equally good when compared to the UK NEQAS HPLC data. Please take in mind, that the UK control values are the mean of about 40 different HPLC users, and contain always one pathological sample per sending. Method Comparison Adrenaline Urine y = 0.85x 0.48 r = 0.97; n = 37 versus LC-MS/MS 9. References/Literature (1) Rostrum et al. Physiological effects of combined thermal and electrical muscle stimulation (ctems) in healthy individuals A pilot study. Scandinavian Journal of Clinical and Laboratory Investigation, 72(3): (2012) (2) Milman et al. Opioid Receptor Blockade Prevents Exercise-Associated Autonomic Failure in Humans. Diabetes, 61(6): (2012) (3) Vele et al. Opioid Receptor Blo ckade Improves Hypoglycemia-Associated Autonomic Failure in Type 1 Diabetes Mellitus. The Journal of Clinical Endocrinology & Metabolism, 96(11): (2011) Symbols: For updated literature or any other information please contact your local supplier. Storage temperature Expiry date Consult instructions for use Caution Manufacturer Batch code Content Catalogue number Contains sufficient for <n> tests For in-vitro diagnostic use only! CE labelled Version: 15.0 Effective: /17
10 2-CAT RIA 1. Einleitung Fast Track Deutsch 1.1 Verwendungszweck und Testprinzip 125 I Radioimmunoassay zur quantitativen Bestimmung von Adrenalin und Noradrenalin in Plasma und Urin. Adrenalin und Noradrenalin werden mittels eines cis-diol-spezifischen Boronat-Affinitätsgels extrahiert, danach azyliert und anschließend enzymatisch umgewandelt. Die Durchführung des RIA-Tests erfolgt nach den Grundprinzipien des Radioimmunoassays. Radioaktiv markiertes Antigen und nicht markiertes Antigen binden kompetitiv an eine definierte Anzahl von Antikörperbindungsstellen. Anschließend werden die Antigen-Antikörper-Komplexe mit einem zweiten Antikörper in Anwesenheit von PEG gefällt. Das Präzipitat wird nach zentrifugieren und dekantieren oder absaugen des Überstands in einem Gamma-Counter gemessen. Die Menge an radioaktiv gebundenem Antigen ist indirekt proportional zur Antigenkonzentration der Probe. Die Konzentrationen der unbekannten Proben werden mit Hilfe einer Standardkurve und Abgleich der gemessenen Aktivitäten ermittelt. 1.2 Klinische Anwendung Die Katecholamine Adrenalin (Epinephrine), Noradrenalin (Norepinephrine) und Dopamin sind Neurotransmitter des sympathischen Nervensystems und bewirken zahlreiche physiologische Prozesse im Menschen. Der Sympathikus versetzt den Körper in eine erhöhte Alarmbereitschaft. Folglich ist über die sekretierte Menge der Katecholamine und deren Abbauprodukte im Menschen die Adaption des Körpers an akuten und chronischen Stress bestimmbar. In der Diagnostik und Verlaufsbeurteilung von Tumoren des sympatho-adrenalen Systems wie z.b. dem Phäochromozytom, spielen die Katecholamine neben den Metanephrinen/Normetanephrinen eine entscheidende Rolle. Während für die Diagnosestellung die quantitative Bestimmung der Urinausscheidung bevorzugt wird, ist bei klinischen Funktionstesten sowie zur Lokalisation eines Tumors die Katecholaminbestimmung im Plasma sinnvoll. Werte oberhalb der Referenzbereiche können ein Hinweis auf neuroendokrine Tumore sein. Des Weiteren werden in der Literatur noch zahlreiche Krankheitsbilder wie z.b. Hypertonie, degenerativer Erkrankung des Herz-Kreislaufsystems, Schizophrenie und manische Depression mit einem erhöhten oder erniedrigten Sekretionslevel der Katecholamine beschrieben. Therapeutische Konsequenzen dürfen niemals allein auf Grund von Laborwerten herangezogen werden, auch wenn diese Werte in Übereinstimmung mit den Qualitätskriterien der Methode beurteilt werden. Jedes Laborergebnis trägt immer nur zu einem Teil des klinischen Bildes bei. Nur wenn die Laborergebnisse in akzeptabler Übereinstimmung mit dem klinischen Gesamtbild stehen, dürfen daraus therapeutische Konsequenzen abgeleitet werden. Die Laborwerte selbst dürfen niemals der alleinige Grund für daraus abgeleitete therapeutische Konsequenzen sein. 2. Verfahrenshinweise, Richtlinien, Warnungen und Anwendungsgrenzen 2.1 Verfahrenshinweise, Richtlinien und Warnungen (1) Dieses Kit ist nur für den gewerblichen Gebrauch bestimmt. Für eine erfolgreiche Anwendung dieses Kits benötigen die Anwender ein umfassendes Verständnis dieses Protokolls. Einzig die im Kit enthaltene Testanleitung ist gültig und bei der Durchführung des Assays zu verwenden. Für eine zuverlässige Leistung müssen die mitgelieferten Anweisungen genau und sorgfältig befolgt werden. (2) Dieser Assay wurde für die unter Verwendungszweck (siehe Kapitel 1) angegebene Probenart validiert. Jede nicht zugelassene Anwendung dieses Kits obliegt der Verantwortung des Anwenders und entbindet den Hersteller von jeglicher Haftung. (3) Die Grundsätze der Guten Laborpraxis (GLP) sind zu befolgen. (4) Bei Bedarf Laborkittel, geeignete Einweghandschuhe und Schutzbrille tragen, um die Exposition gegenüber potenziell gesundheitsgefährdenden Stoffen zu reduzieren. (5) Alle Reagenzien des Kits, mit Ausnahme des PREC-REAG, sowie die Proben sollten vor der Verwendung auf Raumtemperatur gebracht und vorsichtig gemischt werden. Wiederholtes Einfrieren und Auftauen von Reagenzien und Proben vermeiden. (6) Wenn die Verdünnung oder Rekonstitution mit Wasser erfolgen soll, hierfür deionisiertes, destilliertes oder ultra-pures Wasser verwenden. (7) Das radioaktive Material ( 125 Iod, Halbwertszeit 60 Tage, gibt eine ionisierende Röntgenstrahlung mit 28 kev und eine Gammastrahlung mit 35,5 kev ab) darf nur von Ärzten, Laboren oder Krankenhäusern in Empfang genommen, erworben, besessen und verwendet werden. Der Vertrieb des Produktes erfolgt unter Beachtung der strahlenschutzrechtlichen Bestimmungen. (8) Es ist sehr empfehlenswert, eine Doppelbestimmung der Proben durchzuführen, um mögliche Pipettierfehler erkennen zu können. Version: 15.0 Effective: /17
11 (9) Sobald der Test begonnen wurde, sollten alle Schritte ohne Unterbrechung ausgeführt werden. Es muss dafür gesorgt werden, dass die erforderlichen Reagenzien, Materialien und Geräte zur vorgesehenen Zeit einsatzbereit sind. (10) Die Inkubationszeiten haben Einfluss auf die Ergebnisse. Alle Röhrchen sollten in der gleichen Reihenfolge und zeitlichen Abfolge behandelt werden. (11) Zur Vermeidung einer Kontamination der Reagenzien ist bei jeder Abgabe eines Reagenzes, einer Probe, eines Standards und einer Kontrolle eine neue Einwegpipettenspitze zu verwenden. (12) Bei jeder Testanwendung muss eine Standardkurve erstellt werden. (13) Bei jeder Testanwendung sollten Kontrollen mitgetestet werden, deren Werte innerhalb der bekannten Vertrauensgrenzen liegen müssen. Die gültigen Vertrauensgrenzen der Kitkontrollen können dem QC- Report entnommen werden, der dem Kit beiliegt. (14) Komponenten von Kits mit unterschiedlichen Chargenbezeichnungen nicht im selben Test verwenden. Reagenzien nach dem auf dem Kitetikett angegebenen Verfalldatum nicht mehr benutzen. (15) Für Informationen zu den im Kit enthaltenen gesundheitsgefährdenden Stoffen siehe die Sicherheitsdatenblätter (SDS). Das Sicherheitsdatenblatt dieses Produkts ist direkt auf der Webseite des Herstellers abrufbar oder auf Anfrage erhältlich. (16) Die in dieser Testanleitung angegebenen erwarteten Referenzwerte dienen nur als Hinweis. Es wird empfohlen, dass jedes Labor seine eigenen Referenzbereiche erstellt. (17) Jegliche therapeutische Maßnahme (z.b. die Verabreichung von Medikamenten vor einer planmäßigen Operation) darf sich nicht allein auf die mit diesem Testkit erzielten Ergebnisse stützen, sondern muss im Zusammenhang mit anderen diagnostischen Untersuchungen und klinischen Beobachtungen abgewogen werden. (18) Die Reagenzien des Kits sind als gesundheitsgefährdende Abfälle zu betrachten und gemäß den nationalen Vorschriften zu entsorgen. 2.2 Grenzen des Tests Jede unsachgemäße Behandlung der Proben oder Modifikationen dieses Tests können die Ergebnisse beeinflussen Interferenzen Plasma Proben, die ein Präzipitat oder die Fibrinfäden enthalten oder die hämolytisch oder lipämisch sind, können zu ungenauen Ergebnissen führen. Sammelurin Probenvorbereitung beachten! Ist der Säuregehalt des 24 Stunden-Sammelurins zu hoch, führt dies zu falschen Ergebnissen der Urinproben Beeinflussung durch Medikamente Bislang sind uns keine Stoffe (Medikamente) bekannt, deren Einnahme die Bestimmung des Katecholamin- Gehaltes in der Probe beeinflusst High-Dose-Hook Effekt Ein Hook-Effekt tritt in diesem Test nicht auf. 3. Lagerung und Haltbarkeit Die ungeöffneten Reagenzien sind bei 2-8 C bis zum Verfallsdatum aufzubewahren. Die Reagenzien dürfen nach Überschreiten des Verfallsdatums nicht mehr verwendet werden. Einmal geöffnet sind die Reagenzien 1 Monat stabil, wenn sie bei 2 8 C gelagert werden. 4. Materialien 4.1 Reagenzien im Kit BA D-0090 Adhesive Foil - Gebrauchsfertig 4 Klebefolien in einem wiederverschließbaren Beutel 1 x 4 Folien BA R-0025 Precipitating Reagent - Gebrauchsfertig Ziege anti-kaninchen Serum in PEG Phosphatpuffer 2 x 55 ml/ Fläschchen, Deckel weiß BA R-0050 Adjustment Buffer - Gebrauchsfertig TRIS Puffer 1 x 4 ml/fläschchen, Deckel grün Version: 15.0 Effective: /17
12 BA R-0120 Mögliche Gefahren: BA R-0220 Mögliche Gefahren: BA R I Adrenaline - Gebrauchsfertig 125 I markiertes Adrenalin, rot gefärbt 1 x 5,5 ml/ Fläschchen, Deckel blau Radioaktiv, Aktivität < 200 kbq 125 I Noradrenaline - Gebrauchsfertig 125 I markiertes Noradrenalin, rot gefärbt 1 x 5,5 ml/ Fläschchen, Deckel gelb Radioaktiv, Aktivität < 200 kbq Adrenaline Antiserum - Gebrauchsfertig Kaninchen Anti- Adrenalin Antikörper, blau gefärbt 1 x 5,25 ml/fläschchen, Deckel blau BA R-6210 BA R-6611 BA R-6612 Mögliche Gefahren: Noradrenaline Antiserum - Gebrauchsfertig Kaninchen Anti- Noradrenalin Antikörper, gelb gefärbt 1 x 5,25 ml/fläschchen, Deckel gelb Puffer mit leicht basischem ph 1 x 20 ml/fläschchen, Deckel weiß Acylation Buffer - Gebrauchsfertig Acylation Reagent - Gebrauchsfertig Azylierungsreagenz in DMF und DMSO 1 x 3 ml/fläschchen, Deckel hellrot H226 Flüssigkeit und Dampf entzündbar. H360D Kann das Kind im Mutterleib schädigen. H312 + H332 Gesundheitsschädlich bei Hautkontakt oder Einatmen. H319 Verursacht schwere Augenreizung. Standards und Controls - Gebrauchsfertig Artikelnr. Komponente Deckelfarbe Konzentration ng/ml Konzentration nmol/l Volumen/ Fläschchen BA R-6601 weiß ml BA R-6602 hellgelb ml BA R-6603 orange ml BA R-6604 dunkelblau ml BA R-6605 hellgrau ml BA R-6606 schwarz ml BA R-6651 hellgrün Die zu erwartenden Konzentrationen und 4 ml BA R-6652 dunkelrot Akzeptanzbereiche sind auf dem QC-Report angegeben. 4 ml Umrechnung: Adrenalin (ng/ml) x 5,46 = Adrenalin (nmol/l) Noradrenalin (ng/ml) x 5,91 = Noradrenalin (nmol/l) Saurer Puffer mit quecksilberfreien Stabilisatoren, aufgestockt mit definierten Mengen Adrenalin und Noradrenalin BA R-6613 Assay Buffer - Gebrauchsfertig 1M Salzsäure mit quecksilberfreien Stabilisatoren 1 x 6 ml/fläschchen, Deckel hellgrau Version: 15.0 Effective: /17
13 BA R-6614 BA R-6615 BA R-6617 BA R-6618 S-adenosyl-L-methionine 1 x 4 ml/fläschchen, Deckel lila Coenzyme - Gebrauchsfertig Enzyme - Lyophilisat Catechol-O-methyltransferase 4 Fläschchen, Deckel hellrosa Carbonatpuffer 1 x 6 ml/fläschchen, Deckel braun Extraction Buffer - Gebrauchsfertig Extraction Plate - Gebrauchsfertig 2 x 48 Well Platte beschichtet mit Boronat Affinitätsgel in einem wiederverschließbaren Beutel. BA R M Salzsäure, gelb gefärbt Hydrochloric Acid - Gebrauchsfertig 1 x 20 ml/fläschchen, Deckel dunkelgrün 4.2 Nicht im Kit enthaltene aber zur Durchführung erforderliche Geräte und Reagenzien Kalibrierte Präzisionspipetten zum Pipettieren von µl RIA-Röhrchen (Polystyrol) mit passendem Ständer Absaug- oder Dekantiervorrichtung Wasserbad, Heizblock oder Wärmeschrank (37 C) Zentrifuge (möglichst mit Kühlung), mind x g Plattenschüttler (Schüttelhub von 3 mm, ca. 600 rpm) Vortex-Mischer Gamma-Counter Wasser (deionisiert, destilliert oder ultra-pur) saugfähige Unterlage 5. Probenmaterial und Lagerung Plasma Das durch Venenpunktion entnommene Vollblut in einer für EDTA-Plasma vorgesehenen Monovette (z.b. von Sarstedt) sammeln und das EDTA-Plasma direkt durch Zentrifugation (nach Angaben des Herstellers) von den übrigen Blutbestandteilen trennen. Lagerung: bis zu 6 Stunden bei 2-8 C; für längere Zeit (bis zu 6 Monate) bei -20 C Wiederholtes Einfrieren und Auftauen der Proben sollte vermieden werden. Urin Es kann Spontanurin oder 24 Stunden-Sammelurin verwendet werden (im Sammelbehälter werden zur Stabilisierung des Sammelurins ml 6 M HCl vorgelegt). Wird 24 Stunden-Sammelurin verwendet, ist es notwendig, das Volumen des Sammelurins zu bestimmen und für die spätere Auswertung der Ergebnisse zu notieren. Lagerung: bis zu 48 Stunden bei 2-8 C, bis zu 24 Stunden bei Raumtemperatur und für längere Zeit (bis zu 6 Monate) bei -20 C. Wiederholtes Einfrieren und Auftauen der Proben, sowie direktes Sonnenlicht vermeiden. 6. Testdurchführung Alle Reagenzien und Proben, mit Ausnahme des PREC-REAG, müssen vor dem Gebrauch auf Raumtemperatur gebracht und vorsichtig gemischt werden. Das Beschriften der Röhrchen ist erforderlich. Es empfiehlt sich, Doppelbestimmungen anzusetzen. Es ist erforderlich, die Röhrchen 1 Min bei 500 x g zu zentrifugieren, falls sich nach den jeweiligen Pipettierschritten Flüssigkeitsreste am Röhrchenrand befinden. Version: 15.0 Effective: /17
14 6.1 Vorbereitung der Reagenzien Enzymlösung Den Inhalt des Fläschchens ENZYME mit 1 ml Wasser (deionisiert, destilliert oder ultra-pur) lösen und gut mischen. 0,3 ml COENZYME und 0,7 ml ADJUST-BUFF dazu pipettieren (Endvolumen 2,0 ml). Die Enzymlösung darf erst Minuten vor Gebrauch angesetzt werden! Nach Gebrauch verwerfen! 6.2 Probenvorbereitung, Extraktion und Azylierung 1. Jeweils 10 µl der Standards, Kontrollen, Urinproben und 300 µl der Plasmaproben in die entsprechenden Kavitäten der ECTRACT-PLATE 48 pipettieren. 2. Jeweils 250 µl Wasser (deionisiert, destilliert oder ultra-pur) zu den Standards, Kontrollen und Urinproben hinzugeben. 3. Je 50 µl ASSAY-BUFF in alle Kavitäten pipettieren. 4. Je 50 µl ECTRACT-BUFF in alle Kavitäten pipettieren. 5. Platte mit FOIL abdecken und für 30 Min bei RT (20 25 C) auf einem Schüttler (ca. 600 rpm) inkubieren. 6. FOIL entfernen. Die Platte ausleeren und Restflüssigkeit durch Ausklopfen auf einer saugfähigen Unterlage entfernen ml Wasser (deionisiert, destilliert oder ultra-pur) in alle Kavitäten pipettieren. 5 Min bei RT (20 25 C) auf einem Schüttler (ca. 600 rpm) inkubieren. Die Platte ausleeren und Restflüssigkeit durch Ausklopfen auf einer saugfähigen Unterlage entfernen. 8. Jeweils 150 µl ACYL-BUFF in alle Kavitäten pipettieren. 9. Jeweils 25 µl ACYL-REAG in alle Kavitäten pipettieren Min bei RT (20 25 C) auf einem Schüttler (ca. 600 rpm) inkubieren. 11. Die Platte ausleeren und Restflüssigkeit durch Ausklopfen auf einer saugfähigen Unterlage entfernen. 12. Je 1 ml Wasser (deionisiert, destilliert oder ultra-pur) in alle Kavitäten pipettieren. 5 Min bei RT (20 25 C) auf einem Schüttler (ca. 600 rpm) inkubieren. Die Platte ausleeren und Restflüssigkeit durch Ausklopfen auf einer saugfähigen Unterlage entfernen. 13. Jeweils 150 µl HCL in alle Kavitäten pipettieren. 14. Platte mit FOIL abdecken und für 10 Min bei RT (20 25 C) auf einem Schüttler (ca. 600 rpm) schütteln. Überstand anschließend nicht verwerfen bzw. Platte nicht ausleeren! Von den Überständen werden für den nachfolgenden RIA folgende Volumina benötigt: Adrenalin 100 µl Noradrenalin 20 µl 6.3 Adrenalin RIA 1. Jeweils 100 µl HCL in die Röhrchen für die NSB pipettieren. 2. Jeweils 100 µl der extrahierten Standards, Kontrollen und Proben in die entsprechenden Röhrchen pipettieren. 3. Jeweils 25 µl Enzymlösung (siehe 6.1) in alle Röhrchen (außer Totalaktivität T) pipettieren. 4. Röhrchen gut mischen und 30 Min bei 37 C inkubieren. 5. Je 50 µl 125 I ADR MN in alle Röhrchen pipettieren. 6. Je 50 µl AS ADR MN in alle Röhrchen (außer Totalaktivität T und NSB) pipettieren. 7. Röhrchen abdecken und Stunden (über Nacht) bei 2 8 C inkubieren. Alternativ 2 Stunden bei RT (20 25 C) auf einem Schüttler (ca. 600 rpm) inkubieren. 8. Das vorgekühlte (2-8 C) PREC-REAG gründlich aufschütteln und jeweils 500 µl in alle Röhrchen (außer Totalaktivität T) pipettieren. Kurz mischen Min bei 2-8 C inkubieren Min bei 3000 x g - möglichst mit Kühlung - zentrifugieren. 11. Überstand absaugen oder vorsichtig dekantieren (außer Totalaktivität T). Röhrchen ausklopfen und für 2 Minuten umgedreht stehen lassen. 12. Röhrchen 1 Minute in einem Gamma-Counter messen. Version: 15.0 Effective: /17
15 6.4 Noradrenalin RIA 1. Jeweils 20 µl HCL in die Röhrchen für die NSB pipettieren. 2. Jeweils 20 µl der extrahierten Standards, Kontrollen und Proben in die entsprechenden Röhrchen pipettieren. 3. Jeweils 25 µl Enzymlösung (siehe 6.1) alle Röhrchen (außer Totalaktivität T) pipettieren. 4. Röhrchen gut mischen und 30 Min bei 37 C inkubieren. 5. Je 50 µl 125 I NAD NMN in alle Röhrchen pipettieren. 6. Je 50 µl AS NAD in alle Röhrchen (außer Totalaktivität T und NSB) pipettieren. 7. Röhrchen abdecken und Stunden (über Nacht) bei 2 8 C inkubieren. Alternativ 2 Stunden bei RT (20 25 C) auf einem Schüttler (ca. 600 rpm) inkubieren. 8. Das vorgekühlte (2-8 C) PREC-REAG gründlich aufschütteln und jeweils 500 µl in alle Röhrchen (außer Totalaktivität T) pipettieren. Kurz mischen Min bei 2-8 C inkubieren Min bei 3000 x g - möglichst mit Kühlung - zentrifugieren. 11. Überstand absaugen oder vorsichtig dekantieren (außer Totalaktivität T). Röhrchen ausklopfen und für 2 Minuten umgedreht stehen lassen. 12. Röhrchen 1 Minute in einem Gamma-Counter messen. 7. Berechnung der Ergebnisse Messbereich Adrenalin Noradrenalin Urin 0, ng/ml 1, ng/ml Plasma pg/ml pg/ml Der Mittelwert der cpm der Nicht-Spezifischen-Bindung NSB wird von den Mittelwerten der cpm der Standards, Kontrollen und Proben abgezogen. Die Standardkurve, mit deren Hilfe die Konzentration der unbekannten Proben ermittelt werden kann, wird nach Auftragen der (B-NSB)/(B 0 -NSB) für die Standards im linearen Maßstab auf der y-achse gegen die entsprechende Konzentration im logarithmischen Maßstab auf der x-achse, erstellt. Zur Kurvenberechnung wird eine nicht-lineare Regression (z.b.: spline, 4- parameter, akima) verwendet. Dieser Assay ist ein kompetitiver Assay. Das bedeutet, dass die Counts mit zunehmender Konzentration des Analyten sinken. Counts die unterhalb der Counts der Standardkurve liegen, entsprechen einer sehr hohen Konzentration des Analyten in der gemessenen Probe und müssen als positiv gewertet werden. Urinproben und Kontrollen Die Konzentrationen der Urinproben und Kontrollen 1 & 2 können direkt von der Standardkurve abgelesen werden. Berechnung der 24 Stunden Urinproben: µg/24h = µg/l x l/24h Plasmaproben Die aus der Kurve abgelesenen Konzentrationen müssen durch 30 dividiert werden. Umrechnung Adrenalin (ng/ml) x 5,46 = Adrenalin (nmol/l) Noradrenalin (ng/ml) x 5,91 = Noradrenalin (nmol/l) Erwartete Referenzwerte Es wird empfohlen, dass jedes Labor seine eigenen Referenzwerte ermittelt. Adrenalin Noradrenalin Sammelurin < 20 µg/tag (110 nmol/tag) < 90 µg/tag (535 nmol/tag) Plasma < 100 pg/ml < 600 pg/ml 7.1 Qualitätskontrolle Es wird empfohlen, mit jeder Testserie die Kitkontrollen und andere kommerzielle Kontrollproben im physiologischen und pathologischen Bereich mitzubestimmen, um die Leistungsfähigkeit des Tests zu überprüfen. Die Kontrollproben müssen innerhalb der angegebenen Vertrauensbereiche liegen. Die Vertrauensbereiche der Kitkontrollen sind im QC-Report aufgeführt. Version: 15.0 Effective: /17
16 7.2 Typische Standardkurven Beispiele, bitte nicht für die Auswertung verwenden! Adrenalin Noradrenalin B/B 0 (%) 8. Testcharakteristika ng/ml Analytische Sensitivität (Limit of Detection) Analytische Spezifität (Kreuzreaktion) Präzision ng/ml Adrenalin Noradrenalin Urin 0,2 ng/ml 1,1 ng/ml Plasma 4,1 pg/ml 42 pg/ml Substanz Kreuzreaktion (%) Adrenalin Noradrenalin Derivatisiertes Adrenalin 100 0,08 Derivatisiertes Noradrenalin 1,1 100 Derivatisiertes Dopamin 0,1 0,03 Metanephrin 0,7 < 0,01 Normetanephrin < 0,01 0,16 3-Methoxytyramin < 0,01 < 0,01 3-Methoxy-4-hydroxyphenylglycol < 0,01 < 0,01 Tyramin < 0,01 < 0,01 Phenylalanin, Coffeinsäure, L-Dopa, Homovanillinsäure, Tyrosin, 3-Methoxy-4-hydroxymandelsäure < 0,01 < 0,01 Intra-Assay Urin (n = 40) Intra-Assay Plasma (n = 40) Probe Bereich Bereich CV (%) Probe (ng/ml) (pg/ml) CV (%) 1 5,2 ± 0,7 12, ± 15,4 14,8 Adrenalin 2 9,1 ± 0,9 9,5 Adrenalin ± 24,4 9,4 3 21,1 ± 11,3 11, ± 60,5 7,1 1 86,8 ± 6,8 7, ± 85,8 9,3 Noradrenalin ± 10,9 8,9 Noradrenalin ± , ± 21,9 8, ± ,4 Version: 15.0 Effective: /17
17 Inter-Assay Urin (n = 13) Inter-Assay Plasma (n = 14) Probe Bereich Bereich CV (%) Probe (ng/ml) (pg/ml) CV (%) 1 4,9 ± 0,52 10,4 1 78,7 ± 13,6 17,2 Adrenalin 2 8,6 ± 0,88 10,2 Adrenalin ± 33,5 13,7 3 28,3 ± 4,9 17, ± 93,6 12,3 1 77,7 ± 8,5 10, ± ,4 Noradrenalin ± 9,4 9,1 Noradrenalin ± , ± 22,7 11, ± 391 9,7 Linearität Adrenalin Noradrenalin Serielle Mittelwert Bereich (%) Verdünnung bis: (%) Urin 1: Plasma 1: Urin 1: Plasma 1: Wiederfindung Methodenvergleich zur HPLC* Adrenalin Noradrenalin Noradrenalin Konzentrationsbereich Bereich (%) Mittelwert (%) Urin 1,8 32 ng/ml Plasma 14, pg/ml Urin 62,9 292 ng/ml Plasma pg/ml Urin HPLC = 1,23 RIA 0,12 r = 0,99; n = 21 Plasma HPLC = 1,27 RIA 0,14 r = 0,99; n = 20 *Die Konzentrationen wurden durch RIA und HPLC Messungen ermittelt (externe QC Proben von UK NEQAS). Die Ergebnisse der RIA und HPLC Messungen korrelieren sehr gut. Bitte beachten Sie, dass es sich bei den externen Kontrollwerten um einen Mittelwert aus über 40 verschiedenen HPLC Usern handelt, und dass immer eine der Proben im pathologischen Bereich liegt. Methodenvergleich zur LC-MS/MS Adrenalin Urin y = 0,85x 0,48 r = 0,97; n = Referenzen/Literatur (1) Rostrum et al. Physiological effects of combined thermal and electrical muscle stimulation (ctems) in healthy individuals A pilot study. Scandinavian Journal of Clinical and Laboratory Investigation, 72(3): (2012) (2) Milman et al. Opioid Receptor Blockade Prevents Exercise-Associated Autonomic Failure in Humans. Diabetes, 61(6): (2012) (3) Vele et al. Opioid Receptor Blockade Improves Hypoglycemia-Associated Autonomic Failure in Type 1 Diabetes Mellitus. The Journal of Clinical Endocrinology & Metabolism, 96(11): (2011) Aktuelle Literatur oder weitere Informationen zum Test werden Ihnen auf Anforderung von Ihrem Anbieter gerne zu Verfügung gestellt. Symbole: Lagertemperatur Hersteller Enthält Testmaterial für <n> Teste Verwendbar bis Chargennummer In vitro Diagnostikum Vor Gebrauch Packungsbeilage lesen Achtung Inhalt Katalog-Nummer CE gekennzeichnet Version: 15.0 Effective: /17
Instructions for use. Noradrenaline RIA KIPL0200
 Instructions for use RIA KIPL0200 Fast Track RIA 1. Introduction 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative determination of noradrenaline (norepinephrine) in
Instructions for use RIA KIPL0200 Fast Track RIA 1. Introduction 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative determination of noradrenaline (norepinephrine) in
Instructions for use. Fast Track 3-CAT RIA. Please use only the valid version of the Instructions for Use provided with the kit BA R-6600
 Instructions for use 3-CAT RIA Fast Track BA R-6600 3-CAT RIA Fast Track 1. Introduction English 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative determination of
Instructions for use 3-CAT RIA Fast Track BA R-6600 3-CAT RIA Fast Track 1. Introduction English 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative determination of
Simplex Easy DNA kit
 Simplex Easy DNA INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH Simplex Easy DNA kit Schnelle DNA-Extraktion aus Bakterien und Hefen Fast DNA-extraction from bacteria and yeast Art. Nr./ Order No.: SE 0100;
Simplex Easy DNA INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH Simplex Easy DNA kit Schnelle DNA-Extraktion aus Bakterien und Hefen Fast DNA-extraction from bacteria and yeast Art. Nr./ Order No.: SE 0100;
Normetanephrine Urine RIA
 Instructions for use Normetanephrine Urine RIA Fast Track KIPL0400 Normetanephrine Urine RIA 1. Introduction Fast Track 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative
Instructions for use Normetanephrine Urine RIA Fast Track KIPL0400 Normetanephrine Urine RIA 1. Introduction Fast Track 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative
Instructions for use 3-CAT ELISA KAPL
 Instructions for use 3-CAT ELISA KAPL10-1600 3-CAT ELISA 1. Introduction Fast Track English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of adrenaline
Instructions for use 3-CAT ELISA KAPL10-1600 3-CAT ELISA 1. Introduction Fast Track English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of adrenaline
Arbeitsanleitung. Dopamin ELISA. Enzymimmunoassay für die quantitative Bestimmung von. Dopamin in Plasma und Urin REF EA608/96.
 Arbeitsanleitung Dopamin ELISA Enzymimmunoassay für die quantitative Bestimmung von Dopamin in Plasma und Urin I V D REF EA608/96 12 x 8 2 8 C DLD Gesellschaft für Diagnostika und medizinische Geräte mbh
Arbeitsanleitung Dopamin ELISA Enzymimmunoassay für die quantitative Bestimmung von Dopamin in Plasma und Urin I V D REF EA608/96 12 x 8 2 8 C DLD Gesellschaft für Diagnostika und medizinische Geräte mbh
Melatonin Saliva Direct RIA
 Instructions for use Saliva Direct RIA KIPL3400 Saliva Direct RIA 1. Introduction 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the direct quantitative determination of melatonin
Instructions for use Saliva Direct RIA KIPL3400 Saliva Direct RIA 1. Introduction 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the direct quantitative determination of melatonin
3-Methoxytyramine Plasma RIA
 Instructions for use 3-Methoxytyramine Plasma RIA BA R-8800 3-Methoxytyramine Plasma RIA English 1. Introduction 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative determination
Instructions for use 3-Methoxytyramine Plasma RIA BA R-8800 3-Methoxytyramine Plasma RIA English 1. Introduction 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative determination
BCA Protein Assay (Pierce)
 BCA Protein Assay (Pierce) BCA assay: geeignet für geringe Proteinmengen!!! Die Proteine bilden mit Cu2+-Ionen in alkalischer Lösung einen Komplex (Biuret-Reaktion). Die Cu2+-Ionen des Komplexes werden
BCA Protein Assay (Pierce) BCA assay: geeignet für geringe Proteinmengen!!! Die Proteine bilden mit Cu2+-Ionen in alkalischer Lösung einen Komplex (Biuret-Reaktion). Die Cu2+-Ionen des Komplexes werden
WESAMIN GmbH & Co. KG
 WESAMIN GmbH & Co. KG Arbeitsanleitung AN-CAT - ELISA Enzymimmunoassay für die quantitative Bestimmung von Adrenalin / Noradrenalin in Plasma und Urin Inhaltsverzeichnis 1. Einführung und Testprinzip Seite
WESAMIN GmbH & Co. KG Arbeitsanleitung AN-CAT - ELISA Enzymimmunoassay für die quantitative Bestimmung von Adrenalin / Noradrenalin in Plasma und Urin Inhaltsverzeichnis 1. Einführung und Testprinzip Seite
Arbeitsanleitung CAT ELISA. Enzymimmunoassays für die quantitative Bestimmung von. Adrenalin / Noradrenalin / Dopamin in Plasma und Urin
 Arbeitsanleitung CAT ELISA Enzymimmunoassays für die quantitative Bestimmung von Adrenalin / Noradrenalin / Dopamin in Plasma und Urin I V D REF EA603/288 3 x 96 2 8 C DLD Gesellschaft für Diagnostika
Arbeitsanleitung CAT ELISA Enzymimmunoassays für die quantitative Bestimmung von Adrenalin / Noradrenalin / Dopamin in Plasma und Urin I V D REF EA603/288 3 x 96 2 8 C DLD Gesellschaft für Diagnostika
WESAMIN GmbH & Co. KG
 WESAMIN GmbH & Co. KG Arbeitsanleitung Noradrenalin - ELISA Enzymimmunoassay für die quantitative Bestimmung von Noradrenalin in Plasma und Urin j I V D REF N00 96 2 8 C WESAMIN GmbH & Co.KG / Gesellschaft
WESAMIN GmbH & Co. KG Arbeitsanleitung Noradrenalin - ELISA Enzymimmunoassay für die quantitative Bestimmung von Noradrenalin in Plasma und Urin j I V D REF N00 96 2 8 C WESAMIN GmbH & Co.KG / Gesellschaft
Normetanephrine Plasma RIA
 Instructions for use Normetanephrine Plasma RIA BA R-8200 Normetanephrine Plasma RIA 1. Introduction English 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative determination
Instructions for use Normetanephrine Plasma RIA BA R-8200 Normetanephrine Plasma RIA 1. Introduction English 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative determination
QuickGEN Sample Preparation Filtration
 QuickGEN Filtration INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH QuickGEN Sample Preparation Filtration Art. Nr./ Order No.: FSE 0100 Version 11/16 GEN-IAL GmbH Tel: 0049 2241 2522980 Fax: 0049 2241 2522989
QuickGEN Filtration INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH QuickGEN Sample Preparation Filtration Art. Nr./ Order No.: FSE 0100 Version 11/16 GEN-IAL GmbH Tel: 0049 2241 2522980 Fax: 0049 2241 2522989
Simplex Easy Wine Kit
 Simplex Easy Wine INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH Simplex Easy Wine Kit Schnelle DNA-Extraktion von Mikroorganismen aus Wein und Most Fast DNA-extraction from microorganisms in wine and grape
Simplex Easy Wine INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH Simplex Easy Wine Kit Schnelle DNA-Extraktion von Mikroorganismen aus Wein und Most Fast DNA-extraction from microorganisms in wine and grape
Instructions for use. Melatonin Direct RIA KIPL3300
 Instructions for use Melatonin Direct RIA KIPL3300 Melatonin Direct RIA 1. Introduction 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the direct quantitative determination of melatonin
Instructions for use Melatonin Direct RIA KIPL3300 Melatonin Direct RIA 1. Introduction 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the direct quantitative determination of melatonin
Normetanephrine Urine ELISA
 Instructions for use Urine ELISA Fast Track BA E-8500 Urine ELISA 1. Introduction Fast Track 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of in urine
Instructions for use Urine ELISA Fast Track BA E-8500 Urine ELISA 1. Introduction Fast Track 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of in urine
Instructions for use. Serotonin RIA KIPL0900
 Instructions for use RIA KIPL0900 RIA Fast Track 1. Introduction English 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative determination of in serum, urine, and platelets.
Instructions for use RIA KIPL0900 RIA Fast Track 1. Introduction English 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the quantitative determination of in serum, urine, and platelets.
ATEX-Check list. Compiled by: Date: Signature: Acceptable practice at the determination of flash point: Closed cup according to ISO 2719
 Fire and explosion hazard ATEX 137 1999/92/EG und ATEX 95 2014/34/EU Danger assessment and determination of explosion protection zone for the test space as well as the installation site ATEX-Check list
Fire and explosion hazard ATEX 137 1999/92/EG und ATEX 95 2014/34/EU Danger assessment and determination of explosion protection zone for the test space as well as the installation site ATEX-Check list
Reference Copy Only - DO NOT USE
 Instructions for use Normetanephrine Urine RIA Fast Track BA R-8500 Normetanephrine Urine RIA 1. Introduction Fast Track English 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the
Instructions for use Normetanephrine Urine RIA Fast Track BA R-8500 Normetanephrine Urine RIA 1. Introduction Fast Track English 1.1 Intended use and principle of the test 125 I Radioimmunoassay for the
Instructions for use. Fast Track. 2-MET Plasma ELISA. Please use only the valid version of the Instructions for Use provided with the kit BA E-8300
 Instructions for use 2-MET Plasma ELISA BA E-8300 2-MET Plasma ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of free Metanephrine
Instructions for use 2-MET Plasma ELISA BA E-8300 2-MET Plasma ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of free Metanephrine
QS Laborkompetenztest Frühjahr 2011
 Qualitätssicherung. Vom Erzeuger bis zur Ladentheke. QS Laborkompetenztest Frühjahr 2011 Bewertungsschema Laborkompetenztest Frühjahr 2011 Bestanden alle 6 Wirkstoffe identifiziert und mindestens 4 Wirkstoffe
Qualitätssicherung. Vom Erzeuger bis zur Ladentheke. QS Laborkompetenztest Frühjahr 2011 Bewertungsschema Laborkompetenztest Frühjahr 2011 Bestanden alle 6 Wirkstoffe identifiziert und mindestens 4 Wirkstoffe
Instructions for use. Dopamine ELISA KAPL10-0300
 Instructions for use ELISA KAPL10-0300 ELISA 1. Introduction Fast Track 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of dopamine in plasma and urine.
Instructions for use ELISA KAPL10-0300 ELISA 1. Introduction Fast Track 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of dopamine in plasma and urine.
Instructions for use. Noradrenaline ELISA KAPL
 Instructions for use e ELISA KAPL10-0200 e ELISA 1. Introduction Fast Track 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of noradrenaline (norepinephrine)
Instructions for use e ELISA KAPL10-0200 e ELISA 1. Introduction Fast Track 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of noradrenaline (norepinephrine)
Instructions for use. Fast Track. 2-MET Urine ELISA. Please use only the valid version of the Instructions for Use provided with the kit BA E-8600
 Instructions for use 2-MET Urine ELISA Fast Track BA E-8600 Fast Track 2-MET Urine ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination
Instructions for use 2-MET Urine ELISA Fast Track BA E-8600 Fast Track 2-MET Urine ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination
Metanephrine Plasma ELISA
 Instructions for use Metanephrine Plasma ELISA BA E-8100 Metanephrine Plasma ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination
Instructions for use Metanephrine Plasma ELISA BA E-8100 Metanephrine Plasma ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination
Dopamin High Sensitive ELISA
 Arbeitsanleitung Dopamin High Sensitive ELISA Enzymimmunoassay für die quantitative Bestimmung von Dopamin REF EA634/96 12 x 8 2 8 C DLD Gesellschaft für Diagnostika und medizinische Geräte mbh Adlerhorst
Arbeitsanleitung Dopamin High Sensitive ELISA Enzymimmunoassay für die quantitative Bestimmung von Dopamin REF EA634/96 12 x 8 2 8 C DLD Gesellschaft für Diagnostika und medizinische Geräte mbh Adlerhorst
Instructions for use GABA ELISA BA E-2500
 Instructions for use GABA ELISA BA E-2500 GABA ELISA 1. Introduction 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of Gamma-aminobutyric acid (GABA) in
Instructions for use GABA ELISA BA E-2500 GABA ELISA 1. Introduction 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of Gamma-aminobutyric acid (GABA) in
Electrical tests on Bosch unit injectors
 Valid for Bosch unit injectors with order numbers 0 414 700 / 0 414 701 / 0 414 702 Parts Kit Magnet*: - F00H.N37.925 - F00H.N37.933 - F00H.N37.934 * For allocation to the 10-place Bosch order number,
Valid for Bosch unit injectors with order numbers 0 414 700 / 0 414 701 / 0 414 702 Parts Kit Magnet*: - F00H.N37.925 - F00H.N37.933 - F00H.N37.934 * For allocation to the 10-place Bosch order number,
Instructions for use. Histamine ELISA DEE1000
 Instructions for use Histamine ELISA DEE1000 Histamine ELISA 1. Introduction 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of Histamine in plasma and
Instructions for use Histamine ELISA DEE1000 Histamine ELISA 1. Introduction 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of Histamine in plasma and
Testanleitung. Quantitative Bestimmung der Tumor M2-PK Stuhltest Instruction Manual. Quantitative Determination of the Tumor M2-PK Stool Test
 Testanleitung Quantitative Bestimmung der Tumor M2-PK Stuhltest Instruction Manual Quantitative Determination of the Tumor M2-PK Stool Test Tumor M2-PK ELISA Stuhltest/Stool Test REF Artikel-Nr./Catalog
Testanleitung Quantitative Bestimmung der Tumor M2-PK Stuhltest Instruction Manual Quantitative Determination of the Tumor M2-PK Stool Test Tumor M2-PK ELISA Stuhltest/Stool Test REF Artikel-Nr./Catalog
Special Documentation CY80PH
 SD01506C/07/A2/02.16 71327299 Products Solutions Services Special Documentation CY80PH für/for Liquiline System CA80PH Mischen der Reagenzien / Mixing of the reagent Reagenz CY80PH-E1+SB 1 Reagenz CY80PH-E1+SB
SD01506C/07/A2/02.16 71327299 Products Solutions Services Special Documentation CY80PH für/for Liquiline System CA80PH Mischen der Reagenzien / Mixing of the reagent Reagenz CY80PH-E1+SB 1 Reagenz CY80PH-E1+SB
Rat Control HZ-DEV99RC 001 2016-04. Rat control sera suitable for internal control quality of the following HOELZEL ELISAs:
 Rat Control Rat control sera suitable for internal control quality of the following HOELZEL ELISAs: Testosterone rat/mouse Corticosterone rat/mouse Prolactin rat TSH rat (HZ-DEV9911) (HZ-DEV9922) (HZ-DEV9966)
Rat Control Rat control sera suitable for internal control quality of the following HOELZEL ELISAs: Testosterone rat/mouse Corticosterone rat/mouse Prolactin rat TSH rat (HZ-DEV9911) (HZ-DEV9922) (HZ-DEV9966)
COMPARISON of SMART HBA1C Analyser against Central Laboratory Analysis November 2008 K.Danzmayer
 COMPARISON of SMART HBA1C Analyser against Central Laboratory Analysis 12-14. November 2008 K.Danzmayer Estermannstraße 17 A-4020 Linz Tel.+43/732/77 10 77 Fax.+43/732/77 10 77-391 mail:diagnostika@diateam.at
COMPARISON of SMART HBA1C Analyser against Central Laboratory Analysis 12-14. November 2008 K.Danzmayer Estermannstraße 17 A-4020 Linz Tel.+43/732/77 10 77 Fax.+43/732/77 10 77-391 mail:diagnostika@diateam.at
MyPaclitaxel Control Kit
 PTX- MyPaclitaxel Control Kit This package insert must be read carefully prior to product use. Package insert instructions must be followed accordingly. Reliability of assay results cannot be guaranteed
PTX- MyPaclitaxel Control Kit This package insert must be read carefully prior to product use. Package insert instructions must be followed accordingly. Reliability of assay results cannot be guaranteed
WESAMIN GmbH & Co. KG
 WESAMIN GmbH & Co. KG Arbeitsanleitung Dopamin High Sensitive ELISA (Hochsensitiv und für kleine Probenvolumina) Enzymimmunoassay für die quantitative Bestimmung von Dopamin j REF DS00 96 2 8 C WESAMIN
WESAMIN GmbH & Co. KG Arbeitsanleitung Dopamin High Sensitive ELISA (Hochsensitiv und für kleine Probenvolumina) Enzymimmunoassay für die quantitative Bestimmung von Dopamin j REF DS00 96 2 8 C WESAMIN
RIDA QUICK Soya accessory pack Art. No. Z7103
 RIDA QUICK Soya accessory pack Art. No. Z7103 Zubehör für die Verwendung mit RIDA QUICK Soya (Art. Nr. R7103) Accessories for the use of the RIDA QUICK Soya (Art. No. R7103) In vitro Test Lagerung bei
RIDA QUICK Soya accessory pack Art. No. Z7103 Zubehör für die Verwendung mit RIDA QUICK Soya (Art. Nr. R7103) Accessories for the use of the RIDA QUICK Soya (Art. No. R7103) In vitro Test Lagerung bei
ITALY CONTACT: Meridian Healthcare srl Instructions for use Kynurenine ELISA BA E-2200
 ITALY CONTACT: Meridian Healthcare srl Via G. Guglielmino, 68-95030 Tremestieri Etneo - CT Tel. 095 725 68 69 - Fax: 095 725 44 54 e-mail: info@meridianhealthcare.it Instructions for use Kynurenine ELISA
ITALY CONTACT: Meridian Healthcare srl Via G. Guglielmino, 68-95030 Tremestieri Etneo - CT Tel. 095 725 68 69 - Fax: 095 725 44 54 e-mail: info@meridianhealthcare.it Instructions for use Kynurenine ELISA
Electrical testing of Bosch common rail piezo injectors
 Applies to generation CRI 3: Bosch 10-position order number 0 445 115 = CRI 3-16 (CRI 3.0) 1600 bar 0 445 116 = CRI 3-18 (CRI 3.2) 1800 bar 0 445 117 = CRI 3-20 (CRI 3.3) 2000 bar Tools required: Hybrid
Applies to generation CRI 3: Bosch 10-position order number 0 445 115 = CRI 3-16 (CRI 3.0) 1600 bar 0 445 116 = CRI 3-18 (CRI 3.2) 1800 bar 0 445 117 = CRI 3-20 (CRI 3.3) 2000 bar Tools required: Hybrid
QuickGEN Sample Preparation Centrifugation
 QuickGEN Centrifugation INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH QuickGEN Sample Preparation Centrifugation Art. Nr./ Order No.: CSE 0100 Version 11/16 GEN-IAL GmbH Tel: 0049 2241 2522980 Fax: 0049 2241
QuickGEN Centrifugation INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH QuickGEN Sample Preparation Centrifugation Art. Nr./ Order No.: CSE 0100 Version 11/16 GEN-IAL GmbH Tel: 0049 2241 2522980 Fax: 0049 2241
Adrenaline Plasma ELISA
 - Instructions for use Adrenaline Plasma ELISA High Sensitive BA E-4100 Adrenaline Plasma ELISA 1. Introduction High Sensitive English 1.1 Intended use and principle of the test Enzyme Immunoassay for
- Instructions for use Adrenaline Plasma ELISA High Sensitive BA E-4100 Adrenaline Plasma ELISA 1. Introduction High Sensitive English 1.1 Intended use and principle of the test Enzyme Immunoassay for
Wissen schafft Fortschritt
 Wissen schafft Fortschritt» Thermal analysis of six heat-reflective exterior paints on concrete under irradiation 20130730 Dr. Julius Nickl Geschäftsführer Senior-Experte für industrielle Prozesse und
Wissen schafft Fortschritt» Thermal analysis of six heat-reflective exterior paints on concrete under irradiation 20130730 Dr. Julius Nickl Geschäftsführer Senior-Experte für industrielle Prozesse und
Instructions for use. Fast Track. Histamine ELISA BA E-1700
 Instructions for use Histamine ELISA Fast Track BA E-1700 Histamine ELISA Fast Track (Urine and Whole blood) 1. Introduction 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative
Instructions for use Histamine ELISA Fast Track BA E-1700 Histamine ELISA Fast Track (Urine and Whole blood) 1. Introduction 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative
Metanephrine Urine ELISA
 Instructions for use Metanephrine Urine ELISA Fast Track KAPL10-0500 Metanephrine Urine ELISA 1. Introduction Fast Track 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative
Instructions for use Metanephrine Urine ELISA Fast Track KAPL10-0500 Metanephrine Urine ELISA 1. Introduction Fast Track 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative
VGM. VGM information. HAMBURG SÜD VGM WEB PORTAL USER GUIDE June 2016
 Overview The Hamburg Süd VGM Web portal is an application that enables you to submit VGM information directly to Hamburg Süd via our e-portal Web page. You can choose to enter VGM information directly,
Overview The Hamburg Süd VGM Web portal is an application that enables you to submit VGM information directly to Hamburg Süd via our e-portal Web page. You can choose to enter VGM information directly,
Newest Generation of the BS2 Corrosion/Warning and Measurement System
 Newest Generation of the BS2 Corrosion/Warning and Measurement System BS2 System Description: BS2 CorroDec 2G is a cable and energyless system module range for detecting corrosion, humidity and prevailing
Newest Generation of the BS2 Corrosion/Warning and Measurement System BS2 System Description: BS2 CorroDec 2G is a cable and energyless system module range for detecting corrosion, humidity and prevailing
Snap-in switch for switches PSE, MSM and MCS 30
 Product manual Snap-in switch for switches PSE, MSM and MCS 30 CONTENTS 1. PRODUCT DESCRIPTION 2. DATA AND DIMENSIONAL DRAWINGS 2.1. Technical Data 2.2. Dimensions of PSE with a Mounting Diameter 19 mm
Product manual Snap-in switch for switches PSE, MSM and MCS 30 CONTENTS 1. PRODUCT DESCRIPTION 2. DATA AND DIMENSIONAL DRAWINGS 2.1. Technical Data 2.2. Dimensions of PSE with a Mounting Diameter 19 mm
Nor- / Metanephrin ELISA in Urin
 WESA MIN GmbH & Co. KG Arbeitsanleitung Nor- / Metanephrin ELISA in Urin Enzymimmunoassay für die quantitative Bestimmung von Metanephrin und Normetanephrin in Urin REF MNUE00 2 x 96 2 8 C I V D WESAMIN
WESA MIN GmbH & Co. KG Arbeitsanleitung Nor- / Metanephrin ELISA in Urin Enzymimmunoassay für die quantitative Bestimmung von Metanephrin und Normetanephrin in Urin REF MNUE00 2 x 96 2 8 C I V D WESAMIN
DURCARE SET CRISTADUR
 DURCARE SET CRISTADUR DURCARE PRECLEANER DURCARE VORREINIGER ANWENDUNG: Mit DurCare Vorreiniger und einem fusselfreiem Tuch die bereits mit Spülmittel abgereinigte Oberfläche behandeln. Anschließend die
DURCARE SET CRISTADUR DURCARE PRECLEANER DURCARE VORREINIGER ANWENDUNG: Mit DurCare Vorreiniger und einem fusselfreiem Tuch die bereits mit Spülmittel abgereinigte Oberfläche behandeln. Anschließend die
VGM. VGM information. HAMBURG SÜD VGM WEB PORTAL - USER GUIDE June 2016
 Overview The Hamburg Süd VGM-Portal is an application which enables to submit VGM information directly to Hamburg Süd via our e-portal web page. You can choose to insert VGM information directly, or download
Overview The Hamburg Süd VGM-Portal is an application which enables to submit VGM information directly to Hamburg Süd via our e-portal web page. You can choose to insert VGM information directly, or download
Electrical testing of Bosch common rail solenoid valve (MV) injectors
 Applies to MV injector, generation: -CRI 1.0 / 2.0 / 2.1 / 2.2 -CRIN 1 / 2 / 3, with K oder AK plug Bosch 10-position order number Bosch-Bestellnummer CRI: 0 445 110 xxx Bosch-Bestellnummer CRIN: 0 445
Applies to MV injector, generation: -CRI 1.0 / 2.0 / 2.1 / 2.2 -CRIN 1 / 2 / 3, with K oder AK plug Bosch 10-position order number Bosch-Bestellnummer CRI: 0 445 110 xxx Bosch-Bestellnummer CRIN: 0 445
DENTAL IMPLANTS BY CAMLOG medical
 IMPLANT PASS DENTAL IMPLANTS BY CAMLOG medical devices made in germany for your well-being and a natural appearance. Personal data Surname First name Address ZIP code City Date of birth Health insurance
IMPLANT PASS DENTAL IMPLANTS BY CAMLOG medical devices made in germany for your well-being and a natural appearance. Personal data Surname First name Address ZIP code City Date of birth Health insurance
Gebrauchsanleitung Histamin Elisa BA E - 1000
 Gebrauchsanleitung Elisa BA E - 1000 ELISA 1. Verwendungszweck und Testprinzip Enzymimmunoassay zur quantitativen Bestimmung von in Plasma und Urin In Kombination mit dem Zusatzkit e Release ELISA ( BA
Gebrauchsanleitung Elisa BA E - 1000 ELISA 1. Verwendungszweck und Testprinzip Enzymimmunoassay zur quantitativen Bestimmung von in Plasma und Urin In Kombination mit dem Zusatzkit e Release ELISA ( BA
iid software tools QuickStartGuide iid USB base driver installation
 iid software tools QuickStartGuide iid software tools USB base driver installation microsensys Nov 2016 Introduction / Einleitung This document describes in short form installation of the microsensys USB
iid software tools QuickStartGuide iid software tools USB base driver installation microsensys Nov 2016 Introduction / Einleitung This document describes in short form installation of the microsensys USB
Instructions for use. Fast Track. Serotonin ELISA. Please use only the valid version of the Instructions for Use provided with the kit BA E-8900
 Instructions for use ELISA Fast Track BA E-8900 ELISA 1. Introduction Fast Track English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of in serum, urine
Instructions for use ELISA Fast Track BA E-8900 ELISA 1. Introduction Fast Track English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of in serum, urine
Cleaning & Disinfection of Eickview Videoendoscopes
 Cleaning & Disinfection of Eickview Videoendoscopes EICKEMEYER KG Eltastrasse 8 78532 Tuttlingen T +497461 96 580 0 F +497461 96 580 90 E info@eickemeyer.de www.eickemeyer.de Preparation Cleaning should
Cleaning & Disinfection of Eickview Videoendoscopes EICKEMEYER KG Eltastrasse 8 78532 Tuttlingen T +497461 96 580 0 F +497461 96 580 90 E info@eickemeyer.de www.eickemeyer.de Preparation Cleaning should
SAMPLE EXAMINATION BOOKLET
 S SAMPLE EXAMINATION BOOKLET New Zealand Scholarship German Time allowed: Three hours Total marks: 24 EXAMINATION BOOKLET Question ONE TWO Mark There are three questions. You should answer Question One
S SAMPLE EXAMINATION BOOKLET New Zealand Scholarship German Time allowed: Three hours Total marks: 24 EXAMINATION BOOKLET Question ONE TWO Mark There are three questions. You should answer Question One
Instructions for use. Kynurenine ELISA BA E-2200
 Instructions for use Kynurenine ELISA BA E-2200 Kynurenine ELISA 1. Introduction 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of L-Kynurenine in serum
Instructions for use Kynurenine ELISA BA E-2200 Kynurenine ELISA 1. Introduction 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of L-Kynurenine in serum
Electrical testing of Bosch common rail Injectors
 Electrical testing of Bosch common rail Injectors Contents: 1. Adapter cable for Hybridtester FSA 050 (article number 0 684 010 050 / 1 687 023 571) 2. Electrical testing of Bosch common rail solenoid
Electrical testing of Bosch common rail Injectors Contents: 1. Adapter cable for Hybridtester FSA 050 (article number 0 684 010 050 / 1 687 023 571) 2. Electrical testing of Bosch common rail solenoid
Metanephrine Plasma ELISA
 Instructions for use Metanephrine Plasma ELISA Fast Track KAPL10-0700 Metanephrine Plasma ELISA 1. Introduction Fast Track 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative
Instructions for use Metanephrine Plasma ELISA Fast Track KAPL10-0700 Metanephrine Plasma ELISA 1. Introduction Fast Track 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative
Magic Figures. We note that in the example magic square the numbers 1 9 are used. All three rows (columns) have equal sum, called the magic number.
 Magic Figures Introduction: This lesson builds on ideas from Magic Squares. Students are introduced to a wider collection of Magic Figures and consider constraints on the Magic Number associated with such
Magic Figures Introduction: This lesson builds on ideas from Magic Squares. Students are introduced to a wider collection of Magic Figures and consider constraints on the Magic Number associated with such
Hazards and measures against hazards by implementation of safe pneumatic circuits
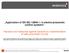 Application of EN ISO 13849-1 in electro-pneumatic control systems Hazards and measures against hazards by implementation of safe pneumatic circuits These examples of switching circuits are offered free
Application of EN ISO 13849-1 in electro-pneumatic control systems Hazards and measures against hazards by implementation of safe pneumatic circuits These examples of switching circuits are offered free
Tube Analyzer LogViewer 2.3
 Tube Analyzer LogViewer 2.3 User Manual Stand: 25.9.2015 Seite 1 von 11 Name Company Date Designed by WKS 28.02.2013 1 st Checker 2 nd Checker Version history Version Author Changes Date 1.0 Created 19.06.2015
Tube Analyzer LogViewer 2.3 User Manual Stand: 25.9.2015 Seite 1 von 11 Name Company Date Designed by WKS 28.02.2013 1 st Checker 2 nd Checker Version history Version Author Changes Date 1.0 Created 19.06.2015
Hinweisblatt. Für den Einsatz des MAX! Heizungssteuerungssystems haben Sie zwei Alternativen: Die MAX! Einzelraumlösung und die MAX! Hauslösung.
 Hinweisblatt MAX! Heizkörperthermostat BC-RT-TRX-CyG Art.-Nr. 99017 MAX! Fensterkontakt BC-SC-Rd-WM Art.-Nr. 99023 Für den Einsatz des MAX! Heizungssteuerungssystems haben Sie zwei Alternativen: Die MAX!
Hinweisblatt MAX! Heizkörperthermostat BC-RT-TRX-CyG Art.-Nr. 99017 MAX! Fensterkontakt BC-SC-Rd-WM Art.-Nr. 99023 Für den Einsatz des MAX! Heizungssteuerungssystems haben Sie zwei Alternativen: Die MAX!
RIDASCREEN Foodscreen Blood Collection Card Art. No.: A8025-BCC
 RIDASCREEN Foodscreen Blood Collection Card Art. No.: A8025-BCC Zubehör für RIDASCREEN Spec. IgG Foodscreen Accessory for RIDASCREEN Spec. IgG Foodscreen 1. filling in patient data Procedure: 2. filling
RIDASCREEN Foodscreen Blood Collection Card Art. No.: A8025-BCC Zubehör für RIDASCREEN Spec. IgG Foodscreen Accessory for RIDASCREEN Spec. IgG Foodscreen 1. filling in patient data Procedure: 2. filling
Word-CRM-Upload-Button. User manual
 Word-CRM-Upload-Button User manual Word-CRM-Upload for MS CRM 2011 Content 1. Preface... 3 2. Installation... 4 2.1. Requirements... 4 2.1.1. Clients... 4 2.2. Installation guidelines... 5 2.2.1. Client...
Word-CRM-Upload-Button User manual Word-CRM-Upload for MS CRM 2011 Content 1. Preface... 3 2. Installation... 4 2.1. Requirements... 4 2.1.1. Clients... 4 2.2. Installation guidelines... 5 2.2.1. Client...
Userś Manual. Histamine ELISA. Enzyme Immunoassay for the quantitative determination of Histamine in plasma and urine HZ-4005
 Userś Manual ELISA Enzyme Immunoassay for the quantitative determination of in plasma and urine HZ-4005 96 Version 6.0 Effective, December 2010 (02-Jul-2010) Please use only the valid version of the package
Userś Manual ELISA Enzyme Immunoassay for the quantitative determination of in plasma and urine HZ-4005 96 Version 6.0 Effective, December 2010 (02-Jul-2010) Please use only the valid version of the package
Reference Copy Only - DO NOT USE
 Instructions for use ELISA Fast Track BA E-8900 ELISA 1. Introduction Fast Track English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of in serum, urine
Instructions for use ELISA Fast Track BA E-8900 ELISA 1. Introduction Fast Track English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of in serum, urine
Guidance Notes for the eservice 'Marketing Authorisation & Lifecycle Management of Medicines' Contents
 Guidance Notes for the eservice 'Marketing Authorisation & Lifecycle Management of Medicines' Contents Login... 2 No active procedure at the moment... 3 'Active' procedure... 4 New communication (procedure
Guidance Notes for the eservice 'Marketing Authorisation & Lifecycle Management of Medicines' Contents Login... 2 No active procedure at the moment... 3 'Active' procedure... 4 New communication (procedure
POST MARKET CLINICAL FOLLOW UP
 POST MARKET CLINICAL FOLLOW UP (MEDDEV 2.12-2 May 2004) Dr. med. Christian Schübel 2007/47/EG Änderungen Klin. Bewertung Historie: CETF Report (2000) Qualität der klinischen Daten zu schlecht Zu wenige
POST MARKET CLINICAL FOLLOW UP (MEDDEV 2.12-2 May 2004) Dr. med. Christian Schübel 2007/47/EG Änderungen Klin. Bewertung Historie: CETF Report (2000) Qualität der klinischen Daten zu schlecht Zu wenige
DIBELS TM. German Translations of Administration Directions
 DIBELS TM German Translations of Administration Directions Note: These translations can be used with students having limited English proficiency and who would be able to understand the DIBELS tasks better
DIBELS TM German Translations of Administration Directions Note: These translations can be used with students having limited English proficiency and who would be able to understand the DIBELS tasks better
Instructions for use. Kynurenine ELISA BA E-2200
 Instructions for use Kynurenine ELISA BA E-2200 Kynurenine ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of L-Kynurenine
Instructions for use Kynurenine ELISA BA E-2200 Kynurenine ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of L-Kynurenine
Histamine Stool ELISA
 Instructions for use Histamine Stool ELISA BA E-1200 Histamine Stool ELISA 1. Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of Histamine in stool. Histamine
Instructions for use Histamine Stool ELISA BA E-1200 Histamine Stool ELISA 1. Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of Histamine in stool. Histamine
Instructions for use. Histamine ELISA. Please use only the valid version of the Instructions for Use provided with the kit BA E-1000
 Instructions for use Histamine ELISA BA E-1000 Histamine ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of Histamine in plasma
Instructions for use Histamine ELISA BA E-1000 Histamine ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of Histamine in plasma
Statistics, Data Analysis, and Simulation SS 2015
 Mainz, June 11, 2015 Statistics, Data Analysis, and Simulation SS 2015 08.128.730 Statistik, Datenanalyse und Simulation Dr. Michael O. Distler Dr. Michael O. Distler
Mainz, June 11, 2015 Statistics, Data Analysis, and Simulation SS 2015 08.128.730 Statistik, Datenanalyse und Simulation Dr. Michael O. Distler Dr. Michael O. Distler
Wissenschaftliche Dienste. Sachstand. Payment of value added tax (VAT) (EZPWD-Anfrage ) 2016 Deutscher Bundestag WD /16
 Payment of value added tax (VAT) (EZPWD-Anfrage ) 2016 Deutscher Bundestag Seite 2 Payment of value added tax (VAT) (EZPWD-Anfrage ) Aktenzeichen: Abschluss der Arbeit: 07.04.2016 Fachbereich: WD 4: Haushalt
Payment of value added tax (VAT) (EZPWD-Anfrage ) 2016 Deutscher Bundestag Seite 2 Payment of value added tax (VAT) (EZPWD-Anfrage ) Aktenzeichen: Abschluss der Arbeit: 07.04.2016 Fachbereich: WD 4: Haushalt
1. General information... 2 2. Login... 2 3. Home... 3 4. Current applications... 3
 User Manual for Marketing Authorisation and Lifecycle Management of Medicines Inhalt: User Manual for Marketing Authorisation and Lifecycle Management of Medicines... 1 1. General information... 2 2. Login...
User Manual for Marketing Authorisation and Lifecycle Management of Medicines Inhalt: User Manual for Marketing Authorisation and Lifecycle Management of Medicines... 1 1. General information... 2 2. Login...
Registration of residence at Citizens Office (Bürgerbüro)
 Registration of residence at Citizens Office (Bürgerbüro) Opening times in the Citizens Office (Bürgerbüro): Monday to Friday 08.30 am 12.30 pm Thursday 14.00 pm 17.00 pm or by appointment via the Citizens
Registration of residence at Citizens Office (Bürgerbüro) Opening times in the Citizens Office (Bürgerbüro): Monday to Friday 08.30 am 12.30 pm Thursday 14.00 pm 17.00 pm or by appointment via the Citizens
Evidence of Performance
 Air permeability, Watertightness, Resistance to wind load, Operating forces, Mechanical properties, Mechanical durability, Impact resistance Expert Statement No. 15-002226-PR01 (02) Product Designation
Air permeability, Watertightness, Resistance to wind load, Operating forces, Mechanical properties, Mechanical durability, Impact resistance Expert Statement No. 15-002226-PR01 (02) Product Designation
Outdoor-Tasche. Operating Instructions Bedienungsanleitung GB D
 00 181243 Outdoor Case Outdoor-Tasche Splish Splash Operating Instructions Bedienungsanleitung GB D A B C D OPEN G Operating instruction 1. Important Notes Children are not permitted to play with the device.
00 181243 Outdoor Case Outdoor-Tasche Splish Splash Operating Instructions Bedienungsanleitung GB D A B C D OPEN G Operating instruction 1. Important Notes Children are not permitted to play with the device.
Mock Exam Behavioral Finance
 Mock Exam Behavioral Finance For the following 4 questions you have 60 minutes. You may receive up to 60 points, i.e. on average you should spend about 1 minute per point. Please note: You may use a pocket
Mock Exam Behavioral Finance For the following 4 questions you have 60 minutes. You may receive up to 60 points, i.e. on average you should spend about 1 minute per point. Please note: You may use a pocket
OncoBEAM Anleitung zur Probenentnahme und Versand
 OncoBEAM Anleitung zur Probenentnahme und Versand Go Beyond Biopsy with Blood www.sysmex-inostics.com Deutsch Anleitung zur Probenentnahme und Versand Anleitung zur Blutentnahme 1. Beschriftung des Entnahmeröhrchens
OncoBEAM Anleitung zur Probenentnahme und Versand Go Beyond Biopsy with Blood www.sysmex-inostics.com Deutsch Anleitung zur Probenentnahme und Versand Anleitung zur Blutentnahme 1. Beschriftung des Entnahmeröhrchens
Chromogranin A ELISA
 Instructions for use Chromogranin A ELISA TM E-9000 Chromogranin A ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of human
Instructions for use Chromogranin A ELISA TM E-9000 Chromogranin A ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of human
Level 2 German, 2015
 91126 911260 2SUPERVISOR S Level 2 German, 2015 91126 Demonstrate understanding of a variety of written and / or visual German text(s) on familiar matters 2.00 p.m. Friday 4 December 2015 Credits: Five
91126 911260 2SUPERVISOR S Level 2 German, 2015 91126 Demonstrate understanding of a variety of written and / or visual German text(s) on familiar matters 2.00 p.m. Friday 4 December 2015 Credits: Five
Instructions for use. Chromogranin A ELISA TM E-9000
 Instructions for use Chromogranin A ELISA TM E-9000 Chromogranin A ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of human
Instructions for use Chromogranin A ELISA TM E-9000 Chromogranin A ELISA 1. Introduction English 1.1 Intended use and principle of the test Enzyme Immunoassay for the quantitative determination of human
Ex-Barriere für Diagnoseeinheit SITRANS DA400 / Ex-barrier for diagnostics unit SITRANS DA400 7MJ2010-1AA 0032
 Ex-Barriere für Diagnoseeinheit SITRANS DA400 / Ex-barrier for diagnostics unit SITRANS DA400 7MJ2010-1AA 0032 Warnung Elektrischer Anschluss in explosionsgefährdeten Bereichen Anschluss und Inbetriebnahme
Ex-Barriere für Diagnoseeinheit SITRANS DA400 / Ex-barrier for diagnostics unit SITRANS DA400 7MJ2010-1AA 0032 Warnung Elektrischer Anschluss in explosionsgefährdeten Bereichen Anschluss und Inbetriebnahme
Ölmess-Stäbe-Satz für Motor und Automatikgetriebe Mercedes-Benz
 Anwendung Anwendungshinweis V2112 Ölmess-Stäbe-Satz für Motor und Automatikgetriebe Mercedes-Benz Mercedes liefert die unten aufgeführten Motoren-Codes werksseitig ohne Ölmessstäbe aus. Nach jedem Ölwechsel
Anwendung Anwendungshinweis V2112 Ölmess-Stäbe-Satz für Motor und Automatikgetriebe Mercedes-Benz Mercedes liefert die unten aufgeführten Motoren-Codes werksseitig ohne Ölmessstäbe aus. Nach jedem Ölwechsel
Konfiguration von eduroam. Configuring eduroam
 eduroam Windows 8.1 / 10 Konfiguration von eduroam Configuring eduroam 08.10.2018 kim.uni-hohenheim.de kim@uni-hohenheim.de Wissenschaftliche Einrichtungen und Universitäten bieten einen weltweiten Internetzugang
eduroam Windows 8.1 / 10 Konfiguration von eduroam Configuring eduroam 08.10.2018 kim.uni-hohenheim.de kim@uni-hohenheim.de Wissenschaftliche Einrichtungen und Universitäten bieten einen weltweiten Internetzugang
Safety action Inspection of welds
 Knott GmbH Obinger Straße 15 D 83125 Eggstätt Receiver final custormer Ihre Nachricht Your letter Ihr Zeichen Your references Datum Date Abteilung Department Bearbeitet durch Contact person Unser Zeichen
Knott GmbH Obinger Straße 15 D 83125 Eggstätt Receiver final custormer Ihre Nachricht Your letter Ihr Zeichen Your references Datum Date Abteilung Department Bearbeitet durch Contact person Unser Zeichen
