Skript zum Workshop Chemie für die Jahrgangsstufen 9 und 10
|
|
|
- Annika Wolf
- vor 7 Jahren
- Abrufe
Transkript
1 Skript zum Workshop Chemie für die Jahrgangsstufen 9 und 10 Erstellt von: Michael Müller Erstellungsdatum: michael.mueller@rwth-aachen.de
2 2
3 1.0 Das Atommodell (nach NielsBohr) Der dänische Physiker Niels Bohr fasste 1913 die Erkenntnisse seiner Zeit zu einem neuen Atommodell zusammen, das man heute ihm zu Ehren Bohrsche Atommodell nennt. Die klassische Newtonsche Mechanik konnte die neuen Entdeckungen um die atomaren Teilchen in Zusammenhang mit Licht nicht erklären. Danach müßte ein um den positiv geladenen Kern sich beschleunigt bewegendes, negativ geladenes Elektron Licht emittieren, also Energie verlieren und allmählich in den Kern stürzen. (Gesetze der Elektrodynamik) Bohr formuliert deshalb neue Gesetze, die den zunächst widersprüchlichen Eigenschaften der Atome gerecht wurden. Damit konnte zunächst das Wasserstoffatom erklärt und die Spektren von H berechnet werden. Bohrsche Postulate: 1 Elektronen bewegen sich auf bestimmten Kreisbahnen, die einem bestimmten Energieniveau entsprechen. Solange sie sich auf einer Bahn bewegen, bleibt ihre Energie konstant. Ansonsten gelten die Gesetze der klassischen Mechanik (z.b. Anziehung durch den Kern) 2 Die Bewegungsenergie der Elektronen und die elektrostatische Wechselwirkung mit dem Kern kompensieren sich (heben sich gegenseitig auf). Man könnte ein Atom nach Bohr auch mit einem Planetensystem vergleichen, bei dem die Elektronen -wie die Planeten um die Sonne- um den Kern kreisen. Die einzelnen Bahnen (früher Schalen) werden mit n=1, 2, 3 usw. bezeichnet und Hauptquantenzahlen genannt. 2.0 Atommasse, Stoffmenge, Avogadro & Co Chemie ist die Wissenschaft der Stoffe und ihren Umwandlungen. Um jedoch quantitative Aussagen über den Verlauf einer chemischen Reaktion machen zu können muss man sie in Zahlen beschreiben können. Eine wichtige Einheit ist die Atommasse. Diese ist wichtig um etwas über die Verhältnisse der Stoffportionen bei einer chemischen Reaktion aussagen zu können. Hierbei bezieht man sich wiederum auf das Kohlenstoff-Iotop C-12. Die eingeführte Einheit wird mit u (Atommasseneinheit) abgekürtzt. 3
4 1u = 0, g = 1, g 1u = entspricht 1/12 der Masse von einem C-12-Atom Die Atommassen im Periodensystem sind alle am C-12-Isotop orientiert. So hat beispielsweise Wasserstoff 1/12 der Atommasse des Kohlenstoffs oder Sauerstoff besitzt die Atommasse 15,9994u. Nimmt man nun 12g Kohlenstoff oder 15,9994g Sauerstoff so besitzen diese Mengen die gleiche Anzahl von Atomen. Diese Anzahl an Atome bezeichnet der Chemiker als 1 Mol. Die Anzahl der Atome eines Mols kann mit Hilfe eines Dreisatz bestimmt werden und wird als Avogadrozahl bezeichnet. Man nennt diese Stoffgröße Stoffmenge und kürzt sie mit n ab. Avogadro-Konstante oder Loschmidt'sche Zahl Da es sehr aufwändig wäre wenn man die Mengenverhältnisse in Atomzahlen angeben würde führte Avogadro die Avogadro-Zahl (oder auch Loschmidt'sche Zahl) ein. Er bezog sich dabei auf genau 12g Kohlenstoff. Demnach enthalten 12,0g Kohlenstoff (des C-12-Kohlenstoff-Isotops) 6, Atome (der Wert ist gerundet). Wenn ein Chemiker die Masse eines Mols für eine chemische Verbindung herausfinden will, addiert er die Atommassen der einzelnen Atome des Moleküls. Für die Verbindung Wasser (H 2 O) würde der Chemiker folgendes rechnen: 2 u(h) + u(o) = 2 1,00794g + 15,9994g = 18,01528g wiegt 1 Mol Wasser Für diese Masse hat man den Begriff molare Masse eingeführt, welcher angibt wie viel eine chemische Verbindung pro Mol wiegt. Die Einheit ist daher g/mol. Der Zusammenhang zwischen molarer Masse, Masse und Stoffmenge stellt die folgende Formel her: 3.0 Die Grundgesetze der Chemie 3.1 Gesetz der Erhaltung der Masse Bei jeder Reaktion die man durch führt stellt man fest, dass die Masse aller Edukte gleich der Masse aller Produkte ist. Daraus leitet sich das Massenerhaltungsgesetz ab: Bei jeder chemischen Reaktion bleibt die Gesamtmasse der Reaktionspartner erhalten. 4
5 Verbrennt man beispielsweise Eisenwolle an der Luft und wiegt, sie vor und nach dem Versuch, so stellt man fest, dass es einen Massenzuwachs gegeben hat, welcher laut des oben genannten Gesetzes nicht auftreten kann. Bei diesem Versuch wird jedoch durch das Wiegen der Eisenwolle nur ein Teil der Eduktmasse berücksichtigt. Man vernachlässigt dabei den Sauerstoffanteil der Reaktion: 4Fe + 3O 2 2 Fe 2 O 3 Wenn man also korrekt alle beteiligten Massen berücksichtigen möcht, so muss man den Versuch in einem Reagenzglas durchführen. Man wird dabei feststellen, dass das Reagenzglas vor dem Versuch genauso viel wie nachdem Versuch. 3.2 Gesetz der konstanten Massenverhältnisse Der französische Chemiker Joseph Louis Proust ( ) formulierte als erster das Gesetz der konstanten Massenverhältnisse: Gesetz der konstanten Massenverhältnisse: In einer chemischen Verbindung sind die Atome stets in einem bestimmten Massenverhältnis enthalten. Bei einer chemischen Reaktion reagieren die beteiligten Stoffe stets in typischen, konstanten Massenverhältnissen. Joseph Louis Proust 3.3 Volumengesetz von Gay-Lussac: Der französische Physiker und Chemiker Joseph Louis Gay-Lussac ( ) formulierte das Volumengesetz: Volumengesetz von Gay-Lussac: Gase reagieren stets in Volumenverhältnissen kleiner ganzer Zahlen, z.b.: H 2 und Chlor im Verhältnis 1:1 H 2 und Sauerstoff im Verhältnis 2:1 H 2 und Stickstoff im Verhältnis 3:1 5
6 3.4 Avogadro-Gesetz Der Italiener Amedeo Avogadro ( ) stellte auf der Grundlage dieser Erkenntnisse folgende Hypothese auf: Satz des Avogadro: In einem bestimmten Gasvolumen sind bei gleichen äußeren Bedingungen (Druck, Temperatur) immer gleich viele zählbare Einheiten (Teilchen) enthalten, unabhängig um welches Gas es sich handelt. Amedeo Avogadro Diese auch als Satz des Avogadro bekannte Aussage besagt, dass z.b. in einem Liter Wasserstoff, Stickstoff, Sauerstoff oder Wasserdampf gleich viele Wasserstoff-, Stickstoff, Sauerstoff- oder Wasser-Moleküle enthalten sind. 4.0 Was ist eine chemische Reaktion? Die wohl einfachste und nicht ganz richtige Definition für die Oxidation ist: Eine Oxidation ist eine Reaktion bei der Sauerstoff verbraucht wird. Diese Definition ist nur zum Teil richtig. Mit dieser Definition ist es zwar möglich klassische Oxidationen zu erklären. So kann sie beispielsweise die Reaktion von Sauerstoff mit Eisen erklären. Um die einfache Definition der Oxidation zu erläutern wird im folgenden ein Lehrversuch beschrieben um die Oxidation von Eisen zu beweisen. Erhitzt man ein Stück Eisenwolle an der Luft, so glüht es und wird schwarz. Bestimmt man nun vor und nach dem Versuch das Gewicht, so stellt man fest, dass das Gewicht der Eisenwolle zugenommen hat. Es muss also eine Reaktion mit dem in der Luft enthaltenen Sauerstoff reagiert haben. Tatsächlich erhält man bei der Verbrennung von Eisen Eisenoxid (FeO, Fe 2 O 3 bzw. Fe 3 O 4 ; je nach Versuchsbedingungen). Alle anderen Metalle lassen sich ebenso wie Eisen an der Luft durch Erhitzen oxidieren. Mit der oben genannten Definition lassen sich also derartige Reaktionen erklären und verstehen. Ein weiteres wichtiges Beispiel für die Oxidation im klassischen Sinne ist der Antrieb von Space Shuttles und Raketen. Space Shuttles enthalten in ihren Tanks flüssigen Sauerstoff und Wasserstoff. Bei der Verbrennung eines 1:2- Gemisch von Sauerstoff und Wasserstoff entsteht ein großer Energiebetrag, welcher als Schubenergie umgesetzt wird. Als Reaktionsprodukt entsteht Wasser und somit ist diese Form des Antriebs auch für die Umwelt bedenkenlos einsetzbar. 2 H 2 + O 2 2 H 2 O H R = -572kJ/mol 6
7 Ein weiteres Beispiel für die klassische Oxidation ist die Energiegewinnung im menschlichen Körper. Dazu werden mit der Nahrung Kohlenhydrate aufgenommen, welche im Körper zu wasserlöslicher Glucose umgesetzt werden. In den Muskeln und im Gehirn wird die Glucose dann unter Wärmeabstrahlung verbrannt. Als Produkte erhält man Wasser und CO 2 : C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Die klassische Definition der Oxidation stößt aber auch an ihre Grenzen. Sieht man sich beispielsweise die stark exotherme Reaktion von Natrium mit Chlor an, so kann die bisherige Definition der Oxidation diesen Vorgang nicht erklären: 2Na + Cl 2 2 NaCl Um derartige Reaktionen erklären zu können muss ein allgemeinerer Begriff der Oxidation eingeführt werden: Eine Oxidation ist eine Reaktion bei der Elektronen abgegeben werden. Da Elektronen nicht einfach verschwinden können muss mit jeder Oxidation eine Reduktion verbunden sein, also einer Aufnahme von Elektronen. Eine Reduktion ist eine Reaktion bei der Elektronen aufgenommen werden. Man nennt somit Reaktionen wie die oben beschriebene Redoxreaktionen. In diesem Beispiel wird ein Elektron des Natriumatoms auf das Sauerstoffatom übertragen. Die Richtung der Elektronenübertragung ist dabei abhängig von der Elektronegativität der jeweiligen Elemente. Elemente mit hohen Elektronegativitätswerte werden die Elektronen eher aufnehmen und Elemente mit niedrigen Werten für die Elektronegativität geben Elektronen leicht ab. Bei ionischen Verbindungen ist es leicht festzustellen welches Atom ein Atom aufgenommen hat und welches eins augenommen hat. Das negative geladene Teilchen hat das Elektron des positiv geladenen Ions aufgenommen. Bei polaren und unpolaren Verbindungen ist dies nichht so leicht zu sehen. Um dennoch Aussagen über die fiktiven Elektronenübertragungen machen zu können hat man die Oxidationszahlen eingeführt. Demnach werden die Elektronen einer Bindung immer formal dem elektronegativeren Element zugeordnet. 7
8 Beispiel: 5.0 Das Periodensystem der Elemente 5.1 Historisches Das Periodensystem der Elemente ist so konzipiert, dass Elemente mit ähnlichen physikalischen und chemischen Eigenschaften nahe beieinander Liegen. Die Gemeinsamkeiten ergeben sich aufgrund der ähnlichen Elektronenkonfigurationen, wobei die Hauptgruppenzahl die Anzahl der Valenzelektronen widerspiegelt. Beispiele für die chemische und physikalische Verwandtschaft sind die erste Hauptgruppe, die so genannten Alkalimetalle, die zweite Hauptgruppe (Erdalkalimetalle), die Chalkogene (Hauptgruppe 6) und die Halogene (7. Hauptgruppe). Es stellt sich jedoch dabei die Frage wie man zu dieser speziellen Anordnung der Elemente gekommen ist. Schon zu Anfang des 19.Jahrhunderts gab es erste Versuche die Elemente nach ihren Eigenschaften zu ordnen. Johann W. Döbereiner entschied sich zwischen 1817 und 1829 für eine Triaden-Schreibweise. Diese Form der Anordnung spiegelt sich noch heute im PSE wieder. Beispielweise ordnete Döbereiner Chlor - Brom - Iod einer Triade zu, ebenso stellte er Calcium - Strontium - Barium sowie Lithium - Natrium - Kalium zu jeweils einer Triade zusammen. Mehr als 30 Jahre später (1864) postulierte der britische Chemiker John A. R. Newlands das Gesetz der Oktaven, demnach wurden die Elemente nach ihrer Atommasse sortiert. Dabei fiel ihm auf, dass nach 7 Elemente wieder ein Element folgt welches mit seinen chemischen und physikalischen dem ersten ähnelt. Nur 5 Jahre später leitete der russische Forscher Dimitrij I. Mendelejew sowie der deutsche Wissenschaftler Lothar Meyer (unabhängig voneinander) aus den Erkenntnissen Newlands das Periodensystem der Elemente her. Diese Anordnung der Elemente hatte schon große Ähnlichkeit mit dem heute bekannten PSE. Allerdings blieben einige Lücken offen, da noch nicht alle Elemente bekannt waren. Jedoch war Mendelejew in der Lage die chemischen und physikalischen Eigenschaften der fehlenden Elemente vorauszusagen (Beispiele dafür sind Germanium uns Scandium). Jedoch erkannte Mendeljew das die Anordnung nach dem Oktaven-Gesetzt nicht immer zutraf. Er behauptete, dass eine andere Größe für die Periodizität 8
9 verantwortlich sein muss. Diese Größe sollte direkt von der Ordnungszahl des Elements abgängen. Henry G. J. Moseley löste das Problem. Er untersuchte Aluminium(13) und Gold(79) im Röntgenspektrum und stellte fest, dass für bestimmte Linien im Spektrum eine lineare Beziehung zur zugehörigen Frequenz und der Ordnungszahl gab. Somit konnte er belegen, dass die Elemente eine andere Reihenfolge haben mussten als die Atommassen vorgeben. Außerdem konnte er zeigen, dass dem Element Lanthan noch 14 weitere Elemente folgen müssen. Nach diesen Erkenntnissen wurde das PSE geändert wobei die chemischen und physikalischen Eigenschaften der elemente eine Funktion der Ordnungszahl sind. 5.2 Die Gruppen des Periodensystems I. Erste Hauptgruppe: Die Alkalimetalle (Lithium, Natrium, Kalium, Rubidium, Cäsium und Francium) Die Elemente der ersten Hauptgruppe mit Ausnahme des Wasserstoffs bilden die Gruppe der Alkalimetalle. Die Bezeichnung leitet sich vom arabischen al kali, womit das Kaliumcarbonat meint ist welches sich in der Asche von Pflanzen ableitet. Für Metalle sind sie ungewöhnlich weich und lassen sich sogar mit einem Messer. Die Alkalimetalle zeichnen sich besonders durch ihre enorme Reaktivität aus. Dabei ist zu beobachten, dass die Reaktivität der Elemente in der 1. Hauptgruppe von oben nach unten zu nimmt. Bei der Reaktion mit Wasser sind die Alkalimetalle in der Lage den Wasserstoff zu reduzieren. Dabei entsteht ihr entsprechendes Hydroxid und Wasserstoff: Beispiel: 2 Na + 2 H 2 O 2 NaOH + H 2 [V: Alkalimetalle] Alle Alkalimetalle reagieren an der Luft sofort mit dem Luftsauerstoff und bilden einen grau/schwarzen Überzug. Die hohe Reaktionsfähigkeit (sie sind starke Reduktionsmittel) der Alkalimetalle lässt sich mit ihrer Elektronenkonfiguration deuten. Sie besitzen jeweils nur ein einziges Valenzelektron in ihrer äußersten Elektronenschale. Dies lässt sich leicht abspalten, da die Metalle nur eine sehr geringe Elektronegativität besitzen. Außerdem ist nur wenig Ionisierungsenergie für diesen Vorgang nötig. Gefördert wird die Abgabe des einzigen Valenzelektron auch durch die hohe Hydratationsenergie der Alkalimetalle. Zusammen mit Wasserstoff bilden die Alkalimetalle sogenannte Hydride, in welchen der Wasserstoff eine negative Oxidationszahl besitzt. Eine II. Zweite Hauptgruppe: Die Erdalkalimetalle (Beryllium, Magnesium, Calcium, Struntium, Barium und Radium) Die Erdalkalimetalle verhalten sich ähnlich wie die Alkalimetalle. Sie reagieren mit Ausnahme des Beryllium mit Wasser zu Wasserstoff und ihren entsprechenden Hydroxiden. Beispiel: Ca + 2 H 2 O Ca(OH) 2 + H 2 [V: Alkalimetalle und Erdalkalimetalle] Analog zu den Alkalimetallen geben auch die Erdalkalimetalle gerne Elektronen ab, das heißt sie besitzen eine geringe Elektronegativität und eine geringe Ionisierungsenergie. Generell geben sie 2 Valenzelektronen ab um die stabilere Edelgaskonfiguration zu erreichen. Aus diesem Grunde tauchen sie in Verbindungen 9
10 auch meist mit der Oxidationzahl +2 auf. Zusammen mit Wasserstoff bilden sie Hydride in denen der Wasserstoff eine negative Oxidationszahl erhält. III. Sechste Hauptgruppe: Die Chalkogene (Sauerstoff, Schwefel, Selen, Tellur, Polonium und Ununhexium) Die sechste Hauptgruppe wird von den so genannten Chalkogenen gebildet. Der Name leitet sich vom griechischen ab und bedeutet Erzbildner. Der Name weist darauf hin, dass die Elemente der 6. Hauptgruppe häufig in Erzen auftauchen. Sie besitzen eine hohe Elektronegativität. Der Sauerstoff besitz sogar nach Fluor die zweithöchste Elektronegativität. Zum erreichen ihrer Edelgaskonfiguration nehmen sie zwei Elektronen auf und tragen daher meist die Oxidationszahlen -2 (Ausnahme ist beispielsweise das Wasserstoffperoxid). IV. Siebte Hauptgruppe: Die Halogene (Fluor, Chlor, Brom, Iod und Astat) Die siebte Hauptgruppe des Periodensystems wird von den Halogenen gebildet. Ihr Name leitet sich aus dem griechischen ab und bedeutet Salzbildner. Sie bilden als Elemente dimere Moleküle aus der Form X 2. Besonders auffallend ist ihr stechender chloriger Geruch. Sie besitzen eine hohe Reaktivität in Verbindung mit Metallen, wobei sie die entsprechenden Salze bilden. Die Halogene besitzen 7 Valenzelektronen und nehmen zum erreichen ihrer Edelgaskonfiguration ein Elektron auf. Sie erhalten daher meist die Oxidationszahl -1. Zusammen mit Wasser bilden Halogene Sauerstoffsäuren mit Wasserstoff bilden sie Gase der Form HX, welche in Wasser eingeleitet starke Säuren darstellen. V. Achte Hauptgruppe: Die Edelgase (Helium, Neon, Argon, Krypton, Xenon Radon und Ununoctium) Die achte Hauptgruppe des PSE wird von den Edelgasen gestellt. Sie sind gasförmige nicht Metalle die besonders reaktionsträge sind, da sie schon Edelgaskonfiguration besitzen. Um Elektronen aus der äußersten Elektronenschale zu entfernen muss eine enorm große Ionisierungsenergie aufgewendet, sodass Edelgasverbindungen nur sehr selten sind. 10
Integration von Schülerinnen und Schülern mit einer Sehschädigung an Regelschulen. Didaktikpool
 Integration von Schülerinnen und Schülern mit einer Sehschädigung an Regelschulen Didaktikpool Periodensystem der Elemente für blinde und hochgradig sehgeschädigte Laptop-Benutzer Reinhard Apelt 2008 Technische
Integration von Schülerinnen und Schülern mit einer Sehschädigung an Regelschulen Didaktikpool Periodensystem der Elemente für blinde und hochgradig sehgeschädigte Laptop-Benutzer Reinhard Apelt 2008 Technische
Periodensystem der Elemente - PSE
 Periodensystem der Elemente - PSE Historische Entwicklung Möglichkeiten der Reindarstellung seit 18. Jhdt. wissenschaftliche Beschreibung der Elemente 1817 Johann Wolfgang Döbereiner: ähnliche Elemente
Periodensystem der Elemente - PSE Historische Entwicklung Möglichkeiten der Reindarstellung seit 18. Jhdt. wissenschaftliche Beschreibung der Elemente 1817 Johann Wolfgang Döbereiner: ähnliche Elemente
Grundwissenkarten Hans-Carossa-Gymnasium. 9. Klasse. Chemie SG
 Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Periodensystem (PSE)
 Periodensystem (PSE) - Wie sind die Elemente im PSE angeordnet? - Warum und nach welchen Kritierien können sie so angeordnet werden? - Was kann man aus dem PSE ablesen, außer der Massenzahl? Fragen zum
Periodensystem (PSE) - Wie sind die Elemente im PSE angeordnet? - Warum und nach welchen Kritierien können sie so angeordnet werden? - Was kann man aus dem PSE ablesen, außer der Massenzahl? Fragen zum
Arbeitsmaterialien Arbeitsblätter (mit Lösungsvorschlägen)
 Arbeitsmaterialien Arbeitsblätter (mit Lösungsvorschlägen) 1. Erkundung Kapitel 1 1. Welche Element-Symbole kennst du? Füge zusammen, was zusammengehört! Ag Al Au Br Ca CI Cu F Fe H He Hg K N Na Mg O P
Arbeitsmaterialien Arbeitsblätter (mit Lösungsvorschlägen) 1. Erkundung Kapitel 1 1. Welche Element-Symbole kennst du? Füge zusammen, was zusammengehört! Ag Al Au Br Ca CI Cu F Fe H He Hg K N Na Mg O P
Was haben wir gelernt?
 Was haben wir gelernt? - Gesetze chemischer Reaktionen - Atommodell von Dalton - Elementsymbole - Die atomare Masseneinheit u - Die Avogadro-Zahl und deren Umkehrung - Von Massenverhältnissen zu Teilchenverhältnissen
Was haben wir gelernt? - Gesetze chemischer Reaktionen - Atommodell von Dalton - Elementsymbole - Die atomare Masseneinheit u - Die Avogadro-Zahl und deren Umkehrung - Von Massenverhältnissen zu Teilchenverhältnissen
CHEMIE KAPITEL 1 AUFBAU DER MATERIE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2014 / 2015
 CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Valenzelektronen und Atomeigenschaften Valenzelektronen (Außenelektronen) bestimmen
CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Valenzelektronen und Atomeigenschaften Valenzelektronen (Außenelektronen) bestimmen
CHEMIE KAPITEL 1 AUFBAU DER MATERIE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2014 / 2015
 CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Atombau und Elementarteilchen Folie 3 Atommasse und Stoffmenge Stoffmenge [mol]: 12,000
CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Atombau und Elementarteilchen Folie 3 Atommasse und Stoffmenge Stoffmenge [mol]: 12,000
1 Chemische Elemente und chemische Grundgesetze
 1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
2. Verhalten der Elemente bei einer Reaktion: Warum funkt s bei unterschiedlichen
 1. Atombau und Periodensystem 1a) Nach welchem Gesichtspunkt sind die Elemente im Periodensystem von 1- ca. 103 angeordnet? 1b) Nach welchem Gesichtspunkt ist ein Element einer PERIODE zugeordnet? 1c)
1. Atombau und Periodensystem 1a) Nach welchem Gesichtspunkt sind die Elemente im Periodensystem von 1- ca. 103 angeordnet? 1b) Nach welchem Gesichtspunkt ist ein Element einer PERIODE zugeordnet? 1c)
Kapitel 03. Aufbau der Materie (Buch ab Seite 17)
 Kapitel 03 Aufbau der Materie (Buch ab Seite 17) ATOME SIND DIE BAUSTEINE DER CHEMIE Film1 Geschichtliches Kern-Hülle-Modell 8min ATOME SIND DIE BAUSTEINE DER CHEMIE Alle Stoffe im Universum (Sonne, Mond,
Kapitel 03 Aufbau der Materie (Buch ab Seite 17) ATOME SIND DIE BAUSTEINE DER CHEMIE Film1 Geschichtliches Kern-Hülle-Modell 8min ATOME SIND DIE BAUSTEINE DER CHEMIE Alle Stoffe im Universum (Sonne, Mond,
Besetzung der Orbitale
 Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Einführung Brennendes Magnesiumband reagiert mit Sauerstoff
CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Einführung Brennendes Magnesiumband reagiert mit Sauerstoff
A. Allgemeine Chemie. 1 Aufbau der Materie 2 Trennverfahren für Stoffgemenge 3 Grundgesetze der Chemie 4 Atomaufbau 5 Periodensystem
 A. Allgemeine Chemie 1 Aufbau der Materie 2 Trennverfahren für Stoffgemenge 3 Grundgesetze der Chemie 4 Atomaufbau 5 Periodensystem Periodensystem der Elemente - PSE Historische Entwicklung Möglichkeiten
A. Allgemeine Chemie 1 Aufbau der Materie 2 Trennverfahren für Stoffgemenge 3 Grundgesetze der Chemie 4 Atomaufbau 5 Periodensystem Periodensystem der Elemente - PSE Historische Entwicklung Möglichkeiten
Was passiert denn genau?
 Was passiert denn genau? - Bei chemischen Reaktionen entstehen neue Stoffe, mit neuen Eigenschaften. - Im Teilchenmodell stellen wir uns vor, dass Kugelteilchen (Edukte) neu kombiniert werden. - Wenn wir
Was passiert denn genau? - Bei chemischen Reaktionen entstehen neue Stoffe, mit neuen Eigenschaften. - Im Teilchenmodell stellen wir uns vor, dass Kugelteilchen (Edukte) neu kombiniert werden. - Wenn wir
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Atombau und PSE. Das komplette Material finden Sie hier: School-Scout.
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Atombau und PSE Das komplette Material finden Sie hier: School-Scout.de Chemiekonzept Pro Unterrichtsreihen Sekundarstufe I Band 11
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Atombau und PSE Das komplette Material finden Sie hier: School-Scout.de Chemiekonzept Pro Unterrichtsreihen Sekundarstufe I Band 11
Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen
 Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu?
Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu?
Wie sind Atome aufgebaut Welche Informationen enthält das Periodensystem?
 2. DIE KLEINSTEN TEILCHEN ARBEITSBLATT 2.1 DER ATOMAUFBAU FRAGE Wie sind Atome aufgebaut Welche Informationen enthält das Periodensystem? Bausteine der Atome Ladung (+, -, 0) Masse (hoch, sehr gering)
2. DIE KLEINSTEN TEILCHEN ARBEITSBLATT 2.1 DER ATOMAUFBAU FRAGE Wie sind Atome aufgebaut Welche Informationen enthält das Periodensystem? Bausteine der Atome Ladung (+, -, 0) Masse (hoch, sehr gering)
Musterprüfung Welche der Elemente Lithium, Kohlenstoff, Wasserstoff, Sauerstoff, Magnesium, Aluminium und Calcium sind Nichtmetalle?
 Module: Atombau und Periodensystem Chemische Bindungen Chemische Reaktionen 1 Musterprüfung 1. Teil: Atombau und Periodensystem 1.1. Welche Art von Teilchen befinden sich a) im Atomkern b) in der Elektronenhülle
Module: Atombau und Periodensystem Chemische Bindungen Chemische Reaktionen 1 Musterprüfung 1. Teil: Atombau und Periodensystem 1.1. Welche Art von Teilchen befinden sich a) im Atomkern b) in der Elektronenhülle
Bundesrealgymnasium Imst. Chemie Klasse 4. Aufbauprinzipien der Materie Periodensystem de Elemente
 Bundesrealgymnasium Imst Chemie 2010-11 Periodensystem de Elemente Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff
Bundesrealgymnasium Imst Chemie 2010-11 Periodensystem de Elemente Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff
Eigenschaften Reinstoffe Elemente Kugelteilchen Elementes Atom
 Einstieg: Atom Der Chemiker will alles genau untersuchen, um die Eigenschaften von Stoffen heraus zu finden. Er trennt Gemische in Reinstoffe. Er analysiert Reinstoffe, so dass sie in ihre Elemente zerfallen.
Einstieg: Atom Der Chemiker will alles genau untersuchen, um die Eigenschaften von Stoffen heraus zu finden. Er trennt Gemische in Reinstoffe. Er analysiert Reinstoffe, so dass sie in ihre Elemente zerfallen.
Lösung Sauerstoff: 1s 2 2s 2 2p 4, Bor: 1s 2 2s 2 2p 1, Chlor: 1s 2 2s 2 2p 6 3s 2 3p 5 Neon: 1s 2 2s 2 2p 6
 1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
Klausur 1 Basiswissen I. Chemie. Klasse 11c. Erwartungshorizont
 Paula Fürst Schule (Gemeinschaftsschule) Berlin Klausur 1 Basiswissen I Chemie Klasse 11c Erwartungshorizont Vor und Nachname: Zeitvorgabe: 80 min Liebe Schülerin, lieber Schüler, tragen Sie bitte auf
Paula Fürst Schule (Gemeinschaftsschule) Berlin Klausur 1 Basiswissen I Chemie Klasse 11c Erwartungshorizont Vor und Nachname: Zeitvorgabe: 80 min Liebe Schülerin, lieber Schüler, tragen Sie bitte auf
Atomverbände. In stabilen Verbindungen, die auf der Erde existieren besitzen die Elemente meist die Elektronenkonfiguration
 Atomverbände Möglichkeit 1: Abgabe von Elektronen bei gleichzeitiger Aufnahme durch einen Reaktionspartner --> SALZE In stabilen Verbindungen, die auf der Erde existieren besitzen die Elemente meist die
Atomverbände Möglichkeit 1: Abgabe von Elektronen bei gleichzeitiger Aufnahme durch einen Reaktionspartner --> SALZE In stabilen Verbindungen, die auf der Erde existieren besitzen die Elemente meist die
CHEMIE. Katherina Standhartinger. für Ahnungslose. von Katherina Standhartinger, Memmingen. Mit 17 Abbildungen und 30 Tabellen
 Katherina Standhartinger CHEMIE für Ahnungslose von Katherina Standhartinger, Memmingen Mit 17 Abbildungen und 30 Tabellen S. Hirzel Verlag Stuttgart VII Inhaltsverzeichnis Vorwort 1 Einführung 1 2 Übersicht
Katherina Standhartinger CHEMIE für Ahnungslose von Katherina Standhartinger, Memmingen Mit 17 Abbildungen und 30 Tabellen S. Hirzel Verlag Stuttgart VII Inhaltsverzeichnis Vorwort 1 Einführung 1 2 Übersicht
Die Anzahl der Protonen und Neutronen entspricht der Atommassenzahl.
 Atom Der Begriff Atom leitet sich von atomos her, was unteilbar heisst. Diese Definition ist alt, da man heutzutage fähig ist, Atome zu teilen. Atommassenzahl Die Anzahl der Protonen und Neutronen entspricht
Atom Der Begriff Atom leitet sich von atomos her, was unteilbar heisst. Diese Definition ist alt, da man heutzutage fähig ist, Atome zu teilen. Atommassenzahl Die Anzahl der Protonen und Neutronen entspricht
Hewlett-Packard Company. [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten.
![Hewlett-Packard Company. [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten. Hewlett-Packard Company. [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten.](/thumbs/95/126174167.jpg) Hewlett-Packard Company [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten Johanika [Datum] Walter Whites Chemie Quiz Fragen 1. Aus wie vielen Atomen besteht
Hewlett-Packard Company [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten Johanika [Datum] Walter Whites Chemie Quiz Fragen 1. Aus wie vielen Atomen besteht
Grundwissen Chemie 9. Klasse SG
 Grundwissen Chemie 9. Klasse SG Stoffe und Reaktionen - bestehen aus kleinsten Teilchen - lassen sich aufgliedern in Reinstoffe und Stoffgemische Stoffe Reinstoff Stoffe Stoffgemisch Atome Moleküle heterogen
Grundwissen Chemie 9. Klasse SG Stoffe und Reaktionen - bestehen aus kleinsten Teilchen - lassen sich aufgliedern in Reinstoffe und Stoffgemische Stoffe Reinstoff Stoffe Stoffgemisch Atome Moleküle heterogen
N & T 5 Periodensystem der Elemente 01 Name: Vorname: Datum:
 N & T 5 Periodensystem der Elemente 01 Name: Vorname: Datum: Dalton definierte sein Atommodell um 1803. Schon bald stellten die Chemiker fest, dass das Modell zwar gut war, doch nicht alle Fragen klären
N & T 5 Periodensystem der Elemente 01 Name: Vorname: Datum: Dalton definierte sein Atommodell um 1803. Schon bald stellten die Chemiker fest, dass das Modell zwar gut war, doch nicht alle Fragen klären
Übungsaufgaben zum Atomaufbau und Periodensystem
 Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten
Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten
Wasser à. Nachweis: Wasser ist
 Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
[ ] 1. Stoffe und Reaktionen (Kartei 8.8, 8.10 und 8.13) Stoffe + - Moleküle aus gleichen Atomen. Ionen. Moleküle aus verschiedenen Atomen
![[ ] 1. Stoffe und Reaktionen (Kartei 8.8, 8.10 und 8.13) Stoffe + - Moleküle aus gleichen Atomen. Ionen. Moleküle aus verschiedenen Atomen [ ] 1. Stoffe und Reaktionen (Kartei 8.8, 8.10 und 8.13) Stoffe + - Moleküle aus gleichen Atomen. Ionen. Moleküle aus verschiedenen Atomen](/thumbs/68/58264490.jpg) 1. Stoffe und Reaktionen (Kartei 8.8, 8.10 und 8.13) Stoffe Gemische Reinstoffe Elemente Verbindungen gleiche Atome Moleküle aus gleichen Atomen Moleküle aus verschiedenen Atomen Ionen + Kation Anion z.b.
1. Stoffe und Reaktionen (Kartei 8.8, 8.10 und 8.13) Stoffe Gemische Reinstoffe Elemente Verbindungen gleiche Atome Moleküle aus gleichen Atomen Moleküle aus verschiedenen Atomen Ionen + Kation Anion z.b.
Elektronenkonfiguration
 Um die chemischen Eigenschaften von Elementen zu verstehen, muss man deren Elektronenkonfiguration kennen. Als Elektronenkonfiguration bezeichnet man die Verteilung der Elektronen auf Schalen um den Kern
Um die chemischen Eigenschaften von Elementen zu verstehen, muss man deren Elektronenkonfiguration kennen. Als Elektronenkonfiguration bezeichnet man die Verteilung der Elektronen auf Schalen um den Kern
Curriculum Fach: Chemie Klasse: 8 Hölderlin-Gymnasium Nürtingen. Chemie
 Klassenstufe 8 BS (nach S. 196/197) Curriculum Fach: Chemie Klasse: 8 Chemie Kerncurriculum Inhalte Zeit Kompetenzen: die Schülerinnen und Schüler können Stoffe und ihre Eigenschaften Bemerkungen Wichtige
Klassenstufe 8 BS (nach S. 196/197) Curriculum Fach: Chemie Klasse: 8 Chemie Kerncurriculum Inhalte Zeit Kompetenzen: die Schülerinnen und Schüler können Stoffe und ihre Eigenschaften Bemerkungen Wichtige
Grundwissen 9. Klasse Chemie
 Grundwissen 9. Klasse Chemie 1. Formelzeichen und Einheiten 2. Was versteht man unter der Stoffmenge und der Avogadro- Konstante N A? Eine Stoffportion hat die Stoffmenge n = 1 mol, wenn sie 6 * 10 23
Grundwissen 9. Klasse Chemie 1. Formelzeichen und Einheiten 2. Was versteht man unter der Stoffmenge und der Avogadro- Konstante N A? Eine Stoffportion hat die Stoffmenge n = 1 mol, wenn sie 6 * 10 23
Unterschied zwischen Physik und Chemie:
 Unterschied zwischen Physik und Chemie: Der Begriff Physik bezeichnet die Lehre über Zustände und Zustandsänderungen die Chemie hingegen beschäftigt sich mit Stoffen und stofflichen Veränderungen. Unterteilung
Unterschied zwischen Physik und Chemie: Der Begriff Physik bezeichnet die Lehre über Zustände und Zustandsänderungen die Chemie hingegen beschäftigt sich mit Stoffen und stofflichen Veränderungen. Unterteilung
Einheiten und Einheitenrechnungen
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
3. Übung Allgemeine Chemie AC01
 Allgemeine und Anorganische Chemie Aufgabe 1: 3. Übung Allgemeine Chemie AC01 Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten im Kern immer die
Allgemeine und Anorganische Chemie Aufgabe 1: 3. Übung Allgemeine Chemie AC01 Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten im Kern immer die
Grundwissen Chemie 9. Jahrgangsstufe G8
 Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Atomphysik NWA Klasse 9
 Atomphysik NWA Klasse 9 Atome wurden lange Zeit als die kleinsten Teilchen angesehen, aus denen die Körper bestehen. Sie geben den Körpern ihre chemischen und physikalischen Eigenschaften. Heute wissen
Atomphysik NWA Klasse 9 Atome wurden lange Zeit als die kleinsten Teilchen angesehen, aus denen die Körper bestehen. Sie geben den Körpern ihre chemischen und physikalischen Eigenschaften. Heute wissen
Vom Atombau zum Königreich der Elemente
 Vom Atombau zum Königreich der Elemente Wiederholung: Elektronenwellenfunktionen (Orbitale) Jedes Orbital kann durch einen Satz von Quantenzahlen n, l, m charakterisiert werden Jedes Orbital kann maximal
Vom Atombau zum Königreich der Elemente Wiederholung: Elektronenwellenfunktionen (Orbitale) Jedes Orbital kann durch einen Satz von Quantenzahlen n, l, m charakterisiert werden Jedes Orbital kann maximal
Was passiert denn genau?
 Was passiert denn genau? - Bei chemischen Reaktionen entstehen neue Stoffe, mit neuen Eigenschaften. - Im Teilchenmodell stellen wir uns vor, dass Kugelteilchen (Edukte) neu kombiniert werden. - Wenn wir
Was passiert denn genau? - Bei chemischen Reaktionen entstehen neue Stoffe, mit neuen Eigenschaften. - Im Teilchenmodell stellen wir uns vor, dass Kugelteilchen (Edukte) neu kombiniert werden. - Wenn wir
Atombau und Periodensystem
 Atombau und Periodensystem Patrick Bucher 15. August 2011 Inhaltsverzeichnis 1 Die chemischen Grundlagen und Daltons Atomhypothese 1 2 Modelle zum Atombau 2 2.1 Die elektrische Ladung..............................
Atombau und Periodensystem Patrick Bucher 15. August 2011 Inhaltsverzeichnis 1 Die chemischen Grundlagen und Daltons Atomhypothese 1 2 Modelle zum Atombau 2 2.1 Die elektrische Ladung..............................
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Ordnung in der Vielfalt - das verstehen und lesen lernen Das komplette aterial finden Sie hier: School-Scout.de 1 von 10 Ordnung in
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Ordnung in der Vielfalt - das verstehen und lesen lernen Das komplette aterial finden Sie hier: School-Scout.de 1 von 10 Ordnung in
Redoxreaktionen. Redoxreaktionen: Reaktionen bei denen Elektronen zwischen den Komponenten übertragen werden
 Nach Lavoisier: : Redoxreaktionen Redoxreaktionen: Reaktionen bei denen Elektronen zwischen den Komponenten übertragen werden Aufnahme von Sauerstoff zb.: Verbrennen von Magnesium : Abgabe von Sauerstoff
Nach Lavoisier: : Redoxreaktionen Redoxreaktionen: Reaktionen bei denen Elektronen zwischen den Komponenten übertragen werden Aufnahme von Sauerstoff zb.: Verbrennen von Magnesium : Abgabe von Sauerstoff
Allgemeine und Anorganische Chemie
 Norbert Kuhn Thomas M. Klapötke Allgemeine und Anorganische Chemie Eine Einführung Unter Mitarbeit von Isabel Walker ^ Springer Spektrum Inhaltsverzeichnis 1 Einleitung 1 2 Definitionen 5 3 Chemische Stoffe
Norbert Kuhn Thomas M. Klapötke Allgemeine und Anorganische Chemie Eine Einführung Unter Mitarbeit von Isabel Walker ^ Springer Spektrum Inhaltsverzeichnis 1 Einleitung 1 2 Definitionen 5 3 Chemische Stoffe
Periodensystem der Elemente (PSE)
 Periodensystem der Elemente (PSE) 1 2 H 1.0079 4.0026 3 4 5 6 7 8 9 10 Li 6.941 Be 9.0122 B 10.811 C 12.011 N 14.007 O 15.999 F 18.998 Ne 20.180 11 12 13 14 15 16 17 18 Na Mg Al Si P S Cl Ar 22.990 24.305
Periodensystem der Elemente (PSE) 1 2 H 1.0079 4.0026 3 4 5 6 7 8 9 10 Li 6.941 Be 9.0122 B 10.811 C 12.011 N 14.007 O 15.999 F 18.998 Ne 20.180 11 12 13 14 15 16 17 18 Na Mg Al Si P S Cl Ar 22.990 24.305
Musterprüfung Welche der Elemente Lithium, Kohlenstoff, Wasserstoff, Sauerstoff, Magnesium, Aluminium und Calcium sind Nichtmetalle?
 1 Module: Atombau und Periodensystem Chemische Bindungen Chemische Reaktionen Musterprüfung 1. Teil: Atombau und Periodensystem 1.1. Welche Art von Teilchen befinden sich a) im Atomkern b) in der Elektronenhülle
1 Module: Atombau und Periodensystem Chemische Bindungen Chemische Reaktionen Musterprüfung 1. Teil: Atombau und Periodensystem 1.1. Welche Art von Teilchen befinden sich a) im Atomkern b) in der Elektronenhülle
Lernmaterial Lernfeld 1 Grundlagen Physik und Chemie. Chemische Grundlagen, Bindungsarten. Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms
 Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
1 Das Periodensystem der Elemente (PSE)
 1 DAS PERIODENSYSTEM DER ELEMENTE (PSE) 1 G P E R I U P P E O D E Abbildung 1: Perioden und Gruppen 1 Das Periodensystem der Elemente (PSE) Man unterscheidet Perioden von Gruppen (siehe Abbildung auf dieser
1 DAS PERIODENSYSTEM DER ELEMENTE (PSE) 1 G P E R I U P P E O D E Abbildung 1: Perioden und Gruppen 1 Das Periodensystem der Elemente (PSE) Man unterscheidet Perioden von Gruppen (siehe Abbildung auf dieser
In reiner Form bestehen sie aus 6,022 10 23 Atomen. Sie können weder chemisch noch physikalisch zerlegt werden.
 1. Welches der folgenden Gemische ist ein Gemenge? Kalkmilch Granit Rauch 2. Wodurch sind chemische Elemente charakterisiert? In reiner Form bestehen sie aus 6,022 10 23 Atomen. Sie sind unteilbar. Sie
1. Welches der folgenden Gemische ist ein Gemenge? Kalkmilch Granit Rauch 2. Wodurch sind chemische Elemente charakterisiert? In reiner Form bestehen sie aus 6,022 10 23 Atomen. Sie sind unteilbar. Sie
Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch
 Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch Verbindungen untersuchen, ihre Zusammensetzung verstehen und
Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch Verbindungen untersuchen, ihre Zusammensetzung verstehen und
Atome. Chemie. Zusammenfassungen. Prüfung Mittwoch, 14. Dezember Dalton-Modell. Reaktionsgrundgesetze. Chemische Formeln.
 Chemie Atome Zusammenfassungen Prüfung Mittwoch, 14. Dezember 2016 Dalton-Modell Reaktionsgrundgesetze Chemische Formeln Avogadro Relative Massen Quantitative Beziehungen Stöchiometrie Steffi, Tom, Marvin
Chemie Atome Zusammenfassungen Prüfung Mittwoch, 14. Dezember 2016 Dalton-Modell Reaktionsgrundgesetze Chemische Formeln Avogadro Relative Massen Quantitative Beziehungen Stöchiometrie Steffi, Tom, Marvin
Elektronenpaarbindung (oder Atombindung) Nichtmetallatom + Nichtmetallatom Metallatom + Nichtmetallatom 7. Welche Bindungsart besteht jeweils?
 LÖSUNGEN Probetest 1 Kap. 03 Theorie Name: 1. C = Kohlenstoff Ag = Silber Br = Brom Schwefel = S Lithium = Li Uran = U 2. Aluminium - Finde die richtigen Zahlen mit Hilfe deines PSE: Massenzahl: 27 Ordnungszahl:
LÖSUNGEN Probetest 1 Kap. 03 Theorie Name: 1. C = Kohlenstoff Ag = Silber Br = Brom Schwefel = S Lithium = Li Uran = U 2. Aluminium - Finde die richtigen Zahlen mit Hilfe deines PSE: Massenzahl: 27 Ordnungszahl:
10TG. Training II2. 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene.
 Training II2 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene. (4X4=1 X4=16P) a. Verbrennung von Kohlenstoff C + O2 CO2 Kohlenstoffdioxid b. Thermolyse
Training II2 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene. (4X4=1 X4=16P) a. Verbrennung von Kohlenstoff C + O2 CO2 Kohlenstoffdioxid b. Thermolyse
Chemie Chemie - Klasse 8 - Version 1 (Juli 2004)
 Fehler! Kein Text mit angegebener Formatvorlage im Dokument. - Chemie Chemie Chemie - Klasse 8 - Version 1 (Juli 2004) Themenfeld Kerncurriculum
Fehler! Kein Text mit angegebener Formatvorlage im Dokument. - Chemie Chemie Chemie - Klasse 8 - Version 1 (Juli 2004) Themenfeld Kerncurriculum
Chemieepoche Klasse 11. Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen
 Chemieepoche Klasse 11 Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen Eisengewinnung (Schülervortrag) Fortsetzung Chemische Bindungen Warum sind im Wassermolekül zwei Wasserstoffatome mit
Chemieepoche Klasse 11 Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen Eisengewinnung (Schülervortrag) Fortsetzung Chemische Bindungen Warum sind im Wassermolekül zwei Wasserstoffatome mit
1 Aufbau der Materie. 1.1 Anfänge und Kernhüllenmodell. Bauchemie / Bauphysik II Modul M-T 6
 1 Aufbau der Materie 1.1 Anfänge und Kernhüllenmodell 400 J. v. Chr. suchte Demokrit als erster die kleinsten Teile der Materie. Und weil auch er diese damals nicht sehen konnte, entwickelte er eine Modellvorstellung
1 Aufbau der Materie 1.1 Anfänge und Kernhüllenmodell 400 J. v. Chr. suchte Demokrit als erster die kleinsten Teile der Materie. Und weil auch er diese damals nicht sehen konnte, entwickelte er eine Modellvorstellung
Kerncurriculum und Schulcurriculum (2 Wochenstunden) Themen und Inhalte. Bezug zu den Standards. Kerncurriculum / Schulcurriculum
 Chemie: Klasse 9 Kerncurriculum und Schulcurriculum (2 Wochenstunden) Zeit Themen und Inhalte Umsetzung Bezug zu den Standards Kerncurriculum / Schulcurriculum 10 Atombau und Periodensystem - Das Kern-Hülle-Modell
Chemie: Klasse 9 Kerncurriculum und Schulcurriculum (2 Wochenstunden) Zeit Themen und Inhalte Umsetzung Bezug zu den Standards Kerncurriculum / Schulcurriculum 10 Atombau und Periodensystem - Das Kern-Hülle-Modell
bestimmte mehratomige Anionen mit Sauerstoff werden mit dem lateinischen Namen benannt und enden auf at.
 DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
Chemie Fragenkatalog Jahrgang 8
 Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Element. Verbindung. Reinstoff. homogenes Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Grundwissen 9.Klasse SG 1 Grundwissen 9.Klasse SG 1. Grundwissen 9.Klasse SG 2 Grundwissen 9.Klasse SG 2. Stoffebene.
 Grundwissen 9.Klasse SG 1 Grundwissen 9.Klasse SG 1 Stoff Reinstoff mischen Gemisch Einteilung der Stoffe Bei gleichen Bedingungen (Temp., Druck) immer gleiche Eigenschaften (z.b. Schmelz- /Siedetemp.,
Grundwissen 9.Klasse SG 1 Grundwissen 9.Klasse SG 1 Stoff Reinstoff mischen Gemisch Einteilung der Stoffe Bei gleichen Bedingungen (Temp., Druck) immer gleiche Eigenschaften (z.b. Schmelz- /Siedetemp.,
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Chemie. Die Chemie beschäftigt sich mit materiellen Dingen; Sie ist die Lehre von den Stoffen.
 Chemie Die Chemie beschäftigt sich mit materiellen Dingen; Sie ist die Lehre von den Stoffen. Stoffeinteilung: Stoffdefinition: Ein Stoff liegt dann vor, wenn dieser ein Volumen einnimmt und eine Masse
Chemie Die Chemie beschäftigt sich mit materiellen Dingen; Sie ist die Lehre von den Stoffen. Stoffeinteilung: Stoffdefinition: Ein Stoff liegt dann vor, wenn dieser ein Volumen einnimmt und eine Masse
N & T (R) 5 Periodensystem der Elemente 01 Name: Vorname: Datum:
 N & T (R) 5 Periodensystem der Elemente 01 Name: Vorname: Datum: Dalton definierte sein Atommodell um 1803. Schon bald stellten die Chemiker fest, dass das Modell zwar gut war, doch nicht alle Fragen klären
N & T (R) 5 Periodensystem der Elemente 01 Name: Vorname: Datum: Dalton definierte sein Atommodell um 1803. Schon bald stellten die Chemiker fest, dass das Modell zwar gut war, doch nicht alle Fragen klären
H Wasserstoff. O Sauerstoff
 He Helium Ordnungszahl 2 Atommasse 31,8 268,9 269,7 0,126 1,25 H Wasserstoff Ordnungszahl 1 Atommasse 14,1 252,7 259,2 2,1 7,14 1 3,45 1,38 Li Lithium Ordnungszahl 3 Atommasse 13,1 1330 180,5 1,0 0,53
He Helium Ordnungszahl 2 Atommasse 31,8 268,9 269,7 0,126 1,25 H Wasserstoff Ordnungszahl 1 Atommasse 14,1 252,7 259,2 2,1 7,14 1 3,45 1,38 Li Lithium Ordnungszahl 3 Atommasse 13,1 1330 180,5 1,0 0,53
Chemische Reaktionen. Wir erzeugen Wasser
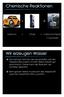 hemische Reaktionen + Natrium + -> hlor -> Natriumchlorid = Kochsalz Wir erzeugen Wasser Die kleinsten Teilchen des Sauerstoffes und des Wasserstoffes waren im roten Ballon bereits gut durchmischt. Daher
hemische Reaktionen + Natrium + -> hlor -> Natriumchlorid = Kochsalz Wir erzeugen Wasser Die kleinsten Teilchen des Sauerstoffes und des Wasserstoffes waren im roten Ballon bereits gut durchmischt. Daher
Schuljahrgänge 9 und Schwierige Geburt Chemie wird
 Schuljahrgänge 9 und 10 5.1 Schwierige Geburt Chemie wird - ordnen Elemente bestimmten Naturwissenschaft 5.2 In Reih und Glied das Periodensystem - ordnen Elemente bestimmten - verknüpfen Stoff- und Teilchenebene.
Schuljahrgänge 9 und 10 5.1 Schwierige Geburt Chemie wird - ordnen Elemente bestimmten Naturwissenschaft 5.2 In Reih und Glied das Periodensystem - ordnen Elemente bestimmten - verknüpfen Stoff- und Teilchenebene.
Grundpraktikum für Biologen 2016
 Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Die wichtigsten Elementfamilien
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Die wichtigsten Elementfamilien Das komplette Material finden Sie hier: Download bei School-Scout.de SCHOOL-SCOUT Elementfamilien
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Die wichtigsten Elementfamilien Das komplette Material finden Sie hier: Download bei School-Scout.de SCHOOL-SCOUT Elementfamilien
Stoffgemisch. Reinstoff. Homogenes Gemisch. Heterogenes Gemisch. ( 9. Kl. SG - WSG 1 / 56 ) ( 9. Kl. SG - WSG 2 / 56 ) ( 9. Kl.
 Stoffgemisch ( 9. Kl. SG - WSG 1 / 56 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 9. Kl.
Stoffgemisch ( 9. Kl. SG - WSG 1 / 56 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 9. Kl.
Bauchemie 1. 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle?
 Bauchemie 1 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle? a) Der Atomkern besteht aus Neutronen und Protonen, die zusammen auch Nukleonen genannt werden. Er befindet sich
Bauchemie 1 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle? a) Der Atomkern besteht aus Neutronen und Protonen, die zusammen auch Nukleonen genannt werden. Er befindet sich
Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch. Reinstoff, Element, Verbindung. Zweiatomige Elemente.
 Einteilung der Stoffe: Stoff Reinstoff Mischen Gemisch Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b. Farbe,
Einteilung der Stoffe: Stoff Reinstoff Mischen Gemisch Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b. Farbe,
Lernaufgabe: Periodensystem Erklärung von Tendenzen in der Reaktionsfähigkeit der Alkali-, Erdalkalimetalle und der Halogene
 ETH Institut für Verhaltenswissenschaften Seite 1/5 Lernaufgabe: Periodensystem Erklärung von Tendenzen in der Reaktionsfähigkeit der Alkali-, Erdalkalimetalle und der Halogene Hilfreiche Angaben: 1. Unterrichtsfach:
ETH Institut für Verhaltenswissenschaften Seite 1/5 Lernaufgabe: Periodensystem Erklärung von Tendenzen in der Reaktionsfähigkeit der Alkali-, Erdalkalimetalle und der Halogene Hilfreiche Angaben: 1. Unterrichtsfach:
Themenheft. Chemie. chemische Gesetze, Atombau und Formeln. Arbeitsblätter für den deutschsprachigen Fachunterricht an Auslandsschulen
 Themenheft Chemie chemische Gesetze, Atombau und Formeln Arbeitsblätter für den deutschsprachigen Fachunterricht an Auslandsschulen Inhaltsverzeichnis: Blatt 1: Die Masse bei chemischen Reaktionen Blatt
Themenheft Chemie chemische Gesetze, Atombau und Formeln Arbeitsblätter für den deutschsprachigen Fachunterricht an Auslandsschulen Inhaltsverzeichnis: Blatt 1: Die Masse bei chemischen Reaktionen Blatt
Stoffmenge. Isotope Radioaktivität. Aufgabe 1-1: Welche Aussagen zum Atomaufbau treffen zu bzw. sind falsch?
 Zusammenfassung Atome bestehen aus Protonen (p + ), Elektronen (e - ) und Neutronen (n) Elemente sind durch ihre Ordnungszahl und Massezahl definiert Stoffmenge n ist ein Maß für die Teilchenanzahl (Atome,
Zusammenfassung Atome bestehen aus Protonen (p + ), Elektronen (e - ) und Neutronen (n) Elemente sind durch ihre Ordnungszahl und Massezahl definiert Stoffmenge n ist ein Maß für die Teilchenanzahl (Atome,
IV. Chemische Formeln und Massenverhältnisse. Themen dieses Kapitels:
 Hinweise zum Kapitel IV. Chemische Formeln und Massenverhältnisse Themen dieses Kapitels: - Berechnung molarer Massen - Stoffnamen und dazugehörige Formeln - Aufstellen und Bedeutung von Verhältnisformeln
Hinweise zum Kapitel IV. Chemische Formeln und Massenverhältnisse Themen dieses Kapitels: - Berechnung molarer Massen - Stoffnamen und dazugehörige Formeln - Aufstellen und Bedeutung von Verhältnisformeln
Oxidation und Reduktion Redoxreaktionen Blatt 1/5
 Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Grundlagen Chemie. Dipl.-Lab. Chem. Stephan Klotz. Freiwill ige Feuerwehr Rosenheim
 Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
Basiskonzept: Stoff-Teilchen
 OHG Springe: FS Chemie Kompetenzen für die Jahrgänge 9 und 10I (KC NaWi 2015) Seite 1 von 6 Basiskonzept: Stoff-Teilchen Gase sind aus Atomen oder Molekülen aufgebaut beschreiben den Molekülbegriff. beschreiben
OHG Springe: FS Chemie Kompetenzen für die Jahrgänge 9 und 10I (KC NaWi 2015) Seite 1 von 6 Basiskonzept: Stoff-Teilchen Gase sind aus Atomen oder Molekülen aufgebaut beschreiben den Molekülbegriff. beschreiben
Anorganische Peroxide und Radikale. von Benjamin Scharbert
 Anorganische Peroxide und Radikale von Benjamin Scharbert Inhalt: 1. Anorganische Peroxide: 2. Radikale: 1.1 Grundsätzliches 1.2 Na 2 O 2 1.3 BaO 2 1.4 H 2 O 2 2.1 Grundsätzliches 2.2 Sauerstoff 2.3 Stickstoffmonoxid
Anorganische Peroxide und Radikale von Benjamin Scharbert Inhalt: 1. Anorganische Peroxide: 2. Radikale: 1.1 Grundsätzliches 1.2 Na 2 O 2 1.3 BaO 2 1.4 H 2 O 2 2.1 Grundsätzliches 2.2 Sauerstoff 2.3 Stickstoffmonoxid
Orientierungstest für angehende Industriemeister. Vorbereitungskurs Chemie
 Orientierungstest für angehende Industriemeister Vorbereitungskurs Chemie Weiterbildung Technologie Erlaubte Hilfsmittel: Periodensystem der Elemente Taschenrechner Maximale Bearbeitungszeit: 60 Minuten
Orientierungstest für angehende Industriemeister Vorbereitungskurs Chemie Weiterbildung Technologie Erlaubte Hilfsmittel: Periodensystem der Elemente Taschenrechner Maximale Bearbeitungszeit: 60 Minuten
Kohlenwasserstoffe und das Orbitalmodell
 Kohlenwasserstoffe und das Orbitalmodell Material I Material I Sie erhalten drei unterschiedliche Kohlenwasserstoffe Stoff A, Stoff B und Stoff, die sie zuordnen sollen. Infrage kommen 1- Octen, n- Octan
Kohlenwasserstoffe und das Orbitalmodell Material I Material I Sie erhalten drei unterschiedliche Kohlenwasserstoffe Stoff A, Stoff B und Stoff, die sie zuordnen sollen. Infrage kommen 1- Octen, n- Octan
Aggregatzustände. Atomradien
 Elementgruppen Aggregatzustände Atomradien Biologische Bedeutung Dichte Elektronegativität Entdeckung der Elemente Ionenradien Ionisierungsenergie Natürliche Isotope Kovalenzradien Metalle und Nichtmetalle
Elementgruppen Aggregatzustände Atomradien Biologische Bedeutung Dichte Elektronegativität Entdeckung der Elemente Ionenradien Ionisierungsenergie Natürliche Isotope Kovalenzradien Metalle und Nichtmetalle
Chemie-Grundwissen der 9.Klasse
 Chemie-Grundwissen der 9.Klasse Stoffebene = Makroskopische (sichtbare) Ebene Betrachtung einer Stoffportion mit den erkennbaren und messbaren Eigenschaften Teilchenebene = Submikroskopische Ebene Betrachtung
Chemie-Grundwissen der 9.Klasse Stoffebene = Makroskopische (sichtbare) Ebene Betrachtung einer Stoffportion mit den erkennbaren und messbaren Eigenschaften Teilchenebene = Submikroskopische Ebene Betrachtung
Robert-Koch-Gymnasium Deggendorf. Grundwissen Chemie. 8. Jahrgangsstufe
 Robert-Koch-Gymnasium Deggendorf Grundwissen Chemie 8. Jahrgangsstufe Teilchenmodell und Stoffeigenschaften Teilchenmodell: Alle Stoffe bestehen aus kleinsten Teilchen, vereinfacht dargestellt als Kugeln.
Robert-Koch-Gymnasium Deggendorf Grundwissen Chemie 8. Jahrgangsstufe Teilchenmodell und Stoffeigenschaften Teilchenmodell: Alle Stoffe bestehen aus kleinsten Teilchen, vereinfacht dargestellt als Kugeln.
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Bist Du nicht "FIT", dann musst Du nacharbeiten.
 Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006
 Übungsaufgaben zur Vorlesung hemie für Biologen, WS 2005/2006 Themenbereiche Atombau, chemische Bindung, Stöchiometrie, Aggregatzustände 1. Ergänzen Sie folgende Tabelle: Symbol Z M Protonen eutronen Elektronen
Übungsaufgaben zur Vorlesung hemie für Biologen, WS 2005/2006 Themenbereiche Atombau, chemische Bindung, Stöchiometrie, Aggregatzustände 1. Ergänzen Sie folgende Tabelle: Symbol Z M Protonen eutronen Elektronen
Schuleigener Arbeitsplan für das Fach Chemie (vorläufige Fassung, gültig ab Schuljahr 2008/09)
 Laurentius-Siemer-Gymnasium Saterland Schuleigener Arbeitsplan für das Fach Chemie (vorläufige Fassung, gültig ab Schuljahr 2008/09) Jahrgangsstufe: 9 Lehrwerke / Hilfsmittel: Elemente Chemie 1, Klett
Laurentius-Siemer-Gymnasium Saterland Schuleigener Arbeitsplan für das Fach Chemie (vorläufige Fassung, gültig ab Schuljahr 2008/09) Jahrgangsstufe: 9 Lehrwerke / Hilfsmittel: Elemente Chemie 1, Klett
Atomaufbau. Elektronen e (-) Atomhülle
 Atomaufbau Institut für Elementarteilchen Nukleonen Protonen p (+) Neutronen n (o) Elektronen e (-) Atomkern Atomhülle Atom WIBA-NET 2005 Prof. Setzer 1 Elementarteilchen Institut für Name Symbol Masse
Atomaufbau Institut für Elementarteilchen Nukleonen Protonen p (+) Neutronen n (o) Elektronen e (-) Atomkern Atomhülle Atom WIBA-NET 2005 Prof. Setzer 1 Elementarteilchen Institut für Name Symbol Masse
