Anti-Human-Globulin GRÜN 0123 (IgG + C3d) monoklonal
|
|
|
- Renate Stein
- vor 7 Jahren
- Abrufe
Transkript
1 DE GEBRAUCHSINFORMATION Anti-Human-Globulin GRÜN 0123 (IgG + C3d) monoklonal REF 6912 REF x 10 ml 10 x 10 ml IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Das polyspezifische Anti-Human-Globulin GRÜN besteht aus einem Gemisch von Zellkulturüberständen verschiedener muriner Hybridomzelllinien. Das fertige Produkt enthält Material aus zwei Anti-IgG-Zelllinien (5H4 und 8D2-8), einer Anti-C3c-Zelllinie (86 5A2) und einer Anti-C3d-Zelllinie (139 4B4). Das Reagenz ist so zusammengesetzt, dass es optimal mit Zellen reagiert, die mit IgG und/oder C3 (C3b und/oder C3d) beladen sind. Das für dieses Reagenz verwendete Verdünnungsmedium enthält Natriumchlorid, Rinderserumalbumin und ausgewählte Puffer. Als Konservierungsmittel ist NaN 3 in einer Endkonzentration von 0,1% zugesetzt. Das polyspezifische Anti-Human-Globulin GRÜN enthält als Farbstoffe Acid Blue # 1 and Acid Yellow # 23. Anti-Human-Globulin wird im direkten Antiglobulintest (DAT) und im indirekten Antiglobulintest (ICT) eingesetzt. Im direkten Antiglobulintest werden in vivo an Erythrozyten gebundene Antikörper und/oder Komplementfaktoren nachgewiesen. Direkte Antiglobulinteste können die Diagnose bei autoimmunhämolytischen Anämien (AIHA), hämolytischen Anämien bei Föten und Neugeborenen und bei verzögerten hämolytischen Transfusionsreaktionen unterstützen. Im indirekten Antiglobulintest werden in vitro an Erythrozyten gebundene Antikörper und/oder Komplementfaktoren nachgewiesen. Der indirekte Antiglobulintest wird bei Tests auf D weak, bei Kreuzproben, beim Nachweis und der Identifizierung von irregulären Blutgruppen-Antikörpern und bei der Phänotypisierung von Erythrozyten eingesetzt. Antiglobulinteste werden auch bei Verdacht auf eine Medikamenten-induzierte Erythrozytensensibilisierung angewandt. Die Reaktivität von Anti-IgG, Anti-C3b und Anti-C3d wird in serologischen Tests mit IgG oder C3 beladenen Erythrozyten entsprechend anerkannter Testverfahren bewertet. Die Spezifität wird durch Tests gegen eine Vielzahl von mit verschiedenen humanen Proteinen beladenen Zellen überprüft. Die Abwesenheit kontaminierender Heteroagglutinine wird durch serologische Tests gegen unsensibilisierte Zellen aller AB0-Gruppen getestet. Die Abwesenheit von nachweisbarem Anti-C4 wird in serologischen Tests gegen mit C4b und C4d beladenen Zellen bestätigt. Dieses Reagenz reagiert speziell mit humanem IgG bzw. C3 (C3b und C3d) beladenen Erythrozyten, wenn es gemäß der empfohlenen Gebrauchsinformation verwendet wird. 2. Testprinzip Mit einem Antiglobulintest wird in vivo oder in vitro an Erythrozyten gebundenes humanes IgG oder gebundene humane Komplementfaktoren mit Hilfe von Anti-Humanglobulinen nachgewiesen. Die in diesem Reagenz vorliegenden Anti-Humanglobuline sind monoklonale Antikörper, die mittels Hybridomazellen von mit humanen Immunglobulinen oder humanen Komplementfaktoren immunisierten Mäusen gewonnen werden. Diese Anti-Humanglobuline reagieren sowohl mit humanen Immunglobulinen bzw. Komplementfaktoren, die an die Erythrozytenmembran gebunden sind, als auch mit denjenigen, die in der flüssigen Phase vorhanden sind. Zum spezifischen Nachweis von nur an Erythrozyten gebundenen Immun-
2 globulinen bzw. Komplementfaktoren müssen zunächst die freien Immunglobuline/ Komplementfaktoren durch eine Reihe aufeinanderfolgender Waschprozesse entfernt werden, damit gewährleistet ist, dass nur noch an Erythrozyten gebundene Immunglobuline/Komplementfaktoren vorhanden sind und mit dem Anti-Humanglobulin reagieren können. Wenn die Erythrozyten mit Immunglobulinen/Komplementfaktoren beladen sind, binden die Anti-Humanglobuline spezifisch an diese Proteine und bilden Brücken zwischen den Erythrozyten. Diese Reaktion ist optisch durch die Agglutination der Erythrozyten erkennbar. Sind die Erythrozyten nicht beladen, kann keine Reaktion mit dem Anti- Humanglobulin und somit auch keine Agglutination stattfinden. 3. Lagerung und Haltbarkeit Anti-Human-Globulin GRÜN (IgG + C3d) monoklonal bei C lagern. Nicht einfrieren! Das Reagenz vor Gebrauch auf Raumtemperatur ( C) erwärmen lassen und unmittelbar nach dem Gebrauch wieder bei C lagern. Das Reagenz ist bei Einhaltung der angegebenen Lagerbedingungen nach dem ersten Öffnen bis zum auf dem Etikett angegebenen Haltbarkeitsdatum verwendbar, wenn es keine Trübungen oder andere Anzeichen für eine Kontamination aufweist. Das Reagenz nicht nach Ablauf des auf dem Etikett angegebenen Haltbarkeitsdatums benutzen. Kontaminierte Reagenzien nicht mehr benutzen! 4. Probenvorbereitung Für die Probennahme ist keine besondere Vorbereitung des Patienten bzw. des Spenders notwendig. Die Blutproben sollten entsprechend den üblichen medizinischen Verfahren entnommen werden. Direkter Antiglobulintest: Um eine signifikante in vitro Komplement-Bindung zu vermeiden, sollte antikoaguliertes Blut in EDTA gesammelt werden, wodurch der spezifische Nachweis einer in vivo Komplement-Sensibilisierung von Erythrozyten möglich wird. Andere Antikoagulanzien wie ACD und CPD sind zwar weniger wirksam als EDTA, können jedoch ebenfalls verwendet werden. Blutproben sollten so bald wie möglich nach der Entnahme untersucht werden. Wenn nur geronnenes Blut zur Verfügung steht, sollte dieses vor dem Einsatz im direkten Antiglobulintest nicht gekühlt werden (siehe Wichtige Hinweise / Grenzen der Methode). Indirekter Antiglobulintest: Serumproben sollten von frisch entnommenem geronnenem Blut gewonnen werden. Plasma sollte nicht verwendet werden, wenn ein optimaler Nachweis komplementbindender Erythrozyten-Antikörper gewünscht wird, da die Komplementaktivierung durch Blutgruppen-Antikörper durch die Wirkung mancher Antikoagulanzien, die als Chelatbildner Ca ++ - und Mg ++ -Ionen binden, gehemmt werden kann. Die aktive Serumkomplement-Konzentration nimmt während der Aufbewahrung ab, daher kann ein optimaler Nachweis von komplementbindenden Antikörpern nur mit Serum von frisch entnommenen Blutproben erzielt werden. Wenn eine Testung nicht ohne zeitliche Verzögerung möglich ist, sollte das Serum von den Erythrozyten getrennt werden und bei C für maximal 48 Stunden gelagert werden. Alternativ kann das Serum auch eingefroren werden. Plasma kann verwendet werden, wenn kein Serum zur Verfügung steht bzw. der Test nur zum Nachweis einer IgG-Sensibilisierung durchgeführt wird. 5. Zusätzlich benötigte Materialien Isotonische NaCl-Lösung, ph 6,5 7,5 Reagenzgläser (75 x 12 mm) Einweg-Pasteur-Pipetten Wasserbad/Brutschrank (37 C ± 1 C) Zentrifuge ( x g) Testerythrozyten für den Nachweis bzw. die Identifikation von Antikörpern IgG-beladene Testerythrozyten (Coombs Control)
3 6. Testdurchführung Direkter Antiglobulintest 1. Die zu untersuchenden Erythrozyten mindestens einmal in isotonischer NaCl-Lösung waschen und eine ca. 2-5%ige Erythrozytensuspension in isotonischer NaCl-Lösung herstellen Tropfen (ca µl) der gewaschenen 2-5%igen Erythrozytensuspension in ein gekennzeichnetes Röhrchen geben. 3. Die Erythrozyten mindestens 3 x mit reichlich isotonischer NaCl-Lösung waschen. Den Überstand nach jedem Waschvorgang vollständig dekantieren und bei jedem Waschschritt auf eine gründliche Resuspendierung und gutes Vermischen der Erythrozyten mit der neu zugefügten NaCl-Lösung achten. 4. Nach dem letzten Waschschritt den Überstand vollständig dekantieren, sodass man ein trockenes Erythrozytensediment erhält Tropfen (ca µl) Anti-Human-Globulin GRÜN (IgG + C3d) monoklonal zu dem Erythrozytensediment geben und vorsichtig, aber gründlich mischen, um die Erythrozyten zu resuspendieren Sekunden bei x g oder bei alternativer Drehzahl mit angepasster Zeit zentrifugieren. 7. Unter vorsichtigem Aufschütteln des Röhrchens auf Agglutination prüfen. 8. Negative oder nur schwach positive Ergebnisse durch Zugabe von IgG-beladenen Testzellen überprüfen (entsprechend den Herstellerangaben in der Gebrauchsinformation der IgG-beladenen Testzellen). Bitte beachten: Ein Mikroskop oder ein anderes optisches Hilfsmittel kann zur Bestätigung schwacher oder negativer Hämagglutinationsreaktionen verwendet werden. Die Anti-Komplement-Reaktionen können durch 5 10 Minuten Inkubation bei Raumtemperatur (~ C) verstärkt werden. Anschließend erneut zentrifugieren und prüfen (entsprechend Punkt 6 und 7). Der erste Zentrifugationsschritt sollte jedoch niemals übersprungen werden, da Anti-IgG-Reaktionen durch die Inkubation bzw. erneute Zentrifugation beeinträchtigt werden können. Zur Kontrolle sollte das Anti-Human-Globulin routinemäßig mit schwach IgG-sensibilisierten Erythrozyten und mit Erythrozyten, die mit C3b oder C3d beladen sind, überprüft werden. Nicht beladene Erythrozyten sollten als negative Kontrolle parallel mitgeführt werden. Indirekter Antiglobulintest Für Antikörpernachweis, Antikörperidentifizierung und Kreuzprobe Bitte beachten: Die folgende Testmethode ist nur eine Empfehlung. Änderungen der Testmethode nach anerkannten und gut dokumentierten immunhämatologischen Verfahren (wie z.b. eine Erhöhung des Verhältnisses von Serum zu Zellen und/oder der Inkubationszeit) können erforderlich sein, um den Anforderungen individueller Labors zu entsprechen. Bei der Verwendung von Supplementen (Reaktionsverstärkern mit geringer Ionenstärke oder anderen Reaktionsverstärkern) muss die Gebrauchsanweisung des jeweiligen Herstellers strikt befolgt werden. Die Phänotypisierung von Erythrozyten mit spezifischen Blutgruppen- Testreagenzien sollte gemäß den Gebrauchsanweisungen des jeweiligen Herstellers durchgeführt werden. Vom Benutzer vorgenommene Änderungen beim Testverfahren müssen validiert werden. Im Folgenden ist als Beispiel ein häufig angewandtes Testprotokoll für den Nachweis bzw. die Identifikation von Antikörpern oder für die Kreuzprobe angegeben:
4 1. Für jede zu testende Spenderzelle, Screening-Zelle oder Panelzelle ein Röhrchen beschriften. 2. Mindestens 2 Tropfen (ca µl) Serum und 1 Tropfen einer 2-5%igen Suspension von Spenderzellen oder Testerythrozyten (Screening-Zellen oder Panelzellen) in die gekennzeichneten Röhrchen geben und gründlich mischen Sekunden bei x g oder bei alternativer Drehzahl mit angepasster Zeit zentrifugieren. 4. Den Überstand auf sichtbare Hämolyse prüfen. 5. Unter vorsichtigem Aufschütteln des Röhrchens makroskopisch auf Agglutination prüfen. 6. Den Inhalt der Röhrchen erneut mischen und Minuten bei 37 C ± 1 C inkubieren Sekunden bei x g oder bei alternativer Drehzahl mit angepasster Zeit zentrifugieren. 8. Den Überstand auf sichtbare Hämolyse prüfen. 9. Unter vorsichtigem Aufschütteln des Röhrchens makroskopisch auf Agglutination prüfen. 10. Den Inhalt der Röhrchen erneut vorsichtig, aber gründlich mischen und die Erythrozyten 3 4 x mit isotonischer NaCl-Lösung waschen. Den Überstand nach jedem Waschvorgang vollständig dekantieren und bei jedem Waschschritt auf eine gründliche Resuspendierung und gutes Vermischen der Erythrozyten mit der neu zugefügten NaCl- Lösung achten. 11. Nach dem letzten Waschschritt den Überstand vollständig dekantieren, sodass man ein trockenes Erythrozytensediment erhält Tropfen (ca µl) Anti-Human-Globulin GRÜN (IgG + C3d) monoklonal zu jedem Erythrozytensediment geben und vorsichtig, aber gründlich mischen, um die Erythrozyten zu resuspendieren Sekunden bei x g oder bei alternativer Drehzahl mit angepasster Zeit zentrifugieren. 14. Unter vorsichtigem Aufschütteln des Röhrchens auf Agglutination prüfen. 15. Negative oder nur schwach positive Ergebnisse durch Zugabe von IgG-beladenen Testzellen überprüfen (entsprechend den Herstellerangaben in der Gebrauchsinformation der IgG-beladenen Testzellen). Bitte beachten: Ein Mikroskop oder ein anderes optisches Hilfsmittel kann zur Bestätigung schwacher oder negativer Hämagglutinationsreaktionen verwendet werden. Zur Kontrolle sollte das Anti-Human-Globulin routinemäßig mit schwach mit IgG-sensibilisierten Erythrozyten und mit Erythrozyten, die mit C3b oder C3d beladen sind, überprüft werden. Nicht beladene Erythrozyten sollten als negative Kontrolle parallel mitgeführt werden. Bei Testungen, die nicht in einem Milieu mit geringer Ionenstärke durchgeführt werden, ist es ein übliches und gut dokumentiertes Verfahren, die Serummenge zu erhöhen (Erhöhung des Verhältnisses von Serum zu Zellen) und/oder eine längere Inkubation (mehr als 15 Minuten) durchzuführen, um die Sensitivität des Testverfahrens zu erhöhen. Bei der Verwendung von Reaktionsverstärkern mit geringer Ionenstärke muss die Gebrauchsanweisung des jeweiligen Herstellers strikt befolgt werden. 7. Interpretation der Ergebnisse Eine Agglutination der Erythrozyten in der Antiglobulintestphase des direkten oder indirekten Antiglobulintests zeigt ein positives Testergebnis an und weist innerhalb der Grenzen der Testmethode auf das Vorhandensein von IgG und/oder Komplement (C3) auf den Erythrozyten hin. Findet keine Agglutination der Erythrozyten in der Antiglobulintestphase des direkten oder indirekten Antiglobulintests statt, zeigt dies ein negatives Testergebnis an und weist innerhalb der Grenzen der Testmethode auf die Abwesenheit von serologisch nachweisbarem IgG und/oder Komplement (C3) auf den Erythrozyten hin.
5 Das Testergebnis kann nicht gewertet werden, wenn die Kontrollen wie folgt reagieren: - keine Agglutination nach Zugabe von IgG-beladenen Testzellen zu einem negativen Antiglobulintest - keine Agglutination der Kontrollerythrozyten, die schwach mit IgG beladen sind - keine Agglutination der Kontrollerythrozyten, die mit C3b oder C3d beladen sind - Agglutination der Kontrollerythrozyten, die nicht mit IgG/Komplement beladen sind Bei der Interpretation der Ergebnisse müssen die Grenzen der Methode (s. 9. Wichtige Hinweise/Grenzen der Methode) beachtet werden. 8. Stabilität der Reaktionen Alle Testergebnisse müssen unmittelbar nach Beendigung der Testdurchführung beurteilt werden. 9. Wichtige Hinweise / Grenzen der Methode 1. Anti-Human-Globulin GRÜN (IgG + C3d) monoklonal ist nur für den in vitro diagnostischen Gebrauch geeignet und darf nur von geschultem Fachpersonal eingesetzt werden. 2. Positive Ergebnisse im direkten Antiglobulintest (DAT) in Verbindung mit einer Komplementsensibilisierung sind nicht unbedingt auf eine in vivo Komplementbindung zurückzuführen, wenn die Testzellen von einer gekühlten geronnenen Blutprobe stammen. 3. Das Auslassen der Inkubationsphase von 5 10 Minuten mit darauffolgender erneuter Zentrifugation für den optimalen Nachweis einer schwachen Komplementsensibilisierung im direkten Antiglobulintest (DAT), kann zu schwachen oder falsch negativen Ergebnissen führen. 4. Ein negatives Ergebnis im direkten Antiglobulintest schließt nicht unbedingt eine klinische Diagnose auf eine hämolytische Anämie bei Föten und Neugeborenen durch AB0-Inkompatibilität oder eine autoimmunhämolytische Anämie aus. 5. Erythrozyten, die im direkten Antiglobulintest (DAT) positiv reagieren, können nicht im indirekten Antiglobulintest eingesetzt werden. 6. Bestimmte Krankheitsstadien und medikamentöse Therapien können einen positiven direkten bzw. indirekten Antiglobulintests verursachen. 7. Eine Inaktivierung durch humane Serumproteinreste bedingt durch nicht sorgfältig durchgeführte Waschschritte oder eine Verdünnung des Anti-Human-Globulins aufgrund zu hoher Restmengen an NaCl-Lösung nach dem Waschen können zu schwachen oder falsch negativen Ergebnissen im Antiglobulintest führen. 8. Verzögerungen während der Durchführung des Antiglobulintests können zu schwachen oder falsch negativen Ergebnissen führen. Insbesondere Anti-IgG Reaktionen können nachteilig durch Inkubation oder erneute Zentifugation beeinflusst werden. 9. Ein zu starkes oder unangemessenes Aufschütteln des Erythrozytensediments im Antiglobulintest kann zu schwächeren oder falsch negativen Ergebnissen führen. 10. Um falsche Ergebnisse zu vermeiden, sollte das Reagenz auch nicht zu kalt sein, wenn es für Testungen benutzt wird. Das Reagenz und die zu untersuchenden Proben sowie die Kontrollmaterialien sollten vor der Testdurchführung Raumtemperatur ( C) erreicht haben. 11. Falsche Ergebnisse können auch durch eine zu lange Lagerung der zu untersuchenden Proben und/oder ungeeignete Lagerbedingungen bzw. durch ungeeignetes Probenmaterial verursacht werden. 12. Ungeeignete Techniken, falsche Zentrifugation oder Inkubation, unsaubere Röhrchen, falscher ph-wert der isotonischen NaCl-Lösung und/oder kontaminierte Materialien können zu falsch negativen oder falsch positiven Ergebnissen führen. 13. Es ist nicht möglich, für alle verfügbaren Zentrifugentypen eine allgemein verbindliche Zentrifugationsgeschwindigkeit oder zeit anzugeben. Zentrifugen müssen individuell kalibriert werden, um die optimale Zeit und Geschwindigkeit zu ermitteln, die benötigt
6 wird, um eine starke Agglutination mit positiven Zellen zu erhalten und die eine vollständige und leichte Resuspendierung bei negativen Reaktionen ermöglicht. 14. Eine Kontamination des Anti-Humanglobulins mit menschlichem Serum kann das Reagenz neutralisieren. Eine mikrobielle Kontamination des Reagenzes sollte ebenfalls unbedingt vermieden werden, weil dies die Haltbarkeit des Produkts verkürzen und zu falschen Ergebnissen führen kann. Das Testreagenz deshalb nicht mehr benutzen, wenn eine Trübung oder andere sichtbare Veränderungen festgestellt werden. Dies kann auf eine mikrobielle Kontamination hinweisen. 15. Die Verwendung von Anti-Human-Globulin Grün schließt nicht die Notwendigkeit aus, die Reaktivität des Anti-Human-Globulins angemessen zu kontrollieren und zu bestätigen. Das Färbemittel zeigt optisch an, dass das Anti-Human-Globulin hinzugefügt wurde, bietet aber keine Garantie für die Reaktionsfähigkeit des Reagenzes. 16. Bei der Interpretation der Ergebnisse sollte immer berücksichtigt werden, ob Transfusionen oder Transplantationen stattgefunden haben. Die Transfusions- und/oder Transplantationsanamnese, aber auch die Medikamentenanamnese, sollte zur Interpretation herangezogen werden. 17. Anti-Human-Globulin GRÜN (IgG + C3d) monoklonal nicht verdünnen und nur wie in dieser Gebrauchsinformation angegeben einsetzen. 18. Abweichungen von der vorliegenden Gebrauchsinformation können zu einer nicht optimalen Produktleistung führen. Vom Benutzer vorgenommene Änderungen der Testverfahren müssen validiert werden. 10. Warn- und Entsorgungshinweise Sämtliche für den Test verwendete Materialien biologischen Ursprungs, insbesondere die zu testenden humanen Proben, sollten als potentiell infektiös betrachtet werden. Die Abwesenheit von murinen Viren wurde nicht untersucht. Für die Herstellung dieses Produkts verwendetes Material bovinen Ursprungs stammt von Tieren aus den USA, die von Veterinärinspektoren kontrolliert und als krankheitsfrei deklariert wurden. Das TSE (Transmissible Spongioform Encephalopathy)-Risiko dieses von Rindern stammenden Produkts wird als gering betrachtet. Beim Umgang mit biologischen Materialien werden angemessene Sicherheitsvorkehrungen empfohlen (nicht mit dem Mund pipettieren; Schutzhandschuhe bei der Testdurchführung tragen; Händedesinfektion nach der Testdurchführung). Biologische Materialien müssen vor der Entsorgung inaktiviert werden (z.b. durch Autoklavieren). Einwegmaterialien sind nach Gebrauch zu autoklavieren oder zu verbrennen. Verschüttetes potentiell infektiöses Material sollte unverzüglich mit einem saugfähigen Papiertuch entfernt werden und der kontaminierte Bereich mit einem geeigneten Desinfektionsmittel oder 70%igem Ethanol desinfiziert werden. Material, das für die Entfernung von Verschüttetem benutzt wurde, muss vor der Entsorgung inaktiviert werden (z.b. durch Autoklavieren). Die Tropfsaughütchen der Fläschchen enthalten Latex. Latex kann allergische Reaktionen hervorrufen. Das Testreagenz enthält 0,1% NaN 3 als Konservierungsmittel. Natriumazid ist toxisch. Nicht schlucken und Kontakt mit der Haut und Schleimhäuten vermeiden. Kupfer und Blei, die in einigen Rohrsystemen eingesetzt werden, können mit Azid explosive Salze bilden, deshalb sollte bei der Beseitigung von Azid-haltigem Material mit reichlich Wasser nachgespült werden. Die Entsorgung aller Proben und Testmaterialien sollte entsprechend der gesetzlichen Richtlinien erfolgen. 11. Literatur Coombs RRA, Mourant AE, Race RR. Detection of weak and incomplete Rh agglutinins; A new test. Lancet 1945; ii:15 Coombs RRA, Mourant AE, Race RR. A new test for the detection of weak and incomplete antibodies. Brit J Exp Pathol 1945; 26:255.
7 Garratty G, Petz LD. The significance of red cell bound complement components in the development of standards and quality assurance for the anti-complement components of antiglobulin sera. Transfusion 1976; 19: Howell P, Giles CM. A detailed serological study of five anti-jk a sera reacting by the antiglobulin technique. Vox Sang 1983; 45: ISBT/ICSH Working Party. International reference polyspecific anti-human globulin reagents. Vox Sang 1987; 53: Issitt PD. Applied Blood Group Serology. 4 th edition. Montgomery Scientific, Durham, SC Lachmann PJ, Pangburn MK, Oldroyd RG. Breakdown of C3 after complement activation. J Exp Med 1982; 156: Moore BPL. Serological and Immunological Methods of the Canadian Red Cross Blood Transfusion Service. 8 th Edition. Toronto: Hunter Rose, Voak D, Downie DM, Moore BPL et al. Quality control of anti-human globulin tests: use of replicate tests to improve performance. Bio Bull. 1986; 1: Wright MS, Issitt PD. Anticomplement and the indirect antiglobulin test. Transfusion 1979; 19: Walker RH, ed. Technical Manual. 13 th Edition. American Association of Blood Banks. Bethesda, MD Köhler G, Milstein C. Continuous cultures of fused cells secreting antibody of predefined specificity. Nature 1975; 256:495. FDA Docket No. 84S-0182 Recommended methods for evaluating potency, specificity and reactivity of Anti-Human Globulin. Draft March Gebrauchsinformation Version: 1/2015 / Stand: Auftragsannahme/Ordering: Customer Service: BAG Health Care GmbH Tel.: +49 (0) 6404 / Tel.: +49 (0) 6404 / Amtsgerichtsstraße 1-5 Tel.: +49 (0) 6404 / Fax: +49 (0) 6404 / Fax: +49 (0) 6404 / Lich / Germany Fax: +49 (0) 6404 / info@bag-healthcare.com verkauf@bag-healthcare.com service@bag-healthcare.com
8 EN INSTRUCTIONS FOR USE Anti-Human-Globulin GREEN 0123 (IgG + C3d) monoclonal REF 6912 REF x 10 ml 10 x 10 ml FOR IN VITRO DIAGNOSTIC USE 1. Description of product The polyspecific Anti-Human-Globulin GREEN is prepared by blending cell culture supernatants produced by individual murine hybridoma cell lines. The final product contains material from two Anti-IgG cell lines (5H4 und 8D2-8), one Anti-C3c cell line (86 5A2) and one Anti-C3d cell line (139 4B4). This reagent is blended to react optimally with cells coated with IgG and/or C3 (C3b and/or C3d). The diluent used for this reagent contains sodium chloride, bovine serum albumin and selected buffers. Sodium azide, at a final concentration of 0.1%, is added as an antimicrobial agent. The polyspecific Anti-Human-Globulin GREEN contains Acid Blue # 1 and Acid Yellow # 23 as colouring agents. Anti-Human-Globulin is used in a Direct Antiglobulin Test (DAT) and in an Indirect Antiglobulin Test (IAT). A Direct Antiglobulin Test is used to detect antibodies and/or complement bound to red cells in vivo. Direct antiglobulin test results may support the diagnosis of Autoimmune Hemolytic Anemia (AIHA), Hemolytic Disease of the Fetus and Newborn (HDFN) and Delayed Hemolytic Transfusion Reactions (DHTR). An Indirect Antiglobulin Test detects antibodies and/or complement bound to red cells in vitro. This technique is used in tests for weak D, crossmatch tests, detection and identification of unexpected blood group antibodies and red cell phenotyping. Antiglobulin tests are also used by suspicion on drug induced red cell sensitization. Anti-IgG, Anti-C3b and Anti-C3d potencies are assessed in serological tests with red cells coated specifically with IgG or C3 according to approved test procedures. Defined specificity is verified by tests against a variety of cells coated with different human proteins. The absence of contaminating heteroagglutinins is confirmed in serological tests against unsensitized cells of all ABO groups. The absence of detectable Anti-C4 is verified in serological tests against cells coated with C4b and C4d. This reagent reacts specifically with red cells coated with human IgG and/or C3 (C3b and C3d) when used in accordance with the recommended Instructions for Use. 2. Principle of the test Antiglobulin tests detect human complement or human IgG bound in vivo or in vitro to red cells with the aid of anti-human globulins. The anti-human globulins contained in this reagent are monoclonal antibodies produced by hybridoma cells. The hybridoma cells derive from mice immunized with human complement or human immunoglobulins. The anti-human globulins will react with human complement and/or human immunoglobulins whether bound to the red cell membrane or present in the fluid phase. For the specific detection of red cell bound complement and/or immunoglobulins only, free serum immunoglobulins/complement must first be removed by a series of sequential wash procedures to ensure that only cell bound immunoglobulins/complement is present to react with the antihuman globulins. If red cells are coated with immunoglobulins/complement, anti-human globulins will bind specific to these proteins and forming bridges between the red cells. This
9 reaction is optically recognizable by the agglutination of the red cells. If the red cells are not coated, no reaction can occur with the anti-human globulins and therefore no agglutination take place. 3. Storage and Shelf Life Store Anti-Human-Globulin GREEN (IgG + C3d) monoclonal at C. Do not freeze! Allow the reagent to equilibrate to ambient room temperature ( C) prior to use. Return reagent to C for storage as appropriate, immediately after use. Once Anti-Human-Globulin GREEN (IgG + C3d) monoclonal has been opened the first time, the reagent may be used up to the expiration date indicated on the label if the specified storage conditions are observed and no turbidity or other signs of contamination are observed. Do not use the reagent after the expiry date printed on the label. Do not use contaminated reagents! 4. Specimen Preparation No special preparation of the patient/donor is required prior to specimen collection. Blood samples should be collected by approved medical procedures. Direct Antiglobulin Test: To prevent significant in vitro fixation of complement, anticoagulated blood should be collected into EDTA, thereby allowing the specific detection of in vivo red cell complement sensitization. Other anticoagulants such as ACD or CPD may be less effective than EDTA, but remain acceptable for use. Blood samples should be tested as soon as possible following collection. If only clotted blood is available, it should not be refrigerated prior to direct antiglobulin testing (refer to Important Directions/Limitations of Procedure). Indirect Antiglobulin Test: Serum samples should be prepared from freshly drawn clotted blood. Plasma should not be used if optimal detection of complement-binding red cell antibodies is desired, since complement activation by blood group antibodies may be inhibited by the action of some anticoagulants that chelate Ca ++ - and Mg ++ ions. Active serum complement levels are depleted during storage, therefore optimal detection of complementbinding antibodies is achieved by testing serum from freshly drawn blood samples. If unavoidable delays in testing occur, the serum should be separated from the red cells and stored at C for no more than 48 hours. Alternatively, the serum may be frozen. Plasma may be used if serum is unavailable and/or the test is performed solely to detect IgG sensitization. 5. Additional materials required Isotonic saline, ph Test tubes (75 x 12 mm), glass Single-use Pasteur pipettes Waterbath/Incubator (37 C ± 1 C) Centrifuge ( rcf) Reagent red blood cells with known phenotype for antibody detection and identification Control cells sensitized with IgG (Coombs Control) 6. Test procedure Direct Antiglobulin Test 1. Wash the test red cells at least once in isotonic saline and prepare a 2-5% red cell suspension in isotonic saline. 2. Add 1-2 drops ( µl) of the washed, 2-5% red cell suspension to an appropriately labeled test tube. 3. Wash the red cells at least three times with large volumes of isotonic saline. Decant supernatant saline completely following each wash and ensure thorough resuspension and mixing of red cells with each new addition of saline for subsequent washes.
10 4. Following the final wash, completely decant the supernatant saline to ensure removal of all residual saline and a resultant dry red cell botton. 5. Add 2 drops ( µl) of Anti-Human-Globulin GREEN (IgG + C3d) monoclonal to each tube containing a dry botton of washed red cells and mix gently, but thoroughly, to resuspend the red cells. 6. Centrifuge for 15 seconds at rcf or of equivalent force with adapted time. 7. Gently resuspend the red cell button and examine for agglutination. 8. Negative or weak positive antiglobulin test results should be appropriately controlled by the addition of IgG sensitized reagent control cells (refer to the relevant manufacturer s Instructions for Use for IgG sensitized control cells). Please note: A microscope or other optical aid, may be used to confirm weak or negative hemagglutination reactions. The strength of anti-complement reactions may be enhanced following a 5 10 minute incubation at room temperature (~ C) with subsequent re-centrifugation, as outlined above (steps 6 and 7). However, the immediate spin phase should never be omitted since anti-igg reactions may be adversely affected by incubation and/or re-centrifugation. As routine control the Anti-Human-Globulin should be tested against red cells weakly sensitized with IgG and against red cells coated with either C3b or C3d. Unsensitized red cells should be tested in parallel as a negative control. Indirect Antiglobulin Test For Antibody Detection, Identification or Compatibility Testing Please note: The following test method is recommended only as a guide. Modifications to the test procedure following accepted and well documented immunohematology practices (such as an increase in serum:cell ratio and/or incubation time) may be desirable to comply with the requirements of individual laboratories. However, the application of low ionic strength antibody enhancement or potentiating reagents requires strict adherence to the respective manufacturer s recommended Instructions for Use. Red cell phenotyping with specific Blood Grouping Reagents should be performed in accordance with the manufacturer s Instructions for Use. User-defined modifications to test procedure may require validation. The following is one example of a commonly used test protocol that may be used for antibody detection, antibody identification or compatibility testing: 1. Appropriately label one test tube for each donor cell, Screening Cell or Panel Cell to be tested. 2. Dispense at least 2 drops (~ µl) of serum and 1 drop of a 2-5% donor cell or reagent red cell (Screening Cell or Panel Cell) suspension to the appropriate test tube and mix thoroughly. 3. Centrifuge for 15 seconds at rcf or of equivalent force with adapted time. 4. Examine supernatant for visible hemolysis. 5. Gently resuspend the red cell button and examine macroscopically for agglutination. 6. Mix tube contents again and incubate test tubes at 37 C ± 1 C for minutes. 7. Centrifuge for 15 seconds at rcf or of equivalent force with adapted time. 8. Examine supernatant for visible hemolysis. 9. Gently resuspend the red cell button and examine macroscopically for agglutination. 10. Mix tube contents gently, but thoroughly, and wash red cells 3 4 times with isotonic saline. Decant supernatant saline completely following each wash and ensure thorough resuspension and mixing of red cells with each new addition of saline for subsequent washes. 11. Following the final wash, completely decant the supernatant saline to ensure removal of all residual saline and a resultant dry red cell button.
11 12. Add 2 ( µl) drops Anti-Human-Globulin GREEN (IgG + C3d) monoclonal to each tube containing a dry button of washed red cells and mix gently, but thoroughly, to resuspend red cells. 13. Centrifuge for 15 seconds at rcf or of equivalent force with adapted time. 14. Gently resuspend the red cell button and examine macroscopically for agglutination. 15. Negative or weak positive antiglobulin test results should be appropriately controlled by the addition of IgG sensitized reagent control cells (refer to the relevant manufacturer s Instructions for Use for IgG sensitized control cells). Please note: A microscope or other optical aid, may be used to confirm weak or negative hemagglutination reactions. As routine control the Anti-Human-Globulin should be tested against red cells weakly sensitized with IgG and against red cells coated with either C3b or C3d. Unsensitized red cells should be tested in parallel as a negative control. In other than low ionic test systems, it is a common and well-documented practice to increase the quantity of serum used in the test system (increase in serum:cell ratio) and/or to increase the incubation time beyond 15 minutes in order to increase the sensitivity of antibody detection/identification test procedures. When using low ionic enhancement techniques, however, the low ionic reagents must be used exactly as outlined in the respective Instructions for Use. 7. Interpretation Of Test Results Agglutination of test red cells in the antiglobulin test phase of the direct or indirect antiglobulin test procedure constitutes a positive test result and, within the accepted limitations of the test procedure, indicates the presence of IgG and/or complement (C3) on the red cells. No agglutination of test red cells in the antiglobulin test phase of the direct or indirect antiglobulin test procedure constitutes a negative test result and, within the accepted limitations of the test procedure, indicates the absence of serological detectable IgG or complement (C3) on the red cells. When the controls react as followed, the test results cannot be interpreted: - no agglutination with IgG sensitized cells added to a negative antiglobulin test - no agglutination with control red cells weakly sensitized with IgG - no agglutination with control red cells coated with C3b or C3d - agglutination with unsensitized red cells The limitations of the procedure must be considered when interpreting the results (see 9. Important directions/limitations of procedure). 8. Stability of the reactions All test results should be interpreted immediately upon completion of the test. 9. Important Directions/Limitations of Procedure 1. Anti-Human-Globulin GREEN (IgG + C3d) monoclonal is designed for in vitro diagnostic use only and should be used by properly trained staff. 2. Positive direct antiglobulin test (DAT) results associated with complement sensitization may not reflect in vivo complement fixation if the test cells are from a previously refrigerated clotted blood sample. 3. Omission of the 5 10 minute incubation phase with subsequent re-centrifugation (for optimal detection of weak complement sensitization in the direct antiglobulin test (DAT) procedure) may result in weak or false negative results. 4. A negative direct antiglobulin (DAT) test result does not necessarily preclude clinical diagnosis of ABO Hemolytic Disease of the Fetus and Newborn (HDFN) or Autoimmune Hemolytic Anemia (AIHA).
12 5. Red cells with a positive direct antiglobulin test (DAT) result cannot be used in indirect antiglobulin test procedures. 6. Certain disease states and medication therapy may be associated with positive direct and/or indirect antiglobulin tests. 7. Weak or false negative antiglobulin test results may occur due to inactivation by residual human serum protein following inadequate wash procedures or dilution of the Anti- Human-Globulin reagent associated with excess residual saline following wash procedures. 8. Procedural delays in antiglobulin test performance may result in weak or false negative results. Anti-IgG reactions, in particular, may be adversely affected by incubation and/or re-centrifugation. 9. Overly vigorous or inappropriate resuspension of red cells in antiglobulin test procedures may result in weak or false negative results. 10. To minimize risks for false results, this reagent must not be used when cold. Ensure that this reagent, specimen to be tested and control reagents are allowed to equilibrate to ambient room temperature ( C) prior to testing. 11. False results may occur with specimen that have been subjected to prolonged and/or inappropriate storage conditions or if improper specimens are used. 12. Other variables such as improper technique, inappropriate centrifugation or incubation, improperly cleaned glassware, incorrect saline ph and/or contaminated materials may cause false negative or false positive results. 13. The centrifugal force applied should be the minimum required to produce a clear supernatant and a clearly delineated red cell button that can be easily resuspended. No single centrifugation speed or time can be recommended for all types of available centrifuges or test applications. Centrifuges should be calibrated individually to determine the optimal time and speed required to achieve the desired results. 14. Contamination of Anti-Human-Globulin with human serum may cause reagent neutralisation. Microbial contamination of Anti-Human-Globulin must be avoided as this may reduce the shelf life of the product and cause erroneous results. Do not use the reagent if marked turbidity or other observable indications of product alteration occur. These signs may indicate microbial contamination and/or product deterioration. 15. The use of green Anti-Human-Globulin does not preclude the necessity for adequate control and confirmation of antiglobulin reactivity. This dye provides a visual indication that the antiglobulin reagent has been added, but does not assure the reactivity of the reagent. 16. For interpretation of the test results, consider if transfusion or transplantation had happened. Take the case history of the transfusion or transplantation and also medicaments into consideration. 17. Do not dilute Anti-Human-Globulin GREEN (IgG + C3d) monoclonal. Use as supplied and as described in this Instructions for Use. 18. Deviation from the recommended Instructions for Use may result in less than optimal product performance. User-defined modifications to test procedures may require validation. 10. Warnings and instructions for disposal All materials of biological origin used for the test, especially the human specimen to be tested, should be regarded as potentially infectious. The absence of murine virus has not been determined. Any bovine source material used in the manufacture of this product is sourced from donor animals that have been inspected and certified by US veterinary service inspectors to be disease-free. This ruminant-based product is deemed to have low TSE (Transmissible Spongioform Encephalopathy) risk. When handling biological material appropriate safety precautions are recommended (do not pipette by mouth; wear disposable gloves while handling biological material and performing the test; disinfect hands when finished the test). Biological material should be inactivated before disposal (e.g. in an autoclave). Disposables should be autoclaved or incinerated after use. Spillage of potentially infectious materials
13 should be removed immediately with absorbent paper tissue and the contaminated areas swabbed with a suitable standard disinfectant or 70% alcohol. Material used to clean spills, including gloves, should be inactivated before disposal (e.g. in an autoclave). The dropper bulbs of these product contain natural rubber latex, which is known to cause allergic reactions in some individuals. The reagent contains 0.1% NaN 3 as preservative. Sodium azide is toxic. Do not ingest, avoid contact with the skin and mucous membranes. The copper and lead used in some plumbing systems can react with azides to form explosive salts. Therefore, when disposing of azidecontaining materials, they should be flushed away with a large volume of water. The disposal of all samples and test materials should be carried out according to legal directives. 11. References Coombs RRA, Mourant AE, Race RR. Detection of weak and incomplete Rh agglutinins; A new test. Lancet 1945; ii:15 Coombs RRA, Mourant AE, Race RR. A new test for the detection of weak and incomplete antibodies. Brit J Exp Pathol 1945; 26:255 Garratty G, Petz LD. The significance of red cell bound complement components in the development of standards and quality assurance for the anti-complement components of antiglobulin sera. Transfusion 1976; 19: Howell P, Giles CM. A detailed serological study of five anti-jk a sera reacting by the antiglobulin technique. Vox Sang 1983; 45: ISBT/ICSH Working Party. International reference polyspecific anti-human globulin reagents. Vox Sang 1987; 53: Issitt PD. Applied Blood Group Serology. 4 th edition. Montgomery Scientific, Durham, SC Lachmann PJ, Pangburn MK, Oldroyd RG. Breakdown of C3 after complement activation. J Exp Med 1982; 156: Moore BPL. Serological and Immunological Methods of the Canadian Red Cross Blood Transfusion Service. 8 th Edition. Toronto: Hunter Rose, 1980 Voak D, Downie DM, Moore BPL et al. Quality control of anti-human globulin tests: use of replicate tests to improve performance. Bio Bull. 1986; 1:41-52 Wright MS, Issitt PD. Anticomplement and the indirect antiglobulin test. Transfusion 1979; 19: Walker RH, ed. Technical Manual. 13 th Edition. American Association of Blood Banks. Bethesda, MD Köhler G, Milstein C. Continuous cultures of fused cells secreting antibody of predefined specificity. Nature 1975; 256:495 FDA Docket No. 84S-0182 Recommended methods for evaluating potency, specificity and reactivity of Anti-Human Globulin. Draft March 1992 Instructions for Use Version 1/2015 / Issue: Instructions for use in other languages see: or phone +49 (0)
14 Erklärung der Symbole auf den Etiketten / Explanation of symbols used on Labelling IVD In-vitro-Diagnostikum / For in vitro diagnostic use Lagertemperatur / Storage temperature LOT Lot-Nr. / Batch code Verwendbar bis / Use by REF Bestell-Nr. / Catalogue number Gebrauchsinformation beachten / Consult instructions for use MONOCL CLONE ORIG MURIN CONT NaN 3 TIT Monoklonal / Monoclonal Klon / Clone Ursprung: Maus / Origin: mouse Enthält Natriumazid / Contains Natriumazide Titer / Titer Achtung / Warning R 22 Gesundheitsschädlich beim Verschlucken. / Harmful if swallowed. Auftragsannahme/Ordering: Customer Service: BAG Health Care GmbH Tel.: +49 (0) 6404 / Tel.: +49 (0) 6404 / Amtsgerichtsstraße 1-5 Tel.: +49 (0) 6404 / Fax: +49 (0) 6404 / Fax: +49 (0) 6404 / Lich / Germany Fax: +49 (0) 6404 / info@bag-healthcare.com verkauf@bag-healthcare.com service@bag-healthcare.com
Rh-Kontrolle für monoklonale Testreagenzien Negativ-Kontrolle für monoklonale Testreagenzien
 GEBRAUCHSINFORMATION Rh-Kontrolle für monoklonale Testreagenzien Negativ-Kontrolle für monoklonale Testreagenzien IN VITRO DIAGNOSTIKUM 0123 1. Produktbeschreibung Die Rh-Kontrolle für monoklonale Testreagenzien
GEBRAUCHSINFORMATION Rh-Kontrolle für monoklonale Testreagenzien Negativ-Kontrolle für monoklonale Testreagenzien IN VITRO DIAGNOSTIKUM 0123 1. Produktbeschreibung Die Rh-Kontrolle für monoklonale Testreagenzien
Anti-H monoklonal (IgM)
 GEBRAUCHSINFORMATION Anti-H monoklonal (IgM) Klon: 10934C11 IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Anti-H monoklonal wird aus monoklonalen Maus-IgM-Antikörpern (Klon: 10934C11) hergestellt. Das Testreagenz
GEBRAUCHSINFORMATION Anti-H monoklonal (IgM) Klon: 10934C11 IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Anti-H monoklonal wird aus monoklonalen Maus-IgM-Antikörpern (Klon: 10934C11) hergestellt. Das Testreagenz
Anti-Human-Globulin GRÜN 0123 (IgG + C3d) monoklonal
 GEBRAUCHSINFORMATION Anti-Human-Globulin GRÜN 0123 (IgG + C3d) monoklonal IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Das polyspezifische Anti-Human-Globulin GRÜN besteht aus einem Gemisch von Überständen
GEBRAUCHSINFORMATION Anti-Human-Globulin GRÜN 0123 (IgG + C3d) monoklonal IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Das polyspezifische Anti-Human-Globulin GRÜN besteht aus einem Gemisch von Überständen
Anti-c monoklonal (IgM), Klon MS35 Anti-E monoklonal (IgM), Klon MS12/260
 GEBRAUCHSINFORMATION Anti-c monoklonal (IgM), Klon MS35 Anti-E monoklonal (IgM), Klon MS12/260 0123 IN VITRO DIAGNOSTIKA 1. Produktbeschreibung Anti-c und Anti-E monoklonal (IgM) werden aus monoklonalen
GEBRAUCHSINFORMATION Anti-c monoklonal (IgM), Klon MS35 Anti-E monoklonal (IgM), Klon MS12/260 0123 IN VITRO DIAGNOSTIKA 1. Produktbeschreibung Anti-c und Anti-E monoklonal (IgM) werden aus monoklonalen
Bromelin, flüssig GEBRAUCHSINFORMATION IN VITRO DIAGNOSTIKUM
 GEBRAUCHSINFORMATION Bromelin, flüssig IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Die Bromelinlösung ist ein stabiles, gebrauchsfertiges Reagenz für den Bromelintest. Das Enzym Bromelin wird aus der
GEBRAUCHSINFORMATION Bromelin, flüssig IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Die Bromelinlösung ist ein stabiles, gebrauchsfertiges Reagenz für den Bromelintest. Das Enzym Bromelin wird aus der
Elektronische Gebrauchsinformation siehe
 DE Anti-A 1 (Lektin) GEBRAUCHSINFORMATION Elektronische Gebrauchsinformation siehe www.bag-healthcare.com REF 6811 1 x 5 ml IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Anti A 1 (Lektin) ist ein aus Dolichos
DE Anti-A 1 (Lektin) GEBRAUCHSINFORMATION Elektronische Gebrauchsinformation siehe www.bag-healthcare.com REF 6811 1 x 5 ml IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Anti A 1 (Lektin) ist ein aus Dolichos
Anti-D Blend (IgM + IgG) monoklonal
 GEBRAUCHSINFORMATION Anti-D Blend (IgM + IgG) monoklonal 0123 IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Anti-D Blend (IgM + IgG) monoklonal besteht aus humanem monoklonalen Anti-D (IgM) (Klon D175-2)
GEBRAUCHSINFORMATION Anti-D Blend (IgM + IgG) monoklonal 0123 IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Anti-D Blend (IgM + IgG) monoklonal besteht aus humanem monoklonalen Anti-D (IgM) (Klon D175-2)
GEBRAUCHSINFORMATION IN VITRO DIAGNOSTIKA
 GEBRAUCHSINFORMATION Anti-Kp a Anti-Lu a Anti-S Anti-k (Cellano) Anti-Kp b Anti-Lu b Anti-s Anti-Wr a Anti-Fy a (Duffy a ) Anti-Jk a (Kidd a ) 0123 Anti-Fy b (Duffy b ) Anti-Jk b (Kidd b ) IN VITRO DIAGNOSTIKA
GEBRAUCHSINFORMATION Anti-Kp a Anti-Lu a Anti-S Anti-k (Cellano) Anti-Kp b Anti-Lu b Anti-s Anti-Wr a Anti-Fy a (Duffy a ) Anti-Jk a (Kidd a ) 0123 Anti-Fy b (Duffy b ) Anti-Jk b (Kidd b ) IN VITRO DIAGNOSTIKA
BAG-Elutions-Kit für die Säure-Elution von Antikörpern
 DE GEBRAUCHSINFORMATION BAG-Elutions-Kit für die Säure-Elution von Antikörpern IN VITRO DIAGNOSTIKUM REF 69501 1. Produktbeschreibung Mit dem BAG-Elutions-Kit können Antikörper, die sich in vivo oder in
DE GEBRAUCHSINFORMATION BAG-Elutions-Kit für die Säure-Elution von Antikörpern IN VITRO DIAGNOSTIKUM REF 69501 1. Produktbeschreibung Mit dem BAG-Elutions-Kit können Antikörper, die sich in vivo oder in
Anti-D Blend (IgM + IgG) monoklonal
 DE GEBRAUCHSINFORMATION Anti-D Blend (IgM + IgG) monoklonal 0123 REF 6785 REF 6786 1 x 10 ml 10 x 10 ml IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Anti-D Blend (IgM + IgG) monoklonal besteht aus humanem
DE GEBRAUCHSINFORMATION Anti-D Blend (IgM + IgG) monoklonal 0123 REF 6785 REF 6786 1 x 10 ml 10 x 10 ml IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Anti-D Blend (IgM + IgG) monoklonal besteht aus humanem
Simplex Easy DNA kit
 Simplex Easy DNA INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH Simplex Easy DNA kit Schnelle DNA-Extraktion aus Bakterien und Hefen Fast DNA-extraction from bacteria and yeast Art. Nr./ Order No.: SE 0100;
Simplex Easy DNA INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH Simplex Easy DNA kit Schnelle DNA-Extraktion aus Bakterien und Hefen Fast DNA-extraction from bacteria and yeast Art. Nr./ Order No.: SE 0100;
QuickGEN Sample Preparation Filtration
 QuickGEN Filtration INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH QuickGEN Sample Preparation Filtration Art. Nr./ Order No.: FSE 0100 Version 11/16 GEN-IAL GmbH Tel: 0049 2241 2522980 Fax: 0049 2241 2522989
QuickGEN Filtration INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH QuickGEN Sample Preparation Filtration Art. Nr./ Order No.: FSE 0100 Version 11/16 GEN-IAL GmbH Tel: 0049 2241 2522980 Fax: 0049 2241 2522989
Anti-D monoklonal (IgM) 0123
 GEBRAUCHSINFORMATION Anti-D monoklonal (IgM) 023 saline / human IN VITRO DIAGNOSTIKUM. Produktbeschreibung Anti-D monoklonal (IgM) wird aus monoklonalem, humanem Anti-D (IgM) (Klone: 597 Euclon und NaTH28-3c)
GEBRAUCHSINFORMATION Anti-D monoklonal (IgM) 023 saline / human IN VITRO DIAGNOSTIKUM. Produktbeschreibung Anti-D monoklonal (IgM) wird aus monoklonalem, humanem Anti-D (IgM) (Klone: 597 Euclon und NaTH28-3c)
Electrical tests on Bosch unit injectors
 Valid for Bosch unit injectors with order numbers 0 414 700 / 0 414 701 / 0 414 702 Parts Kit Magnet*: - F00H.N37.925 - F00H.N37.933 - F00H.N37.934 * For allocation to the 10-place Bosch order number,
Valid for Bosch unit injectors with order numbers 0 414 700 / 0 414 701 / 0 414 702 Parts Kit Magnet*: - F00H.N37.925 - F00H.N37.933 - F00H.N37.934 * For allocation to the 10-place Bosch order number,
Anti-Le a (Lewis a ) Anti-Le b (Lewis b )
 GEBRAUCHSINFORMATION Anti-Le a (Lewis a ) Anti-Le b (Lewis b ) monoklonal (IgM) IN VITRO DIAGNOSTIKA 1. Produktbeschreibung Anti-Le a (Klon LEA2) und Anti-Le b (Klon LEB2) werden aus monoklonalen Maus
GEBRAUCHSINFORMATION Anti-Le a (Lewis a ) Anti-Le b (Lewis b ) monoklonal (IgM) IN VITRO DIAGNOSTIKA 1. Produktbeschreibung Anti-Le a (Klon LEA2) und Anti-Le b (Klon LEB2) werden aus monoklonalen Maus
Chloroquin-Diphosphat für die Absprengung Erythrozyten-gebundener Antikörper
 GEBRAUCHSINFORMATION Chloroquin-Diphosphat für die Absprengung Erythrozyten-gebundener Antikörper IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Chloroquin-Diphosphat wird eingesetzt, um an Erythrozyten
GEBRAUCHSINFORMATION Chloroquin-Diphosphat für die Absprengung Erythrozyten-gebundener Antikörper IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Chloroquin-Diphosphat wird eingesetzt, um an Erythrozyten
Anti-A (AB01) Anti-B (AB02) Anti-A,B (AB01,2)
 GEBRAUCHSINFORMATION AntiA (AB01) AntiB (AB02) AntiA,B (AB01,2) monoklonal (IgM) 0123 Klone: AntiA: F98 7C6 AntiB: F84 3D6 ; F97 2D6 AntiA,B: F98 7C6 ; F84 3D6 ; F97 2D6 ; F125 7B6 IN VITRO DIAGNOSTIKA
GEBRAUCHSINFORMATION AntiA (AB01) AntiB (AB02) AntiA,B (AB01,2) monoklonal (IgM) 0123 Klone: AntiA: F98 7C6 AntiB: F84 3D6 ; F97 2D6 AntiA,B: F98 7C6 ; F84 3D6 ; F97 2D6 ; F125 7B6 IN VITRO DIAGNOSTIKA
RIDASCREEN Foodscreen Blood Collection Card Art. No.: A8025-BCC
 RIDASCREEN Foodscreen Blood Collection Card Art. No.: A8025-BCC Zubehör für RIDASCREEN Spec. IgG Foodscreen Accessory for RIDASCREEN Spec. IgG Foodscreen 1. filling in patient data Procedure: 2. filling
RIDASCREEN Foodscreen Blood Collection Card Art. No.: A8025-BCC Zubehör für RIDASCREEN Spec. IgG Foodscreen Accessory for RIDASCREEN Spec. IgG Foodscreen 1. filling in patient data Procedure: 2. filling
Cleaning & Disinfection of Eickview Videoendoscopes
 Cleaning & Disinfection of Eickview Videoendoscopes EICKEMEYER KG Eltastrasse 8 78532 Tuttlingen T +497461 96 580 0 F +497461 96 580 90 E info@eickemeyer.de www.eickemeyer.de Preparation Cleaning should
Cleaning & Disinfection of Eickview Videoendoscopes EICKEMEYER KG Eltastrasse 8 78532 Tuttlingen T +497461 96 580 0 F +497461 96 580 90 E info@eickemeyer.de www.eickemeyer.de Preparation Cleaning should
Anti-Jk a (Kidd a ), Anti-Jk b (Kidd b ) Anti-N, -S, -P 1 monoklonal (IgM) Anti-M monoklonal (IgG) GEBRAUCHSINFORMATION
 GEBRAUCHSINFORMATION Anti-Jk a (Kidd a ), Anti-Jk b (Kidd b ) 0123 Anti-N, -S, -P 1 monoklonal (IgM) Anti-M monoklonal (IgG) Klone: Anti-Jk a : MS15 Anti-Jk b : MS8 Anti-N : 1422 C 7 Anti-S: MS94 Anti-P
GEBRAUCHSINFORMATION Anti-Jk a (Kidd a ), Anti-Jk b (Kidd b ) 0123 Anti-N, -S, -P 1 monoklonal (IgM) Anti-M monoklonal (IgG) Klone: Anti-Jk a : MS15 Anti-Jk b : MS8 Anti-N : 1422 C 7 Anti-S: MS94 Anti-P
Testanleitung. Quantitative Bestimmung der Tumor M2-PK Stuhltest Instruction Manual. Quantitative Determination of the Tumor M2-PK Stool Test
 Testanleitung Quantitative Bestimmung der Tumor M2-PK Stuhltest Instruction Manual Quantitative Determination of the Tumor M2-PK Stool Test Tumor M2-PK ELISA Stuhltest/Stool Test REF Artikel-Nr./Catalog
Testanleitung Quantitative Bestimmung der Tumor M2-PK Stuhltest Instruction Manual Quantitative Determination of the Tumor M2-PK Stool Test Tumor M2-PK ELISA Stuhltest/Stool Test REF Artikel-Nr./Catalog
Word-CRM-Upload-Button. User manual
 Word-CRM-Upload-Button User manual Word-CRM-Upload for MS CRM 2011 Content 1. Preface... 3 2. Installation... 4 2.1. Requirements... 4 2.1.1. Clients... 4 2.2. Installation guidelines... 5 2.2.1. Client...
Word-CRM-Upload-Button User manual Word-CRM-Upload for MS CRM 2011 Content 1. Preface... 3 2. Installation... 4 2.1. Requirements... 4 2.1.1. Clients... 4 2.2. Installation guidelines... 5 2.2.1. Client...
Simplex Easy Wine Kit
 Simplex Easy Wine INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH Simplex Easy Wine Kit Schnelle DNA-Extraktion von Mikroorganismen aus Wein und Most Fast DNA-extraction from microorganisms in wine and grape
Simplex Easy Wine INSTITUT FÜR ANGEWANDTE LABORANALYSEN GMBH Simplex Easy Wine Kit Schnelle DNA-Extraktion von Mikroorganismen aus Wein und Most Fast DNA-extraction from microorganisms in wine and grape
CABLE TESTER. Manual DN-14003
 CABLE TESTER Manual DN-14003 Note: Please read and learn safety instructions before use or maintain the equipment This cable tester can t test any electrified product. 9V reduplicated battery is used in
CABLE TESTER Manual DN-14003 Note: Please read and learn safety instructions before use or maintain the equipment This cable tester can t test any electrified product. 9V reduplicated battery is used in
Anti-A (AB01) 0123 Anti-B (AB02) Anti-A,B (AB01,2)
 DE GEBRAUCHSINFORMATION AntiA (AB01) 0123 AntiB (AB02) AntiA,B (AB01,2) monoklonal (IgM) Klone: AntiA: F98 7C6 AntiB: F84 3D6 ; F97 2D6 AntiA,B: F98 7C6 ; F84 3D6 ; F97 2D6 ; F125 7B6 AntiA REF 6790 1
DE GEBRAUCHSINFORMATION AntiA (AB01) 0123 AntiB (AB02) AntiA,B (AB01,2) monoklonal (IgM) Klone: AntiA: F98 7C6 AntiB: F84 3D6 ; F97 2D6 AntiA,B: F98 7C6 ; F84 3D6 ; F97 2D6 ; F125 7B6 AntiA REF 6790 1
Electrical testing of Bosch common rail solenoid valve (MV) injectors
 Applies to MV injector, generation: -CRI 1.0 / 2.0 / 2.1 / 2.2 -CRIN 1 / 2 / 3, with K oder AK plug Bosch 10-position order number Bosch-Bestellnummer CRI: 0 445 110 xxx Bosch-Bestellnummer CRIN: 0 445
Applies to MV injector, generation: -CRI 1.0 / 2.0 / 2.1 / 2.2 -CRIN 1 / 2 / 3, with K oder AK plug Bosch 10-position order number Bosch-Bestellnummer CRI: 0 445 110 xxx Bosch-Bestellnummer CRIN: 0 445
Tube Analyzer LogViewer 2.3
 Tube Analyzer LogViewer 2.3 User Manual Stand: 25.9.2015 Seite 1 von 11 Name Company Date Designed by WKS 28.02.2013 1 st Checker 2 nd Checker Version history Version Author Changes Date 1.0 Created 19.06.2015
Tube Analyzer LogViewer 2.3 User Manual Stand: 25.9.2015 Seite 1 von 11 Name Company Date Designed by WKS 28.02.2013 1 st Checker 2 nd Checker Version history Version Author Changes Date 1.0 Created 19.06.2015
Evidence of Performance
 Air permeability, Watertightness, Resistance to wind load, Operating forces, Mechanical properties, Mechanical durability, Impact resistance Expert Statement No. 15-002226-PR01 (02) Product Designation
Air permeability, Watertightness, Resistance to wind load, Operating forces, Mechanical properties, Mechanical durability, Impact resistance Expert Statement No. 15-002226-PR01 (02) Product Designation
Anti-C, -c, -E, -e, -Kell monoklonal (IgM) 0123 Anti-C w monoklonal (IgM)
 GEBRAUCHSINFORMATION Anti-C, -c, -E, -e, -Kell monoklonal (IgM) 0 Anti-C w monoklonal (IgM) Klone: Anti-C: 24 273 Anti-C w : 1 Anti-c: 33 c1.16c.15a Anti-E: 2 E1.16C.F Anti-e: 62/69 16/21/63 Anti-Kell:
GEBRAUCHSINFORMATION Anti-C, -c, -E, -e, -Kell monoklonal (IgM) 0 Anti-C w monoklonal (IgM) Klone: Anti-C: 24 273 Anti-C w : 1 Anti-c: 33 c1.16c.15a Anti-E: 2 E1.16C.F Anti-e: 62/69 16/21/63 Anti-Kell:
Electrical testing of Bosch common rail piezo injectors
 Applies to generation CRI 3: Bosch 10-position order number 0 445 115 = CRI 3-16 (CRI 3.0) 1600 bar 0 445 116 = CRI 3-18 (CRI 3.2) 1800 bar 0 445 117 = CRI 3-20 (CRI 3.3) 2000 bar Tools required: Hybrid
Applies to generation CRI 3: Bosch 10-position order number 0 445 115 = CRI 3-16 (CRI 3.0) 1600 bar 0 445 116 = CRI 3-18 (CRI 3.2) 1800 bar 0 445 117 = CRI 3-20 (CRI 3.3) 2000 bar Tools required: Hybrid
VGM. VGM information. HAMBURG SÜD VGM WEB PORTAL USER GUIDE June 2016
 Overview The Hamburg Süd VGM Web portal is an application that enables you to submit VGM information directly to Hamburg Süd via our e-portal Web page. You can choose to enter VGM information directly,
Overview The Hamburg Süd VGM Web portal is an application that enables you to submit VGM information directly to Hamburg Süd via our e-portal Web page. You can choose to enter VGM information directly,
Guidelines on the Details of the Various Categories of Variations
 Guidelines on the Details of the Various Categories of Variations 31.03.2009 DI Susanne Stotter AGES PharmMed, Wien 2 Entstehung der Leitlinie BWP (2) QWP (3) IWP (1) CMD (2) EMEA (3) Guideline vom EMEA
Guidelines on the Details of the Various Categories of Variations 31.03.2009 DI Susanne Stotter AGES PharmMed, Wien 2 Entstehung der Leitlinie BWP (2) QWP (3) IWP (1) CMD (2) EMEA (3) Guideline vom EMEA
Snap-in switch for switches PSE, MSM and MCS 30
 Product manual Snap-in switch for switches PSE, MSM and MCS 30 CONTENTS 1. PRODUCT DESCRIPTION 2. DATA AND DIMENSIONAL DRAWINGS 2.1. Technical Data 2.2. Dimensions of PSE with a Mounting Diameter 19 mm
Product manual Snap-in switch for switches PSE, MSM and MCS 30 CONTENTS 1. PRODUCT DESCRIPTION 2. DATA AND DIMENSIONAL DRAWINGS 2.1. Technical Data 2.2. Dimensions of PSE with a Mounting Diameter 19 mm
BCA Protein Assay (Pierce)
 BCA Protein Assay (Pierce) BCA assay: geeignet für geringe Proteinmengen!!! Die Proteine bilden mit Cu2+-Ionen in alkalischer Lösung einen Komplex (Biuret-Reaktion). Die Cu2+-Ionen des Komplexes werden
BCA Protein Assay (Pierce) BCA assay: geeignet für geringe Proteinmengen!!! Die Proteine bilden mit Cu2+-Ionen in alkalischer Lösung einen Komplex (Biuret-Reaktion). Die Cu2+-Ionen des Komplexes werden
POST MARKET CLINICAL FOLLOW UP
 POST MARKET CLINICAL FOLLOW UP (MEDDEV 2.12-2 May 2004) Dr. med. Christian Schübel 2007/47/EG Änderungen Klin. Bewertung Historie: CETF Report (2000) Qualität der klinischen Daten zu schlecht Zu wenige
POST MARKET CLINICAL FOLLOW UP (MEDDEV 2.12-2 May 2004) Dr. med. Christian Schübel 2007/47/EG Änderungen Klin. Bewertung Historie: CETF Report (2000) Qualität der klinischen Daten zu schlecht Zu wenige
MyPaclitaxel Control Kit
 PTX- MyPaclitaxel Control Kit This package insert must be read carefully prior to product use. Package insert instructions must be followed accordingly. Reliability of assay results cannot be guaranteed
PTX- MyPaclitaxel Control Kit This package insert must be read carefully prior to product use. Package insert instructions must be followed accordingly. Reliability of assay results cannot be guaranteed
Electrical testing of Bosch common rail Injectors
 Electrical testing of Bosch common rail Injectors Contents: 1. Adapter cable for Hybridtester FSA 050 (article number 0 684 010 050 / 1 687 023 571) 2. Electrical testing of Bosch common rail solenoid
Electrical testing of Bosch common rail Injectors Contents: 1. Adapter cable for Hybridtester FSA 050 (article number 0 684 010 050 / 1 687 023 571) 2. Electrical testing of Bosch common rail solenoid
VGM. VGM information. HAMBURG SÜD VGM WEB PORTAL - USER GUIDE June 2016
 Overview The Hamburg Süd VGM-Portal is an application which enables to submit VGM information directly to Hamburg Süd via our e-portal web page. You can choose to insert VGM information directly, or download
Overview The Hamburg Süd VGM-Portal is an application which enables to submit VGM information directly to Hamburg Süd via our e-portal web page. You can choose to insert VGM information directly, or download
LOC Pharma. Anlage. Lieferantenfragebogen Supplier Questionnaire. 9. Is the warehouse temperature controlled or air-conditioned?
 Please complete this questionnaire and return to: z.h. Leiter Qualitätsmanagement info@loc-pharma.de Name and position of person completing the questionnaire Signature Date 1. Name of Company 2. Address
Please complete this questionnaire and return to: z.h. Leiter Qualitätsmanagement info@loc-pharma.de Name and position of person completing the questionnaire Signature Date 1. Name of Company 2. Address
Outdoor-Tasche. Operating Instructions Bedienungsanleitung GB D
 00 181243 Outdoor Case Outdoor-Tasche Splish Splash Operating Instructions Bedienungsanleitung GB D A B C D OPEN G Operating instruction 1. Important Notes Children are not permitted to play with the device.
00 181243 Outdoor Case Outdoor-Tasche Splish Splash Operating Instructions Bedienungsanleitung GB D A B C D OPEN G Operating instruction 1. Important Notes Children are not permitted to play with the device.
Benannte Stelle nach Richtlinie 98/79/EG Notified Body according to Directive 98/79/EC
 Benannte Stelle nach Richtlinie 98/79/EG Notified Body according to Directive 98/79/EC mdc medical device certification GmbH Kriegerstr. 6 D 70191 Stuttgart Telefon Phone Telefax Fax E-Mail E-mail Website
Benannte Stelle nach Richtlinie 98/79/EG Notified Body according to Directive 98/79/EC mdc medical device certification GmbH Kriegerstr. 6 D 70191 Stuttgart Telefon Phone Telefax Fax E-Mail E-mail Website
QS Laborkompetenztest Frühjahr 2011
 Qualitätssicherung. Vom Erzeuger bis zur Ladentheke. QS Laborkompetenztest Frühjahr 2011 Bewertungsschema Laborkompetenztest Frühjahr 2011 Bestanden alle 6 Wirkstoffe identifiziert und mindestens 4 Wirkstoffe
Qualitätssicherung. Vom Erzeuger bis zur Ladentheke. QS Laborkompetenztest Frühjahr 2011 Bewertungsschema Laborkompetenztest Frühjahr 2011 Bestanden alle 6 Wirkstoffe identifiziert und mindestens 4 Wirkstoffe
Guidance Notes for the eservice 'Marketing Authorisation & Lifecycle Management of Medicines' Contents
 Guidance Notes for the eservice 'Marketing Authorisation & Lifecycle Management of Medicines' Contents Login... 2 No active procedure at the moment... 3 'Active' procedure... 4 New communication (procedure
Guidance Notes for the eservice 'Marketing Authorisation & Lifecycle Management of Medicines' Contents Login... 2 No active procedure at the moment... 3 'Active' procedure... 4 New communication (procedure
Safety action Inspection of welds
 Knott GmbH Obinger Straße 15 D 83125 Eggstätt Receiver final custormer Ihre Nachricht Your letter Ihr Zeichen Your references Datum Date Abteilung Department Bearbeitet durch Contact person Unser Zeichen
Knott GmbH Obinger Straße 15 D 83125 Eggstätt Receiver final custormer Ihre Nachricht Your letter Ihr Zeichen Your references Datum Date Abteilung Department Bearbeitet durch Contact person Unser Zeichen
PeliCase 1 Best.-Nr
 PeliCase 1 Best.-Nr. 546009 Charge: 8000233305 Verfallsdatum: 2016-12-13 Name: Krankenhaus: Unterschrift: Station: Fall: Frau Claasen (63 Jahre alt) wurde in die chirurgische Abteilung Ihres Krankenhauses
PeliCase 1 Best.-Nr. 546009 Charge: 8000233305 Verfallsdatum: 2016-12-13 Name: Krankenhaus: Unterschrift: Station: Fall: Frau Claasen (63 Jahre alt) wurde in die chirurgische Abteilung Ihres Krankenhauses
Wissen schafft Fortschritt
 Wissen schafft Fortschritt» Thermal analysis of six heat-reflective exterior paints on concrete under irradiation 20130730 Dr. Julius Nickl Geschäftsführer Senior-Experte für industrielle Prozesse und
Wissen schafft Fortschritt» Thermal analysis of six heat-reflective exterior paints on concrete under irradiation 20130730 Dr. Julius Nickl Geschäftsführer Senior-Experte für industrielle Prozesse und
Ex-Barriere für Diagnoseeinheit SITRANS DA400 / Ex-barrier for diagnostics unit SITRANS DA400 7MJ2010-1AA 0032
 Ex-Barriere für Diagnoseeinheit SITRANS DA400 / Ex-barrier for diagnostics unit SITRANS DA400 7MJ2010-1AA 0032 Warnung Elektrischer Anschluss in explosionsgefährdeten Bereichen Anschluss und Inbetriebnahme
Ex-Barriere für Diagnoseeinheit SITRANS DA400 / Ex-barrier for diagnostics unit SITRANS DA400 7MJ2010-1AA 0032 Warnung Elektrischer Anschluss in explosionsgefährdeten Bereichen Anschluss und Inbetriebnahme
Lukas Hydraulik GmbH Weinstraße 39 D Erlangen. Mr. Sauerbier. Lukas Hydraulik GmbH Weinstraße 39 D Erlangen
 Technical Report No. 028-71 30 95685-350 of 22.02.2017 Client: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen Mr. Sauerbier Manufacturing location: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen
Technical Report No. 028-71 30 95685-350 of 22.02.2017 Client: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen Mr. Sauerbier Manufacturing location: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen
Rev. Proc Information
 Rev. Proc. 2006-32 Information 2006, CPAs 1 Table 1-Total loss of the home Table 2- Near total loss is water to the roofline. Completely gut the home from floor to rafters - wiring, plumbing, electrical
Rev. Proc. 2006-32 Information 2006, CPAs 1 Table 1-Total loss of the home Table 2- Near total loss is water to the roofline. Completely gut the home from floor to rafters - wiring, plumbing, electrical
1. General information... 2 2. Login... 2 3. Home... 3 4. Current applications... 3
 User Manual for Marketing Authorisation and Lifecycle Management of Medicines Inhalt: User Manual for Marketing Authorisation and Lifecycle Management of Medicines... 1 1. General information... 2 2. Login...
User Manual for Marketing Authorisation and Lifecycle Management of Medicines Inhalt: User Manual for Marketing Authorisation and Lifecycle Management of Medicines... 1 1. General information... 2 2. Login...
Das ABO System. Praktikum für Medizinstudenten im IV Jahrgang. Zsuzsa Faust MD, PhD Zita Csernus MD
 Das ABO System Praktikum für Medizinstudenten im IV Jahrgang Zsuzsa Faust MD, PhD Zita Csernus MD Regionale Bluttransfusionszentrale von Pécs Nationaler Bluttransfusionsdienst faust.zsuzsanna@ovsz.hu Blutgruppensysteme
Das ABO System Praktikum für Medizinstudenten im IV Jahrgang Zsuzsa Faust MD, PhD Zita Csernus MD Regionale Bluttransfusionszentrale von Pécs Nationaler Bluttransfusionsdienst faust.zsuzsanna@ovsz.hu Blutgruppensysteme
Hazards and measures against hazards by implementation of safe pneumatic circuits
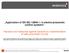 Application of EN ISO 13849-1 in electro-pneumatic control systems Hazards and measures against hazards by implementation of safe pneumatic circuits These examples of switching circuits are offered free
Application of EN ISO 13849-1 in electro-pneumatic control systems Hazards and measures against hazards by implementation of safe pneumatic circuits These examples of switching circuits are offered free
Test Report. Test of resitance to inertia effects of Zirkona Backwall. Sled Test (Frontal Impact) 20 g / 30 ms
 Test Report Test of resitance to inertia effects of Zirkona Backwall Sled Test (Frontal Impact) 20 g / 30 ms This report serves solely as a documentation of test results. 93XS0002-00_TdC.doc Page 1 1.
Test Report Test of resitance to inertia effects of Zirkona Backwall Sled Test (Frontal Impact) 20 g / 30 ms This report serves solely as a documentation of test results. 93XS0002-00_TdC.doc Page 1 1.
ScanGel COOMBS Anti-IgG,-C 3 d 86431 48 Karten 86432 1080 Karten
 ScanGel COOMBS Anti-IgG,-C 3 d 86431 48 Karten 86432 1080 Karten MIT EINEM POLYSPEZIFISCHEN ANTI-HUMAN-GLOBULIN FORMULIERTES GEL (POLYKLONALE UND MONOKLONALE MAUS-FRAKTIONEN) Ak Suchtest, Verträglichkeitsprobe,
ScanGel COOMBS Anti-IgG,-C 3 d 86431 48 Karten 86432 1080 Karten MIT EINEM POLYSPEZIFISCHEN ANTI-HUMAN-GLOBULIN FORMULIERTES GEL (POLYKLONALE UND MONOKLONALE MAUS-FRAKTIONEN) Ak Suchtest, Verträglichkeitsprobe,
Magic Figures. We note that in the example magic square the numbers 1 9 are used. All three rows (columns) have equal sum, called the magic number.
 Magic Figures Introduction: This lesson builds on ideas from Magic Squares. Students are introduced to a wider collection of Magic Figures and consider constraints on the Magic Number associated with such
Magic Figures Introduction: This lesson builds on ideas from Magic Squares. Students are introduced to a wider collection of Magic Figures and consider constraints on the Magic Number associated with such
DENTAL IMPLANTS BY CAMLOG medical
 IMPLANT PASS DENTAL IMPLANTS BY CAMLOG medical devices made in germany for your well-being and a natural appearance. Personal data Surname First name Address ZIP code City Date of birth Health insurance
IMPLANT PASS DENTAL IMPLANTS BY CAMLOG medical devices made in germany for your well-being and a natural appearance. Personal data Surname First name Address ZIP code City Date of birth Health insurance
OncoBEAM Anleitung zur Probenentnahme und Versand
 OncoBEAM Anleitung zur Probenentnahme und Versand Go Beyond Biopsy with Blood www.sysmex-inostics.com Deutsch Anleitung zur Probenentnahme und Versand Anleitung zur Blutentnahme 1. Beschriftung des Entnahmeröhrchens
OncoBEAM Anleitung zur Probenentnahme und Versand Go Beyond Biopsy with Blood www.sysmex-inostics.com Deutsch Anleitung zur Probenentnahme und Versand Anleitung zur Blutentnahme 1. Beschriftung des Entnahmeröhrchens
Brand Label. Daimler Brand & Design Navigator
 Daimler Brand & Design Navigator 30. März 2016 Brand Label FUSO Financial uses the FUSO letters in combination with the word Financial in the font Daimler CS for name and label. Black lettering is set
Daimler Brand & Design Navigator 30. März 2016 Brand Label FUSO Financial uses the FUSO letters in combination with the word Financial in the font Daimler CS for name and label. Black lettering is set
Bayerisches Landesamt für Gesundheit und Lebensmittelsicherheit Pool water quality the German philosophy
 Bayerisches Landesamt für Gesundheit und Lebensmittelsicherheit Pool water quality the German philosophy Christiane Höller Bavarian Health and Food Safety Authority Legal regulations 1979 Federal Law on
Bayerisches Landesamt für Gesundheit und Lebensmittelsicherheit Pool water quality the German philosophy Christiane Höller Bavarian Health and Food Safety Authority Legal regulations 1979 Federal Law on
Lukas Hydraulik GmbH Weinstraße 39 D Erlangen. Mr. Sauerbier. Lukas Hydraulik GmbH Weinstraße 39 D Erlangen. edraulic rescue equipment
 Technical Report No. 028-7130 95685-050 of 22.02.2017 Client: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen Mr. Sauerbier Manufacturing location: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen
Technical Report No. 028-7130 95685-050 of 22.02.2017 Client: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen Mr. Sauerbier Manufacturing location: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen
Mock Exam Behavioral Finance
 Mock Exam Behavioral Finance For the following 4 questions you have 60 minutes. You may receive up to 60 points, i.e. on average you should spend about 1 minute per point. Please note: You may use a pocket
Mock Exam Behavioral Finance For the following 4 questions you have 60 minutes. You may receive up to 60 points, i.e. on average you should spend about 1 minute per point. Please note: You may use a pocket
Benannte Stelle nach Richtlinie 98/79/EG Notified Body according to Directive 98/79/EC
 Benannte Stelle nach Richtlinie 98/79/EG Notified Body according to Directive 98/79/EC Ridlerstraße 65 D 80339 München Telefon Phone Telefax Fax E-Mail E-mail Website Website Kennnummer Identification
Benannte Stelle nach Richtlinie 98/79/EG Notified Body according to Directive 98/79/EC Ridlerstraße 65 D 80339 München Telefon Phone Telefax Fax E-Mail E-mail Website Website Kennnummer Identification
Konfiguration von eduroam. Configuring eduroam
 eduroam Windows 8.1 / 10 Konfiguration von eduroam Configuring eduroam 08.10.2018 kim.uni-hohenheim.de kim@uni-hohenheim.de Wissenschaftliche Einrichtungen und Universitäten bieten einen weltweiten Internetzugang
eduroam Windows 8.1 / 10 Konfiguration von eduroam Configuring eduroam 08.10.2018 kim.uni-hohenheim.de kim@uni-hohenheim.de Wissenschaftliche Einrichtungen und Universitäten bieten einen weltweiten Internetzugang
prorm Budget Planning promx GmbH Nordring Nuremberg
 prorm Budget Planning Budget Planning Business promx GmbH Nordring 100 909 Nuremberg E-Mail: support@promx.net Content WHAT IS THE prorm BUDGET PLANNING? prorm Budget Planning Overview THE ADVANTAGES OF
prorm Budget Planning Budget Planning Business promx GmbH Nordring 100 909 Nuremberg E-Mail: support@promx.net Content WHAT IS THE prorm BUDGET PLANNING? prorm Budget Planning Overview THE ADVANTAGES OF
Bedienungsanleitung SUNNYHEAT Standfuß (Art. Nr )
 Bedienungsanleitung SUNNYHEAT Standfuß (Art. Nr. 221012) Der SUNNYHEAT Standfuß ist zur Positionierung Ihres Heizpaneels auf dem Standfuß gedacht. Anwendung findet der Standfuß bei allen Paneelen außer
Bedienungsanleitung SUNNYHEAT Standfuß (Art. Nr. 221012) Der SUNNYHEAT Standfuß ist zur Positionierung Ihres Heizpaneels auf dem Standfuß gedacht. Anwendung findet der Standfuß bei allen Paneelen außer
p^db=`oj===pìééçêíáåñçêã~íáçå=
 p^db=`oj===pìééçêíáåñçêã~íáçå= Error: "Could not connect to the SQL Server Instance" or "Failed to open a connection to the database." When you attempt to launch ACT! by Sage or ACT by Sage Premium for
p^db=`oj===pìééçêíáåñçêã~íáçå= Error: "Could not connect to the SQL Server Instance" or "Failed to open a connection to the database." When you attempt to launch ACT! by Sage or ACT by Sage Premium for
ATEX-Check list. Compiled by: Date: Signature: Acceptable practice at the determination of flash point: Closed cup according to ISO 2719
 Fire and explosion hazard ATEX 137 1999/92/EG und ATEX 95 2014/34/EU Danger assessment and determination of explosion protection zone for the test space as well as the installation site ATEX-Check list
Fire and explosion hazard ATEX 137 1999/92/EG und ATEX 95 2014/34/EU Danger assessment and determination of explosion protection zone for the test space as well as the installation site ATEX-Check list
FEM Isoparametric Concept
 FEM Isoparametric Concept home/lehre/vl-mhs--e/folien/vorlesung/4_fem_isopara/cover_sheet.tex page of 25. p./25 Table of contents. Interpolation Functions for the Finite Elements 2. Finite Element Types
FEM Isoparametric Concept home/lehre/vl-mhs--e/folien/vorlesung/4_fem_isopara/cover_sheet.tex page of 25. p./25 Table of contents. Interpolation Functions for the Finite Elements 2. Finite Element Types
RIDA QUICK Soya accessory pack Art. No. Z7103
 RIDA QUICK Soya accessory pack Art. No. Z7103 Zubehör für die Verwendung mit RIDA QUICK Soya (Art. Nr. R7103) Accessories for the use of the RIDA QUICK Soya (Art. No. R7103) In vitro Test Lagerung bei
RIDA QUICK Soya accessory pack Art. No. Z7103 Zubehör für die Verwendung mit RIDA QUICK Soya (Art. Nr. R7103) Accessories for the use of the RIDA QUICK Soya (Art. No. R7103) In vitro Test Lagerung bei
Parameter-Updatesoftware PF-12 Plus
 Parameter-Updatesoftware PF-12 Plus Mai / May 2015 Inhalt 1. Durchführung des Parameter-Updates... 2 2. Kontakt... 6 Content 1. Performance of the parameter-update... 4 2. Contact... 6 1. Durchführung
Parameter-Updatesoftware PF-12 Plus Mai / May 2015 Inhalt 1. Durchführung des Parameter-Updates... 2 2. Kontakt... 6 Content 1. Performance of the parameter-update... 4 2. Contact... 6 1. Durchführung
Normenausschüsse in der Labormedizin
 Normenausschüsse in der Labormedizin - Überblick - Historie - Konsequenzen - Aktivitäten - Vorteile/Nachteile 9/19/2007 1 Internationale Organisationen im IVD/MD Bereich GHTF (Global Harmonization Task
Normenausschüsse in der Labormedizin - Überblick - Historie - Konsequenzen - Aktivitäten - Vorteile/Nachteile 9/19/2007 1 Internationale Organisationen im IVD/MD Bereich GHTF (Global Harmonization Task
ScanGel ScanBrom ml
 ScanGel ScanBrom 86445 12 ml BROMELAIN FÜR KOMPATIBILITÄTSTEST IVD Alle von der Firma Bio-Rad hergestellten und verkauften Produkte unterliegen einem Qualitätssicherungssystem vom Rohstoffeingang bis zur
ScanGel ScanBrom 86445 12 ml BROMELAIN FÜR KOMPATIBILITÄTSTEST IVD Alle von der Firma Bio-Rad hergestellten und verkauften Produkte unterliegen einem Qualitätssicherungssystem vom Rohstoffeingang bis zur
SAMPLE EXAMINATION BOOKLET
 S SAMPLE EXAMINATION BOOKLET New Zealand Scholarship German Time allowed: Three hours Total marks: 24 EXAMINATION BOOKLET Question ONE TWO Mark There are three questions. You should answer Question One
S SAMPLE EXAMINATION BOOKLET New Zealand Scholarship German Time allowed: Three hours Total marks: 24 EXAMINATION BOOKLET Question ONE TWO Mark There are three questions. You should answer Question One
Test Report No
 TFI Charlottenburger Allee 41 52068 Aachen Germany Charlottenburger Allee 41 52068 Aachen Germany Egetaepper A/S Postafch 1 90 7400 Herning DÄNEMARK Fon +49.241.9679 00 Fax +49.241.9679 200 postmaster@tfi-online.de
TFI Charlottenburger Allee 41 52068 Aachen Germany Charlottenburger Allee 41 52068 Aachen Germany Egetaepper A/S Postafch 1 90 7400 Herning DÄNEMARK Fon +49.241.9679 00 Fax +49.241.9679 200 postmaster@tfi-online.de
rot red braun brown rot red RS-8 rot red braun brown R S V~
 Kleiner Ring 9 /Germany Phone: 0049 4122 / 977 381 Fax: 0049 4122 / 977 382 Sample connections: Feedback module with integrated detection of occupied tracks for the RS-feedback bus (Lenz Digital plus)
Kleiner Ring 9 /Germany Phone: 0049 4122 / 977 381 Fax: 0049 4122 / 977 382 Sample connections: Feedback module with integrated detection of occupied tracks for the RS-feedback bus (Lenz Digital plus)
Level 2 German, 2013
 91126 911260 2SUPERVISOR S Level 2 German, 2013 91126 Demonstrate understanding of a variety of written and / or visual German text(s) on familiar matters 9.30 am Monday 11 November 2013 Credits: Five
91126 911260 2SUPERVISOR S Level 2 German, 2013 91126 Demonstrate understanding of a variety of written and / or visual German text(s) on familiar matters 9.30 am Monday 11 November 2013 Credits: Five
RhD-Bestimmung. Bedside-Test Antikörpersuchtest Dr. Vera Pászthy
 RhD-Bestimmung Bedside-Test Antikörpersuchtest 2013. 11. 18. Dr. Vera Pászthy Nationaler Bluttransfusionsdienst Regionale Bluttransfusionszentrale Pécs natürlich vorkommende Antikörper (REGULÄRE) A - anti-b
RhD-Bestimmung Bedside-Test Antikörpersuchtest 2013. 11. 18. Dr. Vera Pászthy Nationaler Bluttransfusionsdienst Regionale Bluttransfusionszentrale Pécs natürlich vorkommende Antikörper (REGULÄRE) A - anti-b
NEWSLETTER. FileDirector Version 2.5 Novelties. Filing system designer. Filing system in WinClient
 Filing system designer FileDirector Version 2.5 Novelties FileDirector offers an easy way to design the filing system in WinClient. The filing system provides an Explorer-like structure in WinClient. The
Filing system designer FileDirector Version 2.5 Novelties FileDirector offers an easy way to design the filing system in WinClient. The filing system provides an Explorer-like structure in WinClient. The
Blutgruppen. Dr. Gerhard Mehrke 2009/10 1
 Blutgruppen Dr. Gerhard Mehrke 2009/10 1 Transfusion Mischung blutgruppenungleicher Blutsorten führt zur Agglutination der Erythrozyten 70% der Fälle Agglutination / Hämolyse Dr. Gerhard Mehrke 2009/10
Blutgruppen Dr. Gerhard Mehrke 2009/10 1 Transfusion Mischung blutgruppenungleicher Blutsorten führt zur Agglutination der Erythrozyten 70% der Fälle Agglutination / Hämolyse Dr. Gerhard Mehrke 2009/10
Efficacy of Biocides against Gram-negative Bacteria. Dr. Peter Goroncy-Bermes R & D Department
 against Gram-negative Bacteria Dr. Peter Goroncy-Bermes R & D Department Three important groups of weapons can be used to fight infectious agents Antibiotics Antimycotics Biocides 30.11.2015 Titel der
against Gram-negative Bacteria Dr. Peter Goroncy-Bermes R & D Department Three important groups of weapons can be used to fight infectious agents Antibiotics Antimycotics Biocides 30.11.2015 Titel der
Level 1 German, 2014
 90886 908860 1SUPERVISOR S Level 1 German, 2014 90886 Demonstrate understanding of a variety of German texts on areas of most immediate relevance 9.30 am Wednesday 26 November 2014 Credits: Five Achievement
90886 908860 1SUPERVISOR S Level 1 German, 2014 90886 Demonstrate understanding of a variety of German texts on areas of most immediate relevance 9.30 am Wednesday 26 November 2014 Credits: Five Achievement
New Forms of Risk Communication Workshop 6: Arzneimitteltherapiesicherheit (AMTS) Dr. Norbert Paeschke, BfArM
 New Forms of Risk Communication Workshop 6: Arzneimitteltherapiesicherheit (AMTS) Dr. Norbert Paeschke, BfArM Bundesinstitut für Arzneimittel und Medizinprodukte Das BfArM ist ein Bundesinstitut im Geschäftsbereich
New Forms of Risk Communication Workshop 6: Arzneimitteltherapiesicherheit (AMTS) Dr. Norbert Paeschke, BfArM Bundesinstitut für Arzneimittel und Medizinprodukte Das BfArM ist ein Bundesinstitut im Geschäftsbereich
CHARACTERIAZTION OF PREEXISTING ANTIBODIES TO S-303 PATHOGEN INACTIVATED RED BLOOD CELLS (S-303 RBC) SCREENING OF IN 10.
 CHARACTERIAZTION OF PREEXISTING ANTIBODIES TO S-303 PATHOGEN INACTIVATED RED BLOOD CELLS (S-303 RBC) SCREENING OF IN 10.721 PATIENT SERA Geisen C, Brixner V, Stempniewski L, North A, Kiessling A.-H, Müller
CHARACTERIAZTION OF PREEXISTING ANTIBODIES TO S-303 PATHOGEN INACTIVATED RED BLOOD CELLS (S-303 RBC) SCREENING OF IN 10.721 PATIENT SERA Geisen C, Brixner V, Stempniewski L, North A, Kiessling A.-H, Müller
Registration of residence at Citizens Office (Bürgerbüro)
 Registration of residence at Citizens Office (Bürgerbüro) Opening times in the Citizens Office (Bürgerbüro): Monday to Friday 08.30 am 12.30 pm Thursday 14.00 pm 17.00 pm or by appointment via the Citizens
Registration of residence at Citizens Office (Bürgerbüro) Opening times in the Citizens Office (Bürgerbüro): Monday to Friday 08.30 am 12.30 pm Thursday 14.00 pm 17.00 pm or by appointment via the Citizens
MILLING UNIT 5X. Anleitung zur Durchführung der Autokalibrierung. Instructions for use Instructions for autocalibration. DE Gebrauchsanweisung 2-4
 MILLING UNIT 5X DE Gebrauchsanweisung 2-4 Anleitung zur Durchführung der Autokalibrierung EN Instructions for use 5-7 Instructions for use Instructions for autocalibration ANLEITUNG ZUR DURCHFÜHRUNG DER
MILLING UNIT 5X DE Gebrauchsanweisung 2-4 Anleitung zur Durchführung der Autokalibrierung EN Instructions for use 5-7 Instructions for use Instructions for autocalibration ANLEITUNG ZUR DURCHFÜHRUNG DER
Praktikum Transfusionsmedizin
 Praktikum Transfusionsmedizin Humanmedizin 1. klinisches Jahr ÜBUNGEN: 1. Blutgruppenbestimmung AB0-System Die Blutgruppenbestimmung im AB0-System erfolgt: 1. durch Bestimmung der AB0-Antigene (Erythrozyteneigenschaften)
Praktikum Transfusionsmedizin Humanmedizin 1. klinisches Jahr ÜBUNGEN: 1. Blutgruppenbestimmung AB0-System Die Blutgruppenbestimmung im AB0-System erfolgt: 1. durch Bestimmung der AB0-Antigene (Erythrozyteneigenschaften)
Taxation in Austria - Keypoints. CONFIDA Klagenfurt Steuerberatungsgesellschaft m.b.h
 Taxation in Austria - Keypoints 1 CONFIDA TAX AUDIT CONSULTING Our history: Founded in 1977 Currently about 200 employees Member of International Association of independent accounting firms since1994 Our
Taxation in Austria - Keypoints 1 CONFIDA TAX AUDIT CONSULTING Our history: Founded in 1977 Currently about 200 employees Member of International Association of independent accounting firms since1994 Our
Wissenschaftliche Dienste. Sachstand. Payment of value added tax (VAT) (EZPWD-Anfrage ) 2016 Deutscher Bundestag WD /16
 Payment of value added tax (VAT) (EZPWD-Anfrage ) 2016 Deutscher Bundestag Seite 2 Payment of value added tax (VAT) (EZPWD-Anfrage ) Aktenzeichen: Abschluss der Arbeit: 07.04.2016 Fachbereich: WD 4: Haushalt
Payment of value added tax (VAT) (EZPWD-Anfrage ) 2016 Deutscher Bundestag Seite 2 Payment of value added tax (VAT) (EZPWD-Anfrage ) Aktenzeichen: Abschluss der Arbeit: 07.04.2016 Fachbereich: WD 4: Haushalt
Newest Generation of the BS2 Corrosion/Warning and Measurement System
 Newest Generation of the BS2 Corrosion/Warning and Measurement System BS2 System Description: BS2 CorroDec 2G is a cable and energyless system module range for detecting corrosion, humidity and prevailing
Newest Generation of the BS2 Corrosion/Warning and Measurement System BS2 System Description: BS2 CorroDec 2G is a cable and energyless system module range for detecting corrosion, humidity and prevailing
Can I use an older device with a new GSD file? It is always the best to use the latest GSD file since this is downward compatible to older versions.
 EUCHNER GmbH + Co. KG Postfach 10 01 52 D-70745 Leinfelden-Echterdingen MGB PROFINET You will require the corresponding GSD file in GSDML format in order to integrate the MGB system: GSDML-Vx.x-EUCHNER-MGB_xxxxxx-YYYYMMDD.xml
EUCHNER GmbH + Co. KG Postfach 10 01 52 D-70745 Leinfelden-Echterdingen MGB PROFINET You will require the corresponding GSD file in GSDML format in order to integrate the MGB system: GSDML-Vx.x-EUCHNER-MGB_xxxxxx-YYYYMMDD.xml
Johannes Bachmann, Silvia Keilholz
 Johannes Bachmann, Silvia Keilholz Spring mortality *common carps die with few or without any pathological signs *average body condition *no death causing organisms/ explanations *First detection of CEV
Johannes Bachmann, Silvia Keilholz Spring mortality *common carps die with few or without any pathological signs *average body condition *no death causing organisms/ explanations *First detection of CEV
Franke & Bornberg award AachenMünchener private annuity insurance schemes top grades
 Franke & Bornberg award private annuity insurance schemes top grades Press Release, December 22, 2009 WUNSCHPOLICE STRATEGIE No. 1 gets best possible grade FFF ( Excellent ) WUNSCHPOLICE conventional annuity
Franke & Bornberg award private annuity insurance schemes top grades Press Release, December 22, 2009 WUNSCHPOLICE STRATEGIE No. 1 gets best possible grade FFF ( Excellent ) WUNSCHPOLICE conventional annuity
Mitglied der Leibniz-Gemeinschaft
 Methods of research into dictionary use: online questionnaires Annette Klosa (Institut für Deutsche Sprache, Mannheim) 5. Arbeitstreffen Netzwerk Internetlexikografie, Leiden, 25./26. März 2013 Content
Methods of research into dictionary use: online questionnaires Annette Klosa (Institut für Deutsche Sprache, Mannheim) 5. Arbeitstreffen Netzwerk Internetlexikografie, Leiden, 25./26. März 2013 Content
* * * IMPORTANT * * IMPORTANT * * IMPORTANT * * * Read these instructions carefully before using this product and save them for future use.
 Change bag Instructions [UK] * * * IMPORTANT * * IMPORTANT * * IMPORTANT * * * Read these instructions carefully before using this product and save them for future use. Your child may be injured if you
Change bag Instructions [UK] * * * IMPORTANT * * IMPORTANT * * IMPORTANT * * * Read these instructions carefully before using this product and save them for future use. Your child may be injured if you
USBASIC SAFETY IN NUMBERS
 USBASIC SAFETY IN NUMBERS #1.Current Normalisation Ropes Courses and Ropes Course Elements can conform to one or more of the following European Norms: -EN 362 Carabiner Norm -EN 795B Connector Norm -EN
USBASIC SAFETY IN NUMBERS #1.Current Normalisation Ropes Courses and Ropes Course Elements can conform to one or more of the following European Norms: -EN 362 Carabiner Norm -EN 795B Connector Norm -EN
STRATEGISCHES BETEILIGUNGSCONTROLLING BEI KOMMUNALEN UNTERNEHMEN DER FFENTLICHE ZWECK ALS RICHTSCHNUR FR EIN ZIELGERICHTETE
 BETEILIGUNGSCONTROLLING BEI KOMMUNALEN UNTERNEHMEN DER FFENTLICHE ZWECK ALS RICHTSCHNUR FR EIN ZIELGERICHTETE PDF-SBBKUDFZARFEZ41-APOM3 123 Page File Size 5,348 KB 3 Feb, 2002 TABLE OF CONTENT Introduction
BETEILIGUNGSCONTROLLING BEI KOMMUNALEN UNTERNEHMEN DER FFENTLICHE ZWECK ALS RICHTSCHNUR FR EIN ZIELGERICHTETE PDF-SBBKUDFZARFEZ41-APOM3 123 Page File Size 5,348 KB 3 Feb, 2002 TABLE OF CONTENT Introduction
Big Data Analytics. Fifth Munich Data Protection Day, March 23, Dr. Stefan Krätschmer, Data Privacy Officer, Europe, IBM
 Big Data Analytics Fifth Munich Data Protection Day, March 23, 2017 C Dr. Stefan Krätschmer, Data Privacy Officer, Europe, IBM Big Data Use Cases Customer focused - Targeted advertising / banners - Analysis
Big Data Analytics Fifth Munich Data Protection Day, March 23, 2017 C Dr. Stefan Krätschmer, Data Privacy Officer, Europe, IBM Big Data Use Cases Customer focused - Targeted advertising / banners - Analysis
s 120; s 311; s 312; s 330; s 510; s 511; s 530; s 700
 Technical Report No. 028-7130 95685-250 of 02.12.2016 Client: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen Mr. Sauerbier Manufacturing location: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen
Technical Report No. 028-7130 95685-250 of 02.12.2016 Client: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen Mr. Sauerbier Manufacturing location: Lukas Hydraulik GmbH Weinstraße 39 D-91058 Erlangen
