Die alkalische Brennstoffzelle (AFC)
|
|
|
- Joachim Tobias Holst
- vor 7 Jahren
- Abrufe
Transkript
1 Die alkalische Brennstoffzelle (AFC) von Mathis Fomferra Fachoberschule Winsen/Luhe Mai 2010
2 Index Vorwort Wieso die Brennstoffzelle Die Geschichte der Brennstoffzelle Die alkalische Brennstoffzelle Quellenangaben Vorwort In Zeiten steigender Energiekosten liegt es nahe alternative Energiequellen wie z.b. die Brennstoffzelle im Alltag einzusetzen. Die AFC Brennstoffzelle wird schon seit vielen Jahren in Raumfähren und seit einigen Jahren auch in U-Booten eingesetzt. Wieso die Brennstoffzelle und nicht der Verbrennungsmotor? Da die Energieresourcen immer geringer werden, liegt es nahe erneuerbare Energien einzusetzen, sei es in der Automobilbranche oder in anderen Gebieten. Also stellt sich die Frage, wieso sollte man nicht die Brennstoffzelle statt des Verbrennungsmotors einsetzen. Der Verbrennungsmotor ist eigentlich eine überholte Technik, er hat zwar den Vorteil, dass er seit Jahrzehnten zuverlässig funktioniert und ausreichend Energie zur Verfügung stellt aber er hat einen sehr geringen Wirkungsgrad von weniger als 35%. Der Wirkungsgrad würde bei 90% liegen, wenn man Verbrennungstemperaturen von über 2000 C hätte, diese werden aber nicht erreicht. Des Weiteren bringt der hohe Kraftstoffverbrauch auch einen hohen CO2 Ausstoß mit sich, der schon seit Jahren immer wieder diskutiert wird. Trotz allem bringt der Verbrennungsmotor auch einige Vorteile mit sich, er ist in der Produktion, aufgrund der hohen Stückzahlen, sehr günstig geworden. Hinzu kommt, dass der Motor sehr robust ist und somit viele Einsatzgebiete hat. Nun zu der Brennstoffzelle: sie ist in der Anwendung sehr umweltfreundlich, da sie als Reaktionsrückstand nur Wasser ausscheidet und keine Schadstoffe in die Umwelt bläst. Des Weiteren ist sie geräuscharm, die Brennstoffzelle hat aber einen deutlich höheren Wirkungsgrad als der Verbrennungsmotor. Bei normaler Betriebstemperatur von 60 C bis 90 C beträgt der Wirkungsgrad 60%-70%. Allerdings sind die hohen Produktionskosten ein Problem, die man allerdings mit einer Massenproduktion senken könnte.
3 Die Geschichte der Brennstoffzelle Geschichte kurz gefasst Groves Brennstoffzelle Experimente Damalige Konkurrenten Geschichte kurz gefasst Die Erfindung der Brennstoffzelle wird dem englischen Physiker Sir William Robert Grove zugeschrieben, da er 1839 mit dem Grovsche Element die erste vergleichbare Zelle zu Versuchszwecken baute. Das Foto zeigt Sir William Robert Grove Die Brennstoffzelle konnte sich allerdings nicht gegen den von Werner von Siemens entwickelten Dynamo durchsezten, da er in Verbindung mit einer Dampfmaschine eine wesentlich effektivere, industriell nutzbare Spannungsquelle war. Wilhelm Ostwald, Direktor des ersten Lehrstuhls für physikalische Chemie in Leipzig, erkannte jedoch schon 1887 das Potenzial von Groves Brennstoffzelle. Seine Theorien bescheinigten der Brennstoffzelle einen Wirkungsgrad von 83% und lösten in den ersten 20er Jahren des 20. Jahrhunderts eine Welle von Konstruktionsvorschlägen aus. In den 1920er Jahren wurden erste Verbesserungen an der Zelle vorgenommen, mit denen man unter anderem die Korrosion der Elektroden in den Griff bekam. In den 1960ern wurde die alkalische Brennstoffzelle erstmals in einem Satelliten eingesetzt und später auch in der Apollo Mission. Die Kosten und die Reinheit der Gase spielten keine Rolle.
4 Groves Brennstoffzelle Das Bild zeigt das Prinzip des Groschen Elements. Diese erste Brennstoffzelle bestand aus zwei Platinelektroden, die in Schwefelsäure getaucht wurden. Um diese wurden Wasserstoff und Sauerstoff gespült. Experimente Das Bild zeigt ein Wasserstoffmotorrad von Karl Kordesch
5 Damalige Konkurrenten Als damalige Konkurrenten kann man nur den Dynamo in Verbindung mit einer Dampfmaschine und den Verbrennungsmotor sehen. Der Dynamo Der Verbrennungsmotor Die alkalische Brennstoffzelle Grundlagen Wieso keine Umgebungsluft? Allgemeine Funktionsweise Die verschiedenen Zellentypen Anwendungsgebiete Grundlagen Die alkalische Brennstoffzelle (engl. Alkaline Fuel Cell, AFC). Bei dieser Brennstoffzelle wird Kalilauge als Elektrolyt verwendet. Als Brenngas wird an der Anode reinster Wasserstoff und an der Kathode reinster Sauerstoff verwendet. Die übliche Betriebstemperatur liegt bei 60 C 90 C, bei einem Wirkungsgrad von 60% - 70%.
6 Wieso keine Umgebungsluft? Bei der alkalischen Brennstoffzelle darf als Kathodengas keine Umgebungsluft verwendet werden. Da das in der Luft enthaltene CO 2 mit der Kalilauge zu Kaliumkarbonat reagieren würde und so die Poren der Elektroden verstopfen würde. Das würde zu einem Ausfall der Zelle kommen. CO2 + 2OH- -> CO3 ²- Allgemeine Funktionsweise + H2O
7 Der Ablauf der Brennstoffzelle Schritt 1 -Die in zwei Kreisläufen getrennten Gase Sauerstoff und Wasserstoff wandern vom Gasraum in den Katalysator. Schritt 2 -Die Wasserstoffmoleküle (H2) werden durch den Katalysator in zwei H+ Atome (Protonen) gespalten. Dabei gibt jedes Wasserstoffatom sein Elektron ab. Schritt 3 -Die Elektronen fließen von der Anode zur Kathode und bewirken einen elektrischen Stromfluß. Der Verbraucher wird mit elektrischer Energie versorgt. Schritt 4 -Jeweils vier Elektronen an der Kathode rekombinieren mit einem Sauerstoffmolekül. Schritt 5 -Die nun entstandenen Sauerstoff-Ionen reagieren mit Wasser zu OH- -Ionen. Schritt 6 -Die Hydroxid-Ionen wandern durch den Elektrolyten (Kalilauge) zur Anode. Schritt 7 -Die Hydroxidionen reagieren an der Anode mit den Protonen zu Wasser. Ein Teil des entstandenen Wassers wird wieder an die Kathode transportiert, wo es für eine weitere Reaktion zur Verfügung steht.
8 Die verschieden Zellentypen 1. Klassische Zellen der ersten Generation mit einem freiem Elektrolytfluss zwischen den Elektroden des Elektrodenpaares. 2. ELOFLUX-Zellen mit kompakten Elektrodenpaaren. 3. Matrix-Zellen, bei denen der Elektrolyt in einer porösen, mit den Elektroden verbundenen Struktur fixiert ist. Die Reaktionsgleichungen 1. Die klassische Zelle Die erste Generation der AFC besteht aus zwei Elektroden, die durch den Elektrolyten Kalilauge voneinander getrennt sind. Zur besseren Katalyse sind die Elektroden jeweils mit einem Katalysator beschichtet. Auf der Wasserstoffseite (Anode) wird Nickel, Platin oder Palladium als Katalysator verwendet, für die Sauerstoffseite kommen Platin, Silber, Mangan oder alle Kohlenstoffe (Graphit, Ruß, Kohle,usw.) in Frage. Die mobilen Ionen in der AFC sind Hydroxid-Ionen (OH-). Die Reaktion in der Zelle kann bei hoher Temperatur der Kalilauge besser ablaufen. Die Kalilauge wird bei zunehmender Temperatur allerdings auch agressiver, ätzender, deswegen liegt die reguläre Betriebstemperatur bei ca. 60 C.
9 Bei dieser Art von Brennstoffzelle zirkuliert die Kalilauge durch die Zelle hindurch. Dies hat zahlreiche Vorteile: Aufgrund der Kalilauge können verschiedene preiswerte Katalysatoren eingesetzt werden Die Lauge transportiert Verschmutzungen weg Die Lauge kühlt die Zelle Die Lauge transportiert das Produktwasser weg Die Lauge kann einfach ausgetauscht werden Die Lauge kann extern regeneriert bzw. gereinigt werden Als Nachteil ist aber bekannt, dass diese Zelle nicht mit Umgebungsluft betrieben werden kann. 2. Die Eloflux Zelle In einer ELOFLUX-Zelle dagegen liegen die Elektroden sehr dicht beieinander und sind nur durch einen porösen Separator von 0,3mm Dicke getrennt. Die Gasversorgung erfolgt über kleine Gaskanäle in den Elektroden, und der freie Elektrolyt strömt von den Stirnseiten her durch die Elektrodenpakete hindurch. Die Wasserstoffelektrode wird mit Nickel als Katalysator beschichtet, die Sauerstoffelektrode mit Silber als Katalysator. Der ursprüngliche Asbest-Separator besteht heute aus einem Material aus PolyolyphynBasis. Die Vorteile der Eloflux-Zelle ligen vor allem in der sehr kompakten Bauweise, die Zelle ist nur 4mm dick. Weitere Vorteile sind der nochmals höhere Wirkungsgrad und die einfache Fertigung. Des Weiteren ist die gute Kohlenstoffdioxid Verträglichkeit ein weiterer positiver Vorteil.
10 3. Die Matrix Zelle In der Matrix-Zelle ist der Elektrolyt in einer porösen, mit den Elektroden verbundenen Struktur fixiert und kann nicht zirkulieren. Die Elektroden befinden sich zwischen einem mit Gas durchströmten Gasraum und einem Diaphragma aus Asbest. Bei den Elektroden handelt es sich um gestützte Pulverelektroden. Die Partikel einer solchen Elektrode werden durch den rechts- und linksseitig der Zelle erzeugten Druck (sog. Druckkissen) aufeinander gepresst und die Elektrode damit zusammen gehalten. Das Katalysatormaterial der Wasserstoffelektrode ist Nickel, dotiert mit Titan und Platin, das der Sauerstoffelektrode Silber mit Zusätzen von Nickel, Titan, Platin und Wismut.
11 Die Reaktionsgleichungen Die Umsetzung von Wasserstoff und Sauerstoff zu Wasser läuft in zweiteilreaktionen ab: Reaktion auf der Wasserstoffseite (Anodenseite): -Die Wasserstoffmoleküle (H2) diffundieren in die Lauge und werden durch den Katalysator in zwei H+ Atome aufgespalten. Dabei gibt jedes Wasserstoffatom sein Elektron ab. Nun reagiert H+ mit OH- zu Wasser (H2O). H2 + 2OH- 2H2O + 2eReaktion auf der Sauerstoffseite (Kathodenseite): -Die Sauerstoffmoleküle diffundieren in die Lauge. Jeweils vier Elektronen rekombinieren mit einem Sauerstoffmolekül. Die nun entstandenen Sauerstoff-Ionen reagieren mit Wasser zu OH-. O2 + 2H2O + 4e- 4OH Anhand der beiden Teilreaktionen lässt sich die Gesamtreaktion aufstellen: 2H2 + O2 2H2O + (4e- * 1,23V) -Die Elektronen, die auf der Wasserstoffseite entstehen, können den Elektrolyten nicht passieren. Sie fließen daher von der Anode über einen elektrischen Verbraucher zur Kathode.
12 Anwendungsgebiete Zu den Anwendungsgebieten der alkalischen Brennstoffzelle sind unter anderem zu zählen: Die Raumfahrt Die Fahrzeugtechnik Die Energiespeicherung Anwendung in der Raumfahrt Zu den Anwendungsgebieten in der Raumfahrt zählen unter anderem Projekte der NASA sowie europäische Projekte. Das Bild zeigt die AFC Brennstoffzelle des Apollo Raumfahrtprojekts der NASA Ende der 1960er Jahre. Im Space Shuttle wird seit des ersten Projekts die alkalische Brennstoffzelle eingebaut.
13 Die alkalische Brennstoffzelle wurde auch in dem europäischen Raumfahrtprojet Hermes angewendet. Anwendung in der Fahrzeugtechnik Zu den Anwendungsgebieten zählen unter anderem: Das Bild zeigt einen, mit einer AFC Brennstoffzelle betriebenen Gabelstabler der Firma STILL. Der deutsche Automobilhersteller Volkswagen hat in einigen VWBussen neuerer Generation, Brennstoffzellen zu Testzwecken eingebaut.
14 Das Bild zeigt ein, mit der AFC Brennstoffzelle betriebenes U-Boot (U212) der deutschen Marine. Die Anwendung in der Energiespeicherung Bildausschnitt aus der SolarWasserstoff-Anlage in Neunburg vorm Wald. In der Solar-Wasserstoff-Anlage in Neunburg vorm Wald wird elektrische Energie mithilfe von Solarzellen gewonnen. Mit diesem Strom erzeugen sie Wasserstoff aus Wasser. Dieser wird wiederum verwendet um mit Brennstoffzellen elektrischen Strom zu erzeugen.
15 Quellenangaben
Inhalt. History Prinzip der Brennstoffzelle Wasserstoff-Sauerstoff-BZ. Polymer Elektrolyte Membrane Fuel Cell Direct Methanol Fuel Cell.
 Brennstoffzellen Inhalt History Prinzip der Brennstoffzelle Wasserstoff-Sauerstoff-BZ Polymer Elektrolyte Membrane Fuel Cell Direct Methanol Fuel Cell o Stacks o Anwendung o Fazit History Erste BZ vor
Brennstoffzellen Inhalt History Prinzip der Brennstoffzelle Wasserstoff-Sauerstoff-BZ Polymer Elektrolyte Membrane Fuel Cell Direct Methanol Fuel Cell o Stacks o Anwendung o Fazit History Erste BZ vor
Die Wirkungsweise einer Brennstoffzelle. Ein Vortrag von Bernard Brickwedde
 Die Wirkungsweise einer Brennstoffzelle Ein Vortrag von Bernard Brickwedde Inhalt Allgemein Definition Geschichte Anwendungsgebiete Aufbau Theoretische Grundlagen Redoxreaktion Wirkungsgrad Elektrochemische
Die Wirkungsweise einer Brennstoffzelle Ein Vortrag von Bernard Brickwedde Inhalt Allgemein Definition Geschichte Anwendungsgebiete Aufbau Theoretische Grundlagen Redoxreaktion Wirkungsgrad Elektrochemische
Brennstoffzellen. Schüler: Julia Schürkamp Fach: Technik Thema: Brennstoffzellen Lehrer: Herr Menne
 Brennstoffzellen Schüler: Julia Schürkamp Fach: Technik Thema: Brennstoffzellen Lehrer: Herr Menne Inhaltsangabe Was ist sind Brennstoffzellen? 1 Wie funktionieren Brennstoffzellen? 2-3 Anwendung der verschiedenen
Brennstoffzellen Schüler: Julia Schürkamp Fach: Technik Thema: Brennstoffzellen Lehrer: Herr Menne Inhaltsangabe Was ist sind Brennstoffzellen? 1 Wie funktionieren Brennstoffzellen? 2-3 Anwendung der verschiedenen
Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse
 Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Die Brennstoffzelle. Von: Ismail Nasser
 Die Brennstoffzelle Gliederung Was ist eine Brennstoffzelle? Geschichte der Brennstoffzelle Aufbau und Funktionsweise der Brennstoffzelle Unterschiedliche Arten Gesamtwirkungsgrad Kosten Was ist eine Brennstoffzelle?
Die Brennstoffzelle Gliederung Was ist eine Brennstoffzelle? Geschichte der Brennstoffzelle Aufbau und Funktionsweise der Brennstoffzelle Unterschiedliche Arten Gesamtwirkungsgrad Kosten Was ist eine Brennstoffzelle?
JUFOTech. wko.at/tirol/jufotech DATENBLATT. Jugend forscht in der Technik. Titel der Projektarbeit: Fachgebiet:
 Datenblatt (dient als Titelblatt für die Projektarbeit) Seite 1/2 JUFOTech Jugend forscht in der Technik wko.at/tirol/jufotech DATENBLATT Wir nehmen am Wettbewerb Jugend forscht in der Technik Auf den
Datenblatt (dient als Titelblatt für die Projektarbeit) Seite 1/2 JUFOTech Jugend forscht in der Technik wko.at/tirol/jufotech DATENBLATT Wir nehmen am Wettbewerb Jugend forscht in der Technik Auf den
HappyEvening am Brennstoffzellen zur mobilen Energiebereitstellung
 HappyEvening am 15.10.2008 Brennstoffzellen zur mobilen Energiebereitstellung T. Pröll 15.10.2008 Inhalt Grundlagen Zelltypen und Anwendungen PEM-Brennstoffzelle (Prinzip) Direkt-Methanol-Brennstoffzelle
HappyEvening am 15.10.2008 Brennstoffzellen zur mobilen Energiebereitstellung T. Pröll 15.10.2008 Inhalt Grundlagen Zelltypen und Anwendungen PEM-Brennstoffzelle (Prinzip) Direkt-Methanol-Brennstoffzelle
Betrieb einer alkalischen Brennstoffzelle mit CO 2 -haltiger Luft
 Betrieb einer alkalischen Brennstoffzelle mit CO 2 -haltiger Luft S. Schudt, H.J. Kohnke, G. Sauer Gaskatel GmbH, Holländische Str. 195, D-34127 Kassel, info@gaskatel.de Schlüsselwörter: Alkalische Brennstoffzelle,
Betrieb einer alkalischen Brennstoffzelle mit CO 2 -haltiger Luft S. Schudt, H.J. Kohnke, G. Sauer Gaskatel GmbH, Holländische Str. 195, D-34127 Kassel, info@gaskatel.de Schlüsselwörter: Alkalische Brennstoffzelle,
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Elektrochemie 1 Abbildung 1: I. VERSUCHSZIEL
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Elektrochemie 1 Abbildung 1: I. VERSUCHSZIEL
Wasserstoff als Energieträger Gliederung:
 Wasserstoff als Energieträger Gliederung: Wasserstoff: Energie speichern und verteilen Die Brennstoffzelle Wasserstoff aus der Ptm6 Alge Wasserstoff als Energiespeicher Der umweltfreundliche Akku: Um Wasserstoff
Wasserstoff als Energieträger Gliederung: Wasserstoff: Energie speichern und verteilen Die Brennstoffzelle Wasserstoff aus der Ptm6 Alge Wasserstoff als Energiespeicher Der umweltfreundliche Akku: Um Wasserstoff
Die elektrische Energie wird durch Ionen transportiert. Ionen sind elektrisch geladene Atome bzw. Elektrolyt
 Galvanische Elemente Galvanische (Galvani ital.physiker) Elemente wandeln chemische in elektrische um. Sie bestehen aus zwei Elektroden (Anode, Kathode) und einer elektrisch leitenden Flüssigkeit, dem
Galvanische Elemente Galvanische (Galvani ital.physiker) Elemente wandeln chemische in elektrische um. Sie bestehen aus zwei Elektroden (Anode, Kathode) und einer elektrisch leitenden Flüssigkeit, dem
Die Brennstoffzelle Technologie der Zukunft?
 Westfälische Wilhelms-Universität Münster Institut für Physikalische Chemie Die Brennstoffzelle Technologie der Zukunft? Sommersemester 2005 Julia Hederer Carolin Eiersbrock Übersicht Einleitung Geschichte
Westfälische Wilhelms-Universität Münster Institut für Physikalische Chemie Die Brennstoffzelle Technologie der Zukunft? Sommersemester 2005 Julia Hederer Carolin Eiersbrock Übersicht Einleitung Geschichte
GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN
 10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
Ich schwitze sagte die Solarzelle. Bei Dir piepst s wohl antwortete der Geigerzähler.
 Ich schwitze sagte die Solarzelle. Bei Dir piepst s wohl antwortete der Geigerzähler. Eine strahlende Reise von der Brennstoffzelle zum Urgestein. Hartmut Abele, Jacqueline Erhart, Christoph Gösselsberger,
Ich schwitze sagte die Solarzelle. Bei Dir piepst s wohl antwortete der Geigerzähler. Eine strahlende Reise von der Brennstoffzelle zum Urgestein. Hartmut Abele, Jacqueline Erhart, Christoph Gösselsberger,
1. Geschichte Im Jahr 1838 fand der Professor Christian Friedrich Schönbein (1799 bis 1868) von der Universität Basel experimentell heraus, dass
 Die Brennstoffzelle 1. Geschichte Im Jahr 1838 fand der Professor Christian Friedrich Schönbein (1799 bis 1868) von der Universität Basel experimentell heraus, dass Elektrizität freigesetzt werden kann,
Die Brennstoffzelle 1. Geschichte Im Jahr 1838 fand der Professor Christian Friedrich Schönbein (1799 bis 1868) von der Universität Basel experimentell heraus, dass Elektrizität freigesetzt werden kann,
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 9 & 10. Die Brennstoffzelle
 Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 9 & 10 Die Brennstoffzelle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll sind drei Lehrerversuche
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 9 & 10 Die Brennstoffzelle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll sind drei Lehrerversuche
Elektrolyse Basics III
 Elektrolyse Basics III Funktionsprinzip der Elektrolyse Funktionsprinzip der elektrochemischen Wasserspaltung (Elektrolyse) Für alle erneuerbaren Energiewandler, die elektrische Energie erzeugen, ist die
Elektrolyse Basics III Funktionsprinzip der Elektrolyse Funktionsprinzip der elektrochemischen Wasserspaltung (Elektrolyse) Für alle erneuerbaren Energiewandler, die elektrische Energie erzeugen, ist die
Chlor-Alkali-Elektrolyse
 Chlor-Alkali-Elektrolyse 1. Allgemeine Erklärung der Elektrolyse 2. Verfahren 2.1 Diaphragmaverfahren 2.2 Membranverfahren 2.3 Amalgamverfahren 3.Vorteile und Nachteile der Verfahren 4. Überspannung 1.
Chlor-Alkali-Elektrolyse 1. Allgemeine Erklärung der Elektrolyse 2. Verfahren 2.1 Diaphragmaverfahren 2.2 Membranverfahren 2.3 Amalgamverfahren 3.Vorteile und Nachteile der Verfahren 4. Überspannung 1.
Power, der die Puste nie ausgeht!
 Fuel Cells Die Brennstoffzelle im Westerwald-Treff Power, der die Puste nie ausgeht! Die Brennstoffzelle im Westerwald-Treff Die Projektpartner Das Brennstoffzellen-Projekt im Hotelpark Westerwald-Treff
Fuel Cells Die Brennstoffzelle im Westerwald-Treff Power, der die Puste nie ausgeht! Die Brennstoffzelle im Westerwald-Treff Die Projektpartner Das Brennstoffzellen-Projekt im Hotelpark Westerwald-Treff
Brennstoffzellenantriebe für US Militär Hybridauto
 Brennstoffzellenantriebe für US Militär Hybridauto PKW mit antrieb wurden von führenden Fahrzeugherstellern bereits in den 80iger Jahren entwickelt. Die anfänglichen Schwierigkeiten hinsichtlich der Tankgröße,
Brennstoffzellenantriebe für US Militär Hybridauto PKW mit antrieb wurden von führenden Fahrzeugherstellern bereits in den 80iger Jahren entwickelt. Die anfänglichen Schwierigkeiten hinsichtlich der Tankgröße,
diebrennstoffzelle.de
 PEM-Brennstoffzelle PEM-FC? Proton Exchange Membrane Fuel Cell Polymermembran (Methanol)* (Methan)* Temperatur -8 C bis 25kW Wirkungsgrad 6% (H2) 4% (CH4) Anwendungen Stromversorgung Pkw/Bus Hausversorgung
PEM-Brennstoffzelle PEM-FC? Proton Exchange Membrane Fuel Cell Polymermembran (Methanol)* (Methan)* Temperatur -8 C bis 25kW Wirkungsgrad 6% (H2) 4% (CH4) Anwendungen Stromversorgung Pkw/Bus Hausversorgung
Gasdiffusionselektroden in Wasserstoffelektroden und Metall/Luft Batterien
 Dechema Fortbildungstag Gasdiffusionselektroden in Wasserstoffelektroden und Metall/Luft Batterien Dr. Hans-Joachim Kohnke Gaskatel 4.12.2012 Frankfurt / Main Gegründet 1997 Spin off Universität Kassel
Dechema Fortbildungstag Gasdiffusionselektroden in Wasserstoffelektroden und Metall/Luft Batterien Dr. Hans-Joachim Kohnke Gaskatel 4.12.2012 Frankfurt / Main Gegründet 1997 Spin off Universität Kassel
Alkalische Brennstoffzelle: Sauerstoffreduktion und Kohlendioxidabbau
 München GDCh-Jahrestagung 2003 Alkalische Brennstoffzelle: Sauerstoffreduktion und Kohlendioxidabbau Dr. H.-J. Kohnke, J. Helmke, M. Wünsche Gaskatel GmbH Holländische Str. 195 Kassel / Germany Products
München GDCh-Jahrestagung 2003 Alkalische Brennstoffzelle: Sauerstoffreduktion und Kohlendioxidabbau Dr. H.-J. Kohnke, J. Helmke, M. Wünsche Gaskatel GmbH Holländische Str. 195 Kassel / Germany Products
EinFaCh 1. Studienvorbereitung Chemie. Einstieg in Freibergs anschauliches Chemiewissen Teil 1: Redoxreaktionen und Elektrochemie.
 Studienvorbereitung Chemie EinFaCh 1 Einstieg in Freibergs anschauliches Chemiewissen Teil 1: Redoxreaktionen und Elektrochemie www.tu-freiberg.de http://tu-freiberg.de/fakultaet2/einfach Was ist eine
Studienvorbereitung Chemie EinFaCh 1 Einstieg in Freibergs anschauliches Chemiewissen Teil 1: Redoxreaktionen und Elektrochemie www.tu-freiberg.de http://tu-freiberg.de/fakultaet2/einfach Was ist eine
Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle
 Lehrer-/Dozentenblatt Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Alle Brennstoffzellen bestehen prinzipiell aus zwei
Lehrer-/Dozentenblatt Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Alle Brennstoffzellen bestehen prinzipiell aus zwei
Erklärt euch die Aufgabe. Erklärt euch die Aufgabe gegenseitig noch einmal in euren eigenen Worten. euren eigenen Worten.
 Erklärt euch die Aufgabe gegenseitig noch einmal in euren eigenen Worten. Klärt dabei, wie ihr die Aufgabe verstanden habt und was euch noch unklar ist. Erklärt euch die Aufgabe gegenseitig noch einmal
Erklärt euch die Aufgabe gegenseitig noch einmal in euren eigenen Worten. Klärt dabei, wie ihr die Aufgabe verstanden habt und was euch noch unklar ist. Erklärt euch die Aufgabe gegenseitig noch einmal
ALTERNATIVE ANTRIEBE BRENNSTOFFZELLE. Die Brennstoffzelle
 Die Brennstoffzelle Um aus (regenerativ gewonnenem) Wasserstoff Strom zu erzeugen, verwendet man Brennstoffzellen. Bei einer Brennstoffzelle handelt es sich um eine besondere Art eines galvanischen Elements.
Die Brennstoffzelle Um aus (regenerativ gewonnenem) Wasserstoff Strom zu erzeugen, verwendet man Brennstoffzellen. Bei einer Brennstoffzelle handelt es sich um eine besondere Art eines galvanischen Elements.
Bedienungsanleitung. F109 Fuel Cell Stack 5. F110 Fuel Cell Stack 10
 Bedienungsanleitung F109 Fuel Cell Stack 5 F110 Fuel Cell Stack 10 H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel.: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com
Bedienungsanleitung F109 Fuel Cell Stack 5 F110 Fuel Cell Stack 10 H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel.: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com
Was ist Elektrochemie? Elektrochemie. Elektrochemie ist die Lehre von der Beziehung
 Was ist Elektrochemie? Elektrochemie Elektrochemie ist die Lehre von der Beziehung zwischen elektrischen und chemischen Prozessen. 131 Stromleitung in einem Metall Wir haben gelernt, dass die Stromleitung
Was ist Elektrochemie? Elektrochemie Elektrochemie ist die Lehre von der Beziehung zwischen elektrischen und chemischen Prozessen. 131 Stromleitung in einem Metall Wir haben gelernt, dass die Stromleitung
Alkalische Kleinelektrolyseure für Laborgas, Schweissen, Brennstoffzellen
 Alkalische Kleinelektrolyseure für Laborgas, Schweissen, Brennstoffzellen H.-J. Kohnke, J. Helmke, H. Klüver Gaskatel GmbH, Holländische Str. 195, 34127 Kassel, info@gaskatel.de Schlüsselwörter: Wasserstofferzeugung,
Alkalische Kleinelektrolyseure für Laborgas, Schweissen, Brennstoffzellen H.-J. Kohnke, J. Helmke, H. Klüver Gaskatel GmbH, Holländische Str. 195, 34127 Kassel, info@gaskatel.de Schlüsselwörter: Wasserstofferzeugung,
Elektroautos mit Brennstoffzellen-Energieversorgung Antrieb mit Wasserstoff ohne Schadstoffe
 Elektroautos mit Brennstoffzellen-Energieversorgung Antrieb mit Wasserstoff ohne Schadstoffe Dipl.-Ing. Andreas Brinner, Dipl.-Ing. FH Tilo Maag, Dipl.-Ing. Sonia Urbano Pfaffenwaldring 38-40, D-70569
Elektroautos mit Brennstoffzellen-Energieversorgung Antrieb mit Wasserstoff ohne Schadstoffe Dipl.-Ing. Andreas Brinner, Dipl.-Ing. FH Tilo Maag, Dipl.-Ing. Sonia Urbano Pfaffenwaldring 38-40, D-70569
Elektrochemie. Grundbegriffe. Oxidation: Ist die Teilreaktion bei der Elektronen abgegeben werden.
 Grundbegriffe Elektrochemische Reaktionen sind Redoxreaktionen, d.h Reaktionen mit Elektronenübergang. Sie können freiwillig ablaufen (galvanische Zelle) oder durch anlegen einer Spannung erzwungen werden
Grundbegriffe Elektrochemische Reaktionen sind Redoxreaktionen, d.h Reaktionen mit Elektronenübergang. Sie können freiwillig ablaufen (galvanische Zelle) oder durch anlegen einer Spannung erzwungen werden
Martin Raiber 21.02.07 Elektrolyse: Strom - Spannungskurven
 Martin Raiber 21.02.07 Elektrolyse: Strom - Spannungskurven Geräte: U-Rohr, verschiedene Platin-Elektroden (blank, platiniert), Graphit-Elektroden, spannungsstabilisierte Gleichspannungsquelle, CASSY-Spannungs/Stromstärkemessgerät
Martin Raiber 21.02.07 Elektrolyse: Strom - Spannungskurven Geräte: U-Rohr, verschiedene Platin-Elektroden (blank, platiniert), Graphit-Elektroden, spannungsstabilisierte Gleichspannungsquelle, CASSY-Spannungs/Stromstärkemessgerät
EnBW Cell Plus. Die Hausenergieversorgung der Zukunft. BRENNSTOFFZELLE
 EnBW Cell Plus. Die Hausenergieversorgung der Zukunft. BRENNSTOFFZELLE EnBW Wir denken weiter. Mit Energie was unternehmen. So lautet unsere Philosophie, die unser tägliches Denken und Handeln bestimmt.
EnBW Cell Plus. Die Hausenergieversorgung der Zukunft. BRENNSTOFFZELLE EnBW Wir denken weiter. Mit Energie was unternehmen. So lautet unsere Philosophie, die unser tägliches Denken und Handeln bestimmt.
Elektrizität. = C J m. Das Coulomb Potential φ ist dabei:
 Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Brenstoff-Zellen-Text zum Unterricht
 Brenstoff-Zellen-Text zum Unterricht Ein experimenteller Aufbau zeigt eine Kette an Energieumwandlungen vom Sonnenlicht bis hin zum Wind. Verschiedene experimentelle Varianten werden angeboten: Dynamot-Variante
Brenstoff-Zellen-Text zum Unterricht Ein experimenteller Aufbau zeigt eine Kette an Energieumwandlungen vom Sonnenlicht bis hin zum Wind. Verschiedene experimentelle Varianten werden angeboten: Dynamot-Variante
Redoxgleichungen: Massenerhaltung Elektronenaufnahme/ -abgabe Halbreaktion: Getrennter Prozess (Reduktion, Oxidation getrennt anschauen)
 AChe 2 Kapitel 20: Elektrochemie Oxidationszahlen: Ladung des Atomes wenn es als Ion vorliegen würde. Oxidation: OX-Zahl steigt, Reduktion: OX-Zahl sinkt. Redoxgleichungen: Massenerhaltung Elektronenaufnahme/
AChe 2 Kapitel 20: Elektrochemie Oxidationszahlen: Ladung des Atomes wenn es als Ion vorliegen würde. Oxidation: OX-Zahl steigt, Reduktion: OX-Zahl sinkt. Redoxgleichungen: Massenerhaltung Elektronenaufnahme/
Grundlagen: Galvanische Zellen:
 E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
Spannungs-Stromquellen
 Spannungs-Stromquellen 1. Galvanische Spannungsreihe 2. Primärelemente 3. Sekundärelemente 4. Brennstoffzelle 5. Thermoelektrizität i) Seebeck-effekt ii) Peltier-effekt Strom/Spannungsquellen Damit Strom
Spannungs-Stromquellen 1. Galvanische Spannungsreihe 2. Primärelemente 3. Sekundärelemente 4. Brennstoffzelle 5. Thermoelektrizität i) Seebeck-effekt ii) Peltier-effekt Strom/Spannungsquellen Damit Strom
Simulation elektrochemischer Abläufe in Direkt-Methanolbrennstoffzellen
 Simulation elektrochemischer Abläufe in Direkt-Methanolbrennstoffzellen Torsten Köhler Mohrenstr. 39 10117 Berlin +49 30 2 03 72 0 www.wias-berlin.de Februar 2005 1/19 Inhalt 1. Elektrochemische Grundlagen
Simulation elektrochemischer Abläufe in Direkt-Methanolbrennstoffzellen Torsten Köhler Mohrenstr. 39 10117 Berlin +49 30 2 03 72 0 www.wias-berlin.de Februar 2005 1/19 Inhalt 1. Elektrochemische Grundlagen
ACHTUNG! Nur zum Gebrauch für Kinder über
 P ROFI FUEL CELL KIT BEDIENUNGSANLEITUNG D ACHTUNG! Nur zum Gebrauch für Kinder über 10 Jahren. Benutzung nur unter der genauen Aufsicht von Erwachsenen, die sich mit den im Experimentierkasten beschriebenen
P ROFI FUEL CELL KIT BEDIENUNGSANLEITUNG D ACHTUNG! Nur zum Gebrauch für Kinder über 10 Jahren. Benutzung nur unter der genauen Aufsicht von Erwachsenen, die sich mit den im Experimentierkasten beschriebenen
Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle. Inhaltsfeld: Elektrochemie
 Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle Inhaltsfeld: Elektrochemie Inhaltliche Schwerpunkte: Mobile Energiequellen Elektrochemische Gewinnung von Stoffen Zeitbedarf: ca. 5 Std. à 45
Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle Inhaltsfeld: Elektrochemie Inhaltliche Schwerpunkte: Mobile Energiequellen Elektrochemische Gewinnung von Stoffen Zeitbedarf: ca. 5 Std. à 45
Energiespeichersysteme
 Speichersysteme - D-1 Energiespeichersysteme 1. Wasserstofftechnologie a) Gewinnung von Wasserstoff b) Sicherheitsproblematik c) Speicherung, Systemlösungen 2. Konventionelle Blockheizkraftwerke - Kraft-Wärme-(Kälte-)Kopplung
Speichersysteme - D-1 Energiespeichersysteme 1. Wasserstofftechnologie a) Gewinnung von Wasserstoff b) Sicherheitsproblematik c) Speicherung, Systemlösungen 2. Konventionelle Blockheizkraftwerke - Kraft-Wärme-(Kälte-)Kopplung
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Von der Knallgasexplosion zur Brennstoffzelle
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Von der Knallgasexplosion zur Brennstoffzelle Das komplette Material finden Sie hier: School-Scout.de 19. Von der Knallgasexplosion
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Von der Knallgasexplosion zur Brennstoffzelle Das komplette Material finden Sie hier: School-Scout.de 19. Von der Knallgasexplosion
6.3 Stromerzeugung mit galvanischen Zellen. Aufbauprinzip + Kontakte Abdichtung
 6.3 Stromerzeugung mit galvanischen Zellen Aufbauprinzip + Kontakte Abdichtung Elektrolyt Anode Stromkollektor Kathode Behälter Separator (Diaphragma) Anode: Kathode: Elektrolyt: Separator: Oxidation eines
6.3 Stromerzeugung mit galvanischen Zellen Aufbauprinzip + Kontakte Abdichtung Elektrolyt Anode Stromkollektor Kathode Behälter Separator (Diaphragma) Anode: Kathode: Elektrolyt: Separator: Oxidation eines
πάντα ῥεῖ alles fließt Karlsruhe 18. Dezember 2012 Gekoppelte Ströme
 πάντα ῥεῖ alles fließt Karlsruhe 18. Dezember 2012 Gekoppelte Ströme Hans M. Strauch Kurfürst-Ruprecht-Gymnasium, 67433 Neustadt/W. HansMStrauch@t-online.de Gekoppelte Ströme Ein Stoff mehrere Energieträger
πάντα ῥεῖ alles fließt Karlsruhe 18. Dezember 2012 Gekoppelte Ströme Hans M. Strauch Kurfürst-Ruprecht-Gymnasium, 67433 Neustadt/W. HansMStrauch@t-online.de Gekoppelte Ströme Ein Stoff mehrere Energieträger
Übersicht Lambdasonde Funktion und Aufbau Einsatzgebiete KFZ-Katalysator Oxidationskatalysator Speicherkatalysator SCR-Kat 2
 Übersicht Lambdasonde Funktion und Aufbau Einsatzgebiete KFZ-Katalysator Oxidationskatalysator Speicherkatalysator SCR-Kat 2 Lambdasonde Misst den Restsauerstoffgehalt in einem Abgas Vergleicht diesen
Übersicht Lambdasonde Funktion und Aufbau Einsatzgebiete KFZ-Katalysator Oxidationskatalysator Speicherkatalysator SCR-Kat 2 Lambdasonde Misst den Restsauerstoffgehalt in einem Abgas Vergleicht diesen
Elektrochemie. C 11 EuG Inhalt
 1 C 11 EuG Inhalt Elektrochemie 1 Stromerzeugung 1.1 Vorüberlegung: Zink-Kupfer-Lokal-Element a) xidation von Metallen mit Nichtmetallen b) xidation von Nichtmetallanionen mit Nichtmetallen c) xidation
1 C 11 EuG Inhalt Elektrochemie 1 Stromerzeugung 1.1 Vorüberlegung: Zink-Kupfer-Lokal-Element a) xidation von Metallen mit Nichtmetallen b) xidation von Nichtmetallanionen mit Nichtmetallen c) xidation
Einführung in Technik und Funktionsweise von Brennstoffzellen und Batterieantrieben Prof. Dr. K. Andreas Friedrich
 Einführung in Technik und Funktionsweise von Brennstoffzellen und Batterieantrieben Prof. Dr. K. Andreas Friedrich Folie 1 > Friedrich, Ungethüm > Institut für Technische Thermodynamik, Institut für Fahrzeugkonzepte
Einführung in Technik und Funktionsweise von Brennstoffzellen und Batterieantrieben Prof. Dr. K. Andreas Friedrich Folie 1 > Friedrich, Ungethüm > Institut für Technische Thermodynamik, Institut für Fahrzeugkonzepte
Die Brennstoffzelle als neue energetische Möglichkeit Auswege statt Apokalypse
 3 Die Brennstoffzelle als neue energetische Möglichkeit Auswege statt Apokalypse Name: Michael Müller Franz- Meyers- Gymnasium Kurs: 12 PaLk Hoffmann Schuljahr: 2000/2001 Fachlehrer: Herr Dr. Loosen 4
3 Die Brennstoffzelle als neue energetische Möglichkeit Auswege statt Apokalypse Name: Michael Müller Franz- Meyers- Gymnasium Kurs: 12 PaLk Hoffmann Schuljahr: 2000/2001 Fachlehrer: Herr Dr. Loosen 4
Wirtschaftlichkeitsanalyse
 Präsentation November 2002 Präsentiert von Flugzeugbauingenieur Diplomand Wirtschaftlichkeitsanalyse Vergleich eines Wassergenerierungssystems mit dem konventionellen Wassersystem in Flugzeugen Inhalt
Präsentation November 2002 Präsentiert von Flugzeugbauingenieur Diplomand Wirtschaftlichkeitsanalyse Vergleich eines Wassergenerierungssystems mit dem konventionellen Wassersystem in Flugzeugen Inhalt
Brennstoffzelle - Kosten
 Brennstoffzelle - Kosten Die Kosten für eine Brennstoffzelle sind schwer festzulegen zumal man vorab unterscheiden müsste für welchen Zweck die Brennstoffzelle eingesetzt werden soll und vor allem, welche
Brennstoffzelle - Kosten Die Kosten für eine Brennstoffzelle sind schwer festzulegen zumal man vorab unterscheiden müsste für welchen Zweck die Brennstoffzelle eingesetzt werden soll und vor allem, welche
Elektrolysekammer mit Kohle-Elektroden Best.- Nr. MD04073
 Elektrolysekammer mit Kohle-Elektroden Best.- Nr. MD04073 1. Beschreibung Die Elektrolysekammern sind in drei Varianten lieferbar: MD04071 MD04072 MD04073 mit Nickel-Elektroden mit Platin-Elektroden mit
Elektrolysekammer mit Kohle-Elektroden Best.- Nr. MD04073 1. Beschreibung Die Elektrolysekammern sind in drei Varianten lieferbar: MD04071 MD04072 MD04073 mit Nickel-Elektroden mit Platin-Elektroden mit
Galvanische Zellen aus Nichtmetallen (Artikelnr.: P )
 Lehrer-/Dozentenblatt Galvanische Zellen aus Nichtmetallen (Artikelnr.: P7400900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische Chemie Unterthema:
Lehrer-/Dozentenblatt Galvanische Zellen aus Nichtmetallen (Artikelnr.: P7400900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische Chemie Unterthema:
BRENNSOFFZELLE HOTMODULE. Biogas zur Stromerzeugung mit der Brennstoffzelle. Manuel Lutz Kassel, Februar 2010
 BRENNSOFFZELLE HOTMODULE. Biogas zur Stromerzeugung mit der Brennstoffzelle Manuel Lutz Kassel, Februar 2010 STARKE MARKEN UND UNTERNEHMEN Marken Produkte Dieselmotoren und komplette Antriebssysteme Gasbetriebene
BRENNSOFFZELLE HOTMODULE. Biogas zur Stromerzeugung mit der Brennstoffzelle Manuel Lutz Kassel, Februar 2010 STARKE MARKEN UND UNTERNEHMEN Marken Produkte Dieselmotoren und komplette Antriebssysteme Gasbetriebene
Brennstoffzelle für die Serie: 175 Jahre und kein bisschen greise
 Auto-Medienportal.Net: 30.11.2014 Brennstoffzelle für die Serie: 175 Jahre und kein bisschen greise Von Thomas Lang Als Pionier alternativer Antriebstechnologien für Automobile hat Toyota spätestens seit
Auto-Medienportal.Net: 30.11.2014 Brennstoffzelle für die Serie: 175 Jahre und kein bisschen greise Von Thomas Lang Als Pionier alternativer Antriebstechnologien für Automobile hat Toyota spätestens seit
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.de 2 von 18 6. Wir bauen eine Zitronenbatterie (Kl. 9/10) Chemische
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.de 2 von 18 6. Wir bauen eine Zitronenbatterie (Kl. 9/10) Chemische
Was ist wichtig für die siebte Kursarbeit?
 Was ist wichtig für die siebte Kursarbeit? Redoxreaktion: Oxidation (Elektronen-Donator) und Reduktion (Elektronen-Akzeptor) korrespondierende Redoxpaare. Prinzip der Lösungstension, Betrachtung der Halbzellenreaktion
Was ist wichtig für die siebte Kursarbeit? Redoxreaktion: Oxidation (Elektronen-Donator) und Reduktion (Elektronen-Akzeptor) korrespondierende Redoxpaare. Prinzip der Lösungstension, Betrachtung der Halbzellenreaktion
Die Standard Reduktions-Halbzellenpotentiale. Die Standard Reduktions. Wird die Halbzellenreaktion Zn 2+ /Zn gegen die Standard-Wassersoffelektrode
 Die Standard Reduktions Die Standard Reduktions-Halbzellenpotentiale Wird die Halbzellenreaktion Zn 2+ /Zn gegen die Standard-Wassersoffelektrode in einer galvanischen Zelle geschaltet, ergibt sich eine
Die Standard Reduktions Die Standard Reduktions-Halbzellenpotentiale Wird die Halbzellenreaktion Zn 2+ /Zn gegen die Standard-Wassersoffelektrode in einer galvanischen Zelle geschaltet, ergibt sich eine
What comes down must go up
 What comes down must go up Eine einheitliche Beschreibung der Wasserstoff-Brennstoff-Zelle und des Thermoelements Michael Pohlig WHG-Durmersheim Didaktik der Physik an der Uni-KA michael@pohlig.de What
What comes down must go up Eine einheitliche Beschreibung der Wasserstoff-Brennstoff-Zelle und des Thermoelements Michael Pohlig WHG-Durmersheim Didaktik der Physik an der Uni-KA michael@pohlig.de What
4. Workshop. Mobile Energieversorgung militärische Anwendungen. Elektroden in alkalischen Brennstoffzelle. Gaskatel GmbH, Kassel
 4. Workshop Mobile Energieversorgung militärische Anwendungen Elektroden in alkalischen Brennstoffzelle Gaskatel GmbH, Kassel Dr. Hans-Joachim Kohnke 22.11.2007 Pfinztal Gaskatel Gegründet 1997 in Kassel
4. Workshop Mobile Energieversorgung militärische Anwendungen Elektroden in alkalischen Brennstoffzelle Gaskatel GmbH, Kassel Dr. Hans-Joachim Kohnke 22.11.2007 Pfinztal Gaskatel Gegründet 1997 in Kassel
10TG. Training II2. 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene.
 Training II2 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene. (4X4=1 X4=16P) a. Verbrennung von Kohlenstoff C + O2 CO2 Kohlenstoffdioxid b. Thermolyse
Training II2 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene. (4X4=1 X4=16P) a. Verbrennung von Kohlenstoff C + O2 CO2 Kohlenstoffdioxid b. Thermolyse
Brennstoffzelle. Tim Kösterke Bernd Hasken 15. 06. 2005
 Brennstoffzelle Tim Kösterke Bernd Hasken 15. 06. 2005 Verschiedene Brennstoffzellen Niedertemperaturbereich PEM Brennstoffzelle (PEMFC) Direkt-Methanol Brennstoffzelle (DMFC) Alkalische Brennstoffzelle
Brennstoffzelle Tim Kösterke Bernd Hasken 15. 06. 2005 Verschiedene Brennstoffzellen Niedertemperaturbereich PEM Brennstoffzelle (PEMFC) Direkt-Methanol Brennstoffzelle (DMFC) Alkalische Brennstoffzelle
Energieerzeugung für ein modernes Zuhause.
 Willkommen in der Zukunft. Energieerzeugung für ein modernes Zuhause. Wer hätte vor 30 Jahren auch nur im Traum daran gedacht, was heute alles möglich ist? Jedes Kind kennt sie, diese Faszination, wenn
Willkommen in der Zukunft. Energieerzeugung für ein modernes Zuhause. Wer hätte vor 30 Jahren auch nur im Traum daran gedacht, was heute alles möglich ist? Jedes Kind kennt sie, diese Faszination, wenn
1. Elektrolysen 1.1. Chemikalien: Zn-Pulver Bromwasser (T) dest. Wasser
 1. Elektrolysen 1.1 Elektrolysen Redoxreaktion und Elektrolyse Redoxreaktionen und Elektrolysen hängen eng miteinander zusammen. Die folgenden Versuche mögen dies verdeutlichen: Redoxreaktion Zn + Bromwasser
1. Elektrolysen 1.1 Elektrolysen Redoxreaktion und Elektrolyse Redoxreaktionen und Elektrolysen hängen eng miteinander zusammen. Die folgenden Versuche mögen dies verdeutlichen: Redoxreaktion Zn + Bromwasser
KORROSION UND KORROSIONSSCHUTZ VON METALLEN
 11. Einheit: KORROSION UND KORROSIONSSCHUTZ VON METALLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 16 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Korrosion und Korrosionsschutz von Metallen..
11. Einheit: KORROSION UND KORROSIONSSCHUTZ VON METALLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 16 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Korrosion und Korrosionsschutz von Metallen..
Der Mensch kann ohne Gold, nicht aber ohne Salz leben.
 Text aus Schroedel, Chemieheute: Chloralkali-Elektrolyse "Der Mensch kann ohne Gold, nicht aber ohne Salz leben." Dieser Satz stammt von dem römischen Geschichtsschreiber CASSIODORUS, der vor etwa 1500
Text aus Schroedel, Chemieheute: Chloralkali-Elektrolyse "Der Mensch kann ohne Gold, nicht aber ohne Salz leben." Dieser Satz stammt von dem römischen Geschichtsschreiber CASSIODORUS, der vor etwa 1500
Das Brennstoffzellen-Radio
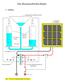 Das Brennstoffzellen-Radio 1. Aufbau Auffangbehälter (Haushaltstrichter) Solarpaneel (KOSMOS) 10 10 20 20 30 30 40 50 destilliertes Wasser Gastanks (Einwegspritzen) 40 50 60 70 80 60 Plexiglas 90 ml 100
Das Brennstoffzellen-Radio 1. Aufbau Auffangbehälter (Haushaltstrichter) Solarpaneel (KOSMOS) 10 10 20 20 30 30 40 50 destilliertes Wasser Gastanks (Einwegspritzen) 40 50 60 70 80 60 Plexiglas 90 ml 100
-1 (außer in Verbindung mit Sauerstoff: variabel) Sauerstoff -2 (außer in Peroxiden: -1)
 1) DEFINITIONEN DIE REDOXREAKTION Eine Redoxreaktion = Reaktion mit Elektronenübertragung sie teilt sich in Oxidation = Elektronenabgabe Reduktion = Elektronenaufnahme z.b.: Mg Mg 2 + 2 e z.b.: Cl 2 +
1) DEFINITIONEN DIE REDOXREAKTION Eine Redoxreaktion = Reaktion mit Elektronenübertragung sie teilt sich in Oxidation = Elektronenabgabe Reduktion = Elektronenaufnahme z.b.: Mg Mg 2 + 2 e z.b.: Cl 2 +
Schuleigener Lehrplan Chemie (Grundlage: KLP 2008) Klasse 9. Schuleigener Lehrplan. Chemie - Klasse 9 -
 Schuleigener Lehrplan Chemie - Klasse 9 - 9 Saure und alkalische Lösungen Ionen in sauren und alkalischen Lösungen Neutralisation Protonenaufnahme und Abgabe an einfachen Beispielen Stöchiometrische Berechnungen
Schuleigener Lehrplan Chemie - Klasse 9 - 9 Saure und alkalische Lösungen Ionen in sauren und alkalischen Lösungen Neutralisation Protonenaufnahme und Abgabe an einfachen Beispielen Stöchiometrische Berechnungen
Schulversuchspraktikum. Marie-Lena Gallikowski. Sommersemester Klassenstufen 9 & 10. Die Brennstoffzelle. Kurzprotokoll
 Schulversuchspraktikum Marie-Lena Gallikowski Sommersemester 2015 Klassenstufen 9 & 10 Die Brennstoffzelle Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll enthält weitere Lehrerversuche für die Klassenstufen
Schulversuchspraktikum Marie-Lena Gallikowski Sommersemester 2015 Klassenstufen 9 & 10 Die Brennstoffzelle Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll enthält weitere Lehrerversuche für die Klassenstufen
Wasserstoffautos. Leon Bentrup. 20. Januar Funktionsweise, Kritik und Gründe
 GFS NwT 2014 Fr. Maschner Wasserstoffautos Funktionsweise, Kritik und Gründe Leon Bentrup 20. Januar 2014 Inhaltsverzeichnis 1 Vorwort 3 2 Wasserstoff 4 2.1 Eigenschaften.................................
GFS NwT 2014 Fr. Maschner Wasserstoffautos Funktionsweise, Kritik und Gründe Leon Bentrup 20. Januar 2014 Inhaltsverzeichnis 1 Vorwort 3 2 Wasserstoff 4 2.1 Eigenschaften.................................
E 3 Brennstoffzelle. 1 Aufgabenstellung
 E 3 Brennstoffzelle 1 Aufgabenstellung 1.1 Ermitteln Sie den Wirkungsgrad eines Elektrolyseurs. 1. Nehmen Sie die Strom-Spannungs-Kennlinie eines Brennstoffzellensystems auf und erläutern Sie den erhaltenen
E 3 Brennstoffzelle 1 Aufgabenstellung 1.1 Ermitteln Sie den Wirkungsgrad eines Elektrolyseurs. 1. Nehmen Sie die Strom-Spannungs-Kennlinie eines Brennstoffzellensystems auf und erläutern Sie den erhaltenen
Innovative Kraft-Wärme-Kopplung mit einer Brennstoffzelle
 Innovative Kraft-Wärme-Kopplung mit einer Brennstoffzelle Martin Barnsteiner Projektleitung Bild 1 Was ist Kraft-Wärme-Kopplung (KWK)? Strom und Wärme wird gleichzeitig z. B. in einen Erdgas-Motor erzeugt.
Innovative Kraft-Wärme-Kopplung mit einer Brennstoffzelle Martin Barnsteiner Projektleitung Bild 1 Was ist Kraft-Wärme-Kopplung (KWK)? Strom und Wärme wird gleichzeitig z. B. in einen Erdgas-Motor erzeugt.
6.1 Elektrodenpotenzial und elektromotorische Kraft
 6.1 Elektrodenpotenzial und elektromotorische Kraft Zinkstab Kupferstab Cu 2+ Lösung Cu 2+ Lösung Zn + 2e Cu Cu 2+ + 2e Cu 2+ Eine Elektrode ist ein metallisch leitender Gegenstand, der zur Zu oder Ableitung
6.1 Elektrodenpotenzial und elektromotorische Kraft Zinkstab Kupferstab Cu 2+ Lösung Cu 2+ Lösung Zn + 2e Cu Cu 2+ + 2e Cu 2+ Eine Elektrode ist ein metallisch leitender Gegenstand, der zur Zu oder Ableitung
Brennstoffzelle für den Hausgebrauch: Die Gamma 1 von Baxi Innotech
 Brennstoffzelle für den Hausgebrauch: Die Gamma 1 von Baxi Innotech Nicht viel größer als ein herkömmlicher Heizkessel liefert das Brennstoffzellen-Heizgerät GAMMA 1.0 übers Jahr fast Dreiviertel des benötigten
Brennstoffzelle für den Hausgebrauch: Die Gamma 1 von Baxi Innotech Nicht viel größer als ein herkömmlicher Heizkessel liefert das Brennstoffzellen-Heizgerät GAMMA 1.0 übers Jahr fast Dreiviertel des benötigten
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)
 Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... zeigen Vor- und Nachteile ausgewählter Produkte des Alltags (u.a. Aromastoffe, Alkohole) und ihre Anwendung auf, gewichten diese und beziehen
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... zeigen Vor- und Nachteile ausgewählter Produkte des Alltags (u.a. Aromastoffe, Alkohole) und ihre Anwendung auf, gewichten diese und beziehen
Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1 Ch-GK Q1/IHF 3: Unterrichtsvorhaben I:
 Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1 Ch-GK Q1/IHF 3: Unterrichtsvorhaben I: Kontext: Mobile Energiequellen: von der Batterie über den Akkumulator
Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1 Ch-GK Q1/IHF 3: Unterrichtsvorhaben I: Kontext: Mobile Energiequellen: von der Batterie über den Akkumulator
Unterrichtsvorhaben Q1 Grundkurs Chemie
 Unterrichtsvorhaben Q1 Grundkurs Chemie Jahrgangsstufe: Q1 GK Jahresthema (Inhaltsfeld 2): Säuren, Basen und analytische Verfahren Eigenschaften und Struktur von Säuren und Basen / Säuren und Basen in
Unterrichtsvorhaben Q1 Grundkurs Chemie Jahrgangsstufe: Q1 GK Jahresthema (Inhaltsfeld 2): Säuren, Basen und analytische Verfahren Eigenschaften und Struktur von Säuren und Basen / Säuren und Basen in
Brenstoffzelle (BRZ)
 Seite 1 Themengebiet: Thermodynamik 1 Literatur A. Macdonald, M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris, Berlin, 2007 A.J. Bard, L.R. Faulkner, Electrochemical Methods Fundamentals
Seite 1 Themengebiet: Thermodynamik 1 Literatur A. Macdonald, M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris, Berlin, 2007 A.J. Bard, L.R. Faulkner, Electrochemical Methods Fundamentals
Schuleigener Lehrplan. Chemie - Klasse 9 -
 Schuleigener Lehrplan Chemie - Klasse 9 - Hinweis: Sie finden zu jedem Inhaltsfeld einen Vorschlag für eine Unterrichtsreihe mit dem zugeordneten Kontext auf der umseitigen CD! 9 Saure und alkalische Lösungen
Schuleigener Lehrplan Chemie - Klasse 9 - Hinweis: Sie finden zu jedem Inhaltsfeld einen Vorschlag für eine Unterrichtsreihe mit dem zugeordneten Kontext auf der umseitigen CD! 9 Saure und alkalische Lösungen
Brennstoffzelle. Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes. Schüler-Skript und Versuchsanleitung
 Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes Bearbeitet von Markus Beckert, Sheila Sabock Stand 12.09.2013 Inhaltsverzeichnis 1 Einführung... 3 1.1 Vorbereitung, Vorwissen, Vorüberlegungen...
Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes Bearbeitet von Markus Beckert, Sheila Sabock Stand 12.09.2013 Inhaltsverzeichnis 1 Einführung... 3 1.1 Vorbereitung, Vorwissen, Vorüberlegungen...
Meine Energiequelle. das effizienteste Kleinkraftwerk der Welt
 Meine Energiequelle das effizienteste Kleinkraftwerk der Welt Aus Gas wird Strom Innovative Brennstoffzellen-Technologie Der BlueGEN wird mit Ihrem Gasanschluss verbunden und erzeugt aus Erdgas oder Bioerdgas
Meine Energiequelle das effizienteste Kleinkraftwerk der Welt Aus Gas wird Strom Innovative Brennstoffzellen-Technologie Der BlueGEN wird mit Ihrem Gasanschluss verbunden und erzeugt aus Erdgas oder Bioerdgas
Fachbereich Ingenieurwissenschaften und Mathematik. Praktikum Dezentrale Energiesysteme. DEZ 1 Brennstoffzellen
 Fachbereich Ingenieurwissenschaften und Mathematik Praktikum Dezentrale Energiesysteme DEZ 1 Brennstoffzellen Lehrgebiet Regenerative Energiesysteme und Elektrotechnik Prof.-Dr.-Ing. Jens Haubrock Inhalt
Fachbereich Ingenieurwissenschaften und Mathematik Praktikum Dezentrale Energiesysteme DEZ 1 Brennstoffzellen Lehrgebiet Regenerative Energiesysteme und Elektrotechnik Prof.-Dr.-Ing. Jens Haubrock Inhalt
Reformierung von Kohlenwasserstoffen PEM-Elektrolyse
 Bereitstellung von Wasserstoff Reformierung von Kohlenwasserstoffen PEM-Elektrolyse Ursula Wittstadt Fraunhofer-Institut für Solare Energiesysteme ISE Wasserstoff Expo 2002 Hamburg, 10.10.2002 Fraunhofer
Bereitstellung von Wasserstoff Reformierung von Kohlenwasserstoffen PEM-Elektrolyse Ursula Wittstadt Fraunhofer-Institut für Solare Energiesysteme ISE Wasserstoff Expo 2002 Hamburg, 10.10.2002 Fraunhofer
Dotierung. = gezieltes Verunreinigen des Si-Kristalls mit bestimmten Fremdatomen. n-dotierung Einbau. von Atomen mit 3 Valenzelektronen
 Halbleiter Dotierung = gezieltes Verunreinigen des Si-Kristalls mit bestimmten Fremdatomen. n-dotierung Einbau von Atomen mit 5 Valenzelektronen = Donatoren Elektronengeber (P, Sb, As) p-dotierung Einbau
Halbleiter Dotierung = gezieltes Verunreinigen des Si-Kristalls mit bestimmten Fremdatomen. n-dotierung Einbau von Atomen mit 5 Valenzelektronen = Donatoren Elektronengeber (P, Sb, As) p-dotierung Einbau
Batterien. Überblick über die verschiedenen Typen und allgemeinen Funktionsweisen. ... wie es im Lexikon steht:
 Batterien Überblick über die verschiedenen Typen und allgemeinen Funktionsweisen... wie es im Lexikon steht: Batterie, die; -, -n [.. i-en] Stromquelle, deren erhöhte Leistung durch die Vereinigung
Batterien Überblick über die verschiedenen Typen und allgemeinen Funktionsweisen... wie es im Lexikon steht: Batterie, die; -, -n [.. i-en] Stromquelle, deren erhöhte Leistung durch die Vereinigung
Wasserstoff. - Den Antrieb eines Fahrzeuges durch die direkte Verbrennung von Wasserstoff in einem Verbrennungsmotor
 Wasserstoff Einführung Der so genannte Treibhauseffekt dürfte wohl jedem spätestens durch die aktuelle Diskussion um den UNO-Klimabericht 2007 ein Begriff sein. Auch dürfte allgemein bekannt sein, dass
Wasserstoff Einführung Der so genannte Treibhauseffekt dürfte wohl jedem spätestens durch die aktuelle Diskussion um den UNO-Klimabericht 2007 ein Begriff sein. Auch dürfte allgemein bekannt sein, dass
Verfahrenstechnisches Tutorium Prof. Dr.-Ing. M. J. Hampe
 Verfahrenstechnisches Tutorium Prof. Dr.-Ing. M. J. Hampe Wintersemester 2012/13 4. Versuch: Brennstoffzelle Dipl.-Ing. Sebastian Lang Learning outcome Nachdem Sie sich mit diesem Versuch auseinandergesetzt
Verfahrenstechnisches Tutorium Prof. Dr.-Ing. M. J. Hampe Wintersemester 2012/13 4. Versuch: Brennstoffzelle Dipl.-Ing. Sebastian Lang Learning outcome Nachdem Sie sich mit diesem Versuch auseinandergesetzt
Chemie Zusammenfassung JII.2 #1
 Chemie Zusammenfassung JII.2 #1 Oxidation/Reduktion/Oxidationsmittel/Reduktionsmittel/Redoxpaar In einer elektrochemischen Reaktion gehen Elektronen von einem Stoff zu einem anderen über. Wenn ein Stoff
Chemie Zusammenfassung JII.2 #1 Oxidation/Reduktion/Oxidationsmittel/Reduktionsmittel/Redoxpaar In einer elektrochemischen Reaktion gehen Elektronen von einem Stoff zu einem anderen über. Wenn ein Stoff
Photovoltaik-Module mm Länge eines Moduls 4.1A Strom bei max. Leistung
 Photovoltaik-Module Photovoltaik-Module wandeln Sonnenenergie in elektrische Energie um. Dazu nutzen Solarzellen den photoelektrischen Effekt, der mittels Absorption von Sonnenlicht Elektronen in Bewegung
Photovoltaik-Module Photovoltaik-Module wandeln Sonnenenergie in elektrische Energie um. Dazu nutzen Solarzellen den photoelektrischen Effekt, der mittels Absorption von Sonnenlicht Elektronen in Bewegung
Übungsaufgaben zu den LPE 16: Wärmekraftwerke und 17: Abgasreinigung
 Übungsaufgaben zu den LPE 16: Wärmekraftwerke und 17: Abgasreinigung Themenbereiche Clausius-Rankine-Prozess T,s-Diagramm Abgasreinigung Inhaltsverzeichnis 2 Übungsaufgaben zur LPE 17 (Abgasreinigung)...1
Übungsaufgaben zu den LPE 16: Wärmekraftwerke und 17: Abgasreinigung Themenbereiche Clausius-Rankine-Prozess T,s-Diagramm Abgasreinigung Inhaltsverzeichnis 2 Übungsaufgaben zur LPE 17 (Abgasreinigung)...1
Nanotechnologie in der Brennstoffzelle
 Nanotechnologie in der Brennstoffzelle Vortrag zur Vorlesung Nanostrukturphysik WS 10/11 Nicolas Jäckel 1 Übersicht Wie Funktioniert eine Brennstoffzelle? Arten von Brennstoffzellen Nanotechnologische
Nanotechnologie in der Brennstoffzelle Vortrag zur Vorlesung Nanostrukturphysik WS 10/11 Nicolas Jäckel 1 Übersicht Wie Funktioniert eine Brennstoffzelle? Arten von Brennstoffzellen Nanotechnologische
Die wärmegeführte Kraft-Wärme-Kopplung
 Verantwortung für Energie und Umwelt Die wärmegeführte Kraft-Wärme-Kopplung Technische Lösungen und Wirkungsweisen Markus Telian, Leiter Marketing & Entwicklung Heiztechnik, Hovalwerk Vaduz Inhalt KWK
Verantwortung für Energie und Umwelt Die wärmegeführte Kraft-Wärme-Kopplung Technische Lösungen und Wirkungsweisen Markus Telian, Leiter Marketing & Entwicklung Heiztechnik, Hovalwerk Vaduz Inhalt KWK
Bitte decken Sie die schraffierte Fläche mit einem Bild ab. Please cover the shaded area with a picture. (24,4 x 7,6 cm)
 Bitte decken Sie die schraffierte Fläche mit einem Bild ab. Please cover the shaded area with a picture. (24,4 x 7,6 cm) Historisches Museum Frankfurt 26.09.2018 Prof. Peter Säger Head of Search Field
Bitte decken Sie die schraffierte Fläche mit einem Bild ab. Please cover the shaded area with a picture. (24,4 x 7,6 cm) Historisches Museum Frankfurt 26.09.2018 Prof. Peter Säger Head of Search Field
Ergebnisse des Forscherteams Energie des 2 Campus 2016
 Wie ist es möglich das elektrolytische Verfahren Power-to-Gas hinsichtlich Nachhaltigkeit und Effizienz zu optimieren? Ergebnisse des Forscherteams Energie des 2 Campus 2016 WWF Deutschland Westfälische
Wie ist es möglich das elektrolytische Verfahren Power-to-Gas hinsichtlich Nachhaltigkeit und Effizienz zu optimieren? Ergebnisse des Forscherteams Energie des 2 Campus 2016 WWF Deutschland Westfälische
Einfache Elektrolysen und Leitfähigkeit
 Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 9&10 Einfache Elektrolysen und Leitfähigkeit Auf einen Blick: Zum Thema Einfache Elektrolysen und Leitfähigkeit können zahlreiche anschauliche
Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 9&10 Einfache Elektrolysen und Leitfähigkeit Auf einen Blick: Zum Thema Einfache Elektrolysen und Leitfähigkeit können zahlreiche anschauliche
