Klinische Chemie Theorie Wasserhaushalt, Elektrolyte
|
|
|
- Bella Gerber
- vor 8 Jahren
- Abrufe
Transkript
1 Wissen Phase 1b: Grundlagen aus Physik und Chemie werden vorausgesetzt. Sie kennen die Kompartimente des Wassergehalts im menschlichen Organismus und die Ionenzusammensetzung des IZR /EZR Sie können Osmolalität beschreiben und kennen deren Messverfahren. Sie kennen detailliert die hormonelle Regulation des Wasserhaushaltes. Sie können die Elektrolyte Natrium und Kalium näher beschreiben (Erhöhung und Verminderung, Alarmwerte) und wissen, wie man sie messen kann. Sie kennen die Regulation des Calciumhaushalts und wissen, welche Form des Calciums biologisch wirksam ist. Sie wissen ausserdem, was präanalytisch die Calciumbestimmung stören kann. Sie kennen die Atomabsorptionsfotometrie, sowie die Flammenemissionsfotometrie aus der Physik. Sie kennen grob das Prinzip der ISE und die Bestandteile deren Messkette. medi, Bildungsgang medizinisches Labor 1 P. Hirschi
2 Inhaltsverzeichnis: 1. Flüssigkeitsräume, Kompartimente Osmotischer und kolloidosmotischer Druck Osmotischer Druck Kolloidosmotischer Druck Osmoregulation Osmolalitätsmessung Der Wasserhaushalt Die Herkunft des Wassers Störungen im Wasserhaushalt Hormonelle Regulation des Wasserhaushalts Elektrolyte Natrium Kalium Bedeutung und Regulation des Calciums Verfahren zur Messung von Elektrolyten Flammenfotometrie FFM Atomabsorptionsfotometrie Potentiometrie mit ISE medi, Bildungsgang medizinisches Labor 2 P. Hirschi
3 1. FLÜSSIGKEITSRÄUME, KOMPARTIMENTE Der Wassergehalt des menschlichen Organismus beträgt je nach Menge des Körperfettes 50 70% des Körpergewichtes. Das Gesamtkörperwasser lässt sich in einzelne Kompartimente ( Räume ) unterteilen und zwar zunächst in einen intra- (IZR) und extrazellulären (EZR) Flüssigkeitsraum. DER EXTRAZELLULÄRRAUM (EZR): Der EZR umfasst das Blutplasma (=intravasaler Raum); den interstitiellen Raum, der dem zwischen den Zellen liegenden Flüssigkeitsvolumen entspricht; sowie die transzelluläre Flüssigkeit (engl. third space), die den Liquor cerebrospinalis, die Flüssigkeit in den Körperhöhlen und das Wasser der Augenkammer umfasst. Beispiel: Bei einem Mann mit einem Körpergewicht von 70 kg und einem Wasseranteil von 60% verteilt sich das Wasser im Organismus wie folgt: 2/3 im IZR = 28 L Wasser 70 kg Körpergewicht, davon 60% Wasser = 42 L Wasser 1/3 im EZR = 14 L Wasser 10.5 L interstitiell 3 L intravasal 0.5 L transzellulär Neben dem Wasser sind die Elektrolyte von entscheidender Bedeutung für die Zusammensetzung der Flüssigkeitskompartimente. Allgemein chemisch sind Elektrolyte Salze, Säuren und Basen, die in wässriger Lösung den elektrischen Strom leiten können. Unter Elektrolyte im Organismus werden in der Medizin in der Regel verstanden: Kationen Natrium (Na + ) Kalium (K +) Calcium (Ca 2 + ) Magnesium (Mg 2 + ) und die Anionen Chlorid (Cl - ) Anorganisches Phosphat (HPO 4 2- ) Bicarbonat (HCO 3 - ) Die Konzentration der einzelnen Elektrolyte ist in den Flüssigkeitsräumen sehr unterschiedlich und weist ein charakteristisches Muster auf. Proteine liegen bei physiologischem ph ( ) grösstenteils als Anionen vor. Die Konzentration der Proteine ist in den Zellen weitaus höher als im EZR Die Ungleichverteilung von Natrium und Kalium ist Voraussetzung für die Erregbarkeit von Membranen, wie sie z. B. bei Nerven und Muskelzellen benötigt medi, Bildungsgang medizinisches Labor 3 P. Hirschi
4 wird. Die Verteilung wird durch einen aktiven Transport hergestellt und aufrechterhalten. Im EZR überwiegen Na + - und Cl -_ Ionen, im IZR dagegen herrschen K + und Phosphationen vor. Dieser Unterschied wird durch eine Natrium-Kalium-Pumpe aufrechterhalten, die unter Energieverbrauch (ATP) Natrium im Austausch gegen Kalium aus der Zelle transportiert. 2. OSMOTISCHER UND KOLLOIDOSMOTISCHER DRUCK 2.1. Osmotischer Druck Definition: Unter Osmolalität bzw. Osmolarität versteht man in der Medizin die Konzentration osmotisch wirksamer Teilchen, unabhängig von deren Art, Zusammensetzung, oder elektrischer Ladung. Osmose ist die passive Diffusion von Lösungsmittel (meist Wasser) durch eine semipermeable Membran in Richtung der Lösung mit der grösseren Teilchenkonzentration. Triebkraft hierfür ist ein Konzentrationsunterschied osmotisch wirksamer Teilchen zwischen zwei Kompartimenten. Osmotisch wirksam ist ein Teilchen dann, wenn es Wasser anzieht". Physiologischerweise ist die Osmolalität des IZR gleich der des EZR, beide Kompartimente enthalten also isotonische Lösungen. Der Unterschied zwischen Osmolalität und Osmolarität besteht in der Bezugsgrösse: Osmolalität = osmol/kg Wasser Die Osmolalität bezieht sich auf die Masse des Lösungsmittels, d.h. auf 1 kg reines Wasser. Die in der klinischen Routine eingesetzten Osmometer messen die Osmolalität. Beispiel: Werden 1 mmol Glukose (180 mg) in einem kg Wasser gelöst, so beträgt die Osmolalität 1 mosmol/kg Wasser. Osmolarität = osmol/l Lösung Die Osmolarität weist als Bezugsgrösse das Volumen einer Lösung auf. Beispiel: Befinden sich in einem Liter Glukoselösung 1 mmol Glukose so beträgt die Osmolarität 1 mosmol/l. Bei Substanzen die in wässrigen Lösungen dissoziieren, tragen alle Teilchen zur Osmolalität bei: Beispiel: 1 mmol NaCl in 1 kg Wasser gelöst führt zu einer Osmolalität von 1.75 mosmol/kg Wasser, da NaCl fast vollständig in Na + und Cl - dissoziiert (0.75 Na +, 0.75 Cl - und 0.25 NaCl. medi, Bildungsgang medizinisches Labor 4 P. Hirschi
5 Blutplasma weist eine Osmolalität von ungefähr 290 mosmol/kg auf, davon werden etwa 50% durch Natriumsalze aufgebracht. Der IZR und der EZR stehen im osmotischen Gleichgewicht, d. h. Veränderungen im osmotischen Druck in IZR oder EZR werden durch Wasserverschiebungen zwischen diesen Kompartimenten ausgeglichen. Die messbare Serumosmolalität ist daher repräsentativ für beide Räume. - EZR: Bestimmend für den osmotischen Druck sind hier wegen ihrer hohen Konzentration vor allem Natrium, Harnstoff, Glucose, Proteine, usw. - IZR: Für den osmotischen Druck im Zellinneren ist dagegen die Konzentration des Kaliums entscheidend Kolloidosmotischer Druck Der Anteil des osmotischen Drucks, der durch Proteine (auch Kolloide genannt) hervorgerufen wird, bezeichnet man als kolloidosmotischen oder onkotischen Druck. Er ist mitverantwortlich dafür, dass Flüssigkeit aus dem Interstitium wieder in die Kapillaren aufgenommen wird. Obwohl er gegenüber der osmotischen Wirkung von Natrium vernachlässigbar klein ist, spielt er für die Flüssigkeitsverteilung im Organismus eine Rolle, da die Proteine nicht einfach durch die Gefässwand diffundieren können, im Gegensatz zu Natrium. In den Blutgefässen ist der Proteingehalt grösser (v. a. Albumin) als in der interstitiellen Flüssigkeit. Sinkt die Proteinkonzentration im Plasma, so tritt vermehrt Wasser aus dem Gefässystem in den interstitiellen Raum. Beispiel: Bei Nierenerkrankungen kann es zu einem renalen Verlust von Albumin kommen, dies führt zu einem Austritt von Wasser in das Gewebe, was als Ödeme bezeichnet wird Osmoregulation Wir unterscheiden 2 Arten von Messsensoren : Mechanorezeptoren registrieren Druck- und Dehnungsreize, die wiederum volumenabhängig sind. Das effektive intraarterielle Blutvolumen (EABV). welches durch Rezeptoren, lokalisiert an Karotissinus, Aortenbogen, juxtaglomerulärem Apparat, gemessen wird, ist eine besonders empfindliche Messgrösse (körperintern) des EZV. Bei Abfall des EABV werden entsprechende gegenregulatorische Massnahmen getroffen. Die Osmoregulatoren sind im Hypothalalmus lokalisiert, diese spezialisierten Zellen vergleichen intra- mit extrazellulärer Osmolalität und passen dementsprechend die Sekretion des Hormons ADH (siehe weiter unten) im Hypothalamushinterlappen an, welches die Wasserrückresorption in den Nieren reguliert. Eine erhöhte Osmolalität fördert, eine erniedrigte Osmolalität hemmt die ADH-Ausschüttung. medi, Bildungsgang medizinisches Labor 5 P. Hirschi
6 2.4. Die Osmolalitätsmessung Klinische Chemie Theorie Zur Messung der Osmolalität eignet sich besonders die Messung der Gefrierpunktserniedrigung mit dem Gefrierpunktsosmometer (Kryoskop). Prinzip der Gefrierpunktsmessung Durch die gelösten Bestandteile wird der Gefrierpunkt einer wässrigen Lösung, verglichen mit reinem Wasser, herabgesetzt. Diese Gefrierpunktserniedrigung ist proportional der Zahl der gelösten Teilchen (nicht nur Ionen, sondern alle osmotisch wirksamen Teilchen), hauptsächlich Glucose, Natrium, Harnstoff, oder auch körperfremde Substanzen wie Alkohole). Eine Lösung mit 1 mol/l gelöster Substanz gefriert bei C. Umgekehrt kann man aus der genauen Messung des Gefrierpunktes auf die Konzentration schliessen. Die Messung des Gefrierpunktes einer Lösung ermöglicht daher eine Aussage über die Konzentration an gelösten Teilchen. Osmometer sind allerdings bereits in Osmolalitätseinheiten geeicht. Abb. 1: Messung mit dem Osmometer. die Gefrierpunktserniedrigung fällt umso grösser aus, je mehr gelöste Teilchen in der Lösung sind. Durchführung der Messung: Die Probe wird thermoelektrisch auf ca. -6 C abgekühlt = Unterkühlung ohne zu gefrieren da die Probe nicht in Bewegung ist. Auslösen des Gefriervorganges, z.b. durch einen vibrierenden Metalldraht. Durch die Bildung von Eis wird Wärme frei, die zu einem Temperaturanstieg in der Probe führt. Die Temperatur bleibt einige Zeit auf einem Plateau stehen, dies entspricht dem Gefrierpunkt der Lösung. Die Differenz zwischen dieser Temperatur und 0 C, dem Gefrierpunkt von reinem Wasser, wird vom Gerät erfasst und in mosmol/kg umgerechnet. Wenn die ganze Probe durchgefroren ist sinkt die Temperatur weiter ab. medi, Bildungsgang medizinisches Labor 6 P. Hirschi
7 Die Gefrierpunktserniedrigung in obigem Beispiel beträgt 0.56 C (Differenz zu reinem Wasser, das bei 0 C gefriert), entsprechend einer Osmolalität von 290 mosmol/kg. Folgende Berechnung kann zur Kontrolle der gemessenen Werte (nur der Plasma- Osmolalität) eingesetzt werden. Eine Diskrepanz zwischen Messung und Berechnung weist nicht immer auf einen Messfehler hin. Für erhöhte Osmolalitätswerte können auch andere, körperfremde, osmotisch wirksame Substanzen verantwortlich sein, (z.b. Alkohol 0,8 = 18 mosmol/kg). Formel: (Einheiten in mmol/l) Serumosmolalität mosmol/kg = 2x Na + + Glucose + Harnstoff Da mit der Formel nicht alle Teilchen, die zur gesamten Osmolalität beitragen, erfasst werden, ist die berechnete Osmolalität immer kleiner als die gemessene. Normalerweise beträgt die Differenz ca. 10 mmol/l. Ist der Unterschied grösser, so liegt eine signifikante Lücke vor, dies z.b. bei einem hohen Blutalkoholspiegel. Referenzwerte: Serum: mosmol/kg Urin: mosmol/kg Erhöhung der Osmolalität durch: Urämie Hyperglykämie Alkoholintoxikation Austrocknung (z.b. Durchfälle) Therapie mit konzentrierten Infusionen von Proteinen 3. DER WASSERHAUSHALT Innerhalb der Flüssigkeitsräume, aber auch zwischen dem Organismus und der Umwelt findet ständig ein Wasseraustausch statt. Abb. 2: Mittlere Zufuhr 2 Liter pro Tag 3.1. Die Herkunft des Wassers Wasser wird durch flüssige und feste Nahrung aufgenommen, entsteht jedoch auch im Stoffwechsel (Oxidationswasser). medi, Bildungsgang medizinisches Labor 7 P. Hirschi
8 Beispiel: Der Abbau von einem Molekül Glukose liefert 6 Wassermoleküle (und 6 Kohlendioxid) C 6 H C H 2 O Beim Abbau von 100 g Neutralfett werden 100 g Wasser produziert; 100 g Kohlenhydrate ergeben 60 g und 100 g Proteine 44 g Wasser Störungen im Wasserhaushalt Die Wasserabgabe erfolgt durch Ausscheidung in Urin und Faeces, sowie über Haut und Lungen. Störungen in diesem Gleichgewicht von Aufnahme und Abgabe manifestieren sich klinisch mit: - Negativer Wasserbilanz "Wassermangel" DEHYDRATATION - Positive Wasserbilanz "Wasserüberschuss" HYPERHYDRATION Verluste in den Wasserkompartimenten machen sich folgendermassen bemerkbar: o Intrazelluläre Flüssigkeitsverluste beeinträchtigen die zelluläre Funktion und führen zu zentralnervösen Symptomen wie Lethargie, Konfusion und Koma. o Bei Verlusten aus dem EZR, z. B. bei Blutungen, kommt es zu Kreislaufkollaps, Nierenversagen und Schock. Die gute Permeabilität von Wasser, die mit einer gleichmässigen Verteilung auf die Kompartimente verbunden ist, kann dazu führen, dass klinische Zeichen des Flüssigkeitsmangels nicht gleich erkennbar werden. Der Wasserbestand des Organismus kann im fortgeschrittenen Stadium anhand folgender klinischer Parameter beurteilt werden: Hauptsymptome bei Volumenverminderung sind: Verminderter Hauttugor (Elastizität der Haut) Trockene Mundschleimhaut Verminderte Schweiss-Sekretion Blutdruckabfall bei stärkerem Volumenverlust. Abb. 3: Verminderter Hauttugor Ein verändertes EZV (intravasal) kann bei der optische Beurteilung von Serum- Hämatokrit-Anteilen bei einem zentrifugierten Probenröhrchen erkannt werden. Durch Veränderung des EZV ist der Plasmaanteil gegenüber dem Hämatokrit verschoben und es kommt zu einem falschen Ergebnis bei den Serumparametern sowie dem HK wenn dieser nicht berechnet sondern gemessen wurde. medi, Bildungsgang medizinisches Labor 8 P. Hirschi
9 3.3. Hormonelle Regulation des Wasserhaushalts: Die Steuerung der Wasserausscheidung und damit die Feinregulation der Wasserbilanz erfolgt vorwiegend über hormonelle Signale an die Nieren. Dabei steuern drei Hormone, bzw. Hormongruppen den Wasserhaushalt und gleichzeitig auch den Salzhaushalt (v.a. Natrium): ADH: ANTIDIURETISCHES HORMON, Synonyme: Adiuretin, Vasopressin; synthetisiert im Hypothalamus; fördert die Rückresorption von Wasser im distalen Tubulus und den Sammelrohren, wodurch die Urinkonzentration erhöht und das Urinvolumen erniedrigt wird. ADH erhöht zudem den Blutdruck ("Vasopressin") durch Erhöhung des Plasmavolumens. Die Steuerung der ADH-Ausschüttung erfolgt durch verschiedene Messsensoren, über das extrazelluläre Volumen und der Serumosmolalität, d. h. nicht nur über den Wassergehalt allein, sondern über das Verhältnis Salze zu Wasser. ADH wird nicht routinemässig gemessen, als Ersatz wird die Serumosmolalität bestimmt. RENIN-ANGIOTENSIN-ALDOSTERON-SYSTEM, Abb 4: RAAS Bei Blutdruckabfall, Abnahme des Blutvolumens (durch Wasserverlust) und Natriummangel wird von den juxtaglomerulären Zellen der Nieren vermehrt Renin abgegeben. In der Blutbahn spaltet Renin das von der Leber gebildete Angiotensinogen zu Angiotensin I, dieses wird durch weitere Abspaltung (durch das Angiotensin-Converting-Enzym ACE) zu Angiotensin II umgewandelt. Angiotensin II wirkt gefässverengend und damit blutdruckerhöhend, es fördert die Produktion von Aldosteron in den medi, Bildungsgang medizinisches Labor 9 P. Hirschi
10 Nebennieren, bewirkt eine ADH-Ausschüttung und erhöht den Durst. Aldosteron, ein Mineralkortikoid, steigert die Rückresorption von Natrium und damit osmotisch bedingt die Wasserrückresorption in den Nierentubuli. Gleichzeitig fördert es die Ausscheidung von Kalium und Wasserstoffionen. ATRIALE NATRIURETISCHE PEPTIDE (ANP, BNP): Kleine Gruppe von Peptiden mit Hormonwirkung, deren Hauptfunktion die Reduktion des Plasmavolumens und des Blutdrucks ist. Dies bewirken sie über die Hemmung der ADH- und Reninfreisetzung - dadurch hemmen sie die Wasserrückresorption und die Aldosteronproduktion - sowie über eine Erhöhung der glomerulären Filtrationsrate. Damit wird weniger Natrium (und Wasser) rückresorbiert, das Plasmavolumen sinkt und somit auch der BD. ANP und BNP werden in den Vorhöfen des Herzens aufgrund erhöhter Wandspannung im Herz gebildet 4. ELEKTROLYTE: Natrium und Kalium Elektrolyte dienen der Beurteilung des Gesundheitszustandes oder des Krankheitsgeschehens helfen bei der Diagnosestellung erlauben in vielen Fällen eine Therapiekontrolle. Für uns in der klinischen Chemie sind folgende Elektrolyte wichtig: Die Kationen Die Anionen - Natrium (Na + ) - Chlorid (Cl - ) - Kalium (K + ) - Anorg. Phosphat (HPO 2-4 ) - Calcium (Ca 2+ ) - Bicarbonat (HCO - 3 ) (s. Säure/Basen) - Magnesium (Mg 2+ ) 4.1. Natrium Vorkommen und Wirkung: Natrium ist das häufigste extrazelluläre Kation im Organismus. Es macht einen grossen Anteil der osmotisch wirksamen Teilchen im Plasma aus und spielt eine wesentliche Rolle bei der Aufrechterhaltung des osmotischen Gleichgewichts und der normalen Wasserverteilung des EZR. Natriumionen spielen zudem eine wichtige Rolle für die Erregungsfortleitung in Nerven- und Muskelzellen. Die Aufnahme von Natrium mit der Nahrung liegt ungefähr zwischen 100 und 200 mmol/tag. Natrium wird zwar aktiv im Dünndarm resorbiert, die eigentliche Regulation des Natriumgehaltes erfolgt aber durch die Nieren. Natrium wird glomerulär filtriert, jedoch im Tubulussystem unter Einwirkung von Aldosteron bis zu 99% wieder rückresorbiert, oder unter ANP-Wirkung ausgeschieden. medi, Bildungsgang medizinisches Labor 10 P. Hirschi
11 Natrium in Verbindung mit dem Wasserhaushalt: Wasser- und Natriumbestand sind eng miteinander verknüpft. Änderungen des Wasserbestandes verteilen sich gleichmässig auf IZV und EZV zur Aufrechterhaltung der Isotonie. Hypo- und Hypernatriämie sind daher meistens Ausdruck eines veränderten Wasserbestandes. Störungen des Natriumbestandes werden in der Regel durch Wasserverschiebungen ausgeglichen, was mit Änderungen des EZV einhergeht. Hyponatriämie = Plasmanatrium < 135 mmol/l Natriummenge und Wasservolumen bestimmen die Serumkonzentration, so dass sich ein Natriumverlust, veränderte Wasserretention (renale Rückresorption) oder Einstrom von Wasser in den intravasalen Raum bei erhöhter Osmolalität als mögliche Abnahme der Natriumkonzentration ergeben. URSACHEN: - Natriumverlust: Gastrointestinal (Durchfall, Erbrechen); renal (Aldosteronmangel); Diuretika welche die Natriumrückresorption blockieren. - Zufuhr Mengen an elektrolytfreiem Wasser, z. B. Glucoseinfusion. - Inadequate ADH-Sekretion (SIADH) zuviel ADH wird freigesetzt, die Wasserrückresorption steigt Verdünnungseffekt. Dies kommt z. B. bei Infektionen, Tumore oder Verletzungen vor, oder wird durch Medikamente verursacht. - Hyponatriämie als Folge von Hyperglykämie: Anstieg des osmotischen Drucks in den Gefässen führt zum Einstrom von Wasser aus dem Gewebe Verdünnungseffekt. - Volumenverdränkungseffekt bei der Messung von lipid- und proteinreichen Proben fehlendes Lösungsvolumen für Natrium. Falsch tiefe Konzentration, da nur Ionen gemessen werden. FOLGEN EINER HYPONATRIÄMIE: Bedingt durch den osmotischen Gradienten kommt es bei Hypoosmolalität im Plasma zum Einstrom von Wasser in die Zellen. Die Folgen davon sind: Störungen des ZNS mit Übelkeit, Erbrechen und Krampfanfällen bis zum Koma oder sogar Tod. Hypernatriämie = Plasmanatrium > 145 mmol/l URSACHEN: - Zunahme des Natriumbestandes: Natriumbicarbonat-Infusionen; primärer Hyperaldosterinismus (Morbus-Conn-Syndrom): mehr Aldosteron Natriumreabsorption steigt. - Wasserverlust: Verminderte Wasseraufnahme; Diabetes insipidus: Verminderte ADH-Sekretion (zentraler D. i.), oder Rezeptordefekt für ADH in den Sammelrohren der Niere (peripherer D. i.) FOLGEN EINER HYPERNATRIÄMIE: Ein erhöhter Natriumgehalt des Organismus führt zu Entzug von Wasser aus den Zellen. Die Folgen davon sind Durst, Verwirrtheit und Koma medi, Bildungsgang medizinisches Labor 11 P. Hirschi
12 ANALYTIK Die Messung des Natriums kann durchgeführt werden mit: Ionenselektiven Elektroden (ISE): Direkte und indirekte Potentiometrie Flammenemissionsphotometrie FFM Atomabsorptionsphotometrie (eher selten, da zu aufwändig für die Routine) Die FFM ist heute weitgehend durch die ISE ersetzt worden. Die ISE wird in diesem Skript noch besprochen. Bestimmungsindikationen Störungen im Wasser- und Elektrolythaushalt Störungen im Säure-Basen-Haushalt Nierenerkrankungen, gastroenterale Erkrankungen Referenzwerte: Im Serum/Plasma mmol/l Alarmwerte: < 120 mmol/l und > 155 mmol/l 4.2. Kalium Vorkommen und Wirkung: Vorkommen: Kalium ist das dominierende intrazelluläre Kation. Der Konzentrationsgradient zwischen dem IZR (160 mmol/l) und dem EZR (4 mmol/l intravasal) ist gewaltig, so dass schon geringe Kaliumverluste aus den Zellen die Konzentration im EZR stark ansteigen lassen. Nur gerade 2% des Gesamtkörperkaliums zirkulieren im Plasma. Dieser Gradient wird durch die Na-K- ATPase-Pumpe (siehe oben) aufrechterhalten. Wirkung: Kalium beeinflusst: Die Regulation der neuromuskulären Erregbarkeit Die Kontraktion der Herzmuskulatur Das intrazelluläre Volumen Die Bildung und Wirkung von camp (intrazellulärer Signalübermittler). Kalium wird ausserdem vom Säure-Basen-Haushalt beeinflusst Die wichtigste Wirkung von Kalium ist die Beeinflussung der Herztätigkeit, die Erregbarkeit der Herzmuskelzellen ist auf einen Gradienten der Kaliumkonzentration von intra- zu extrazellulär angewiesen.. Bei hohen Kaliumkonzentrationen im Plasma verlangsamt sich die Herzfrequenz (Bradykardie). Erniedrigte Kaliumkonzentrationen erhöhen die Erregbarkeit der Herzmuskulatur (Tachykardie), was zu Herzrhythmusstörungen führen kann. Bei einer Azidose, d. h. einem Überschuss von H + -Ionen im Blut, treten vermehrt H + - Ionen in die Zelle ein. Im Austausch (zur Wahrung der Elektroneutralität) verlässt dafür Kalium die Zelle, so dass es zu einer Hyperkaliämie kommt. Bei einer medi, Bildungsgang medizinisches Labor 12 P. Hirschi
13 Alkalose (Verminderung der H+-Ionen im Blut) ist entsprechend mit einer Hypokaliämie zu rechnen. Regulation des Kaliumbestandes: Das glomerulär filtrierte Kalium wird im proximalen Tubulussystem praktisch vollständig rückresorbiert. Im distalen Tubulus und in den Sammelrohren wird unter dem Einfluss von Aldosteron, im Austausch mit Natrium, Kalium sezerniert. Verschieden Faktoren beeinflussen die Verteilung von Kalium zwischen IZR und EZR: Bei einer Hemmung der Na-K-ATPase Pumpe kann es zu Kaliumverlust aus dem IZR kommen, z. B. bei Hypoxämie Insulin fördert den raschen Übertritt von Kalium aus dem EZR in die Zellen. Katecholamine (Adreanalin, Noradrenalin) fördern den Eintritt von Kalium in die Zellen, Betablocker (Herzmedikamente) hemmen ihn. Medikamente die die Wasserauscheidung über die Nieren fördern (Diuretika) können auch die Kaliumausscheidung erhöhen. Kalium sparende Präparate führen dagegen zu einem Anstieg der Plasmakonzentration von Kalium. Hypokaliämie = Plasmakalium < 3.5 mmol/l URSACHEN: - Diuretika: Eine Überdosierung von Diuretika, die NICHT kaliumsparend sind, führt zu einer gesteigerten Kaliumausscheidung. - Aldosteronerhöhung: Beim Hyperaldosteronismus (Conn-Syndrom) ist die renale Kaliumrückresorption vermindert, da vermehrt Natrium rückresorbiert und Kalium dafür ausgeschieden wird. - Durchfall: Durchfall, Erbrechen führen zu enteralem Kaliumverlust. - Alkalose: Kaliumionen werden im Austausch gegen Protonen (H + ) in die Zellen aufgenommen. - Zuviel Insulin: Insulin bewirkt eine rasche Aufnahme von Glucose und Kalium in den IZR. - Verdünnungseffekte durch Infusionen (ohne Kalium!) usw. - Hohe Leukozytenzahl: Leukozyten nehmen in vitro Kalium aus dem Plasma auf. - Volumenverdränkungseffekt bei der Messung von lipid- und proteinreichen Proben fehlendes Lösungsvolumen für Kalium. Falsch tiefe Konzentration, da nur Ionen gemessen werden. FOLGEN EINER HYPOKALIÄMIE: Muskelschwäche und Lähmungen, in sehr schweren Fällen mit Versagen der Atmung Tachykardie (Beschleunigung der Herzfrequenz), Extrasystolen Gefahr eines systolischen Herzstillstands (in der Auswurfphase) Hyperkaliämie = Plasmakalium > 5 mmol/l URSACHEN: Hämolyse: In vivo (z. B. bei Verbrennungen oder künstlichen Herzklappen) Gabe von Blutkonserven: Das Plasma von Blutkonserven ist durch andauernde langsame Hämolyse der Blutzellen kaliumreich. Kaliumsubstitution: Übermässige Zufuhr von kaliumreicher Infusion. medi, Bildungsgang medizinisches Labor 13 P. Hirschi
14 Verletzungen/postoperativer Zustand: Freisetzung von Kalium aus traumatisiertem (verletztem) Gewebe. Azidose: Bei Säuerung des Blutes verdrängen die einströmenden Protonen (H + -Ionen) zelluläres Kalium, z. B. bei Ketoazidose nach Hyperglykämien. Gabe von kaliumsparenden Diuretika: Fördern die Ausscheidungsfunktion der Nieren. Wenn kaliumsparende Diuretika in zu hohen Dosen eingesetzt werden, führt dies zur vermehrten Wasserausscheidung ohne entsprechende Kaliumausscheidung. Niereninsuffizienz: Abnahme der Kaliumausscheidung als Folge. Aldosteronmangel: Bei NNR-Insuffizienz (Addison Syndrom) kommt es zum Natriumverlust und darum zu einer erhöhten Kaliumretention (zur Erinnerung: Kalium wird im Austausch gegen Natrium rückresorbiert). Fehler bei der Blutentnahme: Pumpen mit der Faust, lange Stauung falsch Kaliumkonzentration. Thrombozyten: TC sind sehr zerstörungsempfindlich und reich an Kalium, dieses wird bei der Gerinnung (Serum höhere Kaliumkonzentration als Plasma) und beim Auflösen der TC in vitro frei. Hohe (lysierende) Leukozytenzahl: Kalium kann bei der Lyse aus den Zellen in vitro freigesetzt werden FOLGEN DER HYPERKALIÄMIE Über 5.5 mmol/l - Bradykardie (Verlangsamung des Herzschlages), Veränderung des EKGs, Asystolie Über 8 mmol/l herabgesetzte kardiale Erregbarkeit Über 9 mmol/l Kammerflimmern, Gefahr eines diastolischen Herzstillstands (Füllphase der Herztätigkeit). ANALYTIK Blutentnahme: - Keine langen Stauungen, kein Pumpen Kaliumkonzentration. - Wird anstelle Plasma Serum verwendet, so ist daran zu denken, dass bei der Gerinnung Kalium aus dem TC freigesetzt wird. Dieser Effekt ist bei einer Thrombozytose besonders ausgeprägt. - Bei starkem Abkühlen von Vollblut kann Kalium aus den BZ freigesetzt werden daher rasche Abtrennung des Plasma/Serum und Aufbewahrung bei RT. - Hämolyse bei der BE führt zur Erhöhung der Kaliumkonzentration. Messung: Kalium sollte aus obigen Gründen innerhalb ½ - 1 Stunde bestimmt werden mittels: Ionensensitive Elektroden (ISE): Direkte und indirekte Potentiometrie Flammenemissionsphotometrie Bestimmungsindikation: Infusionstherapie Schock und Herz-Kreislaufinsuffizienz Diuretikatherapie und/oder Niereninsuffizienz Durchfälle und/oder Missbrauch von Abführmitteln Störungen im Säure-Basenstatus medi, Bildungsgang medizinisches Labor 14 P. Hirschi
15 Referenzwerte: Im Plasma: mmol/l Alarmwerte: < 3 und > 5 mmol/l Klinische Chemie Theorie 5. BEDEUTUNG UND REGULATION DES CALCIUMS Bedeutung: Calcium ist ein Kation und zählt chemisch zu den Erdalkalimetallen. Es ist wichtig für: Den Knochenstoffwechsel, die Zähne Neuromuskuläre Erregungsvorgänge: Steuerung von Nerven und Muskeln Kontraktion der Muskeln Den Herzrhythmus Stoffwechselvorgänge in den Zellen, z. B. Enzymaktivitäten Die Blutgerinnung. Stoffwechsel und Verteilung Die tägliche Calciumaufnahme beträgt mmol ( g), vorwiegend aus Milch und Milchprodukten, Getreideprodukten und Leitungswasser. Täglich sollten wir etwa 800 mg aufnehmen, dies entspricht etwa ¾ L Milch oder 70 Gramm Emmentaler. Ein Drittel davon wird im Jejunum (Dünndarm) absorbiert, der Rest mit den Faeces ausgeschieden. Im Urin werden täglich etwa 5 mmol ausgeschieden. Calcium wird glomerulär filtriert und ein Grossteil davon wieder tubulär rückresorbiert. Bei 70 kg Körpergewicht beträgt der Calcium-Bestand etwa 25 mol (1 kg), davon sind 100 mmol rasch austauschbar. Verteilung: 99% in den Knochen (extrazellulär als kristalliner Hydroxylapatit) und Zähnen 1 % in EZR und IZR Die Calciumfraktion im Plasma von ca. 2.5 mmol/l verteilt sich folgendermassen: - 40% an Proteine gebunden (vorwiegend an Albumin), dieses Calcium wird z. B. zu den Knochen und Zähnen transportiert - 10 % komplexgebunden, d.h. an andere Substanzen gebunden (Phosphat, Citrat, Lactat, Bicarbonat) - 50% ionisiertes (Ca 2+ ) Calcium nur dieses wird als biologisch aktiv betrachtet, ist also beteiligt an der Aktivierung von Enzymen, der Gerinnung, der neuromuskulären Erregbarkeit und anderen Stoffwechseltätigkeiten. Die Ca 2+ -Konzentration unterliegt der Kontrolle durch die Calciumhormone Calcitriol, Parathormon und Cacitonin. Die Bindung von Calcium an Proteine ist ph-abhängig. Alkalose begünstigt die Bindung, da durch den alkalischen ph-wert mehr negative Bindungsstellen für Calcium frei werden, dies führt zur Abnahme des ionisierten Calciums (Ca 2+ ). Azidose hemmt die Proteinbindung und führt zur Zunahme von Ca 2+. medi, Bildungsgang medizinisches Labor 15 P. Hirschi
16 REGULATION DES PLASMACALCIUMSPIEGELS Der Plasmaspiegel wird durch 3 Hormone beeinflusst: Calcitriol: Plasmacalcium Parathormon: Plasmacalcium Calcitonin: Plasmacalcium CALCITRIOL (Vitamin-D-Hormon) Erhöht den Calciumspiegel im Plasma durch: Förderung der Calciumaufnahme aus der Nahrung im Darm Verminderung der Calciumausscheidung im Urin. Es ist notwendig um starke Knochen zu bilden. Calcitriol entsteht aus Cholecalciferol aus der Nahrung (Fisch, Pilze, Spinat) oder aus endogenem Cholesterin das zuerst in der Haut umgewandelt werden muss (photochemisch durch Sonnenlicht katalysiert). Cholecalciferol wird in der Leber und anschliessend in der Niere in das aktive Vitamin-D- Hormon Calcitriol überführt. Ein Mangel kann durch fehlende Sonnenbestrahlung, Leber- und Niereninsuffizienz entstehen und führt im Kindesalter zu Rachitis und bei Erwachsenen zu Osteomalazie. Dem kann man durch Vitamin-D- Tabletten vorbeugen. Abb. 5: Das Vitamin-D-Hormons Calcitriol PARATHORMON PTH: Erhöht den Calciumspiegel im Plasma durch: Steigerung der Reabsorption von Ca 2+ im distalen Tubulus Mobilisierung von Calcium aus den Knochen Stimulierung der renalen Calcitriolbildung (siehe oben) Die PTH-Sekretion aus den Zellen der Nebenschilddrüsen wird vermittelt über einen calciumsensitiven Rezeptor, der auf die extrazelluläre Konzentration des ionisierten Calciums anspricht. Das Parathormon senkt ausserdem den Phosphatspiegel im Plasma, durch Reabsorption von Calcium in der Niere wird im Gegenzug Phosphat ausgeschieden. Abb. 6: Hinter der Schilddrüse befinden sich die 4 kleinen Nebenschilddrüsen (Epithelkörperchen) medi, Bildungsgang medizinisches Labor 16 P. Hirschi
17 CALCITONIN: Senkt den Calciumspiegel im Plasma durch: Hemmung der Osteoklastentätigkeit (Hemmung des Knochenabbaus und damit der Calciumfreisetzung) Hemmung der tubulären Reabsorption von Calcium. Die Wirkung des Calcitonins liegt in der vermehrten Ablagerung von Calcium in den Knochen. Calcitonin wird in den C-Zellen der Schilddrüse gebildet, seine physiologische Relevanz ist weitaus geringer als die der beiden oben genannten Hormone. Abb. 7: C-Zellen der Schilddrüse Hypocalcämie = Plasmacalcium < 2.2 mmol/l URSACHEN: Längerdauernde Verdauungsstörungen, z. B. bei chronisch entzündlichen Darmerkrankungen (Morbus Crohn, Colitis ulcerosa), Zoeliakie.. Hier ist die Aufnahme von Vorstufen des Vitamin D gestört oder die Ca-Aufnahme selbst. Vitamin-D-Mangel / bzw. ein Vit-D-Hormonmangel: Zuwenig Vitamin D- Hormon-Vorstufen in der Nahrung; Sonnenlichtmangel; Leber und Nierenschaden (hier werden Vit-D-Vorstufen nicht in Calcitriol umgewandelt). Parathormonwirkung vermindert / Unterfunktion der N-Schilddrüse = Hypoparathyreodismus: Kommt vor, wenn die Nebenschilddrüsen entfernt wurden (unabsichtlich bei einer Schilddrüsen-OP), bei PTH-Rezeptordefekt (Parathormon wirkt nicht) und bei Autoimmunerkrankungen mit AK gegen die Nebenschilddrüse. Nierenerkrankungen: Bei bestimmten Nierenschäden wird zuviel Calcium ausgeschieden. Knochenbildende Tumore: Gewisse Tumore bauen Knochensubstanz auf und verbrauchen somit Calcium. Erniedrigung des Gesamt-Calciums kommt bei Hypoproteinämien vor. Der Anteil des an Albumin gebundenen Calciums nimmt ab, das biologisch wirksame ionisierte Calcium (Ca 2+ ) ist aber normal, es wird weniger Ca. resorbiert und mobilisiert bei fehlendem Albumin als Transporter. FOLGEN EINER HYPOCALCÄMIE: Neurologisch: Tetanische Krämpfe, Übererregbarkeit Nerven u. Muskeln Kardial: EKG-Veränderungen (QT-Verlängerung) Störungen der Knochenmineralisation Trübung der Augenlinse = Cataract (grauer Star) Hypercalcämie = Plasmacalcium >2.6 mmol/l URSACHEN: Tumorerkrankungen: Bei Knochen-zersetzendem Tumorwachstum Überfunktion der Nebenschilddrüse = primärer Hyperparathyreodismus Bettlägrigkeit oder mangelnde Bewegung: führt zu Knochenabbau Calcium wird frei medi, Bildungsgang medizinisches Labor 17 P. Hirschi
18 Vitamin D-Überdosierung FOLGEN EINER HYPERCALCÄMIE: Calcium > 4 mmol/l führt zu Herzrythmusstörungen und Koma Werte sofort weitergeben. Neurologisch: Psychosen, Somnolenz (Schläfrigkeit), Koma Kardiovaskulär: Hypertonie, EKG-Veränderung (QT-Verkürzung) Gastrointestinal: Übelkeit, Erbrechen, Pankreatitis Renal: Polyurie, Urolithiasis (Harnsteine), Verkalkung der Niere durch Ca-Ablagerungen Niereninsuffizienz. Allgemeine Calcifikationen an den inneren Organen, Gefässwänden und der Hornhaut. ANALYTIK Probenmaterial: Gesamtcalcium: Heparinplasma kein EDTA-Plasma (komplexiert Ca-Ionen)!! Ionisiertes Calcium (Ca 2+ ): Anaerob behandeltes Heparinblut, z. B. Blutgasspritzen Messung: Gesamtcalcium: Atomabsorption (heute eher selten, da aufwändig) Flammenphotometrie (selten) Photometrische Farbtests (häufigste Methode) Ionisiertes Calcium: Calciumelektrode Bestimmungsindikationen: Störungen der PTH-Synthese in der Nebenschilddrüse Vitamin-D-Mangel oder Überdosierung Nierensteinerkrankungen Entfernung (unabsichtliche) der Epithelkörperchen (Nebenschilddrüsen) Krampfleiden Tumorerkrankungen Referenzwerte: Gesamtcalcium Serum/Plasma: mmol/l Ionisiertes Calcium: mmol/l medi, Bildungsgang medizinisches Labor 18 P. Hirschi
19 6. VERFAHREN ZUR MESSUNG VON ELEKTROLYTEN 6.1. Flammenemissionsfotometrie (s. auch Physik) Alkali- und Erdalkalimetalle (Natrium, Kalium, Calcium, Lithium). Prinzip: Metallionen im Probenmaterial werden in einer Flamme verdampft und dadurch zurückverwandelt in Atome. Anschliessend werden sie durch thermische Energie (Propan/Acetylen-Pressluftflamme C) in einen angeregten Zustand versetzt. Dabei emittieren diese Atome beim Übergang in den Grundzustand Licht einer bestimmter WL. Diese Emissionsstrahlung wird je nach WL einem Element zugeordnet und zur Konzentrationsbestimmung beim Patienten verwendet. Die FFM wird künftig mehr und mehr durch Ionenselektive Elektroden ISE ersetzt Abb. 8: Angeregtes Atom 6.2. Atomabsorptionsfotometrie (s. auch Physik) Elektrolyte, Spurenelemente, Schwermetalle Prinzip: Metallionen werden in einer Flamme verdampft und so in Atome umgewandelt. Die Einstrahlung von Emissionsstrahlung des zu bestimmenden Elements (zur Messung von Kupfer, z.b. Licht einer Kupferhohlkathoden-Lampe) wird von den Atomen absorbiert. Die Messung des abgeschwächten, axialen Lichtstrahls (Transmission) und Umrechnung in Extinktion dient zur Ermittlung der Konzentration. 6.3.Potentiometrie, Ionenselekive Elektrode ISE Potentiometrie = analytische Verfahren, die auf der Messung von Elektrodenpotentialen basieren. Ionenselektive-Elektroden-Einheiten (ISE) bestehen aus einer Messkette, diese ist wie folgt aufgebaut: Referenzelektrode Voltmeter Messelektrode medi, Bildungsgang medizinisches Labor 19 P. Hirschi
20 Das Voltmeter misst ein elektrisches Potential (Spannungsdifferenz) zwischen Referenz und Messelektrode, welches proportional der Ionenaktivität in der Messlösung ist. Die ionenselektive Membran der Messelektrode ermöglicht die potentiometrische Messung der Aktivität eines bestimmten Ions. Komplexgebundene (proteingebundene) Ionen werden nicht erfasst. Wichtig: Ionenselektive Elektroden messen nicht die Ionenkonzentration, sondern die Aktivität des betreffenden Ions. DAS ELEKTRODENPOTENTIAL Wenn ein Metallstreifen in eine Lösung seines Salzes getaucht wird, so gelangen einige Metallionen in die Flüssigkeit, wobei sie Elektronen auf dem Metallstreifen zurücklassen. Dies führt zu einer kleinen, negativen Ladung des Metallstreifens und gleichzeitig zu einer entsprechenden positiven Ladung der Salzlösung. Abb. 9: Das elektrische Potential das sich zwischen Metallstreifen und Flüssigkeit ausbildet, wird als Elektrodenpotential bezeichnet. Es ist abhängig von der Art des Metalls und der Konzentration der Salzlösung. Je mehr Zinkionen in der Salzlösung sind desto mehr werden auch auf den Zinkstreifen gelangen in obigem Beispiel. Der Metallstreifen und die Salzlösung bilden eine so genannte halbe Zelle. Verbindet man zwei halbe Zellen, die eine unterschiedliche Konzentration der Salzlösung enthalten (Plasma ist auch eine Salzlösung), über einen elektrischen Leiter (z.b. eine Salzbrücke) miteinander, so kann die Potentialdifferenz (= Potential der Halbzelle 1 verglichen mit dem Potential der Zelle 2) mit einem empfindlichen Voltmeter gemessen werden. Abb.10: Halbzelle 1 Halbzelle 2 Elektroden funktionieren nach diesem Prinzip. medi, Bildungsgang medizinisches Labor 20 P. Hirschi
Sie können während der PPT bereits am Auftrag arbeiten.
 Sie können während der PPT bereits am Auftrag arbeiten. FLÜSSIGKEITSR SSIGKEITSRÄUME, KOMPARTIMENTE Wassergehalt: 50 70% des Körpergewichtes. davon (2 % transzellulär) Ungleichverteilung von Na + und K
Sie können während der PPT bereits am Auftrag arbeiten. FLÜSSIGKEITSR SSIGKEITSRÄUME, KOMPARTIMENTE Wassergehalt: 50 70% des Körpergewichtes. davon (2 % transzellulär) Ungleichverteilung von Na + und K
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Klinische Chemie und Hämatologie Vorlesung: Wasser- & Elektrolythaushalt
 Klinische Chemie und Hämatologie Vorlesung: Wasser- & Elektrolythaushalt Prof. Dr. med. Michael Walter Institut für Klinische Chemie und Laboratoriumsmedizin/Zentrallaboratorium Westfälische Wilhelms-Universität
Klinische Chemie und Hämatologie Vorlesung: Wasser- & Elektrolythaushalt Prof. Dr. med. Michael Walter Institut für Klinische Chemie und Laboratoriumsmedizin/Zentrallaboratorium Westfälische Wilhelms-Universität
Behandlung von Diabetes
 04 Arbeitsanweisung Arbeitsauftrag Anhand des Foliensatzes werden die verschiedenen Behandlungsmethoden bei Diabetes Typ 1 und Typ 2 besprochen. Anschliessend werden noch kurz die Folgen bei einer Nichtbehandlung
04 Arbeitsanweisung Arbeitsauftrag Anhand des Foliensatzes werden die verschiedenen Behandlungsmethoden bei Diabetes Typ 1 und Typ 2 besprochen. Anschliessend werden noch kurz die Folgen bei einer Nichtbehandlung
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Gefährlich hohe Blutzuckerwerte
 Gefährlich hohe Blutzuckerwerte In besonderen Situationen kann der Blutzuckerspiegel gefährlich ansteigen Wenn in Ausnahmefällen der Blutzuckerspiegel sehr hoch ansteigt, dann kann das für Sie gefährlich
Gefährlich hohe Blutzuckerwerte In besonderen Situationen kann der Blutzuckerspiegel gefährlich ansteigen Wenn in Ausnahmefällen der Blutzuckerspiegel sehr hoch ansteigt, dann kann das für Sie gefährlich
1.6 ph-werte. Einführung Chemie Seite 19
 Seite 19 1.6 ph-werte Säuren und Basen werden stets als Lösungen in verschiedenen Konzentrationen gebraucht. Die Stärke einer Säure wird durch ihren ph Wert festgelegt, während die Stärke einer Base durch
Seite 19 1.6 ph-werte Säuren und Basen werden stets als Lösungen in verschiedenen Konzentrationen gebraucht. Die Stärke einer Säure wird durch ihren ph Wert festgelegt, während die Stärke einer Base durch
Kapitel 13: Laugen und Neutralisation
 Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010
 1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
Klinische Chemie und Laboratoriumsdiagnostik. Teil 9. Wasser- und Elektrolythaushalt
 Klinische Chemie und Laboratoriumsdiagnostik Teil 9 Wasser- und Elektrolythaushalt Prof. Dr. Ralf Lichtinghagen Medizinische Hochschule Hannover Klinische Chemie Tel.: 0511-5323940 Elektrolytverteilung
Klinische Chemie und Laboratoriumsdiagnostik Teil 9 Wasser- und Elektrolythaushalt Prof. Dr. Ralf Lichtinghagen Medizinische Hochschule Hannover Klinische Chemie Tel.: 0511-5323940 Elektrolytverteilung
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren
 Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Bei einer Zunahme des Natriums besteht ja eine Hypernatriämie und damit zu eine Erhöhung der Osmolalität.
 Elektrolythaushalt Natrium Natrium und Wasserhaushalt: Da Störungen des Wasser- oder Natriumhaushaltes praktisch nie isoliert auftreten und sich zudem über den osmotischen Druck und die Regelmechanismen
Elektrolythaushalt Natrium Natrium und Wasserhaushalt: Da Störungen des Wasser- oder Natriumhaushaltes praktisch nie isoliert auftreten und sich zudem über den osmotischen Druck und die Regelmechanismen
Geschichte. 1807/08 Herstellung von elementarem Natrium durch Humphry Davy
 NATRIUM Geschichte 1807/08 Herstellung von elementarem Natrium durch Humphry Davy 1930 erkannte St. John die Essentialität (Lebensnotwendigkeit) des Natriums für normales Wachstum Clark erkannte die Bedeutung
NATRIUM Geschichte 1807/08 Herstellung von elementarem Natrium durch Humphry Davy 1930 erkannte St. John die Essentialität (Lebensnotwendigkeit) des Natriums für normales Wachstum Clark erkannte die Bedeutung
2. Zusammensetzung des Körpers nach ausgewählten Elementen : Element Gew.-% ca. Masse ca.
 1 Teil C: Tabellen und Richtwerte (Körperzusammensetzung u. Energiehaushalt) Physiologie Cluster B4 Vegetative Regulation II 1. Elektolytkonzentrationen in den Flüssigkeitsräumen des Körpers ( aus Schmidt,Thews,Lang
1 Teil C: Tabellen und Richtwerte (Körperzusammensetzung u. Energiehaushalt) Physiologie Cluster B4 Vegetative Regulation II 1. Elektolytkonzentrationen in den Flüssigkeitsräumen des Körpers ( aus Schmidt,Thews,Lang
Geschichte. 1807/08 Herstellung von elementarem Natrium durch Humphry Davy
 NATRIUM Geschichte 1807/08 Herstellung von elementarem Natrium durch Humphry Davy 1930 erkannte St. John die Essentialität (Lebensnotwendigkeit) des Natriums für normales Wachstum Clark erkannte die Bedeutung
NATRIUM Geschichte 1807/08 Herstellung von elementarem Natrium durch Humphry Davy 1930 erkannte St. John die Essentialität (Lebensnotwendigkeit) des Natriums für normales Wachstum Clark erkannte die Bedeutung
Wie oft soll ich essen?
 Wie oft soll ich essen? Wie sollen Sie sich als Diabetiker am besten ernähren? Gesunde Ernährung für Menschen mit Diabetes unterscheidet sich nicht von gesunder Ernährung für andere Menschen. Es gibt nichts,
Wie oft soll ich essen? Wie sollen Sie sich als Diabetiker am besten ernähren? Gesunde Ernährung für Menschen mit Diabetes unterscheidet sich nicht von gesunder Ernährung für andere Menschen. Es gibt nichts,
Diabetes mellitus : Folgeschäden
 Diabetes mellitus : Folgeschäden Warum ist der Diabetes mellitus eine wichtige Erkrankung? a. Akute Probleme: Hypoglykämie Hyperglykämie Ketoazidose b. Chronische Probleme: Folgeschäden: Typische Schäden:
Diabetes mellitus : Folgeschäden Warum ist der Diabetes mellitus eine wichtige Erkrankung? a. Akute Probleme: Hypoglykämie Hyperglykämie Ketoazidose b. Chronische Probleme: Folgeschäden: Typische Schäden:
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
Oxidation und Reduktion Redoxreaktionen Blatt 1/5
 Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
WICHTIG Der normale Blutzuckerspiegel liegt zwischen 70 und 100 mg/100 ml Blut.
 Leberzellen herabgesetzt wird. Auf Dauer stumpfen diese ab die Basis für die Insulinresistenz wird gelegt. Zugleich gibt es Hinweise, dass ein Überangebot von Entzündungsmediatoren im Blut sogar den völligen
Leberzellen herabgesetzt wird. Auf Dauer stumpfen diese ab die Basis für die Insulinresistenz wird gelegt. Zugleich gibt es Hinweise, dass ein Überangebot von Entzündungsmediatoren im Blut sogar den völligen
Normalwerte: 1-3% < 1%: Verminderung des effektiv zirkulierenden Volumen (prärenales ANV) >3%: renaler Natriumverlust (z.b. akuter Tubulusschaden)
 Erklärungen Formel 1: Fraktionelle Natriumexkretion (%) Fe (Natrium) = (Natrium (Harn) *Kreatinin (Serum) )/((Natrium (Blut) *Kreatinin (Serum) )*100 Normalwerte: 1-3% < 1%: Verminderung des effektiv zirkulierenden
Erklärungen Formel 1: Fraktionelle Natriumexkretion (%) Fe (Natrium) = (Natrium (Harn) *Kreatinin (Serum) )/((Natrium (Blut) *Kreatinin (Serum) )*100 Normalwerte: 1-3% < 1%: Verminderung des effektiv zirkulierenden
Kapiteltest 1.1. Kapiteltest 1.2
 Kapiteltest 1.1 a) Perchlorsäure hat die Formel HClO 4. Was geschieht bei der Reaktion von Perchlorsäure mit Wasser? Geben Sie zuerst die Antwort in einem Satz. Dann notieren Sie die Reaktionsgleichung.
Kapiteltest 1.1 a) Perchlorsäure hat die Formel HClO 4. Was geschieht bei der Reaktion von Perchlorsäure mit Wasser? Geben Sie zuerst die Antwort in einem Satz. Dann notieren Sie die Reaktionsgleichung.
Selbst-Test zur Vorab-Einschätzung zum Vorkurs Chemie für Mediziner
 Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
Parotis Pankreas. Dünndarm Bürstensaum. Amylose Amylopektin Glykogen. Maltose. Glucose. Isomaltose. Saccharose. Fructose. Lactose. Galaktose.
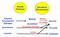 Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Mineralstoffe Arbeitsblatt
 Lehrerinformation 1/6 Arbeitsauftrag Ziel Material Die Sch lesen den Informationstext und recherchieren eigenständig Informationen zu einem Mineralstoff. Sie erstellen einen Steckbrief und ein inkl. Lösung.
Lehrerinformation 1/6 Arbeitsauftrag Ziel Material Die Sch lesen den Informationstext und recherchieren eigenständig Informationen zu einem Mineralstoff. Sie erstellen einen Steckbrief und ein inkl. Lösung.
Das Nahrungsmittel Ei Lehrerinformation
 Lehrerinformation 1/7 Arbeitsauftrag Die Sch erhalten eine umfassende Betrachtung der Inhaltsstoffe inkl. intensiver Befassung mit der Nahrungsmittelpyramide und der Wichtigkeit des Eis in diesem Zusammenhang.
Lehrerinformation 1/7 Arbeitsauftrag Die Sch erhalten eine umfassende Betrachtung der Inhaltsstoffe inkl. intensiver Befassung mit der Nahrungsmittelpyramide und der Wichtigkeit des Eis in diesem Zusammenhang.
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Wortschema Reaktionsschema Beispiel 1: Kupfer und Schwefel Vorzahlen
 6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
Finanzierung: Übungsserie III Innenfinanzierung
 Thema Dokumentart Finanzierung: Übungsserie III Innenfinanzierung Lösungen Theorie im Buch "Integrale Betriebswirtschaftslehre" Teil: Kapitel: D1 Finanzmanagement 2.3 Innenfinanzierung Finanzierung: Übungsserie
Thema Dokumentart Finanzierung: Übungsserie III Innenfinanzierung Lösungen Theorie im Buch "Integrale Betriebswirtschaftslehre" Teil: Kapitel: D1 Finanzmanagement 2.3 Innenfinanzierung Finanzierung: Übungsserie
Chemotherapie -ein Bilderbuch für Kinder
 Chemotherapie -ein Bilderbuch für Kinder Unser Körper besteht aus verschiedenen Zellen, die ganz unterschiedlich aussehen. Jede Art erfüllt eine besondere Aufgabe. Da gibt es zum Beispiel Gehirnzellen,
Chemotherapie -ein Bilderbuch für Kinder Unser Körper besteht aus verschiedenen Zellen, die ganz unterschiedlich aussehen. Jede Art erfüllt eine besondere Aufgabe. Da gibt es zum Beispiel Gehirnzellen,
Milch und Milchprodukte
 Tag der Apotheke 2014: Kurztexte zu acht häufigen Wechselwirkungen Rückfragen an Dr. Ursula Sellerberg, ABDA-Pressestelle, Mail: u.sellerberg@abda.aponet.de Milch und Milchprodukte 95 % 1 der Bundesbürger
Tag der Apotheke 2014: Kurztexte zu acht häufigen Wechselwirkungen Rückfragen an Dr. Ursula Sellerberg, ABDA-Pressestelle, Mail: u.sellerberg@abda.aponet.de Milch und Milchprodukte 95 % 1 der Bundesbürger
Labortests für Ihre Gesundheit. Knochen Osteoporose-Prävention 17
 Labortests für Ihre Gesundheit Knochen Osteoporose-Prävention 17 01IPF Labortests für Ihre Gesundheit Knochen Osteoporose-Prävention Per Blut- und Urintests Risiko frühzeitig erkennen Die Osteoporose ist
Labortests für Ihre Gesundheit Knochen Osteoporose-Prävention 17 01IPF Labortests für Ihre Gesundheit Knochen Osteoporose-Prävention Per Blut- und Urintests Risiko frühzeitig erkennen Die Osteoporose ist
APP-GFP/Fluoreszenzmikroskop. Aufnahmen neuronaler Zellen, mit freund. Genehmigung von Prof. Stefan Kins, TU Kaiserslautern
 Über die Herkunft von Aβ42 und Amyloid-Plaques Heute ist sicher belegt, dass sich die amyloiden Plaques aus einer Vielzahl an Abbaufragmenten des Amyloid-Vorläufer-Proteins (amyloid-precursor-protein,
Über die Herkunft von Aβ42 und Amyloid-Plaques Heute ist sicher belegt, dass sich die amyloiden Plaques aus einer Vielzahl an Abbaufragmenten des Amyloid-Vorläufer-Proteins (amyloid-precursor-protein,
Regulation des Kalium- Calcium- und Phosphathaushalts
 Regulation des Kalium- Calcium- und Phosphathaushalts Lernziele: 80, 81 Dr. Attila Nagy 2019 1 Normalwerte K + -Aufnahme/Ausscheidung: 50-100 mmol/tag Ca 2+ -Aufnahme/Absorption: 1000/200 mg/tag; auch
Regulation des Kalium- Calcium- und Phosphathaushalts Lernziele: 80, 81 Dr. Attila Nagy 2019 1 Normalwerte K + -Aufnahme/Ausscheidung: 50-100 mmol/tag Ca 2+ -Aufnahme/Absorption: 1000/200 mg/tag; auch
Regulation des K + - Calcium- und Phosphathaushalts. Lernziele: 80, 81. Dr. Attila Nagy
 Regulation des K + - Calcium- und Phosphathaushalts Lernziele: 80, 81 Dr. Attila Nagy 2018 Normalwerte K + -Aufnahme/Ausscheidung: 50-100 mmol/tag Ca 2+ -Aufnahme/Absorption: 1000/200 mg/tag; auch 25/5
Regulation des K + - Calcium- und Phosphathaushalts Lernziele: 80, 81 Dr. Attila Nagy 2018 Normalwerte K + -Aufnahme/Ausscheidung: 50-100 mmol/tag Ca 2+ -Aufnahme/Absorption: 1000/200 mg/tag; auch 25/5
ph Werte im Organismus Alle im Organismus gebildeten Flüssigkeiten haben einen bestimmten ph-wert. Am wichtigsten ist der ph - Wert des Blutes.
 Jede Sekunde finden im menschlichen Körper Millionen von chemischen Prozessen statt: Stoffe werden aufgenommen, aufgebaut, umgebaut, abgebaut und ausgeschieden. Bei diesen hochkomplexen Abläufen spielen
Jede Sekunde finden im menschlichen Körper Millionen von chemischen Prozessen statt: Stoffe werden aufgenommen, aufgebaut, umgebaut, abgebaut und ausgeschieden. Bei diesen hochkomplexen Abläufen spielen
!!! Folgeerkrankungen
 Ein zu hoher Blutzuckerspiegel kann Folgen auf Ihr Herzkreislaufsystem haben und zu Erkrankungen wie der Schaufensterkrankheit, einer Angina pectoris, einem Herzinfarkt oder einem Schlaganfall führen.
Ein zu hoher Blutzuckerspiegel kann Folgen auf Ihr Herzkreislaufsystem haben und zu Erkrankungen wie der Schaufensterkrankheit, einer Angina pectoris, einem Herzinfarkt oder einem Schlaganfall führen.
Thermodynamik. Basics. Dietmar Pflumm: KSR/MSE. April 2008
 Thermodynamik Basics Dietmar Pflumm: KSR/MSE Thermodynamik Definition Die Thermodynamik... ist eine allgemeine Energielehre als Teilgebiet der Chemie befasst sie sich mit den Gesetzmässigkeiten der Umwandlungsvorgänge
Thermodynamik Basics Dietmar Pflumm: KSR/MSE Thermodynamik Definition Die Thermodynamik... ist eine allgemeine Energielehre als Teilgebiet der Chemie befasst sie sich mit den Gesetzmässigkeiten der Umwandlungsvorgänge
Chemie Zusammenfassung KA 2
 Chemie Zusammenfassung KA 2 Wärmemenge Q bei einer Reaktion Chemische Reaktionen haben eine Gemeinsamkeit: Bei der Reaktion wird entweder Energie/Wärme frei (exotherm). Oder es wird Wärme/Energie aufgenommen
Chemie Zusammenfassung KA 2 Wärmemenge Q bei einer Reaktion Chemische Reaktionen haben eine Gemeinsamkeit: Bei der Reaktion wird entweder Energie/Wärme frei (exotherm). Oder es wird Wärme/Energie aufgenommen
geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Gehen wir einmal davon aus, dass die von uns angenommenen
 geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Vollständigkeit halber aufgeführt. Gehen wir einmal davon aus, dass die von uns angenommenen 70% im Beispiel exakt berechnet sind. Was würde
geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Vollständigkeit halber aufgeführt. Gehen wir einmal davon aus, dass die von uns angenommenen 70% im Beispiel exakt berechnet sind. Was würde
Hepar-SL. Für ein ausgeglichenes Leben auch ohne Gallenblase
 Hepar-SL Für ein ausgeglichenes Leben auch ohne Gallenblase Ein Leben ohne Gallenblase betrifft immer mehr Menschen. Auch Ihre Gallenblase wurde operativ entfernt, da Sie möglicherweise unter immer wieder
Hepar-SL Für ein ausgeglichenes Leben auch ohne Gallenblase Ein Leben ohne Gallenblase betrifft immer mehr Menschen. Auch Ihre Gallenblase wurde operativ entfernt, da Sie möglicherweise unter immer wieder
24-STUNDEN-SAMMELURIN
 Blutfarbstoffs (Hämoglobin), wird normalerweise nicht mit dem Urin ausgeschieden. Erst bei einer erhöhten Konzentration im Blutserum enthält auch der Urin Bilirubin dies ist der Fall, wenn eine Funktionsstörung
Blutfarbstoffs (Hämoglobin), wird normalerweise nicht mit dem Urin ausgeschieden. Erst bei einer erhöhten Konzentration im Blutserum enthält auch der Urin Bilirubin dies ist der Fall, wenn eine Funktionsstörung
Allgemeine Pathologie. Störungen im Kupfer- Stoffwechsel
 Allgemeine Pathologie Störungen im Kupfer- Stoffwechsel Physiologie (1): - das Übergangsmetall Kupfer ist als essentielles Spurenelement Bestandteil einer Reihe wichtiger Enzyme: - Ferro-oxidase I (Coeruloplasmin),
Allgemeine Pathologie Störungen im Kupfer- Stoffwechsel Physiologie (1): - das Übergangsmetall Kupfer ist als essentielles Spurenelement Bestandteil einer Reihe wichtiger Enzyme: - Ferro-oxidase I (Coeruloplasmin),
Foliensatz; Arbeitsblatt; Internet. Je nach chemischem Wissen können die Proteine noch detaillierter besprochen werden.
 03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
Bewertung des Blattes
 Bewertung des Blattes Es besteht immer die Schwierigkeit, sein Blatt richtig einzuschätzen. Im folgenden werden einige Anhaltspunkte gegeben. Man unterscheidet: Figurenpunkte Verteilungspunkte Längenpunkte
Bewertung des Blattes Es besteht immer die Schwierigkeit, sein Blatt richtig einzuschätzen. Im folgenden werden einige Anhaltspunkte gegeben. Man unterscheidet: Figurenpunkte Verteilungspunkte Längenpunkte
Professionelle Seminare im Bereich MS-Office
 Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Thermodynamik Wärmeempfindung
 Folie 1/17 Warum fühlt sich 4 warmes wesentlich heißer an als warme? Und weshalb empfinden wir kühles wiederum kälter als kühle? 7 6 5 4 2 - -2 32 32 Folie 2/17 Wir Menschen besitzen kein Sinnesorgan für
Folie 1/17 Warum fühlt sich 4 warmes wesentlich heißer an als warme? Und weshalb empfinden wir kühles wiederum kälter als kühle? 7 6 5 4 2 - -2 32 32 Folie 2/17 Wir Menschen besitzen kein Sinnesorgan für
Säure-Base Titrationen. (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen)
 Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2
 Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2 1. Wie viel mol Eisen sind in 12 x 10 23 Molekülen enthalten? ca. 2 Mol 2. Welches Volumen Litern ergibt sich wenn ich 3 mol
Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2 1. Wie viel mol Eisen sind in 12 x 10 23 Molekülen enthalten? ca. 2 Mol 2. Welches Volumen Litern ergibt sich wenn ich 3 mol
Protokoll des Versuches 7: Umwandlung von elektrischer Energie in Wärmeenergie
 Name: Matrikelnummer: Bachelor Biowissenschaften E-Mail: Physikalisches Anfängerpraktikum II Dozenten: Assistenten: Protokoll des Versuches 7: Umwandlung von elektrischer Energie in ärmeenergie Verantwortlicher
Name: Matrikelnummer: Bachelor Biowissenschaften E-Mail: Physikalisches Anfängerpraktikum II Dozenten: Assistenten: Protokoll des Versuches 7: Umwandlung von elektrischer Energie in ärmeenergie Verantwortlicher
Berechnung der Erhöhung der Durchschnittsprämien
 Wolfram Fischer Berechnung der Erhöhung der Durchschnittsprämien Oktober 2004 1 Zusammenfassung Zur Berechnung der Durchschnittsprämien wird das gesamte gemeldete Prämienvolumen Zusammenfassung durch die
Wolfram Fischer Berechnung der Erhöhung der Durchschnittsprämien Oktober 2004 1 Zusammenfassung Zur Berechnung der Durchschnittsprämien wird das gesamte gemeldete Prämienvolumen Zusammenfassung durch die
Name: Klasse: Datum:
 Arbeitsblatt 10.1 Versuch 1: Man füllt eine mittelgroße Glasschale mit Wasser und legt vorsichtig eine Büroklammer auf die Oberfläche des Wassers. Anschließend gibt man mit einer Pipette am Rand der Glasschale
Arbeitsblatt 10.1 Versuch 1: Man füllt eine mittelgroße Glasschale mit Wasser und legt vorsichtig eine Büroklammer auf die Oberfläche des Wassers. Anschließend gibt man mit einer Pipette am Rand der Glasschale
3.4. Leitungsmechanismen
 a) Metalle 3.4. Leitungsmechanismen - Metall besteht aus positiv geladenen Metallionen und frei beweglichen Leitungselektronen (freie Elektronengas), Bsp.: Cu 2+ + 2e - - elektrische Leitung durch freie
a) Metalle 3.4. Leitungsmechanismen - Metall besteht aus positiv geladenen Metallionen und frei beweglichen Leitungselektronen (freie Elektronengas), Bsp.: Cu 2+ + 2e - - elektrische Leitung durch freie
Schließen Sie gezielt Vitaminlücken bei Epilepsie.
 Schließen Sie gezielt Vitaminlücken bei Epilepsie. Weitere Fragen zum Thema Vitaminlücken bei Epilepsie beantworten wir Ihnen gerne: Desitin Arzneimittel GmbH Abteilung Medizin Weg beim Jäger 214 22335
Schließen Sie gezielt Vitaminlücken bei Epilepsie. Weitere Fragen zum Thema Vitaminlücken bei Epilepsie beantworten wir Ihnen gerne: Desitin Arzneimittel GmbH Abteilung Medizin Weg beim Jäger 214 22335
Reaktionsgleichungen verstehen anhand der Verbrennung von Magnesium
 Reaktionsgleichungen verstehen anhand der Verbrennung von Magnesium Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Sprachliche Kompetenzen Zeitbedarf Material- & Medienbedarf
Reaktionsgleichungen verstehen anhand der Verbrennung von Magnesium Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Sprachliche Kompetenzen Zeitbedarf Material- & Medienbedarf
Nährstoffe Lehrerinformation
 Lehrerinformation 1/6 Arbeitsauftrag Die LP gibt den Sch den Auftrag, einen Kreis zu zeichnen. Aus diesem sollen sie ein Kreisdiagramm erstellen, indem sie die prozentualen Anteile der Wasser, Fett, Eiweiss,
Lehrerinformation 1/6 Arbeitsauftrag Die LP gibt den Sch den Auftrag, einen Kreis zu zeichnen. Aus diesem sollen sie ein Kreisdiagramm erstellen, indem sie die prozentualen Anteile der Wasser, Fett, Eiweiss,
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6
 Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
Übung 5 : G = Wärmeflussdichte [Watt/m 2 ] c = spezifische Wärmekapazität k = Wärmeleitfähigkeit = *p*c = Wärmediffusität
![Übung 5 : G = Wärmeflussdichte [Watt/m 2 ] c = spezifische Wärmekapazität k = Wärmeleitfähigkeit = *p*c = Wärmediffusität Übung 5 : G = Wärmeflussdichte [Watt/m 2 ] c = spezifische Wärmekapazität k = Wärmeleitfähigkeit = *p*c = Wärmediffusität](/thumbs/26/9283097.jpg) Übung 5 : Theorie : In einem Boden finden immer Temperaturausgleichsprozesse statt. Der Wärmestrom läßt sich in eine vertikale und horizontale Komponente einteilen. Wir betrachten hier den Wärmestrom in
Übung 5 : Theorie : In einem Boden finden immer Temperaturausgleichsprozesse statt. Der Wärmestrom läßt sich in eine vertikale und horizontale Komponente einteilen. Wir betrachten hier den Wärmestrom in
1. Theorie: Kondensator:
 1. Theorie: Aufgabe des heutigen Versuchstages war es, die charakteristische Größe eines Kondensators (Kapazität C) und einer Spule (Induktivität L) zu bestimmen, indem man per Oszilloskop Spannung und
1. Theorie: Aufgabe des heutigen Versuchstages war es, die charakteristische Größe eines Kondensators (Kapazität C) und einer Spule (Induktivität L) zu bestimmen, indem man per Oszilloskop Spannung und
PCD Europe, Krefeld, Jan 2007. Auswertung von Haemoccult
 Auswertung von Haemoccult Ist das positiv? Nein! Ja! Im deutschen Krebsfrüherkennungsprogramm haben nur etwa 1 % der Frauen und 1,5 % der Männer ein positives Haemoccult -Ergebnis, da dieser Test eine
Auswertung von Haemoccult Ist das positiv? Nein! Ja! Im deutschen Krebsfrüherkennungsprogramm haben nur etwa 1 % der Frauen und 1,5 % der Männer ein positives Haemoccult -Ergebnis, da dieser Test eine
Osteoporose. Ein echtes Volksleiden. Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen
 Osteoporose Osteoporose 9 Osteoporose Ein echtes Volksleiden Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen in den entwickelten Ländern zu den häufigsten Erkrankungen
Osteoporose Osteoporose 9 Osteoporose Ein echtes Volksleiden Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen in den entwickelten Ländern zu den häufigsten Erkrankungen
Patienteninformation. AcrySof IQ Toric. GraueN star UND Hornhautverkrümmung
 Patienteninformation AcrySof IQ Toric GraueN star UND Hornhautverkrümmung in einem Schritt behandeln Während der Operation des Grauen Stars (Katarakt) wird die von der Katarakt betroffene körpereigene
Patienteninformation AcrySof IQ Toric GraueN star UND Hornhautverkrümmung in einem Schritt behandeln Während der Operation des Grauen Stars (Katarakt) wird die von der Katarakt betroffene körpereigene
Geschichte. Entdeckung 1808 durch Humphry Davy (zusammen mit Natrium) 1926 Entdeckung der Essenzialität für normales Wachstum
 Kalium Geschichte Entdeckung 1808 durch Humphry Davy (zusammen mit Natrium) 1926 Entdeckung der Essenzialität für normales Wachstum Chemie Ist ein Alkalimetal Erste Hauptgruppe Ordnungszahl 19 Massezahl
Kalium Geschichte Entdeckung 1808 durch Humphry Davy (zusammen mit Natrium) 1926 Entdeckung der Essenzialität für normales Wachstum Chemie Ist ein Alkalimetal Erste Hauptgruppe Ordnungszahl 19 Massezahl
Einheiten und Einheitenrechnungen
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Projekt 2HEA 2005/06 Formelzettel Elektrotechnik
 Projekt 2HEA 2005/06 Formelzettel Elektrotechnik Teilübung: Kondensator im Wechselspannunskreis Gruppenteilnehmer: Jakic, Topka Abgabedatum: 24.02.2006 Jakic, Topka Inhaltsverzeichnis 2HEA INHALTSVERZEICHNIS
Projekt 2HEA 2005/06 Formelzettel Elektrotechnik Teilübung: Kondensator im Wechselspannunskreis Gruppenteilnehmer: Jakic, Topka Abgabedatum: 24.02.2006 Jakic, Topka Inhaltsverzeichnis 2HEA INHALTSVERZEICHNIS
Membran- und Donnanpotentiale. (Zusammenfassung)
 Membranund Donnanpotentiale (Zusammenfassung) Inhaltsverzeichnis 1. Elektrochemische Membranen...Seite 2 2. Diffusionspotentiale...Seite 2 3. Donnanpotentiale...Seite 3 4. Zusammenhang der dargestellten
Membranund Donnanpotentiale (Zusammenfassung) Inhaltsverzeichnis 1. Elektrochemische Membranen...Seite 2 2. Diffusionspotentiale...Seite 2 3. Donnanpotentiale...Seite 3 4. Zusammenhang der dargestellten
Zeichen bei Zahlen entschlüsseln
 Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
Organische Chemie I Chemie am 16.11.2012. Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2
 Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
ε 0 = Normalpotential Potentiometrie
 Potentiometrie Unter dem Name Potentiometrie werden diejenige analytische Methoden zusammengefasst, die auf der Messung des Elektrodenpotentials zurückzuführen sind (siehe dazu auch Mortimer, Kapitel 21,
Potentiometrie Unter dem Name Potentiometrie werden diejenige analytische Methoden zusammengefasst, die auf der Messung des Elektrodenpotentials zurückzuführen sind (siehe dazu auch Mortimer, Kapitel 21,
Die Forschung mit embryonalen Stammzellen ist ethisch nicht akzeptabel
 Die Forschung mit embryonalen Stammzellen ist ethisch nicht akzeptabel Das Schweizer Volk soll sich selber äussern bezüglich der Gesetzgebung zur embryonalen Stammzellenforschung. Die ethische Bedeutung
Die Forschung mit embryonalen Stammzellen ist ethisch nicht akzeptabel Das Schweizer Volk soll sich selber äussern bezüglich der Gesetzgebung zur embryonalen Stammzellenforschung. Die ethische Bedeutung
WAS IST DIABETES? 1. Zucker - Kraftstoff des Menschen
 WAS IST DIABETES? 1. Zucker - Kraftstoff des Menschen Traubenzucker liefert Energie Bei jedem Menschen ist ständig eine geringe Menge Traubenzucker (Glukose) im Blut gelöst. Dieser Blutzucker ist der Kraftstoff
WAS IST DIABETES? 1. Zucker - Kraftstoff des Menschen Traubenzucker liefert Energie Bei jedem Menschen ist ständig eine geringe Menge Traubenzucker (Glukose) im Blut gelöst. Dieser Blutzucker ist der Kraftstoff
Das große ElterngeldPlus 1x1. Alles über das ElterngeldPlus. Wer kann ElterngeldPlus beantragen? ElterngeldPlus verstehen ein paar einleitende Fakten
 Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
Trockenes Auge. Haben Sie Trockene Augen?
 Trockenes Auge Jeder 3 bis 5 Patient, der den Augenarzt besucht, an der Krankheit Trockenes Auge leidet. Ein Trockenes Auge entsteht, wenn der Körper zu wenig Tränenflüssigkeit produziert oder die Zusammensetzung
Trockenes Auge Jeder 3 bis 5 Patient, der den Augenarzt besucht, an der Krankheit Trockenes Auge leidet. Ein Trockenes Auge entsteht, wenn der Körper zu wenig Tränenflüssigkeit produziert oder die Zusammensetzung
Protokoll des Versuches 5: Messungen der Thermospannung nach der Kompensationsmethode
 Name: Matrikelnummer: Bachelor Biowissenschaften E-Mail: Physikalisches Anfängerpraktikum II Dozenten: Assistenten: Protokoll des Versuches 5: Messungen der Thermospannung nach der Kompensationsmethode
Name: Matrikelnummer: Bachelor Biowissenschaften E-Mail: Physikalisches Anfängerpraktikum II Dozenten: Assistenten: Protokoll des Versuches 5: Messungen der Thermospannung nach der Kompensationsmethode
? Kann ich mit Karotten zu viel Vitamin A
 Schwangere aus sozial schwachen Schichten Schwangere, die alkohol-, drogen- oder nikotinabhängig sind Schwangere, die aufgrund einer chronischen Erkrankung Medikamente einnehmen müssen, welche die Nährstoffverwertung
Schwangere aus sozial schwachen Schichten Schwangere, die alkohol-, drogen- oder nikotinabhängig sind Schwangere, die aufgrund einer chronischen Erkrankung Medikamente einnehmen müssen, welche die Nährstoffverwertung
1) Warum sollten Sie die Bindehautentzündung grundsätzlich vom Arzt behandeln lassen? 4. 2) Was ist eine Bindehautentzündung? 5
 1) Warum sollten Sie die Bindehautentzündung grundsätzlich vom Arzt behandeln lassen? 4 2) Was ist eine Bindehautentzündung? 5 3) Durch welche Symptome kann sich eine Bindehautentzündung bemerkbar machen?
1) Warum sollten Sie die Bindehautentzündung grundsätzlich vom Arzt behandeln lassen? 4 2) Was ist eine Bindehautentzündung? 5 3) Durch welche Symptome kann sich eine Bindehautentzündung bemerkbar machen?
Proteinbestimmung. Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der Proteinbestimmung mit den folgenden Lehrzielen:
 Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der mit den folgenden Lehrzielen: Verständnis der Prinzipien der sowie deren praktischer Durchführung Unterscheidung zwischen
Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der mit den folgenden Lehrzielen: Verständnis der Prinzipien der sowie deren praktischer Durchführung Unterscheidung zwischen
Hören eines der wichtigsten Sinnesorgane
 Amplifon AG Sihlbruggstrasse 109 CH-6340 Baar Hören eines der wichtigsten Sinnesorgane Nicht sehen trennt uns von den Dingen. Nicht hören trennt uns von den Menschen!, lautet ein berühmter Ausspruch von
Amplifon AG Sihlbruggstrasse 109 CH-6340 Baar Hören eines der wichtigsten Sinnesorgane Nicht sehen trennt uns von den Dingen. Nicht hören trennt uns von den Menschen!, lautet ein berühmter Ausspruch von
Der Umgang mit der Flüssigkeitsbeschränkung. Avitum
 Der Umgang mit der Flüssigkeitsbeschränkung Avitum Warum muss ich darauf achten, wie viel ich trinke? Eine der Hauptfunktionen der Niere besteht darin, die Flüssigkeitsmenge des Körpers im Gleichgewicht
Der Umgang mit der Flüssigkeitsbeschränkung Avitum Warum muss ich darauf achten, wie viel ich trinke? Eine der Hauptfunktionen der Niere besteht darin, die Flüssigkeitsmenge des Körpers im Gleichgewicht
Labortests für Ihre Gesundheit. Therapie nach Maß 26
 Labortests für Ihre Gesundheit Therapie nach Maß 26 01IPF Labortests für Ihre Gesundheit Therapie nach Maß Die individuelle Dosis finden Jeder Mensch ist einzigartig. Keiner gleicht dem anderen nicht nur
Labortests für Ihre Gesundheit Therapie nach Maß 26 01IPF Labortests für Ihre Gesundheit Therapie nach Maß Die individuelle Dosis finden Jeder Mensch ist einzigartig. Keiner gleicht dem anderen nicht nur
6 Schulungsmodul: Probenahme im Betrieb
 6 Schulungsmodul: Probenahme im Betrieb WIEDNER Wie schon im Kapitel VI erwähnt, ist die Probenahme in Betrieben, die Produkte nach dem Lebensmittel- und Futtermittelgesetzbuch herstellen oder in den Verkehr
6 Schulungsmodul: Probenahme im Betrieb WIEDNER Wie schon im Kapitel VI erwähnt, ist die Probenahme in Betrieben, die Produkte nach dem Lebensmittel- und Futtermittelgesetzbuch herstellen oder in den Verkehr
BCM - BodyCellMass. Ihr BCM Diätplan
 MODI CUR Ihr BCM Diätplan Jetzt starten! Jetzt in drei Schritten zum Erfolg - Starten, abnehmen und Gewicht halten. 1 Tag 1-2: gewohnte Ernährung durch fünf Portionen BCM Startkost ersetzen. 3-4 Std. 3-4
MODI CUR Ihr BCM Diätplan Jetzt starten! Jetzt in drei Schritten zum Erfolg - Starten, abnehmen und Gewicht halten. 1 Tag 1-2: gewohnte Ernährung durch fünf Portionen BCM Startkost ersetzen. 3-4 Std. 3-4
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Übungsbuch für den Grundkurs mit Tipps und Lösungen: Analysis
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Übungsbuch für den Grundkurs mit Tipps und Lösungen: Analysis Das komplette Material finden Sie hier: Download bei School-Scout.de
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Übungsbuch für den Grundkurs mit Tipps und Lösungen: Analysis Das komplette Material finden Sie hier: Download bei School-Scout.de
Hyperkalzämie. Institut für Klinische Chemie und Laboratoriumsdiagnostik. Dr. Derik Hermsen
 Hyperkalzämie Institut für Klinische Chemie und Laboratoriumsdiagnostik Dr. Derik Hermsen 1 Calciumstoffwechsel Nahrung 1000 mg 300 mg Extrazelluläres 500 mg Darm 175 mg Calcium 900 mg Knochen 125 mg 500
Hyperkalzämie Institut für Klinische Chemie und Laboratoriumsdiagnostik Dr. Derik Hermsen 1 Calciumstoffwechsel Nahrung 1000 mg 300 mg Extrazelluläres 500 mg Darm 175 mg Calcium 900 mg Knochen 125 mg 500
Ein neues System für die Allokation von Spenderlungen. LAS Information für Patienten in Deutschland
 Ein neues System für die Allokation von Spenderlungen LAS Information für Patienten in Deutschland Ein neues System für die Allokation von Spenderlungen Aufgrund des immensen Mangels an Spenderorganen
Ein neues System für die Allokation von Spenderlungen LAS Information für Patienten in Deutschland Ein neues System für die Allokation von Spenderlungen Aufgrund des immensen Mangels an Spenderorganen
Abgestufte Lernhilfen
 Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
«Eine Person ist funktional gesund, wenn sie möglichst kompetent mit einem möglichst gesunden Körper an möglichst normalisierten Lebensbereichen
 18 «Eine Person ist funktional gesund, wenn sie möglichst kompetent mit einem möglichst gesunden Körper an möglichst normalisierten Lebensbereichen teilnimmt und teilhat.» 3Das Konzept der Funktionalen
18 «Eine Person ist funktional gesund, wenn sie möglichst kompetent mit einem möglichst gesunden Körper an möglichst normalisierten Lebensbereichen teilnimmt und teilhat.» 3Das Konzept der Funktionalen
oder: AK Analytik 32. NET ( Schnellstarter All-Chem-Misst II 2-Kanäle) ToDo-Liste abarbeiten
 Computer im Chemieunterricht einer Glühbirne Seite 1/5 Prinzip: In dieser Vorübung (Variante zu Arbeitsblatt D01) wird eine elektrische Schaltung zur Messung von Spannung und Stromstärke beim Betrieb eines
Computer im Chemieunterricht einer Glühbirne Seite 1/5 Prinzip: In dieser Vorübung (Variante zu Arbeitsblatt D01) wird eine elektrische Schaltung zur Messung von Spannung und Stromstärke beim Betrieb eines
Die Online-Meetings bei den Anonymen Alkoholikern. zum Thema. Online - Meetings. Eine neue Form der Selbsthilfe?
 Die Online-Meetings bei den Anonymen Alkoholikern zum Thema Online - Meetings Eine neue Form der Selbsthilfe? Informationsverhalten von jungen Menschen (Quelle: FAZ.NET vom 2.7.2010). Erfahrungen können
Die Online-Meetings bei den Anonymen Alkoholikern zum Thema Online - Meetings Eine neue Form der Selbsthilfe? Informationsverhalten von jungen Menschen (Quelle: FAZ.NET vom 2.7.2010). Erfahrungen können
6. Tag: Chemisches Gleichgewicht und Reaktionskinetik
 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1. Das chemische Gleichgewicht Eine chemische Reaktion läuft in beiden Richtungen ab. Wenn
6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1. Das chemische Gleichgewicht Eine chemische Reaktion läuft in beiden Richtungen ab. Wenn
Die spezifische Vitaminkombination in nur einer Tablette.
 Die spezifische Vitaminkombination in nur einer Tablette. Die gezielte Vitaminergänzung bei medikamentös behandelter Epilepsie. Schließen Sie Ihre Vitaminlücken ganz gezielt. Hinweis EPIVIT ist ein ernährungsmedizinisch
Die spezifische Vitaminkombination in nur einer Tablette. Die gezielte Vitaminergänzung bei medikamentös behandelter Epilepsie. Schließen Sie Ihre Vitaminlücken ganz gezielt. Hinweis EPIVIT ist ein ernährungsmedizinisch
Soja-Lebensmittel - Quelle von hochwertigem Eiweiß
 Soja-Lebensmittel - Quelle von hochwertigem Eiweiß Thesenpapier des wissenschaftlichen Beirats der ENSA Einleitung Eiweiß ist ein wichtiger Grundnährstoff, der für das Wachstum und die Reparatur aller
Soja-Lebensmittel - Quelle von hochwertigem Eiweiß Thesenpapier des wissenschaftlichen Beirats der ENSA Einleitung Eiweiß ist ein wichtiger Grundnährstoff, der für das Wachstum und die Reparatur aller
4. Wässrige Lösungen schwacher Säuren und Basen
 4. Wässrige Lösungen schwacher Säuren und Basen Ziel dieses Kapitels ist es, das Vorgehenskonzept zur Berechnung von ph-werten weiter zu entwickeln und ph-werte von wässrigen Lösungen einprotoniger, schwacher
4. Wässrige Lösungen schwacher Säuren und Basen Ziel dieses Kapitels ist es, das Vorgehenskonzept zur Berechnung von ph-werten weiter zu entwickeln und ph-werte von wässrigen Lösungen einprotoniger, schwacher
2.8 Grenzflächeneffekte
 - 86-2.8 Grenzflächeneffekte 2.8.1 Oberflächenspannung An Grenzflächen treten besondere Effekte auf, welche im Volumen nicht beobachtbar sind. Die molekulare Grundlage dafür sind Kohäsionskräfte, d.h.
- 86-2.8 Grenzflächeneffekte 2.8.1 Oberflächenspannung An Grenzflächen treten besondere Effekte auf, welche im Volumen nicht beobachtbar sind. Die molekulare Grundlage dafür sind Kohäsionskräfte, d.h.
Der Kälteanlagenbauer
 Der Kälteanlagenbauer Band : Grundkenntnisse Bearbeitet von Karl Breidenbach., überarbeitete und erweiterte Auflage. Buch. XXVIII, S. Gebunden ISBN 00 Format (B x L):,0 x,0 cm Zu Inhaltsverzeichnis schnell
Der Kälteanlagenbauer Band : Grundkenntnisse Bearbeitet von Karl Breidenbach., überarbeitete und erweiterte Auflage. Buch. XXVIII, S. Gebunden ISBN 00 Format (B x L):,0 x,0 cm Zu Inhaltsverzeichnis schnell
Primzahlen und RSA-Verschlüsselung
 Primzahlen und RSA-Verschlüsselung Michael Fütterer und Jonathan Zachhuber 1 Einiges zu Primzahlen Ein paar Definitionen: Wir bezeichnen mit Z die Menge der positiven und negativen ganzen Zahlen, also
Primzahlen und RSA-Verschlüsselung Michael Fütterer und Jonathan Zachhuber 1 Einiges zu Primzahlen Ein paar Definitionen: Wir bezeichnen mit Z die Menge der positiven und negativen ganzen Zahlen, also
ST. NIKOLAUS-HOSPITAL EUPEN Hufengasse 4-8 B - 4700 EUPEN Tel.: 087/59 95 99. Transoesophageale Echokardiographie (TEE) PATIENT
 D ST. NIKOLAUS-HOSPITAL EUPEN Hufengasse 4-8 B - 4700 EUPEN Tel.: 087/59 95 99 Transoesophageale Echokardiographie (TEE) PATIENT Seite 2 Liebe Patientin, lieber Patient, Ihr Arzt hat Ihnen zu einer transoesophagealen
D ST. NIKOLAUS-HOSPITAL EUPEN Hufengasse 4-8 B - 4700 EUPEN Tel.: 087/59 95 99 Transoesophageale Echokardiographie (TEE) PATIENT Seite 2 Liebe Patientin, lieber Patient, Ihr Arzt hat Ihnen zu einer transoesophagealen
Inhaltsverzeichnis Przedmowa... 2 Vorwort... 3 Inhaltsverzeichnis... 5
 Inhaltsverzeichnis Przedmowa... 2 Vorwort... 3 Inhaltsverzeichnis... 5 Kapitel 1 Von der Zelle zum Menschen....11 1.1. Bau des menschlichen Organismus... 13 Übungen.... 16 Kapitel 2 Bewegungsapparat...19
Inhaltsverzeichnis Przedmowa... 2 Vorwort... 3 Inhaltsverzeichnis... 5 Kapitel 1 Von der Zelle zum Menschen....11 1.1. Bau des menschlichen Organismus... 13 Übungen.... 16 Kapitel 2 Bewegungsapparat...19
Comenius Schulprojekt The sun and the Danube. Versuch 1: Spannung U und Stom I in Abhängigkeit der Beleuchtungsstärke E U 0, I k = f ( E )
 Blatt 2 von 12 Versuch 1: Spannung U und Stom I in Abhängigkeit der Beleuchtungsstärke E U 0, I k = f ( E ) Solar-Zellen bestehen prinzipiell aus zwei Schichten mit unterschiedlichem elektrischen Verhalten.
Blatt 2 von 12 Versuch 1: Spannung U und Stom I in Abhängigkeit der Beleuchtungsstärke E U 0, I k = f ( E ) Solar-Zellen bestehen prinzipiell aus zwei Schichten mit unterschiedlichem elektrischen Verhalten.
Die spezifische Vitaminkombination in nur einer Tablette.
 Die spezifische Vitaminkombination in nur einer Tablette. Die gezielte Vitaminergänzung bei medikamentös behandeltem Morbus Parkinson. Schließen Sie Ihre Vitaminlücken ganz gezielt. Hinweis PARKOVIT ist
Die spezifische Vitaminkombination in nur einer Tablette. Die gezielte Vitaminergänzung bei medikamentös behandeltem Morbus Parkinson. Schließen Sie Ihre Vitaminlücken ganz gezielt. Hinweis PARKOVIT ist
GFR / Kreatinin Clearance < 60 ml/min/ 1,73m 2. Δ Serum Kreatinin Anstieg > 50% Niereninsuffizienz ja oder nein? Wie heisst der Referent?
 Quelle: youtube.com Wie heisst der Referent? Niereninsuffizienz ja oder nein? GFR / Kreatinin Clearance < 60 ml/min/ 1,73m 2 Soll man die Kreatinin Clearance messen oder berechnen?? Δ Serum Kreatinin Anstieg
Quelle: youtube.com Wie heisst der Referent? Niereninsuffizienz ja oder nein? GFR / Kreatinin Clearance < 60 ml/min/ 1,73m 2 Soll man die Kreatinin Clearance messen oder berechnen?? Δ Serum Kreatinin Anstieg
