Fortgeschrittenenpraktikum. Physikalische Chemie. Versuch B3. Magnetische Suszeptibilität
|
|
|
- Waltraud Diefenbach
- vor 7 Jahren
- Abrufe
Transkript
1 Fortgeschrittenenpraktikum Physikalische Chemie Wintersemester 1998/99 Versuch B3 Magnetische Suszeptibilität Durchgeführt von: Assistent: 1. Abgabe: Abgabe: Abgabe:
2 Theoretische Grundlagen 1. Materie im elektrischen und magnetischen Feld 1.1 Materie im elektrischen Feld Die Atome bestehen aus dem Z-fach positiv geladenen Atomkern und der diesen Kern umgebenden Z-fach negativ geladenen Elektronenhülle. Da beide Ladungen gleich groß sind, erscheinen uns die Atome als elektrisch neutral. Wenn die Atome in ein elektrisches Feld gebracht werden, übt dieses auf die Ladungen eine Kraft aus, die in die entgegengesetzte Richtung wirkt. Es kommt im elektrischen Feld zur Ladungstrennung, wodurch ein elektrisches Dipolmoment entsteht. Die Größe eines induzierten Dipolmoments ist proportional zur elektrischen Feldstärke. = α E (1) ind ind = Induziertes Dipolmoment E = elektrische Feldstärke Der Proportionalitätsfaktor α heißt Polarisierbarkeit. Entsprechend ihrer entstehungsweise nennt man diese Art der Polarisation Verschiebungspolarisation. Man unterscheidet zwei Fälle: 1. Das induzierte Dipolmoment entsteht durch eine Verschiebung von Elektronen ativ zu den viel schwereren positiven Kernen (Elektronenpolarisation) 2. Das induzierte Dipolmoment entsteht durch eine Verschiebung schwerer positiver Ionen ativ zu schweren negativen Ionen (Ionenpolarisation). Polare Moleküle besitzen ein permanentes Dipolmoment. In Abwesenheit eines elektrischen Feldes zeigen diese molekularen Dipolmomente eine völlig zufällige Orientierung im Raum, so daß die Vektorsumme Null ist. In Gegenwart eines elektrischen Feldes sind Orientierungen, bei denen das Dipolmoment parallel zum Feld liegt, energetisch begünstigt. Diese Art der Polarisation bezeichnet man als Orientierungspolarisation. Bei polaren Molekülen treten sowohl die Verschiebungs- als auch die Orientierungspolarisation auf. 1.2 Materie im magnetischen Feld Analog zu den beschriebenen elektrischen Eigenschaften wird die Materie auch im magnetischen Feld polarisiert: Die Größe wird als Magnetisierung M bezeichnet. Der Proportionalitätsfaktor zwischen der Magnetisierung M und der Feldstärke H ist die magnetische Suszeptibilität. M = H (2) Wie in der Elektrostatik die Größe D für die elektrische Verschiebungsdichte eingeführt wurde, wird B als magnetische Flußdichte eingeführt. Das magnetische Moment ist der Quotient aus der Flußdichte und der Feldstärke. B = (3) H 2
3 Die magnetische Flußdichte B 0 hängt mit der Feldstärke H und der Magnetisierung M über die Beziehung B 0 = ( H + M ) = 0 ( 1 + ) H (4) zusammen. 0 ist die Permeabilität im Vakuum, sie entspricht im übertragenen Sinne der Dielektrizitätskonstante ε 0. Ist >0 nimmt B, also die Dichte der Feldlinien, zu. Damit sind auch die vektoriellen Größen H und M gleichgerichtet. Der Stoff wird dann als paramagnetisch bezeichnet. Im anderen Fall, <0, sind H und M entgegengesetzt, und der Stoff wird aus dem magnetischen Feld herausgedrängt. Er wird als diamagnetisch bezeichnet. 1.3 Dia- und Paramagnetismus Das magnetische Moment ist die Folge der Kreisbewegung der Elektronen um den Kern oder um ihre eigene Achse. Setzt man die Stoffe nun plötzlich einem äußeren Feld aus, so muß in jeder dieser Kreisbahnen ein Induktionsstrom auftreten. Nach der Lenzschen Regel muß er so gerichtet sein, daß er seiner Enstehungsachse entgegenwirkt, daß er also ein Magnetfeld erzeugt, das dem verursachenden Feld entgegen gerichtet ist. Damit ist auch das induzierte magnetische Moment dem äußeren Feld entgegen gerichtet. Im Fall des Diamagnetismus ist die magnetische Suszeptibilität stets negativ. Im Gegensatz zum Diamagnetismus, der immer auftritt, ist der Paramagnetismus an das Vorhandensein eines magnetischen Moments gebunden. Er kann also nicht vorliegen, wenn der Gesamtdrehimpuls Null ist. Mit = h 2π und h = Planksche Wirkungsquantum = 6.626*10-34 Js ergibt sich: ( +1) l = h l l Bahndrehimpuls (5) ( + 1) s = h s s Spin (6) Besitzt das Elektron einen Bahndrehimpuls, so werden Bahndrehimpuls und Spin über die durch sie erzeugten Magnetfelder koppeln, d.h. es wird zu einer vektoriellen Addition zu einem Gesamtdrehimpuls kommen. r r r j = l + s (7) r j = h ( j ) j * + 1 Gesamtdrehimpuls (8) Atome, deren Gesamtdrehimpuls von Null verschieden ist, sollten ein permanentes magnetisches Moment besitzen und paramagnetisch sein. Die Suszeptibilität eines paramagnetischen Stoffes setzt sich aus dem paramagnetischen und dem diamagnetischen Teil, der immer vorhanden ist, zusammen. 3
4 + m = (9) para dia = Suszeptibilität Da die paramagnetische Suszeptibilität sehr viel größer als die diamagnetische ist ( mal so groß) wird der diamagnetische Anteil häufig vernachlässigt. Die Temperaturabhängigkeit der paramagnetischen Suszeptibilität ist nach dem Curie-Weiss schen Gesetz gegeben als: C = T θ para (10) T = Temperatur θ = Curie-Temperatur C = Curie-Konstante Der Proportionalitätsfaktor C ist die Curie-Konstante. Ihr Wert kann berechnet werden: N = (11) 3k 0 A 2 C magn N A = Avogadro-Zahl [6.022*10 23 mol -1 ] k = Boltzmann-Konstante [1.3807*10-23 JK -1 ] Das magnetische Moment paramagnetischer Stoffe läßt sich berechnen: 3kT = N A m T (12) In der Komplexchemie kann man anhand dieses Wertes eine Aussage über die Elektronenanordnung im Ligandenfeld getroffen werden. Der Paramagnetismus wächst mit der Zahl der ungepaarten Elektronen. Da jedes Elektron einen Beitrag von s=1/2 zum Gesamtspin liefert, kann die Anzahl der ungepaarten Elektronen n als S=n/2 berechnet werden. ( n + ) n = 2 2 n = (13) (14) 4
5 1.4 Aufbau der Atomhülle Zur Beschreibung der Elektronenhüllen benutzt man die Postulate von Hund und Pauli. 1. Pauli Verbot In einem Atom kann ein durch alle vier Quantenzahlen charakterisierter Zustand nur mit einem Elektron besetzt werden. Daraus folgt, daß bei der Charakterisierung eines Elektronenzustandes entweder die Hauptquantenzahl n, die Nebenquantenzahl l, die magnetische Quantenzahl m oder die Spinquantenzahl s, einen unterschiedlichen Wert haben muß. 2. Stabilitätsregeln nach Hund für den Grundzustand 2.1 Unter mehreren möglichen Elektronenanordnungen ist diejenige mit dem größten Gesamtspin am stabilsten. 2.2 Unter mehreren möglichen Elektronenanordnungen ist die mit gleichem Gesamtspin und diejenige mit dem größtmöglichen Gesamtbahndrehimpuls l am stabilsten. 2.3 Bei Unterschalen, die weniger als zur Hälfte besetzt sind, ist der Term mit dem kleinsten Wert für den Gesamtdrehimpuls j am stabilsten (reguläres Multiplett) 2.4 Bei Unterschalen, die mehr als zur Hälfte besetzt sind, ist der Term mit dem größten Wert für den Gesamtimpuls am stabilsten (inverses Multiplett) 1.5 Messung der magnetischen Suszeptibilität Die Messung der Suszeptibilität erfolgt mit der Hilfe der Faradayschen Magnetwaage, indem man mittels der scheinbaren Massenzunahme (paramagnetische Stoffe) bzw. abnahme die Kraft ermittelt, die durch eine Masse in einem inhomogenen Magnetfeld ausgeübt wird. Die Kraft wächst mit der Suszeptibilität und mit der Stärke des magnetischen Feldes. Die Kraftänderung entspricht: ν =Suszeptibilität der Probe =Suszeptibilität des verdrängten Mediums ν,1 V =verdrängtes Volumen z =Richtung, in der das Magnetfeld wirkt Üblicherweise wird nicht der Quotient H F = ( ν ν, 1) V H (15) z H z bestimmt, sondern man kalibriert die Waage auf eine Substanz mit bekannter Suszeptibilität (im Versuch: CuSO 4 *5H 2 O, 10 = 183,5 10 ). mol m 3 5
6 Dann kann die Suszeptibilität über die gemessenen Massendifferenzen bestimmt werden. Sie wird als molare Größe bestimmt, d.h. bezogen auf die Molmasse der Substanz, um sie mit Werten für andere Substanzen vergleichen zu können. Aus der obigen Gleichung erhält man durch folgende Rechnung die Versuchsgleichung: Durch Integration: F 1 H V ( ν ν l ) V H = A 2 z z =, (16) 1 F = mg = l ( ) A ( H H ) ν ν, 0 0 (17) = 2mg ν ν, l 2 2 ν,l m 0 A ( H H 0 ) ν (18) ν ν m m, l = const. (19) ν m 1 ν, l ν 2,l = Massensuszeptibilität (20) m m m 1 ν 2 Division durch die Stoffmenge n-> Molsuszeptibilität M 1 M 2 M 1 = M 2 M = m (21) n M = molare Masse n m M1 1 2 M2 (22) n2 m1 = Da nur Stoffe mit wenigstens einem ungepaarten Elektron paramagnetisch stationäre Zustände liefern, ist es möglich, aufgrund der Kraft, mit der solche Stoffe in ein inhomogenes Magnetfeld gezogen werden, auf die Anzahl der ungepaarten Elektronen geschlossen werden. Das experimentell bestimmte magnetische Moment mag wird mit den für die verschiedenen Strukturmöglichkeiten berechneten Momenten verglichen. Die Vorausberechnung ist kompliziert, ihr liegen die Überlegungen der Kopplung zugrunde. Bei zwei- und dreiwertigen Ionen der ersten Übergangsperiode ist sie noch ativ einfach, da das Bahndrehmoment vernachlässigt werden kann, so daß sich das magnetische Moment (im Bohrschen- mag 6
7 Magneton) aus den Spinmomenten der Gleichung, wobei n die Anzahl der ungepaarten Elektronen entspricht, berechnet werden. mag ( n + ) B = n 2 (23) B ist das elektrische Elementarquantum des Magnetismus. Es ist das magnetische Moment des Kreisstroms, daß ein Elektron verursacht, das auf einer Kreisbahn mit dem Bohrschen Radius mit dem geringstmöglichen Bahndrehimpuls umläuft. Für n ungepaarte Elektronen ergeben sich die Werte (in ): n ,73 2,83 3,87 4,9 5,92 [ ] mag B Da das magnetische Moment praktisch nur von der Elektronenzahl, aber nicht von der Kernladung abhängt, haben Ionen verschiedener Kernladung, aber mit gleicher Elektronenzahl gleiche magnetische Momente (Kossel scher Verschiebungssatz). B 1.7 Abschätzung der Anzahl der ungepaarten Elektronen mit der Ligandenfeldtheorie Bei der Ligandenfeldtheorie wird die Wechselwirkung der Liganden eines Komplexes mit den d-elektronen des Zentralatoms beschrieben. Die Liganden werden als punktförmige Ladungen oder Dipole angenommen. Jeder Ligand, der ein Anion oder Dipol ist, bildet um sich ein elektrisches Feld aus. Wenn in einem Komplex mehrere Liganden gebunden sind, überlagern sich deren elektrische Felder und bilden ein gemeinsames Feld aus (Ligandenfeld). Wir wollen bei der weiteren Betrachtung nur das starke Feld behandeln. Die Bezeichnung starkes Feld bedeutet, daß die Kopplung der d-elektronen untereinander durch das Ligandenfeld verhindert wird und somit fünf nicht gekoppelte und voneinander unabhängige d-orbitale vorliegen. Bei der Konzentrierung der Elektronen in einem Orbital resultiert eine Abstoßung der Elektronen, die als Spinpaarungsenergie bezeichnet wird. Wenn die Aufspaltung größer ist als die Spinpaarungsenergie, entsteht ein low-spin-komplex. Wenn die Spinpaarungsenergie größer ist als die Aufspaltung, entsteht ein high-spin-komplex. Die Aufspaltung ist abhängig von der Ladung und der Ordnungszahl des Metallions und von der Natur der Liganden. Ordnet man die Liganden nach deren Fähigkeit, d-orbitale aufzuspalten, erhält man eine Reihe, die spektrochemische Reihe genannt wird. CO,CN> en > NH 3 > H 2 O > OH - > F - > Cl - > I - Starkes F. mittleres F. schwaches F. Bei gleichen Liganden wächst die Aufspaltung mit der Hauptquantenzahl der d-orbitale der Metallionen. Eine Zunahme der Aufspaltung erfolgt auch, wenn die Ladung des Zentralions erhöht wird. 7
8 Nach der Ligandenfeldtheorie sind folgende Werte zu erwarten. 1. CuSO 4 *5H 2 O Beim Cu(II) handelt es sich um ein d 9 -System. Ihre Elektronenanordnung enthält ein ungepaartes Elektron. Der Komplex ist aufgrund des Jahn-Teller-Effekts oktaedrisch verzerrt. 2. CrCl 3 *6H 2 O Die Elektronenkonfiguration liefert bei oktaedrischer Koordination eine große Ligandenfeldstabilisierungsenergie (LFSE), es ist ein d-high-spin-komplex mit drei ungepaarten Elektronen zu erwarten. 3. K 3 Fe(CN) 6 CN ist ein starker Ligand. Er steht am Ende der spektrochemischen Reihe, in der Liganden nach zunehmender LFSE geordnet sind. Gegenüber anderen Liganden (wie z.b. Halogeniden) kann CN eine Rückbindung vom Metall bilden.: Me = C = N < > Me C = N. Die leeren Orbitale werden vom Metall durch die Rückbindung aufgefüllt. Es ist ein oktaedrischer d- low-spin-komplex zu erwarten mit einem ungepaarten Elektron. 4. Fe(NO 3 ) 3 *9H 2 O Auch hier liegt Fe(III) vor. Allerdings ist Nitrat ein schwacher Ligand, so daß vermutlich ein oktaedrischer high-spin-komplex mit fünf ungepaarten Elektronen bildet. 5. NiC l 2 *6H 2 O Ni(II)-Komplexe sind in der Regel oktaedrisch. In diesem Fall ist ein d-high-spin-komplex mit zwei ungepaarten Elektronen zu erwarten. 8
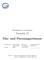
9 2. Versuchsaufbau 2.1. Versuchsbeschreibung Abb.1 Aufbau der magnetischen Waage, G=Waage, S und N sind die Pole des Magneten, P=Probe, z=richtung der resultierenden Kraft. Mit einem Elektromagneten wird ein inhomogenes Magnetfeld zwischen den Polschuhen erzeugt. Zwischen den beiden Polen befindet sich das Probenrohr mit der zu bestimmenden Probe. Da das Magnetfeld in einer Richtung (z-richtung; siehe Abb.1) inhomogen ist, wird eine Kraft auf das Volumenelement V in z-richtung ausgeübt. In einem homogenen Magnetfeld erfährt ein magnetischer Dipol zwar ein Drehmoment aber keine Gesamtkraft Versuchsdurchführung Zunächst wird eine Meßreihe mit leerem Probenglasrohr durchgeführt, um den Betrag der magnetische Suszeptibilität des Probenglasrohrs zu bestimmen, wobei die Waageanzeige bei 0, 4, 8, 12, 16, 19, 16, 12, 8, 4, 0 A (aus den verschiedenen Stromstärken resultiert ein unterschiedlich starkes Magnetfeld) notiert wird. Nach der Messung wurde die Bestimmung des Leergewichts in der selben Weise wiederholt, um zu überprüfen, ob der Nullwert sich verändert hat. Aus den erhaltenen Werten wurde der Mittelwert gebildet. Es wurde jeweils die zu untersuchende Probe in das Probenrohr gefüllt und ebenfalls die Waageanzeige bei den oben genannten Werten notiert. Jede Probe viermal durchgemessen und aus den erhaltenen Werten wurde ebenfalls der Mittelwert gebildet. Die Kräfte die auf die Probe eingewirkt haben, ergaben sich aus der Differenz der Kräfte auf das gefüllte Probenrohr bei einer bestimmten Stromstärke und bei I=0. Die so erhaltenen Werte wurden um die in der Leermessung erhaltenen Werte korrigiert. Es wurden folgende Salze NiCl 2 *6H 2 O, CrCl 3 *6H 2 O, Fe(NO 3 ) 3 *9H 2 O und K3Fe(CN) 6 untersucht. 9
10 3. Auswertung 3.1 Berechnung der magnetischen Suszeptibilität Zunächst werden die Massendifferenzen der scheinbaren Massenänderung bei angelegtem Feld und ohne Feld aus der Folgenden Gleichung bestimmt. ( xa) m( A) m = m 0 (24) Tab.1: Massendifferenz [ g ] verschiedener Substanzen im Magnetfeld bei verschiedenen Stromstärken Stromstärke 4 [A] 8 [A] 12 [A] 16 [A] 19 [A] CuSO 4 *5H 2 O CrCl 3 *6H 2 O NiCl 2 *6H 2 O Fe(NO 3 )*9H 2 O K 3 (Fe(CN) 6 ) Die so erhaltenen Massen müssen noch um den diamagnetischen Anteil des Probegefäßes vermindert werden. Tab.2: Massendifferenzen [ g ] des leeren Kolbens bei verschiedenen Stromstärken Stromstärke 4 [A] 8 [A] 12 [A] 16 [A] 19 [A] Tab.3: Effektive Massendifferenz [ g ] im Magnetfeld bei verschiedenen Stromstärken Stromstärke 4 [A] 8 [A] 12 [A] 16 [A] 19 [A] CuSO 4 *5H 2 O CrCl 3 *6H 2 O NiCl 2 *6H 2 O Fe(NO 3 )*9H 2 O K 3 (Fe(CN) 6 )
11 Berechnung der Stoffmenge: m( x) n ( x) = (25) M ( x) n=stoffmenge, m=masse, M=Molare Masse Tab.4: Stoffmengenberechnung Einwaage [mg] Molmasse [g/mol] Stoffmenge [mol] CuSO 4 *5H 2 O 15,8 249,68 6,33*10-5 CrCl 3 *6H 2 O 11,8 266,36 4,43*10-5 NiCl 2 *6H 2 O 11,5 237,71 4,84*10-5 Fe(NO 3 )*9H 2 O 16,1 403,97 3,99*10-5 K 3 (Fe(CN) 6 ) 15,7 329,26 4,77*10-5 Mit dem Literaturwert für Kupfersulfat Molsuszeptibilitäten berechnet werden m m = 183,5*10 können die anderen mol n m M1 1 2 M 2 (26) n2 m1 = Tab.5: Molsuszeptibilität [1*10-10 m 3 /mol] Substanz 4 [A] 8 [A] 12 [A] 16 [A] 19 [A] CuSO 4 *5H 2 O 183,5 183,5 183,5 183,5 183,5 183,5 CrCl 3 *6H 2 O 707,4 638,6 650,9 625,7 625,6 649,6 NiCl 2 *6H 2 O 674,0 658,8 672,8 699,1 698,4 680,6 Fe(NO 3 )*9H 2 O 1699,9 1842,5 1942,7 1966,4 1401,6 1770,6 K 3 (Fe(CN) 6 ) 346,7 399,3 413,0 341,0 415,8 383,1 Die so erhaltenen Werte für die Suszeptibilität werden für jeweils gleiche Substanzen gemittelt ( ). Dieser Schritt ist mit folgender Überlegung zu begründen: Die experimentell bestimmten Werte müßten eigentlich konstantes Verhalten bei verschiedenen Stromstärke zeigen wie die Eichsubstanz. Das ist damit zu begründen, daß sich die Massenänderung der Eichsubstanz proportional zu der Massenänderung der Meßsubstanz verhält. Da in der Rechnung dann das Verhältnis dieser Änderung gebildet wird, wäre Konstanz innerhalb einer Zeile zu erwarten. 11
12 3.2 Berechnung der Anzahl der ungepaarten Elektronen Bei Bildung eines Komplexes spalten sich die d-energieniveaus des Zentralatoms auf. Je nach Größe der Ligandenfeldaufspaltung kommt es dann zu high-spin- oder low-spin-anordnung der Elektronen. Also ist für die Anzahl der ungepaarten Elektronen nur das magnetische Moment, genauer die magnetische Suszeptibilität, des Zentralatoms entscheidend. Deshalb wird die in Teil 1 der Auswertung berechnete Gesamtsuszeptibilität der Substanz um den Betrag der Suszeptibilität der Liganden korrigiert. Tab.5: Anteil des Zentralatoms an der Molsuszeptibilität Substanz 3 10 m M 1,0*10 mol CuSO 4 *5H 2 O 191,65 CrCl 3 *6H 2 O 514,14 K 3 [Fe(CN) 6 ] 250,32 Fe(NO 3 ) 3 *9H 2 O 1791,75 NiCl 2 *6H 2 O 534,35 Mit diesen Werten kann nun das ative magnetische Moment berechnet werden. Das Verhältnis zwischen dem magnetischen Moment und dem Bohrschen Magneton gibt diesen Wert an. Das ative magnetische Moment ist also dimensionslos und gibt das Vielfache des Bohrschen Magnetons an, um daß das magnetische Moment größer als der mögliche Minimalbetrag ist. = Anzahl der Bohrschen Magnetone M 3RT = 2 0 N A (27) B J R = 8, 3144 mol K 23 1 N A = 6, mol 24 J B = 9, T 7 m kg 0 = 4π s A Durch Einsetzen der Werte vereinfacht sich die Gleichung (28) =, T 12
13 Tab.7: atives magnetisches Moment Substanz CuSO 4 *5H 2 O 1,8596 CrCl 3 *6H 2 O 3,4989 K 3 [Fe(CN) 6 ] 2,6870 Fe(NO 3 ) 3 *9H 2 O 5,7766 NiCl 2 *6H 2 O 3,5814 Durch Einsetzen von Elektronen: in die folgende Gleichung, erhält man die Anzahl der ungepaarten 2 n (29) = Tab.8: Anzahl der ungepaarten Elektronen Substanz n CuSO 4 *5H 2 O 1 CrCl 3 *6H 2 O 3 K 3 [Fe(CN) 6 ] 2 Fe(NO 3 ) 3 *9H 2 O 5 NiCl 2 *6H 2 O 3 13
14 4. Fehlerrechnung Bestimmung der Fehlergrenzen: Waage: m = 0, 0001g 4.1 Fehler der Stoffmenge mi n = i ni (30) mi Tab.9: Fehler der Stoffmenge Substanz [mol]*10-7 n i CuSO 4 *5H 2 O 4,01 CrCl 3 *6H 2 O 3,75 K 3 [Fe(CN) 6 ] 3,04 Fe(NO 3 ) 3 *9H 2 O 2,48 NiCl 2 *6H 2 O 4, Fehler der magnetischen Suszeptibilität ( m ) = + ( m ) i CuSO n n 4 i CuSO4 + + M M (31) mi mcuso n 4 i ncuso4 Tab.10: Fehler der magnetischen Suszeptibilität Substanz CrCl 3 *6H 2 O 27,95 K 3 [Fe(CN) 6 ] 51,55 Fe(NO 3 ) 3 *9H 2 O 55,80 NiCl 2 *6H 2 O 52,80 m m mol 14
15 4.3 Fehler für die Anzahl der Bohrschen Magnetone Bestimmung der Fehlergrenzen: Thermometer T = 1K Die Raumtemperatur betrug 296,15 K. 1 T M = + 2 M T (32) Tab.11: Fehler für die Anzahl der Bohrschen Magnetone Substanz CrCl 3 *6H 2 O 3 K 3 [Fe(CN) 6 ] 2 Fe(NO 3 ) 3 *9H 2 O 5 NiCl 2 *6H 2 O 3 5. Darstellung der Ergebnisse 5.1 Molare Suszeptibilität Substanz Experimentell 3 10 m m 1 10 mol m Literatur 1/ CrCl 3 *6H 2 O 650 ± K 3 [Fe(CN) 6 ] 380 ± Fe(NO 3 ) 3 *9H 2 O 1770 ± NiCl 2 *6H 2 O 681 ± m mol 5.2 Anzahl der ungepaarten Elektronen Substanz ( exp ) ( exp ) n (Lit.3) n (Lit.3) CrCl 3 *6H 2 O 3,5 ± 0,1 2 3,87 3 K 3 [Fe(CN) 6 ] 2,7 ± 0,2 1 1,73 1 Fe(NO 3 ) 3 *9H 2 O 5,8 ± 0,1 5 5,92 5 NiCl 2 *6H 2 O 3,6 ± 0,2 2 2,
16 6. Diskussion der Ergebnisse Es könne folgende Fehler vorliegen: a.) b.) c.) d.) Fehler beim Einhängen der Probe in die Apperatur Fehler bei der Einwaage der Substanzproben Temperaturschwankungen Hygroskopie der Analysensubstanzen ad a.) Die Analysensubstanz wird in einem Behälter aus Gals, an dem ein Draht für die Aufhängung befestigt ist, in der Apparatur zwischen den beiden Polschuhen aufgehängt. Bei einer zu tiefen Lage des Glasbehälters, befindet sich dieser nicht in dem geforderten Einfluß des inhomogenen Magnetfeldes. Dadurch kommt es zu einem Meßfehler, in deren Folge es zu einem niedrigeren Meßwert führt. ad b.) Bei der verwendeten Waage handelte es sich um eine halbautomatische handelsübliche Analysenwaage. Einen Fehler von 1 mg bei der Ablesung der Einwaage würde zu einem Fehler bei der Bestimmung von ca. ± 10% führen. ad c.) Eine Temperaturschwankung als mögliche Fehlerquelle ist auszuschließen, da die Temperatur bei der Berechnung des ativen magnetischen Moment, sich nur um den Faktor von ca. 1,0017 (=0,17%) pro 1 K bemerkbar machen würde. ad d.) Da die verwendeten Substanzen allesamt mehr oder weniger hygroskopisch sind, kann von einem gewissen Anteil von Wasser, außer dem Kristallwasser, ausgegangen werden. Befinden sich weitere Wassermoleküle am Zentralatom, so vergrößert sich der Anteil der Suszeptibilität für die Liganden. Im Gegensatz dazu verringert sich bei der Berechnung der Anteil der molaren Suszeptibilität des Zentralatoms. Abschließend kann bemerkt werden, daß die Methode von Faradey eigentlich eine gute Möglichkeit zur Bestimmung der magnetischen Suszeptibilität ist. Die erhaltenen Ergebnisse stimmen in den Größen mit den Literaturdaten überein, jedoch streuen sie aufgrund des diskutierten Fehlers so weit, daß eine exakte Aussage über die Brauchbarkeit der Methode nicht gemacht werden kann. Um dies zu korrigieren müßte der Versuch unter Umständen wiederholt werden, unter den Aspekten wie Verwendung von hochreinen trockenen Substanzen sowie eine bessere Koordination der Versuchsdurchführung. 16
17 7. Literatur 1 Röth, E.P.: Versuchsanleitung Praktikum PC II, Essen Weast/Astle/Beyer: Handbook of Chemistry and Physics, 61 Aufl Holleman, Wiberg: Lehrbuch der Anorganischen Chemie, Walter de Gruyter, Atkins, Peter W.: Physikalische Chemie, Weinheim 1990, VCH-Verlag 17
Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment
 1 Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment Zusatzaufgaben zu Versuch 316 : 1. Berechnen Sie das magnetische Moment des Co + - Ions.. Welche Niveaus der Valenzelektronen sind beim Co +
1 Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment Zusatzaufgaben zu Versuch 316 : 1. Berechnen Sie das magnetische Moment des Co + - Ions.. Welche Niveaus der Valenzelektronen sind beim Co +
F2 Magnetische Waage
 F Magnetische Waage 1. Aufgabenstellung: Für anorganische Komplexverbindungen soll aus der Messung der magnetischen Suszeptibilität die Zahl der ungepaarten Elektronen und aus der Messung der UV- Spektren
F Magnetische Waage 1. Aufgabenstellung: Für anorganische Komplexverbindungen soll aus der Messung der magnetischen Suszeptibilität die Zahl der ungepaarten Elektronen und aus der Messung der UV- Spektren
Mößbauer-Spektroskopie
 Mößbauer-Spektroskopie Westfälische Wilhelms-Universität Münster Ansgar Stüken & Thomas Dröge 12.05.2005 Überblick Elektrische Monopolwechselwirkung (Isomerieverschiebung) Elektrische Quadrupolwechselwirkung
Mößbauer-Spektroskopie Westfälische Wilhelms-Universität Münster Ansgar Stüken & Thomas Dröge 12.05.2005 Überblick Elektrische Monopolwechselwirkung (Isomerieverschiebung) Elektrische Quadrupolwechselwirkung
Versuch Nr. 9 Magnetische Suszeptibilität
 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: 1.1.4 1. Ziel des Versuches Versuch Nr. Magnetische Suszeptibilität Bei diesem Versuch soll die Suszeptibilität von verschiedenen Komplexsalzen
Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: 1.1.4 1. Ziel des Versuches Versuch Nr. Magnetische Suszeptibilität Bei diesem Versuch soll die Suszeptibilität von verschiedenen Komplexsalzen
Dia- und Paramagnetismus. Brandner Hannes Schlatter Nicola
 Dia- und Paramagnetismus Brandner Hannes Schlatter Nicola Ursachen des magnetischen Moments eines freien Atoms Spin der Elektronen (paramagn.) Deren Bahndrehimpuls bezüglich ihrer Bewegung um den Kern
Dia- und Paramagnetismus Brandner Hannes Schlatter Nicola Ursachen des magnetischen Moments eines freien Atoms Spin der Elektronen (paramagn.) Deren Bahndrehimpuls bezüglich ihrer Bewegung um den Kern
Suszeptibilitätsmessungen mit der Gouy-Waage 1. Theorie 2. Versuchsdurchführung:
 Protokoll zum Versuch Suszeptibilitätsmessungen mit der Gouy-Waage Betreuerin: Kirsten Feddern 1. Theorie Materie, die einem magnetischen Feld ausgesetzt ist, zeigt verschiedene Effekte. Einige davon sind
Protokoll zum Versuch Suszeptibilitätsmessungen mit der Gouy-Waage Betreuerin: Kirsten Feddern 1. Theorie Materie, die einem magnetischen Feld ausgesetzt ist, zeigt verschiedene Effekte. Einige davon sind
PD Para- und Diamagnetismus
 PD Para- und Diamagnetismus Blockpraktikum Herbst 2007 (Gruppe 2b) 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Magnetfeld in Materie............................ 2 1.2 Arten von Magnetismus...........................
PD Para- und Diamagnetismus Blockpraktikum Herbst 2007 (Gruppe 2b) 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Magnetfeld in Materie............................ 2 1.2 Arten von Magnetismus...........................
Elektrizitätslehre und Magnetismus
 Elektrizitätslehre und Magnetismus Othmar Marti 05. 05. 2008 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Physik Klassische und Relativistische Mechanik 05. 05.
Elektrizitätslehre und Magnetismus Othmar Marti 05. 05. 2008 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Physik Klassische und Relativistische Mechanik 05. 05.
Das Periodensystem der Elemente
 Q34 LK Physik 17. November 2015 Aufbau Die ermittelten Zusammenhänge der Elektronenzustände in der Atomhülle sollen dazu dienen, den der Elemente zu verstehen. Dem liegen folgende Prinzipien zugrunde:
Q34 LK Physik 17. November 2015 Aufbau Die ermittelten Zusammenhänge der Elektronenzustände in der Atomhülle sollen dazu dienen, den der Elemente zu verstehen. Dem liegen folgende Prinzipien zugrunde:
Magnetismus der Materie. Bernd Fercher David Schweiger
 Magnetismus der Materie Bernd Fercher David Schweiger Einleitung Erste Beobachtunge in China und Kleinasien Um 1100 Navigation von Schiffen Magnetismus wird durch Magnetfeld beschrieben dieses wird durch
Magnetismus der Materie Bernd Fercher David Schweiger Einleitung Erste Beobachtunge in China und Kleinasien Um 1100 Navigation von Schiffen Magnetismus wird durch Magnetfeld beschrieben dieses wird durch
3.6 Materie im Magnetfeld
 3.6 Materie im Magnetfeld Vorversuche Die magnetische Feldstärke, gemessen mit einer sog. Hall-Sonde, ist am Ende einer stromdurchflossenen Spule deutlich höher, wenn sich in der Spule ein Eisenkern statt
3.6 Materie im Magnetfeld Vorversuche Die magnetische Feldstärke, gemessen mit einer sog. Hall-Sonde, ist am Ende einer stromdurchflossenen Spule deutlich höher, wenn sich in der Spule ein Eisenkern statt
10. Der Spin des Elektrons
 10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
15.Magnetostatik, 16. Induktionsgesetz
 Ablenkung von Teilchenstrahlen im Magnetfeld (Zyklotron u.a.): -> im Magnetfeld B werden geladene Teilchen auf einer Kreisbahn abgelenkt, wenn B senkrecht zu Geschwindigkeit v Kräftegleichgewicht: 2 v
Ablenkung von Teilchenstrahlen im Magnetfeld (Zyklotron u.a.): -> im Magnetfeld B werden geladene Teilchen auf einer Kreisbahn abgelenkt, wenn B senkrecht zu Geschwindigkeit v Kräftegleichgewicht: 2 v
Physik I TU Dortmund SS2018 Götz Uhrig Shaukat Khan Kapitel 1
 Physik I TU Dortmund SS18 Götz Uhrig Shaukat Khan Kapitel 1 Kugelkondensator Radien a (innen) und b (außen), Ladung ±. In der inneren Hohlkugel ist das E-Feld null (wie in jeder Hohlkugel, s. oben), außerhalb
Physik I TU Dortmund SS18 Götz Uhrig Shaukat Khan Kapitel 1 Kugelkondensator Radien a (innen) und b (außen), Ladung ±. In der inneren Hohlkugel ist das E-Feld null (wie in jeder Hohlkugel, s. oben), außerhalb
Materie im Magnetfeld
 . Stromschleifen - Permanentmagnet Materie im Magnetfeld EX-II SS007 = > µmag = I S ˆn S = a b µ bahn = e m L µ spin = e m S Stromschleife im Magnetfeld Magnetisierung inhomogenes Magnetfeld = D = µmag
. Stromschleifen - Permanentmagnet Materie im Magnetfeld EX-II SS007 = > µmag = I S ˆn S = a b µ bahn = e m L µ spin = e m S Stromschleife im Magnetfeld Magnetisierung inhomogenes Magnetfeld = D = µmag
PN 2 Einführung in die Experimentalphysik für Chemiker
 PN 2 Einführung in die Experimentalphysik für Chemiker 4. Vorlesung 9.5.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
PN 2 Einführung in die Experimentalphysik für Chemiker 4. Vorlesung 9.5.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
Magnetismus. Prof. DI Michael Steiner
 Magnetismus Prof. DI Michael Steiner www.htl1-klagenfurt.at Magnetismus Natürlicher Künstlicher Magneteisenstein Magnetit Permanentmagnete Stabmagnet Ringmagnet Hufeisenmagnet Magnetnadel Temporäre Magnete
Magnetismus Prof. DI Michael Steiner www.htl1-klagenfurt.at Magnetismus Natürlicher Künstlicher Magneteisenstein Magnetit Permanentmagnete Stabmagnet Ringmagnet Hufeisenmagnet Magnetnadel Temporäre Magnete
Dia- und Paramagnetismus
 Physikalisches Praktikum für das Hauptfach Physik Versuch 19 Dia- und Paramagnetismus Wintersemester 2005 / 2006 Name: Mitarbeiter: EMail: Gruppe: Daniel Scholz Hauke Rohmeyer physik@mehr-davon.de B9 Assistent:
Physikalisches Praktikum für das Hauptfach Physik Versuch 19 Dia- und Paramagnetismus Wintersemester 2005 / 2006 Name: Mitarbeiter: EMail: Gruppe: Daniel Scholz Hauke Rohmeyer physik@mehr-davon.de B9 Assistent:
Elektrische und magnetische Materialeigenschaften
 Die elektrischen Eigenschaften von Dielektrika und Paraelektrika sind keine speziellen Eigenschaften fester oder kristalliner Substanzen. So sind diese Eigenschaften z.b. auch in Molekülen und Flüssigkeiten
Die elektrischen Eigenschaften von Dielektrika und Paraelektrika sind keine speziellen Eigenschaften fester oder kristalliner Substanzen. So sind diese Eigenschaften z.b. auch in Molekülen und Flüssigkeiten
Versuch 15 Dia- und Paramagnetismus
 Physikalisches A-Praktikum Versuch 15 Dia- und Paramagnetismus Praktikanten: Gruppe: Julius Strake Niklas Bölter B006 Betreuer: Johannes Schmidt Durchgeführt: 07.09.2012 Unterschrift: E-Mail: niklas.boelter@stud.uni-goettingen.de
Physikalisches A-Praktikum Versuch 15 Dia- und Paramagnetismus Praktikanten: Gruppe: Julius Strake Niklas Bölter B006 Betreuer: Johannes Schmidt Durchgeführt: 07.09.2012 Unterschrift: E-Mail: niklas.boelter@stud.uni-goettingen.de
Komplexchemie des Nickels Ligandenaustauschreaktionen
 Komplexchemie des Nickels Ligandenaustauschreaktionen Jorge Ferreiro, 1. Semester, D-CHAB, fjorge@student.ethz.ch Assistent: Kyrill Stanek Abstract: In diesem Versuch ging es darum, verschiedene Ligandenaustauschreaktionen
Komplexchemie des Nickels Ligandenaustauschreaktionen Jorge Ferreiro, 1. Semester, D-CHAB, fjorge@student.ethz.ch Assistent: Kyrill Stanek Abstract: In diesem Versuch ging es darum, verschiedene Ligandenaustauschreaktionen
E19 Magnetische Suszeptibilität
 Aufgabenstellung: 1. Untersuchen Sie die räumliche Verteilung des Magnetfeldes eines Elektromagneten und dessen Abhängigkeit vom Spulenstrom. 2. Bestimmen Sie die magnetische Suszeptibilität vorgegebener
Aufgabenstellung: 1. Untersuchen Sie die räumliche Verteilung des Magnetfeldes eines Elektromagneten und dessen Abhängigkeit vom Spulenstrom. 2. Bestimmen Sie die magnetische Suszeptibilität vorgegebener
Magnetisierung der Materie
 Magnetisierung der Materie Das magnetische Verhalten unterschiedlicher Materialien kann auf mikroskopische Eigenschaften zurückgeführt werden. Magnetisches Dipolmoment hängt von Symmetrie der Atome und
Magnetisierung der Materie Das magnetische Verhalten unterschiedlicher Materialien kann auf mikroskopische Eigenschaften zurückgeführt werden. Magnetisches Dipolmoment hängt von Symmetrie der Atome und
Atom-, Molekül- und Festkörperphysik
 Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 11. Vorlesung, 4.7. 2013 Para-, Dia- und Ferromagnetismus Isingmodell, Curietemperatur,
Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 11. Vorlesung, 4.7. 2013 Para-, Dia- und Ferromagnetismus Isingmodell, Curietemperatur,
Magnetochemie. Lehrbücher:H. Lueken, Magnetochemie, Teubner Studienbücher, R. L. Carlin, Magnetochemistry, Springer-Verlag, 1986.
 Magnetochemie Lehrbücher:H. Lueken, Magnetochemie, Teubner Studienbücher, 2000 R. L. Carlin, Magnetochemistry, Springer-Verlag, 1986. Grundbegriffe des Magnetismus Magnetische Flußdichte Magnetisierung
Magnetochemie Lehrbücher:H. Lueken, Magnetochemie, Teubner Studienbücher, 2000 R. L. Carlin, Magnetochemistry, Springer-Verlag, 1986. Grundbegriffe des Magnetismus Magnetische Flußdichte Magnetisierung
Das magnetische Feld
 Das Magnetfeld wird durch Objekte erzeugt und wirkt gleichzeitig auf Objekte repräsentiert die Kraftwirkung aufgrund des physikalischen Phänomens Magnetismus ist gerichtet und wirkt vom Nordpol zum Südpol
Das Magnetfeld wird durch Objekte erzeugt und wirkt gleichzeitig auf Objekte repräsentiert die Kraftwirkung aufgrund des physikalischen Phänomens Magnetismus ist gerichtet und wirkt vom Nordpol zum Südpol
Ligandenfeldtheorie Magnetismus von Komplexen
 Arbeitsblätter zum Ausdrucken von sofatutor.com Ligandenfeldtheorie Magnetismus von Komplexen Schildere die Unterschiede zwischen highspin- und lowspin-komplexen. 2 Gib die Orbitale an, die im oktaedrischen
Arbeitsblätter zum Ausdrucken von sofatutor.com Ligandenfeldtheorie Magnetismus von Komplexen Schildere die Unterschiede zwischen highspin- und lowspin-komplexen. 2 Gib die Orbitale an, die im oktaedrischen
E2: Wärmelehre und Elektromagnetismus 18. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 18. Vorlesung 21.06.2018 Barlow-Rad Heute: Telefon nach Bell - Materie im Magnetfeld: Dia-, Para-, Ferromagnetismus - Supraleitung - Faradaysches Induktionsgesetz
E2: Wärmelehre und Elektromagnetismus 18. Vorlesung 21.06.2018 Barlow-Rad Heute: Telefon nach Bell - Materie im Magnetfeld: Dia-, Para-, Ferromagnetismus - Supraleitung - Faradaysches Induktionsgesetz
Besetzung der Orbitale
 Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
HAW Hamburg Fachbereich HWI Hamburg, Prof. Dr. Badura B. Hamraz, O. Zarenko, M. Behrens. Chemie Testat 2. Name: Vorname: Matrikelnummer:
 Chemie Testat 2 Name: Vorname: Matrikelnummer: Bearbeitungszeit: 1 Stunde Zugelassene Hilfsmittel: Stifte, unbeschriebenes Papier, ein nichtprogrammierbarer Taschenrechner und ein Periodensystem Bitte
Chemie Testat 2 Name: Vorname: Matrikelnummer: Bearbeitungszeit: 1 Stunde Zugelassene Hilfsmittel: Stifte, unbeschriebenes Papier, ein nichtprogrammierbarer Taschenrechner und ein Periodensystem Bitte
Aufspaltung der Energieniveaus von Atomen im homogenen Magnetfeld
 Simon Lewis Lanz 2015 simonlanzart.de Aufspaltung der Energieniveaus von Atomen im homogenen Magnetfeld Zeeman-Effekt, Paschen-Back-Effekt, Fein- und Hyperfeinstrukturaufspaltung Fließt elektrischer Strom
Simon Lewis Lanz 2015 simonlanzart.de Aufspaltung der Energieniveaus von Atomen im homogenen Magnetfeld Zeeman-Effekt, Paschen-Back-Effekt, Fein- und Hyperfeinstrukturaufspaltung Fließt elektrischer Strom
Experimentalphysik 2
 Ferienkurs Experimentalphysik 2 Sommer 2014 Vorlesung 4 Thema: Elektromagnetische Schwingungen, elektromagnetische Wellen und Spezielle Relativitätstheorie Technische Universität München 1 Fakultät für
Ferienkurs Experimentalphysik 2 Sommer 2014 Vorlesung 4 Thema: Elektromagnetische Schwingungen, elektromagnetische Wellen und Spezielle Relativitätstheorie Technische Universität München 1 Fakultät für
Magnetische Momente (Gouysche Waage)
 Stand: 7/3 III.5.1 Magnetische Momente (Gouysche Waage) Ziel des Versuches Der Versuch dient dem ennenlernen der Grundbegriffe des magnetischen Feldes (Feldstärke, magnetische Induktion, Suszeptibilität,
Stand: 7/3 III.5.1 Magnetische Momente (Gouysche Waage) Ziel des Versuches Der Versuch dient dem ennenlernen der Grundbegriffe des magnetischen Feldes (Feldstärke, magnetische Induktion, Suszeptibilität,
in Molekülen: möglicherweise unterschiedliche Polarisierbarkeiten in verschiedenen Richtungen p = ᾱ E
 orlesung Dienstag. Maxwellgleichungen der Elektrostatik E = ρ ɛ 0 () B = 0 (2) E = 0 (3) B = µ 0 j (4).2 Polarisation Einteilung der Materie - Leiter (freie Ladungsträger) - Isolatoren (nur gebundene Ladungsträger)
orlesung Dienstag. Maxwellgleichungen der Elektrostatik E = ρ ɛ 0 () B = 0 (2) E = 0 (3) B = µ 0 j (4).2 Polarisation Einteilung der Materie - Leiter (freie Ladungsträger) - Isolatoren (nur gebundene Ladungsträger)
Elektrizitätslehre und Magnetismus
 Elektrizitätslehre und Magnetismus Othmar Marti 30. 06. 2008 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Physik Klassische und Relativistische Mechanik 30. 06.
Elektrizitätslehre und Magnetismus Othmar Marti 30. 06. 2008 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Physik Klassische und Relativistische Mechanik 30. 06.
Darstellung von Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4]
![Darstellung von Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4] Darstellung von Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4]](/thumbs/72/67239082.jpg) Versuch M3: Darstellung von Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4] Es sollen 3 g Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4] (wasserfrei) nach beiliegender Vorschrift dargestellt
Versuch M3: Darstellung von Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4] Es sollen 3 g Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4] (wasserfrei) nach beiliegender Vorschrift dargestellt
1.12. MAKROSKOPISCHE ELEKTROSTATIK 87. In den vorangegangenen Abschnitten hatten wir die beiden Grundgleichungen der Elektrostatik.
 .. MAKROSKOPISCHE ELEKTROSTATIK 87. Makroskopische Elektrostatik.. Polarisation, dielektrische erschiebung In den vorangegangenen Abschnitten hatten wir die beiden Grundgleichungen der Elektrostatik rot
.. MAKROSKOPISCHE ELEKTROSTATIK 87. Makroskopische Elektrostatik.. Polarisation, dielektrische erschiebung In den vorangegangenen Abschnitten hatten wir die beiden Grundgleichungen der Elektrostatik rot
Versuch 19 Dia- und Paramagnetismus
 Physikalisches Praktikum Versuch 19 Dia- und Paramagnetismus Praktikanten: Johannes Dörr Gruppe: 14 mail@johannesdoerr.de physik.johannesdoerr.de Datum: 12.02.2007 Katharina Rabe Assistent: Tobias Liese
Physikalisches Praktikum Versuch 19 Dia- und Paramagnetismus Praktikanten: Johannes Dörr Gruppe: 14 mail@johannesdoerr.de physik.johannesdoerr.de Datum: 12.02.2007 Katharina Rabe Assistent: Tobias Liese
Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen Mechanik).
 phys4.017 Page 1 10.4.2 Bahndrehimpuls des Elektrons: Einheit des Drehimpuls: Der Bahndrehimpuls des Elektrons ist quantisiert. Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen
phys4.017 Page 1 10.4.2 Bahndrehimpuls des Elektrons: Einheit des Drehimpuls: Der Bahndrehimpuls des Elektrons ist quantisiert. Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen
 Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
An welche Stichwörter von der letzten Vorlesung
 An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Der magnetische Fluss durch eine Schleife: da Φ = Das faradaysche Induktionsgesetz: Die Induktivität: l A L = NF i Die Spannung
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Der magnetische Fluss durch eine Schleife: da Φ = Das faradaysche Induktionsgesetz: Die Induktivität: l A L = NF i Die Spannung
Anorganische Chemie II
 Anorganische Chemie II Magnetismus Skript zur Vorlesung Magnetismus Mai 2007 Dieses Skript soll einen kurzen Überblick über Magnetismus und magnetische Phänome geben. Es ist als Ergänzung zum Skript zur
Anorganische Chemie II Magnetismus Skript zur Vorlesung Magnetismus Mai 2007 Dieses Skript soll einen kurzen Überblick über Magnetismus und magnetische Phänome geben. Es ist als Ergänzung zum Skript zur
Frage 1. Klausuraufgaben Grundvorlesung Testat vom , Seite 1 Punkte. Bitte eintragen: Matrikelnummer: Bitte ankreuzen: Biotechnologie Pharmazie
 Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Punkte Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Skizzieren Sie die
Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Punkte Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Skizzieren Sie die
Musterlösung 02/09/2014
 Musterlösung 0/09/014 1 Streuexperimente (a) Betrachten Sie die Streuung von punktförmigen Teilchen an einer harten Kugel vom Radius R. Bestimmen Sie die Ablenkfunktion θ(b) unter der Annahme, dass die
Musterlösung 0/09/014 1 Streuexperimente (a) Betrachten Sie die Streuung von punktförmigen Teilchen an einer harten Kugel vom Radius R. Bestimmen Sie die Ablenkfunktion θ(b) unter der Annahme, dass die
Praktikum Instrumentelle Analytik
 Praktikum Instrumentelle Analytik Sommersemester 2004 Protokoll zum Teil Magnetochemie Gruppe 1 Jasmin Fischer 1 1.1 Kurze Zusammenfassung der theoretischen Grundlagen für den Versuch Grundlage dieser
Praktikum Instrumentelle Analytik Sommersemester 2004 Protokoll zum Teil Magnetochemie Gruppe 1 Jasmin Fischer 1 1.1 Kurze Zusammenfassung der theoretischen Grundlagen für den Versuch Grundlage dieser
Frage 1. Klausuraufgaben Grundvorlesung Testat vom , Seite 1 Musterlösung. Bitte eintragen: Matrikelnummer: 0815 Name: Musterstudi.
 Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
Ferienkurs Experimentalphysik Lösung zur Übung 2
 Ferienkurs Experimentalphysik 4 01 Lösung zur Übung 1. Ermitteln Sie für l = 1 a) den Betrag des Drehimpulses L b) die möglichen Werte von m l c) Zeichnen Sie ein maßstabsgerechtes Vektordiagramm, aus
Ferienkurs Experimentalphysik 4 01 Lösung zur Übung 1. Ermitteln Sie für l = 1 a) den Betrag des Drehimpulses L b) die möglichen Werte von m l c) Zeichnen Sie ein maßstabsgerechtes Vektordiagramm, aus
Messung der Leitfähigkeit wässriger Elektrolytlösungen
 Versuch Nr. 10: Messung der Leitfähigkeit wässriger Elektrolytlösungen 1. Ziel des Versuchs In diesem Versuch sollen die Leitfähigkeiten von verschiedenen Elektrolyten in verschiedenen Konzentrationen
Versuch Nr. 10: Messung der Leitfähigkeit wässriger Elektrolytlösungen 1. Ziel des Versuchs In diesem Versuch sollen die Leitfähigkeiten von verschiedenen Elektrolyten in verschiedenen Konzentrationen
Musterlösung Übung 9
 Musterlösung Übung 9 Aufgabe 1: Elektronenkonfiguration und Periodensystem a) i) Lithium (Li), Grundzustand ii) Fluor (F), angeregter Zustand iii) Neon (Ne), angeregter Zustand iv) Vanadium (V), angeregter
Musterlösung Übung 9 Aufgabe 1: Elektronenkonfiguration und Periodensystem a) i) Lithium (Li), Grundzustand ii) Fluor (F), angeregter Zustand iii) Neon (Ne), angeregter Zustand iv) Vanadium (V), angeregter
Farbe der anorganischen Pigmente
 Farbe der anorganischen Pigmente 1. Farbigkeit der Komplex-Ionen (Ligandenfeld-Theorie) Einführung Versuch 1 Geben Sie einen halben Löffel festes Kupfersulfat in ein grosses Reagenzglas (RG) und erwärmen
Farbe der anorganischen Pigmente 1. Farbigkeit der Komplex-Ionen (Ligandenfeld-Theorie) Einführung Versuch 1 Geben Sie einen halben Löffel festes Kupfersulfat in ein grosses Reagenzglas (RG) und erwärmen
CHEMIE KAPITEL 1 AUFBAU DER MATERIE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2014 / 2015
 CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Atombau und Elementarteilchen Folie 3 Atommasse und Stoffmenge Stoffmenge [mol]: 12,000
CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Atombau und Elementarteilchen Folie 3 Atommasse und Stoffmenge Stoffmenge [mol]: 12,000
AC II Praktikum SoSe 04
 AC II Praktikum SoSe 04 Julia Blechinger Saal K Assistent: Constanze Vogler Durchführung: 05.05.04 Protokoll zur Präparategruppe 8: Übergangsmetallkomplexe Darstellung von [Co(NH 3 ) 5 Br]Br 2 I. Theoretischer
AC II Praktikum SoSe 04 Julia Blechinger Saal K Assistent: Constanze Vogler Durchführung: 05.05.04 Protokoll zur Präparategruppe 8: Übergangsmetallkomplexe Darstellung von [Co(NH 3 ) 5 Br]Br 2 I. Theoretischer
III Elektrizität und Magnetismus
 20. Vorlesung EP III Elektrizität und Magnetismus 19. Magnetische Felder 20. Induktion Versuche: Diamagnetismus, Supraleiter Induktion Leiterschleife, bewegter Magnet Induktion mit Änderung der Fläche
20. Vorlesung EP III Elektrizität und Magnetismus 19. Magnetische Felder 20. Induktion Versuche: Diamagnetismus, Supraleiter Induktion Leiterschleife, bewegter Magnet Induktion mit Änderung der Fläche
Elektrizitätslehre und Magnetismus
 Elektrizitätslehre und Magnetismus Othmar Marti 06. 07. 2009 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Physik Elektrizitätslehre und Magnetismus 06. 07. 2009
Elektrizitätslehre und Magnetismus Othmar Marti 06. 07. 2009 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Physik Elektrizitätslehre und Magnetismus 06. 07. 2009
Magnetismus. Prinzip: Kein Monopol nur Dipole. Kräfte:
 Elektromagnetismus Magnetismus Prinzip: Kein Monopol nur Dipole Kräfte: S N Richtung des Magnetischen Feldes I B Kraft auf Ladungen im B-Feld + Proportionalitätskonstante B FM = q v B Durch Messung: LORENTZ
Elektromagnetismus Magnetismus Prinzip: Kein Monopol nur Dipole Kräfte: S N Richtung des Magnetischen Feldes I B Kraft auf Ladungen im B-Feld + Proportionalitätskonstante B FM = q v B Durch Messung: LORENTZ
Magnetische Eigenschaften von Materie
 Magnetische Eigenschaften von Materie Abb. 1: Magnetisches Fluid im Feld eines starken, kugelförmigen Magneten zieht sich zu symmetrischen Mustern zusammen Geräteliste: Gasverflüssiger, Sauerstoff, Dewar
Magnetische Eigenschaften von Materie Abb. 1: Magnetisches Fluid im Feld eines starken, kugelförmigen Magneten zieht sich zu symmetrischen Mustern zusammen Geräteliste: Gasverflüssiger, Sauerstoff, Dewar
2.3. Atome in äusseren Feldern
 .3. Atome in äusseren Feldern.3.1. Der Zeeman-Effekt Nobelpreis für Physik 19 (...researches into the influence of magnetism upon radiation phenomena ) H. A. Lorentz P. Zeeman Die Wechselwirkung eines
.3. Atome in äusseren Feldern.3.1. Der Zeeman-Effekt Nobelpreis für Physik 19 (...researches into the influence of magnetism upon radiation phenomena ) H. A. Lorentz P. Zeeman Die Wechselwirkung eines
Elektronenspinresonanz-Spektroskopie
 Elektronenspinresonanz-Spektroskopie (ESR-Spektroskopie) engl.: Electron Paramagnetic Resonance Spectroscopy (EPR-Spectroscopy) Stephanie Dirksmeyer, 671197 Inhalt 1. Grundidee 2. physikalische Grundlagen
Elektronenspinresonanz-Spektroskopie (ESR-Spektroskopie) engl.: Electron Paramagnetic Resonance Spectroscopy (EPR-Spectroscopy) Stephanie Dirksmeyer, 671197 Inhalt 1. Grundidee 2. physikalische Grundlagen
Die zu dieser Zeit bekannten 63 Elemente konnten trotzdem nach ihren chemischen Eigenschaften in einem periodischen System angeordnet werden.
 phys4.022 Page 1 12.4 Das Periodensystem der Elemente Dimitri Mendeleev (1869): Ordnet man die chemischen Elemente nach ihrer Ladungszahl Z, so tauchen Elemente mit ähnlichen chemischen und physikalischen
phys4.022 Page 1 12.4 Das Periodensystem der Elemente Dimitri Mendeleev (1869): Ordnet man die chemischen Elemente nach ihrer Ladungszahl Z, so tauchen Elemente mit ähnlichen chemischen und physikalischen
LK Lorentzkraft. Inhaltsverzeichnis. Moritz Stoll, Marcel Schmittfull (Gruppe 2) 25. April Einführung 2
 LK Lorentzkraft Blockpraktikum Frühjahr 2007 (Gruppe 2) 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Magnetfeld dünner Leiter und Spulen......... 2 2.2 Lorentzkraft........................
LK Lorentzkraft Blockpraktikum Frühjahr 2007 (Gruppe 2) 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Magnetfeld dünner Leiter und Spulen......... 2 2.2 Lorentzkraft........................
c = Ausbreitungsgeschwindigkeit (2, m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 )
 2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
Theta (deg.)
 NaCl, MoKα, λ = 0.7107 Å Intensity (a.u.) 40000 31400 22800 14200 5600-3000 10 20 30 40 50 60 70 80 2 Theta (deg.) Atomare und molekulare Bewegung in Kristallen Temperaturbewegung erniedrigt die Auflösung
NaCl, MoKα, λ = 0.7107 Å Intensity (a.u.) 40000 31400 22800 14200 5600-3000 10 20 30 40 50 60 70 80 2 Theta (deg.) Atomare und molekulare Bewegung in Kristallen Temperaturbewegung erniedrigt die Auflösung
Ferienkurs Experimentalphysik 4
 Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Komplexchemie und Molekülgeometrie. Aufbau und Nomenklatur von Komplexverbindungen
 Aufbau und Nomenklatur von Komplexverbindungen Komplexverbindungen sind chemische Verbindungen, die aus einem Zentralatom und Molekülen bzw. Ionen gebildet werden. Aufbau von Komplexverbindungen Zentralatom
Aufbau und Nomenklatur von Komplexverbindungen Komplexverbindungen sind chemische Verbindungen, die aus einem Zentralatom und Molekülen bzw. Ionen gebildet werden. Aufbau von Komplexverbindungen Zentralatom
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+
![Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ Elektronenspektrum von [Ti(H 2 O) 6 ] 3+](/thumbs/66/55543366.jpg) Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
F. Atomare Ursachen des Magnetismus
 F. Atomare Ursachen des Magnetismus Im Folgenden sollen die atomaren Ursachen für den Magnetismus fester Stoffe erläutert werden. Die meisten Zusammenhänge lassen sich dabei auch auf flüssige gasförmige
F. Atomare Ursachen des Magnetismus Im Folgenden sollen die atomaren Ursachen für den Magnetismus fester Stoffe erläutert werden. Die meisten Zusammenhänge lassen sich dabei auch auf flüssige gasförmige
2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten
 Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Verwandte Begriffe Maxwell-Gleichungen, elektrisches Wirbelfeld, Magnetfeld von Spulen, magnetischer Fluss, induzierte Spannung.
 Verwandte Begriffe Maxwell-Gleichungen, elektrisches Wirbelfeld, Magnetfeld von Spulen, magnetischer Fluss, induzierte Spannung. Prinzip In einer langen Spule wird ein Magnetfeld mit variabler Frequenz
Verwandte Begriffe Maxwell-Gleichungen, elektrisches Wirbelfeld, Magnetfeld von Spulen, magnetischer Fluss, induzierte Spannung. Prinzip In einer langen Spule wird ein Magnetfeld mit variabler Frequenz
Magnetische Eigenschaften von periodisch angeordneten Nanopartikeln aus Nickel
 Naturwissenschaft Martina Meincken Magnetische Eigenschaften von periodisch angeordneten Nanopartikeln aus Nickel Diplomarbeit Magnetische Eigenschaften von periodisch angeordneten Nanopartikeln aus Nickel
Naturwissenschaft Martina Meincken Magnetische Eigenschaften von periodisch angeordneten Nanopartikeln aus Nickel Diplomarbeit Magnetische Eigenschaften von periodisch angeordneten Nanopartikeln aus Nickel
Zusammenfassung v13 vom 20. Juni 2013
 Zusammenfassung v13 vom 20. Juni 2013 Magnetfeldberechnungen Gerader Leiter im Abstand r: B = µ 0 I/(2 r) (57) Auf der Achse einer Leiterschleife mit Radius R im Abstand x von der Mitte der Schleife: B
Zusammenfassung v13 vom 20. Juni 2013 Magnetfeldberechnungen Gerader Leiter im Abstand r: B = µ 0 I/(2 r) (57) Auf der Achse einer Leiterschleife mit Radius R im Abstand x von der Mitte der Schleife: B
Versuch E11 - Hysterese Aufnahme einer Neukurve. Abgabedatum: 24. April 2007
 Versuch E11 - Hysterese Aufnahme einer Neukurve Sven E Tobias F Abgabedatum: 24. April 2007 Inhaltsverzeichnis 1 Ziel des Versuchs 3 2 Physikalischer Zusammenhang 3 2.1 Magnetisches Feld..........................
Versuch E11 - Hysterese Aufnahme einer Neukurve Sven E Tobias F Abgabedatum: 24. April 2007 Inhaltsverzeichnis 1 Ziel des Versuchs 3 2 Physikalischer Zusammenhang 3 2.1 Magnetisches Feld..........................
A. Mezzetti Fragenkatalog X
 Anorganische Chemie I Elektronenespektren A. Mezzetti ragenkatalog X 1. K n [V 6 ] (n muss bestimmt werden) (B) hat µ eff = 2.66 BM. Sein UV-VIS-Spektrum enthält eine sehr schwache Bande (10'000 cm 1 )
Anorganische Chemie I Elektronenespektren A. Mezzetti ragenkatalog X 1. K n [V 6 ] (n muss bestimmt werden) (B) hat µ eff = 2.66 BM. Sein UV-VIS-Spektrum enthält eine sehr schwache Bande (10'000 cm 1 )
 Übungen zu Experimentalphysik 4 - Lösungsvorschläge Prof. S. Paul Sommersemester 005 Dr. Jan Friedrich Nr. 5 16.05.005 Email Jan.Friedrich@ph.tum.de Telefon 089/89-1586 Physik Department E18, Raum 3564
Übungen zu Experimentalphysik 4 - Lösungsvorschläge Prof. S. Paul Sommersemester 005 Dr. Jan Friedrich Nr. 5 16.05.005 Email Jan.Friedrich@ph.tum.de Telefon 089/89-1586 Physik Department E18, Raum 3564
VL11. Das Wasserstofatom in der QM II Energiezustände des Wasserstoffatoms Radiale Abhängigkeit (Laguerre-Polynome)
 VL 13 VL11. Das Wasserstofatom in der QM II 11.1. Energiezustände des Wasserstoffatoms 11.2. Radiale Abhängigkeit (Laguerre-Polynome) VL12. Spin-Bahn-Kopplung (I) 12.1 Bahnmagnetismus (Zeeman-Effekt) 12.2
VL 13 VL11. Das Wasserstofatom in der QM II 11.1. Energiezustände des Wasserstoffatoms 11.2. Radiale Abhängigkeit (Laguerre-Polynome) VL12. Spin-Bahn-Kopplung (I) 12.1 Bahnmagnetismus (Zeeman-Effekt) 12.2
11. Elektrodynamik Das Gaußsche Gesetz 11.2 Kraft auf Ladungen Punktladung im elektrischen Feld Dipol im elektrischen Feld
 Inhalt 11. Elektrodynamik 11.1 Das Gaußsche Gesetz 11.2 Kraft auf Ladungen 11.2.1 Punktladung im elektrischen Feld 11. Elektromagnetische Kraft 11 Elektrodynamik 11. Elektrodynamik (nur Vakuum = Ladung
Inhalt 11. Elektrodynamik 11.1 Das Gaußsche Gesetz 11.2 Kraft auf Ladungen 11.2.1 Punktladung im elektrischen Feld 11. Elektromagnetische Kraft 11 Elektrodynamik 11. Elektrodynamik (nur Vakuum = Ladung
Magnetismus. Referat zu Theoretische Physik für das Lehramt 2, WS 2013/2014
 Magnetismus Andreas Wiederin David Gröbner Referat zu Theoretische Physik für das Lehramt 2, WS 2013/2014 Vorbemerkungen Ein grundlegendes (klassisches) Verständnis des Magnetismus, wie in den Lehrveranstaltungen
Magnetismus Andreas Wiederin David Gröbner Referat zu Theoretische Physik für das Lehramt 2, WS 2013/2014 Vorbemerkungen Ein grundlegendes (klassisches) Verständnis des Magnetismus, wie in den Lehrveranstaltungen
Beispielaufgaben IChO 2. Runde 2019 Koordinationschemie
 Beispiel 1 Metalle und Elektronen Bei der Besetzung von Atomorbitalen werden die Elektronen ausgehend vom energetisch am tiefsten liegenden Atomorbital in Richtung ansteigender Energie mit den Elektronen
Beispiel 1 Metalle und Elektronen Bei der Besetzung von Atomorbitalen werden die Elektronen ausgehend vom energetisch am tiefsten liegenden Atomorbital in Richtung ansteigender Energie mit den Elektronen
Atombau. Chemie. Zusammenfassungen. Prüfung Mittwoch, 14. Dezember Elektrische Ladung. Elementarteilchen. Kern und Hülle
 Chemie Atombau Zusammenfassungen Prüfung Mittwoch, 14. Dezember 2016 Elektrische Ladung Elementarteilchen Kern und Hülle Atomsorten, Nuklide, Isotope Energieniveaus und Schalenmodell Steffi Alle saliorel
Chemie Atombau Zusammenfassungen Prüfung Mittwoch, 14. Dezember 2016 Elektrische Ladung Elementarteilchen Kern und Hülle Atomsorten, Nuklide, Isotope Energieniveaus und Schalenmodell Steffi Alle saliorel
EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel )
 EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel 5.4.6.1-3) 1 1. Definition eines Komplexes (A. Werner ca. 1900): Ein Komplex ist eine Koordinationsverbindung, in der das Zentralatom (eine Lewis-Säure)
EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel 5.4.6.1-3) 1 1. Definition eines Komplexes (A. Werner ca. 1900): Ein Komplex ist eine Koordinationsverbindung, in der das Zentralatom (eine Lewis-Säure)
11. Elektrodynamik Das Gaußsche Gesetz 11.2 Kraft auf Ladungen Punktladung im elektrischen Feld Dipol im elektrischen Feld
 11. Elektrodynamik Physik für ETechniker 11. Elektrodynamik 11.1 Das Gaußsche Gesetz 11.2 Kraft auf Ladungen 11.2.1 Punktladung im elektrischen Feld 11.2.2 Dipol im elektrischen Feld 11. Elektrodynamik
11. Elektrodynamik Physik für ETechniker 11. Elektrodynamik 11.1 Das Gaußsche Gesetz 11.2 Kraft auf Ladungen 11.2.1 Punktladung im elektrischen Feld 11.2.2 Dipol im elektrischen Feld 11. Elektrodynamik
2 Elektrostatik. 2.1 Coulomb-Kraft und elektrische Ladung. 2.1 Coulomb-Kraft und elektrische Ladung
 2.1 Coulomb-Kraft und elektrische Ladung 2 Elektrostatik 2.1 Coulomb-Kraft und elektrische Ladung Abb. 2.1 Durch Reiben verschiedener Stoffe aneinander verbleiben Elektronen der Atomhüllen überwiegend
2.1 Coulomb-Kraft und elektrische Ladung 2 Elektrostatik 2.1 Coulomb-Kraft und elektrische Ladung Abb. 2.1 Durch Reiben verschiedener Stoffe aneinander verbleiben Elektronen der Atomhüllen überwiegend
Magnetismus. Prinzip: Kein Monopol nur Dipole. Kräfte:
 Elektromagnetismus Magnetismus Prinzip: Kein Monopol nur Dipole Kräfte: S N Richtung des Magnetischen Feldes I B Kraft auf Ladungen im B-Feld + Proportionalitätskonstante B FM = q v B Durch Messung: LORENTZ
Elektromagnetismus Magnetismus Prinzip: Kein Monopol nur Dipole Kräfte: S N Richtung des Magnetischen Feldes I B Kraft auf Ladungen im B-Feld + Proportionalitätskonstante B FM = q v B Durch Messung: LORENTZ
E5: Faraday-Konstante
 E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Mößbauer-Spektroskopie Vortrag zum apparativen Praktikum SS 05. Hella Berlemann Nora Obermann
 Mößbauer-Spektroskopie Vortrag zum apparativen Praktikum SS 05 Hella Berlemann Nora Obermann Übersicht: Mößbauer (1958): rückstoßfreie Kernresonanzabsorption von γ-strahlen γ-strahlung: kurzwellige, hochenergetische,
Mößbauer-Spektroskopie Vortrag zum apparativen Praktikum SS 05 Hella Berlemann Nora Obermann Übersicht: Mößbauer (1958): rückstoßfreie Kernresonanzabsorption von γ-strahlen γ-strahlung: kurzwellige, hochenergetische,
Demonstration der "Elektronenreibung" in Metallen
 Stromdurchflossene Leiter im Magnetfeld Barlowsches Rad: Demonstration der "Elektronenreibung" in Metallen Anlegen einer Spannung zwischen Achse und Quecksilberwanne führt zu einem Strom durch die Scheibe
Stromdurchflossene Leiter im Magnetfeld Barlowsches Rad: Demonstration der "Elektronenreibung" in Metallen Anlegen einer Spannung zwischen Achse und Quecksilberwanne führt zu einem Strom durch die Scheibe
10. Elektrodynamik Physik für E-Techniker. 10. Elektrodynamik Kraft auf Ladungen Dipol im elektrischen Feld. Doris Samm FH Aachen
 10. Elektrodynamik 10.11 Das Gaußsche Gesetz 10.2 Kraft auf Ladungen 1021P 10.2.1 Punktladung im elektrischen kti Feld 10.2.2 Dipol im elektrischen Feld Einleitung (wir hatten) Es gibt (genau) zwei Arten
10. Elektrodynamik 10.11 Das Gaußsche Gesetz 10.2 Kraft auf Ladungen 1021P 10.2.1 Punktladung im elektrischen kti Feld 10.2.2 Dipol im elektrischen Feld Einleitung (wir hatten) Es gibt (genau) zwei Arten
E2: Wärmelehre und Elektromagnetismus 18. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 18. Vorlesung 21.06.2018 Barlow-Rad Heute: Telefon nach Bell - Materie im Magnetfeld: Dia-, Para-, Ferromagnetismus - Supraleitung - Faradaysches Induktionsgesetz
E2: Wärmelehre und Elektromagnetismus 18. Vorlesung 21.06.2018 Barlow-Rad Heute: Telefon nach Bell - Materie im Magnetfeld: Dia-, Para-, Ferromagnetismus - Supraleitung - Faradaysches Induktionsgesetz
Ferienkurs Experimentalphysik Übung 2 - Musterlösung
 Ferienkurs Experimentalphysik 4 00 Übung - Musterlösung Kopplung von Drehimpulsen und spektroskopische Notation (*) Vervollständigen Sie untenstehende Tabelle mit den fehlenden Werten der Quantenzahlen.
Ferienkurs Experimentalphysik 4 00 Übung - Musterlösung Kopplung von Drehimpulsen und spektroskopische Notation (*) Vervollständigen Sie untenstehende Tabelle mit den fehlenden Werten der Quantenzahlen.
Magnetische Suszeptibilität: Magnetismusarten
 agnetische Suszeptibilität, agnetismusarten agnetische Suszeptibilität: Im allgemeinen ist H: = χ m H χ m = magnetische Suszeptibilität [χ m ] = 1 Damit wird: at = µ 0 ( H + ) = µ 0 (1 + χ m ) }{{} =µ
agnetische Suszeptibilität, agnetismusarten agnetische Suszeptibilität: Im allgemeinen ist H: = χ m H χ m = magnetische Suszeptibilität [χ m ] = 1 Damit wird: at = µ 0 ( H + ) = µ 0 (1 + χ m ) }{{} =µ
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl
Anorganische Chemie für Biologen. Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/
 Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Inhalte Stöchiometrie chemisches Rechnen Chemisches Gleichgewicht
Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Inhalte Stöchiometrie chemisches Rechnen Chemisches Gleichgewicht
3.7 Elektronenspinresonanz, Bestimmung des g-faktors
 1 Einführung Physikalisches Praktikum für Anfänger - Teil 1 Gruppe 3 - Atomphysik 3.7 Elektronenspinresonanz, Bestimmung des g-faktors Die Elektronenspinresonanz (ESR) ist ein Verfahren, das in vielen
1 Einführung Physikalisches Praktikum für Anfänger - Teil 1 Gruppe 3 - Atomphysik 3.7 Elektronenspinresonanz, Bestimmung des g-faktors Die Elektronenspinresonanz (ESR) ist ein Verfahren, das in vielen
Aufbau von Atomen. Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem
 Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
3.5. Materie im Magnetfeld. Exp. 36: Dipol im Magnetfeld. Exp. 25b Magnetisierung eines Stahldrahtes Magnetisches Moment
 - 205-3.5. Materie im Magnetfeld 3.5.1. Magnetisches Moment Wie wir bei der Diskussion der stromdurchflossenen Leiterschleife gesehen hatten erzeugen elektrische Kreisströme magnetische Dipolmomente Exp.
- 205-3.5. Materie im Magnetfeld 3.5.1. Magnetisches Moment Wie wir bei der Diskussion der stromdurchflossenen Leiterschleife gesehen hatten erzeugen elektrische Kreisströme magnetische Dipolmomente Exp.
Physikalisches Praktikum 3. Semester
 Torsten Leddig 3.November 004 Mathias Arbeiter Betreuer: Dr.Hoppe Physikalisches Praktikum 3. Semester - Feldmessung - 1 Aufgaben: 1. Elektrisches Feld 1.1 Nehmen Sie den Potenziallinienverlauf einer der
Torsten Leddig 3.November 004 Mathias Arbeiter Betreuer: Dr.Hoppe Physikalisches Praktikum 3. Semester - Feldmessung - 1 Aufgaben: 1. Elektrisches Feld 1.1 Nehmen Sie den Potenziallinienverlauf einer der
2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment
 Prof. Dieter Suter / Prof. Roland Böhmer Magnetische Resonanz SS 03 2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment 2.1.1 Felder und Dipole; Einheiten Wir beginnen mit einer
Prof. Dieter Suter / Prof. Roland Böhmer Magnetische Resonanz SS 03 2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment 2.1.1 Felder und Dipole; Einheiten Wir beginnen mit einer
4.7 Magnetfelder von Strömen Magnetfeld eines geraden Leiters
 4.7 Magnetfelder von Strömen Aus den vorherigen Kapiteln ist bekannt, dass auf stromdurchflossene Leiter im Magnetfeld eine Kraft wirkt. Die betrachteten magnetischen Felder waren bisher homogene Felder
4.7 Magnetfelder von Strömen Aus den vorherigen Kapiteln ist bekannt, dass auf stromdurchflossene Leiter im Magnetfeld eine Kraft wirkt. Die betrachteten magnetischen Felder waren bisher homogene Felder
