Checkliste für den Beginn, den Verlauf und den Abschluss einer Behandlung mit Gilenya (Fingolimod)
|
|
|
- Georg Eberhardt
- vor 6 Jahren
- Abrufe
Transkript
1 Checkliste für den Beginn, den Verlauf und den Abschluss einer Behandlung mit Gilenya (Fingolimod) Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen, siehe Abschnitt 4.8 der Fachinformation. Diese Checkliste für Ärzte wurde als Teil der Zulassungsauflagen erstellt und mit dem Bundesinstitut für Arzneimittel und Medizinprodukte abgestimmt. Im Rahmen des Risikomanagement-Plans wurden über die Routinemaßnahmen hinaus zusätzliche risikominimierende Maßnahmen mit der Zulassung des Arzneimittels beauflagt, um das Risiko des Auftretens von schwerwiegenden Nebenwirkungen zu reduzieren und das Nutzen-Risiko-Verhältnis von Fingolimod zu erhöhen. Diese Checkliste ist damit verpflichtender Teil der Zulassung, um sicherzustellen, dass Angehörige der Heilberufe, die Fingolimod verschreiben und zur Anwendung bringen, die besonderen Sicherheitsanforderungen kennen und berücksichtigen. Folgende Checkliste und schematische Darstellung sind als Hilfestellung im Rahmen des Therapiemanagements von Patienten mit Fingolimod gedacht. Wichtige Schritte und Hinweise werden für den Therapiebeginn, den Zeitraum während der Therapie und bei Behandlungsende mit Fingolimod beschrieben. Angaben zum Patienten Vorname Nachname männlich weiblich Geburtsdatum Datum der Aufklärung Datum des Therapiebeginns 1
2 Vor Therapiebeginn Vor Behandlungsbeginn mit Fingolimod muss die gleichzeitige Einnahme folgender Arzneimittel ausgeschlossen werden: keine gleichzeitige Gabe von Fingolimod und Antiarrhythmika der Klasse Ia (z. B. Chinidin, Disopyramid) oder der Klasse III (z. B. Amiodaron, Sotalol) oder antineoplastischen, immunsuppressiven oder immunmodulierenden Therapien. Bei gleichzeitiger Anwendung besteht das Risiko von additiven Effekten auf das Immunsystem. Wird bei Patienten eine Kombinationstherapie mit Kortikosteroiden über einen längeren Zeitraum in Betracht gezogen, ist zu prüfen, ob der zu erwartende Nutzen die möglichen Risiken überwiegt. Sind die Transaminasen (ALT, AST) und Bilirubin bestimmt worden (nicht älter als 6 Monate)? Liegt ein aktuelles großes Blutbild vor (nicht älter als 6 Monate oder nach Absetzung der vorherigen Therapie)? Ist beachtet worden, dass bei Patienten mit schweren aktiven Infektionen der Behandlungsbeginn mit Fingolimod verschoben werden sollte, bis die Infektion abgeklungen ist? Wurde vor der Erstgabe von Fingolimod ein EKG durchgeführt und der Blutdruck gemessen? Liegt eine der folgenden kardiovaskulären Erkrankungen bei dem Patienten vor? Fingolimod sollte nicht verabreicht werden bei Patienten mit diesen kardiovaskulären Erkrankungen: Bradyarrhythmie, beinhaltet: AV-Block 2. Grades Typ Mobitz 2 oder einen AV-Block höheren Grades, Sick-Sinus-Syndrom, sinuatriale Blockierungen. Signifikante QT-Verlängerungen (QTc > 470 ms (Frauen) oder > 450 ms (Männer)). (QTc: frequenzkorrigierte QT-Zeit) Anamnestisch bekannte symptomatische Bradykardie oder rezidivierende Synkopen, signifikante kardiovaskuläre Erkrankungen (beinhaltet: bekannte ischämische Herzerkrankung (einschließlich Angina pectoris), anamnestisch bekannter Myokardinfarkt, kongestive Herzinsuffizienz, anamnestisch bekannter Herzstillstand), unkontrollierte Hypertonie, zerebrovaskuläre Erkrankung oder schwere Schlafapnoe. Wird bei diesen Patienten eine Behandlung mit Fingolimod in Betracht gezogen, ist zu prüfen: Überwiegt der zu erwartende Nutzen die möglichen Risiken? Ist die Konsultation eines Kardiologen erfolgt? Wird die Behandlung mit Fingolimod in Betracht gezogen, ist eine verlängerte Überwachung, mindestens über Nacht, für den Therapiebeginn empfohlen. Nimmt der Patient eine der folgenden Herzfrequenz-senkenden Medikationen ein? 2
3 Die Therapie mit Fingolimod sollte nicht bei Patienten begonnen werden, welche folgende antiarrhythmische Medikationen erhalten, die die Herzfrequenz verlangsamen: Beta-Blocker Kalziumkanal-Blocker, die eine Abnahme der Herzfrequenz herbeiführen (z. B. Verapamil, Diltiazem oder Ivabradin) andere Wirkstoffe, die die Herzfrequenz verlangsamen können (z. B. Digoxin, Cholinesterasehemmer oder Pilocarpin) Wird bei diesen Patienten eine Behandlung mit Fingolimod in Betracht gezogen, ist zu prüfen: Überwiegt der zu erwartende Nutzen die möglichen Risiken? Ist die Konsultation eines Kardiologen erfolgt, um auf ein Arzneimittel zu wechseln, das keine Abnahme der Herzfrequenz herbeiführt? Wenn ein Therapiewechsel nicht möglich ist, wird eine verlängerte Überwachung, mindestens über Nacht, für den Therapiebeginn empfohlen. Hierzu sollte ein Kardiologe konsultiert werden, um eine geeignete Überwachung während des Therapiebeginns zu gewährleisten. Bei negativer Windpockenanamnese oder negativer VZV-Impfanamnese: Ist eine Bestimmung des VZV-Antikörper-Titers erfolgt? Bei negativem Antikörpertest ist eine VZV-Impfung durchzuführen und der Behandlungsbeginn entsprechend um einen Monat aufzuschieben, damit die Impfung ihre volle Wirkung entfalten kann. Hat eine ophthalmologische Untersuchung vor der Behandlung bei Patienten mit anamnestisch bekannter Uveitis oder Diabetes mellitus stattgefunden? Wurde die Erinnerungskarte für Patienten ausgehändigt? Aufklärung über potentielle Risiken für das ungeborene Kind und Maßnahmen zur Empfängnisverhütung Liegt ein negatives Ergebnis eines Schwangerschaftstests vor? Erfolgt eine aktive Empfängnisverhütung? Ist eine Überweisung an den behandelnden Gynäkologen zur Abklärung und Einleitung einer Empfängnisverhütung erforderlich? Eine Umstellung auf ein anderes Kontrazeptivum durch einen Gynäkologen kann erforderlich sein. 3
4 Die Patientin wurde aufgeklärt über das potentielle teratogene Risiko für das ungeborene Kind. über die Notwendigkeit einer zuverlässigen Empfängnisverhütung. während der letzten vier Wochen vor dem Beginn der Behandlung. für die gesamte Dauer der Behandlung, auch während einer Therapiepause. während der ersten 2 Monate nach Beendigung der Behandlung. oder alternativ über die Notwendigkeit des absoluten und ununterbrochenen Verzichts auf jeglichen Geschlechtsverkehr während der Behandlung. dass sie selbst bei Vorliegen einer Amenorrhoe die Hinweise zur Kontrazeption beachten muss. über die potentiellen Folgen einer Schwangerschaft und die Notwendigkeit, die Behandlung unverzüglich abzubrechen und sofort ärztlichen Rat zu suchen, falls die Möglichkeit einer Schwangerschaft besteht. Die Patientin stellt eine wirksame Empfängnisverhütungsmethode durch folgende Maßnahme sicher: Ein Schwangerschaftstest sollte in regelmäßigen Abständen wiederholt werden. Therapiebeginn Es wird eine kontinuierliche (Echtzeit-) EKG-Überwachung während der ersten 6 Stunden nach der Erstgabe von Fingolimod empfohlen. Hat eine kontinuierliche 6-stündige (Echtzeit-) EKG-Überwachung nach der Erstgabe von Fingolimod stattgefunden? Wurden während der 6-stündigen Überwachung stündlich Puls und Blutdruck gemessen? Wurde ein EKG 6 Stunden nach Therapiebeginn durchgeführt? 4
5 Überwachung für mindestens 6 Stunden EKG und Blutdruckmessung vor Erstgabe. Stündliche Messungen von Puls und Blutdruck während der ersten 6 Stunden nach Verabreichung der ersten Fingolimod- Dosis auf Zeichen und Symptome einer Bradykardie. Falls der Patient symptomatisch wird, sollte die Überwachung bis zur Rückbildung verlängert werden. Kontinuierliche (Echtzeit-) EKG-Überwachung während der ersten 6 Stunden empfohlen. EKG nach 6 Stunden. War eine medikamentöse Intervention während der Überwachungsphase notwendig? Verlängerte Überwachung über Nacht in einer medizinischen Einrichtung. Die Maßnahmen zur Überwachung der Erstgabe sollten bei der Zweitgabe von Fingolimod erneut durchgeführt werden. Ist ein AV-Block 3. Grades zu jeglichem Zeitpunkt während der Überwachungsphase aufgetreten? Trifft eines der folgenden Kriterien am Ende der Überwachungsphase zu? Herzfrequenz < 45 Schläge pro Minute QTc Intervall 500ms EKG zeigt neu aufgetretenen AV-Block 2. Grades oder höhergradigen AV-Block Verlängerte Überwachung bis zur Rückbildung, mindestens über Nacht. Ist die Herzfrequenz 6 Stunden nach der ersten Dosis am niedrigsten? Verlängerte Überwachung mindestens 2 weitere Stunden bis die Herzfrequenz wieder steigt. 6-Stunden-Überwachung ist abgeschlossen. QTc: frequenzkorrigierte QT-Zeit 5
6 Während der Therapie Regelmäßig: Regelmäßige Bestimmung des großen Blutbildes während der Behandlung, in Monat 3, danach mindestens jährlich und bei Anzeichen von Infektionen. Bei einer bestätigten Gesamtlymphozytenzahl von < 0,2 x 10 9 /l soll die Behandlung bis zur Besserung unterbrochen werden. In den Monaten 1, 3, 6, 9 und 12 nach Behandlungsbeginn und regelmäßig danach sowie bei Anzeichen einer Leberfunktionsstörung: Bestimmung der Lebertransaminasen (ALT, AST). Falls die Werte der Lebertransaminasen das 5-Fache des ULN übersteigen, sollte die Leberfunktion häufiger überwacht werden und die Therapie bei anhaltend hohen Lebertransaminasen-Werten bis zu einer Erholung unterbrochen werden. Wenn die Behandlung wie folgt unterbrochen wurde: innerhalb der ersten zwei Behandlungswochen einen oder mehr als einen Tag während der 3. und 4. Woche mehr als sieben Tage oder nach dem ersten Behandlungsmonat mehr als zwei Wochen sind bei Wiederaufnahme der Therapie, für den Zeitraum von mindestens 6 Stunden, die gleichen kardiovaskulären Maßnahmen (inkl. EKG, Puls- und Blutdruckkontrolle) wie bei der Erstgabe durchzuführen. 3 4 Monate nach Behandlungsbeginn: Wurde eine umfassende ophthalmologische Untersuchung zur Früherkennung eines Makulaödems und Beeinträchtigung des Sehvermögens durchgeführt? Regelmäßige ophthalmologische Untersuchung bei Patienten mit einer Uveitis oder Diabetes mellitus in der Anamnese. Wurde der Patient darauf hingewiesen, jegliche Verschlechterung der Sehfähigkeit zu berichten? Falls sich die Sehfähigkeit verschlechtert: Wurde eine Funduskopie inklusive Untersuchung der Makula durchgeführt und die Behandlung unterbrochen, sofern ein Makulaödem bestätigt wurde? Wurde der Patient darauf hingewiesen, jegliche Anzeichen und Symptome einer Infektion zu berichten? Bei Anzeichen einer Infektion: Sofern indiziert, wurde eine antimikrobielle Behandlung initiiert? Wurden bei Symptomen einer Kryptokokkenmeningitis (z. B. Kopfschmerzen, die mit psychischen Veränderungen wie Verwirrtheit, Halluzinationen und / oder Veränderungen der Persönlichkeit einhergehen) umgehend diagnostische Maßnahmen eingeleitet? Wurde bei Diagnose einer Kryptokokkenmeningitis eine entsprechende Behandlung eingeleitet? Gibt es klinische Symptome oder MRT-Befunde, die auf eine PML hindeuten könnten? Wurde bei Hinweisen auf eine PML die Therapie unterbrochen bis eine PML ausgeschlossen werden konnte? Wurde die Behandlung mit Fingolimod während schwerer Infektionen abgesetzt? 6
7 Bei Impfungen: Wurde darauf hingewiesen, dass während der Behandlung und bis zu 2 Monate nach Behandlungsende: Impfungen möglicherweise weniger effektiv sind und attenuierte Lebendimpfstoffe das Risiko einer Infektion erhöhen und vermieden werden sollten? Bei einer Schwangerschaft: Wurde in regelmäßigen Abständen ein Schwangerschaftstest durchgeführt? Wurde die Behandlung abgebrochen, als die Patientin schwanger wurde? Wurde an Novartis per Fax ( ) oder elektronisch (ams.novartis@novartis.com) von schwangeren Patientinnen berichtet, welche während der Schwangerschaft oder auch während 8 Wochen vor der letzten Menstruation Fingolimod eingenommen haben? Wurde im Falle einer Schwangerschaft die Patientin an das Gilenya /Fingolimod Schwangerschaftsregister gemeldet? Nähere Informationen finden sich in der Informationsbroschüre sowie unter Bei Veränderungen der Haut: Wurde eine Überwachung verdächtiger Hautläsionen (bezüglich Basalzellkarzinom) vorgenommen? Nach Behandlungsende Wenn die Behandlung wie folgt unterbrochen wurde: innerhalb der ersten zwei Behandlungswochen einen oder mehr als einen Tag während der 3. und 4. Woche mehr als sieben Tage oder nach dem ersten Behandlungsmonat mehr als zwei Wochen sind bei Wiederaufnahme der Therapie, für den Zeitraum von mindestens 6 Stunden, die gleichen kardiovaskulären Maßnahmen (inkl. EKG, Puls- und Blutdruckkontrolle) wie bei der Erstgabe durchzuführen. Ist die Patientin im gebärfähigen Alter auf die notwendige Kontrazeption bis zu 2 Monate nach Beendigung der Therapie mit Fingolimod hingewiesen worden? Hat eine Aufklärung des Patienten stattgefunden, dass jegliche Anzeichen oder Symptome einer Infektion bis zu 2 Monate nach Beendigung der Therapie mit Fingolimod dem behandelnden Arzt zu berichten sind? 7
8 Der Patient/die Patientin wurde aufgeklärt dass das verschriebene Medikament nicht an andere Personen weitergegeben werden darf. dass nicht verwendetes Fingolimod an die Apotheke zurückgegeben werden muss. dass während der Einnahme von Fingolimod und während der ersten 2 Monate nach Beendigung der Einnahme kein Blut gespendet werden darf. Novartis Pharma GmbH Roonstr Nürnberg Version 8.1 Stand 02/2016 Genehmigung XX/201XX Art.Nr
Überarbeitete Empfehlung, wann die Überwachung analog zur Erstgabe von Gilenya (Fingolimod) wiederholt werden sollte
 Novartis Pharma GmbH Postfachadresse 90327 Nürnberg Tel 0911/273-0 Fax 0911/273-12160 www.novartis.de Überarbeitete Empfehlung, wann die Überwachung analog zur Erstgabe von Gilenya (Fingolimod) wiederholt
Novartis Pharma GmbH Postfachadresse 90327 Nürnberg Tel 0911/273-0 Fax 0911/273-12160 www.novartis.de Überarbeitete Empfehlung, wann die Überwachung analog zur Erstgabe von Gilenya (Fingolimod) wiederholt
Wichtige Informationen für medizinische Fachkräfte über die ernsten Risiken im Zusammenhang mit CAPRELSA -Tabletten
 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert,
Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert,
Erivedge (Vismodegib): Wichtige Informationen für die sichere Anwendung, einschließlich Informationen zum Schwangerschaftsverhütungs-Programm
 Erivedge (Vismodegib): Wichtige Informationen für die sichere Anwendung, einschließlich Informationen zum Schwangerschaftsverhütungs-Programm Sehr geehrte Frau Doktor, sehr geehrter Herr Doktor, Dieses
Erivedge (Vismodegib): Wichtige Informationen für die sichere Anwendung, einschließlich Informationen zum Schwangerschaftsverhütungs-Programm Sehr geehrte Frau Doktor, sehr geehrter Herr Doktor, Dieses
Therapie mit Acitretin-haltigen Arzneimitteln: Was Sie wissen müssen
 Therapie mit Acitretin-haltigen Arzneimitteln: Was Sie wissen müssen Informationsbroschüre für männliche Patienten und Patientinnen, die nicht im gebärfähigen Alter sind Diese Informationsbroschüre wurde
Therapie mit Acitretin-haltigen Arzneimitteln: Was Sie wissen müssen Informationsbroschüre für männliche Patienten und Patientinnen, die nicht im gebärfähigen Alter sind Diese Informationsbroschüre wurde
INFORMATIONSBROSCHÜRE FÜR PERSONEN MIT TRUVADA ZUR PRÄ-EXPOSITIONS-PROPHYLAXE (PrEP)
 INFORMATIONSBROSCHÜRE FÜR PERSONEN MIT TRUVADA ZUR PRÄ-EXPOSITIONS-PROPHYLAXE (PrEP) Wichtige Informationen zu Truvada (Emtricitabin/ Tenofovirdisoproxilfumarat), um das Risiko einer Infektion mit dem
INFORMATIONSBROSCHÜRE FÜR PERSONEN MIT TRUVADA ZUR PRÄ-EXPOSITIONS-PROPHYLAXE (PrEP) Wichtige Informationen zu Truvada (Emtricitabin/ Tenofovirdisoproxilfumarat), um das Risiko einer Infektion mit dem
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit.
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit.
Anhang III. Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage
 Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
Informationsbroschüre für Patienten Was Sie wissen müssen
 Europa hat Bedingungen für die Markteinführung des Arzneimittels VOLIBRIS gestellt (europaweit eingetragen). Dieser in Belgien und Luxemburg obligatorische Risikomanagementplan, zu dem dieses Informationsschreiben
Europa hat Bedingungen für die Markteinführung des Arzneimittels VOLIBRIS gestellt (europaweit eingetragen). Dieser in Belgien und Luxemburg obligatorische Risikomanagementplan, zu dem dieses Informationsschreiben
FORMULAR FÜR DEN START DER BEHANDLUNG MIT TYSABRI
 Die europäischen Gesundheitsbehörden haben für die Markteinführung von TYSABRI Bedingungen auferlegt. Dieser verpflichtende Plan zur Risikoeinschränkung in Belgien - zu dem diese Information gehört - ist
Die europäischen Gesundheitsbehörden haben für die Markteinführung von TYSABRI Bedingungen auferlegt. Dieser verpflichtende Plan zur Risikoeinschränkung in Belgien - zu dem diese Information gehört - ist
WICHTIGE INFORMATIONEN FÜR PATIENTEN
 WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung der mittelschweren bis schweren Plaque-Psoriasis bzw. aktiven psoriatischen Arthritis verschrieben wurde 2 Version 5 (Stand: Februar 2017)
WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung der mittelschweren bis schweren Plaque-Psoriasis bzw. aktiven psoriatischen Arthritis verschrieben wurde 2 Version 5 (Stand: Februar 2017)
Broschüre zur Aufklärung von Patienten
 Broschüre zur Aufklärung von Patienten Ihnen wurde Jinarc verordnet, weil Sie eine autosomal-dominante polyzystische Nierenerkrankung bzw. ADPKD haben, die ein Wachstum von Zysten in den Nieren verursacht.
Broschüre zur Aufklärung von Patienten Ihnen wurde Jinarc verordnet, weil Sie eine autosomal-dominante polyzystische Nierenerkrankung bzw. ADPKD haben, die ein Wachstum von Zysten in den Nieren verursacht.
Anhang III. Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage
 Anhang III Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage Hinweis: Änderungen an der Fachinformation und der Packungsbeilage müssen unter Umständen im Anschluss durch
Anhang III Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage Hinweis: Änderungen an der Fachinformation und der Packungsbeilage müssen unter Umständen im Anschluss durch
(Telavancin) Leitfaden für medizinisches Fachpersonal. 16. Januar 2015
 VIBATIV (Telavancin) Leitfaden für medizinisches Fachpersonal 16. Januar 2015 Dieser Leitfaden zur Anwendung von Telavancin wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen des Risikomanagement-Plans
VIBATIV (Telavancin) Leitfaden für medizinisches Fachpersonal 16. Januar 2015 Dieser Leitfaden zur Anwendung von Telavancin wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen des Risikomanagement-Plans
Anhang III. Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilagen
 Anhang III Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilagen Anmerkung: Diese Änderungen der entsprechenden Abschnitte der Zusammenfassung
Anhang III Änderungen der entsprechenden Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilagen Anmerkung: Diese Änderungen der entsprechenden Abschnitte der Zusammenfassung
Fachinformation (Zusammenfassung der Merkmale des Arzneimittels/SmPC)
 Januar 2016 MS 02/16 V 019 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen
Januar 2016 MS 02/16 V 019 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen
Therapiepass Thalidomide Celgene TM
 Hinweis: Dieser Therapiepass gilt allein für die Verordnung und Anwendung der darin aufgeführten Originalprodukte von Celgene und darf nur dafür verwendet werden. Insbesondere unsere Empfehlungen zu Anwendungsgebieten,
Hinweis: Dieser Therapiepass gilt allein für die Verordnung und Anwendung der darin aufgeführten Originalprodukte von Celgene und darf nur dafür verwendet werden. Insbesondere unsere Empfehlungen zu Anwendungsgebieten,
WICHTIGE INFORMATIONEN FÜR PATIENTEN. denen STELARA zur Behandlung des mittelschweren bis schweren aktiven Morbus Crohn verschrieben wurde
 WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung des mittelschweren bis schweren aktiven Morbus Crohn verschrieben wurde 2 Version 2 (Stand: Februar 2017) Erstellt in Abstimmung mit dem
WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung des mittelschweren bis schweren aktiven Morbus Crohn verschrieben wurde 2 Version 2 (Stand: Februar 2017) Erstellt in Abstimmung mit dem
Anhang III. Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale
Anhang III Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale
Dokumentationsbroschüre mit Checkliste für die Verordnung von Acitretin-haltigen Arzneimitteln
 für den Arzt: Dokumentationsbroschüre mit Checkliste für die Verordnung von Acitretin-haltigen Arzneimitteln Teil des Schwangerschaftsverhütungsprogramms Diese Informationsbroschüre als Bestandteil des
für den Arzt: Dokumentationsbroschüre mit Checkliste für die Verordnung von Acitretin-haltigen Arzneimitteln Teil des Schwangerschaftsverhütungsprogramms Diese Informationsbroschüre als Bestandteil des
Ihr Wegweiser zur Therapie mit YERVOY (Ipilimumab)
 Behördlich genehmigtes Schulungsmaterial Ihr Wegweiser zur Therapie mit YERVOY (Ipilimumab) Informationsbroschüre für Patienten Diese Patientenbroschüre zur Anwendung von Ipilimumab wurde als Teil der
Behördlich genehmigtes Schulungsmaterial Ihr Wegweiser zur Therapie mit YERVOY (Ipilimumab) Informationsbroschüre für Patienten Diese Patientenbroschüre zur Anwendung von Ipilimumab wurde als Teil der
Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome
 Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome Basisinformation FACHINFORMATION Lang wirksame Beta-Mimetika - Long Acting Beta Agonists
Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome Basisinformation FACHINFORMATION Lang wirksame Beta-Mimetika - Long Acting Beta Agonists
Anhang III. Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale des Arzneimittels, der Etikettierung und
Anhang III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale des Arzneimittels, der Etikettierung und
Checkliste für die Verordnung von Tocino
 Wirkstoff: Alitretinoin. Indikation: Zur Behandlung von Erwachsenen mit therapierefraktärem, schwerem chronischem Handekzem, die eine ausgebaute lokale Behandlung für mindestens 4 Wochen erhalten und nicht
Wirkstoff: Alitretinoin. Indikation: Zur Behandlung von Erwachsenen mit therapierefraktärem, schwerem chronischem Handekzem, die eine ausgebaute lokale Behandlung für mindestens 4 Wochen erhalten und nicht
PATIENTENPASS FÜR PATIËNTEN, DIE MIT TYSABRI (NATALIZUMAB) BEHANDELT WERDEN
 (RMA angepasste Version 10/2016). PATIENTENPASS FÜR PATIËNTEN, DIE MIT TYSABRI (NATALIZUMAB) BEHANDELT WERDEN Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Zeigen Sie diesen Pass jedem
(RMA angepasste Version 10/2016). PATIENTENPASS FÜR PATIËNTEN, DIE MIT TYSABRI (NATALIZUMAB) BEHANDELT WERDEN Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Zeigen Sie diesen Pass jedem
Datum: Kontakt: Abteilung: Tel. / Fax: Unser Zeichen: Ihr Zeichen:
 BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 25.06.2015 Mag. pharm. Dr. Ulrike Rehberger REGA +43 (0) 505 55 36258 pv-implementation@ages.at
BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 25.06.2015 Mag. pharm. Dr. Ulrike Rehberger REGA +43 (0) 505 55 36258 pv-implementation@ages.at
MEDIKAMENTE, DIE MYCOPHENOLAT ENTHALTEN Informationsbroschüre für Patienten. Informationen über die Risiken für den Fötus
 Die Gesundheitsbehörden der Europäischen Union haben für Medikamente mit dem Wirkstoff Mycophenolat eine bedingte Zulassung erteilt. Diese Informationsbroschüre ist Teil des verbindlichen Plans zur Risikominimierung
Die Gesundheitsbehörden der Europäischen Union haben für Medikamente mit dem Wirkstoff Mycophenolat eine bedingte Zulassung erteilt. Diese Informationsbroschüre ist Teil des verbindlichen Plans zur Risikominimierung
Patienteninformation Lamotrigin Desitin 04/2007
 Information für Patientinnen und Patienten Lesen Sie diese Packungsbeilage sorgfältig, bevor Sie das Arzneimittel einnehmen bzw. anwenden. Dieses Arzneimittel ist Ihnen persönlich verschrieben worden und
Information für Patientinnen und Patienten Lesen Sie diese Packungsbeilage sorgfältig, bevor Sie das Arzneimittel einnehmen bzw. anwenden. Dieses Arzneimittel ist Ihnen persönlich verschrieben worden und
Patienteninformation
 I Patientenaufklärung und Einverständniserklärung Liebe Patientin, lieber Patient! Sie leiden unter einer Erkrankung des rheumatischen Formenkreises. Dazu zählen sowohl entzündliche (Arthritis) als auch
I Patientenaufklärung und Einverständniserklärung Liebe Patientin, lieber Patient! Sie leiden unter einer Erkrankung des rheumatischen Formenkreises. Dazu zählen sowohl entzündliche (Arthritis) als auch
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Therapie mit Cyclophosphamid
 PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Therapie mit Cyclophosphamid Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden unter einer schwerwiegenden entzündlichen Erkrankung des rheumatischen
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Therapie mit Cyclophosphamid Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden unter einer schwerwiegenden entzündlichen Erkrankung des rheumatischen
Mukherjee. EKG Fälle. pocket. Börm Bruckmeier Verlag
 Mukherjee EKG Fälle pocket Börm Bruckmeier Verlag Fall 34 151 Fall 34 Klinische Fallbeschreibung Ein 67 Jahre alter Mann erscheint in der Notaufnahme und klagt über Schmerzen im linken Arm während der
Mukherjee EKG Fälle pocket Börm Bruckmeier Verlag Fall 34 151 Fall 34 Klinische Fallbeschreibung Ein 67 Jahre alter Mann erscheint in der Notaufnahme und klagt über Schmerzen im linken Arm während der
Leitfaden für Ärzte und Apotheker zur Verordnung und Abgabe von Acitretin-haltigen Arzneimitteln
 Leitfaden für Ärzte und Apotheker zur Verordnung und Abgabe von Acitretin-haltigen Arzneimitteln Teil des Schwangerschaftsverhütungsprogramms Diese Informationsbroschüre als Bestandteil des Schwangerschaftsverhütungsprogramms
Leitfaden für Ärzte und Apotheker zur Verordnung und Abgabe von Acitretin-haltigen Arzneimitteln Teil des Schwangerschaftsverhütungsprogramms Diese Informationsbroschüre als Bestandteil des Schwangerschaftsverhütungsprogramms
WICHTIGE INFORMATIONEN ÜBER CYPROTERONACETAT- UND ETHINYLESTRADIOL-HALTIGE KOMBINATIONSPRÄPARATE UND DAS RISIKO FÜR BLUTGERINNSEL
 Patienteninformationskarte, DE Version: 29.06.2014 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie
Patienteninformationskarte, DE Version: 29.06.2014 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie
Sehr geehrte Patientin! Sehr geehrter Patient!
 Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
Geplante Änderungen an den relevanten Abschnitten der Packungsbeilage
 Geplante Änderungen an den relevanten Abschnitten der Packungsbeilage 1 B. Packungsbeilage 1. Was ist und wofür wird es angewendet? [Dieser Abschnitt soll wie folgt gefasst werden:]
Geplante Änderungen an den relevanten Abschnitten der Packungsbeilage 1 B. Packungsbeilage 1. Was ist und wofür wird es angewendet? [Dieser Abschnitt soll wie folgt gefasst werden:]
Betreff: Citalopram hältige Arzneispezialitäten Änderungen der Fach- und Gebrauchsinformationen
 Datum: 15.11.2011 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43(0)505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-111114-23425-A-PHV Ihr Zeichen: Betreff:
Datum: 15.11.2011 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43(0)505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-111114-23425-A-PHV Ihr Zeichen: Betreff:
Sildenafil. Wechselwirkungen
 Sildenafil Wechselwirkungen Ihr Arzt hat Ihnen ein Sildenafil-haltiges Arzneimittel verschrieben. Wie bei anderen Medikamenten wurden auch bei Sildenafil nach der Einnahme Nebenwirkungen und Wechselwirkungen
Sildenafil Wechselwirkungen Ihr Arzt hat Ihnen ein Sildenafil-haltiges Arzneimittel verschrieben. Wie bei anderen Medikamenten wurden auch bei Sildenafil nach der Einnahme Nebenwirkungen und Wechselwirkungen
Mitteilung des Bundesamts für Sicherheit im Gesundheitswesen über Maßnahmen zur Gewährleistung der Arzneimittelsicherheit:
 Landeshauptleute Landessanitätsdirektionen Österreichische Apothekerkammer Österreichische Ärztekammer Landesärztekammern Anstaltsapotheken d. Universitätskliniken Datum: 16.11.2015 Kontakt: Mag. Rudolf
Landeshauptleute Landessanitätsdirektionen Österreichische Apothekerkammer Österreichische Ärztekammer Landesärztekammern Anstaltsapotheken d. Universitätskliniken Datum: 16.11.2015 Kontakt: Mag. Rudolf
Sehr geehrte Patientin! Sehr geehrter Patient!
 Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
INFLECTRA (INFLIXIMAB): SICHERHEITSINFORMATION FÜR VERSCHREIBENDE ÄRZTE
 INFLECTRA (INFLIXIMAB): SICHERHEITSINFORMATION FÜR VERSCHREIBENDE ÄRZTE Infliximab kann mit schwerwiegenden, potentiell lebensbedrohlichen Nebenwirkungen einhergehen, die verhindert oder identifiziert
INFLECTRA (INFLIXIMAB): SICHERHEITSINFORMATION FÜR VERSCHREIBENDE ÄRZTE Infliximab kann mit schwerwiegenden, potentiell lebensbedrohlichen Nebenwirkungen einhergehen, die verhindert oder identifiziert
Cefavora - Tropfen. Gebrauchsinformation: Information für Anwender
 1 von 5 Cefavora - Tropfen Gebrauchsinformation: Information für Anwender Wirkstoffe: Ginkgo biloba Ø / Viscum album Ø / Crataegus Ø Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor sie mit
1 von 5 Cefavora - Tropfen Gebrauchsinformation: Information für Anwender Wirkstoffe: Ginkgo biloba Ø / Viscum album Ø / Crataegus Ø Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor sie mit
Bekanntmachung. zu lenalidomid- und thalidomidhaltigen Arzneimitteln. vom 8. Dezember 2008
 Bekanntmachung zu lenalidomid- und thalidomidhaltigen Arzneimitteln vom 8. Dezember 2008 Die nachfolgenden Anforderungen gelten mit Datum vom 08.02.2009. Thalidomide Pharmion 50 mg Hartkapseln in Kombination
Bekanntmachung zu lenalidomid- und thalidomidhaltigen Arzneimitteln vom 8. Dezember 2008 Die nachfolgenden Anforderungen gelten mit Datum vom 08.02.2009. Thalidomide Pharmion 50 mg Hartkapseln in Kombination
Wissenswertes rund um Ihre Therapietreue bei Gilenya. Ihre Therapietreue unter GILENYA
 Wissenswertes rund um Ihre Therapietreue bei Gilenya 1 Ihre Therapietreue unter GILENYA Liebe Patientin, Lieber Patient, um bestmöglich von Ihrer Therapie zu profitieren, ist die Treue zu Ihrer Therapie
Wissenswertes rund um Ihre Therapietreue bei Gilenya 1 Ihre Therapietreue unter GILENYA Liebe Patientin, Lieber Patient, um bestmöglich von Ihrer Therapie zu profitieren, ist die Treue zu Ihrer Therapie
Sehr geehrte Patientin! Sehr geehrter Patient!
 Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
Toctino Bestätigungsformular für Patienten
 Cutterguide: N/A Printing Process: Offset GD: SD428639 Size: A5: 148 X 210 mm Pages: 12 Colors: C M Y K (4 Color) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller XI Datum Name des Patienten
Cutterguide: N/A Printing Process: Offset GD: SD428639 Size: A5: 148 X 210 mm Pages: 12 Colors: C M Y K (4 Color) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller XI Datum Name des Patienten
Ödeme, Hypertonie und Herzinsuffizienz wurden im Zusammenhang mit NSAID - Behandlung berichtet.
 Alle rezeptpflichtigen nicht-selektiven NSAIDs zur systemischen Anwendung Für alle Präparate ohne fixes Dosierungsschema: 4.2. Dosierung, Art und Dauer der Anwendung 4.3. Gegenanzeigen Schwere Herzinsuffizienz
Alle rezeptpflichtigen nicht-selektiven NSAIDs zur systemischen Anwendung Für alle Präparate ohne fixes Dosierungsschema: 4.2. Dosierung, Art und Dauer der Anwendung 4.3. Gegenanzeigen Schwere Herzinsuffizienz
Diabetiker-Pass Ein SErvicE von WörWag Pharma
 Diabetiker-Pass Ein Service von Wörwag Pharma 02 Hinweise zur Benutzung Liebe Diabetikerin, lieber Diabetiker, dieser Diabetiker-Pass hat für Ihre Gesundheit eine doppelte Funktion: Er ist sowohl für die
Diabetiker-Pass Ein Service von Wörwag Pharma 02 Hinweise zur Benutzung Liebe Diabetikerin, lieber Diabetiker, dieser Diabetiker-Pass hat für Ihre Gesundheit eine doppelte Funktion: Er ist sowohl für die
Periodisches Fieber mit Aphthöser Stomatitis, Pharyngitis und Adenitis (PFAPA)
 www.printo.it/pediatric-rheumatology/de/intro Periodisches Fieber mit Aphthöser Stomatitis, Pharyngitis und Adenitis (PFAPA) Version von 2016 1. ÜBER PFAPA 1.1 Was ist das? PFAPA steht für periodisches
www.printo.it/pediatric-rheumatology/de/intro Periodisches Fieber mit Aphthöser Stomatitis, Pharyngitis und Adenitis (PFAPA) Version von 2016 1. ÜBER PFAPA 1.1 Was ist das? PFAPA steht für periodisches
Dokumentation Broschüre mit Checkliste für die Verordnung von Neotigason Patientin/Patient Teil des Schwangerschafts- verhütungsprogramms
 Dokumentation Broschüre mit Checkliste für die Verordnung von Neotigason für den Arzt Patientin/Patient Teil des Schwangerschaftsverhütungsprogramms Acitretin ist sehr teratogen. Selbst während der Einnahme
Dokumentation Broschüre mit Checkliste für die Verordnung von Neotigason für den Arzt Patientin/Patient Teil des Schwangerschaftsverhütungsprogramms Acitretin ist sehr teratogen. Selbst während der Einnahme
Gebrauchsinformation: Information für Patienten. Tabletten gegen Magen-Darm-Beschwerden Similasan
 1 Gebrauchsinformation: Information für Patienten Tabletten gegen Magen-Darm-Beschwerden Similasan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
1 Gebrauchsinformation: Information für Patienten Tabletten gegen Magen-Darm-Beschwerden Similasan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Anlage 3: Arbeitshilfe zum Umgang mit Multimedikation Stand:
 Anlage 3: Arbeitshilfe zum Umgang mit Multimedikation Stand: 21.1.2014 Arbeitshilfen aus der hausärztlichen Leitlinie Multimedikation der Leitliniengruppe Hessen, Stand: 29.10.2013 (http://www.arztbibliothek.de/bibliothek/leitlinie/multimedikation-hausaerztliche-leitlinie)
Anlage 3: Arbeitshilfe zum Umgang mit Multimedikation Stand: 21.1.2014 Arbeitshilfen aus der hausärztlichen Leitlinie Multimedikation der Leitliniengruppe Hessen, Stand: 29.10.2013 (http://www.arztbibliothek.de/bibliothek/leitlinie/multimedikation-hausaerztliche-leitlinie)
Die NovoTTF Therapie als Option. Eine neuartige Behandlung beim rezidivierenden Glioblastom
 Die NovoTTF Therapie als Option Eine neuartige Behandlung beim rezidivierenden Glioblastom Wichtige Sicherheitsinformationen Anwendungsindikation Das NovoTTF-100-A-System NovoTTF-100A ist ist für für die
Die NovoTTF Therapie als Option Eine neuartige Behandlung beim rezidivierenden Glioblastom Wichtige Sicherheitsinformationen Anwendungsindikation Das NovoTTF-100-A-System NovoTTF-100A ist ist für für die
Gebrauchsinformation: Information für Patienten. Osanit Hustenkügelchen Wirkstoff: Drosera D6
 Osanit Hustenkügelchen Seite 1 von 5 Gebrauchsinformation: Information für Patienten Osanit Hustenkügelchen Wirkstoff: Drosera D6 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Osanit Hustenkügelchen Seite 1 von 5 Gebrauchsinformation: Information für Patienten Osanit Hustenkügelchen Wirkstoff: Drosera D6 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Gebrauchsinformation: Information für Anwender. Wirkstoff: Moxonidin
 Gebrauchsinformation: Information für Anwender moxonidin-corax 0,2 mg Filmtabletten Wirkstoff: Moxonidin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Anwender moxonidin-corax 0,2 mg Filmtabletten Wirkstoff: Moxonidin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Anwender. GILENYA 0,5 mg Hartkapseln Fingolimod
 Gebrauchsinformation: Information für Anwender GILENYA 0,5 mg Hartkapseln Fingolimod Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse
Gebrauchsinformation: Information für Anwender GILENYA 0,5 mg Hartkapseln Fingolimod Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CORASAN Tropfen Wirkstoffe: Crataegus D1, Selenicereus grandiflorus (Cactus) D2, Digitalis purpurea D6, Strophanthus gratus D6. Lesen Sie die
Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CORASAN Tropfen Wirkstoffe: Crataegus D1, Selenicereus grandiflorus (Cactus) D2, Digitalis purpurea D6, Strophanthus gratus D6. Lesen Sie die
Ihr Wegweiser zur. Therapie mit YERVOY (Ipilimumab)
 Ihr Wegweiser zur Therapie mit YERVOY (Ipilimumab) Informationsbroschüre für Patienten Yervoy unterliegt einer zusätzlichen Überwachung. Dies ermögicht eine schnelle Identifizierung neuer Erkenntnisse
Ihr Wegweiser zur Therapie mit YERVOY (Ipilimumab) Informationsbroschüre für Patienten Yervoy unterliegt einer zusätzlichen Überwachung. Dies ermögicht eine schnelle Identifizierung neuer Erkenntnisse
ANHANG III ÄNDERUNGEN DER ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND PACKUNGSBEILAGE
 ANHANG III ÄNDERUNGEN DER ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND PACKUNGSBEILAGE 25 KORREKTUREN, DIE IN DIE JEWEILIGEN ABSCHNITTE DER ZUSAMMENFASSUNG DER PRODUKTEIGENSCHAFTEN FÜR BROMOCRIPTIN-HALTIGE
ANHANG III ÄNDERUNGEN DER ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND PACKUNGSBEILAGE 25 KORREKTUREN, DIE IN DIE JEWEILIGEN ABSCHNITTE DER ZUSAMMENFASSUNG DER PRODUKTEIGENSCHAFTEN FÜR BROMOCRIPTIN-HALTIGE
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER AFLUBIN chronisch- Hustentropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER AFLUBIN chronisch- Hustentropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn sie
Ihr Wegweiser zu. Information für Patienten
 Ihr Wegweiser zu Information für Patienten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie können
Ihr Wegweiser zu Information für Patienten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie können
Gebrauchsinformation: Information für Patienten. Aspecton Hustentropfen Flüssigkeit zum Einnehmen Thymiankraut-Dickextrakt
 Gebrauchsinformation: Information für Patienten Aspecton Hustentropfen Flüssigkeit zum Einnehmen Thymiankraut-Dickextrakt Für Erwachsene und Kinder ab 2 Jahren Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Patienten Aspecton Hustentropfen Flüssigkeit zum Einnehmen Thymiankraut-Dickextrakt Für Erwachsene und Kinder ab 2 Jahren Lesen Sie die gesamte Packungsbeilage sorgfältig
Was macht eine Therapie gut?
 Was macht eine Therapie gut? Wirksam gegen das Problem, für das sie eingesetzt wird Verhältnis von Wirkung und Nebenwirkungen akzeptabel Berücksichtigt individuelle Faktoren, z.b. Blutdruck Leber- und
Was macht eine Therapie gut? Wirksam gegen das Problem, für das sie eingesetzt wird Verhältnis von Wirkung und Nebenwirkungen akzeptabel Berücksichtigt individuelle Faktoren, z.b. Blutdruck Leber- und
VALDOXAN (Agomelatin)
 Die EU-Gesundheidsbehörden verknüpfen die Zulassung von Valdoxan 25 mg mit bestimmten Bedingungen. Der verbindliche Risikominimierungsplan in Belgien, von dem diese Informationen ein Teil ist, ist eine
Die EU-Gesundheidsbehörden verknüpfen die Zulassung von Valdoxan 25 mg mit bestimmten Bedingungen. Der verbindliche Risikominimierungsplan in Belgien, von dem diese Informationen ein Teil ist, ist eine
Hinweise zur Ausfüllanleitung. zum indikationsspezifischen Datensatz. für das strukturierte Behandlungsprogramm KHK
 Hinweise zur Ausfüllanleitung zum indikationsspezifischen Datensatz für das strukturierte Behandlungsprogramm KHK Für Rückfragen: Frau Claudia Scherbath, Tel. (0391) 627 63 39 Hinweis zur zusätzlichen
Hinweise zur Ausfüllanleitung zum indikationsspezifischen Datensatz für das strukturierte Behandlungsprogramm KHK Für Rückfragen: Frau Claudia Scherbath, Tel. (0391) 627 63 39 Hinweis zur zusätzlichen
Behandlung von Migräne-Anfällen (insbesondere sehr lange Anfälle), wenn andere Therapien nicht wirksam oder nicht indiziert sind.
 Gebrauchsinformation: Information für Patienten Ergo-Kranit Migräne 2 mg Tabletten Wirkstoff: Ergotamintartrat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten Ergo-Kranit Migräne 2 mg Tabletten Wirkstoff: Ergotamintartrat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Wichtige Informationen zur Assoziation von Sprycel (Dasatinib) mit pulmonaler arterieller Hypertonie (PAH)
 2. August 2011 Wichtige Informationen zur Assoziation von Sprycel (Dasatinib) mit pulmonaler arterieller Hypertonie (PAH) Sehr geehrte Frau Doktor, sehr geehrter Herr Doktor, sehr geehrte Frau Apothekerin,
2. August 2011 Wichtige Informationen zur Assoziation von Sprycel (Dasatinib) mit pulmonaler arterieller Hypertonie (PAH) Sehr geehrte Frau Doktor, sehr geehrter Herr Doktor, sehr geehrte Frau Apothekerin,
Chloropotassuril 1 g/10 ml Lösung zum Einnehmen
 Roundup Var. IB.c.I.z. Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Chloropotassuril 1 g/10 ml Lösung zum Einnehmen Kaliumchlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Roundup Var. IB.c.I.z. Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Chloropotassuril 1 g/10 ml Lösung zum Einnehmen Kaliumchlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
EKG Bradykardie AV Blockierungen
 EKG Bradykardie AV Blockierungen Lars Eckardt Abteilung für Rhythmologie Dep. für Kardiologie und Angiologie Universitätsklinikum Münster Überblick Definition Bradykardie: Frequenz
EKG Bradykardie AV Blockierungen Lars Eckardt Abteilung für Rhythmologie Dep. für Kardiologie und Angiologie Universitätsklinikum Münster Überblick Definition Bradykardie: Frequenz
Behindert Datenschutz die Arzneimittelsicherheit? Wechselwirkungen von Arzneimitteln - eine unterschätzte Gefahr für die Patienten
 Behindert Datenschutz die Arzneimittelsicherheit? Wechselwirkungen von Arzneimitteln - eine unterschätzte Gefahr für die Patienten APS Jahrestagung 16. April 2015 Stefanie Wobbe Vorstandsreferat Versorgungsforschung
Behindert Datenschutz die Arzneimittelsicherheit? Wechselwirkungen von Arzneimitteln - eine unterschätzte Gefahr für die Patienten APS Jahrestagung 16. April 2015 Stefanie Wobbe Vorstandsreferat Versorgungsforschung
Angina pectoris: I. Angina pectoris bei koronarer Herzerkrankung
 Angina pectoris: Zur Diagnose der Angina pectoris werden technische Geräte nicht benötigt, allein ausschlaggebend ist die Anamnese. Der Begriff Angina pectoris beinhaltet nicht jedes "Engegefühl in der
Angina pectoris: Zur Diagnose der Angina pectoris werden technische Geräte nicht benötigt, allein ausschlaggebend ist die Anamnese. Der Begriff Angina pectoris beinhaltet nicht jedes "Engegefühl in der
Gebrauchsinformation: Information für Patienten
 Tropfen gegen Akne Similasan 1 Gebrauchsinformation: Information für Patienten Tropfen gegen Akne Similasan Acidum arsenicosum D 12, Clematis recta D 8, Graphites D 12 Lesen Sie die gesamte Packungsbeilage
Tropfen gegen Akne Similasan 1 Gebrauchsinformation: Information für Patienten Tropfen gegen Akne Similasan Acidum arsenicosum D 12, Clematis recta D 8, Graphites D 12 Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER VENODRIL Tropfen Wirkstoffe: Aesculus hippocastanum Dil. D6, Hamamelis virginiana Dil. D4, Melilotus officinalis Dil. D6, Silybum marianum Dil. D4 Lesen Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER VENODRIL Tropfen Wirkstoffe: Aesculus hippocastanum Dil. D6, Hamamelis virginiana Dil. D4, Melilotus officinalis Dil. D6, Silybum marianum Dil. D4 Lesen Sie
Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid
 10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei akuten Hals- und Rachenschmerzen Belladonna D4/D6/D12
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei akuten Hals- und Rachenschmerzen Belladonna D4/D6/D12 Wirkstoff: Atropa bella-donna D4/D6/D12 Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei akuten Hals- und Rachenschmerzen Belladonna D4/D6/D12 Wirkstoff: Atropa bella-donna D4/D6/D12 Lesen Sie die gesamte Packungsbeilage
NeuroBloc. Botulinumtoxin Typ B Injektionslösung 5000 E/ml. Wichtige Informationen zur Sicherheit für Ärzte
 NeuroBloc Botulinumtoxin Typ B Injektionslösung 5000 E/ml Wichtige Informationen zur Sicherheit für Ärzte Dieses Handbuch dient dazu, Ärzte, die für die Verschreibung und die Verabreichung von NeuroBloc
NeuroBloc Botulinumtoxin Typ B Injektionslösung 5000 E/ml Wichtige Informationen zur Sicherheit für Ärzte Dieses Handbuch dient dazu, Ärzte, die für die Verschreibung und die Verabreichung von NeuroBloc
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei trockenem Krampf- und Reizhusten Drosera D3/D4/D6
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei trockenem Krampf- und Reizhusten Drosera D3/D4/D6 Wirkstoff: Drosera D3/D4/D6 Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei trockenem Krampf- und Reizhusten Drosera D3/D4/D6 Wirkstoff: Drosera D3/D4/D6 Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender. Apozema Dreiklang Globuli bei sekretreichem Husten Ipecacuanha D4/D6/D12
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei sekretreichem Husten Ipecacuanha D4/D6/D12 Wirkstoff: Psychotria ipecacuanha D4/D6/D12 Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei sekretreichem Husten Ipecacuanha D4/D6/D12 Wirkstoff: Psychotria ipecacuanha D4/D6/D12 Lesen Sie die gesamte Packungsbeilage
Evaluation ( 137f Abs. 2 Satz 2 Nr. 6 des Fünften Buches Sozialgesetzbuch) Diabetes mellitus Typ 1 Erstdokumentation
 - 33-4.2 Schulungen der Versicherten Patientinnen und Patienten mit Diabetes mellitus Typ 1 profitieren in besonderem Maße von einer eigenständig durchgeführten Insulintherapie, einschließlich einer eigenständigen
- 33-4.2 Schulungen der Versicherten Patientinnen und Patienten mit Diabetes mellitus Typ 1 profitieren in besonderem Maße von einer eigenständig durchgeführten Insulintherapie, einschließlich einer eigenständigen
Checkliste für die Verordnung von Toctino
 SCHWANGERSCHAFTSVERHÜTUNGSPROGRAMM Checkliste für die Verordnung von Toctino für die ärztliche Dokumentation Name der Patientin Alitretinoin Bestätigungsformular für behandelnde Ärzte Die Patientin kam
SCHWANGERSCHAFTSVERHÜTUNGSPROGRAMM Checkliste für die Verordnung von Toctino für die ärztliche Dokumentation Name der Patientin Alitretinoin Bestätigungsformular für behandelnde Ärzte Die Patientin kam
imedication Identifizierung und Überwachung von unerwünschten Arzneimittelwirkungen
 imedication Identifizierung und Überwachung von unerwünschten Arzneimittelwirkungen DI Manuela Plößnig, MSc Salzburg Research 21. November 2012 Heilen ist eine Frage der Zeit, mitunter aber auch eine Frage
imedication Identifizierung und Überwachung von unerwünschten Arzneimittelwirkungen DI Manuela Plößnig, MSc Salzburg Research 21. November 2012 Heilen ist eine Frage der Zeit, mitunter aber auch eine Frage
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CRIMAX Haarvitaltropfen Wirkstoffe: Acidum hydrofluoricum Dil. D12, Graphites Dil. D8, Pel talpae Dil. D8, Selenium amorphum Dil. D12 Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CRIMAX Haarvitaltropfen Wirkstoffe: Acidum hydrofluoricum Dil. D12, Graphites Dil. D8, Pel talpae Dil. D8, Selenium amorphum Dil. D12 Lesen Sie die gesamte
Aripiprazol. Antworten auf häufig gestellte Fragen (FAQ) Für Ärzte und andere Angehörige der Gesundheitsberufe. Stand November 2016
 Broschüre Aripiprazol für Ärzte 1 Aripiprazol Antworten auf häufig gestellte Fragen (FAQ) Für Ärzte und andere Angehörige der Gesundheitsberufe Stand November 2016 Aripiprazol ist für die bis zu 12 Wochen
Broschüre Aripiprazol für Ärzte 1 Aripiprazol Antworten auf häufig gestellte Fragen (FAQ) Für Ärzte und andere Angehörige der Gesundheitsberufe Stand November 2016 Aripiprazol ist für die bis zu 12 Wochen
nachrichtlich: Stufenplanbeteiligte, Zul. mit DE= CMS V /
 Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn pharmazeutische Unternehmer mit DE=RMS, nat. Zul., Parallelimp. nachrichtlich: Stufenplanbeteiligte,
Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn pharmazeutische Unternehmer mit DE=RMS, nat. Zul., Parallelimp. nachrichtlich: Stufenplanbeteiligte,
Einleitung und Leseanweisung
 VII Einleitung und Leseanweisung Für wen ist dieses Buch? Der Pocket Guide ist für alle klinisch tätigen Psychiater geschrieben, denen das Kompendium der Psychiatrischen Pharmakotherapie für die Kitteltasche
VII Einleitung und Leseanweisung Für wen ist dieses Buch? Der Pocket Guide ist für alle klinisch tätigen Psychiater geschrieben, denen das Kompendium der Psychiatrischen Pharmakotherapie für die Kitteltasche
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Aspirine 500 Brause, 500 mg, Brausetabletten Acetylsalicylsäure
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Aspirine 500 Brause, 500 mg, Brausetabletten Acetylsalicylsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Aspirine 500 Brause, 500 mg, Brausetabletten Acetylsalicylsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Kipptisch Untersuchung
 Kipptisch Untersuchung Allgemeines: Die Kipptisch Untersuchung ist eine aufwendige, ambulant durchführbare diagnostische Methode zur Erkennung von Reflexsynkopen (neurokardiogenen Synkopen) bei den wenigen
Kipptisch Untersuchung Allgemeines: Die Kipptisch Untersuchung ist eine aufwendige, ambulant durchführbare diagnostische Methode zur Erkennung von Reflexsynkopen (neurokardiogenen Synkopen) bei den wenigen
Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
Toctino Bestätigungsformular für Patienten
 * Toctino wird zur Behandlung von Patientinnen/Patienten unter 18 Jahren nicht empfohlen. Datum Unterschrift des Patienten Geburtsdatum Name des Patienten (Druckschrift) Mein behandelnder Dermatologe hat
* Toctino wird zur Behandlung von Patientinnen/Patienten unter 18 Jahren nicht empfohlen. Datum Unterschrift des Patienten Geburtsdatum Name des Patienten (Druckschrift) Mein behandelnder Dermatologe hat
1. Was ist Apis/Belladonna cum Mercurio und wofür wird es angewendet?
 WALA Gebrauchsinformation: Information für Anwender Apis/Bella-donna cum Mercurio Wirkstoffe: Apis mellifica ex animale toto Gl Dil. D4, Atropa bella-donna e fructibus maturis ferm 33a Dil. D3, Mercurius
WALA Gebrauchsinformation: Information für Anwender Apis/Bella-donna cum Mercurio Wirkstoffe: Apis mellifica ex animale toto Gl Dil. D4, Atropa bella-donna e fructibus maturis ferm 33a Dil. D3, Mercurius
auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Siehe Abschnitt 4.
 Seite 4 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Folsäure Heumann 5 mg Tabletten Folsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Seite 4 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Folsäure Heumann 5 mg Tabletten Folsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Aufklärung über Verhütungsmittel
 Aufklärung über Verhütungsmittel Univ.-Prof. Dr. Helmut Ofner LL.M. Universität Wien - Juridicum Themen Aufklärungspflicht Behandlungsfehler Mögliche Schäden: Unterhaltskosten bei Geburt eines Kindes Nebenwirkungen
Aufklärung über Verhütungsmittel Univ.-Prof. Dr. Helmut Ofner LL.M. Universität Wien - Juridicum Themen Aufklärungspflicht Behandlungsfehler Mögliche Schäden: Unterhaltskosten bei Geburt eines Kindes Nebenwirkungen
Patientenpass CML. Für. (Name des Patienten) Bitte bei jedem Arztbesuch mitbringen
 Patientenpass CML Für (Name des Patienten) Bitte bei jedem Arztbesuch mitbringen 1 Inhaltsverzeichnis Seite Vorwort 3 Patientendaten und Ersterhebung 4-5 Übersicht Medikamenteneinnahme 6 Bedeutung der
Patientenpass CML Für (Name des Patienten) Bitte bei jedem Arztbesuch mitbringen 1 Inhaltsverzeichnis Seite Vorwort 3 Patientendaten und Ersterhebung 4-5 Übersicht Medikamenteneinnahme 6 Bedeutung der
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Ihr Wegweiser zu. Information für Patienten
 Ihr Wegweiser zu Information für Patienten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie können
Ihr Wegweiser zu Information für Patienten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie können
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic )
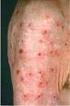 Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
Koronare Herzkrankheit Ziffer 5 Dokumentation
 Koronare Herzkrankheit Ziffer 5 Dokumentation 1 DMP-Fallnummer vom Arzt zu vergeben Administrative Daten 2 Krankenkasse bzw. Kostenträger Name der Kasse Name der Kasse 3 Name, Vorname des Versicherten
Koronare Herzkrankheit Ziffer 5 Dokumentation 1 DMP-Fallnummer vom Arzt zu vergeben Administrative Daten 2 Krankenkasse bzw. Kostenträger Name der Kasse Name der Kasse 3 Name, Vorname des Versicherten
Grundlagen der Medizinischen Klinik I + II. Dr. Friedrich Mittermayer Dr. Katharina Krzyzanowska
 Grundlagen der Medizinischen Klinik I + II Dr. Friedrich Mittermayer Dr. Katharina Krzyzanowska 1 Was ist Bluthochdruck? Der ideale Blutdruck liegt bei 120/80 mmhg. Bluthochdruck (Hypertonie) ist eine
Grundlagen der Medizinischen Klinik I + II Dr. Friedrich Mittermayer Dr. Katharina Krzyzanowska 1 Was ist Bluthochdruck? Der ideale Blutdruck liegt bei 120/80 mmhg. Bluthochdruck (Hypertonie) ist eine
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien
 Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
rund 200 ausgewählte Wirkstoffe
 rund 200 ausgewählte Wirkstoffe Von der Wirkstoffverordnung sind insbesondere folgende Darreichungsformen ausgeschlossen: - Arzneimittel, die auf die Haut aufgetragen werden (z.b. Salben, Gele) - Arzneimittel
rund 200 ausgewählte Wirkstoffe Von der Wirkstoffverordnung sind insbesondere folgende Darreichungsformen ausgeschlossen: - Arzneimittel, die auf die Haut aufgetragen werden (z.b. Salben, Gele) - Arzneimittel
