9 Aromaten. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
|
|
|
- Axel Schäfer
- vor 6 Jahren
- Abrufe
Transkript
1 Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter Doppelbindungen auf. 3. Die Anzahl der delokalisierten Elektronen beträgt 4n 2 (n = 0,1,2 ) (ückel-regel), d. h., die Anzahl der delokalisierten Elektronenpaare ist ungerade. 4. Das Molekül zeigt eine besondere Stabilisierungsenergie. A2 Elektrophiler Angriff und heterolytische Spaltung des Iodchloridmoleküls: d d Ø l All 3 Ø All 4 Deprotonierung und Rearomatisierung: Ø All 4 Ø l All 3 Das polare Iodchloridmolekül wird durch das Aluminiumchlorid noch stärker polarisiert. Es tritt mit den delokalisierten Ringelektronen des Benzolmoleküls in Wechselwirkung und wird heterolytisch gespalten. Das hloratom hat eine höhere Elektronegativität als das Iodatom (E(l) = 3,0; E(I) = 2,5), deshalb wird das hloratom formel zum hloridion und vom Aluminiumchlorid gebunden. Das Iodatom wird formal zum Iodkation und wird an ein -Atom des Benzolmoleküls gebunden. Es bildet sich ein arbokation, in dem die positive Ladung über mehrere Atome deloklisiert ist. Unter Abgabe eines Protons und der Bildung eines hlorwasserstoffmoleküls erfolgt die Rearomatisierung zum Produkt Iodbenzol. A3 Die Aminogruppe ist ein aktivierender Substituent. Ein freies Elektronenpaar des -Atoms tritt mit dem delokalisierten Ringelektronensystem in Wechselwirkung. Dadurch wird die Elektronendichte im Ring insgesamt größer (M-Effekt): Die negative Teilladung im Ring erleichtert den Angriff eines elektrophilen Teilchens. 1 Elemente hemie berstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
2 A4 a) Die erste (linke) Grenformel weist keine Ladungstrennung auf. Sie ist daher energetisch am günstigsten und trägt am meisten zur Mesomerie bei. inweis: Diese Lösung folgt aus Kap Der Beitrag der anderen vier Grenzformeln zusammen ist allerdings größer. Dies führt dazu, dass das Stickstoffatom im Pyrrolmolekül eine positive Partialladung trägt (0,24 Elementarladungen), obwohl es das elektronegativste Element im Molekül ist. b) Pyrrol weist nur eine sehr geringe Basizität auf (K B 2, ), da das freie Elektronenpaar am Stickstoffatom delakolisiert ist. Es ist mit in die Konjugation eingebunden, wodurch das Elektronenpaar kaum für die Bindung eines Protons zur Verfügung steht. Das Stickstoffatom bzw. Pyrrolmolekül ist nur schwer zu protonieren. inweise: Pyrrol gehört zu den aromatischen eterocyclopentadienen, wie auch Furan und Thiophen. An Pyrrol ist (ähnlich wie an Benzol) eine elektrophile Substitution möglich. Der pk B -Wert von Pyrrol ist 13,6. Pyrrol ist also eine schwächere Base als das S 4 2 -Ion. Wenn ein Pyrrolmolekül als Base reagiert, wird eines der -Atome protoniert, da das -Atom eine positve Partial ladung trägt. Die -Gruppe des Protons kann jedoch deprotoniert werden, ohne dass der aromatische Zustand verloren geht. Trotzdem ist Pyrrol ist eine extrem schwache Säure (pk S 25). Eine Lösung der Aufgabe mit energetischer Begründung könnte folgendermaßen aussehen: Pyrrol hat 6 delokalisierte Elektronen im Ring und gehört damit nach der ückel-regel zu den aromatischen Verbindungen. Der aromatische Zustand ist besonders stabil. Reagiert Pyrrol als Base, werden zwei der delokalisierten Elektronen zur Bindung des Protons benötigt. Das Kation ist folglich nicht aromatisch und damit viel weniger stabil. Das Gleichgewicht der Protonierungs reaktion liegt daher auf der Seite der Edukte. A5 1. erstellung von Toluol: l Katalysator l 2. xidation von Toluol: xidation inweise: Der erste Reaktionsschritt ist eine elektrophile Substitution. Man bezeichnet ihn als Friedel- rafts-alkylierung; als Katalysator ist z. B. Aluminiumchlorid geeignet. Der zweite Reak tionsschritt ist im Schülerbuch in Kap. 9.8 kurz beschrieben (Lesetext und B4). Er kann in folgende kleinere Schritte unterteilt werden: [] [] 2 [] Als xidationsmittel ist eine Lösung von Kaliumpermanganat mit einigen Tropfen konz. Schwefelsäure geeignet. 2 Elemente hemie berstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
3 A6 6.1 Die Ausgangsstoffe für die Synthese von Salicylsäuremethylester sind Salicylsäure und Methanol. Schwefelsäure wird als Katalysator eingesetzt. Die Salicylsäure wird in einem deutlichen Überschuss an Methanol gelöst. Dadurch ist sichergestellt, dass die Salicylsäure sich vollständig löst. Die Veresterung ist eine Gleichgewichtsreaktion. Der Überschuss an Methanol führt dazu, dass das Gleichgewicht stärker in Richtung des Reaktionsproduktes verschoben wird. Der Kolben ist das Reaktionsgefäß. Der Rückflusskühler sorgt dafür, dass während des Erhitzens kein Methanol an die Umgebung abgegeben wird. Außerdem beschleunigt das Erhitzen des Reaktionsgemisches die Geschwindigkeit der Reaktion. Das Reaktionsgemisch wird nach dem Abkühlen in kaltes Wasser gegeben. In dem kalten Wasser sind die Schwefelsäure, das Wasser und das überschüssige Methanol und die geringe nicht umgesetzte Salicylsäureportion gut löslich. Salicylsäuremethylester sammelt sich aufgrund seiner sehr geringen Löslichkeit in Wasser und seiner größeren Dichte als Wasser unterhalb der Wasserschicht. Die Zugabe der alciumchloridkörner dient zum Trocknen des Esters. alciumchlorid bindet Wasser. Die Siedetemperatur bestätigt, dass Salicylsäuremethylester als Reaktionsprodukt gewonnen worden ist. 6.2 Reaktionsgleichung: 2 S 4 2 Salicylsäure Methanol Salicylsäuremethylester 3 Elemente hemie berstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
4 Reaktionsschritt: Salicylsäure Kation 1 (formal) 2. Reaktionsschritt: 3 Kation 1 (real) Methanol Kation Reaktionsschritt: Kation Reaktionsschritt: 3 3 Kation 3 5. Reaktionsschritt: 3 3 Kation 3 Kation 4 6. Reaktionsschritt: 3 3 Kation 4 Salicylsäuremethylester 1. Reaktionsschritt: Das arbonyl-sauerstoffatom der Salicylsäure wird von der als Katalysator zugegebenen Schwefelsäure protoniert. 4 Elemente hemie berstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
5 2. Reaktionsschritt: Das Kation1 ist symmetrisch aufgebaut; es weist zwei gleich lange --Bindungen auf. Zwei bindende Elektronen sind delokalisiert und das Kohlenstoffatom der arboxygruppe ist stark positiviert. Dies erleichtert den nucleophilen Angriff des des Methanolmoleküls und die Bildung des Kations Reaktionsschritt: Das Kation 2 gibt im nächsten Schritt ein Proton ab, wodurch der Katalysator wieder gebildet wird. Gleichzeitig ist damit die Addition des Alkoholmoleküls abgeschlossen. Vorläufiges Ergebnis ist ein Molekül, das zwei ydroxygruppen an einem Kohlenstoffatom aufweist. Derartige Moleküle sind nicht stabil. 4. Reaktionsschritt: Eine dieser beiden ydroxygruppen wird protoniert. Reaktionschritt 3 und 4 verlaufen wahrscheinlich eher gleichzeitig, d. h., aus dem Kation 2 entsteht das Kation Reaktionsschritt: Im Kation 3 ist ein Wassermolekül als Abgangsgruppe vorhanden; es spaltet sich ab. 6. Reaktionsschritt: Das Kation 4 spaltet ein Proton ab. Aus dem Kation 4 ist damit ein Salicylsäuremethylestermolekül entstanden. Die Kondensationsreaktion ist abgeschlossen. 6.4 Das Salicylsäuremolekül besteht aus einem Benzolring (Phenylring), einer ydroxygruppe und einer arboxygruppe. Das Methanolmolekül ist aus einer Methylgruppe und einer ydroxygruppe aufgebaut. Das Molekül des Salicylsäuremethylesters besteht aus einem Benzolring (Phenylring), einer ydroxygruppe und einer Estergruppe. Methanol ist in jedem Verhältnis in Wasser löslich, weil der Einfluss der polaren ydroxygruppe auf die Methanolmoleküle groß ist. Die Methanolmoleküle können mit den Wassermolekülen Wasserstoffbrücken ausbilden. Auch in Ethanol löst sich Methanol in jedem Verhältnis; auch hier werden zwischen den unterschiedlichen Alkoholmolekülen Wasserstoffbrücken ausgebildet. Außerdem wirken zwischen den Methyl- und Ethylgruppen Van-der-Waals-Kräfte. Salicylsäure und Salicylsäuremethylester lösen sich in Wasser nur wenig, weil der unpolare Anteil ihrer Moleküle im Vergleich zum polaren Anteil relativ groß ist. Salicylsäure löst sich etwas besser als Salicylsäuremethylester, da ihre arboxygruppe mit den Wassermolekülen Wasserstoffbrücken ausbilden kann. In Ethanol sind beide Stoffe gut löslich, da zwischen der Ethylgruppe des Ethanols und dem unpolaren Teil der aromatischen Moleküle Van-der-Waals-Kräfte wirken. Die Schmelztemperatur der Stoffe wird durch die Anordnung der Moleküle im Gitter und den zwischen den Molekülen wirksamen Anziehungskräften bestimmt. Die Siedetemperatur der Stoffe wird durch die zwischen den Molekülen wirkenden Kräfte bestimmt. Methanol hat die niedrigste Schmelz- und Siedetemperatur, obwohl die Methanolmoleküle untereinander sehr gut Wasserstoffbrücken ausbilden können. Allerdings sind die Van-der-Waals- Kräfte wegen der kleinen Methylgruppe schwach. Zwischen den Salicylsäuremolekülen wirken Van-der-Waals-Kräfte und Wasserstoffbrücken. Die Van-der-Waals-Kräfte sind auf den Benzolring (Phenylring), die Wasserstoffbrücken auf die ydroxy- und die arboxygruppe zurückzuführen. Eventuell wirken zwischen den Salicylsäuremolekülen auch Dipol-Dipol-Kräfte. Zwischen den Salicylsäuremethylestermolekülen können Van-der-Waals-Kräfte, Wasserstoffbrücken und Dipol-Dipol-Kräfte wirken. Die Van-der-Waals-Kräfte sind wiederum im Wesentlichen auf den Benzolring (Phenylring) zurückzuführen. Über die ydroxygruppe können Wasserstoffbrücken gebildet werden, über die arbonylgruppe der Estergruppierung können Dipol-Dipol-Kräfte wirken. Zwischen den Salicylsäuremolekülen sind mehr Wasserstoffbrücken möglich als zwischen den Salicylsäuremethylestermolekülen. Deshalb hat Salicylsäure eine deutlich höhere Schmelztemperatur als Salicylsäuremethylester. Das Gleiche gilt für die Siedetemperatur. Bei der Angabe der Siedetemperatur der Salicylsäure ist die Angabe des Druckes zu beachten. Die Siedetemperatur ist für einen Druck von 27 hpa angegeben, dieser liegt weiter unter dem ormdruck (1013 hpa). ffensichtlich sind die Anziehungskräfte zwischen den Salicylsäuremolekülen so groß, dass die Salicylsäure sich beim Erhitzen unter ormdruck vor Erreichen einer Siedetemperatur zersetzt. 5 Elemente hemie berstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
6 A7 7.1 In alkalischer Lösung reagiert Phenol zum Phenolat: Das negativ geladene Sauerstoffatom übt einen M-Effekt aus. Ein freies Elektronenpaar des Sauerstoffatoms tritt in Wechselwirkung mit dem delokalisierten Ringelektronensystem des Benzolrings, wodurch die Elektronendichte im Ring erhöht wird. Dies erleichtert einen elektrophilen Angriff, sodass die elektrophile Substitution auch ohne Katalysator ablaufen kann. Vergleicht man die Grenzformeln des Phenolations, so fällt auf, dass in den Ringpositionen 2, 6 (ortho-stellungen) und 4 (para-stellung) eine negative Ladung auftritt. Ein elektrophiles Teilchen wird bevorzugt an diesen Postionen angreifen: 7.3 Das negativ geladene Sauerstoffatom übt einen M-Effekt aus. Es ist also ein Substituent 1. rdnung und damit ortho/para-dirigierend. Die Grenzformeln der arbokationen für mögliche Zweit substitutionen zeigen, dass bei Zweitsubstitution in ortho- oder para-stellung eine Grenzformel formuliert werden kann, in der das Sauerstoffatom die positive Ladung übernommen hat. Dies bedeutet, dass die positive Ladung über den Ring hinaus und damit über einen größeren Raum delokalisiert ist. Die Zweitsubstitution in ortho- bzw. para-stellung führt damit zu einem stabileren arbokation als die Zweit sub stitution in meta-stellung. Zweitsubstitution in ortho-stellung: Zweitsubstitution in meta-stellung: Zweitsubstitution in para-stellung: 6 Elemente hemie berstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
7 7.4 Man gibt eine Säure zu, z. B. verd. Schwefelsäure. In saurer Lösung reagiert ortho- bzw. para-omphenolat zu ortho- bzw. para-omphenol: rtho- und para-omphenol sind (wie Phenol) schwache Säuren, sodass sie nur in alkalischer Lösung hauptsächlich als omphenolate vorliegen. 7 Elemente hemie berstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang
 Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
3. Aromatische Verbindungen Benzol(en)
 3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte
 Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
1.2 Vergleichen Sie die Reaktionsbedingungen für die Bromierung von A und B und begründen Sie unter Mitverwendung von Grenzformeln den Unterschied!
 Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
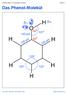 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
 hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
8 Organische Verbindungen und ihre Reaktionswege
 Lösungen zu den Durchblick-Seiten 8 rganische Verbindungen und ihre Reaktionswege 8.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 a) 2 b) Es handelt sich um eine ydrierung. Die ydrierung gehört
Lösungen zu den Durchblick-Seiten 8 rganische Verbindungen und ihre Reaktionswege 8.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 a) 2 b) Es handelt sich um eine ydrierung. Die ydrierung gehört
Reaktionstypen der Aromate
 Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Übungen zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe. 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit
 O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Bundesrealgymnasium Imst. Chemie Klasse 8. Aromaten und deren Reaktionen
 Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 Carbonylgruppen und eine C=C Doppelbindung.
 rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Aromatische Kohlenwasserstoffe.
 Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
10. Jahrgangsstufe Organische Chemie Skript Einführungsklasse
 4. Die Eigenschaften von Alkanen 4.1 Der Aggregatszustand bzw. die Siedetemperatur Der Aggregatszustand von Alkanen bei Raumtemperatur ist von der Siedetemperatur abhängig und steht in Zusammenhang mit
4. Die Eigenschaften von Alkanen 4.1 Der Aggregatszustand bzw. die Siedetemperatur Der Aggregatszustand von Alkanen bei Raumtemperatur ist von der Siedetemperatur abhängig und steht in Zusammenhang mit
(Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.)
 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
8 Aromaten. vorläufige Fassung. 8.1 Erforschung des Benzols
 8.1 Erforschung des Benzols vorläufige Fassung A1 Im Vergleich mit einem Alkan der Summenformel 6 14 fehlen im Molekül der Verbindung mit der Summenformel 6 6 acht -Atome, d. h., ein offenkettiges Molekül
8.1 Erforschung des Benzols vorläufige Fassung A1 Im Vergleich mit einem Alkan der Summenformel 6 14 fehlen im Molekül der Verbindung mit der Summenformel 6 6 acht -Atome, d. h., ein offenkettiges Molekül
Chemie Alkohole, Aldehyde & Ketone, Carbonsäuren
 Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Indanon ist das Produkt einer Friedel-Crafts-Acylierung Geben Sie die Reaktionsgleichung zu seiner Synthese an.
 Aromatenchemie für Fortgeschrittene 1.Wiederholung: Elektrophile aromatische Substitutionen 1.1. Geben Sie die Bruttogleichung für die zweistufige Synthese von Styren an. 1.2. Formulieren Sie die Reaktionsgleichung
Aromatenchemie für Fortgeschrittene 1.Wiederholung: Elektrophile aromatische Substitutionen 1.1. Geben Sie die Bruttogleichung für die zweistufige Synthese von Styren an. 1.2. Formulieren Sie die Reaktionsgleichung
Herstellung und Oxidation von 2,4,6-Tri-tert-butylphenol
 2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
Lösungen 3. Übungsblatt SS 2002
 Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten!
 Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
H δ+ H H H H. Addition von HBr an Ethen. Zufällig kommt ein HBr-Molekül in die Nähe der elektronenreichen Doppelbindung. Schritt 1
 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 1 1/ Zufällig kommt ein -Molekül in die Nähe der elektronenreichen δ- δ+ Ulrich elmich 2015
hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 1 1/ Zufällig kommt ein -Molekül in die Nähe der elektronenreichen δ- δ+ Ulrich elmich 2015
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )
![Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 ) Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )](/thumbs/74/69784240.jpg) 1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2
![Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2](/thumbs/95/126253543.jpg) Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag)
 Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Rückblick. 1 Elemente Chemie Oberstufe Einführungsphase NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Aufgaben. Rückblick Aufgaben
 Lösungen zu den Aufgaben Rückblick Aufgaben A1 Je stärker die Anziehungskräfte zwischen den kleinsten Teilchen eines Stoffes sind, desto höher ist die Siedetemperatur des Stoffes, denn zum Verdampfen müssen
Lösungen zu den Aufgaben Rückblick Aufgaben A1 Je stärker die Anziehungskräfte zwischen den kleinsten Teilchen eines Stoffes sind, desto höher ist die Siedetemperatur des Stoffes, denn zum Verdampfen müssen
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
2. Elektroneneffekte in den organischen Molekülen
 2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
Aromatische Kohlenwasserstoffe
 Benzol: 6 6 (Faraday 1825) Aromatische Kohlenwasserstoffe OI_folie201 Vorgeschlagene Konstitutionen von Benzol 1,3,5-yclohexatrien-Struktur 1858 Kekulé Erklärt nicht, warum es nur drei regioisomere disubstituierte
Benzol: 6 6 (Faraday 1825) Aromatische Kohlenwasserstoffe OI_folie201 Vorgeschlagene Konstitutionen von Benzol 1,3,5-yclohexatrien-Struktur 1858 Kekulé Erklärt nicht, warum es nur drei regioisomere disubstituierte
Beispiel für eine Anionenaustausch-Matrix. Als funktionelle Gruppe dient hier eine Diethylaminoethylgruppe.
 Aufgabe 1 Essigsäure exansäure Der Laugenverbrauch ist im Falle der Essigsäure höher. Essigsäure verteilt sich besser in die Wasserphase, exansäure aufgrund der höheren Anzahl unpolarer Alkylreste besser
Aufgabe 1 Essigsäure exansäure Der Laugenverbrauch ist im Falle der Essigsäure höher. Essigsäure verteilt sich besser in die Wasserphase, exansäure aufgrund der höheren Anzahl unpolarer Alkylreste besser
Gruppenarbeit : Zwischenmolekulare Kräfte
 Expertengruppe A Zwischenmolekulare Kräfte Allgemeines Zwischenmolekulare Kräfte dürfen nicht mit der Kovalenzbindung verwechselt werden. Bei der Kovalenzbindung geht es um Kräfte innerhalb der Moleküle
Expertengruppe A Zwischenmolekulare Kräfte Allgemeines Zwischenmolekulare Kräfte dürfen nicht mit der Kovalenzbindung verwechselt werden. Bei der Kovalenzbindung geht es um Kräfte innerhalb der Moleküle
11 Organische Farbstoffe
 Lösungen zu den Durchblick-Seiten 11.11 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 Das Phenolmolekül ist reaktiver als das unsubstituierte Benzolmolekül, da in ihm durch Mesomerie negative
Lösungen zu den Durchblick-Seiten 11.11 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 Das Phenolmolekül ist reaktiver als das unsubstituierte Benzolmolekül, da in ihm durch Mesomerie negative
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
N N. Chinolin. Pyridin. Imidazol
 6. eterocyclische Verbindungen 51 Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen aufgebaut sind. In den sogenannten eterocyclen ist mindestens ein Kohlenstoff des ings
6. eterocyclische Verbindungen 51 Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen aufgebaut sind. In den sogenannten eterocyclen ist mindestens ein Kohlenstoff des ings
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 CE 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 6. eterocyclische Verbindungen Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen
CE 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 6. eterocyclische Verbindungen Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen
ALDEHYDE & KETONE. Referat über die Carbonylverbindungen: Aldehyde und Ketone Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium
 ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Organische Chemie, Reaktionsmechanismen
 , Reaktionen, Teil 3-1 - hemieskript Dr. R. Steiger rganische hemie, Reaktionsmechanismen Das Lernziel dieser Unterrichtseinheit beinhaltet folgende Punkte: Wie können funktionelle Gruppen ineinander überführt
, Reaktionen, Teil 3-1 - hemieskript Dr. R. Steiger rganische hemie, Reaktionsmechanismen Das Lernziel dieser Unterrichtseinheit beinhaltet folgende Punkte: Wie können funktionelle Gruppen ineinander überführt
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2018
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
Aufgaben zur Chemie der Alkohole und Ether (incl. deren Herstellung)
 Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) TGJ Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer Lösung?
Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) TGJ Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer Lösung?
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Synthese von Essigsäureisopropylester (1) Präparat 1
 Synthese von Essigsäureisopropylester (1) Präparat 1 1. Reaktionstyp: Azeotrope Veresterung 2. Reaktionsgleichung: 3 3 3 3 2 3 3 Essigsäure Isopropanol Essigsäureisopropylester Wasser 60,05 g/mol 60,1
Synthese von Essigsäureisopropylester (1) Präparat 1 1. Reaktionstyp: Azeotrope Veresterung 2. Reaktionsgleichung: 3 3 3 3 2 3 3 Essigsäure Isopropanol Essigsäureisopropylester Wasser 60,05 g/mol 60,1
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
a81 a Carbonylverbindungen (I)
 Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
a81 a Carbonylverbindungen (I)
 Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
12 Naturstoffe. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
 Lösungen zu den Durchblick-Seiten 12.27 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 a) Fette dienen im Körper als Speicherstoff ( Brennstoff ), Wärmeisolator, Stoßdämpfer, Baustoff und Stoffwechselbaustein.
Lösungen zu den Durchblick-Seiten 12.27 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 a) Fette dienen im Körper als Speicherstoff ( Brennstoff ), Wärmeisolator, Stoßdämpfer, Baustoff und Stoffwechselbaustein.
Doppelbindung. einfach besetztes Orbital. Resonanzstruktur II so auch nicht! (Seitensprungsituation) C C C
 RGANISE EMIE 1 Teil 2 Einfache Symbolik zur Beschreibung solcher ybridbindungen: Verwendung der schon bekannten Lewis-Punkt/Strich-Symbolik Einfachbindung l Doppelbindung n-elektronen (nicht bindendes
RGANISE EMIE 1 Teil 2 Einfache Symbolik zur Beschreibung solcher ybridbindungen: Verwendung der schon bekannten Lewis-Punkt/Strich-Symbolik Einfachbindung l Doppelbindung n-elektronen (nicht bindendes
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Organik-Beispiel. Inhaltsverzeichnis
 Inhaltsverzeichnis I. Säure-Basen-Gleichungen... 2 a) Nach Arrhenius:... 2 b) Nach Broensted:... 2 c) Nach Lewis:... 2 II. H 2 O + HCl?... 4 a) Was ist in der Reaktion passiert? Welche Produkte entstehen?...
Inhaltsverzeichnis I. Säure-Basen-Gleichungen... 2 a) Nach Arrhenius:... 2 b) Nach Broensted:... 2 c) Nach Lewis:... 2 II. H 2 O + HCl?... 4 a) Was ist in der Reaktion passiert? Welche Produkte entstehen?...
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Orbital. Atombindung, Bindung. Elektronegativität. Dipol
 GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon
 Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Name, Vorname: Matrikelnummer: Studienrichtung: Fragen auf den folgenden Seiten: Musterlösung zur Klausur zur Experimentalvorlesung Organische Chemie
 rganisch-chemisches nstitut Fakultät für Chemie und Geowissenschaften Universität eidelberg 23. Juni 2015 Musterlösung zur Klausur zur Experimentalvorlesung rganische Chemie von Prof. Stephen ashmi Name,
rganisch-chemisches nstitut Fakultät für Chemie und Geowissenschaften Universität eidelberg 23. Juni 2015 Musterlösung zur Klausur zur Experimentalvorlesung rganische Chemie von Prof. Stephen ashmi Name,
NH 3. CCl 4 CO 2. Lösungen zur Lernzielkontrolle Sekunda. Hilfsmittel: PSE, Taschenrechner
 Lösungen zur Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (1) 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) leitfähig,
Lösungen zur Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (1) 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) leitfähig,
Lösungsblatt 11: Carbonsäuren und Aromaten
 1 Lösungsblatt 11: Carbonsäuren und Aromaten Warm Up Benennen Sie die folgenden Verbindungen nach IUPAC. Finden Sie gegebenenfalls die Trivialnamen: Aufgaben 1) Carbonsäuren i. Begründen Sie aufgrund der
1 Lösungsblatt 11: Carbonsäuren und Aromaten Warm Up Benennen Sie die folgenden Verbindungen nach IUPAC. Finden Sie gegebenenfalls die Trivialnamen: Aufgaben 1) Carbonsäuren i. Begründen Sie aufgrund der
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie Das komplette Material finden Sie hier: Download bei School-Scout.de B201 LÖSUNG:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie Das komplette Material finden Sie hier: Download bei School-Scout.de B201 LÖSUNG:
Versuch: Bromierung von Phenol
 Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Organische Chemie für MST 5. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Bromierung von Cycloalkenen
 hemie Q1 / 4. Reaktionswege der organischen hemie / 4.2 Alkene und elektrophile Addition 1/ omierung von ycloalkenen Zufällig kommt ein 2-Molekül in die Nähe der elektronenreichen Doppelbindung. Ulrich
hemie Q1 / 4. Reaktionswege der organischen hemie / 4.2 Alkene und elektrophile Addition 1/ omierung von ycloalkenen Zufällig kommt ein 2-Molekül in die Nähe der elektronenreichen Doppelbindung. Ulrich
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Rückblick Aufgaben. 4 Elemente Chemie Bayern 11
 Zu den Aufgaben A1 Im ydrogenchloridmolekül sind ein Wasserstoffatom und ein hloratom über eine Elektronenpaarbindung miteinander verbunden. Die Elektronenwolke ist dabei zum hloratom hin verschoben, da
Zu den Aufgaben A1 Im ydrogenchloridmolekül sind ein Wasserstoffatom und ein hloratom über eine Elektronenpaarbindung miteinander verbunden. Die Elektronenwolke ist dabei zum hloratom hin verschoben, da
Bist Du nicht "FIT", dann musst Du nacharbeiten.
 Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Vergleichende Reaktionsmechanismen
 Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME 1 Vergleichende Reaktionsmechanismen 1. rdnen Sie die angegebenen Reaktionen einem Reaktionstyp zu und formulieren Sie den Reaktionsmechanismus. Radikalische
Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME 1 Vergleichende Reaktionsmechanismen 1. rdnen Sie die angegebenen Reaktionen einem Reaktionstyp zu und formulieren Sie den Reaktionsmechanismus. Radikalische
Grundwissen Chemie 9. Jahrgangsstufe G8
 Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Element. Verbindung. Reinstoff. homogenes Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Basiskonzepte. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Cl C H O. Lösungen zu den Aufgaben
 Lösungen zu den Aufgaben Struktur-Eigenschafts-Konzept Zu den Aufgaben A1 Eine Lösung in Tabellenform kann so aussehen: Stoff Ethan Ethanal Ethanol Ethansäure Siedetemperatur 88 21 78 118 Struktur- formeln
Lösungen zu den Aufgaben Struktur-Eigenschafts-Konzept Zu den Aufgaben A1 Eine Lösung in Tabellenform kann so aussehen: Stoff Ethan Ethanal Ethanol Ethansäure Siedetemperatur 88 21 78 118 Struktur- formeln
2.Präparat: 1,2 Dibrom -1-phenylethan
 Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden!
 Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Claisen-Kondensation
 Quelle: gerlicher.de In dieser Datei soll der Mechanismus der Biosynthese wichtiger Bausteine von Ölen und festen Fetten näher betrachtet werden, nämlich die Biosynthese der Fettsäuren. Quelle: gerlicher.de
Quelle: gerlicher.de In dieser Datei soll der Mechanismus der Biosynthese wichtiger Bausteine von Ölen und festen Fetten näher betrachtet werden, nämlich die Biosynthese der Fettsäuren. Quelle: gerlicher.de
13. Amine und ihre Derivate
 Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Lösung 3 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Zum Nachlesen/Vertiefen des Vorlesungsstoffs von heute siehe Maitland
1 Lösung 3 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Zum Nachlesen/Vertiefen des Vorlesungsstoffs von heute siehe Maitland
Polare Bindungen. Die Elektronen eines bindenden. Elektronenpaares sind in Wirklichkeit eher zwei Elektronen, die sich mehrheitlich
 Moleküle Polare Bindungen Die Elektronen eines bindenden (gemeinsamen) Elektronenpaares sind in Wirklichkeit eher zwei Elektronen, die sich mehrheitlich zwischen den beiden Atomkernen der Bindungspartner
Moleküle Polare Bindungen Die Elektronen eines bindenden (gemeinsamen) Elektronenpaares sind in Wirklichkeit eher zwei Elektronen, die sich mehrheitlich zwischen den beiden Atomkernen der Bindungspartner
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
Prüfungsaufgaben von und zu Aromaten (incl. Aryldiazoniumsalzen)
 Prüfungsaufgaben von und zu Aromaten (incl. Aryldiazoniumsalzen) Die Aufgaben lehnen sich an Prüfungsaufgaben aus der Abschlussprüfung für Chemielaboranten der vergangenen Jahre an. äufig erstrecken sich
Prüfungsaufgaben von und zu Aromaten (incl. Aryldiazoniumsalzen) Die Aufgaben lehnen sich an Prüfungsaufgaben aus der Abschlussprüfung für Chemielaboranten der vergangenen Jahre an. äufig erstrecken sich
Organische Chemie für Mediziner WS 2016/2017. Übungsblatt 3: Ausgewählte Substanzklassen
 1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
Grundwissenkarten Hans-Carossa-Gymnasium
 Grundwissenkarten Hans-Carossa-Gymnasium Oberstufe Chemie SG Es sind insgesamt 27 Karten für die Oberstufe erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa-Gymnasium Oberstufe Chemie SG Es sind insgesamt 27 Karten für die Oberstufe erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle
 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
Funktionelle Gruppen Alkohol
 Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
1. Vervollständigen Sie folgende Tabelle:
 Die Zwischenmolekularen Kräfte LÖSUG Seite 1 von 8 ÜBUGE 1. Vervollständigen Sie folgende Tabelle: e e Ar Kr Xe Elektronenzahl 2 10 18 36 54 Stärke der Van der Waals Kräfte nimmt in Pfeilrichtung zu Siede-
Die Zwischenmolekularen Kräfte LÖSUG Seite 1 von 8 ÜBUGE 1. Vervollständigen Sie folgende Tabelle: e e Ar Kr Xe Elektronenzahl 2 10 18 36 54 Stärke der Van der Waals Kräfte nimmt in Pfeilrichtung zu Siede-
Grundwissen C8 NTG. 1. Stoffe und Reaktionen. Reinstoff
 Grundwissen C8 NTG 1. Stoffe und Reaktionen Reinstoff Stoffgemisch - besitzt unter bestimmten Bedingungen (z.b. Temperatur, Druck ) kennzeichnende Eigenschaften, z.b. Farbe, Geruch, Geschmack, Dichte,
Grundwissen C8 NTG 1. Stoffe und Reaktionen Reinstoff Stoffgemisch - besitzt unter bestimmten Bedingungen (z.b. Temperatur, Druck ) kennzeichnende Eigenschaften, z.b. Farbe, Geruch, Geschmack, Dichte,
Feststellungsprüfung Chemie Lösungen. Wegen seiner hohen Reaktivität kommt Chlor in der Natur nicht elementar vor. = 26, ,957=35,45
 Thema I 1a 1b 1c 1d 1e 2a 2b Feststellungsprüfung Chemie Lösungen Wegen seiner hohen Reaktivität kommt Chlor in der Natur nicht elementar vor.,,,, = 26,496 8,957=35,45 Die relative Isotopenmasse ist die
Thema I 1a 1b 1c 1d 1e 2a 2b Feststellungsprüfung Chemie Lösungen Wegen seiner hohen Reaktivität kommt Chlor in der Natur nicht elementar vor.,,,, = 26,496 8,957=35,45 Die relative Isotopenmasse ist die
Organische Chemie. Kapitel 1. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Organische Verbindungen enthalten Kohlenstoff
 rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
Organische Chemie 2 SPF BCH am Inhaltsverzeichnis Sie kennen alle Karteikärtchen zum Thema... 2
 Organische Chemie 2 Inhaltsverzeichnis Sie kennen alle Karteikärtchen zum Thema.... 2 Sie kennen vier Grundtypen von Reaktionen mit ihren Mechanismen (S. 239) mit aliphatischen, organischen Stoffen und
Organische Chemie 2 Inhaltsverzeichnis Sie kennen alle Karteikärtchen zum Thema.... 2 Sie kennen vier Grundtypen von Reaktionen mit ihren Mechanismen (S. 239) mit aliphatischen, organischen Stoffen und
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 23.11.2010 Gruppe 4: Aromaten Versuch (elektr.
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 23.11.2010 Gruppe 4: Aromaten Versuch (elektr.
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Posten 1a. Wie sieht das Kugelwolkenmodell aus von einem Sauerstoffatom? Antworten: a) (=> Posten 9o) b) (=> Posten 16l) c) (=> Posten 8k)
 Posten 1a Wie sieht das Kugelwolkenmodell aus von einem Sauerstoffatom? a) (=> Posten 9o) b) (=> Posten 16l) c) (=> Posten 8k) d) (=> Posten 13f) Posten 1d Welcher der beiden Stoffe hat den tieferen Siedepunkt?
Posten 1a Wie sieht das Kugelwolkenmodell aus von einem Sauerstoffatom? a) (=> Posten 9o) b) (=> Posten 16l) c) (=> Posten 8k) d) (=> Posten 13f) Posten 1d Welcher der beiden Stoffe hat den tieferen Siedepunkt?
Grundwissen Chemie 9. Jahrgangsstufe. Basiskonzepte
 1 Grundwissen Chemie 9. Jahrgangsstufe Basiskonzepte Wesentlich zur Strukturierung und zum Verständnis chemischer Sachverhalte tragen die fünf Basiskonzepte bei, welche fachtypische Betrachtungs- und Deutungsweisen
1 Grundwissen Chemie 9. Jahrgangsstufe Basiskonzepte Wesentlich zur Strukturierung und zum Verständnis chemischer Sachverhalte tragen die fünf Basiskonzepte bei, welche fachtypische Betrachtungs- und Deutungsweisen
