Regenwasseranalyse. Fachspezifische Themenstellung. Verena Burgstaller und Lisa Lienbacher
|
|
|
- Joseph Kappel
- vor 7 Jahren
- Abrufe
Transkript
1 Regenwasseranalyse Fachspezifische Themenstellung Verena Burgstaller und Lisa Lienbacher
2 Inhaltsverzeichnis
3 Einleitung Das wichtigste und zugleich auch schwerste bei diesem Projekt ist es, zu regelmäßigen Zeiten, Regen von allen Standorten zu beziehen, was nicht so einfach ist, da es nicht immer überall regnet. Als Standorte wählten wir Euratsfeld, Neukirchen und Wien. Die Proben werden im Jänner, Februar und März gezogen. Diese Proben werden auf einzelne Parameter analysiert. Als Parameter wählten wir: Ammonium Nitrit Nitrat Phosphat Blei Kupfer Leitfähigkeit ph-wert Diese Parameter werden mit dem Photometer, dem Gaschromatographen, ph-meter und Leitfähigkeitsmesser analysiert, anschließend wird eine Tabelle erstellt und die Proben werden miteinander verglichen. Es wird verglichen wo saurer Regen auftritt und was wir aus den Werten schließen können.
4 Aufgabenstellung/Arbeitshypothese Die Aufgabe der Fachspezifischen Themenstellung besteht darin Regenwasser zu analysieren. Das Wasser wird auf viele verschiedenen Parameter auf drei verschiedenen Standorten, und zwar Euratsfeld (Bez. AM), Wien, Neukirchen (Bez. ME), getestet. Die Parameter sind Nitrit, Nitrat, Ammonium, Phosphat, ph-wert, Leitfähigkeit und Schwermetalle (Blei und Kupfer). Es wird mit verschiedenen Messgeräten gemessen, den ph-meter, das Photometer und das Graphitrohr-AAS. Die Ergebnisse werden ausgewertet und interpretiert, um zu sehen, ob sie mit unseren Hypothesen übereinstimmen, oder ob diese widerlegt werden. Die Hypothesen besagen, dass in der Stadt höhere Werte vorzuweisen sein werden, da hier mehr Emissionen in die Luft gelangen. Auch der ph-wert wird in Stadt höher sein, wegen der vielen Abgase. Nur Stickstoff könnte auch am Land mehr im Regenwasser sein, dass diese auch durch die Landwirtschaft verursacht werden kann. Dann kann man sehen, ob heut zu Tage Saurer Regen noch eine Rolle spielt oder nicht.
5 Theoretische Grundlagen Was ist Regen? Durch Erwärmung von Seen, Meeren und sonstigen Feuchtflächen verdunstet das Wasser und steigt auf. In höheren und kälteren Lagen kondensiert der Wasserdampf zu Wasser-tropfen. Diese fallen dann in Form von Regen, Schnee oder Hagel wieder zurück zur Erde. Viele Stoffe sind aufgrund ihrer Löslichkeit in Wasser gut löslich. Somit können Stoffe, die in der Luft enthalten sind ins Regenwasser übergehen. Der Niederschlag wird dadurch sozusagen zum Abwasser. Daher kann man Aussagen über die Luftverschmutzung durch Landwirtschaft, Industrie- und Fahrzeugabgase und deren Folgen auf Böden und Gewässer treffen. Überwiegend wird Saurer Regen von Menschenhand verursacht. Durch die Emissionen die die eine neue Verbindung mit Regen eingehen können, entsteht saurer Regen. Saurer Regen besteht meist aus Schwefelsäure und Salpetersäure, die sich durch die Verbindung des Wassers mit Schwefeloxid oder Stickoxid entwickeln. Seit 1980 geht in Mitteleuropa die Intensität des sauren Regens zurück. Basischer Regen ist Niederschlag, der einen höheren ph-wert als reines Wasser aufweist. Dieser entsteht durch den natürlichen Kohlendioxid-Gehalt der aus der Erdatmosphäre stammt. Basischer Regen ist örtlich begrenzt und ist das Gegenstück zum sauren Regen.
6 Saurer Regen Saurer Regen ist Niederschlag mit einem ph-wert niedriger als 5,5. Das natürliche Vorhandensein von CO 2 hat einen normalen ph-wert von 5-7. Verursacher Hauptverursacher ist die Luftverschmutzung durch Abgase. Dazu zählen Verkehr, Industrie und Kleinverbraucher. Vor allem durch die Verbrennung von fossilen Brennstoffen, denn dabei entsteht Schwefeloxid, das mit Wasser und Sauerstoff Schwefelsäure bilden kann. Dieser Reaktionsmechanismus benötigt das Wasser erst zur Bildung der Schwefelsäure aus dem Schwefeltrioxid: 2 SO 2 + O 2 2 SO 3 SO 3 + H 2 O H 2 SO 4 Diese Reaktion erfolgt komplett in wässriger Lösung, z. B. Wassertropfen im Nebel: SO 2 + H 2 O H 2 SO 3 2 H 2 SO 3 + O 2 2 H 2 SO 4 Weiterhin entstehen bei jeder Verbrennung Stickoxide (NOx) durch Umwandlung des im Brennstoff und in der Luft enthaltenen Stickstoffes. Diese bilden mit Wasser und Sauerstoff Salpetersäure (HNO3). 2 NO 2 + H 2 O HNO 2 + HNO 3 N 2 O 4 + H 2 O HNO 2 + HNO 3 Kohlendioxid kann sich auch im Wasser lösen und reagiert zu Kohlensäure. CO 2 + H 2 O H 2 CO 3 In tropischen Gebieten können auch organische Säuren zur Absenkung des ph- Wertes von Niederschlägen beitragen.
7 Auswirkungen Pflanzen Saurer Regen kann Waldsterben verursachen, dieser kommt vor allem in Regionen mit häufigen und ergiebigen Niederschlägen, mit niedriger Jahresdurchschnittstemperatur vor. Es kann aber auch die Übersäuerung des Bodens verursacht werden. Dabei werden giftige Schwermetallionen freigesetzt, die die Feinwurzeln der Pflanzen absterben lassen. Dadurch sind die Bäume anfälliger für Krankheiten, natürliche Belastungen und Schädlingsbefall. Gewässer Gewässer sind nicht direkt von der Aufnahme des Sauren Regens über die Oberfläche betroffen, sondern durch das Eindringen des Bodenabflusses. Metall- Kationen, wie Al 3+, die als Zellgifte wirken können zur Artenverarmung führen. Durch die Übersäuerung der Gewässer können Mikroorganismen, aber auch Schnecken, Muscheln, Kleinkrebse, Eintagsfliegen und Fische sterben. Gebäude und Gesteine Saurer Regen lässt die Verwitterung von Gebäuden schneller voranschreiten. So werden auch zahlreiche Gebäude und Kulturdenkmäler beschädigt. Calciumcarbonat reagiert mit den gelösten Wasserstoffionen im sauren Regen. Bei dieser Reaktion zerfällt es in Calciumionen, Kohlendioxid und Wasser: CaCO3 + 2H+ CO2 +H2O + Ca2+ Dann reagieren die Sulfationen der Schwefelsäure mit den Calciumionen und überziehen den Marmor oder Kalkstein mit einer weißen Schicht von Gips: Ca2+ +SO42 + 2H2O CaSO4 + 2H2O Der Regen trägt mit der Zeit einen Teil der Gipskruste ab. Dies führt zu kleinen Rissen und zunehmender Erosion. Menschen Saurer Regen ist auch für den Menschen ein Störfaktor, denn vor allem Schwefeldioxid und Stickoxide können die Atemwege, wie Lunge und Schleimhäute schädigen und Asthma hervorrufen. Auch die Blutgefäße können beeinträchtigt werden.
8 Gegenmaßnahmen Man versucht mit Kalk die Übersäuerung zu neutralisieren, in dem man Kalk per Hubschrauber verstreut. Doch eigentlich ist es besser, wenn man die Ursachen bekämpft. Seit den 80er Jahren entschwefelt man schon Rauchgase. Deswegen werden heute in den Autos Katalysatoren verwendet, um die Stickstoffoxide zu entfernen. Wichtig ist es auch, Verkehrsmittel sinnvoll zu nutzen, dass bedeutet die Emissionen zu reduzieren und die Regierungen sollten härtere Auflagen einbringen. Trinkwasserverordnung Parameter Grenzwert mg/l Nitrat 50 Blei 0,01 Kupfer 2 Nitrit 0,5 Ammonium 0,5 Phosphat Kein Grenzwert
9 Ammonium Ammonium gehört zu den wichtigsten Indikatoren bei der Verschmutzung von Gewässern. Bei Trink- und Flusswasser üblichen ph-werten liegt Ammoniak (NH3) ausschließlich als Ammonium NH4+ vor. Ammonium entsteht bei der Zersetzung von stickstoffhaltigen organischen Substanzen durch Mikroorganismen unter sauerstoffarmen Bedingungen. Eine direkt giftige Wirkung ist nicht bekannt, im Gegensatz zu Ammoniak. Jedoch entsteht Ammonium durch die mikrobiologische Zersetzung von Abfallstoffen und Fäkalien. Liegt also ein erhöhter Ammoniumwert im Wasser vor ist mit einer ernstzunehmenden Verschmutzung zu rechnen. Ammonium gelangt durch Überdüngung und Düngerausschwemmungen direkt in Fluss und Grundwasser. Ist der Ammoniumgehalt erhöht ist meist auch der Nitratgehalt dementsprechend hoch. Der Ammoniumgehalt ist auch ein wichtiger Faktor bei der Bewertung der Badewasserqualität, da es auch beim enzymatischen Abbau von Harnstoff entsteht. Die Konzentration von Ammonium, Nitrit und Nitrat ist wichtig bei der Überwachung von Kläranlagen. Die Nitrifikation (Umwandlung von Ammonium zu Nitrat) ist eine der wichtigsten Aufgaben von Kläranlagen. Grenzwerte & Richtlinien Trinkwasserverordnung (TVO) max. 0,5 mg/l EU-Trinkwasserrichtlinie Richtwert max. 0,5 mg/l 0,05 mg/l
10 Nitrat Stickstoffoxide gelangen auf verschiedenste Weiße in die Umwelt.Die Oxidation des in der Atmosphäre vorhandenen Stickstoffes findet durch die Natur selbst statt durch elektrische Entladungen und Blitze. Auch durch die Technik, wie durch Fahrzeuge und Verbrennungsanlagen kommt es zur Oxidation von Stickstoff. Die Stickstoffoxide die in der Atmosphäre vorhanden sind werden zum Teil mit dem Regen ausgewaschen und bilden so Nitrite und Nitrate. Durch Katalysatoren die in Abgasanlagen von Kraftfahrzeugen eingebaut sind mindern drastisch die Emissionen. Nitrate sind Hauptnährstoffe und haben somit einen sehr positiven Einfluss auf das Pflanzenwachstum. Deshalb werden im Gartenbau so wie in der Landwirtschaft oft mineralische Dünger die auf Stickstoff basieren eingesetzt. Durch die Auswaschung kommt es oftmals zu einer hohen Nitratgehalten in nahe gelegenen Gewässern. Dieser hohe Nitratgehalt fördert das Pflanzen- und Algenwachstum in Teich- und Flussgewässern. Durch die starke Überdüngung kann es zum Kippen von Gewässern kommen, das Ökosystem kommt somit aus seinem Gleichgewicht. Es kommt zur Ausbildung eines Fäulnismilieus. Das Milieu ist somit arm an Sauerstoff, dies hat meist katastrophale Folgen für die Lebewesen die in diesen Gewässern leben. Die Gefahr des kippens ist bei stehenden Gewässern wesentlich höher als bei Fließgewässern. Eine direkt giftige Wirkung geht vom Nitrat nicht aus. Aufgenommenes Nitrat wird relativ schnell wieder vom Körper ausgeschieden. Für Säuglinge ist Nitrat jedoch gefährlich, weil es im Körper zur Umwandlung von Nitrat in Nitrit kommt. Der Sauerstofftransport von Säuglingen kann somit gehemmt werden. Es kommt zur inneren Erstickung man spricht von Blausucht. Bei Erwachsenen gibt es dieses Problem nicht da die Bindung des Sauerstoffs an die roten Blutkörperchen auf eine nicht durch Nitrat desaktivierbare Weise erfolgt. Die einzige Gefahr die vom Nitrat wirklich aus geht ist ihre Verbindung mit Eiweißstoffen im Körpern man spricht dann von sogenannten Notrosaminen. Nitrosamine sind Krebserzeugend und verändern die Erbsubstanz. Das Gefährdungspotential für die Gesundheit von Nitrat im Trink- und Oberflächengewässer ist noch relativ unbekannt. Eine regelmäßige Kontrolle ist somit unerlässlich. Trinkwasserverordnung (TVO) max. 50 mg/ L EU-Trinkwasserrichtlinie max. 50 mg/l
11 Phosphat Bedingt durch eine Vielzahl von phosphorhaltigen Produkten in Haushalt und Industrie ist in den letzten Jahrzehnten eine ernstzunehmende Phosphorbelastung der Umwelt eingetreten. Ein Großteil des konsumierten Phosphors ist als natürlicher Bestandteil in Nahrungsmitteln enthalten. Der Rest stammt aus Wasch-, Reinigungsund Spülmitteln. Der größte Teil des Phosphors wird über die kommunale Kanalisation den Kläranlagen zugeführt. Phosphatreiche Substanzen gelten als bewährte Düngestoffe (Gülle, Kunstdünger). Durch einen übermäßigen Gebrauch können so hohe Phosphatkonzentrationen im Boden entstehen. Durch das Auswaschen kommt es wiederum zu erhöhten Phosphatgehalten im Grund- und Oberflächenwasser. Ein großer Fortschritt war die Entwicklung von phosphatfreien Waschmitteln. Dies ist ein wichtiger Fortschritt zur Entlastung der Umwelt. Phosphor weißt keine nachgewiesenen gesundheitsschädlichen Eigenschaften auf. Aufgrund des hohen Gehaltes von Phosphor in Pflanzen kann es jedoch zur Eutrophierung von Gewässern kommen. Dies hat somit dieselbe Folge wie bei Nitrat, Gewässer können kippen. Ein erhöhter Phosphorgehalt ist genauso wie bei Ammonium und Nitrat ein wichtiger Hinweis auf die mögliche Verschmutzung des Wassers durch Fäkalien. Aufgrund der verschiedenen Verbindungen gibt es auch verschiedene Richt- und Grenzwerte. Nitrit Kommt im Boden und Gewässern vor sowie in Kläranlagen in Form von Nitritbakterien. Nitritionen bilden sich durch Oxidation aus Ammoniumionen unter Verbrauch von Sauerstoff und sind somit das Zwischenprodukt bei der vollständigen Oxidation von Stickstoff zu Nitrat.
12 Blei Blei in der Luft wird durch bleihaltige Stäube verursacht, diese stammen aus der bleierzeugenden Industrie, der Verbrennung von Kohle und aus dem Verkehr. Das Blei im Wasser kommt hauptsächlich von der Ausschwemmung von Bleibelasteten Böden. Auch im Regen sind geringe Anteile von Blei zu finden. Durch den Bau von Kläranlagen ist die Verschmutzung der Gewässer durch Blei stark zurückgegangen. Durch die Belastung von Luft, Boden und Wasser kann Blei in die Nahrungskette gelangen. Wasserleitungen aus Blei können das Trinkwasser belasten. Kupfer Kupfer kann durch die Landwirtschaft in die Umwelt gelangen. Kupfer wird auch als Zusatz zu Grünfutter bei Kupfermangel verwendet. Andere Verbindungen werden als Insektizid, Fungizid oder Bakterizid genutzt. Kupfer kann aber auch durch Dachmateralien ins Regenwasser gelangen. Kupfer hat für viele Lebewesen einen essentielle Bedeutung. Bei Pflanzen kann bei einer Konzentration unter 5 ppm eine Mangelerscheinung auftreten. Jedoch für Pilze, Bakterien und Algen ist Kupfer sehr giftig. Kupfer verursacht auch indirekt Umweltschäden, da es die Bildung von Dioxinen und Furanen bei der Müllverbrennung katalysiert. Für den Menschen ist Kupfer ein essentielles Element. Es ist Bestandteil vieler Enzyme. Jedoch soll eine Einnahme von 5 mg Kupfer/Tag nicht überschritten werden. Die Einnahme von Kupfer kann zu Brechreiz führen, so bleibt dieser Stoff nicht lange im Körper. Kupfervergiftungen sind bei Kindern deutlich gefährlich als bei Erwachsenen.
13 Elektrische Leitfähigkeit Ist eine materialspezifische Fähigkeit um elektrischen Strom zu leiten, die elektrolytische Stromleitfähigkeit wässriger Lösungen hängt somit ab von der Konzentration der Wasserinhaltsstoffe und deren Ionenleitfähigkeit. Die Wertigkeit der Anionen und Kationen wird somit gemessen, deren Beweglichkeit wird von der Temperatur beeinflusst. Die Leitfähigkeit gilt als Summenparameter für die Ionenkonzentration und damit somit auch für den Salzgehalt im Abwasser. Die Messwerte werden auf eine Bezugstemperatur, in der Regel meist 25 C umgerechnet angeben. Bei kleineren Gewässern liefert die elektrische Leitfähigkeit vor allem Anhaltspunkte über die Einträge von Niederschlags- und Abwasser und die dadurch ausgelösten Veränderungen der Wasserbeschaffenheit. Hohe Werte der Leitfähigkeit können relativ schnell zu einer Aussage über den Gesamtgehalt an gelösten Salzen in Gewässern führen. Die Salze können natürlichen Ursprungs sein zum Beispiel durch Verwitterung von Gesteinen oder aber auch aus menschlicher Herkunft stammen zum Beispiel durch Streusalz und Industrieabwässer. der ph-wert Der ph-wert sagt aus ob eine wässrige Lösung sauer oder basisch ist. Er ist der negative dekadische Logarithmus (=Zehnerlogarithmus) der Wasserstoffionen- Aktivität. ph = -log 10 (a H ) Einteilung:
14 ph = < 7 saure wässrige Lösung ph = 7 neutrale wässrige Lösung absolut reines Wasser ph > 7 basische wässrige Lösung
15 Methodik Die Parameter Ammonium, Nitrit, Nitrat und Phosphat werden mit einem Photometer gemessen. Man verwendet dazu das Photometer MERCK SQ 118. Nun ein Beispiel, wie die Messung und die Vorbereitung durchzuführen ist. Nitrat: Man stellt bei dem Photometer die Methodennummer ein. Man versetzt die Reagenzgläser (Proben und 1 Blindprobe) mit 1 blauem Microlöffel NO 3-1A. Dann werden die Reagenzgläser mit je 5 ml NO 3-2A (=Schwefelsäure) versetzt. Anschließend wird je 1,5 ml Probe dazugegeben und gemischt. Bei der Blindprobe wird destilliertes Wasser beigegeben. Dann drückt man die Blindwert-Taste und wartet die Reaktionszeit von 10 Minuten ab. Bei dem Signalton werden die Proben in die Küvette gefüllt und mit dem Photometer gemessen. Es wurden folgende Methodennummern verwendet. Ammonium... 5 Nitrit Nitrat Phosphat Blei und Kupfer wurden mit dem Grapitrohr AAS gemessen. Mit PERKIN ELMER, Zeeman Atom Absorption Spectrometer 4100 ZL. Dazu musste am Anfang eine Stammlösung hergestellt werden und auch daraus 4 Standards. Für die Kupfer- und Bleistammlösung werden die vorgegebenen Standards 1000 mg/l verdünnt auf 1000 µg/l. Dann werden 4 Standards hergestellt. Für Blei: 10, 20, 50 und 100 µg/l. Für Kupfer: 10, 25, 50 und 100 µg/l. Der ph-wert wurde mit einem ph-meter gemessen: WTW ph 340i. Dazu musste das Gerät vorher kalibriert werden. Die Leitfähigkeit wurde mit dem Microprocessor Conductivity Meter LF 537 (WTW) gemessen, welches auch vorher kalibriert wurde. Standorte: gekennzeichnet mit grünem Punkt
16 Ergebnisse
17 Interpretation Der ph-wert zeigt, dass alle Proben im eher sauren Bereich liegen. Es ist jedoch zu sehen, dass der Regen vom Standort Euratsfeld immer am höchsten ist. Bis auf 2 Messungen von Euratsfeld (Februar, März) befinden sich die Proben unter 5,5 und zählen so eigentlich schon zu Saurem Regen. Jedoch überschreiten sie diese Grenze nur sehr gering.
18 Die Leitfähigkeit gibt Auskunft über die gelösten Salze und die Ionenkonzentration im Wasser. Es ist zu sehen, dass sich in Neukirchen wenig gelöste Salze im Wasser befinden, da nur eine geringe Leitfähigkeit nachzuweisen war. Auch hier ist zu sehen, dass im Standort Neukirchen wenig Nitrit im Regenwasser vorhanden ist. Bei der letzten Messung war sogar weniger vorhanden als zu bestimmen möglich war. Euratsfeld zeigt bei beiden Messungen einen hohen Wert auf und überschreitet sogar die Grenzwerte des Trinkwassers. Das bedeutet, dass man das Wasser nicht trinken sollte. Auch in der Probe von Wien war viel Nitrit zu finden im März. Hier bestätigt sich unsere These jedoch nicht, dass am Land mehr Nitrit vorzufinden ist, dies kann jedoch aber auch vom Zeitraum der Beobachtung abhängen, da wir im Winter unser Projekt durchgeführt haben, und zu dieser Zeit die Landwirtschaft nicht intensiv betrieben wird.
19 Die Nitratwerte sind relativ gering und befinden sich weit unter dem Grenzwert von Trinkwasser. Das heißt, dass Wasser könnte laut diesem Parameter als Trinkwasser verwendet werden. Hier sind am Land und in der Stadt die Unterschiede der Nitratgehalte sehr gering.
20
21 Zusammenfassung
Regenwasseranalyse. Fachspezifische Themenstellung. Verena Burgstaller und Lisa Lienbacher
 Regenwasseranalyse Fachspezifische Themenstellung Verena Burgstaller und Lisa Lienbacher INHALT Einleitung... 3 Aufgabenstellung/Arbeitshypothese... 4 Theoretische Grundlagen... 5 Methodik... 14 Ergebnisse...
Regenwasseranalyse Fachspezifische Themenstellung Verena Burgstaller und Lisa Lienbacher INHALT Einleitung... 3 Aufgabenstellung/Arbeitshypothese... 4 Theoretische Grundlagen... 5 Methodik... 14 Ergebnisse...
Was bedeutet das für den See:
 Es wird viel über Düngung Phosphat, Nitrat, NOx und was sonst noch unsere Umwelt bedroht geredet. Hier wird ein Versuch gemacht die Wirkung von Phosphat und den Stickstoffweg über die Gülle ins Wasser
Es wird viel über Düngung Phosphat, Nitrat, NOx und was sonst noch unsere Umwelt bedroht geredet. Hier wird ein Versuch gemacht die Wirkung von Phosphat und den Stickstoffweg über die Gülle ins Wasser
Die Qualität der Fliessgewässer im Kanton Schaffhausen. Übersicht 2002 Publikation zum UNO-Jahr des Süsswassers
 Die Qualität der Fliessgewässer im Kanton Schaffhausen Übersicht 2002 Publikation zum UNO-Jahr des Süsswassers Die Schaffhauser Fliessgewässer Gesetzlicher Auftrag des ALU s Das Amt für Lebensmittelkontrolle
Die Qualität der Fliessgewässer im Kanton Schaffhausen Übersicht 2002 Publikation zum UNO-Jahr des Süsswassers Die Schaffhauser Fliessgewässer Gesetzlicher Auftrag des ALU s Das Amt für Lebensmittelkontrolle
Bericht Zur Chemischen, Biologischen und Ökologischen Untersuchung der mittleren " Aisch" zwischen Dietersheim und Landkreisgrenze b.
 1 Bericht Zur Chemischen, Biologischen und Ökologischen Untersuchung der mittleren " Aisch" zwischen Dietersheim und Landkreisgrenze b. Mailach 2015 2 Sauerstoff-Gehalt O² Sättigung in % 3 ANMERKUNGEN:
1 Bericht Zur Chemischen, Biologischen und Ökologischen Untersuchung der mittleren " Aisch" zwischen Dietersheim und Landkreisgrenze b. Mailach 2015 2 Sauerstoff-Gehalt O² Sättigung in % 3 ANMERKUNGEN:
Analyse der Chemischen Wasseruntersuchungen der Aisch 2009
 Analyse der Chemischen Wasseruntersuchungen der Aisch 2009 Gemessen wurde an 3 verschiedenen Stellen der Aisch (Meßstellen lagen an der Brücke Birkenfeld/Schauerheim, oberhalb Wehr Pahres, Trafo Dachsbach)
Analyse der Chemischen Wasseruntersuchungen der Aisch 2009 Gemessen wurde an 3 verschiedenen Stellen der Aisch (Meßstellen lagen an der Brücke Birkenfeld/Schauerheim, oberhalb Wehr Pahres, Trafo Dachsbach)
Schnellbericht Elbe. Sächsischer Elbe - Längsschnitt. Dresden
 Abteilung Wasser, Boden, Wertstoffe Zur Wetterwarte 11, 01109 Dresden Internet: http://www.smul.sachsen.de/lfulg Schnellbericht Elbe Sächsischer Elbe - Längsschnitt Zehren/ Dresden Ausgewählte Untersuchungsergebnisse
Abteilung Wasser, Boden, Wertstoffe Zur Wetterwarte 11, 01109 Dresden Internet: http://www.smul.sachsen.de/lfulg Schnellbericht Elbe Sächsischer Elbe - Längsschnitt Zehren/ Dresden Ausgewählte Untersuchungsergebnisse
Chemie Mathematik * Jahrgangsstufe 10 * ph-wert und Logarithmen
 Chemie Mathematik * Jahrgangsstufe 10 * p-wert und Logarithmen Vorkenntnisse über Säuren und Basen Säuren sind Protonendonatoren: Cl 2 O Cl O Salzsäure Cl Clor-Ion Cl Oxonium-Ion O Basen sind Protonenakzeptoren:
Chemie Mathematik * Jahrgangsstufe 10 * p-wert und Logarithmen Vorkenntnisse über Säuren und Basen Säuren sind Protonendonatoren: Cl 2 O Cl O Salzsäure Cl Clor-Ion Cl Oxonium-Ion O Basen sind Protonenakzeptoren:
Natürliche ökologische Energie- und Stoffkreisläufe
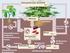 Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
Fact Sheet Beurteilung der Wasserqualität
 bericht 2008 Fact Sheet Beurteilung der Wasserqualität Inhalt Entwicklung der Wasserqualität 1984-2008 Gesamtbeurteilung der Wasserqualität 2004-2008 Beurteilung BSB 5 2004-2008 Beurteilung DOC 2004-2008
bericht 2008 Fact Sheet Beurteilung der Wasserqualität Inhalt Entwicklung der Wasserqualität 1984-2008 Gesamtbeurteilung der Wasserqualität 2004-2008 Beurteilung BSB 5 2004-2008 Beurteilung DOC 2004-2008
Biologie-Projekt. Saurer Regen ATHENE SAKELLARIOU HEIMBERGER HOLGER INA. -Team LANGLOTZ DANIEL VOLLBRECHT
 Biologie-Projekt Saurer Regen AT INA HO VO -Team ATHENE SAKELLARIOU INA HEIMBERGER HOLGER LANGLOTZ DANIEL VOLLBRECHT Präsentationsgliederung Vorversuch Hauptversuch Auswertung Recherche Ina Daniel Daniel
Biologie-Projekt Saurer Regen AT INA HO VO -Team ATHENE SAKELLARIOU INA HEIMBERGER HOLGER LANGLOTZ DANIEL VOLLBRECHT Präsentationsgliederung Vorversuch Hauptversuch Auswertung Recherche Ina Daniel Daniel
Geplanter Verlauf. Einführung Beurteilung nach abiotischen Faktoren Pause Beurteilung nach biotischen Faktoren Auswertung und Diskussion
 Ökosystem See Geplanter Verlauf Einführung Beurteilung nach abiotischen Faktoren Pause Beurteilung nach biotischen Faktoren Auswertung und Diskussion Schulbiologiezentrum Hannover - Ökologie stehender
Ökosystem See Geplanter Verlauf Einführung Beurteilung nach abiotischen Faktoren Pause Beurteilung nach biotischen Faktoren Auswertung und Diskussion Schulbiologiezentrum Hannover - Ökologie stehender
Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch 2013
 Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch 2013 Meßstellen: Pegel-Birkenfeld Flß/km 60,7 ; oberhalb Wehr Pahres Flß/km49,1; Trafo vor Dachsbach Flß./km 43,1 Anlagen: Diagramme und
Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch 2013 Meßstellen: Pegel-Birkenfeld Flß/km 60,7 ; oberhalb Wehr Pahres Flß/km49,1; Trafo vor Dachsbach Flß./km 43,1 Anlagen: Diagramme und
Reines Wasser ist Lebensqualität
 Reines Wasser ist Lebensqualität Der menschliche Körper besteht zu rund zwei Dritteln aus Wasser. Es ist offensichtlich, dass das Wasser eines der wichtigsten Elemente auf der Erde und für unseren Körper
Reines Wasser ist Lebensqualität Der menschliche Körper besteht zu rund zwei Dritteln aus Wasser. Es ist offensichtlich, dass das Wasser eines der wichtigsten Elemente auf der Erde und für unseren Körper
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Es liegt was in der Luft Emissionen, Schadstoffe und Grenzwerte
 Emissionen, Schadstoffe und Grenzwerte Definitionen: Emission: (= Aussendung ) Alle von einer Anlage ausgehenden Abgaben an die Umgebung. Emissionen können Stoffe sein, aber auch Energien: Stoffe: feste
Emissionen, Schadstoffe und Grenzwerte Definitionen: Emission: (= Aussendung ) Alle von einer Anlage ausgehenden Abgaben an die Umgebung. Emissionen können Stoffe sein, aber auch Energien: Stoffe: feste
Schwefeldioxid. Schwefel (S) verbindet sich bei der Verbrennung mit Sauerstoff (O 2 ). Das Ergebnis ist Schwefeldioxid: SO 2.
 Standzylinder Verbrennungslöffel Deckglas Schwefel Brenner Gib etwas Schwefel auf den Verbrennungslöffel und entzünde ihn mit der rauschenden Brennerflamme. Baue den Versuch nach der Abbildung auf und
Standzylinder Verbrennungslöffel Deckglas Schwefel Brenner Gib etwas Schwefel auf den Verbrennungslöffel und entzünde ihn mit der rauschenden Brennerflamme. Baue den Versuch nach der Abbildung auf und
Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch 2012
 Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch 2012 Meßstellen: Pegel-Birkenfeld Flß/km60,7 ; oberhalb Wehr Pahres Flß/km49,1 ; Trafo vor Dachsbach Flß/km43,1 Anlagen: Diagramme Chem.
Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch 2012 Meßstellen: Pegel-Birkenfeld Flß/km60,7 ; oberhalb Wehr Pahres Flß/km49,1 ; Trafo vor Dachsbach Flß/km43,1 Anlagen: Diagramme Chem.
Essigsäure färbt ph-papier rot. Natronlauge färbt ph-papier blau
 5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
Die Qualität der Fliessgewässer im Kanton Schaffhausen. Übersicht 20011/12
 Die Qualität der Fliessgewässer im Kanton Schaffhausen Übersicht 20011/12 Titelbild: Halbbach bei Oberhallau - Probennahmestelle "SH2" im europäischen Interreg-IV-Projekt Ökotoxikologischer Index zur Gewässerbewertung
Die Qualität der Fliessgewässer im Kanton Schaffhausen Übersicht 20011/12 Titelbild: Halbbach bei Oberhallau - Probennahmestelle "SH2" im europäischen Interreg-IV-Projekt Ökotoxikologischer Index zur Gewässerbewertung
Akkreditierungsumfang der Prüfstelle (EN ISO/IEC 17025:2005) K+U Umwelttechnik, Labor und Hydrologie GmbH / (Ident.Nr.: 0323)
 1 2 3 4 5 6 BGBl. II 304/2001 DIN 38402-11 DIN 38402-12 DIN 38402-13 DIN 38402-15 DIN 38402-19 2001-08 Verordnung des Bundesministers für soziale Sicherheit und Generationen über die Qualität von Wasser
1 2 3 4 5 6 BGBl. II 304/2001 DIN 38402-11 DIN 38402-12 DIN 38402-13 DIN 38402-15 DIN 38402-19 2001-08 Verordnung des Bundesministers für soziale Sicherheit und Generationen über die Qualität von Wasser
Gewässerüberwachung im Bereich der Kaliindustrie durch das HLUG Stand
 Gewässerüberwachung im Bereich der Kaliindustrie durch das HLUG Stand 31.12.2008 Inhaltsverzeichnis Gewässerüberwachung im Bereich der Kaliindustrie durch das HLUG - Erläuterungen. Übersichtskarte HLUG-Messstellen
Gewässerüberwachung im Bereich der Kaliindustrie durch das HLUG Stand 31.12.2008 Inhaltsverzeichnis Gewässerüberwachung im Bereich der Kaliindustrie durch das HLUG - Erläuterungen. Übersichtskarte HLUG-Messstellen
Kapitel 2. März Stefanie Hellbach 1
 Kapitel 2 Auswirkungen der industriellen Nutzung von Wasser, Säuren, Basen und Salzen auf Menschen und Umwelt Behandlung von Materialien Schutzmaßnahmen für Mensch und Umwelt Stefanie Hellbach 1 Säuren
Kapitel 2 Auswirkungen der industriellen Nutzung von Wasser, Säuren, Basen und Salzen auf Menschen und Umwelt Behandlung von Materialien Schutzmaßnahmen für Mensch und Umwelt Stefanie Hellbach 1 Säuren
DÜNGE- LEHRE Abendschule für Gartenbau 2003/2004
 DÜNGE- LERE Abendschule für Gartenbau 2003/2004 ELEMENTE die für Pflanzen wichtig sind Na Wasserstoff in Form von Wasser Natrium K Kalium für die Wiederstandsfähigkeit, Wasserhaushalt Mg Magnesium Zentralatom
DÜNGE- LERE Abendschule für Gartenbau 2003/2004 ELEMENTE die für Pflanzen wichtig sind Na Wasserstoff in Form von Wasser Natrium K Kalium für die Wiederstandsfähigkeit, Wasserhaushalt Mg Magnesium Zentralatom
Inhalt 4. Wasserqualität
 Inhalt 4. Wasserqualität Wasserqualität Blatt 4/1 Wasserqualität und -kontrolle Blatt 4/2 Wasserhärte Blatt 4/3 ph-wert Blatt 4/4 4/1 Wasserqualität Welche Qualität hat unser Trinkwasser Trinkwasser ist
Inhalt 4. Wasserqualität Wasserqualität Blatt 4/1 Wasserqualität und -kontrolle Blatt 4/2 Wasserhärte Blatt 4/3 ph-wert Blatt 4/4 4/1 Wasserqualität Welche Qualität hat unser Trinkwasser Trinkwasser ist
der Jahre 1978 bis 2011 Betreiber: Landesamt für Umwelt, Wasserwirtschaft und Gewerbeaufsicht Rheinland-Pfalz
 der Jahre 1978 bis 2011 Betreiber: Landesamt für Umwelt, Wasserwirtschaft und Gewerbeaufsicht Rheinland-Pfalz Die Rheinwasser-Untersuchungsstation (RUSt) Mainz-Wiesbaden befindet sich unmittelbar neben
der Jahre 1978 bis 2011 Betreiber: Landesamt für Umwelt, Wasserwirtschaft und Gewerbeaufsicht Rheinland-Pfalz Die Rheinwasser-Untersuchungsstation (RUSt) Mainz-Wiesbaden befindet sich unmittelbar neben
Nitratsanierung WASSER GEOTHERMIE MARKIERVERSUCHE SCHADSTOFFE FILTERTECHNIK LEBENSMITTEL NACHWACHSENDE ROHSTOFFE ISOTOPE
 Nitratsanierung WASSER GEOTHERMIE MARKIERVERSUCHE SCHADSTOFFE FILTERTECHNIK LEBENSMITTEL NACHWACHSENDE ROHSTOFFE HYDROISOTOP GMBH Woelkestraße 9 85301 Schweitenkirchen Tel. +49 (0)8444 / 92890 Fax +49
Nitratsanierung WASSER GEOTHERMIE MARKIERVERSUCHE SCHADSTOFFE FILTERTECHNIK LEBENSMITTEL NACHWACHSENDE ROHSTOFFE HYDROISOTOP GMBH Woelkestraße 9 85301 Schweitenkirchen Tel. +49 (0)8444 / 92890 Fax +49
Bestimmung des ph-wertes des Bodens
 Bestimmung des ph-wertes des Bodens Durch den ph-wert erhältst du eine Angabe zum Säuregehalt. Er wird im Bereich zwischen 1 (sehr sauer!!!) und 14 (sehr basisch!) angegeben. Bei einem ph-wert von 7 spricht
Bestimmung des ph-wertes des Bodens Durch den ph-wert erhältst du eine Angabe zum Säuregehalt. Er wird im Bereich zwischen 1 (sehr sauer!!!) und 14 (sehr basisch!) angegeben. Bei einem ph-wert von 7 spricht
I feel goo o d! Wissenschaftliche Grundlagen für klares Wasser. in tropischen Süßwasseraquarien
 I feel goo o d! Wissenschaftliche Grundlagen für klares Wasser in tropischen Süßwasseraquarien Philips hat diesen Wasserreiniger für tropische Aquarien in enger Zusammenarbeit mit Aquarien- und Wasserexperten
I feel goo o d! Wissenschaftliche Grundlagen für klares Wasser in tropischen Süßwasseraquarien Philips hat diesen Wasserreiniger für tropische Aquarien in enger Zusammenarbeit mit Aquarien- und Wasserexperten
Stoffe oder Teilchen, die Protonen abgeben kånnen, werden als SÄuren bezeichnet (Protonendonatoren).
 5 10 15 20 25 30 35 40 45 O C 50 Chemie Technische BerufsmaturitÄt BMS AGS Basel Kapitel 6 SÄuren und Basen Baars, Kap. 12.1; 12.2; 13 Versuch 1 Ein Becherglas mit Thermometer enthält violette FarbstofflÅsung
5 10 15 20 25 30 35 40 45 O C 50 Chemie Technische BerufsmaturitÄt BMS AGS Basel Kapitel 6 SÄuren und Basen Baars, Kap. 12.1; 12.2; 13 Versuch 1 Ein Becherglas mit Thermometer enthält violette FarbstofflÅsung
Pflanz en und ihre ph-vorlieben
 Pflanz en und ihre ph-vorlieben Extrablatt 1 zu Arbeitsblatt 1, Aufgabe 2 Beispiele für Wildpflanzen als Zeigerpflanzen Stark sauer (ph unter 4,5) Sauer (ph 4,5 bis 5,2) Basisch/alkalisch Borstengras Schafschwingel
Pflanz en und ihre ph-vorlieben Extrablatt 1 zu Arbeitsblatt 1, Aufgabe 2 Beispiele für Wildpflanzen als Zeigerpflanzen Stark sauer (ph unter 4,5) Sauer (ph 4,5 bis 5,2) Basisch/alkalisch Borstengras Schafschwingel
Die Qualität der Fliessgewässer im Kanton Schaffhausen. Übersicht 2007/08
 Die Qualität der Fliessgewässer im Kanton Schaffhausen Übersicht 2007/08 Die Schaffhauser Fliessgewässer Gesetzlicher Auftrag Nitrat Das Qualitätsziel für Fliessgewässer beträgt max. 25 mg Nitrat pro Liter.
Die Qualität der Fliessgewässer im Kanton Schaffhausen Übersicht 2007/08 Die Schaffhauser Fliessgewässer Gesetzlicher Auftrag Nitrat Das Qualitätsziel für Fliessgewässer beträgt max. 25 mg Nitrat pro Liter.
Im Mülleimer einer Schulklasse findet die Reinigungskraft verschiedene Dinge: Leerer Joghurtbecher Gratiszeitung
 Mülltrennung Im Mülleimer einer Schulklasse findet die Reinigungskraft verschiedene Dinge: Farbige Glasflaschen Leerer Joghurtbecher Gratiszeitung Kaputte Glühbirne Plastiksackerl Farblose Gläser von Fruchtmischungen
Mülltrennung Im Mülleimer einer Schulklasse findet die Reinigungskraft verschiedene Dinge: Farbige Glasflaschen Leerer Joghurtbecher Gratiszeitung Kaputte Glühbirne Plastiksackerl Farblose Gläser von Fruchtmischungen
Umwelt. Umwelt. Kein Leben ohne Wasser 1/18. Kein Leben ohne Wasser 2/18
 Kein Leben ohne Wasser 1/18 Stell dir vor, du sitzt auf dem Mond und siehst mit dem Fernrohr auf die Erde. Was siehst du? Eine nahezu blaue Scheibe. Das kommt daher, dass weit mehr als die Hälfte der Oberfläche
Kein Leben ohne Wasser 1/18 Stell dir vor, du sitzt auf dem Mond und siehst mit dem Fernrohr auf die Erde. Was siehst du? Eine nahezu blaue Scheibe. Das kommt daher, dass weit mehr als die Hälfte der Oberfläche
Was verschmutzt die Luft?
 6A Lehrerkommentar MST Ziele Arbeitsauftrag Material Sozialform Zeit Die Kinder wissen, dass die Verbrennung von Energieträgern in vielen Fällen zu Luftverschmutzung führt. Sie kennen zudem einige Abgasverursacher
6A Lehrerkommentar MST Ziele Arbeitsauftrag Material Sozialform Zeit Die Kinder wissen, dass die Verbrennung von Energieträgern in vielen Fällen zu Luftverschmutzung führt. Sie kennen zudem einige Abgasverursacher
Chemie aquatischer Systeme. Herbstsemester 2013
 Chemie aquatischer Systeme Herbstsemester 2013 Ziele der Vorlesung Verständnis der chemischen Zusammensetzung der Gewässer aufgrund chemischer Prozesse Verknüpfung chemischer Prozesse mit biologischen
Chemie aquatischer Systeme Herbstsemester 2013 Ziele der Vorlesung Verständnis der chemischen Zusammensetzung der Gewässer aufgrund chemischer Prozesse Verknüpfung chemischer Prozesse mit biologischen
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Station 7: Klares Wasser, sonst nichts? Ein Experiment
 Station 7: Klares Wasser, sonst nichts? Ein Experiment Material: 1 Wasserteststreifen Vergleichstabelle auf der Verpackung 100 ml Wasserprobe (z. B. Teichwasser, Aquarienwasser in Becherglas Wasserprobe
Station 7: Klares Wasser, sonst nichts? Ein Experiment Material: 1 Wasserteststreifen Vergleichstabelle auf der Verpackung 100 ml Wasserprobe (z. B. Teichwasser, Aquarienwasser in Becherglas Wasserprobe
äßiger und chemischer Zustand Grundwasserkörper
 Mengenmäß äßiger und chemischer Zustand Grundwasserkörper rper Parameter für den mengenmäßigen und den chemischen Zustand Grundwasserstand (Quellschüttung) & Auswirkungen auf das Grundwasserdargebot
Mengenmäß äßiger und chemischer Zustand Grundwasserkörper rper Parameter für den mengenmäßigen und den chemischen Zustand Grundwasserstand (Quellschüttung) & Auswirkungen auf das Grundwasserdargebot
Analyse der Chemischen/Biologischen Wasseruntersuchungen der mittleren Aisch 2011
 Analyse der Chemischen/Biologischen Wasseruntersuchungen der mittleren Aisch 2011 Meßstellen: Pegel-Birkenfeld Flß/km60,7 ; oberhalb Wehr Pahres Flß/km49,1 ; Trafo vor Dachsbach Flß/km43,1 Anlagen: Diagramme
Analyse der Chemischen/Biologischen Wasseruntersuchungen der mittleren Aisch 2011 Meßstellen: Pegel-Birkenfeld Flß/km60,7 ; oberhalb Wehr Pahres Flß/km49,1 ; Trafo vor Dachsbach Flß/km43,1 Anlagen: Diagramme
SÄUREN, BASEN, ph-wert
 8. Einheit: SÄUREN, BASEN, ph-wert Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 23 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Säuren, Basen, ph-wert.. können Sie die Begriffe Säure und Base in
8. Einheit: SÄUREN, BASEN, ph-wert Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 23 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Säuren, Basen, ph-wert.. können Sie die Begriffe Säure und Base in
Was verstehen wir unter Säuren und Basen?
 Was verstehen wir unter Säuren und Basen? Säuren: Unter Säuren verstehen wir alle organischen und anorganischen Verbindungen, die in Lösungen Wasserstoffionen H + abgeben. Sie werden auch Protonen Donatoren
Was verstehen wir unter Säuren und Basen? Säuren: Unter Säuren verstehen wir alle organischen und anorganischen Verbindungen, die in Lösungen Wasserstoffionen H + abgeben. Sie werden auch Protonen Donatoren
Inhaltsverzeichnis. Vorwort Zur Gestaltung des Buches
 Hans Rudolf Christen Struktur Stoff Reaktion Allgemeine und anorganische Chemie Sekundarstufe I 5401 Diesterweg Salle Frankfurt am Main Berlin München Verlag Sauerländer Aarau Vorwort Zur Gestaltung des
Hans Rudolf Christen Struktur Stoff Reaktion Allgemeine und anorganische Chemie Sekundarstufe I 5401 Diesterweg Salle Frankfurt am Main Berlin München Verlag Sauerländer Aarau Vorwort Zur Gestaltung des
Biologie Referat für Felix
 Biologie Referat für Felix Sehr geehrter Herr Professor, liebe Mitschüler. Wir möchten euch mit unserem heutigen Referat das Wasser ein bißchen näher vorstellen. Wir haben unser Referat in 3 Abschnitte
Biologie Referat für Felix Sehr geehrter Herr Professor, liebe Mitschüler. Wir möchten euch mit unserem heutigen Referat das Wasser ein bißchen näher vorstellen. Wir haben unser Referat in 3 Abschnitte
Biologische und chemische Vorgänge in stehenden Gewässern. Eine zusammenfassende Betrachtung der Zusammenhänge in einem Gewässer
 Eine zusammenfassende Betrachtung der Zusammenhänge in einem Gewässer Der ph-wert Das Karbonathärte-Puffersystem Algen verstehen und bekämpfen Phosphatfrachten Der Teich Symbiose aller Lebewesen In einem
Eine zusammenfassende Betrachtung der Zusammenhänge in einem Gewässer Der ph-wert Das Karbonathärte-Puffersystem Algen verstehen und bekämpfen Phosphatfrachten Der Teich Symbiose aller Lebewesen In einem
Kreislauf 15/24 Winde verblasen die Wolken auch auf andere Teile der Erde. Wenn es an der Erdoberfläche windstill ist, weht in der Höhe trotzdem Wind.
 Kreislauf 13/24 Manche Quellen sind sehr klein: Es rinnt nur ein schmales Rinnsal daraus hervor. Aus manchen Quellen aber sprudelt ein richtiger Bach. Immer wieder fließen kleinere Bäche in den Bach, er
Kreislauf 13/24 Manche Quellen sind sehr klein: Es rinnt nur ein schmales Rinnsal daraus hervor. Aus manchen Quellen aber sprudelt ein richtiger Bach. Immer wieder fließen kleinere Bäche in den Bach, er
die WASSER WERKSTATT
 die WASSER WERKSTATT Inhalt: Die Mehrheit der Organismen auf unserer Erde lebt in Gewässern. Und alle egal, ob Mensch, Tier oder Pflanze sind abhängig vom Wasser. Die meisten Lebewesen bestehen sogar zu
die WASSER WERKSTATT Inhalt: Die Mehrheit der Organismen auf unserer Erde lebt in Gewässern. Und alle egal, ob Mensch, Tier oder Pflanze sind abhängig vom Wasser. Die meisten Lebewesen bestehen sogar zu
2 NIEDERSCHLAGSQUALITÄT
 2 NIEDERSCHLAGSQUALITÄT Regen und Schnee sind durch Schadstoffe und Nährstoffe, zum Beispiel durch Schwermetalle und Stickstoff aus der Luft belastet. Diese Stoffe gelangen mit dem Niederschlagswasser
2 NIEDERSCHLAGSQUALITÄT Regen und Schnee sind durch Schadstoffe und Nährstoffe, zum Beispiel durch Schwermetalle und Stickstoff aus der Luft belastet. Diese Stoffe gelangen mit dem Niederschlagswasser
Die chemische Zusammensetzung natiirlicher Gewasser
 Inhaltsverzeichnis Vorwort XI KAPITEL 1 KAPITEL 2 Die chemische Zusammensetzung natiirlicher Gewasser 1.1 Einleitung 1.2 Verwitterungsprozesse 1.3 Wechselwirkungen zwischen Organismen und Wasser 1.4 Das
Inhaltsverzeichnis Vorwort XI KAPITEL 1 KAPITEL 2 Die chemische Zusammensetzung natiirlicher Gewasser 1.1 Einleitung 1.2 Verwitterungsprozesse 1.3 Wechselwirkungen zwischen Organismen und Wasser 1.4 Das
S Eutrophierung >> Watt für Fortgeschrittene Naturschule Wattenmeer
 Eutrophierung des Wattenmeeres EUTROPHIERUNG ist die Anreicherung von Nährstoffen in einem Gewässer, die meist von menschlichen Aktivitäten verursacht wird. Das Wort eutroph stammt aus dem Griechischen
Eutrophierung des Wattenmeeres EUTROPHIERUNG ist die Anreicherung von Nährstoffen in einem Gewässer, die meist von menschlichen Aktivitäten verursacht wird. Das Wort eutroph stammt aus dem Griechischen
Eigenschaften von H 2 S
 Eigenschaften von H 2 S sehr giftiges, brennbares, unangenehm faulig riechendes Gas Smp. -86 C, Sdp. -60,2 C mäßig wasserlöslich, gesättigte Lösung hat c = 0,1 mol/l schwache, zweiprotonige Säure H 2 S
Eigenschaften von H 2 S sehr giftiges, brennbares, unangenehm faulig riechendes Gas Smp. -86 C, Sdp. -60,2 C mäßig wasserlöslich, gesättigte Lösung hat c = 0,1 mol/l schwache, zweiprotonige Säure H 2 S
Boden- und Gewässerverschmutzung Seite 1 von 7. Ihr könnt den Aufbau un die Funktionsweise einer Pflanzenkläranalge beschreiben...
 Boden- und Gewässerverschmutzung Seite 1 von 7 SPF BCH. 3. Kanti Lernblatt zur Prüfung am 15.09.2011 Autor: Version: Veröffentlichung: Linus Metzler 1.0b 11.09.2011 BODEN- UND ZUNG GEWÄSSERVERSCHMUT- INHALTSVERZEICHNIS
Boden- und Gewässerverschmutzung Seite 1 von 7 SPF BCH. 3. Kanti Lernblatt zur Prüfung am 15.09.2011 Autor: Version: Veröffentlichung: Linus Metzler 1.0b 11.09.2011 BODEN- UND ZUNG GEWÄSSERVERSCHMUT- INHALTSVERZEICHNIS
Anlage 3. Beispiel zur Beschreibung der hydrochemischen Verhältnisse. bearb. nach C&E Consulting und Engineering GmbH (2006)
 Anlage 3 Beispiel zur Beschreibung der hydrochemischen Verhältnisse bearb. nach C&E Consulting und Engineering GmbH (6) Allgemeine hydrochemische Charakterisierung des Rohwassers Für den Sammelbrunnenzulauf
Anlage 3 Beispiel zur Beschreibung der hydrochemischen Verhältnisse bearb. nach C&E Consulting und Engineering GmbH (6) Allgemeine hydrochemische Charakterisierung des Rohwassers Für den Sammelbrunnenzulauf
fest, nicht gelöst: Na + Cl -
 Salzsäure + Natriumlauge Natriumchlorid + Wasser / exotherm HCl + NaOH NaCl + H 2 O / exotherm H + (aq) + Cl (aq) + Na + (aq) + OH (aq) Na + (aq) + Cl (aq) + H 2 O / exotherm fest, nicht gelöst: Na + Cl
Salzsäure + Natriumlauge Natriumchlorid + Wasser / exotherm HCl + NaOH NaCl + H 2 O / exotherm H + (aq) + Cl (aq) + Na + (aq) + OH (aq) Na + (aq) + Cl (aq) + H 2 O / exotherm fest, nicht gelöst: Na + Cl
Geplanter Verlauf. Einführung Beurteilung nach biotischen Faktoren Pause Beurteilung nach abiotischen Faktoren Auswertung und Diskussion
 Ökosystem See Geplanter Verlauf Einführung Beurteilung nach biotischen Faktoren Pause Beurteilung nach abiotischen Faktoren Auswertung und Diskussion Schulbiologiezentrum Hannover - Ökologie stehende Gewässer
Ökosystem See Geplanter Verlauf Einführung Beurteilung nach biotischen Faktoren Pause Beurteilung nach abiotischen Faktoren Auswertung und Diskussion Schulbiologiezentrum Hannover - Ökologie stehende Gewässer
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau
 Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Der Einfluss des Wassers auf die Qualität der Kühlschmierstoff-Emulsion
 Der Einfluss des Wassers auf die Qualität der KühlschmierstoffEmulsion Markus Kühni, Leiter Kundendienst Blaser Swisslube AG Winterseistrasse 3415 HasleRüegsau Tel: 034 460 01 01 email: contact@blaser.com
Der Einfluss des Wassers auf die Qualität der KühlschmierstoffEmulsion Markus Kühni, Leiter Kundendienst Blaser Swisslube AG Winterseistrasse 3415 HasleRüegsau Tel: 034 460 01 01 email: contact@blaser.com
Nährstoffe in Fließgewässern ein Problem?
 3. Workshop Gewässerkunde in Lüneburg am 18. September 2018 Nährstoffe in Fließgewässern ein Problem? Stephanie Gudat / Oliver Melzer NLWKN Hannover Hildesheim Geschäftsbereich III Gewässerbewirtschaftung/
3. Workshop Gewässerkunde in Lüneburg am 18. September 2018 Nährstoffe in Fließgewässern ein Problem? Stephanie Gudat / Oliver Melzer NLWKN Hannover Hildesheim Geschäftsbereich III Gewässerbewirtschaftung/
Regenwasseranalyse. Sommersemester Studienprojekt. Verfasst durch: Markus Siemssen. Lara Kreft. Betreuender Professor: Prof. Dr.
 Regenwasseranalyse Sommersemester 2014 Studienprojekt Verfasst durch: Markus Siemssen Lara Kreft Betreuender Professor: Prof. Dr. Elsholz Hochschule für Angewandte Wissenschaften Hamburg Campus Bergedorf
Regenwasseranalyse Sommersemester 2014 Studienprojekt Verfasst durch: Markus Siemssen Lara Kreft Betreuender Professor: Prof. Dr. Elsholz Hochschule für Angewandte Wissenschaften Hamburg Campus Bergedorf
Mikrobiologie der Gewässer
 Mikrobiologie der Gewässer Gerhard Rheinheimer Fünfte, überarbeitete Auflage Mit 110 Abbildungen Gustav Fischer Verlag Jena Stuttgart 1991 Inhaltsverzeichnis Vorworte 5 1. Einleitung» 11 2. Die Gewässer
Mikrobiologie der Gewässer Gerhard Rheinheimer Fünfte, überarbeitete Auflage Mit 110 Abbildungen Gustav Fischer Verlag Jena Stuttgart 1991 Inhaltsverzeichnis Vorworte 5 1. Einleitung» 11 2. Die Gewässer
Anhang Zustand Solothurner Gewässer_Inhalt_def.indd :15
 Anhang Beurteilungskriterien für Oberflächengewässer und Grundwasser Beurteilungskriterien für Oberflächengewässer Biochemischer Sauerstoffbedarf (BSB 5 2 bis 4 mg/l O 2 Gelöster organischer Kohlenstoff
Anhang Beurteilungskriterien für Oberflächengewässer und Grundwasser Beurteilungskriterien für Oberflächengewässer Biochemischer Sauerstoffbedarf (BSB 5 2 bis 4 mg/l O 2 Gelöster organischer Kohlenstoff
BlueAir. Unser Beitrag zu sauberer Luft.
 BlueAir. Unser Beitrag zu sauberer Luft. Die Kraft des Lebens. Licht ist der Ursprung allen Lebens: Es gibt Wärme, Kraft und Energie. Tag und Nacht, Sommer und Winter die Anwesenheit und Intensität des
BlueAir. Unser Beitrag zu sauberer Luft. Die Kraft des Lebens. Licht ist der Ursprung allen Lebens: Es gibt Wärme, Kraft und Energie. Tag und Nacht, Sommer und Winter die Anwesenheit und Intensität des
Gründe für Abwasserbelastung und Möglichkeiten zur Verbesserung der Abwasserqualität
 Nachhaltigkeit in der gewerblichen Wäscherei Modul 1 Wasseranwendung Kapitel 4 Gründe für Abwasserbelastung und Möglichkeiten zur Verbesserung der Abwasserqualität Modul 1 Wasseranwendung Kapitel 4 Gründe
Nachhaltigkeit in der gewerblichen Wäscherei Modul 1 Wasseranwendung Kapitel 4 Gründe für Abwasserbelastung und Möglichkeiten zur Verbesserung der Abwasserqualität Modul 1 Wasseranwendung Kapitel 4 Gründe
Trinkwasserverordnung in der Fassung der ersten Änderungsverordnung vom 3. Mai 2011 (TrinkwV 2011)
 Anlage 1 (zu 5 Absatz 2 und 3) Mikrobiologische Parameter Allgemeine Anforderungen an Trinkwasser Lfd. Nr. Parameter Grenzwert 1 Escherichia coli (E. coli) 0/100 ml 2 Enterokokken 0/100 ml Anforderungen
Anlage 1 (zu 5 Absatz 2 und 3) Mikrobiologische Parameter Allgemeine Anforderungen an Trinkwasser Lfd. Nr. Parameter Grenzwert 1 Escherichia coli (E. coli) 0/100 ml 2 Enterokokken 0/100 ml Anforderungen
Trinkwasseranalyse Versorgungsgebiet Kernbereich Friedrichsdorf
 Seite 1 von 3 Stadtwerke Friedrichsdorf Färberstraße 13-15 Trinkwasseranalyse Versorgungsgebiet Kernbereich Friedrichsdorf Ergebnisse der Trinkwasseranalysen 2014 und 2015 vom Institut Fresenius, Taunusstein
Seite 1 von 3 Stadtwerke Friedrichsdorf Färberstraße 13-15 Trinkwasseranalyse Versorgungsgebiet Kernbereich Friedrichsdorf Ergebnisse der Trinkwasseranalysen 2014 und 2015 vom Institut Fresenius, Taunusstein
1.5 Säuren und Basen und der ph-wert
 Seite 14 1.5 Säuren und Basen und der ph-wert 1.5.1 Säuren Geschichtlich bedingte Definition: Eine Säure ist ein Stoff, dessen wässrige Lösung sauer schmeckt oder ätzend wirkt, bzw. andere Stoffe angreift.
Seite 14 1.5 Säuren und Basen und der ph-wert 1.5.1 Säuren Geschichtlich bedingte Definition: Eine Säure ist ein Stoff, dessen wässrige Lösung sauer schmeckt oder ätzend wirkt, bzw. andere Stoffe angreift.
Anlage zur Akkreditierungsurkunde D-PL nach DIN EN ISO/IEC 17025:2018
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-19140-01-00 nach DIN EN ISO/IEC 17025:2018 Urkundeninhaber: bioplan Institut für angewandte Biologie und Landschaftsplanung GmbH
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-19140-01-00 nach DIN EN ISO/IEC 17025:2018 Urkundeninhaber: bioplan Institut für angewandte Biologie und Landschaftsplanung GmbH
Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch zwischen Flß. km 60,7 und Flß. km 43,1 im Jahr 2014
 Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch zwischen Flß. km 60,7 und Flß. km 43,1 im Jahr 2014 Meßstellen: Brücke Birkenfeld Flß.km 60,7 und Trafo oberhalb Dachsbach Anlagen: Diagramme
Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch zwischen Flß. km 60,7 und Flß. km 43,1 im Jahr 2014 Meßstellen: Brücke Birkenfeld Flß.km 60,7 und Trafo oberhalb Dachsbach Anlagen: Diagramme
präsentiert Ihnen die Oberflächen-Technologie des 21. Jahrhunderts TITAN Shield Photokatalytisches Titandioxid TiO2
 Um elt Innovationen m präsentiert Ihnen die Oberflächen-Technologie des 21. Jahrhunderts Photokatalytisches Titandioxid TiO2 Mit veredelte Oberflächen reinigen sich selbst. Sie sind antibakteriell, antifungizid
Um elt Innovationen m präsentiert Ihnen die Oberflächen-Technologie des 21. Jahrhunderts Photokatalytisches Titandioxid TiO2 Mit veredelte Oberflächen reinigen sich selbst. Sie sind antibakteriell, antifungizid
STADTWERKE FRIEDRICHSDORF Eigenbetrieb der Stadt Friedrichsdorf
 STADTWERKE FRIEDRICHSDORF Eigenbetrieb der Stadt Friedrichsdorf Postanschrift: Hugenottenstraße 55 61381 Friedrichsdorf Telefonzenzentrale: 0 61 72 / 731-0 Postfach 13 40 61364 Friedrichsdorf Telefax:
STADTWERKE FRIEDRICHSDORF Eigenbetrieb der Stadt Friedrichsdorf Postanschrift: Hugenottenstraße 55 61381 Friedrichsdorf Telefonzenzentrale: 0 61 72 / 731-0 Postfach 13 40 61364 Friedrichsdorf Telefax:
Der ph-wert. Warum ist der so wichtig?
 Der ph-wert Warum ist der so wichtig? Den Hinweis dafür, daß Ihr Schwimmbadwasser und alles drumherum. nur dann in Ordnung sein kann wenn der ph-wert stimmt, den bekommen Sie täglich aus Broschüren, Büchern
Der ph-wert Warum ist der so wichtig? Den Hinweis dafür, daß Ihr Schwimmbadwasser und alles drumherum. nur dann in Ordnung sein kann wenn der ph-wert stimmt, den bekommen Sie täglich aus Broschüren, Büchern
Interpretation der chemischen und physikalischen Untersuchungen
 Interpretation der chemischen und physikalischen Untersuchungen in Fliessgewässern Für die Interpretation der chemischen (ph, Nitrat, Sauerstoff, Alkalinität), physikalischen (Temperatur, Transparenz,
Interpretation der chemischen und physikalischen Untersuchungen in Fliessgewässern Für die Interpretation der chemischen (ph, Nitrat, Sauerstoff, Alkalinität), physikalischen (Temperatur, Transparenz,
1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss
 1 Uebungen zur Prüfungsvorbereitung 4.12.14 1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss Die folgenden Tiefenprofile von gelöstem Mangan, Eisen und Sulfid (S 2- ) sowie die
1 Uebungen zur Prüfungsvorbereitung 4.12.14 1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss Die folgenden Tiefenprofile von gelöstem Mangan, Eisen und Sulfid (S 2- ) sowie die
Versorgungsgebiet Erbach-Schönnen (mit Erbach-Ebersberg)
 Trinkwasser Versorgungsgebiet ErbachSchönnen (mit ErbachEbersberg) Technisch relevante Analysenwerte nach DIN 50930 Teil 6 Einheit Aussehen, Trübung Farbe Sensorische Prüfung Temperatur C 6,5 24,7 Calcitlösekapazität
Trinkwasser Versorgungsgebiet ErbachSchönnen (mit ErbachEbersberg) Technisch relevante Analysenwerte nach DIN 50930 Teil 6 Einheit Aussehen, Trübung Farbe Sensorische Prüfung Temperatur C 6,5 24,7 Calcitlösekapazität
WIE GUT IST DAS WASSER VON MAIN, NIDDA UND URSELBACH?
 WIE GUT IST DAS WASSER VON MAIN, NIDDA UND URSELBACH? GK 13 Chemie & Dirk Schüpke Wenn man diese Frage beantworten will, dann muss man früh aufstehen und um 7 Uhr in Kelsterbach die erste Wasserprobe nehmen.
WIE GUT IST DAS WASSER VON MAIN, NIDDA UND URSELBACH? GK 13 Chemie & Dirk Schüpke Wenn man diese Frage beantworten will, dann muss man früh aufstehen und um 7 Uhr in Kelsterbach die erste Wasserprobe nehmen.
Bodenfruchtbarkeit potentielle Säure und Melioration
 Rochuspark I Erdbergstraße 10/33 I 1020 Wien T (+43 1) 236 10 30 33 I M (+43 0) 676 364 10 30 E office@bodenoekologie.com I www.bodenoekologie.com Bodenfruchtbarkeit potentielle Säure und Melioration Univ.
Rochuspark I Erdbergstraße 10/33 I 1020 Wien T (+43 1) 236 10 30 33 I M (+43 0) 676 364 10 30 E office@bodenoekologie.com I www.bodenoekologie.com Bodenfruchtbarkeit potentielle Säure und Melioration Univ.
Zusammenfassung: Säure Base Konzept
 Zusammenfassung: Säure Base Konzept 1. Grundlegende Eigenschaften von Säuren und Laugen Säure und Laugen ätzen sie werden durch Indikatoren für uns erkenntlich gemacht. Oft verwendet man Universalindikator.
Zusammenfassung: Säure Base Konzept 1. Grundlegende Eigenschaften von Säuren und Laugen Säure und Laugen ätzen sie werden durch Indikatoren für uns erkenntlich gemacht. Oft verwendet man Universalindikator.
Trinkwasser Versorgungsgebiet:
 Trinkwasser Versorgungsgebiet: ENTEGA AG Telefon: 065 708022 Telefax: 065 70409 in Zusammenarbeit mit Hessenwasser GmbH & Co. KG Darmstadt (alle Ortsteile), Riedstadt (alle Ortsteile), Weiterstadt (alle
Trinkwasser Versorgungsgebiet: ENTEGA AG Telefon: 065 708022 Telefax: 065 70409 in Zusammenarbeit mit Hessenwasser GmbH & Co. KG Darmstadt (alle Ortsteile), Riedstadt (alle Ortsteile), Weiterstadt (alle
Wie sauber ist unser Wasser?
 Wie sauber ist unser Wasser? Untersuchung von Oberflächengewässern und Grundwässern auf ausgewählte Schadstoffe aus Industrie, Haushalt und Landwirtschaft. Blick in die 60er und 70er-Jahre Filteranlage:
Wie sauber ist unser Wasser? Untersuchung von Oberflächengewässern und Grundwässern auf ausgewählte Schadstoffe aus Industrie, Haushalt und Landwirtschaft. Blick in die 60er und 70er-Jahre Filteranlage:
Schäden durch chemisch lösenden Angriff
 Schäden durch chemisch lösenden Angriff Einleitung Ein chemisch lösender Angriff kann durch die Einwirkung von Säuren, austauschfähigen Salzen, weichem Wasser oder starken Basen stattfinden (Tab. 8.6.1).
Schäden durch chemisch lösenden Angriff Einleitung Ein chemisch lösender Angriff kann durch die Einwirkung von Säuren, austauschfähigen Salzen, weichem Wasser oder starken Basen stattfinden (Tab. 8.6.1).
Vital leben mit vitalem Wasser.
 Vital leben mit vitalem Wasser www.trinkwasser.global Die Oberfläche der Erde besteht zu 70 % aus Wasser Das Wasser der Erde 97,2 % Salzwasser 0,01 % Atmosphäre 2,14 % Eis 0,65 % Süßwasser Nur ein Drittel
Vital leben mit vitalem Wasser www.trinkwasser.global Die Oberfläche der Erde besteht zu 70 % aus Wasser Das Wasser der Erde 97,2 % Salzwasser 0,01 % Atmosphäre 2,14 % Eis 0,65 % Süßwasser Nur ein Drittel
Teste dein Wasser-Wissen!
 Teste dein Wasser-Wissen! Das Wasser auf der Erde befindet sich in einem unendlichen Kreislauf. Überall dort, wo die Sonne das Land oder ein Gewässer oder Meer erwärmt, steigt unsichtbarer Wasserdampf
Teste dein Wasser-Wissen! Das Wasser auf der Erde befindet sich in einem unendlichen Kreislauf. Überall dort, wo die Sonne das Land oder ein Gewässer oder Meer erwärmt, steigt unsichtbarer Wasserdampf
Neutralisation Die Wirkung von Antazida im Körper
 Neutralisation Die Wirkung von Antazida im Körper Stand: 01.08.2018 Jahrgangsstufen 11 Fach/Fächer Chemie Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material 45 Minuten Antazida, demineralisiertes
Neutralisation Die Wirkung von Antazida im Körper Stand: 01.08.2018 Jahrgangsstufen 11 Fach/Fächer Chemie Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material 45 Minuten Antazida, demineralisiertes
Was sagt mein Wasserbefund aus?
 Was sagt mein Wasserbefund aus? Themen Formale Anforderungen Dimensionen Parameter und deren Bedeutung Ergebnisse Volluntersuchungen 2008/2009 Formale Anforderungen Anschrift Auftraggeber Datum Ausfertigung
Was sagt mein Wasserbefund aus? Themen Formale Anforderungen Dimensionen Parameter und deren Bedeutung Ergebnisse Volluntersuchungen 2008/2009 Formale Anforderungen Anschrift Auftraggeber Datum Ausfertigung
NO x eine Bestandsaufnahme
 NO x eine Bestandsaufnahme Prof. Dr. Rainer Friedrich Institut für Energiewirtschaft und Rationelle Energieanwendung Abt. Technikfolgenabschätzung und Umwelt Universität Stuttgart, Wien NO x die wichtigsten
NO x eine Bestandsaufnahme Prof. Dr. Rainer Friedrich Institut für Energiewirtschaft und Rationelle Energieanwendung Abt. Technikfolgenabschätzung und Umwelt Universität Stuttgart, Wien NO x die wichtigsten
Baden in der Aare. Qualitätsklasse C Qualitätsklasse D. Qualitätsklasse B. Spielen am Wasser (Foto: creato)
 Erholung und Freizeit Baden in der Aare Das kantonale Labor des Gesundheitsamtes überprüft während der Badesaison an ausgewählten Stellen die hygienische Qualität des Aarewassers und des Wassers des Burgäschisees.
Erholung und Freizeit Baden in der Aare Das kantonale Labor des Gesundheitsamtes überprüft während der Badesaison an ausgewählten Stellen die hygienische Qualität des Aarewassers und des Wassers des Burgäschisees.
Aktuelles zur Kalkdüngung. Kaspar Grünig, Beratung Pflanzenbau, Inforama
 Aktuelles zur Kalkdüngung Kaspar Grünig, Beratung Pflanzenbau, Inforama Inhalt Einige Kalkformen und ihre Gehalte Bedarf und Berechnung Kalkverluste Kalkwirkung Spezialfall Branntkalk Calziumschwefel Merkblatt
Aktuelles zur Kalkdüngung Kaspar Grünig, Beratung Pflanzenbau, Inforama Inhalt Einige Kalkformen und ihre Gehalte Bedarf und Berechnung Kalkverluste Kalkwirkung Spezialfall Branntkalk Calziumschwefel Merkblatt
Lösung: Gruppenarbeit Thema A
 Lösung: Gruppenarbeit Thema A Landwirtschaft als Quelle der Wasserverschmutzung Um Nahrungsmittel zu produzieren, bewirtschaften die Landwirte den Boden, verwenden auf Äckern und Wiesen Dünger und Pflanzenschutzmittel,
Lösung: Gruppenarbeit Thema A Landwirtschaft als Quelle der Wasserverschmutzung Um Nahrungsmittel zu produzieren, bewirtschaften die Landwirte den Boden, verwenden auf Äckern und Wiesen Dünger und Pflanzenschutzmittel,
Prüfbericht über Wasseruntersuchungen gemäß TrinkwV 2001
 Zweckverband Wassererversorgung und Abwasserbeseitigung Grimmen Grellenberger Straße 6 1857 Grimmen Tel. ( 38326 ) 63- / Fax ( 38326 ) 63-12 Zweckverband Wasserversorgung und Abwasserbeseitigung Grimmen
Zweckverband Wassererversorgung und Abwasserbeseitigung Grimmen Grellenberger Straße 6 1857 Grimmen Tel. ( 38326 ) 63- / Fax ( 38326 ) 63-12 Zweckverband Wasserversorgung und Abwasserbeseitigung Grimmen
Bodenuntersuchungen im Koblenzer Stadtwald. H.Groenert
 Bodenuntersuchungen im Koblenzer Stadtwald H.Groenert Untersuchungen der Bodentypen (1) A-C-Boden (Ranker) im Steinbruch an der Talflanke Bimsschicht vom Ausbruch des Laacher See Vulkans (2. Julihälfte
Bodenuntersuchungen im Koblenzer Stadtwald H.Groenert Untersuchungen der Bodentypen (1) A-C-Boden (Ranker) im Steinbruch an der Talflanke Bimsschicht vom Ausbruch des Laacher See Vulkans (2. Julihälfte
Nitrifikation Nitritoxidation. Von Patrycja Kosnik und Nico Tennigkeit
 Nitrifikation Nitritoxidation Von Patrycja Kosnik und Nico Tennigkeit Als Nitrifikation bezeichnet man die Oxidation von Ammoniak über Nitrit zu Nitrat Die Oxidation ist in zwei Schritte unterteilt, wobei
Nitrifikation Nitritoxidation Von Patrycja Kosnik und Nico Tennigkeit Als Nitrifikation bezeichnet man die Oxidation von Ammoniak über Nitrit zu Nitrat Die Oxidation ist in zwei Schritte unterteilt, wobei
3. Übung Grundlagen der Hauptgruppenchemie
 Allgemeine und Anorganische Chemie 3. Übung Grundlagen der Hauptgruppenchemie Aufgabe 1: Beschreiben Sie die Herstellung von Schwefelsäure nach dem Kontaktverfahren mit Hilfe von chemischen Gleichungen
Allgemeine und Anorganische Chemie 3. Übung Grundlagen der Hauptgruppenchemie Aufgabe 1: Beschreiben Sie die Herstellung von Schwefelsäure nach dem Kontaktverfahren mit Hilfe von chemischen Gleichungen
Biomasse/Biomüll. Biogas/Biogasanlage. Blockheizkraftwerk. Müllheizkraftwerk. Pelletheizung
 Biomasse/Biomüll Biogas/Biogasanlage Blockheizkraftwerk Müllheizkraftwerk Pelletheizung Christoph Hennemann 10 a 09.03.2010 Biomasse: Als Biomasse wird die gesamte organische Substanz bezeichnet. Basis
Biomasse/Biomüll Biogas/Biogasanlage Blockheizkraftwerk Müllheizkraftwerk Pelletheizung Christoph Hennemann 10 a 09.03.2010 Biomasse: Als Biomasse wird die gesamte organische Substanz bezeichnet. Basis
Der Magistrat der Schöfferstadt Gernsheim Postfach Gernsheim Telefon:
 Trinkwasser Technisch relevante Analysenwerte nach DIN 50930 Teil 6 Einheit Aussehen, Trübung Farbe Sensorische Prüfung Temperatur C 8,9 9,5 Calcitlösekapazität mg/l CaCO 3 32,0 29,0 phwert 7,3 7,4 phwert
Trinkwasser Technisch relevante Analysenwerte nach DIN 50930 Teil 6 Einheit Aussehen, Trübung Farbe Sensorische Prüfung Temperatur C 8,9 9,5 Calcitlösekapazität mg/l CaCO 3 32,0 29,0 phwert 7,3 7,4 phwert
Name: Punktzahl: von 57 Note:
 Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Pfäffikersee Fassung Nr.3
 Pfäffikersee - - Fassung Nr. Interpretation der AWEL-Daten des Pfäffikersees Heinrich Bührer Temperatur: Die Daten haben in probater Manier eine Lücke bis Mitte März. Die wirklichen Temperaturen lagen
Pfäffikersee - - Fassung Nr. Interpretation der AWEL-Daten des Pfäffikersees Heinrich Bührer Temperatur: Die Daten haben in probater Manier eine Lücke bis Mitte März. Die wirklichen Temperaturen lagen
Themengebiet: 1 HA + H 2 O A - + H 3 O + H 3 O + : Oxonium- oder Hydroxoniumion. Themengebiet: 2 B + H 2 O BH + + OH - OH - : Hydroxidion
 1 1 Säuren sind Protonendonatoren, d.h. Stoffe, die an einen Reaktionspartner ein oder mehrere Protonen abgeben können; Säuredefinition nach Brönsted Im Falle von Wasser: HA + H 2 O A - + H 3 O + H 3 O
1 1 Säuren sind Protonendonatoren, d.h. Stoffe, die an einen Reaktionspartner ein oder mehrere Protonen abgeben können; Säuredefinition nach Brönsted Im Falle von Wasser: HA + H 2 O A - + H 3 O + H 3 O
A B - AB K D. Elektrolytische Dissoziation. AB(aq) Stoffe, die in Lösung Ionen bilden, heißen Elektrolyte. Es gilt das Massenwirkungsgesetz
 Elektrolytische Dissoziation AB(aq) A + (aq) + B - (aq) Stoffe, die in Lösung Ionen bilden, heißen Elektrolyte. Es gilt das Massenwirkungsgesetz K D A B - AB K D : Dissoziationskonstante Dissoziation ist
Elektrolytische Dissoziation AB(aq) A + (aq) + B - (aq) Stoffe, die in Lösung Ionen bilden, heißen Elektrolyte. Es gilt das Massenwirkungsgesetz K D A B - AB K D : Dissoziationskonstante Dissoziation ist
