Handbuch der Präanalytik und Primärprobengewinnung. Inhalt. Pränatal-Medizin München
|
|
|
- Sigrid Kaufer
- vor 5 Jahren
- Abrufe
Transkript
1 Handbuch der und Primärprobengewinnung Inhalt 1. Anschrift und Kontakte... 2 Laboratorien Allgemeine Hinweise zur Probengewinnung Fruchtwasserpunktion (Amniozentese) Chorionzottenbiopsie / Plazentazentese Entnahme von Abortmaterial Entnahme von Fetalblut Entnahme von peripherem Venenblut Abstrich von Mundschleimhaut Probengefäße Diagnostik / Untersuchungsmaterial / Lagerung Probenbeschriftung und Auftragserteilung Probentransport / Probenversand Kostenlose Probenabholung durch unseren Fahrdienst Stadtgebiet München Kostenlose Probenabholung durch unseren Fahrdienst außerhalb von München Probenversand auf dem Postweg Materialarchivierung Befundmitteilung Unterauftrag / Fremdanalysen Leistungsverzeichnis: Dokumente Qualitätsmanagement (QM) Anlagen Handbuch der und Primärprobengewinnung Seite 1 von 22
2 Handbuch der und Primärprobengewinnung 1. Anschrift und Kontakte Pränatal-Medizin München Dr. med. Karl-Philipp Gloning Dr. med. Sabine Minderer Priv.-Doz. Dr. med. Thomas Schramm Dr. med. Cornelia Daumer-Haas Lachnerstr München Internet: Sekretariat: Tel.: Fax: Probenannahme: Montag Freitag 8: Uhr Sprechstunden: Montag Freitag 8: Uhr nach Vereinbarung Laboratorien Zytogenetisches Labor Lachnerstraße München Telefon Techn. Leitung: Andrea Brans, MTLA, und Eva Kahles, MTLA Labor für molekulare Genetik Lachnerstraße München Telefon Techn. Leitung: Marion Huber, M.Sc. Handbuch der und Primärprobengewinnung Seite 2 von 22
3 Handbuch der und Primärprobengewinnung Laborservice 1. Probenabholung und Organisation von Probentransport über die angegebenen Kontakte 2. Befundabfrage Diagnostik FISH 21, 18, 13, X, Y am Tag nach der Punktion ab 14 Uhr Zotten-Direktpräparation am Tag nach der Punktion 17 bis 18 Uhr Molekulargenetische Befunde Montag bis Freitag von 16 bis 17 Uhr Labor Zytogenetisches Labor Telefon Labor für molekulare Genetik Telefon Handbuch der und Primärprobengewinnung Seite 3 von 22
4 Handbuch der und Primärprobengewinnung 2. Allgemeine Hinweise zur Die Gewinnung und Vorbereitung der Proben für die Laboruntersuchungen erfordert in allen Abläufen eine systematische Qualitätssicherung. Der Gesamtprozess der umfasst die Vorbereitung des Patienten für die Probengewinnung, die Probenentnahme, Kennzeichnung der Probe, den Probentransport ins Labor, die Probenannahme und die Festlegung der Untersuchungsverfahren mit Indikationsstellung. Für eine qualitativ hochwertige Labordiagnostik ist der korrekte Ablauf der präanalytischen Phase durch den für die Probenahme verantwortlichen Arzt und unsere Laboratorien von größter Bedeutung. Präanalytische Fehler können zu schwerwiegenden Folgefehlern in Indikation, Analytik, Befundinterpretation und bei der Therapieplanung führen. Alle Einsender bitten wir dringend, die nachfolgenden Hinweise zur zu beachten! 3. Probengewinnung Allen Probeentnahmen geht ein ausführliches Patientengespräch voraus! Dabei müssen folgende Punkte besprochen und dokumentiert werden (je nach Art der Probeentnahme sind nicht alle Punkte zutreffend): Anamnese Erstellung eines Stammbaumes auf Formblatt Indikation zur Untersuchung (mit Vorbefunden) Aufklärung über Zweck, Art, Umfang und Aussagekraft der genetischen Untersuchung (GenDG 9): Erläuterung der Chromosomendiagnostik, speziell Aussagekraft und Grenzen der Methode, Mosaikbefunde, Direktpräparation bzw. FISH-Diagnostik, Langzeitkultur, Array-CGH, Diagnostik von Genmutationen, Besprechung spezieller Untersuchungen der molekularen Genetik (CF-Diagnostik), Klärung der Frage, ob eine schnelle Untersuchung der Chromosomen 21/18/13/XY durch FISH erfolgen soll, ggf. Unterschrift zur Kostenübernahme der Untersuchungen Einwilligung gemäß Gendiagnostikgesetz (GenDG 8), Unterschrift auf Aufklärungsbögen und Einwilligung Ausfüllen aller notwendiger Unterlagen für die zytogenetische und molekulargenetische Diagnostik (Probenbegleitschein) Vereinbarung über Befundmitteilung, Ergebnisbesprechung und genetische Beratung Sonographie vor Probenahme: Bei einer Amniozentese: Aufsuchen eines geeigneten Fruchtwasserdepots. Besondere Bedeutung des Amnions (innere Eihaut), Entnahme von Fruchtwasser nur bei anliegendem Amnion. Punktion paraplazentar oder transplazentar. Handbuch der und Primärprobengewinnung Seite 4 von 22
5 Handbuch der und Primärprobengewinnung Bei einer Chorionzottenbiopsie bzw. Plazentazentese: Aufsuchen eines geeigneten Plazentaareals. Falls nötig: Anpassen der Blasenfüllung und Aufrichten des Uterus. Bei einer Chordozentese: Aufsuchen der plazentaren Insertion der Nabelschnur oder einer anderen geeigneten Punktionsstelle (freie Schlinge, intrahepatischer Teil der Vena umbilicalis, Cardiozentese) Bei Entnahme von peripherem Venenblut: den Patienten eine bequeme Position einnehmen lassen, eine geeignete Vene suchen und unter sterilen Bedingungen eine entsprechende Menge Blut (mit den, für die angeforderten Untersuchungen erforderlichen Zusätzen (siehe Tabelle)) entnehmen. Röhrchen sofort beschriften! Beim Abstrich von Mundschleimhaut bitte unbedingt jegliche Kontamination vermeiden. Den Abstrich immer doppelt durchführen (2 Abstriche mit je 2 Abstrichstäbchen.) Die Röhrchen sofort beschriften! 3.1 Fruchtwasserpunktion (Amniozentese) ml Fruchtwasser mit steriler Einmalnadel in sterile Einmalspritze oder Vacutainer unter sterilen Bedingungen entnehmen. Eine maternale Kontamination muss durch geeignete Punktionstechnik jedenfalls vermieden werden. Spritze mit sterilem Kombi-Stopfen (rot) verschließen. Für eine korrekte Diagnostik muss die Fruchtwasserprobe klar und nicht frisch blutig sein. Bei frisch-blutigem Fruchtwasser muss Heparin (0,5 ml Na-Heparin) steril zugegeben werden, um eine Koagelbildung zu vermeiden! Amniozentese: sterile Einmalspritze gefüllt mit 20 ml Fruchtwasser, klar gelblich. 3.2 Chorionzottenbiopsie / Plazentazentese Die Entnahme des Zottenmaterials sollte in eine 10 ml Standard-Einmalspritze unter sterilen Bedingungen erfolgen. Die Spritze muss mit ca. 2 ml sterilem, heparinisiertem Medium, das vom Labor (Zytogenetik) zur Verfügung gestellt wird (alternativ steriles NaCl), gefüllt sein. Die Probe soll mg Zotten umfassen. Für eine zytogenetische und gleichzeitige molekulargenetische Diagnostik werden mehr als 25 mg benötigt. Zottenmaterial mit Medium oder Kochsalz spülen und in Transportgefäße mit CVS-Medium überführen. Handbuch der und Primärprobengewinnung Seite 5 von 22
6 Handbuch der und Primärprobengewinnung Chorionzottenbiopsie / Plazentazentese: Steriles Zentrifugenspitzröhrchen gefüllt mit 25 mg Zottenmaterial. 3.3 Entnahme von Abortmaterial Die Entnahme von Abortmaterial (Chorionzotten, Fetalgewebe, ggf. Achillessehne) sollte unter sterilen Bedingungen erfolgen. Zotten/Fetalgewebe von Blutbeimengungen freispülen. Nur geeignete Probe einsenden, keine Feten. Das entnommene Material wird in ein Transportgefäß mit Medium, das vom Labor (Zytogenetik) zur Verfügung gestellt wird (alternativ steriles NaCl), überführt. 3.4 Entnahme von Fetalblut Die Entnahme von Fetalblut erfolgt unter sterilen Bedingungen in mehrere 2 ml Standard- Einmalspritzen. Insgesamt werden ca. 3 5 ml Blut aus der kindlichen Nabelschnurvene entnommen. Für eine zytogenetische Untersuchung wird das fetale Blut mit Heparin versetzt, für eine molekulargenetische Diagnostik wird EDTA zugegeben (siehe Tabelle). 3.5 Entnahme von peripherem Venenblut Reihenfolge bei der Entnahme von Venenblut: o Nativblut (Serum) (immer zuerst, vor Röhrchen mit Zusätzen) o Citratblut o EDTA- / Heparinblut Blutproben mit Zusatz von Antikoagulantien müssen sofort vorsichtig gemischt werden - nicht schütteln! Handbuch der und Primärprobengewinnung Seite 6 von 22
7 Handbuch der und Primärprobengewinnung 3.6 Abstrich von Mundschleimhaut Es sollten Handschuhe getragen werden. Für den Abstrich von Mundschleimhaut verwenden wir Abstrich-Tupfer ( Swab Pack ) der Firma Isohelix ( Den Abstrich-Tupfer aus der sterilen Verpackung entnehmen. (Bitte nie den Tupfer selbst mit der Hand berühren!) Den Abstrich-Tupfer aus dem Plastikröhrchen herausnehmen. Streichen Sie für mind. 20 Sekunden (besser: 60 Sekunden) langsam mit dem weißen Tupfer / Bürstchen auf der Innenseite der Wange (oder über bzw. unter dem Bereich der Ober- und Unterlippe). Bitte führen Sie diesen Vorgang mit starkem, aber angemessenen Druck durch. Drehen sie das Stäbchen während der Anwendung. Dann bitte den Plastikdeckel über das Stäbchen führen, wobei der Verschluss des Deckels nach oben zeigen muss (wenn der Abstrich-Tupfer / Bürstchen nach unten zeigt). Als nächstes bitte Abstrich-Tupfer in das beiliegende sterile Plastik-Röhrchen stecken und den Deckel fest in das Röhrchen stecken. Jetzt halten Sie das verschlossene Röhrchen am Deckel fest und ziehen den Stab an dem der Tupfer befestigt ist einfach aus dem Röhrchen heraus. Das Plastikröhrchen bitte sofort verschließen und beschriften! Bitte wiederholen Sie den Vorgang mit einem neuen Abstrich-Tupfer 2-3 mal pro Patient. Wählen Sie für die Wiederholung auch die andere Wangenseite des Patienten aus. ( Handbuch der und Primärprobengewinnung Seite 7 von 22
8 Handbuch der und Primärprobengewinnung 4. Probengefäße Benötigte Probengefäße und Medien werden von uns kostenfrei zur Verfügung gestellt. Die Materialanforderung erfolgt über das zytogenetische Labor unter der Telefonnummer oder Fax oder Den Anforderungsschein finden sie als PDF hier. Diagnostik Probengefäße Chromosomenanalyse aus Fruchtwasser (Amniozentese) ggf. ergänzende FISH-Analyse / PCR Diagnostik (siehe auch molekulargenetische Diagnostik) Chromosomenanalyse aus Chorionzotten oder Plazentazotten (Chorionzottenbiopsie / Plazentazentese) (siehe auch molekulargenetische Diagnostik) Molekulare Chromosomenanalyse (Array- CGH) aus Abortmaterial (Plazentazotten, fetales Gewebe oder Archillessehne) Chromosomenanalyse aus Blut / Nabelschnurblut (Chordozentese) (siehe auch molekulargenetische Diagnostik) Molekulargenetische Diagnostik aus Blut / Nabelschnurblut Fruchtwasser Chorionzotten / Plazentazotten Abortmaterial Mundschleimhautabstrich - Sterile Einmalspritzen ohne Naturkautschuk 5 ml, 10 ml, 20 ml - Kombistopfen (rot) für Punktions-Spritzen - oder Probenspitzröhrchen - Transportgefäße mit Saugeinlage und Versandtüten - Sterile Einmalspritzen ohne Naturkautschuk (5 ml, 10 ml) - CVS - Röhrchen mit Heparin / Medium - CVS - Röhrchen mit Spülmedium - CVS - Röhrchen mit Transportmedium - Transportgefäße mit Saugeinlage und Versandtüten - Röhrchen mit Transportmedium oder steriler Kochsalzlösung - Transportgefäße mit Saugeinlage und Versandtüten - Na-Heparin-Monovette (grün) Sarstedt 2,6 ml, 7,5 ml - Na-Heparin-Vacutainer (grün) BD - peripheres Blut im Verhältnis 1:10 gemischt mit Na-Heparin i.u./ml in Probenspitzröhrchen oder vergleichbaren Gefäßen - Li-Heparin-Monovetten (gelb) Sarstedt - Transportgefäße mit Saugeinlage und Versandtüten Blut: - EDTA-Monovetten (rot) Sarstedt 2,7 ml, 7,5 ml Mundschleimhautabstrich: Abstrich-Tupfer der Firma Isohelix Alle anderen Materialien: wie für Chromosomenanalyse - Transportgefäße mit Saugeinlage und Versandtüten Handbuch der und Primärprobengewinnung Seite 8 von 22
9 Handbuch der und Primärprobengewinnung 5. Diagnostik / Untersuchungsmaterial / Lagerung Diagnostik / Untersuchungsmaterial Chromosomenanalyse aus Fruchtwasser* (Amniozentese) *ggf. ergänzende FISH-Analyse / PCR- Diagnostik / molekulargenetische Analysen / Array-CGH Volumen und Gefäß ml Fruchtwasser* in sterilen Einmalspritzen / Zentrifugenspitzröhrchen *Bei gleichzeitiger molekulargenetischer Diagnostik - wenn möglich- plus 5 ml und zusätzlich EDTA-Blut der Mutter einsenden (Kontaminationskontrolle) Lagerung bis Abholung / Versand am selben Tag: bei Raumtemperatur später: im Kühlschrank bei 8 C (keinesfalls einfrieren) Hinweis: Bei geringen Fruchtwassermengen und / oder sehr früher Schwangerschaftswoche (<14+0) kann die Kulturzeit aufgrund der geringen Zellzahl stark verlängert sein. Chromosomenanalyse aus Chorionzotten* (Chorionzottenbiopsie) *ggf. ergänzende molekulargenetische Analysen / Array-CGH mg Zottenmaterial* in Medium im sterilen Transportröhrchen oder direkt in Punktionsspitze *Bei molekulargenetischer Diagnostik wenn möglich - mehr Material gewinnen und zusätzlich EDTA-Blut der Mutter einsenden (Kontaminationskontrolle) am selben Tag: bei Raumtemperatur später: im Kühlschrank bei 8 C (keinesfalls einfrieren) Hinweis: Bei geringen Mengen an Zottenmaterial kann a) nur eine Langzeitkultur anstelle der sonst üblichen zwei Kulturen angelegt werden oder b) keine Direktpräparation erfolgen (eingeschränkter Befund). Molekulare Chromosomenanalyse (Array-CGH) aus Abortmaterial* (vorzugsweise Plazentazotten) *Bitte schicken Sie EDTA-Blut der Mutter zur Kontaminationskontrolle mit! mg Zottenmaterial in steriler Kochsalzlösung oder Medium in sterilem Transportröhrchen EDTA-Blut der Mutter einsenden (Kontaminationskontrolle) am selben Tag: bei Raumtemperatur später: im Kühlschrank bei 8 C (keinesfalls einfrieren) Hinweis: Abortmaterial nicht in Formalin einlegen. Durch Formalin werden die Zellen abgetötet, ein weiteres Wachstum / Kultivierung ist damit nicht mehr möglich. Bitte keine Feten schicken. Chromosomenanalyse aus Blut / Nabelschnurblut* *ggf. ergänzende FISH-Analyse 3 5 ml Na-Heparin-Blut (3 5 ml Li-Heparin-Blut) am selben Tag: bei Raumtemperatur später: im Kühlschrank bei 8 C (keinesfalls einfrieren) Nabelschnurblut: 2 3 ml Na-Heparin-Blut Hinweis: EDTA-Blut oder geronnenes Blut ist für die zytogenetische Chromosomenanalyse nicht geeignet. Molekulargenetische Diagnostik aus Blut / Nabelschnurblut Molekulargenetische Diagnostik aus Mundschleimhautabstrich 2 4 ml EDTA-Blut am selben Tag: bei Raumtemperatur später: im Kühlschrank bei 8 C (keinesfalls einfrieren) Sterile Abstrich-Tupfern der Fa. Isohelix ; Transport im am selben Tag: bei Raumtemperatur Handbuch der und Primärprobengewinnung Seite 9 von 22
10 Handbuch der und Primärprobengewinnung zugehörigen sterilem Röhrchen später: im Kühlschrank bei 8 C 6. Probenbeschriftung und Auftragserteilung Bitte schicken Sie zu jeder Probe einen vollständig ausgefüllten Probenbegleitschein! Andernfalls kann die Probe nicht bearbeitet werden! Je nach angeforderter Diagnostik verwenden Sie bitte einen Probenbegleitschein Zytogenetisches Labor und / oder Labor für molekulare Genetik. (PDF Zytogenetisches Labor / PDF Labor für molekulare Genetik) Auf dem Probengefäß sind zur Identitätssicherung folgende Angaben erforderlich: Name Vorname Geburtsdatum (alternativ der Zusatz Fetus oder Patienten-ID) Die Beschriftung muss sich auf dem Probengefäß und nicht auf der Umverpackung befinden! Infektiöses Material (z.b. HIV-/Hepatitis C positiv) muss als solches gekennzeichnet sein! Achtung: unbeschriftete Proben können nicht bearbeitet werden! Auf dem Probenbegleitschein sind folgende Angaben erforderlich (Rückseite beachten!): Name, Geburtsdatum und Anschrift der Patientin Name des verantwortlichen Arztes Art des Untersuchungsmaterials Datum der Probeentnahme Untersuchungsauftrag Indikation für die angeforderte Untersuchung Schwangerschaftswoche klinische Angaben (z.b. sonographische Befunde, Schwangerschaftsverlauf) Vorbefunde / Ergebnisse von Voruntersuchungen Angaben zur Aufklärung über die angeforderte genetische Untersuchung Angaben über die Aufbewahrung / Vernichtung der gewonnenen Probe Einwilligung der Patientin / des Patienten zur genetischen Untersuchung Nennung der Ärzte, die eine Befundmitteilung erhalten sollen Unterschrift der Patientin / des Patienten Hinweis: Nach dem Gendiagnostikgesetz (GenDG 8) darf eine genetische Analyse nur vorgenommen werden, wenn der beauftragten Person oder Einrichtung der Nachweis der Einwilligung des Patienten vorliegt. Auf dem Überweisungsschein (Laboranforderung Überweisungsformular 10 (weiß)) sind folgende Angaben erforderlich: Art des Untersuchungsmaterials Untersuchungsauftrag Indikation Handbuch der und Primärprobengewinnung Seite 10 von 22
11 Handbuch der und Primärprobengewinnung klinische Angaben Hinweis: Ohne Überweisungsschein oder Nachweis des Kostenträgers keine Untersuchung! 7. Probentransport / Probenversand Für den Transport müssen die gewonnenen Proben (sauber, verschlossen und beschriftet!) zusätzlich in ein weiteres Transportröhrchen mit Saugeinlage verpackt werden. Diese kommen dann zusammen mit dem Probenbegleitschein und dem Überweisungsschein in eine Versandtüte. Die Versandtüte ist bereits versehen mit unserer Adresse und dem Vermerk Medizinisches Untersuchungsgut. Die Transportgefäße und Transporttüten müssen den aktuell gültigen Bestimmungen zum Versand biologischer Stoffe entsprechen, um eine Gefährdung des Transport- und Laborpersonals zu vermeiden und werden von uns zur Verfügung gestellt. Da im Bereich der Zytogenetik in der Regel Kulturen aus lebenden Zellen angelegt werden müssen, ist der Probentransport zeitkritisch. Die Abholung der Fruchtwasser- und Chorionzotten-Proben durch unseren Fahrdienst sollte am Punktionstag erfolgen. Abortmaterial kann bis zum nächsten Tag problemlos gelagert werden. Bitte bestellen Sie den Fahrdienst im Zytogenetischen Labor und melden Sie dort ihre Probe an. Wir organisieren einen möglichst zeitnahen Abholungstermin. (Fruchtwasser kann eine Nacht im Kühlschrank bi 8 C gelagert werden, darf aber auf keinen Fall eingefroren werden!) Bei molekulargenetischer Diagnostik ist der Probentransport weniger zeitkritisch, sollte aber nicht länger als 3 Tage dauern. Diese Frist wird aber im Normalfall selbst bei Versand mit der Post / Paketdienst eingehalten. Ggf. soll bereits extrahierte DNA verschickt werden. 7.1 Kostenlose Probenabholung durch unseren Fahrdienst Stadtgebiet München Im Stadtgebiet München beauftragen wir einen Fahrrad-Kurierdienst mit der Abholung ihrer Probe. Dieser Fahrdienst steht Ihnen routinemäßig oder auf Anforderung zur Verfügung. Ein Anruf in unserem Labor genügt, wir holen Ihre Proben ab! Telefon 089 / Kostenlose Probenabholung durch unseren Fahrdienst außerhalb von München Eine Abholung ihrer Proben in der Praxis / Klinik durch einen externen Kurierdienst ist auch außerhalb des Stadtgebiets München (bis etwa 100 km) möglich. Dieser Service bietet Ihnen eine optimale Sicherheit für die Zustellung Ihrer Proben innerhalb von 24 Stunden! Ein Anruf in unserem Labor genügt, wir organisieren den Abholdienst! Telefon 089 / Probenversand auf dem Postweg (außerhalb von München, insbesondere bei einer größeren Distanz als 100 km) Insbesondere bei Proben für molekulargenetische Untersuchungen ist ein Versand mit der Post Handbuch der und Primärprobengewinnung Seite 11 von 22
12 Handbuch der und Primärprobengewinnung unproblematisch, da hier im Normalfall keine Kulturen angelegt werden müssen. Aber auch der Versand von Material für eine anschließende Kultivierung ist möglich. Wir stellen Ihnen hierfür gerne geeignetes Versandmaterial zur Verfügung. Bitte fordern Sie dieses zusammen mit Ihrer Materialbestellung an. Beachten Sie beim Versand die adäquate Verpackung der Proben! Bei extremen Temperaturen muss der Versand in einer Styroporbox erfolgen (gekühlt und / oder vor Einfrieren geschützt!) Material Transport Fruchtwasser für Chromosomenanalyse Chorionzotten / Plazentazotten für Chromosomenanalyse Abortmaterial für molekulare Chromosomenanalyse (Array-CGH) Na-Heparin-Blut für Chromosomenanalyse EDTA-Blut für molekulargenetische Diagnostik Mundschleimhautabstrich für molekulargenetische Diagnostik Versand arbeitstäglich durch unseren Fahrdienst arbeitstäglich durch unseren Fahrdienst arbeitstäglich durch unseren Fahrdienst Probenversand auf dem Postweg arbeitstäglich durch unseren Fahrdienst Probenversand auf dem Postweg arbeitstäglich durch unseren Fahrdienst Probenversand auf dem Postweg arbeitstäglich durch unseren Fahrdienst Probenversand auf dem Postweg 8. Materialarchivierung Nach Abschluss der Diagnostik wird die gewonnene Probe gemäß Gendiagnostikgesetz (GenDG 13) vernichtet. In besonderen Fällen kann nach abschließender genetischer Beratung ein anderes Vorgehen festgelegt werden (z.b. Proben von Indexpatienten). 9. Befundmitteilung Die Befundmitteilung erfolgt immer schriftlich am Tag der Fertigstellung des Befundes (auch von Teilbefunden, wie z.b. einer FISH-Diagnostik oder einer Zotten-Direktpräparation). Resultate können unter Beachtung des Gendiagnostikgesetzes (GenDG 11) auch telefonisch von den Patienten abgefragt werden. Den betreuenden Ärzten kann der Befund nach Einwilligung der betroffenen Person, ggf. auch per Fax, übermittelt werden. Zeitkritische, auffällige (pathologische) Befunde werden dem betreuenden Arzt nach Möglichkeit zuerst telefonisch und ggf. per Fax mitgeteilt. Nach Absprache mit dem verantwortlichen Arzt, im Zweifelsfall auch unaufgefordert, wird die Patientin von uns aus über den Befund informiert und mit ihr eine genetische Beratung vereinbart, um die Befunde ausführlich mitzuteilen und zu besprechen. Sie kann diese Beratung ablehnen. Handbuch der und Primärprobengewinnung Seite 12 von 22
13 Handbuch der und Primärprobengewinnung 10. Unterauftrag / Fremdanalysen Seltene Spezialuntersuchungen, die wir nicht in unserem Labor durchführen, können an andere labormedizinische/humangenetische Institute als Unterauftrag weitergeleitet werden. Die Weiterleitung des Materials erfolgt schnellstmöglich und unter Einhaltung der präanalytischen Bestimmungen. Die Unterauftragsvergabe erfolgt ausschließlich an kompetente Fachlabore. Soweit möglich werden von uns hierfür akkreditierte Laborinstitutionen (DIN EN ISO/IEC 17025, DIN EN ISO 15189) in Anspruch genommen. Alle Analysen, die als Unteraufträge vorgenommen werden, sind im aktuellen Leistungsverzeichnis sowie in unseren Befundmitteilungen eindeutig gekennzeichnet. 11. Leistungsverzeichnis: Labor für molekulargenetische Diagnostik Krankheit Untersuchungs material Untersuchungstech nik Achondrogenesis Ib (SLC26A2) genomische DNA PCR, DNA Achondrogenesis II SEDC (COL2A1) genomische DNA PCR, DNA, MLPA Achondrogenesis/Chondrodysplasie (TRIP11) genomische DNA PCR, DNA Achondroplasie (FGFR3) genomische DNA PCR, DNA Adrenogenitales Syndrom (CYP21A2/CYP11B1) genomische DNA PCR, DNA, MLPA Albinismus (Oculocutaneous Albinism Typ1) (TYR, OCA1)) genomische DNA PCR, DNA Alpha1-Antitrypsin-Mangel (A1-AT) (SERPINA1) genomische DNA PCR, DNA Alport-Syndrom (COL4A3, COL4A4) genomische DNA PCR, DNA Androgen-Resistenz (AR) genomische DNA PCR, DNA, MLPA Angelman-Syndrom (UBE3A) genomische DNA PCR, DNA, MLPA Antithrombin-III-Mangel (SERPINC1) genomische DNA PCR, DNA Apert-Syndrom (FGFR2) genomische DNA PCR, DNA Atelosteogenesis I(FLNB) genomische DNA PCR, DNA Handbuch der und Primärprobengewinnung Seite 13 von 22
14 Handbuch der und Primärprobengewinnung Autosomal-dominate polyzystische Nierenerkrankung/ADPKD (PKD1) genomische DNA PCR, DNA Autosomal-rezessive polyzystische Nierenerkrankung/ ARPKD (PKHD1) genomische DNA PCR, DNA Baraitser-Winter- Syndrom (ACTB, ACTG1) genomische DNA PCR, DNA Blepharophimosis-Epicanthus-inversus-Syndrom BPES (FOXL2) genomische DNA PCR, DNA BOR-Syndrom (EYA1) genomische DNA PCR, DNA Campomele Dysplasie (SOX9) genomische DNA PCR, DNA Carpenter Syndrom (RAB23) genomische DNA PCR, DNA CHARGE-Syndrom (CHD7) genomische DNA PCR, DNA, MLPA Chondrodysplasia punctata AR (PEX7/GNPAT/AGPS) genomische DNA PCR, DNA Chondrodysplasia punctata XD (EBP) genomische DNA PCR, DNA Chondrodysplasia punctata XR (ARSE) genomische DNA PCR, DNA Coffin-Lowry Syndrom (RPS6KA3) genomische DNA PCR, DNA Crouzon-Syndrom (FGFR2) genomische DNA PCR, DNA Cystische Fibrose (CFTR) genomische DNA PCR, Fragmentanalyse, MLPA Diastrophe Dysplasie (SLC26A2) genomische DNA PCR, DNA Ehlers-Danlos-Syndrom Typ 6 (PLOD1) genomische DNA PCR, DNA Ellis-van-Creveld-Syndrom (EvC/EvC2) genomische DNA PCR, DNA Epilepsie-Panel genomische DNA PCR, Next Generation Sequencing (NGS) Familiäre Adenomatöse Polyposis (FAP2) (APC, MUTYH) genomische DNA PCR, DNA,MLPA Fetale Akinesie FADS ( RAPSN / DOK7) genomische DNA PCR, DNA Fragiles X-Syndrom (FMR1) genomische DNA PCR, Fragmentanalyse Fraser-Syndrom (FRAS1/FREM2/GRIP1) genomische DNA PCR, DNA G6PD-Mangel (Favismus) (G6PD) genomische DNA PCR, DNA Gehörlosigkeit / Taubheit (GJB2 / GJB6) genomische DNA PCR, DNA, MLPA Handbuch der und Primärprobengewinnung Seite 14 von 22
15 Handbuch der und Primärprobengewinnung GLI3-assoziierte Krankheitsbilder (GLI3) genomische DNA PCR, DNA, MLPA Glykogen Speicher Krankheit Typ 5 (McArdle Disease) (PYGM) genomische DNA PCR, DNA Glykogenose Typ 1 A (G6PC) genomische DNA PCR, DNA Gorlin-Goltz Syndrom (PTCH1, PTCH2, SUFU) genomische DNA PCR, DNA, MLPA Hämochromatose (HFE) genomische DNA PCR, DNA Hämoglobin-beta (HBB) genomische DNA PCR, DNA, MLPA Hereditäre Brust- und Eierstockkrebs (BRCA1, BRCA2, CHEK2, RAD51C, TP53) genomische DNA PCR, NGS, MLPA Heterotaxie (Panel: FOXH1, NODAL, ZIC3, LEFTY2, GDF1, ACVR2B, CRELD, NKX2.5, CITED2, CFC1, GALNT11) genomische DNA PCR, DNA Holoprosenzephalie (SHH, ZIC2, SIX3, TGIF1) genomische DNA PCR, DNA, MLPA Holt-Oram (TBX5) genomische DNA PCR, DNA, MLPA Hydrocephalus (X-linked) (L1CAM) genomische DNA PCR, DNA Hypochondroplasie (FGFR3) genomische DNA PCR, DNA Hypophosphatasie (ALPL) genomische DNA PCR, DNA Intrakranielle Hämorrhagie (COL4A1, COL4A2) genomische DNA PCR, DNA Kabuki-Syndrom (MLL2) genomische DNA PCR, DNA, MLPA Kartagener Syndrom (DNAH5/DNAI1) genomische DNA PCR, DNA Kongenitale Fasertypdisproportion (CFTD) (MYH7) genomische DNA PCR, DNA,MLPA Kongenitales myasthenisches Syndrom /CMS (MUSK,CHAT, CHRNE, COLQ, GFPT1, CHRNA1, CHRNA2, CHRNB, CHRNB2, CHRND) genomische DNA PCR, DNA Kraniosynostosen (Pfeiffer) (FGFR1 / FGFR2 / FGFR3) genomische DNA PCR, DNA Kurzrippen-Polydaktylie-Syndrome (EvC1, EvC2, IFT80, WDR19) genomische DNA PCR, DNA Leopard-Syndrom (BRAF) genomische DNA PCR, DNA Leri-Weill Dyschondrosteose (LWD) / Kleinwuchs (SHOX) genomische DNA PCR, DNA, MLPA Handbuch der und Primärprobengewinnung Seite 15 von 22
16 Handbuch der und Primärprobengewinnung Lissenzephalie / subkortikale Bandheterotopie/ Double-cortex- Syndrom (LIS1, DCX, TUBA1A) genomische DNA PCR, DNA, MLPA Marfan Syndrom (FBN1) genomische DNA PCR, DNA, MLPA MCAD-Defizienz (ACADM) genomische DNA PCR, DNA McKusick-Kaufmann-Syndrom/ Bardet-Biedl-Syndrom6 (MKKS) genomische DNA PCR, DNA Meckel-Gruber Syndrom (TMEM216, MKS1) genomische DNA PCR, DNA Mehrlinge: monozygot / dizygot genomische DNA PCR, DNA Fragmentanalyse Metachromatische Leukodystrophie (ARSA) genomische DNA PCR, DNA MSX-2 assoziierte Kraniosynostose/Kraniosynostose Typ II (MSX- 2) genomische DNA PCR, DNA Muenke-Syndrom ( FGFR3) genomische DNA PCR, DNA Multi-Gen-Panel-Diagnostik genomische DNA New Sequencing Generation (NGS) Multiple epiphysäre Dysplasie Typ I / Pseudoachondroplasie (COMP/MATN3/COL2A1/SLC26A2) genomische DNA PCR, DNA Multiple kartilaginäre Exostosen Typ 1 und 2 (EXT1, EXT2) genomische DNA PCR, DNA, MLPA Muskeldystrophie Duchenne/Becker (DMD) genomische DNA PCR, DNA, MLPA Nager-Syndrom (SF3B4) genomische DNA PCR, DNA Nail-Patella Syndrom (LMX1B) genomische DNA PCR, DNA Neurofobromatose (NF1) genomische DNA PCR, DNA, MLPA Nierenzysten und Diabetes-Syndrom (HNF1B) genomische DNA PCR, DNA, MLPA Noonan Syndrom (PTPN11, SOS1, RAF1, KRAS, BRAF, RIT1), Rasopathie (Panel: HRAS, RAF1, MEK1, MEK2, CBL) genomische DNA PCR, DNA Opsismodysplasie (INPPL1) genomische DNA PCR, DNA Osteogenesis imperfecta AD (COL1A1/COL1A2) genomische DNA PCR, DNA, MLPA Osteogenesis imperfecta AR (CRTAP/LEPRE1/PPIB) genomische DNA PCR, DNA Periodisches Fieber-Syndrom (NLRP3, TRAPS, MEFV, MVK) genomische DNA PCR, Next Generation Sequencing (NGS) Phenylketonurie (PKU) (PAH) genomische DNA PCR, DNA, MLPA Handbuch der und Primärprobengewinnung Seite 16 von 22
17 Handbuch der und Primärprobengewinnung Pitt-Hopkins-ähnliches Syndrom 2 (PTHSL2) (NRXN1) genomische DNA PCR, DNA, MLPA Polymikrogyrie (TUBB2B) genomische DNA PCR, DNA Pränatal Gen-Panel Analysen (auch postnatal) genomische DNA PCR, Next Generation Sequencing (NGS) Pränatal Gen-Panel Analysen (im Kindesalter) genomische DNA PCR, Next Generation Sequencing (NGS) Primäre/vorzeitige Ovarialinsuffizienz POF (FMR1 / BMP15 / FSHR) genomische DNA PCR, DNA Protein C-Defizienz (PROC) genomische DNA PCR, DNA Protein S-Mangel (PROS) genomische DNA PCR, DNA, MLPA Pseudohypoaldosteronismus Typ 1 (PHA1A) (NR3C2) genomische DNA PCR, DNA Restriktive Dermatopathie (ZMPSTE24) genomische DNA PCR, DNA Rhesus C/c, D, E/e genomische DNA PCR, DNA Analyse im Agarosegel Rolando-Epilepsie (SRPX2) genomische DNA PCR, Next Generation Sequencing (NGS) Saethre Chotzen Syndrom/Kraniosynostose Typ I (TWIST1) genomische DNA PCR, DNA Schizenzephalie (SIX3/SHH) genomische DNA PCR, DNA Simpson-Golabi-Behmel-Syndrom Typ1 (GCP3, GCP4, OFD1) genomische DNA PCR, DNA, MLPA Smith-Lemli-Opitz Syndrom (DHCR7) genomische DNA PCR, DNA SMN1-Überträgerdiagnostik (SMN1/SMN2) genomische DNA MLPA Sotos-Syndrom/Großwuchs (NSD1), genomische DNA PCR, DNA,MLPA Spondylocostale Dysosostis Typ 4 (DLL3, MESP2, HES7, LFNG) genomische DNA PCR, DNA Spondylocostale Dysosostis Typ 5 (SCDO5) (TBX6) genomische DNA PCR, DNA Startle-Syndrom (GLRA1, GLRB, GPHN, SLC6A5) genomische DNA PCR, DNA Stickler-Syndrom (COL2A1 / COL11A1) genomische DNA PCR, DNA, MLPA TAR-Syndrom (RBM8A) genomische DNA PCR, DNA Thanatophore Dysplasie I / II (FGFR3) genomische DNA PCR, DNA Thrombophilie (Faktor-II-Mutation, Faktor-V-Mutation, MTHFR C677T, MTHFR A1298C) genomische DNA Quantitative PCR; Real- Time-PCR Handbuch der und Primärprobengewinnung Seite 17 von 22
18 Handbuch der und Primärprobengewinnung Treacher-Collins-Franceschetti-Syndrom (TCOF1/POLR1C/POLR1D) genomische DNA PCR, DNA Truncus arteriosus isoliert (PLXND1) genomische DNA PCR, DNA Tuberöse Sklerose (TSC1, TSC2) genomische DNA PCR, DNA, MLPA West-Syndrom (MEF2C, STXBP1, CDKL5, ARFGEF2, ARX) genomische DNA PCR, DNA, MLPA Y-chromosomale Mikrodeletionen (Azoospermiefaktor, AZF) genomische DNA PCR, DNA Analyse im Agarosegel Untersuchungsverfahren der Hybridisierungsverfahren Krankheit Untersuchungsmaterial Untersuchungstechnik chromosomale Imbalance genomische DNA Array-CGH TAR-Syndrom (RBM8A) genomische DNA Array-CGH Handbuch der und Primärprobengewinnung Seite 18 von 22
19 Handbuch der und Primärprobengewinnung Leistungsverzeichnis: Zytogenetisches Labor Untersuchungsverfahren der Chromosomenanalyse Krankheit Untersuchungsmaterial Untersuchungstechnik Chromosomenanalyse Fruchtwasser Zellkultur, Metaphasepräparation, Färbungen, Karyotypisierung Chromosomenanalyse Chromosomenanalyse Chromosomenanalyse Chorionzotten, Plazentagewebe Zellkultur von Chorionzotten, Plazentagewebe, Abortgewebe und Nabelschnur Lymphozyten aus peripherem Blut, Nabelschnurblut Chromosomen- Direktpräparation aus Chorionzotten/Plazentagewebe, Färbungen, Karyotypisierung Chorionzotten/Plazentagewebe- Zellkultur, Metaphasepräparation, Färbungen, Karyotypisierung Zellkultur, Chromosomenpräparation aus kultivierten peripheren Lymphozyten, Färbungen, Karyotypisierung Handbuch der und Primärprobengewinnung Seite 19 von 22
20 Handbuch der und Primärprobengewinnung Leistungsverzeichnis: Molekular-Zytogenetisches Labor Untersuchungsverfahren der Fluoreszenz In-situ Hybridisierung Krankheit Untersuchungsmaterial Untersuchungstechnik FISH 21,18,13,X,Y (pränataler Schnelltest) strukturelle Chromosomenstörungen, chromosome painting Mosaik- bzw. Markerabklärung Subtelomeranalyse DiGeorge-Syndrom Mikrodeletionssyndrom Prader-Willi-Syndrom Mikrodeletionssyndrom Angelman-Syndrom Mikrodeletionssyndrom Smith-Magenis-Syndrom Mikrodeletionssyndrom unkultivierte Amnionzellen und Lymphozyten, Zotten- Direktpräparationen Amnionzellen, Lymphozyten, Plazentazotten, Amnionzellen, Lymphozyten, Plazentazotten, Amnionzellen, Lymphozyten, Plazentazotten, Amnionzellen, Lymphozyten, Plazentazotten, kultivierte Amnionzellen, kultivierte Lymphozyten, Plazentazottenkultur, Amnionzellen, Lymphozyten, Plazentazotten, Amnionzellen, Lymphozyten, Plazentazotten, Interphase-Untersuchungen durch FISH auf Metaphasen auf Metaphasen / Zellkernen auf Metaphasen / Zellkernen auf Metaphasen / Zellkernen auf Metaphasen / Zellkernen auf Metaphasen / Zellkernen auf Metaphasen / Zellkernen Handbuch der und Primärprobengewinnung Seite 20 von 22
21 Handbuch der und Primärprobengewinnung Cri-du-Chat-Syndrom Mikrodeletionssyndrom Wolf-Hirschhorn-Syndrom Mikrodeletionssyndrom Miller-Dieker-Syndrom Mikrodeletionssyndrom Kallmann-Syndrom Mikrodeletionssyndrom Williams-Beuren-Syndrom Mikrodeletionssyndrom Amnionzellen, Lymphozyten, Plazentazotten, Amnionzellen, Lymphozyten, Plazentazotten, Amnionzellen, Lymphozyten, Plazentazotten, Amnionzellen, Lymphozyten, Plazentazotten, Amnionzellen, Lymphozyten, Plazentazotten, auf Metaphasen / Zellkernen auf Metaphasen / Zellkernen auf Metaphasen / Zellkernen auf Metaphasen / Zellkernen auf Metaphasen / Zellkernen 12. Dokumente Alle für die Probeneinsendung benötigten Dokumente und Formulare gemäß Gendiagnostikgesetz (GenDG) sowie Einsender- und Patienteninformationen finden Sie unter downloads unter www. praenatal-medizin.de. Sie können Sie diese auch telefonisch bei uns bestellen (Telefon: 089/ ). Handbuch der und Primärprobengewinnung Seite 21 von 22
22 Handbuch der und Primärprobengewinnung 13. Qualitätsmanagement (QM) Der Bereich Praxis der Pränatal-Medizin München wurde im November 2011 nach DIN ISO 9001:2008 vom TÜV Süd zertifiziert. Eine Begutachtung durch die Deutsche Akkreditierungsstelle GmbH (DAkkS) fand im Juli 2012 statt. Die Erstakkreditierung (gemäß DIN EN ISO 15189:2007) vor Ort wurde für folgende Akkreditierungsbereiche durchgeführt: Labor für Zytogenetik Labor für molekulare Genetik Die Akkreditierungsurkunde (pdf) finden Sie unter downloads unter www. praenatalmedizin.de. Ziel unseres QM-Systems (Qualitätsmanagementsystems) ist es, die diagnostische Qualität unserer Laboruntersuchungen sicherzustellen und kontinuierlich weiter zu verbessern. Dies gewährleisten wir durch: eine umfassende Dokumentenlenkung standardisierte Arbeitsanweisungen jährliche Überprüfung und Aktualisierung aller Dokumente jährliches Qualitätsmanagementsystem-Review durch die Geschäftsleitung Fortbildungen aller Mitarbeiter zu aktuellen Themen regelmäßige Schulungen aller Mitarbeiter regelmäßige Teilnahme an Ringversuchen Beschwerdemanagement Fehlermanagement Einweiserzufriedenheit Anregungen, Fragen und Kritik helfen uns, unsere Qualität kontinuierlich zu verbessern. Ihre Ansprechpartner in der QM-Abteilung sind Kristina Tiltz und Dr. Daniela Köhler Telefon: 089 / tiltz@praenatal-medizin.de 14. Anlagen Probenbegleitschein Zytogenetisches Labor Probenbegleitschein Labor für molekulargenetische Genetik Leistungsverzeichnis Flyer Pränatale Diagnostik aus Fruchtwasser Flyer Pränatale Diagnostik aus Chorionzotten und Plazentazotten Flyer Array-CGH (vergleichende Genom-Hybridisierung) / Pränatale CHIP-Diagnostik Handbuch der und Primärprobengewinnung Seite 22 von 22
Handbuch der Präanalytik und Primärprobengewinnung. Inhalt. Pränatal-Medizin München
 Inhalt 1. Anschrift und Kontakte... 2 Laboratorien... 2 2. Allgemeine Hinweise zur... 4 3. Probengewinnung... 4 3.1 Fruchtwasserpunktion (Amniozentese)... 5 3.2 Chorionzottenbiopsie / Plazentazentese...
Inhalt 1. Anschrift und Kontakte... 2 Laboratorien... 2 2. Allgemeine Hinweise zur... 4 3. Probengewinnung... 4 3.1 Fruchtwasserpunktion (Amniozentese)... 5 3.2 Chorionzottenbiopsie / Plazentazentese...
Anlage zur Akkreditierungsurkunde D-ML-17482-01-00 nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-17482-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer:19.08.2015 bis 29.11.2017 Ausstellungsdatum: 19.08.2015 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-17482-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer:19.08.2015 bis 29.11.2017 Ausstellungsdatum: 19.08.2015 Urkundeninhaber:
Handbuch der Präanalytik und Primärprobengewinnung. Inhalt. Pränatal-Medizin München
 Inhalt 1. Anschrift und Kontakte... 2 Laboratorien... 2 2. Allgemeine Hinweise zur... 4 3. Probengewinnung... 4 3.1 Fruchtwasserpunktion (Amniozentese)... 5 3.2 Chorionzottenbiopsie / Plazentazentese...
Inhalt 1. Anschrift und Kontakte... 2 Laboratorien... 2 2. Allgemeine Hinweise zur... 4 3. Probengewinnung... 4 3.1 Fruchtwasserpunktion (Amniozentese)... 5 3.2 Chorionzottenbiopsie / Plazentazentese...
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13250-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 17.07.2014 bis 16.07.2019 Urkundeninhaber: genetikum - Genetische Beratung
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13250-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 17.07.2014 bis 16.07.2019 Urkundeninhaber: genetikum - Genetische Beratung
Handbuch der Primärprobengewinnung
 Inhaltsverzeichnis Inhaltsverzeichnis...1 1. Anschrift und Telefonverbindungen...2 2. Allgemeine Hinweise zur Präanalytik...2 3. Probengewinnung...3 3.1 Fruchtwasserpunktion (Amniocentese)...3 3.2 Chorionzottenbiopsie...3
Inhaltsverzeichnis Inhaltsverzeichnis...1 1. Anschrift und Telefonverbindungen...2 2. Allgemeine Hinweise zur Präanalytik...2 3. Probengewinnung...3 3.1 Fruchtwasserpunktion (Amniocentese)...3 3.2 Chorionzottenbiopsie...3
Handbuch der Primärprobengewinnung
 Handbuch der Primärprobengewinnung Inhaltsverzeichnis Inhaltsverzeichnis...1 1. Anschrift und Telefonverbindungen...2 2. Allgemeine Hinweise zur Präanalytik...2 3. Probengewinnung...3 3.1 Fruchtwasserpunktion
Handbuch der Primärprobengewinnung Inhaltsverzeichnis Inhaltsverzeichnis...1 1. Anschrift und Telefonverbindungen...2 2. Allgemeine Hinweise zur Präanalytik...2 3. Probengewinnung...3 3.1 Fruchtwasserpunktion
Handbuch der Primärprobengewinnung
 Handbuch der Primärprobengewinnung Probenentnahme/ Versand/ Abrechnung Telefon: 0621-822742 Telefax: 0621-827483 E-Mail: humangenetik-louis.hentze@t-online.de Gerne beantworten wir Ihre Fragen zu Probeneingang
Handbuch der Primärprobengewinnung Probenentnahme/ Versand/ Abrechnung Telefon: 0621-822742 Telefax: 0621-827483 E-Mail: humangenetik-louis.hentze@t-online.de Gerne beantworten wir Ihre Fragen zu Probeneingang
1 Allgemeine Hinweise 2 2 Anschrift und Ansprechpartner 2. 3 Leistungsverzeichnis 3
 Inhaltsverzeichnis 1 Allgemeine Hinweise 2 2 Anschrift und Ansprechpartner 2 2.1 Ansprechpartner für fachlich kompetente Beratung 3 3 Leistungsverzeichnis 3 3.1 Welche Untersuchung soll durchgeführt werden
Inhaltsverzeichnis 1 Allgemeine Hinweise 2 2 Anschrift und Ansprechpartner 2 2.1 Ansprechpartner für fachlich kompetente Beratung 3 3 Leistungsverzeichnis 3 3.1 Welche Untersuchung soll durchgeführt werden
Deutsche Akkreditierungsstelle GmbH
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D ML 13293 01 00 nach DIN EN ISO 15189:2007 Gültigkeitsdauer: 08.08.2012 bis 07.08.2017 Urkundeninhaber: Zentrum für Humangenetik Mannheim,
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D ML 13293 01 00 nach DIN EN ISO 15189:2007 Gültigkeitsdauer: 08.08.2012 bis 07.08.2017 Urkundeninhaber: Zentrum für Humangenetik Mannheim,
Leitfaden zur Präanalytik
 Seite 1 von 5 Leitfaden zur Präanalytik Der vorliegende Leitfaden unterstützt unsere Einsender bei der Veranlassung eines Analyseauftrages und ermöglicht optimale Voraussetzungen für eine effektive Zusammenarbeit
Seite 1 von 5 Leitfaden zur Präanalytik Der vorliegende Leitfaden unterstützt unsere Einsender bei der Veranlassung eines Analyseauftrages und ermöglicht optimale Voraussetzungen für eine effektive Zusammenarbeit
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13117-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 24.02.2014 bis 23.02.2019 Ausstellungsdatum: 24.02.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13117-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 24.02.2014 bis 23.02.2019 Ausstellungsdatum: 24.02.2014 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13362-03-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 19.03.2015 bis 17.12.2019 Ausstellungsdatum: 19.03.2015 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13362-03-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 19.03.2015 bis 17.12.2019 Ausstellungsdatum: 19.03.2015 Urkundeninhaber:
Hinweise zur Entnahme von Probenmaterial und zum Probenversand
 Hinweise zur Entnahme von Probenmaterial und zum Probenversand Die Humangenetik des MVZ der UMG ist im Bereich der Medizinischen Laboratoriumsdiagnostik in den Untersuchungsgebieten Molekulare Humangenetik
Hinweise zur Entnahme von Probenmaterial und zum Probenversand Die Humangenetik des MVZ der UMG ist im Bereich der Medizinischen Laboratoriumsdiagnostik in den Untersuchungsgebieten Molekulare Humangenetik
Leitfaden zur Präanalytik
 Seite 1 von 5 Leitfaden zur Präanalytik Der vorliegende Leitfaden unterstützt unsere Kunden bei der Veranlassung eines Analyseauftrages und ermöglicht optimale Voraussetzungen für eine effektive Zusammenarbeit
Seite 1 von 5 Leitfaden zur Präanalytik Der vorliegende Leitfaden unterstützt unsere Kunden bei der Veranlassung eines Analyseauftrages und ermöglicht optimale Voraussetzungen für eine effektive Zusammenarbeit
Labor für Humangenetische Diagnostik Dr. med. Sabine Hentze * Dr. rer. nat. Anja Louis
 Allgemeine Entnahme-, Versand- und Abrechnungshinweise Probenentnahme/Versand/Abrechnung Telefon: 0621-822742 Telefax: 0621-827483 E-Mail: humangenetik-louis-hentze@t-online.de Gerne beantworten wir Ihre
Allgemeine Entnahme-, Versand- und Abrechnungshinweise Probenentnahme/Versand/Abrechnung Telefon: 0621-822742 Telefax: 0621-827483 E-Mail: humangenetik-louis-hentze@t-online.de Gerne beantworten wir Ihre
Anlage zur Akkreditierungsurkunde D-PL nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18616-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 14.12.2015 bis 26.06.2019 Ausstellungsdatum: 14.12.2015 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18616-01-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 14.12.2015 bis 26.06.2019 Ausstellungsdatum: 14.12.2015 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-20454-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 23.01.2018 bis 22.01.2023 Ausstellungsdatum: 23.01.2018 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-20454-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 23.01.2018 bis 22.01.2023 Ausstellungsdatum: 23.01.2018 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13135-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 08.08.2017 bis 21.08.2019 Ausstellungsdatum: 08.08.2017 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13135-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 08.08.2017 bis 21.08.2019 Ausstellungsdatum: 08.08.2017 Urkundeninhaber:
Qualitätssicherungsvereinbarung Molekulargenetik
 1 Qualitätssicherungsvereinbarung Molekulargenetik Indikationskriterien für ausgewählte molekulargenetische Untersuchungen/ Krankheitsbilder Stand: vom 1. Juli 2015 Gemäß 4 Abs.1 muss der Arzt, der molekulargenetische
1 Qualitätssicherungsvereinbarung Molekulargenetik Indikationskriterien für ausgewählte molekulargenetische Untersuchungen/ Krankheitsbilder Stand: vom 1. Juli 2015 Gemäß 4 Abs.1 muss der Arzt, der molekulargenetische
Hinweise zur Entnahme von Probenmaterial und zum Probenversand
 Hinweise zur Entnahme von Probenmaterial und zum Probenversand Die Humangenetik des MVZ der UMG ist im Bereich der Medizinischen Laboratoriumsdiagnostik in den Untersuchungsgebieten Molekulare Humangenetik
Hinweise zur Entnahme von Probenmaterial und zum Probenversand Die Humangenetik des MVZ der UMG ist im Bereich der Medizinischen Laboratoriumsdiagnostik in den Untersuchungsgebieten Molekulare Humangenetik
Die Deutsche Akkreditierungsstelle. die Kompetenz nach DIN EN ISO 15189:2013 besitzt, Untersuchungen in folgenden Bereichen durchzuführen:
 ----------------------------------------------------------------~------ ~. (~~~~~~erung"telle Deutsche Akkreditierungsstelle GmbH Beliehene gemäß 8 Absatz 1 AkkStelieG i.v.m. 1 Absatz 1 AkkStelleGBV Unterzeichnerin
----------------------------------------------------------------~------ ~. (~~~~~~erung"telle Deutsche Akkreditierungsstelle GmbH Beliehene gemäß 8 Absatz 1 AkkStelieG i.v.m. 1 Absatz 1 AkkStelleGBV Unterzeichnerin
Anlage zur Akkreditierungsurkunde D-ML-13294-03-00 nach DIN EN ISO 15189:2007
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13294-03-00 nach DIN EN ISO 15189:2007 Gültigkeitsdauer: 17.12.2014 bis 19.02.2017 Ausstellungsdatum: 17.12.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13294-03-00 nach DIN EN ISO 15189:2007 Gültigkeitsdauer: 17.12.2014 bis 19.02.2017 Ausstellungsdatum: 17.12.2014 Urkundeninhaber:
Allgemeine Indikationen zur Genetischen Beratung
 ZENTRUM FÜR HUMANGENETIK UND LABORATORIUMSMEDIZIN Dr. Klein und Dr. Rost GENETIK IN DER PÄDIATRIE Beratung und Diagnostik www.medizinische-genetik.de Version 05-07 Genetik in der Kinderheilkunde Bei der
ZENTRUM FÜR HUMANGENETIK UND LABORATORIUMSMEDIZIN Dr. Klein und Dr. Rost GENETIK IN DER PÄDIATRIE Beratung und Diagnostik www.medizinische-genetik.de Version 05-07 Genetik in der Kinderheilkunde Bei der
Hinweise zur Entnahme von Probenmaterial und zum Probenversand
 Hinweise zur Entnahme von Probenmaterial und zum Probenversand Zur besseren Lesbarkeit dieser Hinweise wurde die neutrale Formulierung gewählt, die im Deutschen mit der männlichen identisch ist. Dieses
Hinweise zur Entnahme von Probenmaterial und zum Probenversand Zur besseren Lesbarkeit dieser Hinweise wurde die neutrale Formulierung gewählt, die im Deutschen mit der männlichen identisch ist. Dieses
BLUTPROBEN FÜR DIE MOLEKULARGENETISCHE ANALYSE VON ERBKRANKHEITEN
 Klinik für Dermatologie & Venerologie Zertifiziert nach DIN EN ISO 9001 UNIVERSITÄTSKLINIKUM FREIBURG Klinik für Dermatologie und Venerologie. Hauptstr. 7. 79104 Freiburg Epidermolysis bullosa-zentrum
Klinik für Dermatologie & Venerologie Zertifiziert nach DIN EN ISO 9001 UNIVERSITÄTSKLINIKUM FREIBURG Klinik für Dermatologie und Venerologie. Hauptstr. 7. 79104 Freiburg Epidermolysis bullosa-zentrum
Zur Registrierung der Proben sind folgende Angaben auf dem Auftragsschein wichtig:
 Probentransport Zur Registrierung der Proben sind folgende Angaben auf dem Auftragsschein wichtig: Datum der Probenentnahme Uhrzeit der Probenentnahme Vollständige Patientendaten (Name, Vorname, Geburtsdatum
Probentransport Zur Registrierung der Proben sind folgende Angaben auf dem Auftragsschein wichtig: Datum der Probenentnahme Uhrzeit der Probenentnahme Vollständige Patientendaten (Name, Vorname, Geburtsdatum
Einsendeschein für Zytogenetik / Molekulargenetik
 Ambulanzzentrum des UKSH ggmbh Einsendeschein für Zytogenetik / Molekulargenetik Patient/in Kostenübernahme Name, Vorname: ambulant, Überweisungsschein Muster 10 beigefügt 1 Geburtsdatum: Geschlecht: w
Ambulanzzentrum des UKSH ggmbh Einsendeschein für Zytogenetik / Molekulargenetik Patient/in Kostenübernahme Name, Vorname: ambulant, Überweisungsschein Muster 10 beigefügt 1 Geburtsdatum: Geschlecht: w
Gültig ist nur die Version des Handbuchs im Internet! Alle gedruckten Exemplare sind nur Informationsexemplare und werden nicht aktualisiert!
 Handbuch zur Primärprobenentnahme Institut für Humangenetik Universitätsklinikum der RWTH Aachen Pauwelsstr. 30 52074 Aachen Tel. 0241 80-80178 Fax 0241 80-82580 E-Mail: humangenetik@ukaachen.de www.humangenetik.ukaachen.de
Handbuch zur Primärprobenentnahme Institut für Humangenetik Universitätsklinikum der RWTH Aachen Pauwelsstr. 30 52074 Aachen Tel. 0241 80-80178 Fax 0241 80-82580 E-Mail: humangenetik@ukaachen.de www.humangenetik.ukaachen.de
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13154-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 31.08.2016 bis 07.01.2019 Ausstellungsdatum: 31.08.2016 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13154-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 31.08.2016 bis 07.01.2019 Ausstellungsdatum: 31.08.2016 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13425-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 01.03.2018 bis 28.02.2023 Ausstellungsdatum: 01.03.2018 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13425-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 01.03.2018 bis 28.02.2023 Ausstellungsdatum: 01.03.2018 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13425-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 29.08.2014 bis 13.03.2018 Ausstellungsdatum: 29.08.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13425-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 29.08.2014 bis 13.03.2018 Ausstellungsdatum: 29.08.2014 Urkundeninhaber:
Handbuch zur Probenentnahme
 Seite: 1 / 9 Universitätsklinikum Tübingen Institut für Medizinische Genetik und Angewandte Genomik Ärztlicher Direktor: Prof. Dr. med. Olaf Rieß Kontakt Institut für Medizinische Genetik und Angewandte
Seite: 1 / 9 Universitätsklinikum Tübingen Institut für Medizinische Genetik und Angewandte Genomik Ärztlicher Direktor: Prof. Dr. med. Olaf Rieß Kontakt Institut für Medizinische Genetik und Angewandte
RUHR-UNIVERSITÄT BOCHUM Humangenetik Prof. Dr. med. Jörg Thomas Epplen Universitätsstraße 150, Bochum
 RUHR-UNIVERSITÄT BOCHUM Humangenetik Prof. Dr. med. Jörg Thomas Epplen Universitätsstraße 150, 44801 Bochum Handbuch zur Entnahme von Primärproben der Humangenetik RUB Kontakt Humangenetik Tel.: +49 234
RUHR-UNIVERSITÄT BOCHUM Humangenetik Prof. Dr. med. Jörg Thomas Epplen Universitätsstraße 150, 44801 Bochum Handbuch zur Entnahme von Primärproben der Humangenetik RUB Kontakt Humangenetik Tel.: +49 234
UNIVERSITÄTS-HAUTKLINIK Zertifiziert nach DIN EN ISO 9001:2000
 UNIVERSITÄTSKLINIKUM Universitäts-Hautklinik, Hauptstraße 7, D-79104 Freiburg UNIVERSITÄTS-HAUTKLINIK Zertifiziert nach DIN EN ISO 9001:2000 Ärztliche Direktorin Univ.-Prof. Dr. L. Bruckner-Tuderman Epidermolysis
UNIVERSITÄTSKLINIKUM Universitäts-Hautklinik, Hauptstraße 7, D-79104 Freiburg UNIVERSITÄTS-HAUTKLINIK Zertifiziert nach DIN EN ISO 9001:2000 Ärztliche Direktorin Univ.-Prof. Dr. L. Bruckner-Tuderman Epidermolysis
Praxis für Humangene k Tübingen Dr. med. Dr. rer. nat. Saskia Biskup Fachärz n für Humangene k
 Allgemeine Informationen Fötus von Name Mutter: Vorname Mutter: Geburtsdatum Mutter: Geschlecht des Fötus: q männlich q weiblich q unbekannt Ausschluss MCC bereits erfolgt? Untersuchungsmaterial q Fruchtwasser
Allgemeine Informationen Fötus von Name Mutter: Vorname Mutter: Geburtsdatum Mutter: Geschlecht des Fötus: q männlich q weiblich q unbekannt Ausschluss MCC bereits erfolgt? Untersuchungsmaterial q Fruchtwasser
Parameterkatalog MedGen
 Version 1 GEN HKH DOK Parameterkatalog MedGen *** Freigegeben*** Ersteller Dr. K. Roetzer 17.01.2017 QM Prüfung: Dr. K. Roetzer 17.01.2017 Freigabe: Univ.Prof.Dr. G. Uyanik 17.01.2017 Allgemeine Informationen
Version 1 GEN HKH DOK Parameterkatalog MedGen *** Freigegeben*** Ersteller Dr. K. Roetzer 17.01.2017 QM Prüfung: Dr. K. Roetzer 17.01.2017 Freigabe: Univ.Prof.Dr. G. Uyanik 17.01.2017 Allgemeine Informationen
Anlage zur Akkreditierungsurkunde D-ML-13135-02-00 nach DIN EN ISO 15189:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13135-02-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 22.08.2014 bis 21.08.2019 Ausstellungsdatum: 22.08.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13135-02-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 22.08.2014 bis 21.08.2019 Ausstellungsdatum: 22.08.2014 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13294-03-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 06.06.2018 bis 28.02.2021 Ausstellungsdatum: 06.06.2018 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13294-03-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 06.06.2018 bis 28.02.2021 Ausstellungsdatum: 06.06.2018 Urkundeninhaber:
HANDBUCH ZUR PRIMÄRPROBENENTNAHME. Zentrum Medizinische Genetik Innsbruck (ZMGI) Ärztl. Leiter: Univ.Prof.DDr.med.
 HANDBUCH ZUR PRIMÄRPROBENENTNAHME Zentrum Medizinische Genetik Innsbruck (ZMGI) Ärztl. Leiter: Univ.Prof.DDr.med. Johannes Zschocke Sektion für Humangenetik Medizinische Universität Innsbruck Peter-Mayr-Str.
HANDBUCH ZUR PRIMÄRPROBENENTNAHME Zentrum Medizinische Genetik Innsbruck (ZMGI) Ärztl. Leiter: Univ.Prof.DDr.med. Johannes Zschocke Sektion für Humangenetik Medizinische Universität Innsbruck Peter-Mayr-Str.
STS-Verzeichnis Akkreditierungsnummer: STS 0460
 Internationale Norm: ISO/IEC 17025:2005 & ISO 15189:2012 Schweizer Norm: SN EN ISO/IEC 17025:2005 & SN EN ISO 15189:2013 Institut für Medizinische Genetik der Universität Zürich Wagistrasse 12 CH-8952
Internationale Norm: ISO/IEC 17025:2005 & ISO 15189:2012 Schweizer Norm: SN EN ISO/IEC 17025:2005 & SN EN ISO 15189:2013 Institut für Medizinische Genetik der Universität Zürich Wagistrasse 12 CH-8952
Humangenetik. Dr. Sabine Hentze
 Humangenetik Diagnostik Indikationen Ethische Fragen Dr. Sabine Hentze 1 Genetik ist Medizin Forschung Technologie und Informatik Politik 2 Humangenetik Diagnostik Indikationen Ethische Fragen 3 Diagnostische
Humangenetik Diagnostik Indikationen Ethische Fragen Dr. Sabine Hentze 1 Genetik ist Medizin Forschung Technologie und Informatik Politik 2 Humangenetik Diagnostik Indikationen Ethische Fragen 3 Diagnostische
Merkblatt und Einverständniserklärung zur Fruchtwasserentnahme (Amniozentese)
 11 Abteilung für Geburtshilfe und Pränatale Medizin Universitätsklinikum Bonn Sigmund-Freud-Str. 25 53127 Bonn Prof. Dr. U. Gembruch Geburtshilfe und Pränatale Medizin Zentrum für Geburtshilfe und Frauenheilkunde,
11 Abteilung für Geburtshilfe und Pränatale Medizin Universitätsklinikum Bonn Sigmund-Freud-Str. 25 53127 Bonn Prof. Dr. U. Gembruch Geburtshilfe und Pränatale Medizin Zentrum für Geburtshilfe und Frauenheilkunde,
Vorgeburtliche Untersuchung aus dem Blut der Schwangeren zur Abklärung einer möglichen fetalen Trisomie 21, 18 und 13
 Patientinneninformation zum NIPT ( nicht-invasiver pränataler Test ) Vorgeburtliche Untersuchung aus dem Blut der Schwangeren zur Abklärung einer möglichen fetalen Trisomie 21, 18 und 13 Sehr geehrte Patientin,
Patientinneninformation zum NIPT ( nicht-invasiver pränataler Test ) Vorgeburtliche Untersuchung aus dem Blut der Schwangeren zur Abklärung einer möglichen fetalen Trisomie 21, 18 und 13 Sehr geehrte Patientin,
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-17482-01 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 13.09.2017 bis 12.09.2022 Ausstellungsdatum: 13.09.2017 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-17482-01 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 13.09.2017 bis 12.09.2022 Ausstellungsdatum: 13.09.2017 Urkundeninhaber:
Logbuch für das Praktische Jahr. Institut für Humangenetik Name:
 Logbuch für das Praktische Jahr Institut für Humangenetik Name: Liebe PJ-Studierende, herzlich Willkommen im Institut für Humangenetik des Universitätsklinikums Leipzig AöR. Wir freuen uns sehr, dass Sie
Logbuch für das Praktische Jahr Institut für Humangenetik Name: Liebe PJ-Studierende, herzlich Willkommen im Institut für Humangenetik des Universitätsklinikums Leipzig AöR. Wir freuen uns sehr, dass Sie
11. Gebiet Humangenetik
 Auszug aus der Weiterbildungsordnung der Ärztekammer Niedersachsen und Richtlinien vom 01.05.2005, geändert zum 01.02.2012 (siehe jeweilige Fußnoten) 11. Gebiet Humangenetik Definition: Das Gebiet Humangenetik
Auszug aus der Weiterbildungsordnung der Ärztekammer Niedersachsen und Richtlinien vom 01.05.2005, geändert zum 01.02.2012 (siehe jeweilige Fußnoten) 11. Gebiet Humangenetik Definition: Das Gebiet Humangenetik
Seminar Fetale Nierenerkrankungen. Obstruktive Uropathie Bildgebung und Genetik der zystischen Dysplasie. 1. Juni 2016.
 Seminar 2016 Fetale Nierenerkrankungen Obstruktive Uropathie Bildgebung und Genetik der zystischen Dysplasie 1. Juni 2016 Seminarraum Seminar 2016 Fetale Nierenerkrankungen Obstruktive Uropathie Bildgebung
Seminar 2016 Fetale Nierenerkrankungen Obstruktive Uropathie Bildgebung und Genetik der zystischen Dysplasie 1. Juni 2016 Seminarraum Seminar 2016 Fetale Nierenerkrankungen Obstruktive Uropathie Bildgebung
ZENTRUM MEDIZINISCHE GENETIK INNSBRUCK (ZMGI) Ärztl. Leiter: Univ.Prof.DDr.med. Johannes Zschocke
 DOK Seite 1 von 6 ZENTRUM MEDIZINISCHE GENETIK INNSBRUCK (ZMGI) Ärztl. Leiter: Univ.Prof.DDr.med. Johannes Zschocke Sektion für Humangenetik Universität Innsbruck Peter-Mayr-Str. 1, A 6020 Innsbruck E-Mail:
DOK Seite 1 von 6 ZENTRUM MEDIZINISCHE GENETIK INNSBRUCK (ZMGI) Ärztl. Leiter: Univ.Prof.DDr.med. Johannes Zschocke Sektion für Humangenetik Universität Innsbruck Peter-Mayr-Str. 1, A 6020 Innsbruck E-Mail:
Teil A Rili-BÄK 2008 Vertiefungsmodul. Peter Ackermann, Bio-Rad Laboratories GmbH
 Teil A Rili-BÄK 2008 Vertiefungsmodul Peter Ackermann, Bio-Rad Laboratories GmbH Neue Rili-BÄK Teil A Beschreibt die grundlegenden Anforderungen an die Qualitätssicherung laboratoriumsmedizinischer Untersuchungen
Teil A Rili-BÄK 2008 Vertiefungsmodul Peter Ackermann, Bio-Rad Laboratories GmbH Neue Rili-BÄK Teil A Beschreibt die grundlegenden Anforderungen an die Qualitätssicherung laboratoriumsmedizinischer Untersuchungen
zytogenetische Diagnostik (Chromosomenanalyse) molekularzytogenetische Diagnostik (Fluoreszenz-in-situ-Hybridisierung)
 Kepler Universitätsklinikum Zentrum Medizinische Genetik Linz Präanalytikhandbuch Das Zentrum Medizinische Genetik Linz des Kepler Universitätsklinikums bietet in Zusammenarbeit mit anderen Kooperationspartnern
Kepler Universitätsklinikum Zentrum Medizinische Genetik Linz Präanalytikhandbuch Das Zentrum Medizinische Genetik Linz des Kepler Universitätsklinikums bietet in Zusammenarbeit mit anderen Kooperationspartnern
Akkreditierungsumfang des medizinischen Laboratoriums (EN ISO 15189:2012) Genome Center Graz / (Ident.Nr.: 0304)
 1 AAP 06 2011-12 CFTR-ARMS-aus isolierter DNA 2 AAP 16 2011-11 GAG Chromosomen Zytogenetik aus Vollblut 3 AAP 17 2011-11 GAG Chromosomen Zytogenetik aus Fruchtwasser 4 AAP 18 2011-11 GAG Chromosomen Zytogenetik
1 AAP 06 2011-12 CFTR-ARMS-aus isolierter DNA 2 AAP 16 2011-11 GAG Chromosomen Zytogenetik aus Vollblut 3 AAP 17 2011-11 GAG Chromosomen Zytogenetik aus Fruchtwasser 4 AAP 18 2011-11 GAG Chromosomen Zytogenetik
Abrechnung: BEK gemäß VdEK-Vertrag
 Krankenkasse bzw. Kostenträger Name, Vorname des Versicherten geb. am Institut für Humangenetik Barcode Humangenetik Versichertenstatus: Kassennr. Versichertennr. Status Betriebsstätten-Nr. Arzt-Nr. Datum
Krankenkasse bzw. Kostenträger Name, Vorname des Versicherten geb. am Institut für Humangenetik Barcode Humangenetik Versichertenstatus: Kassennr. Versichertennr. Status Betriebsstätten-Nr. Arzt-Nr. Datum
Anlage zur Akkreditierungsurkunde D-ML-13168-01-00 nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13168-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 10.09.2015 bis 04.03.2019 Ausstellungsdatum: 10.09.2015 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13168-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 10.09.2015 bis 04.03.2019 Ausstellungsdatum: 10.09.2015 Urkundeninhaber:
Screening vs. Testing
 Symposion Winter 2014 Verstehen, was man sieht! Screening vs. Testing Array-CGH und Panel-Diagnostik Syndrom-Diagnostik (Pränatal und beim geborenen Kind) 15. Februar 2014 Vortragssaal in der Frauenklinik
Symposion Winter 2014 Verstehen, was man sieht! Screening vs. Testing Array-CGH und Panel-Diagnostik Syndrom-Diagnostik (Pränatal und beim geborenen Kind) 15. Februar 2014 Vortragssaal in der Frauenklinik
Praxis für Humangene k Tübingen Dr. med. Dr. rer. nat. Saskia Biskup Fachärz n für Humangene k
 Allgemeine Informationen Patient / Ratsuchender Geschlecht: q männlich q weiblich Einsender / Klinik Name, Einrichtung: Straße: PLZ/Stadt: Telefon: Untersuchungsmaterial E-Mail: q Blut ml (mind. 3 ml EDTA-Blut)
Allgemeine Informationen Patient / Ratsuchender Geschlecht: q männlich q weiblich Einsender / Klinik Name, Einrichtung: Straße: PLZ/Stadt: Telefon: Untersuchungsmaterial E-Mail: q Blut ml (mind. 3 ml EDTA-Blut)
HLA- / HPA-Diagnostik: Stand
 HLA- / HPA-Diagnostik: Stand 11.01.2019 HLA-Antikörper-Screening / -Differenzierung Vor und nach Organtransplantation, V.a. Transfusionsreaktion, Refraktärzustand bei Thrombozytentransfusion Lymphozytotoxizitätstest,
HLA- / HPA-Diagnostik: Stand 11.01.2019 HLA-Antikörper-Screening / -Differenzierung Vor und nach Organtransplantation, V.a. Transfusionsreaktion, Refraktärzustand bei Thrombozytentransfusion Lymphozytotoxizitätstest,
Zentrum Medizinische Genetik Medizinisches Versorgungszentrum Venusberg
 Gültig seit: 14.12.2015 Nächste Prüfung: 14.12.2016 Dokumentenart: Mitgeltende Unterlagen HumGen: Handbuch zur Primärprobenentnahme Handbuch zur Primärprobenentnahme Zentrum Medizinische Genetik Medizinisches
Gültig seit: 14.12.2015 Nächste Prüfung: 14.12.2016 Dokumentenart: Mitgeltende Unterlagen HumGen: Handbuch zur Primärprobenentnahme Handbuch zur Primärprobenentnahme Zentrum Medizinische Genetik Medizinisches
BVDH e. V. Koordinationsstelle Qualitätssicherung
 unfällige als unfällig 2022 7 ja nein ja ja nein ja z.b. Hydrolethalus Syndrom ja ja ja ja ja ++: Diagnostik aus fetalen Lymphozyten bei fortgeschrittenem Gestationsalter. 2023 6 ja nein ja ja nein ja
unfällige als unfällig 2022 7 ja nein ja ja nein ja z.b. Hydrolethalus Syndrom ja ja ja ja ja ++: Diagnostik aus fetalen Lymphozyten bei fortgeschrittenem Gestationsalter. 2023 6 ja nein ja ja nein ja
Deutsche Akkreditierungsstelle GmbH. Anlage zur Akkreditierungsurkunde D-ML-13117-01-00 nach DIN EN ISO 15189:2013
 eutsche kkreditierungsstelle GmbH nlage zur kkreditierungsurkunde -ML-13117-01-00 nach IN EN ISO 15189:2013 Gültigkeitsdauer: 24.02.2014 bis 23.02.2019 usstellungsdatum: 24.02.2014 Urkundeninhaber: Praxis
eutsche kkreditierungsstelle GmbH nlage zur kkreditierungsurkunde -ML-13117-01-00 nach IN EN ISO 15189:2013 Gültigkeitsdauer: 24.02.2014 bis 23.02.2019 usstellungsdatum: 24.02.2014 Urkundeninhaber: Praxis
SCQM BIOBANK. Prozessbeschreibung für Spitäler und Praxen. März
 März 16 SCQM BIOBANK Prozessbeschreibung für Spitäler und Praxen SCQM Foundation, Aargauerstrasse 250, 8048 Zuerich, Tel.: +41 (0)43 268 55 77, Fax:+41 (0)43 268 55 79, Email: info@scqm.ch Inhaltsverzeichnis
März 16 SCQM BIOBANK Prozessbeschreibung für Spitäler und Praxen SCQM Foundation, Aargauerstrasse 250, 8048 Zuerich, Tel.: +41 (0)43 268 55 77, Fax:+41 (0)43 268 55 79, Email: info@scqm.ch Inhaltsverzeichnis
Pränatale array-cgh. Abklären und erkennen. Für eine erweiterte pränatale Vorsorge
 Pränatale array-cgh Abklären und erkennen Für eine erweiterte pränatale Vorsorge Untersuchung für Schwangere mit speziellen Risiken Array-CGH: Warum kann sie nötig sein? Chromosomen: Die Träger der Erbinformationen
Pränatale array-cgh Abklären und erkennen Für eine erweiterte pränatale Vorsorge Untersuchung für Schwangere mit speziellen Risiken Array-CGH: Warum kann sie nötig sein? Chromosomen: Die Träger der Erbinformationen
REGISTER ALL-REZ BFM. Übersicht Referenzlabore REGISTER ALL-REZ BFM. 1. Morphologie
 Übersicht Referenzlabore Ansprechpartner Versandadresse 1. Morphologie PD Dr. A. von Stackelberg Tel: (030) 450-666 833 arend.stackelberg@charite.de 2. MRD PCR, Molekulargenetik Biobanking PD Dr. C. Eckert
Übersicht Referenzlabore Ansprechpartner Versandadresse 1. Morphologie PD Dr. A. von Stackelberg Tel: (030) 450-666 833 arend.stackelberg@charite.de 2. MRD PCR, Molekulargenetik Biobanking PD Dr. C. Eckert
Pränatal-Medizin München. Seminar Sonographie Improve your skills. Weiterbildung sonographische Diagnostik im ersten und zweiten Trimenon
 Seminar Sonographie 2015 Improve your skills. Weiterbildung sonographische Diagnostik im ersten und zweiten Trimenon 23. Oktober 2015 Vortragssaal in der Frauenklinik Rotkreuzklinikum München Seminar Sonographie
Seminar Sonographie 2015 Improve your skills. Weiterbildung sonographische Diagnostik im ersten und zweiten Trimenon 23. Oktober 2015 Vortragssaal in der Frauenklinik Rotkreuzklinikum München Seminar Sonographie
Abstrich, Blutkultur und Co. Infektionen richtig abklären
 Abstrich, Blutkultur und Co Infektionen richtig abklären He, Gaston, was brauchst Du zur Untersuchung? Kommt ganz drauf an, was Du wissen willst!!! 3 Fehlerquellen Prae-Analyse Was ist meine Frage? Welche
Abstrich, Blutkultur und Co Infektionen richtig abklären He, Gaston, was brauchst Du zur Untersuchung? Kommt ganz drauf an, was Du wissen willst!!! 3 Fehlerquellen Prae-Analyse Was ist meine Frage? Welche
Kontakt: Molekulargenetik Tel.: 0551 / Fax: 0551 /
 Postadresse und Probenversand: Heinrich-Düker-Weg 12 37073 Göttingen Kontakt: Molekulargenetik Tel.: 0551 / 39-9019 Fax: 0551 / 39-9303 E-Mail: silke.kaulfuss@med.uni-goettingen.de Untersuchungsauftrag
Postadresse und Probenversand: Heinrich-Düker-Weg 12 37073 Göttingen Kontakt: Molekulargenetik Tel.: 0551 / 39-9019 Fax: 0551 / 39-9303 E-Mail: silke.kaulfuss@med.uni-goettingen.de Untersuchungsauftrag
Chorionzottenbiopsie Punktion des Mutterkuchens
 Chorionzottenbiopsie Punktion des Mutterkuchens Sehr geehrte Schwangere, sie haben sich heute in unserer Praxis vorgestellt, um eine Chorionzottenbiopsie durchführen zu lassen. Vor dem Eingriff ist es
Chorionzottenbiopsie Punktion des Mutterkuchens Sehr geehrte Schwangere, sie haben sich heute in unserer Praxis vorgestellt, um eine Chorionzottenbiopsie durchführen zu lassen. Vor dem Eingriff ist es
Einverständniserklärung nach Gendiagnostikgesetz
 Kooperationspartner: Zertifiziert nach: PATIENT/IN (ggf. Aufkleber) Name: Vorname(n): Geburtsdatum: Geschlecht: m Anschrift: w Probegang: Institut für Humangenetik/ MVZ Uniklinik Köln Kerpener Str. 34,
Kooperationspartner: Zertifiziert nach: PATIENT/IN (ggf. Aufkleber) Name: Vorname(n): Geburtsdatum: Geschlecht: m Anschrift: w Probegang: Institut für Humangenetik/ MVZ Uniklinik Köln Kerpener Str. 34,
Humangenetische Untersuchungen in der Pränataldiagnostik
 Humangenetische Untersuchungen in der Pränataldiagnostik 1 Humangenetische Untersuchungen in der Pränataldiagnostik U. Köhler, E. Holinski-Feder Einleitung Eine pränatale genetische Diagnostik beinhaltet
Humangenetische Untersuchungen in der Pränataldiagnostik 1 Humangenetische Untersuchungen in der Pränataldiagnostik U. Köhler, E. Holinski-Feder Einleitung Eine pränatale genetische Diagnostik beinhaltet
Methoden der invasiven Pränataldiagnostik. Methoden zur Beurteilung der fetalen Kondition
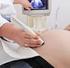 Pränataldiagnostik Nicht-invasive invasive Methoden der Pränataldiagnostik Sonographie-Screening (10., 20., 30. SSW) und weiterführende Sonographie Ersttrimesterscreening Methoden der invasiven Pränataldiagnostik
Pränataldiagnostik Nicht-invasive invasive Methoden der Pränataldiagnostik Sonographie-Screening (10., 20., 30. SSW) und weiterführende Sonographie Ersttrimesterscreening Methoden der invasiven Pränataldiagnostik
REGISTER ALL-REZ BFM. Übersicht Materialversand REGISTER ALL-REZ BFM. Diagnose. Verlaufskontrollen
 Übersicht Materialversand Diagnose 5 ungefärbte KM-Ausstriche (aus der 1. Spritze) 5 ungefärbte Blut-Ausstriche 2 ungefärbte Liquor-Präparate Referenzlabor (Adresse siehe Übersicht Referenzlabore) 1. Morphologie
Übersicht Materialversand Diagnose 5 ungefärbte KM-Ausstriche (aus der 1. Spritze) 5 ungefärbte Blut-Ausstriche 2 ungefärbte Liquor-Präparate Referenzlabor (Adresse siehe Übersicht Referenzlabore) 1. Morphologie
Allgemeine Angaben des Instituts für Humangenetik
 B-34.1 Allgemeine Angaben des Instituts für Humangenetik Fachabteilung: Art: Institut für Humangenetik nicht Betten führend Ärztlicher Direktor: Prof. Dr. med. Christian Kubisch Ansprechpartner: Regina
B-34.1 Allgemeine Angaben des Instituts für Humangenetik Fachabteilung: Art: Institut für Humangenetik nicht Betten führend Ärztlicher Direktor: Prof. Dr. med. Christian Kubisch Ansprechpartner: Regina
Leistungsverzeichnis LV_IMMST
 Seite 1 von 5 1. Klinische Indikation Analyt: Immunstatus (Lymphocytentypisierung) HIV-Infektion: Verlaufsuntersuchung und Therapiesteuerung Erkennung von Vermehrungen oder Verminderungen einzelner Lymphocytensubpopulationen
Seite 1 von 5 1. Klinische Indikation Analyt: Immunstatus (Lymphocytentypisierung) HIV-Infektion: Verlaufsuntersuchung und Therapiesteuerung Erkennung von Vermehrungen oder Verminderungen einzelner Lymphocytensubpopulationen
GENTECHNIKBUCH: 4. KAPITEL
 GENTECHNIKBUCH: 4. KAPITEL CHECKLISTE FÜR KONTROLLEN VON EINRICHTUNGEN, DIE GENETISCHE ANALYSEN ZU MEDIZINISCHEN ZWECKEN GEMÄSS 68 GTG DURCHFÜHREN TEIL 2: ZYTOGENETISCHE UNTERSUCHUNGEN (beschlossen von
GENTECHNIKBUCH: 4. KAPITEL CHECKLISTE FÜR KONTROLLEN VON EINRICHTUNGEN, DIE GENETISCHE ANALYSEN ZU MEDIZINISCHEN ZWECKEN GEMÄSS 68 GTG DURCHFÜHREN TEIL 2: ZYTOGENETISCHE UNTERSUCHUNGEN (beschlossen von
Pränatale genetische Diagnostik
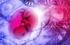 Pränatale genetische Diagnostik Vorgeburtliche Diagnostik Überblick der Testverfahren Die pränatale Diagnostik ermöglicht den Nachweis von genetisch bedingten Erkrankungen und Entwicklungsstörungen vor
Pränatale genetische Diagnostik Vorgeburtliche Diagnostik Überblick der Testverfahren Die pränatale Diagnostik ermöglicht den Nachweis von genetisch bedingten Erkrankungen und Entwicklungsstörungen vor
Anlage zur Akkreditierungsurkunde D-ML-18291-01-00 nach DIN EN ISO 15189:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-18291-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 05.03.2014 bis 04.03.2019 Ausstellungsdatum: 05.03.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-18291-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 05.03.2014 bis 04.03.2019 Ausstellungsdatum: 05.03.2014 Urkundeninhaber:
Untersuchungsverfahren Molekulargenetik
 Untersuchungsverfahren Molekulargenetik Gefäßmalformationen CCM-Gendiagnostik Kavernöse Angiome (CCM) NGS bzw. Sanger-Sequenzierung der Gene CCM1-, CCM2- und CCM3, MLPA Bearbeitungsdauer: Paneldiagnostik
Untersuchungsverfahren Molekulargenetik Gefäßmalformationen CCM-Gendiagnostik Kavernöse Angiome (CCM) NGS bzw. Sanger-Sequenzierung der Gene CCM1-, CCM2- und CCM3, MLPA Bearbeitungsdauer: Paneldiagnostik
ZLG. *.* Checkliste Humangenetik Zytogenetische Untersuchungen. Sektorkomitee Medizinische Laboratorien. K. Miller, H. Rieder
 Sektorkomitee Medizinische Laboratorien ZLG *.* Checkliste Humangenetik Zytogenetische Untersuchungen K. Miller, H. Rieder Anwendungsbereich 3 Personal 3 Räumlichkeiten 4 Geräte und Einrichtungen 4 Reagenzien
Sektorkomitee Medizinische Laboratorien ZLG *.* Checkliste Humangenetik Zytogenetische Untersuchungen K. Miller, H. Rieder Anwendungsbereich 3 Personal 3 Räumlichkeiten 4 Geräte und Einrichtungen 4 Reagenzien
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13314-06-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 08.10.2018 bis 17.05.2020 Ausstellungsdatum: 08.10.2018 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13314-06-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 08.10.2018 bis 17.05.2020 Ausstellungsdatum: 08.10.2018 Urkundeninhaber:
Qualität aus ärztlichen Händen. Nicht invasiver Pränataltest (NIPT) Information für werdende Mütter
 Qualität aus ärztlichen Händen Nicht invasiver Pränataltest (NIPT) Information für werdende Mütter Liebe Schwangere, als werdende Mutter befinden Sie sich wahrscheinlich in einer der emotionalsten Phasen
Qualität aus ärztlichen Händen Nicht invasiver Pränataltest (NIPT) Information für werdende Mütter Liebe Schwangere, als werdende Mutter befinden Sie sich wahrscheinlich in einer der emotionalsten Phasen
Kontakt: Molekulargenetik Tel.: 0551 / Fax: 0551 /
 Postadresse und Probenversand: Heinrich-Düker-Weg 12 37073 Göttingen Kontakt: Molekulargenetik Tel.: 0551 / 39-9019 Fax: 0551 / 39-9303 E-Mail: silke.kaulfuss@med.uni-goettingen.de Untersuchungsauftrag
Postadresse und Probenversand: Heinrich-Düker-Weg 12 37073 Göttingen Kontakt: Molekulargenetik Tel.: 0551 / 39-9019 Fax: 0551 / 39-9303 E-Mail: silke.kaulfuss@med.uni-goettingen.de Untersuchungsauftrag
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13253-07-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 19.03.2018 bis 18.03.2023 Ausstellungsdatum: 19.03.2018 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13253-07-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 19.03.2018 bis 18.03.2023 Ausstellungsdatum: 19.03.2018 Urkundeninhaber:
Vaterschaftstest. Für wen? Warum? Wie? Zweifel ausräumen und Fragen beantworten
 Vaterschaftstest Für wen? Warum? Wie? Zweifel ausräumen und Fragen beantworten Was ist ein Vaterschaftstest und warum kann er nötig sein? Das genetikum: Kompetenter Partner bei allen Abstammungsfragen
Vaterschaftstest Für wen? Warum? Wie? Zweifel ausräumen und Fragen beantworten Was ist ein Vaterschaftstest und warum kann er nötig sein? Das genetikum: Kompetenter Partner bei allen Abstammungsfragen
Leistungsverzeichnis LV_SBGR. Antikörper gegen Systemische Sklerose-assoziierte Antigene (Immunoblot)
 Seite 1 von 5 1. Klinische Indikation Analyt: Antikörper gegen Systemische Sklerose-assoziierte Antigene (Immunoblot) V. a. und Differentialdiagnostik der progressiven Systemsklerose (), begrenzte (limitierte)
Seite 1 von 5 1. Klinische Indikation Analyt: Antikörper gegen Systemische Sklerose-assoziierte Antigene (Immunoblot) V. a. und Differentialdiagnostik der progressiven Systemsklerose (), begrenzte (limitierte)
Patientenaufklärung vor genetischen Analysen gemäß Gendiagnostikgesetz
 Patientenaufklärung vor genetischen Analysen gemäß Gendiagnostikgesetz (Exemplar für den Patienten) Die Deutsche Gesellschaft für Humangenetik (GfH) und der Berufsverband Deutscher Humangenetiker (BVDH)
Patientenaufklärung vor genetischen Analysen gemäß Gendiagnostikgesetz (Exemplar für den Patienten) Die Deutsche Gesellschaft für Humangenetik (GfH) und der Berufsverband Deutscher Humangenetiker (BVDH)
Probenahme. gültig ab: ersetzt: erstellt: überarbeitet: überprüft: am: von: K. Maier/ D. Enderlein L.
 S.0.024.01 Standardarbeitsanweisung Seite 1 von 5 gültig ab: 15.01.2016 ersetzt: genehmigt: M. Lierz erstellt: überarbeitet: überprüft: am: 28.09.2015 13.01.2016 von: K. Maier/ D. Enderlein L. Schmidt
S.0.024.01 Standardarbeitsanweisung Seite 1 von 5 gültig ab: 15.01.2016 ersetzt: genehmigt: M. Lierz erstellt: überarbeitet: überprüft: am: 28.09.2015 13.01.2016 von: K. Maier/ D. Enderlein L. Schmidt
Einverständniserklärung nach Gendiagnostikgesetz
 Kooperationspartner: Zertifiziert nach: PATIENT/IN (ggf. Aufkleber) Name: Vorname(n): Geburtsdatum: Geschlecht: m Anschrift: w Probeneingang: Institut für Humangenetik/ MVZ Uniklinik Köln Kerpener Str.
Kooperationspartner: Zertifiziert nach: PATIENT/IN (ggf. Aufkleber) Name: Vorname(n): Geburtsdatum: Geschlecht: m Anschrift: w Probeneingang: Institut für Humangenetik/ MVZ Uniklinik Köln Kerpener Str.
Handbuch zur Primärprobenentnahme
 Prüfungs- und Freigabeprotokoll Name: Erstellt am: Unterschrift: Verfasser: S. Bens 10.09.2018 H. 13.09.2018 GEPRÜFT VON: M. Hillmer 14.09.2018 QMB: M. Miersch 14.09.2018 Leitung zur Freigabe: R. Siebert
Prüfungs- und Freigabeprotokoll Name: Erstellt am: Unterschrift: Verfasser: S. Bens 10.09.2018 H. 13.09.2018 GEPRÜFT VON: M. Hillmer 14.09.2018 QMB: M. Miersch 14.09.2018 Leitung zur Freigabe: R. Siebert
Leistungsverzeichnis LV_MBGR. Dermatomyositis (hochspezifisch, 15 30%) Idiopathische Myositis 88 12%) Polymyositis Mi-2beta
 Seite 1 von 5 1. Klinische Indikation Analyt: Dermato- und Polymyositis Idiopathische Myositis Anti-Synthetase-Syndrom Überlappungssyndrome Klinische Bedeutung: Antigen: Myositis-Antikörper (Immunoblot)
Seite 1 von 5 1. Klinische Indikation Analyt: Dermato- und Polymyositis Idiopathische Myositis Anti-Synthetase-Syndrom Überlappungssyndrome Klinische Bedeutung: Antigen: Myositis-Antikörper (Immunoblot)
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 ~ (~~~!~~ecung,,telle Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-19730-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 10.09.2015 bis 08.09.2020 Ausstellungsdatum: 10.09.2015
~ (~~~!~~ecung,,telle Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-19730-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 10.09.2015 bis 08.09.2020 Ausstellungsdatum: 10.09.2015
