Faltung, Dynamik und strukturelle Evolution der Proteine (Voet Kapitel 8)
|
|
|
- Annegret Kohler
- vor 7 Jahren
- Abrufe
Transkript
1 Faltung, Dynamik und strukturelle Evolution der Proteine (Voet Kapitel 8) 1. Proteinfaltung: Theorie und Experiment 2. Proteindynamik 3. Strukturelle Evolution
2
3 A. Protein-Renaturierung Denaturierung in 8M Harnstoff Dialyse und stehenlassen an Luft 100% aktives Enzym keine zufällige Renaturierung Wahrscheinlichkeit für korrekte Faltung bei Gleichwertigkeit aller SH: 1/7 x 1/5 x 1/3 x 1/1 = 1/105 native Konformation thermodynamisch günstig sein. Reduktive Denaturierung und oxidative Renaturierung der RNAse A
4 Enzymatische Renaturierung von Disulfid-Brücken Protein-Disulfid-Isomerase (PDI) kontinuierliches Öffnen der S-S Brücken. Thermodynamisch günstigste Proteinkonformation bestimmt die bevorzugten S-S Brücken.
5 Posttranslationell modifizierte Proteine können sich einer spontanen Renaturierung widersetzen Primärstruktur von Proinsulin Insulin wird aus einer AS-Kette gebildet, dem Proinsulin. Spezifische proteolytische Reaktion führt zur Abspaltung eines internen Peptides (C chain) zwei kettiges Insulin kann nicht mehr spontan ursprüngliche Konformation einnehmen und andere S-S Brücken ausbilden
6 Proteinfaltung wird hauptsächlich durch innere Reste gesteuert Modifikation von AS an Proteinoberfläche verändern die native Konformation kaum Mutationen von Oberflächenresten verändern native Konformationkaum AS an Oberfläche evolutionär weniger stark konserviert als innere Reste (hydrophobe Reste) Denaturierende Agenzien interagieren mit hydrophoben inneren Resten Die Proteinfaltung ist ein von hydrophoben Kräften getriebener Prozess
7 B. Faltungsabläufe Es werden nicht alle möglichen Konformationen ausprobiert (bräuchte Mia von Jahren) Faltung mehrstufiger, kooperativer Prozess. 1. zufällige Bildung kurzer Abschnitte von Sekundärstrukturen (α Helices, β Faltblätter) Nuclei für weitere Faltung 2. Nuclei wachsen in kooperativer Weise. Helices und Faltblätter gruppieren sich. 3. in Multidomänenprot. kommen Domänen zusammen. Molten Globule Hydrophobe Seitenketten sind noch dem Lsm ausgesetzt. 4. Kompaktere Tertiärstruktur bildet sich aus kleine konformationelle Anpassungen. 5. Untereineheiten kommen zusammen 6. konformationlelle Anpassungen führen zu nativer Konformation. Hypothethscher Faltungsablauf einer dimeren Proteins.
8 BPTI faltet sich in geordneter Abfolge in seine native Konformation BPTI = Basic Pancreatic Trypsin Inhibitor Inaktiviert Trypsin im Pankreas, welcher Trypsin sezerniert. Dadurch wird dieser vor Selbstzerstörung geschützt. 3 Disulfid-Brücken Natives BPTI
9 BPTI wählt eine begrenzte Anzahl Faltungswege 30% 70 %
10 C. Faltungs Hilfsproteine Hilfsproteine die Faltung von Proteinen erleichtern während sie synthetisiert werden = Beschleunigung der Faltung 1. Protein Disulfid Isomerasen (PDI) 2. Peptidyl prolyl cis-trans isomerasen 3. Chaperone PDI (siehe vorher) beschleunigt korrekte S-S Brückenbildung durch shuffling von Disulfidbrücken. Ähnliches Enzym in Bacterien = DsbA Protein mit Ähnlichkeit zu thioredoxin. Schwefel Atom 90 gedreht negativ geladene Gruppen positiv geladene Gruppen exponiertes Schwefelatom Molekulare Oberfläche und Ladungsverteilung
11 Peptidyl prolyl cis-trans isomerasen (PPI) In globulären Proteinen Xaa-Pro Peptid Bindungen in trans Konformation, aber 10% in cis Konformation. Cis Konformation wird durch PPI (auch Rotamase genannt) begünstigt 2 Familien von PPI s (Immunophiline): cyclophiline FK506 binding protein (FKBP) Diese Proteine haben auch immunsupressive Eigenschaften, die jedoch nichts mit ihren enzymatischen Aktivitäten als Rotamasen zu tun haben.
12 Molekulare Chaperons verhindern falsche Faltung und Agregation von Proteinen Hydrophobe Regionen haben Tendenz zu agregieren. Solche Agregate können siche in einem Peptidstrang selber bilden oder zwischen Peptidsträngen. Molekulare Chaperone verhindern eine solche ungünstigen Assoziationen und kehren sie um. Chaperone binden an hydrophobe Regionen die Lösungsmittel exponiert sind und verhindern so ungewollte Agregationen. Der genaue Mechanismus ist unbekannt jedoch haben viele Chaperone ATPase Aktivität. ATP hydrolyse scheint die Energie für die Funktion der Chaperone zu liefern. Peptid wird in gestreckter Konformation gehalten Verankerung des C-Terms an Chaperon Boomerang Gestalt von PapD E. coli PapD ein molekulares Chaperon das die korrekte Faltung von Pili fördert.
13 Verschiedene Klassen von Chaperons 1. Heat shock protein 70 (Hsp70) so benannt da Synthese dieser Proteine erhöht bei angehobener Temperatur. Sie kehren Denaturierung und Agregation in Prokaryoten als auch in Eukaryoten um. 2. Chaperonine (Hsp60, Hsp10) Multisubunit, käfigähnliche Moleküle Erhöhen nicht die Rate der Proteinfaltung sondern erhöhen die Ausbeute an richtig gefalteten Proteinen 3. Nucleoplasmine steuern in vivo die Zusammensetzung von der Nucleosomen Hsp60 Molekül von Rhodobacter spheroides ist aus 14 identischen Untereinheiten.
14 hydrophobische Bindungsstellen Reaktionszyklus der E. coli chaperonine GroEL (Hsp60) und GroES (Hsp10) ATP-abhängige Freisetzung von ungefalteten Proteinen von den Bindungstellen im GroEL chaperon.
15 Nucleoplasmine Nucleosomen werden durch Nucleoplasmine aus den Histoneinheiten zusammengefügt. An Nucleosomen ist die DNA aufgewickelt und stellt eine sehr kompakte Form der Verpackung dar.
16 C. Vorhersage der Proteinstruktur Primärstruktur bestimmt Faltung. Theoretisch Berechungen möglich um Struktur zu bestimmen, praktisch aber kaum durchführbar Empirische Methoden 1. Chou-Fasman-Schema Frequenz f = Frequenz mit der ein bestimmter Rest in einer α-helix auftritt f = n n n = Anzahl AS eines Typs in α-helix n = Gesamtzahl der AS dieses Typs im Protein Tendenz P einer bestimmten AS in einer α-helix aufzutreten P = f f f = Durchschnittswert von f für alle 20 AS P > 1 heisst AS mit grösserer als durchschnittlicher Wahrscheinlichkeit in α-helix Tendenz P einer bestimmten AS in einem β-faltblatt aufzutreten analog definiert.
17 Empirische Regeln zu Chou-Fasman-Schema: 1. Vier Helix bildende Reste in sechs aufeinanderfolgenden Resten dienen als Helixnucleus. Helixsegment pflanzt sich in beide Richtungen fort bis der durchschnittliche Wert von P < 1 ist. Ein Pro-Rest nur am N-Term einer Helix. 2. Drei β Faltblatt bildenden Reste in fünf aufeinanderfolgenden Resten starten ein β Faltblatt. Pflanzt sich in beide Richtungen fort bis P < Wenn α und β bildende Sequenzen überlappen gilt Überlappungsregion als helical wenn P > P α-helix P > P β Faltblatt Zuverlässigkeit ist bis zu 80 % 2. Regel von Rose Umkehrschleifen sind durch ein Hydrophobizitäts-Minimum entlang der Polypeptidkette charakterisiert. Dies gilt nur wenn die Region nicht gleichzeitig ein helicaler Abschnitt darstellt.
18 Vorhersage von α-helices, β Faltblatt Strukturen und β Schleifen
19 Faltung, Dynamik und strukturelle Evolution der Proteine (Voet Kapitel 8) 1. Proteinfaltung: Theorie und Experiment 2. Proteindynamik 3. Strukturelle Evolution
20 2. Proteindynamik - Röntgenstruktur liefert zeitlich gemittelte Schnappschüsse der Proetinstruktur - Proteine sind aber flexibel fluktuierende Moleküle, deren strukturelle Mobilität eine funktionelle Signifikanz hat. 3 Arten von Atmungsbewegungen : 1. atomare Fluktuationen: vibrationen von individuellen Bindungen pm 2. kollektive Bewegungen: Gruppen von kovalent verknüpften Atomen bewegen sich pm 3. induzierte Konformationsveränderungen: Atomgruppen und ganze Untereinheiten können können sich nach Stimulus (z.b. O2 an Hämoglobin) bewegen pm
21 O2 Molekül Häm Gruppe Darstellung der atmenden Bewegungen im Myoglobin, die das Austreten eines gebundenen O2 Moleküls zulassen
22 Proteine haben mobile Strukturen His-Rest Häm Seitenketten H-Brücken Mehrere Schnappschüsse von Myoglobin überlagert α Helix
23 Faltung, Dynamik und strukturelle Evolution der Proteine (Voet Kapitel 8) 1. Proteinfaltung: Theorie und Experiment 2. Proteindynamik 3. Strukturelle Evolution
24 3. Strukturelle Evolution Hydrophobe Kräfte sehr wichtig für Faltung. Innere AS können nur konservativ substituiert werden damit Struktur erhalten bleibt. Konservierung der Proteinstruktur wichtig, nicht Aminosäuresequenz. A. Struktur des Cytochroms c Häm Nische wichtig. AS die Häm fixieren sind evolutionär konserviert strukturell wichtige AS Häm
25 Primärstruktur verschiedener Cytochrome c Aminosäuresequenz nicht sehr konserviert. Strukturelemete aber sehr. Kritische Aminosäuren sind konwerviert
26 Dreidimensionale Struktur von Cytochromen c Struktur ist sehr konserviert im Gegensatz zur Primärstruktur
27 B. Gen-Duplikation strukturell ähnliche Domänen von Rhodanase In Multidomän Proteinen können Domänen ähnlich sein. Konvergente Evolution ist unwahrscheinlich, Gen-Duplikation und dievergente Evolution eher wahrscheinlich Redox- Enzyme (Dehydrogenasen) aus 2 verschiednen Domänen: Coenzym bindende Domäne und Substrat bindende Domäne Funktion aus 2 Einheiten Genetische Kombination neue Funktion
2. Tertiärstruktur. Lernziele: 1) Verstehen wie Röntgenstrukturanalyse und NMR Spektroskopie gebraucht werden um Proteinstrukturen zu bestimmen.
 2. Tertiärstruktur Lernziele: 1) Verstehen wie Röntgenstrukturanalyse und NMR Spektroskopie gebraucht werden um Proteinstrukturen zu bestimmen. 2) Verstehen warum nicht polare Reste im inneren eines Proteins
2. Tertiärstruktur Lernziele: 1) Verstehen wie Röntgenstrukturanalyse und NMR Spektroskopie gebraucht werden um Proteinstrukturen zu bestimmen. 2) Verstehen warum nicht polare Reste im inneren eines Proteins
Aminosäuren. Seitenkette. -Kohlenstoffatom. Karboxilgruppe. Aminogruppe
 Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine Bildung der Disulfidbrücke
Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine Bildung der Disulfidbrücke
Aminosäuren. Seitenkette. -Kohlenstoffatom. Karboxilgruppe. Aminogruppe
 Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine 18 Primär Struktur Aminosäuer
Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine 18 Primär Struktur Aminosäuer
3. Quartärstruktur und Symmetrie. Lernziel:
 3. Quartärstruktur und Symmetrie Lernziel: 1) Verstehen dass einige Proteine mehrere Untereinheiten haben können, welche normalerweise symmetrisch angeordnet sind. U.Albrecht BC1 Polypeptid-Untereinheiten
3. Quartärstruktur und Symmetrie Lernziel: 1) Verstehen dass einige Proteine mehrere Untereinheiten haben können, welche normalerweise symmetrisch angeordnet sind. U.Albrecht BC1 Polypeptid-Untereinheiten
1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur
 Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur - Eigenschaften eines Proteins werden durch
Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur - Eigenschaften eines Proteins werden durch
8. ZUSAMMENFASSUNG DER FORSCHUNGSERGEBNISSE ZUR APIKALEN DOMÄNE VON GROEL
 8. ZUSAMMENFASSUNG DER FORSCHUNGSERGEBNISSE ZUR APIKALEN DOMÄNE VON GROEL 8.1. Thermodynamische Stabilität und Faltung von Fragmenten des Chaperonins GroEL (apikale Domäne, Minichaperone) Durch limitierte
8. ZUSAMMENFASSUNG DER FORSCHUNGSERGEBNISSE ZUR APIKALEN DOMÄNE VON GROEL 8.1. Thermodynamische Stabilität und Faltung von Fragmenten des Chaperonins GroEL (apikale Domäne, Minichaperone) Durch limitierte
Aufgabe 5 (Supersekundärstruktur)
 Aufgabe 5 (Supersekundärstruktur) Fragestellung Bei der Untereinheit des Arthropodenhämocyanins aus Limulus polyphemus werden folgende Fragestellungen untersucht: - Welche Supersekundärstrukturen gibt
Aufgabe 5 (Supersekundärstruktur) Fragestellung Bei der Untereinheit des Arthropodenhämocyanins aus Limulus polyphemus werden folgende Fragestellungen untersucht: - Welche Supersekundärstrukturen gibt
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion. Mag. Gerald Trutschl
 Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Hemmung der Enzym-Aktivität
 Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Aufbau und Konformation von Polypeptiden
 1 Aufbau und Konformation von Polypeptiden Peter Güntert, Sommersemester 2009 Hierarchie von Proteinstrukturen Primärstruktur: Aminosäuresequenz Sekundärstruktur: Helices, Faltblätter, Turns, Loops Tertiärstruktur:
1 Aufbau und Konformation von Polypeptiden Peter Güntert, Sommersemester 2009 Hierarchie von Proteinstrukturen Primärstruktur: Aminosäuresequenz Sekundärstruktur: Helices, Faltblätter, Turns, Loops Tertiärstruktur:
1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur
 Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 4. Protein-Stabilisierung Proteine sind
Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 4. Protein-Stabilisierung Proteine sind
3. Strukturen und Faltung von Proteinen
 3. Strukturen und Faltung von Proteinen 71 3.1. Vokabular Primary structure (AA Sequenz) Proteinfaltung Supramolekulare Assemblierung 72 73 Proteinkonformation: Anordnung aller Atome im Raum (3D Struktur)
3. Strukturen und Faltung von Proteinen 71 3.1. Vokabular Primary structure (AA Sequenz) Proteinfaltung Supramolekulare Assemblierung 72 73 Proteinkonformation: Anordnung aller Atome im Raum (3D Struktur)
β-blatt Proteine Wintersemester 2011/12 Peter Güntert 3 Hauptklassen von Proteinstrukturen
 β-blatt Proteine Wintersemester 2011/12 Peter Güntert 3 Hauptklassen von Proteinstrukturen Die meisten Proteinstrukturen (genauer: Domänenstrukturen) fallen in eine von drei Klassen: α-domänen: Der Kern
β-blatt Proteine Wintersemester 2011/12 Peter Güntert 3 Hauptklassen von Proteinstrukturen Die meisten Proteinstrukturen (genauer: Domänenstrukturen) fallen in eine von drei Klassen: α-domänen: Der Kern
und Reinstruktur Die Sekundärstruktur ist die Anordnung der Aminosäurenkette, wobei man in zwei Arten unterscheidet: o Faltblatt- oder β- Struktur
 Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
Falschfaltung von Proteinen
 Falschfaltung von Proteinen - Aggregation - domain swapping - amyloidogene Strukturen Was determiniert die Faltung von Proteinen? Einfachstes System: Zwei-Zustandsmodell N U Energie U dg ÜS dg* N Molekulare
Falschfaltung von Proteinen - Aggregation - domain swapping - amyloidogene Strukturen Was determiniert die Faltung von Proteinen? Einfachstes System: Zwei-Zustandsmodell N U Energie U dg ÜS dg* N Molekulare
Posttranskriptionale RNA-Prozessierung
 Posttranskriptionale RNA-Prozessierung Spaltung + Modifikation G Q Spleissen + Editing U UUU Prozessierung einer prä-trna Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende
Posttranskriptionale RNA-Prozessierung Spaltung + Modifikation G Q Spleissen + Editing U UUU Prozessierung einer prä-trna Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende
Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen. Abb. aus Stryer (5th Ed.)
 Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen Die verschiedenen Ribosomen-Komplexe können im Elektronenmikroskop beobachtet werden Durch Röntgenkristallographie wurden
Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen Die verschiedenen Ribosomen-Komplexe können im Elektronenmikroskop beobachtet werden Durch Röntgenkristallographie wurden
Proteine. Claudia Schierbaum WS 04/05 Löffler / Petrides: Biochemie & Pathobiochemie, 7.Auflage, Springer-Verlag Berlin Kapitel 3.4 und 3.
 Proteine Claudia Schierbaum WS 04/05 Löffler / Petrides: Biochemie & Pathobiochemie, 7.Auflage, Springer-Verlag Berlin Kapitel 3.4 und 3.5 Faltung, Fehlfaltung und Denaturierung von Proteinen Denaturierung
Proteine Claudia Schierbaum WS 04/05 Löffler / Petrides: Biochemie & Pathobiochemie, 7.Auflage, Springer-Verlag Berlin Kapitel 3.4 und 3.5 Faltung, Fehlfaltung und Denaturierung von Proteinen Denaturierung
Zusammensetzung und Struktur der Proteine. Stryer (6. Auflage) Kapitel 2
 Zusammensetzung und Struktur der Proteine Stryer (6. Auflage) Kapitel 2 Vielfalt der Proteine Wie kommt diese Vielfalt an Proteinen zustande? 1. Peptide und Polypeptide sind Ketten aus 20 verschiedenen
Zusammensetzung und Struktur der Proteine Stryer (6. Auflage) Kapitel 2 Vielfalt der Proteine Wie kommt diese Vielfalt an Proteinen zustande? 1. Peptide und Polypeptide sind Ketten aus 20 verschiedenen
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Intensivkurs Biologie
 Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
Eukaryotische messenger-rna
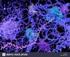 Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende u.u. nicht-codierende Bereiche (Introns) Spleißen von prä-mrna Viele Protein-codierende Gene in Eukaryoten sind durch nicht-codierende
Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende u.u. nicht-codierende Bereiche (Introns) Spleißen von prä-mrna Viele Protein-codierende Gene in Eukaryoten sind durch nicht-codierende
UAufgabe 12: (evolutiv konservierte Aminosäuren)
 UAufgabe 12: (evolutiv konservierte Aminosäuren) Aufgabenstellung Wählen Sie zur Darstellung evolutiv konservierter Aminosäure-Positionen in "1lla" eine ihnen sinnvoll erscheinende Anfärbung. Exportieren
UAufgabe 12: (evolutiv konservierte Aminosäuren) Aufgabenstellung Wählen Sie zur Darstellung evolutiv konservierter Aminosäure-Positionen in "1lla" eine ihnen sinnvoll erscheinende Anfärbung. Exportieren
0.1 Eiweißstoffe (Proteine)
 1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Praktikum Biochemie B.Sc. Water Science WS Enzymregulation. Marinja Niggemann, Denise Schäfer
 Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Proteinstrukturklassen α-helikale Proteine
 Proteinstrukturklassen α-helikale Proteine Wintersemester 2011/12 Peter Güntert Domäne Modul Faltung Domäne (domain): Polypeptidkette (oder Teil davon), die unabhängig in eine stabile, kompakte Tertiärstruktur
Proteinstrukturklassen α-helikale Proteine Wintersemester 2011/12 Peter Güntert Domäne Modul Faltung Domäne (domain): Polypeptidkette (oder Teil davon), die unabhängig in eine stabile, kompakte Tertiärstruktur
Tyrosinkinase- Rezeptoren
 Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine
 Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka Übungen zur Vorlesung Aminosäuren, Peptide, Proteine Dr. Katja
Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka Übungen zur Vorlesung Aminosäuren, Peptide, Proteine Dr. Katja
1. Peptide und Proteine
 1. Peptide und Proteine 1.1 Einleitung Peptide und Proteine sind ubiquitär in allen Organismen vorhanden. Sie sind die Moleküle des Lebens. Sie sind die Funktionsreagenzien in den Zellen und verantwortlich
1. Peptide und Proteine 1.1 Einleitung Peptide und Proteine sind ubiquitär in allen Organismen vorhanden. Sie sind die Moleküle des Lebens. Sie sind die Funktionsreagenzien in den Zellen und verantwortlich
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Funktion von Proteinen:
 Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Vertiefendes Seminar zur Vorlesung Biochemie
 Vertiefendes Seminar zur Vorlesung Biochemie 07.11.2014 Proteine: Faltung Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Vertiefendes Seminar zur Vorlesung Biochemie 07.11.2014 Proteine: Faltung Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Translation benötigt trnas und Ribosomen. Genetischer Code. Initiation Elongation Termination
 8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation Elongation Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse huma n bacter
8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation Elongation Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse huma n bacter
Wege des Proteintransports, Proteinsortierung
 Wege des Proteintransports, Proteinsortierung 3 Möglichkeiten: Gated Transport Transmembran transport Vesikeltransport Figure 15-5 Essential Cell Biology ( Garland Science 2010) Weitere Funktionen des
Wege des Proteintransports, Proteinsortierung 3 Möglichkeiten: Gated Transport Transmembran transport Vesikeltransport Figure 15-5 Essential Cell Biology ( Garland Science 2010) Weitere Funktionen des
Protein-Protein Bindungsstellen. Lennart Heinzerling
 Protein-Protein Bindungsstellen Lennart Heinzerling 1 Worum geht es in den nächsten 45 Minuten? Auffinden von Protein- Protein Komplexen aus einer großen Menge potentieller Komplexe z.b. für -Interaction
Protein-Protein Bindungsstellen Lennart Heinzerling 1 Worum geht es in den nächsten 45 Minuten? Auffinden von Protein- Protein Komplexen aus einer großen Menge potentieller Komplexe z.b. für -Interaction
Hemmung der Enzym-Aktivität
 Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
U. Helmich, Intensivkurs "Proteine" Seite 1
 U. Helmich, Intensivkurs "Proteine" Seite 1 Crashkurs "Proteine" Proteine bestehen aus Aminosäuren, von denen es rund 20 verschiedene gibt. Die meisten Proteine bestehen mehreren hundert oder sogar mehreren
U. Helmich, Intensivkurs "Proteine" Seite 1 Crashkurs "Proteine" Proteine bestehen aus Aminosäuren, von denen es rund 20 verschiedene gibt. Die meisten Proteine bestehen mehreren hundert oder sogar mehreren
Proteinsortierungswege in der Zelle
 5.4 Proteinsortierung Die Proteinbiosynthese findet im eukaryontischen Cytosol statt. Dabei können die Ribosomen entweder frei vorliegen oder an das endoplasmatische Retikulum (ER) gebunden sein. Proteine,
5.4 Proteinsortierung Die Proteinbiosynthese findet im eukaryontischen Cytosol statt. Dabei können die Ribosomen entweder frei vorliegen oder an das endoplasmatische Retikulum (ER) gebunden sein. Proteine,
Übungsaufgaben. Aufbau und Konformation von Polypeptiden. Einführung in die räumliche Struktur von Proteinen
 Computergestützte Strukturbiologie (Strukturelle Bioinformatik) SS09 P. Güntert Übungsaufgaben Aufbau und Konformation von Polypeptiden 1. Warum haben Proteine im Unterschied zu DNA komplizierte und vielfältige
Computergestützte Strukturbiologie (Strukturelle Bioinformatik) SS09 P. Güntert Übungsaufgaben Aufbau und Konformation von Polypeptiden 1. Warum haben Proteine im Unterschied zu DNA komplizierte und vielfältige
- Biochemieklausur Name: Matrikelnr.:
 07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016
 Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 4 (20.06. 24.06.) Regulation der Transkription II, Translation
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 4 (20.06. 24.06.) Regulation der Transkription II, Translation
Bioorganische Chemie Enzymatische Katalyse 2011
 Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Einführung in die räumliche Struktur von Proteinen
 1 Einführung in die räumliche Struktur von Proteinen Peter Güntert, Sommersemeter 2009 Literatur C. Branden & J. Tooze, Introduction to Protein Structure, Garland, 2 1999. T. E. Creighton, Proteins, Structures
1 Einführung in die räumliche Struktur von Proteinen Peter Güntert, Sommersemeter 2009 Literatur C. Branden & J. Tooze, Introduction to Protein Structure, Garland, 2 1999. T. E. Creighton, Proteins, Structures
Translation benötigt trnas und Ribosomen. Genetischer Code. Initiation Elongation Termination
 8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation Elongation Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse huma n bacter
8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation Elongation Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse huma n bacter
MM Proteinmodelling. Michael Meyer. Vorlesung XVII
 Proteinmodelling Vorlesung XVII Proteinstrukturen Es besteht ein sehr großer Bedarf an Proteinstrukturen: Die Kenntnis der 3D-Struktur hat große Vorteile für das Design neuer Wirkstoffe. Experimentelle
Proteinmodelling Vorlesung XVII Proteinstrukturen Es besteht ein sehr großer Bedarf an Proteinstrukturen: Die Kenntnis der 3D-Struktur hat große Vorteile für das Design neuer Wirkstoffe. Experimentelle
Proteine: Dreidimensionale Struktur
 Proteine: Dreidimensionale Struktur 1. Sekundärstruktur A. Die Peptidgruppe B. Reguläre Sekundärstrukktur: α-helix und β-faltblatt C. Faserproteine D. Nichtrepetitive Proteinstruktur 2. Tertiärstruktur
Proteine: Dreidimensionale Struktur 1. Sekundärstruktur A. Die Peptidgruppe B. Reguläre Sekundärstrukktur: α-helix und β-faltblatt C. Faserproteine D. Nichtrepetitive Proteinstruktur 2. Tertiärstruktur
Kapitel II Elemente, kleine Moleküle, Makromoleküle Wiederholung
 Kapitel II Elemente, kleine Moleküle, Makromoleküle Wiederholung Biologie für Physikerinnen und Physiker Kapitel II Elemente, Moleküle, Makromoleküle 1 Anteil der Elemente die im menschlichen Körper und
Kapitel II Elemente, kleine Moleküle, Makromoleküle Wiederholung Biologie für Physikerinnen und Physiker Kapitel II Elemente, Moleküle, Makromoleküle 1 Anteil der Elemente die im menschlichen Körper und
Proteinchemische Charakterisierung und Rontgenstrukturanalyse der Glucose-Oxidase aus Penicillium amaaasakiense
 Proteinchemische Charakterisierung und Rontgenstrukturanalyse der Glucose-Oxidase aus Penicillium amaaasakiense Von der Naturwissenschaftlichen Fakultät der Technischen Universität Carolo-Wilhelmina zu
Proteinchemische Charakterisierung und Rontgenstrukturanalyse der Glucose-Oxidase aus Penicillium amaaasakiense Von der Naturwissenschaftlichen Fakultät der Technischen Universität Carolo-Wilhelmina zu
Aufbau, Struktur, Funktion von DNA, RNA und Proteinen
 Aufbau, Struktur, Funktion von DNA, RNA und Proteinen Mitarbeiterseminar der Medizinischen Fakultät Ruhr-Universität Bochum Andreas Friebe Abteilung für Pharmakologie und Toxikologie Aufbau, Struktur,
Aufbau, Struktur, Funktion von DNA, RNA und Proteinen Mitarbeiterseminar der Medizinischen Fakultät Ruhr-Universität Bochum Andreas Friebe Abteilung für Pharmakologie und Toxikologie Aufbau, Struktur,
Vertiefendes Seminar zur Vorlesung Biochemie I Bearbeitung Übungsblatt 4
 Vertiefendes Seminar zur Vorlesung Biochemie I 20.11.2015 Bearbeitung Übungsblatt 4 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Vertiefendes Seminar zur Vorlesung Biochemie I 20.11.2015 Bearbeitung Übungsblatt 4 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
16. Biomoleküle : Nucleinsäuren
 Inhalt Index 16. Biomoleküle : Nucleinsäuren Die gesamte Erbinformation ist in den Desoxyribonucleinsäuren (DNA) enthalten. Die Übersetzung dieser Information in die Synthese der Proteine wird von den
Inhalt Index 16. Biomoleküle : Nucleinsäuren Die gesamte Erbinformation ist in den Desoxyribonucleinsäuren (DNA) enthalten. Die Übersetzung dieser Information in die Synthese der Proteine wird von den
Aufgabe 6 (Quartärstruktur)
 Aufgabe 6 (Quartärstruktur) Fragestellung Folgende Fragestellungen sollen beim Hämocyanin-Hexamer von Limulus polyphemus (1lla_Hexamer.pdb) untersucht werden: - Welche Symmetrien sind erkennbar? - Wenn
Aufgabe 6 (Quartärstruktur) Fragestellung Folgende Fragestellungen sollen beim Hämocyanin-Hexamer von Limulus polyphemus (1lla_Hexamer.pdb) untersucht werden: - Welche Symmetrien sind erkennbar? - Wenn
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Charakterisierung von Einzelbindungs-Konformationsänderungen in Polypeptiden durch chemische Modifikation und Enzymkatalyse. 1.
 harakterisierung von Einzelbindungs-Konformationsänderungen in Polypeptiden durch chemische Modifikation und Enzymkatalyse 1. Einleitung Peptide sind u. a. in Form von ormonen, Transmittern und Modulatoren
harakterisierung von Einzelbindungs-Konformationsänderungen in Polypeptiden durch chemische Modifikation und Enzymkatalyse 1. Einleitung Peptide sind u. a. in Form von ormonen, Transmittern und Modulatoren
Mechanismus der Enzymkatalyse
 Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine
 4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
BIOCHEMIE. Teil 2: Aminosäuren, Proteine, Enzyme. Urheberrechtlich geschütztes Material. Lernkarteikarten Veterinärmedizin - BIOCHEMIE
 Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Transkription und Translation sind in Eukaryoten räumlich und zeitlich getrennt. Abb. aus Stryer (5th Ed.)
 Transkription und Translation sind in Eukaryoten räumlich und zeitlich getrennt Die Initiation der Translation bei Eukaryoten Der eukaryotische Initiationskomplex erkennt zuerst das 5 -cap der mrna und
Transkription und Translation sind in Eukaryoten räumlich und zeitlich getrennt Die Initiation der Translation bei Eukaryoten Der eukaryotische Initiationskomplex erkennt zuerst das 5 -cap der mrna und
Theorie der Proteinfaltung
 Theorie der Proteinfaltung Strukturelle Bioinformatik WS15/16 Dr. Stefan Simm, 09.12.2015 simm@bio.uni-frankfurt.de Proteinfaltung EINLEITUNG Proteinfaltung physikalischer Prozeß, mit dem ein Polypeptid
Theorie der Proteinfaltung Strukturelle Bioinformatik WS15/16 Dr. Stefan Simm, 09.12.2015 simm@bio.uni-frankfurt.de Proteinfaltung EINLEITUNG Proteinfaltung physikalischer Prozeß, mit dem ein Polypeptid
-Klausur Biochemie Name: Matrikelnr.: 1. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist.
 4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
Stufen der Genexpression. Wie wird die Basensequenz der RNA in die Aminosäuresequenz der Proteine umgewandelt?
 Stufen der Genexpression Wie wird die Basensequenz der RNA in die Aminosäuresequenz der Proteine umgewandelt? Posttranslationale Prozesse Sobald das Polypetid aus dem Ribosom austritt steht es vor 2 wichtigen
Stufen der Genexpression Wie wird die Basensequenz der RNA in die Aminosäuresequenz der Proteine umgewandelt? Posttranslationale Prozesse Sobald das Polypetid aus dem Ribosom austritt steht es vor 2 wichtigen
1. Beschriften Sie in der Abbildung die verschiedenen Bereiche auf der DNA und beschreiben Sie ihre Funktion! nicht-codogener Strang.
 ARBEITSBLATT 1 Transkription 1. Beschriften Sie in der Abbildung die verschiedenen Bereiche auf der DNA und beschreiben Sie ihre Funktion! Bindungsstelle für RNA-Polymerase RNA-Polymerase nicht-codogener
ARBEITSBLATT 1 Transkription 1. Beschriften Sie in der Abbildung die verschiedenen Bereiche auf der DNA und beschreiben Sie ihre Funktion! Bindungsstelle für RNA-Polymerase RNA-Polymerase nicht-codogener
Referat : Aufbau v. Proteinen u. ihre Raumstruktur
 Referat : Aufbau v. Proteinen u. ihre Raumstruktur 1. Einleitung Unsere Körperzellen enthalten einige Tausend verschiedene Proteine wobei man schätzt, das insgesamt über 50 000 verschiedene Eiweißstoffe
Referat : Aufbau v. Proteinen u. ihre Raumstruktur 1. Einleitung Unsere Körperzellen enthalten einige Tausend verschiedene Proteine wobei man schätzt, das insgesamt über 50 000 verschiedene Eiweißstoffe
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Grundlagen der Zellulären Biochemie
 Grundlagen der Zellulären Biochemie Proteinstruktur Vorlesung zum Modul BCB P07 im Bachelor-Studiengang Biochemie Hannover Prof. J. Alves, Institut für Biophysikalische Chemie, MHH Damit liegen die fünf
Grundlagen der Zellulären Biochemie Proteinstruktur Vorlesung zum Modul BCB P07 im Bachelor-Studiengang Biochemie Hannover Prof. J. Alves, Institut für Biophysikalische Chemie, MHH Damit liegen die fünf
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Vertiefendes Seminar zur Vorlesung Biochemie
 Vertiefendes Seminar zur Vorlesung Biochemie 31.10.2014 Proteine: Struktur Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Vertiefendes Seminar zur Vorlesung Biochemie 31.10.2014 Proteine: Struktur Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Prionen. Prionen (K. Berendes, S. Lingan)
 Prionen Gliederung 1. Struktur eines Proteins und ihre Analyse 2. Allgemeines 3. Infektionsformen 4. Prionkrankheiten bei Mensch und Tier 5. BSE 6. Creutzfeldt-Jakob-Krankheit 7. Therapieansätze 1. Struktur
Prionen Gliederung 1. Struktur eines Proteins und ihre Analyse 2. Allgemeines 3. Infektionsformen 4. Prionkrankheiten bei Mensch und Tier 5. BSE 6. Creutzfeldt-Jakob-Krankheit 7. Therapieansätze 1. Struktur
Biophysikalisches Seminar
 Biophysikalisches Seminar Naturwissenschaftliche Fakultät III Institut für Biophysik und physikalische Biochemie Datum: 12.1./13.1.07 Thema: Die Bedeutung von Chaperonen und Verfasser: Claudia Seidl Chaperone
Biophysikalisches Seminar Naturwissenschaftliche Fakultät III Institut für Biophysik und physikalische Biochemie Datum: 12.1./13.1.07 Thema: Die Bedeutung von Chaperonen und Verfasser: Claudia Seidl Chaperone
Kohlenhydrate Aminosäuren Peptide
 Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!!
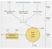 Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Eukaryontische DNA-Bindedomänen
 1. Viele eukaryotische (und auch prokaryotische) Transkriptionsfaktoren besitzen eine DNA-bindende Domäne, die an eine ganz bestimmte DNA- Sequenz binden kann. Aufgrund von Ähnlichkeiten in der Struktur
1. Viele eukaryotische (und auch prokaryotische) Transkriptionsfaktoren besitzen eine DNA-bindende Domäne, die an eine ganz bestimmte DNA- Sequenz binden kann. Aufgrund von Ähnlichkeiten in der Struktur
Konformation von Polypeptiden
 1 Konformation von Polypeptiden Peter Güntert, Wintersemester 2011/12 Primärstruktur Polypeptide sind lineare Ketten, die aus 20 verschiedenen Typen von Bausteinen (Aminosäureresten, AS) aufgebaut sind.
1 Konformation von Polypeptiden Peter Güntert, Wintersemester 2011/12 Primärstruktur Polypeptide sind lineare Ketten, die aus 20 verschiedenen Typen von Bausteinen (Aminosäureresten, AS) aufgebaut sind.
Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R , Tel /Sekretariat Frau Endrias Tel.
 Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R.1.2.34, Tel. 55157/Sekretariat Frau Endrias Tel. 53337) Tutoren: Dr. Kristina Kirchberg, Alex Boreham 6-stündig
Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R.1.2.34, Tel. 55157/Sekretariat Frau Endrias Tel. 53337) Tutoren: Dr. Kristina Kirchberg, Alex Boreham 6-stündig
Proteine. Dr. Katja Arndt Institut für Biologie III.
 Proteine Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka K. M. Arndt, 2007 Proteine Bezeichnung Protein wurde 1838 von Jöns Jakob Berzelius aus der griechischen Sprache
Proteine Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka K. M. Arndt, 2007 Proteine Bezeichnung Protein wurde 1838 von Jöns Jakob Berzelius aus der griechischen Sprache
Fettsäurebiosynthese
 Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Kapitel 1 Einleitung
 1 Kapitel 1 Einleitung Proteine übernehmen in einem funktionierenden Organismus vielfältige Funktionen, unter anderem dienen sie als Biokatalysatoren, bestimmen den Zellaufbau als Strukturproteine oder
1 Kapitel 1 Einleitung Proteine übernehmen in einem funktionierenden Organismus vielfältige Funktionen, unter anderem dienen sie als Biokatalysatoren, bestimmen den Zellaufbau als Strukturproteine oder
Übungsblatt 9: Reaktionsdiversität
 1 Übungsblatt 9: Reaktionsdiversität Warm Up Benennen Sie die folgenden (Thio )Ether: Aufgaben 1) Alkohole und Thiole i. Während das 1,2 Dibromethan bevorzugt in der fully staggered Konformation vorliegt,
1 Übungsblatt 9: Reaktionsdiversität Warm Up Benennen Sie die folgenden (Thio )Ether: Aufgaben 1) Alkohole und Thiole i. Während das 1,2 Dibromethan bevorzugt in der fully staggered Konformation vorliegt,
Name:... EHA-code:... Gruppe:...
 D-2008/09. I. 1. KLAUSUR 29. 09. 08. Name:... EHA-code:... Gruppe:... 1 Studieren Sie die Abbildung und beantworten Sie die Fragen! Einfache Antwortmöglichkeit (Bei diesem Fragentyp handelt es sich um
D-2008/09. I. 1. KLAUSUR 29. 09. 08. Name:... EHA-code:... Gruppe:... 1 Studieren Sie die Abbildung und beantworten Sie die Fragen! Einfache Antwortmöglichkeit (Bei diesem Fragentyp handelt es sich um
1 Einleitung. Einleitung 1
 Einleitung 1 1 Einleitung Die Supramolekulare Chemie ist die Chemie der intermolekularen Bindung. Sie beschäftigt sich mit Strukturen und Funktionen von Einheiten, die durch Assoziation zweier oder mehrerer
Einleitung 1 1 Einleitung Die Supramolekulare Chemie ist die Chemie der intermolekularen Bindung. Sie beschäftigt sich mit Strukturen und Funktionen von Einheiten, die durch Assoziation zweier oder mehrerer
Molekularbiologie 6c Proteinbiosynthese. Bei der Proteinbiosynthese geht es darum, wie die Information der DNA konkret in ein Protein umgesetzt wird
 Molekularbiologie 6c Proteinbiosynthese Bei der Proteinbiosynthese geht es darum, wie die Information der DNA konkret in ein Protein umgesetzt wird 1 Übersicht: Vom Gen zum Protein 1. 2. 3. 2 Das Dogma
Molekularbiologie 6c Proteinbiosynthese Bei der Proteinbiosynthese geht es darum, wie die Information der DNA konkret in ein Protein umgesetzt wird 1 Übersicht: Vom Gen zum Protein 1. 2. 3. 2 Das Dogma
Protokoll Versuch B1 Modellbau, Elektronendichtekarten und Symmetrie
 Protokoll Versuch B1 Modellbau, Elektronendichtekarten und Symmetrie Gruppe 8 Susanne Duncker und Friedrich Hahn Gruppe 8 Susanne Duncker Friedrich Hahn Versuch B1: Modellbau, Elektronendichtekarten und
Protokoll Versuch B1 Modellbau, Elektronendichtekarten und Symmetrie Gruppe 8 Susanne Duncker und Friedrich Hahn Gruppe 8 Susanne Duncker Friedrich Hahn Versuch B1: Modellbau, Elektronendichtekarten und
Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur ( )
 Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur (6.2.2015) Aufgabe 1: Erläutern Sie die Primär-, Sekundär- und die Tertiärstruktur von Proteinen. [3 P] Aufgabe 2: Erklären
Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur (6.2.2015) Aufgabe 1: Erläutern Sie die Primär-, Sekundär- und die Tertiärstruktur von Proteinen. [3 P] Aufgabe 2: Erklären
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
A. Peptide und Proteine Teil 1 ( )
 A. Peptide und Proteine Teil 1 (5.01.2017) 1. Einleitung Peptide und Proteine sind ubiquitär in allen Organismen vorhanden. Sie sind die Moleküle des Lebens. Sie sind die Funktionsreagenzien in den Zellen
A. Peptide und Proteine Teil 1 (5.01.2017) 1. Einleitung Peptide und Proteine sind ubiquitär in allen Organismen vorhanden. Sie sind die Moleküle des Lebens. Sie sind die Funktionsreagenzien in den Zellen
1.1 Was versteht man unter sauren bzw. basischen Aminosäureresten? Die Aminosäuren unterscheiden sich in ihren Seitenketten.
 Fragenkatalog Proteinchemie Vorlesung 1-12 SS 2011 1.1 Was versteht man unter sauren bzw. basischen Aminosäureresten? Die Aminosäuren unterscheiden sich in ihren Seitenketten. 1.2 Zeichnen Sie die Strukturen
Fragenkatalog Proteinchemie Vorlesung 1-12 SS 2011 1.1 Was versteht man unter sauren bzw. basischen Aminosäureresten? Die Aminosäuren unterscheiden sich in ihren Seitenketten. 1.2 Zeichnen Sie die Strukturen
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Nanotechnologie der Biomoleküle. Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie. Aufbau Struktur Funktion
 anotechnologie der Biomoleküle Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie Aufbau Struktur Funktion Zentrum für Mikro- und anotechnologien Das Miller-Urey-Experiment (auch
anotechnologie der Biomoleküle Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie Aufbau Struktur Funktion Zentrum für Mikro- und anotechnologien Das Miller-Urey-Experiment (auch
Proteinfaltungen enthüllen den Ursprung des Lebens
 Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/proteinfaltungen-enthuellenden-ursprung-des-lebens/ Proteinfaltungen enthüllen den Ursprung des Lebens Computeranalysen
Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/proteinfaltungen-enthuellenden-ursprung-des-lebens/ Proteinfaltungen enthüllen den Ursprung des Lebens Computeranalysen
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler
 Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
HORMONE!!! Synthese von Peptid- und Proteohormone
 Synthese von Peptid- und Proteohormone Synthese von Peptid- und Proteohormone: der Anfang ist die Erstellung der mrna für das jeweilige Hormon! (jetzt wissen wir auch wofür wir die Nukleinsäuren gelernt
Synthese von Peptid- und Proteohormone Synthese von Peptid- und Proteohormone: der Anfang ist die Erstellung der mrna für das jeweilige Hormon! (jetzt wissen wir auch wofür wir die Nukleinsäuren gelernt
Die Persistenzlänge ist sequenzabhängig, für Poly-Serin etwa 5 AS. Der entfaltete Zustand ist Gegenstand intensiver Untersuchungen
 Die Bildung von Quartärstruktur ermöglicht den Bau großer, aber auch multifunktionaler Proteine 9.2 Proteinfaltung Proteine können unter bestimmten Bedingungen denaturiert (entfaltet) werden, das heißt,
Die Bildung von Quartärstruktur ermöglicht den Bau großer, aber auch multifunktionaler Proteine 9.2 Proteinfaltung Proteine können unter bestimmten Bedingungen denaturiert (entfaltet) werden, das heißt,
Asparaginsäure(=Aspartat) Alanin (Seitenkette rot)
 Übungsaufgaben R. Glockshuber 1.) Ein kleines Eindomänenprotein liegt bei 20 C zu 99.990% nativ vor. Wie gross ist seine Faltungsenergie? Nullpunkt der Temperaturskala: -273.15 C. R= 8.315 J K -1 mol -1.
Übungsaufgaben R. Glockshuber 1.) Ein kleines Eindomänenprotein liegt bei 20 C zu 99.990% nativ vor. Wie gross ist seine Faltungsenergie? Nullpunkt der Temperaturskala: -273.15 C. R= 8.315 J K -1 mol -1.
Wie man den Zellzyklus versteht
 Kernmodul Kapitel 3! WS2008/2009! Allgemeines!! Curriculum für das Kernmodul im Masterstudiengang!! Zell- und Molekularbiologie!! "!! Lehrbuch zur Vorlesung: Molecular Biology of the Cell (Alberts, et
Kernmodul Kapitel 3! WS2008/2009! Allgemeines!! Curriculum für das Kernmodul im Masterstudiengang!! Zell- und Molekularbiologie!! "!! Lehrbuch zur Vorlesung: Molecular Biology of the Cell (Alberts, et
Transkription Teil 2. - Transkription bei Eukaryoten -
 Transkription Teil 2 - Transkription bei Eukaryoten - Inhalte: Unterschiede in der Transkription von Pro- und Eukaryoten Die RNA-Polymerasen der Eukaryoten Cis- und trans-aktive Elemente Promotoren Transkriptionsfaktoren
Transkription Teil 2 - Transkription bei Eukaryoten - Inhalte: Unterschiede in der Transkription von Pro- und Eukaryoten Die RNA-Polymerasen der Eukaryoten Cis- und trans-aktive Elemente Promotoren Transkriptionsfaktoren
Zentrum für Bioinformatik. Übung 4: Revision. Beispielfragen zur Klausur im Modul Angewandte Bioinformatik (erste Semesterhälfte)
 Andrew Torda Björn Hansen Iryna Bondarenko Zentrum für Bioinformatik Übung zur Vorlesung Angewandte Bioinformatik Sommersemester 2014 20./23.06.2014 Übung 4: Revision Beispielfragen zur Klausur im Modul
Andrew Torda Björn Hansen Iryna Bondarenko Zentrum für Bioinformatik Übung zur Vorlesung Angewandte Bioinformatik Sommersemester 2014 20./23.06.2014 Übung 4: Revision Beispielfragen zur Klausur im Modul
Empfohlene Literatur: Branden, C., Tooze, J.: Introduction to Protein Structure. Garland Publishing Inc. 1999
 Empfohlene Literatur: Branden, C., Tooze, J.: Introduction to Protein Structure. Garland Publishing Inc. 1999 Alberts et al.: Molecular Biology of the Cell, 4th ed. 2002 Walsh, G. : Proteins: Biochemistry
Empfohlene Literatur: Branden, C., Tooze, J.: Introduction to Protein Structure. Garland Publishing Inc. 1999 Alberts et al.: Molecular Biology of the Cell, 4th ed. 2002 Walsh, G. : Proteins: Biochemistry
Literatur: Proteine Struktur und Struktur-Funktions-Beziehungen. Proteins Structure and structure-function relationships
 Biochemie II LVA 166.163 (WS 2015) Vortragender: Ao.Univ.Prof. Dr. Ewald Srebotnik ewald.srebotnik@tuwien.ac.at Modul 1: Proteine Struktur und Struktur-Funktions-Beziehungen Proteins Structure and structure-function
Biochemie II LVA 166.163 (WS 2015) Vortragender: Ao.Univ.Prof. Dr. Ewald Srebotnik ewald.srebotnik@tuwien.ac.at Modul 1: Proteine Struktur und Struktur-Funktions-Beziehungen Proteins Structure and structure-function
