422 - Spektralphotometer
|
|
|
- Florian Grosse
- vor 9 Jahren
- Abrufe
Transkript
1 422 - Spektralphotometer 1. Aufgaben 1.1 Nehmen Sie die Transmissionskurven zweier Farbfilter auf! 1.2 Messen Sie die Transmission in Abhängigkeit von der Dicke der durchstrahlten Schicht! 1.3 Nehmen Sie das Absorptionsspektrum einer Fuchsinlösung auf! Erklären Sie damit die Farbe der Lösung! 1.4 Ermitteln Sie aus dem gegebenen Absorptionsquerschnitt die Menge des gelösten Farbstoffes. 2. Grundlagen Stichworte: Streuung, Absorption, Reflexion, Extinktion, Transmission, Spektrum, Spektralphotometer, Absorptionsquerschnitt 2.1 Lichtschwächung beim Durchgang durch Stoffe Für die Abnahme der ntensität einer Lichtwelle beim Durchgang durch Stoffe ( Extinktion ) gibt es zwei Ursachen: 1. die Streuung (Ablenkung eines Teils des gerichteten Energieflusses der Lichtwelle aus der Einfallsrichtung) und 2. die Absorption (Umwandlung von Licht- in Wärmeenergie). Desweiteren sind Reflexionsverluste an den Grenzflächen (z.b. Luft-Wasser oder Glas-Wasser) zu beachten, die von den Eigenschaften der beteiligten Medien (Brechzahldifferenz) sowie vom Strahlengang abhängen. Streuung: Alltägliche Beispiel für im sichtbaren Spektralbereich stark streuende Medien sind Milch oder Nebel. Durch Streuung an Rauch, kleinen Staubteilchen, Wassertröpfchen und anderen Schwebeteilchen werden z.b. Scheinwerferkegel, die nicht in Blickrichtung verlaufen, von der Seite her sichtbar. Die Strahlungsintensität des gestreuten Lichtes ist stark wellenlängenabhängig (proportional zu 1/λ 4 für Streuteilchengrößen < λ, proportional zu 1/λ für Teilchengrößen λ), wodurch z.b. die blaue Farbe des Himmels zustande kommt. Bei den zu untersuchenden Proben spielt Streuung allerdings nur eine untergeordnete Rolle und wird deshalb nicht weiter betrachtet. Reflexion führt an einer Grenzfläche Luft/Glas zu einem ntensitätsverlust von etwa 4% (Reflexionsgrad R = 0.04). Bei mehreren Flächen bzw. schrägem Lichteinfall ist dieser Wert noch deutlich größer. Bei quantitativen Messungen muss dieser Effekt unbedingt beachtet und am besten durch Vergleich mit einer Referenzprobe korrigiert werden. 422 Spektralphotometer Seite 1 von 6 10/11
2 Absorption: Unsere eigentliche Aufmerksamkeit gilt hier der Absorption. Genau wie bei der Lichterzeugung (Anregung von Atomen z.b. durch Wärme, Elektronen gelangen auf höhere Energieniveaus, beim Zurückspringen werden Lichtquanten ausgesendet) hängt die Absorption vom Aufbau der Elektronenhüllen der beteiligten Atome ab, speziell davon, welche Energieübergänge möglich sind und von eingestrahltem Licht angeregt werden können. Wegen E = hν (E... Energie des Photons, h... Plancksches Wirkungsquantum, ν... Frequenz der Lichtwelle) ist jedem Übergang eindeutig eine Frequenz zugeordnet und die Absorption eines Stoffes somit in charakteristischer Weise frequenzabhängig. Diese Abhängigkeit nennt man Spektrum. Es gibt Linien-, Banden- und kontinuierliche Spektren. Ein Spektrum kann sowohl als Absorptions- als auch Emissionsspektrum aufgenommen werden. Spektren bieten z.b. den Astronomen die Möglichkeit, noch aus Entfernungen von Millionen von Lichtjahren den Aufbau von Himmelsobjekten zu untersuchen und sogar (aufgrund der Dopplerverschiebung der Spektrallinien) auf ihre Bewegungsrichtung und -geschwindigkeit zu schließen. n unserem Versuch haben wir es mit Bandenspektren, quasi einer Folge von sehr eng zusammenliegenden Spektrallinien zu tun, wie sie für Farbstoffe charakteristisch sind. Es werden dabei ganze Bereiche des sichtbaren Spektrums geschwächt, dafür andere kaum bzw. gar nicht, wodurch sich eine bestimmte Färbung des Stoffes ergibt. Farbfilter kommen dort zum Einsatz, wo nur ein kleiner wellenlängenbegrenzter Teil des Spektrums (eine Farbe) benötigt wird bzw. in seiner Passage durch den Filter behindert werden soll (seltenerer Fall). Durch die selektive Absorption im optischen Spektralbereich erscheinen uns die Filter farbig. Farbfilter haben z.b. in der digitalen Fotografie eine große Bedeutung. Typische CCD-Kameradetektoren besitzen eine Sensitivität über den gesamten optischen Spektralbereich und darüber hinaus. Um Farbinformationen in einem Bild festzuhalten, werden auf dem Chip naheliegende CCD-Pixel mosaikartig mit verschiedenen Farbfiltern (z.b. rot, grün, blau) versehen, so dass ein Bild zeitgleich in drei Farben aufgenommen wird. Das Ergebnisbild entsteht durch Farbinformationsinterpolation aus den benachbarten Pixeln. Die für den sichtbaren Spektralbereich dargestellten Zusammenhänge und Gleichungen gelten natürlich auch für andere Gebiete des elektromagnetischen Spektrums, z.b. für Röntgen-, UV- oder nfrarotstrahlung. 2.2 Extinktionskoeffizent Bei senkrechtem Durchgang einer Lichtwelle der ntensität 0 durch eine planparallele Schicht der Dicke d erhält man für die ntensität hinter der Schicht = o (1 R) 2 e -k d (1) Der Faktor (1 R) 2 berücksichtigt die Reflexion an Vorder- und Rückseite der planparallelen Schicht. R ist der Reflexionsgrad der Grenzfläche. Man erkennt, dass die ntensität exponentiell mit der Dicke d abnimmt. Dabei ist k der sogenannte Extinktionskoeffizent. Für verdünnte Lösungen (Vernachlässigung der Wechselwirkung der Moleküle) ist k proportional zur Konzentration c der gelösten Moleküle: k = ε c mit [c] = mol/l. Die Größe heißt molarer Extinktionskoeffizient. Eingesetzt in Gl. 1 erhält man das Lambert- Beersches-Gesetz : 422 Spektralphotometer Seite 2 von 6 10/11
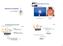
3 = o (1 R) 2 e -ε c d bzw. = o (1 R) 2 e -E (2) Die dimensionslose Größe E wird als Extinktion bezeichnet. E = k d = ε c d (3) Da in unserem Versuch (Aufgabe 1.3) durch eine Vergleichsmessung sowohl Reflexion an der Glasküvette als auch Absorption des Lösungsmittels (Wasser) eliminiert werden und Streuung keine messbare Rolle spielt, vereinfacht sich Gl. 2 zu = o e -E (4) und das Photometer liefert uns einen direkten Wert für die Absorption der gelösten Farbstoffmoleküle. Der Transmissionsgrad T, also das Verhältnis von durchgelassener zu einfallender Lichtintensität ist T = = e -E (5) o 2.3 Absorptionsquerschnitt Während es in der Chemie (speziell: Spektroskopie) üblich ist, die Absorption über den molaren Extinktionskoeffizienten zu charakterisieren: Dimension: (Länge) 2 mol -1 gebräuchliche Einheit in der Praxis: Liter mol 1 cm 1 wird in der Physik (speziell: Laser-Physik) gerne der Absorptionsquerschnitt q (in cm 2 ) verwendet. Diesen erhält man, wenn in der Gl. 3 die rechte Seite mit der Avogadro-Konstanten N A erweitert wird: ( ) E(λ) = N A c d (6) N A ( ) Hier ist jetzt N = q(λ) der (wellenlängenabhängige) Absorptionsquerschnitt und c N A = n A die Zahl der absorbierenden Moleküle (oder Atome) pro Volumen (Molekülzahldichte). Die Gleichung für die Extinktion lautet nun: E(λ) = q(λ) n d (7) Bitte beachten: Der Absorptionsquerschnitt ist ein Wirkungsquerschnitt und keine geometrische Fläche. Für resonante Atome (z.b. Hg-Dampf) liegt q in der Größenordnung von λ 2 max. Bei Farbstoffmolekülen ist q(λ max ) um etwa sieben Größenordnungen kleiner (z.b cm 2 ; dazu ist im Vergleich der Molekülquerschnitt von Fuchsin ca cm 2 ). 422 Spektralphotometer Seite 3 von 6 10/11
4 Bild 1: Symbolhafter Vergleich: Absorptionsquerschnitt und Moleküldurchmesser 3. Versuchsdurchführung 3.1 Messanordnung und Messverfahren Wir verwenden das kommerzielle Spektralphotometer SPEKOL 11 (vgl. Bild 2). Der erfassbare Wellenlängenbereich liegt zwischen 330 nm und 850 nm. Als Lichtquelle dient eine Halogenlampe. Die Lichtquelle wird mit einem Kondensor auf den Eintrittsspalt des Monochromators abgebildet. Das Licht wird vom Kollimatorobjektiv parallel gerichtet und durch das Reflexionsgitter spektral zerlegt. Die Spaltbreite des Monochromators ist fest vorgegeben. Die spektrale Bandbreite beträgt 11 nm. Das aus dem Austrittsspalt tretende Licht durchsetzt einen Extinktionsmessansatz, der zwei Küvettenhalter zur Aufnahme der Küvetten besitzt, die sich abwechselnd in den Strahlengang einschieben lassen. Von einer Photozelle wird das ankommende Licht in ein elektrisches Signal umgewandelt, das dem Verstärker zugeführt und vom Messinstrument angezeigt wird. Bild 2: Aufbau des Spektralphotometers 422 Spektralphotometer Seite 4 von 6 10/11
5 Das hier genutzte Messverfahren kann zur Bestimmung unbekannter Konzentrationen (z.b. von Farbstofflösungen) oder zur dentifizierung von Stoffen anhand des gemessenen Absorptions- bzw. Transmissionsspektrums genutzt werden. 3.2 Prinzipielle Durchführung der Messung Gerät einschalten, Taste T (Transmission) oder E (Extinktion E ) drücken (vor Beginn der eigentlichen Messung Gerät einige Minuten warmlaufen lassen) Wellenlänge einstellen, Auswahl blauempfindliche (< 600 nm) oder rotempfindliche ( 600 nm) Fotozelle Vergleichsprobe (z.b. Küvette mit Lösungsmittel Wasser) in den Küvettenraum stellen, Taste R (Referenz) drücken Gerät kalibriert (T = 100% bzw. E = 0) Farbfilter bzw. Küvette mit der zu untersuchenden Lösung in den Strahlengang bringen, Zahlenwert T bzw. E ablesen Bei zu hoher bzw. zu niedriger Lichtintensität (Anzeige OFL bzw. OFL ) muss die Blende dazwischengeschaltet bzw. herausgenommen werden. Bitte beachten: n der messtechnischen Praxis verwendet man häufig Zehnerpotenzen anstelle der Exponentialfunktion. Damit ändert sich Gl. 4 bzw. Gl. 5 in = o 10 -E bzw. T = o = 10 E (8) Die dekadische Extinktion E ist um einen Faktor ln10 kleiner als E E = E ln10 (9) Überprüfen Sie, welche der beiden Größen (E oder E ) von dem verwendeten Spektralphotometer SPEKOL 11 angezeigt wird. 3.3 Hinweise zum Versuchsablauf Die Transmission T des Grünfilters ist im Wellenlängenbereich 400 bis 700 nm, die des Rotfilters zwischen 550 und 800 nm auszumessen. Die geeignete Schrittweite beträgt etwa 25 nm und kann, dort wo es sinnvoll erscheint, auf 10nm verringert werden. Eine Berücksichtigung der Reflexionsverluste ist nicht erforderlich. Stellen Sie die Transmissionskurven grafisch in einem gemeinsamen Diagramm dar und diskutieren Sie das Ergebnis! Die Dicke der durchstrahlten Schicht wird geändert, indem man mehrere Grünfilter hintereinander anordnet. Messen Sie für n = 0, 1, 2,, 5 Filtergläser jeweils T und E, und stellen Sie die Abhängigkeiten T(n) und E (n) grafisch dar! Welcher Kurvenverlauf ergibt sich? 422 Spektralphotometer Seite 5 von 6 10/11
6 Als zu untersuchender synthetischer Farbstoff steht eine Fuchsinlösung zur Verfügung. Bei deren Herstellung wurde eine sehr kleine Menge Fuchsin (molare Masse M = 338 g/mol) in einem Liter Wasser gelöst. Die Konzentration der Lösung soll im Zuge der Auswertung bestimmt werden (Aufg. 1.4). Die Extinktion E der Lösung ist im Wellenlängenbereich 400 bis 600 nm in 10 nm-schritten zu messen (in der Nähe des Maximums in 5 nm-schritten) und grafisch darzustellen. Machen Sie anhand des Spektrums Aussagen über das Zustandekommen der charakteristischen Farbe der Fuchsinlösung! Der Absorptionsquerschnitt beträgt für Fuchsin q = cm 2 (bei der Wellenlänge maximaler Extinktion). Berechnen Sie aus E max und q die Molekülzahldichte n (Gl. 7, 9) und daraus die Konzentration der Fuchsinlösung! Wie groß war die Menge des Farbstoffes (in kristalliner Form), die in 1 Liter Wasser aufgelöst wurde? Frage an die Experten: Welche Farbe hatten die Kristalle? 422 Spektralphotometer Seite 6 von 6 10/11
 Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
21-1. K=f c I=I0 e f c d
 21-1 Lichtabsorption 1. Vorbereitung : Extinktions- und Absorptionskonstante, mittlere Reichweite, Unterscheidung zwischen stark und schwach absorbierenden Stoffen, Lambert-Beersches Gesetz, Erklärung
21-1 Lichtabsorption 1. Vorbereitung : Extinktions- und Absorptionskonstante, mittlere Reichweite, Unterscheidung zwischen stark und schwach absorbierenden Stoffen, Lambert-Beersches Gesetz, Erklärung
422 Optische Spektroskopie
 422 Optische Spektroskopie Ziele Aufbau und Funktionsweise von Spektrometern erläutern Lichtquellen anhand ihres Spektrums charakterisieren Absorptions- und Transmissionsspektren qualitativ diskutieren
422 Optische Spektroskopie Ziele Aufbau und Funktionsweise von Spektrometern erläutern Lichtquellen anhand ihres Spektrums charakterisieren Absorptions- und Transmissionsspektren qualitativ diskutieren
Laborpraktikum Sensorik. Versuch. Optische Konzentrations- bestimmung MS 2
 Otto-von-Guericke-Universität Magdeburg Fakultät für Elektrotechnik und Informationstechnik Institut für Mikro- und Sensorsysteme (IMOS) Laborpraktikum Sensorik Versuch Optische Konzentrations- bestimmung
Otto-von-Guericke-Universität Magdeburg Fakultät für Elektrotechnik und Informationstechnik Institut für Mikro- und Sensorsysteme (IMOS) Laborpraktikum Sensorik Versuch Optische Konzentrations- bestimmung
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1. Lambert Beer sches Gesetz - Zerfall des Manganoxalations
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Seminar: Photometrie
 Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Abiturprüfung Physik, Grundkurs
 Seite 1 von 5 Abiturprüfung 2012 Physik, Grundkurs Aufgabenstellung: Aufgabe: Farbstoffmoleküle In der Spektroskopie unterscheidet man zwei grundsätzliche Typen von Spektren: Emissionsspektren, wie sie
Seite 1 von 5 Abiturprüfung 2012 Physik, Grundkurs Aufgabenstellung: Aufgabe: Farbstoffmoleküle In der Spektroskopie unterscheidet man zwei grundsätzliche Typen von Spektren: Emissionsspektren, wie sie
Photom etrieren Photometrie Fraunhofer sche Linien
 17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
GRUNDLAGEN DER SPEKTROPHOTOMETRIE
 11 GRUNDLAGEN DER SPEKTROPHOTOMETRE Materie erscheint uns farbig, wenn sie aus dem einfallenden weißen Licht einen bestimmten spektralen Teil absorbiert. Als Farbe nehmen wir den reflektierten Anteil des
11 GRUNDLAGEN DER SPEKTROPHOTOMETRE Materie erscheint uns farbig, wenn sie aus dem einfallenden weißen Licht einen bestimmten spektralen Teil absorbiert. Als Farbe nehmen wir den reflektierten Anteil des
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Protokoll zum Versuch 50: Photometrie vom Thema: Photometrische Fe 2+ -Konzentrationsbestimmung mit Phenanthrolin
 Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Versuch K2 Photometrische Messung
 Versuch K2 Photometrische Messung Aufgaben: 1. Messung der Extinktion von Mangan(III)-oxalat bei verschiedenen Wellenlängen. 2. Bestimmung der Geschwindigkeitskonstanten des Zerfalls des komplexen Mangan(III)-oxalations
Versuch K2 Photometrische Messung Aufgaben: 1. Messung der Extinktion von Mangan(III)-oxalat bei verschiedenen Wellenlängen. 2. Bestimmung der Geschwindigkeitskonstanten des Zerfalls des komplexen Mangan(III)-oxalations
1. Blue-curacao 1.1. Die durchgelassene Lichtintensität I ist bei konstanter Konzentration von der Schichtdicke abhängig: d 1 < d 2
 1. Blue-curacao 1.1 Viele Getränke sind aus rein optischen Gründen mit Lebensmittelfarbstoffen angefärbt. So auch Blue-curacao. Der Likör enthält den Lebensmittelfarbstoff E 133. (Erioglaucin A (Brillant
1. Blue-curacao 1.1 Viele Getränke sind aus rein optischen Gründen mit Lebensmittelfarbstoffen angefärbt. So auch Blue-curacao. Der Likör enthält den Lebensmittelfarbstoff E 133. (Erioglaucin A (Brillant
Physikalische Chemie: Kinetik
 Physikalische Chemie: Kinetik Prof. Thiemann SS 2002 Protokoll Versuch 2 «Die ph-abhängigkeit der Solvolysegeschwindigkeit von Malachitgrün» 1 Inhalt: 1. Theorie 2. Zusatzfragen Bau eines UV-Spektralphotometers
Physikalische Chemie: Kinetik Prof. Thiemann SS 2002 Protokoll Versuch 2 «Die ph-abhängigkeit der Solvolysegeschwindigkeit von Malachitgrün» 1 Inhalt: 1. Theorie 2. Zusatzfragen Bau eines UV-Spektralphotometers
Lösungen zu den Übungen zur Einführung in die Spektroskopie für Studenten der Biologie (SS 2011)
 Universität Konstanz Fachbereich Biologie Priv.-Doz. Dr. Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Datum: 26.5.211 Lösungen zu den Übungen zur Einführung in die Spektroskopie
Universität Konstanz Fachbereich Biologie Priv.-Doz. Dr. Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Datum: 26.5.211 Lösungen zu den Übungen zur Einführung in die Spektroskopie
Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002
 Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002 30. Juli 2002 Gruppe 17 Christoph Moder 2234849 Michael Wack 2234088 Sebastian Mühlbauer 2218723
Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002 30. Juli 2002 Gruppe 17 Christoph Moder 2234849 Michael Wack 2234088 Sebastian Mühlbauer 2218723
Versuch: Reaktionskinetik
 Versuch: Reaktionskinetik Befindet sich eine chemische Reaktion im thermodynamischen Gleichgewicht, so lassen sich die Bedingungen für diesen Zustand durch eine energetische Betrachtungsweise mithilfe
Versuch: Reaktionskinetik Befindet sich eine chemische Reaktion im thermodynamischen Gleichgewicht, so lassen sich die Bedingungen für diesen Zustand durch eine energetische Betrachtungsweise mithilfe
425 Polarisationszustand des Lichtes
 45 Polarisationszustand des Lichtes 1. Aufgaben 1.1 Bestimmen Sie den Polarisationsgrad von Licht nach Durchgang durch einen Glasplattensatz, und stellen Sie den Zusammenhang zwischen Polarisationsgrad
45 Polarisationszustand des Lichtes 1. Aufgaben 1.1 Bestimmen Sie den Polarisationsgrad von Licht nach Durchgang durch einen Glasplattensatz, und stellen Sie den Zusammenhang zwischen Polarisationsgrad
2 Einführung in Licht und Farbe
 2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
K1: Lambert-Beer`sches Gesetz
 K1: Lambert-Beer`sches Gesetz Einleitung In diesem Versuch soll die Entfärbung von Kristallviolett durch atronlauge mittels der Absorptionsspektroskopie untersucht werden. Sowohl die Reaktionskinetik als
K1: Lambert-Beer`sches Gesetz Einleitung In diesem Versuch soll die Entfärbung von Kristallviolett durch atronlauge mittels der Absorptionsspektroskopie untersucht werden. Sowohl die Reaktionskinetik als
1. Ziel des Versuchs. 2. Versuchsaufbau und Durchführung. Dennis Fischer Gruppe 9 Magdalena Boeddinghaus
 Versuch Nr. 7: Lambert-Beersches Gesetz 1. Ziel des Versuchs Ziel des Versuches ist es, die Abhängigkeiten der Absorption eines Stoffes von der Konzentration, der Schichtdicke und der Wellenlänge zu ermitteln.
Versuch Nr. 7: Lambert-Beersches Gesetz 1. Ziel des Versuchs Ziel des Versuches ist es, die Abhängigkeiten der Absorption eines Stoffes von der Konzentration, der Schichtdicke und der Wellenlänge zu ermitteln.
Wie Heavy Metal ist der Boden?
 Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
Optik, Reflexion und Brechung
 Optik, Reflexion und Brechung 2.9.216 1 Einführung 1.1 Licht als geometrischer Strahl Warum können wir Dinge sehen? Damit wir mit unseren ugen überhaupt etwas wahrnehmen können, muss Licht in unser uge
Optik, Reflexion und Brechung 2.9.216 1 Einführung 1.1 Licht als geometrischer Strahl Warum können wir Dinge sehen? Damit wir mit unseren ugen überhaupt etwas wahrnehmen können, muss Licht in unser uge
Kontrollaufgaben zur Optik
 Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Gymnasium / Realschule. Atomphysik 2. Klasse / G8. Aufnahme und Abgabe von Energie (Licht)
 Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Spektroskopie im sichtbaren und UV-Bereich
 Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Abiturprüfung Physik, Grundkurs
 Seite 1 von 6 Abiturprüfung 2010 Physik, Grundkurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer Bedeutung.
Seite 1 von 6 Abiturprüfung 2010 Physik, Grundkurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer Bedeutung.
8. Simultane UV/VIS-Zweikomponentenanalyse
 Simultane UV/VIS-Zweikomponentenanalyse 89 8. Simultane UV/VIS-Zweikomponentenanalyse Einleitung Polycyclische Aromaten treten als Begleiter des bei der Verbrennung entstehenden Rußes, z. B. beim Betrieb
Simultane UV/VIS-Zweikomponentenanalyse 89 8. Simultane UV/VIS-Zweikomponentenanalyse Einleitung Polycyclische Aromaten treten als Begleiter des bei der Verbrennung entstehenden Rußes, z. B. beim Betrieb
Lösung: a) b = 3, 08 m c) nein
 Phy GK13 Physik, BGL Aufgabe 1, Gitter 1 Senkrecht auf ein optisches Strichgitter mit 100 äquidistanten Spalten je 1 cm Gitterbreite fällt grünes monochromatisches Licht der Wellenlänge λ = 544 nm. Unter
Phy GK13 Physik, BGL Aufgabe 1, Gitter 1 Senkrecht auf ein optisches Strichgitter mit 100 äquidistanten Spalten je 1 cm Gitterbreite fällt grünes monochromatisches Licht der Wellenlänge λ = 544 nm. Unter
Spektroskopie-Seminar SS UV-Vis-Spektroskopie. UV-Vis-Spektroskopie
 UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre?
 Spektren 1 Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre? Der UV- und höherenergetische Anteil wird fast
Spektren 1 Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre? Der UV- und höherenergetische Anteil wird fast
SPEKTRALANALYSE. entwickelt um 1860 von: GUSTAV ROBERT KIRCHHOFF ( ; dt. Physiker) + ROBERT WILHELM BUNSEN ( ; dt.
 SPEKTRALANALYSE = Gruppe von Untersuchungsmethoden, bei denen das Energiespektrum einer Probe untersucht wird. Man kann daraus schließen, welche Stoffe am Zustandekommen des Spektrums beteiligt waren.
SPEKTRALANALYSE = Gruppe von Untersuchungsmethoden, bei denen das Energiespektrum einer Probe untersucht wird. Man kann daraus schließen, welche Stoffe am Zustandekommen des Spektrums beteiligt waren.
Spektralapparat. Schriftliche VORbereitung:
 Das ist die Idee: Jeder Stoff absorbiert Licht auf bestimmten, für ihn charakteristischen Wellenlängen. Mit einem ermittelt man diese Wellenlängen und kann so den Stoff identifizieren. In diesem Versuch
Das ist die Idee: Jeder Stoff absorbiert Licht auf bestimmten, für ihn charakteristischen Wellenlängen. Mit einem ermittelt man diese Wellenlängen und kann so den Stoff identifizieren. In diesem Versuch
Grundlagen. Dies bedeutet, dass die Elektronenemission unabhängig von der Lichtintensität und unabhängig von der Bestrahlungsdauer. A.
 Grundlagen Die Wissenschaft beschäftigte sich lange mit der Frage um die Natur des Lichts. Einerseits besitzt Licht viele Welleneigenschaften, weshalb es häufig als solche betrachtet wird. Doch andererseits
Grundlagen Die Wissenschaft beschäftigte sich lange mit der Frage um die Natur des Lichts. Einerseits besitzt Licht viele Welleneigenschaften, weshalb es häufig als solche betrachtet wird. Doch andererseits
Hallwachs-Experiment. Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe
 Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
Versuch 33: Messung mit einer Vakuum-Photozelle Seite 1
 Versuch 33: Messung mit einer Vakuum-Photozelle Seite Aufgabe: Messverfahren: Vorkenntnisse: Lehrinhalt: Bestimmung der Charakteristik einer Photozelle Messung des Photostroms mit Hilfe eines Galvanometers
Versuch 33: Messung mit einer Vakuum-Photozelle Seite Aufgabe: Messverfahren: Vorkenntnisse: Lehrinhalt: Bestimmung der Charakteristik einer Photozelle Messung des Photostroms mit Hilfe eines Galvanometers
Elektromagnetische Wellen
 Elektromagnetische Wellen Im Gegensatz zu Schallwellen sind elektromagnetische Wellen nicht an ein materielles Medium gebunden -- sie können sich auch in einem perfekten Vakuum ausbreiten. Sie sind auch
Elektromagnetische Wellen Im Gegensatz zu Schallwellen sind elektromagnetische Wellen nicht an ein materielles Medium gebunden -- sie können sich auch in einem perfekten Vakuum ausbreiten. Sie sind auch
Seminar zum Praktikumsversuch: Optische Spektroskopie. Tilman Zscheckel Otto-Schott-Institut
 Seminar zum Praktikumsversuch: Optische Spektroskopie Tilman Zscheckel Otto-Schott-Institut Optische Spektroskopie Definition: - qualitative oder quantitative Analyse, die auf der Wechselwirkung von Licht
Seminar zum Praktikumsversuch: Optische Spektroskopie Tilman Zscheckel Otto-Schott-Institut Optische Spektroskopie Definition: - qualitative oder quantitative Analyse, die auf der Wechselwirkung von Licht
Bestimmung des Planckschen Wirkungsquantums h mit Hilfe des Fotoelektrischen Effektes
 Versuchsdurchführung Bestimmung des Planckschen Wirkungsquantums h mit Hilfe des Fotoelektrischen Effektes Auf einer optischen Bank sind eine Quecksilberniederdrucklampe, ein verstellbarer Spalt, eine
Versuchsdurchführung Bestimmung des Planckschen Wirkungsquantums h mit Hilfe des Fotoelektrischen Effektes Auf einer optischen Bank sind eine Quecksilberniederdrucklampe, ein verstellbarer Spalt, eine
Versuchsanleitung. Einleitung. Benötigtes Material. Seite 1 von 14
 Versuchsanleitung Spektrometische Bestimmung der Konzentration von Lösungen mit dem ipad (Lambert-Beersches Gesetz) [ VAD_Physik_Beers_Gesetz.doc ] Einleitung Der folgende Versuch zeigt eine einfache Möglichkeit
Versuchsanleitung Spektrometische Bestimmung der Konzentration von Lösungen mit dem ipad (Lambert-Beersches Gesetz) [ VAD_Physik_Beers_Gesetz.doc ] Einleitung Der folgende Versuch zeigt eine einfache Möglichkeit
HANDOUT. Vorlesung: Glasanwendungen. Überblick optische Eigenschaften
 Materialwissenschaft und Werkstofftechnik an der Universität des Saarlandes HANDOUT Vorlesung: Glasanwendungen Überblick optische Eigenschaften Leitsatz: 21.04.2016 Die Ausbreitung von Licht durch ein
Materialwissenschaft und Werkstofftechnik an der Universität des Saarlandes HANDOUT Vorlesung: Glasanwendungen Überblick optische Eigenschaften Leitsatz: 21.04.2016 Die Ausbreitung von Licht durch ein
In der Abbildung ist ein vereinfachtes Energieniveauschema eines Lasers dargestellt.
 Klausur Physik III, 7.3.2016 Aufg. 1/5 Aufgabe 1) In der Abbildung ist ein vereinfachtes Energieniveauschema eines Lasers dargestellt. 1. Nennen Sie die wesentlichen Prozesse, die bei der Erzeugung von
Klausur Physik III, 7.3.2016 Aufg. 1/5 Aufgabe 1) In der Abbildung ist ein vereinfachtes Energieniveauschema eines Lasers dargestellt. 1. Nennen Sie die wesentlichen Prozesse, die bei der Erzeugung von
NG Brechzahl von Glas
 NG Brechzahl von Glas Blockpraktikum Frühjahr 2007 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Geometrische Optik und Wellenoptik.......... 2 2.2 Linear polarisiertes
NG Brechzahl von Glas Blockpraktikum Frühjahr 2007 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Geometrische Optik und Wellenoptik.......... 2 2.2 Linear polarisiertes
Physikpraktikum für Pharmazeuten Universität Regensburg Fakultät Physik. 9. Versuch: Spektralphotometer
 Physikpraktikum für Pharmazeuten Universität Regensburg Fakultät Physik 9. Versuch: Spektralphotometer 1 Einführung Im achten Versuch haben wir gelernt, dass ein Lichtstrahl, welcher durch ein Ensemble
Physikpraktikum für Pharmazeuten Universität Regensburg Fakultät Physik 9. Versuch: Spektralphotometer 1 Einführung Im achten Versuch haben wir gelernt, dass ein Lichtstrahl, welcher durch ein Ensemble
Medizinische Biophysik 6
 Eigenschaften des Lichtes Medizinische Biophysik 6 Geradlinige Ausbreitung Energietransport Licht in der Medizin. 1 Geometrische Optik Wellennatur Teilchennatur III. Teilchencharakter des Lichtes a) Lichtelektrischer
Eigenschaften des Lichtes Medizinische Biophysik 6 Geradlinige Ausbreitung Energietransport Licht in der Medizin. 1 Geometrische Optik Wellennatur Teilchennatur III. Teilchencharakter des Lichtes a) Lichtelektrischer
Grundpraktikum Physikalische Chemie. Versuch 16 Kinetischer Salzeffekt
 Grundpraktikum Physikalische Chemie Versuch 16 Kinetischer Salzeffekt Version: März 2016 1. Theorie 1.1. Kinetischer Salzeffekt Eine bimolekulare chemische Reaktion lässt sich mithilfe von Konzepten der
Grundpraktikum Physikalische Chemie Versuch 16 Kinetischer Salzeffekt Version: März 2016 1. Theorie 1.1. Kinetischer Salzeffekt Eine bimolekulare chemische Reaktion lässt sich mithilfe von Konzepten der
1 Beugungsmuster am Gitter. 2 Lautsprecher. 3 Der Rote Punkt am Mond. 4 Phasengitter
 1 Beugungsmuster am Gitter Ein Gitter mit 1000 Spalten, dessen Spaltabstand d = 4, 5µm und Spaltbreite b = 3µm ist, werde von einer kohärenten Lichtquelle mit der Wellenlänge λ = 635nm bestrahlt. Bestimmen
1 Beugungsmuster am Gitter Ein Gitter mit 1000 Spalten, dessen Spaltabstand d = 4, 5µm und Spaltbreite b = 3µm ist, werde von einer kohärenten Lichtquelle mit der Wellenlänge λ = 635nm bestrahlt. Bestimmen
Strukturaufklärung (BSc-Chemie): Einführung
 Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Die Natriumlinie. und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz
 Die Natriumlinie und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz Absorption & Emissionsarten Absorption (Aufnahme von Energie) Atome absorbieren Energien, z.b. Wellenlängen,
Die Natriumlinie und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz Absorption & Emissionsarten Absorption (Aufnahme von Energie) Atome absorbieren Energien, z.b. Wellenlängen,
Lernziele zu Farbigkeit von Stoffen
 Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Thema: Spektroskopische Untersuchung von Strahlung mit Gittern
 Thema: Spektroskopische Untersuchung von Strahlung mit Gittern Gegenstand der Aufgaben ist die spektroskopische Untersuchung von sichtbarem Licht, Mikrowellenund Röntgenstrahlung mithilfe geeigneter Gitter.
Thema: Spektroskopische Untersuchung von Strahlung mit Gittern Gegenstand der Aufgaben ist die spektroskopische Untersuchung von sichtbarem Licht, Mikrowellenund Röntgenstrahlung mithilfe geeigneter Gitter.
= 6,63 10 J s 8. (die Plancksche Konstante):
 35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
Praktikum Optische Technologien, Protokoll Versuch Absorptionsmessung
 Praktikum Optische Technologien, Protokoll Versuch Absorptionsmessung 09.0.204 Ort: Laserlabor der Fachhochschule Aachen Campus Jülich Inhaltsverzeichnis Einleitung 2 Fragen zur Vorbereitung 2 3 Geräteliste
Praktikum Optische Technologien, Protokoll Versuch Absorptionsmessung 09.0.204 Ort: Laserlabor der Fachhochschule Aachen Campus Jülich Inhaltsverzeichnis Einleitung 2 Fragen zur Vorbereitung 2 3 Geräteliste
Grundlagen der Quantentheorie
 Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
1. Die Abbildung zeigt den Strahlenverlauf eines einfarbigen
 Klausur Klasse 2 Licht als Wellen (Teil ) 26..205 (90 min) Name:... Hilfsmittel: alles verboten. Die Abbildung zeigt den Strahlenverlauf eines einfarbigen Lichtstrahls durch eine Glasplatte, bei dem Reflexion
Klausur Klasse 2 Licht als Wellen (Teil ) 26..205 (90 min) Name:... Hilfsmittel: alles verboten. Die Abbildung zeigt den Strahlenverlauf eines einfarbigen Lichtstrahls durch eine Glasplatte, bei dem Reflexion
Natürliches Licht und Farbfilter
 4. Versuchsdurchführung 4.1. Bestimmen der Gitterkonstante abor zum Physikalisches Praktikum Natürliches icht und Farbfilter Die Entfernung zwischen Gitter und Intensitätsmeßgerät beträgt 1,20m. Der Abstand
4. Versuchsdurchführung 4.1. Bestimmen der Gitterkonstante abor zum Physikalisches Praktikum Natürliches icht und Farbfilter Die Entfernung zwischen Gitter und Intensitätsmeßgerät beträgt 1,20m. Der Abstand
Licht als Teilchenstrahlung
 Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
Abiturprüfung Physik, Grundkurs
 Seite 1 von 7 Abiturprüfung 2011 Physik, Grundkurs Aufgabenstellung: Aufgabe 1: Der Doppelspalt 1.1 Interferenzen bei Licht In einem ersten Experiment untersucht man Interferenzen von sichtbarem Licht,
Seite 1 von 7 Abiturprüfung 2011 Physik, Grundkurs Aufgabenstellung: Aufgabe 1: Der Doppelspalt 1.1 Interferenzen bei Licht In einem ersten Experiment untersucht man Interferenzen von sichtbarem Licht,
Besprechung am
 PN2 Einführung in die Physik für Chemiker 2 Prof. J. Lipfert SS 2016 Übungsblatt 10 Übungsblatt 10 Besprechung am 27.6.2016 Aufgabe 1 Interferenz an dünnen Schichten. Weißes Licht fällt unter einem Winkel
PN2 Einführung in die Physik für Chemiker 2 Prof. J. Lipfert SS 2016 Übungsblatt 10 Übungsblatt 10 Besprechung am 27.6.2016 Aufgabe 1 Interferenz an dünnen Schichten. Weißes Licht fällt unter einem Winkel
PS4. Grundlagen-Vertiefung Version vom 2. März 2012
 PS4 Grundlagen-Vertiefung Version vom 2. März 2012 Inhaltsverzeichnis 1 Vertiefende Grundlagen zu Auösungsvermögen eines Gitters. 2 3 2.1 Entstehung optischer Spektren......................... 3 2.2 Einteilung
PS4 Grundlagen-Vertiefung Version vom 2. März 2012 Inhaltsverzeichnis 1 Vertiefende Grundlagen zu Auösungsvermögen eines Gitters. 2 3 2.1 Entstehung optischer Spektren......................... 3 2.2 Einteilung
Physikalisches Praktikum
 Physikalisches Praktikum MI2AB Prof. Ruckelshausen Versuch 3.2: Wellenlängenbestimmung mit dem Gitter- und Prismenspektrometer Inhaltsverzeichnis 1. Theorie Seite 1 2. Versuchsdurchführung Seite 2 2.1
Physikalisches Praktikum MI2AB Prof. Ruckelshausen Versuch 3.2: Wellenlängenbestimmung mit dem Gitter- und Prismenspektrometer Inhaltsverzeichnis 1. Theorie Seite 1 2. Versuchsdurchführung Seite 2 2.1
Grundlagen der photometrischen Messung
 Grundlagen der photometrischen Messung Teil 1: Grundlagen, Optik, AQS, Testsätze (I) 2015 WTW GmbH. [ Juni 2015] Einführung Phos (griech.) für Licht => Photometrie ist ein Messverfahren, bei dem mit Hilfe
Grundlagen der photometrischen Messung Teil 1: Grundlagen, Optik, AQS, Testsätze (I) 2015 WTW GmbH. [ Juni 2015] Einführung Phos (griech.) für Licht => Photometrie ist ein Messverfahren, bei dem mit Hilfe
Molekülsymmetrie und Kristallographie
 Optische Aktivität Wie schon im Skriptum 5 erwähnt ist es nicht einfach, aus experimentellen Daten auf die Absolutkonfiguration einer chiralen Verbindung zu schließen. In den meisten Fällen verwendet man
Optische Aktivität Wie schon im Skriptum 5 erwähnt ist es nicht einfach, aus experimentellen Daten auf die Absolutkonfiguration einer chiralen Verbindung zu schließen. In den meisten Fällen verwendet man
Aufnahme einer Extinktionskurve. Themen. Prinzip. Material TEAS Photometrie, Extinktion, Verdünnung, Extinktionskurve
 Aufnahme einer TEAS Themen Photometrie, Extinktion, Verdünnung, Prinzip Eine Farbstofflösung wird zunächst hergestellt und anschließend die Extinktion bei verschiedenen Wellenlängen gemessen. Anschließend
Aufnahme einer TEAS Themen Photometrie, Extinktion, Verdünnung, Prinzip Eine Farbstofflösung wird zunächst hergestellt und anschließend die Extinktion bei verschiedenen Wellenlängen gemessen. Anschließend
Fluoreszenzspektroskopie
 A 60 Fluoreszenzspektroskopie Aufgabe: Bestimmen Sie das Absorptions- und Fluoreszenzspektrum des Farbstoffs Rhodamin 6G in ethanolischer Lösung. Bestimmen Sie in beiden Spektren jeweils die Wellenlänge
A 60 Fluoreszenzspektroskopie Aufgabe: Bestimmen Sie das Absorptions- und Fluoreszenzspektrum des Farbstoffs Rhodamin 6G in ethanolischer Lösung. Bestimmen Sie in beiden Spektren jeweils die Wellenlänge
Physik für Maschinenbau. Prof. Dr. Stefan Schael RWTH Aachen
 Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Im folgenden Kapitel soll nun die Teilcheneigenschaften des Lichts untersucht werden.
 9. Quantenphysik Albert Einstein entwickelte Anfang des 20. Jahrhunderts seine spezielle und allgemeine Relativitätstheorie für die er bis heute bekannt ist. Zur gleichen Zeit leistete Einstein jedoch
9. Quantenphysik Albert Einstein entwickelte Anfang des 20. Jahrhunderts seine spezielle und allgemeine Relativitätstheorie für die er bis heute bekannt ist. Zur gleichen Zeit leistete Einstein jedoch
Abiturprüfung Physik, Leistungskurs
 Seite 1 von 8 Abiturprüfung 2010 Physik, Leistungskurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer
Seite 1 von 8 Abiturprüfung 2010 Physik, Leistungskurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer
Physik für Naturwissenschaften. Dr. Andreas Reichert
 Physik für Naturwissenschaften Dr. Andreas Reichert Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Termine Klausur: 5. Februar?, 12-14 Uhr,
Physik für Naturwissenschaften Dr. Andreas Reichert Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Termine Klausur: 5. Februar?, 12-14 Uhr,
P H Y S I K - Spektroskopie - Helene Plank Stephan Giglberger
 P H Y S I K - Spektroskopie - Helene Plank Stephan Giglberger Warum Spektroskopie auf dem Mars? Befindet sich Wasser auf dem Mars? Gibt es eine Atmosphäre? Aus welchen Elemente besteht sie? Gibt es Leben?
P H Y S I K - Spektroskopie - Helene Plank Stephan Giglberger Warum Spektroskopie auf dem Mars? Befindet sich Wasser auf dem Mars? Gibt es eine Atmosphäre? Aus welchen Elemente besteht sie? Gibt es Leben?
Club Apollo 13, 14. Wettbewerb Aufgabe 1.
 Club Apollo 13, 14. Wettbewerb Aufgabe 1. (1) a) Grundlagenteil: Basteln und Experimentieren Wir haben den Versuchsaufbau entsprechend der Versuchsanleitung aufgebaut. Den Aufbau sowie die Phase des Bauens
Club Apollo 13, 14. Wettbewerb Aufgabe 1. (1) a) Grundlagenteil: Basteln und Experimentieren Wir haben den Versuchsaufbau entsprechend der Versuchsanleitung aufgebaut. Den Aufbau sowie die Phase des Bauens
Medizinische Biophysik Licht in der Medizin.
 4. Transmission Medizinische Biophysik Licht in der Medizin. VI. Wechselwirkungen des Lichts mit der Materie 3. Absorption e) Schwächungsgesetz f) Anwendungen (Absorptionsspektrometrie, Lambert-Beer-Gesetz)
4. Transmission Medizinische Biophysik Licht in der Medizin. VI. Wechselwirkungen des Lichts mit der Materie 3. Absorption e) Schwächungsgesetz f) Anwendungen (Absorptionsspektrometrie, Lambert-Beer-Gesetz)
Zentralabitur 2011 Physik Schülermaterial Aufgabe I ga Bearbeitungszeit: 220 min
 Thema: Eigenschaften von Licht Gegenstand der Aufgabe 1 ist die Untersuchung von Licht nach Durchlaufen von Luft bzw. Wasser mit Hilfe eines optischen Gitters. Während in der Aufgabe 2 der äußere lichtelektrische
Thema: Eigenschaften von Licht Gegenstand der Aufgabe 1 ist die Untersuchung von Licht nach Durchlaufen von Luft bzw. Wasser mit Hilfe eines optischen Gitters. Während in der Aufgabe 2 der äußere lichtelektrische
Vorlesung Messtechnik 2. Hälfte des Semesters Dr. H. Chaves
 Vorlesung Messtechnik 2. Hälfte des Semesters Dr. H. Chaves 1. Einleitung 2. Optische Grundbegriffe 3. Optische Meßverfahren 3.1 Grundlagen dρ 3.2 Interferometrie, ρ(x,y), dx (x,y) 3.3 Laser-Doppler-Velozimetrie
Vorlesung Messtechnik 2. Hälfte des Semesters Dr. H. Chaves 1. Einleitung 2. Optische Grundbegriffe 3. Optische Meßverfahren 3.1 Grundlagen dρ 3.2 Interferometrie, ρ(x,y), dx (x,y) 3.3 Laser-Doppler-Velozimetrie
Simultane UV/VIS-Zweikomponentenanalyse
 Einleitung Polycyclische Aromaten treten als Begleiter des bei der Verbrennung entstehenden Rußes, z. B. beim Betrieb von Dieselfahrzeugen, auf. Da Substanzen aus dieser Stoffklasse stark cancerogen wirken,
Einleitung Polycyclische Aromaten treten als Begleiter des bei der Verbrennung entstehenden Rußes, z. B. beim Betrieb von Dieselfahrzeugen, auf. Da Substanzen aus dieser Stoffklasse stark cancerogen wirken,
Spektralapparat und Absorptionsspektrum
 Ziele Spektralapparat und Absorptionsspektrum Das ist die Idee: Jeder Stoff absorbiert Licht auf bestimmten, für ihn charakteristischen Wellenlängen. Mit einem Spektralapparat ermittelt man diese Wellenlängen
Ziele Spektralapparat und Absorptionsspektrum Das ist die Idee: Jeder Stoff absorbiert Licht auf bestimmten, für ihn charakteristischen Wellenlängen. Mit einem Spektralapparat ermittelt man diese Wellenlängen
Photochemische Reaktion
 TU Ilmenau Chemisches Praktikum Versuch Fachgebiet Chemie 1. Aufgabe Photochemische Reaktion V5 Es soll die Reduktion des Eisen(III)-trisoxalats nach Gleichung (1) unter der Einwirkung von Licht untersucht
TU Ilmenau Chemisches Praktikum Versuch Fachgebiet Chemie 1. Aufgabe Photochemische Reaktion V5 Es soll die Reduktion des Eisen(III)-trisoxalats nach Gleichung (1) unter der Einwirkung von Licht untersucht
Fluoreszenz. Abb. 1: Möglicher Versuchsaufbau
 Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
Solubilisierung in Mizellen. hydrophobe Kette. hydrophile Kopfgruppe. -nicht-ionische. -anionische. -kationische. -zwitterionische Tenside.
 Solubilisierung in Mizellen Abstract 1 Theoretische Grundlagen Tenside sind Moleküle, die aus einem hydrophilen (polaren) und einem hydrophoben (unpolaren) Molekülteil bestehen(abbildung 1). hydrophile
Solubilisierung in Mizellen Abstract 1 Theoretische Grundlagen Tenside sind Moleküle, die aus einem hydrophilen (polaren) und einem hydrophoben (unpolaren) Molekülteil bestehen(abbildung 1). hydrophile
Moderne Physik. Elektromagnetische Schwingungen und Wellen Photonen als Quantenobjekte. LC-Kreis - Schwingkreis. Sinusoszillator (HF-Generator)
 LC-Kreis - Schwingkreis Moderne Physik Kondensator (C Kapazität) Spule (L Induktivität) Elektromagnetische Schwingungen und Wellen Photonen als Quantenobjekte I max I max U max U max Elektromagnetische
LC-Kreis - Schwingkreis Moderne Physik Kondensator (C Kapazität) Spule (L Induktivität) Elektromagnetische Schwingungen und Wellen Photonen als Quantenobjekte I max I max U max U max Elektromagnetische
Spektralapparat. Schriftliche VORbereitung:
 Das ist die Idee: Jeder Stoff absorbiert Licht auf bestimmten, für ihn charakteristischen Wellenlängen. Mit einem ermittelt man diese Wellenlängen und kann so den Stoff identifizieren. In diesem Versuch
Das ist die Idee: Jeder Stoff absorbiert Licht auf bestimmten, für ihn charakteristischen Wellenlängen. Mit einem ermittelt man diese Wellenlängen und kann so den Stoff identifizieren. In diesem Versuch
Aufgabensammlung. zum. RCL "Fotoeffekt"
 Aufgabensammlung zum RCL "Fotoeffekt" S. Gröber Technische Universität Kaiserslautern März 2009 Inhaltsverzeichnis I. Aufgaben 1. Intensität von Licht 2 2. Versuchsaufbau zum RCL Fotoeffekt 2 3. Einsteinsche
Aufgabensammlung zum RCL "Fotoeffekt" S. Gröber Technische Universität Kaiserslautern März 2009 Inhaltsverzeichnis I. Aufgaben 1. Intensität von Licht 2 2. Versuchsaufbau zum RCL Fotoeffekt 2 3. Einsteinsche
Fachbereich Mathematik und Informatik Wintersemester 2013/14 der Universität Marburg Dr. Helga Lohöfer
 Fachbereich Mathematik und nformatik Wintersemester 23/4 der Universität Marburg Dr. Helga Lohöfer Grundlagen der Mathematik für Biologen - Blatt - Abgabe: Montag, den 2..23, vor der Vorlesung, spätestens4:5
Fachbereich Mathematik und nformatik Wintersemester 23/4 der Universität Marburg Dr. Helga Lohöfer Grundlagen der Mathematik für Biologen - Blatt - Abgabe: Montag, den 2..23, vor der Vorlesung, spätestens4:5
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2
 Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 9. Spektralphotometrische Bestimmung einer Gleichgewichtskonstanten: Lambert-Beer und Massenwirkungsgesetz
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 9. Spektralphotometrische Bestimmung einer Gleichgewichtskonstanten: Lambert-Beer und Massenwirkungsgesetz
Zentralabitur 2012 Physik Schülermaterial Aufgabe I ga Bearbeitungszeit: 220 min
 Thema: Wellen und Quanten Interferenzphänomene werden an unterschiedlichen Strukturen untersucht. In Aufgabe 1 wird zuerst der Spurabstand einer CD bestimmt. Thema der Aufgabe 2 ist eine Strukturuntersuchung
Thema: Wellen und Quanten Interferenzphänomene werden an unterschiedlichen Strukturen untersucht. In Aufgabe 1 wird zuerst der Spurabstand einer CD bestimmt. Thema der Aufgabe 2 ist eine Strukturuntersuchung
LD DIDACTIC Leyboldstrasse 1 D Hürth Phone: (02233) Fax: (02233)
 Optik Lichtintensität Strahlungsgesetze LD Handblätter Physik P5.5.2.4 Das Wien sche Verschiebungsgesetz spektrale Aufnahme der Schwarzkörperstrahlung Beschreibung aus SpectraLab (467 250) LD DIDACTIC
Optik Lichtintensität Strahlungsgesetze LD Handblätter Physik P5.5.2.4 Das Wien sche Verschiebungsgesetz spektrale Aufnahme der Schwarzkörperstrahlung Beschreibung aus SpectraLab (467 250) LD DIDACTIC
Raman- Spektroskopie. Natalia Gneiding. 5. Juni 2007
 Raman- Spektroskopie Natalia Gneiding 5. Juni 2007 Inhalt Einleitung Theoretische Grundlagen Raman-Effekt Experimentelle Aspekte Raman-Spektroskopie Zusammenfassung Nobelpreis für Physik 1930 Sir Chandrasekhara
Raman- Spektroskopie Natalia Gneiding 5. Juni 2007 Inhalt Einleitung Theoretische Grundlagen Raman-Effekt Experimentelle Aspekte Raman-Spektroskopie Zusammenfassung Nobelpreis für Physik 1930 Sir Chandrasekhara
So messen Sie die Absorption
 Versuch 9 b Absorptionsspektroskopie, Beer-Lambert-Gesetz Einleitung Das Spektrophotometer ist ein wichtiges Hilfsmittel für den Lebenswissenschaftler. Wenn wir die molekularen Grundlagen biologischer
Versuch 9 b Absorptionsspektroskopie, Beer-Lambert-Gesetz Einleitung Das Spektrophotometer ist ein wichtiges Hilfsmittel für den Lebenswissenschaftler. Wenn wir die molekularen Grundlagen biologischer
Alle Atome haben Massen ungefähr einem vielfachen der Masse des Wasserstoff Atoms.
 02. Atom Page 1 2. Das Atom Atom: kleinster unveränderbarer Bestandteil eines chemischen Elements Charakteristische Eigenschaften von Atomen: Masse, Volumen, Ladung 2.1 Bestimmung der Atommasse expt. Befund:
02. Atom Page 1 2. Das Atom Atom: kleinster unveränderbarer Bestandteil eines chemischen Elements Charakteristische Eigenschaften von Atomen: Masse, Volumen, Ladung 2.1 Bestimmung der Atommasse expt. Befund:
Übungen zur Experimentalphysik 3
 Übungen zur Experimentalphysik 3 Prof. Dr. L. Oberauer Wintersemester 21/211 13. Übungsblatt - 31. Januar 211 Musterlösung Franziska Konitzer ([email protected]) Aufgabe 1 ( ) (2 Punkte) Der Mensch
Übungen zur Experimentalphysik 3 Prof. Dr. L. Oberauer Wintersemester 21/211 13. Übungsblatt - 31. Januar 211 Musterlösung Franziska Konitzer ([email protected]) Aufgabe 1 ( ) (2 Punkte) Der Mensch
Weitere Wellenmerkmale des Lichtes
 Weitere Wellenmerkmale des Lichtes Farben an einer CD/DVD: Oberflächenstruktur: Die Erhöhungen und Vertiefungen (Pits/Lands) auf einer CD-Oberfläche wirkt als Reflexionsgitter. d Zwischen den reflektierten
Weitere Wellenmerkmale des Lichtes Farben an einer CD/DVD: Oberflächenstruktur: Die Erhöhungen und Vertiefungen (Pits/Lands) auf einer CD-Oberfläche wirkt als Reflexionsgitter. d Zwischen den reflektierten
Versuchsanleitung. Vergleichen Sie das direkt hinter dem Monochomator und das hinter der Faser gemessene Spektrum. Wie gut ist die Einkoppeleffizienz?
 Versuch 38: Optische und elektrische Eigenschaften von mikrostrukturierten Halbleitern Versuchsanleitung Vorbemerkung: Dieser Versuch bietet Ihnen viele Möglichkeiten, die gegebenen Proben mit den zur
Versuch 38: Optische und elektrische Eigenschaften von mikrostrukturierten Halbleitern Versuchsanleitung Vorbemerkung: Dieser Versuch bietet Ihnen viele Möglichkeiten, die gegebenen Proben mit den zur
Polarisation durch Reflexion
 Version: 27. Juli 2004 Polarisation durch Reflexion Stichworte Erzeugung von polarisiertem Licht, linear, zirkular und elliptisch polarisiertes Licht, Polarisator, Analysator, Polarisationsebene, optische
Version: 27. Juli 2004 Polarisation durch Reflexion Stichworte Erzeugung von polarisiertem Licht, linear, zirkular und elliptisch polarisiertes Licht, Polarisator, Analysator, Polarisationsebene, optische
Einfaches Spektroskop aus alltäglichen Gegenständen
 Illumina-Chemie.de - Artikel Physik aus alltäglichen Gegenständen Im Folgenden wird der Bau eines sehr einfachen Spektroskops aus alltäglichen Dingen erläutert. Es dient zur Untersuchung von Licht im sichtbaren
Illumina-Chemie.de - Artikel Physik aus alltäglichen Gegenständen Im Folgenden wird der Bau eines sehr einfachen Spektroskops aus alltäglichen Dingen erläutert. Es dient zur Untersuchung von Licht im sichtbaren
