Aus der Klinik und Poliklinik für Strahlentherapie der. Friedrich- Alexander- Universität. Erlangen- Nürnberg. Direktor: Prof. Dr. med.
|
|
|
- Michaela Straub
- vor 7 Jahren
- Abrufe
Transkript
1 Ergebnisse der Brachytherapie bei Vaginal- und Vulvakarzinom mit Analyse des rezidivfreien Überlebens, des tumorfreien Überlebens und des Gesamtüberlebens unter Evaluation einzelner Prognosefaktoren. Aus der Klinik und Poliklinik für Strahlentherapie der Friedrich- Alexander- Universität Erlangen- Nürnberg Direktor: Prof. Dr. med. Rainer Fietkau Der Medizinischen Fakultät der Friedrich-Alexander-Universität Erlangen-Nürnberg zur Erlangung des Doktorgrades Dr. med. Vorgelegt von Camilla Wekenborg Aus Erlangen
2 Als Dissertation genehmigt von der Medizinischen Fakultät der Friedrich-Alexander-Universität Erlangen-Nürnberg Vorsitzender des Promotionsorgans: Gutachter: Gutachter: Prof. Dr. Dr. h. c. J. Schüttler Prof. Dr. V. Strnad Prof. Dr. R. Fietkau Tag der mündlichen Prüfung: 29. November 2016
3 Inhaltsverzeichnis Inhaltsverzeichnis... I Tabellenverzeichnis... III Abbildungsverzeichnis... IV Abkürzungsverzeichnis... V 1. Zusammenfassung Hintergrund und Ziele Methoden (Patienten, Material und Untersuchungsmethoden) Ergebnisse und Beobachtungen Praktische Schlussfolgerungen Abstract Einleitung Ziel der Arbeit Epidemiologie und Ätiologie Klassifikation und Stadieneinteilung Patienten und Methoden Studiendesign und angewandte Methoden Patientinnen mit Vaginalkarzinom Patientinnen mit Vulvakarzinom Chirurgie Perkutane Strahlentherapie und Brachytherapie Chemotherapie Nebenwirkungen und Nachsorge Ergebnisse Analyse der Patientinnen mit Vaginalkarzinom Deskriptive Analyse Kaplan- Meier- Analyse bezüglich des RFS Kaplan- Meier- Analyse bezüglich des DFS Kaplan- Meier- Analyse bezüglich des OS Subanalyse der primär behandelten Patientinnen Analyse der Patientinnen mit Vulvakarzinom Deskriptive Analyse Kaplan- Meier- Analyse bezüglich des RFS I
4 Kaplan- Meier- Analyse bezüglich des DFS Kaplan- Meier- Analyse bezüglich des OS Subanalyse der primär behandelten Patientinnen Diskussion Methoden Ergebnisse Ausblick Literaturverzeichnis II
5 Tabellenverzeichnis Tabelle 1: Stadieneinteilung des Vaginal CA; FIGO und TNM Klassifikation Tabelle 2: Stadieneinteilung des Vulva CA; FIGO und TNM Klassifikation mit Therapieempfehlung Tabelle 3: Simultane Chemotherapie zur perkutanen Radiotherapie bei Vaginal CA Tabelle 4: Grad der Hautreaktion akut nach Brachytherapie bei Vaginal CA Tabelle 5: Grad der Mukositis akut nach Brachytherapie bei Vaginal CA Tabelle 6: Grad der Hautreaktion akut nach perk. RT bei Vaginal CA Tabelle 7: Grad der Mukositis akut nach perk. RT bei Vaginal CA Tabelle 8: Andere späte Nebenwirkungen der Brachytherapie bei Vaginal CA Tabelle 9: Remission 6 Wochen nach Therapie bei Vaginal CA Tabelle 10: Metastasenlokalisation bei Vaginalkarzinom Tabelle 11: Nebenwirkungsprofil Vaginal CA (primär bestrahlt) Tabelle 12: Grad der Hautreaktion akut nach Brachytherapie bei Vulva CA Tabelle 13: Grad der Mukositis akut nach Brachytherapie bei Vulva CA Tabelle 14: Grad der Hautreaktion akut nach perk. RT bei Vulva CA Tabelle 15: Grad der Mukositis akut nach perk. RT bei Vulva CA Tabelle 16: Andere späte Nebenwirkungen der Brachytherapie bei Vulva CA Tabelle 17: Remission 6 Wochen nach Therapie bei Vulva CA Tabelle 18: Metastasenlokalisation bei Vulvakarzinom Tabelle 19: Nebenwirkungsprofil Vulva CA (primär bestrahlt) Tabelle 20: Publizierte Daten zu DFS bei Vaginal CA im Überblick III
6 Abbildungsverzeichnis Abbildung 1: KMA bezüglich des RFS bei Vaginal CA (Alter bei Therapie) Abbildung 2: KMA bezüglich des RFS bei Vaginal CA (Dosis der PDR-BT in Gy) Abbildung 3: KMA bezüglich des DFS bei Vaginal CA (Alter bei Therapie). Abbildung 4: KMA bezüglich des DFS bei Vaginal CA (Histologisches Grading) Abbildung 5: KMA bezüglich des DFS Vaginal CA (N- Stadium) Abbildung 6: KMA bezüglich des DFS Vaginal CA (primär behandelt) Alter bei Therapie Abbildung 7: KMA bezüglich des RFS Vulva CA (Alter bei Therapie) Abbildung 8: KMA bezüglich des RFS bei Vulva CA (R- Status) Abbildung 9: KMA bezüglich des DFS Vulva CA (Alter bei Therapie) Abbildung 10: KMA bezüglich des OS bei Vulva CA (N- Stadium) Abbildung 11: KMA bezüglich des RFS bei Vulva CA (primär behandelt) Alter bei Therapie Abbildung 12: KMA bezüglich des DFS bei Vulva CA (primär behandelt) Alter bei Therapie Abbildung 13: KMA bezüglich des DFS bei Vulva CA (primär behandelt) R- Status Abbildung 14: KMA bezüglich des OS bei Vulva CA (primär behandelt) N- Stadium IV
7 Abkürzungsverzeichnis Bds BT Bzw CA CIS DFS FIGO Ggf Gy HDR KMA MRT OS PDR RFS RT TNM Vs WHO beidseits Brachytherapie beziehungsweise Carcinom Carcinoma In Situ Disease Free Survival (krankheitsfreies Überleben) Fédération Internationale de Gynécologie et d'obstétrique gegebenenfalls Gray (physikalische Einheit) High Dose Rate Kaplan- Meier- Analyse Magnetresonanztomographie Overall Survival (Gesamtüberleben) Pulsed Dose Rate Recurrence Free Survival (rezidivfreies Überleben) Radiotherapie Tumor Nodes Metastasis (Klassifikation) versus (im Gegensatz zu) World Health Organisation V
8 1. Zusammenfassung 1.1. Hintergrund und Ziele Karzinome der Vagina und Vulva sind selten und Ziel dieser Arbeit war es, die Ergebnisse der Brachytherapie (BT) unter Berücksichtigung der aktuellen Literatur zu evaluieren und mehr über die Prognosefaktoren herauszufinden, die das RFS, DFS und OS beeinflussen Methoden (Patienten, Material und Untersuchungsmethoden) In der retrospektiven Studie wurden die Daten von 53 Patientinnen erhoben, die im Zeitraum von 1998 bis 2009 an der Strahlenklinik der Universität Erlangen- Nürnberg therapiert worden sind. Die Analyse der Überlebensraten erfolgte mit der Kaplan- Meier- Methode. Vaginalkarzinom (n=30): Das Alter betrug 69 Jahre im Median, 70% (21/30) Patientinnen erhielten vor der Brachytherapie eine kombinierte Radiochemotherapie. Das Follow-up lag im Median bei 71 Monaten. Die applizierte Dosis der BT betrug 25 Gy im Median. Vulvakarzinom (n=23): Im Median lag das Alter der Patientinnen bei 71 Jahren, 48% (11/23) Patientinnen erhielten zusätzlich eine perkutane Radiochemotherapie. Das Follow-up betrug im Mittelwert 47 Monate. Die applizierte Dosis der BT betrug 55 Gy im Median Ergebnisse und Beobachtungen Folgende Zahlen beziehen sich auf alle Patientinnen- primär behandelte Patientinnen und Rezidiv-Patientinnen, Zahlen zur Subanalyse primär behandelter Patientinnen finden sich in Klammern. Vaginalkarzinom: Die 5 JÜR des RFS betrug 46,7% (50%). Das DFS betrug nach 5 Jahren für FIGO I/II 35,7% (44,4%) und für FIGO III/IV 50% (38,9%), wobei FIGO IV 40% darstellte. Das OS betrug nach 5 Jahren 31,6% (26,7%). Nach der BT zeigten 6,6% der Patientinnen eine lokale Hautreaktion (Grad 2, 3) und 20% eine Mukositis (Grad 2,3). 1
9 Eine Behandlung mit PDR-BT mit einer Dosis von >50 Gy zeigte nach 5 Jahren 33,3% vs 13,3% OS (p<0,05). Vulvakarzinom: Die 5 JÜR des RFS bezifferte sich auf 21,7% (23,8%) und des OS auf 11,1% (12,5%). Eine signifikant bessere Prognosen zeigten Patientinnen unter 65 Jahre mit einer 5 JÜR von 57,1% (66,7%) vs 12,5% (6,7%) im RFS (p<0,05). In 30% der Fälle wurde eine Mukositis Grad 1 bis 3 und in 21,7% der Fälle eine Hautreaktion Grad 1 bis 4 festgestellt. Gute Ergebnisse wurden durch vorherige Operation erzielt (23,5% vs 16,7% 5 JÜR DFS) Praktische Schlussfolgerungen Die signifikant beste Prognose haben Patientinnen unter 70 Jahren mit niedrigem Tumorstadium. Bei Patientinnen mit Vaginalkarzinom ist eine höhere Dosis in der PDR- BT, bei Vulvakarzinom eine Operation ein wichtiger prognostischer Faktor. Die beste Prävention bleibt die regelmäßige gynäkologische Untersuchung. 2
10 1.5. Abstract Purpose: The Carcinoma of the vagina and vulva is a rare disease. By taking recent studies under advisement, the purpose of this study is to evaluate the results of brachytherapy (BT) and to point out factors that influence RFS, DFS and OS. Methods and Materials: 53 patients, who received treatment between 1998 and 2009 at the university of Erlangen-Nürnberg, were retrospectively reviewed. RFS, DFS and OS were analyzed by Kaplan-Meier- Method. Carcinoma of the vagina (n=30): The median age was 69 years and 21/30 patients have been treated with chemoradiotherapy. The median follow-up was 71 months. The median applied dose in PDR-BT was 25 Gray. Carcinoma of the vulva (n=23): The median age was 71 years. Almost half (11/23) received chemoradiotherapy also. The mean follow-up was 47 months. In PDR- BT the median applied dosage was 55 Gray. Results: Following numbers are concerning all patients- with or without recurrent tumor, results of the analysis primarily treated patients can be found inside the parenthesis. Carcinoma of the vagina: The 5 year RFS and OS were 46.7% (50%) and 31.6% (26.7%), respectively. Patients with FIGO I/II showed 35.7% (44.4%) and FIGO III/IV 50% (38.9%) 5-year DFS. 40% of all patients were classified as FIGO IV. After BT mainly local toxicity were observed (skin 6.6% and mucosa 20%). Patient with PDR- BT treatment in higher dosage (>50 Gray) lived significantly longer with a 5 year OS of 66.7% as opposed to 13.3% concerning patient treated with PDR-BT in lower dosage (p<0.05). Carcinoma of the vulva: The 5- year RFS and OS were 21.7% (23.8%) and 11.1% (12.5%), respectively. Best prognosis factor was an age younger than 65 years with a 5- year RFS of 57.1% (66.7%) versus 12.5% (6.7%) of the elderly (p<0.05). Mainly local toxicity was observed (30% mucosa, 21.3% skin). Good results were achieved with a prior operation (5-year DFS of 23.5% vs 16.7%). Conclusion: The significantly best prognosis showed patients younger than 70 years with low grade tumor. Patients with carcinoma of the vagina benefit of PDR-BT in higher dosage (>50Gy). A prior operation and adjuvant BT is the best option for patients with carcinoma of the vulva. Best prevention would still be a frequent gynecological examination. 3
11 2. Einleitung In der gynäkologischen Onkologie spielen die malignen Neoplasien der Vagina und Vulva eine untergeordnete Rolle. Es betrifft im Vergleich eher wenige, vor allem ältere Patientinnen und es handelt sich hier um einen sensiblen Bereich der weiblichen Anatomie [5]. Dennoch gebührt es sich, diesen Patientinnen die nötige Aufmerksamkeit entgegen zu bringen und ein fundiertes und evidenzbasiertes Therapiekonzept anbieten zu können, was eine lokale Tumorkontrolle gewährleistet und die Lebensqualität nicht zu sehr einschränkt. Laut Robert- Koch- Institut gehört das Vulvakarzinom allerdings zu den Tumoren mit steigender Inzidenz in den letzten Jahren erkrankten Frauen an einem Vulvakarzinom, im Jahr 2000 waren es weniger als die Hälfte [26]. Das Vaginalkarzinom zeigt eine unverändert niedrige Inzidenz bei 0,4/ Frauen pro Jahr [3]. Histologisch findet man, sowohl beim Vaginal- als auch beim Vulvakarzinom, vor allem Plattenepithelkarzinome (90%), deren Ursprung HPV assoziiert sein kann [3; 26]. Zur optimalen Therapieplanung der Patientinnen ist es heute Standard, das individuelle Therapiekonzept in interdisziplinären Tumorboards festzulegen (Operation, Chemotherapie und Strahlentherapie)[1]. Auf Grund der anatomischen Gegebenheiten des weiblichen äußeren Genitale und kleinen Beckens ist die Planung einer Strahlentherapie auf diesem Gebiet eine Herausforderung. Die Brachytherapie ermöglicht, vor allem mit 3D Techniken der MRT-gestützten Brachytherapie (Imageguided brachytherapy) und mit speziell entwickelten Applikatoren, auch auf engstem Raum eine gezielte Bestrahlung des Tumorgewebes unter Schonung der umliegenden wichtigen Strukturen des kleinen Beckens (Harnblase, Harnleiter und Rektum) [2; 16]. 4
12 2.1. Ziel der Arbeit In der vorliegenden Arbeit wird über die Ergebnisse der Brachytherapie bei Vaginalund Vulvakarzinom berichtet. Besondere Aufmerksamkeit galt hier dem rezidivfreien Überleben, dem Überleben ohne Tumor und dem Gesamtüberleben. Es wurde außerdem die Therapieverträglichkeit durch Erhebung eines Nebenwirkungsprofils überprüft Epidemiologie und Ätiologie Vaginalkarzinom Mit 2-3% macht das Vaginalkarzinom einen kleinen Teil der malignen Erkrankungen des weiblichen Genitaltraktes aus [3; 13; 25]. Die Inzidenz liegt bei 0,4/ Frauen pro Jahr, die eines Carcinoma in situ (CIS) sogar nur bei 0,2/ Frauen pro Jahr. [3]. Primäre Vaginalkarzinome sind sehr selten, oft handelt es sich auch um einen Tumor der Nachbarorgane im kleinen Becken, der infiltrierend eingewachsen ist. Außerdem metastasieren häufig andere gynäkologische Tumore sekundär in die Vagina (30% aller Patientinnen mit Vaginalkarzinom hatten in den 5 Jahren davor ein intraepitheliales oder invasives Zervixkarzinom). Auch das maligne Melanom kann sich hier manifestieren [3; 33]. Die Ätiologie des primären Vaginalkarzinoms ist unklar, es betrifft häufiger postmenopausale Frauen jedoch ist die Anzahl von HPV- assoziierten Erkrankungen bei jungen Frauen steigend und der Ätiologie des Zervixkarzinom ähnlich [25; 33]. Vulvakarzinom Das Vulvakarzinom und seine Vorstufen gehören zu den Tumoren mit steigender Inzidenz. Insgesamt liegt sie bei 2/ Frauen pro Jahr, wobei nur 0,4/ Einwohner unter den 30 Jährigen erkranken und schon 20/ Frauen unter den 5
13 70 jährigen Patientinnen betroffen sind [3]. Dennoch sind auch zunehmend jüngere Frauen betroffen [1]. Die Ätiologie des Vulvakarzinoms zeigt ein sehr buntes Bild. Am häufigsten ist dennoch das primäre Plattenepithelkarzinom der Vulva [14; 26; 33]. Es finden sich außerdem auch Maligne Melanome, Adenokarzinome (zum Beispiel ausgehend von einem Rektumkarzinom), Basaliome (insbesondere ausgehend von der Bartholin- Drüse) und Sarkome [24]. An dieser Stelle soll auch erwähnt werden, dass eine Patientin in dieser Arbeit eine vulväre Metastase eines uterinen Karzinosarkoms (Müllerscher Mischtumor) aufzuweisen hatte [18]. Am häufigsten finden sich jedoch Metastasen anderer gynäkologischen Tumore, wie der Mamma, des Endometriums und der Zervix [26; 1; 33]. Als besondere Tumorentität ist noch der Morbus Paget zu nennen (2% aller Vulvaneoplasien), der streng genommen kein Plattenepithelkarzinom darstellt, sondern von Hautanhangsdrüsen abstammt und nicht mit dem Morbus Paget der Mamille zu verwechseln ist [33]. Eindeutige Risikofaktoren konnten bisher nicht ermittelt werden, jedoch zeigen sich Hinweise auf einen Zusammenhang der Erkrankung mit einer HPV- Infektion, Immunsupression, Rauchen, langjähriger Alkoholmissbrauch so wie andere intraepitheliale Neoplasien des Anogenitalbereichs vor allem bei jüngeren Patientinnen (mittleres Alter 55 Jahre) [1]. Eine Erkrankung unabhängig von einer HPV- Infektion ist häufiger (65-80% der Fälle) und zeigt sich vor allem bei älteren Patientinnen (mittleres Alter 70 Jahre). Hier zeigten sich chronisch entzündliche Hauterkrankungen wie der Lichen sklerosus als wichtiger Risikofaktor [26; 1] Klassifikation und Stadieneinteilung Intraepitheliale Neoplasien der Vagina und Vulva werden durch die WHO in verschiedene Schweregrade eingeteilt (VIN Stadien). VIN I bedeutet eine leichte, VIN II eine mäßige und VIN III eine schwere Dysplasie/intraepitheliale Neoplasie [33]. 6
14 Im onkologischen Bereich wird vor allem für Staging und Therapieempfehlung mit der FIGO und TNM Klassifikation gearbeitet. R- Status beschreibt den Residualtumor. Zur definitiven Therapieplanung ist eine detaillierte Bildgebung mittels Magnetresonanztomographie, am Besten in 3D Technik und mit Applikatorsystem, unerlässlich [1; 3; 25; 28; 31 33]. Vaginalkarzinom Einteilung des T- Stadium: Stadium 0: Carcinoma in situ Stadium I: Die Ausdehnung beschränkt sich auf die Vaginalwand. Stadium II: Ausdehnung auf das paravaginale Gewebe, Beckenwand frei Stadium III: Das Karzinom erreicht die Beckenwand. Stadium IV A: Ausbreitung über das kleine Becken hinaus mit Mukosabefall von Rektum und Blase Stadium IV B: Ausbreitung auf entfernte Organe (Fernmetastasen) Einteilung des N- Stadium: Ein negativer Lymphknotenstatus entspricht N0, positiver Lymphknotenstatus N1/N2 (je nach Menge befallener Lymphknoten) und unklarer Lymphknotenstatus NX. Einteilung des M- Stadium: Liegt eine Fernmetastase vor, wird mit M1 klassifiziert. Bei unklarem Status MX und M0 bedeutet frei von Fernmetastasen. FIGO T- Stadium N- Stadium M- Stadium I T1 N0 M0 II T2 N0 M0 III T3/ T1-3 N0/N1 M0 IV A T4 Jedes N M0 IV B Jedes T Jedes N M1 Tabelle 1: Stadieneinteilung des Vaginal CA; FIGO und TNM Klassifikation [3; 14; 33] 7
15 Vulvakarzinom FIGO TNM Kriterien Therapieempfehlung 0 Tis Carcinoma in situ, VIN III I A T1a N0 M0 Durchmesser 2mm, Invasionstiefe 1mm, negative Leistenlymphknoten I B T1b N0 M0 Tumor begrenzt auf Vulva und Perineum, Durchmesser> 2mm, Invasionstiefe >1mm II T2 N0 M0 Tumor jeder Größe mit Infiltration einer oder mehrerer folgender Strukturen: unteres Drittel der Urethra, Vagina oder Anus mit negativem Lymphknotenstatus III T1-2 N1-2 M0 Wie FIGO II mit Infiltration unteres Drittel der Urethra, Vagina oder Anus mit positivem Exzision im Gesunden Radikale Exzision des Tumors ohne inguinale Lymphonodektomie Radikale Exzision des Tumors mit bds inguinaler Lymphonodektomie (bei einseitigem Tumorsitz ipsilateral) Radikale Exzision ggf Vulvektomie, einseitige ggf beidseiteige Lymphonodektomie, Resektion der betroffenen Strukturen, ggf primäre Radiochemotherapie wenn Kontinezerhalt nicht möglich Wie FIGO II mit radikaler Vulvektomie und beidseitiger Lymphonodektomie 8
16 Lmyphknotenstatus IV A T3 N0-3 M0 Wie FIGO III mit Wie FIGO III T1-2 N3 Befall der Mukosa in Blase/Rektum oder Fixierung am Beckenknochen IV B T1-3 N0-3 M1 Fernmetastasierung Palliative Operation Ggf primäre Radiochemotherapie Tabelle 2: Stadieneinteilung des Vulva CA; FIGO und TNM Klassifikation mit Therapieempfehlung [33] Generell gilt bei N2 (3 oder mehr betroffene Lymphknoten und/oder intranodaler Befall >5mm und/oder extrakapsulare Ausbreitung) auch die pelvine Lymphonodektomie [1; 14; 25; 26; 33]. 3. Patienten und Methoden 3.1. Studiendesign und angewandte Methoden Von April 2013 bis Juli 2015 wurden Daten von den Patientinnen gesammelt, die in einem Zeitraum von Mai 1998 bis September 2009 in der Universitätsstrahlenklinik in Erlangen an einem Vaginal- oder Vulvakarzinom mittels Brachytherapie behandelt worden sind. Bei einem untersuchten Patientenkollektiv von n=53 Patientinnen waren 23 (43,4%) von einem Vulvakarzinom betroffen, 30 Patientinnen litten an einem Vaginalkarzinom (56,6%). 9
17 Die gesammelten Patientendaten wurden in einer retrospektiv statistischen Studie erfasst. Für die Sammlung, Verwaltung und Verwertung dieser Daten wurde mit der Software IBM SPSS Statistics 22 gearbeitet. Die Auswertung erfolgte für Patientinnen mit Vaginalkarzinom getrennt von den Patientinnen mit Vulvakarzinom. Es wurden die Eigenschaften der Gruppen eingehend untersucht, wie Alter bei Therapie, Therapieintention, Rezidivstatus, Histologie des Tumors, Vorbestrahlung mit Aufschlüsselung der applizierten Dosis, Art der vorausgegangen Therapie, Operationsformen, genaue Tumorklassifikation, Art der Brachytherapie, Art der Chemotherapie, Art der perkutanen Radiotherapie, Nebenwirkungen und die akute Reaktion auf Bestrahlung mittels Brachytherapie und/oder perkutaner Strahlentherapie (Grad der Hautreaktionen und Mukositis). Besonders ausführlich erfolge die Analyse der geschätzten Überlebenswahrscheinlichkeit mit der Kaplan- Meier- Methode. Diese spezielle Formel berechnet die Wahrscheinlichkeit für eine Gruppe von Patientinnen, das ein bestimmtes Ereignis innerhalb eines festgesetzten Zeitraumes (zum Beispiel 5 oder 10 Jahre) nicht eintritt. So wurden die 5 und 10 JÜR errechnet und graphisch zur Darstellung gebracht mit der Angabe der mittleren Überlebenszeit [15; 27]. Die Kaplan- Meier- Analyse wurde bei Vaginalkarzinom und Vulvakarzinom getrennt berechnet und somit die 5 JÜR bezüglich des Recurrence Free Survival RFS (geschätzte Wahrscheinlichkeit der Anzahl der Patientinnen in %, die nach 5 Jahren frei von einem lokalen Rezidiv sind), des Disease Free Survial DFS (geschätzte Wahrscheinlichkeit der Anzahl der Patientinnen in %, die nach 5 Jahren weder ein lokales Rezidiv noch eine Fernmetastasierung haben) und des OS (geschätzte Wahrscheinlichkeit der Anzahl der Patientinnen in %, die nach 5 Jahren noch am Leben sind) ermittelt. Die Variablen, die hinsichtlich ihres Einflusses auf die 5 und 10 JÜR des RFS, des DFS und des OS untersucht wurden, waren: Alter bei Therapie, Rezidivbehandlung, Vorbestrahlung, Vorausgegangene Operationen, Histologisches Grading des Tumors, Klassifikation und Stadieneinteilung, einzelne Parameter der Brachytherapie, verwendete Chemotherapeutika und perkutane Radiotherapie. 10
18 Bei jeder Analyse wurden außerdem der Log-Rank- Test (vergleicht die Gleichheit der Überlebensverteilungen, wobei alle Zeitpunkte in diesem Test gleich gewichtet werden) und der Breslow- Test (vergleicht die Gleichheit der Überlebensverteilungen, wobei die Zeitpunkte mit der Anzahl der gefährdeten Fälle zu jedem Zeitpunkt gewichtet werden) erhoben [4]. Das Signifikanzniveau wurde auf p<0,05 festgelegt. [9] Patientinnen mit Vaginalkarzinom Von den n=30 Patientinnen mit Vaginalkarzinom litten 18 an einem Karzinom (60%), 2 an einem Malignen Melanom (6,7%) und 10 an einer Metastase in der Vagina (33,3%). Die Patientinnen waren zum Zeitpunkt der Therapie im Median 69,42 Jahre alt (min=42; max=84). Die Intention der Therapie war bei 14 Patientinnen kurativ mit alleiniger Radiotherapie (46,7%), bei 10 Patientinnen kurativ postoperativ (33,3%) und bei 6 Patientinnen palliativ (20,0%). Bei 17 Patientinnen wurde das Rezidiv behandelt (56,7%), während bei 13 Patientinnen der Primärtumor bestrahlt wurde (43,3%). Von den 17 Patientinnen mit Rezidiv lagen folgende Primärtumoren vor: in 7 Fällen ein Endometriumkarzinom (41,1%), in 3 Fällen ein Vaginalkarzinom (17,6%), in 2 Fällen um ein Vulvakarzinom (11,8%), in 2 Fällen um ein Zervixkarzinom (11,8%) und in jeweils einem Fall (5,9%) um ein Mammakarzinom, Müllerscher Mischtumor des Uterus und ein Rektumkarzinom. 24 Patientinnen (80%) sind zum ersten Mal bestrahlt worden. 6 Patientinnen (20%) waren vorbestrahlt mit einem Median 54,9 Gy (min=50; max=62,4gy) am Primärtumor und einem Median von 50 Gy (min=40; max= 60) am Lymphabflussgebiet. Zwischen der Vorbestrahlung und der Brachytherapie lag ein Median von 28,20 Monaten (min=5; max=99). 11 Patientinnen wurden vor der Brachytherapie operiert (36,7%). Die Mehrheit von 4 Patientinnen unterzogen sich einer Tumorresektion (13,3%), 3 erhielten eine Tumorresektion mit Lymphknotenresektion inguinal (10%), 2 Patientinnen wurden mit 11
19 einer Hysterektomie nach Wertheim- Meigs behandelt (6,7%) und jeweils eine Patientin unterzog sich einem Tumordebulking (3,3%) und einer Exenteration des kleinen Beckens (3,3%). Das Zeitintervall zwischen Operation und Brachytherapie betrug im Median 90 Tage (min=30; max=150). 19 Patientinnen wurden ohne Operation bestrahlt (63,3%). In der Histologie wiesen die 30 Patientinnen folgende Diagnosen auf: in 16 Fällen ein Plattenepithelkarzinom (53,3%), in 10 Fällen ein Adenokarzinom (33,3%), in 2 Fällen ein Malignes Melanom (6,7%) und in jeweils einem Fall (3,3%) ein Sarkom und ein Müllerscher Mischtumor. Die bestrahlten Tumore der Patientinnen waren in 11 Fällen mit G2 (36,7%), in 10 Fällen mit G3 (33,3%) und in 9 Fällen mit GX klassifiziert (30%). Als L0 wurden 23 Patientinnen klassifiziert (76,7%), L1 lag in 7 Fällen vor (23,3%). Die Tumorgröße war im Median 26,5mm (min= 6; max= 60) bei n=18. Die Infiltrationstiefe war im Median 10mm (min=2; max=30) bei n=11. Folgende FIGO Klassifikationen waren vorhanden: 9 Fälle mit FIGO I (30%), 5 Fälle mit FIGO II (16,7%), 4 Fälle mit FIGO III (13,3%) und 12 Fälle mit FIGO IV (40%). 2 Patientinnen hatten R-Status RO (6,7%), 8 Patientinnen R1 (26,7%) und die Mehrheit der Patientinnen hatten R2 (66,7%). Die Mehrheit der Patientinnen erhielten eine Brachytherapie nach dem PDR-Verfahren n=22 (73,3%), 7 Patientinnen erhielten eine Brachytherapie mit kombinierten PDR/HDR-Verfahren (23,3%) und nur 1 Patientin erhielt eine Brachytherapie mit HDR- Verfahren (3,3%). Im Median war die Dosis der Brachytherapie im PDR-Verfahren 25 Gy (min=10; max= 85) mit einer Pulsdosis von 0,51 Gy im Median (min=0,30; max=0,75). Im HDR-Verfahren war die applizierte Dosis im Median 18 Gy (min= 5; max= 35). Die Dauer der Brachytherapie im PDR-Verfahren betrug im Median 40 Stunden (min=13; max=125). In den 29 Fällen, in denen mit PDR-Verfahren gearbeitet wurde, wurde in 19 Fällen ein Template benutzt (63,3%) und in 10 Fällen nicht (33,3%). Im Median wurden 7 Tubes benutzt (min=3; max=18). Die Referenzisodosis betrug im Median 85 % (min=70; max=105). 12
20 Die Mehrheit der Patientinnen (n=26) erhielt keine simultane Chemotherapie während der Brachytherapie, 4 Patientinnen schon (13,3%), mit jeweils DTCI/Cisplatin/Tamoxifen, Cisplatin Monotherapie, Carboplatin Monotherapie und Taxol. 21 Patientinnen erhielten eine perkutane Radiotherapie (70%). 19 davon erhielten die perkutane Radiotherapie vor der Brachytherapie (63,3%)- mit einem Zeitintervall von 7 Tagen im Median (min=1; max=30)- und 2 Patientinnen während der Brachytherapie (6,7%). Die applizierte Dosis in der perkutanen Radiotherapie betrug bei allen Patientinnen (n=21) am Primärtumor und im Lymphabflussgebiet 50,4 Gy im Median (min=27,15; max=55,8). 9 von diesen 21 Patientinnen erhielten eine simultane Chemotherapie zur perkutanen Radiotherapie (42,9%). Folgende Chemotherapeutika waren vertreten: Chemotherapie simultan zur perkutanen Radiotherapie Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig 5-Fluorouracil 1 3,3 11,1 11,1 Cisplatin 3 10,0 33,3 44,4 Cisplatin + 5-FU 1 3,3 11,1 55,6 5-FU + Mitomycin 1 3,3 11,1 66,7 Carboplatin 1 3,3 11,1 77,8 Cisplatin/Detimedac 1 3,3 11,1 88,9 Taxol 1 3,3 11,1 100,0 Gesamtsumme 9 30,0 100,0 Fehlend System 21 70,0 Gesamtsumme ,0 Tabelle 3: Simultane Chemotherapie zur perkutanen Radiotherapie bei Vaginal CA 3.3. Patientinnen mit Vulvakarzinom Von diesen 23 Patientinnen litten 15 an einem Vulvakarzinom (65,2%), 4 an einer Vulvametastase (17,4%), 2 an einem Malignen Melanom der Vulva (8,7%) und jeweils eine Patientin an einem Siegelringzellhaltigen Adenokarzinom (4,3%) und einem Morbus Paget (4,3%). 13
21 Das Alter dieser Patientinnen lag im Median bei 71 Jahren (min=44; max=89). Bei den meisten Patientinnen (n=15) wurde nach einer Operation kurativ behandelt (65,2%). Bei 5 Patientinnen war die Intention kurativ zu behandeln mit alleiniger Radiotherapie (21,7%) und bei 3 Patientinnen wurde palliativ bestrahlt (13%). Der bestrahlte Tumor war bei 14 Patientinnen der Primärtumor (60,9%) und bei 9 Patientinnen ein Rezidiv (39,1%). Von den 9 Patientinnen lag in der Mehrheit der Fälle (n=5) ein Rezidiv eines Vulvakarzinoms vor (55,6%). In jeweils einem Fall lag ein Rezidiv der folgenden Tumore vor: Adenoid-zystisches Karzinom der Bartholin-Drüse (11,1%), Malignes Melanom (11,1%), Merkel-Zell-Karzinom an der Vulva (11,1%) und ein Endometriumkarzinom (11,1%). Die deutliche Mehrheit aller Patientinnen war nicht vorbestrahlt (n=21/91,3%), nur ein kleiner Teil hat sich schon einmal einer radiotherapeutischen Behandlung unterzogen (n=2/8,7%). Die Therapie lag in einem Fall 26 Monate (Dosis am Primärtumor 63 Gy und am Lymphabflussgebiet 50,40 Gy) zurück. Im anderen Fall war die Therapie bereits 228 Monate her, mit einer damals applizierten Dosis am Primärtumor von 20 Gy. Die meisten Patientinnen wurden vor der Brachytherapie operiert (n=17/73,9%). 6 Patientinnen unterzogen sich keiner OP (26,1%). Bei den operierten Patientinnen wurden in den meisten Fällen (n=10/43,5%) eine Tumorresektion mit Lymphknotenresektion inguinal durchgeführt. In 5 Fällen wurde eine alleinige Tumorresektion durchgeführt (21,7%) und in jeweils einem Fall ein Debulking (4,3%) und eine Exenteration des kleinen Beckens (4,3%). Das Zeitintervall zwischen Operation und Brachytherapie lag im Median bei 60 Tagen (min=8; max= 90). In der Histologie ließen sich bei den 23 Patientinnen in 15 Fällen ein Plattenepithelkarzinom nachweisen (65,2%), in 3 Fällen ein Malignes Melanom (13%), in ebenfalls 3 Fällen ein Adenokarzinom (13%) und in jeweils einem Fall ein Morbus Paget (4,3%) und ein Merkel-Zell-Tumor (4,3%). Mit G1 wurden 5 Patientinnen klassifiziert (21,7%), mit G2 6 Patientinnen (26,1%), mit G3 7 Patientinnen (30,4%) und mit GX 5 Patientinnen (21,7%). Somit war die Mehrheit der Patientinnen (30,4%) mit G3 klassifiziert. Bei 14 Patientinnen lag L0 vor (60,9%) und bei 9 Patientinnen L1 14
22 (39,1%). Die Tumorgröße lag bei 25mm im Median (min=8; max=120) mit n=17. Die Infiltrationstiefe lag bei 5mm im Median (min=0; max= 30) mit n=11. Folgende FIGO Klassifikationen waren vorhanden: FIGO I in 2 Fällen (8,7%), FIGO II in 5 Fällen (21,7%), FIGO III in 7 Fällen (30,4%) und in 9 Fällen FIGO IV (39,1%). Die meisten Patientinnen hatten R-Status R1 (n=9/39,1%), direkt danach R0 (n=8/34,8%). 5 Patientinnen hatten R2 (21,7%) und in einem Fall kam RX vor mit 4,3%. Alle 23 Patientinnen erhielten eine Brachytherapie im PDR-Verfahren (100%). Die Dosis der PDR-Brachytherapie lag bei 50 Gy im Median (min=12; max=62,4) mit einer Pulsdosis von 0,55 Gy im Median (min=0,4; max=0,7). Die Dauer der PDR- Brachytherapie lag bei 95 Stunden im Median (min=20; max=139). Bei 15 Patientinnen wurde ein Template benutzt (65,2%) und bei der Minderheit von 8 Patientinnen nicht (34,8%). Im Median wurden 7 Tubes verwendet (min=4; max=20). Die Referenzisodosis betrug im Median 85% (min=70; max=100). Die große Mehrheit erhielt keine simultane Chemotherapie zur Brachytherapie (n=19/82,6%). Von den 4 Patientinnen, die eine Chemotherapie erhalten haben (17,4%), wurden 2 mit Cisplatin Monotherapie behandelt und 2 erhielten ein Kombinationspräparat von 5-Fluoruracil und Cisplatin. Die knappe Mehrheit von 12 Patientinnen erhielt keine perkutane Radiotherapie (52,2%). 11 Patientinnen wurden mit perkutaner Radiotherapie behandelt (47,8%). Davon wurden 5 Patientinnen vor der Brachytherapie bestrahlt (21,7%) und 6 Patientinnen danach (26,1%). Im Median lagen 5,5 Tage (min=2; max=40) zwischen perkutaner Radiotherapie und Brachytherapie bzw. umgekehrt. Die applizierte Dosis lag beim Primärtumor bei 46,6 Gy im Median (min=39,6; max=52,2) und am Lymphabflussgebiet bei 48,2 Gy im Median (min= 0; max=52,2). 5 von 11 Patientinnen (45,5%) erhielten zur perkutanen Radiotherapie eine simultane Chemotherapie. 4 Patientinnen Cisplatin und eine Patientin ein Kombinationspräparat von Cisplatin und 5-Fluoruracil. 15
23 3.4. Chirurgie Vor allem beim Vulvakarzinom gilt als erster Schritt der Standardtherapie die Tumorexzision (mittels Skalpell oder Laserevaporation) im Gesunden [1].Bei einer Laserevaporation ist eine vorherige histologische Sicherung von Tumorgewebe unabdingbar [3; 14; 33]. Je nach Ausdehnung des Befundes kann eine Tumorexzision auch einer partiellen Vulvektomie entsprechen [1; 31]. Die Indikationen für eine Hemivulvektomie beziehungsweise Vulvektomie mit Lymphonodektomie sind dem Gliederungspunkt 2.3. Klassifikation und Stadieneinteilung zu entnehmen. Auch beim Vaginalkarzinom wird bei lokal begrenzten Befunden eine lokale Exzision im Gesunden per Skalpell oder Laserevaporation (histologische Sicherung von Gewebe sollte unbedingt vorher erfolgt sein [3; 14; 33]) bevorzugt. Bei größeren Befunden ist das operative Vorgehen von der Lokalisation in der Scheide abhängig. Ist der Befall des Tumors im oberen Scheidendrittel zu finden, ist eine radikale Hysterektomie mit oberer Kolpektomie und pelviner Lymphonodektomie indiziert. Bei tieferer Lokalisation des Tumors im mittleren Scheidendrittel wird die oben beschriebene Operation ergänzt durch die totale Kolpektomie mit zusätzlicher inguinaler Lymphonodektomie. Im unteren Scheidendrittel ist eine untere Kolpektomie, eine partielle Vulvektomie mit inguinaler Lymphonodektomie indiziert [24; 33] Perkutane Strahlentherapie und Brachytherapie Die interdisziplinäre S2K Leitlinie von 2009 zum Vulvakarzinom empfiehlt eine primäre Strahlentherapie nur bei nicht operablen Befunden mit palliativer Zielsetzung. Die Dosis am Primärtumor sollte dabei Gy und die Dosis am Lymphabflussgebiet 50 Gy betragen. Eine adjuvante Strahlentherapie des Vulvakarzinoms wird bei unvollständigen R0 oder R1- Resektionen empfohlen (<10 mm Sicherheitsrand), wobei eine Bestrahlung des Lymphabflussgebietes bei negativem Lymphknotenstatus entfällt [1; 3]. 16
24 Anders als beim Vulvakarzinom, ist die primäre Bestrahlung beim primären Vaginalkarzinom durchaus empfohlen. Hier wird eine Kombinationstherapie aus perkutaner Bestrahlung, Brachytherapie und simultaner Chemotherapie angewandt. Je nach Zielvolumen werden die inguinalen und iliakalen Lymphabflussgebiete mit eingeschlossen (abhängig vom Tumorsitz). Die Gesamtdosis sollte 70 Gy im Tumorbett und Gy im Lymphabflussgebiet betragen[23; 32]. Die Brachytherapie ist fester Bestandteil der Therapieplanung beim Vaginalkarzinom. Kleinere Tumore können ausschließlich mit Brachytherapie behandelt werden, größere und extensivere Tumore werden kombiniert bestrahlt beziehungsweise mit Brachytherapie aufgesättigt [28; 32]. Beim Vulvakarzinom ist die Brachytherapie streng abhängig von der Tumorgröße und postoperativem Risikoprofil zu indizieren und durchzuführen. Oft wird sich für eine operative Sanierung entschieden, bei großen und fortgeschrittenen Befunden steht die Radiochemotherapie im Vordergrund. Allerdings bietet sich hier die Möglichkeit, als alleinige interstitielle Brachytherapie oder als Boost den Tumor lokal zu kontrollieren ohne Operation und Chemotherapie. Gerade für ältere Patientinnen, kann die alleinige Brachytherapie eine gute Alternative darstellen [23; 28]. Wichtig zur Therapieplanung bei Karzinomen der Vagina und Vulva- ist vor allem die genaue Anamnese, die ausführlich gynäkologische Untersuchung mit zeichnerischer Darstellung des Befundes und gegebenenfalls ein Vaginalabdruck. Zur genauen Berechnung der Tumorausdehnung in allen Ebenen ist ein MRT unerlässlich, wobei eine 3D Darstellung mit intravaginalem Applikatorsystem zu bevorzugen ist [10; 21]. In diesem Anwendungsbereich wird die interstitielle PDR Brachytherapie bevorzugt. Hier wird mittels Nadeln (entspricht Tubes) über ein Applikatorsystem ein Radionuklid in das Tumorgewebe appliziert und zwar nicht die gesamte Dosis auf einmal, sondern in Pulsen (Pulsed- Dose- Rate Brachytherapy). Bei der Berechnung der zu applizierenden Dosis sind zum einen eine Entfernung von 5mm von der Applikatoroberfläche als Referenzisodosis zu beachten, zum anderen die Toleranzdosen des umliegenden Gewebes (Urethra, Blase und Rektum). Da im Bereich des Septum recto- und vesicovaginale bei zu hoher Strahlenbelastung eine Fistelbildung entstehen kann, gilt 17
25 hier vor allem bei älteren Patientinnen besondere Vorsicht. Die Septen sind hier dünner als bei jüngeren Patientinnen [28] Chemotherapie Bei Vaginalkarzinomen wird eine primäre Radiochemotherapie empfohlen [1; 3; 33]. Eine alleinige Chemotherapie ist bei Vaginal- und Vulvakarzinom wenig erfolgversprechend. Die hauptsächlich eingesetzten Chemotherapeutika in diesem Bereich sind 5- Fluorouracil, Cisplatin und Mitomycin C, welche sich als hocheffektiv im Rahmen einer kombinierten Radiochemotherapie erwiesen haben [32]. Eine simultane Radiochemotherapie beim Vulvakarzinom ist eine individuelle Entscheidung Nebenwirkungen und Nachsorge Bei der Strahlentherapie der gynäkologischen Tumore sind vor allem die Haut, der Darm, die Harnwege und der Lymphabfluss belastet. Speziell typisch für die Bestrahlung des Vulvakarzinoms sind Vulvomukositis und Epitheliolysen der Vulva und Analfalte. Die Desquamation der betroffenen Haut gestaltet sich oft sehr schmerzhaft und macht einen stationären Aufenthalt mit symptomatischer Therapie (lokale Kortikoide und Adstringenzien, sowie Analgetika) notwendig. Generell sollte es jedoch innerhalb von Wochen folgenlos ausheilen [1; 32]. Häufig sind auch Irritationen des Darms insbesondere Diarrhoen, die sowohl in der Literatur als auch in der vorliegenden Arbeit beobachtet wurden [30]. Eine strahleninduzierte Proktitis, die topisch mit Butyraten behandelt werden kann, ist auch eine gefürchtete Komplikation. Bei persistierenden Beschwerden und bleibenden radiogenen Veränderungen der Schleimhaut muss jedoch ein interdisziplinäres Therapiekonzept gefunden werden [1; 32]. Eine Mikro- oder Makrohämaturie weist auf eine Zystitis hin, welche symptomatisch (Spasmolytika und Analgesie) therapiert wird. Bei bakterieller Superinfektion kann eine antibiotische Therapie nötig werden[1]. Selten (in 1,3% der Fälle) kann eine Schambeinnekrose auftreten [32]. Als Spätfolgen 18
26 sind Vulvaindurationen und Stenosen des Introitus und/oder Harnröhre zu beobachten, so wie hartnäckige Lymphödeme die nicht selten chronifizieren [32]. Des Weiteren sollte hier die häufige Nebenwirkung einer Vaginalstenose und Vaginaltrockenheit erwähnt werden, was häufig mit lokaler Östrogenisierung und Gleitgel verbessert werden kann, jedoch bei Beschwerdepersistenz eine mechanische Dilatation indizieren kann. Nicht nur wegen möglicher sexueller Funktionsstörungen im Langzeitverlauf, sondern auch wegen der sehr belastenden Therapie empfiehlt es sich - leitliniengerecht- eine frühzeitige psychoonkologische Einbindung der Patientinnen anzustreben [1]. Als Nachsorge ist nach wie vor, die regelmäßige klinisch gynäkologische Untersuchung unersetzlich [3; 32; 1; 14; 33]. 4. Ergebnisse 4.1. Analyse der Patientinnen mit Vaginalkarzinom Deskriptive Analyse Einzelheiten zur Hautreaktion nach Brachytherapie sind folgender Tabelle zu entnehmen: Grad der Hautreaktion akut nach Brachytherapie Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Grad ,3 93,3 93,3 Grad 2 1 3,3 3,3 96,7 Grad 3 1 3,3 3,3 100,0 Gesamtsumme ,0 100,0 Tabelle 4: Grad der Hautreaktion akut nach Brachytherapie bei Vaginal CA Eine Reaktion auf die Brachytherapie in Form von einer Mukositis sind folgender Tabelle zu entnehmen: 19
27 Grad der Mukositis akut nach Brachytherapie Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Grad ,0 80,0 80,0 Grad ,7 16,7 96,7 Grad 2 1 3,3 3,3 100,0 Gesamtsumme ,0 100,0 Tabelle 5: Grad der Mukositis akut nach Brachytherapie bei Vaginal CA Zum Grad der Hautreaktion nach perkutaner Radiotherapie liegt folgende Tabelle vor: Grad der Hautreaktion akut nach perk. RT Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Grad ,7 66,7 66,7 Grad 1 2 6,7 9,5 76,2 Grad 2 1 3,3 4,8 81,0 Grad ,3 19,0 100,0 Gesamtsumme 21 70,0 100,0 Fehlend System 9 30,0 Gesamtsumme ,0 Tabelle 6: Grad der Hautreaktion akut nach perk. RT bei Vaginal CA Einzelheiten der Mukositis nach perkutaner RT gestalten sich wie folgt: Grad der Mukositis akut nach perk. RT Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Grad ,3 76,2 76,2 Grad ,0 14,3 90,5 Grad 2 1 3,3 4,8 95,2 Grad 3 1 3,3 4,8 100,0 Gesamtsumme 21 70,0 100,0 Fehlend System 9 30,0 Gesamtsumme ,0 Tabelle 7: Grad der Mukositis akut nach perk. RT bei Vaginal CA 20
28 Nach der Brachytherapie wurden folgende späte Nebenwirkungen dokumentiert: Andere späte Nebenwirkungen Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Nein 24 80,0 80,0 80,0 BB-Veränderungen 1 3,3 3,3 83,3 Diarrhoe 3 10,0 10,0 93,3 strahleninduzierte Proktitis 1 3,3 3,3 96,7 Vaginalstenose 1 3,3 3,3 100,0 Gesamtsumme ,0 100,0 Tabelle 8: Andere späte Nebenwirkungen der Brachytherapie bei Vaginal CA Remission 6 Wochen nach Therapie Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Voll 25 83,3 83,3 83,3 Partiell 5 16,7 16,7 100,0 Gesamtsumme ,0 100,0 Tabelle 9: Remission 6 Wochen nach Therapie bei Vaginal CA) Nur 4 Patientinnen erhielten nach der Bestrahlung eine Erhaltungschemotherapie (13,3%) und zwar jeweils eine Patientin mit: DTIC/Cisplatin/Tamoxifen, Taxol, Interferon, Carboplatin/Paclitaxel. 26 Patientinnen erhielten keine Erhaltungschemotherapie (86,7%). Bei 10 Patientinnen wurde eine Fernmetastase diagnostiziert (33,3%), die wie folgt lokalisiert waren: Metastasenlokalisation Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig 20 66,7 66,7 66,7 Haut,LK,Knochen,Zerebral, 1 3,3 3,3 70,0 Knochen, Blase 1 3,3 3,3 73,3 21
29 Knochen, Leber 1 3,3 3,3 76,7 LK 1 3,3 3,3 80,0 LK Leiste 1 3,3 3,3 83,3 Lunge 1 3,3 3,3 86,7 Lunge, Brust 1 3,3 3,3 90,0 Lunge, Leber 1 3,3 3,3 93,3 Lunge, Leber, Knochen 1 3,3 3,3 96,7 zerebral,leber,lunge 1 3,3 3,3 100,0 Gesamtsumme ,0 100,0 Tabelle 10: Metastasenlokalisation bei Vaginalkarzinom Das Follow- up lag im Mittelwert bei 86 Monaten und bei 71 Monaten im Median Kaplan- Meier- Analyse bezüglich des RFS Alter bei Therapie <70 Jahre vs 70 Jahre Die Patientinnen, die bei Therapie unter 70 Jahre alt waren, zeigten eine 5 JÜR von 60% und eine 10 JÜR von 48% bis zum Auftreten eines Lokalrezidivs oder Tod. Die ältere Gruppe (70 Jahre oder älter) zeigte eine 5 JÜR von 26,7% und eine 10 JÜR von 17,8%. Somit hatten Patientinnen unter 70 Jahren eine mittlere Überlebenszeit von 98,8 Monaten. Die Patientinnen, die 70 Jahre oder älter waren konnten nur eine mittlere Überlebenszeit von 52,3 Monaten aufweisen bis zum Auftreten eines Lokalrezidivs. Diese Analyse zeigte statistische Signifikanz (p<0,05). 22
30 Abbildung 1: KMA bezüglich des RFS bei Vaginal CA (Alter bei Therapie) Rezidivbehandlung Ob ein Rezidiv oder der Primärtumor behandelt worden ist, zeigte keinen großen Unterschied in der Prognose ein Lokalrezidiv zu entwickeln. Patientinnen mit Primärtumor zeigten eine 5 JÜR von 46,2% (mittlere Überlebenszeit von 76,8 Monaten) und Patientinnen, die an einem Rezidiv behandelt worden sind zeigten eine 5 JÜR von 41,2% (mittlere Überlebenszeit von 72 Monaten). Diese Analyse blieb ohne statistische Signifikanz (p>0,05) Vorbestrahlung Die Patientinnen, die erstmalig einer Strahlenexposition ausgesetzt waren (n=24) wiesen eine 5 JÜR von 45,8% auf und eine mittlere Überlebenszeit von 76 Monaten bis zum Auftreten eines lokalen Rezidivs oder Tod. Wohingegen die Patientinnen, die 23
31 bereits vorher bestrahlt wurden, eine schlechtere 5 JÜR von 33,3% aufwiesen und eine mittlere Überlebenszeit von 66,1 Monaten (p>0,05). Vorausgegangene Operation Patientinnen, die im Rahmen der Strahlentherapie operiert wurden, zeigten in der Analyse eine leicht bessere Prognose als Patientinnen ohne Operation. Die 5 JÜR lag bei 45,5% und die mittlere Überlebenszeit bei 83,4 Monaten. Dabei hatte der Zeitraum zwischen Operation und Brachytherapie keinerlei Auswirkung auf das geschätzte Überleben. Die Patientinnen, die nur strahlentherapeutisch behandelt wurden kamen auf eine 5 JÜR von 42,1% mit einer mittleren Überlebenszeit von 70 Monaten. Allerdings blieb diese Analyse ohne statistische Signifikanz (p>0,05). Histologisches Grading des Tumors Die Patientinnen mit niedrigem Grading (G1 und G2) zeigten eine deutlich bessere Prognose mit einer 5 JÜR von 63,6% und einer 10 JÜR von 47,7% mit einer mittleren Überlebenszeit von 100,7 Monaten. In den Fällen mit höherem Grading Score (G2, G3 und GX), lag die Wahrscheinlichkeit ein Lokalrezidiv zu entwickeln deutlich höher mit einer 5 JÜR von 36,8% und einer 10 JÜR von nur 21,1% mit einer mittleren Überlebenszeit von 56,4 Monaten. Diese Analyse blieb jedoch auf Grund der geringen Patientenzahl ohne statistische Relevanz (p>0,05). R- Status Da nur 2 Patientinnen einen R0 Status aufwiesen, ist eine Analyse des Einflusses von R0 gegenüber alle anderen R-Stadien auf das Überleben nicht repräsentativ. FIGO Stadium In der Gruppe mit FIGO I und FIGO II, zeigte sich eine 5 JÜR von 42,9% und eine 10 JÜR von 23,8% mit einer mittleren Überlebenszeit von 67,3 Monaten. Die Vergleichsgruppe (FIGO III und IV) wies eine etwas bessere Prognose auf mit einer 5 JÜR von 50% und einer 10 JÜR von 40% mit einer mittleren Überlebenszeit von 78,9 Monaten. Aufgrund der geringen Patientenzahl blieb dieses Ergebnis ohne statistische Signifikanz (p>0,05). 24
32 T- Stadium Die eine Patientengruppe (T0 und T1) hatte mit einer 5 JÜR von 50% und einer mittleren Überlebenszeit von 80,4 Monaten, die bessere Prognose. Die andere Patientengruppe (T2, T3, T4 und TX) wies eine 5 JÜR von 41,7% und eine mittlere Überlebenszeit von 61,9 Monaten auf. Somit ging ein Tumorstadium von T0 oder T1 mit einer deutlich besseren Prognose einher, im Verlauf kein Lokalrezidiv im Verlauf zu entwickeln. Leider blieb auch diese Analyse aufgrund der geringen Patientenzahl ohne statistische Signifikanz (p>0,05). N- Stadium Patientinnen mit Lymphknotenstatus N0 hatten erwartungsgemäß die bessere Prognose mit einer 5 JÜR von 50% und einer mittleren Überlebenszeit von 81,7 Monaten. Die Patientinnen mit Lymphknotenstatus N1 oder NX wiesen eine 5 JÜR von nur 30% und eine mittlere Überlebenszeit von 62,3 Monaten auf. Somit hatte letztere Patientengruppe ein höheres Risiko ein Lokalrezidiv zu entwickeln. Leider war aufgrund der geringen Patientenzahlen diese Analyse ohne statistische Signifikanz (p>0,05). M- Stadium Patientinnen mit Stadium M0 hatten eine minimal bessere Prognose kein Lokalrezidiv zu entwickeln (5 JÜR von 50% und mittlere Überlebenszeit von 74,4 Monaten) als Patientinnen mit Stadium M1 oder MX (5 JÜR 43,8% und mittlere Überlebenszeit von 78,5 Monaten). Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Dosis der Brachytherapie im PDR Verfahren <50 Gy vs 50 Gy Die eine Patientengruppe (Dosis der Brachytherapie im PDR Verfahren von <50 Gy) wies eine 5 JÜR von 36,4% und 10 JÜR von 27,3% auf (mittlere Überlebenszeit von 64,9 Monaten), während die andere Gruppe (Dosis 50 Gy) mit einer 5 JÜR von 71,4% und einer 10 JÜR von 47,6% deutlich besser abschnitt. Die mittlere Überlebenszeit lag hier bei 112,3 Monaten. Diese Analyse blieb knapp ohne statistische Signifikanz (p>0,05). 25
33 Abbildung 2: KMA bezüglich der RFS bei Vaginal CA (Dosis der PDR- BT in Gy) Pulsdosis der Brachytherapie <0,50 Gy vs 0,50 Gy Die kleinere Gruppe (n=5) wurde mit einer Pulsdosis <0,50 Gy in der PDR- BT bestrahlt und wies eine 5 JÜR von 20% auf. Die deutlich größere Gruppe mit 24 Mitgliedern wurde mit einer Pulsdosis 0,50 Gy in der PDR- BT bestrahlt. Hier wurde eine 5 JÜR von 50% ermittelt. Dieser große Unterschied zeigte sich auch in der mittleren Überlebenszeit: 44,6 Monaten im ersten Fall, 66 Monaten im zweiten Fall. Es scheint so, als würden die Patientinnen mit einer Pulsdosis von 0,50 Gy bezüglich der Entwicklung eines Lokalrezidives profitieren. Leider blieben diese Daten ohne statistische Signifikanz (p>0,05). Dauer der Brachytherapie <70 Stunden vs 70 Stunden Die eine Patientengruppe wurde unter 70 Stunden lang bestrahlt, die andere Gruppe länger. Die erste Gruppe wies eine 5 JÜR von 45,5% und 10 JÜR von 34,1% auf und eine mittlere Überlebenszeit von 77,5 Monaten. Die Gruppe mit Bestrahlungsdauer von 70 26
34 Stunden oder länger zeigte eine 5 JÜR von 42,9% und eine 10 JÜR von 28,6% mit einer mittleren Überlebenszeit von 76,7 Monaten. Die Prognose in Bezug auf die Entwicklung eines Lokalrezidives unterschied sich hier also nicht wesentlich. Die Analyse blieb ohne statistische Signifikanz (p>0,05). Anzahl der benutzten Tubes <8 Stück vs 8 Stück Die größere Gruppe (n=18) wurde mit einer Anzahl von 1 bis 7 Tubes therapiert und hatte eine 5 JÜR von 50% mit einer mittleren Überlebenszeit von 78,3 Monaten. Die etwas kleinere Gruppe (n=11) wurde mit 8 Tubes oder mehr therapiert und wies eine leicht schlechtere Prognose auf, mit einer 5 JÜR von 45,5% und einer mittleren Überlebenszeit von 73,8 Monaten. Diese Analyse blieb aufgrund der geringen Patientenzahl ohne statistische Signifikanz (p>0,05). Referenzisodosis 85% vs >85% Die Patientinnen, die mit einer Referenzisodosis von 85% oder weniger behandelt wurden, hatten eine deutlich geringere Wahrscheinlichkeit ein Lokalrezidiv zu entwickeln. Die 5 JÜR lag hier bei 50% und 10 JÜR bei 41,7% (mittlere Überlebenszeit 83,7 Monate). Die Patientinnen, die mit einer höheren Referenzisodosis behandelt wurden (bis 105%), zeigten eine 5 JÜR von 28,6% und eine 10 JÜR von 14,3% mit einer mittleren Überlebenszeit von 59 Monaten. Die statistische Signifikanz lag bei p>0,05. Simultane Chemotherapie zur Brachytherapie Nur auf 4 Patientinnen traf dies zu, jedoch erlitt keine von ihnen ein Rezidiv. Somit ist keine Aussage über den Einfluss einer simultanen Chemotherapie zur Brachytherapie möglich. Perkutane Radiotherapie Die Patientinnen die keine perkutane Radiotherapie im Rahmen ihrer Brachytherapie erhielten (n=9) wiesen eine 5 JÜR von 44,4% und eine mittlere Überlebenszeit von 76,9 Monaten auf. Es zeigte sich hier keine große Verbesserung der Prognose im Vergleich zu den Patientinnen (n=21), die eine perkutane Radiotherapie erhielten (5 JÜR 42,9% 27
35 und mittlere Überlebenszeit von 73,8 Monaten). Diese Analyse blieb aufgrund der geringen Patientenzahl ohne statistische Signifikanz p>0,05. Simultane Chemotherapie zur perkutanen Radiotherapie Patientinnen ohne simultane Chemotherapie zur perkutanen Radiotherapie hatten mit einer 5 JÜR von 38,1% und einer mittleren Überlebenszeit von 61,5 Monaten ein höheres Risiko ein Lokalrezidiv zu entwickeln als die Patientinnen, die simultan behandelt wurden (5 JÜR 66,7% und mittlere Überlebenszeit von 113,3 Monaten). Diese Analyse blieb ohne statistische Signifikanz (p>0,05) Kaplan- Meier- Analyse bezüglich des DFS Alter bei Therapie <60 Jahre vs 60 Jahre Patientinnen in der jüngeren Altersgruppe (<60 Jahre) haben ein signifikant (p<0,05) längeres Überleben ohne Metastase oder Rezidiv als die Vergleichsgruppe ( 60 Jahre).Die 5 und 10 Jahresüberlebensrate bis zum Auftreten eines Rezidivs oder Metastase war bei den jüngeren Patientinnen bei 77,8% und 58,3%, während bei den Patientinnen ab 60 Jahren die 5 und 10 JÜR bei nur 28,6% und 17,1% lagen. Auch die mittlere Überlebenszeit der jüngeren Gruppe lag bei 115,1 Monaten, während die älteren Patientinnen nur eine mittlere Überlebenszeit von 51,1 Monaten aufweisen konnten. 28
36 Abbildung 3: KMA bezüglich des DFS bei Vaginal CA (Alter bei Therapie) Rezidivbehandlung Es hatte keinen großen Einfluss auf die Prognose ein Lokalrezidiv oder Metastase zu entwickeln ob an einem Rezidiv oder dem Primärtumor bestrahlt wurde. Patientinnen mit Rezidiv zeigten einen 5 JÜR von 41,2% und Patientinnen, die am Primärtumor bestrahlt wurden zeigten eine 5 JÜR von 38,5%. Bei beiden Gruppen lag die mittlere Überlebenszeit bei 70,9 Monaten. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). Vorbestrahlung Der weit größere Teil der Patientinnen wurde zum ersten Mal bestrahlt (n=24) und es ergab sich eine 5 JÜR von 45% mit einer mittlere Überlebenszeit von 71,7 Monaten. Die 6 Patientinnen, die schon einmal bestrahlt worden sind, wiesen eine 5 JÜR von 29
37 33,3% und eine mittlere Überlebenszeit von 66,1 Monaten auf. Auch diese Analyse blieb auf Grund der geringen Patientenzahlen ohne statistische Signifikanz (p>0,05). Vorausgegangene Operationen Eine vorausgegangene Operation zeigte einen Vorteil in Bezug auf die Prognose ohne Lokalrezidiv oder Metastase zu sein. In der 5 JÜR noch nicht so deutlich (45% bei Patientinnen mit OP, 42% bei Patientinnen ohne OP). Aber in der 10 JÜR zeigte sich deutlich, dass Patientinnen von einer Operation profitieren (36,4% vs 24,1%). Auch die mittlere Überlebenszeit war länger bei Patientinnen mit Operation (81,7 Monate) im Vergleich zu den Patientinnen ohne Operation (65,3 Monate). Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). Histologisches Grading des Tumors Die Gruppe mit den Tumoren Grad 1 und Grad 2 schnitt mit einer 5 JÜR von 63,6% und einer 10 JÜR von 47,7% deutlich besser ab als die andere Gruppe (Grad 3,4, und X), die nur eine 5 JÜR von 31,6% und eine 10 JÜR von 16,8% aufweisen konnte. Auch die mittlere Überlebenszeit lag bei der ersten Gruppe mit 100,6 Monaten deutlich besser als 51,5 Monate der Vergleichsgruppe. Auf Grund der niedrigen Patientenzahlen blieb diese Analyse ohne statistische Signifikanz (p>0,05). 30
38 Abbildung 4: KMA bezüglich des DFS bei Vaginal CA (Histologisches Grading) R- Status Nur 2 Patientinnen wiesen einen R0- Status auf, somit ist ein Vergleich nicht repräsentativ. FIGO Stadium Die Patientinnen mit niedrigeren FIGO Stadien I und II wiesen eine 5 JÜR von 35,7% und eine 10 JÜR von 23,8% auf. Die höheren FIGO Stadien III und IV zeigten zuerst eine 5 JÜR von 50%, die 10 JÜR sank dann aber auf 34,3%. Die mittlere Überlebensdauer lag bei 67,3 Monaten in der Gruppe mit niedrigem FIGO Stadium, im Vergleich dazu lag die mittlere Überlebensdauer bei den Patientinnen mit höherem FIGO Stadium bei 74,4 Monaten. Diese Analyse blieb auf Grund der geringen Patientenzahl ohne statistische Signifikanz (p>0,05). 31
39 T-Stadium Die Patienten mit T0/T1 Stadium wiesen mit einer 5 und 10 JÜR von 44,4% und 35,6% und einer mittlere Überlebenszeit von 78,6 Monaten eine deutlich bessere Prognose auf als die Gruppe mit Stadium T2, 3, 4 und X. Diese konnte nur eine 5 und 10 JÜR von 33,3% und 16,7% und eine mittlere Überlebenszeit von 57,5 Monaten aufweisen. Leider blieb diese Analyse auf Grund der geringen Patientenzahl ohne statistische Relevanz (p>0,05). N- Stadium Deutlich war der Unterschied bei diesen beiden Gruppen zu beobachten. Die Gruppe mit negativem Lymphknotenstatus (N0) zeigte eine 5 JÜR von 50% (10 JÜR 34,3%) und eine mittlere Überlebenszeit von 81 Monaten. Die Patientinnen mit positivem oder unklarem Lymphknotenstatus (N1 oder NX) zeigten eine deutlich schlechtere 5 JÜR von 30% (10 JÜR 20%) mit einer mittleren Überlebenszeit von nur 51,7 Monaten. Leider blieb auch diese Analyse auf Grund der geringen Patientenzahl ganz knapp ohne statistische Signifikanz (p>0,05). 32
40 Abbildung 5: KMA bezüglich des DFS Vaginal CA (N- Stadium) M- Stadium Bezüglich des Fernmetastasen Status waren die Unterschiede zwischen den Gruppen minimal. Die Gruppe mit M0 wies eine 5 JÜR von 42,9% (10 JÜR 25,7%) von und eine mittlere Überlebenszeit von 37 Monaten auf. Die Gruppe mit positiven oder unklaren Fernmetastasen Status (M1/MX) zeigte eine 5 JÜR von 43,8% (10 JÜR 36,5%) und eine mittleren Überlebenszeit von 71,6 Monaten. Auf Grund der geringen Zahl von Patientinnen blieb diese Analyse ohne statistische Signifikanz (p>0,05) Dosis Brachytherapie im PDR Verfahren <50 Gy vs 50 Gy Die weitaus größere Zahl der Patientinnen wurde mit einer Dosis <50 Gy in der BT im PDR Verfahren bestrahlt. Diese schnitten mit einer 5 JÜR von 36,4% und einer mittleren Überlebenszeit von 64 Monaten deutlich schlechter ab, als die Vergleichsgruppe. Diese Gruppe wurde mindestens 50 Gy in der BT im PDR Verfahren 33
41 ausgesetzt und zeigte eine 5 JÜR von 57,1% auf und einer mittlere Überlebenszeit von 101 Monaten. Da diese Gruppe allerdings deutlich kleiner war (n=7), blieb diese Analyse ohne statistische Signifikanz (p>0,05). Pulsdosis der Brachytherapie <0,50 Gy vs 0,50 Gy Nur 5 Patientinnen wurden mit einer Pulsdosis <0,50 Gy bestrahlt und es zeigte sich eine 5 JÜR von 20% mit einer mittleren Überlebenszeit von 44,3 Monaten. Der Rest der Patientinnen mit Vaginalkarzinom bildete die Vergleichsgruppe, die mit einer Pulsdosis von 0,50 Gy oder mehr bestrahlt wurden. Hier zeigte sich eine 5 JÜR von 50% mit einer mittleren Überlebenszeit von 77 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Dauer der Brachytherapie <80 Stunden vs 80 Stunden Nur 7 Patientinnen wurden 80 Stunden oder länger bestrahlt. Die 5 JÜR lag hier bei 42,9% und die mittlere Überlebenszeit bei 74,1 Monate. Die größere Gruppe wies eine 5 JÜR von 45,5% und eine mittlere Überlebenszeit von 73,1 Monaten auf. Somit zeigte sich kein großer Unterschied bezüglich der Prognose. Die statistische Signifikanz lag bei p>0,05. Anzahl der Tubes <8 Stück vs Stück Beide Gruppen waren in etwa gleich groß und zeigten auch ähnliche Ergebnisse auf. Die erste Gruppe (1 bis 7 Tubes) zeigte eine 5 JÜR von 44,4% mit einer mittleren Überlebenszeit von 77 Monaten. Die andere Gruppe (8 oder mehr Tubes) hatte eine 5 JÜR von 36,4% und eine mittlere Überlebenszeit von 66,6 Monaten. Diese Analyse blieb auf Grund der geringen Patientenzahl ohne statistische Signifikanz (p>0,05). Referenzisodosis 85% vs >85% Die Mehrzahl der Patientinnen zeigte im Bestrahlungsprotokoll eine Referenzisodosis von 85% oder weniger auf. Die 5 JÜR lag bei 45% und die mittlere Überlebenszeit bei 78,7 Monaten. Die Gruppe mit einer Referenzisodosis von >85% zeigte eine 5 JÜR von 34
42 nur 28,6% und eine mittlere Überlebenszeit von 58,2 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur Brachytherapie Nur 4 Patientinnen erhielten eine simultane Chemotherapie zur Brachytherapie. Zwei wiesen nach nur kurzer Zeit (6 und 8 Monaten) eine Fernmetastasierung auf. Darunter waren ein Malignes Melanom und ein Adenokarzinom der Vagina. Ein repräsentativer Vergleich ist somit nicht möglich. Perkutane Radiotherapie Etwa zwei Drittel der Patientinnen erhielt eine perkutane Radiotherapie, die 5 JÜR lag hier bei 42,9%. Die mittlere Überlebenszeit lag hier bei 69,4 Monaten. Somit erhielt etwa ein Drittel der Patientinnen keine perkutane Radiotherapie und wies eine 5 JÜR von 33,3% und eine mittlere Überlebenszeit von 74,7 Monaten auf. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur perkutanen Radiotherapie Patientinnen ohne simultane Chemotherapie zur perkutanen Radiotherapie hatten mit einer 5 JÜR von 33,3% und einer mittlere Überlebenszeit von 57,1 Monaten, ein höheres Risiko ein Rezidiv oder eine Fernmetastasierung zu entwickeln als die Patientinnen, die simultan behandelt worden waren (5 JÜR 66,7% und mittlere Überlebenszeit von 112,5 Monaten). Diese Analyse blieb ohne statistische Signifikanz (p>0,05) Kaplan- Meier- Analyse bezüglich des OS Alter bei Therapie <70 Jahre vs 70 Jahre Die Patientinnen <70 Jahre waren in der Unterzahl und zeigten eine deutlich bessere 5 JÜR von 42,9% und eine mittlere Überlebenszeit von 60,4 Monaten. Bei den Patientinnen, die bei Therapie 70 Jahre oder älter waren, konnte nur eine 5 JÜR von 35
43 25% mit einer mittleren Überlebenszeit von 32 Monaten ermittelt werden. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Rezidivbehandlung In den Fällen, wo ein Rezidiv behandelt worden ist, lagen die 5 JÜR nur bei 18,2% und die mittlere Überlebenszeit bei 33,3 Monaten. In den Fällen, wo der Primärtumor behandelt worden ist, lagen die 5 JÜR bei deutlich besseren 37,5% und die mittlere Überlebenszeit bei 55 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Vorbestrahlung Nur 4 Patientinnen wurden vorbestrahlt und zeigten somit eine 5 JÜR von 25% mit einer mittleren Überlebenszeit von 60,7 Monaten. Die restlichen Patientinnen wurden vorher nicht bestrahlt und zeigten eine 5 JÜR von 26,7% und eine mittlere Überlebenszeit von 37,6 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Vorausgegangene Operationen Die meisten Patientinnen wurden nicht operiert und es zeigte sich eine 5 JÜR von nur 8,3% und eine mittlere Überlebenszeit von 26,4 Monaten. Die Patientinnen mit Operation zeigten mit einer 5 JÜR von 42,9% und einer mittleren Überlebenszeit von 70 Monaten ein deutlich besseres Ergebnis. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Histologisches Grading des Tumors Die Gruppe mit den niedrig gradierten Tumoren (G1 und G2) zeigte erwartungsgemäß die bessere Prognose mit einer 5 JÜR von 40% und einer mittleren Überlebenszeit von 57,2 Monaten. Die Gruppe mit G3, G4 und GX erreichte nur eine 5 JÜR von 21,4 % und eine mittlere Überlebenszeit von 37,2 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). 36
44 R- Status Nur 2 Patientinnen wurden mir R0- Status der Strahlentherapie zugänglich. Ein Vergleich ist somit nicht möglich. FIGO Stadium In den Fällen mit diagnostizierten FIGO Stadien I oder II zeigten sich eine 5 JÜR von 50% und eine mittlere Überlebenszeit von 60 Monaten. Die FIGO Stadien III und IV zeigten eine schlechtere Prognose im Bezug aufs Gesamtüberleben mit einer 5 JÜR von nur 11,1% und einer mittlere Überlebenszeit von 23 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). T- Stadium Initial lag die Gruppe mit kleinen T-Stadien (T0 oder T1) etwas besser im Bezug aufs Gesamtüberleben. Ungefähr bei 40 Monaten allerdings kreuzen sich die Kurven und diese Gruppe (n=11) zeigte eine 5 JÜR von 18,2% mit einer mittleren Überlebenszeit von 40,8 Monaten. Somit war die Vergleichsgruppe mit höheren T-Stadien (T2, T3, T4 oder TX) zuerst zwar etwas schlechter, holte dann aber auf und endete bei einer besseren 5 JÜR von 25% und einer mittleren Überlebenszeit von 44,8 Monaten (n=8). Diese Analyse blieb ohne statistische Signifikanz (p>0,05). N- Stadium N0 Patientinnen zeigten eine erwartungsgemäß eine bessere 5 JÜR von 33,3% und eine mittlere Überlebenszeit von 49,8 Monaten. N1 oder NX Patientinnen zeigten eine 5 JÜR von nur 14,3% mit einer mittleren Überlebenszeit von 29,9 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). M- Stadium Die Patientinnen mit M0- Stadium zeigten eine bessere Prognose mit einer 5 JÜR von 30 % und einer mittleren Überlebenszeit von 54 Monaten. Hingegen die Patientinnen mit Stadium M1 oder MX zeigten eine 5 JÜR von nur 11 % mit einer mittleren Überlebenszeit von 29 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). 37
45 Dosis der Brachytherapie im PDR Verfahren <50 Gy vs 50 Gy Der weitaus größere Teil der Patientinnen wurde mit einer Dosis von <50 Gy in der PDR- BT bestrahlt. Nur 3 Patientinnen erhielten eine PDR- BT Dosis von 50 Gy oder mehr. Interessanterweise, zeigten diese Patientinnen eine statistisch signifikant bessere Prognose mit einer 5 JÜR von 33,3% und einer mittleren Überlebenszeit von 103,3 Monaten (p<0,05). Wohingegen die größere Gruppe (mit Dosis <50 Gy) nur eine 5 JÜR von 13,3% und eine mittlere Überlebenszeit von 28,4 Monaten aufzeigen konnte. Pulsdosis der Brachytherapie <0,50 Gy vs 0,50 Gy Die Patientinnen, die eine Pulsdosis <0,50 Gy erhielten, zeigten eine etwas bessere Prognose in Bezug auf das Gesamtüberleben als die Patientinnen, die eine Pulsdosis von mindestens 0,50 Gy erhielten. Erstere lagen bei einer 5 JÜR von 25% bei einer mittleren Überlebenszeit von 58 Monaten, letztere lagen etwas schlechter bei einer 5 JÜR von 21,4% bei einer mittleren Überlebenszeit von 35 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Dauer der Brachytherapie <95 Stunden vs 95 Stunden Die Patientengruppe, die weniger als 95 Stunden therapiert wurde, hatte eine signifikant schlechtere Prognose mit einer 5 JÜR von nur 13,3% und einer mittleren Überlebenszeit von 28,4 Monaten. Die Patientengruppe, die 95 Stunden oder länger bestrahlt worden ist konnte mit einer 5 JÜR von 66,7% und einer mittleren Überlebenszeit von 103,3 Monaten aufweisen. Diese Analyse war statistisch signifikant (p<0,05). Anzahl der Tubes <8 Stück vs 8 Stück Insgesamt lagen die Analysen bezüglich des Gesamtüberlebens dieser beiden Gruppen nicht so sehr voneinander entfernt. Die Gruppe mit weniger als 8 Tubes zeigte eine 5 JÜR von 36,4% und eine mittlere Überlebenszeit von 48,4 Monaten. Die Patientinnen mit 8 Tubes oder mehr zeigten eine 5 JÜR von 14,3% mit einer mittleren Überlebenszeit von 29,1 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). 38
46 Referenzisodosis 85% vs >85% Die Patientinnen, die eine Referenzisodosis unter 85% im Bestrahlungsprotokoll aufwiesen, zeigten ab ca. 18 Monaten nach Therapie eine deutliche Verschlechterung im Gegensatz zur Gruppe, die eine Referenzisodosis von >85% im Protokoll hatte. Erstere lag bei einer 5 JÜR von nur 16,7% und einer mittleren Überlebenszeit von 25,2 Monaten. Letztere zeigte eine 5 JÜR von 50% mit einer mittleren Überlebenszeit von 72,1 Monaten(n=6). Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur Brachytherapie Von allen bereits verstorbenen Patientinnen mit Vaginalkarzinom, sind nur zwei mit einer simultanen Chemotherapie zur Brachytherapie behandelt worden. Die eine verstarb 9 Monate, die andere 11 Monate nach Therapie. Somit ist keine Aussage bezüglich der 5 JÜR und der mittleren Überlebenszeit im Vergleich der beiden Gruppen möglich. Perkutane Radiotherapie Die kleinere Gruppe wurde nur mit Brachytherapie behandelt und zeigte eine bessere 5 JÜR von 50 % mit einer mittleren Überlebenszeit von 44 Monaten. Die etwas größere Gruppe, die auch eine perkutane Radiotherapie erhalten hat, zeigte eine 5 JÜR von 23% und einer mittlere Überlebenszeit von 41,7 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur perkutanen Radiotherapie Nur 3 Patientinnen wurden zur perkutanen Radiotherapie simultan mit einer Chemotherapie behandelt. Sie verstarben 4, 11 und 147 Monate nach Therapie. Somit ist keine Aussage bezüglich der 5 JÜR im Vergleich der beiden Gruppen möglich Subanalyse der primär behandelten Patientinnen Im Folgenden werden die Patientinnen von der Analyse ausgeschlossen, die in der Vergangenheit bereits bestrahlt wurden (n=6). 39
47 Kaplan- Meier- Analyse des RFS Alter bei Therapie <70 Jahren vs 70 Jahre Die Patientinnen, die bei Therapie unter 70 Jahre alt waren, zeigten eine bessere Prognose mit einer 5 JÜR von 75% und einer mittleren Überlebenszeit von 108,6 Monaten. Die Patientinnen, die 70 Jahre oder älter waren zeigten eine 5 JÜR von 31,3% und eine mittlere Überlebenszeit von 58,9 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Vorausgegangene Operationen In den Fällen, wo vorher eine Operation stattgefunden hat, lagen die 5 JÜR bei 50% und die mittlere Überlebenszeit bei 86,3 Monaten. Die Patientinnen, die vorher nicht operiert worden sind zeigten eine 5 JÜR von 43,8% und eine mittlere Überlebenszeit von 62 Monaten. Eine eindeutiger Vorteil beziehungsweise Nachteil einer vorausgegangen Operation ist somit hier nicht zu erheben, zumal diese Analyse keine statistische Signifikanz zeigte (p>0,05). Histologisches Grading des Tumors Die höhergradigen Tumore (G3, G4 und GX) zeigten eine etwas bessere Prognose in Bezug auf die 5 JÜR von 40%. Die mittlere Überlebenszeit lag hier allerdings nur bei 52,2 Monaten. Die Tumore mit Stadium G1 und G2 zeigten zwar eine 5 JÜR von 66,7% aber eine mittlere Überlebenszeit von 100,8 Monaten. Auch diese Analyse blieb ohne statistische Signifikanz (p>0,05). R- Status Hier konnten keine Statistiken berechnet werden, da in nur einem Fall ein R0- Status vorlag. FIGO Stadium Die höheren FIGO Stadien (FIGO III und IV) zeigten eine etwas schlechtere Prognose mit einer 5 JÜR von 46,7% und einer mittleren Überlebenszeit von 74,5 Monaten. Die FIGO Stadien I und II hingegen zeigten eine 5 JÜR von 55,6% und einer mittleren 40
48 Überlebenszeit von 79,1 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). T- Stadium Die Patientinnen mit Stadium T0 oder T1 zeigten eine 5 JÜR von 50%, genau wie die Patientinnen mit T2, 3 und 4. Lediglich die 10 JÜR war bei den niedrigen T-Stadien etwas besser (28,6%) als bei den höheren T-Stadien (25%). Auch die mittlere Überlebenszeit unterschied sich kaum (77,5 Monate versus 67,6 Monate). Diese Analyse blieb ohne statistische Signifikanz (p>0,05). N- Stadium Patientinnen mit negativem Lymphknotenstatus (N0) zeigten erwartungsgemäß die bessere Prognose kein Lokalrezidiv zu entwickeln mit einer 5 JÜR von 57,1% und einer mittleren Überlebenszeit von 85,1 Monaten. Patientinnen mit N1/NX Status zeigten eine 5 JÜR von 30% und eine mittlere Überlebenszeit von 62,3 Monaten. Diese Analyse blieb auf Grund der geringen Patientenzahl ohne statistische Signifikanz (p>0,05). M- Stadium Erwartungsgemäß zeigten die Patientinnen mit M0 Status eine etwas bessere Prognose (5 JÜR 60% und mittlere Überlebenszeit von 82 Monaten). Die Patientinnen mit Fernmetastasierung (M1 oder MX) zeigten eine 5 JÜR von 42,9% und eine mittlere Überlebenszeit von 60,6 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Dosis der Brachytherapie im PDR Verfahren <50 Gy vs 50 Gy Patientinnen mit einer Bestrahlung von <50 Gy zeigten eine 5 JÜR von 40% und eine mittlere Überlebenszeit von 70,6 Monaten. Bei dem kleineren Teil der Patientinnen betrug die Dosis der Bestrahlung 50 Gy oder mehr und die 5 JÜR lag hier bei 75% und die mittlere Überlebenszeit bei 86,7 Monaten. Die Analyse blieb ohne statistische Signifikanz (p>0,05). 41
49 Pulsdosis der Brachytherapie <0,50 Gy vs 0,50 Gy Die Patientinnen, die mit einer Pulsdosis von 0,50 Gy oder mehr bestrahlt worden sind, zeigten mit einer 5 JÜR von 50% und einer mittleren Überlebenszeit von 79,2 Monaten die etwas bessere Prognose kein Lokalrezidiv zu entwickeln. Die Patientinnen, die mit einer Pulsdosis von weniger als 0,50 Gy bestrahlt wurden zeigten eine 5 JÜR von 25% und eine mittlere Überlebenszeit von 46,1 Monaten. Leider blieb diese Analyse auf Grund der geringen Patientenzahl ohne statistische Signifikanz (p>0,05). Dauer der Brachytherapie < 60 Stunden vs 60 Stunden Die Patientinnen mit der besseren Prognose kein Lokalrezidiv zu entwickeln, wurden weniger als 60 Stunden bestrahlt. Hier lagen die 5 JÜR bei 47,4% und die mittlere Überlebenszeit bei 81,2 Monaten. Die Patientinnen, die 60 Stunden oder mehr therapiert wurden, zeigten eine 5 JÜR von 40% und eine mittlere Überlebenszeit von 54,6 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Anzahl der Tubes <8 Stück vs 8 Stück Die Patientinnen, die mit weniger als 8 Tubes therapiert worden sind zeigten eine 5 JÜR von 57,1% und eine mittlere Überlebenszeit von 83,4 Monaten. Die Patientinnen, die mit 8 Tubes oder mehr behandelt worden sind zeigten eine 5 JÜR von 40% und eine mittlere Überlebenszeit von 63,6 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Referenzisodosis 85% vs >85% In den Fällen, wo mit einer Referenzisodosis von 85% oder weniger gearbeitet worden ist, zeigte sich eine 5 JÜR von 50% und eine mittlere Überlebenszeit von 82 Monaten. Die höhere Wahrscheinlichkeit ein Lokalrezidiv zu erleiden zeigte sich bei den Patientinnen, wo mit mehr als 85% Referenzisodosis gearbeitet worden ist. Hier lagen die 5 JÜR bei 33,3% und die mittlere Überlebenszeit bei 62,3 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). 42
50 Simultane Chemotherapie Brachytherapie Hier konnten keine Statistiken berechnet werden, da in nur 2 Fällen eine simultane Chemotherapie zur Brachytherapie stattgefunden hat. Perkutane Radiotherapie Patientinnen, die zusätzlich eine perkutane Radiotherapie erhalten haben zeigten die etwas bessere Prognose frei von einem Lokalrezidiv zu bleiben mit einer 5 JÜR von 47,4% und einer mittleren Überlebenszeit von 79,3 Monaten. In den wenigen Fällen, wo nur BT verwendet worden ist lagen die 5 JÜR bei 40% und die mittlere Überlebenszeit bei 60,4 Monaten. Die Analyse blieb ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur perkutanen Radiotherapie In den Fällen, wo zur perkutanen Radiotherapie zusätzlich Chemotherapeutika verwendet wurden lagen die 5 JÜR bei 75% und die mittlere Überlebenszeit bei 122 Monaten. Deutlich schlechter zeigte sich die Prognose in den Fällen ohne Chemotherapie mit einer 5 JÜR von 37,5% und einer mittleren Überlebenszeit von 57,1 Monaten. Diese Analyse blieb leider auf Grund der geringen Patientenzahlen ohne statistische Signifikanz (p>0,05) Kaplan- Meier- Analyse des DFS Alter bei Therapie <60 Jahren vs 60 Jahren Die jüngeren Patientinnen (<60 Jahre bei Therapie) zeigten eine signifikant bessere Prognose mit einer 5 JÜR von 75% und einer mittleren Überlebenszeit von 108,4 Monaten (p<0,05). Die Patientinnen, die bei Therapie 60 Jahre oder älter waren, lagen bei einer 5 JÜR von nur 31,3% und einer mittleren Überlebenszeit von 51,5 Monaten. 43
51 Abbildung 6: KMA bezüglich des DFS Vaginal CA (primär bestrahlt) Alter bei Therapie Vorausgegangene Operationen In den Fällen, wo eine Operation vorausgegangen war, lagen die 5 JÜR bei 50% und die mittlere Überlebenszeit bei 83,8 Monaten. In den Fällen, wo initial nicht operiert worden ist, war die Prognose etwas schlechter mit einer 5 JÜR von 43,8% und einer mittleren Überlebenszeit von 38,1 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Histologisches Grading des Tumors Die Patientinnen mit G1 und G2 Stadium des Tumors zeigten erwartungsgemäß die bessere Prognose mit einer 5 JÜR von 66,7% und einer mittleren Überlebenszeit von 100,6 Monaten. Die Patientinnen mit G3 und G4 Stadium lagen bei einer 5 JÜR von 33,3% und einer mittleren Überlebenszeit von 47,6 Monaten. Diese Analyse zeigte keine statistische Signifikanz (p>0,05). 44
52 R- Status Nur in einem Fall ist eine R0- Resektion beschrieben, eine Analyse ist hier nicht möglich. FIGO Stadium Die höheren FIGO Stadien III und IV zeigten die schlechtere Prognose mit einer 5 JÜR von 38,9% und einer mittleren Überlebenszeit von 68,1 Monaten. Die Patientinnen mit FIGO Stadium I und II lagen bei einer 5 JÜR von 44,4% und einer mittleren Überlebenszeit von 77,1 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). T- Stadium Die Patientinnen mit T0 oder T1 Stadium lagen etwas besser mit ihrer 5 JÜR von 42,9% und der mittleren Überlebenszeit von 75,2 Monaten. Bei den Stadien T2, T3, T4 oder TX lagen die 5 JÜR bei 40% und die mittlere Überlebenszeit bei 62,3 Monaten. Somit lagen diese beiden Gruppen eng beieinander und die Analyse zeigte keine statistische Signifikanz (p>0,05). N- Stadium Die Patientinnen mit N0 Stadium zeigten eine bessere Prognose mit einer 5 JÜR von 57,1% und einer mittleren Überlebenszeit von 84,1 Monaten (p<0,05). Die Patientinnen mit positivem Lymphknotenstatus (N1 oder NX) lagen bei einer 5 JÜR von 30% und einer mittleren Überlebenszeit von 51,7 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). M- Stadium Die Patientinnen ohne Fernmetastasierung (M0) zeigten erwartungsgemäß die bessere Prognose mit einer 5 JÜR von 50% und einer mittleren Überlebenszeit von 880 Monaten. Die Patientinnen mit M1 oder MX Status lagen bei einer 5 JÜR von 42,9% und einer mittleren Überlebenszeit von 55,8 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). 45
53 Dosis der Brachytherapie im PDR Verfahren <50 Gy vs 50 Gy In den Fällen, wo die Dosis der Bestrahlung mit der PDR-BT weniger als 50 Gy betrug, lagen die 5 JÜR bei 40% und die mittlere Überlebenszeit bei 69,5 Monaten. Die Patientinnen, die mit 50 Gy oder mehr bestrahlt wurden, zeigten eine 5 JÜR von 50% und einer mittlere Überlebenszeit von 79,2 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Pulsdosis der Brachytherapie <0,50 Gy vs 0,50 Gy Die Patientinnen, bei denen die Pulsdosis unter 0,50 Gy lag, zeigte sich eine schlechtere Prognose mit einer 5 JÜR von 25% und einer mittleren Überlebenszeit von 45,7 Monaten. In der Vergleichsgruppe (Pulsdosis 0,50 Gy oder mehr) lagen die 5 JÜR bei 50% und die mittlere Überlebenszeit bei 74,1 Monaten. Diese Analyse blieb ohne statische Signifikanz (p>0,05). Dauer der Brachytherapie < 60 Stunden versus 60 Stunden Die Patientinnen, die weniger als 60 Stunden therapiert wurden, zeigten eine bessere Prognose mit einer 5 JÜR von 50% und einer mittleren Überlebenszeit von 79,7 Monaten. Die Patientinnen, die 60 Stunden oder länger therapiert wurden, lagen bei einer 5 JÜR von 33,3% und einer mittleren Überlebenszeit von 44 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Anzahl der Tubes <8 Stück vs 8 Stück In den Fällen, wo mit weniger als 8 Tubes gearbeitet wurde lagen die 5 JÜR bei 50% und die mittlere Überlebenszeit bei 81,6 Monaten. Etwas schlechter waren die Ergebnisse der Vergleichsgruppe bei einer 5 JÜR von 30% und einer mittleren Überlebenszeit von 56,4 Monaten. Die Analyse zeigte keine statistische Signifikanz (p>0,05). Referenzisodosis 85% vs >85% Mit einer Referenzisodosis von 85% oder weniger, zeigten die Patientinnen eine 5 JÜR von 50% und eine mittlere Überlebenszeit von 76,1 Monaten. Mit einer Referenzisodosis von über 85%, zeigten die Patientinnen eine schlechtere Prognose 46
54 mit einer 5 JÜR von 33,3% und einer mittleren Überlebenszeit von 61,5 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur Brachytherapie Nur 2 Patientinnen erhielten eine simultane Chemotherapie zur Brachytherapie und beide entwickelten ein Rezidiv. Somit ist eine vergleichende Aussage beider Gruppen nicht möglich. Perkutane Radiotherapie Die Patientinnen, die zusätzlich perkutan bestrahlt worden sind, profitierten davon mit einer 5 JÜR von 47,4% und einer mittleren Überlebenszeit von 74,4 Monaten. Die Vergleichsgruppe (nur Brachytherapie) zeigte eine 5 JÜR von 40% und eine mittlere Überlebenszeit von 56,6 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur perkutanen Radiotherapie Die Patientinnen, die simultan zur perkutanen Radiotherapie eine Chemotherapie erhalten haben, zeigten die deutlich bessere Prognose mit einer 5 JÜR von 75% und einer mittleren Überlebenszeit von 121,7 Monaten. Die Patientinnen, die nicht auf diese Weise therapiert wurden, zeigten eine 5 JÜR von 31,3% und eine mittlere Überlebenszeit von 52,1 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05) Kaplan- Meier- Analyse des OS Alter bei Therapie <70 Jahren vs 70 Jahre Die 5 JÜR bei den Patientinnen, die bei Therapie 70 Jahre oder älter waren lag bei 25% und die mittlere Überlebenszeit bei 33 Monaten. Die jüngere Patientengruppe zeigte naturgemäß die bessere Prognose mit einer 5 JÜR von 33,3% und einer mittleren Überlebenszeit von 55 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). 47
55 Vorausgegangene Operationen Die Patientinnen, die vorher operiert worden sind, zeigten die deutlich bessere Prognose mit einer 5 JÜR von 40% und einer mittleren Überlebenszeit von 54,4 Monaten. Die Patientinnen, die ohne Operation bestrahlt worden sind, zeigten eine 5 JÜR von nur 10% und eine mittlere Überlebenszeit von 29 Monaten. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). Histologisches Grading des Tumors Erwartungsgemäß zeigten die Tumore mit niedrigem Grading von G1 oder G2 die bessere Prognose mit einer 5 JÜR von 50% und einer mittleren Überlebenszeit von 53,7 Monaten. Die Tumore mit G3 und G4 Status lagen bei einer 5 JÜR von 18,2% und einer mittleren Überlebenszeit von 31,7 Monaten. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). R- Status Eine R0-Resektion kam nur in einem Fall vor, eine Analyse war hier nicht möglich. FIGO Stadium Die Patientinnen mit FIGO Stadium I und II zeigten die deutlich bessere Prognose mit einer 5 JÜR von 50% und einer mittleren Überlebenswahrscheinlichkeit von 59,5 Monaten. Die Patientinnen mit höheren FIGO Stadien II und IV zeigten eine 5 JÜR von nur 11,1% und eine mittlere Überlebenszeit von 23 Monaten. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). T- Stadium Die Patientinnen mit T0 oder T1 Stadium zeigten die besseren Ergebnisse mit einer 5 JÜR von 33,3% und einer mittleren Überlebenszeit von 47,1 Monaten. Die Vergleichsgruppe mit Stadium T2, T3, T4 oder TX zeigte eine 5 JÜR von 16,7% und eine mittlere Überlebenszeit von 23,4 Monaten. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). 48
56 N- Stadium Die Patientinnen mit negativem Lymphknotenstatus (N0) zeigten eine 5 JÜR von 25% und eine mittlere Überlebenszeit von 44,3 Monaten. Die Patientinnen mit N1 oder NX Status schnitten erwartungsgemäß etwas schlechter ab, mit einer 5 JÜR von 14,3% und einer mittleren Überlebenszeit von 29,9 Monaten. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). M- Stadium Die Patientinnen, die M0 Stadium vorzuweisen hatten, zeigten eine 5 JÜR von 42,9% und eine mittlere Überlebenszeit von 52,9 Monaten. Bei den Patientinnen, wo bereits eine Fernmetastasierung vorlag, zeigte sich eine 5 JÜR von nur 12,5% und eine mittlere Überlebenszeit von 24,2 Monaten. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). Dosis der Brachytherapie im PDR Verfahren <50 Gy vs 50 Gy Nur 2 Patientinnen erhielten eine PDR Dosis von 50 Gy oder mehr, somit ist eine repräsentativ vergleichende Aussage der beiden Gruppen nicht möglich. Pulsdosis der Brachytherapie <0,50 Gy vs 0,50 Gy Da nur 3 Patientinnen mit einer Pulsdosis von 0,50 Gy oder mehr bestrahlt worden sind und keine davon länger als 5 Jahre überlebt hat, ist eine repräsentativ vergleichende Aussage der beiden Gruppen nicht möglich. Dauer der Brachytherapie < 60 Stunden vs 60 Stunden Interessanterweise zeigten die beiden Gruppen kaum Unterschiede in Bezug auf das Gesamtüberleben. Die Patientinnen die weniger als 60 Stunden therapiert wurden zeigten eine 5 JÜR von 20%, ebenso die Gruppe die 60 Stunden oder länger in Therapie war. Die mittleren Überlebenszeiten lagen auch eng beieinander mit 37 Monaten bei der Gruppe mit weniger Therapiestunden und 38,8 Monaten bei der Vergleichsgruppe. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). 49
57 Anzahl der Tubes <8 Stück vs 8 Stück Die Patientinnen, die mit weniger als 8 Tubes in Behandlung waren, zeigten ein 5 JÜR von 37,5% und eine mittlere Überlebenszeit von 45 Monaten. Die Vergleichsgruppe zeigte eine etwas schlechtere Prognose mit einer 5 JÜR von 14,3% und einer mittleren Überlebenszeit von 29,1 Monaten. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). Referenzisodosis 85% vs >85% Die Patientinnen die mit einer Referenzisodosis von 85% oder weniger bestrahlt wurden, zeigten die deutlich schlechtere Prognose mit einer 5 JÜR von 20% und einer mittleren Überlebenszeit von 27,8 Monaten. Die Patientinnen mit einer Referenzisodosis von über 85% zeigten eine 5 JÜR von 40% und eine mittlere Überlebenszeit von 57,2 Monaten. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur Brachytherapie Nur 2 Patientinnen erhielten eine simultane Chemotherapie zur Brachytherapie und beide verstarben innerhalb des 1. Jahres nach der Therapie. Somit ist keine repräsentative Aussage möglich. Perkutane Radiotherapie Die schlechtere Prognose in Bezug aufs Gesamtüberleben zeigten die Patientinnen, die keine zusätzliche perkutane Radiotherapie erhalten haben. Hier lagen die 5 JÜR bei 25% und die mittlere Überlebenszeit bei 45 Monaten. Die Vergleichsgruppe zeigte eine 5 JÜR von 18,2% und eine mittlere Überlebenszeit von 34,7 Monaten. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur perkutanen Radiotherapie Auch hier erhielten nur 2 Patientinnen eine simultane Chemotherapie zur Brachytherapie und beide verstarben innerhalb des 1. Jahres nach der Therapie. Somit ist keine repräsentative Aussage möglich. 50
58 Nebenwirkungen Siehe folgende Tabelle: Nebenwirkungen Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Nein 18 75,0 75,0 75,0 BB-Veränderungen 1 4,2 4,2 79,2 Diarrhoe 3 12,5 12,5 91,7 Strahleninduzierte Proktitis 1 4,2 4,2 95,8 Vaginalstenose 1 4,2 4,2 100,0 Gesamtsumme ,0 100,0 Tabelle 11: Nebenwirkungsprofil Vaginal CA (primär bestrahlt) 4.2. Analyse der Patientinnen mit Vulvakarzinom Deskriptive Analyse Bezüglich der akuten Nebenwirkung nach der Brachytherapie siehe folgende Tabellen: Grad der Hautreaktion akut nach Brachytherapie Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Grad ,3 78,3 78,3 Grad 1 1 4,3 4,3 82,6 Grad 2 1 4,3 4,3 87,0 Grad 3 2 8,7 8,7 95,7 Grad 4 1 4,3 4,3 100,0 Gesamtsumme ,0 100,0 Tabelle 12: Grad der Hautreaktion akut nach Brachytherapie bei Vulva CA 51
59 Grad der Mukositis akut nach Brachytherapie Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Grad ,6 69,6 69,6 Grad ,0 13,0 82,6 Grad ,0 13,0 95,7 Grad 3 1 4,3 4,3 100,0 Gesamtsumme ,0 100,0 Tabelle 13: Grad der Mukositis akut nach Brachytherapie bei Vulva CA Bezüglich der akuten Nebenwirkungen nach perkutaner Bestrahlung siehe folgende Tabellen: Grad der Hautreaktion akut nach perk. RT Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Grad ,4 36,4 36,4 Grad 1 2 8,7 18,2 54,5 Grad 2 1 4,3 9,1 63,6 Grad ,4 36,4 100,0 Gesamtsumme 11 47,8 100,0 Fehlend System 12 52,2 Gesamtsumme ,0 Tabelle 14: Grad der Hautreaktion akut nach perk. RT bei Vulva CA Grad der Mukositis akut nach perk. RT Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Grad ,1 54,5 54,5 Grad ,0 27,3 81,8 Grad 3 2 8,7 18,2 100,0 Gesamtsumme 11 47,8 100,0 Fehlend System 12 52,2 Gesamtsumme ,0 Tabelle 15: Grad der Mukositis akut nach perk. RT bei Vulva CA 52
60 Folgende späte Nebenwirkungen sind ermittelt worden: Andere späte Nebenwirkungen Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Nein 21 91,3 91,3 91,3 Diarrhoe 1 4,3 4,3 95,7 Ödem 1 4,3 4,3 100,0 Gesamtsumme ,0 100,0 Tabelle 16: Andere späte Nebenwirkungen der Brachytherapie bei Vulva CA Siehe folgende Tabelle zur Remission: Remission 6 Wochen nach Therapie Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig Voll 16 69,6 69,6 69,6 Partiell 7 30,4 30,4 100,0 Gesamtsumme ,0 100,0 Tabelle 17: Remission 6 Wochen nach Therapie bei Vulva CA Keine der 23 Patientinnen mit Vulvakarzinom erhielt eine Erhaltungschemotherapie. Ein Lokalrezidiv nach Therapie wurde nur bei 11 Patientinnen festgestellt (47,8%). Zur Metastasenentwicklung wurde folgendes gezeigt: Metastasenlokalisation Häufigkeit Prozent Gültige Prozent Kumulative Prozente Gültig 19 82,6 82,6 82,6 Leber 1 4,3 4,3 87,0 Leber, paraaortale LK, linkes Nierenbecken 1 4,3 4,3 91,3 LK 1 4,3 4,3 95,7 Lunge, Knochen, Leber, Muskel 1 4,3 4,3 100,0 Gesamtsumme ,0 100,0 Tabelle 18: Metastasenlokalisation bei Vulvakarzinom 53
61 Die Länge des Follow-up lag in der vorliegenden Arbeit im Mittelwert bei 47,49 Monaten (von 4 bis 141 Monaten) Kaplan- Meier- Analyse bezüglich des RFS Alter bei Therapie <65 Jahre vs 65 Jahre Die Gruppe <65 Jahre bei Therapie zeigte eine signifikant bessere Prognose kein Lokalrezidiv zu entwickeln mit einer 5 JÜR von 57,1% mit einer mittleren Überlebenszeit von 82,2 Monaten. Die ältere Gruppe zeigte eine deutlich schlechtere 5 JÜR von 12,5% und die mittlere Überlebenszeit lag auch nur bei 27,5 Monaten (p<0,05). Abbildung 7: KMA bezüglich des RFS Vulva CA (Alter bei Therapie) 54
62 Rezidivbehandlung Die kleinere Gruppe (n=9), wo ein initial ein Rezidiv behandelt worden ist wies eine 5 JÜR von 11,1% und eine mittlere Überlebenszeit von 29,6 Monaten auf. Deutlich besser schnitt hingegen die Gruppe ab, wo initial kein Rezidiv behandelt worden ist mit einer 5 JÜR von 28,6% und einer mittleren Überlebenszeit von 56,8 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Vorbestrahlung Nur zwei Patientinnen wurden in ihrer Vergangenheit bereits einmal bestrahlt und beide erlitten ein Rezidiv nach 9 beziehungsweise nach 21 Monaten. Somit ist hier keine Aussage möglich. Vorausgegangene Operationen Die meisten Patientinnen unterzogen sich vor der Brachytherapie einer Operation und profitierten davon hinsichtlich der Entwicklung eines Lokalrezidivs. Hier lagen die 5 JÜR bei 23,5% und die mittlere Überlebenszeit bei 49,2 Monaten. Die Patientinnen ohne vorausgegangene Operation zeigten eine 5 JÜR von 16,7% und eine mittlere Überlebenszeit von 36,5 Monaten. Diese Analyse blieb auf Grund der geringen Patientenzahl ohne statistische Signifikanz (p>0,05). Histologisches Grading des Tumors Interessanterweise schnitt die erste Gruppe (G1 und G2) schlechter ab, als die andere Gruppe (G3, G4 und GX). Erstere erreichte eine 5 JÜR von 18,2% und eine mittlere Überlebenszeit von 39,7 Monaten. Wohingegen die Vergleichsgruppe eine 5 JÜR von 25% und eine mittlere Überlebenszeit von 47,1 Monaten erreichen konnte. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). R- Status Die Patientinnen mit R- Status R0 (n=8) zeigten eine deutlich bessere Prognose kein Lokalrezidiv zu entwickeln mit einer 5 JÜR von 37,5% und einer mittleren Überlebenszeit von 67,5 Monaten. Die Patientinnen mit R-Status R1, R2 oder RX lagen bei einer 5 JÜR von 13,3% und einer mittleren Überlebenszeit von 32,8 Monaten. Diese 55
63 Analyse blieb leider auf Grund der geringen Patientenzahlen ohne statistische Signifikanz (p>0,05). Abbildung 8: KMA bezüglich des RFS bei Vulva CA (R- Status) FIGO Stadium Die niedrigeren FIGO Stadien (FIGO I und II) zeigten schlechtere Ergebnisse als die höheren FIGO Stadien (FIGO III und IV). Erstere erreichte nur eine 5 JÜR von 14,3% und eine mittlere Überlebenszeit von 35 Monaten. Letztere lag immerhin bei einer 5 JÜR von 25% und einer mittleren Überlebenszeit von 51,8 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). T- Stadium Die erste Gruppe (T0 und T1) zeigte einen besseren Verlauf als die andere Gruppe (T2, T3, T4 und TX). Bei der ersten lagen 5 JÜR bei 28,6% und die mittlere Überlebenszeit bei 50,2 Monaten. Bei der Vergleichsgruppe lagen die 5 JÜR bei 18,8% und die mittlere 56
64 Überlebenszeit bei 42,5 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). N- Stadium Beide Gruppen waren etwa gleich groß, zeigten aber einen variablen Verlauf. Patientinnen mit negativem Lymphknotenstatus (N0) zeigten eine 5 JÜR von 16,7%, wohingegen Patientinnen mit N1/NX Status eine 5 JÜR von 27,3% aufweisen konnten. Bei der mittleren Überlebenszeit lagen beide Gruppen bei 45,8 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). M- Stadium Die Gruppe, die keine Fernmetastase aufweisen konnten (M0) hatte eine deutlich geringere Wahrscheinlichkeit ein Lokalrezidiv zu entwickeln als die Gruppe mit initialer Fernmetastasierung (M1 oder MX). Die 5 JÜR von der ersten Gruppe lag bei 22,2% und die mittlere Überlebenszeit bei 44,3 Monaten. Die Gruppe mit Fernmetastasen zeigte eine 5 JÜR von 20% und eine mittlere Überlebenszeit von 53 Monaten. Diese Analyse blieb auf Grund der geringen Patientenzahl ohne statistische Signifikanz (p>0,05). Dosis der Brachytherapie im PDR Verfahren <50 Gy vs 50 Gy Die Gruppe, die einer Dosis von <50 Gy in der PDR-Brachytherapie ausgesetzt war, zeigte die bessere Prognose in Bezug auf die Entwicklung eines Lokalrezidivs (5 JÜR 27,3% und mittlere Überlebenszeit 49,8 Monate). In der Gruppe, die mit 50 Gy in der PDR Brachytherapie bestrahlt wurde, war es etwas wahrscheinlicher ein Lokalrezidiv zu entwickeln mit einer 5 JÜR von 16,7% und einer mittleren Überlebenszeit von 42,2 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Pulsdosis der Brachytherapie <0,50 Gy vs 0,50 Gy Die Gruppe mit Pulsdosis <0,50 Gy schnitt mit einer 5 JÜR von 50% und einer mittleren Überlebenszeit von 78 Monaten deutlich besser ab als die Gruppe mit Pulsdosis 0,50 Gy. Hier zeigten sich eine 5 JÜR von 15,8% und eine mittlere Überlebenszeit von 38,1 Monaten. Diese Analyse blieb auf Grund der geringen Patientenzahl ohne statistische Signifikanz (p>0,05). 57
65 Dauer der Brachytherapie <60 Stunden vs 60 Stunden Die Patientinnen, die mit 60 oder mehr Therapiestunden bestrahlt wurden, zeigten eine höhere Wahrscheinlichkeit ein Lokalrezidiv zu entwickeln mit einer 5 JÜR von 15,4% und einer mittleren Überlebenszeit von 39,5 Monaten. Im Verglich zeigte die Gruppe mit Bestrahlungsdauer von <60 Stunden eine 5 JÜR von 25% und eine mittlere Überlebenszeit von 39,5 Monaten. Diese Analyse blieb auf Grund der geringen Patientenzahl ohne statistische Signifikanz (p>0,05). Anzahl der Tubes <8 Stück vs 8 Stück Die Patientinnen, die mit weniger als 8 Tubes behandelt worden sind, zeigten eine etwas bessere Prognose bezüglich der Entwicklung eines Lokalrezidivs mit einer 5 JÜR von 23,1% und einer mittleren Überlebenszeit von 53,7 Monaten. Die Gruppe, die mit 8 Tubes oder mehr behandelt worden ist, schnitt mit einer 5 JÜR von 20% und einer mittleren Überlebenszeit von 32 Monaten etwas schlechter ab. Auf Grund der geringen Patientenzahl bleibt diese Analyse ohne statistische Signifikanz (p>0,05). Referenzisodosis 85% vs >85% Die Mehrzahl der Patientinnen wurde mit 85% oder weniger Referenzisodosis bestrahlt und wies eine deutlich bessere Prognose auf mit einer 5 JÜR von 25% und einer mittleren Überlebenszeit von 54,1 Monaten. Nur 7 Patientinnen wurden mit einer Referenzisodosis von >85% behandelt und zeigten eine deutlich schlechtere 5 JÜR von 14,3% und eine mittlere Überlebenszeit von 28 Monaten. Auf Grund der geringen Patientenzahl blieb diese Analyse ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur Brachytherapie Nur vier Patientinnen erhielten eine simultane Chemotherapie zur Brachytherapie. 3 davon verstarben oder entwickelten ein Lokalrezidiv innerhalb von 2 Jahren. Somit ist leider keine repräsentative Analyse möglich. Perkutane Radiotherapie Die Patientinnen mit zusätzlicher perkutaner Radiotherapie (n=11) zeigten eine 5 JÜR von 27,3% und eine mittlere Überlebenszeit von 49,8 Monaten, somit profitierte diese 58
66 Gruppe in Bezug auf die Entwicklung eines Lokalrezidives deutlich gegenüber der Gruppe ohne perkutane Radiotherapie. Hier zeigte sich eine 5 JÜR von 16,7% und einer mittleren Überlebenszeit von 42,2 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie perkutane Radiotherapie Die Minderzahl der Patientinnen erhielt eine Chemotherapie simultan zur perkutanen Radiotherapie (n=5). Diese Gruppe zeigte auch die bessere Prognose mit einer 5 JÜR von 40% und einer mittleren Überlebenszeit von 52 Monaten. Die Mehrzahl der Patientinnen wurde ohne simultane Chemotherapie zur perkutanen Radiotherapie behandelt und zeigte eine 5 JÜR von 16,7% und eine mittlere Überlebenszeit von 42,9 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05) Kaplan- Meier- Analyse bezüglich des DFS Alter bei Therapie <70 Jahre vs 70 Jahre Die erste Gruppe war bei Therapie unter 70 Jahre alt, die Vergleichsgruppe 70 Jahre oder älter. Die etwas jüngeren Patientinnen hatten eine signifikant höhere Wahrscheinlichkeit weder ein Rezidiv noch eine Fernmetastasierung zu erleiden (p<0,05). Die 5 JÜR lag hier bei 57,1% und die mittlere Überlebenszeit bei 82,2 Monaten. Die älteren Patientinnen zeigten eine 5 JÜR von nur 6,3% und eine mittlere Überlebenszeit von 23,6 Monaten. 59
67 Abbildung 9: KMA bezüglich des DFS Vulva CA (Alter bei Therapie) Rezidivbehandlung Die Minderheit der Patientinnen wurde am Rezidiv behandelt (n=9) und wies auch die schlechtere Prognose auf mit einer 5 JÜR von 11,1% und einer mittleren Überlebenszeit von 23,5 Monaten. Die andere Gruppe wies im Vergleich eine etwas bessere 5 JÜR von 28,6% und eine mittlere Überlebenszeit von 56,2 Monaten auf. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Vorbestrahlung Nur zwei Patientinnen wurden vorbestrahlt, beide sind mit Tumor nach 9 beziehungsweise 21 Monaten verstorben. In wie fern nun die Vorbestrahlung Einfluss auf die Entwicklung eines Rezidivs oder Fernmetastasierung hat, ist somit nicht zu beurteilen. 60
68 Vorausgegangene Operationen Die Mehrheit der Patientinnen wurde im Vorfeld operiert und es zeigte sich, dass sie davon hinsichtlich des DFS profitieren. Die Zahlen im Vergleich: Die Patientinnen ohne Operation lagen bei einer 5 JÜR von 16,7% und einer mittleren Überlebenszeit von 27,3 Monaten. Die Patientinnen mit Operation lagen bei einer 5 JÜR von 23,5% und einer mittleren Überlebenszeit von 48,7 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Histologisches Grading des Tumors Die Patientinnen mit niedrigem Grading (G1 oder G2) schnitten im Vergleich zu den Patientinnen mit G3, G4 oder GX etwas schlechter ab. Erstere zeigten eine 5 JÜR von 18,2% und eine mittlere Überlebenszeit von 39,7 Monaten. Letztere lagen bei einer 5 JÜR von 25% und einer mittleren Überlebenszeit von 41,9 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). R- Status Die Patientinnen mit R0- Resektion (n=8) zeigten mit einer 5 JÜR von 37,5% und einer mittleren Überlebenszeit von 66,5 Monaten eine bessere Prognose als die Patientinnen mit R-Status R1, R2 oder RX. Hier lagen die 5 JÜR bei 13,3% und die mittlere Überlebenszeit bei 29,2 Monaten. Leider blieb diese Analyse auf Grund der geringen Patientenzahl ohne statistische Signifikanz (p>0,05). FIGO Stadium Die Gruppe von Patientinnen mit höheren FIGO Stadien (FIGO III oder IV) zeigte etwas bessere Zahlen mit einer 5 JÜR von 25% und einer mittleren Überlebenszeit von 47,8 Monaten. Die Gruppe mit FIGO Stadium I oder II zeigte eine 5 JÜR von 14,3% und eine mittlere Überlebenszeit von 35 Monaten. Die Analyse blieb ohne statistische Signifikanz (p>0,05). T- Stadium Die Patientinnen mit T0 oder T1 zeigten eine 5 JÜR von 28,6%. Die Patientinnen mit T2, T3, T4 oder TX zeigten eine 5 JÜR von 18,8% und beide Gruppen eine mittlere 61
69 Überlebenszeit von 42 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). N- Stadium Die Patientinnen mit negativem Lymphknotenstatus (NO) zeigten entgegen der Erwartungen eine etwas schlechtere Prognose mit einer 5 JÜR von 16,7% und einer mittleren Überlebenszeit von 40 Monaten. Die Patientinnen mit positiven oder unklaren Lymphknotenstatus (N1 oder NX) zeigten eine 5 JÜR von 27,3% und eine mittlere Überlebenszeit von 45 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). M- Stadium Die große Mehrheit der Patientinnen (n=18) zeigte keine Fernmetastasen bei Diagnosestellung (M0) und zeigte eine 5 JÜR von 22,2% mit einer mittleren Überlebenszeit von 44,3 Monaten. Die 5 Patientinnen mit M1 Stadium lagen etwas schlechter in der Prognose mit einer 5 JÜR von 20% und einer mittleren Überlebenszeit von 40,4 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Dosis der Brachytherapie im PDR Verfahren <50 Gy vs 50 Gy Die Gruppe, die mit einer Dosis von weniger als 50 Gy bestrahlt wurde, zeigte eine 5 JÜR von 27,3% und eine mittlere Überlebenszeit von 44,8 Monaten. Die Vergleichsgruppe (Dosis von 50 Gy) zeigte JÜR von 16,7% und einer mittleren Überlebenszeit von 41,5 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Pulsdosis der Brachytherapie <0,50 Gy vs 0,50 Gy Nur 4 Patientinnen erhielten eine Pulsdosis < 0,50 Gy. Die Hälfte davon blieb mit Tumor. Somit ist die 5 JÜR hier 50% und die mittlere Überlebenszeit 78 Monate. Die Patientinnen, die mit einer Pulsdosis von 0,50 Gy therapiert wurden, zeigten eine 5 JÜR von 15,8% und eine mittlere Überlebenszeit von 34,7 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). 62
70 Dauer der Brachytherapie <60 Stunden vs 60 Stunden In den Fällen unter 60 Stunden Therapiedauer zeigte sich eine 5 JÜR von 25%, die mittlere Überlebenszeit lag bei 39,7 Monaten. Die Gruppe mit Bestrahlungsdauer 60 Stunden zeigte eine schlechtere Prognose mit einer 5 JÜR von 15,4% und einer mittleren Überlebenszeit von 38,9 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Anzahl der Tubes <8 Stück vs 8 Stück Die Gruppe mit <8 Tubes schnitt etwas besser ab mit einer 5 JÜR von 23,1% und einer mittleren Überlebenszeit von 48,9 Monaten. Die Gruppe mit 8 Tubes oder mehr zeigte eine 5 JÜR von 20% mit einer mittleren Überlebenszeit von 32 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Referenzisodosis 85% vs >85% Nach fünf Jahre zeigte Gruppe mit 85% Referenzisodosis eine Überlebensrate 25% und eine mittlere Überlebenszeit von 50,2 Monaten. Wohingegen die Gruppe mit >85% Referenzisodosis nur eine 5 JÜR von 14,3% und eine mittlere Überlebenszeit von 28 Monaten aufweisen konnte. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur Brachytherapie Nur 4 Patientinnen erhielten zur Brachytherapie eine simultane Chemotherapie. Davon waren 3 mit Tumor oder bereits verstorben nach 2 Jahren. Eine vergleichende Aussage ist hier nicht möglich. Perkutane Radiotherapie Die Patientinnen die keine perkutane Radiotherapie erhielten, zeigten eine schlechtere Prognose mit einer 5 JÜR von 16,7% und einer mittleren Überlebenszeit von 41,5 Monaten. Die Patientinnen mit perkutaner Radiotherapie im Therapiekonzept erzielten eine 5 JÜR von 27,3% und eine mittlere Überlebenszeit von 44,8 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). 63
71 Simultane Chemotherapie zur perkutanen Radiotherapie Die fünf Patientinnen, die eine simultane Chemotherapie zur perkutanen Radiotherapie erhielten, scheinen davon zu profitieren mit einer 5 JÜR von 40% und einer mittleren Überlebenszeit von 52 Monaten. Die Mehrheit der Patientinnen erhielt die perkutane Radiotherapie ohne Chemotherapeutika und zeigte eine 5 JÜR von 16,7% und eine mittlere Überlebenszeit von 39,4 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05) Kaplan- Meier- Analyse bezüglich des OS Alter bei Therapie <60 Jahre vs 60 Jahre Die Patientinnen, die bei Therapie <60 Jahre alt waren, zeigten eine etwas bessere Prognose mit einer 5 JÜR von 16,7% und einer mittleren Überlebenszeit von 36,3 Monaten. Die ältere Gruppe zeigte eine 5 JÜR von nur 8,3% und eine mittlere Überlebenszeit von 26,7 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Rezidivbehandlung Die Patientinnen, die am Ersttumor behandelt wurden, zeigten eine 5 JÜR von 20% (2 JÜR 40%) und eine mittlere Überlebenszeit von 38,1 Monaten. Die Patientinnen, die am Rezidiv bestrahlt worden sind konnten nur eine 2 JÜR von 12,5% zeigen. Die mittlere Überlebenszeit lag hier bei 19,7 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Vorbestrahlung Es wurden nur 2 Patientinnen vorbestrahlt, die nach 21 Monaten, beziehungsweise nach 53 Monaten, verstarben. 64
72 Vorausgegangene Operationen Die meisten Patientinnen wurden im Vorfeld operiert und diese zeigten auch die bessere Prognose mit einer 5 JÜR von 15,4% und einer mittleren Überlebenszeit von 35,8 Monaten. Nur 5 Patientinnen wurden ohne Operation bestrahlt und die verstarben in einem Zeitraum von 5 bis 26 Monaten nach Therapie. Die mittlere Überlebenszeit betrug somit 14,6 Monate. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Histologisches Grading des Tumors Die Gruppe mit G1 und G2 zeigte in der 5 JÜR von 11,1% die gleiche Prognose wie die Vergleichsgruppe (G3, G4 oder GX). Die mittlere Überlebenszeit ging etwas auseinander und die Gruppe höhergradiger Tumore schnitt besser ab mit 33,1 Monaten, wohingegen die erste Gruppe nur 26 Monate aufweisen konnte. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). R- Status Die Patientinnen mit R- Status R0 waren alle nach 5 Jahren bereits verstorben. Ein Vergleich ist somit hier nicht möglich. FIGO Stadium Im Verlauf lagen die beiden Gruppen eng beieinander. In der Langzeitprognose hingegen, zeigte die Gruppe mit FIGO I und II eine bessere Prognose mit einer 5 JÜR von 16,7% und einer mittleren Überlebenszeit von 37,0 Monaten. Die Gruppe mit FIGO III und IV zeigte eine 5 JÜR von nur 8,3% und eine mittlere Überlebenszeit von 26,4 Monaten. Auch diese Analyse blieb ohne statistische Signifikanz (p>0,05). T- Stadium Die Gruppe mit T-Stadium 0,1 oder 2 zeigte eine 5 JÜR von 8,3% und eine mittlere Überlebenszeit von 24,9 Monaten und schnitt, etwas überraschend, schlechter ab als die Gruppe mit T- Stadium 3,4 oder X. Hier zeigte sich immerhin eine 5 JÜR von 16,7% und eine mittlere Überlebenszeit von 40 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). 65
73 N- Stadium Die Patientinnen mit negativem Lymphknotenstatus (N0) zeigten eine signifikant bessere Prognose mit einer 5 JÜR von 20% und einer mittleren Überlebenszeit von 40,6 Monaten. Die Gruppe mit positivem Lymphknotenstatus (N1 oder NX) verstarben innerhalb von 5 bis 53 Monaten nach Therapie und zeigten eine mittlere Überlebenszeit von 16,6 Monaten. Diese Analyse zeigte eine statistische Signifikanz (p<0,05). Abbildung 10: KMA bezüglich des OS bei Vulva CA (N- Stadium) M- Stadium Die Patientinnen, die ohne Fernmetastasierung therapiert wurden, zeigten erwartungsgemäß die bessere Prognose mit einer 5 JÜR von 7,1% und einer mittleren Überlebenszeit von 30,7 Monaten. Von den Patientinnen, die schon M1 oder MX Stadium bei Diagnosestellung hatten, lebte keine mehr nach 5 Jahren (5 JÜR 0%) und 66
74 die mittlere Überlebenszeit lag aber nur knapp unter der anderen Gruppe mit 27,2 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Dosis der Brachytherapie im PDR Verfahren <50 Gy vs 50 Gy Die Gruppen waren in etwa gleich groß. Die Gruppe mit Dosisapplikation <50 Gy verstarb vollständig innerhalb von 5 bis 27 Monaten nach Therapie. Die mittlere Überlebenszeit lag bei 11,2 Monaten. Die Gruppe mit 50 Gy Dosisapplikation zeigte eine signifikant bessere Prognose mit einer 5 JÜR von 20% und einer mittleren Überlebenszeit von 44,9 Monaten (p<0,05). Pulsdosis der Brachytherapie 0,50 Gy vs >0,50 Gy Die Patientinnen die mit 0,50 Gy Pulsdosis bestrahlt worden sind, zeigten eine 5 JÜR von 14,3% und eine mittlere Überlebenszeit von 27,1 Monaten. Die Gruppe, die mit >0,50 Gy Pulsdosis bestrahlt worden ist, zeigte eine leicht bessere Prognose mit einer 5 JÜR von 18,2% und einer mittleren Überlebenszeit von 31,7 Monaten. Insgesamt lagen die beiden Gruppen eng beieinander und die Analyse blieb ohne statistische Signifikanz (p>0,05). Dauer der Brachytherapie <60 Stunden vs 60 Stunden Alle Patientinnen, die weniger als 60 Stunden therapiert wurden (n=6) verstarben innerhalb von 5 bis 14 Monaten nach Therapie (mittlere Überlebenszeit von 8,8 Monaten). Ein Vergleich ist hier nicht aussagekräftig. Anzahl der Tubes <8 Stück vs 8 Stück Die Patientinnen die mit weniger als 8 Tubes therapiert wurden, zeigten anfangs eine ähnliche Prognose wie die Vergleichsgruppe. Allerdings verbesserte sich dann die Prognose deutlich auf eine 5 JÜR von 20% und eine mittlere Überlebenszeit von 40,5 Monaten. Die Patientinnen die mit 8 oder mehr Tubes behandelt worden sind verstarben alle innerhalb von 5 bis 41 Monaten nach Therapie und die mittlere Überlebenszeit lag hier bei nur 16,7 Monaten. Diese Analyse blieb leider ohne statistische Signifikanz (p>0,05). 67
75 Referenzisodosis 85% vs >85% Die erste Gruppe (Referenzisodosis 85%) zeigte eine leicht bessere Prognose mit einer 5 JÜR von 16,7% und einer mittleren Überlebenszeit von 32,5 Monaten. In der Vergleichsgruppe (Referenzisodosis >85%) verstarben alle Patientinnen innerhalb von 9 bis 53 Monaten nach Therapie und die mittlere Überlebenszeit lag bei 24,6 Monaten. Diese Analyse blieb ohne statistische Signifikanz (p>0,05). Simultane Chemotherapie zur Brachytherapie Nur 3 Patientinnen erhielten eine simultane Chemotherapie zur Brachytherapie und sie verstarben 5 bis 27 Monate nach der Therapie. Die mittlere Überlebenszeit betrug somit 17,6 Monate. Ein Vergleich der 5 JÜR ist hier nicht möglich. Perkutane Radiotherapie Die Patientinnen ohne zusätzliche perkutane Radiotherapie zeigten eine 5 JÜR von 20% und eine mittlere Überlebenszeit von 44, 9 Monaten. Die Patientinnen die eine perkutane Radiotherapie erhielten (n=8) verstarben in einem Zeitraum zwischen 5 und 27 Monaten nach Therapie. Ein Vergleich ist hier nicht repräsentativ. Simultane Chemotherapie zur perkutanen Radiotherapie Nur 3 Patientinnen erhielten eine simultane Chemotherapie zur perkutanen Radiotherapie und alle verstarben in einem Zeitraum von 5 bis 27 Monaten nach Therapie. Auch hier ist ein Vergleich nicht möglich Subanalyse der primär behandelten Patientinnen Im Folgenden werden die Patientinnen (n=2), die in ihrer Vorgeschichte bereits bestrahlt wurden von der Analyse ausgeschlossen. 68
76 Kaplan- Meier- Analyse des RFS Alter bei Therapie < 65 Jahre vs 65 Jahre Die Patientinnen, die bei Therapie unter 65 Jahre alt waren, zeigten eine signifikant bessere Prognose kein Lokalrezidiv zu entwickeln (p<0,05). Mit einer 5 JÜR von 66,7% und einer mittleren Überlebenszeit von 92,5 Monaten lagen die jüngeren Patientinnen deutlich besser als die Patientinnen die über 65 Jahre oder älter waren (5 JÜR 6,7% und mittlere Überlebenszeit von 28,8 Monaten). Abbildung 11: KMA bezüglich des RFS bei Vulva CA (primär behandelt) Alter bei Therapie Vorausgegangene Operationen Die Patientinnen ohne Operation zeigten eine 5 JÜR von 20% und eine mittlere Überlebenszeit von 39,6 Monaten. Die Patientinnen, die vorher operiert worden sind, 69
Thomas G. Wendt Stand 31. Januar 2013
 Thomas G. Wendt Stand 31. Januar 2013 Prätherapeutisch: Posttherapeutisch: FIGO ptnm (UICC) ( Féderation Internationale de Gynécologie et d Obstétrique) TNM (UICC) (UICC= Union International Contre le
Thomas G. Wendt Stand 31. Januar 2013 Prätherapeutisch: Posttherapeutisch: FIGO ptnm (UICC) ( Féderation Internationale de Gynécologie et d Obstétrique) TNM (UICC) (UICC= Union International Contre le
1 Einleitung Das Mammakarzinom Epidemiologie Ätiologie Risikofaktoren Protektive Faktoren 3
 Inhaltsverzeichnis 1 Einleitung 1 1.1 Das Mammakarzinom 1 1.1.1 Epidemiologie 1 1.1.2 Ätiologie 2 1.1.2.1 Risikofaktoren 2 1.1.2.2 Protektive Faktoren 3 1.1.3 Prognosefaktoren 4 1.2 Rezeptorstatus 5 1.2.1
Inhaltsverzeichnis 1 Einleitung 1 1.1 Das Mammakarzinom 1 1.1.1 Epidemiologie 1 1.1.2 Ätiologie 2 1.1.2.1 Risikofaktoren 2 1.1.2.2 Protektive Faktoren 3 1.1.3 Prognosefaktoren 4 1.2 Rezeptorstatus 5 1.2.1
Vulvakarzinom Epitheliales Ovarialkarzinom Zervixkarzinom Endometriumkarzinom
 Vulvakarzinom Epitheliales Ovarialkarzinom Zervixkarzinom Endometriumkarzinom Verantwortlich: M. Bossart, K.Henne Freigabe: interdisziplinärer Qualitätszirkel Stand: 06/16, gültig bis 07/18 Version 3.1
Vulvakarzinom Epitheliales Ovarialkarzinom Zervixkarzinom Endometriumkarzinom Verantwortlich: M. Bossart, K.Henne Freigabe: interdisziplinärer Qualitätszirkel Stand: 06/16, gültig bis 07/18 Version 3.1
Tumor des Gebärmutterhalses (Zervixtumor) (1)
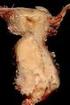 Tumor des Gebärmutterhalses (Zervixtumor) (1) Epidemiologie: Die Inzidenz des Zervixkarzinoms wird vom Robert-Koch-Institut für 2004 mit 14,7 pro 100 000 Frauen pro Jahr angegeben (rohe Rate+). Eine Abnahme
Tumor des Gebärmutterhalses (Zervixtumor) (1) Epidemiologie: Die Inzidenz des Zervixkarzinoms wird vom Robert-Koch-Institut für 2004 mit 14,7 pro 100 000 Frauen pro Jahr angegeben (rohe Rate+). Eine Abnahme
Hauptvorlesung Gynäkologie und Geburtshilfe
 Hauptvorlesung Gynäkologie und Geburtshilfe X. Diagnostik und Therapie der Tumoren von Cervix, Vagina und Vulva 1 2 3 08.11. Pat. stellt sich mit Schmerzen und zunehmender Blutung in der 10. SSW vor. Ein
Hauptvorlesung Gynäkologie und Geburtshilfe X. Diagnostik und Therapie der Tumoren von Cervix, Vagina und Vulva 1 2 3 08.11. Pat. stellt sich mit Schmerzen und zunehmender Blutung in der 10. SSW vor. Ein
Tumor des Gebärmutterkörpers (1)
 Tumor des Gebärmutterkörpers (1) Epidemiologie: Das Korpuskarzinom (auch Endometriumkarzinom) ist der häufigste weibliche Genitaltumor. Das Robert-Koch-Institut gibt die Inzidenz in Deutschland für 2004
Tumor des Gebärmutterkörpers (1) Epidemiologie: Das Korpuskarzinom (auch Endometriumkarzinom) ist der häufigste weibliche Genitaltumor. Das Robert-Koch-Institut gibt die Inzidenz in Deutschland für 2004
Pathologie, Typisierung, Ausbreitungsstadien
 1 24 Anal(kanal)karzinom H. Wiesinger Pathologie, Typisierung, Ausbreitungsstadien Tumoren der Analregion werden in solche des Analkanals und des Analrandes unterteilt. Der Analkanal erstreckt sich vom
1 24 Anal(kanal)karzinom H. Wiesinger Pathologie, Typisierung, Ausbreitungsstadien Tumoren der Analregion werden in solche des Analkanals und des Analrandes unterteilt. Der Analkanal erstreckt sich vom
Analtumor (1) D01.3 Carcinoma in situ des Analkanals und des Anus (ohne Haut)
 Analtumor (1) Epidemiologie: Das Analkarzinom tritt eher selten auf. Insgesamt erkranken in Deutschland pro Jahr 0,5-1,5 pro 100.000 Einwohner daran, mit steigender Tendenz. Frauen sind etwa dreimal so
Analtumor (1) Epidemiologie: Das Analkarzinom tritt eher selten auf. Insgesamt erkranken in Deutschland pro Jahr 0,5-1,5 pro 100.000 Einwohner daran, mit steigender Tendenz. Frauen sind etwa dreimal so
Pathologie und Prognoseparameter. AGO e.v. in der DGGG e.v. sowie in der DKG e.v. Dietmar Schmidt Institut für Pathologie A2,2; Mannheim
 Pathologie und Prognoseparameter Dietmar Schmidt Institut für Pathologie A2,2; Mannheim Endometriales Adenokarzinom Histologische Typen (WHO 2003) Endometrioid Muzinös Serös Klarzellig Undifferenziert
Pathologie und Prognoseparameter Dietmar Schmidt Institut für Pathologie A2,2; Mannheim Endometriales Adenokarzinom Histologische Typen (WHO 2003) Endometrioid Muzinös Serös Klarzellig Undifferenziert
kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ
 WS 2014/2015 kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ (zur Symptomlinderung) wenn lokale Beschwerden
WS 2014/2015 kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ (zur Symptomlinderung) wenn lokale Beschwerden
Absolute Neuerkrankungen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Absolute Neuerkrankungen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate alterstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015 männlich
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate alterstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015 männlich
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung
 Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.01.2006 bis 30.06.2006 Erstellungstag: 30.06.2006 Erstellungssoftware: Rückmeldesystem
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.01.2006 bis 30.06.2006 Erstellungstag: 30.06.2006 Erstellungssoftware: Rückmeldesystem
Originalarbeit: James et al., N Engl J Med 2012; 366:
 Originalarbeit: James et al., N Engl J Med 2012; 366: 1477-1488 Kommentar zur Originalarbeit: Shipley & Zietman N Engl J Med 2012; 366: 1540-41 Meilenstein BC2001-Studie: Design randomisierte Studie mit
Originalarbeit: James et al., N Engl J Med 2012; 366: 1477-1488 Kommentar zur Originalarbeit: Shipley & Zietman N Engl J Med 2012; 366: 1540-41 Meilenstein BC2001-Studie: Design randomisierte Studie mit
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung
 Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.07.2005 bis 31.12.2005 Erstellungstag: 15.05.2006 Erstellungssoftware: Rückmeldesystem
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.07.2005 bis 31.12.2005 Erstellungstag: 15.05.2006 Erstellungssoftware: Rückmeldesystem
Operative und systemische Therapie des Zervixkarzinoms
 Operative und systemische Therapie des Zervixkarzinoms J. Huober Workshop DESO St.Gallen 20./21. Februar 2015 Univ.-Frauenklinik Ulm Integratives Tumorzentrum des Universitätsklinikums und der Medizinischen
Operative und systemische Therapie des Zervixkarzinoms J. Huober Workshop DESO St.Gallen 20./21. Februar 2015 Univ.-Frauenklinik Ulm Integratives Tumorzentrum des Universitätsklinikums und der Medizinischen
Welche Informationen finden Sie in Ihrem Befund?
 Welche Informationen finden Sie in Ihrem Befund? Impressum Herausgeberin UniversitätHamburg,MIN-Fakultät,Gesundheitswissenschaften Martin-Luther-King-Platz6 20146Hamburg Internet: www.spupeo.de www.chemie.uni-hamburg.de/igtw/gesundheit/gesundheit.htm
Welche Informationen finden Sie in Ihrem Befund? Impressum Herausgeberin UniversitätHamburg,MIN-Fakultät,Gesundheitswissenschaften Martin-Luther-King-Platz6 20146Hamburg Internet: www.spupeo.de www.chemie.uni-hamburg.de/igtw/gesundheit/gesundheit.htm
arithm. Alter Jahre medianes Alter Jahre
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter 2011-2016 118 2,7 1,6 69,5
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter 2011-2016 118 2,7 1,6 69,5
Empfehlungen für die Diagnostik und Therapie des Endometriumkarzinoms
 Empfehlungen für die Diagnostik und Therapie des Endometriumkarzinoms Aktualisierte Empfehlungen der Kommission Uterus auf Grundlage der S2k Leitlinie (Version 1.0, 1.6.2008) ohne Angabe der Evidenzlevel
Empfehlungen für die Diagnostik und Therapie des Endometriumkarzinoms Aktualisierte Empfehlungen der Kommission Uterus auf Grundlage der S2k Leitlinie (Version 1.0, 1.6.2008) ohne Angabe der Evidenzlevel
Diagnostik und Therapie primärer und metastasierter Mammakarzinome
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Loko-regionäres Rezidiv Version 2002-2009: Brunnert / Simon/ Audretsch / Bauerfeind / Costa / Dall/ Gerber / Göhring / Lisboa / Rezai
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Loko-regionäres Rezidiv Version 2002-2009: Brunnert / Simon/ Audretsch / Bauerfeind / Costa / Dall/ Gerber / Göhring / Lisboa / Rezai
Cervix uteri. 3.5 Cervix uteri
 87 3.5 Das Zervixkarzinom ist der zweithäufigste bösartige Tumor der Frau in der Welt [Par97]. In Deutschland steht es an sechster Stelle (nach Brust- und Darmkrebs, Tumoren der Atmungsorgane und der Gebärmutter,
87 3.5 Das Zervixkarzinom ist der zweithäufigste bösartige Tumor der Frau in der Welt [Par97]. In Deutschland steht es an sechster Stelle (nach Brust- und Darmkrebs, Tumoren der Atmungsorgane und der Gebärmutter,
Chemnitz, Stadt, Erzgebirgskreis, Mittelsachsen, Zwickau. medianes Alter Jahre. arithm. Alter Jahre
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter 2011-2015 52 2,5 1,5 69,3
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter 2011-2015 52 2,5 1,5 69,3
Uterine Sarkome. S2k Leitlinie AWMF-Nummer 015/074
 S2k Leitlinie AWMF-Nummer 015/074 Version 1 Gültig 08/15 07/18 Federführende Autoren: Dominik Denschlag Falk C. Thiel Matthias W. Beckmann Mitglieder der Arbeitsgruppe: Sven Ackermann Lars Christian Horn
S2k Leitlinie AWMF-Nummer 015/074 Version 1 Gültig 08/15 07/18 Federführende Autoren: Dominik Denschlag Falk C. Thiel Matthias W. Beckmann Mitglieder der Arbeitsgruppe: Sven Ackermann Lars Christian Horn
Harnröhrentumor (1) D09.1 Carcinoma in situ sonstiger und nicht näher bezeichneter Harnorgane
 Harnröhrentumor (1) Epidemiologie: Malignome der Urethra sind sehr selten. Ihre Inzidenz pro 100 000 Einwohner und Jahr wird auf 0,4 bei Männern und 1,5 bei Frauen geschätzt. Frauen sind aufgrund ihrer
Harnröhrentumor (1) Epidemiologie: Malignome der Urethra sind sehr selten. Ihre Inzidenz pro 100 000 Einwohner und Jahr wird auf 0,4 bei Männern und 1,5 bei Frauen geschätzt. Frauen sind aufgrund ihrer
Aspekte zur Indikation und Auswahl der Radiotherapie
 Aspekte zur Indikation und Auswahl der Radiotherapie Kurative oder palliative Therapie (medianes Überleben 1 2 Jahre) Zielvolumen Sequenz Neoadjuvant (vor OP) Postoperativ adjuvant Definitiv bei Inoperabilität
Aspekte zur Indikation und Auswahl der Radiotherapie Kurative oder palliative Therapie (medianes Überleben 1 2 Jahre) Zielvolumen Sequenz Neoadjuvant (vor OP) Postoperativ adjuvant Definitiv bei Inoperabilität
Ergebnis-Cockpit Anlage zum Erhebungsbogen für die Zertifizierung von Brustgesundheitszentren (BGZ)
 von Brustgesundheitszentren Ergebnis-Cockpit Anlage zum Erhebungsbogen für die von Brustgesundheitszentren (BGZ) Version 4.0 vom 20.04.2015 Angaben des Name des Brustgesundheitszentrums Straße Ort Name
von Brustgesundheitszentren Ergebnis-Cockpit Anlage zum Erhebungsbogen für die von Brustgesundheitszentren (BGZ) Version 4.0 vom 20.04.2015 Angaben des Name des Brustgesundheitszentrums Straße Ort Name
Was ist Strahlentherapie?
 Was ist Strahlentherapie? Ionisierende Strahlen werden gezielt eingesetzt um Tumorgewebe zu beeinflussen / zu zerstören Wirkung erfolgt über zellbiologische Mechanismen lokale / lokoregionäre Therapieform
Was ist Strahlentherapie? Ionisierende Strahlen werden gezielt eingesetzt um Tumorgewebe zu beeinflussen / zu zerstören Wirkung erfolgt über zellbiologische Mechanismen lokale / lokoregionäre Therapieform
1. Vorbemerkung Ziel der vorliegenden Arbeit Das Mammakarzinom Historischer Überblick 2
 INHALTSVERZEICHNIS Seite I. EINLEITUNG 1. Vorbemerkung 1 2. Ziel der vorliegenden Arbeit 1 3. Das Mammakarzinom 2 3.1. Historischer Überblick 2 3.2. Ätiologie 4 3.2.1. Genetische und familiäre Disposition
INHALTSVERZEICHNIS Seite I. EINLEITUNG 1. Vorbemerkung 1 2. Ziel der vorliegenden Arbeit 1 3. Das Mammakarzinom 2 3.1. Historischer Überblick 2 3.2. Ätiologie 4 3.2.1. Genetische und familiäre Disposition
Radiotherapie beim Prostatakarzinom Innovative Therapiestrategien
 KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Radiotherapie beim Prostatakarzinom Innovative Therapiestrategien Ziele der Strahlentherapie Verbesserung der
KLINIK UND POLIKLINIK FÜR STRAHLENTHERAPIE UND RADIO-ONKOLOGIE UNIVERSITÄTSKLINIKUM LEIPZIG Radiotherapie beim Prostatakarzinom Innovative Therapiestrategien Ziele der Strahlentherapie Verbesserung der
Empfehlungen für die Diagnostik und Therapie des Endometriumkarzinoms
 Empfehlungen für die Diagnostik und Therapie des Endometriumkarzinoms Aktualisierte Empfehlungen der Kommission Uterus auf Grundlage der S2k Leitlinie (Version 1.0, 1.6.2008) ohne Angabe der Evidenzlevel
Empfehlungen für die Diagnostik und Therapie des Endometriumkarzinoms Aktualisierte Empfehlungen der Kommission Uterus auf Grundlage der S2k Leitlinie (Version 1.0, 1.6.2008) ohne Angabe der Evidenzlevel
Langzeit-follow-up Datenbanken bei Mammakarzinom unter besonderer Berücksichtigung der Therapiewahl
 Aus dem Robert-Bosch-Krankenhaus Stuttgart (Akademisches Lehrkrankenhaus der Universität Tübingen) Abteilung für Gynäkologie und Geburtshilfe Chefarzt Professor Dr. W. E. Simon Langzeit-follow-up Datenbanken
Aus dem Robert-Bosch-Krankenhaus Stuttgart (Akademisches Lehrkrankenhaus der Universität Tübingen) Abteilung für Gynäkologie und Geburtshilfe Chefarzt Professor Dr. W. E. Simon Langzeit-follow-up Datenbanken
Netter's Gynäkologie
 Netter's Gynäkologie 1. Auflage 2005. Buch. 480 S. Hardcover ISBN 978 3 13 141011 5 Format (B x L): 12,5 x 19 cm Weitere Fachgebiete > Medizin > Klinische und Innere Medizin > Gynäkologie, Geburtshilfe,
Netter's Gynäkologie 1. Auflage 2005. Buch. 480 S. Hardcover ISBN 978 3 13 141011 5 Format (B x L): 12,5 x 19 cm Weitere Fachgebiete > Medizin > Klinische und Innere Medizin > Gynäkologie, Geburtshilfe,
2. Material und Methoden
 9 2. Material und Methoden 2.1. Auswahlkriterien und Untersuchungsvorgang Dieser Arbeit liegen die Daten von 107 Patienten zugrunde, die im Zeitraum vom 01.01.1993 bis 31.12.1998 an der Klinik für Orthopädie
9 2. Material und Methoden 2.1. Auswahlkriterien und Untersuchungsvorgang Dieser Arbeit liegen die Daten von 107 Patienten zugrunde, die im Zeitraum vom 01.01.1993 bis 31.12.1998 an der Klinik für Orthopädie
Absolute Neuerkrankungszahlen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre median. Alter Jahre Vergleich median. Alter 2010-2014 männlich 378 25,4 15,4
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre median. Alter Jahre Vergleich median. Alter 2010-2014 männlich 378 25,4 15,4
Studienzentrum der Deutschen Gesellschaft für f. SYNCHRONOUS Trial
 Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
ENDOMETRIUM- KARZINOM
 ENDOMETRIUM- KARZINOM 1 ENDOMETRIUMKARZINOM Epidemiologie und Ätiologie Das Endometriumkarzinom (Gebärmutterkörperkrebs), ist die vierthäufigste Krebserkrankung der Frau. 12% aller Krebsarten der Frau
ENDOMETRIUM- KARZINOM 1 ENDOMETRIUMKARZINOM Epidemiologie und Ätiologie Das Endometriumkarzinom (Gebärmutterkörperkrebs), ist die vierthäufigste Krebserkrankung der Frau. 12% aller Krebsarten der Frau
Diskussion Radiotherapie Osteosarkome Osteosarkome des appendikulären Skeletts werden in der Regel nicht intensiv mit Bestrahlung therapiert, da
 Diskussion Radiotherapie Osteosarkome Osteosarkome des appendikulären Skeletts werden in der Regel nicht intensiv mit Bestrahlung therapiert, da entweder durch Amputation oder durch gliedmaßenerhaltende
Diskussion Radiotherapie Osteosarkome Osteosarkome des appendikulären Skeletts werden in der Regel nicht intensiv mit Bestrahlung therapiert, da entweder durch Amputation oder durch gliedmaßenerhaltende
Orthopädische Klinik König Ludwig Haus
 ZMF Problematik meist erst späte Diagnosestelllung Erschwerte Resektabilität * Problematik R0 Resektion schwierig / unmöglich Postoperative Strahlentherapie indiziert * Indikation zur adjuvanten Radiotherapie
ZMF Problematik meist erst späte Diagnosestelllung Erschwerte Resektabilität * Problematik R0 Resektion schwierig / unmöglich Postoperative Strahlentherapie indiziert * Indikation zur adjuvanten Radiotherapie
8. PLZ String 5 Postleitzahl 9. Diagnosedatum Datumsformat yyyymmdd Diagnosedatum Frühestes Datum mit mindestens klinischer Sicherung
 grundsätzlich jedes im definierten Zeitraum (2000-2008) neu diagnostizierte Mammakarzinom melden; Mammatumoren bds. extra melden 1. Importquelle String 30 Datenherkunft, Register Benutzung von Kürzeln
grundsätzlich jedes im definierten Zeitraum (2000-2008) neu diagnostizierte Mammakarzinom melden; Mammatumoren bds. extra melden 1. Importquelle String 30 Datenherkunft, Register Benutzung von Kürzeln
Absolute Neuerkrankungszahlen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre median. Alter Jahre Vergleich median. Alter 2010-2014 männlich 986 27,2 16,7
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre median. Alter Jahre Vergleich median. Alter 2010-2014 männlich 986 27,2 16,7
Erhebungsbogen für Gynäkologische Krebszentren
 zum Erhebungsbogen für der Deutschen Krebsgesellschaft Vorsitz der Zertifizierungskommission: Prof. Dr. M.W. Beckmann Im Rahmen der Zertifizierungsverfahren treten regelmäßig Fragestellungen auf, die eine
zum Erhebungsbogen für der Deutschen Krebsgesellschaft Vorsitz der Zertifizierungskommission: Prof. Dr. M.W. Beckmann Im Rahmen der Zertifizierungsverfahren treten regelmäßig Fragestellungen auf, die eine
GI-ONCOLOGY INTERDISZIPLINÄRES UPDATE. Die neue TNM-Klassifikation von Tumoren. des oberen Gastrointestinaltrakts
 GI-ONCOLOGY 2010 6. INTERDISZIPLINÄRES UPDATE Die neue TNM-Klassifikation von Tumoren des oberen Gastrointestinaltrakts Christian Wittekind, Institut für Pathologie des UKL, Liebigstrasse 26, 04103 Leipzig
GI-ONCOLOGY 2010 6. INTERDISZIPLINÄRES UPDATE Die neue TNM-Klassifikation von Tumoren des oberen Gastrointestinaltrakts Christian Wittekind, Institut für Pathologie des UKL, Liebigstrasse 26, 04103 Leipzig
Ausgangssituation und Zielsetzung
 Ausgangssituation und Zielsetzung Beim lokalisierten Prostatakarzinom ist eine Therapie nicht immer nötig; aktive Überwachung kommt für viele Patienten als beste Option in Frage Wenn eine lokale Therapie
Ausgangssituation und Zielsetzung Beim lokalisierten Prostatakarzinom ist eine Therapie nicht immer nötig; aktive Überwachung kommt für viele Patienten als beste Option in Frage Wenn eine lokale Therapie
Stephanie Rieger Dr.med.
 Stephanie Rieger Dr.med. Maligne Tumoren am knöchernen Becken, einschließlich des Multiplen Myeloms Untersuchung am Patientengut der Orthopädischen Universitätsklinik Heidelberg von 1974 bis 1998 Geboren
Stephanie Rieger Dr.med. Maligne Tumoren am knöchernen Becken, einschließlich des Multiplen Myeloms Untersuchung am Patientengut der Orthopädischen Universitätsklinik Heidelberg von 1974 bis 1998 Geboren
Absolute Neuerkrankungszahlen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Prostatakarzinom lokal Dr. med. J. Heß
 Prostatakarzinom lokal 30.11.2011 Dr. med. J. Heß Risiko für Prostatakarzinom: 40% Risiko für klinisch relevantem PCA: 10% Risiko für PCA-spezifischen Tod.: 3% Prostata, Lung, Colorectal and Ovarian Cancer
Prostatakarzinom lokal 30.11.2011 Dr. med. J. Heß Risiko für Prostatakarzinom: 40% Risiko für klinisch relevantem PCA: 10% Risiko für PCA-spezifischen Tod.: 3% Prostata, Lung, Colorectal and Ovarian Cancer
Brustkrebs. Patientenratgeber zu den AGO-Empfehlungen 2015 III
 II III Brustkrebs Patientenratgeber zu den AGO-Empfehlungen 2015 herausgegeben von Anton Scharl im Namen der Kommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie e.v. (AGO) für Patientinnen,
II III Brustkrebs Patientenratgeber zu den AGO-Empfehlungen 2015 herausgegeben von Anton Scharl im Namen der Kommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie e.v. (AGO) für Patientinnen,
Harnblasenkrebs (1) C C67.9 entsprechen den Lokalisationsschlüsseln nach ICD-O-3 von 2013.
 Harnblasenkrebs (1) Epidemiologie: Das Robert-Koch-Institut in Berlin gibt für 2008 die Zahl der Harnblasenkrebs-Neuerkrankungen pro 100 000 Einwohner für Männer mit 28,5 und für Frauen mit 10,8 pro Jahr
Harnblasenkrebs (1) Epidemiologie: Das Robert-Koch-Institut in Berlin gibt für 2008 die Zahl der Harnblasenkrebs-Neuerkrankungen pro 100 000 Einwohner für Männer mit 28,5 und für Frauen mit 10,8 pro Jahr
Organbegrenztes Prostatakarzinom
 Organbegrenztes Prostatakarzinom Michael Stöckle Klinik für Urologie und Kinderurologie Universitätsklinikum des Saarlandes, Homburg/Saar Seite Ausgangssituation Prostata-Ca ist häufigh 3% aller Männer
Organbegrenztes Prostatakarzinom Michael Stöckle Klinik für Urologie und Kinderurologie Universitätsklinikum des Saarlandes, Homburg/Saar Seite Ausgangssituation Prostata-Ca ist häufigh 3% aller Männer
Chemnitz, Stadt, Erzgebirgskreis, Mittelsachsen, Zwickau. arithm. Alter Jahre
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Absolute Neuerkrankungen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Primärtherapie des malignen Melanoms. B. Knopf, Zwickau
 Primärtherapie des malignen Melanoms B. Knopf, Zwickau Therapie des malignen Melanoms - Chirurgie - Radiatio - chirurgische Exzision + Radiatio - adjuvante medikamentöse Therapie - Chemotherapie - Immuntherapie
Primärtherapie des malignen Melanoms B. Knopf, Zwickau Therapie des malignen Melanoms - Chirurgie - Radiatio - chirurgische Exzision + Radiatio - adjuvante medikamentöse Therapie - Chemotherapie - Immuntherapie
Uterine Leiomyosarkome
 Uterine Leiomyosarkome U. A. Ulrich Martin-Luther-Krankenhaus, Berlin AGO State-of-the-Art München, 6. 8. April 2017 LMS: Epidemiologie 1,3 % der uterinen Malignome, 50 % der uterinen Sarkome medianes
Uterine Leiomyosarkome U. A. Ulrich Martin-Luther-Krankenhaus, Berlin AGO State-of-the-Art München, 6. 8. April 2017 LMS: Epidemiologie 1,3 % der uterinen Malignome, 50 % der uterinen Sarkome medianes
Absolute Neuerkrankungszahlen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Klinik und Dokumentation des Prostatakarzinoms. M.Niewald
 17. Informationstagung Tumordokumentation Klinik und Dokumentation des Prostatakarzinoms M.Niewald Klinik für Strahlentherapie und Radioonkologie Universitätsklinikum des Saarlandes Homburg/Saar Herrn
17. Informationstagung Tumordokumentation Klinik und Dokumentation des Prostatakarzinoms M.Niewald Klinik für Strahlentherapie und Radioonkologie Universitätsklinikum des Saarlandes Homburg/Saar Herrn
Kosmetisches Ergebnis, Spätnebenwirkungen und Lebensqualität nach brusterhaltender Operation und Strahlentherapie des Mammakarzinoms
 Aus der Universitätsklinik und Poliklinik für Strahlentherapie an der Martin-Luther-Universität Halle-Wittenberg (Komm. Direktorin: PD Dr. med. G. Hänsgen) Kosmetisches Ergebnis, Spätnebenwirkungen und
Aus der Universitätsklinik und Poliklinik für Strahlentherapie an der Martin-Luther-Universität Halle-Wittenberg (Komm. Direktorin: PD Dr. med. G. Hänsgen) Kosmetisches Ergebnis, Spätnebenwirkungen und
Intraoperative Strahlentherapie bei Brustkrebs. Patienteninformation zur intraoperativen Strahlentherapie des Tumorbettes (Boost)
 Intraoperative Strahlentherapie bei Brustkrebs Patienteninformation zur intraoperativen Strahlentherapie des Tumorbettes (Boost) 1 Kein Grund für Verzweiflung Wenn die Diagnose Brustkrebs festgestellt
Intraoperative Strahlentherapie bei Brustkrebs Patienteninformation zur intraoperativen Strahlentherapie des Tumorbettes (Boost) 1 Kein Grund für Verzweiflung Wenn die Diagnose Brustkrebs festgestellt
Brustkrebs von der Diagnose bis zur Nachsorge
 Brustkrebs von der Diagnose bis zur Nachsorge Schaffhausen 28.10.2014 Dr. U.R. Meier Direktor Klinik für Radio-Onkologie Kantonsspital Winterthur Radio-Onkologie Die Lehre von der Behandlung bösartiger
Brustkrebs von der Diagnose bis zur Nachsorge Schaffhausen 28.10.2014 Dr. U.R. Meier Direktor Klinik für Radio-Onkologie Kantonsspital Winterthur Radio-Onkologie Die Lehre von der Behandlung bösartiger
H. Wilsdorf-Köhler, R. Stabenow. der Länder Berlin, Brandenburg, Mecklenburg-Vorpommern, Sachsen-Anhalt und der Freistaaten Sachsen und Thüringen
 Wie haben sich die Überlebenszeiten bei älteren (über 75 Jahre) im Vergleich zu jüngeren Krebspatienten (unter 65 Jahre) in den letzten 20 Jahren entwickelt? H. Wilsdorf-Köhler, R. Stabenow der Länder
Wie haben sich die Überlebenszeiten bei älteren (über 75 Jahre) im Vergleich zu jüngeren Krebspatienten (unter 65 Jahre) in den letzten 20 Jahren entwickelt? H. Wilsdorf-Köhler, R. Stabenow der Länder
Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom
 Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom Prof. Dr. med. R. Fietkau Strahlenklinik Ngan et al. 2012 Rectal-Ca: 5 x 5 Gy vs. RCT (50,4 Gy + 5-FU) 5 x 5Gy (N=163) RCT (N=163) Locoreg. recurrences
Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom Prof. Dr. med. R. Fietkau Strahlenklinik Ngan et al. 2012 Rectal-Ca: 5 x 5 Gy vs. RCT (50,4 Gy + 5-FU) 5 x 5Gy (N=163) RCT (N=163) Locoreg. recurrences
Duktales Carcinoma in situ (DCIS)
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Duktales Carcinoma in situ (DCIS) Duktales Carcinoma In Situ (DCIS) Version 2002: Gerber Version 2003 2011: Audretsch / Brunnert / Costa
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Duktales Carcinoma in situ (DCIS) Duktales Carcinoma In Situ (DCIS) Version 2002: Gerber Version 2003 2011: Audretsch / Brunnert / Costa
Was ist die beste Nachsorge? 2. Berliner Tag des Eierstock- und Bauchfellkrebses am 11. September 2010
 Was ist die beste Nachsorge? 2. Berliner Tag des Eierstock- und Bauchfellkrebses am 11. September 2010 Jochem Potenberg Ev. Waldkrankenhaus Berlin Einführung 8500 Neuerkrankungen in Deutschland pro Jahr
Was ist die beste Nachsorge? 2. Berliner Tag des Eierstock- und Bauchfellkrebses am 11. September 2010 Jochem Potenberg Ev. Waldkrankenhaus Berlin Einführung 8500 Neuerkrankungen in Deutschland pro Jahr
Darum liegt in mehr als der Hälfte der Fälle bereits bei Diagnosestellung ein fortgeschritteneres Stadium der Erkrankung vor.
 OVARIALKARZINOM EPIDEMIOLOGIE Das Ovarialkarzinom (Eierstockkrebs) stellt die häufigste Todesursache durch ein Malignom bei der Frau dar. In Österreich erkranken jährlich rund 936 Frauen an einem Eierstockkrebs.
OVARIALKARZINOM EPIDEMIOLOGIE Das Ovarialkarzinom (Eierstockkrebs) stellt die häufigste Todesursache durch ein Malignom bei der Frau dar. In Österreich erkranken jährlich rund 936 Frauen an einem Eierstockkrebs.
Lokalisiertes Prostatakarzinom: high risk Prostatakarzinom, nodal positives Prostatakarzinom. aus radioonkologischer Sicht
 November 2013 St.Gallen Lokalisiertes Prostatakarzinom: high risk Prostatakarzinom, nodal positives Prostatakarzinom aus radioonkologischer Sicht Gregor Goldner Medizinische Universität Wien lokalisiertes
November 2013 St.Gallen Lokalisiertes Prostatakarzinom: high risk Prostatakarzinom, nodal positives Prostatakarzinom aus radioonkologischer Sicht Gregor Goldner Medizinische Universität Wien lokalisiertes
3. Schwerpunkt: Maligne gynäkologische Tumoren aus klinisch-epidemiologischer
 Gynäkologische Tumoren 58 3. Schwerpunkt: Maligne gynäkologische Tumoren aus klinisch-epidemiologischer Sicht 3.1. Epidemiologische Kenngrößen Zur klinisch-epidemiologischen Beschreibung der gynäkologischen
Gynäkologische Tumoren 58 3. Schwerpunkt: Maligne gynäkologische Tumoren aus klinisch-epidemiologischer Sicht 3.1. Epidemiologische Kenngrößen Zur klinisch-epidemiologischen Beschreibung der gynäkologischen
Absolute Neuerkrankungszahlen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2010-2014
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2010-2014
Aus dem Fachbereich Medizin der Johann Wolfgang Goethe-Universität Frankfurt am Main
 Aus dem Fachbereich Medizin der Johann Wolfgang Goethe-Universität Frankfurt am Main Klinik für Hals-, Nasen-, Ohrenheilkunde Direktor. Prof. Dr. med. Timo Stöver Prävalenz der high-risk HP-Viren 16 und
Aus dem Fachbereich Medizin der Johann Wolfgang Goethe-Universität Frankfurt am Main Klinik für Hals-, Nasen-, Ohrenheilkunde Direktor. Prof. Dr. med. Timo Stöver Prävalenz der high-risk HP-Viren 16 und
Strahlentherapie des alten Menschen. Hans Geinitz Abteilung für Radio-Onkologie, Linz
 Strahlentherapie des alten Menschen Hans Geinitz Abteilung für Radio-Onkologie, Linz RT des alten Patienten Indikationen Alleinige Strahlentherapie Radiochemotherapie Indikationen Im Prinzip wie bei Jüngeren!
Strahlentherapie des alten Menschen Hans Geinitz Abteilung für Radio-Onkologie, Linz RT des alten Patienten Indikationen Alleinige Strahlentherapie Radiochemotherapie Indikationen Im Prinzip wie bei Jüngeren!
Zur Qualität der Versorgung in Deutschland: Karzinome von Lunge, Prostata, Kolon- Rektum, Mamma
 Zur Qualität der Versorgung in Deutschland: Karzinome von Lunge, Prostata, Kolon- Rektum, Mamma Benchmarking Krebskongress 2008 - Teilnehmende Tumorzentren - Ausgewertete Karzinome: Karzinome von Lunge,
Zur Qualität der Versorgung in Deutschland: Karzinome von Lunge, Prostata, Kolon- Rektum, Mamma Benchmarking Krebskongress 2008 - Teilnehmende Tumorzentren - Ausgewertete Karzinome: Karzinome von Lunge,
Mammakarzinom II. Diagnostik und Therapie
 Mammakarzinom II Diagnostik und Therapie MR - Mammographie Empfehlung einer MRT: lokales Staging (Exzisionsgrenzen) beim lobulären Mammakarzinom Multizentrizität? okkultes Mammakarzinom? MR - Mammographie
Mammakarzinom II Diagnostik und Therapie MR - Mammographie Empfehlung einer MRT: lokales Staging (Exzisionsgrenzen) beim lobulären Mammakarzinom Multizentrizität? okkultes Mammakarzinom? MR - Mammographie
AGO-OP 8 / SHAPE (NCIC CTG CX.5) Kurzprotokoll
 AGO-OP 8 / SHAPE (NCIC CTG CX.5) Kurzprotokoll TITEL SPONSOR STUDIENLEITER FÜR DEUTSCHLAND RATIONALE Eine randomisierte Phase III Studie zum Vergleich der radikalen Hysterektomie und pelvinen Lymphonodektomie
AGO-OP 8 / SHAPE (NCIC CTG CX.5) Kurzprotokoll TITEL SPONSOR STUDIENLEITER FÜR DEUTSCHLAND RATIONALE Eine randomisierte Phase III Studie zum Vergleich der radikalen Hysterektomie und pelvinen Lymphonodektomie
Corpus uteri. 3.4 Corpus uteri
 77 Corpus uteri 3.4 Corpus uteri Das Korpuskarzinom ist nach Brust- und Darmkrebs gleich häufig wie Tumoren der Atmungsorgane und somit die dritthäufigste Krebserkrankung der Frau in Deutschland, die allerdings
77 Corpus uteri 3.4 Corpus uteri Das Korpuskarzinom ist nach Brust- und Darmkrebs gleich häufig wie Tumoren der Atmungsorgane und somit die dritthäufigste Krebserkrankung der Frau in Deutschland, die allerdings
Duktales Carcinoma in situ (DCIS)
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Duktales Carcinoma in situ (DCIS) Duktales Carcinoma in situ (DCIS) Version 2002: Gerber Versionen 2003 2012: Audretsch / Brunnert / Costa
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Duktales Carcinoma in situ (DCIS) Duktales Carcinoma in situ (DCIS) Version 2002: Gerber Versionen 2003 2012: Audretsch / Brunnert / Costa
Dr. med. D. Helbling
 Behandlung: Mastdarmkreb / Rektumkarzinom Dr. med. D. Helbling Medizinischer Onkologe FMH Spezielles Interessegebiet: Tumore des Magendarmtrakts www.magendarmkrebs.ch 1 Mastdarmkrebs: grundsätzliches zur
Behandlung: Mastdarmkreb / Rektumkarzinom Dr. med. D. Helbling Medizinischer Onkologe FMH Spezielles Interessegebiet: Tumore des Magendarmtrakts www.magendarmkrebs.ch 1 Mastdarmkrebs: grundsätzliches zur
Versorgungssituation beim kolorektalen Karzinom in Deutschland (Beitrag ADT GEKID) Prof. Dr. med. Stefan Benz
 Versorgungssituation beim kolorektalen Karzinom in Deutschland (Beitrag ADT GEKID) Prof. Dr. med. Stefan Benz Klinikum Böblingen-Sindelfingen Klinik f. Allgemein, Viszeral- und Kinderchirurgie 5. Bundesweite
Versorgungssituation beim kolorektalen Karzinom in Deutschland (Beitrag ADT GEKID) Prof. Dr. med. Stefan Benz Klinikum Böblingen-Sindelfingen Klinik f. Allgemein, Viszeral- und Kinderchirurgie 5. Bundesweite
Ergebnisse. Klinische Charakteristik
 25 Ergebnisse 19 der 105 Patientinnen waren bis zum Zeitpunkt der Nachuntersuchung bereits verstorben, in 13 Fällen als Folge des Tumorleidens. Die durchschnittliche Überlebenszeit betrug 6,72 Jahren (95%
25 Ergebnisse 19 der 105 Patientinnen waren bis zum Zeitpunkt der Nachuntersuchung bereits verstorben, in 13 Fällen als Folge des Tumorleidens. Die durchschnittliche Überlebenszeit betrug 6,72 Jahren (95%
Auslegungshinweise Kennzahlenbogen Darm (Stand ) - basierend auf dem Erhebungsbogen vom
 Allgemeine Anmerkungen In dem Dokument Auslegungshinweise Kennzahlenbogen Darm werden weitergehende ErlÄuterungen zu den einzelnen Kennzahlen gemacht. Dieses Dokument befindet sich im Moment in Diskussion
Allgemeine Anmerkungen In dem Dokument Auslegungshinweise Kennzahlenbogen Darm werden weitergehende ErlÄuterungen zu den einzelnen Kennzahlen gemacht. Dieses Dokument befindet sich im Moment in Diskussion
Was steht in meinem Befund?
 Basiskurs Krebswissen 09.11.2016 Was steht in meinem Befund? (Staging, Grading, TNM, ) Rainer Hamacher, MUW-AKH, Univ. Klinik für Innere Medizin I / Onkologie TNM STAGING & GRADING Tumorstaging (=Staging)
Basiskurs Krebswissen 09.11.2016 Was steht in meinem Befund? (Staging, Grading, TNM, ) Rainer Hamacher, MUW-AKH, Univ. Klinik für Innere Medizin I / Onkologie TNM STAGING & GRADING Tumorstaging (=Staging)
Berno Tanner. State of the Art Ovar 19.06.2009
 Pathologie und Konsequenzen für die Klinik Histologische Tumortypen Friedrich Kommoss Berno Tanner State of the Art Ovar 19.06.2009 Histologische Tumortypen benigne borderline maligne Histologische Tumortypen
Pathologie und Konsequenzen für die Klinik Histologische Tumortypen Friedrich Kommoss Berno Tanner State of the Art Ovar 19.06.2009 Histologische Tumortypen benigne borderline maligne Histologische Tumortypen
3.1. Überlebenszeiten Zum Ende der Nachuntersuchung waren 19 Patienten (17,8%) am Leben und 88 (82,2%) verstorben (Tab. 3.1.).
 18 3. Ergebnisse 3.1. Überlebenszeiten Zum Ende der Nachuntersuchung waren 19 Patienten (17%) am Leben und 88 (82%) verstorben (Tab. 3.1.). Tabelle 3.1. Häufigkeit der lebenden und verstorbenen Patienten
18 3. Ergebnisse 3.1. Überlebenszeiten Zum Ende der Nachuntersuchung waren 19 Patienten (17%) am Leben und 88 (82%) verstorben (Tab. 3.1.). Tabelle 3.1. Häufigkeit der lebenden und verstorbenen Patienten
Die Therapie des Ovarialkarzinoms in Deutschland. Die Therapie des Ovarialkarzinoms in Deutschland
 Die Therapie des Ovarialkarzinoms in Deutschland eine Qualitätssicherungserhebung tssicherungserhebung Q III 2004 A. du Bois, J. Rochon 2, C. Lamparter 3, J. Pfisterer 4 für r die AGO Organkommission OVAR
Die Therapie des Ovarialkarzinoms in Deutschland eine Qualitätssicherungserhebung tssicherungserhebung Q III 2004 A. du Bois, J. Rochon 2, C. Lamparter 3, J. Pfisterer 4 für r die AGO Organkommission OVAR
Up-Date zur adjuvanten endokrinen Therapie des Mammakarzinoms
 Up-Date zur adjuvanten endokrinen Therapie des Mammakarzinoms München 10. Januar 2008 Franz Edler von Koch Klinik und Poliklinik für Frauenheilkunde und Geburtshilfe Großhadern Ludwig-Maximilians-Universität
Up-Date zur adjuvanten endokrinen Therapie des Mammakarzinoms München 10. Januar 2008 Franz Edler von Koch Klinik und Poliklinik für Frauenheilkunde und Geburtshilfe Großhadern Ludwig-Maximilians-Universität
3 Ergebnisse. 3.1 Lokoregionäre Rezidive und Fernmetastasierung
 Multivariate Analysen wurden mit dem Cox-Regressions-Modell berechnet. Dabei wurden die signifikanten Variablen der univariaten Analyse in das Modell eingeschlossen. Die Reduktion der Variablen erfolgte
Multivariate Analysen wurden mit dem Cox-Regressions-Modell berechnet. Dabei wurden die signifikanten Variablen der univariaten Analyse in das Modell eingeschlossen. Die Reduktion der Variablen erfolgte
Bevölkerungsbezogene Analysen neuer Therapieoptionen an einem regionalen Beispiel
 Bevölkerungsbezogene Analysen neuer Therapieoptionen an einem regionalen Beispiel Priv.- Doz. Dr. med. Monika Klinkhammer-Schalke Arbeitsgemeinschaft Deutscher Tumorzentren e.v., Berlin Kooperationsverbund
Bevölkerungsbezogene Analysen neuer Therapieoptionen an einem regionalen Beispiel Priv.- Doz. Dr. med. Monika Klinkhammer-Schalke Arbeitsgemeinschaft Deutscher Tumorzentren e.v., Berlin Kooperationsverbund
Seite Diskussion
 Seite 99 4 Diskussion In der Behandlung lokal fortgeschrittener oder inflammatorischer Mammakarzinome gilt die neoadjuvante Chemotherapie schon lange als Standard. Dass diese Therapieform in Hinblick auf
Seite 99 4 Diskussion In der Behandlung lokal fortgeschrittener oder inflammatorischer Mammakarzinome gilt die neoadjuvante Chemotherapie schon lange als Standard. Dass diese Therapieform in Hinblick auf
Absolute Neuerkrankungszahlen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2010-2014
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2010-2014
Ösophagus. 3.2 Ösophaguskarzinom
 55 3.2 karzinom Das karzinom ist mit einer Inzidenzrate von ca. 8 je 100.000 bzw. 2% aller Krebsneuerkrankungen bei Männern und 2,1 bzw. 0,4% bei Frauen eine seltene Erkrankungsform. 82% der Erkrankten
55 3.2 karzinom Das karzinom ist mit einer Inzidenzrate von ca. 8 je 100.000 bzw. 2% aller Krebsneuerkrankungen bei Männern und 2,1 bzw. 0,4% bei Frauen eine seltene Erkrankungsform. 82% der Erkrankten
Aus der Klinik für Urologie des Vivantes Klinikums im Friedrichshain Berlin DISSERTATION
 Aus der Klinik für Urologie des Vivantes Klinikums im Friedrichshain Berlin DISSERTATION Thema: Entscheidungskriterien vor radikaler Prostatektomie Eine retrospektive Untersuchung der Daten von 427 Patienten
Aus der Klinik für Urologie des Vivantes Klinikums im Friedrichshain Berlin DISSERTATION Thema: Entscheidungskriterien vor radikaler Prostatektomie Eine retrospektive Untersuchung der Daten von 427 Patienten
Aus der Klinik für Allgemein-, Viszeral- und Gefäßchirurgie der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. H.
 Aus der Klinik für Allgemein-, Viszeral- und Gefäßchirurgie der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. H. Dralle Gastric-banding als Operationsmethode bei morbider Adipositas
Aus der Klinik für Allgemein-, Viszeral- und Gefäßchirurgie der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. H. Dralle Gastric-banding als Operationsmethode bei morbider Adipositas
Intraoperative Strahlentherapie bei Brustkrebs
 Intraoperative Strahlentherapie bei Brustkrebs Uniklinik Köln 1 Kein Grund für Verzweiflung Wenn die Diagnose Brustkrebs festgestellt wird, ist erst einmal die Sorge groß. Beruhigend zu wissen, dass es
Intraoperative Strahlentherapie bei Brustkrebs Uniklinik Köln 1 Kein Grund für Verzweiflung Wenn die Diagnose Brustkrebs festgestellt wird, ist erst einmal die Sorge groß. Beruhigend zu wissen, dass es
Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen Abteilung Nuklearmedizin
 Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen 1990-2008 Abteilung Nuklearmedizin Hintergrund Therapie differenzierter SD-CAs: multimodal und interdisziplinär (Chirurgie und
Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen 1990-2008 Abteilung Nuklearmedizin Hintergrund Therapie differenzierter SD-CAs: multimodal und interdisziplinär (Chirurgie und
Multimodale Therapie des Pankreaskarzinoms
 Department Chirurgische of Klinik Surgery und Poliklinik, Munich, Germany Multimodale Therapie des Pankreaskarzinoms Helmut Friess Juli 2010 Neue Fälle Todesfälle 5 Jahres-Überleben (in %) Department of
Department Chirurgische of Klinik Surgery und Poliklinik, Munich, Germany Multimodale Therapie des Pankreaskarzinoms Helmut Friess Juli 2010 Neue Fälle Todesfälle 5 Jahres-Überleben (in %) Department of
Watchful waiting- Strategie
 Watchful waiting- Strategie Individualisierte Behandlung beim lokalisierten Prostatakarzinom- Welche Kriterien erlauben den Entscheid für eine watch und wait Strategie? Dr. Rudolf Morant, ärztlicher Leiter
Watchful waiting- Strategie Individualisierte Behandlung beim lokalisierten Prostatakarzinom- Welche Kriterien erlauben den Entscheid für eine watch und wait Strategie? Dr. Rudolf Morant, ärztlicher Leiter
Chirurgische Therapie primärer und sekundärer Lungentumore
 Chirurgische Therapie primärer und sekundärer Lungentumore Hans-Stefan Hofmann Thoraxchirurgie Regensburg Universitätsklinikum Regensburg KH Barmherzige Brüder Regensburg - und Metastasenverteilung 2009
Chirurgische Therapie primärer und sekundärer Lungentumore Hans-Stefan Hofmann Thoraxchirurgie Regensburg Universitätsklinikum Regensburg KH Barmherzige Brüder Regensburg - und Metastasenverteilung 2009
Führt Versorgungsforschung zu Versorgungsverbesserung?
 Führt Versorgungsforschung zu Versorgungsverbesserung? M. Klinkhammer-Schalke Arbeitsgemeinschaft Deutscher Tumorzentren e.v. (ADT) Deutsches Netzwerk für Versorgungsforschung (DNVF) Was kann Versorgungsforschung
Führt Versorgungsforschung zu Versorgungsverbesserung? M. Klinkhammer-Schalke Arbeitsgemeinschaft Deutscher Tumorzentren e.v. (ADT) Deutsches Netzwerk für Versorgungsforschung (DNVF) Was kann Versorgungsforschung
Kleinzelliges Lungenkarzinom (SCLC)
 Kleinzelliges Lungenkarzinom (SCLC) Verantwortlich: Prof. Dr. Nestle, Dr. Rawluk, Prof. Waller, Dr. Wiesemann Freigabe: interdisziplinärer Qualitätszirkel Stand: 04/2016, gültig bis 10/2017 Version 3.2
Kleinzelliges Lungenkarzinom (SCLC) Verantwortlich: Prof. Dr. Nestle, Dr. Rawluk, Prof. Waller, Dr. Wiesemann Freigabe: interdisziplinärer Qualitätszirkel Stand: 04/2016, gültig bis 10/2017 Version 3.2
Absolute Neuerkrankungen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2009-2013
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2009-2013
