3. Material und Methoden
|
|
|
- Frida Schmitz
- vor 9 Jahren
- Abrufe
Transkript
1 3. Material und Methoden Die Untersuchungen gliederten sich in zwei Teile: einen retrospektiven Teil von 9/98 bis 12/99 und einen prospektiven Teil von 1/2000 bis 8/ Blutgruppenbestimmung Vor der Durchführung der Bluttransfusion wurde sowohl vom Spender als auch vom Empfänger die Blutgruppe mit Hilfe der Objektträgermethode bestimmt. Das hierfür benötigte Anti-A-Serum wurde von Katzen mit der Blutgruppe B gewonnen, 30 Minuten bei 56 C erhitzt und gefiltert. Als Anti-B-Reagenz diente eine Weizenkeim-Lektin- Lösung (Triticum vulgaris, SIGMA L-9640, 64 µg/ml, verdünnt mit 0,01 M phosphatgepufferter Kochsalzlösung, PBS (Dulbecco, Biochrom, Berlin)) (GIGER et al. 1991c). Beide Reagentien wurden portioniert und bei -20 C gelagert. Wurden die Reagentien aufgetaut, so wurden diese bei 4 C über max. 6 Wochen gelagert. Zur Blutgruppenbestimmung wurden 30 µl Anti-A-Serum bzw. 30 µl Anti-B-Lösung mit 15 µl EDTA-Vollblut auf jeweils einem Objektträger vermischt. Nach Schwenken des Objektträgers wurde das Blut auf Agglutination hin überprüft. Eine Katze wies die Blutgruppe A auf, wenn ihre Erythrozyten eine Agglutination mit dem Anti-A-Serum (Abb.1), und die Blutgruppe B eine Agglutination mit dem Anti-B-Reagenz aufwies. Katzen mit der Blutgruppe AB agglutinierten mit beiden Reagentien (GRIOT- WENK und GIGER, 1995), wobei darauf geachtet wurde, dass sie nicht autoagglutinierten, d.h. die Autokontrolle war jeweils negativ. Abb.1: Agglutination mit Anti-A-Serum bei einer Katze mit der Blutgruppe A 45
2 Wenn eine spontane Erythrozytenagglutination beim Patienten vorlag, wurde zunächst ein Waschen der Erythrozyten durchgeführt. Hierzu wurde das Blut 1 Minute bei 1000g zentrifugiert (Minifuge RF, Heraeus Sepatech) und das Plasma abpipettiert. Anschliessend wurde PBS-Lösung hinzugegeben, vermischt, erneut zentrifugiert (1 Minute bei 1000g) und der Überstand abdekantiert. Dieser Vorgang wurde dreimal wiederholt. Eine Bestimmung der Blutgruppe mit Hilfe der Objektträgermethode war nur möglich, wenn nach Erythrozytenwaschung die Agglutination nicht persistierte. Handelte es sich um die Blutgruppe B, wurde zusätzlich das sog. Back typing durchgeführt (GIGER et al., 1991a). Hierbei wurde EDTA-Blut des Probanden 2 Minuten bei 1000g zentrifugiert und 30 µl des gewonnenen Plasmas mit 15 µl EDTA-Vollblut einer Typ A- Katze auf einem Objektträger vermischt. Eine Agglutination bestätigte die Blutgruppe B. In unklaren Fällen und zur Bestätigung der Blutgruppe AB wurde eine Hämagglutinations- Röhrchenmethode durchgeführt (GIGER et al., 1991a). Das Blut wurde zentrifugiert und das Plasma abpipettiert. Das Zentrifugat wurde anschliessend nach der oben beschriebenen Methode gewaschen und mit PBS-Lösung eine 3-5%ige Erythrozytensuspension hergestellt. Anschliessend wurden drei Röhrchen vorbereitet und mit Anti-A-Serum, Anti-B-Lösung und Back typing beschriftet. 25 µl der Erythrozytensuspension wurden mit jeweils 50 µl Anti- A-Serum (Verdünnung Anti-A-Serum, mit PBS 1:4) bzw. Anti-B-Reagenz (Verdünnung Weizenkeim-Lektin-Lösung 64 µg/ml mit PBS 1:8) vermischt. Im 3. Röhrchen wurden 25 µl einer Typ A-Erythrozytensuspension mit 50 µl Plasma des Probanden vermischt. Es folgte eine 15-minütige Inkubation bei Raumtemperatur. Nach Zentrifugation (Labofuge A, Heraeus Sepatech) (15 Sekunden lang bei 1000g) erfolgte die Beurteilung. Zunächst wurde der Überstand auf Hämolyse hin überprüft, nach Resuspension der zellulären Phase durch Tippen gegen das Röhrchen erfolgte die Beurteilung der Agglutination. 3.2 Kreuzprobe Im prospektiven Teil der Studie wurden vor und ca. 1 bzw. 4 Wochen nach der Transfusion Kreuzproben zur Überprüfung der serologischen Kompatibilität durchgeführt. Hierbei wurde zunächst EDTA-Blut des Spenders und des Empfängers zentrifugiert, das Plasma abpipettiert und vom Zentrifugat eine 3-5%ige Erythrozytensuspension nach der oben beschriebenen Methode hergestellt. Anschliessend wurden drei Röhrchen vorbereitet und mit Majorprobe, Minorprobe bzw. Empfängerkontrolle beschriftet. 46
3 Nach folgendem Schema wurden jeweils 50 µl Plasma mit 25 µl Erythrozytensuspension pipettiert (GIGER, 1992b): - Majorprobe: Empfängerplasma + Spendererythrozyten - Minorprobe: Spenderplasma + Empfängererythrozyten - Empfängerkontrolle: Empfängerplasma + Empfängererythrozyten Nach einer 15-minütigen Inkubation bei 37 C und anschliessender Zentrifugation (15 Sekunden bei 1000g) wurde zunächst der Überstand auf Hämolyse untersucht. Bei bereits vor Durchführung der Kreuzprobe vorhandener Hämolyse des Plasmas erfolgte die Beurteilung im Vergleich mit dem Ansatz der Empfängerkontrolle. Durch Tippen gegen das Röhrchen wurde die zelluläre Phase resuspendiert und auf Agglutination überprüft. Fehlte eine makroskopische Agglutination, wurde der Ansatz auch mikroskopisch beurteilt. Der Grad der Agglutination wurde von + bis +++ (1+ bis 3+) angegeben. Die Kreuzprobe wurde als inkompatibel beurteilt, wenn im Major- bzw. Minoransatz eine Agglutination oder Hämolyse auftrat. Die Empfängerkontrolle wurde durchgeführt, um zu überprüfen, ob eine Autoagglutination oder Grundhämolyse vorlag. In diesen Fällen war eine Beurteilung der Kompatibilität nur dann möglich, wenn die Agglutination in der Major- bzw. Minorprobe stärker ausgeprägt war als in der Empfängerkontrolle. Der Ansatz der ersten Kreuzprobe erfolgte in der Regel nach der Transfusion. Die Kreuzprobe diente in diesem Fall nicht allein der Überprüfung der Kompatibilität (dies erfolgte durch die Blutgruppenbestimmung), sondern zusammen mit der 2. und 3. Kreuzprobe als Verlaufskontrolle. So erklärt sich, dass Transfusionen durchgeführt wurden, obwohl eine positive Kreuzprobe vorlag. Die Durchführung einer zweiten und dritten Kreuzprobe war nur möglich, wenn das Empfängertier zu einer erneuten Blutabnahme nach ca. 1 bzw. 4 Wochen zur Verfügung stand. Handelte es sich bei dem Spendertier um ein Tier aus der Privathaltung, wurde das Blut des Spendertieres bis zum Zeitpunkt der zweiten Kreuzprobe bei 4-6 C gelagert. Nur in einigen Fällen war es möglich, eine erneute Blutprobe abzunehmen. Von den klinikeigenen Spenderkatzen wurde jeweils eine frische Blutprobe zur Durchführung der zweiten bzw. dritten Kreuzprobe verwendet. 47
4 3.3 Blutspender Zur Blutentnahme standen sowohl klinikeigene Katzen als auch Katzen aus der Privathaltung zur Verfügung. Der Bedarf an Vollblut war durch die klinikeigenen Spenderkatzen nicht zu decken, so dass die Patientenbesitzer versuchten, Spendertiere zu organisieren. Hierbei handelte es sich um weitere Katzen im eigenen Haushalt oder um ein Tier aus der Nachbarschaft oder dem Bekanntenkreis. Einige Besitzer und Studenten waren auch bereit, ihre Katze regelmässig zur Blutspende vorzustellen (Blutspendekartei). Jedes Spendertier wurde zunächst allgemein klinisch untersucht und es wurde eine hämatologische und klinisch-chemische Blutuntersuchung durchgeführt. Bei den klinikeigenen Spenderkatzen wurde das Blut zur Bestimmung des Hämatokrits in Sedation zusammen mit der Blutspende abgenommen. Zweimal pro Jahr wurde bei den klinikeigenen Spenderkatzen eine komplette Blutuntersuchung (Hämatologie, klinische Chemie) durchgeführt. Katzen waren zur Blutspende geeignet, wenn sie gesund, möglichst gross, entwurmt und geimpft waren. Der Hämatokrit sollte mind. 35% betragen, und es sollte sich möglichst um Katzen aus der Wohnungshaltung handeln. Für Katzen, die regelmässig Blut spendeten, wurde ein Protokoll geführt. Es wurde das Datum, das Gewicht, Laborergebnisse, die Art der Sedation, die Lokalisation der Blutentnahme (rechte/linke V. jugularis), das Spendevolumen, das Auftreten von Nebenwirkungen, Schwierigkeiten bei der Blutentnahme sowie der Name des Empfängers eingetragen. 3.4 Blutentnahme Die Spendertiere wurden durch intramuskulärer Verabreichung von Ketamin (Ketamin 10%, Essex Tierarznei, München) (5-6 mg/kg) und Azepromazin (Vetranquil, Sanofi-Cefa GmbH, Düsseldorf) (0,1 mg/kg) bzw. Midazolam (Midazolam Ratiopharm GmbH) (0,1 mg/kg) sediert. Die Blutentnahme erfolgte mit offenem System unter sterilen Kautelen aus der Abb.2: Durchführung der Blutentnahme 48
5 Vena jugularis mit Hilfe eines Butterfly-Katheters (Vasoflo Perfusionsbesteck, 19G, Dispomed Witt, Gelnhausen). Der Jugularvenenbereich wurde geschoren und mit Alkohol desinfiziert. Zur Blutentnahme wurden drei Hilfspersonen benötigt (Abb.2). Eine Person fixierte die Spenderkatze in Sternallage. Nach Punktion der V. juguaris und Halten des Butterflys durch eine Person wurde das Blut von einer weiteren Person in antikoagulanshaltige Spritzen bei gleichzeitigem Schwenken aspiriert. Das Spendevolumen richtete sich nach dem Körpergewicht, wobei ca. 10% des Blutvolumens entnommen wurden. Bei Katzen mit einem Hkt von 30 - <35% oder Katzen, die älter als 8 Jahre waren, wurde eine geringere Menge Blut abgenommen. Das Blut wurde anschliessend in einen Transferbeutel (Baxter Healthcare Corporation, Unterschleißheim) überführt. War das Blut zur Konservierung bestimmt, so wurde der Blutbeutel sofort durch einen Clip verschlossen. Nach der Blutentnahme wurde das Spendertier mindestens eine Stunde überwacht. Hierbei wurde die Farbe der Schleimhäute, der Puls und die Atmung regelmässig kontrolliert. Alle Spender wurden subkutan oder selten intravenös mit Ringerlaktat (Sterofundin ) in einer Menge von ca. 20 ml/kg infundiert. Wurde das Blut sofort oder innerhalb von 8 Stunden zur Transfusion benötigt, fand Natriumzitrat (3,13% Braun, Melsungen) als Antikoagulans Verwendung (1 Teil Na-Zitrat auf 9 Teile Blut). Zur Blutkonservierung diente als Erythrozytenstabilisator und Antikoagulans CPDA-1 (1,2 ml CPDA-1 auf 8,8 ml Blut), das aus einem Einfachbeutelsystem (Baxter Fenwal, Unterschleissheim) entnommen wurde. Der Blutbeutel wurde mit dem Spendernamen, Blutgruppe, Datum der Blutspende und der Menge des entnommenen Blutes beschriftet. Natriumzitrathaltiges Blut wurde sofort transfundiert und nur in Einzelfällen bei 4-6 C bis zu 8 Stunden gelagert. CPDA-1-haltige Blutkonserven wurden bei 4-6 C bis maximal 15 Tage aufbewahrt. Die Beutel wurden mehrmals pro Woche vorsichtig geschwenkt. Es erfolgte keine Auftrennung in einzelne Blutkomponenten. Von einigen gelagerten Bluteinheiten wurde sowohl nach Zugabe der CPDA-1-Lösung als auch nach der Lagerung zum Zeitpunkt der Transfusion eine geringe Blutmenge zur Bestimmung des Hämatokrits und des Hämolysegrads im Plasma entnommen. Zusätzlich wurde nach 4-10 Tagen Lagerung von einigen Bluteinheiten eine mikrobiologische Untersuchung durchgeführt. 49
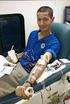
6 3.5 Durchführung der Bluttransfusion Abb.3: Bluttransfusion Die Bluttransfusion wurde über einen venösen Zugang (Vasocan, Braun Melsungen) in die V. saphena oder V. cephalica antebrachii bzw. über einen Jugularkatheter (Cavafix, Braun Melsungen) verabreicht (Abb.3). Für die Transfusion wurde ein spezielles Transfusionsbesteck mit Mikrofilter mit einer Porengrösse von 200µm (Sangofix Air, Braun Melsungen) verwendet. Initial wurde das Blut mit einer geringen Transfusionsgeschwindigkeit (2-3 ml in den ersten 5 Minuten) verabreicht und der Empfänger bezüglich des Auftretens von Transfusionsreaktionen beobachtet. Traten keine Reaktionen auf, erhielten normovolämische Katzen ca. 10 ml/kg/stunde und Katzen mit hypovolämischem Schock bis zu 60 ml/kg/stunde. Patienten mit kardiovaskulärer Dysfunktion wurden langsamer transfundiert (ca. 4ml/kg/Stunde) (GIGER, 1992). Es wurde darauf geachtet, dass das Blut innerhalb von 4 Stunden verabreicht wurde. Das Transfusionsvolumen wurde nach folgender Formel berechnet (GRIOT-WENK und GIGER, 1995): Transfusionsvolumen (ml) = erwünschter Hkt-Anstieg (%) x Körpergewicht des Empfängers x 2 In der Regel war das Transfusionsvolumen jedoch durch die Verfügbarkeit und das Beutelvolumen limitiert. Reichte das Spendevolumen einer Katze nicht aus, um eine hochgradig anämische Katze zu stabilisieren, wurde dem Empfänger am gleichen Tag Blut von zwei oder drei Spendertieren zugeführt. Zwischen den einzelnen Transfusionen erfolgte keine Hkt-Kontrolle, und das gesamte Transfusionsvolumen wurde für die Auswertung addiert und als eine Transfusion zusammengefasst. Während der Transfusion und danach wurde der Empfänger überwacht. Hierbei wurde der Verlauf der Körpertemperatur, die Atem- und Pulsfrequenz und die kapilläre Rückfüllungszeit in etwa 10-minütigen Abständen beurteilt. Gegen Ende der Bluttransfusion wurde das Restblut aus dem Beutel und dem Schlauchsystem mit physiologischer Kochsalzlösung (0,9%) gespült Stunden nach Verabreichung der Bluttransfusion wurde der Patient erneut klinisch untersucht und es erfolgte eine Hkt- und Bilirubinkontrolle. Eine Katze mit einem rupturierten Hämangioendotheliosarkom erhielt eine Infusion mit bovinem 50
7 Hämoglobin (Oxyglobin, Biopure, Corporation) in einer Gesamtdosierung von 25 ml/kg über ca. 2 Stunden. 3.6 Direkter Coombs-Test (DAT, Direkter Antiglobulintest) Die Durchführung des direkten Coombs-Tests zum Nachweis antierythrozytärer Antikörper bzw. Komplement auf der Erythrozytenoberfläche erfolgte an der Tierärztlichen Hochschule Hannover (Arbeitsgruppe Immunologie). Die Erythrozyten wurden dreimal mit PBS gewaschen und 25 µl Erythrozytenkonzentrat mit 975 µl R2F-Lösung (Firma Biochrom, Berlin) gemischt. Zum Nachweis der Antiglobulinklasse wurden monospezifische Antiseren (Goat-Anti-Cat IgM [Bethyl, Montgomery, Texas, USA, Vertrieb über Natutec, Frankfurt/Main], Goat-Anti- Cat IgG H+L [Dianova, Hamburg], Sheep-Anti-Cat C 3 [The Binding Site GmbH, Heidelberg]) verwendet. Auf Mikrotiterplatten wurde von den Antiseren und C 3 mit PBS eine Verdünnungsreihe von 1:20, 1:40, 1:80 und 1:160 hergestellt und jeder Verdünnungsstufe das Gemisch aus Erythrozyten und R2F-Lösung zugegeben. Jeweils ein Ansatz wurde bei 4 C und bei 37 C 90 Minuten inkubiert. Als Negativkontrollen wurden PBS und fetales Kälberserum verwendet. Der Test wurde als positiv beurteilt, wenn eine Erythrozytenagglutination eintrat. 3.7 Auswertung der Bluttransfusionen Die Studie umfasste einen retrospektiven (15 Monate) und eine prospektiven (21 Monate) Teil. Es wurden folgende Parameter in die Auswertung der Bluttransfusionen einbezogen: Signalement des Empfängers Signalement des Spenders Blutgruppen Spendevolumen Indikationen Transfusionsvolumen Transfusionsreaktionen Hkt vor und nach der Bluttransfusion Bestimmung des zu erwartenden Hkt-Anstiegs mit folgender Formel: Hkt-Anstieg (%) = Transfusionsvolumen : (2x kg KG des Empfängers) 51
8 Vergleich des Hkt-Anstiegs mit errechnetem Wert Anzahl der Transfusionen pro Katze Bestimmung der Überlebensrate bis 10 Tage nach der letzten Transfusion Im prospektiven Teil der Studie wurden in einem Teil der Fälle zusätzliche Parameter ausgewertet: Bilirubinmessung vor und nach der Bluttransfusioen Kreuzprobe vor der Bluttransfusion, ca. 1 und 4 Wochen danach Coombs-Test vor und nach der Bluttransfusion 3.8 Statistik Die Auswertung erfolgte mit Angabe von Prozentpunkten (Median) sowie Minimal- und Maximalwerten. In einem Teil der Fälle wurde zusätzlich Mittelwert und Standardabweichung angegeben. Als statistische Software wurde SPSS 10 (SPSS GmbH Software, München) verwendet. 52
Blutgruppenserologie und Immunhämatologie
 Blutgruppenserologie und Immunhämatologie Blutgruppenbestimmung (ABO, RhD, Rh-Untergruppe, Kell, Antikörpersuchtest) Indikation: Serologische Bestimmung der Blutgruppenmerkmale und Durchführung des Antikörpersuchtests,
Blutgruppenserologie und Immunhämatologie Blutgruppenbestimmung (ABO, RhD, Rh-Untergruppe, Kell, Antikörpersuchtest) Indikation: Serologische Bestimmung der Blutgruppenmerkmale und Durchführung des Antikörpersuchtests,
Bluttransfusion bei Katzen:
 Aus der Klinik und Poliklinik für kleine Haustiere des Fachbereichs Veterinärmedizin der Freien Universität Berlin Bluttransfusion bei Katzen: Indikationen, Durchführung, Transfusionsreaktionen und -ergebnisse
Aus der Klinik und Poliklinik für kleine Haustiere des Fachbereichs Veterinärmedizin der Freien Universität Berlin Bluttransfusion bei Katzen: Indikationen, Durchführung, Transfusionsreaktionen und -ergebnisse
Leistungsverzeichnis Erythrozytenimmunologie
 Leistungsverzeichnis Erythrozytenimmunologie DRK-Blutspendedienst West ggmbh DRK-Blutspendedienst Ostwestfalen-Lippe ggmbh DRK-Blutspendedienst Rheinland-Pfalz und Saarland ggmbh Zentrum für Transfusionsmedizin
Leistungsverzeichnis Erythrozytenimmunologie DRK-Blutspendedienst West ggmbh DRK-Blutspendedienst Ostwestfalen-Lippe ggmbh DRK-Blutspendedienst Rheinland-Pfalz und Saarland ggmbh Zentrum für Transfusionsmedizin
4. Ergebnisse. Die 3-jährige Studie umfasste einen retrospektiven und einen prospektiven Teil, der 15 bzw. 21 Monate von 1998 bis 2001 dauerte.
 4. Ergebnisse Die 3-jährige Studie umfasste einen retrospektiven und einen prospektiven Teil, der 15 bzw. 21 Monate von 1998 bis 2001 dauerte. 4.1 Blutspender Bei den 134 felinen Blutspendern handelte
4. Ergebnisse Die 3-jährige Studie umfasste einen retrospektiven und einen prospektiven Teil, der 15 bzw. 21 Monate von 1998 bis 2001 dauerte. 4.1 Blutspender Bei den 134 felinen Blutspendern handelte
Das ABO System. Praktikum für Medizinstudenten im IV Jahrgang. Zsuzsa Faust MD, PhD Zita Csernus MD
 Das ABO System Praktikum für Medizinstudenten im IV Jahrgang Zsuzsa Faust MD, PhD Zita Csernus MD Regionale Bluttransfusionszentrale von Pécs Nationaler Bluttransfusionsdienst [email protected] Blutgruppensysteme
Das ABO System Praktikum für Medizinstudenten im IV Jahrgang Zsuzsa Faust MD, PhD Zita Csernus MD Regionale Bluttransfusionszentrale von Pécs Nationaler Bluttransfusionsdienst [email protected] Blutgruppensysteme
DRK-Blutspendedienst Baden-Württemberg Hessen gemeinnützige GmbH Institut Baden-Baden. Institut für Transfusionsmedizin Baden-Baden gemeinnützige GmbH
 DRK-Blutspendedienst Baden-Württemberg Hessen gemeinnützige GmbH Institut Baden-Baden Institut für Transfusionsmedizin Baden-Baden gemeinnützige GmbH Laborpraxis im DRK-Blutspendedienst Baden-Baden Laborleistungen
DRK-Blutspendedienst Baden-Württemberg Hessen gemeinnützige GmbH Institut Baden-Baden Institut für Transfusionsmedizin Baden-Baden gemeinnützige GmbH Laborpraxis im DRK-Blutspendedienst Baden-Baden Laborleistungen
5. Diskussion. 5.1 Blutspender
 5. Diskussion Bluttransfusionen haben in der Veterinärmedizin im Verlauf der letzten Jahre auch bei der Katze an Bedeutung zugenommen. Während es beim Hund verschiedene Untersuchungen über Bluttransfusionen
5. Diskussion Bluttransfusionen haben in der Veterinärmedizin im Verlauf der letzten Jahre auch bei der Katze an Bedeutung zugenommen. Während es beim Hund verschiedene Untersuchungen über Bluttransfusionen
SOPS Tranfusionskette SOP-6 Version Nr.: 1 vom Dok. Nr.: 6-SEROLOG DOC Seite 1 von 5
 Version Nr.: 1 vom 07.02.1997 Dok. Nr.: 6-SEROLOG-12.11.2006.DOC Seite 1 von 5 1 Titel Auswahl von Blutprodukten unter Berücksichtigung blutgruppenserologischer Befunde 2 Ziel und Zweck Standardisierung
Version Nr.: 1 vom 07.02.1997 Dok. Nr.: 6-SEROLOG-12.11.2006.DOC Seite 1 von 5 1 Titel Auswahl von Blutprodukten unter Berücksichtigung blutgruppenserologischer Befunde 2 Ziel und Zweck Standardisierung
Blutgruppenserologische Untersuchungen und. Transfusion
 Teil I Ernst-Moritz-Arndt-Universität, Praktikum Transfusionsmedizin Blutgruppenserologische Untersuchungen und Transfusion Blutgruppenbestimmung, Antikörperscreening serologische Verträglichkeitsprobe
Teil I Ernst-Moritz-Arndt-Universität, Praktikum Transfusionsmedizin Blutgruppenserologische Untersuchungen und Transfusion Blutgruppenbestimmung, Antikörperscreening serologische Verträglichkeitsprobe
25,0-27,6 g/l 2,94 3,60 g/l 2,38 2,64 g/l 30,3 33,5 g/l 0, 261 0,289 g/l
 Material und Methode III EIGENE UNTERSUCHUNGEN 1 Material und Methode 1.1 Spenderauswahl Während eines 2-jährigen Untersuchungszeitraumes wurden Bluttransfusionen von freiwilligen Blutspendern gewonnen.
Material und Methode III EIGENE UNTERSUCHUNGEN 1 Material und Methode 1.1 Spenderauswahl Während eines 2-jährigen Untersuchungszeitraumes wurden Bluttransfusionen von freiwilligen Blutspendern gewonnen.
2. Literaturübersicht 2.1 Geschichte der Transfusionsmedizin
 2. Literaturübersicht 2.1 Geschichte der Transfusionsmedizin Die Geschichte der veterinärmedizinischen Transfusionsmedizin ist mit der humanmedizinischen eng verbunden, da Tiere häufig zu Forschungszwecken
2. Literaturübersicht 2.1 Geschichte der Transfusionsmedizin Die Geschichte der veterinärmedizinischen Transfusionsmedizin ist mit der humanmedizinischen eng verbunden, da Tiere häufig zu Forschungszwecken
Referenz- und Kreuzprobenlabor Immunhämatologie
 Referenz- und Kreuzprobenlabor Immunhämatologie Blutgruppe Methode: Material: Indikation: Transport: Hämagglutinationtest (Antigenaustestung, Isoagglutinine und Antikörpersuchtest) 10 ml Nativ-Blut (ohne
Referenz- und Kreuzprobenlabor Immunhämatologie Blutgruppe Methode: Material: Indikation: Transport: Hämagglutinationtest (Antigenaustestung, Isoagglutinine und Antikörpersuchtest) 10 ml Nativ-Blut (ohne
Klinische Chemie und Laboratoriumsdiagnostik WS 2017/2018
 Klinische Chemie und Laboratoriumsdiagnostik WS 2017/2018 Lehrmodul Transfusionsmedizinische Labordiagnostik Dieses Lehrmodul ist eine Praktikumseinheit, zu der Sie bitte Schutzkleidung (Kittel) mitbringen.
Klinische Chemie und Laboratoriumsdiagnostik WS 2017/2018 Lehrmodul Transfusionsmedizinische Labordiagnostik Dieses Lehrmodul ist eine Praktikumseinheit, zu der Sie bitte Schutzkleidung (Kittel) mitbringen.
RhD-Bestimmung. Bedside-Test Antikörpersuchtest Dr. Vera Pászthy
 RhD-Bestimmung Bedside-Test Antikörpersuchtest 2013. 11. 18. Dr. Vera Pászthy Nationaler Bluttransfusionsdienst Regionale Bluttransfusionszentrale Pécs natürlich vorkommende Antikörper (REGULÄRE) A - anti-b
RhD-Bestimmung Bedside-Test Antikörpersuchtest 2013. 11. 18. Dr. Vera Pászthy Nationaler Bluttransfusionsdienst Regionale Bluttransfusionszentrale Pécs natürlich vorkommende Antikörper (REGULÄRE) A - anti-b
Klinische Chemie und Laboratoriumsdiagnostik WS 2018/2019
 Klinische Chemie und Laboratoriumsdiagnostik WS 2018/2019 Lehrmodul Transfusionsmedizinische Labordiagnostik Dieses Lehrmodul ist eine Praktikumseinheit, zu der Sie bitte Schutzkleidung (Kittel) mitbringen.
Klinische Chemie und Laboratoriumsdiagnostik WS 2018/2019 Lehrmodul Transfusionsmedizinische Labordiagnostik Dieses Lehrmodul ist eine Praktikumseinheit, zu der Sie bitte Schutzkleidung (Kittel) mitbringen.
1. Blutgruppenserologie und Immunhämatologie
 1. Blutgruppenserologie und Immunhämatologie Vollständige Blutgruppenbestimmung (AB0, Rhesusfaktor, Antikörpersuchtest) Serologische Bestimmung der Blutgruppenmerkmale, z. B. bei möglichem Blutbedarf Bestimmung
1. Blutgruppenserologie und Immunhämatologie Vollständige Blutgruppenbestimmung (AB0, Rhesusfaktor, Antikörpersuchtest) Serologische Bestimmung der Blutgruppenmerkmale, z. B. bei möglichem Blutbedarf Bestimmung
1. Blutgruppenserologie und Immunhämatologie
 1. Blutgruppenserologie und Immunhämatologie Vollständige Blutgruppenbestimmung (AB0, Rhesusfaktor, Antikörpersuchtest) Serologische Bestimmung der Blutgruppenmerkmale, z. B. bei möglichem Blutbedarf Bestimmung
1. Blutgruppenserologie und Immunhämatologie Vollständige Blutgruppenbestimmung (AB0, Rhesusfaktor, Antikörpersuchtest) Serologische Bestimmung der Blutgruppenmerkmale, z. B. bei möglichem Blutbedarf Bestimmung
Praktikum Transfusionsmedizin
 Praktikum Transfusionsmedizin Humanmedizin 1. klinisches Jahr ÜBUNGEN: 1. Blutgruppenbestimmung AB0-System Die Blutgruppenbestimmung im AB0-System erfolgt: 1. durch Bestimmung der AB0-Antigene (Erythrozyteneigenschaften)
Praktikum Transfusionsmedizin Humanmedizin 1. klinisches Jahr ÜBUNGEN: 1. Blutgruppenbestimmung AB0-System Die Blutgruppenbestimmung im AB0-System erfolgt: 1. durch Bestimmung der AB0-Antigene (Erythrozyteneigenschaften)
Immunhämatologische Resultate in der Hausarztpraxis
 Immunhämatologische Resultate in der Hausarztpraxis Interpretation, Konsequenzen Dr. med. T. Braschler, OAmbF Hämatologie 08.03.2018 Inhalt Der Immunhämatologische Befund Type and Screen Untersuchung Bedeutung
Immunhämatologische Resultate in der Hausarztpraxis Interpretation, Konsequenzen Dr. med. T. Braschler, OAmbF Hämatologie 08.03.2018 Inhalt Der Immunhämatologische Befund Type and Screen Untersuchung Bedeutung
ScanGel NEUTRAL Karten Karten
 ScanGel NEUTRAL 86429 48 Karten 86430 1080 Karten NEUTRALES GEL Serumgegenprobe, Ak-Suchtest, Verträglichkeitsprobe IVD Alle von der Firma Bio-Rad hergestellten und verkauften Produkte unterliegen einem
ScanGel NEUTRAL 86429 48 Karten 86430 1080 Karten NEUTRALES GEL Serumgegenprobe, Ak-Suchtest, Verträglichkeitsprobe IVD Alle von der Firma Bio-Rad hergestellten und verkauften Produkte unterliegen einem
Monozyten Monolayer Assay (MMA): Bestimmung der klinischen Relevanz von Alloantikörpern
 Monozyten Monolayer Assay (MMA): Bestimmung der klinischen Relevanz von Alloantikörpern Bern, 18.10.2018 Fabienne Knörr Biomedizinische Analytikerin Interregionale Blutspende SRK AG Immunhämatologisches
Monozyten Monolayer Assay (MMA): Bestimmung der klinischen Relevanz von Alloantikörpern Bern, 18.10.2018 Fabienne Knörr Biomedizinische Analytikerin Interregionale Blutspende SRK AG Immunhämatologisches
Transfusionsmedizin. Urs Schanz Klinik für Hämatologie UniversitätsSpital Zürich
 Transfusionsmedizin Urs Schanz Klinik für Hämatologie UniversitätsSpital Zürich Inhalt der Transfusionsmedizin Herstellung, Lagerung, Bereitstellung und Verabreichung von Blutprodukten Erkennung und Behandlung
Transfusionsmedizin Urs Schanz Klinik für Hämatologie UniversitätsSpital Zürich Inhalt der Transfusionsmedizin Herstellung, Lagerung, Bereitstellung und Verabreichung von Blutprodukten Erkennung und Behandlung
Studiengang (Master) Medizinische Biotechnologie M10.d WS 2014/2015
 Studiengang (Master) Medizinische Biotechnologie M10.d WS 2014/2015 Lehrmodul Serologische Methoden (Antikörper gegen Polymorphismen der Erythrozytenmembran) Dieses Lehrmodul ist eine Praktikumseinheit,
Studiengang (Master) Medizinische Biotechnologie M10.d WS 2014/2015 Lehrmodul Serologische Methoden (Antikörper gegen Polymorphismen der Erythrozytenmembran) Dieses Lehrmodul ist eine Praktikumseinheit,
Bluttransfusionen Indikationen und praktische Durchführung
 Bluttransfusionen Indikationen und praktische Durchführung Rosa Barsnick Leipziger Tierärztekongress 2014 National Archives and Records Administration Indikationen für die Bluttransfusion Hämolyse Arterielle
Bluttransfusionen Indikationen und praktische Durchführung Rosa Barsnick Leipziger Tierärztekongress 2014 National Archives and Records Administration Indikationen für die Bluttransfusion Hämolyse Arterielle
4. Ergebnisse. Tab. 10:
 4. Ergebnisse 4.1 in vitro-ergebnisse Es war aus sicherheitstechnischen und arbeitsrechtlichen Gründen nicht möglich, die für den Tierversuch hergestellten, radioaktiv markierten PMMA-Nanopartikel auf
4. Ergebnisse 4.1 in vitro-ergebnisse Es war aus sicherheitstechnischen und arbeitsrechtlichen Gründen nicht möglich, die für den Tierversuch hergestellten, radioaktiv markierten PMMA-Nanopartikel auf
Hämatologische Diagnostik in der Tiermedizin mit dem XT-2000iV: Fallbeispiel einer immunhämolytischen Anämie bei einer Katze
 Hämatologische Diagnostik in der Tiermedizin mit dem XT-2000iV: Fallbeispiel einer immunhämolytischen Anämie bei einer Katze Eine Anämie ist ein in der tierärztlichen Praxis häufig auftretendes Symptom
Hämatologische Diagnostik in der Tiermedizin mit dem XT-2000iV: Fallbeispiel einer immunhämolytischen Anämie bei einer Katze Eine Anämie ist ein in der tierärztlichen Praxis häufig auftretendes Symptom
ScanGel Monoclonal ABO/RH1/RH Karten Karten
 ScanGel Monoclonal ABO/RH1/RH1 86494 48 Karten 86444 288 Karten MIT MONOKLONALEN REAGENZIEN MURINEN ODER HUMANEN URSPRUNGS FORMULIERTE GELE ABO-Blutgruppenbestimmung. RH1 Ag Bestimmung IVD Alle von der
ScanGel Monoclonal ABO/RH1/RH1 86494 48 Karten 86444 288 Karten MIT MONOKLONALEN REAGENZIEN MURINEN ODER HUMANEN URSPRUNGS FORMULIERTE GELE ABO-Blutgruppenbestimmung. RH1 Ag Bestimmung IVD Alle von der
Blutgruppenserologische Bestimmungen: Stand:
 Blutgruppenserologische Bestimmungen: Stand: 16.12.2016 Blutgruppenbestimmung (AB0, Isoagglutinine, K-Antigen, A-Untergruppe) Serologische Bestimmung der Blutgruppe bei Patienten (z.b. wenn Transfusionen
Blutgruppenserologische Bestimmungen: Stand: 16.12.2016 Blutgruppenbestimmung (AB0, Isoagglutinine, K-Antigen, A-Untergruppe) Serologische Bestimmung der Blutgruppe bei Patienten (z.b. wenn Transfusionen
8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung
 8. Anhang 8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung 1.) Spüllösung (modifizierte PBS-Lösung) modifizierte PBS-Lösung 500
8. Anhang 8.1. Zusammensetzung und Herstellung der verwendeten Medien für die In-vitro-Maturation, -Fertilisation und - Kultivierung 1.) Spüllösung (modifizierte PBS-Lösung) modifizierte PBS-Lösung 500
Verwendung von Blutprodukten in der veterinärmedizinischen Praxis
 Verwendung von Blutprodukten in der veterinärmedizinischen Praxis Dr. Nicole Luckschander-Zeller, PhD Dipl. ACVIM & Dipl. ECVIM-CA Dept. IV, Klinik für Kleintiere Abteilung für Interne Medizin BLUTGRUPPEN
Verwendung von Blutprodukten in der veterinärmedizinischen Praxis Dr. Nicole Luckschander-Zeller, PhD Dipl. ACVIM & Dipl. ECVIM-CA Dept. IV, Klinik für Kleintiere Abteilung für Interne Medizin BLUTGRUPPEN
S E L B S T I N S P E K T I O N
 1 Durchführungsbestätigung Selbstinspektion Verteiler: S E L B S T I N S P E K T I O N gemäß QM-Handbuch Hämotherapie Auditierte Abteilung: Datum / Uhrzeit: Audit-Leiter: Weitere Teilnehmer: Auditbericht
1 Durchführungsbestätigung Selbstinspektion Verteiler: S E L B S T I N S P E K T I O N gemäß QM-Handbuch Hämotherapie Auditierte Abteilung: Datum / Uhrzeit: Audit-Leiter: Weitere Teilnehmer: Auditbericht
RIDA Aviditätsreagenz
 RIDA Aviditätsreagenz Art. No.: LB0023 R-Biopharm AG, An der neuen Bergstraße 17, D-64297 Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0 / Telefax: +49 (0) 61 51 81 02-20 1. Allgemeines Für die in vitro
RIDA Aviditätsreagenz Art. No.: LB0023 R-Biopharm AG, An der neuen Bergstraße 17, D-64297 Darmstadt, Germany Tel.: +49 (0) 61 51 81 02-0 / Telefax: +49 (0) 61 51 81 02-20 1. Allgemeines Für die in vitro
Blutgruppen, AB0-Systems, Antigen, Rhesus-Antigen, monoklonale Antikörper
 Bestimmung der AB0- und Rhesus-n TEAS - 00 Themen n, AB0-Systems, Antigen, Rhesus-Antigen, monoklonale Antikörper Prinzip Seit der Entdeckung der n des AB0-Systems durch Karl Landsteiner im Jahr 1900 und
Bestimmung der AB0- und Rhesus-n TEAS - 00 Themen n, AB0-Systems, Antigen, Rhesus-Antigen, monoklonale Antikörper Prinzip Seit der Entdeckung der n des AB0-Systems durch Karl Landsteiner im Jahr 1900 und
ScanGel ScanBrom ml
 ScanGel ScanBrom 86445 12 ml BROMELAIN FÜR KOMPATIBILITÄTSTEST IVD Alle von der Firma Bio-Rad hergestellten und verkauften Produkte unterliegen einem Qualitätssicherungssystem vom Rohstoffeingang bis zur
ScanGel ScanBrom 86445 12 ml BROMELAIN FÜR KOMPATIBILITÄTSTEST IVD Alle von der Firma Bio-Rad hergestellten und verkauften Produkte unterliegen einem Qualitätssicherungssystem vom Rohstoffeingang bis zur
Muster-Arbeitsanweisung 1. zur
 Muster-Arbeitsanweisung 1 zur Transfusion von Erythrozytenkonzentraten (EK) unter den besonderen Bedingungen des Abschnitts 1.6.2.1 b) ( Transfusion von EK - unter 50 pro Jahr - ausschließlich durch den
Muster-Arbeitsanweisung 1 zur Transfusion von Erythrozytenkonzentraten (EK) unter den besonderen Bedingungen des Abschnitts 1.6.2.1 b) ( Transfusion von EK - unter 50 pro Jahr - ausschließlich durch den
Kurzanleitung. Qualitätssicherung in der Blutgruppenserologie Seite 1 von 11. Wöchentliche und tägliche Qualitätssicherung im Überblick 1
 in der Blutgruppenserologie Seite 1 von 11 Wöchentliche und tägliche im Überblick 1 Blutgruppenserologische Untersuchungen unterliegen den Regeln der der Bundesärztekammer (Hämotherapie-Richtlinien, zweite
in der Blutgruppenserologie Seite 1 von 11 Wöchentliche und tägliche im Überblick 1 Blutgruppenserologische Untersuchungen unterliegen den Regeln der der Bundesärztekammer (Hämotherapie-Richtlinien, zweite
Leistungsverzeichnis LV_SBGR. Antikörper gegen Systemische Sklerose-assoziierte Antigene (Immunoblot)
 Seite 1 von 5 1. Klinische Indikation Analyt: Antikörper gegen Systemische Sklerose-assoziierte Antigene (Immunoblot) V. a. und Differentialdiagnostik der progressiven Systemsklerose (), begrenzte (limitierte)
Seite 1 von 5 1. Klinische Indikation Analyt: Antikörper gegen Systemische Sklerose-assoziierte Antigene (Immunoblot) V. a. und Differentialdiagnostik der progressiven Systemsklerose (), begrenzte (limitierte)
SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen
 GEBRAUCHSANLEITUNG SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen (Kat.-Nr. 42177) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
GEBRAUCHSANLEITUNG SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen (Kat.-Nr. 42177) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
Leistungsverzeichnis. Elektronisch mittels Lauris Laboranforderungssystem. nach Validation über KAS und / oder Netzdruck bzw. Fax
 Seite 1 von 9 1. Klinische Indikation Analyt: Differentialblutbild - Verdacht auf Entzündung, Infektion, Gewebsnekrose, systemische Erkrankung des hämatopoetischen Systems, toxische Störung des hämatopoetischen
Seite 1 von 9 1. Klinische Indikation Analyt: Differentialblutbild - Verdacht auf Entzündung, Infektion, Gewebsnekrose, systemische Erkrankung des hämatopoetischen Systems, toxische Störung des hämatopoetischen
Kapitel 11 B): Spendenanalytik: Blutgruppen-serologische Untersuchungen an Spenderproben
 Vorschriften Blutspendedienst SRK BSD SRK Kapitel 11 B): Spendenanalytik: Blutgruppen-serologische Untersuchungen an REFERENZEN 1 - Heilmittelgesetz (HMG) - Nr. 812.21 - Art. 39 und 40-2000 2 - Verordnung
Vorschriften Blutspendedienst SRK BSD SRK Kapitel 11 B): Spendenanalytik: Blutgruppen-serologische Untersuchungen an REFERENZEN 1 - Heilmittelgesetz (HMG) - Nr. 812.21 - Art. 39 und 40-2000 2 - Verordnung
Leistungsverzeichnis. Elektronisch mittels Lauris Laboranforderungssystem. nach Validation über KAS und / oder Netzdruck bzw. Fax
 Seite 1 von 11 1. Klinische Indikation Analyt: Differentialblutbild - Verdacht auf Entzündung, Infektion, Gewebsnekrose, systemische Erkrankung des hämatopoetischen Systems, toxische Störung des hämatopoetischen
Seite 1 von 11 1. Klinische Indikation Analyt: Differentialblutbild - Verdacht auf Entzündung, Infektion, Gewebsnekrose, systemische Erkrankung des hämatopoetischen Systems, toxische Störung des hämatopoetischen
Fehlerquellen bei der Bestimmung und Berechnung des Antikörperindex (AI)
 Quelle: www.fotolia.com Fehlerquellen bei der Bestimmung und Berechnung des Antikörperindex (AI) Q spez Q IgG Q ges Q IgM Quelle: www.horeiber.de AI Q Alb Q Lim 1. Allgemeine Fehlerquellen: Keinen bluthaltigen
Quelle: www.fotolia.com Fehlerquellen bei der Bestimmung und Berechnung des Antikörperindex (AI) Q spez Q IgG Q ges Q IgM Quelle: www.horeiber.de AI Q Alb Q Lim 1. Allgemeine Fehlerquellen: Keinen bluthaltigen
ScanGel Monoclonal A - B - D Karten Karten
 ScanGel Monoclonal A - B - D 86491 48 Karten 86481 288 Karten MIT MONOKLONALEN REAGENZIEN MURINEN ODER HUMANEN URSPRUNGS FORMULIERTE GELE Bestätigung der ABO/D-Blutgruppenbestimmung IVD Alle von der Firma
ScanGel Monoclonal A - B - D 86491 48 Karten 86481 288 Karten MIT MONOKLONALEN REAGENZIEN MURINEN ODER HUMANEN URSPRUNGS FORMULIERTE GELE Bestätigung der ABO/D-Blutgruppenbestimmung IVD Alle von der Firma
II. MATERIAL UND METHODEN
 II. MATERIAL UND METHODEN 2.1 Patienten Das Patientengut setzte sich aus Katzen verschiedener Rassen, verschiedenen Alters und Geschlechts zusammen. Die Katzen wurden in einem Zeitraum von Januar 1999
II. MATERIAL UND METHODEN 2.1 Patienten Das Patientengut setzte sich aus Katzen verschiedener Rassen, verschiedenen Alters und Geschlechts zusammen. Die Katzen wurden in einem Zeitraum von Januar 1999
1) Prätransfusionelle Diagnostik 2) Transfusionsreaktionen
 1) Prätransfusionelle Diagnostik 2) Transfusionsreaktionen (= Unerwünschte Wirkungen ) Andreas Sputtek http://www.sputtek.de [email protected] Universitätsklinikum Hamburg-Eppendorf Institut für Transfusionsmedizin
1) Prätransfusionelle Diagnostik 2) Transfusionsreaktionen (= Unerwünschte Wirkungen ) Andreas Sputtek http://www.sputtek.de [email protected] Universitätsklinikum Hamburg-Eppendorf Institut für Transfusionsmedizin
Transfusionszwischenfälle
 Querschnittsbereich 4 Immunologie / Infektiologie Transfusionszwischenfälle Univ.-Prof. Dr. Hermann Eichler Institut für Klinische Hämostaseologie und Transfusionsmedizin Universität und Universitätsklinikum
Querschnittsbereich 4 Immunologie / Infektiologie Transfusionszwischenfälle Univ.-Prof. Dr. Hermann Eichler Institut für Klinische Hämostaseologie und Transfusionsmedizin Universität und Universitätsklinikum
Grundbegriffe im Qualitätsmanagement Hämotherapie
 Grundbegriffe im Qualitätsmanagement Hämotherapie Gemeinsamer, modifizierter Foliensatz Prof. Dr. Ulrich Sachs/Prof. Dr. Gregor Bein Zentrum für Transfusionsmedizin und Hämotherapie 08.11.2016 Version
Grundbegriffe im Qualitätsmanagement Hämotherapie Gemeinsamer, modifizierter Foliensatz Prof. Dr. Ulrich Sachs/Prof. Dr. Gregor Bein Zentrum für Transfusionsmedizin und Hämotherapie 08.11.2016 Version
Polymorphismen von Strukturen der Erythrozytenmembran (Blutgruppen)
 Blutgruppen Medizinische Biotechnologie (Master) WS 014/015 Polymorphismen von Strukturen der Erythrozytenmembran (Blutgruppen) V. Kiefel Inst. für Transfusionsmedizin Alloantigene auf Erythrozyten, genetisch
Blutgruppen Medizinische Biotechnologie (Master) WS 014/015 Polymorphismen von Strukturen der Erythrozytenmembran (Blutgruppen) V. Kiefel Inst. für Transfusionsmedizin Alloantigene auf Erythrozyten, genetisch
1. Hämatokrit-Bestimmung, Hämoglobingehalt-Bestimmung (Extinktionsmessung) 2. Gerinnungsfunktionsprüfung nach QUICK
 Praktikumsaufgaben 1. Hämatokrit-Bestimmung, Hämoglobingehalt-Bestimmung (Extinktionsmessung) 2. Gerinnungsfunktionsprüfung nach QUICK Allgemeine Bemerkung: Die Blutproben sind Patientenmaterial. Bitte
Praktikumsaufgaben 1. Hämatokrit-Bestimmung, Hämoglobingehalt-Bestimmung (Extinktionsmessung) 2. Gerinnungsfunktionsprüfung nach QUICK Allgemeine Bemerkung: Die Blutproben sind Patientenmaterial. Bitte
MICORYX Weitere Informationen
 MICORYX Weitere Informationen Im Rahmen der Micoryx-Studie wird eine neue Therapie getestet, die sich noch in der Erprobungsphase befindet. Es handelt sich dabei um eine Impfung gegen den Tumor mit Hilfe
MICORYX Weitere Informationen Im Rahmen der Micoryx-Studie wird eine neue Therapie getestet, die sich noch in der Erprobungsphase befindet. Es handelt sich dabei um eine Impfung gegen den Tumor mit Hilfe
HLA- / HPA-Diagnostik: Stand
 HLA- / HPA-Diagnostik: Stand 11.01.2019 HLA-Antikörper-Screening / -Differenzierung Vor und nach Organtransplantation, V.a. Transfusionsreaktion, Refraktärzustand bei Thrombozytentransfusion Lymphozytotoxizitätstest,
HLA- / HPA-Diagnostik: Stand 11.01.2019 HLA-Antikörper-Screening / -Differenzierung Vor und nach Organtransplantation, V.a. Transfusionsreaktion, Refraktärzustand bei Thrombozytentransfusion Lymphozytotoxizitätstest,
CHARACTERIAZTION OF PREEXISTING ANTIBODIES TO S-303 PATHOGEN INACTIVATED RED BLOOD CELLS (S-303 RBC) SCREENING OF IN 10.
 CHARACTERIAZTION OF PREEXISTING ANTIBODIES TO S-303 PATHOGEN INACTIVATED RED BLOOD CELLS (S-303 RBC) SCREENING OF IN 10.721 PATIENT SERA Geisen C, Brixner V, Stempniewski L, North A, Kiessling A.-H, Müller
CHARACTERIAZTION OF PREEXISTING ANTIBODIES TO S-303 PATHOGEN INACTIVATED RED BLOOD CELLS (S-303 RBC) SCREENING OF IN 10.721 PATIENT SERA Geisen C, Brixner V, Stempniewski L, North A, Kiessling A.-H, Müller
3. Patienten, Material und Methoden Patienten
 3. Patienten, Material und Methoden 3.1. Patienten In der vorliegenden Arbeit wurden 100 Patienten mit hämatologisch-onkologischen Grunderkrankungen untersucht. Einschlusskriterien waren: - Patienten über
3. Patienten, Material und Methoden 3.1. Patienten In der vorliegenden Arbeit wurden 100 Patienten mit hämatologisch-onkologischen Grunderkrankungen untersucht. Einschlusskriterien waren: - Patienten über
mvzlm RUHR REFERENZWERTTABELLE
 Blutgruppe / AK-Suchtest vor erwarteter bzw. wahrscheinlicher Transfusion; vor Therapie mit monoklonalen Antikörpern Material: EDTA, 7,5 ml Häufigkeit: 24 h täglich Meßverfahren: Agglutinationsverfahren
Blutgruppe / AK-Suchtest vor erwarteter bzw. wahrscheinlicher Transfusion; vor Therapie mit monoklonalen Antikörpern Material: EDTA, 7,5 ml Häufigkeit: 24 h täglich Meßverfahren: Agglutinationsverfahren
Transfusionszwischenfälle
 Querschnittsbereich 4 Immunologie / Infektiologie Transfusionszwischenfälle Univ.-Prof. Dr. Hermann Eichler Institut für Klinische Hämostaseologie und Transfusionsmedizin Universität und Universitätsklinikum
Querschnittsbereich 4 Immunologie / Infektiologie Transfusionszwischenfälle Univ.-Prof. Dr. Hermann Eichler Institut für Klinische Hämostaseologie und Transfusionsmedizin Universität und Universitätsklinikum
Inhaltsverzeichnis. 1 Einleitung 1
 Inhaltsverzeichnis 1 Einleitung 1 2 Literaturübersicht 3 2.1. Anämie 3 2.2 Hämatologische Besonderheiten bei der Katze 3 2.2.1 Normoblasten und Retikulozyten 5 2.2.2 Howell-Jolly-Körperchen 7 2.2.3 Knochenmark
Inhaltsverzeichnis 1 Einleitung 1 2 Literaturübersicht 3 2.1. Anämie 3 2.2 Hämatologische Besonderheiten bei der Katze 3 2.2.1 Normoblasten und Retikulozyten 5 2.2.2 Howell-Jolly-Körperchen 7 2.2.3 Knochenmark
Blutgruppenserologische Bestimmungen:
 Blutgruppenserologische Bestimmungen: Blutgruppenbestimmung (AB0, Rhesusfaktor, Kell-Antigen, A-Untergruppe) Serologische Bestimmung der Blutgruppe bei Patienten (z.b. wenn Transfusionen in Betracht kommen,
Blutgruppenserologische Bestimmungen: Blutgruppenbestimmung (AB0, Rhesusfaktor, Kell-Antigen, A-Untergruppe) Serologische Bestimmung der Blutgruppe bei Patienten (z.b. wenn Transfusionen in Betracht kommen,
Grundlagen für die Vorbereitung auf die Klausur. Immunreaktionen gegen Erythrozyten, Granzulozyten
 Immunreaktionen gegen Erythrozyten, Granzulozyten Grundlagen für die Vorbereitung auf die Klausur Medizinische Biotechnologie, 4. Semester Prof. Dr. med. Volker Kiefel Institut für Transfusionsmedizin
Immunreaktionen gegen Erythrozyten, Granzulozyten Grundlagen für die Vorbereitung auf die Klausur Medizinische Biotechnologie, 4. Semester Prof. Dr. med. Volker Kiefel Institut für Transfusionsmedizin
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13253-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 29.11.2016 bis 28.11.2021 Ausstellungsdatum: 29.11.2016 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13253-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 29.11.2016 bis 28.11.2021 Ausstellungsdatum: 29.11.2016 Urkundeninhaber:
Aufgabe: Multiple Choice-Antwort: Abschicken. Experte Vorschau schließen. h p://instand.instruct.eu/author/app/cardtop2.html?docid=
 h p://instand.instruct.eu/author/app/cardtop2.html?docid=1451990907273 1 von 1 09.03.2016 17:21 Der erste Schritt zur Gewinnung einer aussagefähigen Probe ist die Kooperation des Patienten. In vielen Fällen
h p://instand.instruct.eu/author/app/cardtop2.html?docid=1451990907273 1 von 1 09.03.2016 17:21 Der erste Schritt zur Gewinnung einer aussagefähigen Probe ist die Kooperation des Patienten. In vielen Fällen
Nach dem Auftauen erfolgte die Kultivierung der Zellen zunächst in mit Gelatine-Lösung (Bacto Gelatine, 1,5% in PBS) beschichteten 6-Lochplatten.
 4 Methoden 4.1 Zellkultur 4.1.1 Kultivierung der Endothelzellen Nach dem Auftauen erfolgte die Kultivierung der Zellen zunächst in mit Gelatine-Lösung (Bacto Gelatine, 1,5% in PBS) beschichteten 6-Lochplatten.
4 Methoden 4.1 Zellkultur 4.1.1 Kultivierung der Endothelzellen Nach dem Auftauen erfolgte die Kultivierung der Zellen zunächst in mit Gelatine-Lösung (Bacto Gelatine, 1,5% in PBS) beschichteten 6-Lochplatten.
Serologisches Untersuchungsspektrum. Allgemeine Hinweise:
 Serologisches Untersuchungsspektrum Anaplasma phagocytophilum Bartonella henselae Brucella spp. Chlamydia trachomatis Mycobacterium tuberculosis Salmonella spp. Yersinia enterocolitica Allgemeine Hinweise:
Serologisches Untersuchungsspektrum Anaplasma phagocytophilum Bartonella henselae Brucella spp. Chlamydia trachomatis Mycobacterium tuberculosis Salmonella spp. Yersinia enterocolitica Allgemeine Hinweise:
Gesamtüberblick Analysen Labordiagnostik
 Gesamtüberblick Analysen diagnostik Testbezeichnung Analytische AB0-gruppen und Antigen D Bestimmung (inkl. Ausschluss schwaches D Antigen bei Rhesus D negativ) Empfehlungen spende SRK Schweiz AB0-gruppen
Gesamtüberblick Analysen diagnostik Testbezeichnung Analytische AB0-gruppen und Antigen D Bestimmung (inkl. Ausschluss schwaches D Antigen bei Rhesus D negativ) Empfehlungen spende SRK Schweiz AB0-gruppen
Gesamtüberblick Analysenliste Labordiagnostik (Standort Bern)
 Gesamtüberblick Analysenliste diagnostik (Standort Bern) Testbezeichnung Analytische ABO-gruppen und Antigen D Bestimmung (inkl. Ausschluss schwaches D Antigen bei Rhesus D negativ) Empfehlungen spende
Gesamtüberblick Analysenliste diagnostik (Standort Bern) Testbezeichnung Analytische ABO-gruppen und Antigen D Bestimmung (inkl. Ausschluss schwaches D Antigen bei Rhesus D negativ) Empfehlungen spende
Anti-D Blend (IgM + IgG) monoklonal
 GEBRAUCHSINFORMATION Anti-D Blend (IgM + IgG) monoklonal 0123 IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Anti-D Blend (IgM + IgG) monoklonal besteht aus humanem monoklonalen Anti-D (IgM) (Klon D175-2)
GEBRAUCHSINFORMATION Anti-D Blend (IgM + IgG) monoklonal 0123 IN VITRO DIAGNOSTIKUM 1. Produktbeschreibung Anti-D Blend (IgM + IgG) monoklonal besteht aus humanem monoklonalen Anti-D (IgM) (Klon D175-2)
III. Eigene Untersuchungen. 1. Material und Methoden Patienten
 59 III. Eigene Untersuchungen 1. Material und Methoden 1.1. Patienten Das Patientengut setzte sich aus Hunden verschiedener Rassen, verschiedenen Alters und Geschlechts zusammen. Die Hunde wurden im Zeitraum
59 III. Eigene Untersuchungen 1. Material und Methoden 1.1. Patienten Das Patientengut setzte sich aus Hunden verschiedener Rassen, verschiedenen Alters und Geschlechts zusammen. Die Hunde wurden im Zeitraum
Transfusionszwischenfälle
 Querschnittsbereich 4 Immunologie / Infektiologie Transfusionszwischenfälle Univ.-Prof. Dr. Hermann Eichler Institut für Klinische Hämostaseologie und Transfusionsmedizin Universität und Universitätsklinikum
Querschnittsbereich 4 Immunologie / Infektiologie Transfusionszwischenfälle Univ.-Prof. Dr. Hermann Eichler Institut für Klinische Hämostaseologie und Transfusionsmedizin Universität und Universitätsklinikum
PeliCase 1 Best.-Nr
 PeliCase 1 Best.-Nr. 546009 Charge: 8000233305 Verfallsdatum: 2016-12-13 Name: Krankenhaus: Unterschrift: Station: Fall: Frau Claasen (63 Jahre alt) wurde in die chirurgische Abteilung Ihres Krankenhauses
PeliCase 1 Best.-Nr. 546009 Charge: 8000233305 Verfallsdatum: 2016-12-13 Name: Krankenhaus: Unterschrift: Station: Fall: Frau Claasen (63 Jahre alt) wurde in die chirurgische Abteilung Ihres Krankenhauses
Leistungsverzeichnis. nach Validation über KAS und / oder Netzdruck bzw. Fax
 Seite 1 von 7 1. Klinische Indikation Analyt: - Allgemeines Screening Kleines Blutbild - Anämie-, Leukämiediagnostik und andere hämatologische Fragestellungen - Infektdiagnostik - Verlaufsbeurteilung und
Seite 1 von 7 1. Klinische Indikation Analyt: - Allgemeines Screening Kleines Blutbild - Anämie-, Leukämiediagnostik und andere hämatologische Fragestellungen - Infektdiagnostik - Verlaufsbeurteilung und
Zur Registrierung der Proben sind folgende Angaben auf dem Auftragsschein wichtig:
 Probentransport Zur Registrierung der Proben sind folgende Angaben auf dem Auftragsschein wichtig: Datum der Probenentnahme Uhrzeit der Probenentnahme Vollständige Patientendaten (Name, Vorname, Geburtsdatum
Probentransport Zur Registrierung der Proben sind folgende Angaben auf dem Auftragsschein wichtig: Datum der Probenentnahme Uhrzeit der Probenentnahme Vollständige Patientendaten (Name, Vorname, Geburtsdatum
Hämoglobinbestimmung
 Hämoglobinbestimmung TEAS Themen Erythrozyten, Photometrie, Hämoglobin, Cyanhämoglobin, Oxyhämoglobin, Carboxyhämoglobin, Methämoglobin, Anämie. Prinzip Eine quantitative Hämoglobinbestimmung ist unerlässlich,
Hämoglobinbestimmung TEAS Themen Erythrozyten, Photometrie, Hämoglobin, Cyanhämoglobin, Oxyhämoglobin, Carboxyhämoglobin, Methämoglobin, Anämie. Prinzip Eine quantitative Hämoglobinbestimmung ist unerlässlich,
Blutgruppenkompatibilitäten im AB0-System
 Blutgruppenkompatibilitäten im AB0-System Patient EK GFP Pool-TK* A A oder 0 B B oder 0 AB AB, (A, B, 0) 0 0 A, AB B, AB AB 0, A, B, AB A, (AB, 0**, B**) B, (AB, 0**, A**) AB, (A**, B**, 0**) 0, (A, B,
Blutgruppenkompatibilitäten im AB0-System Patient EK GFP Pool-TK* A A oder 0 B B oder 0 AB AB, (A, B, 0) 0 0 A, AB B, AB AB 0, A, B, AB A, (AB, 0**, B**) B, (AB, 0**, A**) AB, (A**, B**, 0**) 0, (A, B,
INFORMATIONEN FÜR SPENDER
 1 INFORMATIONEN FÜR SPENDER Wir freuen uns, dass Sie sich als Spender/in melden wollen. Sie können das Montag Freitag zwischen 09:00 und 15:00 Uhr unter folgender Telefonnummer tun: 01 403 71 93 Vorher
1 INFORMATIONEN FÜR SPENDER Wir freuen uns, dass Sie sich als Spender/in melden wollen. Sie können das Montag Freitag zwischen 09:00 und 15:00 Uhr unter folgender Telefonnummer tun: 01 403 71 93 Vorher
SKILLS LAB Innere Medizin TRANSFUSIONSMEDIZIN
 SKILLS LAB Innere Medizin TRANSFUSIONSMEDIZIN Dr. med. Richard Schäfer Institut für Klinische und Experimentelle Transfusionsmedizin Eberhard-Karls-Universität Tübingen Zentrum für Klinische Transfusionsmedizin
SKILLS LAB Innere Medizin TRANSFUSIONSMEDIZIN Dr. med. Richard Schäfer Institut für Klinische und Experimentelle Transfusionsmedizin Eberhard-Karls-Universität Tübingen Zentrum für Klinische Transfusionsmedizin
PeliCase 1 Best.-Nr
 PeliCase 1 Best.-Nr. 546008 Charge: 8000243353 Verfallsdatum: 2017-12-11 Name: Krankenhaus: Unterschrift: Station: Fall: Herr Berger (67 Jahre alt) ist wegen einer Darmoperation in Ihrem Krankenhaus. Der
PeliCase 1 Best.-Nr. 546008 Charge: 8000243353 Verfallsdatum: 2017-12-11 Name: Krankenhaus: Unterschrift: Station: Fall: Herr Berger (67 Jahre alt) ist wegen einer Darmoperation in Ihrem Krankenhaus. Der
Chlamydia MIF IgG. Leistungsmerkmale. Produktnummer: IF1250G Rev. J. Nicht für den Vertrieb in den USA
 Produktnummer: IF1250G Rev. J Leistungsmerkmale Nicht für den Vertrieb in den USA ERWARTETE WERTE Patienten mit ambulant erworbener Pneumonie Zwei externe Prüfer untersuchten den Focus Chlamydia MIF IgM
Produktnummer: IF1250G Rev. J Leistungsmerkmale Nicht für den Vertrieb in den USA ERWARTETE WERTE Patienten mit ambulant erworbener Pneumonie Zwei externe Prüfer untersuchten den Focus Chlamydia MIF IgM
Institute for Immunology and Thymus Research Laboratory for Autologous Adult Stem Cell Research and Therapy
 Institute for Immunology and Thymus Research Laboratory for Autologous Adult Stem Cell Research and Therapy Rudolf-Huch-Str. 14 D- 38667 Bad Harzburg Tel: +49 (0)5322 96 05 14 Fax: +49 (0)5322 96 05 16
Institute for Immunology and Thymus Research Laboratory for Autologous Adult Stem Cell Research and Therapy Rudolf-Huch-Str. 14 D- 38667 Bad Harzburg Tel: +49 (0)5322 96 05 14 Fax: +49 (0)5322 96 05 16
Look back Kommunikation zwischen Anwender & Pharmazeutischem Hersteller
 Look back Kommunikation zwischen Anwender & Pharmazeutischem Hersteller Blutspendedienst des BRK Dr. Petra Michel Stufenplanbeauftragte Hannover, 27. September 2011 Rückverfolgung Regulatorische Vorgaben
Look back Kommunikation zwischen Anwender & Pharmazeutischem Hersteller Blutspendedienst des BRK Dr. Petra Michel Stufenplanbeauftragte Hannover, 27. September 2011 Rückverfolgung Regulatorische Vorgaben
Stand 08/09. Institut für Transfusionsmedizin Erlanger Allee 101 Laborzentrum Jena. Mit den Laboratorien:
 Einrichtung: Mit den Laboratorien: Institut für Transfusionsmedizin Erlanger Allee 101 Laborzentrum 07740 Jena Arbeitsbereich (AB) Labor Transplantationsimmunologie AB Labor Prätransfusionelle Diagnostik
Einrichtung: Mit den Laboratorien: Institut für Transfusionsmedizin Erlanger Allee 101 Laborzentrum 07740 Jena Arbeitsbereich (AB) Labor Transplantationsimmunologie AB Labor Prätransfusionelle Diagnostik
Prävalenz bei ambulanten Patienten mit ambulant erworbener Pneumonie nach Erreger
 Produktnummer: IF1250M Rev. I Leistungsmerkmale Nicht für den Vertrieb in den USA ERWARTETE WERTE Patienten mit ambulant erworbener Pneumonie Zwei externe Prüfer untersuchten den Focus Chlamydia MIF IgM
Produktnummer: IF1250M Rev. I Leistungsmerkmale Nicht für den Vertrieb in den USA ERWARTETE WERTE Patienten mit ambulant erworbener Pneumonie Zwei externe Prüfer untersuchten den Focus Chlamydia MIF IgM
Standardabweichung und Variationskoeffizient. Themen. Prinzip. Material TEAS Qualitätskontrolle, Standardabweichung, Variationskoeffizient.
 Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
Applications Note 164 Oktober 2007
 Applications Note 164 Oktober 2007 Technical Report Eppendorf Safe-Lock Tubes Höchste Sicherheit bei Zentrifugation und Inkubation von Proben im Labor Natascha Weiß 1, Sophie Freitag 2, Jürgen Löhn 3,
Applications Note 164 Oktober 2007 Technical Report Eppendorf Safe-Lock Tubes Höchste Sicherheit bei Zentrifugation und Inkubation von Proben im Labor Natascha Weiß 1, Sophie Freitag 2, Jürgen Löhn 3,
Leistungsverzeichnis LV_IMMST
 Seite 1 von 5 1. Klinische Indikation Analyt: Immunstatus (Lymphocytentypisierung) HIV-Infektion: Verlaufsuntersuchung und Therapiesteuerung Erkennung von Vermehrungen oder Verminderungen einzelner Lymphocytensubpopulationen
Seite 1 von 5 1. Klinische Indikation Analyt: Immunstatus (Lymphocytentypisierung) HIV-Infektion: Verlaufsuntersuchung und Therapiesteuerung Erkennung von Vermehrungen oder Verminderungen einzelner Lymphocytensubpopulationen
_ 2 Flaschen Antiserum: Anti A und Anti B _ 1 Flasche Rhesusfaktor _ 48 Objektträger mit Mulden zum Mischen (Testdurchführung) _ 40 Zahnstocher
 Simulierte ABO Blutgruppenbestimmung / Schülerversuch INHALT des Kits _ 1 Flasche synthetisches Blut der Blutgruppe A _ 1 Flasche synthetisches Blut der Blutgruppe B _ 1 Flasche synthetisches Blut der
Simulierte ABO Blutgruppenbestimmung / Schülerversuch INHALT des Kits _ 1 Flasche synthetisches Blut der Blutgruppe A _ 1 Flasche synthetisches Blut der Blutgruppe B _ 1 Flasche synthetisches Blut der
Nachweismethoden. Medizin und Mykologie. Nachweismethoden. Seite 1
 Seite 1 ELISA-Test 1604 Enzyme-linked Immunosorbent Assay Am 1. und 2. Tag der Vergiftung lassen sich Amanitine im Blut und Urin nachweisen. Nach dem 3. bis 4. Tag sind nur noch im Urin genügend hohe Amanitin-Konzentrationen
Seite 1 ELISA-Test 1604 Enzyme-linked Immunosorbent Assay Am 1. und 2. Tag der Vergiftung lassen sich Amanitine im Blut und Urin nachweisen. Nach dem 3. bis 4. Tag sind nur noch im Urin genügend hohe Amanitin-Konzentrationen
Leitlinien zur Gewinnung, Lagerung, Transport und Verabreichung von Blut und Blutprodukten im Veterinärbereich
 Leitlinien zur Gewinnung, Lagerung, Transport und Verabreichung von Blut und Blutprodukten im Veterinärbereich Diese Leitlinien betreffen allgemeine Festlegungen zur Gewinnung, Lagerung, Transport und
Leitlinien zur Gewinnung, Lagerung, Transport und Verabreichung von Blut und Blutprodukten im Veterinärbereich Diese Leitlinien betreffen allgemeine Festlegungen zur Gewinnung, Lagerung, Transport und
Massgeschneiderte Dienstleistungen
 Massgeschneiderte Dienstleistungen Blutspendedienst SRK Bern AG kompetenter Partner der Life Science Industrie für Blutprodukte und labordiagnostische Analysen. 2 Über uns Im Rahmen seiner Kernaufgabe
Massgeschneiderte Dienstleistungen Blutspendedienst SRK Bern AG kompetenter Partner der Life Science Industrie für Blutprodukte und labordiagnostische Analysen. 2 Über uns Im Rahmen seiner Kernaufgabe
3. Hämoglobin-Screening bei Blutspendern Spezielle Fragestellung
 3. Hämoglobin-Screening bei Blutspendern 3.1. Spezielle Fragestellung Eine Messung der Hämoglobin-Konzentration ist als Tauglichkeitsuntersuchung vor jeder freiwilligen Blutspende vorgeschrieben. Bei Unterschreiten
3. Hämoglobin-Screening bei Blutspendern 3.1. Spezielle Fragestellung Eine Messung der Hämoglobin-Konzentration ist als Tauglichkeitsuntersuchung vor jeder freiwilligen Blutspende vorgeschrieben. Bei Unterschreiten
Gesamtüberblick Analysen Labordiagnostik
 Gesamtüberblick Analysen diagnostik Testbezeichnung Analytische Matrix *) fragen AB0-Blutgruppen und Antigen D Bestimmung (inkl. Ausschluss schwaches D Antigen bei Rhesus D negativ) Empfehlungen Nativblut,
Gesamtüberblick Analysen diagnostik Testbezeichnung Analytische Matrix *) fragen AB0-Blutgruppen und Antigen D Bestimmung (inkl. Ausschluss schwaches D Antigen bei Rhesus D negativ) Empfehlungen Nativblut,
Klinische Chemie und Laboratoriumsdiagnostik. Teil 13. Immunhämatologie
 Klinische Chemie und Laboratoriumsdiagnostik Teil 13 Immunhämatologie Prof. Dr. Ralf Lichtinghagen Medizinische Hochschule Hannover Klinische Chemie Tel.: 0511-5323940 Antigene und Antikörper Antigene:
Klinische Chemie und Laboratoriumsdiagnostik Teil 13 Immunhämatologie Prof. Dr. Ralf Lichtinghagen Medizinische Hochschule Hannover Klinische Chemie Tel.: 0511-5323940 Antigene und Antikörper Antigene:
Leistungsverzeichnis LV_MBGR. Dermatomyositis (hochspezifisch, 15 30%) Idiopathische Myositis 88 12%) Polymyositis Mi-2beta
 Seite 1 von 5 1. Klinische Indikation Analyt: Dermato- und Polymyositis Idiopathische Myositis Anti-Synthetase-Syndrom Überlappungssyndrome Klinische Bedeutung: Antigen: Myositis-Antikörper (Immunoblot)
Seite 1 von 5 1. Klinische Indikation Analyt: Dermato- und Polymyositis Idiopathische Myositis Anti-Synthetase-Syndrom Überlappungssyndrome Klinische Bedeutung: Antigen: Myositis-Antikörper (Immunoblot)
