67. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom
|
|
|
- Hilko Ackermann
- vor 6 Jahren
- Abrufe
Transkript
1 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 67. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom UTagungsort:U Bundesinstitut für Arzneimittel und Medizinprodukte D Bonn, Kurt-Georg-Kiesinger-Allee 3 UTeilnehmer:U Der Vorsitzende Die Sachverständigen des Ausschusses für Verschreibungspflicht 2BVertreter des Bundesministeriums für Gesundheit (BMG) 3BVertreter des Paul-Ehrlich-Instituts (PEI) Vertreter des BfArM 4BUTagesordnung 1. Eröffnung der Sitzung 2. Annahme der Tagesordnung 3. Dextromethorphan Antrag auf partielle Unterstellung unter die Verschreibungspflicht 4. Nicotin Antrag auf Erhöhung der freigestellten Einzeldosis von 10 mg auf 15 mg 5. a. Triptane vergleichende Analyse Auftrag aus der 66. Sitzung b. Rizatriptan Antrag auf Entlassung aus der Verschreibungspflicht für 10 mg Rizatriptan c. Sumatriptan Nasenspray Antrag auf Entlassung des Nasensprays (Dosierung 20 mg) aus der Verschreibungspflicht - 1 -
2 6. Impfstoffe - zur Anwendung am oder im menschlichen Körper Antrag auf Entlassung von multibakteriellen Totimpfstoffen zur oralen Anwendung aus der Verschreibungspflicht 7. Ketoprofen zur topischen Anwendung Antrag auf Unterstellung unter die Verschreibungspflicht 10. Verschiedenes 0BTOP 1 Eröffnung der Sitzung Der Vorsitzende begrüßt die Anwesenden. Es folgen verfahrenstechnische Informationen. Es wird vereinbart, dass Redebeiträge künftig grundsätzlich auf die Dauer von 10 Minuten begrenzt werden. Der Termin für die 68. Sitzung am wird bestätigt und der wird als Termin für die 69. Sitzung vereinbart. 1BTOP 2 Annahme der Tagesordnung TOP 7 Ketoprofen zur topischen Anwendung wird vorgezogen. TOP 3 Dextromethorphan Antrag auf partielle Unterstellung unter die Verschreibungspflicht Das BfArM führt in das Thema ein (s. Anlage 2). Einer der Sachverständigen ist der Ansicht, dass bei einem postulierten substanzbedingten Missbrauchspotenzial eine generelle Unterstellung von Dextromethorphan (DXM) unter die Verschreibungspflicht die angemessene Maßnahme sei. Das BfArM begründet die Ausnahme der flüssigen Formen von der Verschreibungspflicht mit der geringen Wirkstoffkonzentration. Hier müssten zur Erreichung eines für den Missbrauch ausreichenden Plasmaspiegels so große Mengen getrunken werden, dass die gastrointestinalen Wirkungen (z.b. abführende Wirkung von Sorbitol) vermutlich den vom Nutzer gewünschten Effekt verhindern. Möglicherweise ist dies der Grund dafür, dass Berichte über die missbräuchliche Anwendung von flüssigen Darreichungsformen von DXM fehlen. Diese Ansicht wird nach Angaben eines Sachverständigen durch wissenschaftliche Erkenntnisse gestützt, nach denen zur Erreichung der gewünschten Wirkungen im ZNS Dosen von ca mg notwendig sind. Andererseits sind Fallberichte dokumentiert, in denen Jugendliche nach Einnahme von ca. 400 mg hospitalisiert werden mussten. In den meisten Fällen bleibt allerdings die eingenommene Menge an Wirkstoff unbekannt
3 Ein Sachverständiger erkundigt sich danach, ob der Antrag des BfArM, die im Verkehr befindlichen Granulate, zum Auflösen in Flüssigkeit, sowie die Lutschpastillen einschließt. Da die Lutschpastillen eine gummiartige Konsistenz hätten, können sie nicht für eine missbräuchliche Anwendung zerkleinert oder gemörsert werden. Zudem enthalten auch sie in nicht unerheblichen Mengen Sorbitol. Ein Sachverständiger betont, dass aus seiner Sicht die Evidenz für einen für die Unterstellung von DXM zu fordernden erheblichen Missbrauch sehr gering ist, da dem Verkauf von 6,7 Mio. Packungen (in 2010) lediglich eine niedrige zweistellige Zahl von Apotheken gegenüber steht, die überhaupt über einen vermuteten Missbrauch berichten. Da DXM in Lutschtabletten wie in Kombinationspräparaten für eine missbräuchliche Anwendung unterdosiert sind, blieben aus seiner Sicht lediglich die Kapseln übrig. Da aber DXM in einschlägigen Internetforen nicht empfohlen wird, stellt er den Regelungsbedarf bezüglich DXM grundsätzlich in Frage. Das BfArM erläutert dazu, dass in Internetforen DXM durchaus empfohlen werde. Dabei wird in der Regel dargestellt, dass die Dosis zur Auslösung angenehmer psychischer Effekte subjektiv ermittelt werden muss. Andere Sachverständige stellen den Regelungsbedarf bezüglich DXM ebenfalls in Frage. Ein Sachverständiger führt aus, warum aus seiner Sicht das vorgelegte Datenmaterial die Annahme eines häufigen Missbrauchs in einem erheblichen Umfang in Deutschland nicht stützt. Ein Sachverständiger berichtet, dass die Anwendung von DXM in der flüssigen Form, vor allem in Kombination mit Paracetamol, bei Säuglingen und Kleinkindern nicht ungefährlich ist und fundierte Kenntnisse über die pharmakologischen Wirkungen und Interaktionen bei dieser Altersgruppe fehlen. Ein weiterer Sachverständiger fasst die vorangegangene Argumentation mit den verschiedenen offenen Punkten dahingehend zusammen, dass aus seiner Sicht die vom BfArM angeführte Begründung dem dargestellten Problem nicht gerecht wird. Er plädiert dafür, dass das BfArM seine Stellungnahme hinsichtlich weiterer Quellen zu Missbrauchsberichten sowie hinsichtlich der Argumentation bezüglich Dosierungen und den unterschiedlichen galenischen Zubereitungen überarbeitet. Ein Sachverständiger bittet für diese überarbeitete Fassung darum, die Missbrauchsfälle im Verhältnis zu den verkauften Packungen zu betrachten. Außerdem hält er eine Übersicht über den Status DXM-haltiger Arzneimittel in anderen europäischen Ländern für sinnvoll. Der Vorsitzende lässt daraufhin darüber abstimmen, ob der Antrag zusammen mit einer überarbeiteten Begründung erneut dem Ausschuss vorgelegt werden sollte. Der Sachverständigenausschuss stimmt mehrheitlich dafür, die Behandlung des Antrags auf die nächste Sitzung zu vertagen. TOP 4 Nicotin Antrag auf Erhöhung der freigestellten Einzeldosis von 10 mg auf 15 mg - 3 -
4 Das BfArM führt in das Thema ein (s. Anlage 1). Nach kurzer Diskussion über Risiken und Nutzen einer Raucherentwöhnung mit Nicotin erfolgt die Abstimmung. Abstimmungsergebnis: Der Antrag auf Erhöhung der von der Verschreibungspflicht freigestellten Einzeldosis von 10 mg auf 15 mg und der vom BfArM empfohlene Wortlaut für die Position Nicotin - ausgenommen zur oralen (einschließlich der oral-inhalativen) Anwendung ohne Zusatz weiterer arzneilich wirksamer Bestandteile in einer Menge bis zu 15 mg Nicotin je abgeteilter Arzneiform und in einer Tagesdosis bis zu 64 mg wird mehrheitlich angenommen. 5BTOP 5 a. Triptane vergleichende Analyse Auftrag aus der 66. Sitzung Das BfArM führt in das Thema ein (s. Anlage 2). Aus den dargestellten Daten ergeben sich für viele Sachverständige keine relevanten Unterschiede bezüglich der Anwendungssicherheit einzelner Triptane. Auf Nachfrage von Sachverständigen wird erläutert, dass das BMG die Empfehlung des Ausschusses zur Freistellung von Sumatriptan nicht umgesetzt hat, weil der Antragsteller keine Daten zu Erfahrungen mit Sumatriptan in der Selbstmedikation vorgelegt hat. Außerdem hat der Ausschuss die Freistellung an die Bedingung geknüpft, den Inhalt der Packungsbeilage dem erhöhten Anwendungsrisiko nach Wegfall der ärztlichen Kontrolle anzupassen. Dies ist aber aus regulatorischen Gründen nicht einheitlich für alle Arzneimittel möglich. Das BMG wird dem Ausschuss künftig eine Rückmeldung zu den Gründen geben, wenn ein Votum nicht umgesetzt wird. Ein Sachverständiger führt aus, seitens des Antragstellers sei für die Freistellung von Naratriptan argumentiert worden, dass alle übrigen Triptane nicht für eine Freistellung in Frage kämen. Diese Argumentation wurde dann aber auch für den Freistellungsantrag für das nächste Triptan übernommen. Nach seinem Eindruck seien aufgrund derselben Datenbasis jeweils unterschiedliche Schlussfolgerungen gezogen worden. Ein anderer Sachverständiger ergänzt, dass seitens des Antragstellers während der betreffenden Sitzung in der Diskussion um die Freistellung von Naratriptan die Position vertreten wurde, dass alle Patienten mit einer Migräne, die aufgrund ihrer Schwere nicht ausreichend mit Naratriptan zu behandeln sei, unbedingt in die ärztliche Behandlung gehörten. In den weiteren Gutachten zur Befürwortung der Freistellung der übrigen bereits verhandelten Triptane sei diese Argumentation dann verlassen worden
5 Aus Anlass der Diskussion über die Folgen der Freistellung von Triptanen aus der Verschreibungspflicht äußern mehrere Sachverständige die Ansicht, dass die Entscheidung, die Erstattungsfähigkeit mit der Verschreibungspflicht zu verknüpfen, ein politischer Fehler ist, der korrigiert werden sollte und führen Beispiele dafür an, dass diese Regelung der bevorzugten Anwendung von Wirkstoffen mit vergleichsweise erhöhtem Risikopotenzial Vorschub leistet. Nach den vorgelegten Daten ist aus Sicht mehrerer Sachverständiger eine klare Dosis-(Neben-)Wirkungsbeziehung von Triptanen nicht nachweisbar. Damit fehlen klare Kriterien für die Unterscheidung und verliert auch die vergleichende Betrachtung verschiedener Triptane an Relevanz. Aus der Sicht eines Sachverständigen gehört ein Patient mit wiederkehrenden Migräneattacken in ärztliche Behandlung. TOP 5 b. Rizatriptan Antrag auf Entlassung aus der Verschreibungspflicht für 10 mg Rizatriptan Das BfArM führt in das Thema ein (s. Anlage 2). Nach Informationen eines Sachverständigen liegt der Anteil der Patienten, die gleichzeitig mit einem Triptan Propranolol einnehmen, bei maximal 1%. Aus Sicht mehrerer Sachverständiger gibt es Hinweise darauf, dass Rizatriptan eine höhere Wirksamkeit und damit auch ein höheres Nebenwirkungspotenzial besitzt als andere bereits freigestellte Substanzen. In Schweden wurde Rizatriptan 10 mg bereits kürzlich freigestellt, während die niedrigere Dosierung von 5 mg, wie auch in Deutschland, weiterhin der Verschreibungspflicht unterstellt bleiben soll. Begründet wird dies damit, dass die spezielle Gruppe der nieren- bzw. leberinsuffizienten Patienten und solche mit gleichzeitiger Prophylaxe-Behandlung mit Propranolol nur mit 5 mg Rizatriptan behandelt werden dürfen. In der Diskussion werden hier irreführende Signale an den Patienten gesehen, in dessen Wahrnehmung eine ohne Rezept verfügbare höhere Dosierung von 10 mg fälschlicherweise eine gute Verträglichkeit für alle Patienten suggeriert. Das Konzept der Verschreibungspflichtigkeit einer niedrigen Dosierung bei gleichzeitiger Apothekenpflicht der höheren Dosierung wird grundsätzlich als nicht plausibel bezeichnet. Ein anderer Sachverständiger stellt fest, dass nach den vom Antragsteller eingereichten Unterlagen die klinische Relevanz des Anstiegs der Plasmakonzentration von Rizatriptan bei gleichzeitiger Anwendung von Propranolol nicht bekannt ist. Damit sei ein wesentliches Kriterium für die Freistellung nicht erfüllt, nämlich das bekannte Wirkungs- und Nebenwirkungsprofil des betreffenden Wirkstoffs. Außerdem wird bemängelt, dass im eingereichten Gutachten eine Anfallshäufigkeit von weniger als einer Attacke pro Woche als selten bezeichnet und es für diese - 5 -
6 Patientengruppe als Vorteil einer Freistellung bezeichnet wird, wenn sie nicht auf ein ärztliches Rezept warten muss. Hierzu wird festgestellt, dass der Gutachter seine Ansicht zur ärztlichen Betreuungsbedürftigkeit seit seinem ersten Gutachten zu Naratriptan deutlich geändert habe, wenn nun auch Patienten mit einer Attacke pro 10 Tage auf die Selbstmedikation verwiesen werden. Abstimmungsergebnis: Der Antrag auf Entlassung aus der Verschreibungspflicht für die Position Rizatriptan - zur akuten Behandlung der Kopfschmerzphase von Migräneanfällen mit und ohne Aura bei Erwachsenen zwischen 18 und 65 Jahren, nach der Erstdiagnose einer Migräne durch einen Arzt, in festen Zubereitungen zur oralen Anwendung in Konzentrationen von 10 mg je abgeteilter Form und in einer Gesamtmenge von 20 mg je Packung (2 Schmelztabletten bzw. Tabletten à 10 mg) wird mehrheitlich abgelehnt. Ein Sachverständiger erläutert, dass seine Ablehnung hauptsächlich in der mangelnden Qualität und Inkonsistenz der Argumentation von Gutachter und Antragsteller begründet ist. TOP 5 c. Sumatriptan Nasenspray Antrag auf Entlassung des Nasensprays (Dosierung 20 mg) aus der Verschreibungspflicht Das BfArM führt in das Thema ein (s. Anlage 2). Anschließend trägt ein externer Sachverständiger des Antragstellers vor. Ein Sachverständiger thematisiert die beantragte Freistellung nur für Erwachsene und erkundigt sich danach, wie ein Fehlgebrauch für Kinder und Jugendliche einer Familie vor dem Hintergrund des familiär gehäuften Auftretens von Migräne verhindert werden soll. Diesem Fehlgebrauch sollen nach Aussage des externen Sachverständigen gute Schulungsmaßnahmen von Apothekern und Patienten entgegenwirken. Ein Sachverständiger weist darauf hin, dass die Werte für t max mit 0,8 4 extrem schwanken. Dies bedeutet pharmakologisch eine starke Variabilität des Wirkungseintritts. Nach Aussage des externen Sachverständigen ist diese Variabilität, bedingt durch die nasale Applikation, etwas höher als bei anderen Darreichungsformen. Der externe Sachverständige verlässt den Raum. In der anschließenden Diskussion wird festgestellt, dass Sumatriptan Nasenspray aufgrund der langen Anflutungszeit kein schnell wirksames Mittel gegen Migräneattacken ist. Aus Sicht eines Sachverständigen stützen die eingereichten Daten eine Freistellung nicht. Von mehreren Sachverständigen wird die nasale Applikationsform als überflüssig angesehen. Bei einem um bis zu 4 Stunden verzögerten Wirkungseintritt wird von - 6 -
7 ihm die Aussage, Sumatriptan Nasenspray sei zur akuten Behandlung eines Migräneanfalls geeignet, als nicht nachvollziehbar angesehen. Abstimmungsergebnis: Der Antrag auf Entlassung aus der Verschreibungspflicht für die Position Sumatriptan - zur akuten Behandlung der Kopfschmerzphase von Migräneanfällen mit und ohne Aura bei Erwachsenen zwischen 18 und 65 Jahren, nach der Erstdiagnose einer Migräne durch einen Arzt, als Nasenspray zur intranasalen Anwendung in einer Dosierung von 20 mg (berechnet als Sumatriptan) je abgeteilter Form und in einer Gesamtmenge von 40 mg je Packung wird mehrheitlich abgelehnt. TOP 6 Impfstoffe - zur Anwendung am oder im menschlichen Körper Antrag auf Entlassung von multibakteriellen Totimpfstoffen zur oralen Anwendung aus der Verschreibungspflicht. Das PEI führt in das Thema ein (s. Anlage 2). In der anschließenden Diskussion wird festgestellt, dass das für die Freistellung erforderliche Kriterium der Unbedenklichkeit erfüllt ist, dass diese aber in fehlender Wirksamkeit begründet ist. Aus diesem Grund würde die Freistellung und damit die Aufhebung der Erstattungspflicht von den Kostenträgern begrüßt. Ein Sachverständiger vertritt die Ansicht, dass der Sachverständigenausschuss für Verschreibungspflicht nicht das geeignete Gremium ist, diesen durch die Kopplung von Verschreibungspflicht und Erstattungsfähigkeit bedingten Konflikt auszutragen. Vielmehr sollte die Frage der Erstattungsfähigkeit im G-BA entschieden werden. Dort könnte durch die Änderung der Arzneimittel-Richtlinien eine angemessene Regelung getroffen werden. Zudem seien unter den zugelassenen Indikationen solche wie z.b. bakterielle Pyelonephritis, die nicht in die Selbstmedikation gehörten. Zu diesen Punkten besteht zwischen mehreren Sachverständigen Konsens. Abstimmungsergebnis: Der Antrag auf Entlassung aus der Verschreibungspflicht von multibakteriellen Totimpfstoffen - zur oralen Anwendung wird mehrheitlich abgelehnt. TOP 7 Ketoprofen zur topischen Anwendung Antrag auf Unterstellung unter die Verschreibungspflicht - 7 -
8 Das BfArM führt in das Thema ein (s. Anlage 1). Auf entsprechende Anfrage wird darüber informiert, dass die Zahl der aus Deutschland stammenden Berichte zu Photosensibilisierung niedrig ist, vermutlich, weil die Anwendungshäufigkeit im Vergleich zu der von Diclofenac-haltigem Gel eher gering ist. Aus anderen europäischen Ländern wurden dagegen insgesamt mehrere hundert Fälle gemeldet, allein aus Frankreich stammen mehr als 300 Fallberichte. Ursächlich für die Hautreaktion ist vermutlich die Benzophenon-Gruppe des Wirkstoffs. Die von einer photoallergischen Reaktion betroffenen Patienten entwickeln zumeist Rötung, Bläschen und Juckreiz an der Haut, die auch nach Absetzen mehrere Wochen, in Einzelfällen auch mehrere Monate anhalten können. Die Hälfte der Patienten ist so schwer betroffen, dass eine stationäre Aufnahme erforderlich ist. Zu allen anderen NSAR zusammen wurden aus den europäischen Ländern nur wenige Einzelfälle von photoallergischen Reaktionen berichtet. Der Arzt kann im Fall der Verschreibungspflicht den Patienten darauf aufmerksam machen, dass er seine Haut während und bis 14 Tage nach Ende der Anwendung vor Sonnenbestrahlung schützen muss. Abstimmungsergebnis: Der Antrag auf Unterstellung von Ketoprofen - zur topischen Anwendung wird mehrheitlich angenommen. Termin der nächsten Sitzung: UDienstag, der UBeginn: Uhr USitzungsort: Bonn UKurt-Georg-Kiesinger-Allee 3 Der Vorsitzende dankt allen Anwesenden und Ausschussmitgliedern und schließt die Sitzung
9 UAnlagen Anlage 1: Voten und Begründungen zu Positionen, deren Änderung zugestimmt wird (TOP 4, 7) Anlage 2: Stellungnahmen des BfArM zu TOP 3, 5 und 6-9 -
66. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 66. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom 11.01.2011 Tagungsort:
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 66. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom 11.01.2011 Tagungsort:
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen
 Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
73. Sitzung des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 Abs. 2 AMG vom 13.01.2015
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 73. Sitzung des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 Abs. 2 AMG vom 13.01.2015 Tagungsort: Bundesinstitut
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 73. Sitzung des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 Abs. 2 AMG vom 13.01.2015 Tagungsort: Bundesinstitut
Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 7 Famciclovir
 Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 7 Famciclovir Antrag auf Entlassung aus der Verschreibungspflicht Famciclovir zur oralen Behandlung von rezidivierenden Episoden
Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 7 Famciclovir Antrag auf Entlassung aus der Verschreibungspflicht Famciclovir zur oralen Behandlung von rezidivierenden Episoden
Antrag auf Entlassung aus der Verschreibungspflicht. -Doramectin-
 Antrag auf Entlassung aus der Verschreibungspflicht Antrag auf Entlassung von Doramectin aus der Verschreibungspflicht für die topische Anwendung bei Königspython, Abgottschlange und Bartagame bei einem
Antrag auf Entlassung aus der Verschreibungspflicht Antrag auf Entlassung von Doramectin aus der Verschreibungspflicht für die topische Anwendung bei Königspython, Abgottschlange und Bartagame bei einem
V o t en. Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG
 ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 64. Sitzung, 12.01.2010 zu Positionen, deren Änderung abgestimmt
ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 64. Sitzung, 12.01.2010 zu Positionen, deren Änderung abgestimmt
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Vitagutt Vitamin E 670 mg, Weichkapsel Zur Anwendung bei Erwachsenen Wirkstoff: 1000 mg all-rac-alpha-tocopherolacetat (entsprechend 670 mg RRR-alpha- Tocopherol-Äquivalente).
Gebrauchsinformation: Information für Anwender Vitagutt Vitamin E 670 mg, Weichkapsel Zur Anwendung bei Erwachsenen Wirkstoff: 1000 mg all-rac-alpha-tocopherolacetat (entsprechend 670 mg RRR-alpha- Tocopherol-Äquivalente).
TOP 3: Loperamid (flüssige Darreichungsformen)
 TOP 3: Loperamid (flüssige Darreichungsformen) Antrag auf Ausweitung der Ausnahme von der Verschreibungspflicht auch für flüssige Darreichungsformen 1 Historie und aktuell: Seit 1993 D. h. folgende Darreichungsformen
TOP 3: Loperamid (flüssige Darreichungsformen) Antrag auf Ausweitung der Ausnahme von der Verschreibungspflicht auch für flüssige Darreichungsformen 1 Historie und aktuell: Seit 1993 D. h. folgende Darreichungsformen
akut Die Soforthilfe bei Durchfall GRATIS für Sie zum Mitnehmen!
 akut Die Soforthilfe bei Durchfall GRATIS für Sie zum Mitnehmen! Was ist DuRCHFALL und wie entsteht er? SCHLuSS mit den Durchfall-Mythen! Durchfall ist eine der am weitesten verbreiteten Gesundheitsstörungen.
akut Die Soforthilfe bei Durchfall GRATIS für Sie zum Mitnehmen! Was ist DuRCHFALL und wie entsteht er? SCHLuSS mit den Durchfall-Mythen! Durchfall ist eine der am weitesten verbreiteten Gesundheitsstörungen.
Anhang III. Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage
 Anhang III Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage Hinweis: Änderungen an der Fachinformation und der Packungsbeilage müssen unter Umständen im Anschluss durch
Anhang III Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage Hinweis: Änderungen an der Fachinformation und der Packungsbeilage müssen unter Umständen im Anschluss durch
Wortlaut der für die Packungsbeilage vorgesehenen Angaben
 Zulassungsnummer: 6312395.00.00 Seite 1 von 5 Apothekenpflichtig TUSSISANA Mischung 20 und 50 ml Stoff Darreichungsform Menge Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation:
Zulassungsnummer: 6312395.00.00 Seite 1 von 5 Apothekenpflichtig TUSSISANA Mischung 20 und 50 ml Stoff Darreichungsform Menge Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation:
1. Was ist Apis/Belladonna cum Mercurio und wofür wird es angewendet?
 WALA Gebrauchsinformation: Information für Anwender Apis/Bella-donna cum Mercurio Wirkstoffe: Apis mellifica ex animale toto Gl Dil. D4, Atropa bella-donna e fructibus maturis ferm 33a Dil. D3, Mercurius
WALA Gebrauchsinformation: Information für Anwender Apis/Bella-donna cum Mercurio Wirkstoffe: Apis mellifica ex animale toto Gl Dil. D4, Atropa bella-donna e fructibus maturis ferm 33a Dil. D3, Mercurius
Entschließung des Bundesrates zur Rezeptfreiheit von Notfallkontrazeptiva auf der Basis von Levonorgestrel - Pille danach -
 Bundesrat Drucksache 555/13 (Beschluss) 05.07.13 Beschluss des Bundesrates Entschließung des Bundesrates zur Rezeptfreiheit von Notfallkontrazeptiva auf der Basis von Levonorgestrel - Pille danach - Der
Bundesrat Drucksache 555/13 (Beschluss) 05.07.13 Beschluss des Bundesrates Entschließung des Bundesrates zur Rezeptfreiheit von Notfallkontrazeptiva auf der Basis von Levonorgestrel - Pille danach - Der
Anhang III. Ergänzungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Ergänzungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage 20 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS [Der unten genannte Wortlaut
Anhang III Ergänzungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage 20 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS [Der unten genannte Wortlaut
Cefavora - Tropfen. Gebrauchsinformation: Information für Anwender
 1 von 5 Cefavora - Tropfen Gebrauchsinformation: Information für Anwender Wirkstoffe: Ginkgo biloba Ø / Viscum album Ø / Crataegus Ø Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor sie mit
1 von 5 Cefavora - Tropfen Gebrauchsinformation: Information für Anwender Wirkstoffe: Ginkgo biloba Ø / Viscum album Ø / Crataegus Ø Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor sie mit
MEDICA HALSSPRAY MENTHOL, 20 mg/10 ml; 5 mg/10 ml, Spray zur Anwendung in der Mundhöhle Chlorhexidingluconat - Lidocain Hydrochlorid
 MEDICA HALSSPRAY MENTHOL, 20 mg/10 ml; 5 mg/10 ml, Spray zur Anwendung in der Mundhöhle Chlorhexidingluconat - Lidocain Hydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
MEDICA HALSSPRAY MENTHOL, 20 mg/10 ml; 5 mg/10 ml, Spray zur Anwendung in der Mundhöhle Chlorhexidingluconat - Lidocain Hydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Terbinafin HCL acis 10 mg/g Creme Wirkstoff: Terbinafinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Terbinafin HCL acis 10 mg/g Creme Wirkstoff: Terbinafinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
Duraphat Fluorid 5 mg/g Zahnpaste. Antrag auf Entlassung aus der Verschreibungspflicht
 Duraphat Fluorid 5 mg/g Zahnpaste Antrag auf Entlassung aus der Verschreibungspflicht Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Abs. 2 AMG 68. Sitzung am 27.02.2012 Indikation Zur Prävention
Duraphat Fluorid 5 mg/g Zahnpaste Antrag auf Entlassung aus der Verschreibungspflicht Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Abs. 2 AMG 68. Sitzung am 27.02.2012 Indikation Zur Prävention
Bezeichnung Darreichungsform Stärken Zieltierarten Häufigkeit und Art der Anwendung. Clavulanic acid 10 mg. Clavulanic acid 10 mg
 Anhang I Liste der Bezeichnungen, der Darreichungsform, der Stärke des Tierarzneimittels, der Zieltierarten, der Art der Anwendung sowie des Antragsstellers/Inhabers der Genehmigung für das Inverkehrbringen
Anhang I Liste der Bezeichnungen, der Darreichungsform, der Stärke des Tierarzneimittels, der Zieltierarten, der Art der Anwendung sowie des Antragsstellers/Inhabers der Genehmigung für das Inverkehrbringen
auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Siehe Abschnitt 4.
 Seite 4 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Folsäure Heumann 5 mg Tabletten Folsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Seite 4 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Folsäure Heumann 5 mg Tabletten Folsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Wirkstoff: Natriumchondroitinsulfat
 Gebrauchsinformation: Information für Anwender CONDROSULF 800 mg - Tabletten Wirkstoff: Natriumchondroitinsulfat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender CONDROSULF 800 mg - Tabletten Wirkstoff: Natriumchondroitinsulfat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Heiserkeit und Reizhusten Phosphorus D4/D6/D12
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Heiserkeit und Reizhusten Phosphorus D4/D6/D12 Wirkstoff: Phosphorus D4/D6/D12 Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Heiserkeit und Reizhusten Phosphorus D4/D6/D12 Wirkstoff: Phosphorus D4/D6/D12 Lesen Sie die gesamte Packungsbeilage sorgfältig
Wissenschaftliche Dienste. Sachstand. Einzelfragen zur Impfung gegen Hepatitis B Deutscher Bundestag WD /16
 Einzelfragen zur Impfung gegen Hepatitis B 2016 Deutscher Bundestag Seite 2 Einzelfragen zur Impfung gegen Hepatitis B Aktenzeichen: Abschluss der Arbeit: 18.5.2016 Fachbereich: WD 9: Gesundheit, Familie,
Einzelfragen zur Impfung gegen Hepatitis B 2016 Deutscher Bundestag Seite 2 Einzelfragen zur Impfung gegen Hepatitis B Aktenzeichen: Abschluss der Arbeit: 18.5.2016 Fachbereich: WD 9: Gesundheit, Familie,
Gebrauchsinformation: Information für Patienten. Pronerv-Kapseln
 Gebrauchsinformation: Information für Patienten Pronerv-Kapseln Wirkstoffe: Thiaminmononitrat (Vitamin B 1 ), Pyridoxinhydrochlorid (Vitamin B 6 ) und Cyanocobalamin (Vitamin B 12 ) Lesen Sie die gesamte
Gebrauchsinformation: Information für Patienten Pronerv-Kapseln Wirkstoffe: Thiaminmononitrat (Vitamin B 1 ), Pyridoxinhydrochlorid (Vitamin B 6 ) und Cyanocobalamin (Vitamin B 12 ) Lesen Sie die gesamte
1. WAS IST DAFALGAN Zäpfchen UND WOFÜR WIRD ES ANGEWENDET?
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DAFALGAN Säuglinge 80 mg Zäpfchen DAFALGAN Kleinkinder 150 mg Zäpfchen DAFALGAN große Kinder 300 mg Zäpfchen Paracetamol Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DAFALGAN Säuglinge 80 mg Zäpfchen DAFALGAN Kleinkinder 150 mg Zäpfchen DAFALGAN große Kinder 300 mg Zäpfchen Paracetamol Lesen Sie die gesamte Packungsbeilage
Endfassung vom. 13. März 2006
 DFG - Senatskommission zur Beurteilung der gesundheitlichen Unbedenklichkeit von Lebensmitteln Prof. Dr. G. Eisenbrand - Vorsitzender SKLM Natürliche Lebensmittel-Inhaltsstoffe: Beurteilung der Toxizität
DFG - Senatskommission zur Beurteilung der gesundheitlichen Unbedenklichkeit von Lebensmitteln Prof. Dr. G. Eisenbrand - Vorsitzender SKLM Natürliche Lebensmittel-Inhaltsstoffe: Beurteilung der Toxizität
1. Was sind Dorithricin Halstabletten und wofür werden sie angewendet?
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Dorithricin - Halstabletten Wirkstoffe: Tyrothricin, Benzalkoniumchlorid, Benzocain Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Dorithricin - Halstabletten Wirkstoffe: Tyrothricin, Benzalkoniumchlorid, Benzocain Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
Gebrauchsinformation: Information für Patienten
 1/5 Gebrauchsinformation: Information für Patienten Tropfen gegen starkes Schwitzen Similasan Wirkstoffe: Aristolochia clematitis D12, Salvia officinalis D10, Sambucus nigra D6 Lesen Sie die gesamte Packungsbeilage
1/5 Gebrauchsinformation: Information für Patienten Tropfen gegen starkes Schwitzen Similasan Wirkstoffe: Aristolochia clematitis D12, Salvia officinalis D10, Sambucus nigra D6 Lesen Sie die gesamte Packungsbeilage
Mydocalm Filmtablette mit 50 mg Tolperisonhydrochlorid
 Gebrauchsinformation: Information für den Anwender Mydocalm Filmtablette mit 50 mg Tolperisonhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für den Anwender Mydocalm Filmtablette mit 50 mg Tolperisonhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Ödeme, Hypertonie und Herzinsuffizienz wurden im Zusammenhang mit NSAID - Behandlung berichtet.
 Alle rezeptpflichtigen nicht-selektiven NSAIDs zur systemischen Anwendung Für alle Präparate ohne fixes Dosierungsschema: 4.2. Dosierung, Art und Dauer der Anwendung 4.3. Gegenanzeigen Schwere Herzinsuffizienz
Alle rezeptpflichtigen nicht-selektiven NSAIDs zur systemischen Anwendung Für alle Präparate ohne fixes Dosierungsschema: 4.2. Dosierung, Art und Dauer der Anwendung 4.3. Gegenanzeigen Schwere Herzinsuffizienz
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei akuten Hals- und Rachenschmerzen Belladonna D4/D6/D12
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei akuten Hals- und Rachenschmerzen Belladonna D4/D6/D12 Wirkstoff: Atropa bella-donna D4/D6/D12 Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei akuten Hals- und Rachenschmerzen Belladonna D4/D6/D12 Wirkstoff: Atropa bella-donna D4/D6/D12 Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Patienten. Omega-3-Säurenethylester 90
 Gebrauchsinformation: Information für Patienten omega-3 biomo 1000 mg Weichkapseln Omega-3-Säurenethylester 90 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten omega-3 biomo 1000 mg Weichkapseln Omega-3-Säurenethylester 90 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Leitfaden zur Definition des Generikaabschlages nach 130a Abs. 3b SGB V
 Leitfaden zur Definition des Generikaabschlages nach 130a Abs. 3b SGB V Anknüpfend an die im Bundesgesundheitsministerium getroffenen Absprachen zur Anwendung des Generikaabschlages vom 6. März 2006 haben
Leitfaden zur Definition des Generikaabschlages nach 130a Abs. 3b SGB V Anknüpfend an die im Bundesgesundheitsministerium getroffenen Absprachen zur Anwendung des Generikaabschlages vom 6. März 2006 haben
Gebrauchsinformation: Information für Patienten. Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench)
 Gebrauchsinformation: Information für Patienten Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench) Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Patienten Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench) Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Anwender. Azyter 15 mg/g Augentropfen im Einzeldosisbehältnis Azithromycin 2 H 2 O
 Gebrauchsinformation: Information für Anwender Azyter 15 mg/g Augentropfen im Einzeldosisbehältnis Azithromycin 2 H 2 O Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Gebrauchsinformation: Information für Anwender Azyter 15 mg/g Augentropfen im Einzeldosisbehältnis Azithromycin 2 H 2 O Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Dopaminerge Substanzen und Impulskontrollstörungen
 - 2 - Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn Pharmazeutische Unternehmer (s. Anlage) Nachrichtlich: Stufenplanbeteiligte Postanschrift: Kurt-Georg-Kiesinger-Allee
- 2 - Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn Pharmazeutische Unternehmer (s. Anlage) Nachrichtlich: Stufenplanbeteiligte Postanschrift: Kurt-Georg-Kiesinger-Allee
De-ursil - De-ursil RR - De-ursil RR mite
 Bern, 23.10.2015 Information für Patientinnen und Patienten Lesen Sie diese Packungsbeilage sorgfältig, bevor Sie das Arzneimittel einnehmen bzw. anwenden. Dieses Arzneimittel ist Ihnen persönlich verschrieben
Bern, 23.10.2015 Information für Patientinnen und Patienten Lesen Sie diese Packungsbeilage sorgfältig, bevor Sie das Arzneimittel einnehmen bzw. anwenden. Dieses Arzneimittel ist Ihnen persönlich verschrieben
Der Bundesrat hat ferner die aus der Anlage ersichtliche Entschließung gefasst.
 Bundesrat Drucksache 169/14 (Beschluss) 23.05.14 Beschluss des Bundesrates Verordnung zur Umsetzung der Regelungen der Europäischen Union über die Anerkennung von in anderen Mitgliedstaaten ausgestellten
Bundesrat Drucksache 169/14 (Beschluss) 23.05.14 Beschluss des Bundesrates Verordnung zur Umsetzung der Regelungen der Europäischen Union über die Anerkennung von in anderen Mitgliedstaaten ausgestellten
Gebrauchsinformation: Information für den Anwender
 Gebrauchsinformation: Information für den Anwender Microlax Rektallösung Natriumcitrat 450 mg/5 ml Dodecyl(sulfoacetat), Natriumsalz 70 % 64,5 mg/5 ml Sorbitol-Lösung 70 % (kristallisierend) (Ph.Eur.)
Gebrauchsinformation: Information für den Anwender Microlax Rektallösung Natriumcitrat 450 mg/5 ml Dodecyl(sulfoacetat), Natriumsalz 70 % 64,5 mg/5 ml Sorbitol-Lösung 70 % (kristallisierend) (Ph.Eur.)
MEDIKAMENTE, DIE MYCOPHENOLAT ENTHALTEN Informationsbroschüre für Patienten. Informationen über die Risiken für den Fötus
 Die Gesundheitsbehörden der Europäischen Union haben für Medikamente mit dem Wirkstoff Mycophenolat eine bedingte Zulassung erteilt. Diese Informationsbroschüre ist Teil des verbindlichen Plans zur Risikominimierung
Die Gesundheitsbehörden der Europäischen Union haben für Medikamente mit dem Wirkstoff Mycophenolat eine bedingte Zulassung erteilt. Diese Informationsbroschüre ist Teil des verbindlichen Plans zur Risikominimierung
(1) Die Regelungen der 23 bis 33 über den SE-Betriebsrat kraft Gesetzes finden ab dem Zeitpunkt der Eintragung der SE Anwendung, wenn
 TK Lexikon Arbeitsrecht SE-Beteiligungsgesetz 22-33 Abschnitt 1 SE Betriebsrat kraft Gesetzes HI1311026 22-26 Unterabschnitt 1 Bildung und Geschäftsführung HI1311027 22 Voraussetzung HI1311028 (1) Die
TK Lexikon Arbeitsrecht SE-Beteiligungsgesetz 22-33 Abschnitt 1 SE Betriebsrat kraft Gesetzes HI1311026 22-26 Unterabschnitt 1 Bildung und Geschäftsführung HI1311027 22 Voraussetzung HI1311028 (1) Die
DAFALGAN ODIS darf nur Erwachsenen verabreicht werden.
 PACKUNGSBEILAGE: GEBRAUCHSINFORMATIONEN DAFALGAN ODIS 500 mg, Schmelztabletten Paracetamol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses
PACKUNGSBEILAGE: GEBRAUCHSINFORMATIONEN DAFALGAN ODIS 500 mg, Schmelztabletten Paracetamol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses
Gebrauchsinformation: Information für Patienten
 Gebrauchsinformation: Information für Patienten Esberitox -Tabletten Trockenextrakt aus einer Mischung von Lebensbaumspitzen und -blättern, Purpursonnenhutwurzel, Blassfarbener Sonnenhutwurzel und Färberhülsenwurzel
Gebrauchsinformation: Information für Patienten Esberitox -Tabletten Trockenextrakt aus einer Mischung von Lebensbaumspitzen und -blättern, Purpursonnenhutwurzel, Blassfarbener Sonnenhutwurzel und Färberhülsenwurzel
Kriterien zur Unterscheidung von AM/ NEM und bilanzierten Diäten
 Rechtliche Einteilung Arzneimittel Nahrungsergänzungsmittel Ergänzende bilanzierte Diät Gesetz AMG NemV und LFGB DiätV und LFGB Zweck Vorbeugung, Linderung und Heilung von Krankheiten oder Beeinflussung
Rechtliche Einteilung Arzneimittel Nahrungsergänzungsmittel Ergänzende bilanzierte Diät Gesetz AMG NemV und LFGB DiätV und LFGB Zweck Vorbeugung, Linderung und Heilung von Krankheiten oder Beeinflussung
Dopaminerge Substanzen und Impulskontrollstörungen
 - 2 - Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn Pharmazeutische Unternehmer (s. Anlage) Nachrichtlich: Stufenplanbeteiligte Postanschrift: Kurt-Georg-Kiesinger-Allee
- 2 - Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn Pharmazeutische Unternehmer (s. Anlage) Nachrichtlich: Stufenplanbeteiligte Postanschrift: Kurt-Georg-Kiesinger-Allee
Behandlung von Migräne-Anfällen (insbesondere sehr lange Anfälle), wenn andere Therapien nicht wirksam oder nicht indiziert sind.
 Gebrauchsinformation: Information für Patienten Ergo-Kranit Migräne 2 mg Tabletten Wirkstoff: Ergotamintartrat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten Ergo-Kranit Migräne 2 mg Tabletten Wirkstoff: Ergotamintartrat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. AERIUS 5 mg Schmelztabletten Desloratadin
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Schmelztabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Schmelztabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Wechselwirkungen der Medikamente
 Wechselwirkungen der Medikamente 9. Bayerischer Selbsthilfekongress in Landshut am 25. Oktober 2013 Sonja Stipanitz, Landesbeauftragte für Selbsthilfegruppen Gliederung Was ist eine Wechselwirkung? Welche
Wechselwirkungen der Medikamente 9. Bayerischer Selbsthilfekongress in Landshut am 25. Oktober 2013 Sonja Stipanitz, Landesbeauftragte für Selbsthilfegruppen Gliederung Was ist eine Wechselwirkung? Welche
Sjögren- Betroffene Fragen - Experten Antworten. Die OTC- Liste. (Im Internet einzusehen unter: : www.g-ba.de)
 Sjögren- Betroffene Fragen - Experten Antworten Die OTC- Liste (Im Internet einzusehen unter: : www.g-ba.de) Allgemeine Informationen zur OTC- Liste Die Abkürzung OTC kommt aus dem Englischen und bedeutet:
Sjögren- Betroffene Fragen - Experten Antworten Die OTC- Liste (Im Internet einzusehen unter: : www.g-ba.de) Allgemeine Informationen zur OTC- Liste Die Abkürzung OTC kommt aus dem Englischen und bedeutet:
AZ V /
 Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn An pharmazeutische Unternehmer nachrichtlich: Stufenplanbeteiligte Postanschrift: Kurt-Georg-Kiesinger-Allee
Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn An pharmazeutische Unternehmer nachrichtlich: Stufenplanbeteiligte Postanschrift: Kurt-Georg-Kiesinger-Allee
Gebrauchsinformation: Information für Anwender. Cevitol 500 mg-kautabletten Wirkstoff: Ascorbinsäure (Vitamin C)
 Gebrauchsinformation: Information für Anwender Cevitol 500 mg-kautabletten Wirkstoff: Ascorbinsäure (Vitamin C) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender Cevitol 500 mg-kautabletten Wirkstoff: Ascorbinsäure (Vitamin C) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender. DAFALGAN CODEINE 500mg/30mg, Brausetabletten DAFALGAN CODEINE 500mg/30mg Filmtabletten
 Gebrauchsinformation: Information für Anwender DAFALGAN CODEINE 500mg/30mg, Brausetabletten DAFALGAN CODEINE 500mg/30mg Filmtabletten Paracetamol, halb entwässertes Codeinphosphat Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender DAFALGAN CODEINE 500mg/30mg, Brausetabletten DAFALGAN CODEINE 500mg/30mg Filmtabletten Paracetamol, halb entwässertes Codeinphosphat Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Aspirine 500 Brause, 500 mg, Brausetabletten Acetylsalicylsäure
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Aspirine 500 Brause, 500 mg, Brausetabletten Acetylsalicylsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Aspirine 500 Brause, 500 mg, Brausetabletten Acetylsalicylsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten. Allernon 10 mg-tabletten Wirkstoff: Loratadin
 Gebrauchsinformation: Information für Patienten Allernon 10 mg-tabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Patienten Allernon 10 mg-tabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER SINUTAB 500/30 mg Tabletten SINUTAB FORTE 500/60 mg Tabletten Paracetamol und Pseudoephedrinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER SINUTAB 500/30 mg Tabletten SINUTAB FORTE 500/60 mg Tabletten Paracetamol und Pseudoephedrinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender. Azyter 15 mg/g Augentropfen im Einzeldosisbehältnis Azithromycin 2 H 2 O
 Gebrauchsinformation: Information für Anwender Azyter 15 mg/g Augentropfen im Einzeldosisbehältnis Azithromycin 2 H 2 O Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Gebrauchsinformation: Information für Anwender Azyter 15 mg/g Augentropfen im Einzeldosisbehältnis Azithromycin 2 H 2 O Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Dokumentationshilfe Einzelhändler - Arzneimittelrecht
 Dokumentationshilfe Einzelhändler - Arzneimittelrecht Besichtigung des Bestandes an Arzneimitteln Fertigarzneimittel Der Einzelhändler bringt nur freiverkäufliche Arzneimittel in den Verkehr ( 43 Abs.
Dokumentationshilfe Einzelhändler - Arzneimittelrecht Besichtigung des Bestandes an Arzneimitteln Fertigarzneimittel Der Einzelhändler bringt nur freiverkäufliche Arzneimittel in den Verkehr ( 43 Abs.
Antwort. Drucksache 13/3282. Deutscher Bundestag 13. Wahlperiode. der Bundesregierung
 Deutscher Bundestag 13. Wahlperiode Drucksache 13/3282 07.12. 95 Antwort der Bundesregierung auf die Kleine Anfrage der Abgeordneten Dr. Barbara Höll und der Gruppe der PDS Drucksache 13/3021 Medizinischer
Deutscher Bundestag 13. Wahlperiode Drucksache 13/3282 07.12. 95 Antwort der Bundesregierung auf die Kleine Anfrage der Abgeordneten Dr. Barbara Höll und der Gruppe der PDS Drucksache 13/3021 Medizinischer
FAKTEN. Migräne. von Stefan Evers. 1. Auflage. Thieme Verlag C.H. Beck im Internet: ISBN
 FAKTEN. Migräne von Stefan Evers 1. Auflage Thieme 2006 Verlag C.H. Beck im Internet: www.beck.de ISBN 78 3 13 143631 3 schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG 78 7 Besondere
FAKTEN. Migräne von Stefan Evers 1. Auflage Thieme 2006 Verlag C.H. Beck im Internet: www.beck.de ISBN 78 3 13 143631 3 schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG 78 7 Besondere
Gesundheitstipps Fit bleiben 50plus
 Gesundheitstipps Fit bleiben 50plus Vom richtigen Umgang mit Medikamenten Gut informiert in die zweite Lebenshälfte Wenn Sie heute um die 50 Jahre alt sind, haben Sie weitere drei oder vier Lebensjahrzehnte
Gesundheitstipps Fit bleiben 50plus Vom richtigen Umgang mit Medikamenten Gut informiert in die zweite Lebenshälfte Wenn Sie heute um die 50 Jahre alt sind, haben Sie weitere drei oder vier Lebensjahrzehnte
Gebrauchsinformation: Information für Anwender. Euphrasia D3 Augentropfen Weleda
 1/5 Gebrauchsinformation: Information für Anwender Euphrasia D3 Augentropfen Weleda Wirkstoff: Euphrasia officinalis D3 Dilution Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
1/5 Gebrauchsinformation: Information für Anwender Euphrasia D3 Augentropfen Weleda Wirkstoff: Euphrasia officinalis D3 Dilution Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Niederschrift. 12. öffentliche Sitzung des Beirates für Menschen mit Behinderungen der Stadt Bad Oldesloe
 Beirat für Menschen mit Behinderungen der Stadt Bad Oldesloe Niederschrift 12. öffentliche Sitzung des Beirates für Menschen mit Behinderungen der Stadt Bad Oldesloe Ort: Bürgerhaus, Raum E1, Mühlenstraße
Beirat für Menschen mit Behinderungen der Stadt Bad Oldesloe Niederschrift 12. öffentliche Sitzung des Beirates für Menschen mit Behinderungen der Stadt Bad Oldesloe Ort: Bürgerhaus, Raum E1, Mühlenstraße
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Methylprednisolonaceponat
 1 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Advantan - dermatologische Lösung Methylprednisolonaceponat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
1 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Advantan - dermatologische Lösung Methylprednisolonaceponat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Neu! VITALISIERENDER HAAR & NAGEL KOMPLEX. Für den Aufbau und das gesunde Wachstum von Haaren und Nägeln.
 Neu! VITALISIERENDER HAAR & NAGEL KOMPLEX Für den Aufbau und das gesunde Wachstum von Haaren und Nägeln. DAS FLÜSSIGE BIO-H-TIN FÜr JEDEN TAG. Neu Das Nahrungsergänzungsmittel für den Aufbau und das gesunde
Neu! VITALISIERENDER HAAR & NAGEL KOMPLEX Für den Aufbau und das gesunde Wachstum von Haaren und Nägeln. DAS FLÜSSIGE BIO-H-TIN FÜr JEDEN TAG. Neu Das Nahrungsergänzungsmittel für den Aufbau und das gesunde
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. ALLEGRATAB 120 mg Filmtabletten Fexofenadinhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ALLEGRATAB 120 mg Filmtabletten Fexofenadinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ALLEGRATAB 120 mg Filmtabletten Fexofenadinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
GlaxoSmithKline Consumer Healthcare GmbH & Co. KG, 77815 Bühl
 SEITE 11 Tipps zur Vorbeugung: Lernen Sie Ihre Auslöser kennen Notieren Sie in Ihrem Migräne-Tagebuch die Auslöser der Migräne. So erkennen Sie, worauf Sie achten sollten. Ganz gleich, ob es sich um bestimmte
SEITE 11 Tipps zur Vorbeugung: Lernen Sie Ihre Auslöser kennen Notieren Sie in Ihrem Migräne-Tagebuch die Auslöser der Migräne. So erkennen Sie, worauf Sie achten sollten. Ganz gleich, ob es sich um bestimmte
Faltschachtel. Unverkäufliches Muster (Eindruck auf Linie) Teil einer Klinikpackung, Einzelverkauf unzulässig (Eindruck auf Linie)
 Packmittelmanuskript Nr. 64000/009/94/6 Seite 2 Faltschachtel HEUMANN PHARMA GmbH & Co. Generica KG Südwestpark 50 90449 Nürnberg Urso 400 Heumann Filmtabletten mit 400 mg Ursodeoxycholsäure Zur Auflösung
Packmittelmanuskript Nr. 64000/009/94/6 Seite 2 Faltschachtel HEUMANN PHARMA GmbH & Co. Generica KG Südwestpark 50 90449 Nürnberg Urso 400 Heumann Filmtabletten mit 400 mg Ursodeoxycholsäure Zur Auflösung
Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG)
 Gesetzliche Regelungen für Arzneimittel Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG) 1 Zweck des Gesetzes Es ist der Zweck dieses Gesetzes, im Interesse einer ordnungsgemäßen Arzneimittelversorgung
Gesetzliche Regelungen für Arzneimittel Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG) 1 Zweck des Gesetzes Es ist der Zweck dieses Gesetzes, im Interesse einer ordnungsgemäßen Arzneimittelversorgung
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Clarityn 10 mg - Brausetabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Clarityn 10 mg - Brausetabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
Häufig gestellte Fragen zu Rabattverträgen
 Häufig gestellte Fragen zu Rabattverträgen Teil I (zu den Verträgen selbst) Was sind Rabattverträge? Es handelt sich um Verträge, die zwischen Krankenkassen und pharmazeutischen Herstellern geschlossen
Häufig gestellte Fragen zu Rabattverträgen Teil I (zu den Verträgen selbst) Was sind Rabattverträge? Es handelt sich um Verträge, die zwischen Krankenkassen und pharmazeutischen Herstellern geschlossen
Gebrauchsinformation: Information für Anwender. APOZEMA Blutarmut China complex Nr.38-Tropfen
 Gebrauchsinformation: Information für Anwender APOZEMA Blutarmut China complex Nr.38-Tropfen Wirkstoffe: China Dil. D5, Arsenicum album Dil. D6, Chininum arsenicosum Dil D6 und Pulsatilla Dil. D4 Lesen
Gebrauchsinformation: Information für Anwender APOZEMA Blutarmut China complex Nr.38-Tropfen Wirkstoffe: China Dil. D5, Arsenicum album Dil. D6, Chininum arsenicosum Dil D6 und Pulsatilla Dil. D4 Lesen
Gebrauchsinformation: Information für den Anwender. APOZEMA Bluthochdruck Crataegus complex Nr.10-Tropfen
 Gebrauchsinformation: Information für den Anwender APOZEMA Bluthochdruck Crataegus complex Nr.10-Tropfen Wirkstoffe: Crataegus Dil. D4, Arnica Dil. D4, Aurum chloratum natronatum Dil. D5, Barium jodatum
Gebrauchsinformation: Information für den Anwender APOZEMA Bluthochdruck Crataegus complex Nr.10-Tropfen Wirkstoffe: Crataegus Dil. D4, Arnica Dil. D4, Aurum chloratum natronatum Dil. D5, Barium jodatum
Fragebogen Weisse Liste-Ärzte
 www.weisse-liste.de Fragebogen Weisse Liste-Ärzte Der Fragebogen ist Teil des Projekts Weisse Liste-Ärzte. DIMENSION: Praxis & Personal voll eher zu eher 1. Das Praxispersonal vermittelt mir das Gefühl,
www.weisse-liste.de Fragebogen Weisse Liste-Ärzte Der Fragebogen ist Teil des Projekts Weisse Liste-Ärzte. DIMENSION: Praxis & Personal voll eher zu eher 1. Das Praxispersonal vermittelt mir das Gefühl,
Produkttexte für Ihre Endverbraucherwerbung
 Produkttexte für Ihre Endverbraucherwerbung Sehr geehrte Damen und Herren, nachfolgend stellen wir Ihnen inhaltlich und rechtlich korrekte Texte für Ihre Endverbraucherwerbung, einschließlich der Pflichtangaben
Produkttexte für Ihre Endverbraucherwerbung Sehr geehrte Damen und Herren, nachfolgend stellen wir Ihnen inhaltlich und rechtlich korrekte Texte für Ihre Endverbraucherwerbung, einschließlich der Pflichtangaben
Gebrauchsinformation: Information für Patienten
 Gebrauchsinformation: Information für Patienten AFLUBIN -Grippetabletten Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn sie enthält
Gebrauchsinformation: Information für Patienten AFLUBIN -Grippetabletten Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn sie enthält
Gebrauchsinformation: Information für den Anwender
 Wortlaut der für die Gebrauchsinformation vorgesehenen Angaben Stand: Mai 2008 1 Gebrauchsinformation: Information für den Anwender Harntee-Steiner, Teeaufgusspulver Zur Anwendung bei Heranwachsenden ab
Wortlaut der für die Gebrauchsinformation vorgesehenen Angaben Stand: Mai 2008 1 Gebrauchsinformation: Information für den Anwender Harntee-Steiner, Teeaufgusspulver Zur Anwendung bei Heranwachsenden ab
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Tannalbin-Tabletten
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Tannalbin-Tabletten Tanninalbuminat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Tannalbin-Tabletten Tanninalbuminat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel
Atronase 0,3 mg/ml Nasenspray, Lösung (Ipratropiumbromid)
 GEBRAUCHSINFORMATION ATRONASE 0,3 MG/ML NASENSPRAY, LÖSUNG Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
GEBRAUCHSINFORMATION ATRONASE 0,3 MG/ML NASENSPRAY, LÖSUNG Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
Gesetz zur Änderung von bau- und enteignungsrechtlichen Vorschriften sowie der Baumschutzverordnung
 BREMISCHE BÜRGERSCHAFT Drucksache 18/1355 Landtag 18. Wahlperiode 22.04.2014 Mitteilung des Senats vom 22. April 2014 Gesetz zur Änderung von bau- und enteignungsrechtlichen Vorschriften sowie der Baumschutzverordnung
BREMISCHE BÜRGERSCHAFT Drucksache 18/1355 Landtag 18. Wahlperiode 22.04.2014 Mitteilung des Senats vom 22. April 2014 Gesetz zur Änderung von bau- und enteignungsrechtlichen Vorschriften sowie der Baumschutzverordnung
GEBRAUCHSINFORMATION Eurican SHPPi2L Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Hunde
 GEBRAUCHSINFORMATION Eurican SHPPi2L Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Hunde 1. NAME UND ANSCHRIFT DES PHARMAZEUTISCHEN UNTERNEHMERS UND, WENN UNTERSCHIEDLICH,
GEBRAUCHSINFORMATION Eurican SHPPi2L Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Hunde 1. NAME UND ANSCHRIFT DES PHARMAZEUTISCHEN UNTERNEHMERS UND, WENN UNTERSCHIEDLICH,
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic )
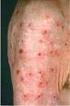 Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Levocetirizin Genericon 5 mg Filmtabletten. Levocetirizindihydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Levocetirizin Genericon 5 mg Filmtabletten Levocetirizindihydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Levocetirizin Genericon 5 mg Filmtabletten Levocetirizindihydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme
was ist das? Reizdarmsyndrom
 1 was ist das? 2 Was ist das? Der Begriff bezeichnet im weitesten Sinne das Zusammentreffen einer Vielzahl von unterschiedlichen Symptomen, die bei den Betroffenen auftreten. Ihr Arzt fasst diese Symptome
1 was ist das? 2 Was ist das? Der Begriff bezeichnet im weitesten Sinne das Zusammentreffen einer Vielzahl von unterschiedlichen Symptomen, die bei den Betroffenen auftreten. Ihr Arzt fasst diese Symptome
PACKUNGBEILAGE: INFORMATIONEN FÜR DEN ANWENDER. Broncho-Pectoralis Carbocystein 250 mg/ 5 ml Sirup Carbocystein
 PACKUNGBEILAGE: INFORMATIONEN FÜR DEN ANWENDER Broncho-Pectoralis Carbocystein 250 mg/ 5 ml Sirup Carbocystein Lesen Sie sich die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
PACKUNGBEILAGE: INFORMATIONEN FÜR DEN ANWENDER Broncho-Pectoralis Carbocystein 250 mg/ 5 ml Sirup Carbocystein Lesen Sie sich die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
Produkttexte für Ihre Endverbraucherwerbung
 Produkttexte für Ihre Endverbraucherwerbung Sehr geehrte Damen und Herren, nachfolgend stellen wir Ihnen inhaltlich und rechtlich korrekte Texte für Ihre Endverbraucherwerbung, einschließlich der Pflichtangaben
Produkttexte für Ihre Endverbraucherwerbung Sehr geehrte Damen und Herren, nachfolgend stellen wir Ihnen inhaltlich und rechtlich korrekte Texte für Ihre Endverbraucherwerbung, einschließlich der Pflichtangaben
MediPreis Produktsteckbrief
 MediPreis Produktsteckbrief DOCPELIN NACHTSTERNE DOCPELIN Nachtsterne Filmtabletten Pelikan-Apotheke PZN: 04386054 Menge: 20 St Art: Filmtabletten Link: https://www.medipreis.de/04386054 Anwendungsgebiete
MediPreis Produktsteckbrief DOCPELIN NACHTSTERNE DOCPELIN Nachtsterne Filmtabletten Pelikan-Apotheke PZN: 04386054 Menge: 20 St Art: Filmtabletten Link: https://www.medipreis.de/04386054 Anwendungsgebiete
GEHT DA MEHR? Fragen und Antworten zum Thema Erektionsstörung
 GEHT DA MEHR? Fragen und Antworten zum Thema Erektionsstörung EREKTIONSSTÖRUNGEN Gute Nachrichten: Man(n) kann was tun! Wenn die Liebe auf kleiner Flamme brennt, kann dies eine vorübergehende Abkühlung
GEHT DA MEHR? Fragen und Antworten zum Thema Erektionsstörung EREKTIONSSTÖRUNGEN Gute Nachrichten: Man(n) kann was tun! Wenn die Liebe auf kleiner Flamme brennt, kann dies eine vorübergehende Abkühlung
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. PROGESTOGEL 1 % Gel. Progesteron
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER PROGESTOGEL 1 % Gel Progesteron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER PROGESTOGEL 1 % Gel Progesteron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
Supracyclin Patienteninformation genehmigt 22.8.11
 Information für Patienten und Patientinnen Lesen Sie diese Packungsbeilage sorgfältig, bevor Sie das Arzneimittel einnehmen. Dieses Arzneimittel ist Ihnen persönlich verschrieben worden, und Sie sollten
Information für Patienten und Patientinnen Lesen Sie diese Packungsbeilage sorgfältig, bevor Sie das Arzneimittel einnehmen. Dieses Arzneimittel ist Ihnen persönlich verschrieben worden, und Sie sollten
Gebrauchsinformation: Information für Patienten. Stärkungsmittel Similasan
 1/5 Gebrauchsinformation: Information für Patienten Stärkungsmittel Similasan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn sie
1/5 Gebrauchsinformation: Information für Patienten Stärkungsmittel Similasan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn sie
SOZIALKOMMISSION I, GESUNDHEITSWESEN
 SOZIALKOMMISSION I, GESUNDHEITSWESEN 07.03.2011 Stellungnahme der BAGFW zum Richtlinienentwurf der GEKO über die Anforderungen an die Qualifikation zur und die Inhalte der genetischen Beratung gemäß 23
SOZIALKOMMISSION I, GESUNDHEITSWESEN 07.03.2011 Stellungnahme der BAGFW zum Richtlinienentwurf der GEKO über die Anforderungen an die Qualifikation zur und die Inhalte der genetischen Beratung gemäß 23
Packungsbeilage GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung. Xylometazolinhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
BAnz AT 11.11.2014 B1. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Dosierung und Einnahmenempfehlung
 Dosierung und Einnahmenempfehlung Allgemeine Dosierung Bei der Dosierung von homöopathischen Arzneien sind mehrere wichtige Sachen zu beachten: Das Alter der zu behandelnden Person: Bei Erwachsenen und
Dosierung und Einnahmenempfehlung Allgemeine Dosierung Bei der Dosierung von homöopathischen Arzneien sind mehrere wichtige Sachen zu beachten: Das Alter der zu behandelnden Person: Bei Erwachsenen und
UND WOFÜR WIRD ES ANGEWENDET?
 Gebrauchsinformation: Information für den Anwender Quadronal comp. gegen Kopfschmerzen 400 mg Paracetamol und 50 mg Coffein, Tablette Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahren Wirkstoffe:
Gebrauchsinformation: Information für den Anwender Quadronal comp. gegen Kopfschmerzen 400 mg Paracetamol und 50 mg Coffein, Tablette Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahren Wirkstoffe:
