66. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom
|
|
|
- Swen Blau
- vor 7 Jahren
- Abrufe
Transkript
1 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 66. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom Tagungsort: Bundesinstitut für Arzneimittel und Medizinprodukte D Bonn, Kurt-Georg-Kiesinger-Allee 3 Teilnehmer: Der Vorsitzende Die Sachverständigen des Ausschusses für Verschreibungspflicht Vertreter des Bundesministeriums für Gesundheit (BMG) Vertreter des Bundesministeriums für Ernährung, Landwirtschaft und Verbraucherschutz (BMELV) Vertreter des Bundesamts für Verbraucherschutz und Lebensmittelsicherheit (BVL) Vertreter des BfArM Tagesordnung 1. Eröffnung der Sitzung 2. Annahme der Tagesordnung 3. Oxybuprocain Proxymetacain Auftrag zur Ergänzung der Liste der Stoffe und Zubereitungen nach 1 Nr.1 der Arzneimittelverschreibungsverordnung 4. Rizatriptan Antrag auf Entlassung aus der Verschreibungspflicht 5. Orlistat Streichung der Worte von der Europäischen Kommission zugelassene, nicht verschreibungspflichtige in der derzeitigen AMVV-Position: - ausgenommen von der Europäischen Kommission zugelassene, nicht - 1 -
2 verschreibungspflichtige Arzneimittel in einer Höchstdosis von 60 mg pro abgeteilter Form 6. Vitamin D (D3, Colecalciferol) Antrag zur Anhebung der unter die Verschreibungspflicht fallenden Tagesdosis von derzeit 1000 I.E. auf künftig 2000 I.E. 7. Linezolid Antrag auf Streichung der Einschränkung - zur Behandlung von Pneumonien oder schweren Haut- und Weichteilinfektionen, wenn diese durch grampositive Erreger verursacht sind 8. Lidocain Antrag auf Unterstellung unter die Verschreibungspflicht von Lidocain - zur Anwendung auf der Haut zur Linderung der Symptome von neuropathischen Schmerzen nach einer Herpes-Zoster-Infektion (Post-Zoster- Neuralgie) 9. Sammelposition Lokalanästhetika Auftrag zur Auflösung der Sammelposition und Aufnahme aller Lokalanästhetika aus der bisherigen Sammelposition als Einzelpositionen, Teil 2: Benzocain, Fomocain, Lidocain, Myrtecain, Prilocain, Procain und Quinisocain 10. Verschiedenes TOP 1 Eröffnung der Sitzung Der Vorsitzende begrüßt die Anwesenden. Er informiert darüber, dass er in seiner Funktion als neuer kommissarischer Leiter der Abteilung Pharmakovigilanz seit dem diese Sitzung leiten wird und stellt sich anschließend kurz vor. Danach richtet der frühere Leiter der Abteilung Pharmakovigilanz und Vorsitzende einige Grußworte an den Ausschuss und verabschiedet sich. Daraufhin bedanken sich verschiedene Ausschussmitglieder bei ihm für die gute und konstruktive Leitung der Sitzungen in den vergangenen Jahren. Nach ihrer Begrüßung durch den Vorsitzenden stellen sich die neu berufenen Mitglieder vor. Der Vorsitzende weist auf die prinzipielle Vertraulichkeit der Sitzungsinhalte (mit Ausnahme der Voten, die zu einer Änderung der AMVV führen) hin. Die im Internet publizierten Sitzungsprotokolle werden künftig keine Liste der Teilnehmer enthalten. Der Vorsitzende informiert, dass nach der Einleitung des BfArM zu TOP 4 ein externer Sachverständiger gehört wird. Da die Stellungnahmen des BfArM u.a. wettbewerbsrelevante Informationen enthalten und daher vertraulich sind, werden externe Sachverständige künftig nur für die Dauer ihrer Präsentation und die anschließenden Fragen der Sachverständigen an der Sitzung teilnehmen. Aus dem - 2 -
3 Kreis der Sachverständigen gibt es dazu die Ansicht, das es externen Sachverständigen erlaubt sein müsste, die Stellungnahme des BfArM selbst zu hören. Dazu stellt der Vorsitzende fest, dass nur für die Sachverständigen aufgrund ihres Amtes die Notwendigkeit besteht, alle Informationen aus erster Hand zu erhalten und dass sie die Möglichkeit haben, die Meinung des externen Sachverständigen zu bestimmten Sachfragen und der vom BfArM vorgebrachten Position in der Diskussion einzuholen. Andere Sachverständige stimmen dem zu und begrüßen diese strikte Trennung im Sinne einer ungestörten Sacharbeit. Ein Sachverständiger berichtet, dass auch die EMA in diesem Sinne aktuell ihre Vorgaben für den Umgang mit Interessenskonflikten überarbeitet. Auf Anregung aus dem Ausschuss hin werden externe Gutachter künftig um Abgabe einer Erklärung zu einem bestehenden Interessenskonflikt gebeten. Als Termine für die nächsten Sitzungen werden der und der vereinbart. TOP 2 Annahme der Tagesordnung TOP 7, Linezolid, wird vorgezogen. TOP 3 Oxybuprocain Proxymetacain Auftrag zur Ergänzung der Liste der Stoffe und Zubereitungen nach 1 Nr.1 der Arzneimittelverschreibungsverordnung Zu diesem Thema gibt es keinen Diskussionsbedarf. Abstimmungsergebnis: Der Antrag auf Aufnahme von Oxybuprocain und Proxymetacain in die Liste der Stoffe und Zubereitungen nach 1 Nr. 1 der Arzneimittelverschreibungsverordnung wird mehrheitlich angenommen. TOP 4 Rizatriptan Antrag auf Entlassung aus der Verschreibungspflicht Das BfArM führt in das Thema ein. Ein Sachverständiger bemängelt, dass in den Unterlagen Daten zu Dosis- Wirkungsbeziehungen fehlen sowie die Tatsache, dass der Switch für die höhere Stärke beantragt wird, während die niedrigere verschreibungspflichtig bleiben soll. So gäbe es in der Dokumentation des Antragstellers eine Tabelle (S.15), nach der 5 bzw. 10 mg Rizatriptan gleich wirksam sind. Außerdem sei in dieser Tabelle der Parameter Keine Unfähigkeit, anders als die übrigen Parameter (z. B. Linderung ), unverständlich. Nach Angaben aus dem Kreis der Sachverständigen sind Triptane nach den 2009 aktualisierten Leitlinien zur Migränebehandlung Mittel der ersten Wahl. Einige Sachverständige bezweifeln, dass der Übergebrauch bzw. der Missbrauch von Triptanen über Einzelfälle hinaus relevant ist und bitten das BfArM darum, - 3 -
4 entsprechende Belege dafür vorzulegen. Unabhängig von der Beantwortung dieser Frage kommen die Sachverständigen zu dem Schluss, dass die vorliegenden Daten eine abschließende Beurteilung des Sicherheitsprofils von Rizatriptan nicht erlauben. Ein anderer Sachverständiger erinnert daran, dass der externe Sachverständige die Freistellung von Naratriptan damals damit begründet hatte, es handele sich um das im Vergleich am schwächsten wirksame Triptan. Sollte es nicht wirksam genug sein, würde der Patient im 2. Schritt einen Arzt aufsuchen, der ihm dann eines der stärker wirksamen Triptane verordnen würde. Damit nicht immer wieder ein neues Triptan nachgeschoben würde, sei aus seiner Sicht daher eine vergleichende Beurteilung aller Triptane bezüglich Wirksamkeit und Nebenwirkungspotential erforderlich, bevor der Ausschuss eine Empfehlung bezüglich der Einstufung eines weiteren Triptans abgäbe. Ein Vertreter des BfArM verweist auf die Stellungnahme des BfArM, nach der speziell für Rizatriptan Dosisreduktionen erforderlich sind bei Störungen der Leber- und/oder Nierenfunktion sowie bei gleichzeitiger Einnahme von Propranolol. Kontraindikationen bestehen außerdem für Patienten mit einem unbehandelten leichten Bluthochdruck, der den Patienten häufig nicht bekannt ist. Aufgrund dieser viele Patienten betreffenden Risiken sieht ein Sachverständiger Rizatriptan als vergleichsweise ungeeignet für die Selbstmedikation. Die Sachverständigen bitten das BfArM darum, dem Ausschuss eine vergleichende Analyse aller Triptane vorzulegen. Mehrere Sachverständige bemängeln die sehr variable Argumentation zugunsten des gerade zur Freistellung anstehenden Triptans in den verschiedenen Gutachten des externen Sachverständigen. Der externe Sachverständige trägt aus seinem Gutachten vor und beantwortet anschließend Fragen der Sachverständigen. Aus seiner Sicht könnten alle Triptane zur oralen Anwendung aus der Verschreibungspflicht entlassen werden. Er bestätigt, dass bei einem Teil der Patienten ein Übergebrauch von Triptanen vorliegt. Nach Beantwortung aller an ihn gerichteten Fragen verlässt er den Sitzungsraum. Ein Sachverständiger stellt fest, dass die Aussage des externen Sachverständigen zur fehlenden Relevanz der Interaktion mit Propranolol der des Antragstellers in den eingereichten Unterlagen widerspricht. Er empfiehlt dem Antragsteller eine gründliche Überarbeitung seines Antrags sowie eine bessere Abstimmung mit seinem Gutachter. Ein Vertreter des BfArM informiert über Verfahrensfragen. Danach kann die Behandlung eines Antrags verschoben werden, wenn die Diskussion ergibt, dass dem Ausschuss für seine Empfehlung wesentliche Informationen (noch) nicht vorliegen. Ein externer Sachverständiger kann nicht nur durch den Antragsteller, sondern auch durch ein sachverständiges Mitglied des Ausschusses bzw. seinen Stellvertreter vorgeschlagen werden. Der Antragsteller wird gebeten, alle wesentlichen Aussagen des Antrags nachträglich durch Daten zu belegen und außerdem zu begründen, warum die niedrigere Stärke weiterhin der Verschreibungspflicht unterstehen soll. Weiterhin sollte er die Frage beantworten, welche klinisch relevanten Auswirkungen Leber- oder Niereninsuffizienz bzw. gleichzeitige Propranololanwendung haben, wenn der Patient ein- oder zweimal eine Tablette Rizatriptan einnimmt. Zusätzlich durch das BfArM zu klärende Fragen sind, wie viele Patienten mit Migräne - 4 -
5 Betablocker einnehmen, wie hoch der Prozentsatz von Menschen mit Leberund/oder Niereninsuffizienz ist und wie sich Unterschiede in der Verträglichkeit der Triptane bei Kindern und Jugendlichen bzw. älteren Patienten auswirken. Der Vorsitzende stellt fest, dass der Ausschuss sein Votum vertagt und dem BfArM den Auftrag zu einer vergleichenden Analyse aller Triptane erteilt. Das BfArM wird zudem um Beantwortung der bereits genannten Fragen einschließlich der Vorlage von Daten zu einem Übergebrauch von Triptanen gebeten. Ein Sachverständiger bittet darum, dem Antragsteller mitzuteilen, dass die Qualität des eingereichten Dossiers nicht den Anforderungen entspricht. Der Sachverständigenausschuss stimmt einstimmig dafür, die Behandlung des Antrags bis zur Vorlage der ergänzenden Unterlagen zu vertagen. TOP 5 Orlistat Streichung der Worte von der Europäischen Kommission zugelassene, nicht verschreibungspflichtige in der derzeitigen AMVV-Position: - ausgenommen von der Europäischen Kommission zugelassene, nicht verschreibungspflichtige Arzneimittel in einer Höchstdosis von 60 mg pro abgeteilter Form - Der Vertreter des BMG erinnert daran, dass die EU-Kommission nach einer bereits im Februar 2009 publizierten Stellungnahme davon ausgeht, dass im Fall einer zentralen Zulassung für ein OTC-Arzneimittel auf nationaler Ebene keine davon abweichenden Regelungen getroffen werden. Nach kurzer Diskussion von Verständnisfragen erfolgt die Abstimmung. Abstimmungsergebnis: Die Änderung der bestehenden Position - ausgenommen von der Europäischen Kommission zugelassene, nicht verschreibungspflichtige Arzneimittel in einer Höchstdosis von 60 mg pro abgeteilter Form in - ausgenommen Arzneimittel zur oralen Anwendung, die in der EU zentral und verschreibungsfrei zugelassen wurden sowie Arzneimittel mit einer Höchstmenge von 60 mg pro abgeteilter Form und einer maximalen Tagesdosis von 180 mg - wird mehrheitlich angenommen. TOP 6 Vitamin D (D3, Colecalciferol) Antrag zur Anhebung der unter die Verschreibungspflicht fallenden Tagesdosis von derzeit 1000 I.E. auf künftig 2000 I.E. Das BfArM führt in das Thema ein. Im Rahmen der kurzen Diskussion erinnert ein Sachverständiger an das Beispiel des - 5 -
6 Beta-Karotins, zu dem vor Beginn der epidemiologischen Studien auch nur toxikologische Daten zur Kurzzeitanwendung vorlagen, wie dies aktuell auf Vitamin D zutrifft. Erst die Analyse von Daten aus der Langzeitanwendung zeigte die für Raucher erhöhte Sterblichkeit. Die Frage der Langzeitfolgen sei in den Antragsunterlagen nicht behandelt worden. Außerdem würden sich die im Dossier genannten Zahlen zur Höhe der Vitamin D-Zufuhr in der Nahrung in Abhängigkeit von der Aussage, die sie belegen sollen, stark unterscheiden. Die meisten Sachverständigen beziehen sich auf die fehlenden Daten zur Wirksamkeit und Sicherheit einer langfristig erhöhten Vitamin D-Zufuhr und sind der Ansicht, dass der Vitamin D-Mangel in bestimmten Bevölkerungsgruppen durch eine Anhebung des Grenzwerts nicht zu beeinflussen ist. Mit der Ablehnung des Antrages sei aber das Problem einer möglichen Mangelversorgung nicht gelöst. Ein Sachverständiger schlägt daher vor, die Supplementierung der Nahrung mit Vitamin D (analog zur Jodierung von Speisesalz) zu einem Anliegen der Gesundheitspolitik zu machen. Außerdem wird bemängelt, dass der Antrag gestellt wurde, ohne einen Bezug zu einer oder mehreren Indikationen herzustellen. Abstimmungsergebnis: Der Antrag auf Anhebung der unter die Verschreibungspflicht fallenden Tagesdosis von derzeit 1000 I.E. auf künftig 2000 I.E. wird mehrheitlich abgelehnt. TOP 7 Linezolid Antrag auf Streichung der Einschränkung - zur Behandlung von Pneumonien oder schweren Haut- und Weichteilinfektionen, wenn diese durch grampositive Erreger verursacht sind - Auf Anfrage bestätigt der Vertreter des BfArM, dass aktuell nur Arzneimittel zugelassen sind mit der zwischen den Spiegelstrichen genannten Indikation. Zu diesem Antrag besteht kein Diskussionsbedarf. Abstimmungsergebnis: Der Antrag auf Streichung der Einschränkung - zur Behandlung von Pneumonien oder schweren Haut- und Weichteilinfektionen, wenn diese durch grampositive Erreger verursacht sind - wird mehrheitlich angenommen. TOP 8 Lidocain Antrag auf Unterstellung unter die Verschreibungspflicht von Lidocain - zur Anwendung auf der Haut zur Linderung der Symptome von neuropathischen Schmerzen nach einer Herpes-Zoster-Infektion (Post-Zoster-Neuralgie) Nach Klärung einiger Fragen erfolgt die Abstimmung
7 Abstimmungsergebnis: Der Antrag auf Unterstellung unter die Verschreibungspflicht von Lidocain zur Anwendung auf der Haut zur Linderung der Symptome von neuropathischen Schmerzen nach einer Herpes-Zoster-Infektion (Post-Zoster-Neuralgie) wird mehrheitlich angenommen. TOP 9 Sammelposition Lokalanästhetika Auftrag zur Auflösung der Sammelposition und Aufnahme aller Lokalanästhetika aus der bisherigen Sammelposition als Einzelpositionen, Teil 2: Benzocain, Fomocain, Lidocain, Myrtecain, Prilocain, Procain und Quinisocain Zu diesem Punkt der Tagesordnung besteht kein Diskussionsbedarf. Die Ausnahme, die sich aus TOP 8 ergibt, wird bei Zustimmung des Verordnungsgebers durch diesen ergänzt. Die Sachverständigen stimmen einstimmig für die Auflösung der Sammelposition und Aufnahme der Einzelpositionen entsprechend der Stellungnahme des BfArM. Abstimmungsergebnis: Der Antrag auf Auflösung der Sammelposition Lokalanästhetika und die Aufnahme der folgenden Lokalanästhetika aus der bisherigen Sammelposition als Einzelpositionen Benzocain Fomocain Lidocain - ausgenommen zur parenteralen Anwendung ohne Zusatz weiterer arzneilich wirksamer Bestandteile in Konzentrationen bis zu 2 % zur intrakutanen Anwendung an der gesunden Haut - ausgenommen zur subkutanen und intramuskulären Infiltrationsanästhesie zur Durchführung von Dammschnitten und zur Naht von Dammschnitten und Dammrissen im Rahmen der Geburt in einer Konzentration bis 1 %, einer Einzeldosis von bis zu 10 ml und einer Menge von bis zu 10 ml je Ampulle zur Abgabe an Hebammen und Entbindungspfleger im Rahmen ihrer Berufsausübung - und am äußeren Gehörgang Myrtecain Prilocain - 7 -
8 Procain - ausgenommen zur parenteralen Anwendung ohne Zusatz weiterer arzneilich wirksamer Bestandteile in Konzentrationen bis zu 2 % zur intrakutanen Anwendung an der gesunden Haut Quinisocain in Anlage 1 der AMVV wird mehrheitlich angenommen. TOP 10 Verschiedenes Packungsgrößenbegrenzungen für Analgetika Auf Nachfrage informiert ein Vertreter des BfArM, dass die Stellungnahmen in Kürze finalisiert und an das BMG weitergeleitet werden. Termin der nächsten Sitzung: Dienstag, der Beginn: Uhr Sitzungsort: Bonn Kurt-Georg-Kiesinger-Allee 3 Der Vorsitzende dankt allen Anwesenden und Ausschussmitgliedern und schließt die Sitzung. Anlagen Anlage 1: Voten und Begründungen zu Positionen, deren Änderung zugestimmt wird (TOP 3, 5, 7, 8, 9) - 8 -
V o t en. Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG
 ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 66. Sitzung, 11.01.2011 zu Positionen, über deren Änderung abgestimmt
ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 66. Sitzung, 11.01.2011 zu Positionen, über deren Änderung abgestimmt
Ergebnisprotokoll. der 64. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht. am 12.
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 64. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 12. Januar 2010 UTagungsort:U
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 64. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 12. Januar 2010 UTagungsort:U
Procain zur Anwendung am äußeren Gehörgang
 Procain zur Anwendung am äußeren Gehörgang Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 Antrag Antrag auf
Procain zur Anwendung am äußeren Gehörgang Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 Antrag Antrag auf
Elfte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 Bundesrat Drucksache 329/11 26.05.11 Verordnung des Bundesministeriums für Gesundheit G Elfte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung A. Problem und Ziel Da Arzneimittel mit bestimmten
Bundesrat Drucksache 329/11 26.05.11 Verordnung des Bundesministeriums für Gesundheit G Elfte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung A. Problem und Ziel Da Arzneimittel mit bestimmten
Colecalciferol. Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017
 Colecalciferol Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Überprüfung der freigestellten Tagesdosis
Colecalciferol Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Überprüfung der freigestellten Tagesdosis
67. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 67. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom 05.07.2011 UTagungsort:U
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 67. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom 05.07.2011 UTagungsort:U
Ibuprofen zur trans-dermalen Anwendung als Pflaster
 Ibuprofen zur trans-dermalen Anwendung als Pflaster Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag
Ibuprofen zur trans-dermalen Anwendung als Pflaster Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag
TOP Nicotin. Anträge der Firma McNeil Consumer Healthcare GmbH auf Änderung der Verkaufsabgrenzung
 TOP 9 + 10 Nicotin Anträge der Firma McNeil Consumer Healthcare GmbH auf Änderung der Verkaufsabgrenzung Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Abs. 2 AMG 69. Sitzung 26.06.2012 Antrag
TOP 9 + 10 Nicotin Anträge der Firma McNeil Consumer Healthcare GmbH auf Änderung der Verkaufsabgrenzung Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Abs. 2 AMG 69. Sitzung 26.06.2012 Antrag
Bundesgesetzblatt Jahrgang 2005 Teil I Nr. 75, S. 3632, ausgegeben zu Bonn am
 Bundesgesetzblatt Jahrgang 2005 Teil I Nr. 75, S. 3632, ausgegeben zu Bonn am 28.12.2005 Verordnung zur Neuordnung der Verschreibungspflicht von Arzneimitteln Es verordnen Vom 21. Dezember 2005 - das Bundesministerium
Bundesgesetzblatt Jahrgang 2005 Teil I Nr. 75, S. 3632, ausgegeben zu Bonn am 28.12.2005 Verordnung zur Neuordnung der Verschreibungspflicht von Arzneimitteln Es verordnen Vom 21. Dezember 2005 - das Bundesministerium
Ergebnisprotokoll. der 57. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht. am 19.
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE 74 Ergebnisprotokoll der 57. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 19. Juni 2006 Tagungsort:
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE 74 Ergebnisprotokoll der 57. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 19. Juni 2006 Tagungsort:
Zubereitung aus Ibuprofen und Coffein
 Zubereitung aus Ibuprofen und Coffein Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag Kombination
Zubereitung aus Ibuprofen und Coffein Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag Kombination
Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 6 Racecadotril
 Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 6 Racecadotril Antrag auf Entlassung aus der Verschreibungspflicht Racecadotril bei Kindern ab 5 Jahren und Jugendlichen gemeinsam
Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 6 Racecadotril Antrag auf Entlassung aus der Verschreibungspflicht Racecadotril bei Kindern ab 5 Jahren und Jugendlichen gemeinsam
Beclometason, Fluticason, Mometason und ihre Ester
 Beclometason, Fluticason, Mometason und ihre Ester Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Seite 1 Hintergrund (I)
Beclometason, Fluticason, Mometason und ihre Ester Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Seite 1 Hintergrund (I)
V o t en. Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG
 ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 64. Sitzung, 12.01.2010 zu Positionen, deren Änderung abgestimmt
ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 64. Sitzung, 12.01.2010 zu Positionen, deren Änderung abgestimmt
Racecadotril. Entlassung aus der Verschreibungspflicht
 Racecadotril Entlassung aus der Verschreibungspflicht Tania Meier Sitzung des Sachverständigen-Ausschuss für Verschreibungspflicht Bonn, 27. Februar 2012 Anlass Antrag der Firma Boehringer Ingelheim GmbH
Racecadotril Entlassung aus der Verschreibungspflicht Tania Meier Sitzung des Sachverständigen-Ausschuss für Verschreibungspflicht Bonn, 27. Februar 2012 Anlass Antrag der Firma Boehringer Ingelheim GmbH
Zubereitung aus Ibuprofen und Coffein
 Zubereitung aus Ibuprofen und Coffein Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 Antrag Kombination aus
Zubereitung aus Ibuprofen und Coffein Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 Antrag Kombination aus
Parenteralia. Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017
 Parenteralia Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Hintergrund Diskussion auf der 76. Sitzung
Parenteralia Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Hintergrund Diskussion auf der 76. Sitzung
Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Absatz 2 des Arzneimittelgesetzes. Ergebnisprotokoll. 77. Sitzung
 Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Absatz 2 des Arzneimittelgesetzes Ergebnisprotokoll 77. Sitzung 17. Januar 2017 Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM),
Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Absatz 2 des Arzneimittelgesetzes Ergebnisprotokoll 77. Sitzung 17. Januar 2017 Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM),
75. Sitzung des Sachverständigen-Ausschusses für Verschreibungspflicht
 Ergebnisprotokoll 75. Sitzung des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 Absatz 2 AMG vom 19. Januar 2016 Sitzungsort Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM)
Ergebnisprotokoll 75. Sitzung des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 Absatz 2 AMG vom 19. Januar 2016 Sitzungsort Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM)
der 65. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 65. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 06.07.2010 Tagungsort:
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 65. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 06.07.2010 Tagungsort:
Thymian / Primel. Sachverständigen-Ausschuss für Apothekenpflicht 13. Juni Sachverständigen-Ausschuss für Apothekenpflicht 13.
 Thymian / Primel Sachverständigen-Ausschuss für Apothekenpflicht 13. Juni 2017 Sachverständigen-Ausschuss für Apothekenpflicht 13. Juni 2017 Seite 1 Antrag Thymiankraut und seine Zubereitungen, auch in
Thymian / Primel Sachverständigen-Ausschuss für Apothekenpflicht 13. Juni 2017 Sachverständigen-Ausschuss für Apothekenpflicht 13. Juni 2017 Seite 1 Antrag Thymiankraut und seine Zubereitungen, auch in
Ergebnisprotokoll. der 60. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht. am 15.
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 60. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 15. Januar 2008 Tagungsort:
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 60. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 15. Januar 2008 Tagungsort:
Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
Ergebnisprotokoll. der 56. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht. am 17.
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE 74 Ergebnisprotokoll der 56. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 17. Januar 2006 Tagungsort:
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE 74 Ergebnisprotokoll der 56. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 17. Januar 2006 Tagungsort:
Ergebnisprotokoll. der 61. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht. am 01.
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 61. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 01. Juli 2008 Tagungsort:
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 61. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 01. Juli 2008 Tagungsort:
Doxylamin zur Behandlung von Schlafstörungen bei Kindern
 Doxylamin zur Behandlung von Schlafstörungen bei Kindern Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 BfArM
Doxylamin zur Behandlung von Schlafstörungen bei Kindern Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 BfArM
70. Sitzung des gemäß 48 Abs. 2 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht nach 53 Abs. 2 AMG vom
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 70. Sitzung des gemäß 48 Abs. 2 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht nach 53 Abs. 2 AMG vom 25.06.2013
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 70. Sitzung des gemäß 48 Abs. 2 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht nach 53 Abs. 2 AMG vom 25.06.2013
(Text von Bedeutung für den EWR)
 30.12.2017 L 351/55 DURCHFÜHRUNGSVERORDNUNG (EU) 2017/2468 R KOMMISSION vom 20. Dezember 2017 zur Festlegung administrativer und wissenschaftlicher Anforderungen an traditionelle Lebensmittel aus Drittländern
30.12.2017 L 351/55 DURCHFÜHRUNGSVERORDNUNG (EU) 2017/2468 R KOMMISSION vom 20. Dezember 2017 zur Festlegung administrativer und wissenschaftlicher Anforderungen an traditionelle Lebensmittel aus Drittländern
Ergebnisprotokoll. der 58. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht. am 16.
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 58. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 16. Januar 2007 Tagungsort:
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 58. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 16. Januar 2007 Tagungsort:
V o t e n. Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG
 ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t e n des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 65. Sitzung, 06.07.2010 zu Positionen, deren Änderung abgestimmt
ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t e n des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 65. Sitzung, 06.07.2010 zu Positionen, deren Änderung abgestimmt
Ergebnisprotokoll. der 62. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht. am 13.
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 62. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für am 13. Januar 2009 Tagungsort: Bundesinstitut
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 62. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für am 13. Januar 2009 Tagungsort: Bundesinstitut
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen
 Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
V o t en. Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG
 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 59. Sitzung, 03.07.2007 zu Positionen, deren Änderung abgestimmt wurde.
Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 59. Sitzung, 03.07.2007 zu Positionen, deren Änderung abgestimmt wurde.
zu Punkt... der 916. Sitzung des Bundesrates am 8. November 2013
 Bundesrat Drucksache 705/1/13 24.10.13 E m p f e h l u n g e n der Ausschüsse G - AV zu Punkt.. der 916. Sitzung des Bundesrates am 8. November 2013 Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
Bundesrat Drucksache 705/1/13 24.10.13 E m p f e h l u n g e n der Ausschüsse G - AV zu Punkt.. der 916. Sitzung des Bundesrates am 8. November 2013 Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
Fachbereich 3 Umwelt, Sicherheit und Ordnung Lübeck,
 Fachbereich 3 Umwelt, Sicherheit und Ordnung Lübeck, 10.09.2007 NIEDERSCHRIFT öffentlicher Teil über die Sitzung des Ausschusses für Sicherheit und Ordnung und Polizeibeirat am Montag, 03.09.2007 um 16:00
Fachbereich 3 Umwelt, Sicherheit und Ordnung Lübeck, 10.09.2007 NIEDERSCHRIFT öffentlicher Teil über die Sitzung des Ausschusses für Sicherheit und Ordnung und Polizeibeirat am Montag, 03.09.2007 um 16:00
Protokoll der 13. Sitzung der Gemeinsamen Expertenkommission zur Einstufung von Stoffen am 16. Februar Stand
 Protokoll der 13. Sitzung der Gemeinsamen Expertenkommission zur Einstufung von Stoffen am 16. Februar 2017 1 Stand 21.06.2017 2 3 4 5 6 7 8 9 10 11 12 Ergebnisprotokoll zur 13. Sitzung der Gemeinsamen
Protokoll der 13. Sitzung der Gemeinsamen Expertenkommission zur Einstufung von Stoffen am 16. Februar 2017 1 Stand 21.06.2017 2 3 4 5 6 7 8 9 10 11 12 Ergebnisprotokoll zur 13. Sitzung der Gemeinsamen
Succimer. Sachverständigen-Ausschuss für Verschreibungspflicht 28. Juni 2016
 Succimer Sachverständigen-Ausschuss für Verschreibungspflicht 28. Juni 2016 Sachverständigen-Ausschuss für Verschreibungspflicht 28. Juni 2016 Seite 1 Hintergrund Nebenwirkungsmeldung zu einem anaphylaktischen
Succimer Sachverständigen-Ausschuss für Verschreibungspflicht 28. Juni 2016 Sachverständigen-Ausschuss für Verschreibungspflicht 28. Juni 2016 Seite 1 Hintergrund Nebenwirkungsmeldung zu einem anaphylaktischen
Verordnung zur Änderung der Arzneimittelverschreibungsverordnung und der Verordnung über apothekenpflichtige und freiverkäufliche Arzneimittel
 Bundesrat Drucksache 705/13 (Beschluss) 08.11.13 Beschluss des Bundesrates Verordnung zur Änderung der Arzneimittelverschreibungsverordnung und der Verordnung über apothekenpflichtige und freiverkäufliche
Bundesrat Drucksache 705/13 (Beschluss) 08.11.13 Beschluss des Bundesrates Verordnung zur Änderung der Arzneimittelverschreibungsverordnung und der Verordnung über apothekenpflichtige und freiverkäufliche
Ergebnisprotokoll. der 63. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht. am 30.
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 63. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 30. Juni 2009 Tagungsort:
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 63. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 30. Juni 2009 Tagungsort:
73. Sitzung des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 Abs. 2 AMG vom 13.01.2015
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 73. Sitzung des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 Abs. 2 AMG vom 13.01.2015 Tagungsort: Bundesinstitut
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 73. Sitzung des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 Abs. 2 AMG vom 13.01.2015 Tagungsort: Bundesinstitut
Zehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 Bundesrat Drucksache 804/10 06.12.10 Verordnung des Bundesministeriums für Gesundheit und des Bundesministeriums für Ernährung, Landwirtschaft und Verbraucherschutz G - AV Zehnte Verordnung zur Änderung
Bundesrat Drucksache 804/10 06.12.10 Verordnung des Bundesministeriums für Gesundheit und des Bundesministeriums für Ernährung, Landwirtschaft und Verbraucherschutz G - AV Zehnte Verordnung zur Änderung
Geschäftsordnung. für das. "Kuratorium Botanische Gärten der Technischen Universität Dresden"
 Neufassung der Geschäftsordnung für das Kuratorium Botanische Gärten der Technischen Universität Dresden (veröffentlicht in den Amtlichen Bekanntmachungen der TUD Nr. 8/1994 vom 26.09.1994) Das Rektoratskollegium
Neufassung der Geschäftsordnung für das Kuratorium Botanische Gärten der Technischen Universität Dresden (veröffentlicht in den Amtlichen Bekanntmachungen der TUD Nr. 8/1994 vom 26.09.1994) Das Rektoratskollegium
Antrag auf Entlassung aus der Verschreibungspflicht. -Diclazuril-
 Antrag auf Entlassung aus der Verschreibungspflicht Antrag der Firma: Erweiterung des Eintrags in der AMVV von derzeit Diclazuril in Diclazuril ausgenommen zur Anwendung bei Bartagame und Leopardgecko
Antrag auf Entlassung aus der Verschreibungspflicht Antrag der Firma: Erweiterung des Eintrags in der AMVV von derzeit Diclazuril in Diclazuril ausgenommen zur Anwendung bei Bartagame und Leopardgecko
Antrag auf Entlassung aus der Verschreibungspflicht
 Antrag auf Entlassung aus der Verschreibungspflicht Zolmitriptan 2,5 mg zur Behandlung des akuten Migräneanfalls (Zomig Filmtabletten und Schmelztabletten) Sachverständigenausschuss für Verschreibungspflicht
Antrag auf Entlassung aus der Verschreibungspflicht Zolmitriptan 2,5 mg zur Behandlung des akuten Migräneanfalls (Zomig Filmtabletten und Schmelztabletten) Sachverständigenausschuss für Verschreibungspflicht
GESCHÄFTSORDNUNG DER VERTRETERVERSAMMLUNG DER ARCHITEKTENKAMMER NIEDERSACHSEN
 GESCHÄFTSORDNUNG DER VERTRETERVERSAMMLUNG DER ARCHITEKTENKAMMER NIEDERSACHSEN vom 7. Mai 1992 (DAB 7/92, BN 132), zuletzt geändert am 23. November 2017 (DAB 2/2018, S. 29, Regionalteil Niedersachsen) 1
GESCHÄFTSORDNUNG DER VERTRETERVERSAMMLUNG DER ARCHITEKTENKAMMER NIEDERSACHSEN vom 7. Mai 1992 (DAB 7/92, BN 132), zuletzt geändert am 23. November 2017 (DAB 2/2018, S. 29, Regionalteil Niedersachsen) 1
Zubereitung aus Aciclovir und Hydrocortison
 Zubereitung aus Aciclovir und Hydrocortison Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag Antrag
Zubereitung aus Aciclovir und Hydrocortison Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag Antrag
Tragende Gründe. Vom 19. Juni 2014
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage VI Off-Label-Use Venlafaxin bei neuropathischen Schmerzen Vom 19. Juni 2014
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage VI Off-Label-Use Venlafaxin bei neuropathischen Schmerzen Vom 19. Juni 2014
TOP 14 Ipratropiumbromid
 TOP 14 Ipratropiumbromid 69. Sitzung SVA Verschreibungspflicht 26. Juni 2012 Aktueller Antrag Zusatz bei der Position Ipratropiumbromid : ausgenommen zur intranasalen Anwendung in einer Konzentration bis
TOP 14 Ipratropiumbromid 69. Sitzung SVA Verschreibungspflicht 26. Juni 2012 Aktueller Antrag Zusatz bei der Position Ipratropiumbromid : ausgenommen zur intranasalen Anwendung in einer Konzentration bis
Analgetika-Gebrauch in Deutschland ( ) im internationalen Vergleich
 Analgetika-Gebrauch in Deutschland (1980-2010) im internationalen Vergleich Quelle: IMS 2010 Der Pro-Kopf-Gebrauch an OTC-Analgetika ist seit 15 Jahren rückläufig; Rx-Analgetika nehmen dagegen zu. Quelle:
Analgetika-Gebrauch in Deutschland (1980-2010) im internationalen Vergleich Quelle: IMS 2010 Der Pro-Kopf-Gebrauch an OTC-Analgetika ist seit 15 Jahren rückläufig; Rx-Analgetika nehmen dagegen zu. Quelle:
Antrag auf Entlassung aus der Verschreibungspflicht. -Praziquantel-
 Antrag auf Entlassung aus der Verschreibungspflicht AMVV Antrag der Firma: Erweiterung des Eintrags um Punkt c Praziquantel ausgenommen zur Anwendung a) bei Hunden und Katzen b) bei Zierfischen der Ordnungen
Antrag auf Entlassung aus der Verschreibungspflicht AMVV Antrag der Firma: Erweiterung des Eintrags um Punkt c Praziquantel ausgenommen zur Anwendung a) bei Hunden und Katzen b) bei Zierfischen der Ordnungen
Satzung des Ethikkomitees der Gesundheitsholding Tauberfranken
 1 Grundsatz 1. Das Ethikkomitee ist eine ständige Einrichtung der Gesundheitsholding Tauberfranken. Es ist ein Forum für schwierige und kontroverse ethisch-moralische Entscheidungen. 2. Seine Mitglieder
1 Grundsatz 1. Das Ethikkomitee ist eine ständige Einrichtung der Gesundheitsholding Tauberfranken. Es ist ein Forum für schwierige und kontroverse ethisch-moralische Entscheidungen. 2. Seine Mitglieder
Ergebnisprotokoll. zur 10. Sitzung der Gemeinsamen Expertenkommission zur Einstufung von Stoffen
 Stand 28.06.2016 Ergebnisprotokoll zur 10. Sitzung der Gemeinsamen Expertenkommission zur Einstufung von Stoffen Kommission zur Einstufung von Borderline-Stoffen, die als Lebensmittel oder Lebensmittelzutat
Stand 28.06.2016 Ergebnisprotokoll zur 10. Sitzung der Gemeinsamen Expertenkommission zur Einstufung von Stoffen Kommission zur Einstufung von Borderline-Stoffen, die als Lebensmittel oder Lebensmittelzutat
MSC der ECHA. Ausschuss der Mitgliedsstaaten
 MSC der ECHA Ausschuss der Mitgliedsstaaten REACH Artikel 76 (1) e Der Ausschuss der Mitgliedstaaten ist zuständig für die Klärung von möglichen Meinungsverschiedenheiten zu: Entscheidungsentwürfen, die
MSC der ECHA Ausschuss der Mitgliedsstaaten REACH Artikel 76 (1) e Der Ausschuss der Mitgliedstaaten ist zuständig für die Klärung von möglichen Meinungsverschiedenheiten zu: Entscheidungsentwürfen, die
Niederschrift über die öffentliche Sitzung der Stadtverordnetenversammlung
 Niederschrift über die öffentliche Sitzung der Stadtverordnetenversammlung am Dienstag, 15.12.2015 im Sitzungssaal des Rathauses, Steinau an der Straße Beginn der Sitzung: Ende der Sitzung: 19:30 Uhr 22:21
Niederschrift über die öffentliche Sitzung der Stadtverordnetenversammlung am Dienstag, 15.12.2015 im Sitzungssaal des Rathauses, Steinau an der Straße Beginn der Sitzung: Ende der Sitzung: 19:30 Uhr 22:21
Tragende Gründe zum Beschluss. des Gemeinsamen Bundesausschusses über die Änderung der Arzneimittel-Richtlinie (AM-RL):
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über die Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage 1 (OTC-Übersicht) Nr. 20 Ginkgo-biloba-Blätter-Extrakt Vom 14. April 2011 Inhaltsverzeichnis
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über die Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage 1 (OTC-Übersicht) Nr. 20 Ginkgo-biloba-Blätter-Extrakt Vom 14. April 2011 Inhaltsverzeichnis
Tragende Gründe. zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Schutzimpfungs-Richtlinie:
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Schutzimpfungs-Richtlinie: Überarbeitung der Spaltenzuordnung in Anlage 1 Vom 17. Juni 2010 Inhaltsverzeichnis 1 Rechtsgrundlagen
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Schutzimpfungs-Richtlinie: Überarbeitung der Spaltenzuordnung in Anlage 1 Vom 17. Juni 2010 Inhaltsverzeichnis 1 Rechtsgrundlagen
N i e d e r s c h r i f t
 1 N i e d e r s c h r i f t über die 6. Sitzung des Rates der Gemeinde Ebergötzen am Dienstag, 25. Juli 2017, 19.00 Uhr, im Gemeindebüro, Bergstraße 18 im Ortsteil Ebergötzen ------------------------------------------------------------------------------------------------------------------------
1 N i e d e r s c h r i f t über die 6. Sitzung des Rates der Gemeinde Ebergötzen am Dienstag, 25. Juli 2017, 19.00 Uhr, im Gemeindebüro, Bergstraße 18 im Ortsteil Ebergötzen ------------------------------------------------------------------------------------------------------------------------
Verwaltungsangestellte Tatjana Herbrandt. I. Eröffnung und Begrüßung:
 NIEDERSCHRIFT über die 4. Sitzung des Jugendhilfeausschusses des Donnersbergkreises in der 10. Wahlperiode 2014/2019 in Kirchheimbolanden, Kreishaus, großer Sitzungssaal am Montag, 14. Dezember 2015, 15.00
NIEDERSCHRIFT über die 4. Sitzung des Jugendhilfeausschusses des Donnersbergkreises in der 10. Wahlperiode 2014/2019 in Kirchheimbolanden, Kreishaus, großer Sitzungssaal am Montag, 14. Dezember 2015, 15.00
Abgrenzung von Arzneimitteln zu Lebensmitteln Arbeitsweise des BfArM
 Abgrenzung von Arzneimitteln zu Lebensmitteln Arbeitsweise des BfArM 10. Sitzung der Gemeinsamen Expertenkommission Dr. Kerstin Stephan Absender Titel 30.03.2016 Seite 1 Zuständigkeiten der Behörden bei
Abgrenzung von Arzneimitteln zu Lebensmitteln Arbeitsweise des BfArM 10. Sitzung der Gemeinsamen Expertenkommission Dr. Kerstin Stephan Absender Titel 30.03.2016 Seite 1 Zuständigkeiten der Behörden bei
Bundestagsmehrheit nutzen Pille danach jetzt aus der Rezeptpflicht entlassen
 Deutscher Bundestag Drucksache 18/3825 18. Wahlperiode 26.01.2015 Beschlussempfehlung und Bericht des Ausschusses für Gesundheit (14. Ausschuss) a) zu dem Antrag der Abgeordneten Cornelia Möhring, Kathrin
Deutscher Bundestag Drucksache 18/3825 18. Wahlperiode 26.01.2015 Beschlussempfehlung und Bericht des Ausschusses für Gesundheit (14. Ausschuss) a) zu dem Antrag der Abgeordneten Cornelia Möhring, Kathrin
Geschäftsordnung für die Ausschüsse und Arbeitskreise der Industrie- und Handelskammer zu Düsseldorf
 Industrie- und Handelskammer zu Düsseldorf Postfachadresse: Postfach 10 10 17. 40001 Düsseldorf Hausadresse: Ernst-Schneider-Platz 1. 40212 Düsseldorf Telefon 0211 3557-0 Geschäftsordnung für die Ausschüsse
Industrie- und Handelskammer zu Düsseldorf Postfachadresse: Postfach 10 10 17. 40001 Düsseldorf Hausadresse: Ernst-Schneider-Platz 1. 40212 Düsseldorf Telefon 0211 3557-0 Geschäftsordnung für die Ausschüsse
Tragende Gründe. Vom 18. Oktober 2018
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der -Richtlinie (AM-RL): Anlage VI Off- Label-Use Teil A Ziffer III: Carboplatin bei fortgeschrittenem nicht-kleinzelligem
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der -Richtlinie (AM-RL): Anlage VI Off- Label-Use Teil A Ziffer III: Carboplatin bei fortgeschrittenem nicht-kleinzelligem
Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 7 Famciclovir
 Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 7 Famciclovir Antrag auf Entlassung aus der Verschreibungspflicht Famciclovir zur oralen Behandlung von rezidivierenden Episoden
Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 7 Famciclovir Antrag auf Entlassung aus der Verschreibungspflicht Famciclovir zur oralen Behandlung von rezidivierenden Episoden
Linezolid, INN zur Behandlung von Pneumonien oder schweren Haut- und Weichteilinfektionen, wenn diese durch grampositive Erreger verursacht sind
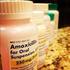 Lincomycin Linezolid Lincomycin, I ATC Antibiotika, Lincosamide (J01FF) BZ Methyl{6,8-didesoxy-6-[(2S,4R)-1-methyl-4-propylpyrrolidin-2-carboxamido]-1- thio-d-erythro-α-d-galacto-octopyranosid} AM z.b.
Lincomycin Linezolid Lincomycin, I ATC Antibiotika, Lincosamide (J01FF) BZ Methyl{6,8-didesoxy-6-[(2S,4R)-1-methyl-4-propylpyrrolidin-2-carboxamido]-1- thio-d-erythro-α-d-galacto-octopyranosid} AM z.b.
Antrag auf Freistellung aus der Verschreibungspflicht für Omeprazol 20 mg
 Antrag auf Freistellung aus der Verschreibungspflicht für Omeprazol 20 mg Sachverständigen-Ausschuss für Verschreibungspflicht 13. Januar 2009 Rationale des Antrags Omeprazol ist eine der effektivsten
Antrag auf Freistellung aus der Verschreibungspflicht für Omeprazol 20 mg Sachverständigen-Ausschuss für Verschreibungspflicht 13. Januar 2009 Rationale des Antrags Omeprazol ist eine der effektivsten
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Deutsche Gesellschaft für Sprachwissenschaft DGfS
 Deutsche Gesellschaft für Sprachwissenschaft DGfS Ordnung der Deutschen Gesellschaft für Sprachwissenschaft zur ethischen Begutachtung von Forschungsprojekten Die vorliegende Ordnung wurde vom Vorstand
Deutsche Gesellschaft für Sprachwissenschaft DGfS Ordnung der Deutschen Gesellschaft für Sprachwissenschaft zur ethischen Begutachtung von Forschungsprojekten Die vorliegende Ordnung wurde vom Vorstand
LANDKREIS TUTTLINGEN GESCHÄFTSORDNUNG DES KREISTAGS UND DER AUSSCHÜSSE
 LANDKREIS TUTTLINGEN GESCHÄFTSORDNUNG DES KREISTAGS UND DER AUSSCHÜSSE - 2 - Stand: 1.1.1986 Der Kreistag hat für sich und die Ausschüsse aufgrund von 31 Abs. 2 LkrO für Baden-Württemberg vom 10. Oktober
LANDKREIS TUTTLINGEN GESCHÄFTSORDNUNG DES KREISTAGS UND DER AUSSCHÜSSE - 2 - Stand: 1.1.1986 Der Kreistag hat für sich und die Ausschüsse aufgrund von 31 Abs. 2 LkrO für Baden-Württemberg vom 10. Oktober
Gemeinsame Expertenkommission des BVL und des BfArM Konstituierende Sitzung
 Gemeinsame Expertenkommission des BVL und des BfArM Konstituierende Sitzung Dr. Helmut Tschiersky-Schöneburg Bundesamt für Verbraucherschutz und Lebensmittelsicherheit Dr. Helmut Tschiersky-Schöneburg
Gemeinsame Expertenkommission des BVL und des BfArM Konstituierende Sitzung Dr. Helmut Tschiersky-Schöneburg Bundesamt für Verbraucherschutz und Lebensmittelsicherheit Dr. Helmut Tschiersky-Schöneburg
Sozialdemokratische Partei Deutschlands - Unterbezirk Düsseldorf - Geschäftsordnung des Unterbezirksparteitages - Stand: 17 November
 Sozialdemokratische Partei Deutschlands - Unterbezirk Düsseldorf - Geschäftsordnung des Unterbezirksparteitages - Stand: 17 November 2001 - Geschäftsordnung des Unterbezirksparteitages 1. Eröffnung und
Sozialdemokratische Partei Deutschlands - Unterbezirk Düsseldorf - Geschäftsordnung des Unterbezirksparteitages - Stand: 17 November 2001 - Geschäftsordnung des Unterbezirksparteitages 1. Eröffnung und
Es gilt das gesprochene Wort! Sehr geehrter Herr Präsident Dr. Tschiersky, meine sehr geehrten Damen und Herren!
 Grußwort von Frau Ministerialdirigentin Dr. Bettina Hartwig anlässlich der Übergabe der Stoffliste Pflanzen und Pflanzenteile des Bundes und der Länder am 9. September 2014 in Berlin Es gilt das gesprochene
Grußwort von Frau Ministerialdirigentin Dr. Bettina Hartwig anlässlich der Übergabe der Stoffliste Pflanzen und Pflanzenteile des Bundes und der Länder am 9. September 2014 in Berlin Es gilt das gesprochene
Ergebnisprotokoll. Herr Prof. Dr. Dr. H. Walach Herr M. Wegner Herr A. Zenner BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 30. Sitzung der Kommission nach 25 Abs. 6 und Abs. 7 AMG für den humanmedizinischen Bereich, homöopathische Therapierichtung (Kommission
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 30. Sitzung der Kommission nach 25 Abs. 6 und Abs. 7 AMG für den humanmedizinischen Bereich, homöopathische Therapierichtung (Kommission
Ortsverwaltung Mörsbach
 S T A D T V E R W A L T U N G Z W E I B R Ü C K E N 10 25 25 St/SM 15.8.2016 Ortsverwaltung Mörsbach Niederschrift über die 11. Sitzung des Ortsbeirates Mörsbach (Sondersitzung) am Donnerstag, dem 11.
S T A D T V E R W A L T U N G Z W E I B R Ü C K E N 10 25 25 St/SM 15.8.2016 Ortsverwaltung Mörsbach Niederschrift über die 11. Sitzung des Ortsbeirates Mörsbach (Sondersitzung) am Donnerstag, dem 11.
Homöopathische und Anthroposophische Arzneimittel - Erfahrungen aus der regulatorischen Praxis -
 Homöopathische und Anthroposophische Arzneimittel - Erfahrungen aus der regulatorischen Praxis - Dr. Christina von der Heidt Christina von der Heidt BfArM im Dialog 26.04.2016 Seite 1 Übersicht Allgemeine
Homöopathische und Anthroposophische Arzneimittel - Erfahrungen aus der regulatorischen Praxis - Dr. Christina von der Heidt Christina von der Heidt BfArM im Dialog 26.04.2016 Seite 1 Übersicht Allgemeine
Art. 107i-Verfahren nach RL 2001/83/EG zu Cyproteronazetat/Ethinylestradiol (2mg/0,035mg): Diane 35 und Generika. 72. Routinesitzung 29.
 Art. 107i-Verfahren nach RL 2001/83/EG zu Cyproteronazetat/Ethinylestradiol (2mg/0,035mg): Diane 35 und Generika 72. Routinesitzung 29. Mai 2013 Hintergrund des Verfahrens Neubewertung des Nutzen-Risiko-Verhältnisses
Art. 107i-Verfahren nach RL 2001/83/EG zu Cyproteronazetat/Ethinylestradiol (2mg/0,035mg): Diane 35 und Generika 72. Routinesitzung 29. Mai 2013 Hintergrund des Verfahrens Neubewertung des Nutzen-Risiko-Verhältnisses
Zusammenfassende Dokumentation. über eine Änderung der Schutzimpfungs-Richtlinie: Überarbeitung der Spaltenzuordnung in Anlage 1. Vom 17.
 Zusammenfassende Dokumentation über eine Änderung der Schutzimpfungs-Richtlinie: Überarbeitung der Spaltenzuordnung in Anlage 1 Vom 17. Juni 2010 Inhaltsverzeichnis A. Tragende Gründe und Beschluss B.
Zusammenfassende Dokumentation über eine Änderung der Schutzimpfungs-Richtlinie: Überarbeitung der Spaltenzuordnung in Anlage 1 Vom 17. Juni 2010 Inhaltsverzeichnis A. Tragende Gründe und Beschluss B.
Protokoll der Jahreshauptversammlung des TuS Nortorf von 1859 e.v. vom 30. Januar Gaststätte Alter Landkrug in Nortorf
 Protokoll der Jahreshauptversammlung des TuS Nortorf von 1859 e.v. vom 30. Januar 2017 Sitzungsbeginn: Sitzungsort: 19.30 Uhr Gaststätte Alter Landkrug in Nortorf Um 19.40 Uhr begrüßt die Jugendwartin
Protokoll der Jahreshauptversammlung des TuS Nortorf von 1859 e.v. vom 30. Januar 2017 Sitzungsbeginn: Sitzungsort: 19.30 Uhr Gaststätte Alter Landkrug in Nortorf Um 19.40 Uhr begrüßt die Jugendwartin
Spezielle Aktivitäten des BfArM im Bereich Abgrenzung
 Spezielle Aktivitäten des BfArM im Bereich Abgrenzung Gerald Kesseler Gerald Kesseler BfArM im Dialog: Abgrenzung 19.09.2016 Seite 1 Inhaltsverzeichnis 1. Gemeinsame Expertenkommission zur Einstufung von
Spezielle Aktivitäten des BfArM im Bereich Abgrenzung Gerald Kesseler Gerald Kesseler BfArM im Dialog: Abgrenzung 19.09.2016 Seite 1 Inhaltsverzeichnis 1. Gemeinsame Expertenkommission zur Einstufung von
Geschäftsordnung für den Kommunalen Nationalparkausschuss (KNPA) des Nationalparks Berchtesgaden. Zusammensetzung und Aufgaben
 Geschäftsordnung für den Kommunalen Nationalparkausschuss (KNPA) des Nationalparks Berchtesgaden 1 Zusammensetzung und Aufgaben Zusammensetzung und Aufgaben des Kommunalen Nationalparkausschusses ergeben
Geschäftsordnung für den Kommunalen Nationalparkausschuss (KNPA) des Nationalparks Berchtesgaden 1 Zusammensetzung und Aufgaben Zusammensetzung und Aufgaben des Kommunalen Nationalparkausschusses ergeben
Informationsveranstaltung für die Antragsteller Beantwortung von Fragen der Antragsteller
 Informationsveranstaltung für die Antragsteller 16.06.2015 Beantwortung von Fragen der Antragsteller ZV1 Verfahren Können später als nach der ersten Bewertungsphase noch weitere Forderungen durch die Bewertungsbehörden
Informationsveranstaltung für die Antragsteller 16.06.2015 Beantwortung von Fragen der Antragsteller ZV1 Verfahren Können später als nach der ersten Bewertungsphase noch weitere Forderungen durch die Bewertungsbehörden
Niederschrift Nr. 4/2011
 Niederschrift Nr. 4/2011 über die Sitzung des Haupt- und Finanzausschusses der Gemeindevertretung der Gemeinde Mühltal am Dienstag, dem 27. September 2011, Brückenmühlensaal des Bürgerzentrums Nieder-Ramstadt
Niederschrift Nr. 4/2011 über die Sitzung des Haupt- und Finanzausschusses der Gemeindevertretung der Gemeinde Mühltal am Dienstag, dem 27. September 2011, Brückenmühlensaal des Bürgerzentrums Nieder-Ramstadt
Niederschrift Nr. 2/ über die Sitzung des Hauptausschusses am 12. November 2013
 Gemeinde Lensahn Niederschrift Nr. 2/2013-2018 über die Sitzung des Hauptausschusses am 12. November 2013 Tagungsort: Rathaus Lensahn, Sitzungszimmer Anwesend: Gemeindevertreter Steffen als Vorsitzender
Gemeinde Lensahn Niederschrift Nr. 2/2013-2018 über die Sitzung des Hauptausschusses am 12. November 2013 Tagungsort: Rathaus Lensahn, Sitzungszimmer Anwesend: Gemeindevertreter Steffen als Vorsitzender
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anlage 2 zur Vereinbarung über die Bildung des Schlichtungsausschusses nach 17c Abs. 3 KHG vom Geschäftsordnung
 Geschäftsordnung für den Schlichtungsausschuss nach 17c Abs. 3 KHG 1 Anrufung des Schlichtungsausschusses (1) Der Schlichtungsausschuss wird durch einen Antrag angerufen. Er kann neben den Vertragsparteien
Geschäftsordnung für den Schlichtungsausschuss nach 17c Abs. 3 KHG 1 Anrufung des Schlichtungsausschusses (1) Der Schlichtungsausschuss wird durch einen Antrag angerufen. Er kann neben den Vertragsparteien
18. Wahlperiode. Da Frau Abg. Pieroth-Manelli (GRÜNE) das Amt der Schriftführerin innehatte, ist das Amt neu zu besetzen.
 Plenar- und Ausschussdienst Beschlussprotokoll Öffentliche Sitzung Ausschuss für Wirtschaft, Energie, Betriebe 20. Sitzung Beginn: Schluss: Vorsitz: 15.06 Uhr 17.20 Uhr Herr Frank-Christian Hansel (AfD)
Plenar- und Ausschussdienst Beschlussprotokoll Öffentliche Sitzung Ausschuss für Wirtschaft, Energie, Betriebe 20. Sitzung Beginn: Schluss: Vorsitz: 15.06 Uhr 17.20 Uhr Herr Frank-Christian Hansel (AfD)
Protokoll. Herr Adam eröffnet die Sitzung. Er begrüßt alle Anwesenden. Frau Keller als neues Mitglied der Stadt Göttingen wird begrüßt.
 Protokoll über die Sitzung der Arbeitsgruppe zur Umsetzung der UN-Konvention über die Rechte von Menschen mit Behinderungen (AG Inklusion) am 24.03.2015, im Neuen Rathaus, Raum 1118, Hiroshimaplatz 1-4,
Protokoll über die Sitzung der Arbeitsgruppe zur Umsetzung der UN-Konvention über die Rechte von Menschen mit Behinderungen (AG Inklusion) am 24.03.2015, im Neuen Rathaus, Raum 1118, Hiroshimaplatz 1-4,
Europäische Verfahren
 Europäische Verfahren Zur Zeit existieren 3 verschieden Zulassungsverfahren in der EU: Verfahren der gegenseitigen Anerkennung (MRP) dezentrales Verfahren (DCP) zentrales Verfahren Alle Biotech Produkte
Europäische Verfahren Zur Zeit existieren 3 verschieden Zulassungsverfahren in der EU: Verfahren der gegenseitigen Anerkennung (MRP) dezentrales Verfahren (DCP) zentrales Verfahren Alle Biotech Produkte
6. Bericht zur Einführung des Bildungs- und Teilhabepaketes in Hagen
 Seite: 1 NIEDERSCHRIFT DER SITZUNG Sitzungsnummer: SOA/04/2011 Gremium: Sozialausschuss Tag: Mittwoch, 06.07.2011 Ort: Rathaus an der Volme, Sitzungsraum A.201 Beginn: 16:00 Uhr A. TAGESORDNUNG I. Öffentlicher
Seite: 1 NIEDERSCHRIFT DER SITZUNG Sitzungsnummer: SOA/04/2011 Gremium: Sozialausschuss Tag: Mittwoch, 06.07.2011 Ort: Rathaus an der Volme, Sitzungsraum A.201 Beginn: 16:00 Uhr A. TAGESORDNUNG I. Öffentlicher
Geschäftsordnung. Kreistag. Main-Tauber-Kreis
 Geschäftsordnung Kreistag Main-Tauber-Kreis -konsolidierte Fassung- Aufgrund von 31 Abs. 2 der Landkreisordnung für Baden-Württemberg vom 10. Oktober 1955 (Ges.Bl. S. 207) i.d.f. der Bekanntmachung vom
Geschäftsordnung Kreistag Main-Tauber-Kreis -konsolidierte Fassung- Aufgrund von 31 Abs. 2 der Landkreisordnung für Baden-Württemberg vom 10. Oktober 1955 (Ges.Bl. S. 207) i.d.f. der Bekanntmachung vom
Theater Putbus. Stefanie Lemcke (Baltic Project GmbH)
 Protokoll der Mitgliederversammlung vom 18.05.2017 Datum: Donnerstag, 18. Mai 2017 Beginn: 14:00 Uhr Ende: 15:30 Uhr Versammlungsort: Theater Putbus Anwesenheit: 31 Mitglieder mit 44 Stimmen, 10 Gäste
Protokoll der Mitgliederversammlung vom 18.05.2017 Datum: Donnerstag, 18. Mai 2017 Beginn: 14:00 Uhr Ende: 15:30 Uhr Versammlungsort: Theater Putbus Anwesenheit: 31 Mitglieder mit 44 Stimmen, 10 Gäste
Geschäftsordnung der Agrarministerkonferenz
 Geschäftsordnung der Agrarministerkonferenz (Stand: 02. April 2009) 1. Teilnahme 1.1 In der Agrarministerkonferenz (AMK) sind die Agrarminister/innen und -senatoren/innen des Bundes und der Länder der
Geschäftsordnung der Agrarministerkonferenz (Stand: 02. April 2009) 1. Teilnahme 1.1 In der Agrarministerkonferenz (AMK) sind die Agrarminister/innen und -senatoren/innen des Bundes und der Länder der
Antrag auf Entlassung aus der Verschreibungspflicht. -Doramectin-
 Antrag auf Entlassung aus der Verschreibungspflicht Antrag auf Entlassung von Doramectin aus der Verschreibungspflicht für die topische Anwendung bei Königspython, Abgottschlange und Bartagame bei einem
Antrag auf Entlassung aus der Verschreibungspflicht Antrag auf Entlassung von Doramectin aus der Verschreibungspflicht für die topische Anwendung bei Königspython, Abgottschlange und Bartagame bei einem
ANHANG. des. Vorschlags für einen BESCHLUSS DES RATES
 EUROPÄISCHE KOMMISSION Brüssel, den 12.10.2016 COM(2016) 620 final ANNEX 1 ANHANG des Vorschlags für einen BESCHLUSS DES RATES über den Standpunkt der Union in dem durch das Kooperationsabkommen zwischen
EUROPÄISCHE KOMMISSION Brüssel, den 12.10.2016 COM(2016) 620 final ANNEX 1 ANHANG des Vorschlags für einen BESCHLUSS DES RATES über den Standpunkt der Union in dem durch das Kooperationsabkommen zwischen
BÜNDNIS 90/DIE GRÜNEN
 Deutscher Bundestag Drucksache 18/4116 18. Wahlperiode 25.02.2015 Beschlussempfehlung und Bericht des Ausschusses für Gesundheit (14. Ausschuss) zu dem Gesetzentwurf der Abgeordneten Kordula Schulz-Asche,
Deutscher Bundestag Drucksache 18/4116 18. Wahlperiode 25.02.2015 Beschlussempfehlung und Bericht des Ausschusses für Gesundheit (14. Ausschuss) zu dem Gesetzentwurf der Abgeordneten Kordula Schulz-Asche,
Geschäftsordnung des Wissenschaftlichen Beirats des Paul-Ehrlich-Instituts vom
 Geschäftsordnung des Wissenschaftlichen Beirats des Paul-Ehrlich-Instituts vom 20.11.2012 Präambel Das Paul-Ehrlich-Institut ist eine Bundesoberbehörde im Geschäftsbereich des Bundesministeriums für Gesundheit.
Geschäftsordnung des Wissenschaftlichen Beirats des Paul-Ehrlich-Instituts vom 20.11.2012 Präambel Das Paul-Ehrlich-Institut ist eine Bundesoberbehörde im Geschäftsbereich des Bundesministeriums für Gesundheit.
10. Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 ARZNEIMITTELRECHT Notfallmedikation bei anaphylaktischen Reaktionen. 10. Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Die Arzneimittelkommission deutscher Heilpraktiker als Stufenplanbeteiligte
ARZNEIMITTELRECHT Notfallmedikation bei anaphylaktischen Reaktionen. 10. Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Die Arzneimittelkommission deutscher Heilpraktiker als Stufenplanbeteiligte
Rat der Europäischen Union Brüssel, den 23. Juli 2014 (OR. en) Herr Uwe CORSEPIUS, Generalsekretär des Rates der Europäischen Union
 Rat der Europäischen Union Brüssel, den 23. Juli 2014 (OR. en) 12140/14 DENLEG 135 AGRI 512 SAN 296 ÜBERMITTLUNGSVERMERK Absender: Europäische Kommission Eingangsdatum: 22. Juli 2014 Empfänger: Nr. Komm.dok.:
Rat der Europäischen Union Brüssel, den 23. Juli 2014 (OR. en) 12140/14 DENLEG 135 AGRI 512 SAN 296 ÜBERMITTLUNGSVERMERK Absender: Europäische Kommission Eingangsdatum: 22. Juli 2014 Empfänger: Nr. Komm.dok.:
Geschäftsordnung Berufsbildungsausschuss Handwerkskammer zu Köln (lt. Beschluss vom )
 Geschäftsordnung Berufsbildungsausschuss Handwerkskammer zu Köln (lt. Beschluss vom 26.04.2005) 1 Zuständigkeit 2 Aufgaben 3 Zusammensetzung, Stellvertretung 4 Vorsitzender, stellvertretender Vorsitzender,
Geschäftsordnung Berufsbildungsausschuss Handwerkskammer zu Köln (lt. Beschluss vom 26.04.2005) 1 Zuständigkeit 2 Aufgaben 3 Zusammensetzung, Stellvertretung 4 Vorsitzender, stellvertretender Vorsitzender,
Satzung der Ethikkommission. Präambel
 Satzung der Ethikkommission der Bundesfachschule für Orthopädie-Technik Präambel (1) Die Bundesfachschule für Orthopädie-Technik, Dortmund, unterhält eine Kommission zur Beurteilung ethischer Fragen von
Satzung der Ethikkommission der Bundesfachschule für Orthopädie-Technik Präambel (1) Die Bundesfachschule für Orthopädie-Technik, Dortmund, unterhält eine Kommission zur Beurteilung ethischer Fragen von
