V o t en. Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG
|
|
|
- Gerhardt Franke
- vor 7 Jahren
- Abrufe
Transkript
1 ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 66. Sitzung, zu Positionen, über deren Änderung abgestimmt wurde. 3. Oxybuprocain Oxybuprocain der Verschreibungspflicht nach 48 AMG zu unterstellen. Arzneimittel mit dem Lokalanästhetikum Oxybuprocain sind zur zugelassen. Diese Arzneimittel sind entsprechend den Angaben der Produktinformationen verschreibungspflichtig. Die Verschreibungspflicht wird uneingeschränkt unterstützt, da ophthalmologische Lokalanästhetika prinzipiell nur durch den Arzt angewendet werden bzw. für den Fall der Selbsttonometrie ärztlich verordnet abgegeben werden sollen. Eine Selbstmedikation birgt erhebliche Risiken für das Auge und das Sehvermögen der Patienten (Hornhautschäden, Selbstverletzung des Auges). 3. Proxymetacain Proxymetacain der Verschreibungspflicht nach 48 AMG zu unterstellen. Arzneimittel mit dem Lokalanästhetikum Proxymetacain sind zur Anwendung am Auge zugelassen. Diese Arzneimittel sind entsprechend den Angaben der Produktinformationen verschreibungspflichtig. Die Verschreibungspflicht wird 1
2 uneingeschränkt unterstützt, da ophthalmologische Lokalanästhetika prinzipiell nur durch den Arzt angewendet werden bzw. für den Fall der Selbsttonometrie ärztlich verordnet abgegeben werden sollen. Eine Selbstmedikation birgt erhebliche Risiken für das Auge und das Sehvermögen der Patienten (Hornhautschäden, Selbstverletzung des Auges). 5. Orlistat die bestehende Position Orlistat - ausgenommen von der Europäischen Kommission zugelassene, nicht verschreibungspflichtige Arzneimittel in einer Höchstmenge von 60 mg pro abgeteilter Form - abzuändern in Orlistat - ausgenommen Arzneimittel zur oralen Anwendung, die in der EU zentral und verschreibungsfrei zugelassen wurden sowie Arzneimittel mit einer Höchstmenge von 60 mg pro abgeteilter Form und einer maximalen Tagesdosis von 180 mg - Orlistat ist seit 1997 in Deutschland als verschreibungspflichtiges Arzneimittel unter dem Produktnamen Xenical in der 120 mg-stärke im Verkehr (empfohlene maximale Tagesdosis 360 mg). Als verschreibungspflichtiges Arzneimittel ist Orlistat in Deutschland zugelassen zur Anwendung in Verbindung mit einer leicht hypokalorischen Kost zur Behandlung von adipösen Patienten mit einem Körpermasseindex (body mass index - BMI) von größer oder gleich 30 kg/m 2 oder von übergewichtigen Patienten (BMI 28 kg/m 2 ) mit begleitenden Risikofaktoren angezeigt. Die Behandlung mit Orlistat sollte nach 12 Wochen abgebrochen werden, wenn der Gewichtsverlust nicht mindestens 5 % des Körpergewichtes zu Beginn der Therapie beträgt. Orlistat ist weiterhin seit Januar 2009 in Deutschland als OTC-Präparat unter dem Produktnamen alli mit 60 mg Orlistat je Hartkapsel zugelassen (empfohlene maximale Tagesdosis 180 mg). Als OTC Arzneimittel ist Orlistat in Deutschland zugelassen zur Gewichtsreduktion von Erwachsenen mit Übergewicht (Body-Mass-Index BMI 28 kg/m2) (indiziert) und sollte in Verbindung mit einer leicht hypokalorischen, fettreduzierten Ernährung angewendet werden. Der CHMP hat für Orlistat im September 2010 eine weitere Formulierung unter dem Produktnamen alli in der 27 mg Stärke je Kautablette (empfohlene Tagesdosis 81 mg) die Zulassung empfohlen. Die Indikationen von alli Kautablette entsprechen denen der alli Hartkapseln. 2
3 Orlistat wäre dann aufgrund der zentralen Zulassungen in allen EU-Ländern in beiden Verkaufsabgrenzungen (verschreibungspflichtig, OTC) erhältlich. Die Ausnahme von der Verschreibungspflicht von allen Formulierungen mit einer Höchstmenge von 60 mg pro abgeteilte Form reicht nicht aus, um hinreichend zwischen den verschreibungspflichtigen und nicht verschreibungspflichtigen Formen zu unterscheiden. So reicht beispielsweise bei einem dieser Arzneimittel mit einer Stärke von 60 mg die Empfehlung, dreimal am Tag 2 Kapseln zu nehmen, um die Tagesdosis der verschreibungspflichtigen Orlistat-Produkte zu erreichen. Es sollten nur die Formulierungen freigestellt werden, die entweder zentral verschreibungsfrei zugelassen sind oder den Formulierungen gleichen. 7. Linezolid Linezolid uneingeschränkt der Verschreibungspflicht nach 48 AMG zu unterstellen. Linezolid ist ein Antibiotikum aus der Klasse der Oxazolidinone, das sich insbesondere durch eine gute Wirksamkeit auch gegenüber resistenten grampositiven Bakterien wie z.b. methicillinresistente Staphylococcus aureus (MRSA) auszeichnet und ausschließlich im Krankenhaus Anwendung findet. Linezolid ist zugelassen für die Therapie einer im Krankenhaus erworbenen Lungenentzündung und von schweren Haut- und Weichteilinfektionen. Für dieses Antibiotikum bestehen nur für die Arzneimittel des Originalherstellers (Zyvoxid ) Zulassung in Deutschland im Rahmen von EU-Verfahren (UK/H/ / ). Als neuer Stoff wurde es im Jahr 2001 mit Bezug auf die zugelassenen Indikationen in die AMVV aufgenommen: Linezolid - zur Behandlung von Pneumonien oder schweren Haut- und Weichteilinfektionen, wenn diese durch grampositive Erreger verursacht sind. Antibiotika sind generell hochwirksame, aber auch mit Risiken behaftete Chemotherapeutika, die zur Behandlung von bakteriellen Infektionen eingesetzt werden und daher eine adäquate Diagnostik, Anamnese und gegebenenfalls auch eine Überwachung der Patienten bedingen. Systemisch wirkende Antiinfektiva sind in Deutschland generell ohne Hinweis auf bestimmte Indikationen der Verschreibungspflicht unterstellt, insbesondere, um bei nicht adäquater Anwendung eine unkontrollierte Entwicklung und Selektion von resistenten Krankheitserregern zu verhindern. Mit der derzeitigen Position könnten Rezepturarzneimittel in anderen Indikationen verschreibungsfrei abgegeben werden. Zudem wäre bei einer Erweiterung der Anwendungsgebiete eine Anpassung der AMVV notwendig. 3
4 Die Streichung des Zusatzes verändert nicht den bestehenden rechtlichen Status der zugelassenen Arzneimittel, erhöht aber die Arzneimittelsicherheit sowie die Konsistenz in der Anlage 1 der AMVV. 8. Lidocain Lidocain - zur Anwendung auf der Haut zur Linderung der Symptome von neuropathischen Schmerzen nach einer Herpes-Zoster-Infektion (Post-Zoster-Neuralgie) - der Verschreibungspflicht nach 48 AMG zu unterstellen. Der Herpes zoster ist eine durch das Varicella-Zoster-Virus bedingte akute neurodermale Erkrankung, die gehäuft bei älteren Menschen ab dem 50. Lebensjahr in Erscheinung tritt. Der Herpes zoster befällt überwiegend die Nervensegmente der unteren Brustwirbelsäule, seltener den Gesichts- bzw. Kopfbereich. Von einer postzosterische Neuralgie spricht man dann, wenn Schmerzen mindestens 3 Monate nach Abheilung persistieren. Man schätzt, dass etwa 10-15% aller Patienten, die an einem Zoster erkranken, später eine postzosterische Neuralgie entwickeln. Begünstigend sind Intensität und Ausmaß der akuten Zoster-Erkrankung, Diabetes mellitus und vor allem das Alter der Patienten. In der Altersgruppe der 60-70jährigen entwickeln bis zu 60% aller Zoster-Patienten eine lang andauernde postzosterische Neuralgie. Der Schmerzcharakter bei der postzosterischen Neuralgie wird von den Patienten uneinheitlich beschrieben: anhaltend tief drückend oder brennend, blitzartig einschießend, stechend oder brennend. Typisch sind ein gesteigertes Schmerzempfinden (Hyperalgesie) und heftigste Berührungsschmerzen (Allodynie). Die manifeste postzosterische Neuralgie ist in den meisten Fällen äußerst schwierig zu therapieren. Dabei wird ein Stufenplan als sinnvoll erachtet, der neben konventionellen Analgetika, trizyklischen Antidepressiva, Antikonvulsiva und Opioiden auch topische Lokalanästhetika mit einschließt. Für jeden Patienten muss ein individuelles Therapieschema bezüglich Art und Dosis der medikamentösen Therapie erarbeitet werden. Leider ist eine komplette Schmerzfreiheit nur selten zu erzielen. Infolge der chronischen Schmerzen entwickeln sich öfters psychische Veränderungen wie depressive Stimmungslage, Schlafstörungen oder Anorexie. Suizidversuche und Suizide sind beschrieben worden. Sowohl die Diagnosestellung als auch die Entscheidung für eine bestimmte Therapie und die Überwachung dieser Therapie bedürfen bei postzosterischer Neuralgie der Kontrolle durch einen Arzt. Die Art des Therapieregimes sollte zwischen Arzt und Patient besprochen werden. Eine frühzeitige Diagnose und adäquate Therapie ist für den Verlauf und die Prognose von erheblicher Bedeutung. 4
5 Versatis wurde als erstes wirkstoffhaltiges Pflaster für die Linderung der Symptome von neuropathischen Schmerzen nach einer Herpes-Zoster-Infektion (Post-Zoster- Neuralgie) zugelassen. Jedes 10x14cm Hydrogenpflaster enthält 700 mg Lidocain. Vermutlich wirkt Lidocain über eine Blockade dermaler Natriumkanäle, wodurch die neuronalen Zellmembranen stabilisiert und die pathologische Überaktivität reduziert wird. Das Pflaster wird einmal täglich bis zu 12 Stunden in einem Zeitraum von 24 Stunden direkt auf die schmerzende Stelle geklebt. Bis zu drei Pflaster dürfen gleichzeitig appliziert werden. Bei der Anwendung des lidocainhaltigen Pflasters bedarf eine Behandlung auch nach Einleitung der Therapie weiterer ärztlicher Überwachung, vor allem um das Ergebnis der Behandlung nach 2-4 Wochen neu zu bewerten. Falls der Patient nach dieser Zeit nicht auf die Therapie angesprochen hat oder wenn der Linderungseffekt ausschließlich auf die kühlenden oder hautschützenden Eigenschaften des Hydrogel- Pflasters zurückgeführt werden kann, ist die Anwendung des wirkstoffhaltigen Pflasters nicht mehr gerechtfertigt und die Behandlung muss abgebrochen werden. Da die Risiken einer Langzeitanwendung von lidocainhaltigen Pflastern derzeit nicht bekannt sind, sollte die Behandlung in regelmäßigen Abständen durch den behandelnden Arzt bewertet werden. Eine Langzeitanwendung von lidocainhaltigen Pflastern ist nur gerechtfertig, wenn ein therapeutischer Nutzen für den Patienten vorliegt. Eine Selbstmedikation durch den Patienten ohne regelmäßige fachärztliche Überwachung ist abzulehnen. 9. Sammelposition Lokalanästhetika die Sammelposition Lokalanästhetika aufzulösen und stattdessen die folgenden, bisher bereits uneingeschränkt der Verschreibungspflicht nach 48 AMG unterstellten Lokalanästhetika einzeln aufzunehmen: Articain, Bupivacain, Cinchocain, Dimethocain, Etidocain, Levobupivacain, Mepivacain, Oxetacain, Ropivacain und Tetracain. Der Sachverständigen-Ausschuss empfiehlt außerdem die Aufnahme der nachfolgend genannten Lokalanästhetika mit den jeweiligen Einschränkungen: Benzocain Fomocain 5
6 Lidocain - ausgenommen zur parenteralen Anwendung ohne Zusatz weiterer arzneilich wirksamer Bestandteile in Konzentrationen bis zu 2 % zur intrakutanen Anwendung an der gesunden Haut - ausgenommen zur subkutanen und intramuskulären Infiltrationsanästhesie zur Durchführung von Dammschnitten und zur Naht von Dammschnitten und Dammrissen im Rahmen der Geburt in einer Konzentration bis 1 %, einer Einzeldosis von bis zu 10 ml und einer Menge von bis zu 10 ml je Ampulle zur Abgabe an Hebammen und Entbindungspfleger im Rahmen ihrer Berufsausübung - und am äußeren Gehörgang Myrtecain Prilocain Procain - ausgenommen zur parenteralen Anwendung ohne Zusatz weiterer arzneilich wirksamer Bestandteile in Konzentrationen bis zu 2 % zur intrakutanen Anwendung an der gesunden Haut Quinisocain Während der 61. Sitzung votierte der Sachverständigen-Ausschuss mehrheitlich für eine Auflösung der Sammelposition Lokalanästhetika. Als Begründung wurde unter anderem genannt, dass auf diese Weise die Einzelsubstanzen leichter und ohne Kenntnis der Substanzklasse in der Liste gefunden werden können. Während der 65. Sitzung wurden zunächst die zuvor in der Position als ohne Einschränkung der Verschreibungspflicht unterliegenden Lokalanästhetika Articain, Bupivacain, Cinchocain, Dimethocain, Etidocain, Levobupivacain, Mepivacain, Oxetacain, Ropivacain und Tetracain in Einzelpositionen überführt und aus der Sammelposition gestrichen. Mit dem oben genannten Vorschlag wird die übrige Sammelposition rechtsneutral in Einzelpositionen überführt. Hinsichtlich Fomocain wird vorgeschlagen, die bisherige Formulierung ausgenommen in Salben und Cremes in einer Konzentration bis zu 4 Gewichtsprozenten durch die Formulierung ausgenommen zum Aufbringen auf die Haut und Schleimhaut zu ersetzen, die bei allen anderen betroffenen Lokalanästhetika verwendet wurde. Auch diese Änderung ist rechtsneutral. 6
7 Der in der Sammelposition enthaltene Hinweis der grundsätzlichen Unterstellung zur muss als Ausschluss zur Ausnahme ausgenommen zum Aufbringen auf die Haut und Schleimhaut aufgenommen werden, da die Konjunktiva des Auges ebenfalls eine Schleimhaut ist. Ebenso muss für Lidocain die Rückausnahme zur Anwendung am äußeren Gehörgang aufgenommen werden, da dieser ebenfalls mit Haut ausgekleidet ist. 7
Elfte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 Bundesrat Drucksache 329/11 26.05.11 Verordnung des Bundesministeriums für Gesundheit G Elfte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung A. Problem und Ziel Da Arzneimittel mit bestimmten
Bundesrat Drucksache 329/11 26.05.11 Verordnung des Bundesministeriums für Gesundheit G Elfte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung A. Problem und Ziel Da Arzneimittel mit bestimmten
66. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 66. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom 11.01.2011 Tagungsort:
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll 66. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht vom 11.01.2011 Tagungsort:
Procain zur Anwendung am äußeren Gehörgang
 Procain zur Anwendung am äußeren Gehörgang Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 Antrag Antrag auf
Procain zur Anwendung am äußeren Gehörgang Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 Antrag Antrag auf
V o t e n. Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG
 ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t e n des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 65. Sitzung, 06.07.2010 zu Positionen, deren Änderung abgestimmt
ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t e n des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 65. Sitzung, 06.07.2010 zu Positionen, deren Änderung abgestimmt
V o t en. Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG
 ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 64. Sitzung, 12.01.2010 zu Positionen, deren Änderung abgestimmt
ANLAGE 1 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 64. Sitzung, 12.01.2010 zu Positionen, deren Änderung abgestimmt
Linezolid, INN zur Behandlung von Pneumonien oder schweren Haut- und Weichteilinfektionen, wenn diese durch grampositive Erreger verursacht sind
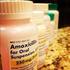 Lincomycin Linezolid Lincomycin, I ATC Antibiotika, Lincosamide (J01FF) BZ Methyl{6,8-didesoxy-6-[(2S,4R)-1-methyl-4-propylpyrrolidin-2-carboxamido]-1- thio-d-erythro-α-d-galacto-octopyranosid} AM z.b.
Lincomycin Linezolid Lincomycin, I ATC Antibiotika, Lincosamide (J01FF) BZ Methyl{6,8-didesoxy-6-[(2S,4R)-1-methyl-4-propylpyrrolidin-2-carboxamido]-1- thio-d-erythro-α-d-galacto-octopyranosid} AM z.b.
Ibuprofen zur trans-dermalen Anwendung als Pflaster
 Ibuprofen zur trans-dermalen Anwendung als Pflaster Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag
Ibuprofen zur trans-dermalen Anwendung als Pflaster Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag
Zehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 Bundesrat Drucksache 804/10 06.12.10 Verordnung des Bundesministeriums für Gesundheit und des Bundesministeriums für Ernährung, Landwirtschaft und Verbraucherschutz G - AV Zehnte Verordnung zur Änderung
Bundesrat Drucksache 804/10 06.12.10 Verordnung des Bundesministeriums für Gesundheit und des Bundesministeriums für Ernährung, Landwirtschaft und Verbraucherschutz G - AV Zehnte Verordnung zur Änderung
Racecadotril. Entlassung aus der Verschreibungspflicht
 Racecadotril Entlassung aus der Verschreibungspflicht Tania Meier Sitzung des Sachverständigen-Ausschuss für Verschreibungspflicht Bonn, 27. Februar 2012 Anlass Antrag der Firma Boehringer Ingelheim GmbH
Racecadotril Entlassung aus der Verschreibungspflicht Tania Meier Sitzung des Sachverständigen-Ausschuss für Verschreibungspflicht Bonn, 27. Februar 2012 Anlass Antrag der Firma Boehringer Ingelheim GmbH
TOP Nicotin. Anträge der Firma McNeil Consumer Healthcare GmbH auf Änderung der Verkaufsabgrenzung
 TOP 9 + 10 Nicotin Anträge der Firma McNeil Consumer Healthcare GmbH auf Änderung der Verkaufsabgrenzung Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Abs. 2 AMG 69. Sitzung 26.06.2012 Antrag
TOP 9 + 10 Nicotin Anträge der Firma McNeil Consumer Healthcare GmbH auf Änderung der Verkaufsabgrenzung Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Abs. 2 AMG 69. Sitzung 26.06.2012 Antrag
Beclometason, Fluticason, Mometason und ihre Ester
 Beclometason, Fluticason, Mometason und ihre Ester Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Seite 1 Hintergrund (I)
Beclometason, Fluticason, Mometason und ihre Ester Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Seite 1 Hintergrund (I)
Doxylamin zur Behandlung von Schlafstörungen bei Kindern
 Doxylamin zur Behandlung von Schlafstörungen bei Kindern Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 BfArM
Doxylamin zur Behandlung von Schlafstörungen bei Kindern Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 BfArM
Zubereitung aus Ibuprofen und Coffein
 Zubereitung aus Ibuprofen und Coffein Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag Kombination
Zubereitung aus Ibuprofen und Coffein Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag Kombination
Ergebnisprotokoll. der 64. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht. am 12.
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 64. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 12. Januar 2010 UTagungsort:U
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 64. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 12. Januar 2010 UTagungsort:U
Succimer. Sachverständigen-Ausschuss für Verschreibungspflicht 28. Juni 2016
 Succimer Sachverständigen-Ausschuss für Verschreibungspflicht 28. Juni 2016 Sachverständigen-Ausschuss für Verschreibungspflicht 28. Juni 2016 Seite 1 Hintergrund Nebenwirkungsmeldung zu einem anaphylaktischen
Succimer Sachverständigen-Ausschuss für Verschreibungspflicht 28. Juni 2016 Sachverständigen-Ausschuss für Verschreibungspflicht 28. Juni 2016 Seite 1 Hintergrund Nebenwirkungsmeldung zu einem anaphylaktischen
Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
Zubereitung aus Aciclovir und Hydrocortison
 Zubereitung aus Aciclovir und Hydrocortison Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag Antrag
Zubereitung aus Aciclovir und Hydrocortison Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Antrag Antrag
V o t en. Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG
 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 59. Sitzung, 03.07.2007 zu Positionen, deren Änderung abgestimmt wurde.
Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 59. Sitzung, 03.07.2007 zu Positionen, deren Änderung abgestimmt wurde.
Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 6 Racecadotril
 Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 6 Racecadotril Antrag auf Entlassung aus der Verschreibungspflicht Racecadotril bei Kindern ab 5 Jahren und Jugendlichen gemeinsam
Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 6 Racecadotril Antrag auf Entlassung aus der Verschreibungspflicht Racecadotril bei Kindern ab 5 Jahren und Jugendlichen gemeinsam
Bundesgesetzblatt Jahrgang 2005 Teil I Nr. 75, S. 3632, ausgegeben zu Bonn am
 Bundesgesetzblatt Jahrgang 2005 Teil I Nr. 75, S. 3632, ausgegeben zu Bonn am 28.12.2005 Verordnung zur Neuordnung der Verschreibungspflicht von Arzneimitteln Es verordnen Vom 21. Dezember 2005 - das Bundesministerium
Bundesgesetzblatt Jahrgang 2005 Teil I Nr. 75, S. 3632, ausgegeben zu Bonn am 28.12.2005 Verordnung zur Neuordnung der Verschreibungspflicht von Arzneimitteln Es verordnen Vom 21. Dezember 2005 - das Bundesministerium
Thymian / Primel. Sachverständigen-Ausschuss für Apothekenpflicht 13. Juni Sachverständigen-Ausschuss für Apothekenpflicht 13.
 Thymian / Primel Sachverständigen-Ausschuss für Apothekenpflicht 13. Juni 2017 Sachverständigen-Ausschuss für Apothekenpflicht 13. Juni 2017 Seite 1 Antrag Thymiankraut und seine Zubereitungen, auch in
Thymian / Primel Sachverständigen-Ausschuss für Apothekenpflicht 13. Juni 2017 Sachverständigen-Ausschuss für Apothekenpflicht 13. Juni 2017 Seite 1 Antrag Thymiankraut und seine Zubereitungen, auch in
Zubereitung aus Ibuprofen und Coffein
 Zubereitung aus Ibuprofen und Coffein Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 Antrag Kombination aus
Zubereitung aus Ibuprofen und Coffein Sachverständigen-Ausschuss für Verschreibungspflicht 27. Juni 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Juni 2017 Seite 1 Antrag Kombination aus
der 65. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht
 BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 65. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 06.07.2010 Tagungsort:
BUNDESINSTITUT FÜR ARZNEIMITTEL UND MEDIZINPRODUKTE Ergebnisprotokoll der 65. Sitzung des gemäß 48 und 53 AMG zu hörenden Sachverständigen- Ausschusses für Verschreibungspflicht am 06.07.2010 Tagungsort:
Parenteralia. Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017
 Parenteralia Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Hintergrund Diskussion auf der 76. Sitzung
Parenteralia Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Hintergrund Diskussion auf der 76. Sitzung
Eine Informationsbroschüre für Patienten mit Nervenschmerzen nach Gürtelrose
 Eine Informationsbroschüre für Patienten mit Nervenschmerzen nach Gürtelrose Liebe Patientin, lieber Patient, Patienten Name Datum der Untersuchung Diagnose Medikation Begleitmedikation Bemerkungen Mit
Eine Informationsbroschüre für Patienten mit Nervenschmerzen nach Gürtelrose Liebe Patientin, lieber Patient, Patienten Name Datum der Untersuchung Diagnose Medikation Begleitmedikation Bemerkungen Mit
während und nach Herpes zoster? Cord Sunderkötter Klinik für Hauterkrankungen und Abteilung für translationale Dermatoinfektiologie, UKMünster
 Was mache ich bei Schmerzen während und nach Herpes zoster? Cord Sunderkötter Klinik für Hauterkrankungen und Abteilung für translationale Dermatoinfektiologie, UKMünster Schmerztherapie des H.zoster (auch
Was mache ich bei Schmerzen während und nach Herpes zoster? Cord Sunderkötter Klinik für Hauterkrankungen und Abteilung für translationale Dermatoinfektiologie, UKMünster Schmerztherapie des H.zoster (auch
Neunte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 Bundesrat Drucksache 332/10 28.05.10 Verordnung des Bundesministeriums für Gesundheit und des Bundesministeriums für Ernährung, Landwirtschaft und Verbraucherschutz G - AV Neunte Verordnung zur Änderung
Bundesrat Drucksache 332/10 28.05.10 Verordnung des Bundesministeriums für Gesundheit und des Bundesministeriums für Ernährung, Landwirtschaft und Verbraucherschutz G - AV Neunte Verordnung zur Änderung
Colecalciferol. Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017
 Colecalciferol Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Überprüfung der freigestellten Tagesdosis
Colecalciferol Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Sachverständigen-Ausschuss für Verschreibungspflicht 17. Januar 2017 Seite 1 Überprüfung der freigestellten Tagesdosis
Analgetika-Gebrauch in Deutschland ( ) im internationalen Vergleich
 Analgetika-Gebrauch in Deutschland (1980-2010) im internationalen Vergleich Quelle: IMS 2010 Der Pro-Kopf-Gebrauch an OTC-Analgetika ist seit 15 Jahren rückläufig; Rx-Analgetika nehmen dagegen zu. Quelle:
Analgetika-Gebrauch in Deutschland (1980-2010) im internationalen Vergleich Quelle: IMS 2010 Der Pro-Kopf-Gebrauch an OTC-Analgetika ist seit 15 Jahren rückläufig; Rx-Analgetika nehmen dagegen zu. Quelle:
Pressemitteilung der EMEA vom in deutscher Übersetzung:
 Pressemitteilung der EMEA vom 9. 12. 2004 in deutscher Übersetzung: Außerordentliche Sitzung des CHMP zu Paroxetin und anderen selektiven Serotonin-Wiederaufnahmehemmern Der Ausschuss für Humanarzneimittel
Pressemitteilung der EMEA vom 9. 12. 2004 in deutscher Übersetzung: Außerordentliche Sitzung des CHMP zu Paroxetin und anderen selektiven Serotonin-Wiederaufnahmehemmern Der Ausschuss für Humanarzneimittel
V o t en. Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG
 Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 58. Sitzung, 16.01.2007 zu Positionen, deren Änderung abgestimmt wurde.
Bundesinstitut für Arzneimittel und Medizinprodukte V o t en des Sachverständigen-Ausschusses für Verschreibungspflicht nach 53 AMG 58. Sitzung, 16.01.2007 zu Positionen, deren Änderung abgestimmt wurde.
Sachverständigenausschuss für Verschreibungspflicht (SVA) 73. Sitzung Mometason zur intranasalen Anwendung
 Sachverständigenausschuss für Verschreibungspflicht (SVA) 73. Sitzung Mometason zur intranasalen Anwendung ANTRAG AUF ENTLASSUNG AUS DER VERSCHREIBUNGSPFLICHT Mometason und seine Ester zur nasalen Anwendung
Sachverständigenausschuss für Verschreibungspflicht (SVA) 73. Sitzung Mometason zur intranasalen Anwendung ANTRAG AUF ENTLASSUNG AUS DER VERSCHREIBUNGSPFLICHT Mometason und seine Ester zur nasalen Anwendung
Antrag auf Entlassung aus der Verschreibungspflicht. -Diclazuril-
 Antrag auf Entlassung aus der Verschreibungspflicht Antrag der Firma: Erweiterung des Eintrags in der AMVV von derzeit Diclazuril in Diclazuril ausgenommen zur Anwendung bei Bartagame und Leopardgecko
Antrag auf Entlassung aus der Verschreibungspflicht Antrag der Firma: Erweiterung des Eintrags in der AMVV von derzeit Diclazuril in Diclazuril ausgenommen zur Anwendung bei Bartagame und Leopardgecko
Antrag auf Änderung der Verordnung über verschreibungspflichtige Arzneimittel für den Wirkstoff Fluticasonpropionat in der Darreichungsform Nasenspray
 Antrag auf Änderung der Verordnung über verschreibungspflichtige Arzneimittel für den Wirkstoff Fluticasonpropionat in der Darreichungsform Nasenspray 1. Juli 2014 Gegenstand des Antrags Aufhebung der
Antrag auf Änderung der Verordnung über verschreibungspflichtige Arzneimittel für den Wirkstoff Fluticasonpropionat in der Darreichungsform Nasenspray 1. Juli 2014 Gegenstand des Antrags Aufhebung der
BESCHLUSS. des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011
 BESCHLUSS des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011 mit Wirkung zum 1. April 2012 bis zum 31. März 2014 Vergütungsvereinbarung für ärztliche Leistungen
BESCHLUSS des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011 mit Wirkung zum 1. April 2012 bis zum 31. März 2014 Vergütungsvereinbarung für ärztliche Leistungen
ZISOP Zentrum für Interdisziplinäre Schmerztherapie, Onkologie und Palliativmedizin, Center of excellence. 81jähriger Patient
 81jähriger Patient Diagnosen: - art. Hypertonie - Lumboischialgie -Coxarthrose li - Meniskusläsion li -KHK -Schlafapnoe - status post Dreifach ACB, 2003 - spastische Bronchitis - chron. Niereninsuff. -
81jähriger Patient Diagnosen: - art. Hypertonie - Lumboischialgie -Coxarthrose li - Meniskusläsion li -KHK -Schlafapnoe - status post Dreifach ACB, 2003 - spastische Bronchitis - chron. Niereninsuff. -
Erratum BESCHLUSS. des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011
 Erratum zum Beschluss des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011 mit Wirkung zum 1. April 2012 bis zum 31. März 2014 In dem Beschluss des Bewertungsausschusses
Erratum zum Beschluss des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011 mit Wirkung zum 1. April 2012 bis zum 31. März 2014 In dem Beschluss des Bewertungsausschusses
Gebrauchsinformation: Information für den Anwender. Koreanischer Reiner Roter Ginseng Kapseln
 Gebrauchsinformation: Information für den Anwender Koreanischer Reiner Roter Ginseng Kapseln Wirkstoff: Ginsengwurzel-Pulver 1 Hartkapsel enthält 300 mg rote (wasserdampfbehandelte) Ginsengwurzel, pulverisiert.
Gebrauchsinformation: Information für den Anwender Koreanischer Reiner Roter Ginseng Kapseln Wirkstoff: Ginsengwurzel-Pulver 1 Hartkapsel enthält 300 mg rote (wasserdampfbehandelte) Ginsengwurzel, pulverisiert.
ANTIBIOTIKA WIRKEN NICHT GEGEN VIREN! Keine Antibiotika gegen Viren
 ANTIBIOTIKA GEGEN VIREN! Keine Antibiotika gegen Viren ANTIBIOTIKA- KEINE WIRKUNG GEGEN VIREN! Eine ansteckende Krankheit (Infektionskrankheit) kann durch einen VIRUS, ein BAKTERIUM oder andere Mikroorganismen
ANTIBIOTIKA GEGEN VIREN! Keine Antibiotika gegen Viren ANTIBIOTIKA- KEINE WIRKUNG GEGEN VIREN! Eine ansteckende Krankheit (Infektionskrankheit) kann durch einen VIRUS, ein BAKTERIUM oder andere Mikroorganismen
Antrag auf Entlassung aus der Verschreibungspflicht. -Praziquantel-
 Antrag auf Entlassung aus der Verschreibungspflicht AMVV Antrag der Firma: Erweiterung des Eintrags um Punkt c Praziquantel ausgenommen zur Anwendung a) bei Hunden und Katzen b) bei Zierfischen der Ordnungen
Antrag auf Entlassung aus der Verschreibungspflicht AMVV Antrag der Firma: Erweiterung des Eintrags um Punkt c Praziquantel ausgenommen zur Anwendung a) bei Hunden und Katzen b) bei Zierfischen der Ordnungen
Antrag auf Freistellung aus der Verschreibungspflicht für Omeprazol 20 mg
 Antrag auf Freistellung aus der Verschreibungspflicht für Omeprazol 20 mg Sachverständigen-Ausschuss für Verschreibungspflicht 13. Januar 2009 Rationale des Antrags Omeprazol ist eine der effektivsten
Antrag auf Freistellung aus der Verschreibungspflicht für Omeprazol 20 mg Sachverständigen-Ausschuss für Verschreibungspflicht 13. Januar 2009 Rationale des Antrags Omeprazol ist eine der effektivsten
ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION
 ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION Diese Änderungen von SPC und Packungsbeilage treten zum Zeitpunkt der Kommissionsentscheidung in Kraft.
ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION Diese Änderungen von SPC und Packungsbeilage treten zum Zeitpunkt der Kommissionsentscheidung in Kraft.
Gebrauchsinformation Roter Ginseng Extrakt Hartkapseln
 Gebrauchsinformation Roter Ginseng Extrakt Hartkapseln Liebe Patientin, lieber Patient, lesen Sie die gesamte Gebrauchsinformation aufmerksam durch, denn sie enthält wichtige Informationen für Sie. Dieses
Gebrauchsinformation Roter Ginseng Extrakt Hartkapseln Liebe Patientin, lieber Patient, lesen Sie die gesamte Gebrauchsinformation aufmerksam durch, denn sie enthält wichtige Informationen für Sie. Dieses
Die Wirkungsmechanismus und die Pharmakologie der Lokalanästhetika. Dr. Noémi Kovács
 Die Wirkungsmechanismus und die Pharmakologie der Lokalanästhetika. Dr. Noémi Kovács Lokalanästhetikum Präparate = 1. Chemisches Anästhetikum +Puffersystem 2. Vasopressor +Stabilisatoren 3. Konzervierungsmittel
Die Wirkungsmechanismus und die Pharmakologie der Lokalanästhetika. Dr. Noémi Kovács Lokalanästhetikum Präparate = 1. Chemisches Anästhetikum +Puffersystem 2. Vasopressor +Stabilisatoren 3. Konzervierungsmittel
Silicea D3 Biochemisches Funktionsmittel Nr. 11
 Registriertes homöopathisches Arzneimittel, daher ohne Angabe einer therapeutischen Indikation. Gebrauchsinformation: Information für den Anwender Silicea D3 Biochemisches Funktionsmittel Nr. 11 Tabletten
Registriertes homöopathisches Arzneimittel, daher ohne Angabe einer therapeutischen Indikation. Gebrauchsinformation: Information für den Anwender Silicea D3 Biochemisches Funktionsmittel Nr. 11 Tabletten
Sicherer Schutz für alle Babys
 Sicherer Schutz für alle Babys Pneumokokken - was ist das? Bakterien Fachname: Pneumokokken oder Streptococcus pneumoniae Das Besondere: dicke Kapsel aus Zuckermolekülen (Polysachariden), schützt den Erreger
Sicherer Schutz für alle Babys Pneumokokken - was ist das? Bakterien Fachname: Pneumokokken oder Streptococcus pneumoniae Das Besondere: dicke Kapsel aus Zuckermolekülen (Polysachariden), schützt den Erreger
1.Was ist Bepanthen Wund und Heilsalbe und wofür wird es angewendet?
 1.Was ist Bepanthen Wund und Heilsalbe und wofür wird es angewendet? 1.1.Welche Eigenschaften hat das Arzneimittel? Bepanthen Wund und Heilsalbe enthält den Wirkstoff Dexpanthenol, ein Arzneimittel aus
1.Was ist Bepanthen Wund und Heilsalbe und wofür wird es angewendet? 1.1.Welche Eigenschaften hat das Arzneimittel? Bepanthen Wund und Heilsalbe enthält den Wirkstoff Dexpanthenol, ein Arzneimittel aus
Akute venösen Thromboembolien (VTE) oder VTE in der Vorgeschichte, einschließlich tiefer Venenthrombose und Lungenembolie.
 Aktualisierte Indikation Behandlung der schweren Osteoporose: bei postmenopausalen Frauen, bei erwachsenen Männern, mit hohem Frakturrisiko, für die eine Behandlung mit anderen für die Osteoporosetherapie
Aktualisierte Indikation Behandlung der schweren Osteoporose: bei postmenopausalen Frauen, bei erwachsenen Männern, mit hohem Frakturrisiko, für die eine Behandlung mit anderen für die Osteoporosetherapie
Wann wird MRSA gefährlich?
 Informationen zu MRSA für Patienten im Krankenhaus Merkblatt Sehr geehrte Patientin, sehr geehrter Patient, im Rahmen Ihrer stationären Behandlung wurde bei einer mikrobiologischen Abstrichuntersuchung
Informationen zu MRSA für Patienten im Krankenhaus Merkblatt Sehr geehrte Patientin, sehr geehrter Patient, im Rahmen Ihrer stationären Behandlung wurde bei einer mikrobiologischen Abstrichuntersuchung
Was sind die Folgen von Resistenzen?
 Was sind die Folgen von Resistenzen? Infektionen werden schwieriger zu behandeln und können lebensbedrohlich verlaufen Die Heilung von Infektionen verzögert sich Für manche Infektionen stehen kaum noch
Was sind die Folgen von Resistenzen? Infektionen werden schwieriger zu behandeln und können lebensbedrohlich verlaufen Die Heilung von Infektionen verzögert sich Für manche Infektionen stehen kaum noch
GÜRTELROSE (HERPES ZOSTER) kann man mit einer Impfung vorbeugen.
 GÜRTELROSE (HERPES ZOSTER) kann man mit einer Impfung vorbeugen. GÜRTELROSE WAS IST DAS? Die Gürtelrose, auch Herpes Zoster genannt, ist eine Viruserkrankung, die von dem selben Varizella - Zoster - Virus
GÜRTELROSE (HERPES ZOSTER) kann man mit einer Impfung vorbeugen. GÜRTELROSE WAS IST DAS? Die Gürtelrose, auch Herpes Zoster genannt, ist eine Viruserkrankung, die von dem selben Varizella - Zoster - Virus
Empfehlungen aus aktuellen evidenzbasierten Leitlinien recherchiert und zusammengestellt
 IQWiG gibt Überblick über Versorgungs-Standard bei Fettleibigkeit Empfehlungen aus aktuellen evidenzbasierten Leitlinien recherchiert und zusammengestellt Berlin (3. April 2009) - Wie in allen Industriestaaten
IQWiG gibt Überblick über Versorgungs-Standard bei Fettleibigkeit Empfehlungen aus aktuellen evidenzbasierten Leitlinien recherchiert und zusammengestellt Berlin (3. April 2009) - Wie in allen Industriestaaten
Labortests für Ihre Gesundheit. Warum und wann Antibiotika? 07
 Labortests für Ihre Gesundheit Warum und wann Antibiotika? 07 01IPF Labortests für Ihre Gesundheit Warum und wann Antibiotika? Infektionskrankheiten und ihre Behandlung heute und morgen Heutzutage ist
Labortests für Ihre Gesundheit Warum und wann Antibiotika? 07 01IPF Labortests für Ihre Gesundheit Warum und wann Antibiotika? Infektionskrankheiten und ihre Behandlung heute und morgen Heutzutage ist
16. Januar 2015 Wichtige Informationen für medizinisches Fachpersonal
 16. Januar 2015 Wichtige Informationen für medizinisches Fachpersonal zur Markteinführung von Vibativ (Telavancin): Anwendungsempfehlungen und bedeutende Risiken (Nephrotoxizität, QTc-Verlängerung, Reproduktionstoxizität
16. Januar 2015 Wichtige Informationen für medizinisches Fachpersonal zur Markteinführung von Vibativ (Telavancin): Anwendungsempfehlungen und bedeutende Risiken (Nephrotoxizität, QTc-Verlängerung, Reproduktionstoxizität
rund 200 ausgewählte Wirkstoffe
 rund 200 ausgewählte Wirkstoffe Von der Wirkstoffverordnung sind insbesondere folgende Darreichungsformen ausgeschlossen: - Arzneimittel, die auf die Haut aufgetragen werden (z.b. Salben, Gele) - Arzneimittel
rund 200 ausgewählte Wirkstoffe Von der Wirkstoffverordnung sind insbesondere folgende Darreichungsformen ausgeschlossen: - Arzneimittel, die auf die Haut aufgetragen werden (z.b. Salben, Gele) - Arzneimittel
Cannabidiol. Sachverständigen-Ausschuss für Verschreibungspflicht Sachverständigen-Ausschuss für Verschreibungspflicht
 Cannabidiol Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Seite 1 Hintergrund Arzneimittelkommission der Deutschen Apotheker
Cannabidiol Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Sachverständigen-Ausschuss für Verschreibungspflicht 19.01.2016 Seite 1 Hintergrund Arzneimittelkommission der Deutschen Apotheker
Mitteilung des Bundesamts für Sicherheit im Gesundheitswesen über Maßnahmen zur Gewährleistung der Arzneimittelsicherheit:
 Landeshauptleute Landessanitätsdirektionen Österreichische Apothekerkammer Österreichische Ärztekammer Landesärztekammern Anstaltsapotheken d. Universitätskliniken Datum: 16.03.2016 Kontakt: Mag. Rudolf
Landeshauptleute Landessanitätsdirektionen Österreichische Apothekerkammer Österreichische Ärztekammer Landesärztekammern Anstaltsapotheken d. Universitätskliniken Datum: 16.03.2016 Kontakt: Mag. Rudolf
Tragende Gründe. Vom 27. November 2015
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der -Richtlinie (AM-RL): Anlage II Lifestyle Ergänzung und Aktualisierung Vom 27. November 2015 Inhalt 1. Rechtsgrundlage...
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der -Richtlinie (AM-RL): Anlage II Lifestyle Ergänzung und Aktualisierung Vom 27. November 2015 Inhalt 1. Rechtsgrundlage...
PATIENTEN- INFORMATIONSKARTE
 PATIENTEN- INFORMATIONSKARTE Diese Patienteninformationskarte ist ein verpflichtender Teil der Zulassung, um sicherzustellen, dass Angehörige der Heilberufe, sowie Patienten die besonderen Sicherheitsanforder
PATIENTEN- INFORMATIONSKARTE Diese Patienteninformationskarte ist ein verpflichtender Teil der Zulassung, um sicherzustellen, dass Angehörige der Heilberufe, sowie Patienten die besonderen Sicherheitsanforder
1.Was sind Neurexan-Tabletten und wofür werden sie angewendet?
 1.Was sind Neurexan-Tabletten und wofür werden sie angewendet? 1.1.Welche Eigenschaften hat das Arzneimittel? Neurexan-Tabletten ist ein Kombinationspräparat sogenannter homöopathischer Arzneimittel. Das
1.Was sind Neurexan-Tabletten und wofür werden sie angewendet? 1.1.Welche Eigenschaften hat das Arzneimittel? Neurexan-Tabletten ist ein Kombinationspräparat sogenannter homöopathischer Arzneimittel. Das
Novellierung des Infektionsschutzgesetzes - Konsequenzen für die Praxis - Christoph Huesmann. Fachkrankenpfleger für Hygiene und Infektionsprävention
 Novellierung des Infektionsschutzgesetzes - Konsequenzen für die Praxis - Christoph Huesmann Fachkrankenpfleger für Hygiene und Infektionsprävention Entwicklung Bundesseuchengesetz Bekämpfung ansteckender
Novellierung des Infektionsschutzgesetzes - Konsequenzen für die Praxis - Christoph Huesmann Fachkrankenpfleger für Hygiene und Infektionsprävention Entwicklung Bundesseuchengesetz Bekämpfung ansteckender
Dossierbewertung A14-26 Version 1.0 Empagliflozin Nutzenbewertung gemäß 35a SGB V
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Empagliflozin gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Empagliflozin gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
Diagnose MS. Leitfaden zur Therapieauswahl
 Diagnose MS Leitfaden zur Therapieauswahl Vorbereitung ist alles Vor einer Entscheidung für eine Behandlung stehen viele Fragen. Zum einzelnen Wirkstoff. Zum Behandlungsplan. Zur Krankheit generell. Alles
Diagnose MS Leitfaden zur Therapieauswahl Vorbereitung ist alles Vor einer Entscheidung für eine Behandlung stehen viele Fragen. Zum einzelnen Wirkstoff. Zum Behandlungsplan. Zur Krankheit generell. Alles
MRSA. (Methicillin-resistenter Staphylococcus aureus)
 MRSA (Methicillin-resistenter Staphylococcus aureus) Gemeinsam auf Nummer sicher Liebe Patientin, lieber Patient, herzlich willkommen in der Fachklinik 360 Die Klinik für Orthopädie und Rheumatologie der
MRSA (Methicillin-resistenter Staphylococcus aureus) Gemeinsam auf Nummer sicher Liebe Patientin, lieber Patient, herzlich willkommen in der Fachklinik 360 Die Klinik für Orthopädie und Rheumatologie der
Stellenwert von Brivudin in der antiviralen Behandlung der Gürtelrose: Aktuelle Virus- und Komplikationsbekämpfung bei Herpes zoster
 17.10.2003 Prof. Dr. med. Sawko Wassilew Deutschland Stellenwert von Brivudin in der antiviralen Behandlung der Gürtelrose: Aktuelle Virus- und Komplikationsbekämpfung bei Herpes zoster Keywords: Herpes
17.10.2003 Prof. Dr. med. Sawko Wassilew Deutschland Stellenwert von Brivudin in der antiviralen Behandlung der Gürtelrose: Aktuelle Virus- und Komplikationsbekämpfung bei Herpes zoster Keywords: Herpes
Antrag auf Entlassung aus der Verschreibungspflicht. -Doramectin-
 Antrag auf Entlassung aus der Verschreibungspflicht Antrag auf Entlassung von Doramectin aus der Verschreibungspflicht für die topische Anwendung bei Königspython, Abgottschlange und Bartagame bei einem
Antrag auf Entlassung aus der Verschreibungspflicht Antrag auf Entlassung von Doramectin aus der Verschreibungspflicht für die topische Anwendung bei Königspython, Abgottschlange und Bartagame bei einem
Anhang II. Wissenschaftliche Schlussfolgerungen und Begründung für die Änderungen der Bedingungen für die Genehmigungen für das Inverkehrbringen
 Anhang II Wissenschaftliche Schlussfolgerungen und Begründung für die Änderungen der Bedingungen für die Genehmigungen für das Inverkehrbringen 14 Wissenschaftliche Schlussfolgerungen Komplette Zusammenfassung
Anhang II Wissenschaftliche Schlussfolgerungen und Begründung für die Änderungen der Bedingungen für die Genehmigungen für das Inverkehrbringen 14 Wissenschaftliche Schlussfolgerungen Komplette Zusammenfassung
MRSA. Informationen für Patienten und Angehörige
 MRSA Informationen für Patienten und Angehörige MRSA MRSA steht für Methicillinresistenter Staphylococcus aureus. Staphylococcus aureus ist ein Bakterium, das auch außerhalb des Krankenhauses bei vielen
MRSA Informationen für Patienten und Angehörige MRSA MRSA steht für Methicillinresistenter Staphylococcus aureus. Staphylococcus aureus ist ein Bakterium, das auch außerhalb des Krankenhauses bei vielen
MAVENCLAD. Informationsmaterial für verschreibende Ärzte. Version 1.0, [Stand Juli 2017]
![MAVENCLAD. Informationsmaterial für verschreibende Ärzte. Version 1.0, [Stand Juli 2017] MAVENCLAD. Informationsmaterial für verschreibende Ärzte. Version 1.0, [Stand Juli 2017]](/thumbs/77/74803261.jpg) MAVENCLAD Informationsmaterial für verschreibende Ärzte Version 1.0, [Stand Juli 2017] Inhalt Einführung Behandlungsschemata Überwachung während der Behandlung Lymphozytenzahlen Schwere Infektionen Progressive
MAVENCLAD Informationsmaterial für verschreibende Ärzte Version 1.0, [Stand Juli 2017] Inhalt Einführung Behandlungsschemata Überwachung während der Behandlung Lymphozytenzahlen Schwere Infektionen Progressive
Gebrauchsinformation: Information für den Anwender
 Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für den Anwender SQUAMASOL Gel Wirkstoff: Salicylsäure Liebe Patientin, lieber Patient! Bitte lesen Sie die gesamte
Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für den Anwender SQUAMASOL Gel Wirkstoff: Salicylsäure Liebe Patientin, lieber Patient! Bitte lesen Sie die gesamte
Kriterien zur Unterscheidung von AM/ NEM und bilanzierten Diäten
 Rechtliche Einteilung Arzneimittel Nahrungsergänzungsmittel Ergänzende bilanzierte Diät Gesetz AMG NemV und LFGB DiätV und LFGB Zweck Vorbeugung, Linderung und Heilung von Krankheiten oder Beeinflussung
Rechtliche Einteilung Arzneimittel Nahrungsergänzungsmittel Ergänzende bilanzierte Diät Gesetz AMG NemV und LFGB DiätV und LFGB Zweck Vorbeugung, Linderung und Heilung von Krankheiten oder Beeinflussung
10. Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 ARZNEIMITTELRECHT Notfallmedikation bei anaphylaktischen Reaktionen. 10. Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Die Arzneimittelkommission deutscher Heilpraktiker als Stufenplanbeteiligte
ARZNEIMITTELRECHT Notfallmedikation bei anaphylaktischen Reaktionen. 10. Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Die Arzneimittelkommission deutscher Heilpraktiker als Stufenplanbeteiligte
Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 7 Famciclovir
 Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 7 Famciclovir Antrag auf Entlassung aus der Verschreibungspflicht Famciclovir zur oralen Behandlung von rezidivierenden Episoden
Sachverständigenausschuss für Verschreibungspflicht (SVA) 72. Sitzung, TOP 7 Famciclovir Antrag auf Entlassung aus der Verschreibungspflicht Famciclovir zur oralen Behandlung von rezidivierenden Episoden
Tragende Gründe zum Beschluss. des Gemeinsamen Bundesausschusses über die Änderung der Arzneimittel-Richtlinie (AM-RL):
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über die Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage 1 (OTC-Übersicht) Nr. 20 Ginkgo-biloba-Blätter-Extrakt Vom 14. April 2011 Inhaltsverzeichnis
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über die Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage 1 (OTC-Übersicht) Nr. 20 Ginkgo-biloba-Blätter-Extrakt Vom 14. April 2011 Inhaltsverzeichnis
MAVENCLAD. Informationsmaterial für Patienten. Version 1.0, [Stand Juli 2017]
![MAVENCLAD. Informationsmaterial für Patienten. Version 1.0, [Stand Juli 2017] MAVENCLAD. Informationsmaterial für Patienten. Version 1.0, [Stand Juli 2017]](/thumbs/78/78512222.jpg) MAVENCLAD Informationsmaterial für Patienten Version 1.0, [Stand Juli 2017] Wichtige Informationen für Patienten, die eine Therapie mit Mavenclad beginnen Inhalt Einführung Wie erfolgt die Behandlung mit
MAVENCLAD Informationsmaterial für Patienten Version 1.0, [Stand Juli 2017] Wichtige Informationen für Patienten, die eine Therapie mit Mavenclad beginnen Inhalt Einführung Wie erfolgt die Behandlung mit
1.Was ist Mutaflor und wofür wird es eingenommen?
 1.Was ist Mutaflor und wofür wird es eingenommen? 1.1.Welche Eigenschaften hat das Arzneimittel? Mutaflor enthält den Wirkstoff Escherichia coli Stamm Nissle 1917, ein Arzneimittel aus der Gruppe der sogenannten
1.Was ist Mutaflor und wofür wird es eingenommen? 1.1.Welche Eigenschaften hat das Arzneimittel? Mutaflor enthält den Wirkstoff Escherichia coli Stamm Nissle 1917, ein Arzneimittel aus der Gruppe der sogenannten
MRSA Schluss mit Mythen
 Stefan Borgmann MRSA Schluss mit Mythen Klinikum Ingolstadt Neue MRSA Antibiotika Name Wirkort Indikation Keine Indikation Nebenwirkungen Kontraindikation Dosierung Kosten / Tag Ceftarolin (Zinforo) (Teflaro)
Stefan Borgmann MRSA Schluss mit Mythen Klinikum Ingolstadt Neue MRSA Antibiotika Name Wirkort Indikation Keine Indikation Nebenwirkungen Kontraindikation Dosierung Kosten / Tag Ceftarolin (Zinforo) (Teflaro)
Daraus machen wir eine natürliche Therapie gegen Nervenschmerzen
 Daraus machen wir eine natürliche Therapie gegen Nervenschmerzen Wenn Nerven schmerzen und Schmerzen nerven! Was sind Nervenschmerzen? Nervenschmerzen, die man in der Fachsprache auch als Neuralgien bezeichnet,
Daraus machen wir eine natürliche Therapie gegen Nervenschmerzen Wenn Nerven schmerzen und Schmerzen nerven! Was sind Nervenschmerzen? Nervenschmerzen, die man in der Fachsprache auch als Neuralgien bezeichnet,
zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage I OTC-Übersicht
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage I OTC-Übersicht Vom 16. August 2018 Inhalt 1. Rechtsgrundlage... 2 2. Eckpunkte
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage I OTC-Übersicht Vom 16. August 2018 Inhalt 1. Rechtsgrundlage... 2 2. Eckpunkte
Herpes simplex Virus A C H T U N G S C H L Ä F E R! M. Janiec
 Herpes simplex Virus A C H T U N G S C H L Ä F E R! M. Janiec Beschreibung Auch als Lippenherpes bekannt Viruserkrankung durch Herpes-simplex-Virus Typ 1 (HSV Typ1) kleine nässende Bläschen, empfindlich,
Herpes simplex Virus A C H T U N G S C H L Ä F E R! M. Janiec Beschreibung Auch als Lippenherpes bekannt Viruserkrankung durch Herpes-simplex-Virus Typ 1 (HSV Typ1) kleine nässende Bläschen, empfindlich,
Antrag auf Entlassung aus der Verschreibungspflicht
 Antrag auf Entlassung aus der Verschreibungspflicht Zolmitriptan 2,5 mg zur Behandlung des akuten Migräneanfalls (Zomig Filmtabletten und Schmelztabletten) Sachverständigenausschuss für Verschreibungspflicht
Antrag auf Entlassung aus der Verschreibungspflicht Zolmitriptan 2,5 mg zur Behandlung des akuten Migräneanfalls (Zomig Filmtabletten und Schmelztabletten) Sachverständigenausschuss für Verschreibungspflicht
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
B E S C H L U S S. des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 316. Sitzung (schriftliche Beschlussfassung)
 B E S C H L U S S des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 316. Sitzung (schriftliche Beschlussfassung) Teil A zur Änderung des Einheitlichen Bewertungsmaßstabes (EBM) mit Wirkung
B E S C H L U S S des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 316. Sitzung (schriftliche Beschlussfassung) Teil A zur Änderung des Einheitlichen Bewertungsmaßstabes (EBM) mit Wirkung
Sachverständigen-Ausschuss für Verschreibungspflicht 74. Sitzung Colocynthidis fructus zur oralen Anwendung
 Sachverständigen-Ausschuss für Verschreibungspflicht 74. Sitzung Colocynthidis fructus zur oralen Anwendung ANTRAG AUF ENTLASSUNG AUS DER VERSCHREIBUNGSPFLICHT Colocynthidis fructus und ihre Zubereitungen
Sachverständigen-Ausschuss für Verschreibungspflicht 74. Sitzung Colocynthidis fructus zur oralen Anwendung ANTRAG AUF ENTLASSUNG AUS DER VERSCHREIBUNGSPFLICHT Colocynthidis fructus und ihre Zubereitungen
Verordnung zur Änderung der Arzneimittelverschreibungsverordnung und der Verordnung über apothekenpflichtige und freiverkäufliche Arzneimittel
 Bundesrat Drucksache 705/13 (Beschluss) 08.11.13 Beschluss des Bundesrates Verordnung zur Änderung der Arzneimittelverschreibungsverordnung und der Verordnung über apothekenpflichtige und freiverkäufliche
Bundesrat Drucksache 705/13 (Beschluss) 08.11.13 Beschluss des Bundesrates Verordnung zur Änderung der Arzneimittelverschreibungsverordnung und der Verordnung über apothekenpflichtige und freiverkäufliche
Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Absatz 2 des Arzneimittelgesetzes. Ergebnisprotokoll. 77. Sitzung
 Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Absatz 2 des Arzneimittelgesetzes Ergebnisprotokoll 77. Sitzung 17. Januar 2017 Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM),
Sachverständigen-Ausschuss für Verschreibungspflicht nach 53 Absatz 2 des Arzneimittelgesetzes Ergebnisprotokoll 77. Sitzung 17. Januar 2017 Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM),
1.Was ist Lasea Kapseln und wofür wird es angewendet?
 1.Was ist Lasea Kapseln und wofür wird es angewendet? 1.1.Welche Eigenschaften hat das Arzneimittel? Lasea Kapseln enthält den Wirkstoff Lavendelöl, ein Arzneimittel aus der Gruppe der sogenannten pflanzlichen
1.Was ist Lasea Kapseln und wofür wird es angewendet? 1.1.Welche Eigenschaften hat das Arzneimittel? Lasea Kapseln enthält den Wirkstoff Lavendelöl, ein Arzneimittel aus der Gruppe der sogenannten pflanzlichen
Beschluss. II. Dieser Beschluss tritt mit Beschlussfassung in Kraft.
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung des Beschlusses zur Änderung des Beschlusses zur Neufassung der Richtlinien über die Früherkennung von Krankheiten bei Kindern bis zur Vollendung
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung des Beschlusses zur Änderung des Beschlusses zur Neufassung der Richtlinien über die Früherkennung von Krankheiten bei Kindern bis zur Vollendung
nachrichtlich: Stufenplanbeteiligte, Zul mit DE= CMS
 - 2 - Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn pharmazeutische Unternehmer mit DE=RMS, nat. Zul, Parallelimp nachrichtlich: Stufenplanbeteiligte,
- 2 - Bundesinstitut für Arzneimittel und Medizinprodukte BfArM Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn pharmazeutische Unternehmer mit DE=RMS, nat. Zul, Parallelimp nachrichtlich: Stufenplanbeteiligte,
Gebrauchsinformation: Information für Patienten
 1/5 Gebrauchsinformation: Information für Patienten Tropfen gegen Rheuma und Gicht Similasan Arnica montana D 8, Ledum palustre D 6, Pulsatilla pratensis D 8, Rhus toxicodendron D 6, Filipendula ulmaria
1/5 Gebrauchsinformation: Information für Patienten Tropfen gegen Rheuma und Gicht Similasan Arnica montana D 8, Ledum palustre D 6, Pulsatilla pratensis D 8, Rhus toxicodendron D 6, Filipendula ulmaria
Antibiotika- Ratgeber. Information für Patienten, Angehörige und Besucher
 Antibiotika- Ratgeber Information für Patienten, Angehörige und Besucher Wie wirkt ein Antibiotikum? Wenn Bakterien in unseren Körper eindringen, sich vermehren, damit das Abwehrsystem unseres Körpers
Antibiotika- Ratgeber Information für Patienten, Angehörige und Besucher Wie wirkt ein Antibiotikum? Wenn Bakterien in unseren Körper eindringen, sich vermehren, damit das Abwehrsystem unseres Körpers
Gebrauchsinformation: Information für Patienten
 Tropfen gegen Akne Similasan 1 Gebrauchsinformation: Information für Patienten Tropfen gegen Akne Similasan Acidum arsenicosum D 12, Clematis recta D 8, Graphites D 12 Lesen Sie die gesamte Packungsbeilage
Tropfen gegen Akne Similasan 1 Gebrauchsinformation: Information für Patienten Tropfen gegen Akne Similasan Acidum arsenicosum D 12, Clematis recta D 8, Graphites D 12 Lesen Sie die gesamte Packungsbeilage
