Protokoll. Gaschromatografie. Assistent: Frau Genest. Gruppe 24: Christine Albrecht Juliane Fink Jörg Kluge Lydia Köhler
|
|
|
- Götz Egger
- vor 6 Jahren
- Abrufe
Transkript
1 Protokoll Gaschromatografie Assistent: Frau Genest Gruppe 24: Christine Albrecht Juliane Fink Jörg Kluge Lydia Köhler Datum des Experiments:
2 Vorbetrachtung Die betrachtete Gas-Flüssigkeits-Chromatografie gehört mit zur Verteilungschromatografie, bei der sich das aufzutrennende Gemisch im Gleichgewicht zwischen einer mobilen und einer stationären Phase befindet. Daneben gibt es aber auch die Adsorptionschromatografie in Form der GSC, Gas-Festkörper-Chromatografie, bei welcher der Analyt an der festen Phase adsorbiert wird. Gleich ist allen Gaschromatografiearten, dass die zu analysierende Probe verdampft und mit Hilfe eines Trägergases durch die Säule transportiert wird. Hieraus resultiert auch eine Nutzungsbeschränkung: Um ein Substanzgemisch mit der Gaschromatografie (GC) untersuchen zu können, müssen dessen Bestandteile eine ausreichende Flüchtigkeit besitzen, dass heißt sie sollten keine zu hohen Siedepunkte besitzen. Zudem dürfen sie sich beim Verdampfen weder zersetzen noch umwandeln. Einen Ausweg bietet die so genannte Headspace-Technik, bei der nur die sich über einer nicht vollständig verdampfbaren Phase befindliche Gasphase genutzt wird. In dieser Phase haben sich die Komponenten angereichert, die leichter flüchtig sind; schwerflüchtige Komponenten gelangen so nicht in die Apparatur und können sie nicht verschmutzen. Der allgemeine Aufbau einer GC-Apparatur ist folgender: Der erste wichtige Bestandteil ist der Injektor: Man kann mit Hilfe einer Injektionsspritze die zu untersuchende Flüssigkeit injizieren, welche dann durch die hohe Temperatur, die dort wie auch in der Säule herrscht, verdampft, oder man injiziert eine gasförmige Probe. Vom Injektor aus transportiert der konstante Strom des Trägergases die Probe durch die Säule. Dort geht die Probe Wechselwirkungen mit der stationären Phase ein. Dadurch kommt es zur Auftrennung des Gemisches: Je flüchtiger eine Komponente ist, desto schneller passiert sie die Säule. Es gibt zwei Arten von Säulen: Gepackte und Kapillarsäulen. Erstere besteht aus einem Mantel aus Glas, Metall oder Teflon und dem festen körnigen Trägermaterial. Genutzt werden sie für präparative Trennung, für Proben größerer Menge oder für Analyten, die mit oder kurz nach der Totzeit eluieren. Insgesamt werden gepackte Säulen allerdings nur noch selten genutzt. Die Kapillarsäulen bestehen ebenso aus einem Mantel und zusätzlich einer dünnen Schicht einer festen Trägersubstanz, einer flüssigen stationären Phase mit fester Trägersubstanz oder einem Flüssigfilm. Diese Säulen werden sowohl in der qualitativen als auch in der quantitativen Analytik bevorzugt verwendet, da sie eine bessere Trennleistung und insgesamt kürzere Analysezeiten besitzen. Eine wichtige Größe ist die Retentionszeit, welche in Brutto- und Nettoretentionszeit unterteilt wird. Dabei gibt erstere (t r ) die Zeit an, in der eine Probe durch das System vom Injektor bis zum Detektor (Peakmaximum) strömt. Die Totzeit t(0) ist die Retentionszeit von mobiler 2
3 Phase /Stoffen ohne Wechselwirkung. Man kann sie experimentell nur annähernd bestimmen, indem man einen nicht mit der stationären Phase interagierenden Stoff zusetzt und dessen Durchlaufzeit bis zum Detektor bestimmt. Dagegen ist die Nettoretentionszeit t n, oder reduzierte Retentionszeit die Differenz von Bruttoretentionszeit und Totzeit, also t n =t r -t 0. Damit entspricht sie der Verweilzeit der Probe, die durch Wechselwirkungen mit der stationären Phase verursacht wurde. Beeinflussen lässt sich diese Größe durch die Temperatur und den Druck. Bei Temperaturerhöhung wird das (theoretische) Gleichgewicht eines Stoffes zwischen mobiler und stationärer Phase zur mobilen verschoben. Wenn man den Druck erhöht, so steigert sich die Strömungsgeschwindigkeit, was einen großen Einfluss auf die Effizienz charakterisierende Bodenhöhe hat. Den Zusammenhang zwischen der Strömungsgeschwindigkeit und theoretischer Bodenhöhe wird durch die van-deemter-gleichung beschrieben: mit H = A + B/u + C u A Konstante für die Eddy-Diffusion; B für die Longitudinaldiffusion; C für den Massenübergang Diese Funktion besitzt ein Minimum, an dem die theoretische Bodenhöhe der Säule am kleinsten ist und damit die Effizienz am größten. Bei dieser Strömungsgeschwindigkeit erfolgt die beste Trennung der Analyten. Die Eddy-Diffusion beschreibt die rein mechanische Hinderung der Moleküle an der stationären Phase, die durch die verschiedenen Größen und damit unterschiedlichen Wegen durch die Säule Zustande kommt und schon eine geringe Vortrennung der Substanzen verursacht. Dieser Effekt ist unabhängig von der Strömungsgeschwindigkeit. Die Konstante B beschreibt die Longitudinaldiffusion, die in Folge von Konzentrationsunterschieden in der Säule auftritt und die durch eine höhere Strömungsgeschwindigkeit der mobilen Phase klein gehalten werden kann. Der eigentlich chromatographische Effekt, die Wechselwirkungen der Analyten mit der stationären Phase, wird durch die Konstante C beschrieben. Es ist also eine Strömungsgeschwindigkeit zu wählen, bei welcher der Term B/u minimal und der Ausdruck C u maximal wird, damit die Bodenhöhe minimiert und somit die Trennleistung so groß wie möglich ist. Am Ende der Säule befindet sich der Detektor. Dieser kann zum Beispiel ein Massenspektrometer, Wärmeleitfähigkeits- (WLD), Flammenionisations- (FID) oder Elektronenanlagerungsdetektoren (ECD) sein. Die Detektion mittels WLD erfolgt durch die unterschiedlichen Wärmeleitfähigkeiten von Gasen, wodurch eine von dem Gas umströmte, von außen geheizte Wendel ihre Temperatur und damit ihren Widerstand ändert. Beim ECD schließlich wird die Probe mit β-strahlen beschossen, die Elektronen aus den Molekülen oder Atomen herausschlagen und nachgewiesen werden. Wir verwendeten einen Flammenionisationsdetektor (FID). Hierbei wird der Analyt in einer Flamme ionisiert, wodurch ein Strom fliesen kann. Dabei werden reinster Wasserstoff und synthetische Luft durch einen Kettenreaktionsmechanismus kontrolliert verbrannt. Die Düse ist die Kathode und die Sammelelektrode die Anode. Beim Erhitzen bilden sich Kohlenwasserstoffradikale und angeregter Sauerstoff, wenn diese zusammen reagieren wird ein Elektron abgegeben und dieses wird in der Sammelelektrode gesammelt und gemessen. Diese Methode ist besonders gut für organische Verbindungen mit C-C- und C-H- Bindung. 3
4 Die Gas-Flüssigkeits-Chromatografie kann zur quantitativen wie qualitativen Auswertung von Proben genutzt werden, wobei die quantitative Bestimmung über die Peakhöhe bzw. fläche und die qualitative über die reduzierten Retentionszeiten erfolgt. Zum Vergleichen von Retentionszeiten wurde der Kovatsindex erstellt, der den Zusammenhang zwischen reduzierter Retentionszeit t R und Kohlenstoffanzahl z einer homologen Reihe beschreibt: lgt Ri lgt Rz I i = 100 zi = 100 z lgt R z t ( + 1) lg Rz Der Komponente i kann hiermit eine Kohlenstoffanzahl z i zugeordnet werde. Durchführung: Die Messparameter des Chromatographen: Kapillarsäule: Filmdicke = 0,25 µm Innendurchmesser = 0,32 µm Länge = 28,5 m Stationäre Phase = Polydimethylsiloxan Trägergas = N 2 GC-Bedingungen: Injektortemperatur = 325 Injektion = Splittless Front-Detektor = WDL Back-Detektor =FID Brenngase =H 2 und synth. Luft Aufbereiten der Bodenproben: Bodenprobe 1: Bodenprobe A: unkontaminiert; Sächsische Schweiz Kletterberg; am aus einer Bodentiefe von 125 cm von Frau Mayer genommen kontaminiert; ehemalige Schlosserei Lukas ; am aus einer Bodentiefe von 128 cm von Frau Mayer genommen Es werden jeweils 20 g der Bodenprobe eingewogen und mit 20 ml Aceton gut geschüttelt. Danach gibt man 1 ml n-hexan hinzu, verschließt die Erlenmeyerkolben und stellt sie für 15 min ins Ultraschallbad. Sodann werden die Proben mit 30ml entionisiertem Wasser versetzt, geschüttelt und zum Absetzten stehen gelassen. Anschließend werden alle Flüssigkeiten abdekantiert, in einen 100ml Maßkolben überführt und bis über die Eichmarke mit destilliertem Wasser aufgefüllt. Dann werden 5 Spatelspitzen NaCl hinzu gegeben, der Maßkolben verschlossen und gut geschüttelt. Die Proben werden 5 min stehen gelassen, damit sich die Phasen trennen, danach werden die obige Phase (n-hexan und Schwebeteilchen) in ein Zentrifugenglas überführt und 5 min bei 3000 U/min zentrifugiert. Es werden etwa 2 ml abpipettiert, mit 3 Spatelspitzen MgSO 4 sowie 3 Spatelspitzen Forisil gut geschüttelt und 5 min absetzen gelassen. Nun wird 1ml klare Lösung in ein GC-Vial überführt. Abfolge der Injektionen: Um sich mit dem Aufbau und der Wirkungsweise des Chromatographen vertraut zu machen, laden wir das Programm ausheize.m und spritzen 1µl n-hexan zur Reinigung ein. 4
5 Damit man entscheiden kann, welche Methode die besseren Ergebnisse liefert, injizieren wir jeweils 1µl Standardmischung aus n-alkanen(c 10 H 22 /C 12 H 26 /C 14 H 30 ) in n-hexan bei den verschiedenen isothermen Programmen alk100.m und alk140.m. Anschließend wird wieder wie zu Beginn gereinigt und 1µl Lösung des Lampenöls mit alk100.m gemessen. Als nächstes wird 1µl Gemisch aus n-alkanen von C 10 H 22 bis C 16 H 34 in n-hexan und die 1µl Lösung des Lampenöls bei einem definierten Temperaturgradienten im Programm alkane.m chromatographiert. Nun werden die Extrakte der Bodenproben mit boden.m gemessen und anschließend wird wieder mit ausheize.m und 1µl n-hexan gereinigt. Programme: Methode alk100.m alk140.m alkane.m boden.m ausheize.m Temperatur Start 100 C 140 C 80 C Temperatur Max 280 C Gradient C/min 25 C/min 50 C/min Verweilzweit 27 min 10 min 2 min 2 min 1 min Start 1 min 5 min 4 min Verweilzeit Ende Gesamtzeit 11 min 17 min 9,5 min Auswertung (Anmerkung: Wenn im Folgenden von C n die Rede ist, wird dies als Kürzel für C n H 2n+2 genutzt.) Messung von n-alkanen (C 10, C 12, C 14 ) bei 100 C bzw. 140 C Bei dem ersten Chromatogramm bei niedrigerer Temperatur erkennt man 3 klar getrennte Peaks, den ersten von C 10 bei 3,668 min, darauf folgt C 12 bei 8,242 min und mit etwas Abstand C 14 mit 24,817 min. Dagegen sind im 2. Chromatogramm bei einer 40 K höheren Temperatur die beiden ersten Peaks zu einem einzigen breiten bei 3,1 min verschmolzen, darauf folgt der Peak von C 14 bei 5,472 min. Die allgemeine Verkürzung der Retentionszeit ergibt sich daraus, dass diese bei unpolaren Phasen größtenteils von dem Dampfdruck der untersuchten Gase beeinflusst wird, der laut der Clausius-Clapeyron-Gleichung folgenden Zusammenhang mit der Temperatur hat: ΔH v ln p = - +C RT Damit ist klar, dass die erste Methode trennungstechnisch zu bevorzugen ist. Zusammenhang zw. reduzierter Retentionszeit t r und Kohlenstoffanzahl n c Zur Berechnung der reduzierten Retentionszeit t r ist zunächst die Totzeit t 0 nach der Methode von Haferkamp zu bestimmen: t * t -(t ) 2 r1 r3 r2 t 0 = t r1 + t r3-2t r2 mit 1 = C10, 2= C12, 3 = C14 2 3,668 * 24,817 - (8,242) t 0 = 3, ,817-2 * 8,242 1,925 [min] 5
6 1,6 1,4 1,2 lg tr 1 0,8 0,6 0,4 0,2 y = 0,2796x - 2,5547 R 2 = Anzahl C Wie man sieht, besteht ein linearer Zusammenhang. Dabei werden längerkettige Alkane stärker von der stationären Phase zurückgehalten als kurzkettige, da die Verdampfungsenthalpie bei jedem weiteren Kohlenstoffatom in der Kette um einen nahezu gleichen Betrag zunimmt. Identifizierung der zusätzlichen Peaks im Lampenöl Es ist zu vermuten, dass die zwischen den Peaks von C 10, C 12 und C 14 liegenden Höhen diejenigen der ausgelassenen Ketten C 11 und C 13 sein sollten. Mit der oben ermittelten Geradengleichung kann man dies überprüfen: Lg t r = 0,2796 * n C 2,5547 n c = (Lg t r + 2,5547) / 0, unbekannter Peak bei t b = 5,25 min n c = (Lg (5,25 1,925) + 2,5547) / 0,2796 = 11, hoher unbekannter Peak bei t b = 14,499 min n c = (Lg (14,499 1,925) + 2,5547) / 0,2796 = 13, Die anfängliche Vermutung hat sich also bestätigt, bei den unbekannten Stoffen handelt es sich um C 11 und C 13. Die kleineren Peakhaufen sind wahrscheinlich durch Isomere zustande gekommen. Messung ohne und mit Temperaturgradient Bei den Messungen mit konstanter Temperatur sind beim Standard wie auch beim Lampenöl die ersten Peaks recht dicht beieinander und die späteren in einem großen Abstand, außerdem geraten sie recht flach und asymmetrisch (die Bezeichnung lautet Fronting für unseren Fall). Mit der Variation der Temperatur versucht man dieses allgemeine Elutionsproblem zu lösen. 6
7 Dazu beginnt man die Messung mit niedrigen Temperaturen an, damit die Anfangspeaks sich nicht überlagern, und steigert T dann. Das Resultat sieht man in unseren späteren Chromatogrammen: Alle Peaks liegen dichter beieinander - mit Zeitunterschieden von etwa einer halben Minute, wo vorher bis zu 9,4 min Unterschied waren (C 13 und C 14 ). Wo sich die Spitze des C14 durch die lange Verweilszeit im System deutlich nach rechts neigte, ist die Symmetrie bei variierter Temperatur eindeutig verbessert. Insgesamt brachte der Temperaturgradient eine große Zeitersparnis; der isotherme Durchlauf benötigte mit ca. 25 Minuten (Abklingen des letzten großen Peaks) etwa 18 Minuten mehr. Dies macht die Nutzung eines Temperaturgradienten wirtschaftlich sehr erstrebenswert, wenn es zum Beispiel in der Forschung um eine große Anzahl von Analysen pro Tag geht. Aufgund all dieser Punkte würden wir bei komplexen Gemischen, deren Siedetemperaturen weit auseinander liegen, die Methode mit Temperatursteigerung wählen. Die Herstellung von Mineralöl, Benzin, Diesel und Lampenöl Mineralöl ist der Sammelbegriff der überwiegend aus Erdöl gewonnen Stoffe wie Benzin, Diesel und Lampenöl, wobei nach einer groben Reinigung des Rohöls dessen flüchtigere und weniger flüchtigere Bestandteile mittels fraktionierter Destillation getrennt werden. Dabei tritt das Öl unten in den Säulenofen ein, wo die heißeste Temperatur von etwa 400 C herrscht. Die jetzt noch flüssigen Bestandteile sind z.b. Teer und Schmieröle, die gasförmigen Steigen nach oben in einen etwas kälteren Boden. Jeder Boden enthält oben Öffnungen mit darüber gestülpten Glocken, damit die Öldämpfe passieren können, und Überlaufrohre, um die flüssigen Teile abzutrennen. Die Reihenfolge ist (Fraktion mit Siedepunkt; Verwendung): - Koks, Schmieröle, Schweröle über 370 C - Mittelschwere Öle von C; Diesel, Heizöl - Kerosin von C; Lampenöl, Heizöl, Turbinentreibstoff, LM - Benzin von C; Kraftstoff, LM - Petrolether von C; LM - Gase unter 30 C; Heizgas In den Kraftstoffen sind auch bis zu 42 % Aromaten und 18% Alkene enthalten (Zusammensetzung von Benzin gemäß EU-Richtlinie), aber zum größten Teil bestehen sie aus Alkanen. Diese werden im Anschluss an die Destillation noch gecrackt; dabei werden langkettige Kohlenwasserstoffe thermisch oder katalytisch in kurzkettige gespalten. Im Vergleich zum Benzin (großteils C 5 bis C 12 ) hat Diesel (hauptsächlich C 10 C 28 ) mehr schwere Anteile, weswegen er auch stärker beim Verbrennen rußt. Lampenöl liegt mit C 10 bis C 16 dazwischen. Ein alternativer Weg zur Benzinherstellung ist die Fischer-Tropsch-Synthese, wobei Synthesegas, ein CO/H2-Gemisch, in Alkane, Alkene und Alkohole umgewandelt wird. n CO + (2 n +1) H 2 C n H 2n+2 + n H 2 O n CO + 2 n H 2 (CH 2 ) n + n H 2 O C n H 2n+1 OH + (n-1) H 2 O 7
8 Schlussendlich kann man annehmen, dass entsprechend der unterschiedlichen Molekülkettenlänge Benzin als Stoff mit der kürzesten C-Kette und dem geringsten Siedepunkt die kürzeste Retentionszeit hat und somit als erster Peak auf dem Chromatogramm erscheint. Danach folgt Lampenöl und abschließend Diesel. Da Letzterer aus mehr Molekülsorten unterschiedlicher Kettenlänge besteht als die anderen beiden Öle, sollte er auch die breitesten Peaks aufweisen. Quellen: Chemie von Flörke / Wolff; Mineralöl und Raffinerien vom MWV, Wikip. Bodenproben Probe I Probe A Unkontaminiert Kontaminiert Sächsische Schweiz Kletterberg ehemalige Schlosserei Lukas genommen am genommen am aus 125 cm Tiefe aus 128 cm Tiefe Auch die unkontaminierte Probe ist nicht vollständig schadstofffrei. Die geringen Spuren von C14 und winzigen Mengen von C12, C13, C15, C16 und höheren Ketten (noch niedrigere Peaks als bei den bisher genannten) können beispielsweise von Bergsteigern eingeschleppt worden sein. Viele andere Leute werden auch nicht zum Fundort, einem Kletterberg in der Sächsischen Schweiz, kommen. Die kontaminierte Probe weist, wenn man ihr Chromatogramm mit dem unseres C10 C16 Standards vergleicht, größere Peaks ab C14 auf. Die hauptsächlichen Öl-Bestandteile sind jedoch Ketten mit einer Länge von um die 24 Kohlenstoffatome. Durch Vergleich mit dem Mineralölkatalog kann man folgende Stoffe hinter den Verunreinigungen vermuten: S1 Sumurol CM10 / Gestrich: Kühlschmierstoff, dient als Lagerschmieröl bei hohen Drehzahlen S10 Sulnit UP (aral): ebenfalls Kühlschmierstoff, wird benutzt beim Schleifen und Schneiden von Buntmetall und Stahllegierungen Rein vom Aussehen der beiden Chromatogramme kann man nicht sagen, welches passender wäre, oder mit Bestimmtheit behaupten, dass die Verunreinigung definitiv eine der beiden Substanzen ist. Jedoch liegt die Schlussfolgerung nahe, dass Öle von der Schlosserei, die sich früher am Fundort befand, den Boden kontaminieren. Die beiden in Erwägung gezogenen Substanzen sind Kühlschmierstoffe, die durchaus in Schlossereien benutzt werden, und passen somit hervorragend in den Rahmen. Retentionszeitfenster Normalerweise wird das Retentionszeitfenster (RTW) bestimmt, um eine Vorstellung von dem Bereich zu bekommen, in welchem die Peaks zu erwarten sind. In unserem Fall lag schon ein gut eingerichtetes System mit bereits erprobtem Temperaturgradienten vor. Außerdem wurden vor der eigentlichen Probenbestimmung Standardlösungen hinzu gegeben, durch die ersichtlich war, in welchem Bereich die Signale von dem Lampenöl bzw. den Bodenproben liegen würden. Zuletzt ist ein Retentionszeitfenster besonders für die Integration der Peaks wichtig, welche in diesem Versuch unnötig war, da dessen Ziel eine rein qualitative Analyse war. 8
Umweltanalytik Praktikum 1. Seminartag
 Umweltanalytik Praktikum 1. Seminartag Inhalt 1. Allgemeines 2. Praktikums-Programm 3. Gaschromatographie - Physikalische Grundlagen - GC-Apparatur - Injektion - GC-Säulen - Detektoren - Trennung und Auflösung
Umweltanalytik Praktikum 1. Seminartag Inhalt 1. Allgemeines 2. Praktikums-Programm 3. Gaschromatographie - Physikalische Grundlagen - GC-Apparatur - Injektion - GC-Säulen - Detektoren - Trennung und Auflösung
Analytische Chemie (für Biol. / Pharm. Wiss.)
 Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst HCI D323 Martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/ Zusammenfassung
Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst HCI D323 Martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/ Zusammenfassung
Überblick Inhalt. Grundlagen Chromatographie. Gaschromatographie. Aufbau. Probenaufgabesysteme. Einsatzgebiete der Gaschromatographie
 Überblick Inhalt Grundlagen Chromatographie Gaschromatographie Aufbau Probenaufgabesysteme Einsatzgebiete der Gaschromatographie Beispielchromatogramm Seite 2 Warum Chromatographie? Zu untersuchende Proben
Überblick Inhalt Grundlagen Chromatographie Gaschromatographie Aufbau Probenaufgabesysteme Einsatzgebiete der Gaschromatographie Beispielchromatogramm Seite 2 Warum Chromatographie? Zu untersuchende Proben
Grundlagen der Chromatographie
 Grundlagen der Chromatographie Was ist Chromatographie? Trennung ähnlicher Moleküle aus komplexen Gemischen o Die Analyte werden in einer mobilen Phase gelöst und darin durch eine stationäre Phase transportiert.
Grundlagen der Chromatographie Was ist Chromatographie? Trennung ähnlicher Moleküle aus komplexen Gemischen o Die Analyte werden in einer mobilen Phase gelöst und darin durch eine stationäre Phase transportiert.
BGI (bisher ZH 1/120.59) Verfahren zur Bestimmung von α-chlortoluol
 BGI 505.59 (bisher ZH 1/120.59) Verfahren zur Bestimmung von α-chlortoluol Hauptverband der gewerblichen Berufsgenossenschaften Fachausschuß "Chemie" Dezember 1996 Erprobtes und von den Berufsgenossenschaften
BGI 505.59 (bisher ZH 1/120.59) Verfahren zur Bestimmung von α-chlortoluol Hauptverband der gewerblichen Berufsgenossenschaften Fachausschuß "Chemie" Dezember 1996 Erprobtes und von den Berufsgenossenschaften
WS 2016/17 R. Vasold. Chromatographie IV. Chromatographie IV. GC Seminar
 GC Seminar 1 Chromatographie II GC Seminar 2 I.1 Einleitung (siehe Skript Praktikum) I.2 Ziele des Praktikums I.3 Die stationäre Phase I.4 Die mobile Phase I.5 Der Säulenofen I.6 Die Injektionseinheit
GC Seminar 1 Chromatographie II GC Seminar 2 I.1 Einleitung (siehe Skript Praktikum) I.2 Ziele des Praktikums I.3 Die stationäre Phase I.4 Die mobile Phase I.5 Der Säulenofen I.6 Die Injektionseinheit
BGI 505.55 (bisher ZH 1/120.55) Verfahren zur Bestimmung von cis- und trans-1,3- Dichlorpropen
 BGI 505.55 (bisher ZH 1/120.55) Verfahren zur Bestimmung von cis- und trans-1,3- Dichlorpropen Hauptverband der gewerblichen Berufsgenossenschaften Fachausschuß "Chemie" November 1994 Erprobtes und von
BGI 505.55 (bisher ZH 1/120.55) Verfahren zur Bestimmung von cis- und trans-1,3- Dichlorpropen Hauptverband der gewerblichen Berufsgenossenschaften Fachausschuß "Chemie" November 1994 Erprobtes und von
Identifizierung und Quantifizierung von ätherischen Ölen mittels Gaschromatographie
 Identifizierung und Quantifizierung von ätherischen Ölen mittels Gaschromatographie Vor der Durchführung der Messung auch allgemeine Hinweise (Punkt 5) durchlesen! 1. Destillation Ca. 20 g der Analysenlösung
Identifizierung und Quantifizierung von ätherischen Ölen mittels Gaschromatographie Vor der Durchführung der Messung auch allgemeine Hinweise (Punkt 5) durchlesen! 1. Destillation Ca. 20 g der Analysenlösung
Ionenchromatographie
 Analytisches Physikalisches Praktikum Ionenchromatographie Version 2, Gruppe M14 Jorge Ferreiro, Studiengang Chemieingenieur 4. Semester, fjorge@student.ethz.ch Natalja Früh, Studiengang Interdisziplinäre
Analytisches Physikalisches Praktikum Ionenchromatographie Version 2, Gruppe M14 Jorge Ferreiro, Studiengang Chemieingenieur 4. Semester, fjorge@student.ethz.ch Natalja Früh, Studiengang Interdisziplinäre
Chromatographie Version 04/2008
 Chromatographie Version 04/2008 1. Erläutern Sie das Prinzip der Chromatographie. 2. In der Dünnschichtchromatographie kann man mit der sogenannten eindimensionalen Mehrfachentwicklung bzw. der zweidimensionalen
Chromatographie Version 04/2008 1. Erläutern Sie das Prinzip der Chromatographie. 2. In der Dünnschichtchromatographie kann man mit der sogenannten eindimensionalen Mehrfachentwicklung bzw. der zweidimensionalen
Endersch, Jonas 09./
 Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol
 4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
Liquidchromatographie
 Gaby Aced, Hermann J. Möckel Liquidchromatographie Apparative, theoretische und methodische Grundlagen der HPLC Weinheim New York Basel Cambridge VCH Inhalt 1 Definition der Methode 1 1.1 Allgemeines über
Gaby Aced, Hermann J. Möckel Liquidchromatographie Apparative, theoretische und methodische Grundlagen der HPLC Weinheim New York Basel Cambridge VCH Inhalt 1 Definition der Methode 1 1.1 Allgemeines über
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol
 4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
Übungsaufgaben zu chromatographischen Verfahren
 Übungsaufgaben zu chromatographischen Verfahren Diese Aufgaben hier, sollen den im Unterricht vermittelten Stoff vertiefen. Viele der Aufgaben wurden in Klassenarbeiten gestekkt. Neben den Aufgaben auf
Übungsaufgaben zu chromatographischen Verfahren Diese Aufgaben hier, sollen den im Unterricht vermittelten Stoff vertiefen. Viele der Aufgaben wurden in Klassenarbeiten gestekkt. Neben den Aufgaben auf
Fossile Rohstoffe. Erdöl
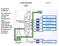 Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
5. Probenaufbereitung
 Analytische Chemie für Biologie, Pharmazie, 75 Teil Chromatographische und 5. Probenaufbereitung Wieso ist eine Probeaufarbeitung für viele Proben notwendig? Störende andere Substanzen sollen entfernt
Analytische Chemie für Biologie, Pharmazie, 75 Teil Chromatographische und 5. Probenaufbereitung Wieso ist eine Probeaufarbeitung für viele Proben notwendig? Störende andere Substanzen sollen entfernt
Theorie. BEACHTE die unterschiedliche Terminologie Chromatographie: Trennprinzip Analysenmethode (Trennung+Detektion+Signalverarbeitung)
 Definition der Chromatographie Theorie Physikalische Trennmethode, bei der die zu trennenden Komponenten zwischen zwei Phasen verteilt werden, von denen eine stationär angeordnet ist und die andere sich
Definition der Chromatographie Theorie Physikalische Trennmethode, bei der die zu trennenden Komponenten zwischen zwei Phasen verteilt werden, von denen eine stationär angeordnet ist und die andere sich
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol OH
 4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
Versuch 6: Rektifikation
 Physikalisch-Chemisches Grundpraktikum Sommersemester 2004 Gruppe B9 Andreas Frintrup / Sven Wolff Versuch 6: Rektifikation Ziel: Die Effizienz zweier verschiedener Trennsäulen, einer fünfbödigen Glockenbodenkolonne
Physikalisch-Chemisches Grundpraktikum Sommersemester 2004 Gruppe B9 Andreas Frintrup / Sven Wolff Versuch 6: Rektifikation Ziel: Die Effizienz zweier verschiedener Trennsäulen, einer fünfbödigen Glockenbodenkolonne
Massenspektrometrie (MS)
 Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
VERSUCH 3: GC - GASCHROMATOGRAPHIE
 VERSUCH 3: GC - GASCHROMATOGRAPHIE Die Gaschromatographie ist eine Trennmethode, die die unterschiedlichen Adsorptions- bzw. Verteilungseigenschaften von Stoffen ausnutzt, um sie in Stoffgemischen zu trennen.
VERSUCH 3: GC - GASCHROMATOGRAPHIE Die Gaschromatographie ist eine Trennmethode, die die unterschiedlichen Adsorptions- bzw. Verteilungseigenschaften von Stoffen ausnutzt, um sie in Stoffgemischen zu trennen.
Erdöl. "... ist eine nutzlose Absonderung der Erde eine klebrige Flüssigkeit, die stinkt und in. keiner Weise verwendet werden kann.
 Erdöl "... ist eine nutzlose Absonderung der Erde eine klebrige Flüssigkeit, die stinkt und in keiner Weise verwendet werden kann." ('Akademie der Wissenschaften' in St. Petersburg 1806) Erdöl, schwarzes
Erdöl "... ist eine nutzlose Absonderung der Erde eine klebrige Flüssigkeit, die stinkt und in keiner Weise verwendet werden kann." ('Akademie der Wissenschaften' in St. Petersburg 1806) Erdöl, schwarzes
Umweltanalytik Praktikum 3. Seminartag
 Umweltanalytik Praktikum 3. Seminartag Versuch 1.8: Diesel - isotherm Linienabstand: p = e - H v RT p = 1 H v e RT (Clausius - Claperon) GC-Praktikum 3. Seminartag 1 21 Versuch 1.8: Isotherme Fahrweise
Umweltanalytik Praktikum 3. Seminartag Versuch 1.8: Diesel - isotherm Linienabstand: p = e - H v RT p = 1 H v e RT (Clausius - Claperon) GC-Praktikum 3. Seminartag 1 21 Versuch 1.8: Isotherme Fahrweise
Kapitel 12: Analyse mittels Gaschromatographie
 Kapitel 12: Analyse mittels Gaschromatographie Sie werden im Laufe Ihrer beruflichen Tätigkeit vermutlich immer wieder mit der Frage konfrontiert, Proben zu analysieren. Dabei ist es wichtig, die richtige
Kapitel 12: Analyse mittels Gaschromatographie Sie werden im Laufe Ihrer beruflichen Tätigkeit vermutlich immer wieder mit der Frage konfrontiert, Proben zu analysieren. Dabei ist es wichtig, die richtige
Gaschromatographie-Praktikum. zum Modul. Grundlagen der Umweltanalytik - Messtechnik
 Gaschromatographie-Praktikum zum Modul Grundlagen der Umweltanalytik - Messtechnik Versuche: 1. Einführung in die Technik der Kapillar-Gaschromatographie und Kraftstoffmessungen 2. Quantifizierung in der
Gaschromatographie-Praktikum zum Modul Grundlagen der Umweltanalytik - Messtechnik Versuche: 1. Einführung in die Technik der Kapillar-Gaschromatographie und Kraftstoffmessungen 2. Quantifizierung in der
 Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Massenspektrometrie (MS)
 Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
Massenspektrometrie (MS) Die Massenspektrometrie ist unter den heute routinemäßig verwendeten Methoden die jüngste, denn ihre Anwendung begann erst um 1960. Seit den Arbeiten von BIEMANN über Fragmentierungsmuster
Analytische Chemie für Biologie Pharmazie Bewegungswissenschaften
 59-1041-00 G HS007 nalytische Chemie für Biologie Pharmazie Bewegungswissenschaften und Sport Theoretische Grundlagen Teil Chromatographische und Elektrophoretische Trennverfahren Oct-9-07 C BPBS HS07
59-1041-00 G HS007 nalytische Chemie für Biologie Pharmazie Bewegungswissenschaften und Sport Theoretische Grundlagen Teil Chromatographische und Elektrophoretische Trennverfahren Oct-9-07 C BPBS HS07
Fossile Rohstoffe. Kohlenwasserstoffe als Energieträger
 nwasserstoffe als Energieträger Erdöl,, Erdgas und Torf sind im Laufe von Millionen von Jahren aus Kleinlebwesen und Pflanzen entstanden und werden deswegen als fossile Energieträger bezeichnet. Da sie
nwasserstoffe als Energieträger Erdöl,, Erdgas und Torf sind im Laufe von Millionen von Jahren aus Kleinlebwesen und Pflanzen entstanden und werden deswegen als fossile Energieträger bezeichnet. Da sie
5 HPLC-Methodenentwicklung zur Isomerentrennung
 HPLC-Untersuchungen 5 HPLC-Untersuchungen 65 5 HPLC-Methodenentwicklung zur Isomerentrennung Die bei der -Substitution des Benzimidazolgrundgerüstes entstehenden Isomere machen eine nachfolgende Trennung
HPLC-Untersuchungen 5 HPLC-Untersuchungen 65 5 HPLC-Methodenentwicklung zur Isomerentrennung Die bei der -Substitution des Benzimidazolgrundgerüstes entstehenden Isomere machen eine nachfolgende Trennung
stationäre Phase: fest oder flüssig - befindet sich in der sog. GC-Säule, bestimmt die Selektivität des Systems
 Einführung Chromatografie ist eine Trenntechnik. Ziel: Auftrennung der einzelnen Bestandteile eines Substanzgemisches Prinzip: Unterschiedliche zeitliche Verzögerung (Retention) der einzelnen Analyten
Einführung Chromatografie ist eine Trenntechnik. Ziel: Auftrennung der einzelnen Bestandteile eines Substanzgemisches Prinzip: Unterschiedliche zeitliche Verzögerung (Retention) der einzelnen Analyten
Applikation. Bestimmung von Kohlenwasserstofftypen in Grundölen. Zusammenfassung. Einleitung
 Applikation Bestimmung von Kohlenwasserstofftypen in Grundölen Kategorie Matrix Methode Schlagwort Analyten ID Chemische Analyse Mineralöle Normalphasen-HPLC Qualitätskontrolle, industrielle Nebenprodukte,
Applikation Bestimmung von Kohlenwasserstofftypen in Grundölen Kategorie Matrix Methode Schlagwort Analyten ID Chemische Analyse Mineralöle Normalphasen-HPLC Qualitätskontrolle, industrielle Nebenprodukte,
Übungsaufgaben zur HPLC für Biolaboranten
 Übungsaufgaben zur HPLC für Biolaboranten 1.1 Trennung von Paracetamol und HPLC Im LTC-Praktikum wurde in einer Kalibrierlösung Paracetamol und Coffein über eine HPLC getrennt. Bedingungen: β(cof) = 12,5
Übungsaufgaben zur HPLC für Biolaboranten 1.1 Trennung von Paracetamol und HPLC Im LTC-Praktikum wurde in einer Kalibrierlösung Paracetamol und Coffein über eine HPLC getrennt. Bedingungen: β(cof) = 12,5
Atomabsorptionsspektrometrie (AAS)
 Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
ETHANOL 70 Prozent Ethanolum 70 per centum. Aethanolum dilutum. Ethanol 70 Prozent ist eine Mischung von Ethanol 96 Prozent und Wasser.
 ÖAB 2008/004 ETHANOL 70 Prozent Ethanolum 70 per centum Aethanolum dilutum Definition Ethanol 70 Prozent ist eine Mischung von Ethanol 96 Prozent und Wasser. Gehalt: Ethanol 70 Prozent enthält mindestens
ÖAB 2008/004 ETHANOL 70 Prozent Ethanolum 70 per centum Aethanolum dilutum Definition Ethanol 70 Prozent ist eine Mischung von Ethanol 96 Prozent und Wasser. Gehalt: Ethanol 70 Prozent enthält mindestens
OSZ Körperpflege Chemie Fachhochschulreife FOS 2009/10
 Name: Klasse: GASCHROMATOGRAFIE Experiment 08 1. Aufgabe: a) Nehmen Sie ein Gaschromatogramm ihres Feuerzeuggases auf. (Füllen Sie dazu 2 ml des Feuerzeuggases in die Spritze!) Siehe Anlage Durchführung!!!
Name: Klasse: GASCHROMATOGRAFIE Experiment 08 1. Aufgabe: a) Nehmen Sie ein Gaschromatogramm ihres Feuerzeuggases auf. (Füllen Sie dazu 2 ml des Feuerzeuggases in die Spritze!) Siehe Anlage Durchführung!!!
Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung)
 Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Organische Chemie II. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
8 Stevia qualitativ aus der Pflanze extrahieren
 8 Stevia qualitativ aus der Pflanze extrahieren 8.1 Vorwort Stevia ist der mit Abstand am teuersten Zuckerersatzstoff den wir untersucht haben, deshalb beschäftigte uns die Frage, wie der hohe Preis zu
8 Stevia qualitativ aus der Pflanze extrahieren 8.1 Vorwort Stevia ist der mit Abstand am teuersten Zuckerersatzstoff den wir untersucht haben, deshalb beschäftigte uns die Frage, wie der hohe Preis zu
Analytische Chemie (für Biol. / Pharm. Wiss.)
 Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst Laboratory of Organic Chemistry HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/
Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst Laboratory of Organic Chemistry HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/
ANALYTISCHE CHEMIE I Trennmethoden 1. Grundlagen Chromatographie WS 2007/2008
 ANALYTISCHE CHEMIE I Trennmethoden 1. Grundlagen Chromatographie WS 2007/2008 Chromatographie Physikalische Trennmethode, bei der die zu trennenden Komponenten zwischen einer feststehenden (stationären)
ANALYTISCHE CHEMIE I Trennmethoden 1. Grundlagen Chromatographie WS 2007/2008 Chromatographie Physikalische Trennmethode, bei der die zu trennenden Komponenten zwischen einer feststehenden (stationären)
6. Chromatographie (LC: Flüssigchromatographie)
 Analytische Chemie 2016/18 6. Chromatographie (LC: Flüssigchromatographie) 1 6. Chromatographie - Gliederung 6.1 Einführung 6.2 Definition 6.3 Prinzip der Chromatographie 6.4 Systematik der Chromatographie
Analytische Chemie 2016/18 6. Chromatographie (LC: Flüssigchromatographie) 1 6. Chromatographie - Gliederung 6.1 Einführung 6.2 Definition 6.3 Prinzip der Chromatographie 6.4 Systematik der Chromatographie
1 Grundlagen der Chromatographie
 1 1 Grundlagen der Chromatographie Chromatographie für Einsteiger. Karl Kaltenböck Copyright 2008 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim ISBN: 978-3-527-32119-3 1389vch01.indd 1 22.06.2008 20:39:43
1 1 Grundlagen der Chromatographie Chromatographie für Einsteiger. Karl Kaltenböck Copyright 2008 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim ISBN: 978-3-527-32119-3 1389vch01.indd 1 22.06.2008 20:39:43
Verteilung von Substanzen zwischen mobiler und stationärer Phase
 3.50 3.25 3.00 2.75 2.50 2.25 2.00 1.75 1.50 1.25 1.00 0.75 0.50 0.25 0.00 uv(x10,000) 2.5 5.0 7.5 10.0 12.5 15.0 17.5 20.0 22.5 25.0 27.5 30.0 32.5 min XIC of Q1: from 1660.0-1661.0 amu from AquCanGig-2,
3.50 3.25 3.00 2.75 2.50 2.25 2.00 1.75 1.50 1.25 1.00 0.75 0.50 0.25 0.00 uv(x10,000) 2.5 5.0 7.5 10.0 12.5 15.0 17.5 20.0 22.5 25.0 27.5 30.0 32.5 min XIC of Q1: from 1660.0-1661.0 amu from AquCanGig-2,
Untersuchung von Sonderproben Bereich Organik. Mineralölkohlenwasserstoffe - Seite 1
 Untersuchung von Sonderproben Bereich Organik Mineralölkohlenwasserstoffe - Seite 1 Untersuchung von Sonderproben Bereich Organik Gliederung: 1. Einleitung 2. Schadensfälle MKW 3. Schadensfälle Fischsterben
Untersuchung von Sonderproben Bereich Organik Mineralölkohlenwasserstoffe - Seite 1 Untersuchung von Sonderproben Bereich Organik Gliederung: 1. Einleitung 2. Schadensfälle MKW 3. Schadensfälle Fischsterben
ANALYTISCHE CHEMIE I Trennmethoden 4. Gaschromatographie WS 2007/2008
 ANALYTISCHE CHEMIE I Trennmethoden 4. Gaschromatographie WS 2007/2008 Prinzip der Gaschromatographie Die Gaschromatographie (GC) ist eine analytische Trennmethode, bei der die mobile Phase gasförmig ist.
ANALYTISCHE CHEMIE I Trennmethoden 4. Gaschromatographie WS 2007/2008 Prinzip der Gaschromatographie Die Gaschromatographie (GC) ist eine analytische Trennmethode, bei der die mobile Phase gasförmig ist.
Skript zum Praktikum Instrumentelle Analytik der Universität Heidelberg im 4. Fachsemester Pharmazie
 HPLC 1 Skript zum Praktikum Instrumentelle Analytik der Universität Heidelberg im 4. Fachsemester Pharmazie 1. Aufgabe In diesem Versuch werden die Retentionszeiten der Substanzen Acetylsalicylsäure (ASS)
HPLC 1 Skript zum Praktikum Instrumentelle Analytik der Universität Heidelberg im 4. Fachsemester Pharmazie 1. Aufgabe In diesem Versuch werden die Retentionszeiten der Substanzen Acetylsalicylsäure (ASS)
Versuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten -
 1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
Protokoll Dampfdruck. Punkte: /10
 Protokoll Dampfdruck Gruppe Biologie Assistent: Olivier Evelyn Jähne, Eva Eickmeier, Claudia Keller Kontakt: claudiakeller@teleport.ch Sommersemester 2006 6. Juni 2006 Punkte: /0 . Einleitung Wenn eine
Protokoll Dampfdruck Gruppe Biologie Assistent: Olivier Evelyn Jähne, Eva Eickmeier, Claudia Keller Kontakt: claudiakeller@teleport.ch Sommersemester 2006 6. Juni 2006 Punkte: /0 . Einleitung Wenn eine
Übungsaufgaben - Analytik
 Übungsaufgaben - Analytik Übung 1 Von einer Substanz soll der molare Extinktionskoeffizient bestimmt werden. Der Laborant hat mässig exakt verdünnt. Er hat jeweils die auf der x-achse angegbene Zahl an
Übungsaufgaben - Analytik Übung 1 Von einer Substanz soll der molare Extinktionskoeffizient bestimmt werden. Der Laborant hat mässig exakt verdünnt. Er hat jeweils die auf der x-achse angegbene Zahl an
Bestimmung des Gehaltes an Kohlenwasserstoffen in Abfällen - LAGA-Richtlinie KW/04
 Bestimmung des Gehaltes an Kohlenwasserstoffen in Abfällen - LAGA-Richtlinie KW/04 Inhalt Mineralöl-Kohlenwasserstoffe (MKW) MKW-Analytik nach LAGA - gestern und heute LAGA-Richtlinie KW/04 Beispiele Zusammenfassung
Bestimmung des Gehaltes an Kohlenwasserstoffen in Abfällen - LAGA-Richtlinie KW/04 Inhalt Mineralöl-Kohlenwasserstoffe (MKW) MKW-Analytik nach LAGA - gestern und heute LAGA-Richtlinie KW/04 Beispiele Zusammenfassung
Phasen, Komponenten, Freiheitsgrade
 Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
Vorbereitungen am Computer: Programm starten: AK Analytik 11
 Prinzip: Mit einem LowCost-Gaschromatografen ist es möglich, fast professionelle Trennungen von Feuerzeuggas zu erzielen. Die Werte erscheinen auf dem Display des Messmoduls AK LCGC 11. Ein Computer ist
Prinzip: Mit einem LowCost-Gaschromatografen ist es möglich, fast professionelle Trennungen von Feuerzeuggas zu erzielen. Die Werte erscheinen auf dem Display des Messmoduls AK LCGC 11. Ein Computer ist
A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit Aufgabe: Es ist die Dampfdruckkurve einer leicht flüchtigen Flüssigkeit zu ermitteln
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit Aufgabe: Es ist die Dampfdruckkurve einer leicht flüchtigen Flüssigkeit zu ermitteln
Protokoll: Hochdruck-Flüssigkeits-Chromatographie (HPLC)
 Protokoll: Hochdruck-Flüssigkeits-Chromatographie (HPLC) Zielstellung: - Bestimmung der Retentionszeiten von Theobromin, Theophyllin und Coffein! - Ermittlung des Coffeingehalts verschiedener ahrungs-
Protokoll: Hochdruck-Flüssigkeits-Chromatographie (HPLC) Zielstellung: - Bestimmung der Retentionszeiten von Theobromin, Theophyllin und Coffein! - Ermittlung des Coffeingehalts verschiedener ahrungs-
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Dünnschichtchromatographie
 PB III/Seminar DC Dünnschichtchromatographie Dr. Johanna Liebl Chromatographie - Prinzip physikalisch-chemische Trennmethoden Prinzip: Verteilung von Substanzen zwischen einer ruhenden (stationären) und
PB III/Seminar DC Dünnschichtchromatographie Dr. Johanna Liebl Chromatographie - Prinzip physikalisch-chemische Trennmethoden Prinzip: Verteilung von Substanzen zwischen einer ruhenden (stationären) und
Praktikum Physikalische Chemie I 30. Januar Aktivierungsenergie. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Versuchsprotokoll: Chromatographie. Gelchromatographische Trennung eines Proteingemischs
 Versuchsprotokoll: Chromatographie Gelchromatographische Trennung eines Proteingemischs 1.1. Einleitung Das Ziel der Gelchromatographie ist es ein vorhandenes Proteingemisch in die einzelnen Proteine zu
Versuchsprotokoll: Chromatographie Gelchromatographische Trennung eines Proteingemischs 1.1. Einleitung Das Ziel der Gelchromatographie ist es ein vorhandenes Proteingemisch in die einzelnen Proteine zu
Schmelzdiagramm eines binären Stoffgemisches
 Praktikum Physikalische Chemie I 30. Oktober 2015 Schmelzdiagramm eines binären Stoffgemisches Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1. Theorie hinter dem Versuch Ein Schmelzdiagramm zeigt
Praktikum Physikalische Chemie I 30. Oktober 2015 Schmelzdiagramm eines binären Stoffgemisches Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1. Theorie hinter dem Versuch Ein Schmelzdiagramm zeigt
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie
 1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
RESOLUTION OIV-OENO ANALYSE FLÜCHTIGER VERBINDUNGEN IN WEIN MITTELS GASCHROMATOGRAPHIE
 RESOLUTION OIV-OENO 553-2016 ANALYSE FLÜCHTIGER VERBINDUNGEN IN WEIN MITTELS GASCHROMATOGRAPHIE DIE GENERALVERSAMMLUNG, gestützt auf Artikel 2 Absatz 2 iv des Übereinkommens vom 3. April 2001 zur Gründung
RESOLUTION OIV-OENO 553-2016 ANALYSE FLÜCHTIGER VERBINDUNGEN IN WEIN MITTELS GASCHROMATOGRAPHIE DIE GENERALVERSAMMLUNG, gestützt auf Artikel 2 Absatz 2 iv des Übereinkommens vom 3. April 2001 zur Gründung
Chemie Fragenkatalog Jahrgang 8
 Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Nitrosamine in Würze und Bier
 2.6.4.2 Nitrosamine in Würze und Bier Der Gruppe der Nitrosamine konnten sehr starke kanzerogene Eigenschaften nachgewiesen werden. In Bier wurde bisher nur Nitrosodimethylamin (NDMA) festgestellt. Prinzip
2.6.4.2 Nitrosamine in Würze und Bier Der Gruppe der Nitrosamine konnten sehr starke kanzerogene Eigenschaften nachgewiesen werden. In Bier wurde bisher nur Nitrosodimethylamin (NDMA) festgestellt. Prinzip
FETTE & ÖLE. Bestimmung des Fettsäuremuster mittels Gaschromatographie
 FETTE & ÖLE Bestimmung des Fettsäuremuster mittels Gaschromatographie 2 Inhaltverzeichnis: Diese Power Point Präsentation informiert über: - Was sind Fette und Öle? - Probenvorbereitung (Umesterung) -
FETTE & ÖLE Bestimmung des Fettsäuremuster mittels Gaschromatographie 2 Inhaltverzeichnis: Diese Power Point Präsentation informiert über: - Was sind Fette und Öle? - Probenvorbereitung (Umesterung) -
5 Analyseverfahren. Qualitative Analyse: Identifikation eines Stoffs bzw. Bestimmung der Zusammensetzung eines Stoffgemischs
 5 Analyseverfahren 1 Qualitative Analyse: Identifikation eines Stoffs bzw. Bestimmung der Zusammensetzung eines Stoffgemischs Quantitative Analyse: Bestimmung der absoluten Menge bzw. des Anteils (Konzentration)
5 Analyseverfahren 1 Qualitative Analyse: Identifikation eines Stoffs bzw. Bestimmung der Zusammensetzung eines Stoffgemischs Quantitative Analyse: Bestimmung der absoluten Menge bzw. des Anteils (Konzentration)
2008 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester
 28 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester H 3 C H 4-Toluolsulfonsäure + Cyclohexan H 3 C H CH 3 + CH 3 H 2 C 3 H 6 2 (74.1) C 4 H 1 (74.1) C 7 H 8 3 S
28 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester H 3 C H 4-Toluolsulfonsäure + Cyclohexan H 3 C H CH 3 + CH 3 H 2 C 3 H 6 2 (74.1) C 4 H 1 (74.1) C 7 H 8 3 S
Anorganische Chemie! der unbelebten Natur keine Kohlenstoffverbindung (Kohlenstoffatome C) Metall Nichtmetallverbindungen Ionenbindung
 3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
1017 Azokupplung von Benzoldiazoniumchlorid mit 2-Naphthol zu 1-Phenylazo-2-naphthol
 OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
H = A + B u +C u. Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese)
 Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst HCI D323 Martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/ Zusammenfassung
Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst HCI D323 Martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/ Zusammenfassung
VERDAMPFUNGSGLEICHGEWICHTE: SIEDEDIAGRAMM EINER BINÄREN MISCHUNG
 VERDAMPFUNGSGLEICHGEWICHTE: RAMM EINER BINÄREN MISCHUNG 1. Lernziel Ziel des Versuchs ist es, ein zu bestimmen, um ein besseres Verständnis für Verdampfungsgleichgewichte und Mischeigenschaften flüssiger
VERDAMPFUNGSGLEICHGEWICHTE: RAMM EINER BINÄREN MISCHUNG 1. Lernziel Ziel des Versuchs ist es, ein zu bestimmen, um ein besseres Verständnis für Verdampfungsgleichgewichte und Mischeigenschaften flüssiger
1. BESTIMMUNG DER DAMPFDRUCKKURVE EINER REINEN FLÜSSIGKEIT ZUR BERECHNUNG DER VER- DAMPFUNGSENTHALPIE DH verd UND -ENTROPIE DS verd
 A1-1 1. BESTIMMUNG DER DAMPFDRUCKKURVE EINER REINEN FLÜSSIGKEIT ZUR BERECHNUNG DER VER- DAMPFUNGSENTHALPIE DH verd UND -ENTROPIE DS verd Bereiten Sie folgende Themengebiete vor Zustandsdiagramme von Einkomponentensystemen
A1-1 1. BESTIMMUNG DER DAMPFDRUCKKURVE EINER REINEN FLÜSSIGKEIT ZUR BERECHNUNG DER VER- DAMPFUNGSENTHALPIE DH verd UND -ENTROPIE DS verd Bereiten Sie folgende Themengebiete vor Zustandsdiagramme von Einkomponentensystemen
Physikalisches Praktikum I
 Fachbereich Physik Physikalisches Praktikum I W21 Name: Verdampfungswärme von Wasser Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Folgende Fragen
Fachbereich Physik Physikalisches Praktikum I W21 Name: Verdampfungswärme von Wasser Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Folgende Fragen
Prof. Dr. Peter Vogl, Thomas Eissfeller, Peter Greck. Übung in Thermodynamik und Statistik 4B Blatt 8 (Abgabe Di 3. Juli 2012)
 U München Physik Department, 33 http://www.wsi.tum.de/33 eaching) Prof. Dr. Peter Vogl, homas Eissfeller, Peter Greck Übung in hermodynamik und Statistik 4B Blatt 8 Abgabe Di 3. Juli 202). Extremalprinzip
U München Physik Department, 33 http://www.wsi.tum.de/33 eaching) Prof. Dr. Peter Vogl, homas Eissfeller, Peter Greck Übung in hermodynamik und Statistik 4B Blatt 8 Abgabe Di 3. Juli 202). Extremalprinzip
Wie verändern sich die Eigenschaften der Alkohole bei Zunahme der Kohlenstoffzahl?
 Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 1- Dampfdruckdiagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Dampfdruckdiagramm wird dieses Vorgespräch durch einen Multiple-Choice
PCG-Grundpraktikum Versuch 1- Dampfdruckdiagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Dampfdruckdiagramm wird dieses Vorgespräch durch einen Multiple-Choice
4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester
 NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
6017 Bromierung von Anisol zu 4-Bromanisol
 6017 Bromierung von Anisol zu 4-Bromanisol OMe OMe + Br 2 Dichlormethan + HBr + Nebenprodukte C 7 H 8 O Br 2 C 7 H 7 BrO (108.1) (159.8) (187.0) Br Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
6017 Bromierung von Anisol zu 4-Bromanisol OMe OMe + Br 2 Dichlormethan + HBr + Nebenprodukte C 7 H 8 O Br 2 C 7 H 7 BrO (108.1) (159.8) (187.0) Br Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
Seminar HPLC. Seminar HPLC / WS 2003/04. Dr. R. Vasold
 Seminar HPLC 1 2 Analytik - Abteilung Institut für Organische Chemie Prof. B. König Kapitel I Theoretischer Teil 3 I.1 Einleitung I.2 Zielsetzung I.3 Die stationäre Phase I.4 Die mobile Phase I.5 Die Pumpe
Seminar HPLC 1 2 Analytik - Abteilung Institut für Organische Chemie Prof. B. König Kapitel I Theoretischer Teil 3 I.1 Einleitung I.2 Zielsetzung I.3 Die stationäre Phase I.4 Die mobile Phase I.5 Die Pumpe
Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt.
 1 Definition: Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt. 2 Erscheinungsformen der Materie Homogen oder
1 Definition: Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt. 2 Erscheinungsformen der Materie Homogen oder
Versuch: Thermisches Cracken von Paraffinöl
 Philipps-Universität Marburg 21.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2, Alkane Versuch: Thermisches Cracken von Paraffinöl
Philipps-Universität Marburg 21.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2, Alkane Versuch: Thermisches Cracken von Paraffinöl
5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester
 NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
Analyse komplexer Proben mit multidimensionaler (Heart-Cut) GC-GCMS und LC-GCMS
 Analyse komplexer Proben mit multidimensionaler (Heart-Cut) GC-GCMS und LC-GCMS Dr. Margit Geißler, Susanne Böhme Shimadzu Europa GmbH, Duisburg info@shimadzu.de www.shimadzu.de Das Problem von Co-Elutionen
Analyse komplexer Proben mit multidimensionaler (Heart-Cut) GC-GCMS und LC-GCMS Dr. Margit Geißler, Susanne Böhme Shimadzu Europa GmbH, Duisburg info@shimadzu.de www.shimadzu.de Das Problem von Co-Elutionen
Phy.- chem. Praktikum. Gaschromatograpie
 Gaschromatograpie Aufgabenstellung: 1. Vorbereitung Notierung der Siedepunkte der Komponenten des zu untersuchenden Gemisches- Auswählen einer geeigneten Trenntemperatur, eines geeignetes Lösungsmittels,
Gaschromatograpie Aufgabenstellung: 1. Vorbereitung Notierung der Siedepunkte der Komponenten des zu untersuchenden Gemisches- Auswählen einer geeigneten Trenntemperatur, eines geeignetes Lösungsmittels,
Prüfungsfragenkatalog für Methoden der Chromatographie (Prof. Werner Seebacher)
 Prüfungsfragenkatalog für Methoden der Chromatographie (Prof. Werner Seebacher) Stand: Mai 2015 Termin: 28.05.2015 1. Zeigen Sie anhand einer einfachen Strukturformel einer Aminosäure wie sie im basischen,
Prüfungsfragenkatalog für Methoden der Chromatographie (Prof. Werner Seebacher) Stand: Mai 2015 Termin: 28.05.2015 1. Zeigen Sie anhand einer einfachen Strukturformel einer Aminosäure wie sie im basischen,
3. Stoffgemische und Ihre Zerlegung
 3. Stoffgemische und Ihre Zerlegung Aus Stoffgemischen lassen sich die einzelnen Bestandteile durch physikalische Trennverfahren isolieren. Wenn ein Stoff mittels physikalischen Methoden nicht weiter zerlegen
3. Stoffgemische und Ihre Zerlegung Aus Stoffgemischen lassen sich die einzelnen Bestandteile durch physikalische Trennverfahren isolieren. Wenn ein Stoff mittels physikalischen Methoden nicht weiter zerlegen
Übungsaufgaben Physikalische Chemie
 Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Lernziele: Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme,
 Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie) Maximale Punktezahl: 20 Notwendige Mindestpunkte: 8
 1. Klausur OC1 (BSc-Studiengang) PIN: 18.02.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
1. Klausur OC1 (BSc-Studiengang) PIN: 18.02.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester
 NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
Arbeitsanleitung. Ermittlung der Fettsäurezusammensetzung von Fetten
 Arbeitsanleitung Ermittlung der Fettsäurezusammensetzung von Fetten Zielsetzung: Es soll festgestellt werden welche Fettsäuren im vorliegenden Fett vorhanden sind und in welchem Verhältnis sie zueinander
Arbeitsanleitung Ermittlung der Fettsäurezusammensetzung von Fetten Zielsetzung: Es soll festgestellt werden welche Fettsäuren im vorliegenden Fett vorhanden sind und in welchem Verhältnis sie zueinander
Hochleistungs-Flüssigchromatographie HPLC
 I. Theoretische Grundlagen 1. Einführung in die II. Praktischer Teil Themen des - s: 1. Optimierung einer chromatographischen Trennung durch a) Veränderung der mobilen Phase und b) der Wellenlängeneinstellung
I. Theoretische Grundlagen 1. Einführung in die II. Praktischer Teil Themen des - s: 1. Optimierung einer chromatographischen Trennung durch a) Veränderung der mobilen Phase und b) der Wellenlängeneinstellung
Analytische Chemie (für Biol. / Pharm. Wiss.)
 Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst HCI D323 Martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/ ETH Zurich Dr.
Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst HCI D323 Martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/ ETH Zurich Dr.
Bei der Wärmeübertragung kann man drei Transportvorgänge voneinander unterscheiden:
 6 ärmeübertragung Bei der ärmeübertragung kann man drei Transportvorgänge voneinander unterscheiden: ärmeleitung ärmeübergang / onvektion ärmestrahlung Der ärmetransport durch Leitung oder onvektion benötigt
6 ärmeübertragung Bei der ärmeübertragung kann man drei Transportvorgänge voneinander unterscheiden: ärmeleitung ärmeübergang / onvektion ärmestrahlung Der ärmetransport durch Leitung oder onvektion benötigt
Synthese von tert Butylchlorid
 Synthese von tert Butylchlorid Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 30.11.2005 Rémy Denzler, D-Biol 1 1. Methode tert-butanol wird in einer nucleophilen Substitution
Synthese von tert Butylchlorid Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 30.11.2005 Rémy Denzler, D-Biol 1 1. Methode tert-butanol wird in einer nucleophilen Substitution
1 LOW-COST-Chromatograph 1 Injektionsspritze, 2 ml Gasfeuerzeug?? AK LCGC04 1 Stoppuhr Feuerzeug- Nachfüll-Gas 1 Stativ Camping-gas Kartusche
 Kappenberg von Feuerzeug - bzw. Camping- Gas Seite 1 / 10 Prinzip: Mit einem LowCost - Gaschromatographen ist es möglich, fast professionelle Trennungen von Feuerzeuggas zu erzielen. Die Wertepaare werden
Kappenberg von Feuerzeug - bzw. Camping- Gas Seite 1 / 10 Prinzip: Mit einem LowCost - Gaschromatographen ist es möglich, fast professionelle Trennungen von Feuerzeuggas zu erzielen. Die Wertepaare werden
Grundlagen der Chromatographie
 Laboratorium für organische Chemie Praktikum physikalische und analytische Chemie Frühjahr 2016 Grundlagen der Chromatographie 1 1. Grundlagen Chromatographie ist ein physikalisch-chemisches Trennverfahren,
Laboratorium für organische Chemie Praktikum physikalische und analytische Chemie Frühjahr 2016 Grundlagen der Chromatographie 1 1. Grundlagen Chromatographie ist ein physikalisch-chemisches Trennverfahren,
Naturwissenschaft Vermutungswissen Alles ist Chemie!!! Analyse Synthese
 SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
Destillation und Alkohol
 Destillation und Alkohol Destillation Veronikas Vater hat die Genehmigung Schnaps zu brennen. Dazu braucht er eine Destillationsanlage: Abb. 1: Destillationsanlage Bei der Destillation wird eine Flüssigkeit
Destillation und Alkohol Destillation Veronikas Vater hat die Genehmigung Schnaps zu brennen. Dazu braucht er eine Destillationsanlage: Abb. 1: Destillationsanlage Bei der Destillation wird eine Flüssigkeit
