Rotkohlindikator. Zusammenfassung. Einordnung in den Unterricht 1
|
|
|
- Arnim Bach
- vor 7 Jahren
- Abrufe
Transkript
1 V19 Rotkohlindikator Fach Klasse Überthema Feinthema Zeit Chemie Q4 Farbstoffe ph-indikator 30 Minuten Zusammenfassung Die Blätter eines Rotkohls werden gekocht und das rotgefärbte Kochwasser als Rotkohlindikator gewonnen. Der so hergestellte ph-indikator, wird anschließend mit verschiedenen Substanzen auf seine Indikatorwirkung getestet. Einordnung in den Unterricht 1 Der Versuch ist nach dem hessischen Lehrplan G8 der Qualifikationsphase Q4 dem Wahlthema angewandte Chemie zuzuordnen. Dort kann er zum Unterrichtsinhalt Farbstoffe und genauer ph-indikatoren durchgeführt werden. Als Vorwissen benötigen die SuS ihre Kenntnisse aus den Halbjahren 9G.2 und Q1, in denen es um die Säure-Base-Theorien und aromatische Kohlenwasserstoffe geht. Durch den Versuch wird den SuS gezeigt, dass ph-indikatoren Farbstoffe sind, die bei Änderung des ph- Wertes ihre Farbe ändern und so anzeigen, ob es sich um eine Säure oder Base handelt. Den SuS sind solche Indikatoren aus dem Unterrichtsalltag bereits bekannt, jedoch kann die dahinter stehende Theorie erst verstanden werden, nachdem den SuS die Prinzipien der Farbigkeit von Stoffen erläutert wurden. Zudem zeigt der Versuch, dass ph- Indikatoren nicht nur synthetisch hergestellte Stoffe sind, die im Chemieunterricht verwendet werden, sondern dass es natürliche Farbstoffe gibt, die als ph-indikatoren fungieren können. Überdies bietet der Versuch einen guten Einstieg in die unterschiedlichen Farbstoffklassen, indem an ein bereits bekanntes Phänomen aus dem Unterricht angeknüpft wird. 1 Vgl. Hirt, A.: Lehrplan Chemie (2010).
2 Der Versuch Die Durchführung 2 Abbildung 1: Materialien zur Herstellung von Rotkohlsaft. Abbildung 2: Versuchsaufbau zur ph-wert-bestimmung mittels Rotkohlsaft. Ein frischer Rotkohl wird gewaschen und in kleinere Stücke zerkleinert. Danach wird er in einen Topf gegeben und mit so viel Wasser versetzt, dass der Rotkohl vollständig bedeckt ist. Der Rotkohl wird anschließend mindestens eine halbe Stunde gekocht, bis das Wasser eine dunkelrote Färbung angenommen hat. Mithilfe eines Siebs werden nun die Blätter vom Saft getrennt. Ist der Saft auf Zimmertemperatur abgekühlt, wird er in dunkle Flaschen abgefüllt und kann nun zu ph-wert-bestimmungen eingesetzt werden. 2 Vgl. Wiechoczek, D.: Die gepufferte Schönheit des Rotkohlsafts oder Wie man Rotkohlsaft kornblumenlbau färbt. In: Prof. Blumes Bildungsserver für Chemie. URL: Letzter Zugriff am:
3 Wird der Saft über längere Zeit verwendet, so sollte er im Kühlschrank aufbewahrt oder sogar eingefroren werden. Um den Indikator zu testen, wird Rotkohlsaft auf 6 Schnappdeckelgläschen aufgeteilt und mit folgenden Stoffen versetzt: Essigessenz, Zitronensaft, Wasser, Kaisernatron, Soda, Rohrfrei/Vollwaschmittel. Die Beobachtung Der Rotkohl hat eine dunkelrote Farbe. Wird er gekocht, so färbt er das Kochwasser tiefrot und bleicht selbst aus. Der Rotkohlsaft ist zu Beginn dunkelrot. Mit der Zeit wird der Saft heller. Abbildung 3: Gekochter Rotkohl mit tiefrot gefärbtem Kochwasser. Wird der Saft auf seine Indikatorwirkung getestet, lassen sich bei Zugabe folgender Stoffe folgende Farbveränderungen festellen: Tabelle Fehler! Kein Text mit angegebener Formatvorlage im Dokument.-1: Farbveränderungen bei Zugabe von Haushaltsstoffen zu Rotkohlindikator. Zugabe von: Zitronensaft Essigessenz Wasser Kaisernatron Soda Rohrfrei Farbveränderung nach: dunkelrot rot unverändert grünblau grün gelb
4 Abbildung 4:Darstellung des ph-farbverlauf des Rotkohlindikators bei Zugabe von verschiedenen Substanzen mit unterschiedlichen ph-werten. Gleiche Reihenfolge wie in der Tabelle. Werden die Proben über Nacht stehen gelassen, so ist am nächsten Morgen zu erkennen, dass sich manche Farben über Nacht noch verändert haben. Abbildung 5: Veränderung der Färbung der vorletzten Probe über Nacht. Entsorgung Die Lösungen können in den Abfluss entsorgt werden. Die Stoffreste kommen in den Hausmüll.
5 Fachlicher Hintergrund Schlage nach, welcher Farbstoff im Rotkohl enthalten ist. Zu welcher Farbstoffklasse gehört der Farbstoff? Wie bei dem Versuch beobachtet werden kann, verfärbt sich der im Rotkohl enthaltene Farbstoff in Abhängigkeit des ph-werts. Dieser Farbstoff zählt zu der Gruppe der Anthocyane, eine Untergruppe der Flavonoide. Die meisten Blütenfarbstoffe gehören dieser Gruppe natürlicher Farbstoffe an. Die Untersuchung der Blütenfarbstoffe begann 1913 mit Willstätter, der die Struktur der blauen Blütenfarbe in der Kornblume, Centaurea cyanus, das Cyanin, aufklärte. Weiterhin befasste er sich mit den Strukturen aller wichtigen Anthocyane und klärte diese auf. 3 Der Begriff Anthocyan setzt sich aus dem griechischen Wort anthos, das Blüte bedeutet und dem griechischen Begriff kyanos, was übersetzt blau heißt, zusammen. 4 Chemisch gesehen sind die Anthocyane Glykoside, bei denen in 3- oder 5- Stellung vorkommende Zuckerreste durch Säurekatalyse leicht abgespalten werden können, wobei es zur Bildung der dazugehörigen Aglycone, den sogenannten Anthocyanidinen, kommt. Die so gebildeten Anthocyanidine unterscheiden sich in ihren Substituenten. Sie zählen zu den Flavyliumsalzen und werden im stark Basischen gespalten. 5 Die Anthocyanidine stellen die chromophore Gruppe dar, also die Gruppe, die durch Lichtabsorption, -reflexion, oder streuung, zum Farbeindruck führt. 6 Die Grundstruktur der Anthocyane und Anthocyanidine ist ein Flavyliumkation, wobei je nachdem, um welches Anthocyan, bzw. Anthocyanidin es sich handelt, die Reste verschieden sind. 3 Vgl. Gotot, T., Kondo, T.: Struktur und molekulare Stapelung von Anthocyanen - Variation der Blütenfarben. In: Angewandte Chemie. Volume 103/Issue 1. S Vgl. Baum, M., Schantz, M., Richling, E.: Rote Farbpigmente mit gesundheitlicher Wirkung. In: Gesellschaft Deutscher Chemiker GDCh. URL: Letzter Zugriff am: Vgl. Nuhn, P.: Naturstoffchemie- Mikrobielle, pflanzliche und tierische Naturstoffe. 4. Auflage Stuttgart S Vgl. Hülsenberg, D., Welsch, N.: Anthocyane. In: Thieme RÖMP nline. URL: Letzter Zugriff am
6 R R 1 R A C R 3 B R 2 R 4 Die Anthocyanidine unterscheiden sich in ihren Substituenten R und R2 im B-Ring Alle Anthocyanidine weisen als R1 und R3 Hydroxy-Gruppen auf. Sind R3 und R4 Zuckerreste, so handelt es sich um die Anthocyanformen. Vorkommende Zuckerreste sind Glucose, Galaktose, Arabinose und Rhamnose. In den Pflanzen liegen meist die glykosidierte Form der Anthocyanidine vor, da diese wasserlöslich und besser stabilisiert sind und so in Pflanzen leichter transportierbar. Es sind bereits mehrere hundert solcher glykosidierter Formen in Pflanzen gefunden worden. Die folgende Tabelle gibt einen Überblick über die wichtigsten Glykoside der Anthocyanidine. Tabelle Fehler! Kein Text mit angegebener Formatvorlage im Dokument.-2: Übersicht über die wichtigsten Glykoside der Anthocyanidine. 7 R R 1 R 6 + B H H H R 5 A 5 C 3 R 2 H Anthocyan Aglycon R R2 Pelargonin Pelargonidin H H Cyanin Cyanidin H Päonin Päonidin CH3 H Delphin Delphinidin Petunin Petunidin CH3 H Malvin Malvinidin CH3 CH3 7 Vgl. Gotot, T., Kondo, T.: Struktur und molekulare Stapelung von Anthocyanen - Variation der Blütenfarben. In: Angewandte Chemie. Volume 103/Issue 1. S
7 Anthocyane kommen in rot bis violetten Früchten und in manchen Gemüsearten, wie dem Rotkohl, vor. Auch Hülsenfrüchte enthalten in ihren Schalen Anthocyane. Die charakteristischen Färbungen sind durch Absorption in einem Wellenlängenbereich von nm gegeben. Das jeweilige Absorptionsmaximum wird durch die spezifische Struktur und den ph-wert beeinflusst. 8 Der Rotkohlindikator: Chemische Hintergründe zu den Farbänderungen der Anthocyane in Abhängigkeit vom ph-wert Im Rotkohl ist das Anthocyan Cyanin enthalten. H A + C 3 B H H H H Cyanidin Cyanin A + C 3 B H In Abhängigkeit vom ph-wert weist Cyanin verschiedene Farbigkeit auf. Prinzipiell besitzen alle Anthocyane eine Indikatorwirkung, allerdings sind die auftretenden Farbschattierungen im Sauren oder Basischen je nachdem, um welches spezielle Anthocyan es sich handelt, verschieden. Das gesamte Elektronensystem ist für die auftretende Farbigkeit verantwortlich. Je größer das konjugierte -Elektronensystem, desto stärker ist seine energieärmste Absorptionsbande in den langwelligen Bereich verschoben. Dieser Effekt wird als bathochrome Verschiebung bezeichnet. Die Größe des Elektronensystems ändert sich durch die jeweiligen Säure-Base-Reaktionen, wodurch ebenfalls die Absorptionsbande verändert wird, was sich im Farbeindruck auswirkt. Im sauren Milieu liegen die Anthocyane als Kationen vor, die rot erscheinen. 9 8 Vgl. Watzl, B., Briviba, K., Rechkemmer, G.: Basiswissen aktualisiert - Anthocyane. In: Ernährungs- Umschau 49/Heft 4. Karlsruhe S URL: Letzter Zugriff am: Das Anthocyan Pelargoninchlorid zeigt eine eher gelbrote Färbung auf, Cyaninchlorid hingegen ist im Sauren eher rotviolett.
8 H + +H 2, - H + H H farblos Flavyliumkation ph-wert < 3 Carbinol Pseudobase ph-wert 4-5 max = 510 nm Im Neutralen liegt überwiegend ein Flavenol mit einer violetten Färbung vor, welches im Gleichgewicht mit der farblosen Pseudobase steht. Eine farblose Lösung kann daher zu keinem Zeitpunkt beobachtet werden. Die zu beobachtende Farbvertiefung ist auf die Bildung eines sogenannten chinoiden Systems zurückzuführen. Im alkalischen Milieu liegt ein Farbanion vor, welches eine blaue Farbe besitzt. In diesem ist die Delokalisierung der -Elektronen über die drei Sechsringe und die Sauerstoffatome der Phenolat-Gruppen möglich. H - - H 2 + -, -H 2 Flavenol ph-wert 6-7 (max)= 575 nm Flavenolatanion ph-wert > 8 (max) = 600 nm Im stark Basischen erfolgt die Zerstörung des Farbstoffs, durch Öffnung des konjugierten, mesomeriestabilisierten Grundgerüsts. Es liegt demnach kein großes delokalisiertes -Elektronensystem mehr vor, sondern zwei kleine. Dies bewirkt, dass
9 das Absorptionsmaximum in den kurzwelligen Bereich verschoben wird, was einen gelben Farbeindruck mit sich bringt Chalkon ph-wert >10 (max) = UV-Bereich Die grünen Farben der Proben ergeben sich aus den Mischfarben des Gleichgewichts von Flavenolatanion (blau) und Chalkon (gelb). 10,11 Abbildung 6: Übersicht über den Farbverlauf des Rotkohlindikators in Abhängigkeit vom ph-wert. Was ist ein ph-indikator? Welche ph-indikatoren kennst du bereits aus dem Unterricht? Wie funktionieren sie? Durch den Versuch wird weiterhin gezeigt, wie ph-indikatoren funktionieren. Indikatoren sind Stoffe, die es ermöglichen, Prozessen zu folgen. Dies bedeutet, dass zum Beispiel der Verlauf einer chemischen Reaktion oder der Zustand, in dem sich ein 10 Vgl. Korhammer, K., Pfeifer, P.: Experimente mit Anthocyanen eine Grundlage für Schülerübungen. In : Naturwissenschaften im Unterricht Chemie. Nr. 52/ S Vgl. Schikor, H.: Blütenzauber dem Geheimnis des Cyanidins auf der Spur: eine Unterrichtsanregung für den Chemiekurs der berstufe. In: Praxis der Naturwissenschaften. 8/47, S
10 chemisches System befindet, sichtbar gemacht wird. 12 Dadurch, dass der Farbstoff seine Farbe in Abhängigkeit des ph-werts ändert, wird dadurch indirekt gezeigt, welcher ph- Wert in der Lösung vorliegt. Durch die unterschiedlichen Farbnuancen kann sogar abgeschätzt werden, ob es sich um eine stark saure oder schwach saure Lösung, bzw. eine schwach basische oder stark basische Lösung, handelt. Allerdings kann durch Cyanin nicht exakt bestimmt werden, welcher ph-wert in der Lösung vorliegt. Dies bedeutet, dass nicht bei jeder ph-stufe ein deutlicher Farbumschlag erfolgt. Daher werden im Labor sogenannte Universalindikatoren eingesetzt. Diese sind Mischungen aus mehreren ph-indikatoren, sodass für weitere ph-bereiche definierte Farbumschläge erkennbar sind und so genauere Angaben über den ph-wert gemacht werden können. 13 Welche Farbigkeit nimmt der Rotkohlsaft bei Zugabe der verschiedenen Substanzen an und was sagt dies über den ph-wert aus? Im Versuch zeigt der ph-indikator Cyanin, dass es sich bei Zitronensaft und Essigessenz um saure Lösungen handelt, Wasser neutral, Kaisernatron bereits schwach basisch, Soda basisch und Rohrfrei sehr basisch ist. Tabelle Fehler! Kein Text mit angegebener Formatvorlage im Dokument.-3: Farbveränderungen bei Zugabe von Haushaltsstoffen zu Rotkohlindikator Zugabe von: Farbveränderung nach: Eigenschaft der Lösung Zitronensaft Intensiv rot sauer Essigessenz hellrot sauer Wasser unverändert violett neutral Kaisernatron grünblau schwach basisch Soda grün basisch Rohrfrei gelb stark basisch 12 Vgl. Neupert, M.: Indikatoren. In: Thieme RÖMPP nline. URL: Letzter Zugriff am: Vgl. Neupert, M.: Indikatoren. In: Thieme RÖMPP nline. URL: Letzter Zugriff am:
11 Die Farbigkeit und die Farbtiefe werden zusätzlich durch weitere Pflanzeninhaltsstoffe beeinflusst, welche mit den Anthocyanen wechselwirken. Rotkohl enthält etwa 1,2 mg Gesamt-Anthocyane/g Frischmasse. Anthocyane wirken wie andere Flavonoide als Antioxidantien, indem sie als Radikalfänger reagieren. Allerdings muss dazu eine sehr hohe Konzentration vorliegen, die im menschlichen Körper schwer zu erreichen ist. Daher ist diese Wirkung in Frage zu stellen. 14 In der Lebensmittelindustrie werden die Anthocyane als Lebensmittelfarbstoffe, E163, verwendet. So lässt sich zum Beispiel mit roten Gummibärchen oder Brausepulver ebenfalls eine Verfärbungsreihe bei unterschiedlichen ph-werten herstellen. Kannst du nun erläutern warum man in Süddeutschland von Blaukraut, in Norddeutschland von Rotkohl redet? Es gibt verschiedene Arten, Rotkohl zuzubereiten. Wird er mit Essig oder Apfel zubereitet, so ist er rot gefärbt. hne Zugabe von Säure bleibt die ursprünglich dunkelviolette bis blaue Farbe erhalten. Daher rühren die unterschiedlichen Bezeichnungen Rotkraut oder Blaukraut. 14 Vgl. Dräger, tteneder, Stintzing. Anthocyane. In: Thieme RÖMP nline. URL: Letzter Zugriff am
Natürliche Indikatoren
 V20 Natürliche Indikatoren Fach Klasse Überthema Feinthema Zeit Chemie Q4 Farbstoffe ph-indikator 90 Minuten Zusammenfassung Der Versuch stellt im Wesentlichen einen Zusatzversuch zu V19 dar. Es werden
V20 Natürliche Indikatoren Fach Klasse Überthema Feinthema Zeit Chemie Q4 Farbstoffe ph-indikator 90 Minuten Zusammenfassung Der Versuch stellt im Wesentlichen einen Zusatzversuch zu V19 dar. Es werden
Die Indigotinbottle. Zusammenfassung. Einordnung in den Unterricht 1
 V22 Die Indigotinbottle Fach Klasse Überthema Feinthema Zeit Chemie Q4 Farbstoffe Redoxindikator 20 Minuten Zusammenfassung Bei dem Versuch wird ein Redoxsystem erzeugt, dass seine Farbe ändert, je nachdem
V22 Die Indigotinbottle Fach Klasse Überthema Feinthema Zeit Chemie Q4 Farbstoffe Redoxindikator 20 Minuten Zusammenfassung Bei dem Versuch wird ein Redoxsystem erzeugt, dass seine Farbe ändert, je nachdem
Arbeitsblatt Wie entstehen Farben?
 Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
Farbstoffe Einleitung
 Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Qualitative Nachweise von Säuren und Basen
 Schulversuchspraktikum Miriam Jarrar Sommersemester 2012 Klassenstufen 9 & 10 Qualitative Nachweise von Säuren und Basen Auf einen Blick: Dieses Protokoll beinhaltet 3 Lehrerversuche und 2 Schülerversuche
Schulversuchspraktikum Miriam Jarrar Sommersemester 2012 Klassenstufen 9 & 10 Qualitative Nachweise von Säuren und Basen Auf einen Blick: Dieses Protokoll beinhaltet 3 Lehrerversuche und 2 Schülerversuche
Säure-Base-Indikatoren und ph-skala
 Säure-Base-Indikatoren und ph-skala Stand: 09.08.2017 Jahrgangsstufen 11/12 Fach/Fächer Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material Chemie Alltagskompetenz und Lebensökonomie
Säure-Base-Indikatoren und ph-skala Stand: 09.08.2017 Jahrgangsstufen 11/12 Fach/Fächer Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material Chemie Alltagskompetenz und Lebensökonomie
*** Bunter Farbenzauber mit Rotkohlsaft ***
 *** Bunter Farbenzauber mit Rotkohlsaft *** Experimentier-Anleitung Willst du ganz einfach, aber spannend und farbig experimentieren? Pink, gelb, grün, blau, violett Mit Rotkohl, Zitronensaft, Duschgel,
*** Bunter Farbenzauber mit Rotkohlsaft *** Experimentier-Anleitung Willst du ganz einfach, aber spannend und farbig experimentieren? Pink, gelb, grün, blau, violett Mit Rotkohl, Zitronensaft, Duschgel,
Saure, neutrale und alkalische Lösungen
 Schulversuchspraktikum Sina Bachsmann Sommersemester 2014 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Im Folgenden
Schulversuchspraktikum Sina Bachsmann Sommersemester 2014 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Im Folgenden
Versuchsprotokoll. Gummibärchen-Indikator
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Gummibärchen-Indikator Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Gummibärchen-Indikator Gruppe
Versuchsprotokoll: Ampel-Bottle - Experiment
 Versuchsprotokoll: Ampel-Bottle - Experiment Zeitaufwand: Aufbau: 5 Minuten Durchführung: 1 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
Versuchsprotokoll: Ampel-Bottle - Experiment Zeitaufwand: Aufbau: 5 Minuten Durchführung: 1 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
Rosa Geheimschrift. Durchführung
 Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Herstellung von Kunsthonig
 V8 erstellung von Kunsthonig Fach Klasse Überthema Feinthema Zeit Chemie Q2 Kohlenhydrate Mono- und Disaccharide 90 Minuten Zusammenfassung Bei dem Versuch wird Saccharose durch Säurehydrolyse in seine
V8 erstellung von Kunsthonig Fach Klasse Überthema Feinthema Zeit Chemie Q2 Kohlenhydrate Mono- und Disaccharide 90 Minuten Zusammenfassung Bei dem Versuch wird Saccharose durch Säurehydrolyse in seine
Schulversuchspraktikum. Isabel Großhennig. Sommersemester Klassenstufen 11 & 12. Farbstoffe. Kurzprotokoll
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 11 & 12 Farbstoffe Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen 11 und 12 zum Thema Farbstoffe enthält
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 11 & 12 Farbstoffe Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen 11 und 12 zum Thema Farbstoffe enthält
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Licht und Farben. Kurzprotokoll
 Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
Stoffeigenschaften auf der Spur
 Stoffeigenschaften auf der Spur Station 1 Welche Stoffe sind magnetisch? Sicherheit Entsorgung:/ Prüfe, welche Stoffe vom Magneten angezogen werden! Trage deine Beobachtungen in die Tabelle in deinem Forscherbuch
Stoffeigenschaften auf der Spur Station 1 Welche Stoffe sind magnetisch? Sicherheit Entsorgung:/ Prüfe, welche Stoffe vom Magneten angezogen werden! Trage deine Beobachtungen in die Tabelle in deinem Forscherbuch
Versuch 1: Rotkohl oder Blaukraut? Die Farbe des Rotkohlfarbstoffes in Abhängigkeit vom ph-wert
 1 Versuch 1: Rotkohl oder Blaukraut? Die Farbe des Rotkohlfarbstoffes in Abhängigkeit vom ph-wert Durchführung: Rotkohlblätter werden in kleine Streifen geschnitten und einige Minuten ausgekocht. Anschließend
1 Versuch 1: Rotkohl oder Blaukraut? Die Farbe des Rotkohlfarbstoffes in Abhängigkeit vom ph-wert Durchführung: Rotkohlblätter werden in kleine Streifen geschnitten und einige Minuten ausgekocht. Anschließend
Untersuche die Wirkung von verschiedenen Säuren auf Gemüse- und Blütenfarbstoffe.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157300) 1.4 Die Wirkung von Säuren auf Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:36:51 intertess (Version 13.06 B200, Export
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157300) 1.4 Die Wirkung von Säuren auf Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:36:51 intertess (Version 13.06 B200, Export
Reinigen mit Zitronensäure
 V4 Reinigen mit Zitronensäure Fach Klasse Überthema Feinthema Zeit Chemie Q1 Alkansäuren und ihre Derivate Zitronensäure 30 Minuten Zusammenfassung: Beim dem Versuch werden zitronenhaltige Lösungen zum
V4 Reinigen mit Zitronensäure Fach Klasse Überthema Feinthema Zeit Chemie Q1 Alkansäuren und ihre Derivate Zitronensäure 30 Minuten Zusammenfassung: Beim dem Versuch werden zitronenhaltige Lösungen zum
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Säuren, Laugen, Salze. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Säuren, Laugen, Salze Das komplette Material finden Sie hier: School-Scout.de Säuren, Laugen, Salze Themenbereich 1.1 - Säuren: Einführung
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Säuren, Laugen, Salze Das komplette Material finden Sie hier: School-Scout.de Säuren, Laugen, Salze Themenbereich 1.1 - Säuren: Einführung
Indigofarbe in Zuckerwaren
 V21 Indigofarbe in Zuckerwaren Fach Klasse Überthema Feinthema Zeit Chemie Q4 Farbstoffe Redoxindikator 25 Minuten Zusammenfassung Bei dem Versuch wird eine verdünnte Lösung blauer, indigotinhaltiger Lebensmittelfarbe
V21 Indigofarbe in Zuckerwaren Fach Klasse Überthema Feinthema Zeit Chemie Q4 Farbstoffe Redoxindikator 25 Minuten Zusammenfassung Bei dem Versuch wird eine verdünnte Lösung blauer, indigotinhaltiger Lebensmittelfarbe
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 14.12.2010 Gruppe 9: Kohlenhydrate Versuch (Assi):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 14.12.2010 Gruppe 9: Kohlenhydrate Versuch (Assi):
Essigsäure färbt ph-papier rot. Natronlauge färbt ph-papier blau
 5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
Protokoll Kurstag 7. Blatt & Blattpigmente. 1) Einleitung
 Datum: 10.12.09 Protokoll Kurstag 7 Blatt & Blattpigmente 1) Einleitung Einige Pflanzenzellen enthalten spezielle Farbstoffe (Pigmente), um Fotosynthese betreiben zu können, zum Schutz vor UV-Strahlung
Datum: 10.12.09 Protokoll Kurstag 7 Blatt & Blattpigmente 1) Einleitung Einige Pflanzenzellen enthalten spezielle Farbstoffe (Pigmente), um Fotosynthese betreiben zu können, zum Schutz vor UV-Strahlung
2-01. Das Ethen-Molekül. Perspektivische Darstellung des Ethen-Moleküls.
 Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
SÄUR E. BASE oder LAU GE SAUE R BASI SCH
 SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
Versuchsprotokoll:Stärkespaltung
 Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Wie kann eine Bräunung von zerkleinertem Obst und Gemüse verhindert werden?
 Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788500) 8.4 Enzymatische Bräunung Experiment von: Anouch Gedruckt: 28.02.204 :7:37 intertess (Version 3.2 B24, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788500) 8.4 Enzymatische Bräunung Experiment von: Anouch Gedruckt: 28.02.204 :7:37 intertess (Version 3.2 B24, Export 2000) Aufgabe
3-01. Triphenylmethan
 Triphenylmethan 3-01 Triphenylmethan ist ein farbloser Feststoff. Die Verbindung kann aus Benzol und Trichlormethan durch FRIEDL-CRAFTS-Alkylierung (elektrophile Substitution) hergestellt werden. Die H-Atome
Triphenylmethan 3-01 Triphenylmethan ist ein farbloser Feststoff. Die Verbindung kann aus Benzol und Trichlormethan durch FRIEDL-CRAFTS-Alkylierung (elektrophile Substitution) hergestellt werden. Die H-Atome
Säuren und Basen. Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17.
 Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
Dokumentation Projekt Entwicklung einer Farbskala PLUS-Kurs SU 4+, GGS Vaalserquartier, Aachen
 Die Arbeitsgruppe Die Gemeinschaftsgrundschule Vaalserquartier ist eine zweizügige Grundschule im westlichsten Stadtteil von Aachen, 400 m von der Grenze zu den Niederlanden gelegen. Sie hat 230 SchülerInnen
Die Arbeitsgruppe Die Gemeinschaftsgrundschule Vaalserquartier ist eine zweizügige Grundschule im westlichsten Stadtteil von Aachen, 400 m von der Grenze zu den Niederlanden gelegen. Sie hat 230 SchülerInnen
Versuchsprotokoll. ph-abhängigkeit der Getränkefarben
 AnnaLena Eicke PhilippsUniversität Marburg OrganischChemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll phabhängigkeit der Getränkefarben
AnnaLena Eicke PhilippsUniversität Marburg OrganischChemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll phabhängigkeit der Getränkefarben
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen
 ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
Buntes im Indikatorlabor Herstellung planzlicher Indikatoren
 20. Buntes im Indikatorlabor 1 von 18 Buntes im Indikatorlabor Herstellung planzlicher Indikatoren Jennifer Marie Kuklinski, Bochum Niveau: Sek. I Dauer: 6 Unterrichtsstunden Kompetenzen: Die Schülerinnen
20. Buntes im Indikatorlabor 1 von 18 Buntes im Indikatorlabor Herstellung planzlicher Indikatoren Jennifer Marie Kuklinski, Bochum Niveau: Sek. I Dauer: 6 Unterrichtsstunden Kompetenzen: Die Schülerinnen
7.9. Experimente zur Gewinnung und Anwendung von Pflanzenfarbstoffen. AGENS Arbeitsgemeinschaft NaturStoffe Leipzig
 7.9. Experimente zur Gewinnung und Anwendung von Geräte und Materialien: 1 Raspel, 1 Esslöffel, Stoff- und Papierproben Materialien die nicht im Experimentiersatz enthalten sind: Möhren Wasser Arbeitsschritte:
7.9. Experimente zur Gewinnung und Anwendung von Geräte und Materialien: 1 Raspel, 1 Esslöffel, Stoff- und Papierproben Materialien die nicht im Experimentiersatz enthalten sind: Möhren Wasser Arbeitsschritte:
1 Herstellung und Anwendung eines natürlichen ph-indikators. Wasser aus der Sicht der Chemie Die ph-skala Experimente
 1/6 Wasser aus der Sicht der Chemie Die ph-skala Experimente Die Untersuchung des Säuregrades (ph-wert) von alltäglichen Lösungen kann sehr einfach mit einem natürlichen ph-indikator gemacht werden. In
1/6 Wasser aus der Sicht der Chemie Die ph-skala Experimente Die Untersuchung des Säuregrades (ph-wert) von alltäglichen Lösungen kann sehr einfach mit einem natürlichen ph-indikator gemacht werden. In
ATTO 565 und ATTO 590
 ATTO 565 und ATTO 590 Allgemeine Informationen ATTO 565 und ATTO 590 sind Fluoreszenzmarker aus der Familie der Rhodamin-Farbstoffe. Diese Farbstoffe besitzen als gemeinsames Strukturelement einen Carboxyphenyl-
ATTO 565 und ATTO 590 Allgemeine Informationen ATTO 565 und ATTO 590 sind Fluoreszenzmarker aus der Familie der Rhodamin-Farbstoffe. Diese Farbstoffe besitzen als gemeinsames Strukturelement einen Carboxyphenyl-
+ MnO MnO 3. Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole. Chemikalien. Materialien
 DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
5.2 L Wie färbt sich Wäsche mit Rotkohlextrakt?
 178 Farbstoffe, Aromaten 5.2 L Wie färbt sich Wäsche mit Rotkohlextrakt? Thematik Unterrichtsmethode Grundlagen: Säure-Base-Gleichgewichte, Wechselwirkungen zwischen Farbstoff- und Faser- Molekülen, Chromophor,
178 Farbstoffe, Aromaten 5.2 L Wie färbt sich Wäsche mit Rotkohlextrakt? Thematik Unterrichtsmethode Grundlagen: Säure-Base-Gleichgewichte, Wechselwirkungen zwischen Farbstoff- und Faser- Molekülen, Chromophor,
Zusammenfassung vom
 Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Nährstoffe und Nahrungsmittel
 1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
Isolierung von Pflanzenfarbstoffen und Untersuchung auf ihre Verwendung als Säure- Base-Indikatoren
 Bodensee-Gymnasium Lindau Januar 2009 Isolierung von Pflanzenfarbstoffen und Untersuchung auf ihre Verwendung als Säure- Base-Indikatoren von Marc Bradenbrink und Florian Gerner Betreuungslehrkraft: StR
Bodensee-Gymnasium Lindau Januar 2009 Isolierung von Pflanzenfarbstoffen und Untersuchung auf ihre Verwendung als Säure- Base-Indikatoren von Marc Bradenbrink und Florian Gerner Betreuungslehrkraft: StR
Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P )
 Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P1145600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P1145600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler
 Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler Alltagserfahrung: sauer Zitrone Essig junger Wein Welcher Stoff bewirkt saure Reaktion? http://www.simplyscience.ch/portal Data/1/Resources/Images_bis_10_
Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler Alltagserfahrung: sauer Zitrone Essig junger Wein Welcher Stoff bewirkt saure Reaktion? http://www.simplyscience.ch/portal Data/1/Resources/Images_bis_10_
Klasse. Schule. Name. Datum. Seite 1
 Schule Name Klasse Datum Seite 1 Inhaltsverzeichnis 1. Reagenzglasständer aus Gips Seite 3 2. Klebstoff aus Milch Seite 4 3. Rotkohl oder Blaukraut? Seite 6 4. Farben mischen und trennen Seite 8 Viel Spaß
Schule Name Klasse Datum Seite 1 Inhaltsverzeichnis 1. Reagenzglasständer aus Gips Seite 3 2. Klebstoff aus Milch Seite 4 3. Rotkohl oder Blaukraut? Seite 6 4. Farben mischen und trennen Seite 8 Viel Spaß
Konzentrationsbestimmung mit Lösungen
 Kapitel 5 Konzentrationsbestimmung mit Lösungen Abb. 5.1: Die Farben von Universalindikatoren sind nützlich für Konzentrationsbestimmungen. Sie lernen auf den folgenden Seiten eine sehr nützliche Methode
Kapitel 5 Konzentrationsbestimmung mit Lösungen Abb. 5.1: Die Farben von Universalindikatoren sind nützlich für Konzentrationsbestimmungen. Sie lernen auf den folgenden Seiten eine sehr nützliche Methode
Nachweis von Säuren und Laugen in Alltagsprodukten
 Kieler Chemiemeile vom 14. bis 17. Mai 2003 1 Chemische Experimente mit Supermarktprodukten Nachweis von Säuren und Laugen in Alltagsprodukten Die Inhaltsangaben von Alltagsprodukten aus dem Supermarkt,
Kieler Chemiemeile vom 14. bis 17. Mai 2003 1 Chemische Experimente mit Supermarktprodukten Nachweis von Säuren und Laugen in Alltagsprodukten Die Inhaltsangaben von Alltagsprodukten aus dem Supermarkt,
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)
 Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... interpretieren den zeitlichen Ablauf chemischer Reaktionen in Abhängigkeit von verschiedenen Parametern (u.a. Oberfläche, Konzentration, Temperatur)
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... interpretieren den zeitlichen Ablauf chemischer Reaktionen in Abhängigkeit von verschiedenen Parametern (u.a. Oberfläche, Konzentration, Temperatur)
Wie bestimmt ein Chemiker Säuren und Laugen?
 Wie bestimmt ein Chemiker Säuren und Laugen? Mit den Zahlen von 0 14 wird der ph Wert angegeben. 1 ist eine sehr starke Säure, 14 ist eine sehr starke Lauge. Aus: onlineenzyklopaedie.de Das Forscherlabor
Wie bestimmt ein Chemiker Säuren und Laugen? Mit den Zahlen von 0 14 wird der ph Wert angegeben. 1 ist eine sehr starke Säure, 14 ist eine sehr starke Lauge. Aus: onlineenzyklopaedie.de Das Forscherlabor
Versuch: Darstellung eines Azofarbstoffes (Methylorange)
 PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Säure-Base-Reaktionen
 Säure-Base-Reaktionen Versuch 1: Wir schmecken Lebensmittel! Material: Kleine Trinkbecher Getränkeproben Füllt von jeder bereitstehenden Probe zunächst etwas in einen Trinkbecher und probiert einen kleinen
Säure-Base-Reaktionen Versuch 1: Wir schmecken Lebensmittel! Material: Kleine Trinkbecher Getränkeproben Füllt von jeder bereitstehenden Probe zunächst etwas in einen Trinkbecher und probiert einen kleinen
Untersuche die Wirkung verschiedener Säuren und Laugen auf natürliche und industriell hergestellte Indikatoren.
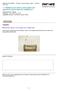 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157400) 1.5 Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:37:56
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157400) 1.5 Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:37:56
SCHÜEX RHEINLAND-PFALZ
 DEUTSCHE GESELLSCHAFT FÜR ZERSTÖRUNGSFREIE PRÜFUNG E.V. ZfP-Sonderpreis der DGZfP beim Landeswettbewerb Jugend forscht SCHÜEX RHEINLAND-PFALZ Die Lebensmittelampel: Verdorben oder noch essbar? Florian
DEUTSCHE GESELLSCHAFT FÜR ZERSTÖRUNGSFREIE PRÜFUNG E.V. ZfP-Sonderpreis der DGZfP beim Landeswettbewerb Jugend forscht SCHÜEX RHEINLAND-PFALZ Die Lebensmittelampel: Verdorben oder noch essbar? Florian
Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren (Artikelnr.: P )
 Lehrer-/Dozentenblatt Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren (Artikelnr.: P7510200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Lehrer-/Dozentenblatt Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren (Artikelnr.: P7510200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Chemie 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter Wasser (= 1000g)?
 Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Versuch: Bromierung von n-hexan. Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Bemerkung
 Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, Natriumsalz) - Azofarbstoff -
 Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Club Apollo 13, 14. Wettbewerb Aufgabe 1.
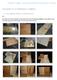 Club Apollo 13, 14. Wettbewerb Aufgabe 1. (1) a) Grundlagenteil: Basteln und Experimentieren Wir haben den Versuchsaufbau entsprechend der Versuchsanleitung aufgebaut. Den Aufbau sowie die Phase des Bauens
Club Apollo 13, 14. Wettbewerb Aufgabe 1. (1) a) Grundlagenteil: Basteln und Experimentieren Wir haben den Versuchsaufbau entsprechend der Versuchsanleitung aufgebaut. Den Aufbau sowie die Phase des Bauens
Aspirin und Paracetamol im chemischen Vergleich
 Aspirin und Paracetamol im chemischen Vergleich Achtung Aspirin und Paracetamol sind geschützte Namen und dürfen nicht ohne weiteres verwendet werden. Strukturformeln Aus den Strukturformeln leiten wir
Aspirin und Paracetamol im chemischen Vergleich Achtung Aspirin und Paracetamol sind geschützte Namen und dürfen nicht ohne weiteres verwendet werden. Strukturformeln Aus den Strukturformeln leiten wir
Allgemeines schulinternes Curriculum für die gymnasiale Oberstufe. Einführungsphase (EF):
 Allgemeines schulinternes Curriculum für die gymnasiale Oberstufe Einführungsphase (EF): Themenfeld A : Reaktionsfolge aus der organischen Chemie: Vom Alkohol zum Aromastoff Themenfeld B : Ein technischer
Allgemeines schulinternes Curriculum für die gymnasiale Oberstufe Einführungsphase (EF): Themenfeld A : Reaktionsfolge aus der organischen Chemie: Vom Alkohol zum Aromastoff Themenfeld B : Ein technischer
Kap.7 ph-wert und ph-indikatoren
 Der ph-wert und ph-indikatoren Kapitel 7 Übung 6.1: Berechnung der Konzentration von Wasser in Wasser Wieviel mol H2O sind in 1 L H2O? M(H2O)= 18.01528 g/mol 1 L(H2O)= 00g H2O n= m/m= 00g/ 18.01528 g/mol
Der ph-wert und ph-indikatoren Kapitel 7 Übung 6.1: Berechnung der Konzentration von Wasser in Wasser Wieviel mol H2O sind in 1 L H2O? M(H2O)= 18.01528 g/mol 1 L(H2O)= 00g H2O n= m/m= 00g/ 18.01528 g/mol
Stelle pflanzliche Farbstoffe her, die zur Säureidentifizierung dienen können.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P757200).3 Pflanzliche Farbstoffe dienen als Indikatoren Experiment von: Phywe Gedruckt: 5.0.203 :9:42 intertess (Version 3.06 B200, Export
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P757200).3 Pflanzliche Farbstoffe dienen als Indikatoren Experiment von: Phywe Gedruckt: 5.0.203 :9:42 intertess (Version 3.06 B200, Export
VERDAUUNG. Der lange Weg durch den Verdauungstrakt
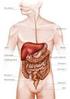 VERDAUUNG Der lange Weg durch den Verdauungstrakt Sonja Zankl SS 2002 DEFINITION Abbau der Nahrungsstoffe im Verdauungstrakt in resorptionsfähige Bestandteile & Aufnahme in Blut bzw. Lymphe Wozu Verdauung?
VERDAUUNG Der lange Weg durch den Verdauungstrakt Sonja Zankl SS 2002 DEFINITION Abbau der Nahrungsstoffe im Verdauungstrakt in resorptionsfähige Bestandteile & Aufnahme in Blut bzw. Lymphe Wozu Verdauung?
Die enzymatische Bräunung
 V23 Die enzymatische Bräunung Fach Klasse Überthema Feinthema Zeit Chemie Q4 Nahrungsmittelzusatzstoffe Antioxidantien 24 h Zusammenfassung Bei dem Versuch wird im Versuchsteil a) die braungefärbte, wässrige
V23 Die enzymatische Bräunung Fach Klasse Überthema Feinthema Zeit Chemie Q4 Nahrungsmittelzusatzstoffe Antioxidantien 24 h Zusammenfassung Bei dem Versuch wird im Versuchsteil a) die braungefärbte, wässrige
Gruppe 4 eigener Versuch. Reduktion von Anthrachinon
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 eigener Versuch Reduktion von Anthrachinon
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 eigener Versuch Reduktion von Anthrachinon
Theorie der Farbigkeit
 1. Theorie der Farbigkeit 1.1 Theorie der Farbigkeit Chromophore Zentraler Bestandteil aller Farbstoffe sind die Chromophore. Als Chromophor (griech. Farbträger) bezeichnet man den Teil eines Farbstoffs,
1. Theorie der Farbigkeit 1.1 Theorie der Farbigkeit Chromophore Zentraler Bestandteil aller Farbstoffe sind die Chromophore. Als Chromophor (griech. Farbträger) bezeichnet man den Teil eines Farbstoffs,
Lebensmittelfarben. Technik beschreiben und benennen. N2 Sachverhalte und einfache Verbindungen zwischen 4
 Lebensmittelfarben Zuordnung zum Kompetenzmodell (KM) Aufgabe(n) KM Beschreibung E3 Ich kann zu Fragestellungen eine passende Untersuchung oder ein Experiment planen, durchführen und protokollieren. N3
Lebensmittelfarben Zuordnung zum Kompetenzmodell (KM) Aufgabe(n) KM Beschreibung E3 Ich kann zu Fragestellungen eine passende Untersuchung oder ein Experiment planen, durchführen und protokollieren. N3
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Kompetenzbereich Umgang mit Fachwissen: Kompetenzbereich Erkenntnisgewinnung: Kompetenzbereich Kommunikation:
 Thema/Kontext: Säuren und Basen in Alltagsprodukten: Konzentrationsbestimmungen von Essigsäure in Lebensmitteln Inhaltsfeld: Säuren, Basen und analytische Verfahren Inhaltliche Schwerpunkte: Eigenschaften
Thema/Kontext: Säuren und Basen in Alltagsprodukten: Konzentrationsbestimmungen von Essigsäure in Lebensmitteln Inhaltsfeld: Säuren, Basen und analytische Verfahren Inhaltliche Schwerpunkte: Eigenschaften
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau
 Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Versuchsprotokoll: Fehling- Spaltung von Saccharose
 Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)
 Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... dokumentieren Experimente in angemessener Fachsprache (u.a. zur Untersuchung der Eigenschaften organischer Verbindungen, zur Einstellung eines
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... dokumentieren Experimente in angemessener Fachsprache (u.a. zur Untersuchung der Eigenschaften organischer Verbindungen, zur Einstellung eines
Versuchsprotokoll: Alginate-Zahnabdruck
 Versuchsprotokoll: Alginate-Zahnabdruck Zeitaufwand: Aufbau: 15 Minuten Durchführung: 15 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalie Menge (in g) R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
Versuchsprotokoll: Alginate-Zahnabdruck Zeitaufwand: Aufbau: 15 Minuten Durchführung: 15 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalie Menge (in g) R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
4. Phthaleine 4.1. Mit den Triphenylmethanfarbstoffen eng verwandt sind die Phthaleine, deren Synthese vom Phthalsäureanhydrid
 4. Phthaleine 4.1 Phthaleine Mit den Triphenylmethanfarbstoffen eng verwandt sind die Phthaleine, deren Synthese vom Phthalsäureanhydrid ausgeht. Phenolphthalein erhält man durch Zusammenschmelzen von
4. Phthaleine 4.1 Phthaleine Mit den Triphenylmethanfarbstoffen eng verwandt sind die Phthaleine, deren Synthese vom Phthalsäureanhydrid ausgeht. Phenolphthalein erhält man durch Zusammenschmelzen von
Lebensmittelfarben. Bitte versucht herauszufinden, welche Farbstoffe sich in Probe 4 befinden und ob E102 darunter ist!
 Liebe Susanne, lieber Philipp!! Lebensmittelfarben Ich möchte euch bitten, mir bei der Lösung eines Problems zu helfen. Ich vertrage schon seit längerer Zeit den Lebensmittelfarbstoff E102 nicht. Jedes
Liebe Susanne, lieber Philipp!! Lebensmittelfarben Ich möchte euch bitten, mir bei der Lösung eines Problems zu helfen. Ich vertrage schon seit längerer Zeit den Lebensmittelfarbstoff E102 nicht. Jedes
Fortbildung am Schülerlabor in Rechtenthal für die Grundschule. Ideen zu weiterführenden Versuchen in der Klasse:
 Fortbildung am 16.11.2012 Schülerlabor in Rechtenthal für die Grundschule Ideen zu weiterführenden Versuchen in der Klasse: Lernziele: -Die Kinder erkennen chemische, physikalische Veränderungen (auch
Fortbildung am 16.11.2012 Schülerlabor in Rechtenthal für die Grundschule Ideen zu weiterführenden Versuchen in der Klasse: Lernziele: -Die Kinder erkennen chemische, physikalische Veränderungen (auch
Glycerin-Projekt Fällt die Fehling Probe mit Glycerin positiv aus?
 Glycerin-Projekt Fällt die Fehling Probe mit Glycerin positiv aus? Melanie Ripsam, Christoph Hille Technische Universität München 13. Dezember 2016 Dieses Werk ist lizenziert unter CC BY 3.0 DE 1 Einleitung
Glycerin-Projekt Fällt die Fehling Probe mit Glycerin positiv aus? Melanie Ripsam, Christoph Hille Technische Universität München 13. Dezember 2016 Dieses Werk ist lizenziert unter CC BY 3.0 DE 1 Einleitung
Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen. Kurzprotokoll. Schulversuchspraktikum.
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
WEGE ZUR BESTIMMUNG EINER SÄURE:
 WEGE ZUR BESTIMMUNG EINER SÄURE: "BESTIMMUNG DES SÄUREGEHALTS IN EINEM HAUSHALTSESSIG" Bestimmung des Säuregehalts in Haushaltsessig In den letzten Chemiestunden versuchten wir, anhand von mehreren Möglichkeiten
WEGE ZUR BESTIMMUNG EINER SÄURE: "BESTIMMUNG DES SÄUREGEHALTS IN EINEM HAUSHALTSESSIG" Bestimmung des Säuregehalts in Haushaltsessig In den letzten Chemiestunden versuchten wir, anhand von mehreren Möglichkeiten
Stationenlauf Volksschulen 28. März 2017, DIE GEHIRNZENTRALE - Neuronenwelt, what s up?
 Hexenküche Verwendung von Pflanzen mit Focus auf die Nutzung in der Apotheke Gemeinsam mit den Kindern wurde ein Honig-Lippenbalsam auf Basis rein natürlicher Zutaten hergestellt. Die einzelnen Rohstoffe
Hexenküche Verwendung von Pflanzen mit Focus auf die Nutzung in der Apotheke Gemeinsam mit den Kindern wurde ein Honig-Lippenbalsam auf Basis rein natürlicher Zutaten hergestellt. Die einzelnen Rohstoffe
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Was ist was? - Identifizierung von Säuren und Basen mit gestuften Hilfen
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Was ist was? - Identifizierung von Säuren und Basen mit gestuften Hilfen Das komplette Material finden Sie hier: School-Scout.de VI
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Was ist was? - Identifizierung von Säuren und Basen mit gestuften Hilfen Das komplette Material finden Sie hier: School-Scout.de VI
LMPG 2, ÜB21, Molekülbau & UV/VIS-Absorption LÖSUNG 1 von 11
 LMPG 2, ÜB21, Molekülbau & UV/VISAbsorption LÖSUG 1 von 11 Übung 1: Charakterisierung von Absorptionsbanden Veränderungen der Molekülstruktur können zu Verschiebungen der einzelnen Absorptionsbanden im
LMPG 2, ÜB21, Molekülbau & UV/VISAbsorption LÖSUG 1 von 11 Übung 1: Charakterisierung von Absorptionsbanden Veränderungen der Molekülstruktur können zu Verschiebungen der einzelnen Absorptionsbanden im
AnC I Protokoll: 3.4 Iodometrische Bestimmung von Ascorbinsäure (Vitamin C)" SS Analytische Chemie I. Versuchsprotokoll
 Analytische Chemie I Versuchsprotokoll 3.4 Iodometrische Bestimmung von Ascorbinsäure (Vitamin C) 1.! Theoretischer Hintergrund Bei dieser Redoxtitration wird Ascorbinsäure mit Hilfe von Triiodid oxidiert.
Analytische Chemie I Versuchsprotokoll 3.4 Iodometrische Bestimmung von Ascorbinsäure (Vitamin C) 1.! Theoretischer Hintergrund Bei dieser Redoxtitration wird Ascorbinsäure mit Hilfe von Triiodid oxidiert.
Schülercode Erste zwei Buchstaben Letzte zwei Buchstaben des Vornamens deiner Geburtstag (TT) deines Vornamens Mutter Kontext Experiment Aufgabe
 Schülercode Letzte zwei Buchstaben deines Vornamens Erste zwei Buchstaben des Vornamens deiner Mutter Geburtstag (TT) Kontext Experiment Aufgabe Erklärung Box 1 Kontext Kohlensäure im Mineralwasser Heute
Schülercode Letzte zwei Buchstaben deines Vornamens Erste zwei Buchstaben des Vornamens deiner Mutter Geburtstag (TT) Kontext Experiment Aufgabe Erklärung Box 1 Kontext Kohlensäure im Mineralwasser Heute
Analytische Chemie. B. Sc. Chemieingenieurwesen. 15. März 2017, Uhr. Prof. Dr. Thomas Jüstel, Dr. Stephanie Möller.
 Analytische Chemie B. Sc. Chemieingenieurwesen 15. März 2017, 12.30 15.30 Uhr Prof. Dr. Thomas Jüstel, Dr. Stephanie Möller Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Analytische Chemie B. Sc. Chemieingenieurwesen 15. März 2017, 12.30 15.30 Uhr Prof. Dr. Thomas Jüstel, Dr. Stephanie Möller Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Triphenylmethanfarbstoffe
 3. Triphenylmethanfarbstoffe 3.1 Triphenylmethanfarbstoffe Diese Farbstoffklasse leitet sich vom Triphenylcarbeniumion als Chromophor ab. Durch Einführung auxochromer Gruppen in Parastellung kann man die
3. Triphenylmethanfarbstoffe 3.1 Triphenylmethanfarbstoffe Diese Farbstoffklasse leitet sich vom Triphenylcarbeniumion als Chromophor ab. Durch Einführung auxochromer Gruppen in Parastellung kann man die
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Anorganische Chemie für Biologen
 Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Arten chemischer Bindung Die entscheidende Größe für den
Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Arten chemischer Bindung Die entscheidende Größe für den
Analytische Chemie. B. Sc. Chemieingenieurwesen. 8. Juli 2015, Uhr. Prof. Dr. T. Jüstel, Stephanie Möller M. Sc.
 Analytische Chemie B. Sc. Chemieingenieurwesen 8. Juli 2015, 12.30 15.30 Uhr Prof. Dr. T. Jüstel, Stephanie Möller M. Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Analytische Chemie B. Sc. Chemieingenieurwesen 8. Juli 2015, 12.30 15.30 Uhr Prof. Dr. T. Jüstel, Stephanie Möller M. Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Von Arrhenius zu Brönsted
 Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Gruppe 13 vorgegebener Versuch. Polyelektrolyte im Haargel
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 17.06.09 SS 09 Gruppe 13 vorgegebener Versuch Polyelektrolyte
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 17.06.09 SS 09 Gruppe 13 vorgegebener Versuch Polyelektrolyte
Der Einfluss verschiedener Hopfenfraktionen auf die Inhibierung der Rotfärbung von Gerstenmalzmaischen
 Technische Universität München Center of Life and Food Sciences Weihenstephan Forschungszentrum für Brau- und Lebensmittelqualität Prof. Dr.-Ing. Fritz Jacob Der Einfluss verschiedener Hopfenfraktionen
Technische Universität München Center of Life and Food Sciences Weihenstephan Forschungszentrum für Brau- und Lebensmittelqualität Prof. Dr.-Ing. Fritz Jacob Der Einfluss verschiedener Hopfenfraktionen
7. Chemische Reaktionen
 7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte Grundlagen Lösung: homogene Phase aus Lösungsmittel und gelösten Stoff Lösungsmittel liegt im Überschuss vor
7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte Grundlagen Lösung: homogene Phase aus Lösungsmittel und gelösten Stoff Lösungsmittel liegt im Überschuss vor
Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1 Ch-GK Q1/IHF 2: Unterrichtsvorhaben I:
 Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1 Ch-GK Q1/IHF 2: Unterrichtsvorhaben I: Kontext: Säuren und Basen in Alltagsprodukten Inhaltsfeld: Säuren,
Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1 Ch-GK Q1/IHF 2: Unterrichtsvorhaben I: Kontext: Säuren und Basen in Alltagsprodukten Inhaltsfeld: Säuren,
Versuch: Seifenherstellung aus Kokosfett
 Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Entscheide bei jeder Aussage, ob es eine reine Beobachtung ist oder nicht, und kreuze an!
 Kerze Eine brennende Kerze wandelt Energie und Stoffe um. N_9d_44 Über eine brennende Rechaudkerze (Teelicht) wird ein «leeres» Glas gestülpt. Schülerinnen und Schüler notieren Aussagen zum Versuch. Entscheide
Kerze Eine brennende Kerze wandelt Energie und Stoffe um. N_9d_44 Über eine brennende Rechaudkerze (Teelicht) wird ein «leeres» Glas gestülpt. Schülerinnen und Schüler notieren Aussagen zum Versuch. Entscheide
