PEM-Elektrolyseur Betriebsanleitung
|
|
|
- Gudrun Steinmann
- vor 7 Jahren
- Abrufe
Transkript
1 R PEM-Elektrolyseur Betriebsanleitung Fig. 1: PEM-Elektrolyseur 1 ZWECK UND BESCHREIBUNG Bei einem PEM-Elektrolyseur besteht der Elektrolyt aus einer protonenleitfähigen Membran und Wasser (PEM = Proton Exchange Membrane = Protonen-Austauch-Membran). Die Membran befindet sich zwischen zwei Elektroden, die mit Katalysatormaterial beschichtet sind. Bei Anlegen einer Gleichspannung, die größer ist als die Zersetzungsspannung der Zelle, setzt die Elektrolyse ein, es entstehen Wasserstoff und Sauerstoff. Dieser PEM-Elektrolyseur ist ausschließlich für Lehr- und Demonstrationszwecke entwickelt worden, eine andere Verwendung ist unzulässig. Mit dem PEM-Elektrolyseur können die Funktionsweise demonstriert und die elektrischen Eigenschaften durch Aufnahme einer Strom-Spannungs-Kennlinie und durch Bestimmung des Wirkungsgrades untersucht werden. 2 SICHERHEITSHINWEIS Der PEM-Elektrolyseur erzeugt Wasserstoff und Sauerstoff, diese können ein explosionsfähiges Gemisch bilden. Es sind daher jede Art von Feuer und Zündquellen vom Versuchsaufbau fernzuhalten! Die allgemeinen Sicherheitsvorschriften beim Umgang mit Wasserstoff und Sauerstoff sind zu beachten. 3 FUNKTIONS- UND BEDIENELEMENTE 1 Vorratsbehälter für destilliertes Wasser (entmineralisiertes Wasser, σ <2 µs/cm) 2 Gummistopfen zum Verschließen der Vorratsbehälter. Dies ist vor allem dann erforderlich, wenn die Gase über Schläuche in die PEM-Brennstoffzelle ( ) oder die Klein-Gasometer der Gasbar ( ) weitergeleitet werden sollen. 3 Elektrolyseur Das Wasser wird dem Elektrolyseur durch Schläuche von unten her zugeführt. Die beiden oberen Schläuche leiten die entstehenden Gase und überschüssiges Wasser in die Vorratsbehälter. Die Gase steigen dann auf. 4 4-mm-Buchse (Minus) 5 4-mm-Buchse (Plus) 4 HANDHABUNG Die Vorratsbehälter werden mindestens bis zwischen die beiden unteren Markierungslinien (min und max) mit destilliertem Wasser (entmineralisiertem Wasser, σ <2 µs/cm) gefüllt. Sollen die entstehenden Gase zur Volumenmessung oder Speicherung weitergeleitet werden werden, so müssen auch die angeschlossenen Schläuche zunächst mit Wasser gefüllt sein, damit kein Gasgemisch entsteht. Dazu werden die Vorratsbehälter bis zur oberen Markierungslinie (Gastest) gefüllt und die Schläuche so gehalten, daß sie sich ebenfalls mit Wasser füllen, dann werden die Stopfen so aufgesetzt, daß darunter keine Luftblasen entstehen (genaue Beschreibung siehe Experiment Wirkungsgrad ). Zum Betrieb des Elektrolyseurs wird eine Gleichspannung zwischen 1,7 V und 2 V angelegt. Achtung: Nur destilliertes Wasser (entmineralisiertes Wasser, σ <2 µs/cm) in die Vorratsbehälter füllen! Mit einer Wasserfüllung sollte der Elektrolyseur höchstens einen Tag lang arbeiten. Nach Gebrauch des Elektrolyseurs wird das Wasser ausgegossen. Die maximale Spannung beträgt 2 V. PHYWE SYSTEME GMBH Robert-Bosch-Breite 10 D Göttingen Telefon (05 51) Telefax (05 51)
2 Bei Anschluß der elektrischen Spannung auf die richtige Polung achten. Eine Diode auf der Unterseite der Grundplatte schützt den Elektrolyseur gegen Verpolung, die ihn sonst zerstören würde. Die maximale Dauer-Stromstärke beträgt 2 A. Ein kurzzeitiger Betrieb mit einer Stromstärke über 2 A, z.b. bei Aufnahme der Strom-Spannungs-Kennlinie, schadet der Zelle jedoch nicht. 5 FUNKTIONSWEISE DES PEM-ELEKTROLYSEURS Das Kernstück des PEM-Elektrolyseurs ist eine Membran- Elektrodeneinheit. Auf die dünne protonenleitfähige Membran (PEM = protone exchange membrane) ist auf beiden Seiten eine Schicht aus Katalysatormaterial aufgebracht. Diese beiden Schichten bilden Anode und Kathode der elektrochemischen Zelle. 6 WARTUNG Die Elektrolyseur benötigt keine besondere Wartung. Das Wasser in den Vorratsgefäßen sollte aber nach Gebrauch entfernt bzw. nach spätestens einem Tag erneuert werden, da sich beim Elektrolyse-Prozess Metallionen im Wasser lösen, die die Membran zerstören können. 7 TECHNISCHE DATEN Elektrodenfläche 16 cm 2 Leistung 2 W Betriebsspannung 1, V max. Dauerstromstärke 2 A Im PEM-Elektrolyseur findet folgende Reaktion statt (Fig. 2): Anode 2H 2 O > 4e - + 4H + + O 2 Kathode 4H + + 4e - > 2H 2 Gesamtreaktion 2H 2 O > 2H 2 + O 2 Auf der Anodenseite entstehen durch die katalytische Wirkung der Elektrode bei angelegter äußerer Spannung gasförmiger Sauerstoff, Elektronen und H + -Ionen. Die H + -Ionen (Protonen) wandern durch die protonenleitende Membran zur Kathode und bilden dort mit den über den äußeren Leiterkreis fließenden Elektronen gasförmigen Wasserstoff. Fig. 2: Funktionsprinzip eines PEM-Elektrolyseurs 2
3 8 EXPERIMENTE 1. Aufnahme der Kennlinie des PEM-Elektrolyseurs Elektrolyse tritt dann in der Zelle auf, wenn die anliegende Gleichspannung größer ist als die sog. Zersetzungsspannung der Zelle. Zur Aufnahme der Kennlinie muß bei jeder angelegten Spannung zunächst ein Gleichgewichtszustand abgewartet werden, bis die Stromstärke einen konstanten Wert annimmt. Es wird empfohlen, die bei hohen Spannungswerten zu beginnen, da sich der Gleichgewichtszustand dann schneller einstellt. Material PEM-Elektrolyseur Spritzflasche 500 ml Digitalmultimeter* (2x) Netzgerät universal Verbindungsleitung, 50 cm, rot (2x) Verbindungsleitung, 50 cm, blau Verbindungsleitung, 75 cm, rot Verbindungsleitung, 75 cm, blau ca. 2 Liter destilliertes Wasser (entmineralisiertes Wasser, σ <2 µs/cm) * oder Demonstrations-Meßinstrumente Aufbau und Durchführung Beide Wasservorratsbehälter bis zwischen die beiden Markierungslinien (min und max) mit destilliertem Wasser füllen (entmineralisiertes Wasser, σ <2 µs/cm). Der Anschluß des Elektrolyseurs an den Gleichspannungsausgang des Netzgerätes erfolgt nach dem Versuchsaufbau in Fig. 3 und der Schaltskizze in Fig. 4. Da der Innenwiderstand des Amperemeters nicht vernachlässigbar ist, wird das Voltmeter direkt an den Elektrolyseur angeschlossen. Es ist empfehlenswert, beim höchsten Spannungswert U = 2 V zu beginnen, dabei darf die Stromstärke kurzzeitig den Wert der maximalen Dauerstromstärke von I = 2 A überschreiten. Nach ca. 1 min stabilisieren sich die Werte für Spannung und Stromstärke. Am Netzgerät den Stellknopf für die Stromregelung schrittweise zurückstellen. Dabei regelt das Netzgerät Fig. 3: Kennlinie des Elektrolyseurs (Versuchsaufbau) die Spannung elektronisch, sodaß die Stromstärke den eingestellten Wert hat. Dies Verfahren hat den Vorteil, daß sich am Elektrolyseur schneller stabile Werte für Spannung und Stromstärke einstellen. Wenn der Stellknopf für die Stromstärke sein Minimum erreicht hat, können kleinere Werte noch mit Hilfe des Stellknopfes für die Spannung gewählt werden. Vor Aufnahme eines Meßwertes ist dann ca. 1 min bis zur Stabilisierung der Strom- und Spannungswerte zu warten. Meßergebnisse Tabelle 1 U / V I / A 2,00 2,69 1,91 2,20 1,81 1,50 1,75 1,00 1,68 0,51 1,61 0,21 1,55 0,11 1,51 0,06 1,40 0,03 0,99 0,02 0,40 0,00 Die Leistungsfähigkeit des Elektolyseurs ist stark vom jeweiligen Betriebszustand abhängig. Wurde er längere Zeit nicht benutzt, kann die Stomstärke bei 2 V kleiner sein als in der Tabelle angegeben, nach längerer Betriebszeit evtl. auch sehr viel größer. Fig. 4: Kennlinie des Elektrolyseurs (Schaltskizze) 3
4 Auswertung Befinden sich eine Wasserstoff- und eine Sauerstoff-Elektrode in einer Elektrolysezelle, so besteht zwischen den beiden Elektroden eine Potentialdifferenz E. Sie ist temperaturabhängig, der theoretische Wert läßt sich aus der freien Reaktionsenthalpie G berechnen und beträgt bei 25 C E = 1,23 V Bei der Elektrolyse muß die angelegte Spannung mindestens so groß sein wie diese theoretische Zellspannung, damit ein Strom fließen kann.es treten aber noch zusätzliche Potentialsprünge an den Elektroden auf: Im elektrochemischen Gleichgewicht treten an den Elektroden noch Phasengrenzpoteniale zwischen Elektrode und Membran auf. Dabei findet ständiger Ladungsaustausch zwischen beiden statt, die Bruttoreaktion ist aber gleich Null. Fließt zusätzlich ein Strom durch den Elektrolyseur, so wird das elektrochemische Gleichgewicht an den Elektroden gestört. Das Elektrodenpotential nimmt durch verschiedene Reaktionen an der Elektrode einen anderen, von der Stromdichte abhängigen Wert an. Die Abweichung vom Gleichgewichtswert heißt Elektrische Polarisation, die Elektrode wird polarisiert. Die Kennlinie des Elektrolyseurs zeigt deshalb erst beim Übergang zu größeren Stromstärken annähernd einen linearen Verlauf, in diesem Bereich ist die Wanderung der Ionen durch die Membran maßgebend. Die Meßwerte aus Tabelle 1 sind in Fig. 5 dargestellt. Aus dem linearen Teil der Kennlinie wird die Zersetzungsspannung U Z als Schnittpunkt der verlängerten Gerade mit der U-Achse ermittelt: U Z = 1,60 V Fig. 5: Strom-Spannungs-Kennlinie eines PEM-Elektrolyseurs 4
5 2. Bestimmung des Wirkungsgrades des PEM-Elektrolyseurs Die bei der Elektrolyse entstehenden Gase werden in den Klein-Gasometern der Gasbar aufgefangen, um die entstehende Menge an Wasserstoff in Abhängigkeit von Stromstärke und Zeit zu messen. Für dieses Experiment sind Gummischläuche besser geeignet, als die zum Lieferumfang des Elektrolyseurs gehörenden Siliconschläuche, da die Gasdiffusion durch Siliconschläuche größer ist (Wasserstoff diffundiert hinaus, Stickstoff hinein in den Schlauch). Material PEM-Elektrolyseur Gasbar Gummischlauch, d i = 4 mm Gummischlauch, d i = 6 mm Schlauchklemme, Breite 10 mm (2x) Schlauchverbinder (Red.) 3-6 / 7-11 mm (2x) Spritzflasche 500 ml Becher 250 ml, Kunststoff Stoppuhr* Handmeßgerät für Druck* Thermometer* Digitalmultimeter* (2x) Netzgerät universal Verbindungsleitung, 50 cm, rot (2x) Verbindungsleitung, 50 cm, blau Verbindungsleitung, 75 cm, rot Verbindungsleitung, 75 cm, blau ca. 2 Liter destilliertes Wasser (entmineralisiertes Wasser, σ <2 µs/cm) *oder entsprechende Demonstrations-Meßinstrumente Aufbau und Durchführung Vorbereitung der Gasbar mit 2 Gasometern: Ein Gasometer besteht jeweils aus einem Erlenmeyerkolben mit aufgesetztem zylindrischen Trichter und einem gewinkelten Glasröhrchen. Die Reduktionsstücke mit einem kurzen Stück Gummischlauch (d i = 6 mm) jeweils an die Glasröhrchen der Gasometer anschließen. Beide Gasometer jeweils über die zylindrischen Trichter mit destilliertem Wasser füllen, bis die Erlenmeyerkolben und die rechtwinkligen Glasröhrchen möglichst blasenfrei gefüllt sind. Überschüssiges Wasser läuft dann über die Glasröhrchen ab und wird in einem Becher aufgefangen. Die zylindrischen Trichter besitzen Markierungen für die Füllhöhe. Es empfiehlt sich, die Genauigkeit dieser Markierungen zu kontrollieren, indem der ganze Trichter mit destilliertem Wasser gefüllt wird, das dann in ein Volumenmeßgerät ausfließt. Der Versuchaufbau zur Wirkungsgrad-Bestimmung des Elektrolyseurs erfolgt nach Fig. 6. An die oberen Auslaufstutzen der Vorratsbehälter des Elektrolyseurs jeweils einen ca. 40 cm langen dünnen Gummischlauch (d i = 4 mm) anschließen. Die Vorratsbehälter bis zur oberen Markierungslinie (Gastest) mit destilliertem Wasser füllen, dabei die Schläuche hochhalten, sodaß auch diese sich mit Wasser füllen. Die mit Wasser gefüllten Gummischläuche ca. 2 cm vor dem Ende mit einer Klemme verschließen und an die Gasometer anschließen. Gummistopfen so auf die Vorratsbehälter aufsetzen, daß sich keine Luftblasen darunter bilden und fest aufdrücken, damit kein Gas entweichen kann. Die Schlauchklemmen öffnen. Den Elektrolyseur nach Fig. 4 an das Netzgerät anschließen und mit dem Stellknopf für Stromstärkeregelung eine Stromstärke von ca. 1 A einstellen. Der Elektrolyseur erzeugt Wasserstoff und Sauerstoff im Verhältnis 2:1. Das Volumen V H2 des entstandenen Wasserstoffes wird in Abhängigkeit von der Zeit t gemessen. Zeit- Fig. 6: Wirkungsgrad des PEM-Elektrolyseurs (Versuchsaufbau) 5
6 messung starten, wenn der Wasserstand im zylindrischen Trichter (H 2 ) die untere Marke (25 ml) überschreitet. - Während der Elektrolyse Spannung U und Stromstärke I messen. - Raumtemperatur ϑ und Umgebungsdruck p amb messen. - Zum Abschluß des Versuches den Elektrolyseur abschalten und die Schläuche zu den Gasometern mit Klemmen verschließen. - Der Versuch kann mit einer anderen Stromstärke wiederholt werden. Auswertung Die bei einer Elektrolyse abgeschiedene Stoffmenge n läßt sich mit Hilfe der Faradayschen Gesetze berechnen. (1) I t n = z F Dabei ist I = Stromstärke, t = Zeit, z = Anzahl der Elektronen, um ein Molekül abzuscheiden, F = As/mol, Faradaykonstante Meßergebnisse Tabelle 2.1 (Stromstärke 1 A) I = 1,02 A U = 1,71 V p amb = 984 hpa ϑ = 21 C V H2 / ml t / min:s t / s 0 0: : : : : : : : Tabelle 2.2 (Stromstärke 2 A) I = 2,01 A U = 1,83 V p amb = 984 hpa ϑ = 21 C V H2 / ml t / min:s t / s 0 0: : : : : : : : In diesem Versuch werden Gase abgeschieden. Das Volumen einer Stoffmenge n läßt sich mit Hilfe der allgemeinen Gasgleichung bestimmen. (2) Dabei ist T = absolute Temperatur, p = Druck, R = 8,31 J/(mol K), allgemeine Gaskonstante Wenn im Elektrolyseur ein Stom I fließt, wird nach Gleichung (1) und (2) folgendes Gasvolumen pro Zeiteinheit erzeugt (3) V V t n R T = p = I R T z F p Die Meßwerte von Tabelle 2.1 und 2.2 sind in Fig. 7 dargestellt. Aus der Steigung der Geraden ergibt sich das erzeugte Volumen pro Zeiteinheit V H2 / t (gemessen). Diese Werte werden mit den theoretischen nach Gleichung (3) verglichen und daraus die Gasausbeute, d.h. der sog. Stromwirkungsgrad berechnet. Für den Druck p kann der Wert des gemessenen Umgebungsdrucks p amb eingesetzt werden. Zwei Korrekturen müßten vorgenommen werden, die sich aber gegenseitig aufheben: Im Gasometer steht eine Wassersäule über dem Gas, ein Druck von ca. 20 hpa müßte addiert werden. Der erzeugte Wasserstoff ist mit Wasserdampf gesättigt, der Sättigungsdampfdruck von 23 hpa müßte subtrahiert werden. Fig. 7: Volumen des vom PEM-Elektrolyseur erzeugten Wasserstoffs in Abhängigkeit von der Zeit bei verschiedenen Stromstärken I. 6
7 Tabelle 2.3 p = p amb = 984 hpa T = 294 K Betriebs- V H2 / t V H2 / t Gasbedingungen gemessen theoretisch ausbeute I = 1,02 A 0,121 ml / s 0,131 ml / s 92 % U = 1,71 V I = 2,01 A 0,243 ml / s 0,258 ml / s 94 % U = 1,83 V Die fehlenden 6 bis 8 % des Gases sind Diffusionsverluste innerhalb der Zelle. Zur Bestimmung des Wirkungsgrades des PEM-Elektrolyseurs werden die elektrische Energie W el und die chemische Energie W H2 des erzeugten bzw. benötigten Wasserstoffs berechnet. (4) (5) Wel = U I t W H 2 = n H Dabei ist U = Spannung, I = Stromstärke, t = Zeit, n = Stoffmenge des Wasserstoffs H = molarer Heizwert (molare Reaktionsenthalpie) des Wasserstoffs Man unterscheidet zwischen dem unteren Heizwert H u und dem oberen Heizwert H 0. Molare Heizwerte von Wasserstoff: H u = 242,0 kj/mol H 0 = 286,1 kj/mol Die Differenz zwischen beiden ist die molare Verdampfungsenthalpie (Kondensationsenthalpie) q von Wasser. Der Wirkungsgrad des Elektrolyseurs berechnet sich nach Gleichung (4) und (5) (7) Die gemessenen Volumina V des Wasserstoffs werden mit Hilfe der allgemeinen Gasgleichung (2) auf Stoffmengen n umgerechnet. Somit erhält man für den Wirkungsgrad (8) WH 2 Ho n η = = W U I t η = el Tabelle 2.4 p = p amb = 984 hpa T = 294 K Ho p V R T U I t Betriebsbedingungen Wirkungsgrad I = 1,02 A 80 % U = 1,71 V I = 2,01 A 76 % U = 1,83 V Der Wirkungsgrad des Elektrolyseurs ist bei 1,71 V / 1,02 A etwas größer als bei 1,83 V / 2,01 A. Die Gasausbeute ist in beiden Fällen etwa gleich groß. (6) H = H + q o u 7
8 3. PEM-Anlage, versorgt durch Solarenergie Der PEM-Elektrolyseur kann auch mit elektrischer Energie aus einer Solarbatterie betrieben werden. Die Solarbatterie muß mindestens 4 in Reihe geschaltete Zellen besitzen, um die für den Elektrolyseur benötigte Spannung zu liefern. Die vom Elektrolyseur erzeugten Gase versorgen die PEM- Brennstoffzelle und mit der von der Brennstoffzelle gelieferten elektrischen Energie wird ein kleiner Motor betrieben. Material PEM-Brennstoffzelle PEM-Elektrolyseur Solarbatterie, 4 Zellen Glühlampe 220V, 120W, m. Refl Lampenfassung E27, Netzanschl Motor, 2V Scheibe für 2V-Motor Dreifuß PASS Tonnenfuß PASS Verbindungsleitung, 50 cm, rot (2x) Verbindungsleitung, 50 cm, blau (2x) Spritzflasche 500 ml ca. 0,5 Liter destilliertes Wasser (entmineralisiertes Wasser, σ <2 µs/cm) Vorbereitung des Versuches: In dieser Anlage werden Wasserstoff und Sauerstoff vom PEM-Elektrolyseur zur PEM-Brennstoffzelle geleitet. Es ist sicherzustellen, daß der Zuleitungsschlauch für Wasserstoff vor Anschluß an die Brennstoffzelle nicht mit Luft gefüllt ist. Dies wird dadurch erreicht, daß der Elektrolyseur einige Minuten lang Gase produziert (bei einer Stromstärke von 1 A ca. 2 min, bei einer Stromstärke von 100 ma (von der Solarbatterie) ca. 20 min), bevor die Schläuche an die Brennstoffzelle angeschlossen werden, zur Kontrolle dieses Vorgangs können die Schläuche auch zunächst vollständig mit Wasser gefüllt werden, das dann von den produzierten Gasen verdrängt wird. Betrieb der Anlage: Der Abstand zwischen Lampe und Solarbatterie sollte 40 cm betragen. Bei größeren Abständen wäre die Stromstärke zu klein, bei kleineren Abständen würde sich die Solarbatterie bei längerer Betriebszeit zu stark erwärmen. Der PEM-Elektrolyseur wird von der Solarbatterie versorgt. An die Brennstoffzelle wird ein kleiner Motor angeschlossen, um zu demonstrieren, daß elektrische Energie erzeugt wird. Aufbau und Durchführung Fig. 8: PEM-Anlage, betrieben mit Solarenergie Ergebnis Bei Anschluß des PEM-Elektrolyseurs an die Solarbatterie liegt der Arbeitspunkt des Elektrolyseurs im Schnittpunkt der Strom-Spannungs-Kennlinien von Elektrolyseur und Solarbatterie (Fig. 9). Die Gasproduktion ist sehr gering. Sie reicht aber aus, um die Brennstoffzelle zu versorgen und damit den kleinen Motor zu betreiben (er benötigt nur wenig Strom und läuft bereits bei Spannungen unter 0,5 V an). Diese Anlage kann mehrere Stunden zur Demonstration verwendet werden. Fig. 9: Strom-Spannungs-Kennlinien, (x) PEM-Elektrolyseur (o) Solarbatterie, Abstand zur Lampe = 40 cm 8
PEM-Brennstoffzelle Betriebsanleitung. 1 auf der Rückseite auf der 6. Rückseite
 R PEM-Brennstoffzelle Betriebsanleitung 3 1 auf der Rückseite 5 4 2 auf der 6 Rückseite Fig. 1: PEM-Brennstoffzelle 1 ZWECK UND BESCHREIBUNG Eine PEM-Brennstoffzelle erzeugt elektrische Energie aus Wasserstoff
R PEM-Brennstoffzelle Betriebsanleitung 3 1 auf der Rückseite 5 4 2 auf der 6 Rückseite Fig. 1: PEM-Brennstoffzelle 1 ZWECK UND BESCHREIBUNG Eine PEM-Brennstoffzelle erzeugt elektrische Energie aus Wasserstoff
Robert-Bosch-Gymnasium
 Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 1 Kennlinie des Elektrolyseurs Versuchszweck Beim
Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 1 Kennlinie des Elektrolyseurs Versuchszweck Beim
Faradayscher und energetischer Wirkungsgrad einer PEM Brennstoffzelle
 Faradayscher und energetischer Wirkungsgrad einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformation Zusatzinformationen Der Wirkungsgrad der Brennstoffzelle ist ein Indikator für die Effizienz
Faradayscher und energetischer Wirkungsgrad einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformation Zusatzinformationen Der Wirkungsgrad der Brennstoffzelle ist ein Indikator für die Effizienz
Robert-Bosch-Gymnasium
 Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 3 Wirkungsgrad der Brennstoffzelle Versuchszweck
Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 3 Wirkungsgrad der Brennstoffzelle Versuchszweck
Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle
 Lehrer-/Dozentenblatt Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Alle Brennstoffzellen bestehen prinzipiell aus zwei
Lehrer-/Dozentenblatt Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Alle Brennstoffzellen bestehen prinzipiell aus zwei
Strom-Spannungs-Kennlinie einer PEM Brennstoffzelle
 Lehrer-/Dozentenblatt Strom-Spannungs-Kennlinie einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusatzinformationen Eine PEM Brennstoffzelle besitzt keine lineare Leistungskurve, sondern
Lehrer-/Dozentenblatt Strom-Spannungs-Kennlinie einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusatzinformationen Eine PEM Brennstoffzelle besitzt keine lineare Leistungskurve, sondern
Strom-Spannungs-Kennlinie und Leistung einer PEM Brennstoffzelle
 Strom-Spannungs-Kennlinie und Leistung ENT Schlüsselworte Brennstoffzelle, Protonen-Austausch-Membran, Kennlinie, elektrische Leistung, Innenwiderstand, Wasserstoff Prinzip In reagieren Wasserstoff und
Strom-Spannungs-Kennlinie und Leistung ENT Schlüsselworte Brennstoffzelle, Protonen-Austausch-Membran, Kennlinie, elektrische Leistung, Innenwiderstand, Wasserstoff Prinzip In reagieren Wasserstoff und
Robert-Bosch-Gymnasium
 Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 2 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 2 Kennlinien der Brennstoffzelle Versuchszweck
Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 2 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 2 Kennlinien der Brennstoffzelle Versuchszweck
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Elektrochemie 1 Abbildung 1: I. VERSUCHSZIEL
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Elektrochemie 1 Abbildung 1: I. VERSUCHSZIEL
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg PROTOKOLL SEKUNDARSTUFE II Modul: Versuch: Elektrochemie 1 Abbildung 1:
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg PROTOKOLL SEKUNDARSTUFE II Modul: Versuch: Elektrochemie 1 Abbildung 1:
Kennlinie der Brennstoffzelle
 E z1 Kennlinie der Material: Zerlegbare mit Membran,3 mg/cm Pt sowie Wasserstoff- und Sauerstoffendplatte montiert nach Aufbauanleitung Komponenten aus Schülerkasten Solar-Wasserstoff-Technologie: Solarmodul
E z1 Kennlinie der Material: Zerlegbare mit Membran,3 mg/cm Pt sowie Wasserstoff- und Sauerstoffendplatte montiert nach Aufbauanleitung Komponenten aus Schülerkasten Solar-Wasserstoff-Technologie: Solarmodul
Ausdehnung von Luft bei konstantem Volumen
 Lehrer-/Dozentenblatt Ausdehnung von Luft bei konstantem Volumen (Artikelnr.: P042800) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema: Wärmeausdehnung
Lehrer-/Dozentenblatt Ausdehnung von Luft bei konstantem Volumen (Artikelnr.: P042800) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema: Wärmeausdehnung
Wind-Wasserstoff-Anlage
 Wind-Wasserstoff-Anlage ENT Schlüsselworte Elektrolyse, Protonen-Austausch-Membran, Brennstoffzelle, Windkraftanlage, Wasserstoff, Energieumwandlung Prinzip Windenergie kann mit Hilfe eines Windgenerators
Wind-Wasserstoff-Anlage ENT Schlüsselworte Elektrolyse, Protonen-Austausch-Membran, Brennstoffzelle, Windkraftanlage, Wasserstoff, Energieumwandlung Prinzip Windenergie kann mit Hilfe eines Windgenerators
Untersuchung der Abhängigkeit des Photostroms von der Entfernung zur Lichtquelle
 E1 S 3 Untersuchung der Abhängigkeit des Photostroms von der Entfernung zur Lichtquelle Name: Datum: Aufgaben: a) Miss die Höhe des Photostroms in Abhängigkeit von der Entfernung zur Lampe. b) Zeichne
E1 S 3 Untersuchung der Abhängigkeit des Photostroms von der Entfernung zur Lichtquelle Name: Datum: Aufgaben: a) Miss die Höhe des Photostroms in Abhängigkeit von der Entfernung zur Lampe. b) Zeichne
Brennstoffzelle. Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes. Schüler-Skript und Versuchsanleitung
 Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes Bearbeitet von Markus Beckert, Sheila Sabock Stand 12.09.2013 Inhaltsverzeichnis 1 Einführung... 3 1.1 Vorbereitung, Vorwissen, Vorüberlegungen...
Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes Bearbeitet von Markus Beckert, Sheila Sabock Stand 12.09.2013 Inhaltsverzeichnis 1 Einführung... 3 1.1 Vorbereitung, Vorwissen, Vorüberlegungen...
E7 Elektrolyse. Versuchsprotokoll von Thomas Bauer und Patrick Fritzsch. Münster, den
 E7 Elektrolyse Versuchsprotokoll von Thomas Bauer und Patrick Fritzsch Münster, den 18.12.2000 INHALTSVERZEICHNIS 1. Einleitung 2. Theoretische Grundlagen 2.1 Elektrolyse 2.2 Die FARADAYschen Gesetze der
E7 Elektrolyse Versuchsprotokoll von Thomas Bauer und Patrick Fritzsch Münster, den 18.12.2000 INHALTSVERZEICHNIS 1. Einleitung 2. Theoretische Grundlagen 2.1 Elektrolyse 2.2 Die FARADAYschen Gesetze der
Ausdehnung von Luft bei konstantem Druck
 Lehrer-/Dozentenblatt Ausdehnung von Luft bei konstantem Druck (Artikelnr.: P042700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema: Wärmeausdehnung
Lehrer-/Dozentenblatt Ausdehnung von Luft bei konstantem Druck (Artikelnr.: P042700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema: Wärmeausdehnung
LEISTUNGSTEST ELEKTROLYSE-STACK
 LEISTUNGSTEST ELEKTROLYSE-STACK Energetischer und Faradayscher Wirkungsgrad Plus, (Thorsten Müller) Bandit, Rubberduck, (Saša Smolčić) 20140225 Dieses Material steht unter der Creative-Commons-Lizenz Namensnennung
LEISTUNGSTEST ELEKTROLYSE-STACK Energetischer und Faradayscher Wirkungsgrad Plus, (Thorsten Müller) Bandit, Rubberduck, (Saša Smolčić) 20140225 Dieses Material steht unter der Creative-Commons-Lizenz Namensnennung
Bedienungsanleitung. D101 Exhibition Set.
 Bedienungsanleitung D101 Exhibition Set www.h-tec.com www.h-tec.com Inhalt Einleitung 4 Bestimmungsgemäße Verwendung 5 Allgemeine Sicherheitshinweise 6 Geräte und Material 8 Funktion des Premium Exhibition
Bedienungsanleitung D101 Exhibition Set www.h-tec.com www.h-tec.com Inhalt Einleitung 4 Bestimmungsgemäße Verwendung 5 Allgemeine Sicherheitshinweise 6 Geräte und Material 8 Funktion des Premium Exhibition
Physikalisches Anfaengerpraktikum. Brennstoffzelle
 Physikalisches Anfaengerpraktikum Brennstoffzelle Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 25. Februar 2005 I. Versuchsaufbau und -beschreibung Die Versuchsapparatur bestand
Physikalisches Anfaengerpraktikum Brennstoffzelle Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 25. Februar 2005 I. Versuchsaufbau und -beschreibung Die Versuchsapparatur bestand
Experimentiertag. Datum: Name: Klasse: Schule:
 Experimentiertag Datum: Name: Klasse: Schule: E1 V 1 Generator, Propeller, Solarmodul Wovon hängt die Spannung ab? 1.) Spannung aus dem Generator: (Taucht in der Spannungsanzeige kein Minuszeichen auf,
Experimentiertag Datum: Name: Klasse: Schule: E1 V 1 Generator, Propeller, Solarmodul Wovon hängt die Spannung ab? 1.) Spannung aus dem Generator: (Taucht in der Spannungsanzeige kein Minuszeichen auf,
LEISTUNGSTEST ELEKTROLYSE-STACK
 LEISTUNGSTEST ELEKTROLYSE-STACK Energetischer und Faradayscher Wirkungsgrad HHO-Generator HG21 Elektrolyse-Stack von Alexander Weis Travelnova TN-S1 Elektrolyse-Stack von Saša Smolčić Dieses Material steht
LEISTUNGSTEST ELEKTROLYSE-STACK Energetischer und Faradayscher Wirkungsgrad HHO-Generator HG21 Elektrolyse-Stack von Alexander Weis Travelnova TN-S1 Elektrolyse-Stack von Saša Smolčić Dieses Material steht
1.) Skizzierieren Sie den Aufbau einer PEM Brennstoffzelle und erläutern Sie deren Funktionsweise.
 E50 Name: Brennstoffzelle Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Dieser Fragebogen muss von jedem Teilnehmer eigenständig (keine Gruppenlösung!)
E50 Name: Brennstoffzelle Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Dieser Fragebogen muss von jedem Teilnehmer eigenständig (keine Gruppenlösung!)
GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN
 10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
Physikalisches Grundpraktikum Taupunktmessung. Taupunktmessung
 Aufgabenstellung: 1. Bestimmen Sie den Taupunkt. Berechnen Sie daraus die absolute und relative Luftfeuchtigkeit. 2. Schätzen Sie die Messunsicherheit ab! Stichworte zur Vorbereitung: Temperaturmessung,
Aufgabenstellung: 1. Bestimmen Sie den Taupunkt. Berechnen Sie daraus die absolute und relative Luftfeuchtigkeit. 2. Schätzen Sie die Messunsicherheit ab! Stichworte zur Vorbereitung: Temperaturmessung,
Verwandte Begriffe Maxwell-Gleichungen, elektrisches Wirbelfeld, Magnetfeld von Spulen, magnetischer Fluss, induzierte Spannung.
 Verwandte Begriffe Maxwell-Gleichungen, elektrisches Wirbelfeld, Magnetfeld von Spulen, magnetischer Fluss, induzierte Spannung. Prinzip In einer langen Spule wird ein Magnetfeld mit variabler Frequenz
Verwandte Begriffe Maxwell-Gleichungen, elektrisches Wirbelfeld, Magnetfeld von Spulen, magnetischer Fluss, induzierte Spannung. Prinzip In einer langen Spule wird ein Magnetfeld mit variabler Frequenz
Elektrizität. = C J m. Das Coulomb Potential φ ist dabei:
 Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Bedienungsanleitung. F109 Fuel Cell Stack 5. F110 Fuel Cell Stack 10
 Bedienungsanleitung F109 Fuel Cell Stack 5 F110 Fuel Cell Stack 10 H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel.: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com
Bedienungsanleitung F109 Fuel Cell Stack 5 F110 Fuel Cell Stack 10 H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel.: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com
Bedienungsanleitung. D103 Fuel Cell Concept Car & Gas Station.
 Bedienungsanleitung D103 Fuel Cell Concept Car & Gas Station www.h-tec.com h-tec Wasserstoff-Energie-Systeme GmbH Lindenstrasse 48a 23558 Lübeck Telefon +49 (0) 451-49 89 5-0 Telefax +49 (0) 451-49 89
Bedienungsanleitung D103 Fuel Cell Concept Car & Gas Station www.h-tec.com h-tec Wasserstoff-Energie-Systeme GmbH Lindenstrasse 48a 23558 Lübeck Telefon +49 (0) 451-49 89 5-0 Telefax +49 (0) 451-49 89
Bedienungsanleitung. T126 TutorialBasic
 Bedienungsanleitung T126 TutorialBasic H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com Website: www.h-tec-education.com
Bedienungsanleitung T126 TutorialBasic H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com Website: www.h-tec-education.com
1. Strom-Spannungs-Kennlinie, Leistungskurve und Wirkungsgrad des Solarmoduls
 1. Strom-Spannungs-Kennlinie, Leistungskurve und Wirkungsgrad des Solarmoduls Hintergrund: Gegeben ist ein Datenblatt eines Solarpanels. Der Schüler soll messtechnisch die Daten eines kleinen Solarmoduls
1. Strom-Spannungs-Kennlinie, Leistungskurve und Wirkungsgrad des Solarmoduls Hintergrund: Gegeben ist ein Datenblatt eines Solarpanels. Der Schüler soll messtechnisch die Daten eines kleinen Solarmoduls
Experimente mit Brennstoffzellen - Kennlinienaufnahme
 Experimente mit Brennstoffzellen - Kennlinienaufnahme Ziel dieses Unterrichtsentwurfes ist es, die Funktionsweise von Brennstoffzellen näher kennen zu lernen. Die Strom-Spannungs-Kennlinie eines Elektrolyseurs
Experimente mit Brennstoffzellen - Kennlinienaufnahme Ziel dieses Unterrichtsentwurfes ist es, die Funktionsweise von Brennstoffzellen näher kennen zu lernen. Die Strom-Spannungs-Kennlinie eines Elektrolyseurs
Das Ohmsche Gesetz (Artikelnr.: P )
 Lehrer-/Dozentenblatt Gedruckt: 22.08.207 0:42:56 P372400 Das Ohmsche Gesetz (Artikelnr.: P372400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Elektrizitätslehre
Lehrer-/Dozentenblatt Gedruckt: 22.08.207 0:42:56 P372400 Das Ohmsche Gesetz (Artikelnr.: P372400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Elektrizitätslehre
Pumpen von Wasser mit Solarenergie
 Lehrer-/Dozentenblatt Pumpen von Wasser mit Solarenergie Aufgabe und Material Lehrerinformationen Zusätzliche Informationen So genannt Pumpspeicherkraftwerk, besitzen große, hoch gelegene Wasserbecken,
Lehrer-/Dozentenblatt Pumpen von Wasser mit Solarenergie Aufgabe und Material Lehrerinformationen Zusätzliche Informationen So genannt Pumpspeicherkraftwerk, besitzen große, hoch gelegene Wasserbecken,
Elektrolytische Stoffabscheidung und Ladungsmenge
 Elektrolytische Stoffabscheidung und Ladungsmenge (Artikelnr.: P1147500) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische Chemie Unterthema: Elektrochemie
Elektrolytische Stoffabscheidung und Ladungsmenge (Artikelnr.: P1147500) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische Chemie Unterthema: Elektrochemie
Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle. Inhaltsfeld: Elektrochemie
 Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle Inhaltsfeld: Elektrochemie Inhaltliche Schwerpunkte: Mobile Energiequellen Elektrochemische Gewinnung von Stoffen Zeitbedarf: ca. 5 Std. à 45
Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle Inhaltsfeld: Elektrochemie Inhaltliche Schwerpunkte: Mobile Energiequellen Elektrochemische Gewinnung von Stoffen Zeitbedarf: ca. 5 Std. à 45
Kennlinie der Methanol- Brennstoffzelle
 E m1 Kennlinie der Methanol- Brennstoffzelle Material: Methanol-Brennstoffzelle Flasche mit 1M Methanol-Lösung Spritztülle Verbraucher-Messbox 4 Kabel Verschlussstopfen Tank Zusätzliche Komponenten: Methanol
E m1 Kennlinie der Methanol- Brennstoffzelle Material: Methanol-Brennstoffzelle Flasche mit 1M Methanol-Lösung Spritztülle Verbraucher-Messbox 4 Kabel Verschlussstopfen Tank Zusätzliche Komponenten: Methanol
Grundlagen: Galvanische Zellen:
 E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
Bedienungsanleitung. E205 Electrolyser H2 10
 Bedienungsanleitung E205 Electrolyser H2 10 Inhaltsverzeichnis 03 04 04 05 07 08 10 12 13 14 15 15 15 Einleitung Zu dieser Anleitung Sicherheitshinweise Inhalt Überblick Inbetriebnahme Bedienung Technische
Bedienungsanleitung E205 Electrolyser H2 10 Inhaltsverzeichnis 03 04 04 05 07 08 10 12 13 14 15 15 15 Einleitung Zu dieser Anleitung Sicherheitshinweise Inhalt Überblick Inbetriebnahme Bedienung Technische
Strom-Spannungs-Kennlinie und Leistung einer Solarzelle
 Strom-Spannungs-Kennlinie und Leistung einer Solarzelle ENT Schlüsselworte Solarzelle, Kennlinie, Spannung, Stromstärke, Leistung, Widerstand, Innenwiderstand, Anpassung Prinzip Die Strom-Spannungs-Kennlinie
Strom-Spannungs-Kennlinie und Leistung einer Solarzelle ENT Schlüsselworte Solarzelle, Kennlinie, Spannung, Stromstärke, Leistung, Widerstand, Innenwiderstand, Anpassung Prinzip Die Strom-Spannungs-Kennlinie
JUFOTech. wko.at/tirol/jufotech DATENBLATT. Jugend forscht in der Technik. Titel der Projektarbeit: Fachgebiet:
 Datenblatt (dient als Titelblatt für die Projektarbeit) Seite 1/2 JUFOTech Jugend forscht in der Technik wko.at/tirol/jufotech DATENBLATT Wir nehmen am Wettbewerb Jugend forscht in der Technik Auf den
Datenblatt (dient als Titelblatt für die Projektarbeit) Seite 1/2 JUFOTech Jugend forscht in der Technik wko.at/tirol/jufotech DATENBLATT Wir nehmen am Wettbewerb Jugend forscht in der Technik Auf den
Bedienungsanleitung. E207 Electrolyser H2/O E206 Electrolyser H2/O2 65
 Bedienungsanleitung E207 Electrolyser H2/O2 230 E206 Electrolyser H2/O2 65 H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Deutschland Tel: +49 451 39941-0 Fax: +49 451 39941-798 E-Mail: info@h-tec-education.com
Bedienungsanleitung E207 Electrolyser H2/O2 230 E206 Electrolyser H2/O2 65 H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Deutschland Tel: +49 451 39941-0 Fax: +49 451 39941-798 E-Mail: info@h-tec-education.com
Seminar zum Quantitativen Anorganischen Praktikum WS 2011/12
 Seminar zum Quantitativen Anorganischen Praktikum WS 211/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 9.1.212, 8-1 Uhr, HS III Allgemeine Einführung in die Quantitative
Seminar zum Quantitativen Anorganischen Praktikum WS 211/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 9.1.212, 8-1 Uhr, HS III Allgemeine Einführung in die Quantitative
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan
 Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
Das ohmsche Gesetz (Artikelnr.: P )
 Das ohmsche Gesetz (Artikelnr.: P1381000) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Der elektrische Widerstand Experiment:
Das ohmsche Gesetz (Artikelnr.: P1381000) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Der elektrische Widerstand Experiment:
Das Brennstoffzellen-Radio
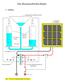 Das Brennstoffzellen-Radio 1. Aufbau Auffangbehälter (Haushaltstrichter) Solarpaneel (KOSMOS) 10 10 20 20 30 30 40 50 destilliertes Wasser Gastanks (Einwegspritzen) 40 50 60 70 80 60 Plexiglas 90 ml 100
Das Brennstoffzellen-Radio 1. Aufbau Auffangbehälter (Haushaltstrichter) Solarpaneel (KOSMOS) 10 10 20 20 30 30 40 50 destilliertes Wasser Gastanks (Einwegspritzen) 40 50 60 70 80 60 Plexiglas 90 ml 100
Praktikum Physikalische Chemie I 26. November Zersetzungsspannung. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum Physikalische Chemie I 26. November 2015 Zersetzungsspannung Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 Aufgabenstellung Die Zersetzungsspannung von HCl und HI wird mit Hilfe einer Strom-Spannungskurve
Praktikum Physikalische Chemie I 26. November 2015 Zersetzungsspannung Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 Aufgabenstellung Die Zersetzungsspannung von HCl und HI wird mit Hilfe einer Strom-Spannungskurve
Betrieb einer LED mit Solarenergie
 Betrieb einer LED mit Solarenergie ENT Schlüsselworte Sonnenenergie, Fotovoltaik, Solarzelle, Leuchtdiode Prinzip Kleine Fotovoltaikanlagen können direkt zur Versorgung kleiner Geräte oder zur Beleuchtung
Betrieb einer LED mit Solarenergie ENT Schlüsselworte Sonnenenergie, Fotovoltaik, Solarzelle, Leuchtdiode Prinzip Kleine Fotovoltaikanlagen können direkt zur Versorgung kleiner Geräte oder zur Beleuchtung
Spannung und Stromstärke bei Reihenschaltung von Solarzellen
 Lehrer-/Dozentenblatt Spannung und Stromstärke bei Reihenschaltung von Solarzellen Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Die Schüler sollen eine Reihenschaltung von Solarzellen
Lehrer-/Dozentenblatt Spannung und Stromstärke bei Reihenschaltung von Solarzellen Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Die Schüler sollen eine Reihenschaltung von Solarzellen
E 3 Brennstoffzelle. 1 Aufgabenstellung
 E 3 Brennstoffzelle 1 Aufgabenstellung 1.1 Ermitteln Sie den Wirkungsgrad eines Elektrolyseurs. 1. Nehmen Sie die Strom-Spannungs-Kennlinie eines Brennstoffzellensystems auf und erläutern Sie den erhaltenen
E 3 Brennstoffzelle 1 Aufgabenstellung 1.1 Ermitteln Sie den Wirkungsgrad eines Elektrolyseurs. 1. Nehmen Sie die Strom-Spannungs-Kennlinie eines Brennstoffzellensystems auf und erläutern Sie den erhaltenen
Versuch: h-bestimmung mit Leuchtdioden
 Lehrer-/Dozentenblatt Gedruckt: 22.08.207 2:35:42 P4800 Versuch: h-bestimmung mit Leuchtdioden Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Das plancksche Wirkungsquantum h ist eine
Lehrer-/Dozentenblatt Gedruckt: 22.08.207 2:35:42 P4800 Versuch: h-bestimmung mit Leuchtdioden Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Das plancksche Wirkungsquantum h ist eine
Stromstärke und Widerstand in Reihenschaltung
 Lehrer-/Dozentenblatt Gedruckt: 30.03.207 7:0:20 P372900 Stromstärke und Widerstand in Reihenschaltung (Artikelnr.: P372900) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema:
Lehrer-/Dozentenblatt Gedruckt: 30.03.207 7:0:20 P372900 Stromstärke und Widerstand in Reihenschaltung (Artikelnr.: P372900) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema:
Galvanoplastik. Elektrochemie B. Lukas Woolley, Rafael Adamek, Peter Krack. 24 Februar ETH Zürich
 Elektrochemie B Lukas Woolley Rafael Adamek Peter Krack ETH Zürich 24 Februar 2017 Programm 1 2 3 4 Garfield Elektrolysezelle + - e e Anode Kathode e Cu CuSO 4 Cu 2+ Cu 2+ e Programm 1 2 3 4 Zelltypen
Elektrochemie B Lukas Woolley Rafael Adamek Peter Krack ETH Zürich 24 Februar 2017 Programm 1 2 3 4 Garfield Elektrolysezelle + - e e Anode Kathode e Cu CuSO 4 Cu 2+ Cu 2+ e Programm 1 2 3 4 Zelltypen
Physik-Übung * Jahrgangsstufe 8 * Elektrische Widerstände Blatt 1
 Physik-Übung * Jahrgangsstufe 8 * Elektrische Widerstände Blatt 1 Geräte: Netzgerät mit Strom- und Spannungsanzeige, 2 Vielfachmessgeräte, 4 Kabel 20cm, 3 Kabel 10cm, 2Kabel 30cm, 1 Glühlampe 6V/100mA,
Physik-Übung * Jahrgangsstufe 8 * Elektrische Widerstände Blatt 1 Geräte: Netzgerät mit Strom- und Spannungsanzeige, 2 Vielfachmessgeräte, 4 Kabel 20cm, 3 Kabel 10cm, 2Kabel 30cm, 1 Glühlampe 6V/100mA,
Hochspannungsleitung. Vorbereitungszeit. 10 Minuten
 Schwierigkeitsgrad Vorbereitungszeit Durchführungszeit mittel 10 Minuten 20 Minuten Prinzip Mithilfe zweier Hochspannungstransformatoren können die Fernleitungsverluste zwischen Kraftwerk und Verbraucher
Schwierigkeitsgrad Vorbereitungszeit Durchführungszeit mittel 10 Minuten 20 Minuten Prinzip Mithilfe zweier Hochspannungstransformatoren können die Fernleitungsverluste zwischen Kraftwerk und Verbraucher
Versuch 17: Kennlinie der Vakuum-Diode
 Versuch 17: Kennlinie der Vakuum-Diode Inhaltsverzeichnis 1 Einleitung 3 2 Theorie 3 2.1 Prinzip der Vakuumdiode.......................... 3 2.2 Anlaufstrom.................................. 3 2.3 Raumladungsgebiet..............................
Versuch 17: Kennlinie der Vakuum-Diode Inhaltsverzeichnis 1 Einleitung 3 2 Theorie 3 2.1 Prinzip der Vakuumdiode.......................... 3 2.2 Anlaufstrom.................................. 3 2.3 Raumladungsgebiet..............................
LF - Leitfähigkeit / Überführung
 Verfasser: Matthias Ernst, Tobias Schabel Gruppe: A 11 Betreuer: G. Heusel Datum: 18.11.2005 Aufgabenstellung LF - Leitfähigkeit / Überführung 1) Es sind die Leitfähigkeiten von zwei unbekanten Elektrolyten
Verfasser: Matthias Ernst, Tobias Schabel Gruppe: A 11 Betreuer: G. Heusel Datum: 18.11.2005 Aufgabenstellung LF - Leitfähigkeit / Überführung 1) Es sind die Leitfähigkeiten von zwei unbekanten Elektrolyten
TE Thermische Emission
 TE Thermische Emission Blockpraktikum Herbst 2007 (Gruppe 2b) 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Kennlinie einer Glühdiode............................. 2 2 Versuch und Auswertung 4
TE Thermische Emission Blockpraktikum Herbst 2007 (Gruppe 2b) 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Kennlinie einer Glühdiode............................. 2 2 Versuch und Auswertung 4
Die Wirkungsweise einer Brennstoffzelle. Ein Vortrag von Bernard Brickwedde
 Die Wirkungsweise einer Brennstoffzelle Ein Vortrag von Bernard Brickwedde Inhalt Allgemein Definition Geschichte Anwendungsgebiete Aufbau Theoretische Grundlagen Redoxreaktion Wirkungsgrad Elektrochemische
Die Wirkungsweise einer Brennstoffzelle Ein Vortrag von Bernard Brickwedde Inhalt Allgemein Definition Geschichte Anwendungsgebiete Aufbau Theoretische Grundlagen Redoxreaktion Wirkungsgrad Elektrochemische
Spannung und Stromstärke einer Solarzelle Einfluss von der Fläche und der Beleuchtungsstärke
 Spannung und Stromstärke einer Solarzelle ENT Schlüsselworte Sonnenenergie, Fotovoltaik, Solarzelle, Lichtintensität, Elektrische Energie, Leerlaufspannung, Kurzschlussstromstärke Prinzip Solarzellen wandeln
Spannung und Stromstärke einer Solarzelle ENT Schlüsselworte Sonnenenergie, Fotovoltaik, Solarzelle, Lichtintensität, Elektrische Energie, Leerlaufspannung, Kurzschlussstromstärke Prinzip Solarzellen wandeln
Hinweise zum Extrapolieren (Versuche 202, 301, 109)
 Hinweise zum Extrapolieren (Versuche 202, 301, 109) Bei vielen physikalischen Experimenten wird das (End-) Messergebnis von Größen mitbestimmt, die in einer einfachen Beschreibung nicht auftauchen (z.b.
Hinweise zum Extrapolieren (Versuche 202, 301, 109) Bei vielen physikalischen Experimenten wird das (End-) Messergebnis von Größen mitbestimmt, die in einer einfachen Beschreibung nicht auftauchen (z.b.
Bedienungsanleitung F107 PEMFC KIT
 Bedienungsanleitung F107 PEMFC KIT H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel.: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com Website: www.h-tec-education.com
Bedienungsanleitung F107 PEMFC KIT H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel.: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com Website: www.h-tec-education.com
Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse
 Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Elektrische Felder und Potentiale im Plattenkondensator (Artikelnr.: P )
 Elektrische Felder und Potentiale im Plattenkondensator (Artikelnr.: P2420100) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Hochschule Lehrplanthema: Elektrizität und Magnetismus Unterthema:
Elektrische Felder und Potentiale im Plattenkondensator (Artikelnr.: P2420100) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Hochschule Lehrplanthema: Elektrizität und Magnetismus Unterthema:
Das ohmsche Gesetz (Artikelnr.: P )
 Lehrer-/Dozentenblatt Gedruckt: 30.03.207 6:59:56 P372400 Das ohmsche Gesetz (Artikelnr.: P372400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Elektrizitätslehre
Lehrer-/Dozentenblatt Gedruckt: 30.03.207 6:59:56 P372400 Das ohmsche Gesetz (Artikelnr.: P372400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Elektrizitätslehre
Spannung und Stromstärke bei Parallelschaltung von Solarzellen
 Lehrer-/Dozentenblatt Spannung und Stromstärke bei Parallelschaltung von Solarzellen Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Die Schüler sollen eine Parallelschaltung von Solarzellen
Lehrer-/Dozentenblatt Spannung und Stromstärke bei Parallelschaltung von Solarzellen Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Die Schüler sollen eine Parallelschaltung von Solarzellen
TU Ilmenau Chemisches Praktikum Versuch Kennlinie der Brennstoffzelle in. Reihenschaltung/Parallelschaltung
 TU Ilmenau Chemisches Praktikum Versuch Kennlinie der Brennstoffzelle in V17 Fachgebiet Chemie Reihenschaltung/Parallelschaltung 1. Aufgabe Bauen Sie die Anordnung nach Bild 1 oder Bild 2 auf. Nehmen Sie
TU Ilmenau Chemisches Praktikum Versuch Kennlinie der Brennstoffzelle in V17 Fachgebiet Chemie Reihenschaltung/Parallelschaltung 1. Aufgabe Bauen Sie die Anordnung nach Bild 1 oder Bild 2 auf. Nehmen Sie
Der spezifische Widerstand von Drähten (Artikelnr.: P )
 Lehrer-/Dozentenblatt Der spezifische Widerstand von Drähten (Artikelnr.: P1372700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema:
Lehrer-/Dozentenblatt Der spezifische Widerstand von Drähten (Artikelnr.: P1372700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema:
Stromstärke und Widerstand bei der Parallelschaltung (Artikelnr.: P )
 Stromstärke und Widerstand bei der Parallelschaltung (Artikelnr.: P1381400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Der elektrische
Stromstärke und Widerstand bei der Parallelschaltung (Artikelnr.: P1381400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Elektrizitätslehre Unterthema: Der elektrische
SV: Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration
 SV: Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration Der Versuch sollte mindestens zu zweit oder in einer Gruppe durchgeführt werden, damit die Messung so genau wie möglich erfolgt. Als
SV: Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration Der Versuch sollte mindestens zu zweit oder in einer Gruppe durchgeführt werden, damit die Messung so genau wie möglich erfolgt. Als
Versuch 5: Zersetzungsspannung
 Gruppe : Christina Sauermann und Johannes Martin 1 Versuch 5: Zersetzungsspannung 1 Darstellung der theoretischen Hintergründe Wird an die beiden Elektroden einer galvanischen Zelle eine Gleichspannung
Gruppe : Christina Sauermann und Johannes Martin 1 Versuch 5: Zersetzungsspannung 1 Darstellung der theoretischen Hintergründe Wird an die beiden Elektroden einer galvanischen Zelle eine Gleichspannung
 Experimente www.fuelcellbox-nrw.de H-TEC EDUCATION GmbH 2016 www.h-tec-education.com Inhalt 1.1. Zersetzung von Wasser unter Betrachtung des entstehenden Wasserstoff- und Sauerstoff-Gasvolumens 4 1.2.
Experimente www.fuelcellbox-nrw.de H-TEC EDUCATION GmbH 2016 www.h-tec-education.com Inhalt 1.1. Zersetzung von Wasser unter Betrachtung des entstehenden Wasserstoff- und Sauerstoff-Gasvolumens 4 1.2.
A 2.6 Wie ist die Zusammensetzung der Flüssigkeit und des Dampfes eines Stickstoff-Sauerstoff-Gemischs
 A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
Brenstoffzelle (BRZ)
 Seite 1 Themengebiet: Thermodynamik 1 Literatur A. Macdonald, M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris, Berlin, 2007 A.J. Bard, L.R. Faulkner, Electrochemical Methods Fundamentals
Seite 1 Themengebiet: Thermodynamik 1 Literatur A. Macdonald, M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris, Berlin, 2007 A.J. Bard, L.R. Faulkner, Electrochemical Methods Fundamentals
E5: Faraday-Konstante
 E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
Faradayscher und energetischer Wirkungsgrad eines PEM Elektrolyseurs
 Faradayscher und energetischer Wirkungsgrad ENT Schlüsselworte Elektrolyse, Protonen-Austausch-Membran, Ladungstrennung, Wasserstoff, Wirkungsgrad, faradaysche Gesetze, universelle Gaskonstante Prinzip
Faradayscher und energetischer Wirkungsgrad ENT Schlüsselworte Elektrolyse, Protonen-Austausch-Membran, Ladungstrennung, Wasserstoff, Wirkungsgrad, faradaysche Gesetze, universelle Gaskonstante Prinzip
Praktikum Physikalische Chemie I 30. Januar Aktivierungsenergie. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Die Brennstoffzelle. Inhaltsverzeichnis. 12. November 2014. 1 Was versteht man unter Wasserstofftechnologie? 2
 Die Brennstoffzelle 12. November 2014 Inhaltsverzeichnis 1 Was versteht man unter Wasserstofftechnologie? 2 2 Funktionsprinzipien der Komponenten 3 2.1 Der Elektrolyseur...................................
Die Brennstoffzelle 12. November 2014 Inhaltsverzeichnis 1 Was versteht man unter Wasserstofftechnologie? 2 2 Funktionsprinzipien der Komponenten 3 2.1 Der Elektrolyseur...................................
1. Messungen an einer Modell-Windanlage
 1. Messungen an einer Modell-Windanlage Georg Begusch, Leopold Mathelitsch, Gerhard Rath, Erich Reichel, Eduard Schittelkopf Zuerst sollen Sie einige physikalische Eigenschaften von Windenergieanlagen
1. Messungen an einer Modell-Windanlage Georg Begusch, Leopold Mathelitsch, Gerhard Rath, Erich Reichel, Eduard Schittelkopf Zuerst sollen Sie einige physikalische Eigenschaften von Windenergieanlagen
Energiediagramme! Energie strömt nicht alleine, sie braucht immer einen Träger. Beispiele: 1) Glühlampe
 Kompetenztage 7 diagramme! strömt nicht alleine, sie braucht immer einen Träger. umwandler träger sind zum Beispiel: Benzin, Nahrungsmittel für chemische, r Strom für diagramm Licht für Lichtenergie fließende
Kompetenztage 7 diagramme! strömt nicht alleine, sie braucht immer einen Träger. umwandler träger sind zum Beispiel: Benzin, Nahrungsmittel für chemische, r Strom für diagramm Licht für Lichtenergie fließende
Aufnahme von Kennlinien eines liniaren Bauelementes
 TFH Berlin Messtechnik Labor Seite1 von 6 Aufnahme von Kennlinien eines liniaren Bauelementes Ort: TFH Berlin Datum: 29.09.03 Uhrzeit: von 8.00h bis 11.30h Dozent: Arbeitsgruppe: Prof. Dr.-Ing. Klaus Metzger
TFH Berlin Messtechnik Labor Seite1 von 6 Aufnahme von Kennlinien eines liniaren Bauelementes Ort: TFH Berlin Datum: 29.09.03 Uhrzeit: von 8.00h bis 11.30h Dozent: Arbeitsgruppe: Prof. Dr.-Ing. Klaus Metzger
Elektrolysekammer mit Kohle-Elektroden Best.- Nr. MD04073
 Elektrolysekammer mit Kohle-Elektroden Best.- Nr. MD04073 1. Beschreibung Die Elektrolysekammern sind in drei Varianten lieferbar: MD04071 MD04072 MD04073 mit Nickel-Elektroden mit Platin-Elektroden mit
Elektrolysekammer mit Kohle-Elektroden Best.- Nr. MD04073 1. Beschreibung Die Elektrolysekammern sind in drei Varianten lieferbar: MD04071 MD04072 MD04073 mit Nickel-Elektroden mit Platin-Elektroden mit
Elektrisches Feld. Aufgabe und Material. Lehrer-/Dozentenblatt. Lehrerinformationen. Zusätzliche Informationen. Lernziel.
 Lehrer-/Dozentenblatt Elektrisches Feld Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Lernziel In diesem Versuch sollen sich die Schüler mit den Begriffen Äquipotentiallinie und Feldlinie
Lehrer-/Dozentenblatt Elektrisches Feld Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Lernziel In diesem Versuch sollen sich die Schüler mit den Begriffen Äquipotentiallinie und Feldlinie
Elektrizität in den Themenfeldern 6 und 9
 Elektrizität in den Themenfeldern 6 und 9 1 Intention TF 6 Entwicklung von Vorstellungen zum Energietransport mit dem Träger Elektrizität Energienutzung im Alltag; Einheiten J und kwh Zusammenhang von
Elektrizität in den Themenfeldern 6 und 9 1 Intention TF 6 Entwicklung von Vorstellungen zum Energietransport mit dem Träger Elektrizität Energienutzung im Alltag; Einheiten J und kwh Zusammenhang von
T5 - Hydratations- und Neutralisationsenthalpie
 T5 - Hydratations- und Neutralisationsenthalpie Aufgaben: 1. Messung der molaren integralen Lösungsenthalpie von Natriumhydrogenphosphat Na 2 HPO 4, Natriumhydrogenphosphat-dihydrat Na 2 HPO 4 2H 2 O,
T5 - Hydratations- und Neutralisationsenthalpie Aufgaben: 1. Messung der molaren integralen Lösungsenthalpie von Natriumhydrogenphosphat Na 2 HPO 4, Natriumhydrogenphosphat-dihydrat Na 2 HPO 4 2H 2 O,
Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease.
 A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
HappyEvening am Brennstoffzellen zur mobilen Energiebereitstellung
 HappyEvening am 15.10.2008 Brennstoffzellen zur mobilen Energiebereitstellung T. Pröll 15.10.2008 Inhalt Grundlagen Zelltypen und Anwendungen PEM-Brennstoffzelle (Prinzip) Direkt-Methanol-Brennstoffzelle
HappyEvening am 15.10.2008 Brennstoffzellen zur mobilen Energiebereitstellung T. Pröll 15.10.2008 Inhalt Grundlagen Zelltypen und Anwendungen PEM-Brennstoffzelle (Prinzip) Direkt-Methanol-Brennstoffzelle
Elektrizitätslehre. Elektrolyse. Ladungstransport und Strom BESTIMMUNG DER FARADAY-KONSTANTE. ALLGEMEINE GRUNDLAGEN
 Elektrizitätslehre Ladungstransport und Strom Elektrolyse BESTIMMUNG DER FARADAY-KONSTANTE. Erzeugung von Wasserstoff durch Elektrolyse und Messung des Wasserstoffvolumens V. Bestimmung der Ladung Q aus
Elektrizitätslehre Ladungstransport und Strom Elektrolyse BESTIMMUNG DER FARADAY-KONSTANTE. Erzeugung von Wasserstoff durch Elektrolyse und Messung des Wasserstoffvolumens V. Bestimmung der Ladung Q aus
4.2 Halbleiter-Dioden und -Solarzellen
 4.2 Halbleiter-Dioden und -Solarzellen Vorausgesetzt werden Kenntnisse über: Grundbegriffe der Halbleiterphysik, pn-übergang, Raumladungszone, Sperrschichtkapazität, Gleichrichterkennlinie, Aufbau und
4.2 Halbleiter-Dioden und -Solarzellen Vorausgesetzt werden Kenntnisse über: Grundbegriffe der Halbleiterphysik, pn-übergang, Raumladungszone, Sperrschichtkapazität, Gleichrichterkennlinie, Aufbau und
Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung)
 Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
LABORÜBUNG Diodenkennlinie
 LABORÜBUNG Diodenkennlinie Letzte Änderung: 30.11.2004 Lothar Kerbl Inhaltsverzeichnis Messaufgabe 1: Kennlinie im Durchlassbereich... 2 Theoretische Kennlinie... 3 Messaufgabe 2 : Kennlinie einer Zenerdiode...
LABORÜBUNG Diodenkennlinie Letzte Änderung: 30.11.2004 Lothar Kerbl Inhaltsverzeichnis Messaufgabe 1: Kennlinie im Durchlassbereich... 2 Theoretische Kennlinie... 3 Messaufgabe 2 : Kennlinie einer Zenerdiode...
Vakuum (VAK)
 Inhaltsverzeichnis TUM Anfängerpraktikum für Physiker Vakuum (VAK) 25.2.26. Einleitung...2 2. Ideale Gase...2 3. Verwendetes Material...2 4. Versuchsdurchführung...2 4.. Eichung der Pirani-Manometer...2
Inhaltsverzeichnis TUM Anfängerpraktikum für Physiker Vakuum (VAK) 25.2.26. Einleitung...2 2. Ideale Gase...2 3. Verwendetes Material...2 4. Versuchsdurchführung...2 4.. Eichung der Pirani-Manometer...2
Galvanische Zellen aus Nichtmetallen (Artikelnr.: P )
 Lehrer-/Dozentenblatt Galvanische Zellen aus Nichtmetallen (Artikelnr.: P7400900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische Chemie Unterthema:
Lehrer-/Dozentenblatt Galvanische Zellen aus Nichtmetallen (Artikelnr.: P7400900) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische Chemie Unterthema:
1 Messung eines konstanten Volumenstroms mit konstanter Dichte
 INHALTE I Inhalte 1 Konstanter Volumenstrom 1 1.1 Auswertung der Messwerte........................ 1 1.2 Berechnung des Volumenstroms...................... 1 1.3 Fehlerbetrachtung.............................
INHALTE I Inhalte 1 Konstanter Volumenstrom 1 1.1 Auswertung der Messwerte........................ 1 1.2 Berechnung des Volumenstroms...................... 1 1.3 Fehlerbetrachtung.............................
Elektrische Grundlagen der Informationstechnik. Laborprotokoll: Nichtlineare Widerstände
 Fachhochschule für Technik und Wirtschaft Berlin Elektrische Grundlagen der Informationstechnik Laborprotokoll: Nichtlineare Widerstände Mario Apitz, Christian Kötz 2. Januar 21 Inhaltsverzeichnis 1 Vorbeitung...
Fachhochschule für Technik und Wirtschaft Berlin Elektrische Grundlagen der Informationstechnik Laborprotokoll: Nichtlineare Widerstände Mario Apitz, Christian Kötz 2. Januar 21 Inhaltsverzeichnis 1 Vorbeitung...
E-Labor im WS / SS. Gruppe: BITTE ANKREUZEN. Messprotokoll Versuchsbericht. Datum der Durchführung:
 Abteilung Maschinenbau im WS / SS ersuch Gruppe: Name orname Matr.-Nr. Semester erfasser(in) Teilnehmer(in) Teilnehmer(in) Professor(in) / Lehrbeauftragte(r): BITTE ANKEZEN Messprotokoll ersuchsbericht
Abteilung Maschinenbau im WS / SS ersuch Gruppe: Name orname Matr.-Nr. Semester erfasser(in) Teilnehmer(in) Teilnehmer(in) Professor(in) / Lehrbeauftragte(r): BITTE ANKEZEN Messprotokoll ersuchsbericht
Erwärmen von Wasser in einem Sonnenkollektor
 Erwärmen von Wasser in einem Sonnenkollektor ENT Schlüsselworte Strahlungsenergie der Sonne, Energieumwandlung, Sonnenkollektor, Solarthermie Prinzip Sonnenenergie lässt sich mit Hilfe des Sonnenkollektors
Erwärmen von Wasser in einem Sonnenkollektor ENT Schlüsselworte Strahlungsenergie der Sonne, Energieumwandlung, Sonnenkollektor, Solarthermie Prinzip Sonnenenergie lässt sich mit Hilfe des Sonnenkollektors
