Mikrobiologie II - Überblick
|
|
|
- Jan Beckenbauer
- vor 5 Jahren
- Abrufe
Transkript
1 Mikrobiologie II - Überblick Vorbemerkungen zum Zellmetabolismus Energiestoffwechsel von Mikroorganismen Gärungsformen, Substratkettenphosphorylierung Energiegewinnung durch die Atmungskette Energiegewinnung durch Photosynthese Mikroorganismen als Infektionserreger Pathogenitätsfaktoren Toxine
2 Mikrobiologie II - Überblick Energiestoffwechsel von Mikroorganismen Gärungsformen, Substratkettenphosphorylierung - Glycolyse (Embden-Meyerhoff-Weg) - Pentosephosphat-Weg - Entner-Douderoff-Weg - Phosphoketolase-Weg, Milchsäurebakterien - Reduktion von Pyruvat - Ethanolbildung in Hefen und Bakterien - Propionsäuregärung, Propionibakterien - Ameisensäuregärung, Enterobacteriaceae - Buttersäuregärung, Butanolgärung, Clostridien - Homoacetatfermentation in Clostridien
3 Mikrobiologie II - Überblick Energiestoffwechsel von Mikroorganismen Energiegewinnung durch die Atmungskette - Zitronensäurezyklus (Krebs-Zyklus) - Elektronentransportkette (Atmungskette) - Anaerober Elektronentransport - Aerobe chemolithotrophe Bakterien - Unvollständige Oxidation - Toxische Wirkung des Sauerstoffs
4 Mikrobiologie II - Überblick Energiestoffwechsel von Mikroorganismen Energiegewinnung durch Photosynthese - Struktur und Funktion photosynthetischer Reaktionszentren - Calvin-Zyklus - Purpurbakterien - Grüne Bakterien - Cyanobakterien - Halobakterien (Archaeen), Bakterienrhodopsin
5 Mikrobiologie II - Überblick Mikroorganismen als Infektionserreger Pathogenitätsmechanismen: Anheften, Invadieren Bakterielle Toxine - Diphtherietoxin - Choleratoxin - Pertussis-Toxin - Clostridien-Neurotoxine
6 Grundprinzipien der Biochemie Um die Vorgänge des Zellmetabolismus verstehen zu können, sind Grundkenntnisse der Thermodynamik (in welche Richtung läuft eine Reaktion, Einfluß von Energie und Entropie) und Kinetik (Reaktionsgeschwindigkeit) unbedingt erforderlich.
7 Energieinhalt (Freie Standard- Enthalpie) wichtiger Energiemetaboliten*
8 Energieinhalt (Freie Standard- Enthalpie) wichtiger Energiemetaboliten Die Werte geben die Enthalpie des jeweiligen Gruppenübertragungspotentials an, also die Enthalpie, die in der Bindung zum (bei ATP äußersten) Phosphat steckt, also keinesfalls eine Art Gesamtenergie des Moleküls (Was wäre das überhaupt? Die Energie, die bei Verbrennung frei würde? Die Energie, die bei Kernreaktionen frei würde?) In der Tabelle auf der vorigen Seite geht es jeweils um die hydrolytische Abspaltung eines Phosphatrestes (also + 1 H 2 O, 1 H 3 PO 4 geht ab).
9 Gibb sche Freie Enthalpie Zur Erinnerung (Physikalische Chemie, Biochemie) ΔG = ΔH - TΔS (Freie Enthalpie = Enthalpie - absolute Temperatur * Entropie Enthalpie H entspricht der Wärme (Wert negativ: exotherme Reaktion, Wärme wird frei). Entropie ist ein Maß für die Unordnung, nimmt insgesamt immer zu (2. Hauptsatz der Thermodynamik)
10 Gibb sche Freie Enthalpie ΔG = ΔH - TΔS Eine Reaktion läuft nur ab, wenn die Freie Enthalpie abnimmt. Eine Teilreaktion mit positivem ΔG kann ablaufen, wenn es mit einer anderen Teilreaktion so gekoppelt ist, dass ΔG insgesamt negativ ist. Das Δ bedeutet immer den Unterschied von Produkten der chemischen Reaktion zu den Edukten (Ausgangsverbindungen).
11 Gibb sche Freie Enthalpie ΔG = ΔH - TΔS Aus der Tabelle der Energiemetaboliten könnte man nun schließen, dass z.b. aus Kreatinphosphat (ΔG =-43,1 kj/mol) und ADP ATP und Kreatin entstehen können, nie aber umgekehrt (ATP>ADP ΔG =-30,5 kj/mol). Tatsächlich spielt aber die Konzentration der Substanzen noch eine entscheidende Rolle. Diese -Zahlen sind Standardwerte, die bei gleichen Konzentrationen (je 1 molar) gelten. Im Muskel liegt viel ATP und wenig ADP vor, dadurch kommt im Gleichgewichtszustand ( steady state ) auch Kreatinphosphat in nutzbaren (Energiespeicher) Mengen vor.
12 ΔG = ΔH - TΔS Gibb sche Freie Enthalpie Die Definition für -Zahlen mit alles ist 1 molar schließt auch Protonen (H + ) ein. Diese Standardbedingungen entsprechen daher einer extrem konzentrierten Säure mit ph=0! Für physiologische (natürliche, zelluläre) Reaktionen nimmt man daher lieber ein (ΔG ) als Standardwert. Dabei ist alles 1 molar, nur der ph ist neutral (ph=7, also H + - Konzentration 10-7 molar), und die Konzentration von Wasser ist 55 molar (wässriges M). Unterschiede zwischen ΔG und ΔG treten nur auf, falls in der Reaktion H + (oder OH - ) oder Wasser vorkommt.
13 Gibb sche Freie Enthalpie ΔG = ΔH - TΔS Diese Konzentrationsabhängigkeit macht das Ziehen einer ungünstigen Reaktion durch eine günstige erst möglich. Vom ungünstigen Zwischenprodukt liegt im steady state immer nur eine geringe Konzentration vor (durch den schnellen Verbrauch durch die ziehende Weiterreaktion).
14 Ermöglichen ungünstiger Reaktionen Beispiel für ein energetisch ungünstiges Zwischenprodukt, das durch günstige Weiterreaktionen ständig abgezogen wird: Das Gleichgewicht der Aldolasereaktion liegt weit auf Seiten des Fructose-bisphosphats (ΔG =+22,8 kj/mol für Aldolspaltung). In der Zelle wird das GAP aber so schnell verbraucht, dass (wegen der extrem niedrigen Konzentration der Edukte GAP und DHAP) die Spaltung abläuft (ΔG=-5,9 kj/mol für die zellulären Konzentrationsverhältnisse).
15 Ermöglichen ungünstiger Reaktionen Im Fall der ATP-Bildung: ADP + P i ATP + H 2 O, ΔG =+30,5 kj/mol, kann der Trick mit der niedrigen Konzentration nicht genutzt werden, da die Zelle eine recht hohe Konzentration des Energielieferanten ATP unbedingt braucht. Ausweg ist hier die Kopplung an stark exergonische (negatives ΔG) Reaktionen, z.b. die GAPDH/PGK-Reaktion: GAP + P i + NAD + 1,3-Diphosphoglycerat + NADH + H + 1,3-Diphosphoglycerat +ADP 3-Phosphoglycerat + ATP Die energieliefernde Reaktion ist dabei die Oxidation des GAP: GAP + NAD + 3-Phosphoglycerat + NADH + H +
16 Ermöglichen ungünstiger Reaktionen In diesem Fall darf kein Enzym die Reaktion ADP + P i ATP + H 2 O katalysieren, da sonst das aufwendig produzierte ATP wieder hydrolysieren würde!
17 Gleichgewichtsreaktionen Überhaupt ist es wichtig, sich klar zu machen, dass prinzipiell alle Reaktionen auf einen Gleichgewichtszustand zulaufen, d.h., es sind am Ende, im Reaktionsgleichgewicht, auch noch Ausgangsverbindungen vorhanden. Ganz in eine Richtung verschoben kann das aber dadurch werden, das ein Produkt entfernt wird (Weiterreaktion, aber auch, wenn ein Gas entsteht und entweicht). Dann läuft die Reaktion (im Versuch, dies Produkt nachzuliefern) immer weiter, bis zum Verschwinden der Edukte.
18 Gleichgewichtsreaktionen Die Mengenverhältnisse von Edukten und Produkten im Gleichgewicht werden durch das Massenwirkungsgesetz beschrieben: Für a A + b B x X + y Y gilt im Reaktionsgleichgewicht: K c = [X] x [Y] y / [A] a [B] b
19 Gleichgewichtsreaktionen Konkret für die Kreatinphosphatbildung: ATP + Kreatin ADP + Kreatinphosphat K c = [ADP][Kreatinphosphat]/[ATP][Kreatin] (die eckigen Klammern bedeuten die Konzentration der jeweiligen Substanz, die Kleinbuchstaben a, b, x, y die Anzahl der Moleküle in der Reaktion, im Beispiel je 1. Das tiefgestellte c zeigt, das die Gleichgewichtskonstante mit Konzentrationen berechnet wurde (es geht auch mit Partialdrucken, das ist dann K p )).
20 Gleichgewichtsreaktionen Zwischen der Gibbschen freien Enthalpie und der Gleichgewichtskonstante besteht folgende Beziehung: ΔG = -RT lnk Dabei ist T die absolute Temperatur (0 C = 273,15 K) und R die allgemeine Gaskonstante, also ein fester Wert: R = 8,314 J/(K mol) Für unser Beispiel errechnen wir aus den Enthalpien der Teilreaktionen (+43,1 kj/mol und -30,5 kj/mol) die Reaktionsenthalpie mit +12,6 kj/mol
21 Gleichgewichtsreaktionen Zwischen der Gibbschen freien Enthalpie und der Gleichgewichtskonstante besteht folgende Beziehung: 12,6 kj/mol = -0, kj/(k mol) 310 K* lnk c *bei 37 C lnk c = -4,889 K c = e -4,889 = 0,00753 (Eulersche Zahl e ca. 2,71) Kleiner Trick mit natürlichen Logarithmen: ln x = 2,303 log x Also ist unser K c (-4,889/2,303) = 10-2,123
22 Gleichgewichtsreaktionen K c = 0,00753 Also ist das Produkt der Ausgangskonzentrationen 133 mal größer als das der Produkte. Klingt schlecht für die Kreatinphosphatbildung. Wenn aber im gut versorgten Muskel das ATP/ADP-Verhältnis 50:1 ist, kann immerhin (133/50 = 2,66, so wäre das Kreatin/Kreatin- Phosphat-Verhältnis) gut ein Viertel des Kreatins in Kreatinphosphat umgewandelt werden. Im Extremfall soll sogar ein ATP/ADP-Verhältnis bis 500 erreicht werden können, wodurch der Großteil des Kreatins in Kreatinphosphat umgewandelt werden könnte.
23 Gleichgewichtsreaktionen Mit steigenden ΔG-Werten verschiebt sich das Gleichgewicht aber bald extrem zu einer Seite. (Die Tabelle geht von 300 K, also Raumtemperatur aus):
24 Gleichgewichtsreaktionen Das schnelle Ausrechnen von K c aus ΔG geht mit 1,493 ΔG = K c für 300 K und 1,474 ΔG = K c für 310 K Wenn der Taschenrechner keine beliebige Basis zum Exponenten erlaubt, hilft die Webseite:
25 Kinetik Auch wenn eine Reaktion thermodynamisch begünstigt ist, also ein stark negatives ΔG hat, heißt das nicht, das sie auch stattfindet. Zwischen Edukt und Produkt liegen meist energetisch sehr ungünstige Übergangszustände, die einen Energieberg darstellen, der die Reaktion verhindert.
26 Kinetik
27 Kinetik - Katalyse Katalysatoren sind Stoffe, die diesen Energieberg vermindern bzw. Umwege mit weniger ungünstigen Übergangszuständen ermöglichen und dadurch chemische Reaktionen enorm beschleunigen oder überhaupt erst möglich machen.
28 Kinetik - Katalyse
29 Kinetik - Enzyme Die effektivsten und in der lebenden Zelle weitaus wichtigsten Katalysatoren sind die Enzyme. Sie biegen die Edukte und bringen sie in Umgebungen (Ladungen, ph, Wasserabschirmung...), die sie in optimale Reaktionsfähigkeit versetzen.
30 Enzymkatalysierte Reaktionen Zwei Punkte sollte man sich dabei immer im Hinterkopf halten: 1. Zwischen den vielen Komponenten der Zelle ist theoretisch eine Unzahl chemischer Reaktionen möglich. Die Enzyme legen fest, welche davon wirklich geschehen. Das müssen keineswegs die energetisch günstigsten sein. Unterschiedliche Organismen setzen dieselben Ausgangsstoffe ganz verschieden um, dazu haben sie verschiedene Sets von Enzymen.
31 Enzymkatalysierte Reaktionen 2. Enzyme können nur Reaktionen beschleunigen, aber sie können keine Reaktionsgleichgewicht verschieben. Ihr Effekt ist nur der, dass das Gleichgewicht schneller erreicht werden kann. Beschleunigt werden immer die Hin- und die Rückreaktion im gleichen Maße! Durch die schon genannte Kopplung mit anderen Reaktionen ermöglichen Enzyme aber scheinbar (!) unmögliche, energetisch ungünstige Umsetzungen.
32 Enzymkatalysierte Reaktionen Enzyme, Proteine mit katalytischen Eigenschaften, sind die Maschinen der Zelle. Sie haben Fähigkeiten, von denen der Chemiker nur träumen kann: Sie können chemische Reaktionen im wässrigen Medium und bei mäßigen Temperaturen (meist C) und neutralem ph durchführen, die im Labor oft nur bei großer Hitze, in konzentrierten Säuren oder in organischen Lösungsmitteln ablaufen. Außerdem sind Enzymreaktionen hochspezifisch, anders als beim Chemiker entstehen praktisch keine Nebenprodukte (Abfall), die Ausbeute der Reaktion ist 100% (davon können Chemiker nur träumen). Außerdem sind Enzyme stereoselektiv.
33 Enzymkatalysierte Reaktionen Durch die Zusammensetzung des aktiven Zentrums und die Abschirmung von der Umgebung verlaufen einige Reaktionen im aktiven Zentrum eines Enzyms in wasserfreiem organischen Lösungsmittel oder bei extremen ph-werten, während die Umgebung wässrig und ph-neutral ist.
34 Enzyme der Glycolyse Hexokinase oder Phosphotransferase Phosphohexose-Isomerase Phosphofruktokinase Fruktosebisphosphat-Aldolase (Aldolase) Triosephosphatisomerase Glycerinaldehydphosphat-Dehydrogenase Phosphoglyceratkinase Phosphoglyceratmutase Enolase Pyruvatkinase
35 Ablauf der Glycolyse - Teil I
36 Der Einstieg in die Glycolyse Bei Eukaryonten wird die Glucose durch Hexokinase phosphoryliert, bei vielen Bakterien durch das Phosphotransferase-System während der Aufnahme in die Zelle. Durch das Anhängen des Phosphats wird der Zucker für die Zelle viel besser handhabbar: er kann nicht mehr entkommen (Phosphotransferasesystem), und kann durch die Ladung in aktiven Zentren schnell und eindeutig orientiert werden.
37 Das Phosphotransferase-System
38 Glucosephosphatisomerase Triosephosphatisomerase Bei beiden Enzymen liegt das Gleichgewicht der Isomere beim falschen : GPI 70% Glucose-6-P, TPI sogar 95% DHAP. Die schnellen Reaktionen liefern das benötigte Isomere aber ausreichend nach, so dass beide Schritte nicht bremsend ( geschwindigkeitsbestimmend ) wirken. Die TPI gilt als ideales Enzym. Ihre Geschwindigkeit ist allein diffusionskontrolliert (das Substrat muß ja mit dem Enzym in Kontakt kommen), d.h., die enzymatische Reaktion selbst geht fast unmeßbar schnell.
39 Aldolase: Aldolkondensation bzw. Aldol-Spaltung Durch die benachbarte Carbonylgruppe wird das C2 azide (Proton kann abgehen) und greift mit dem freien Elektronenpaar den Carbonylkohlenstoff (der durch den Elektronenzug des Carbonylsauerstoffs positiviert ist) des anderen Moleküls an.
40 Ablauf der Glycolyse - Teil II
41 Reaktion der GAPDH Die Glycerinaldehydphosphat-Dehydrogenase sorgt für das Entstehen einer energiereichen Phosphatbindung, die im folgenden Schritt zur ATP-Bildung genutzt wird. Dabei bildet das GAP mit einer Cys-SH-Gruppe des Enzyms zunächst ein energiearmes Thiohalbacetal. Durch Oxidation (mit NAD + ) wird daraus ein energiereicher Thioester, der durch Phosphorolyse zu einem Säureanhydrid gespalten wird.
42 + NAD
43 GAPDH Statt Phosphat kann die GAPDH auch versehentlich Arsenat einbauen. Das Produkt, 1-Arseno-3-Phosphoglycerat, zerfällt in Wasser zu 3-PG, es wird kein ATP gebildet, damit fällt der Energiegewinn durch die Glycolyse komplett aus. Arsenat ist also ein Energiegift.
44 Phosphoglyceratmutase Beim Wandern des Phosphats von -3 nach -2 wird erst ein enzymgebundenes Phosphat auf 2 übertragen (es entsteht 2,3- Bisphosphoglycerat), dann das 3-P aufs Enzym rückübertragen (und landet auf dem nächsten Phosphoglycerat). Zur Erstphosphorylierung des Enzyms und um es bei Verlust des Phosphats (wenn versehentlich 2,3-BPG entkommt) zu regenerieren, werden kleine Mengen 2,3-BPG benötigt (die die PGM mit einer BPG-Mutase-Aktivität aus 1,3-BGP bildet, dasselbe passiert in den Erythrocyten mit einer spezifischen BPG-Mutase in großem Umfang (2,3-BPG erleichtert O 2 - Abgabe vom Hämoglobin)).
45 Phosphoenolpyruvat Bei der zweiten Energiegewinnung in der Glycolyse entsteht die energiereiche Verbindung PEP durch Wasserabspaltung aus dem energiearmen 2-Phosphoglycerat (Enzym Enolase). Die hohe Energie (ΔG=-61,9 kj/mol, ATP-Bildung ΔG=-30,5 kj/mol) steckt nur zu einem kleinen Teil (ΔG=-16 kj/mol) in der Phosphatbindung, sondern überwiegend in der Tautomerisierung des Enols ins Keton (ΔG=-46 kj/mol).
46 Enolase Enolase benötigt zur Substratbindung Mg 2+. Fluorid (F - ) bildet mit dem Magnesium einen Komplex im aktiven Zentrum des Enzyms und blockiert es so. Darauf beruht die Giftigkeit von Fluorid (wieder ein Energiegift).
47 Schicksal der Kohlenstoffatome in der Glycolyse
48 Gleichgewichtsreaktionen Um zu überprüfen, ob eine Reaktion mit den gemessenen Konzentrationen von Substraten und Produkten in die gewünschte Richtung läuft (ob diese Reaktionsrichtung ein negatives ΔG hat), modifiziert man die ΔG -Gleichung zu: ΔG = ΔG RT lnq wobei Q das wirkliche Konzentrationsverhältnis von Produkten/Substraten ist. Ergibt ΔG einen negativen Wert, läuft die Reaktion in die richtige Richtung. Die Beziehung von K und ΔG gilt auch für Q und ΔG, eine Verschiebung des Konzentrationsverhältnisses um 10x ändert die freie Enthalpie um 5,7 kj/mol.
49 Schritte der Glycolyse: Energiebilanz Diese ΔG-Werte sind aus Konzentrationsmessungen errechnet, sollten also den zellulären Bedingungen entsprechen. Der positive Wert der Triosephosphatisomerase muss auf Meßungenauigkeiten* beruhen, oder die Grundlagen der Physikalischen Chemie sind falsch.
50 Schritte der Glycolyse: Energiebilanz * Da hier die GAP-Menge ja extrem niedrig ist (sowohl bei Aldolase wie bei TIM liegt das Gleichgewicht ja weit auf der anderen Seite), bewirkt hier ein kleiner Bestimmungsfehler (ist hier zu viel oder zu wenig GAP bestimmt?) eine starke Verschiebung des Enthalpiewertes. Bei einem ATP:ADP-Verhältnis von 50:1 werden alle ATPverbrauchenden Reaktionen um -10,08 kj/mol (bei 310 K, - 9,775 kj/mol bei 300 K) begünstigt, und alle ATP-bildenden um den gleichen Betrag ungünstiger. Ein NADH:NAD + -Verhältnis von 1:1000 erleichtert Oxidationen (GAPDH) und erschwert Reduktionen um 17,8 kj/mol (bei 310 K).
51 Schritte der Glycolyse: Energiebilanz Die Tabelle zeigt schön, welche (drei) Reaktionen weit vom Gleichgewicht entfernt liegen - und genau da sind die Regulationsstellen:
52 Regulationsschritte in der Glycolyse Zur Regulation eines Ablaufes bieten sich die geschwindigkeitsbestimmenden Schritte an. An zwei Stellen unterscheiden sich Glycolyse und der inverse Weg, die Gluconeogenese: bei der Umsetzung Fructose-6-P und Fructose-1,6-bisphosphat und den Schritten zwischen Phosphoenolpyruvat und Pyruvat. In beiden Fällen erfordert der Rückweg mehr Energie als beim Hinweg gewonnen wird. Liefen beide Prozesse gleichzeitig, würde als Nettobilanz Energie verschwendet ( futile cycle ).
53 Regulationsschritte in der Glycolyse Daher sind die Phosphofruktokinase und die Pyruvatkinase die Haupt-Regulationspunkte der Glycolyse, dazu kommt der Eintritt in die Glycolyse, die Phosphorylierung der Glucose (deren Rückweg durch Hydrolyse des Phosphats ebenfalls zu Energieverlust führt).
54 Bilanz der Glycolyse Beim Umsatz von einer Hexose (Glucose, Fructose...) zu zwei Pyruvat werden zwei ATP reingesteckt, aber vier gewonnen: Gesamtgewinn 2 ATP im Verlauf der Substratmetabolisierung: Substratkettenphosphorylierung. Außerdem sind zwei NAD + zu NADH reduziert worden. Um die Redox-Bilanz neutral zu halten (die NAD + wiederzugewinnen), werden die Reduktionsäquivalente entweder auf die Produkte rückübertragen (Gärung) oder in der Atmungskette auf Elektronenakzeptoren (meist O 2 ) übertragen. Bei diesem Prozeß kommt es zu einer weiteren Energieausnützung (ATP-Bildung).
9. Abbau der Glukose zum Pyruvat
 9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Stoffwechsel. Die Chemie des Lebens ist in Stoffwechselwegen organisiert
 Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
Stoffwechsel. Metabolismus (3)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Grundlagen der Physiologie
 Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Citratzyklus. Citratzyklus
 Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Inhaltsverzeichnis - Kapitel
 Inhaltsverzeichnis - Kapitel 1. Einleitung: Die Chemie des Lebens 2. Kohlenhydrate 3. Lipide und Membranen 4. Nukleinsäuren 5. Aminosäuren und Proteine 6. Enzyme und Katalyse 7. Vitamine & Kofaktoren 8.
Inhaltsverzeichnis - Kapitel 1. Einleitung: Die Chemie des Lebens 2. Kohlenhydrate 3. Lipide und Membranen 4. Nukleinsäuren 5. Aminosäuren und Proteine 6. Enzyme und Katalyse 7. Vitamine & Kofaktoren 8.
Grundzüge des Energiestoffwechsels I
 Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Grundlagen der Physiologie
 Grundlagen der Physiologie Bioenergetik www.icbm.de/pmbio Energieformen Von Lebewesen verwertete Energieformen o Energie ist etwas, das Arbeit ermöglicht. o Lebewesen nutzen nur zwei Formen: -- Licht --
Grundlagen der Physiologie Bioenergetik www.icbm.de/pmbio Energieformen Von Lebewesen verwertete Energieformen o Energie ist etwas, das Arbeit ermöglicht. o Lebewesen nutzen nur zwei Formen: -- Licht --
ENZYME. Teil 1: Grundlagen und Substratbestimmungen
 ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
Thermodynamik & Kinetik
 Thermodynamik & Kinetik Inhaltsverzeichnis Ihr versteht die Begriffe offenes System, geschlossenes System, isoliertes System, Enthalpie, exotherm und endotherm... 3 Ihr kennt die Funktionsweise eines Kalorimeters
Thermodynamik & Kinetik Inhaltsverzeichnis Ihr versteht die Begriffe offenes System, geschlossenes System, isoliertes System, Enthalpie, exotherm und endotherm... 3 Ihr kennt die Funktionsweise eines Kalorimeters
Die Wege des Kohlenstoffes
 Die Wege des Kohlenstoffes 1. Licht vs. Dunkelreaktionen Lichtgetriebene Reaktionen o Dunkle -Reaktionen laufen nicht im Dunklen ab reduzieren CO 2-Zucker für Pflanzen zum Wachsen und für uns zum Nutzen
Die Wege des Kohlenstoffes 1. Licht vs. Dunkelreaktionen Lichtgetriebene Reaktionen o Dunkle -Reaktionen laufen nicht im Dunklen ab reduzieren CO 2-Zucker für Pflanzen zum Wachsen und für uns zum Nutzen
Der Stoffwechsel: Konzepte und Grundmuster
 Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik
 Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
Kapitel 5: 1. Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D.
 Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
PC I Thermodynamik G. Jeschke FS Lösung zur Übung 12
 PC I Thermodynamik G. Jeschke FS 2015 Lösung zur Übung 12 12.1 Die Hydrierung von Ethen zu Ethan a) Die Reaktionsenthalpie ist direkt aus den in der Aufgabenstellung tabellierten Standardbildungsenthalpien
PC I Thermodynamik G. Jeschke FS 2015 Lösung zur Übung 12 12.1 Die Hydrierung von Ethen zu Ethan a) Die Reaktionsenthalpie ist direkt aus den in der Aufgabenstellung tabellierten Standardbildungsenthalpien
Energetik und Kinetik chemischer Reaktionen
 Energetik und Kinetik chemischer Reaktionen Reaktionsenergetik als Teil der Thermodynamik - wann läuft eine chemische Reaktion freiwillig ab? - in welchem Umfang läuft eine Reaktion ab? - wie viel Energie
Energetik und Kinetik chemischer Reaktionen Reaktionsenergetik als Teil der Thermodynamik - wann läuft eine chemische Reaktion freiwillig ab? - in welchem Umfang läuft eine Reaktion ab? - wie viel Energie
Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie
 Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie H S G= H-T S Prozeß 1. (-) (+) (-) immer exergonisch, erfolgt spontan bei allen Temperaturen
Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie H S G= H-T S Prozeß 1. (-) (+) (-) immer exergonisch, erfolgt spontan bei allen Temperaturen
Thermodynamik. Thermodynamik ist die Lehre von den Energieänderungen im Verlauf von physikalischen und chemischen Vorgängen.
 Thermodynamik Was ist das? Thermodynamik ist die Lehre von den Energieänderungen im Verlauf von physikalischen und chemischen Vorgängen. Gesetze der Thermodynamik Erlauben die Voraussage, ob eine bestimmte
Thermodynamik Was ist das? Thermodynamik ist die Lehre von den Energieänderungen im Verlauf von physikalischen und chemischen Vorgängen. Gesetze der Thermodynamik Erlauben die Voraussage, ob eine bestimmte
Allgemeine Chemie für r Studierende der Zahnmedizin
 Allgemeine Chemie für r Studierende der Zahnmedizin Allgemeine und Anorganische Chemie Teil 3 Dr. Ulrich Schatzschneider Institut für Anorganische und Angewandte Chemie, Universität Hamburg Lehrstuhl für
Allgemeine Chemie für r Studierende der Zahnmedizin Allgemeine und Anorganische Chemie Teil 3 Dr. Ulrich Schatzschneider Institut für Anorganische und Angewandte Chemie, Universität Hamburg Lehrstuhl für
Mechanismus der Enzymkatalyse
 Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Die Innere Energie U
 Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O O 2 6 CO H 2 O G kj
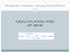 Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Kontrolle der Genexpression auf mrna-ebene. Abb. aus Stryer (5th Ed.)
 Kontrolle der Genexpression auf mrna-ebene Abb. aus Stryer (5th Ed.) RNA interference (RNAi) sirna (small interfering RNA) mirna (micro RNA) Abb. aus Stryer (5th Ed.) Transcriptional silencing Inhibition
Kontrolle der Genexpression auf mrna-ebene Abb. aus Stryer (5th Ed.) RNA interference (RNAi) sirna (small interfering RNA) mirna (micro RNA) Abb. aus Stryer (5th Ed.) Transcriptional silencing Inhibition
Hauptwege des Stoffwechsels
 Hauptwege des Stoffwechsels Auf- und Abbau der Stoffgruppen Kohlenhydrate 1 Enzyme Hauptklassen 1 2 3 4 5 6 Biochemie 08/2 Enzyme 1. Erhöhung der Reaktionsgeschwindigkeit ΔΔG kat = ΔG unkat - ΔG kat Erniedrigung
Hauptwege des Stoffwechsels Auf- und Abbau der Stoffgruppen Kohlenhydrate 1 Enzyme Hauptklassen 1 2 3 4 5 6 Biochemie 08/2 Enzyme 1. Erhöhung der Reaktionsgeschwindigkeit ΔΔG kat = ΔG unkat - ΔG kat Erniedrigung
KOHLENHYDRATE. Die Glykolyse
 Die Glykolyse Hexokinase Glucose Kostet 1ATP Mg 2+ Glucose-6-P Die Glucokinase kann durch Insulin induziert werden in : 1) Den Fettzellen 2) Den ß-Zellen des Pankreas 3) Der Nierenrinde 4) Der Leber Die
Die Glykolyse Hexokinase Glucose Kostet 1ATP Mg 2+ Glucose-6-P Die Glucokinase kann durch Insulin induziert werden in : 1) Den Fettzellen 2) Den ß-Zellen des Pankreas 3) Der Nierenrinde 4) Der Leber Die
KOHLENHYDRATE PYRUVAT-DEHYDROGENASE
 PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
Z11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
Clinical definition of the metabolic syndrome
 Metabolismus: Lehrbuch der Biochemie: Voet/Voet Kapitel 13: Einführung in den Stoffwechsel Kapitel 14: Glucose Katabolismus Kapitel 15: Glycogen Metabolismus und Gluconeogenese Kapitel 16: Citratcyclus
Metabolismus: Lehrbuch der Biochemie: Voet/Voet Kapitel 13: Einführung in den Stoffwechsel Kapitel 14: Glucose Katabolismus Kapitel 15: Glycogen Metabolismus und Gluconeogenese Kapitel 16: Citratcyclus
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Z 11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
Importance of Glucose
 Importance of Glucose C6H12O6 Glucose 2 C3 Glycogen Glucose-6-P Glycolyse 2 Pyruvat 2 C2 2 Acetyl-CoA 2 CO2 2 (C4 + C2) Citrat-Zyklus oder Tricarbonsäure 4 CO2 Zyklus 6 H O 2 6 O2 Atmungskette Als Produkt
Importance of Glucose C6H12O6 Glucose 2 C3 Glycogen Glucose-6-P Glycolyse 2 Pyruvat 2 C2 2 Acetyl-CoA 2 CO2 2 (C4 + C2) Citrat-Zyklus oder Tricarbonsäure 4 CO2 Zyklus 6 H O 2 6 O2 Atmungskette Als Produkt
Spezialfälle. BOYLE-MARIOTT`sches Gesetz p V = n R T bei T, n = konstant: p V = const. GAY-LUSSAC`sches Gesetz. bei V, n = konstant: p = const.
 Spezialfälle BOYLE-MARIOTT`sches Gesetz p V = n R T bei T, n = konstant: p V = const. GAY-LUSSAC`sches Gesetz p V = n R T bei V, n = konstant: p = const. T Druck Druck V = const. Volumen T 2 T 1 Temperatur
Spezialfälle BOYLE-MARIOTT`sches Gesetz p V = n R T bei T, n = konstant: p V = const. GAY-LUSSAC`sches Gesetz p V = n R T bei V, n = konstant: p = const. T Druck Druck V = const. Volumen T 2 T 1 Temperatur
Allgemeine Chemie für r Studierende der Medizin
 Allgemeine Chemie für r Studierende der Medizin Allgemeine und Anorganische Chemie Teil 4+5 Dr. Ulrich Schatzschneider Institut für Anorganische und Angewandte Chemie, Universität Hamburg Lehrstuhl für
Allgemeine Chemie für r Studierende der Medizin Allgemeine und Anorganische Chemie Teil 4+5 Dr. Ulrich Schatzschneider Institut für Anorganische und Angewandte Chemie, Universität Hamburg Lehrstuhl für
SS Thomas Schrader. der Universität Duisburg-Essen. (Teil 8: Redoxprozesse, Elektrochemie)
 Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
4.3 Reaktionsgeschwindigkeit und Katalysator
 4.3 Reaktionsgeschwindigkeit und Katalysator - Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Ein- Einstellung des Gleichgewichts,
4.3 Reaktionsgeschwindigkeit und Katalysator - Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Ein- Einstellung des Gleichgewichts,
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Übung zum chemischen Praktikum für Studierende der Biologie und Medizin Übung Nr. 1, /
 Übung zum chemischen Praktikum für Studierende der Biologie und Medizin Übung Nr. 1, 18.04.11 / 19.04.11 Lösung 1. Proteine sind Biopolymere, welche aus langen Ketten von Aminosäuren bestehen. a) Zeichnen
Übung zum chemischen Praktikum für Studierende der Biologie und Medizin Übung Nr. 1, 18.04.11 / 19.04.11 Lösung 1. Proteine sind Biopolymere, welche aus langen Ketten von Aminosäuren bestehen. a) Zeichnen
Bioenergetik. Prof. Dr. Albert Duschl
 Bioenergetik Prof. Dr. Albert Duschl Gesetze der Thermodynamik 1. Gesetz: Die Summe der Energie im Universum ist gleich. 2. Gesetz: Die Entropie nimmt zu. Geordnete Strukturen, wie Lebewesen, verletzen
Bioenergetik Prof. Dr. Albert Duschl Gesetze der Thermodynamik 1. Gesetz: Die Summe der Energie im Universum ist gleich. 2. Gesetz: Die Entropie nimmt zu. Geordnete Strukturen, wie Lebewesen, verletzen
EinFaCh 3. Studienvorbereitung Chemie. Einstieg in Freibergs anschauliches Chemiewissen Teil 3: Chemische Gleichgewichte. tu-freiberg.
 Studienvorbereitung Chemie EinFaCh 3 Einstieg in Freibergs anschauliches Chemiewissen Teil 3: Chemische Gleichgewichte tu-freiberg.de tu-freiberg.de/fakultaet2/einfach Das chemische Gleichgewicht ist ein
Studienvorbereitung Chemie EinFaCh 3 Einstieg in Freibergs anschauliches Chemiewissen Teil 3: Chemische Gleichgewichte tu-freiberg.de tu-freiberg.de/fakultaet2/einfach Das chemische Gleichgewicht ist ein
Richtung chemischer Reaktionen, chemisches Gleichgewicht. Massenwirkungsgesetz
 Richtung chemischer Reaktionen, chemisches Gleichgewicht a A + b B K [C] [A] c a [D] [B] c C + d D d b K = Gleichgewichtskonstante Massenwirkungsgesetz [ ] = in Lösung: Konzentration (in mol L -1 ), für
Richtung chemischer Reaktionen, chemisches Gleichgewicht a A + b B K [C] [A] c a [D] [B] c C + d D d b K = Gleichgewichtskonstante Massenwirkungsgesetz [ ] = in Lösung: Konzentration (in mol L -1 ), für
Enzyme: Grundlegende Konzepte und Kinetik
 Enzyme: Grundlegende Konzepte und Kinetik Enzyme sind Katalysatoren biologischer Systeme Wichtigste Eigenschaften: katalytische Stärke und Spezifität Nahezu alle bekannten Enzyme sind Proteine, es gibt
Enzyme: Grundlegende Konzepte und Kinetik Enzyme sind Katalysatoren biologischer Systeme Wichtigste Eigenschaften: katalytische Stärke und Spezifität Nahezu alle bekannten Enzyme sind Proteine, es gibt
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Richtung chemischer Reaktionen, Chemisches Gleichgewicht. Massenwirkungsgesetz
 Richtung chemischer Reaktionen, Chemisches Gleichgewicht a A + b B K = [C] [A] c a [D] [B] c C + d D d b Massenwirkungsgesetz K = Gleichgewichtskonstante [ ] = in Lösung: Konzentration (in mol L -1 ),
Richtung chemischer Reaktionen, Chemisches Gleichgewicht a A + b B K = [C] [A] c a [D] [B] c C + d D d b Massenwirkungsgesetz K = Gleichgewichtskonstante [ ] = in Lösung: Konzentration (in mol L -1 ),
Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen.
 1) DEFINITIONEN DIE CHEMISCHE REAKTION Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen. Der Massenerhalt: Die Masse ändert sich im Laufe einer Reaktion
1) DEFINITIONEN DIE CHEMISCHE REAKTION Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen. Der Massenerhalt: Die Masse ändert sich im Laufe einer Reaktion
Enthalpie. Ob eine Reaktion exergonisch ist, entscheidet die Änderung des Wärmeinhalts (heat content) H = Enthalpie
 Enthalpie Ob eine Reaktion exergonisch ist, entscheidet die Änderung des Wärmeinhalts (heat content) H = Enthalpie C 6 H 12 O 6 + 6O 2 6CO 2 + 6 H 2 O H = -2818 kj/mol - bei exergonischen Reaktionen Entropie
Enthalpie Ob eine Reaktion exergonisch ist, entscheidet die Änderung des Wärmeinhalts (heat content) H = Enthalpie C 6 H 12 O 6 + 6O 2 6CO 2 + 6 H 2 O H = -2818 kj/mol - bei exergonischen Reaktionen Entropie
Homogenes Gleichgewicht
 Knoch, Anastasiya Datum der Durchführung: Petri, Guido 08.12.2015 (Gruppe 11) Datum der Korrektur: 02.02.2016 Praktikum Physikalische Chemie I. Thermodynamik Homogenes Gleichgewicht 1. Aufgabenstellung
Knoch, Anastasiya Datum der Durchführung: Petri, Guido 08.12.2015 (Gruppe 11) Datum der Korrektur: 02.02.2016 Praktikum Physikalische Chemie I. Thermodynamik Homogenes Gleichgewicht 1. Aufgabenstellung
Präsentation STOFFWECHSEL STOFFWECHSEL. Fettstoffwechsel im Sport. Biologische Oxidation Zitratzyklus und Atmungskette
 STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
Schrittweise Oxidation und Decarboxylierung von Glucose-6-phosphat zu Ribulose-5- phosphat
 1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
Inhaltsverzeichnis Hinweise zur Benutzung Einführung in die Arbeits- und Denkweise Basis der Thermodynamik
 Inhaltsverzeichnis 1 Hinweise zur Benutzung... 1 1.1 Ausrichtung...... 1 1.2 Lernhilfen und -kontrollen...... 4 2 Einführung in die Arbeits- und Denkweise... 9 2.1 Zielsetzung...... 9 2.2 Wichtige physikalische
Inhaltsverzeichnis 1 Hinweise zur Benutzung... 1 1.1 Ausrichtung...... 1 1.2 Lernhilfen und -kontrollen...... 4 2 Einführung in die Arbeits- und Denkweise... 9 2.1 Zielsetzung...... 9 2.2 Wichtige physikalische
PC I Thermodynamik und Transportprozesse
 13.06.2006 16:37 1 PC I Thermodynamik und Transportprozesse Kapitel 4 13.06.2006 16:37 2 Chemische und Physikalische Umwandlungen Das chemische Gleichgewicht: Minimum der Freien Enthalpie Reaktionslaufzahl
13.06.2006 16:37 1 PC I Thermodynamik und Transportprozesse Kapitel 4 13.06.2006 16:37 2 Chemische und Physikalische Umwandlungen Das chemische Gleichgewicht: Minimum der Freien Enthalpie Reaktionslaufzahl
Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen. c(a) t. v = -
 REAKTIONSKINETIK 1 Reaktionskinetik Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen Anwendung: - Vorgänge in den lebenden Organismen
REAKTIONSKINETIK 1 Reaktionskinetik Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen Anwendung: - Vorgänge in den lebenden Organismen
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
1) Ein offenes System zeichnet sich immer durch eine konstante Temperatur aus. zeichnet sich immer durch eine konstante Masse aus.
 1) Ein offenes System zeichnet sich immer durch eine konstante Temperatur aus. zeichnet sich immer durch eine konstante Masse aus. kann mit der Umgebung Energie austauschen. kann mit der Umgebung Entropie
1) Ein offenes System zeichnet sich immer durch eine konstante Temperatur aus. zeichnet sich immer durch eine konstante Masse aus. kann mit der Umgebung Energie austauschen. kann mit der Umgebung Entropie
Reduction / Oxidation
 H :! H.. C.. H :! H H :! H.. C.. OH :! H H :! H 3 C.. C.. OH :! H O ::! H 3 C.. C.. H O ::! H 3 C.. C.. O -! O=C=O Oxidationszahl Methan -4 Methanol -2 Ethanol -1 Acetaldehyd +1 Acetat +3 Kohlendioxyd
H :! H.. C.. H :! H H :! H.. C.. OH :! H H :! H 3 C.. C.. OH :! H O ::! H 3 C.. C.. H O ::! H 3 C.. C.. O -! O=C=O Oxidationszahl Methan -4 Methanol -2 Ethanol -1 Acetaldehyd +1 Acetat +3 Kohlendioxyd
Redoxprozesse. Warum ist Sauerstoff für uns lebensnotwendig?
 Redoxprozesse Diese Lerneinheit befasst sich mit der Knallgasexplosion und Atmungskette - eine biologische Betrachtung von Redoxreaktionen mit den folgenden Lehrzielen: Warum ist Sauerstoff für uns lebensnotwendig?
Redoxprozesse Diese Lerneinheit befasst sich mit der Knallgasexplosion und Atmungskette - eine biologische Betrachtung von Redoxreaktionen mit den folgenden Lehrzielen: Warum ist Sauerstoff für uns lebensnotwendig?
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I
 Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 23.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 23.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Einführung in die Biochemie Glykolyse
 Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Pentosephosphat-Weg: alternativer Abbau von Glucose. Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet.
 Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Stoffwechsel. Metabolismus (2)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (2) Coenzyme und prosthetische Gruppen 1 Coenzyme Apoenzym + Coenzym fi funktionsfähiges Holoenzym Das Coenzym kann nach der Reaktion verändert
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (2) Coenzyme und prosthetische Gruppen 1 Coenzyme Apoenzym + Coenzym fi funktionsfähiges Holoenzym Das Coenzym kann nach der Reaktion verändert
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Atmung Respiration 1
 Atmung Respiration 1 Atmung Die oxidative Phosphorylierung ist der letzte Schritt einer Serie von Energieumwandlungen, die insgesamt als Zellatmung oder einfach Atmung (Respiration) bezeichnet werden 2
Atmung Respiration 1 Atmung Die oxidative Phosphorylierung ist der letzte Schritt einer Serie von Energieumwandlungen, die insgesamt als Zellatmung oder einfach Atmung (Respiration) bezeichnet werden 2
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Fachbereich Ökotrophologie Prof. Häusler SoSe 2005 Biochemie Definition und Fachgebiete
 Biochemie Definition und Fachgebiete Grenzwissenschaft zwischen Chemie, Biologie, Agrarwissenschaften und Medizin Spezialgebiete wie Immunchemie, Neurochemie, Pathobiologie, Genetik, Molekularbiologie,
Biochemie Definition und Fachgebiete Grenzwissenschaft zwischen Chemie, Biologie, Agrarwissenschaften und Medizin Spezialgebiete wie Immunchemie, Neurochemie, Pathobiologie, Genetik, Molekularbiologie,
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Tabellen und Formelsammlung Chemie
 Tabellen und Forelsalung Cheie Fakultät Maschinenbau Stand SS 2015 Nachfolgende Tabellen und Inforationen staen aus de Lehrbuch G. Kickelbick, Cheie für Ingenieure, Pearson-Verlag, 2008 soweit nicht anderweitig
Tabellen und Forelsalung Cheie Fakultät Maschinenbau Stand SS 2015 Nachfolgende Tabellen und Inforationen staen aus de Lehrbuch G. Kickelbick, Cheie für Ingenieure, Pearson-Verlag, 2008 soweit nicht anderweitig
endotherme Reaktionen
 Exotherme/endotherme endotherme Reaktionen Edukte - H Produkte Exotherme Reaktion Edukte Produkte + H Endotherme Reaktion 101 Das Massenwirkungsgesetz Das Massenwirkungsgesetz Gleichgewicht chemischer
Exotherme/endotherme endotherme Reaktionen Edukte - H Produkte Exotherme Reaktion Edukte Produkte + H Endotherme Reaktion 101 Das Massenwirkungsgesetz Das Massenwirkungsgesetz Gleichgewicht chemischer
Vorlesung Anorganische Chemie
 Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 5 Verhalten von Lösungen Konzentrationen Solvatation und Solvatationsenthalpie Kolligative Eigenschaften Kryoskopie/Ebullioskopie
Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 5 Verhalten von Lösungen Konzentrationen Solvatation und Solvatationsenthalpie Kolligative Eigenschaften Kryoskopie/Ebullioskopie
I. Zellatmung. =Abbau von Kohlenhydraten unter Sauerstoffverbrauch (aerob) KH + O 2 --> CO 2 + H 2 O + Energie
 KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt.
 Übung und Lösung zur Übung Aminosäuren 1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt. 2. Das Tripeptid Glutathion ( -Glu-Cys-Gly)
Übung und Lösung zur Übung Aminosäuren 1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt. 2. Das Tripeptid Glutathion ( -Glu-Cys-Gly)
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Biochemie II. im Wintersemester 2009/2010. Joachim Wegener. Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg
 Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
2. Klausur. 1. Aufgabe
 1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Bei der abschließenden
1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Bei der abschließenden
1. Die Bildung von Methan durch Mikroorganismen erfolgt (2 Punkte)
 Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
Die Glycolyse (Glucose Katabolismus)
 Die Glycolyse (Glucose Katabolismus) 1. Übersicht über die Glykolyse 2. Reaktionschritte der Glykolyse 3. Gärung: Der anaerobe Weg des Pyruvats 4. Kontrolle der Glykolyse 5. Stoffwechsel von anderen Hexosen
Die Glycolyse (Glucose Katabolismus) 1. Übersicht über die Glykolyse 2. Reaktionschritte der Glykolyse 3. Gärung: Der anaerobe Weg des Pyruvats 4. Kontrolle der Glykolyse 5. Stoffwechsel von anderen Hexosen
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
 Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Coulomb-Gesetz, Ionen- (Kristall-)strukturen, NaCl, CsCl, ZnS, Elementarzelle, 7 Kristallsysteme Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Coulomb-Gesetz, Ionen- (Kristall-)strukturen, NaCl, CsCl, ZnS, Elementarzelle, 7 Kristallsysteme Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Chemie für Mediziner. 2., aktualisierte Auflage. Carsten Schmuck Bernd Engels Tanja Schirmeister Reinhold Fink
 Chemie für Mediziner 2., aktualisierte Auflage Carsten Schmuck Bernd Engels Tanja Schirmeister Reinhold Fink 5 Chemische Reaktionen und Energetik K Δ R G Gleichgewicht liegt A+B C+D >1
Chemie für Mediziner 2., aktualisierte Auflage Carsten Schmuck Bernd Engels Tanja Schirmeister Reinhold Fink 5 Chemische Reaktionen und Energetik K Δ R G Gleichgewicht liegt A+B C+D >1
Katalyse. höhere Reaktionsgeschwindigkeit bei derselben Temperatur! Achtung: Gleichgewicht der chemischen Reaktion wird nicht verschoben
 Katalyse Ein Katalysator setzt Aktivierungsenergie einer Reaktion herab, indem er einen anderen Reaktionsweg ermöglicht, so dass der geschwindigkeitsbestimmende Schritt der nicht-katalysierten Reaktion
Katalyse Ein Katalysator setzt Aktivierungsenergie einer Reaktion herab, indem er einen anderen Reaktionsweg ermöglicht, so dass der geschwindigkeitsbestimmende Schritt der nicht-katalysierten Reaktion
a) Welche der folgenden Aussagen treffen nicht zu? (Dies bezieht sind nur auf Aufgabenteil a)
 Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Einführung in die Biochemie Gärung anaerober Abbau
 Gärungen sind ATP liefernde Energiestoffwechsel, die ohne Sauerstoff als xidationsmittel ablaufen. Ein Grund zur Nutzung der Gärung kann ein plötzlich anstehender Bedarf an rasch verfügbarerer Energie
Gärungen sind ATP liefernde Energiestoffwechsel, die ohne Sauerstoff als xidationsmittel ablaufen. Ein Grund zur Nutzung der Gärung kann ein plötzlich anstehender Bedarf an rasch verfügbarerer Energie
ALDEHYDE & KETONE. Referat über die Carbonylverbindungen: Aldehyde und Ketone Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium
 ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
Übungsaufgaben Chemie Nr. 3
 Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
Pentosephosphatzyklus. Synonym: Hexosemonophosphatweg
 Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Praktikum. Enzymkinetik am Beispiel der Protease Trypsin
 Praktikum Methoden der molekularen Biowissenschaften Teil 1: Biochemie Enzymkinetik am Beispiel der Protease Trypsin Prof. Walter Nickel Biochemie-Zentrum der Universität Heidelberg Thermodynamische Eigenschaften
Praktikum Methoden der molekularen Biowissenschaften Teil 1: Biochemie Enzymkinetik am Beispiel der Protease Trypsin Prof. Walter Nickel Biochemie-Zentrum der Universität Heidelberg Thermodynamische Eigenschaften
Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus)
 Kinetik Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus) Klassifizierung chem. Reaktionen nach kinetischen Aspekten a) Reaktionsmolekularität: wie viele Teilchen
Kinetik Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus) Klassifizierung chem. Reaktionen nach kinetischen Aspekten a) Reaktionsmolekularität: wie viele Teilchen
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
