Aufbereitung von Medizinischen Thrombose-Prophylaxe-Strümpfen
|
|
|
- Bärbel Gehrig
- vor 7 Jahren
- Abrufe
Transkript
1 Aufbereitung von Medizinischen Thrombose-Prophylaxe-Strümpfen Sicherheit, Wirtschaftlichkeit & Verantwortlichkeit Hartmut Gamm, Textiling., Qualitätsbeauftragter, LEO System GmbH, Hamburg Die allgemeinen Hygiene- und Sicherheitsanforderungen für müssen auch für Thrombose-Prophylaxe-Strümpfe (TPS) spezifi sch angewandt werden. Den Zusammenhängen und Verantwortlichkeiten von Krankenhaus, Hersteller und kommt dabei eine große Bedeutung zu. Anforderungen an die Hygiene Medizinische Thrombose-Prophylaxe-Strümpfe (TPS), die zur physikalischen Thromboembolie- Prophylaxe eingesetzt werden, sind gemäß ihrer Zweckbestimmung ein Medizinprodukt (MP). Für gelten besondere Gesetze und Verordnungen, um u.a. für die Gesundheit und den erforderlichen Schutz der Patienten zu sorgen. Grundlage aller Regelungen ist die Richtlinie über des Europäischen Rates 93/42/EEC. An, die wie die TPS dazu bestimmt sind mit dem menschlichen Körper in Berührung gebracht zu werden, werden besondere Anforderungen zum Zwecke der Wiederverwendung gestellt. Die Kommission für Krankenhaushygiene und Infektionsprävention beim Robert-Koch-Institut (RKI) und das Bundesinstitut für Arzneimittel und (BfArM) haben dazu im Bundesgesundheitsblatt ( : ) die Empfehlung Anforderungen an die Hygiene bei der Aufbereitung von n veröffentlicht. Risikobewertung Je nach Risikopotenzial eines s sind unterschiedliche Anforderungen zu stellen. Die Risikobewertung gemäß der o.g. RKI-Richtlinie kann für die meisten am Markt erhältlichen Thrombose-Prophylaxe- Strümpfe wie folgt vorgenommen werden. Die Einstufung der erfolgt hinsichtlich der Art ihrer folgenden Anwendung und dem sich daraus ableitenden Risiko in: Einstufung Unkritische Semikritische Kritische Einsatzbereich MP, die lediglich mit intakter Haut in Berührung kommen MP, die mit Schleimhaut oder krankhaft veränderter Haut in Berührung kommen MP; die die Haut oder Schleimhaut durchdringen und dabei in Kontakt. mit Wunden kommen Aufbereitung Ohne besondere Anforderungen Ohne besondere Anforderungen Mit erhöhten Anforderungen Mit erhöhten Anforderungen an die Aufbereitung Mit besonders hohen Anforderungen 47
2 Bei Zweifeln an der Einstufung ist das Medizinprodukt der höheren, kritischeren Risikostufe zuzuordnen. Erstmalige Verwendung Neue Medizinische Thrombose-Prophylaxe- Strümpfe werden bestimmungsgemäß nur mit intakter Haut in Berührung gebracht. Evtl. Wunden sind vor dem Anlegen der TPS fachgerecht zu versorgen und abzudecken. Die TPS sind nach der Benutzung potenziell mit Krankheitserregern kontaminiert. Die Aufbereitung zur Wiederverwendung hat den Zweck, die Risiken aus der vorangegangenen Anwendung zu minimieren, und besteht demnach in der Reinigung und Desinfektion der Produkte. Die Aufbereitung wird gemäß den Hersteller-Vorgaben durch ein desinfizierendes Waschverfahren durchgeführt. Die physikalischen und damit funktionellen Eigenschaften von TPS können bereits durch die erste Anwendung verändert werden. Überdehnung durch nicht sachgerechtes Anziehen der Strümpfe, Materialzerstörung durch lange Fingernägel sowie Beeinträchtigungen des elastischen Anteils der Strümpfe durch im Schweiß des Patienten befi ndliche Medikamentenrückstände sind solche Risikofaktoren. Eine wiederholte, sichere Verwendung des selben Strumpfes nach ordnungsgemäßer Aufbereitung setzt daher voraus, dass bereits bei der Anwendung schädigende Einfl üsse möglichst ausgeschlossen werden. Erhöhte Anforderungen Erhöhte Anforderungen sind laut RKI-Richtlinie zu stellen, wenn 1) die Effektivität der Reinigung nicht durch Inspektion unmittelbar beurteilbar ist, z.b. wegen langer, enger Hohlräume oder schlecht bespülbarer Oberfl äche. TPS sind dreidimensional, aufgrund ihrer Materialstruktur aber sehr gut beurteilbar. Eine weitere Verbesserung wird durch die Benutzung einfacher Hilfsmittel erreicht, die den Strumpf von innen etwas dehnen. Damit sind sowohl Verfleckungen als auch Beschädigungen unmittelbar zu erkennen. 2) die Anwendungs- oder Funktionssicherheit beeinfl ussende Effekte der Aufbereitung auf das MP und seine Materialeigenschaften nicht auszuschließen sind Bei Thrombose-Prophylaxe-Strümpfen handelt es sich um textile Produkte mit einem hohen Anteil elastischen Materials. Dieses Material sorgt in Kombination mit besonderen Fertigungsverfahren dafür, dass der Strumpf gemäß seiner Zweckbestimmung funktionell ist. Chlorhaltige Bleichmittel beim Waschen und zu hohe Temperaturen beim Trocknen können während der Aufbereitung zu einer irreversiblen Schädigung des Materials führen. Die Anwendungs- und Funktionssicherheit wäre damit beeinträchtigt. 3) die Anzahl der Anwendungen oder der Aufbereitungszyklen durch den Hersteller auf eine bestimmte Anzahl begrenzt ist. Alle Hersteller von TPS, die ihre Produkte als nach Aufbereitung wieder verwendbar deklarieren, beschränken die Anwendungs- und Aufbereitungszyklen. I.d.R. ist die Eignung eines TPS nur bis zur 10-ten Verwendung sichergestellt. Ergebnis der Risikobewertung: Thrombose-Prophylaxe-Strümpfe sind semikritische mit erhöhten Anforderungen Sicherheit beim Einsatz wieder verwendbarer TPS Um die Risiken zu minimieren und einen sicheren Einsatz aufbereiteter TPS zu gewährleisten, sind die Verantwortung und Aufgaben der Beteiligten eindeutig festgelegt. (siehe Abbildung auf folgender Seite) Die Hersteller haben Angaben darüber zu machen, ob und wie die TPS aufbereitet werden können. Sie müssen darlegen, dass die genannte Aufbereitungsart geeignet ist, die technisch-funktionelle Sicherheit der TPS nach Aufbereitung zu gewährleisten. Darüber hinaus hat der Hersteller jedem Produkt Informationen beizugeben, die die sichere Anwendung des Produkts möglich ma- 48
3 Pflichten bei der Aufbereitung von Throm bose-prophylaxe-strümpfen Quelle: LEO System GmbH chen (Auszug aus der Europäischen Richtlinie über 93/42/EWG). Diese Informationen werden über so genannte Herstelleranweisungen und ergänzende Schulungen durch den Hersteller und dessen berater vermittelt. Dem Betreiber des s TPS (Krankenhaus) obliegt die korrekte Einstufung der TPS gemäß ihres Risikopotenzials sowie die Festlegung ob, wie oft und mit welchen Verfahren aufbereitet werden soll. Dabei sind die Angaben Risikomatrix TPS des Herstellers zu beachten. Darüber hinaus hat der Betreiber die Anwender durch Schulung und Information in die Lage zu versetzen, die zur Verfügung gestellten sicher anwenden zu können. Auszug aus der -Betreiberverordnung vom dürfen nur von Personen... angewendet... werden, die dafür die erforderliche Ausbildung oder Kenntnis und Erfahrung besitzen. Der Betreiber (das Krankenhaus) darf nur Personen mit dem... Anwenden von n beauftragen, die die o.g. Voraussetzungen erfüllen. Der übernimmt die benutzten TPS vom Krankenhaus (Betreiber) und bereitet sie in dessen Auftrag auf. Die Aufbereitung der TPS ist gemäß den Vorgaben von Hersteller und Betreiber nachvollziehbar mit einem validierten Verfahren durchzuführen. Dazu gehört auch die Identifi kation zum Zwecke der Entscheidung über eine erneute Aufbereitung bei deren zahlenmäßiger Begrenzung. Bereitet das Krankenhaus die TPS selbst auf, gelten die Anforderungen in gleicher Weise. In diesem Fall wäre das Krankenhaus gleichzeitig Betreiber und. Zu den ermittelten Risiken müssen Maßnahmen und Verantwortlichkeiten defi niert werden, um eine sichere Anwendung des aufbereiteten s zu gewährleisten. Risiko Maßnahme Verantwortlich Vorangegangene Anwendung Schulung der Anwender Hersteller und Betreiber Rückstände aus der vorangegangenen Anwendung und Aufbereitung Änderung physikalischer Eigenschaften durch die Aufbereitung Begrenzung Anzahl Aufbereitungszyklen RKI-gelistete Wasch-und Desinfektionsverfahren, Hygienezeugnis RAL 992/2 Validierte Aufbereitungsverfahren,Qualitätsmanagement Einzelteilverfolgung 49
4 Prozesssicherheit in der Aufbereitung Der Aufbereitungskreislauf beginnt bereits mit dem separaten Sammeln der benutzen TPS. Da Krankenhauswäsche vor der Bearbeitung nicht sortiert werden darf, sollten Thrombose-Prophylaxe-Strümpfen nicht vermischt mit der übrigen Wäsche in der Wäscherei angeliefert werden. Die üblichen Wasch- und Trocknungsverfahren für normale Krankenhauswäsche sind für TPS ungeeignet. So bearbeitete Strümpfe sind nicht mehr verwendbar. Die TPS sollten also separat von der sonstigen Wäsche in deutlich gekennzeichneten Wäschesäcken gesammelt werden. Das ist die Voraussetzung, dass die TPS das vorgeschriebene Waschund Trocknungsverfahren durchlaufen können. Die einzelnen Verfahrensschritte der validierten Aufbereitung müssen zur Gewährleistung der kontinuierlichen Erfüllung der Anforderungen in ein Qualitätsmanagementsystem eingebunden sein. Darin sind die festgelegten einzelnen Schritte des Aufbereitungsprozesses incl. der notwendigen Prüfungen in Arbeits- und Betriebsanweisungen festzulegen. Zu diesen Verfahrensschritten gehört unabdingbar die dokumentierte und für den Anwender nachvollziehbare Freigabe des s zur erneuten Verwendung. Damit erklärt der, dass die TPS eine ordnungsgemäße Aufbereitung unter Einhaltung aller Vorgaben durchlaufen haben. Validierung und Einzelteilverfolgung Getragene Thrombose-Prophylaxe-Strümpfe sind potenzielle infektionsverdächtige Wäsche. Unabhängig von spezifi schen Angaben der TPS-Hersteller hat die Reinigung und Desinfektion daher in Übereinstimmung mit der RKI-Richtlinine Krankenhaushygiene und Infektionsprävention, Anforderungen der Hygiene an die Wäsche aus Einrichtungen des Gesundheitsdienstes,.) zu erfolgen. Unter Validierung wird der dokumentierte Nachweis der beständigen Wirksamkeit des Verfahrens unter den am Ort vorhandenen Betriebsbedingungen im Routinebetrieb verstanden. Der hat den Nachweis zu erbringen, dass der jeweilige Prozess in einer Form durchlaufen wird, der die Erzielung der jeweils vorgegebenen Spezifi kationen garantiert. Insbesondere das Gütezeichen RAL-GZ 992/2 für Krankenhauswäsche ist geeignet den betrieblichen Nachweis der beständigen Wirksamkeit der hygienischen Aufbereitung zu dokumentieren. Alle relevanten Vorgaben incl. der bereits genannten RKI-Richtlinien werden über die Güte- und Prüfbestimmungen RAL-GZ 992/2 abgedeckt. Die Überwachung der Betriebe erfolgt durch dokumentierte Eigenkontrollen sowie anhand von neutralen, unangemeldet durchgeführten hygienetechnischen Prüfungen und mikrobiologischen Kontrollen durch das unabhängige Textilforschungszentrum Hohensteiner Institute. Diese Fremdüberwachung bezieht sich auf die Waschverfahren und den gesamten Betriebsablauf sowie auf die Hygiene im Betrieb. Um sicher zu stellen, dass die TPS in der Wäscherei dem vom Hersteller und Betreiber vorgeschriebenen Verfahren zugeführt werden, sollten die TPS individuell gekennzeichnet und über eine elektronische Einzelteilverfolgung erfassbar sein. Ein weiterer Vorteil der Einzelteilverfolgung liegt in der automatischen und eindeutigen Kennzeichnung jedes Strumpfes. So kann verhindert werden, dass z.b. durch Patientenverlegungen in das Krankenhaus gelangte, neutrale Strümpfe als einsatzfähig angesehen und in den Kreislauf integriert werden. Die vielfältigen Anforderungen von Thrombose-Prophylaxe-Strümpfen zum Zwecke der Wiederverwendung sind in der Regel nur von darauf spezialisierten Betrieben bzw. Einrichtungen sicher zu erfüllen. Wirtschaftlichkeit Die Aufbereitung von Thrombose-Prophylaxe- Strümpfen sollte kein Selbstzweck sein. Ausschlaggebend ist eine Wirtschaftlichkeitsbetrachtung der Einmal-Verwendung im Vergleich zur Wiederverwendung nach Aufbereitung. Notwendig ist die Analyse der Gesamtkosten bei vergleichbaren Bedingungen von der Belieferung bis zur Anwendung. Im Einzelnen sind zu beachten: 50
5 Einkaufspreis Neuware pro Paar Ziel einer Wiederverwendung ist immer eine drastische Reduzierung der Einkaufsmenge neuer Strümpfe. Hier ist vor allem auf evtl. Staffelpreise bzw. Rabatte oder Rückvergütungen zu achten. Die aktuellen Einkaufszahlen sind für eine Vergleichsrechnung nur dann geeignet, wenn sie einen echten Einmal-Gebrauch der Produkte widerspiegeln. In vielen Kliniken ist die Wiederverwendung von Thrombose-Prophylaxe-Strümpfen bereits gängige Praxis, auch wenn die o.g. einschlägigen Vorschriften dabei unbeachtet bleiben. Strenge Kontrollen und die das strikte Einhalten der maximalen Zyklenzahl führen bei der Einführung eines sicheren Aufbereitungskreislaufs u. U. sogar zu einer höheren Beschaffungsmenge an Strümpfen. Kosten der Aufbereitung pro Strumpf/ Paar Die Kosten sind bei eigener Aufbereitung durch das Krankenhaus intern zu ermitteln. Wesentliche Faktoren sind die notwendigen Komponenten zur Einzelteilverfolgung und der Gewährleistung der Sicherheit in hygienischer und technisch-funktioneller Hinsicht. Externe nennen häufi g einen Aufbereitungspreis pro Strumpf/Paar. Weitere Kosten können durch Kennzeichnung oder Verpackung entstehen. Die Kosten pro Aufbereitungszyklus sollten signifi kant unter dem Einkaufspreis der Ware (50 70 %) liegen, um entsprechende wirtschaftliche Effekte erzielen zu können. Unter dieser Annahme rechnet sich die Wiederverwendung schon nach der ersten Aufbereitung. Logistik / Umlaufbestand Neue TPS werden normalerweise zentral angeliefert und durch die hausinterne Logistik (Hol- und Bringedienst, Versorgungsassistenten) auf die Stationen geliefert. Den gleichen Versorgungsweg können auch aufbereitete TPS nehmen. Insbesondere bei großen Packeinheiten pro Größe (>10) ist eine zentrale Rücklieferung der TPS vom sinnvoll. Eine stationsweise Zuordnung verringert automatisch die als Produktionseinheit zu verwaltende Menge an TPS und führt i.d.r. zu einem höheren Umlaufbestand und steigenden Kosten. Abbildung: TPS am Bein, Quelle: tyco healthcare. Effektive Aufbereitungszyklen (Durchschnitt) Die mögliche Ersparnis bei der Wiederverwendung von TPS hängt ganz entscheidend davon ab, wie häufi g ein Strumpf wieder verwendet werden kann. Die Zyklenzahl wird durch folgende Sachverhalte beeinfl usst. Vom Hersteller vorgegebene maximale Anzahl Anwendungs- und Aufbereitungszyklen Schwund durch Falschentsorgung oder die Auflage des behandelnden Arztes, die TPS nach der Entlassung noch einige Tage zu Hause weiter zu tragen Vorzeitiges Ende der Einsatzfähigkeit z.b. durch unsachgemäße Behandlung mit färbenden Desinfektionsmitteln, die nicht auswaschbar sind Schädigung während der Anwendung, die die technisch funktionelle Sicherheit des Strumpfes beeinfl ussen Den größten Einfluss auf die Wirtschaftlichkeit der Wiederverwendung von Thrombose-Prophylaxe- Strümpfen hat damit das Krankenhaus selbst. Zusammenfassung Die Aufbereitung und Wiederverwendung von Medizinischen Thrombose-Prophylaxe-Strümpfen bietet gegenüber der Einmal-Verwendung häufi g erhebliches Einsparpotenzial. Voraussetzung eines Aufbereitungskonzeptes muss die Gewährleistung der hygienischen, technisch-funktionellen und anwendungsorientierten Sicherheit sein. Die einschlägigen Vorschriften weisen dazu den Weg: Krankenhaus, und Hersteller müssen ihrer spezifischen Verantwortung in enger Abstimmung und Kooperation nachkommen. Dann sind die gewünschten Effekte ohne zusätzliches Risiko realisierbar. 51
DGKH-Kongress, Berlin Lunch Symposium: Validierbare Aufbereitung von Ultraschallsonden
 DGKH-Kongress, Berlin Lunch Symposium: Validierbare Aufbereitung von Ultraschallsonden 20.3.18 Rechtliche An- und Herausforderungen bei der Aufbereitung von Ultraschallsonden Dr. med. Bärbel Christiansen
DGKH-Kongress, Berlin Lunch Symposium: Validierbare Aufbereitung von Ultraschallsonden 20.3.18 Rechtliche An- und Herausforderungen bei der Aufbereitung von Ultraschallsonden Dr. med. Bärbel Christiansen
Anforderungen an die Aufbereitung von Medizinprodukten Gesundheitssystem Pflichten Reinigung Desinfektion Sterilisation Haftung
 Positionspapier Anforderungen an die Aufbereitung von Medizinprodukten Pflichten der Hersteller und Pflichten der GesundheitssystemAufbereitun Pflichten Reinigung Desinfektion Sterilisation Haftung Hygiene
Positionspapier Anforderungen an die Aufbereitung von Medizinprodukten Pflichten der Hersteller und Pflichten der GesundheitssystemAufbereitun Pflichten Reinigung Desinfektion Sterilisation Haftung Hygiene
Aufbereitung von Medizinprodukten in Zahnarztpraxen Anforderungen nach dem Medizinproduktegesetz
 Aufbereitung von Medizinprodukten in Zahnarztpraxen Anforderungen nach dem Medizinproduktegesetz Kassel - 23. 09. 2016 09/2016 Beate Keim - Dez. 35.1 1 Rechtliche Grundlagen Medizinprodukte-Richtlinie
Aufbereitung von Medizinprodukten in Zahnarztpraxen Anforderungen nach dem Medizinproduktegesetz Kassel - 23. 09. 2016 09/2016 Beate Keim - Dez. 35.1 1 Rechtliche Grundlagen Medizinprodukte-Richtlinie
AMAH Aufbereitung in der Endoskopie
 AMAH Aufbereitung in der Endoskopie Risikobewertung von flexiblen Endoskopen und Folgerungen für die Aufbereitung Christian Roth Olympus Deutschland GmbH OLYMPUS Deutschland GmbH, Medical Systems Hannover,
AMAH Aufbereitung in der Endoskopie Risikobewertung von flexiblen Endoskopen und Folgerungen für die Aufbereitung Christian Roth Olympus Deutschland GmbH OLYMPUS Deutschland GmbH, Medical Systems Hannover,
Die Sicht des Gesetzgebers
 Essen, 23. Februar 2005 Aufbereitung von Medizinprodukten die Verantwortung des Herstellers und des Anwenders Die Sicht des Gesetzgebers Bundesministerium für Gesundheit und Soziale Sicherung 1 Gliederung
Essen, 23. Februar 2005 Aufbereitung von Medizinprodukten die Verantwortung des Herstellers und des Anwenders Die Sicht des Gesetzgebers Bundesministerium für Gesundheit und Soziale Sicherung 1 Gliederung
Aufbereitung von MIC- und Hohlkörper-Instrumenten
 Arbeitskreis Medizinprodukte Aufbereitung Hannover 14. Juni 2014 Aufbereitung von MIC- und Hohlkörper-Instrumenten Jörn Krämer Vertrieb Webeco GmbH An der Trave 14 23923 Selmsdorf Tel.: 0451-2807212 Mobil
Arbeitskreis Medizinprodukte Aufbereitung Hannover 14. Juni 2014 Aufbereitung von MIC- und Hohlkörper-Instrumenten Jörn Krämer Vertrieb Webeco GmbH An der Trave 14 23923 Selmsdorf Tel.: 0451-2807212 Mobil
Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und Aufbereitungsverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen
 Seite 1 von 8 Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und sverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen Inhalt: Unterscheidung aufgrund von Verwendungszweck und sverfahren Risikobewertung
Seite 1 von 8 Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und sverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen Inhalt: Unterscheidung aufgrund von Verwendungszweck und sverfahren Risikobewertung
Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie
 Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie Rechtliche Abgrenzung zwischen Podologie und Fußpflege Ziele des Medizinprodukterechtes: für die Gesundheit und den erforderlichen
Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie Rechtliche Abgrenzung zwischen Podologie und Fußpflege Ziele des Medizinprodukterechtes: für die Gesundheit und den erforderlichen
Neue gesetzliche Anforderungen für Reinigungs- und Desinfektionsgeräte und deren Bedeutung für den Betreiber
 Neue gesetzliche Anforderungen für Reinigungs- und Desinfektionsgeräte und deren Bedeutung für den Betreiber (am Beispiel des Steckbeckenspülers) Referent: Frank Hoffmann Leiter Vertrieb Deutschland Reinigungs-
Neue gesetzliche Anforderungen für Reinigungs- und Desinfektionsgeräte und deren Bedeutung für den Betreiber (am Beispiel des Steckbeckenspülers) Referent: Frank Hoffmann Leiter Vertrieb Deutschland Reinigungs-
Zero Infections was kann und muss die technische Hygiene leisten
 Zero Infections was kann und muss die technische Hygiene leisten S. Werner, F. v. Rheinbaben Facharzt für Hygiene und Umweltmedizin HygCen Germany GmbH, Schwerin / Bochum 13.04.2016 DGKH Kongress Berlin
Zero Infections was kann und muss die technische Hygiene leisten S. Werner, F. v. Rheinbaben Facharzt für Hygiene und Umweltmedizin HygCen Germany GmbH, Schwerin / Bochum 13.04.2016 DGKH Kongress Berlin
Aufbereitung von Medizinprodukten - die Verantwortung des Herstellers und des Anwenders Die Sicht der Krankenhausgesellschaft
 Aufbereitung von Medizinprodukten - die Verantwortung des Herstellers und des Anwenders Die Sicht der Krankenhausgesellschaft Essen, Universitätsklinikum, 23. Februar 2005 Verantwortung des Betreibers/Anwenders
Aufbereitung von Medizinprodukten - die Verantwortung des Herstellers und des Anwenders Die Sicht der Krankenhausgesellschaft Essen, Universitätsklinikum, 23. Februar 2005 Verantwortung des Betreibers/Anwenders
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten
 Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Spezielle Regeln für die Benennung Geltungsbereich Aufbereitung von Medizinprodukten gemäß 10 Abs. 3 Satz 2 MPG 1 Geltungsbereich
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Spezielle Regeln für die Benennung Geltungsbereich Aufbereitung von Medizinprodukten gemäß 10 Abs. 3 Satz 2 MPG 1 Geltungsbereich
Arbeitsbedingungen in der ZSVA aus Sicht der Industrie
 Arbeitsbedingungen in der ZSVA aus Sicht der Industrie Dr. Ulrike Weber Osnabrück 15. September 2015 Miele/GTZ/PI 1 Der Aufbereitungskreislauf Miele/GTZ/PI 2 Wer / was ist am Prozess beteiligt? Logistik
Arbeitsbedingungen in der ZSVA aus Sicht der Industrie Dr. Ulrike Weber Osnabrück 15. September 2015 Miele/GTZ/PI 1 Der Aufbereitungskreislauf Miele/GTZ/PI 2 Wer / was ist am Prozess beteiligt? Logistik
Christian Witte Zertifiziertes Qualitätsmanagement bei Aufbereitung von Kritisch-C Produkten gemäß valider Herstelleranweisung?
 Christian Witte Zertifiziertes Qualitätsmanagement bei Aufbereitung von Kritisch-C Produkten gemäß valider Herstelleranweisung? MPBetreibV vs. KRINKO/BfArM-Empfehlung? Historie und Ausblick Einstufung
Christian Witte Zertifiziertes Qualitätsmanagement bei Aufbereitung von Kritisch-C Produkten gemäß valider Herstelleranweisung? MPBetreibV vs. KRINKO/BfArM-Empfehlung? Historie und Ausblick Einstufung
Kanzlei Lücker MP-Recht. MPBetreibV Relevante Änderungen zum AKI Veranstaltung April 2017 Potsdam / Leipzig
 MPBetreibV 2017 Relevante Änderungen zum 1.1.2017 44. AKI Veranstaltung April 2017 Potsdam / Leipzig MPBetreibV neue Fassung: - Neue Sytematik - Neuer Anwendungsbereich - Definitionen für Betreiber, Anwender,
MPBetreibV 2017 Relevante Änderungen zum 1.1.2017 44. AKI Veranstaltung April 2017 Potsdam / Leipzig MPBetreibV neue Fassung: - Neue Sytematik - Neuer Anwendungsbereich - Definitionen für Betreiber, Anwender,
Aufbereitung von Instrumenten und Medizinprodukten
 Dritter Hygienetag der Kassenärztlichen Vereinigung Bayerns Nürnberg, 10.Mai 2014 Aufbereitung von Instrumenten und Medizinprodukten Vortrag: Validierung der Instrumentenaufbereitung in der Arztpraxis;
Dritter Hygienetag der Kassenärztlichen Vereinigung Bayerns Nürnberg, 10.Mai 2014 Aufbereitung von Instrumenten und Medizinprodukten Vortrag: Validierung der Instrumentenaufbereitung in der Arztpraxis;
Hygienebeauftragte Mitarbeiterinnen und Mitarbeiter in der Arztpraxis (Seminar )
 Hygienebeauftragte Mitarbeiterinnen und Mitarbeiter in der Arztpraxis (Seminar 181301) Allgemeine Faktoren: Teilnehmer: Module: Grundlage: 10 bis maximal 20 Teilnehmer Voraussetzung: Abschluss Arzthelferin
Hygienebeauftragte Mitarbeiterinnen und Mitarbeiter in der Arztpraxis (Seminar 181301) Allgemeine Faktoren: Teilnehmer: Module: Grundlage: 10 bis maximal 20 Teilnehmer Voraussetzung: Abschluss Arzthelferin
3 Jahre Zertifizierungen der Aufbereitung
 ÖGSV-wfhss-Congress 2007, Baden bei Wien, 05.05.2007 3 Jahre Zertifizierungen der Aufbereitung auf Basis der deutschen RKI/BfArM-Empfehlung Ein Erfahrungsbericht Dr. Thomas Kießling Sachverständiger für
ÖGSV-wfhss-Congress 2007, Baden bei Wien, 05.05.2007 3 Jahre Zertifizierungen der Aufbereitung auf Basis der deutschen RKI/BfArM-Empfehlung Ein Erfahrungsbericht Dr. Thomas Kießling Sachverständiger für
Umgang mit hygienisch problematischen (Medizin-)Produkten
 Umgang mit hygienisch problematischen (Medizin-)Produkten Marc Thanheiser Fachgebiet Angewandte Infektionsund Krankenhaushygiene, Robert Koch-Institut, Berlin Hafnersee, 08.06.2017 1 Rechtliche Grundlagen
Umgang mit hygienisch problematischen (Medizin-)Produkten Marc Thanheiser Fachgebiet Angewandte Infektionsund Krankenhaushygiene, Robert Koch-Institut, Berlin Hafnersee, 08.06.2017 1 Rechtliche Grundlagen
Plasmasterilisation. 15. DGSV-Kongress, 3. bis 5. Oktober 2011 in Fulda
 Plasmasterilisation an der Schnittstelle Praxis/Zertifizierung/Recht 15. DGSV-Kongress, 3. bis 5. Oktober 2011 in Fulda Petra Geistberger Klinikum rechts der Isar der Technischen Universität München 4.
Plasmasterilisation an der Schnittstelle Praxis/Zertifizierung/Recht 15. DGSV-Kongress, 3. bis 5. Oktober 2011 in Fulda Petra Geistberger Klinikum rechts der Isar der Technischen Universität München 4.
Einteilung der Medizinprodukte nach RKI (Risikobewertung und Einstufung von Medizinprodukten vor der Aufbereitung)
 ÖGSV Fachkundelehrgang I 11 Einteilung der Medizinprodukte nach RKI (Risikobewertung und Einstufung von Medizinprodukten vor der Aufbereitung) M.T. Enko 2015 Inhalt 1 Ziel des Unterrichtes:... 3 2 Änderungen
ÖGSV Fachkundelehrgang I 11 Einteilung der Medizinprodukte nach RKI (Risikobewertung und Einstufung von Medizinprodukten vor der Aufbereitung) M.T. Enko 2015 Inhalt 1 Ziel des Unterrichtes:... 3 2 Änderungen
Bernd Vogler Fachauditor für hygienische Aufbereitung
 Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
Zusammenfassung der RKI Empfehlung E 4 a / Juli 2002
 Empfehlungen zur Minimierung des Risikos einer iatrogenen Übertragung von vcjk durch potentiell kontaminierte Medizinprodukte, insbesondere chirurgische Instrumente Zusammenfassung der RKI Empfehlung E
Empfehlungen zur Minimierung des Risikos einer iatrogenen Übertragung von vcjk durch potentiell kontaminierte Medizinprodukte, insbesondere chirurgische Instrumente Zusammenfassung der RKI Empfehlung E
1. Vorangestellt Gültigkeit Änderungshinweise... 2
 1/6 Inhaltsverzeichnis 1. Vorangestellt... 2 1.1 Gültigkeit... 2 1.2 Änderungshinweise... 2 1.3 Zweck 2 1.4 Risikobewertung und Einstufung... 3 1.5 Geltungsbereich... 3 1.6 Zuständigkeit... 3 1.7 Mitgeltende
1/6 Inhaltsverzeichnis 1. Vorangestellt... 2 1.1 Gültigkeit... 2 1.2 Änderungshinweise... 2 1.3 Zweck 2 1.4 Risikobewertung und Einstufung... 3 1.5 Geltungsbereich... 3 1.6 Zuständigkeit... 3 1.7 Mitgeltende
Medizinproduktebuch. Blatt 1. Geräte-Stammdaten Funktionsprüfung Geräteeinweisung... 4
 Medizinproduktebuch Nach 7 MPBetreibV für Medizinprodukte 1 Für das Gerät Inhalt Blatt 1. Geräte-Stammdaten... 2 2. Funktionsprüfung... 3 3. Geräteeinweisung... 4 3.1 Einweisung der vom Betreiber beauftragten
Medizinproduktebuch Nach 7 MPBetreibV für Medizinprodukte 1 Für das Gerät Inhalt Blatt 1. Geräte-Stammdaten... 2 2. Funktionsprüfung... 3 3. Geräteeinweisung... 4 3.1 Einweisung der vom Betreiber beauftragten
Aufbereitung von Medizinprodukten Die Sicht des Landes Nordrhein- Westfalen
 Die Sicht Nordrhein- Westfalen Ministerium für Fünfter Abschnitt Überwachung und Schutz vor Risiken 26 MPG Durchführung der Überwachung (1) 1 Betriebe und Einrichtungen mit Sitz in Deutschland, in denen
Die Sicht Nordrhein- Westfalen Ministerium für Fünfter Abschnitt Überwachung und Schutz vor Risiken 26 MPG Durchführung der Überwachung (1) 1 Betriebe und Einrichtungen mit Sitz in Deutschland, in denen
Die Kombination von Medizinprodukten. SystemCheck
 Die Kombination von Medizinprodukten SystemCheck Fachtagung der FKT 12.06.2008 Untertitel Die Prüfung und Bewertung von medizinischen elektrischen Systemen mit rechtssicherer Dokumentation zum Schutz von
Die Kombination von Medizinprodukten SystemCheck Fachtagung der FKT 12.06.2008 Untertitel Die Prüfung und Bewertung von medizinischen elektrischen Systemen mit rechtssicherer Dokumentation zum Schutz von
Umsetzung des Medizinprodukterechts
 Landesamt für Gesundheit und Soziales Abteilung Arbeitsschutz und technische Sicherheit Stofflicher Gefahrenschutz, Strahlenschutz, Verbraucherschutz in der Medizin Umsetzung des Medizinprodukterechts
Landesamt für Gesundheit und Soziales Abteilung Arbeitsschutz und technische Sicherheit Stofflicher Gefahrenschutz, Strahlenschutz, Verbraucherschutz in der Medizin Umsetzung des Medizinprodukterechts
Akkreditierungsumfang der Inspektionsstelle (EN ISO/IEC 17020:2012) HygCen Austria GmbH / (Ident.Nr.: 0196)
 HygCen Austria GmbH / (Ident.: 0196) Titel 1 2 3 21-010 21-011 21-055 2015-11 Hygiene Management-System in Wäschereien 2014-04 Hygiene Management-System - Aufbereitung von textilen OP-Materialien - Überprüfung
HygCen Austria GmbH / (Ident.: 0196) Titel 1 2 3 21-010 21-011 21-055 2015-11 Hygiene Management-System in Wäschereien 2014-04 Hygiene Management-System - Aufbereitung von textilen OP-Materialien - Überprüfung
Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Aufbereitung von Medizinprodukten
 Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Aufbereitung von Medizinprodukten Geltungsbereich: Die vorliegenden Speziellen Regeln legen Anforderungen fest an Zertifizierungsstellen
Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Aufbereitung von Medizinprodukten Geltungsbereich: Die vorliegenden Speziellen Regeln legen Anforderungen fest an Zertifizierungsstellen
Lagerungsschränke mit geregelten Umgebungsbedingungen für aufbereitete, thermolabile Endoskope (Trockenschrank) Validierung und Typprüfung
 Lagerungsschränke mit geregelten Umgebungsbedingungen für aufbereitete, thermolabile Endoskope (Trockenschrank) Validierung und Typprüfung Stefan Fehrmann, M. Feltgen, S. Werner HygCen Germany GmbH, Schwerin
Lagerungsschränke mit geregelten Umgebungsbedingungen für aufbereitete, thermolabile Endoskope (Trockenschrank) Validierung und Typprüfung Stefan Fehrmann, M. Feltgen, S. Werner HygCen Germany GmbH, Schwerin
Medizinprodukte - Aufbereitung in Deutschland - im 17. Jahr nach der Einführung des
 Medizinprodukte - Aufbereitung in Deutschland - im 17. Jahr nach der Einführung des MPG Beantwortete und offene Fragen Prof. Dr. M. Mielke, RKI Patientenschutz bei Medizinprodukten Verpflichtung der Migliedstaaten
Medizinprodukte - Aufbereitung in Deutschland - im 17. Jahr nach der Einführung des MPG Beantwortete und offene Fragen Prof. Dr. M. Mielke, RKI Patientenschutz bei Medizinprodukten Verpflichtung der Migliedstaaten
Vorschlag zur Umsetzung der Medizinprodukte-Betreiberverordnung für Geräte, die im häuslichen Bereich eingesetzt werden
 Vorschlag zur Umsetzung der Medizinprodukte-Betreiberverordnung für Geräte, die im häuslichen 2 Begriffsbestimmungen (2) Betreiber eines Medizinproduktes ist jede natürliche oder juristische Person, die
Vorschlag zur Umsetzung der Medizinprodukte-Betreiberverordnung für Geräte, die im häuslichen 2 Begriffsbestimmungen (2) Betreiber eines Medizinproduktes ist jede natürliche oder juristische Person, die
«Das Schönste am Problem ist die Lösung»
 «Das Schönste am Problem ist die Lösung» Sind mit den Fachkundelehrgängen h die Ausbildungsprobleme des Fachpersonals in MP- Aufbereitungsabteilungen und deren Betreiber gelöst? BG Klinik Bergmannstrost
«Das Schönste am Problem ist die Lösung» Sind mit den Fachkundelehrgängen h die Ausbildungsprobleme des Fachpersonals in MP- Aufbereitungsabteilungen und deren Betreiber gelöst? BG Klinik Bergmannstrost
Validierung hausinterner Aufbereitungsschritte bei Outsourcing
 Validierung hausinterner Aufbereitungsschritte bei Outsourcing Ulrike Prüfert-Freese Leiterin des Hygienelabors der MA 39 Folie 1 Validierung jener Teilprozesse der Aufbereitungsprozesse für Medizinprodukte
Validierung hausinterner Aufbereitungsschritte bei Outsourcing Ulrike Prüfert-Freese Leiterin des Hygienelabors der MA 39 Folie 1 Validierung jener Teilprozesse der Aufbereitungsprozesse für Medizinprodukte
Sachgemäße Wäschepflege nach RAL Deutsches Institut für Gütesicherung und Kennzeichnung e.v.
 Sachgemäße Wäschepflege nach RAL Deutsches Institut für Gütesicherung und Kennzeichnung e.v. Krankenhauswäsche RAL Gütezeichen RAL-GZ 992/2 GÜTEZEICHENTRÄGER: Gütegemeinschaft sachgemäße Wäschepflege e.v.
Sachgemäße Wäschepflege nach RAL Deutsches Institut für Gütesicherung und Kennzeichnung e.v. Krankenhauswäsche RAL Gütezeichen RAL-GZ 992/2 GÜTEZEICHENTRÄGER: Gütegemeinschaft sachgemäße Wäschepflege e.v.
Hygiene in der Praxis
 Hygiene in der Praxis Die praktische Umsetzung von Hygienemaßnahmen im Medizintechnikunternehmen Jan Wolter, Leiter Fachverband Medizintechnik SPECTARIS e.v. Grundlagen Empfehlungen der Kommission für
Hygiene in der Praxis Die praktische Umsetzung von Hygienemaßnahmen im Medizintechnikunternehmen Jan Wolter, Leiter Fachverband Medizintechnik SPECTARIS e.v. Grundlagen Empfehlungen der Kommission für
Praxisbegehung durch die Gewerbeaufsicht: Anforderungen und häufige Mängel
 Praxisbegehung durch die Gewerbeaufsicht: Anforderungen und häufige Mängel Dipl.-Ing. (FH) Frank Krestel Regierung von Schwaben-Gewerbeaufsichtsamt Morellstraße 30 d, 86159 Augsburg Telefon: 0821-327-2825
Praxisbegehung durch die Gewerbeaufsicht: Anforderungen und häufige Mängel Dipl.-Ing. (FH) Frank Krestel Regierung von Schwaben-Gewerbeaufsichtsamt Morellstraße 30 d, 86159 Augsburg Telefon: 0821-327-2825
Überwachung der Aufbereitung von Medizinprodukten im Land Brandenburg Themen. Der rechtliche Rahmen. Der rechtliche Rahmen. - Rechtlicher Rahmen
 Überwachung Aufbereitung von Medizinprodukten im Land Brandenburg Themen Rechtlicher Rahmen Schwerpunkte Überwachung Stand Überwachung 1 Gesetzliche Vorgaben bzw. Verbote zum Schutz von Patienten, Anwenn
Überwachung Aufbereitung von Medizinprodukten im Land Brandenburg Themen Rechtlicher Rahmen Schwerpunkte Überwachung Stand Überwachung 1 Gesetzliche Vorgaben bzw. Verbote zum Schutz von Patienten, Anwenn
ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN
 Zentrale Sterilgut-Versorgung, Geschäftsbereich Bau, Technik und Medizintechnik C 5 ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN Toni Zanette Leiter Zentrale Sterilgutversorgung C 5 Rechtliche Anforderungen
Zentrale Sterilgut-Versorgung, Geschäftsbereich Bau, Technik und Medizintechnik C 5 ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN Toni Zanette Leiter Zentrale Sterilgutversorgung C 5 Rechtliche Anforderungen
Unkritisch Semikritisch Kritisch: Grundlagen zur Aufbereitung und Klassifizierung von Instrumenten und Medizinprodukten
 Unkritisch Semikritisch Kritisch: Grundlagen zur Aufbereitung und Klassifizierung von Instrumenten und Medizinprodukten Workshop zum 3. Hygienetag der KVB Nürnberg Qualitätssicherung, Team Qualitätsmanagement/QZ/Hygiene
Unkritisch Semikritisch Kritisch: Grundlagen zur Aufbereitung und Klassifizierung von Instrumenten und Medizinprodukten Workshop zum 3. Hygienetag der KVB Nürnberg Qualitätssicherung, Team Qualitätsmanagement/QZ/Hygiene
Hygienebeauftragte Mitarbeiterinnen und Mitarbeiter in der Arztpraxis (Seminar )
 Hygienebeauftragte Mitarbeiterinnen und Mitarbeiter in der Arztpraxis (Seminar 151301) Allgemeine Faktoren: Teilnehmer: Module: Grundlage: 10 bis maximal 20 Teilnehmer Voraussetzung: Abschluss Arzthelferin
Hygienebeauftragte Mitarbeiterinnen und Mitarbeiter in der Arztpraxis (Seminar 151301) Allgemeine Faktoren: Teilnehmer: Module: Grundlage: 10 bis maximal 20 Teilnehmer Voraussetzung: Abschluss Arzthelferin
Fit für die Praxisbegehung. * Ein Vortrag von Anne Enbergs * Praxis Zentderma * Mönchengladbach
 Fit für die Praxisbegehung * Ein Vortrag von Anne Enbergs * Praxis Zentderma * Mönchengladbach Welche Behörden können prüfen ü Gesundheitsamt ü Berufsgenossenschaft / Amt für Arbeitsschutz ü Bezirksregierung
Fit für die Praxisbegehung * Ein Vortrag von Anne Enbergs * Praxis Zentderma * Mönchengladbach Welche Behörden können prüfen ü Gesundheitsamt ü Berufsgenossenschaft / Amt für Arbeitsschutz ü Bezirksregierung
Das Thema Desinfektion für die Überwachungsbehörden. Vorschriften. Vorschriften. Landesamt für Gesundheit und Soziales.
 Landesamt für Gesundheit und Soziales Abteilung Gesundheit Krankenhaushygiene, Allgemeine Hygiene Das Thema Desinfektion für die Überwachungsbehörden Michael Biertümpel Krankenhaushygiene/Allgemeine Hygiene
Landesamt für Gesundheit und Soziales Abteilung Gesundheit Krankenhaushygiene, Allgemeine Hygiene Das Thema Desinfektion für die Überwachungsbehörden Michael Biertümpel Krankenhaushygiene/Allgemeine Hygiene
Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen. Referent: Dipl.-Ing. Burkhard Schulze
 Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen Referent: Dipl.-Ing. Burkhard Schulze Definition: Aufbereitung Reinigung, Desinfektion und Sterilisation von bestimmungsgemäß
Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen Referent: Dipl.-Ing. Burkhard Schulze Definition: Aufbereitung Reinigung, Desinfektion und Sterilisation von bestimmungsgemäß
Praktische Umsetzung in der Handhabung von Medizinprodukten
 Praktische Umsetzung in der Handhabung von Medizinprodukten Andreas Clarin Hygieneakademie Ruhr, Essen Definition Medizinprodukte ( 3 MPG) Medizinprodukte sind alle Instrumente, Apparate, Vorrichtungen,
Praktische Umsetzung in der Handhabung von Medizinprodukten Andreas Clarin Hygieneakademie Ruhr, Essen Definition Medizinprodukte ( 3 MPG) Medizinprodukte sind alle Instrumente, Apparate, Vorrichtungen,
Inspektionsstelle Typ A
 Inspektionsstelle Typ A Rechtsperson HygCen Austria GmbH Werksgelände 28, 5500 Bischofshofen Internet www.hygcen.at Ident 0196 Standort HygCen Austria GmbH Werksgelände 28, 5500 Bischofshofen Datum der
Inspektionsstelle Typ A Rechtsperson HygCen Austria GmbH Werksgelände 28, 5500 Bischofshofen Internet www.hygcen.at Ident 0196 Standort HygCen Austria GmbH Werksgelände 28, 5500 Bischofshofen Datum der
Dokumentation in der MP- Aufbereitung mit dem Schwerpunkt Endoskopie Vortrag beim AMAH
 Dokumentation in der MP- Aufbereitung mit dem Schwerpunkt Endoskopie Vortrag beim AMAH Olympus Deutschland Medical Systems Jesco Danylow, Produktmanagement Hannover, 11. Juni 2016 Inhalt 1. Einführung
Dokumentation in der MP- Aufbereitung mit dem Schwerpunkt Endoskopie Vortrag beim AMAH Olympus Deutschland Medical Systems Jesco Danylow, Produktmanagement Hannover, 11. Juni 2016 Inhalt 1. Einführung
Aktualisierung der Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten (KRINKO/BfArM, 2001)
 Aktualisierung der Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten (KRINKO/BfArM, 2001) Hintergrund und Sachstand M. Mielke Robert Koch-Institut Sachgerechte Aufbereitung von Medizinprodukten
Aktualisierung der Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten (KRINKO/BfArM, 2001) Hintergrund und Sachstand M. Mielke Robert Koch-Institut Sachgerechte Aufbereitung von Medizinprodukten
Aktualisierte ÖGHMP Hygiene-Richtlinie für Wäschereien Wäsche in Gesundheitseinrichtungen
 Aktualisierte ÖGHMP Hygiene-Richtlinie für Wäschereien Wäsche in Gesundheitseinrichtungen G. Wewalka Institut für medizinische Mikrobiologie und Hygiene Wien Basis für die aktualisierte Richtlinie Hygiene-Richtlinie
Aktualisierte ÖGHMP Hygiene-Richtlinie für Wäschereien Wäsche in Gesundheitseinrichtungen G. Wewalka Institut für medizinische Mikrobiologie und Hygiene Wien Basis für die aktualisierte Richtlinie Hygiene-Richtlinie
Hygiene bei transvaginalen und transrektalen Ultraschallsonden
 Hygiene bei transvaginalen und transrektalen Ultraschallsonden Marc Thanheiser Fachgebiet Angewandte Infektionsund Krankenhaushygiene, Robert Koch-Institut, Berlin Hafnersee, 09.06.2017 1 Hygienemaßstäbe
Hygiene bei transvaginalen und transrektalen Ultraschallsonden Marc Thanheiser Fachgebiet Angewandte Infektionsund Krankenhaushygiene, Robert Koch-Institut, Berlin Hafnersee, 09.06.2017 1 Hygienemaßstäbe
Projekt Hygienische Aufbereitung flexibler Endoskope
 Projekt Hygienische Aufbereitung Gliederung Einleitung und Darstellung des Projekts Vorgefundene Mängel Schlussfolgerungen Folie 1 Gesetzliche Grundlagen RKI: Anforderungen an die Hygiene bei der Aufbereitung
Projekt Hygienische Aufbereitung Gliederung Einleitung und Darstellung des Projekts Vorgefundene Mängel Schlussfolgerungen Folie 1 Gesetzliche Grundlagen RKI: Anforderungen an die Hygiene bei der Aufbereitung
Akkreditierungsumfang der Inspektionsstelle (EN ISO/IEC 17020:2012) W.H.U. GmbH / (Ident.Nr.: 0289)
 1 2 3 4 5 6 ANSI/AAMI ST 55 BGBl. II 262/2008 BGBl. II 321/2012 Bundesgesundheitsblatt 2012-55: 1244-1310 DIN 10510 DIN 10512 2010-12 Table-top steam sterilizers Sterilisatoren 2008-07 Verordnung des Bundesministers
1 2 3 4 5 6 ANSI/AAMI ST 55 BGBl. II 262/2008 BGBl. II 321/2012 Bundesgesundheitsblatt 2012-55: 1244-1310 DIN 10510 DIN 10512 2010-12 Table-top steam sterilizers Sterilisatoren 2008-07 Verordnung des Bundesministers
Aufbereitung von flexiblen Endoskopen Patientensicher und Gesetzeskonform
 Aufbereitung von flexiblen Endoskopen Patientensicher und Gesetzeskonform Referent: Dr. Michael Sturm Prüfstellenleiter und Geschäftsführer Hygienezentrum Dr. Sturm GmbH Eumigweg 7 2351 Wiener Neudorf
Aufbereitung von flexiblen Endoskopen Patientensicher und Gesetzeskonform Referent: Dr. Michael Sturm Prüfstellenleiter und Geschäftsführer Hygienezentrum Dr. Sturm GmbH Eumigweg 7 2351 Wiener Neudorf
Anforderungen an die hygienische Aufbereitung von Medizinprodukten in NRW
 Anforderungen an die hygienische Aufbereitung von Medizinprodukten in NRW Dr. med. univ. Sebastian Werner 1,2 1 HygCen Germany GmbH, Schwerin / Bochum 2 Abteilung für Hygiene, Sozial- und Umweltmedizin,
Anforderungen an die hygienische Aufbereitung von Medizinprodukten in NRW Dr. med. univ. Sebastian Werner 1,2 1 HygCen Germany GmbH, Schwerin / Bochum 2 Abteilung für Hygiene, Sozial- und Umweltmedizin,
Umsetzung des Medizinprodukterechts
 Landesamt für Gesundheit und Soziales Abteilung Arbeitsschutz und technische Sicherheit Stofflicher Gefahrenschutz, Strahlenschutz, Verbraucherschutz in der Medizin Umsetzung des Medizinprodukterechts
Landesamt für Gesundheit und Soziales Abteilung Arbeitsschutz und technische Sicherheit Stofflicher Gefahrenschutz, Strahlenschutz, Verbraucherschutz in der Medizin Umsetzung des Medizinprodukterechts
IMC Systems GmbH. Instrumentenaufbereitung CHECKLISTE. Rechtsgrundlagen. Zahnarztpraxis. Infektionsschutz - Gesetz. Medizinprodukte Gesetz.
 IMC Systems GmbH CHECKLISTE zur Sicherung und Weiterentwicklung von Qualität und Leistung in der Zahnheilkunde gemäß der aktuellen Gesetzte, Verordnungen, Normen, Richtlinien und Empfehlungen Rechtsgrundlagen
IMC Systems GmbH CHECKLISTE zur Sicherung und Weiterentwicklung von Qualität und Leistung in der Zahnheilkunde gemäß der aktuellen Gesetzte, Verordnungen, Normen, Richtlinien und Empfehlungen Rechtsgrundlagen
Die zertifizierte Wäscherei
 Die zertifizierte Wäscherei Gewerbliche Schulwäscherei der Fachakademie für Landwirtschaft/Fachrichtung Ernährung und Versorgungsmanagement Nebengebäude Die Fachakademie in Triesdorf ist die einzige Fachschule
Die zertifizierte Wäscherei Gewerbliche Schulwäscherei der Fachakademie für Landwirtschaft/Fachrichtung Ernährung und Versorgungsmanagement Nebengebäude Die Fachakademie in Triesdorf ist die einzige Fachschule
Inhalt des Vortrags. Novellierung des Infektionsschutzgesetzes (IfSG) Hygieneverordnung der Länder. Hygiene im Umgang mit multiresistenten Erregern
 Gesundheitsamt Hamburg-Nord Dr. Maren Boyens Herr Max Mustermann, Hamburg Marketing GmbH, 25. Juli 2005 Neue Hygiene-Richtlinien neue Vorschriften mit multiresistenten 15. November 2012 1 2 Novellierung
Gesundheitsamt Hamburg-Nord Dr. Maren Boyens Herr Max Mustermann, Hamburg Marketing GmbH, 25. Juli 2005 Neue Hygiene-Richtlinien neue Vorschriften mit multiresistenten 15. November 2012 1 2 Novellierung
HYGIENISCHE AUFBEREITUNG
 HYGIENISCHE AUFBEREITUNG VON MEDIZINPRODUKTEN IN EINRICHTUNGEN DER PFLEGE Exemplarisch: Sauerstoffkonzentrator, Patientenlifter, Wechseldrucksystem, Absauggerät Georg Scheitzach Sanitätshaus Wöllzenmüller
HYGIENISCHE AUFBEREITUNG VON MEDIZINPRODUKTEN IN EINRICHTUNGEN DER PFLEGE Exemplarisch: Sauerstoffkonzentrator, Patientenlifter, Wechseldrucksystem, Absauggerät Georg Scheitzach Sanitätshaus Wöllzenmüller
Herzlich Willkommen. Anja Demnick Dozentin & Referentin für» Medizinprodukte Aufbereitung
 Herzlich Willkommen Anja Demnick Dozentin & Referentin für» Medizinprodukte Aufbereitung «info@anjademnick.com www.anjademnick.com Antworten aus der Umfrage: Glauben Sie, dass es Schwierigkeiten bei der
Herzlich Willkommen Anja Demnick Dozentin & Referentin für» Medizinprodukte Aufbereitung «info@anjademnick.com www.anjademnick.com Antworten aus der Umfrage: Glauben Sie, dass es Schwierigkeiten bei der
Erstellung einer Anleitung für die Aufbereitung von Ultraschallsonden mittels Wischdesinfektion
 Erstellung einer Anleitung für die Aufbereitung von Ultraschallsonden mittels Wischdesinfektion DGKH-Kongress 2016 Mehr wissen. Weiter denken. Ultraschallsonden Einsatz in vielen unterschiedlichen medizinischen
Erstellung einer Anleitung für die Aufbereitung von Ultraschallsonden mittels Wischdesinfektion DGKH-Kongress 2016 Mehr wissen. Weiter denken. Ultraschallsonden Einsatz in vielen unterschiedlichen medizinischen
Die Hygieneverordnung der ÖÄK. Michael Gehrer
 Die Hygieneverordnung der ÖÄK Michael Gehrer Zweifelsohne: ein Schritt in die richtige Richtung!!! Hygieneverordnung der ÖÄK Sie thematisiert erstmals die Verantwortung, die Ärzte auch im niedergelassenen
Die Hygieneverordnung der ÖÄK Michael Gehrer Zweifelsohne: ein Schritt in die richtige Richtung!!! Hygieneverordnung der ÖÄK Sie thematisiert erstmals die Verantwortung, die Ärzte auch im niedergelassenen
Medizinproduktebuch. nach 12 MP BetreibV für Medizinprodukte. Inhalt. 1 Geräte-Stammdaten Funktionsprüfung Geräteeinweisung...
 1 Medizinproduktebuch nach 12 MP BetreibV für Medizinprodukte Inhalt Blatt 1 Geräte-Stammdaten... 2 2 Funktionsprüfung... 3 3 Geräteeinweisung... 4 4 Sicherheitstechnische Kontrollen... 6 5 Messtechnische
1 Medizinproduktebuch nach 12 MP BetreibV für Medizinprodukte Inhalt Blatt 1 Geräte-Stammdaten... 2 2 Funktionsprüfung... 3 3 Geräteeinweisung... 4 4 Sicherheitstechnische Kontrollen... 6 5 Messtechnische
Probleminstrumente Alle kritisch B, oder was?
 Professionelle Aufbereitung von Medizinprodukten Probleminstrumente Alle kritisch B, oder was? Victoria Kalinitschenko Universitätsklinikum FreiburgLeitung ZSVA, QMB Karin Gehrmann Aesculap AG Tuttlingen
Professionelle Aufbereitung von Medizinprodukten Probleminstrumente Alle kritisch B, oder was? Victoria Kalinitschenko Universitätsklinikum FreiburgLeitung ZSVA, QMB Karin Gehrmann Aesculap AG Tuttlingen
Aufbereitung von Medizinprodukten- Inspektionsergebnisse im Freistaat Sachsen
 Aufbereitung von Medizinprodukten- Inspektionsergebnisse im Freistaat Sachsen Andreas Modes Landesdirektion Dresden Arbeitsschutz- Außenstelle Chemnitz Lothar Streit Straße 24 08056 Zwickau Tel.: 0375/
Aufbereitung von Medizinprodukten- Inspektionsergebnisse im Freistaat Sachsen Andreas Modes Landesdirektion Dresden Arbeitsschutz- Außenstelle Chemnitz Lothar Streit Straße 24 08056 Zwickau Tel.: 0375/
Podiumsdiskussion. Dr. Früh Control GmbH DGSV-Kongress
 Podiumsdiskussion Dr. Früh Control GmbH DGSV-Kongress 10-09 1 Generelle Vorgaben für Medizinprodukte Medizinprodukte-Gesetz 14: Medizinprodukte dürfen nicht betrieben und angewendet werden, wenn sie Mängel
Podiumsdiskussion Dr. Früh Control GmbH DGSV-Kongress 10-09 1 Generelle Vorgaben für Medizinprodukte Medizinprodukte-Gesetz 14: Medizinprodukte dürfen nicht betrieben und angewendet werden, wenn sie Mängel
Bernd Vogler Fachauditor für hygienische Aufbereitung
 Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
1. Vorangestellt Gültigkeit Änderungshinweise... 2
 1/7 Inhaltsverzeichnis 1. Vorangestellt... 2 1.1 Gültigkeit... 2 1.2 Änderungshinweise... 2 1.3 Zweck 2 1.4 Risikobewertung und Einstufung... 2 1.5 Geltungsbereich... 3 1.6 Zuständigkeit... 3 1.7 Mitgeltende
1/7 Inhaltsverzeichnis 1. Vorangestellt... 2 1.1 Gültigkeit... 2 1.2 Änderungshinweise... 2 1.3 Zweck 2 1.4 Risikobewertung und Einstufung... 2 1.5 Geltungsbereich... 3 1.6 Zuständigkeit... 3 1.7 Mitgeltende
Erfahrungen der. DQS GmbH. bei der Zertifizierung von Medizinprodukteherstellern
 Erfahrungen der DQS GmbH bei der Zertifizierung von Medizinprodukteherstellern 2004-11-24, Seite 1 Normensituation Medizinprodukte DIN EN ISO 9001:94 DIN EN ISO 9001:2000 DIN EN 46001/2:1996 DIN EN ISO
Erfahrungen der DQS GmbH bei der Zertifizierung von Medizinprodukteherstellern 2004-11-24, Seite 1 Normensituation Medizinprodukte DIN EN ISO 9001:94 DIN EN ISO 9001:2000 DIN EN 46001/2:1996 DIN EN ISO
EN ISO konforme Gebrauchsanweisung
 EN ISO 17664 konforme Gebrauchsanweisung Monika Feltgen Abteilungsleitung Medizinprodukteprüfung Akkreditiertes Prüflabor HygCen Germany GmbH, Schwerin Laboratorien & Inspektionsstellen Akkreditiert gemäß
EN ISO 17664 konforme Gebrauchsanweisung Monika Feltgen Abteilungsleitung Medizinprodukteprüfung Akkreditiertes Prüflabor HygCen Germany GmbH, Schwerin Laboratorien & Inspektionsstellen Akkreditiert gemäß
Bernd Vogler Fachauditor für hygienische Aufbereitung
 Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
Bernd Vogler Fachauditor für hygienische Aufbereitung Staatliches Gewerbeaufsichtsamt Oldenburg Theodor-Tantzen-Platz 8 26122 Oldenburg Tel. : 04 41 / 799-2535 Fax : 04 41 / 799-2700 / 2017 Bernd.Vogler@gaa-ol.niedersachsen.de
Novellierung IFSG 2011
 Novellierung IFSG 2011 23 (1) Beim Robert Koch-Institut wird eine Kommission für Krankenhaushygiene und Infektionsprävention eingerichtet. Die Kommission erstellt Empfehlungen zur Prävention nosokomialer
Novellierung IFSG 2011 23 (1) Beim Robert Koch-Institut wird eine Kommission für Krankenhaushygiene und Infektionsprävention eingerichtet. Die Kommission erstellt Empfehlungen zur Prävention nosokomialer
Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung
 Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung Dipl.-Kfm. Matthias Klar, IfB Hagenow Tel. 0160 96420022 1 4 Absatz 1 MP BetreibV
Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung Dipl.-Kfm. Matthias Klar, IfB Hagenow Tel. 0160 96420022 1 4 Absatz 1 MP BetreibV
Ringveranstaltung Aufbereitung von Medizinprodukten
 Ringveranstaltung Aufbereitung von Medizinprodukten 21.6.17 Rechtliche und praktische An- und Herausforderungen bei der Aufbereitung flexibler Endoskope und endoskopischem Zusatzinstrumentariums Dr. med.
Ringveranstaltung Aufbereitung von Medizinprodukten 21.6.17 Rechtliche und praktische An- und Herausforderungen bei der Aufbereitung flexibler Endoskope und endoskopischem Zusatzinstrumentariums Dr. med.
Medizinproduktebuch. nach 12 MP BetreibV für Medizinprodukte. Inhalt. 1 Geräte-Stammdaten Funktionsprüfung Geräteeinweisung...
 1 Medizinproduktebuch nach 12 MP BetreibV für Medizinprodukte Inhalt Blatt 1 Geräte-Stammdaten... 2 2 Funktionsprüfung... 3 3 Geräteeinweisung... 4 4 Softwareupdates... 6 5 Sicherheitstechnische Kontrollen...
1 Medizinproduktebuch nach 12 MP BetreibV für Medizinprodukte Inhalt Blatt 1 Geräte-Stammdaten... 2 2 Funktionsprüfung... 3 3 Geräteeinweisung... 4 4 Softwareupdates... 6 5 Sicherheitstechnische Kontrollen...
ZSVA: Zertifizierung + Barcode Klinikum Heidenheim
 ZSVA: Zertifizierung + Barcode Klinikum Heidenheim Jürgen Bierlein Ltg. ZSVA Wir stellen uns Vor 11.1 VZ-Stellen auf 12 Mitarbeiter Ca. 45.000 StE im Jahr Betriebszeit von 6.00-21.00h Rufbereitschaft am
ZSVA: Zertifizierung + Barcode Klinikum Heidenheim Jürgen Bierlein Ltg. ZSVA Wir stellen uns Vor 11.1 VZ-Stellen auf 12 Mitarbeiter Ca. 45.000 StE im Jahr Betriebszeit von 6.00-21.00h Rufbereitschaft am
Anlage zur Akkreditierungsurkunde D-PL nach DIN EN ISO/IEC 17025: und Richtlinie 93/42/EWG 2 und 90/385/EWG 3
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-13125-01-02 nach DIN EN ISO/IEC 17025:2005 1 und Richtlinie 93/42/EWG 2 und 90/385/EWG 3 Gültigkeitsdauer: 30.01.2017 bis 09.09.2020
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-13125-01-02 nach DIN EN ISO/IEC 17025:2005 1 und Richtlinie 93/42/EWG 2 und 90/385/EWG 3 Gültigkeitsdauer: 30.01.2017 bis 09.09.2020
Hygienestraße. Die neue Qualität bei der Reinigung von Hilfsmitteln und Medizinprodukten
 Hygienestraße Die neue Qualität bei der Reinigung von Hilfsmitteln und Medizinprodukten Herausforderung Krankenhausinfektion Reinigung von Hilfsmitteln und Medizinprodukten Krankenhausinfektionen bedeuten
Hygienestraße Die neue Qualität bei der Reinigung von Hilfsmitteln und Medizinprodukten Herausforderung Krankenhausinfektion Reinigung von Hilfsmitteln und Medizinprodukten Krankenhausinfektionen bedeuten
Medizintechnologie.de. Hygiene von Medizinprodukten. Hygiene, Anforderungen und Umsetzungen
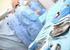 Medizintechnologie.de Hygiene von Medizinprodukten Jährlich infizieren sich circa 600.000 Patienten im Krankenhaus mit einer Nosokomialinfektion. 15.000 davon sterben. Ein hohes Lebensalter, eine vorhandene
Medizintechnologie.de Hygiene von Medizinprodukten Jährlich infizieren sich circa 600.000 Patienten im Krankenhaus mit einer Nosokomialinfektion. 15.000 davon sterben. Ein hohes Lebensalter, eine vorhandene
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten
 Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten über die Verlängerung der Anerkennung der/s Universitätsklinikum Bonn AöR Institut für Hygiene und öffentliche Gesundheit
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten über die Verlängerung der Anerkennung der/s Universitätsklinikum Bonn AöR Institut für Hygiene und öffentliche Gesundheit
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Hygienemanagement. Stand der Revision:
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 04.05.2010 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 04.05.2010 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
8. Hygieneforum Osthessen "Hygiene in der Zahnarztpraxis"
 8. Hygieneforum Osthessen "Hygiene in der Zahnarztpraxis" Aufbereitung von Medizinprodukten in der Zahnarztpraxis Überwachung durch das Regierungspräsidiums Kassel Dipl. -Ing. (FH) Ilker Büyükok, MHBA
8. Hygieneforum Osthessen "Hygiene in der Zahnarztpraxis" Aufbereitung von Medizinprodukten in der Zahnarztpraxis Überwachung durch das Regierungspräsidiums Kassel Dipl. -Ing. (FH) Ilker Büyükok, MHBA
Checkliste für Hygienebegehungen von Zahnarztpraxen. Kommentar der Landeszahnärztekammer Hessen
 Kommentar der Landeszahnärztekammer Hessen Dr. Andreas Dehler Referent für Praxisführung der LZKH Rhonestraße 4 60528 Frankfurt am Main Telefon 069 427275-0 www.lzkh.de 28.04.2016 28.04.2016 Seite 1 Arbeitsgruppe
Kommentar der Landeszahnärztekammer Hessen Dr. Andreas Dehler Referent für Praxisführung der LZKH Rhonestraße 4 60528 Frankfurt am Main Telefon 069 427275-0 www.lzkh.de 28.04.2016 28.04.2016 Seite 1 Arbeitsgruppe
nach unseren Unterlagen haben wir Ihre Einrichtung mit dem o.g. Klinikbetten beliefert.
 An betroffene Betreiber der Krankenhausbetten Seta in Spezialausführung maschinell waschbar 09.07.2014 bb/ent 05221 / 185-0 Dringende Sicherheitsinformation Stiegelmeyer- Krankenhausbett Seta in Spezialausführung:
An betroffene Betreiber der Krankenhausbetten Seta in Spezialausführung maschinell waschbar 09.07.2014 bb/ent 05221 / 185-0 Dringende Sicherheitsinformation Stiegelmeyer- Krankenhausbett Seta in Spezialausführung:
Epicare. Epicondylitis-Spange
 Epicare Epicondylitis-Spange - PRODUKTINFORMATION -GEBRAUCHSANWEISUNG- Sehr geehrte Kunden, Dezember 2015 wir danken Ihnen für Ihr Vertrauen in ein Produkt von inocare. Wir gratulieren Ihnen zu Ihrer Entscheidung.
Epicare Epicondylitis-Spange - PRODUKTINFORMATION -GEBRAUCHSANWEISUNG- Sehr geehrte Kunden, Dezember 2015 wir danken Ihnen für Ihr Vertrauen in ein Produkt von inocare. Wir gratulieren Ihnen zu Ihrer Entscheidung.
ÖNORM FprEN ISO 17664:2017. Vom Medizinprodukt-Hersteller bereitzustellende Informationen für die Aufbereitung von Medizinprodukten
 ÖNORM FprEN ISO 17664:2017 Vom Medizinprodukt-Hersteller bereitzustellende Informationen für die Aufbereitung von Medizinprodukten ÖGSV-Fachtagung 2017 EUROPÄISCHE NORM EUROPEAN STANDARD NORME EUROPÉENNE
ÖNORM FprEN ISO 17664:2017 Vom Medizinprodukt-Hersteller bereitzustellende Informationen für die Aufbereitung von Medizinprodukten ÖGSV-Fachtagung 2017 EUROPÄISCHE NORM EUROPEAN STANDARD NORME EUROPÉENNE
Validierung von Aufbereitungsprozessen für flexible Endoskope
 für flexible Endoskope Holger Zimenga Vortrag auf dem DEGEA Endoskopie-Zirkel Die Zukunft der Endoskopaufbereitung-praxisorientiert und sicher am 10. Dezember 2012 im St.Josefs-Krankenhaus, Freiburg Mehr
für flexible Endoskope Holger Zimenga Vortrag auf dem DEGEA Endoskopie-Zirkel Die Zukunft der Endoskopaufbereitung-praxisorientiert und sicher am 10. Dezember 2012 im St.Josefs-Krankenhaus, Freiburg Mehr
MPBetreibV - ein Jahr nach der Novellierung
 17.05.2018 MPBetreibV - ein Jahr nach der Novellierung Markus Wortmann Helios Kliniken Die Einzelthemen 1 Anwendungsbereich 3 Betreiberpflichten (inkl. 12 Medizinproduktebuch) 4 Einweisungen 6 MPSB 7 Instandhaltungen
17.05.2018 MPBetreibV - ein Jahr nach der Novellierung Markus Wortmann Helios Kliniken Die Einzelthemen 1 Anwendungsbereich 3 Betreiberpflichten (inkl. 12 Medizinproduktebuch) 4 Einweisungen 6 MPSB 7 Instandhaltungen
Vertragliche Regelung der Aufbereitung für Dritte. Maik Roitsch Leiter ZSVA / AEMP
 Vertragliche Regelung der Aufbereitung für Dritte Maik Roitsch Leiter ZSVA / AEMP Die ZSVA der Schlosspark-Klinik Maschinenpark 4 RDG 1 RDG ausschließlich Augeninstrumente 4 Packplätze 1 Packplatz mit
Vertragliche Regelung der Aufbereitung für Dritte Maik Roitsch Leiter ZSVA / AEMP Die ZSVA der Schlosspark-Klinik Maschinenpark 4 RDG 1 RDG ausschließlich Augeninstrumente 4 Packplätze 1 Packplatz mit
Sterilgutversorgung Qualität durch Kompetenz
 Sterilgutversorgung Qualität durch Kompetenz Eine Dienstleistung der Immanuel Diakonie 7. Kommissionierung und Bereitstellung Nach definierten Fahrplänen werden die Sterilgüter von bewährten externen Transportdienstleistern,
Sterilgutversorgung Qualität durch Kompetenz Eine Dienstleistung der Immanuel Diakonie 7. Kommissionierung und Bereitstellung Nach definierten Fahrplänen werden die Sterilgüter von bewährten externen Transportdienstleistern,
Bewohnerwäsche aus Pflegeeinrichtungen
 Sachgemäße Wäschepflege nach RAL Deutsches Institut für Gütesicherung und Kennzeichnung e.v. Bewohnerwäsche RAL Gütezeichen GÜTEZEICHENTRÄGER: Gütegemeinschaft sachgemäße Wäschepflege e.v. PRÜFINSTITUT:
Sachgemäße Wäschepflege nach RAL Deutsches Institut für Gütesicherung und Kennzeichnung e.v. Bewohnerwäsche RAL Gütezeichen GÜTEZEICHENTRÄGER: Gütegemeinschaft sachgemäße Wäschepflege e.v. PRÜFINSTITUT:
W&H Schweiz. Geschäftsführung W&H Schweiz. Instrumentenaufbereitung Hygieneschulung. Seite 1
 W&H Schweiz Dany Badstuber Geschäftsführung W&H Schweiz Instrumentenaufbereitung Hygieneschulung > Sterilisation gemäß Referenznorm EN13060: Zyklus/Ladungstypen > Erste und wiederkehrende Validierung von
W&H Schweiz Dany Badstuber Geschäftsführung W&H Schweiz Instrumentenaufbereitung Hygieneschulung > Sterilisation gemäß Referenznorm EN13060: Zyklus/Ladungstypen > Erste und wiederkehrende Validierung von
MRSA. Umgang mit MRSA im Einsatzdienst. Desinfektoren Feuerwehr Essen
 MRSA Umgang mit MRSA im Einsatzdienst J. Spors Lehranstalt für f Desinfektorinnen und Desinfektoren Feuerwehr Essen Staphylococcus aureus grammpositives, kugelförmiges Bakterium ist relativ lange überlebensfähig
MRSA Umgang mit MRSA im Einsatzdienst J. Spors Lehranstalt für f Desinfektorinnen und Desinfektoren Feuerwehr Essen Staphylococcus aureus grammpositives, kugelförmiges Bakterium ist relativ lange überlebensfähig
Internistische Thorakoskopie Anmerkungen eines Krankenhaushygienikers
 Internistische Thorakoskopie Anmerkungen eines Krankenhaushygienikers h ik Dr. Silvia Fanghänel Praxis für Hygienemanagement Halle/S. Krankenhaushygienikerin Diakoniekrankenhaus Halle/S. Grundsätzliche
Internistische Thorakoskopie Anmerkungen eines Krankenhaushygienikers h ik Dr. Silvia Fanghänel Praxis für Hygienemanagement Halle/S. Krankenhaushygienikerin Diakoniekrankenhaus Halle/S. Grundsätzliche
Damit Hygienesicherheit nicht vor der persönlichen Kleidung von Pflegeheimbewohnern haltmacht
 P R E S S E I N F O R M A T I O N Damit Hygienesicherheit nicht vor der persönlichen Kleidung von Pflegeheimbewohnern haltmacht RAL-Gütezeichen 992/4 für Bewohnerwäsche aus Pflegeeinrichtungen 13.05.2013
P R E S S E I N F O R M A T I O N Damit Hygienesicherheit nicht vor der persönlichen Kleidung von Pflegeheimbewohnern haltmacht RAL-Gütezeichen 992/4 für Bewohnerwäsche aus Pflegeeinrichtungen 13.05.2013
Stacksche Fingerschiene. Stacksche Fingerschiene Für Knopflochfinger
 Stacksche Fingerschiene Fingersplint Stacksche Fingerschiene Für Knopflochfinger Fingersplint - P R O D U K T I N F O R M A T I O N - G E B R A U C H S A N W E I S U N G - Januar 2015 Sehr geehrte Kunden,
Stacksche Fingerschiene Fingersplint Stacksche Fingerschiene Für Knopflochfinger Fingersplint - P R O D U K T I N F O R M A T I O N - G E B R A U C H S A N W E I S U N G - Januar 2015 Sehr geehrte Kunden,
ÖGSV Fachtagung 2013 Thea Enko
 ÖGSV Fachtagung 2013 Thea Enko Leitlinie zur Auswahl von aufbereitbaren Medizinprodukten Ziel: Beschaffung optimieren Fehlkäufe vermeiden Hilfestellung bei der Beschaffung von aufbereitbaren Medizinprodukten
ÖGSV Fachtagung 2013 Thea Enko Leitlinie zur Auswahl von aufbereitbaren Medizinprodukten Ziel: Beschaffung optimieren Fehlkäufe vermeiden Hilfestellung bei der Beschaffung von aufbereitbaren Medizinprodukten
Umgang mit unsteril angelieferten Implantaten
 Kreiskrankenhaus Erding mit Klinik Dorfen Akademisches Lehrkrankenhaus Technische Universität München Umgang mit unsteril angelieferten Implantaten Birgit Wagener 03. März 2011 Gliederung 1. Vorstellung
Kreiskrankenhaus Erding mit Klinik Dorfen Akademisches Lehrkrankenhaus Technische Universität München Umgang mit unsteril angelieferten Implantaten Birgit Wagener 03. März 2011 Gliederung 1. Vorstellung
