Erfahrungsbericht zur Umsetzung der Rili-BÄK aus der Sicht der Überwachungsbehörde. Fortbildungsveranstaltung der Firma Bio-Rad Laboratories GmbH
|
|
|
- Gudrun Minna Geiger
- vor 7 Jahren
- Abrufe
Transkript
1 Erfahrungsbericht zur Umsetzung der Rili-BÄK aus der Sicht der Überwachungsbehörde Fortbildungsveranstaltung der Firma Bio-Rad Laboratories GmbH 11. September 2013 Mainz
2 Was gibt es neues seit der letzten Fortbildung! 1. Bundesärztekammer (BÄK) - Rili-BÄK - Übergangsregelungen, Inkrafttreten - Referenzinstitutionen - FAQ - Ausblick 2. Gesetze - Medizinprodukte Betreiberverordnung (MPBetreibV) 3. Im Landesamt 4. Überwachungsdaten des LME aus dem Jahr 2012
3 Bundesärztekammer Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen Gemäß Beschluss des Vorstands der Bundesärztekammer vom , veröffentlicht im Deutschen Ärzteblatt, Jg. 105, Heft 7, 15. Februar 2008, Seite A zuletzt geändert/ergänzt durch Beschluss des Vorstands der Bundesärztekammer vom , veröffentlicht im Deutschen Ärzteblatt Jg.110, Heft 12, , Seite A Die zur Zeit aktuelle Richtlinie (Rili-BÄK) besteht aus 77 Seiten.
4 Rili-BÄK 2008 Die Richtlinie regelt die Qualitätssicherung laboratoriumsmedizinischer Untersuchungen in der Heilkunde. Die im Teil A der Richtlinie beschriebenen grundlegenden Anforderungen sind für alle laboratoriumsmedizinischen Anforderungen gültig. Spezifische Anforderungen, soweit für letztere ein spezieller Teil B formuliert ist. B1 Quantitative laboratoriumsmedizinische Untersuchungen B2 Qualitative labormedizinische Untersuchungen B3 Direkter Nachweis und Charakterisierung von Infektionserregern B4 Ejakulatuntersuchungen B5 Molekulargenetische und zytologische laboratoriumsmedizinische Untersuchung
5 Inkrafttreten Rili-BÄK 2008 Die Richtlinienteile B 2, D 2 und E 2 treten am in Kraft. Die hierin niedergelegten Anforderungen sind spätestens bis zum zu erfüllen. Die Richtlinienteile B 3, D 3 und E 3 treten am in Kraft. Die hierin niedergelegten Anforderungen sind spätestens bis zum zu erfüllen. Die Richtlinienteile B 5, D 5 und E 5 treten am in Kraft. Die hierin niedergelegten Anforderungen sind spätestens bis zum zu erfüllen. Die Richtlinien der Bundesärztekammer zur Qualitätssicherung in der Immunhämatologie vom (Deutsches Ärzteblatt, Jahrgang 89, Heft 7, Februar 1992) werden mit Wirkung vom außer Kraft gesetzt. Die Richtlinie der Bundesärztekammer zur Qualitätssicherung in der Mikrobiologie vom (Deutsches Ärzteblatt 89 (1992) Heft 7 wird mit Wirkung vom außer Kraft gesetzt.
6 Bundesärztekammer Referenzinstitutionen gemäß Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen Stand: Juni 2013 Quantitative Untersuchungen INSTAND e.v. Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e.v. Ubierstr. 20, Düsseldorf, Telefon: , Telefax: Referenzinstitut für Bioanalytik (RfB) der Stiftung für Pathobiochemie und Molekulare Diagnostik Friesdorfer Straße 153, Bonn, Telefon: / , Telefax: / info@dgkl-rfb.de, Beschluss des Vorstands der Bundesärztekammer vom , Deutsches Ärzteblatt, Jg. 107, Heft 9, 5. März 2010, Seite A-408
7 Bundesärztekammer Referenzinstitutionen gemäß Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen Stand: Juni 2013 Qualitative Untersuchungen INSTAND e.v. Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e.v. Ubierstraße 20, Düsseldorf, Telefon: , Telefax: , Referenzinstitut für Bioanalytik (RfB) der Stiftung für Pathobiochemie und Molekulare Diagnostik,Friesdorfer Straße 153,53175 Bonn Telefon: / Telefax: / sekretariat@dgkl.de, Beschluss des Vorstands der Bundesärztekammer vom 22./ Deutsches Ärzteblatt, Jg. 109, Heft 17, 27 April 2012, Seite A-886
8 Bundesärztekammer Referenzinstitutionen gemäß Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen Stand: Juni 2013 Ejakulatuntersuchungen QuaDeGA GmbH Qualitätskontrolle der Deutschen Gesellschaft für Andrologie cc: Centrum für Reproduktionsmedizin und Andrologie Universitätsklinikum Münster, Domagkstraße 11, Münster Telefon: / oder: / ,Telefax: / info@quadega.uni-muenster.de Beschluss des Vorstands der Bundesärztekammer vom Deutsches Ärzteblatt, Jg. 108, Heft 43, , Seite A-2304
9 Bundesärztekammer Referenzinstitutionen gemäß Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen Stand: Juni 2013 Molekulargenetische Untersuchungen INSTAND e.v. Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e.v. Ubierstr. 20, Düsseldorf, Tel.: , Fax: Referenzinstitut für Bioanalytik (RfB) der Stiftung für Pathobiochemie und Molekulare Diagnostik, Friesdorfer Straße 153, Bonn, Tel.: / , Fax: / info@dgkl-rfb.de, Beschluss des Vorstands der Bundesärztekammer vom Deutsches Ärzteblatt, Jg. 110 Heft 21, , Seite A 1056
10 Bundesärztekammer Referenzinstitutionen gemäß Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen Stand: Juni 2013 Zytogenetische Untersuchungen Berufsverband Deutscher Humangenetiker (BVDH) e. V. Geschäftsstelle, Linienstraße 127, Berlin Tel.: +49 (0) , Fax: +49 (0) Beschluss des Vorstands der Bundesärztekammer vom Deutsches Ärzteblatt, Jg. 110 Heft 21, , Seite A 1056
11 Bundesärztekammer Häufig gestellte Fragen zur Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen (FAQ) Stand: Oktober 2012 Die FAQ werden ständig durch die BÄK fortgeschrieben.
12 Bundesärztekammer Ausblick Was ist weiterhin mit der Rili-BÄK geplant. 1. Anpassung und Überarbeitung der Vorgaben in der Tabelle B1 2. Sprachliche Anpassung der in den Teilen B1 bis B5 genannten Anforderungen.
13 MPBetreibV Rechtliche Grundlage - 4a Medizinprodukte Betreiberverordnung (MPBetreibV) Verankerung der Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen - Rili-BÄK 2008, Teil A und Teil B 1 vom , in Kraft seit Verpflichtung der Anwendung in Laboratorien und Grundlage der Überwachung von Laboratorien durch die Behörden Achtung: Hier werden nach der Änderung der MPBetreibV die weiteren Teile der Rili-BÄK genannt.
14 MPBetreibV Betreiber von medizinischen Laboratorien sind nach 4a MPBetreibV verpflichtet, die Richtlinie der Bundesärztekammer zur Qualitätssicherung labormedizinischer Untersuchungen (Rili-BÄK) einzuhalten und ein Qualitätsmanagementhandbuch (QMH) zu erstellen. (siehe Teil A Rili-BÄK) In diesem QM-Handbuch müssen alle auch qualitative Untersuchen beschrieben werden. Im speziellen Teil B1 sind die Mindestanforderungen an die Sicherung der Qualität der Messergebnisse quantitativer laboratoriumsmedizinischer Untersuchungen festgelegt. Es muss eine Anpassung des 4a der MPBetreibV erfolgen.
15 Umstrukturierung im Landesamt Auswirkung: Der Bereich Überwachung Medizinproduktegesetz (MPG) ist aus der Abteilung 3 zum in der Abteilung 1 angesiedelt worden. Das neue Organigramm können Sie demnächst auf der Homepage des LME einsehen. Nach wie vor sind die drei bekannten Mitarbeiter für Sie zuständig. Möglicherweise erhält der Bereich weitere Mitarbeiter.
16 Wer ist speziell im LME-RLP für Sie zuständig? Fragen zur Rili-BÄK in RLP bitte an das Landesamt für Mess- und Eichwesen (LME-RLP) mit folgenden Ansprechpartnern: Herr A. Bläser, er ist vom Standort Trier im westlichen Teil von RLP inkl. des Westerwaldkreises tätig. Tel.: 0671 / Seine Bereiche sind Arztpraxen, Altenheime, Kurkliniken u. sonstige med. Einrichtungen. Herr B. Zimmermann, vom Standort Bad Kreuznach. Er ist in ganz RLP tätig. Tel.: 0671 / Bereiche: Arztpraxen, Altenheime, Kurkliniken, Krankenhäuser und Laborärzte. Herr für das LME-RLP. Tel.: 0671 / Oder auch per Mail an poststelle@lme.rlp.de Bitte beachten Sie, dass die Mitarbeiter im Außendienst sind, so dass Sie meistens bei telefonischen Anfragen in unserem Servicecenter Tel. 0671/ in Bad Kreuznach landen. Die Kollegen nehmen gerne Ihren Anruf entgegen, so dass wir Sie zurückrufen können.
17 Ergebnisse der Überwachung vor Ort für das Jahr 2012 Bereich Anzahl Anzahl Beanstandungen Prozent Gesamtzahl der Überwachungen * - -* 1. Medizinprodukte mit Messfunktion POCT- Messgeräte Medizinische Laboratorien Personenwaagen * Keine Addition, da Mehrfachnennung
18 Wer wird in RLP überwacht? Arztpraxen Altenheime Krankenhäusern, Kurkliniken Laborgemeinschaften und sonstige Einrichtungen wie Rettungswachen od. Pflegedienste
19 Was wurde geprüft? 1. Medizinprodukte mit Messfunktion ( 11 MPBetreibV) 2. Im Labor 4a MPBetreibV; hier Teil A, Grundlegende Anforderungen an die Qualitätssicherung laboratoriumsmedizinischer Untersuchungen (Nr. 1 bis 7) der Rili-BÄK 3. Teil B1 Quantitative laboratoriumsmendizinische Untersuchungen 1. Grundsätze der Qualitätssicherung 2. Durchführung der Qualitätssicherung 2.1 Interne Qualitätssicherung 2.2 Externe Qualitätssicherung Heute etwas zur internen Qualitätssicherung (QS) und Bewertung der Fehlergrenzen mit dem Blick auf die MPSV. Wissen Sie was MPSV bedeutet? Später dazu mehr.
20 Überwachung Rili-BÄK 2008, Teil B 1 Nr Bewertung der Kontrollprobeneinzelmessungen (KPEM) - Werden Fehlergrenzen in der Tabelle B 1 a bis c, Spalte 3 eingehalten? - Erfolgten Konsequenzen bei Überschreiten der Fehlergrenzen der KPEM? das heißt: * Sperrung des Messverfahrens bis die Ursachen der Abweichung ermittelt und beseitigt wurden? * Entscheidung über Freigabe unter Beachtung der medizinischen Relevanz bzw. weitere Maßnahmen, wie z. B. Wiederholungsmessungen der Kontrollprobe und evtl. der vorhergehenden Patientenproben erfolgt? * ggf. Information an Einsender und eine nachvollziehbare Dokumentation des gesamten Vorgangs?
21 Überwachung Rili-BÄK 2008, Teil B 1 Nr.: Bewertung des Kontrollzyklus - Erfolgt unverzüglich, d. h. ohne schuldhafte Verzögerung die Berechnung und Bewertung des quadratischen Mittelwertes der Messabweichung Mw? - Liegt Mw innerhalb der jeweils vorgeschriebenen Grenzen? - Werden Konsequenzen gezogen bei erstmaligem Überschreiten von Mw? - Sperrung des Verfahrens bis die Funktionsfähigkeit des Untersuchungsverfahrens durch geeignete Maßnahmen nachgewiesen wurde? - Erfolgt eine nachvollziehbare Dokumentation des gesamten Vorgangs?
22 Überwachung Rili-BÄK 2008, Teil B 1 Nr.: Abs. 3 Bewertung des Kontrollzyklus im Folgemonat - Gleiche Verfahrensweise bei erneuter Überschreitung? Maßnahmen nach Abs. 2 durchführen. - Zusätzlich bei Tabelle B 1-Messgrößen: -wenn Ursachen, die der Anwender zu vertreten hat, ausgeschlossen wurden und -der Begriff des Vorkommnisses nach MPSV 2 erfüllt ist? -Maßnahme: Information der zuständigen Bundesbehörde (BfArM, PEI) durch den Anwender, Weitere Informationen auf der Homepage der Bundesbehörden (Siehe Info)
23 Rili-BÄK 2008, Teil B 1, interne QS Verordnung über die Erfassung, Bewertung und Abwehr von Risiken bei Medizinprodukten (Medizinprodukte- Sicherheitsplanverordnung - MPSV) 2 Begriffsbestimmungen Im Sinne dieser Verordnung ist 1. "Vorkommnis" eine Funktionsstörung, ein Ausfall oder eine Änderung der Merkmale oder der Leistung oder eine Unsachgemäßheit der Kennzeichnung oder der Gebrauchsanweisung eines Medizinprodukts, die unmittelbar oder mittelbar zum Tod oder zu einer schwerwiegenden Verschlechterung des Gesundheitszustands eines Patienten, eines Anwenders oder einer anderen Person geführt hat, geführt haben könnte oder führen könnte, (...)
24 Rili-BÄK 2008, Teil B 1, interne QS Verordnung über die Erfassung, Bewertung und Abwehr von Risiken bei Medizinprodukten (Medizinprodukte-Sicherheitsplanverordnung - MPSV) Wie erfolgt eine Meldung? Was muss der Betreiber beachten. Hierzu sind auf der Homepage des BefArM und des PEI Formblätter abgelegt. Z.B.: Formblatt für die Meldung von Vorkommnissen durch sonstige Inverkehrbringer sowie Betreiber und Anwender nach 3 Abs. 2 bis 4 der Medizinprodukte-Sicherheitsplanverordnung. (außer Zahnärzte und zahnmedizinische Einrichtungen) (PEI)
25 Könnte das auch für POCT Blutzuckermessgeräte zutreffen? Meiner Meinung nach Ja. Hierzu folgendes Fallbespiel: Kontrollmessung am BZ Gerät in der 36. Kw. Kontrollwert OK Kontrollmessung am BZ Gerät in der 37. Kw. Kontrollwert nicht OK. Unmittelbare Nachkontrolle, auch der zweite Wert ist nicht OK. Konsequenz: Keine weiteren Messungen mit diesem Gerät! Reparatur bzw. das Gerät wird ausgemustert. Was ist mit den Messwerten (Patientenwerten) die zwischen der 36. und der 37.Kw. gemessen wurden? Gab es einen Vorkommnis? Auch hier muss dokumentiert werden, wenn mit diesem Gerät Patientenwerte ermittelt wurden, die dann zu einem Vorkommnis führten.
26 Umsetzung der MPVS Wichtig ist, dass Sie im medizinischen Bereich, in der Arztpraxis, im Krankenhaus, im Labor auch die MPVS im Blick haben, beachten und wenn nötig umsetzten.
27 Informationen zu weiteren Behörden: - ZLG Tel.: Fax: zlg@zlg.nrw.de Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten, Sebastianstraße 189, Bonn -BfArM Telefon: +49 (0) , Telefax: +49 (0) poststelle@bfarm.de Bundesinstitut für Arzneimittel und Medizinprodukte Kurt-Georg-Kiesinger-Allee 3, Bonn -PEI Telefon: , Fax: , pei@pei.de Paul-Ehrlich-Institut, Paul-Ehrlich-Straße 51-59, Langen - DIMDI Deutsches Institut für Medizinische Dokumentation und Information, Waisenhausgasse 36-38a, Köln
28 Zusammenfassung: Bei der Anwendung des 4a der MPBetreibV und der Rili-BÄK (2008) sind die gesetzlich Vorgaben zu beachten. Weitere werden folgen. Stellen Sie sicher, dass Sie immer auf dem aktuellen Stand sind! Ergänzen Sie Ihre Gesetzeswerke um die MPVS. Mit der Umsetzung der neuen Teile B 2 und B 5 sollten Sie beginnen, denn die Uhren der Übergansfristen sind schon abgelaufen oder ticken noch.
29 Informationen über das Landesamt für Mess- und Eichwesen Rheinland-Pfalz (LME-RLP) erhalten Sie unter
30 Vielen Dank für f r Ihre Aufmerksamkeit Weitere Diskussion?
Sächsisches Landesamt für Mess- und Eichwesen. Bio-Rad Laboratories Fortbildungsprogramm Rili-BÄK 2008, Vertiefungsmodul.
 Bio-Rad Laboratories Fortbildungsprogramm Rili-BÄK 2008, Vertiefungsmodul Rili-BÄK 2008 aus der Sicht der Überwachungsbehörde in Sachsen Gabriele Schmidt Sächsisches Landesamt für Mess- und Eichwesen 11.11.2009
Bio-Rad Laboratories Fortbildungsprogramm Rili-BÄK 2008, Vertiefungsmodul Rili-BÄK 2008 aus der Sicht der Überwachungsbehörde in Sachsen Gabriele Schmidt Sächsisches Landesamt für Mess- und Eichwesen 11.11.2009
Rili-BÄK Spezieller Teil B 2. Carmen Hansen, Bio-Rad Laboratories GmbH
 Rili-BÄK Spezieller Teil B 2 Carmen Hansen, Bio-Rad Laboratories GmbH Rili-BÄK komplett Teil A: Grundlegende Anforderungen seit April 2010 Teil B 1: Quantitativ Teil B 2: Qualitativ Teil B 3: Infektionsserologie
Rili-BÄK Spezieller Teil B 2 Carmen Hansen, Bio-Rad Laboratories GmbH Rili-BÄK komplett Teil A: Grundlegende Anforderungen seit April 2010 Teil B 1: Quantitativ Teil B 2: Qualitativ Teil B 3: Infektionsserologie
Anforderungen an die interne und externe Qualitätskontrolle des POCT
 Anforderungen an die interne und externe Qualitätskontrolle des POCT Dr. rer. nat. Manfred Falck Zentrallabor Zentralinstitut für Klinische Chemie und Laboratoriumsdiagnostik Direktor Univ.-Prof. Dr. F.
Anforderungen an die interne und externe Qualitätskontrolle des POCT Dr. rer. nat. Manfred Falck Zentrallabor Zentralinstitut für Klinische Chemie und Laboratoriumsdiagnostik Direktor Univ.-Prof. Dr. F.
vom 23. November 2007 (Dt. Ärzteblatt 105, Heft 7, 15. Februar 2008, S. A 341)
 Informationsblatt Patientennahe Sofortdiagnostik (POCT) mit Unit-use-Reagenzien nach der Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen (Rili-BÄK 2008)
Informationsblatt Patientennahe Sofortdiagnostik (POCT) mit Unit-use-Reagenzien nach der Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen (Rili-BÄK 2008)
Rili-BÄK 2008 Qualitätssicherung in der patientennahen Sofortdiagnostik (POCT)
 Rili-BÄK 2008 Qualitätssicherung in der patientennahen Sofortdiagnostik (POCT) Gabriele Schmidt 1 Rili-BÄK 2008 Übergangszeit zur Einführung ist am 31.03.2010 abgelaufen. Stand? Laboratorien: - Teil A
Rili-BÄK 2008 Qualitätssicherung in der patientennahen Sofortdiagnostik (POCT) Gabriele Schmidt 1 Rili-BÄK 2008 Übergangszeit zur Einführung ist am 31.03.2010 abgelaufen. Stand? Laboratorien: - Teil A
Warum? Orthopäden; 5336. Dermatologen; 3342. Urologen; 2674. Chirurgen; 3976. Neurochirurgen; 491. Gynäkologen; 9875
 Können Medizinprodukte ohne CE-Kennzeichnung betrieben werden? Warum? Urologen; 2674 Neurochirurgen; 491 MKG; 1027 Allgemeinärzte/ praktische Ärzte; 40.246 Orthopäden; 5336 Chirurgen; 3976 Anästhesisten;
Können Medizinprodukte ohne CE-Kennzeichnung betrieben werden? Warum? Urologen; 2674 Neurochirurgen; 491 MKG; 1027 Allgemeinärzte/ praktische Ärzte; 40.246 Orthopäden; 5336 Chirurgen; 3976 Anästhesisten;
Erfahrungsbericht zur Umsetzung der Teile A und B aus Sicht der Überwachungsbehörde
 Erfahrungsbericht zur Umsetzung der Teile A und B aus Sicht der Überwachungsbehörde Dr. Diana Peters Medizinprodukteüberachung 1 Zuständigkeiten für die Überwachung der Medizinischen Laboratorien Durchführung
Erfahrungsbericht zur Umsetzung der Teile A und B aus Sicht der Überwachungsbehörde Dr. Diana Peters Medizinprodukteüberachung 1 Zuständigkeiten für die Überwachung der Medizinischen Laboratorien Durchführung
Richtlinie Bundesärztekammer Teil B2 Qualitätssicherung qualitativer labormedizinischer Untersuchungen Stand der Beratungen und Anforderungen
 Richtlinie Bundesärztekammer Teil B2 Qualitätssicherung qualitativer labormedizinischer Untersuchungen Stand der Beratungen und Anforderungen Dr. André Schmitz und Andrea Michelsen Zentralstelle der Länder
Richtlinie Bundesärztekammer Teil B2 Qualitätssicherung qualitativer labormedizinischer Untersuchungen Stand der Beratungen und Anforderungen Dr. André Schmitz und Andrea Michelsen Zentralstelle der Länder
Bekanntmachung gemäß 7 und 18 der Medizinprodukte-Sicherheitsplanverordnung
 Bekanntmachung gemäß 7 und 18 der Medizinprodukte-Sicherheitsplanverordnung vom 28. Juni 2002 (BAnz. Nr. 167a vom 6. September 2002), zuletzt geändert durch Bekanntmachung vom 9. Dezember 2002 (BAnz. 2003
Bekanntmachung gemäß 7 und 18 der Medizinprodukte-Sicherheitsplanverordnung vom 28. Juni 2002 (BAnz. Nr. 167a vom 6. September 2002), zuletzt geändert durch Bekanntmachung vom 9. Dezember 2002 (BAnz. 2003
Rili-BÄK Fortbildungsprogramm: Neue Richtlinienteile und Erfahrungen. Carmen Hansen und Olaf Kirchner, Bio-Rad Laboratories GmbH
 Rili-BÄK Fortbildungsprogramm: Neue Richtlinienteile und Erfahrungen Carmen Hansen und Olaf Kirchner, Bio-Rad Laboratories GmbH B 4: Ejakulatuntersuchungen 1 Grundsätze der Qualitätssicherung 2 Durchführung
Rili-BÄK Fortbildungsprogramm: Neue Richtlinienteile und Erfahrungen Carmen Hansen und Olaf Kirchner, Bio-Rad Laboratories GmbH B 4: Ejakulatuntersuchungen 1 Grundsätze der Qualitätssicherung 2 Durchführung
9.5 Medizinprodukte-Betreiberverordnung - MPBetreibV
 9.5 -Betreiberverordnung - MPBetreibV Die -Betreiberverordnung (MPBetreibV) regelt das Errichten, Betreiben und Anwenden von n und von Zubehör für. Zubehör sind Gegenstände, Stoffe, Zubereitungen aus Stoffen
9.5 -Betreiberverordnung - MPBetreibV Die -Betreiberverordnung (MPBetreibV) regelt das Errichten, Betreiben und Anwenden von n und von Zubehör für. Zubehör sind Gegenstände, Stoffe, Zubereitungen aus Stoffen
Die Sicht des Gesetzgebers
 Essen, 23. Februar 2005 Aufbereitung von Medizinprodukten die Verantwortung des Herstellers und des Anwenders Die Sicht des Gesetzgebers Bundesministerium für Gesundheit und Soziale Sicherung 1 Gliederung
Essen, 23. Februar 2005 Aufbereitung von Medizinprodukten die Verantwortung des Herstellers und des Anwenders Die Sicht des Gesetzgebers Bundesministerium für Gesundheit und Soziale Sicherung 1 Gliederung
Medizinprodukte-Sicherheitsplanverordnung
 Hygieneforum Sande 19.06.2014 Meldung von Vorkommnissen nach der Medizinproduke-Sicherheitsplanverordnung www.klinikum-bremen-ldw.de Klinikum Links der Weser Senator-Weßling-Str. 1 28277 Bremen Meldung
Hygieneforum Sande 19.06.2014 Meldung von Vorkommnissen nach der Medizinproduke-Sicherheitsplanverordnung www.klinikum-bremen-ldw.de Klinikum Links der Weser Senator-Weßling-Str. 1 28277 Bremen Meldung
Ihre Überwachungsbehörde stellt sich vor
 Mess- und Eichwesen Baden-Württemberg Fortbildungsprogramm RiliBÄK 2008 Vertiefungsmodul Heidelberg - 13. Oktober 2009 Ihre Überwachungsbehörde stellt sich vor Michael Pernus - Eichamt Freiburg Michael
Mess- und Eichwesen Baden-Württemberg Fortbildungsprogramm RiliBÄK 2008 Vertiefungsmodul Heidelberg - 13. Oktober 2009 Ihre Überwachungsbehörde stellt sich vor Michael Pernus - Eichamt Freiburg Michael
Rili-BÄK 2007 Umsetzung Teil A und Teil B1 mit Ausblick auf Teil B2 B5. Erfahrungsbericht einer Überwachungsbehörde April 2010 bis heute
 Rili-BÄK 2007 Umsetzung Teil A und Teil B1 mit Ausblick auf Teil B2 B5 Erfahrungsbericht einer Überwachungsbehörde April 2010 bis heute Thomas Schade Bayerisches Landesamt für Maß und Gewicht Stand: 10.09.2013
Rili-BÄK 2007 Umsetzung Teil A und Teil B1 mit Ausblick auf Teil B2 B5 Erfahrungsbericht einer Überwachungsbehörde April 2010 bis heute Thomas Schade Bayerisches Landesamt für Maß und Gewicht Stand: 10.09.2013
Erfahrungen der. DQS GmbH. bei der Zertifizierung von Medizinprodukteherstellern
 Erfahrungen der DQS GmbH bei der Zertifizierung von Medizinprodukteherstellern 2004-11-24, Seite 1 Normensituation Medizinprodukte DIN EN ISO 9001:94 DIN EN ISO 9001:2000 DIN EN 46001/2:1996 DIN EN ISO
Erfahrungen der DQS GmbH bei der Zertifizierung von Medizinprodukteherstellern 2004-11-24, Seite 1 Normensituation Medizinprodukte DIN EN ISO 9001:94 DIN EN ISO 9001:2000 DIN EN 46001/2:1996 DIN EN ISO
Stellungnahme der Bundesärztekammer
 Stellungnahme der Bundesärztekammer zum Entwurf einer Verordnung über die Abgabe von Medizinprodukten und zur Änderung medizinprodukterechtlicher Vorschriften Berlin, 01.03.2013 Bundesärztekammer Herbert-Lewin-Platz
Stellungnahme der Bundesärztekammer zum Entwurf einer Verordnung über die Abgabe von Medizinprodukten und zur Änderung medizinprodukterechtlicher Vorschriften Berlin, 01.03.2013 Bundesärztekammer Herbert-Lewin-Platz
Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie
 Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie Rechtliche Abgrenzung zwischen Podologie und Fußpflege Ziele des Medizinprodukterechtes: für die Gesundheit und den erforderlichen
Gesetzliche Vorgaben für die Aufbereitung von Instrumenten in der Podologie Rechtliche Abgrenzung zwischen Podologie und Fußpflege Ziele des Medizinprodukterechtes: für die Gesundheit und den erforderlichen
Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 13.11.2013 Inhaltsübersicht
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 13.11.2013 Inhaltsübersicht
Vorstellung der Überwachungsbehörde
 Vorstellung der Überwachungsbehörde Sybille Döring Landesamt für Mess- und Eichwesen Berlin-Brandenburg Bio-Rad, Berlin 17.11.2009 1 Landesamt für Mess- und Eichwesen Berlin - Brandenburg gemeinsames Landesamt
Vorstellung der Überwachungsbehörde Sybille Döring Landesamt für Mess- und Eichwesen Berlin-Brandenburg Bio-Rad, Berlin 17.11.2009 1 Landesamt für Mess- und Eichwesen Berlin - Brandenburg gemeinsames Landesamt
Inhaltsverzeichnis. Inhaltsverzeichnis. Inhaltsübersicht. Rechtliche Grundlagen des Medizinprodukterechts 1
 Inhaltsverzeichnis Vorwort Inhaltsübersicht III X Rechtliche Grundlagen des Medizinprodukterechts 1 Richtlinie über Medizinprodukte 1 Rechtliche Grundlagen in der Europäischen Union (EU) 1 Rechtliche Grundlagen
Inhaltsverzeichnis Vorwort Inhaltsübersicht III X Rechtliche Grundlagen des Medizinprodukterechts 1 Richtlinie über Medizinprodukte 1 Rechtliche Grundlagen in der Europäischen Union (EU) 1 Rechtliche Grundlagen
Überwachung der Qualitätssicherung laboratoriumsmedizinischer Untersuchungen. Einsenderschulung MLOW, 25. September Geeicht auf Sachsen!
 Überwachung der Qualitätssicherung laboratoriumsmedizinischer Untersuchungen Einsenderschulung MLOW, 25. September 2013 Geeicht auf Sachsen! Gliederung 1. Einleitung 2. Rechtsgrundlage 3. Vorstellung SMS/SME
Überwachung der Qualitätssicherung laboratoriumsmedizinischer Untersuchungen Einsenderschulung MLOW, 25. September 2013 Geeicht auf Sachsen! Gliederung 1. Einleitung 2. Rechtsgrundlage 3. Vorstellung SMS/SME
Erfahrungsbericht zur Umsetzung der RiLi-BÄK aus Sicht der Überwachungsbehörde. Dr. Arno Terhechte
 Erfahrungsbericht zur Umsetzung der RiLi-BÄK aus Sicht der Überwachungsbehörde Dr. Arno Terhechte Münster, 06.11.2013 Fahrplan Zuständigkeit, Aufgabe der BR s Überwachung in NRW Rechtlicher Rahmen (MPG,
Erfahrungsbericht zur Umsetzung der RiLi-BÄK aus Sicht der Überwachungsbehörde Dr. Arno Terhechte Münster, 06.11.2013 Fahrplan Zuständigkeit, Aufgabe der BR s Überwachung in NRW Rechtlicher Rahmen (MPG,
vom 1. März 2006 (BAnz. Nr. 53 S. 1682 und Nr. 59 S. 1980)
 Bekanntmachung der Erreichbarkeit der zuständigen Behörden der Länder zur Meldung von Risiken aus Medizinprodukten außerhalb der Dienstzeit gemäß 18 der Medizinprodukte- Sicherheitsplanverordnung (MPSV)
Bekanntmachung der Erreichbarkeit der zuständigen Behörden der Länder zur Meldung von Risiken aus Medizinprodukten außerhalb der Dienstzeit gemäß 18 der Medizinprodukte- Sicherheitsplanverordnung (MPSV)
Überwachungen nach dem Gesetz über Medizinprodukte in Sachsen - 2008
 Sächsisches Landesamt für Mess- und Eichwesen Überwachungen nach dem Gesetz über Medizinprodukte in Sachsen - 2008 Es werden die Ergebnisse der Tätigkeit des Sächsischen Landesamtes für Mess- und Eichwes~n
Sächsisches Landesamt für Mess- und Eichwesen Überwachungen nach dem Gesetz über Medizinprodukte in Sachsen - 2008 Es werden die Ergebnisse der Tätigkeit des Sächsischen Landesamtes für Mess- und Eichwes~n
Häufig gestellte Fragen zur Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen
 Allgemeine Fragen 1. Wer muss die Richtlinie anwenden? Rechtsgrundlage für die Anwendung der Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen, kurz Rili-BÄK
Allgemeine Fragen 1. Wer muss die Richtlinie anwenden? Rechtsgrundlage für die Anwendung der Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen, kurz Rili-BÄK
Kommentar zur. Qualitätskontrolle. für Laboruntersuchungen in der Arztpraxis. nach der Rili-BÄK 2008 (vom 23.11.2007)
 Kommentar zur Qualitätskontrolle für Laboruntersuchungen in der Arztpraxis nach der Rili-BÄK 2008 (vom 23.11.2007) Laborkommission der Kassenärztlichen Vereinigung Sachsen-Anhalt Dr. rer. nat. Friedrich
Kommentar zur Qualitätskontrolle für Laboruntersuchungen in der Arztpraxis nach der Rili-BÄK 2008 (vom 23.11.2007) Laborkommission der Kassenärztlichen Vereinigung Sachsen-Anhalt Dr. rer. nat. Friedrich
Anforderungen an die Qualitätssicherung quantitativer Laboranalytik gem. Medizinprodukterecht und RiliBÄK 2008
 Anforderungen an die Qualitätssicherung quantitativer Laboranalytik gem. Medizinprodukterecht und RiliBÄK 2008 Frankfurt, 07-10-2009 Kurzfassung 10.2009 Siggi Brilling Dez. 35.3 1 Inhaltliche Skizze II.
Anforderungen an die Qualitätssicherung quantitativer Laboranalytik gem. Medizinprodukterecht und RiliBÄK 2008 Frankfurt, 07-10-2009 Kurzfassung 10.2009 Siggi Brilling Dez. 35.3 1 Inhaltliche Skizze II.
Bayerisches Landesamt Die neuen Richtlinien der Bundesärztekammer zur Stand: 03.08.2010
 Thomas Schade laboratoriumsmedizinischer Untersuchungen POCT Seite 1 von 52 Die neuen Richtlinien der Bundesärztekammer zur laboratoriumsmedizinischer Untersuchungen POCT Rosenheim-Happing 22. September
Thomas Schade laboratoriumsmedizinischer Untersuchungen POCT Seite 1 von 52 Die neuen Richtlinien der Bundesärztekammer zur laboratoriumsmedizinischer Untersuchungen POCT Rosenheim-Happing 22. September
Gesamte Rechtsvorschrift für Konformitätsbewertung von Medizinprodukten, Fassung vom
 Gesamte Rechtsvorschrift für Konformitätsbewertung von Medizinprodukten, Fassung vom 07.03.2014 Langtitel Verordnung der Bundesministerin für Gesundheit und Frauen über die Konformitätsbewertung von Medizinprodukten
Gesamte Rechtsvorschrift für Konformitätsbewertung von Medizinprodukten, Fassung vom 07.03.2014 Langtitel Verordnung der Bundesministerin für Gesundheit und Frauen über die Konformitätsbewertung von Medizinprodukten
Aufgaben der MP-Berater und Sicherheitsbeauftragten im Medizinprodukte-Beobachtungs- und Meldesystem
 Aufgaben der MP-Berater und Sicherheitsbeauftragten im Medizinprodukte-Beobachtungs- und Meldesystem Referent: Ralf Kitschmann Seite 1/ 09-2009 30 MPG*, Sicherheitsbeauftragter für Medizinprodukte * Achtung:
Aufgaben der MP-Berater und Sicherheitsbeauftragten im Medizinprodukte-Beobachtungs- und Meldesystem Referent: Ralf Kitschmann Seite 1/ 09-2009 30 MPG*, Sicherheitsbeauftragter für Medizinprodukte * Achtung:
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ)
 Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
Rili-BÄK Ihre Überwachungsbehörde stellt sich vor: Landesamt für Mess- und Eichwesen Thüringen. Dr. Eckhard Steep
 2008 Ihre Überwachungsbehörde stellt sich vor: Landesamt für Mess- und Eichwesen Thüringen Dr. Eckhard Steep Folie 1 von 19 Folie 2 von 19 Zertifizierungs- Stelle NB 0118 Unterpörlitzer Straße 2 98693
2008 Ihre Überwachungsbehörde stellt sich vor: Landesamt für Mess- und Eichwesen Thüringen Dr. Eckhard Steep Folie 1 von 19 Folie 2 von 19 Zertifizierungs- Stelle NB 0118 Unterpörlitzer Straße 2 98693
Sichere Medizinprodukte besser überwachen
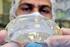 Gemeinsame Pressemitteilung Bonn, 20. März 2012 Sichere Medizinprodukte besser überwachen Im Zusammenhang mit Brustimplantaten des französischen Herstellers PIP (Poly Implant Prothèse) ist Kritik an der
Gemeinsame Pressemitteilung Bonn, 20. März 2012 Sichere Medizinprodukte besser überwachen Im Zusammenhang mit Brustimplantaten des französischen Herstellers PIP (Poly Implant Prothèse) ist Kritik an der
Das gesetzliche Vigilanzsystem - Aufgaben und Risikobewertung des BfArM APS-Jahrestagung, Berlin, 16.04.2015 Dr. Wolfgang Lauer
 Das gesetzliche Vigilanzsystem - Aufgaben und Risikobewertung des BfArM APS-Jahrestagung, Berlin, 16.04.2015 Dr. Wolfgang Lauer Beteiligte bei Inverkehrbringen & Überwachung Hersteller Verantwortlicher
Das gesetzliche Vigilanzsystem - Aufgaben und Risikobewertung des BfArM APS-Jahrestagung, Berlin, 16.04.2015 Dr. Wolfgang Lauer Beteiligte bei Inverkehrbringen & Überwachung Hersteller Verantwortlicher
Medizinproduktebuch gemäß 7 MPBetreibV
 Medizinproduktebuch gemäß 7 MPBetreibV Betreiber Bezeichnung des Medizinprodukts Sonstige Angaben zur Identifikation des Medizinprodukts Art und Typ Nomenklatur f. Medizinprodukte Loscode oder Seriennummer
Medizinproduktebuch gemäß 7 MPBetreibV Betreiber Bezeichnung des Medizinprodukts Sonstige Angaben zur Identifikation des Medizinprodukts Art und Typ Nomenklatur f. Medizinprodukte Loscode oder Seriennummer
Bayerisches Staatsministerium für Umwelt, Gesundheit und Verbraucherschutz Medizinprodukte Information
 Bayerisches Staatsministerium für Umwelt, Gesundheit und Verbraucherschutz Medizinprodukte Information Sicherheitsrisiken von Kranken- und Pflegebetten Erstellt: 02.05.2008 Medizinprodukte Information
Bayerisches Staatsministerium für Umwelt, Gesundheit und Verbraucherschutz Medizinprodukte Information Sicherheitsrisiken von Kranken- und Pflegebetten Erstellt: 02.05.2008 Medizinprodukte Information
Clinic-Master / Vital-Master B C R. Medizinproduktebuch. Walitschek Medizintechnik GmbH 2013 Rev. 1
 B C R Medizinproduktebuch B C R R 1 Hersteller/manufacturer: Walitschek Medizintechnik GmbH Fuldablick 3 D-34355 Staufenberg Tel: 05543 4558 Email: info@clinic-master.com B C R 0044 2 Inhalt Medizinproduktebuch
B C R Medizinproduktebuch B C R R 1 Hersteller/manufacturer: Walitschek Medizintechnik GmbH Fuldablick 3 D-34355 Staufenberg Tel: 05543 4558 Email: info@clinic-master.com B C R 0044 2 Inhalt Medizinproduktebuch
MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT. Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung
 KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung DGSV Kongress 2010 Fulda 08.10.2010 Inhalt Compliance
KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung DGSV Kongress 2010 Fulda 08.10.2010 Inhalt Compliance
Antrag auf Aussetzung/ Anpassung der Mengenbegrenzung im Speziallabor nach Kapitel 32.3 EBM
 Bitte zurücksenden an: Kassenärztliche Vereinigung Nordrhein z. Hd. Frau Beorchia Tersteegenstr. 9 40474 Düsseldorf Körperschaft des öffentlichen Rechts Hauptstelle Antrag auf Aussetzung/ Anpassung der
Bitte zurücksenden an: Kassenärztliche Vereinigung Nordrhein z. Hd. Frau Beorchia Tersteegenstr. 9 40474 Düsseldorf Körperschaft des öffentlichen Rechts Hauptstelle Antrag auf Aussetzung/ Anpassung der
Michael Martin / Die neue RiliBÄK in der Naturheilpraxis März 2010
 Auch für die Naturheilpraxis verbindlich: die neue Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen (RiliBÄK) Ab 1. April 2010 ist die 4. RiliBÄK für alle
Auch für die Naturheilpraxis verbindlich: die neue Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen (RiliBÄK) Ab 1. April 2010 ist die 4. RiliBÄK für alle
Ausbildungskurse. Strahlenschutz. Qualitätssicherung
 Magistrat der Stadt Wien MAGISTRATSABTEILUNG 39 Prüf-, Überwachungs- und Zertifizierungsstelle der Stadt Wien PTPA Labor für Strahlenschutz Standort: Währinger Gürtel 18 20 Ebene 04, Leitstelle 4B A-1090
Magistrat der Stadt Wien MAGISTRATSABTEILUNG 39 Prüf-, Überwachungs- und Zertifizierungsstelle der Stadt Wien PTPA Labor für Strahlenschutz Standort: Währinger Gürtel 18 20 Ebene 04, Leitstelle 4B A-1090
Verteilung der Verantwortlichkeiten zuvor, Anzeigeverfahren
 Das BfArM ist ein Bundesinstitut im Geschäftsbereich des Bundesministeriums für Gesundheit 1 Verteilung der Verantwortlichkeiten zuvor, Anzeigeverfahren Politische Ebene Bundesbehörden Ministerien, insbesondere
Das BfArM ist ein Bundesinstitut im Geschäftsbereich des Bundesministeriums für Gesundheit 1 Verteilung der Verantwortlichkeiten zuvor, Anzeigeverfahren Politische Ebene Bundesbehörden Ministerien, insbesondere
Steffen Wolf Referat II 4 - Technischer Verbraucherschutz, Marktaufsicht
 Die einheitliche Überwachung in Deutschland 15. DGSV-Kongress vom 03.10. 05.10.2011 in Fulda Steffen Wolf Referat II 4 - Technischer Verbraucherschutz, Marktaufsicht 1 Gliederung Kompetenz von Bund und
Die einheitliche Überwachung in Deutschland 15. DGSV-Kongress vom 03.10. 05.10.2011 in Fulda Steffen Wolf Referat II 4 - Technischer Verbraucherschutz, Marktaufsicht 1 Gliederung Kompetenz von Bund und
Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen
 Bundesärztekammer Arbeitsgemeinschaft der deutschen Ärztekammern Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen Gemäß Beschluss des Vorstands der Bundesärztekammer
Bundesärztekammer Arbeitsgemeinschaft der deutschen Ärztekammern Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen Gemäß Beschluss des Vorstands der Bundesärztekammer
Das BASG / AGES PharmMed
 CMI-WORKSHOP Dipl.-Ing. Meinrad Guggenbichler Institut Inspektionen, Medizinprodukte und Hämovigilanz Das BASG / AGES PharmMed Das Bundesamt für Sicherheit im Gesundheitswesen (BASG) ist die Aufsichtsbehörde
CMI-WORKSHOP Dipl.-Ing. Meinrad Guggenbichler Institut Inspektionen, Medizinprodukte und Hämovigilanz Das BASG / AGES PharmMed Das Bundesamt für Sicherheit im Gesundheitswesen (BASG) ist die Aufsichtsbehörde
Die Kombination von Medizinprodukten. SystemCheck
 Die Kombination von Medizinprodukten SystemCheck Fachtagung der FKT 12.06.2008 Untertitel Die Prüfung und Bewertung von medizinischen elektrischen Systemen mit rechtssicherer Dokumentation zum Schutz von
Die Kombination von Medizinprodukten SystemCheck Fachtagung der FKT 12.06.2008 Untertitel Die Prüfung und Bewertung von medizinischen elektrischen Systemen mit rechtssicherer Dokumentation zum Schutz von
BUNDESÄRZTEKAMMER (ARBEITSGEMEINSCHAFT DER DEUTSCHEN ÄRZTEKAMMERN)
 BUNDESÄRZTEKAMMER (ARBEITSGEMEINSCHAFT DER DEUTSCHEN ÄRZTEKAMMERN) Kommentar zur Richtlinie der Bundesärztekammer zur Qualitätssicherung quantitativer laboratoriumsmedizinischer Untersuchungen Stand: März
BUNDESÄRZTEKAMMER (ARBEITSGEMEINSCHAFT DER DEUTSCHEN ÄRZTEKAMMERN) Kommentar zur Richtlinie der Bundesärztekammer zur Qualitätssicherung quantitativer laboratoriumsmedizinischer Untersuchungen Stand: März
https://www.zlg.de/arzneimittel/qualitaetssystem/qualitaetssicherungshandbuch.html
 Anlage 1 PZ-QS01 1 Klinikkopf Checkliste Vor- und Nachbereitung Audits und Inspektionen Checkliste Vor- und Nachbereitung Audits und Inspektionen https://www.zlg.de/arzneimittel/qualitaetssystem/qualitaetssicherungshandbuch.html
Anlage 1 PZ-QS01 1 Klinikkopf Checkliste Vor- und Nachbereitung Audits und Inspektionen Checkliste Vor- und Nachbereitung Audits und Inspektionen https://www.zlg.de/arzneimittel/qualitaetssystem/qualitaetssicherungshandbuch.html
Patientennahe Sofortdiagnostik (POCT) im Labor Umsetzung der Richtlinien der Bundesärztekammer
 Patientennahe Sofortdiagnostik (POCT) im Labor Umsetzung der Richtlinien der Bundesärztekammer Dr. A. Bobrowski 1.Vorsitzender Berufsverband Deutscher Laborärzte Kiel 03. Juni 2015 Richtlinie der Bundesärztekammer
Patientennahe Sofortdiagnostik (POCT) im Labor Umsetzung der Richtlinien der Bundesärztekammer Dr. A. Bobrowski 1.Vorsitzender Berufsverband Deutscher Laborärzte Kiel 03. Juni 2015 Richtlinie der Bundesärztekammer
Medizinprodukte Information des LAGetSi. Sicherheitsrisiken von Kranken- und Pflegebetten 1
 Medizinprodukte Information des LAGetSi Sicherheitsrisiken von Kranken- und Pflegebetten 1 Problem Aufgrund von Fehlfunktionen an Kranken- und Pflegebetten sind in Deutschland seit 1998 mehrere pflegebedürftige
Medizinprodukte Information des LAGetSi Sicherheitsrisiken von Kranken- und Pflegebetten 1 Problem Aufgrund von Fehlfunktionen an Kranken- und Pflegebetten sind in Deutschland seit 1998 mehrere pflegebedürftige
Keine Anwendung ohne Einweisung
 Dietmar Kirchberg Keine Anwendung ohne Einweisung Medizinprodukte sicher anwenden und betreiben pflege kolleg 5 Inhalt Abkürzungsverzeichnis........................................ 9 Vorwort......................................................
Dietmar Kirchberg Keine Anwendung ohne Einweisung Medizinprodukte sicher anwenden und betreiben pflege kolleg 5 Inhalt Abkürzungsverzeichnis........................................ 9 Vorwort......................................................
Endbericht Organisationshandbuch Medizingeräte. Qualitätsförderungsprogramm 2011 des Tiroler Gesundheitsfonds
 Endbericht Organisationshandbuch Medizingeräte Qualitätsförderungsprogramm 2011 des Tiroler Gesundheitsfonds Inhaltsverzeichnis 1. Projektbezeichnung... 3 2. Antragsteller... 3 3. Ansprechpersonen... 3
Endbericht Organisationshandbuch Medizingeräte Qualitätsförderungsprogramm 2011 des Tiroler Gesundheitsfonds Inhaltsverzeichnis 1. Projektbezeichnung... 3 2. Antragsteller... 3 3. Ansprechpersonen... 3
ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN
 Zentrale Sterilgut-Versorgung, Geschäftsbereich Bau, Technik und Medizintechnik C 5 ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN Toni Zanette Leiter Zentrale Sterilgutversorgung C 5 Rechtliche Anforderungen
Zentrale Sterilgut-Versorgung, Geschäftsbereich Bau, Technik und Medizintechnik C 5 ANFORDERUNGEN AN AUFBEREITER VON MEDIZINPRODUKTEN Toni Zanette Leiter Zentrale Sterilgutversorgung C 5 Rechtliche Anforderungen
Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen. Referent: Dipl.-Ing. Burkhard Schulze
 Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen Referent: Dipl.-Ing. Burkhard Schulze Definition: Aufbereitung Reinigung, Desinfektion und Sterilisation von bestimmungsgemäß
Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen Referent: Dipl.-Ing. Burkhard Schulze Definition: Aufbereitung Reinigung, Desinfektion und Sterilisation von bestimmungsgemäß
Laboruntersuchungen in der Arztpraxis Welche Anforderungen stellt die RiliBÄK?
 Laboruntersuchungen in der Arztpraxis Welche Anforderungen stellt die RiliBÄK? Sybille Döring / Sabine Störmer Landesamt für Mess- und Eichwesen Berlin-Brandenburg Berlin 15.03.2013 1 Welche Laboruntersuchungen
Laboruntersuchungen in der Arztpraxis Welche Anforderungen stellt die RiliBÄK? Sybille Döring / Sabine Störmer Landesamt für Mess- und Eichwesen Berlin-Brandenburg Berlin 15.03.2013 1 Welche Laboruntersuchungen
Dietmar Kirchberg Das Medizinproduktegesetz: Was Pflegende wissen müssen Bestimmungen Beispiele Konsequenzen
 Dietmar Kirchberg Das Medizinproduktegesetz: Was Pflegende wissen müssen Bestimmungen Beispiele Konsequenzen Bibliografische Information der Deutschen Bibliothek Die Deutsche Bibliothek verzeichnet diese
Dietmar Kirchberg Das Medizinproduktegesetz: Was Pflegende wissen müssen Bestimmungen Beispiele Konsequenzen Bibliografische Information der Deutschen Bibliothek Die Deutsche Bibliothek verzeichnet diese
Überwachung und Begehung durch die Gewerbeaufsicht Niedersachsen
 Behörde für betrieblichen Arbeits-, Umwelt- und Verbraucherschutz Überwachung und Begehung durch die Gewerbeaufsicht Niedersachsen AMAH 27.06.2015 Fragen, die der Vortrag beantworten soll Warum dürfen
Behörde für betrieblichen Arbeits-, Umwelt- und Verbraucherschutz Überwachung und Begehung durch die Gewerbeaufsicht Niedersachsen AMAH 27.06.2015 Fragen, die der Vortrag beantworten soll Warum dürfen
Rili-BÄK Infomappe zur Umsetzung der Qualitätssicherung
 Rili-BÄK Infomappe zur Umsetzung der Qualitätssicherung Blutzuckermessgerät für den Einsatz in medizinischen Einrichtungen F 01 010 03 215 Zuständige Behörde: Ansprechpartner: Durchführung der Kontrollmessung:
Rili-BÄK Infomappe zur Umsetzung der Qualitätssicherung Blutzuckermessgerät für den Einsatz in medizinischen Einrichtungen F 01 010 03 215 Zuständige Behörde: Ansprechpartner: Durchführung der Kontrollmessung:
Das Referenzinstitut für Bioanalytik. Externe Qualitätskontrolle auf höchstem Niveau
 Das Referenzinstitut für Bioanalytik Externe Qualitätskontrolle auf höchstem Niveau Referenzinstitut für Bioanalytik - Ringversuche zur externen Qualitätskontrolle - Ernannt von der Bundesärztekammer -
Das Referenzinstitut für Bioanalytik Externe Qualitätskontrolle auf höchstem Niveau Referenzinstitut für Bioanalytik - Ringversuche zur externen Qualitätskontrolle - Ernannt von der Bundesärztekammer -
Richtiges Brillen-Management nach dem Medizinprodukte-Gesetz. SPECTARIS-Infoveranstaltung
 Richtiges Brillen-Management nach dem Medizinprodukte-Gesetz SPECTARIS-Infoveranstaltung München, 10. Januar 2014 Was ist zu tun? - Warum ist meine Brille ein Medizinprodukt? - Welche Maßnahmen muss ich
Richtiges Brillen-Management nach dem Medizinprodukte-Gesetz SPECTARIS-Infoveranstaltung München, 10. Januar 2014 Was ist zu tun? - Warum ist meine Brille ein Medizinprodukt? - Welche Maßnahmen muss ich
Empfehlungen der Bundesapothekerkammer. für Richtlinien zum Erwerb des Fortbildungszertifikats
 Empfehlungen der Bundesapothekerkammer für Richtlinien zum Erwerb des Fortbildungszertifikats für pharmazeutisch-technische Assistenten, Apothekerassistenten, Pharmazieingenieure, Apothekenassistenten
Empfehlungen der Bundesapothekerkammer für Richtlinien zum Erwerb des Fortbildungszertifikats für pharmazeutisch-technische Assistenten, Apothekerassistenten, Pharmazieingenieure, Apothekenassistenten
Überwachungsprogramm gemäß 52a Bundes-Immissionsschutzgesetz und 9 Industriekläranlagen-Zulassungs- und Überwachungsverordnung
 Überwachungsprogramm gemäß 52a Bundes-Immissionsschutzgesetz und 9 Industriekläranlagen-Zulassungs- und Überwachungsverordnung Gemäß 52a Bundes-Immissionsschutzgesetz (BImSchG) und 9 Industriekläranlagen-Zulassungs-
Überwachungsprogramm gemäß 52a Bundes-Immissionsschutzgesetz und 9 Industriekläranlagen-Zulassungs- und Überwachungsverordnung Gemäß 52a Bundes-Immissionsschutzgesetz (BImSchG) und 9 Industriekläranlagen-Zulassungs-
Aufgrund von Fehlfunktionen an Kranken- und Pflegebetten sind in Deutschland seit 1998 mehrere pflegebedürftige Menschen zu Tode gekommen.
 Informationen der für Medizinprodukte zuständigen obersten Landesbehörden zu den Sicherheitsrisiken von Kranken- und Pflegebetten (Sicherheitsinformation von Mai 2001, aktualisiert Januar 2014 für NRW)
Informationen der für Medizinprodukte zuständigen obersten Landesbehörden zu den Sicherheitsrisiken von Kranken- und Pflegebetten (Sicherheitsinformation von Mai 2001, aktualisiert Januar 2014 für NRW)
Die neue RiliBÄK 2008 Betreiberüberwachung aus der Sicht der Überwachungsbehörde
 Die neue RiliBÄK 2008 Betreiberüberwachung aus der Sicht der Überwachungsbehörde 22.09 2009 R. Schumacher 1 Rechtliche Vorgaben Medizinproduktegesetz 26: Durchführung der Überwachung...Einrichtungen, in
Die neue RiliBÄK 2008 Betreiberüberwachung aus der Sicht der Überwachungsbehörde 22.09 2009 R. Schumacher 1 Rechtliche Vorgaben Medizinproduktegesetz 26: Durchführung der Überwachung...Einrichtungen, in
Qualitätssicherung bei Transfusionen und Hämotherapie
 ÄRZTEKAMMER Stand: 02.06.2016 Qualitätssicherung bei Transfusionen und Hämotherapie Hinweise zur Anwendung der Richtlinien Hämotherapie Mit der am 5. November 2005 erfolgten vollständigen Novellierung
ÄRZTEKAMMER Stand: 02.06.2016 Qualitätssicherung bei Transfusionen und Hämotherapie Hinweise zur Anwendung der Richtlinien Hämotherapie Mit der am 5. November 2005 erfolgten vollständigen Novellierung
Fortbildungsprogramm zur RiliBÄK Neue Richtlinienteile und Erfahrungen
 Fortbildungsprogramm zur RiliBÄK Neue Richtlinienteile und Erfahrungen Erfahrungsbericht zur Umsetzung der Teile A und B1 aus Sicht der überwachenden Behörde Michael Pernus Eichdirektion Stuttgart BIO-RAD-Seminar
Fortbildungsprogramm zur RiliBÄK Neue Richtlinienteile und Erfahrungen Erfahrungsbericht zur Umsetzung der Teile A und B1 aus Sicht der überwachenden Behörde Michael Pernus Eichdirektion Stuttgart BIO-RAD-Seminar
Regelung der Kassenärztlichen Bundesvereinigung zur Fortbildungsverpflichtung der Vertragsärzte und Vertragspsychotherapeuten nach 95d SGB V
 Regelung der Kassenärztlichen Bundesvereinigung zur Fortbildungsverpflichtung der Vertragsärzte und Vertragspsychotherapeuten nach 95d SGB V Der Vorstand der Kassenärztlichen Bundesvereinigung hat auf
Regelung der Kassenärztlichen Bundesvereinigung zur Fortbildungsverpflichtung der Vertragsärzte und Vertragspsychotherapeuten nach 95d SGB V Der Vorstand der Kassenärztlichen Bundesvereinigung hat auf
1. Allgemeines Geräte Fachliche Befähigung Dokumentation Sonographie der Säuglingshüfte...5
 Inhaltsverzeichnis 1. Allgemeines...1 2. Geräte...2 3. Fachliche Befähigung...3 4. Dokumentation...4 5. Sonographie der Säuglingshüfte...5 1. Allgemeines Behält ein Arzt seine Genehmigung nach der bisher
Inhaltsverzeichnis 1. Allgemeines...1 2. Geräte...2 3. Fachliche Befähigung...3 4. Dokumentation...4 5. Sonographie der Säuglingshüfte...5 1. Allgemeines Behält ein Arzt seine Genehmigung nach der bisher
Häufig gestellte Fragen (FAQ) zu Trinkwasser- Installationen in Gebäuden und Legionellen
 LANDKREIS CLOPPENBURG Der Landrat 53 Gesundheitsamt 53.5 Gesundheitsaufsicht/Infektionsschutz Eschstraße 29 49661 Cloppenburg Trinkwasser@lkclp.de Häufig gestellte Fragen (FAQ) zu Trinkwasser- Installationen
LANDKREIS CLOPPENBURG Der Landrat 53 Gesundheitsamt 53.5 Gesundheitsaufsicht/Infektionsschutz Eschstraße 29 49661 Cloppenburg Trinkwasser@lkclp.de Häufig gestellte Fragen (FAQ) zu Trinkwasser- Installationen
DGEM Qualitätshandbuch zur ernährungsmedizinischen Zertifizierung von Krankenhäusern
 DGEM Qualitätshandbuch zur ernährungsmedizinischen Zertifizierung von Krankenhäusern Johann Ockenga Medizinische Klinik II Gastroenterologie, Hepatologie, Endokrinologie & Ernährungsmedizin Klinikum Bremen
DGEM Qualitätshandbuch zur ernährungsmedizinischen Zertifizierung von Krankenhäusern Johann Ockenga Medizinische Klinik II Gastroenterologie, Hepatologie, Endokrinologie & Ernährungsmedizin Klinikum Bremen
Ideenbörse Krankenhaus - neue Wege der Erlössteigerung
 Zentrum für Labormedizin und Mikrobiologie (ZLM) Ideenbörse Krankenhaus - neue Wege der Erlössteigerung - das ZLM in Essen Berlin 26.02.2010 Gerd Hafner Kennzahlen des ZLM im Jahr 2009 Elisabeth-Krankenhaus
Zentrum für Labormedizin und Mikrobiologie (ZLM) Ideenbörse Krankenhaus - neue Wege der Erlössteigerung - das ZLM in Essen Berlin 26.02.2010 Gerd Hafner Kennzahlen des ZLM im Jahr 2009 Elisabeth-Krankenhaus
Medizinproduktebuch. Ergometer
 Inventar-Nr:... Serien-Nr.:... Medizinproduktebuch Ergometer nach 7 MPBetreibV für medizinische Geräte der Anlagen 1 und 2 bzw. für Medizinprodukte nach der EG-Richtlinie für Medizinprodukte (93/42/EWG)
Inventar-Nr:... Serien-Nr.:... Medizinproduktebuch Ergometer nach 7 MPBetreibV für medizinische Geräte der Anlagen 1 und 2 bzw. für Medizinprodukte nach der EG-Richtlinie für Medizinprodukte (93/42/EWG)
Aktuelles aus dem Medizinprodukterecht
 KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT IN KOOPERATION MIT BERLIN DÜSSELDORF Aktuelles aus dem Medizinprodukterecht DGSV-Kongress 2014 Fulda 09.10.2014 Inhalt 1. AUSBLICK
KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT IN KOOPERATION MIT BERLIN DÜSSELDORF Aktuelles aus dem Medizinprodukterecht DGSV-Kongress 2014 Fulda 09.10.2014 Inhalt 1. AUSBLICK
FAQs Medizinische Hygieneverordnung (MedHygV)
 FAQs Medizinische Hygieneverordnung (MedHygV) 1. Allgemeine Informationen... 2 1.1. Was regelt die MedHygV?... 2 1.2. Für welche ambulanten Einrichtungen ist die MedHygV relevant?... 2 1.3. Was muss der
FAQs Medizinische Hygieneverordnung (MedHygV) 1. Allgemeine Informationen... 2 1.1. Was regelt die MedHygV?... 2 1.2. Für welche ambulanten Einrichtungen ist die MedHygV relevant?... 2 1.3. Was muss der
Medizinprodukte-Überwachung im Land Bremen
 Medizinprodukte-Überwachung im Land Bremen Wiederaufbereitung in HNO- und urologischen Arztpraxen durch die Senatorin für Arbeit, Frauen, Gesundheit, Jugend und Soziales, Referat 34, als zuständige Behörde
Medizinprodukte-Überwachung im Land Bremen Wiederaufbereitung in HNO- und urologischen Arztpraxen durch die Senatorin für Arbeit, Frauen, Gesundheit, Jugend und Soziales, Referat 34, als zuständige Behörde
Freie und Hansestadt Hamburg Behörde für Soziales, Familie, Gesundheit und Verbraucherschutz. Medizinprodukte. Was müssen Betreiber und Anwender tun?
 Freie und Hansestadt Hamburg Behörde für Soziales, Familie, Gesundheit und Verbraucherschutz Medizinprodukte Was müssen Betreiber und Anwender tun? Stand Oktober 2005 Inhalt Leitfaden zum sicheren Betreiben
Freie und Hansestadt Hamburg Behörde für Soziales, Familie, Gesundheit und Verbraucherschutz Medizinprodukte Was müssen Betreiber und Anwender tun? Stand Oktober 2005 Inhalt Leitfaden zum sicheren Betreiben
Umsetzung des Medizinprodukterechts
 Landesamt für Gesundheit und Soziales Abteilung Arbeitsschutz und technische Sicherheit Stofflicher Gefahrenschutz, Strahlenschutz, Verbraucherschutz in der Medizin Umsetzung des Medizinprodukterechts
Landesamt für Gesundheit und Soziales Abteilung Arbeitsschutz und technische Sicherheit Stofflicher Gefahrenschutz, Strahlenschutz, Verbraucherschutz in der Medizin Umsetzung des Medizinprodukterechts
Änderungen der MPBetreibV 2014
 Änderungen der MPBetreibV 2014 3 Instandhaltung von Medizinprodukten (1) Die Instandhaltung von Medizinprodukten umfasst insbesondere Instandhaltungsmaßnahmen und die Instandsetzung. Instandhaltungsmaßnahmen
Änderungen der MPBetreibV 2014 3 Instandhaltung von Medizinprodukten (1) Die Instandhaltung von Medizinprodukten umfasst insbesondere Instandhaltungsmaßnahmen und die Instandsetzung. Instandhaltungsmaßnahmen
Anlage 3. Antrag zur Anerkennung von Praxisnetzen nach 87b Abs. 4 SGB V
 Kassenärztliche Vereinigung Nordrhein E-Mail: praxisnetze@kvno.de Meldestelle -Anerkennung Praxisnetze- Tel.: (02 11) 59 70-8952 Tersteegenstraße 9 Fax: (02 11) 59 70-9952 40474 Düsseldorf Hiermit beantragt
Kassenärztliche Vereinigung Nordrhein E-Mail: praxisnetze@kvno.de Meldestelle -Anerkennung Praxisnetze- Tel.: (02 11) 59 70-8952 Tersteegenstraße 9 Fax: (02 11) 59 70-9952 40474 Düsseldorf Hiermit beantragt
Stand der Bundesimmissionsschutzverordnung zu Legionellen in Verdunstungskühlanlagen
 Für Mensch & Umwelt Stand der Bundesimmissionsschutzverordnung zu Legionellen in Verdunstungskühlanlagen Dr. Regine Szewzyk, Fachgebiet II 1.4 Mikrobiologische Risiken Umweltbundesamt, Berlin Bundesimmissionschutzverrdnung
Für Mensch & Umwelt Stand der Bundesimmissionsschutzverordnung zu Legionellen in Verdunstungskühlanlagen Dr. Regine Szewzyk, Fachgebiet II 1.4 Mikrobiologische Risiken Umweltbundesamt, Berlin Bundesimmissionschutzverrdnung
Monika Rimbach-Schurig Caritas Trägergesellschaft West. Risiken bei von Patienten mitgebrachten Medizingeräten. -Wird das Krankenhaus zum Betreiber?
 Monika Rimbach-Schurig Caritas Trägergesellschaft West Risiken bei von Patienten mitgebrachten Medizingeräten -Wird das Krankenhaus zum Betreiber?- Inhaltsverzeichnis Ausgangslage Betreiberverantwortung
Monika Rimbach-Schurig Caritas Trägergesellschaft West Risiken bei von Patienten mitgebrachten Medizingeräten -Wird das Krankenhaus zum Betreiber?- Inhaltsverzeichnis Ausgangslage Betreiberverantwortung
Anforderungen der Medizinprodukte- Richtlinie an die Entwicklung von Medizinprodukten
 Anforderungen der Medizinprodukte- Richtlinie an die Entwicklung von Medizinprodukten Alexander Fink Hochschule Mannheim SS 2013 A. Fink Seite 1 Steigen wir ein Wo und wie kommt der Medizintechnik-Ingenieur
Anforderungen der Medizinprodukte- Richtlinie an die Entwicklung von Medizinprodukten Alexander Fink Hochschule Mannheim SS 2013 A. Fink Seite 1 Steigen wir ein Wo und wie kommt der Medizintechnik-Ingenieur
ID-Nr.: Serien-Nr.: Medizinproduktebuch. gemäß 7 MPBetreibV
 ID-Nr: Serien-Nr: Medizinproduktebuch gemäß 7 MPBetreibV Anschrift des Betreibers: Gerätebezeichnung: Medizinprodukteverantwortlicher: Gliederung: MPI - Produktebezeichnung / Identifikation / sonstige
ID-Nr: Serien-Nr: Medizinproduktebuch gemäß 7 MPBetreibV Anschrift des Betreibers: Gerätebezeichnung: Medizinprodukteverantwortlicher: Gliederung: MPI - Produktebezeichnung / Identifikation / sonstige
Was geht Qualitätsmanagement/ Qualitätsicherung die Physiotherapeutenan? Beispiel einer zertifizierten Abteilung
 Was geht Qualitätsmanagement/ Qualitätsicherung die Physiotherapeutenan? Beispiel einer zertifizierten Abteilung Angestellten Forum des ZVK Stuttgart 04.03.2016 Birgit Reinecke ZentraleEinrichtungPhysiotherapieund
Was geht Qualitätsmanagement/ Qualitätsicherung die Physiotherapeutenan? Beispiel einer zertifizierten Abteilung Angestellten Forum des ZVK Stuttgart 04.03.2016 Birgit Reinecke ZentraleEinrichtungPhysiotherapieund
Verordnung über das Errichten, Betreiben und Anwenden von Medizinprodukten (Medizinprodukte-Betreiberverordnung MP BetreibV)
 Z A H N Ä R Z T E K A M M E R B R E M E N KÖRPERSCHAFT DES ÖFFENTLICHEN RECHTS Verordnung über das Errichten, Betreiben und Anwenden von Medizinprodukten (Medizinprodukte-Betreiberverordnung MP BetreibV)
Z A H N Ä R Z T E K A M M E R B R E M E N KÖRPERSCHAFT DES ÖFFENTLICHEN RECHTS Verordnung über das Errichten, Betreiben und Anwenden von Medizinprodukten (Medizinprodukte-Betreiberverordnung MP BetreibV)
ARBEITSBOGEN 15: RISIKEN BEI ARZNEIMITTELN UND MEDIZINPRODUKTEN
 I Hinweis zur Bearbeitung des Arbeitsbogens Bearbeiten Sie Meldungen der Arzneimittelkommission der Deutschen Apotheker (AMK), andere Risikomeldungen sowie Berichte über unerwünschte Arzneimittelwirkungen
I Hinweis zur Bearbeitung des Arbeitsbogens Bearbeiten Sie Meldungen der Arzneimittelkommission der Deutschen Apotheker (AMK), andere Risikomeldungen sowie Berichte über unerwünschte Arzneimittelwirkungen
Antrag auf Zertifizierung eines Informationssicherheitsmanagementsystems (ISMS) gem. ISO/IEC 27001:2013 und Fragebogen
 , Hofäckerstr. 32, 74374 Zaberfeld Antrag auf Zertifizierung eines Informationssicherheitsmanagementsystems (ISMS) gem. ISO/IEC 27001:2013 und Fragebogen Das nachfolgend aufgeführte Unternehmen (im Folgenden
, Hofäckerstr. 32, 74374 Zaberfeld Antrag auf Zertifizierung eines Informationssicherheitsmanagementsystems (ISMS) gem. ISO/IEC 27001:2013 und Fragebogen Das nachfolgend aufgeführte Unternehmen (im Folgenden
Überprüfung der Qualifikation des Personals nach 14, 52a, 63a, 72 Abs. 2 und 74a AMG
 Seite 2 von 5 1 Zweck Diese Verfahrensanweisung regelt das Verfahren zur Feststellung der erforderlichen Qualifikation bei Personen, die eine oder mehrere der folgenden Tätigkeiten auszuüben beabsichtigen:
Seite 2 von 5 1 Zweck Diese Verfahrensanweisung regelt das Verfahren zur Feststellung der erforderlichen Qualifikation bei Personen, die eine oder mehrere der folgenden Tätigkeiten auszuüben beabsichtigen:
Guideline für Klasse I Hersteller Abgrenzung und Klassifizierung
 Guideline für Klasse I Hersteller Abgrenzung und Klassifizierung CMI Workshop Medizinprodukte Klasse I Vademecum für den Marktzugang 29.11.2011 Bundesministerium für Gesundheit Seite 1 Aufgabenbereiche
Guideline für Klasse I Hersteller Abgrenzung und Klassifizierung CMI Workshop Medizinprodukte Klasse I Vademecum für den Marktzugang 29.11.2011 Bundesministerium für Gesundheit Seite 1 Aufgabenbereiche
Qualitätsmanagement für die Urindiagnostik (Teil 1)
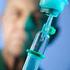 Qualitätsmanagement für die Urindiagnostik (Teil 1) mit praktischen Anmerkungen zur Umsetzung der Qualitätssicherung nach der Richtlinie der Bundesärztekammer Josefine Neuendorf MTLA, Dozentin für Labordiagnostik,
Qualitätsmanagement für die Urindiagnostik (Teil 1) mit praktischen Anmerkungen zur Umsetzung der Qualitätssicherung nach der Richtlinie der Bundesärztekammer Josefine Neuendorf MTLA, Dozentin für Labordiagnostik,
Rahmenvereinbarung 1 für Qualitätssicherungsvereinbarungen gemäß 135 Abs. 2 SGB V
 Rahmenvereinbarung 1 für Qualitätssicherungsvereinbarungen gemäß 135 Abs. 2 SGB V 1 Anwendungsbereich (1) Die nachstehenden Regelungen enthalten für den vertraglich geregelten Bereich der Qualitätssicherung
Rahmenvereinbarung 1 für Qualitätssicherungsvereinbarungen gemäß 135 Abs. 2 SGB V 1 Anwendungsbereich (1) Die nachstehenden Regelungen enthalten für den vertraglich geregelten Bereich der Qualitätssicherung
zu teamwork mit Haken und Ösen.
 vom Spagat der Verantwortlichkeit zur Rechtspflicht zu teamwork mit Haken und Ösen. Seminaris Medizinrecht seminaris.medizinrecht@t-online.de Hans-Werner Röhlig 46047 Oberhausen, Seilerstraße 106 Tel.:
vom Spagat der Verantwortlichkeit zur Rechtspflicht zu teamwork mit Haken und Ösen. Seminaris Medizinrecht seminaris.medizinrecht@t-online.de Hans-Werner Röhlig 46047 Oberhausen, Seilerstraße 106 Tel.:
Richtlinie. des Gemeinsamen Bundesausschusses
 Anlage Richtlinie des Gemeinsamen Bundesausschusses über Maßnahmen zur Qualitätssicherung für die stationäre Versorgung bei der Indikation Bauchaortenaneurysma (Qualitätssicherungs-Richtlinie zum Bauchaortenaneurysma,
Anlage Richtlinie des Gemeinsamen Bundesausschusses über Maßnahmen zur Qualitätssicherung für die stationäre Versorgung bei der Indikation Bauchaortenaneurysma (Qualitätssicherungs-Richtlinie zum Bauchaortenaneurysma,
Die Qualitätsmanagement-Richtlinie des Gemeinsamen Bundesausschusses: Was ist neu?
 Die Qualitätsmanagement-Richtlinie des Gemeinsamen Bundesausschusses: Was ist neu? Dr. Barbara Pietsch Gemeinsamer Bundesausschuss Abteilung Fachberatung Medizin 23. Jahrestagung der GQMG 29.-30.04.2016,
Die Qualitätsmanagement-Richtlinie des Gemeinsamen Bundesausschusses: Was ist neu? Dr. Barbara Pietsch Gemeinsamer Bundesausschuss Abteilung Fachberatung Medizin 23. Jahrestagung der GQMG 29.-30.04.2016,
Anforderungen an die Qualität von Einmalschutzhandschuhen in Gesundheitseinrichtungen
 Anforderungen an die Qualität von Einmalschutzhandschuhen in Gesundheitseinrichtungen Die aktualisierte Richtlinie Nr. 11 des Arbeitskreises für Hygiene in Gesundheitseinrichtungen der MA 15 was ist neu?
Anforderungen an die Qualität von Einmalschutzhandschuhen in Gesundheitseinrichtungen Die aktualisierte Richtlinie Nr. 11 des Arbeitskreises für Hygiene in Gesundheitseinrichtungen der MA 15 was ist neu?
Häufig gestellte Fragen zur Richtlinie der Bundesärztekammer zur Qualitätssicherung laboratoriumsmedizinischer Untersuchungen
 Allgemeine Fragen 1. Wer muss die Richtlinie anwenden? Gemäß 4a Absatz (1) Medizinprodukte-Betreiberverordnung (MPBetreibV) müssen alle Personen, die laboratoriumsmedizinische Untersuchungen durchführen,
Allgemeine Fragen 1. Wer muss die Richtlinie anwenden? Gemäß 4a Absatz (1) Medizinprodukte-Betreiberverordnung (MPBetreibV) müssen alle Personen, die laboratoriumsmedizinische Untersuchungen durchführen,
Effektivität und Effizienz des Medizinprodukt-Vigilanzsystems Potentiale für die Steigerung der Patientensicherheit
 Effektivität und Effizienz des Medizinprodukt-Vigilanzsystems Potentiale für die Steigerung der Patientensicherheit APS Jahrestagung April 2015 Berlin Uvo M. Hölscher Aktionsbündnis Patientensicherheit
Effektivität und Effizienz des Medizinprodukt-Vigilanzsystems Potentiale für die Steigerung der Patientensicherheit APS Jahrestagung April 2015 Berlin Uvo M. Hölscher Aktionsbündnis Patientensicherheit
Medizingeräte-Information 42/06
 Gewerbeaufsicht Medizingeräte-Information 42/06 Medizingeräte Aktion 2005 Überprüfung des sicherheitstechnischen Zustandes von aktiven, nicht implantierbaren Medizinprodukten bei HNO-Ärzten Impressum Herausgeber:
Gewerbeaufsicht Medizingeräte-Information 42/06 Medizingeräte Aktion 2005 Überprüfung des sicherheitstechnischen Zustandes von aktiven, nicht implantierbaren Medizinprodukten bei HNO-Ärzten Impressum Herausgeber:
