Minimale Belastungen und Risiken in der biomedizinischen Forschung mit Menschen
|
|
|
- Hetty Marie Kaufer
- vor 6 Jahren
- Abrufe
Transkript
1 Minimale Belastungen und Risiken in der biomedizinischen Forschung mit Menschen Heiner Raspe Seniorprofessur für Bevölkerungsmedizin Fortbildungsveranstaltung Arbeitskreis Medizinischer Ethikkommissionen Berlin, 17. Juni 2015
2 ZIELE Verfahrensentlastung für Forscher und Ethikkommissionen! Einschluss weiterer vulnerabler Gruppen in die gruppennützige Forschung?
3 Gruppennützige Forschung Nutzen nicht für die Teilnehmer an einer Studie, sondern für externe Personen, auf die alle Ein- und Ausschlusskriterien des Studienprotokolls zutreffen.
4 Belastungen und Risiken (Aspekt Eigenschaden) Belastungen (burden) Alle mit der gesamten Studie unmittelbar verbundenen, nahezu unvermeidbaren und vom Studienteilnehmer erlebbaren leiblichen und seelischen Beeinträchtigungen (oft von kurzer Dauer). Risiken (risks) Alle relevanten negativen Veränderungen des vorherigen körperlichen und seelischen Zustands der Studienteilnehmer, die in einem definierten Folgezeitraum, mit definierter Häufigkeit und länger anhaltend nach der Studienteilnahme zu erwarten sind (enge Definition).
5 Belastungen und Risiken Für wen? Studienteilnehmer Gruppe Angehörige/Umgebungspersonen Umwelt Kostenträger Wissenschaft Wie schwer? Relevanz und Ausmaß (Abstufungen, z.b. NRS 0-10) Wodurch? Spezifische Exposition (Prüfpräparat) Kollaterale Umstände: - Prüfung d. Einschlusskriterien - Provokation - Outcomes-Messung - Fragebogen - insuffizienter Datenschutz Wie wahrscheinlich? Sehr häufig: >1 unter 10 Sehr selten: < 1 von Wie sicher ist die zu Grunde liegende Evidenz? In dubio CONTRA reum
6 Paling Perspective Scale Risks with which we are at home Auftretenswahrscheinlichkeit liegt unter 1 von
7 Subjektivität der Risikoabstufung Mit welchem Risiko, mit welcher Belastung ist ein Allergie-Hauttest (z.b. Pricktest) verbunden? minimal, ein bisschen grösser als minimal oder mehr als nur ein bisschen grösser als minimal?
8 Subjektivität der Risikoabstufung Mit welchem Risiko, welcher Belastung ist ein Allergie-Hauttest (z.b. Pricktest) verbunden? minimal (23 %) ein bisschen grösser als minimal (43 %) mehr als nur ein bisschen grösser als minimal? (27 %) Befragung von 188 EK-Vorsitzenden (s. JAMA 2004; 291: ) A single blood draw was the only procedure categorized as minimal risk by a majority (152 or 81%) of the 188 respondents. An electromyogram was categorized as minimal or a minor increase over minimal risk by 100 (53%) and as more than a minor increase over minimal risk by 77 (41%).
9 Bundesärztekammer: Abstufung von Risiken/Belastungen ein schwieriges Geschäft Trotz zahlreicher Versuche liegt keine allgemein anerkannte Definition der Begriffe minimales Risiko und minimale Belastung vor. Wo diese Begriffe anwendbar sind, kommt der Ethik-Kommission die anspruchsvolle Aufgabe zu, in Abhängigkeit von der jeweiligen Studie zu entscheiden, ob Risiko und Belastung durch eine konkrete Maßnahme noch minimal sind oder nicht. Ein Beispielkatalog minimaler Risiken und Belastungen in einem Leitfaden kann für diese Entscheidung eine hilfreiche Handreichung darstellen. (aus BÄK Stellungnahme zum Leitfaden des Europarats vom )
10 Definitionsversuche (AMG) Minimales Risiko (nach 41 Abs. 2 Nr. 2d AMG) wenn nach Art und Umfang der Intervention zu erwarten ist, dass sie allenfalls zu einer sehr geringfügigen und vorübergehenden Beeinträchtigung der Gesundheit der betroffenen Person führen wird. Minimale Belastung (nach ( 41 Abs. 2 Nr. 2d AMG) wenn zu erwarten ist, dass die Unannehmlichkeiten für die betroffene Person allenfalls vorübergehend auftreten und sehr geringfügig sein werden.
11 Definitionsversuche (Leitfaden Europarat) Studien mit minimalen Risiken bzw. mit minimalen Belastungen sind solche bei denen im Hinblick auf die Art und den Schweregrad der Intervention(en) auch im schlimmsten Fall nur äußerst geringfügige und vorübergehende schädliche Auswirkungen auf die Gesundheit des Forschungsteilnehmers zu erwarten sind. bei denen zu erwarten ist, dass jegliches vorhersehbare Unbehagen aufseiten der Forschungsteilnehmer im Zusammenhang mit dem Forschungsprojekt auch im schlimmsten Fall nur äußerst geringfügig und vorübergehend ist.
12 Genannt sind 4 Beispiele von Studienmaßnahmen mit minimalem Risiko/Belastung nicht-invasive Gewinnung von Körperflüssigkeiten, z. B. eine Speichel- oder Urinprobe oder ein Wangenschleimhautabstrich Blutabnahme aus einer peripheren Vene oder Entnahme von Kapillarblut, bei der Entnahme von Gewebeproben z. B. während eines chirurgischen Eingriffs werden zusätzliche kleine Gewebeproben entnommen, geringfügige Erweiterungen von nicht-invasiven diagnostischen Maßnahmen unter Verwendung technischer Ausrüstung, wie z. B. Ultraschall, ein Ruhe-EKG, eine Röntgenaufnahme, eine CT-Aufnahme oder eine MRT-Aufnahme ohne Kontrastmittel
13 Definitionsversuche (EK Lübeck) Einstufung als Low Risk Studie, wenn einwilligungsfähige Personen rekrutiert werden und eine informierte Einwilligung eingeholt wird und keine genetischen Analysen stattfinden und nicht mehr als minimale Risiken/Belastungen* erkennbar sind. Beispiel minimales Risiko: einmalige venöse Blutentnahme von max. 50 ml Beispiel minimale Belastung: eine Nacht im Schlaflabor verbringen; an einem neuropsychologischen Testverfahren teilnehmen
14 Weitere Beispiele von Studien mit minimalem Risiko/Belastung Fragebogensurvey mit wenigstens sicher pseudonymisierten Daten Nutzung von Überschussmaterialien retrospektive Analyse an der Quelle anonymisierter Patientendaten (aus Akten, Archiven) Nicht-interventionelle Arzneimittelprüfungen ( AWB ) nach 4 (23) Satz 3 AMG. Diese Studien sind ausgezeichnet durch sehr geringfügige und seltene und vorübergehende studienbedingte Belastungen (NRS 0, 1, 2) und durch maximal geringfügige, seltene und vorübergehende studienbedingte Risiken (NRS 0, 1)
15 Aber Zu beachten sind Interaktionseffekte von Qualität x Schwere x Häufigkeit x Sicherheit von Risiken! Daher ist in jedem Fall ein Wert-, Kriterien- und Datenbasiertes Urteil von Nöten. Eine algorithmische Lösung wäre inadäquat.
16 Risikominimierung Es ist denkbar, eine grenzwertig belastende und/oder riskante Studie durch Belastungs- und/oder Risikominimierung in eine low risk -Studie zu verwandeln, z.b. durch angemessenen Datenschutz Umstellung auf nicht-invasive Erhebungen.
17 Und noch eine Frage: WIE HÄLT ES DIE EU-VERORDNUNG MIT MINIMALEM RISIKO BZW. MINIMALER BELASTUNG?
18 1. Aspekt Minimalinterventionelle klinische Prüfung ist eine klinische Prüfung, die alle folgenden Bedingungen erfüllt: a) Prüfpräparate zugelassen b) Verwendung der Prüfpräparate gemäß Zulassungsbedingungen oder evidenzbasierte Verwendung im Mitgliedsstaat (untermauert durch Veröffentlichungen) c) zusätzliche studienbedingte Verfahren im Vergleich zur normalen Praxis nur minimales zusätzliches Risiko bzw. minimale zusätzliche Belastung für Prüfungsteilnehmer Sie sollten weniger strengen Regeln hinsichtlich der Überwachung, der Anforderungen an den Inhalt des Master Files und die Rückverfolgbarkeit des Prüfpräparates unterliegen (bei gleichem Antragsverfahren)
19 2. Aspekt Gruppennützige klinische Prüfungen mit vulnerablen Gruppen (wie nichteinwilligungsfähige Erwachsene, Minderjährige, schwangere o. stillende Frauen, Notfallpatienten) und sofern die Prüfung den betroffenen Prüfungsteilnehmer im Vergleich zur Standardbehandlung seiner Krankheit nur einem minimalen Risiko und einer minimalen Belastung aussetzt (Artikel 31 g ii)
20 Die Interpretation der Begriffe minimales Risiko und minimale Belastung bedarf eines breiten ethischen Diskurses, der noch nicht abgeschlossen ist. (BÄK, Stellungnahme zum Leitfaden des Europarats vom )
EU Verordnung zu Klinischen Prüfungen Teil 1 des Genehmigungsverfahrens Begutachtung durch die Behörde BfArM Elke Stahl
 EU Verordnung zu Klinischen Prüfungen Teil 1 des Genehmigungsverfahrens Begutachtung durch die Behörde BfArM Elke Stahl Verordnung (EU) 536/2014 Europaweite Harmonisierung und Vereinfachung Verordnung
EU Verordnung zu Klinischen Prüfungen Teil 1 des Genehmigungsverfahrens Begutachtung durch die Behörde BfArM Elke Stahl Verordnung (EU) 536/2014 Europaweite Harmonisierung und Vereinfachung Verordnung
Wird die Genehmigung und Durchführung von Low-intervention clinical trials in Zukunft attraktiver? Workshop AGAH u. KKS-Netzwerk, Bonn 06.06.
 Wird die Genehmigung und Durchführung von Low-intervention clinical trials in Zukunft attraktiver? Workshop AGAH u. KKS-Netzwerk, Bonn 06.06.2014 Studienzentrum Bonn www.studienzentrum-bonn.de 1.) Studienzentren
Wird die Genehmigung und Durchführung von Low-intervention clinical trials in Zukunft attraktiver? Workshop AGAH u. KKS-Netzwerk, Bonn 06.06.2014 Studienzentrum Bonn www.studienzentrum-bonn.de 1.) Studienzentren
Patienteninformation und Einverständniserklärung zur Durchführung genetischer Analysen im Zuge einer nichtinterventionelle,
 Patienteninformation und Einverständniserklärung zur Durchführung genetischer Analysen im Zuge einer nichtinterventionelle, prospektive Kohortenstudie Protokoll: Initiator: EuroTARGET: Europäisches Forschungsprojekt
Patienteninformation und Einverständniserklärung zur Durchführung genetischer Analysen im Zuge einer nichtinterventionelle, prospektive Kohortenstudie Protokoll: Initiator: EuroTARGET: Europäisches Forschungsprojekt
Antrag zur Durchführung einer epidemiologischen Untersuchung
 Materialien zu Genetisch-Epidemiologischen Methoden Absender: Antrag zur Durchführung einer epidemiologischen Untersuchung Musterantrag der ad hoc Arbeitsgruppe Epidemiologie des Arbeitskreises Medizinischer
Materialien zu Genetisch-Epidemiologischen Methoden Absender: Antrag zur Durchführung einer epidemiologischen Untersuchung Musterantrag der ad hoc Arbeitsgruppe Epidemiologie des Arbeitskreises Medizinischer
5 Zusammenfassung in Thesenform
 204 5 Zusammenfassung in Thesenform 1. Die im Zuge einer klinischen Prüfung vorgenommene Placeboapplikation unterfällt dem grundsätzlichen Regelungsbereich der 40, 41 AMG und muß sich vorrangig an deren
204 5 Zusammenfassung in Thesenform 1. Die im Zuge einer klinischen Prüfung vorgenommene Placeboapplikation unterfällt dem grundsätzlichen Regelungsbereich der 40, 41 AMG und muß sich vorrangig an deren
07.072. Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA
 07.072 Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA Verfassungsartikel über die Forschung am Menschen Art. 118b Hauptkritikpunkt: Abs 2,Bst c «Fremdnützige Forschung an urteilsunfähigen
07.072 Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA Verfassungsartikel über die Forschung am Menschen Art. 118b Hauptkritikpunkt: Abs 2,Bst c «Fremdnützige Forschung an urteilsunfähigen
NEU! Freundschaftswerbung 150,- Ihre Empfehlung ist uns wichtig!
 Prädiabetiker & Typ2 Diabetiker für unsere Studie gesucht! In dieser Studie werden lediglich Blutproben gesammelt - es wird keine Prüfsubstanz verabreicht! im Alter von 18 bis 64 Jahren Nichtraucher (seit
Prädiabetiker & Typ2 Diabetiker für unsere Studie gesucht! In dieser Studie werden lediglich Blutproben gesammelt - es wird keine Prüfsubstanz verabreicht! im Alter von 18 bis 64 Jahren Nichtraucher (seit
Datenschutz und Recht auf Nichtwissen. Neue ethische Herausforderungen im Rahmen der individualisierten Medizin?
 Datenschutz und Recht auf Nichtwissen. Neue ethische Herausforderungen im Rahmen der individualisierten Medizin? PD Dr. J. Boldt Institut für Ethik und Geschichte der Medizin Universität Freiburg Wozu
Datenschutz und Recht auf Nichtwissen. Neue ethische Herausforderungen im Rahmen der individualisierten Medizin? PD Dr. J. Boldt Institut für Ethik und Geschichte der Medizin Universität Freiburg Wozu
Herzlich Willkommen! Jahrestagung der GMDS Leipzig 2006
 Herzlich Willkommen! Jahrestagung der GMDS Leipzig 2006 Ist-Analyse zur Patientenaufklärung und Einwilligung bei nichteinwilligungsfähigen erwachsenen Patienten Weismüller K, Corvinus U, Ihle P, Harnischmacher
Herzlich Willkommen! Jahrestagung der GMDS Leipzig 2006 Ist-Analyse zur Patientenaufklärung und Einwilligung bei nichteinwilligungsfähigen erwachsenen Patienten Weismüller K, Corvinus U, Ihle P, Harnischmacher
Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz
 Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz 6. Juni 2013 Brigitte Meier Leitung Sektion Forschung am Mensch und Ethik Bundesamt für Gesundheit Inhalt 1.
Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz 6. Juni 2013 Brigitte Meier Leitung Sektion Forschung am Mensch und Ethik Bundesamt für Gesundheit Inhalt 1.
WELTÄRZTEBUND (WMA) DEKLARATION VON HELSINKI Ethische Grundsätze für die medizinische Forschung am Menschen
 Version 2008 WELTÄRZTEBUND (WMA) DEKLARATION VON HELSINKI Ethische Grundsätze für die medizinische Forschung am Menschen Verabschiedet von der 18. WMA Generalversammlung, Juni 1964 Helsinki (Finnland)
Version 2008 WELTÄRZTEBUND (WMA) DEKLARATION VON HELSINKI Ethische Grundsätze für die medizinische Forschung am Menschen Verabschiedet von der 18. WMA Generalversammlung, Juni 1964 Helsinki (Finnland)
AGAH Workshop. Befreiung von der AMG Versicherungspflicht: Voraussetzungen und Implikationen. Markus Ambrosius
 AGAH Workshop 4. Juli 2012 Befreiung von der AMG Versicherungspflicht: Voraussetzungen und Implikationen Rechtsanwalt Markus Ambrosius Sträter Rechtsanwälte Kronprinzenstraße 20 Fon: +49 (0) 228-934 54-0
AGAH Workshop 4. Juli 2012 Befreiung von der AMG Versicherungspflicht: Voraussetzungen und Implikationen Rechtsanwalt Markus Ambrosius Sträter Rechtsanwälte Kronprinzenstraße 20 Fon: +49 (0) 228-934 54-0
Curriculare Fortbildung
 BUNDESÄRZTEKAMMER Bekanntmachungen Der Vorstand der Bundesärztekammer hat in seiner Sitzung vom 19. April 2013 auf Empfehlung der Ständigen Konferenz der Geschäftsführungen und der Vorsitzenden der Ethik-Kommissionen
BUNDESÄRZTEKAMMER Bekanntmachungen Der Vorstand der Bundesärztekammer hat in seiner Sitzung vom 19. April 2013 auf Empfehlung der Ständigen Konferenz der Geschäftsführungen und der Vorsitzenden der Ethik-Kommissionen
Anmerkungen der Bundesärztekammer
 Anmerkungen der Bundesärztekammer ZU DEM BERICHTSENTWURF (2012/0192(COD)) DER BERICHTERSTATTERIN MS. GLENIS WILLMOTT VOM 31.01.2013 zu dem Vorschlag der Europäischen Kommission für eine Verordnung des
Anmerkungen der Bundesärztekammer ZU DEM BERICHTSENTWURF (2012/0192(COD)) DER BERICHTERSTATTERIN MS. GLENIS WILLMOTT VOM 31.01.2013 zu dem Vorschlag der Europäischen Kommission für eine Verordnung des
Sicherheitsgewinn durch den freiwilligen Spenderselbstausschluss?
 Sicherheitsgewinn durch den freiwilligen Spenderselbstausschluss? S. T. Kiessig, MD, PhD Ruhr-Plasma-Center Bochum Ferdinandstr. 13 D-44789 Bochum e-mail: skiessig@ruhrplasma.de EU? COMMISSION DIRECTIVE
Sicherheitsgewinn durch den freiwilligen Spenderselbstausschluss? S. T. Kiessig, MD, PhD Ruhr-Plasma-Center Bochum Ferdinandstr. 13 D-44789 Bochum e-mail: skiessig@ruhrplasma.de EU? COMMISSION DIRECTIVE
WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht. Mittwoch, 13. Januar 2010. Pandemie - Teil X
 Ministerium für,,, und WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht Mittwoch, 13. Januar 2010 Pandemie - Teil X -Dr. Michael Cramer-2010-01-13 Folie 1 Ministerium für,,, und Klinische Prüfungen
Ministerium für,,, und WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht Mittwoch, 13. Januar 2010 Pandemie - Teil X -Dr. Michael Cramer-2010-01-13 Folie 1 Ministerium für,,, und Klinische Prüfungen
EUREKA-Register des Europäischen Leukämienetzes (ELN) Patienteninformation
 Universitätsklinikum Jena Prof. Dr. Andreas Hochhaus Klinik für Innere Medizin II Tel. 03641 932 4201 Abteilung Hämatologie/Onkologie Fax 03641 932 4202 Erlanger Allee 101 cml@med.uni-jena.de 07740 Jena
Universitätsklinikum Jena Prof. Dr. Andreas Hochhaus Klinik für Innere Medizin II Tel. 03641 932 4201 Abteilung Hämatologie/Onkologie Fax 03641 932 4202 Erlanger Allee 101 cml@med.uni-jena.de 07740 Jena
VERGLEICH. von NICHT-INTERVENTIONELLEN STUDIEN (NIS) mit KLINISCHEN PRÜFUNGEN (AMG) Klinische Studienzentrale (CSC UMMD ) Antje Wiede
 1 VERGLEICH von NICHT-INTERVENTIONELLEN STUDIEN (NIS) mit KLINISCHEN PRÜFUNGEN (AMG) Klinische Studienzentrale (CSC UMMD ) Antje Wiede 2 Überblick Definitionen Ziele/Indikation einer NIS Begriff der Intervention
1 VERGLEICH von NICHT-INTERVENTIONELLEN STUDIEN (NIS) mit KLINISCHEN PRÜFUNGEN (AMG) Klinische Studienzentrale (CSC UMMD ) Antje Wiede 2 Überblick Definitionen Ziele/Indikation einer NIS Begriff der Intervention
Hinweise zum Versicherungsschutz
 Hinweise zum Versicherungsschutz 1. Versicherungspflicht a) AMG- und MPG-Studien Studien am Menschen zur Prüfung von Arzneimitteln und Medizinprodukten unterliegen einer gesetzlichen Versicherungspflicht
Hinweise zum Versicherungsschutz 1. Versicherungspflicht a) AMG- und MPG-Studien Studien am Menschen zur Prüfung von Arzneimitteln und Medizinprodukten unterliegen einer gesetzlichen Versicherungspflicht
Nicht-interventionelle Studien - Arten, Einsatzgebiete und Erkenntniswert
 Nicht-interventionelle Studien - Arten, Einsatzgebiete und Erkenntniswert Wie Medikamente wirken, welche Nebenwirkungen sie hervorrufen und zahlreiche andere Fragen rund um das Medikament müssen in wissenschaftlichen
Nicht-interventionelle Studien - Arten, Einsatzgebiete und Erkenntniswert Wie Medikamente wirken, welche Nebenwirkungen sie hervorrufen und zahlreiche andere Fragen rund um das Medikament müssen in wissenschaftlichen
Qualitätsmanagement in der klinischen Forschung. Dr. Marc Barthold Stabsstelle Qualitätsmanagement in der klinischen Forschung
 Qualitätsmanagement in der klinischen Forschung Dr. Marc Barthold Stabsstelle Qualitätsmanagement in der klinischen Forschung KERNAUFGABEN: Sicherstellung eines funktionalen Qualitätsmanagements des Sponsors
Qualitätsmanagement in der klinischen Forschung Dr. Marc Barthold Stabsstelle Qualitätsmanagement in der klinischen Forschung KERNAUFGABEN: Sicherstellung eines funktionalen Qualitätsmanagements des Sponsors
Ethische und rechtliche Aspekte bei Investigator Initiated Trials Prof. Dr. Jochen Taupitz
 Ethische und rechtliche Aspekte bei Investigator Initiated Trials Prof. Dr. Jochen Taupitz Prof. Dr. Jochen Taupitz www.imgb.de Seite 1 Was ist ein Investigator Initiated Trial (IIT)? Keine gesetzliche
Ethische und rechtliche Aspekte bei Investigator Initiated Trials Prof. Dr. Jochen Taupitz Prof. Dr. Jochen Taupitz www.imgb.de Seite 1 Was ist ein Investigator Initiated Trial (IIT)? Keine gesetzliche
Klinik für Transplantationsmedizin Univ.-Prof. Dr. med. Hartmut H.-J. Schmidt [Adresse] Patienteninformation/Einwilligungserklärung
![Klinik für Transplantationsmedizin Univ.-Prof. Dr. med. Hartmut H.-J. Schmidt [Adresse] Patienteninformation/Einwilligungserklärung Klinik für Transplantationsmedizin Univ.-Prof. Dr. med. Hartmut H.-J. Schmidt [Adresse] Patienteninformation/Einwilligungserklärung](/thumbs/33/15930247.jpg) Universitätsklinikum Münster. Klinik für Transplantationsmedizin. 48149 Münster [Adresse] Klinik für Transplantationsmedizin Univ.-Prof. Dr. med. Hartmut H.-J. Schmidt Direktor Albert-Schweitzer-Campus
Universitätsklinikum Münster. Klinik für Transplantationsmedizin. 48149 Münster [Adresse] Klinik für Transplantationsmedizin Univ.-Prof. Dr. med. Hartmut H.-J. Schmidt Direktor Albert-Schweitzer-Campus
Was ändert sich durch die 16.AMG-Novelle? Prof. Dr. med. Sebastian Harder
 Was ändert sich durch die 16.AMG-Novelle? Prof. Dr. med. Sebastian Harder Gesetze und Verordnungen Clinical Trials Directive (CTD) Arzneimittelgesetz (AMG) GCP-Verordnung (GCP-V) Neu ab 19. Oktober 2012:
Was ändert sich durch die 16.AMG-Novelle? Prof. Dr. med. Sebastian Harder Gesetze und Verordnungen Clinical Trials Directive (CTD) Arzneimittelgesetz (AMG) GCP-Verordnung (GCP-V) Neu ab 19. Oktober 2012:
Reorganisation 2009 der Kantonalen Ethikkommission
 Informationsveranstaltung 15.9.2009 Reorganisation 2009 der Kantonalen Ethikkommission Gesundheitsdirektion Grusswort von RR Dr. Thomas Heiniger (s.separates Dokument) Seite 2 Die KEK Reorganisation im
Informationsveranstaltung 15.9.2009 Reorganisation 2009 der Kantonalen Ethikkommission Gesundheitsdirektion Grusswort von RR Dr. Thomas Heiniger (s.separates Dokument) Seite 2 Die KEK Reorganisation im
Anforderungen an eine patientenorientierte Arzneimittelanwendungsforschung
 Anforderungen an eine patientenorientierte Arzneimittelanwendungsforschung Prof. Dr. Marion Schaefer Institut für Klinische Pharmakologie / Charité Universitätsmedizin Berlin 3. Eisensymposium / Basel
Anforderungen an eine patientenorientierte Arzneimittelanwendungsforschung Prof. Dr. Marion Schaefer Institut für Klinische Pharmakologie / Charité Universitätsmedizin Berlin 3. Eisensymposium / Basel
Reglement betreffend den Zugriff auf Personendaten zu Forschungszwecken
 Stadt Zürich Stadtspital Waid Zürich Medizinische Direktion Tièchestrasse 99 8037 Zürich Daniel Grob, Dr.med. MHA Zürich, 12. Oktober 2012 /Gr Reglement betreffend den Zugriff auf Personendaten zu Forschungszwecken
Stadt Zürich Stadtspital Waid Zürich Medizinische Direktion Tièchestrasse 99 8037 Zürich Daniel Grob, Dr.med. MHA Zürich, 12. Oktober 2012 /Gr Reglement betreffend den Zugriff auf Personendaten zu Forschungszwecken
Audit/ Inspektion. praktische Beispiele und Hinweise 12. GCP-Kurs am 08.10. und 15.10.2014. Dr. med. Antje Kristina Belau
 Audit/ Inspektion praktische Beispiele und Hinweise 12. GCP-Kurs am 08.10. und 15.10.2014 Dr. med. Antje Kristina Belau Klinik und Poliklinik für Gynäkologie und Geburtshilfe der Ernst- Moritz- Arndt-
Audit/ Inspektion praktische Beispiele und Hinweise 12. GCP-Kurs am 08.10. und 15.10.2014 Dr. med. Antje Kristina Belau Klinik und Poliklinik für Gynäkologie und Geburtshilfe der Ernst- Moritz- Arndt-
Hotel- und Objektausstattung Bedding products for hotels and contract business
 Hotel- und Objektausstattung Bedding products for hotels and contract business Paradies Bettwaren für den guten Schlaf Paradies bedding products for a good night s sleep Seit mehr als 150 Jahren wird die
Hotel- und Objektausstattung Bedding products for hotels and contract business Paradies Bettwaren für den guten Schlaf Paradies bedding products for a good night s sleep Seit mehr als 150 Jahren wird die
Kurzfassung der Studieninformation
 Kurzfassung der Studieninformation Studientitel: Schlafstörungen und Ehlers-Danlos Syndrom Was wir Ihnen mitteilen wollen: Wir möchten Sie hiermit bitten, an unserem Forschungsprojekt als Kontrollperson
Kurzfassung der Studieninformation Studientitel: Schlafstörungen und Ehlers-Danlos Syndrom Was wir Ihnen mitteilen wollen: Wir möchten Sie hiermit bitten, an unserem Forschungsprojekt als Kontrollperson
Risikoadaptiertes Qualitätsmanagement - das ADAMON-Projekt
 Risikoadaptiertes Qualitätsmanagement - das ADAMON-Projekt O. Brosteanu Zentrum für Klinische Studien Leipzig - KKS TMF Jahreskongress 16. April 2010 1 Motivation Wesentliche Ziele der Good Clinical Practice
Risikoadaptiertes Qualitätsmanagement - das ADAMON-Projekt O. Brosteanu Zentrum für Klinische Studien Leipzig - KKS TMF Jahreskongress 16. April 2010 1 Motivation Wesentliche Ziele der Good Clinical Practice
Aktuelle radiologische Diagnostik und Therapie im Gefäßsystem
 Aktuelle radiologische Diagnostik und Therapie im Gefäßsystem Prof. Dr. med. Frank Wacker Patient mit Schaufensterkrankheit H.B., 54 Jahre alt, Versicherungsvertreter Kann seit 4 Wochen nur 100 m ohne
Aktuelle radiologische Diagnostik und Therapie im Gefäßsystem Prof. Dr. med. Frank Wacker Patient mit Schaufensterkrankheit H.B., 54 Jahre alt, Versicherungsvertreter Kann seit 4 Wochen nur 100 m ohne
Personalisierte Medizin Ende der Solidarität? Heiner Raspe Seniorprofessur für Bevölkerungsmedizin
 Personalisierte Medizin Ende der Solidarität? Heiner Raspe Seniorprofessur für Bevölkerungsmedizin Berlin - Deutscher Ethikrat 24.Mai 2012 Kritische Anmerkungen zur PersoMed Unter falscher Flagge Kritische
Personalisierte Medizin Ende der Solidarität? Heiner Raspe Seniorprofessur für Bevölkerungsmedizin Berlin - Deutscher Ethikrat 24.Mai 2012 Kritische Anmerkungen zur PersoMed Unter falscher Flagge Kritische
Regelungen zum Embryonenschutz
 Einfachgesetzliche Regelungen Regelungen zum Embryonenschutz 1 2 3 Embryonenschutzgesetz Stammzellgesetz Bisher noch nicht erlassen: Fortpflanzungsmedizingesetz Konkurrierende Gesetzgebungskompetenz des
Einfachgesetzliche Regelungen Regelungen zum Embryonenschutz 1 2 3 Embryonenschutzgesetz Stammzellgesetz Bisher noch nicht erlassen: Fortpflanzungsmedizingesetz Konkurrierende Gesetzgebungskompetenz des
Anlage 1 Auszufüllen im operierenden Zentrum Patienteninformation und Einwilligungserklärung NovaSure Register
 Kontaktdaten des operierenden medizinischen Zentrums: (Vom Zentrum einzufügen) Kontaktdaten des nachbehandelnden niedergelassen Arztes: (Vom Zentrum einzufügen) Sehr geehrte Patientin, bitte lesen Sie
Kontaktdaten des operierenden medizinischen Zentrums: (Vom Zentrum einzufügen) Kontaktdaten des nachbehandelnden niedergelassen Arztes: (Vom Zentrum einzufügen) Sehr geehrte Patientin, bitte lesen Sie
Klinische Prüfungen von Arzneimitteln aktuelle Anforderungen
 Klinische Prüfungen von Arzneimitteln aktuelle Anforderungen Aus der Sicht der Überwachungsbehörde Sabine Hofsäss (Regierungspräsidium Karlsruhe) Gemeinsame Ziele: Sicherheit, Rechte und Wohl der Patienten
Klinische Prüfungen von Arzneimitteln aktuelle Anforderungen Aus der Sicht der Überwachungsbehörde Sabine Hofsäss (Regierungspräsidium Karlsruhe) Gemeinsame Ziele: Sicherheit, Rechte und Wohl der Patienten
Klinische Prüfung mit Medizinprodukten nach CE-Kennzeichnung Rechtsanwalt Michael Wimmer
 Klinische Prüfung mit Medizinprodukten nach CE-Kennzeichnung Rechtsanwalt Michael Wimmer RA Michael Wimmer c/o Boehringer Ingelheim GmbH Corp. Legal Biopharmaceuticals // R&D+M Binger Straße 173, 55216
Klinische Prüfung mit Medizinprodukten nach CE-Kennzeichnung Rechtsanwalt Michael Wimmer RA Michael Wimmer c/o Boehringer Ingelheim GmbH Corp. Legal Biopharmaceuticals // R&D+M Binger Straße 173, 55216
«Forgetting or remembering?»
 «Forgetting or remembering?» Wohin steuert die Schweizer Kommunikationsbranche nach Google Spain (EuGH-Rs.C-131/12)? 20. Januar 2015 ZAV Fachgruppe IT Weiterbildungsveranstaltung 2015 Dirk Spacek, Rechtsanwalt,
«Forgetting or remembering?» Wohin steuert die Schweizer Kommunikationsbranche nach Google Spain (EuGH-Rs.C-131/12)? 20. Januar 2015 ZAV Fachgruppe IT Weiterbildungsveranstaltung 2015 Dirk Spacek, Rechtsanwalt,
Trial and error in the Eurozone and the influence to currencies and interest rates.
 Jürgen Meyer Trial and error in the Eurozone and the influence to currencies and interest rates. Sept. 24th, 2012 EURUSD long term chart We re in the 8year cycle south still. Target is set at 1,0220 in
Jürgen Meyer Trial and error in the Eurozone and the influence to currencies and interest rates. Sept. 24th, 2012 EURUSD long term chart We re in the 8year cycle south still. Target is set at 1,0220 in
1. Aushändigen der Informationsschrift an die Patientin Q
 1 universitäts Prof. Dr. med. Annegret Geipel Leitung Pränatale Medizin DEGUM Stufe III Spezielle Geburtshilfe und Perinatalmedizin Studienzentrale PraenaTest Frau Claudia Büthke Fon:+49 (0) 228-287 14728
1 universitäts Prof. Dr. med. Annegret Geipel Leitung Pränatale Medizin DEGUM Stufe III Spezielle Geburtshilfe und Perinatalmedizin Studienzentrale PraenaTest Frau Claudia Büthke Fon:+49 (0) 228-287 14728
Gesetz über den Verkehr mit Arzneimitteln - AMG (Arzneimittelgesetz) Abschnitt 5-8 ( 38-55a)
 Gesetz über den Verkehr mit Arzneimitteln - AMG (Arzneimittelgesetz) Abschnitt 5-8 ( 38-55a) Bekanntgabe der Neufassung Bgbl. I, Nr. 73, S.3394 vom 15.12.2005, geändert durch Bgbl. I, Nr. 39, S.1869, Art.12
Gesetz über den Verkehr mit Arzneimitteln - AMG (Arzneimittelgesetz) Abschnitt 5-8 ( 38-55a) Bekanntgabe der Neufassung Bgbl. I, Nr. 73, S.3394 vom 15.12.2005, geändert durch Bgbl. I, Nr. 39, S.1869, Art.12
1.1 Studientitel: XY 1.2 Studienleiter: XY 1.3 Medizinischer Hintergrund
 1.1 Studientitel: XY 1.2 Studienleiter: XY 1.3 Medizinischer Hintergrund Patienten, welche unter chronischer Herzinsuffizienz leiden erleben häufig Rückfälle nach einem klinischen Aufenthalt. Die Ursache
1.1 Studientitel: XY 1.2 Studienleiter: XY 1.3 Medizinischer Hintergrund Patienten, welche unter chronischer Herzinsuffizienz leiden erleben häufig Rückfälle nach einem klinischen Aufenthalt. Die Ursache
Patienteninformation zur Teilnahme am Register und Biobank des Europäischen Netwerks für Nebennierentumoren ENS@T
 Direktor: Prof. Dr. G. Ertl Schwerpunkt Endokrinologie - Diabetologie Leiter: Prof. Dr. B. Allolio Studienleiter: Prof. Dr. M. Fassnacht Medizinische Klinik und Poliklinik I Oberdürrbacher Str. 6 97080
Direktor: Prof. Dr. G. Ertl Schwerpunkt Endokrinologie - Diabetologie Leiter: Prof. Dr. B. Allolio Studienleiter: Prof. Dr. M. Fassnacht Medizinische Klinik und Poliklinik I Oberdürrbacher Str. 6 97080
KURZANLEITUNG. Firmware-Upgrade: Wie geht das eigentlich?
 KURZANLEITUNG Firmware-Upgrade: Wie geht das eigentlich? Die Firmware ist eine Software, die auf der IP-Kamera installiert ist und alle Funktionen des Gerätes steuert. Nach dem Firmware-Update stehen Ihnen
KURZANLEITUNG Firmware-Upgrade: Wie geht das eigentlich? Die Firmware ist eine Software, die auf der IP-Kamera installiert ist und alle Funktionen des Gerätes steuert. Nach dem Firmware-Update stehen Ihnen
Übergeordnete Ziele der EU Clinical Trials Direc6ve
 Übergeordnete Ziele der EU Clinical Trials Direc6ve Einführung eines gemeinsamen, koordinierten Assessments bei mulanaaonalen klinischen Prüfungen in der EU Aber kein zentrales Genehmigungsverfahren NaAonale
Übergeordnete Ziele der EU Clinical Trials Direc6ve Einführung eines gemeinsamen, koordinierten Assessments bei mulanaaonalen klinischen Prüfungen in der EU Aber kein zentrales Genehmigungsverfahren NaAonale
Dokumentation von Patientendaten in klinischen Studien
 Dokumentation von Patientendaten in klinischen Studien ZKS Kolloquium, 16. November 2010 Dorothee Arenz Stellvertretende Leiterin des Medizinischen Bereichs BMBF 01KN0706 Vorlage für eine SOP Standard
Dokumentation von Patientendaten in klinischen Studien ZKS Kolloquium, 16. November 2010 Dorothee Arenz Stellvertretende Leiterin des Medizinischen Bereichs BMBF 01KN0706 Vorlage für eine SOP Standard
Kostenreduktion durch Prävention?
 Gesundheitsökonomische Aspekte der Prävention: Kostenreduktion durch Prävention? Nadja Chernyak, Andrea Icks Jahrestagung DGSMP September 2012 Agenda Spart Prävention Kosten? Ist Prävention ökonomisch
Gesundheitsökonomische Aspekte der Prävention: Kostenreduktion durch Prävention? Nadja Chernyak, Andrea Icks Jahrestagung DGSMP September 2012 Agenda Spart Prävention Kosten? Ist Prävention ökonomisch
Richtlinien der IBCSG-Gewebebank
 INTERNATIONAL BREAST CANCER STUDY GROUP Richtlinien der IBCSG-Gewebebank Genehmigt durch das Exekutivkomitee der IBCSG am 24. März 2006 Genehmigt durch die Ethikkommission der IBCSG am 24. März 2006 Genehmigt
INTERNATIONAL BREAST CANCER STUDY GROUP Richtlinien der IBCSG-Gewebebank Genehmigt durch das Exekutivkomitee der IBCSG am 24. März 2006 Genehmigt durch die Ethikkommission der IBCSG am 24. März 2006 Genehmigt
Was ist eine gute Klinische Studie - die Sicht der Statistik. Peter Martus Institut für Biometrie und Klinische Epidemiologie
 Was ist eine gute Klinische Studie - die Sicht der Statistik Peter Martus Institut für Biometrie und Klinische Epidemiologie Historisches Beispiel James Lind (1716-1794) entwickelte 1747 als britischer
Was ist eine gute Klinische Studie - die Sicht der Statistik Peter Martus Institut für Biometrie und Klinische Epidemiologie Historisches Beispiel James Lind (1716-1794) entwickelte 1747 als britischer
Abschlussarbeit (Diplomarbeiten, Masterarbeiten, Dissertationen) und Ethikkommission
 Abschlussarbeit (Diplomarbeiten, Masterarbeiten, Dissertationen) und Ethikkommission Mit diesen Unterlagen wollen wir Studierende bei der Antragstellung an die Ethikkommission unterstützen. Das Thema Patientinnen/ProbandInnen
Abschlussarbeit (Diplomarbeiten, Masterarbeiten, Dissertationen) und Ethikkommission Mit diesen Unterlagen wollen wir Studierende bei der Antragstellung an die Ethikkommission unterstützen. Das Thema Patientinnen/ProbandInnen
Update Europäische Datenschutz-Grundverordnung
 Update Europäische Datenschutz-Grundverordnung Boris Reibach Carl von Ossietzky Universität Oldenburg 17.3.2016 8. TMF-Jahreskongress Geplante Verabschiedung Formelle Annahme der Sprachfassungen April
Update Europäische Datenschutz-Grundverordnung Boris Reibach Carl von Ossietzky Universität Oldenburg 17.3.2016 8. TMF-Jahreskongress Geplante Verabschiedung Formelle Annahme der Sprachfassungen April
GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG
 GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG Kursleiter: Prof. Dr. Richard F. Schlenk Datum: 1. Schulungstag: 08.10.2014 Name Vorname Anleitung Tragen
GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG Kursleiter: Prof. Dr. Richard F. Schlenk Datum: 1. Schulungstag: 08.10.2014 Name Vorname Anleitung Tragen
TOP-PAPER ARZNEIMITTELINFORMATION
 CAMPUS GROSSHADERN CAMPUS INNENSTADT TOP-PAPER ARZNEIMITTELINFORMATION Dr. Dorothea Strobach, München THE STEPPER 2 THERE ARE WORLDS WAITING. ALL IT TAKES IS ONE SMALL STEP. Terry Pratchett, Stephen Baxter.
CAMPUS GROSSHADERN CAMPUS INNENSTADT TOP-PAPER ARZNEIMITTELINFORMATION Dr. Dorothea Strobach, München THE STEPPER 2 THERE ARE WORLDS WAITING. ALL IT TAKES IS ONE SMALL STEP. Terry Pratchett, Stephen Baxter.
Inequality Utilitarian and Capabilities Perspectives (and what they may imply for public health)
 Inequality Utilitarian and Capabilities Perspectives (and what they may imply for public health) 1 Utilitarian Perspectives on Inequality 2 Inequalities matter most in terms of their impact onthelivesthatpeopleseektoliveandthethings,
Inequality Utilitarian and Capabilities Perspectives (and what they may imply for public health) 1 Utilitarian Perspectives on Inequality 2 Inequalities matter most in terms of their impact onthelivesthatpeopleseektoliveandthethings,
KURZBEWERTUNG DER EUROPÄISCHEN DATENSCHUTZVERORDNUNG
 1 l 5 KURZBEWERTUNG DER EUROPÄISCHEN DATENSCHUTZVERORDNUNG Die wichtigsten Regelungen im Überblick Am 14. April 2016 hat das Europäische Parlament nach mehr als vierjähriger Ver-handlung die Datenschutzverordnung
1 l 5 KURZBEWERTUNG DER EUROPÄISCHEN DATENSCHUTZVERORDNUNG Die wichtigsten Regelungen im Überblick Am 14. April 2016 hat das Europäische Parlament nach mehr als vierjähriger Ver-handlung die Datenschutzverordnung
Bildgebende und interventionelle Strategien bei pavk und akutem peripheren Arterienverschluss
 Bildgebende und interventionelle Strategien bei pavk und akutem peripheren Arterienverschluss J. Tonak P. Bischoff - J.P. Goltz Jörg Barkhausen Definition pavk: periphere arterielle Verschlusskrankheit
Bildgebende und interventionelle Strategien bei pavk und akutem peripheren Arterienverschluss J. Tonak P. Bischoff - J.P. Goltz Jörg Barkhausen Definition pavk: periphere arterielle Verschlusskrankheit
Fallvignette Grippe. Andri Rauch Universitätsklinik für Infektiologie Inselspital Bern andri.rauch@insel.ch
 Fallvignette Grippe 72-jähriger Patient mit schwerer COPD - Status nach mehreren Infektexazerbationen, aktuell stabil - Grippeimpfung nicht durchgeführt wegen langer Hospitalisation nach Unfall - Partnerin
Fallvignette Grippe 72-jähriger Patient mit schwerer COPD - Status nach mehreren Infektexazerbationen, aktuell stabil - Grippeimpfung nicht durchgeführt wegen langer Hospitalisation nach Unfall - Partnerin
TRANSFoRm: ein flexibles Datenschutz-Rahmenwerk für die integrative Forschung mit medizinischen. Studien. gmds 2011, 28 September 2011, Mainz
 Universitätsklinikum Düsseldorf TRANSFoRm: ein flexibles Datenschutz-Rahmenwerk für die integrative Forschung mit medizinischen Versorgungsdaten, Datenregistern und klinischen Studien Wolfgang Kuchinke
Universitätsklinikum Düsseldorf TRANSFoRm: ein flexibles Datenschutz-Rahmenwerk für die integrative Forschung mit medizinischen Versorgungsdaten, Datenregistern und klinischen Studien Wolfgang Kuchinke
01.10.2012. Warum evidenzbasierte Medizin? Was hat mein Patient und wie kann ich ihm am besten helfen?
 NNT und NNH : evidenzbasierte Bewertung von Studien Warum evidenzbasierte Medizin? Curriculum Entwicklungspsychopharmakologie 29.09.2012 Laura Weninger, MME Gesetzliche Vorgaben Berufspolitisch 137 e,
NNT und NNH : evidenzbasierte Bewertung von Studien Warum evidenzbasierte Medizin? Curriculum Entwicklungspsychopharmakologie 29.09.2012 Laura Weninger, MME Gesetzliche Vorgaben Berufspolitisch 137 e,
Update Medien & Kommunikation 2013 Big Data Social CRM, Targeting & Co. Verena Grentzenberg. Senior Associate - Bird & Bird LLP
 Update Medien & Kommunikation 2013 Big Data Social CRM, Targeting & Co. Verena Grentzenberg Senior Associate - Bird & Bird LLP Big Data und der Datenschutz Big Data Besonders große und unstrukturierte
Update Medien & Kommunikation 2013 Big Data Social CRM, Targeting & Co. Verena Grentzenberg Senior Associate - Bird & Bird LLP Big Data und der Datenschutz Big Data Besonders große und unstrukturierte
Auswirkungen der 12. AMG- Novelle auf wissenschaftsgesteuerte Studien die Sicht eines Klinikers -
 Auswirkungen der 12. AMG- Novelle auf wissenschaftsgesteuerte Studien die Sicht eines Klinikers - Priv.-Doz. Dr. A. Erhardt Klinik für Gastroenterologie, Hepatologie und Infektiologie Heinrich-Heine-Universität
Auswirkungen der 12. AMG- Novelle auf wissenschaftsgesteuerte Studien die Sicht eines Klinikers - Priv.-Doz. Dr. A. Erhardt Klinik für Gastroenterologie, Hepatologie und Infektiologie Heinrich-Heine-Universität
Beitrag 7 - Prof. Dr. Rittner, 6. Sommertagung, Berlin, 3.-4.6.2005. Versicherungsfragen
 Versicherungsfragen Christian Rittner im Namen der Versicherungsgruppe (Prof.Dr.Ch.Rittner;Prof.Dr. I.Walter-Sack; Prof.Dr. J.Taupitz; Prof.Dr. I.Wessler) Inhalt Ausgangspunkt: Versicherungsfragen auf
Versicherungsfragen Christian Rittner im Namen der Versicherungsgruppe (Prof.Dr.Ch.Rittner;Prof.Dr. I.Walter-Sack; Prof.Dr. J.Taupitz; Prof.Dr. I.Wessler) Inhalt Ausgangspunkt: Versicherungsfragen auf
RASTERZEUGNIS INNERE MEDIZIN
 An die Ärztekammer RASTERZEUGNIS FÜR DIE AUSBILDUNG ZUR FACHÄRZTIN/ZUM FACHARZT IM HAUPTFA C H INNERE MEDIZIN Herr/Frau geboren am hat sich gemäß den Bestimmungen des Ärztegesetz 1998, i.d.g.f., / (Zutreffendes
An die Ärztekammer RASTERZEUGNIS FÜR DIE AUSBILDUNG ZUR FACHÄRZTIN/ZUM FACHARZT IM HAUPTFA C H INNERE MEDIZIN Herr/Frau geboren am hat sich gemäß den Bestimmungen des Ärztegesetz 1998, i.d.g.f., / (Zutreffendes
FAKULTÄT FÜR HUMAN- UND SOZIALWISSENSCHAFTEN. Projektplan
 Projektplan zur Einreichung bei der Ethikkommission der Fakultät für Human und Sozialwissenschaften der Technischen Universität Chemnitz PROJEKTBEZEICHNUNG Datum des Projektplans: Professur: Studienleitung:
Projektplan zur Einreichung bei der Ethikkommission der Fakultät für Human und Sozialwissenschaften der Technischen Universität Chemnitz PROJEKTBEZEICHNUNG Datum des Projektplans: Professur: Studienleitung:
Veräußerung von Emissionsberechtigungen in Deutschland
 Veräußerung von Emissionsberechtigungen in Deutschland Monatsbericht September 2008 Berichtsmonat September 2008 Die KfW hat im Zeitraum vom 1. September 2008 bis zum 30. September 2008 3,95 Mio. EU-Emissionsberechtigungen
Veräußerung von Emissionsberechtigungen in Deutschland Monatsbericht September 2008 Berichtsmonat September 2008 Die KfW hat im Zeitraum vom 1. September 2008 bis zum 30. September 2008 3,95 Mio. EU-Emissionsberechtigungen
(Text von Bedeutung für den EWR)
 L 324/38 DURCHFÜHRUNGSBESCHLUSS (EU) 2015/2301 R KOMMISSION vom 8. Dezember 2015 zur Änderung der Entscheidung 93/195/EWG hinsichtlich der tierseuchenrechtlichen Bedingungen und der Beurkundung für die
L 324/38 DURCHFÜHRUNGSBESCHLUSS (EU) 2015/2301 R KOMMISSION vom 8. Dezember 2015 zur Änderung der Entscheidung 93/195/EWG hinsichtlich der tierseuchenrechtlichen Bedingungen und der Beurkundung für die
EWOG-SAA 2010 Genetische und immunologische Charakterisierung der Schweren Aplastischen Anämie (SAA) bei Kindern und Jugendlichen
 Studienbeschreibung Titel der Studie EWOG-SAA 2010 Genetische und immunologische Charakterisierung der Schweren Aplastischen Anämie (SAA) bei Kindern und Jugendlichen Studienakronym EWOG-SAA 2010 Internetseite
Studienbeschreibung Titel der Studie EWOG-SAA 2010 Genetische und immunologische Charakterisierung der Schweren Aplastischen Anämie (SAA) bei Kindern und Jugendlichen Studienakronym EWOG-SAA 2010 Internetseite
EURAP EUROPÄISCHES REGISTER FÜR SCHWANGERSCHAFTEN UNTER ANTIEPILEPTIKA
 EURAP EUROPÄISCHES REGISTER FÜR SCHWANGERSCHAFTEN UNTER ANTIEPILEPTIKA Aufruf zur Teilnahme an der Studie zur Pharmakokinetik in der Schwangerschaft und Stillzeit Studie zur Pharmakokinetik in Schwangerschaft
EURAP EUROPÄISCHES REGISTER FÜR SCHWANGERSCHAFTEN UNTER ANTIEPILEPTIKA Aufruf zur Teilnahme an der Studie zur Pharmakokinetik in der Schwangerschaft und Stillzeit Studie zur Pharmakokinetik in Schwangerschaft
Evaluationskonzepte bei neuen Methoden. Analyse und Konsequenz des GKV.SV
 Evaluationskonzepte bei neuen Methoden Analyse und Konsequenz des GKV.SV Dr. Diedrich Bühler Dr. Diedrich Bühler Überblick I) Situation und Position des GKV SV II) Methodenbewertung, Selbstverwaltung /
Evaluationskonzepte bei neuen Methoden Analyse und Konsequenz des GKV.SV Dr. Diedrich Bühler Dr. Diedrich Bühler Überblick I) Situation und Position des GKV SV II) Methodenbewertung, Selbstverwaltung /
http://www.mig.tu-berlin.de
 Management im Gesundheitswesen IV: Gesundheitsökonomische Evaluation Studientypen und Datenquellen; Erfassung und Bewertung von klinischen Ergebnisparametern Querschnittstudie Überblick Studientypen Beobachtungsstudien
Management im Gesundheitswesen IV: Gesundheitsökonomische Evaluation Studientypen und Datenquellen; Erfassung und Bewertung von klinischen Ergebnisparametern Querschnittstudie Überblick Studientypen Beobachtungsstudien
Monitoring und Evaluation nach 2013 Planungen und Ansätze
 Monitoring und Evaluation nach 2013 Planungen und Ansätze Dr. Ines Hartwig Referat für Evaluation und Impact Assessment GD Beschäftigung, Soziale Angelegenheiten und Integration Wien, 7. April 2011 1 Rahmenbedingungen:
Monitoring und Evaluation nach 2013 Planungen und Ansätze Dr. Ines Hartwig Referat für Evaluation und Impact Assessment GD Beschäftigung, Soziale Angelegenheiten und Integration Wien, 7. April 2011 1 Rahmenbedingungen:
XV. Fortbildungsveranstaltung der ARGE Plasmapherese e.v. 20.-21. November 2015 in Berlin
 XV. Fortbildungsveranstaltung der ARGE Plasmapherese e.v. 20.-21. November 2015 in Berlin Dr. iur. Bita Bakhschai Rechtsanwältin Fachanwältin für Medizinrecht Wirtschaftsjuristin (Univ. Bayreuth) Rechtsanwälte
XV. Fortbildungsveranstaltung der ARGE Plasmapherese e.v. 20.-21. November 2015 in Berlin Dr. iur. Bita Bakhschai Rechtsanwältin Fachanwältin für Medizinrecht Wirtschaftsjuristin (Univ. Bayreuth) Rechtsanwälte
Anzahl klinischer Prüfungen und Studien
 Ergebnisse zur PHARMIG Umfrage Klinische Forschung in Österreich 201 ein Überblick zu den Leistungen der pharmazeutischen Industrie in Österreich Anzahl klinischer Prüfungen und Studien Anzahl der klinischen
Ergebnisse zur PHARMIG Umfrage Klinische Forschung in Österreich 201 ein Überblick zu den Leistungen der pharmazeutischen Industrie in Österreich Anzahl klinischer Prüfungen und Studien Anzahl der klinischen
Umgang mit Daten in der Medizinischen Forschung Bedeutung von Datenbrücken
 Umgang mit Daten in der Medizinischen Forschung Bedeutung von Datenbrücken Wolfgang Kuchinke Heinrich-Heine Universität Düsseldorf RDA Deutschland Treffen, Potsdam 20.11.-21.11.2014 Medizinische Forschung
Umgang mit Daten in der Medizinischen Forschung Bedeutung von Datenbrücken Wolfgang Kuchinke Heinrich-Heine Universität Düsseldorf RDA Deutschland Treffen, Potsdam 20.11.-21.11.2014 Medizinische Forschung
17 HmbDSG - Übermittlung an Stellen außerhalb der Bundesrepublik Deutschland
 Stabsstelle Recht / R16 05.01.2015 Datenschutzbeauftragter 42838-2957 Hamburgisches Datenschutzgesetz (HmbDSG) mit Kommentierung des Hamburgischen Beauftragten für Datenschutz und Informationsfreiheit
Stabsstelle Recht / R16 05.01.2015 Datenschutzbeauftragter 42838-2957 Hamburgisches Datenschutzgesetz (HmbDSG) mit Kommentierung des Hamburgischen Beauftragten für Datenschutz und Informationsfreiheit
20 Bildgebende Diagnostik bei Brustimplantaten
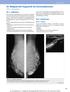 20.2 Implantate 20 Bildgebende Diagnostik bei Brustimplantaten S. Barter, S. H. Heywang-Köbrunner 20.1 Indikation Die kosmetische Augmentation der Brust findet heutzutage eine breite Anwendung. Die Brustrekonstruktion
20.2 Implantate 20 Bildgebende Diagnostik bei Brustimplantaten S. Barter, S. H. Heywang-Köbrunner 20.1 Indikation Die kosmetische Augmentation der Brust findet heutzutage eine breite Anwendung. Die Brustrekonstruktion
Antragstellung an die Ethik-Kommission Formalismen zum Schutz von Patient und eigener Approbation...
 BIOMETRIE-SPLITTER / BIOMETRY BITS 331 C. Baulig 1, J. Hirsch 1, F. Krummenauer 1 Antragstellung an die Ethik-Kommission Formalismen zum Schutz von Patient und eigener Approbation... Vote application to
BIOMETRIE-SPLITTER / BIOMETRY BITS 331 C. Baulig 1, J. Hirsch 1, F. Krummenauer 1 Antragstellung an die Ethik-Kommission Formalismen zum Schutz von Patient und eigener Approbation... Vote application to
Bodenuntersuchungen in Lünen
 Bodenuntersuchungen in Lünen Auftraggeber: Kreis Unna, Fachbereich Natur und Umwelt Durchführung: 45879 Gelsenkirchen Professor Dr. Ulrich Ewers Dipl.-Ing. Michael Sauerwald 1 Bodenuntersuchungen in Lünen
Bodenuntersuchungen in Lünen Auftraggeber: Kreis Unna, Fachbereich Natur und Umwelt Durchführung: 45879 Gelsenkirchen Professor Dr. Ulrich Ewers Dipl.-Ing. Michael Sauerwald 1 Bodenuntersuchungen in Lünen
3 Materialien und Methoden
 3 Materialien und Methoden Insgesamt wurden 526 Dauerblutspender (289 Männer und 237 Frauen) in die Studie eingeschlossen. 3.1 Aufklärung, Einverständniserklärung und Versicherung Ein positives Votum der
3 Materialien und Methoden Insgesamt wurden 526 Dauerblutspender (289 Männer und 237 Frauen) in die Studie eingeschlossen. 3.1 Aufklärung, Einverständniserklärung und Versicherung Ein positives Votum der
Sicherheit um jeden Preis? Bietet die zertifizierte Sicherheit garantierte Sicherheit?
 Sicherheit um jeden Preis? Bietet die zertifizierte Sicherheit garantierte Sicherheit? Roman Haltinner Senior Manager, KPMG Head Information Protection and Business Resilience Glattbrugg, 13.03.2014 Vorstellung
Sicherheit um jeden Preis? Bietet die zertifizierte Sicherheit garantierte Sicherheit? Roman Haltinner Senior Manager, KPMG Head Information Protection and Business Resilience Glattbrugg, 13.03.2014 Vorstellung
Aktuelle Problemfelder der medizinischen Rehabilitation Bedarf - Zugang Prozess - Nachsorge
 Aktuelle Problemfelder der medizinischen Rehabilitation Bedarf - Zugang Prozess - Nachsorge Heiner Raspe Seniorprofessur für Bevölkerungsmedizin Nordrhein-Westfälischer Forschungsverbund Rehabilitationswissenschaften
Aktuelle Problemfelder der medizinischen Rehabilitation Bedarf - Zugang Prozess - Nachsorge Heiner Raspe Seniorprofessur für Bevölkerungsmedizin Nordrhein-Westfälischer Forschungsverbund Rehabilitationswissenschaften
Die Rolle des Sponsors bei der Durchführung Klinischer Prüfungen nach dem Arzneimittelgesetz (AMG) bei Investigator Initiated Trials (IITs)
 1 Die Rolle des Sponsors bei der Durchführung Klinischer Prüfungen nach dem Arzneimittelgesetz (AMG) bei Investigator Initiated Trials (IITs) Klinische Studienzentrale (CSC) Juliane Thapa 2 Inhaltsverzeichnis
1 Die Rolle des Sponsors bei der Durchführung Klinischer Prüfungen nach dem Arzneimittelgesetz (AMG) bei Investigator Initiated Trials (IITs) Klinische Studienzentrale (CSC) Juliane Thapa 2 Inhaltsverzeichnis
Evaluationssatzung für Lehre, Studium, Weiterbildung, Forschung und administrative Dienstleistungen der Pädagogischen Hochschule Weingarten
 Evaluationssatzung für Lehre, Studium, Weiterbildung, Forschung und administrative Dienstleistungen der Pädagogischen Hochschule Weingarten vom 14. Dezember 2012 Aufgrund von 8 Abs. 5 in Verbindung mit
Evaluationssatzung für Lehre, Studium, Weiterbildung, Forschung und administrative Dienstleistungen der Pädagogischen Hochschule Weingarten vom 14. Dezember 2012 Aufgrund von 8 Abs. 5 in Verbindung mit
WMA Deklaration von Helsinki - Ethische Grundsätze für die medizinische Forschung am Menschen
 WMA Deklaration von Helsinki - Ethische Grundsätze für die medizinische Forschung am Menschen Verabschiedet von der 18. WMA-Generalversammlung, Juni 1964 Helsinki (Finnland) und revidiert durch die 29.
WMA Deklaration von Helsinki - Ethische Grundsätze für die medizinische Forschung am Menschen Verabschiedet von der 18. WMA-Generalversammlung, Juni 1964 Helsinki (Finnland) und revidiert durch die 29.
Grosser Preis der Schweiz und Weltcup Finale 2010
 Grosser Preis der Schweiz und Weltcup Finale 2010 13. 15. August 2010 - Dübendorf Seite 1 von 5 Fon: +41 55 647 30 80 Fax: +41 55 647 30 83 E-mail: h.freuler@marelcom.ch Homepage: Turnier / Tournament:
Grosser Preis der Schweiz und Weltcup Finale 2010 13. 15. August 2010 - Dübendorf Seite 1 von 5 Fon: +41 55 647 30 80 Fax: +41 55 647 30 83 E-mail: h.freuler@marelcom.ch Homepage: Turnier / Tournament:
Workshop on the EU Clinical Trials Directive. GMP für Prüfpräparate und die Rolle der sachkundigen Person
 Workshop on the EU Clinical Trials Directive GMP für Prüfpräparate und die Rolle der sachkundigen Person Dr. Gabriele Wanninger Bayer. Landesamt für Klinische Prüfung von Arzneimitteln Ethikkommission
Workshop on the EU Clinical Trials Directive GMP für Prüfpräparate und die Rolle der sachkundigen Person Dr. Gabriele Wanninger Bayer. Landesamt für Klinische Prüfung von Arzneimitteln Ethikkommission
Shareholder Activism by Hedge Funds
 Reihe Alternative Investments Bd. 5 Mihaela Butu Shareholder Activism by Hedge Funds Motivations and Market s Perceptions of Hedge Fund Diplomica Verlag Butu, Mihaela: Shareholder Activism by Hedge Funds:
Reihe Alternative Investments Bd. 5 Mihaela Butu Shareholder Activism by Hedge Funds Motivations and Market s Perceptions of Hedge Fund Diplomica Verlag Butu, Mihaela: Shareholder Activism by Hedge Funds:
Medizinische Klinik und Poliklinik III Direktor: Prof. Dr. med. S. Bornstein
 Medizinische Klinik und Poliklinik III Direktor: Prof. Dr. med. S. Bornstein Patienteninformation zur Teilnahme am Register und Biobank des European Network for the Study of Adrenal Tumours (ENS@T) Sehr
Medizinische Klinik und Poliklinik III Direktor: Prof. Dr. med. S. Bornstein Patienteninformation zur Teilnahme am Register und Biobank des European Network for the Study of Adrenal Tumours (ENS@T) Sehr
Überlastung hat Folgen - Effekte der Arbeitszeit auf gesundheitliche und soziale Beeinträchtigungen. Dr. Anna Arlinghaus
 Überlastung hat Folgen - Effekte der Arbeitszeit auf gesundheitliche und soziale Beeinträchtigungen Dr. Anna Arlinghaus Gesellschaft für Arbeits-, Wirtschafts- und Organisationspsychologische Forschung
Überlastung hat Folgen - Effekte der Arbeitszeit auf gesundheitliche und soziale Beeinträchtigungen Dr. Anna Arlinghaus Gesellschaft für Arbeits-, Wirtschafts- und Organisationspsychologische Forschung
Zertifikate: Nutzen für wen?
 Zertifikate: Nutzen für wen? Zertifikate = Bessere Qualität? Hans Ulrich Rothen, Vorsitzender Qualitätskommission Inselspital Zertifizierungen Überprüfung von Prozessen (Arbeitsabläufen) und deren Ergebnisse
Zertifikate: Nutzen für wen? Zertifikate = Bessere Qualität? Hans Ulrich Rothen, Vorsitzender Qualitätskommission Inselspital Zertifizierungen Überprüfung von Prozessen (Arbeitsabläufen) und deren Ergebnisse
9.4.2005 Amtsblatt der Europäischen Union L 91/13
 9.4.2005 Amtsblatt der Europäischen Union L 91/13 RICHTLINIE 2005/28/EG DER KOMMISSION vom 8. April 2005 zur Festlegung von Grundsätzen und ausführlichen Leitlinien der guten klinischen Praxis für zur
9.4.2005 Amtsblatt der Europäischen Union L 91/13 RICHTLINIE 2005/28/EG DER KOMMISSION vom 8. April 2005 zur Festlegung von Grundsätzen und ausführlichen Leitlinien der guten klinischen Praxis für zur
Die Revision der gemeinsamen Sicherheitsmethoden für die Evaluierung und Bewertung von Risiken 4. Symposium der VPI Hamburg, 14.01.
 Die Revision der gemeinsamen Sicherheitsmethoden für die Evaluierung und Bewertung von Risiken 4. Symposium der VPI Hamburg, 14.01.2014 1 Themen 1. Einführung 2. Revision der CSM Risikobewertung (EU VO
Die Revision der gemeinsamen Sicherheitsmethoden für die Evaluierung und Bewertung von Risiken 4. Symposium der VPI Hamburg, 14.01.2014 1 Themen 1. Einführung 2. Revision der CSM Risikobewertung (EU VO
Zum Risiko vorgeburtlicher Schädigungen
 Zum Risiko vorgeburtlicher Schädigungen Reinhard Meister Beuth Hochschule für Technik, Berlin Meister (Beuth Hochschule Berlin) Arzneimittelsicherheit in der Schwangerschaft Berlin 19.04.2013 1 / 1 Arzneimittel
Zum Risiko vorgeburtlicher Schädigungen Reinhard Meister Beuth Hochschule für Technik, Berlin Meister (Beuth Hochschule Berlin) Arzneimittelsicherheit in der Schwangerschaft Berlin 19.04.2013 1 / 1 Arzneimittel
REACh, die Chemikalienverordnung der EU und ihre Auswirkungen auf CNT?!
 REACh, die Chemikalienverordnung der EU und ihre Auswirkungen auf CNT?! INNO.CNT Jahreskongress 2013 Fellbach, den 20.02.2013 Umgang mit Stoffverboten, 20.06.2012 1 Nanotechnologie und REACh Nanotechnologie
REACh, die Chemikalienverordnung der EU und ihre Auswirkungen auf CNT?! INNO.CNT Jahreskongress 2013 Fellbach, den 20.02.2013 Umgang mit Stoffverboten, 20.06.2012 1 Nanotechnologie und REACh Nanotechnologie
SOP Abdomen auf Station
 Klinik für diagnostische und interventionelle Radiologie/ Nuklearmedizin Version:1.0 SOP Abdomen auf Station Erstellung Änderung Freigabe Name Kaysler Datum 08.03.2010 Unterschrift Verteiler 1 Ziel und
Klinik für diagnostische und interventionelle Radiologie/ Nuklearmedizin Version:1.0 SOP Abdomen auf Station Erstellung Änderung Freigabe Name Kaysler Datum 08.03.2010 Unterschrift Verteiler 1 Ziel und
Bewertungsbestätigung
 201509.428 Delpe Schutzplatte Das erfüllt die höchsten Anforderungen von eco-bau und MINERGIE-ECO im Hinblick auf Röntgenstrasse 44, 8005 Zürich Tel. 044 241 27 22 201509.429 Rewinkel Schutzwinkel für
201509.428 Delpe Schutzplatte Das erfüllt die höchsten Anforderungen von eco-bau und MINERGIE-ECO im Hinblick auf Röntgenstrasse 44, 8005 Zürich Tel. 044 241 27 22 201509.429 Rewinkel Schutzwinkel für
Sjögren- Betroffene Fragen - Experten Antworten. Die OTC- Liste. (Im Internet einzusehen unter: : www.g-ba.de)
 Sjögren- Betroffene Fragen - Experten Antworten Die OTC- Liste (Im Internet einzusehen unter: : www.g-ba.de) Allgemeine Informationen zur OTC- Liste Die Abkürzung OTC kommt aus dem Englischen und bedeutet:
Sjögren- Betroffene Fragen - Experten Antworten Die OTC- Liste (Im Internet einzusehen unter: : www.g-ba.de) Allgemeine Informationen zur OTC- Liste Die Abkürzung OTC kommt aus dem Englischen und bedeutet:
Von OMT lern für OMT ler Newsletter 2/2012. Herzlich willkommen zum dritten Newsletter von proomt e.v.!
 Herzlich willkommen zum dritten Newsletter von proomt e.v.! Wir freuen uns auf diesem Wege Kontakt zu allen proomt e.v. Mitgliedern und allen Interessierten halten zu können. In unseren Newslettern finden
Herzlich willkommen zum dritten Newsletter von proomt e.v.! Wir freuen uns auf diesem Wege Kontakt zu allen proomt e.v. Mitgliedern und allen Interessierten halten zu können. In unseren Newslettern finden
Stellen Gesundheits- und Medizin Apps ein Sicherheitsrisiko dar?
 Stellen Gesundheits- und Medizin Apps ein Sicherheitsrisiko dar? 04.06.2013 Medical Apps 2013 Kathrin Schürmann, Rechtsanwältin 1 2013 ISiCO Datenschutz GmbH All rights reserved 2 1 Chancen und Risiken
Stellen Gesundheits- und Medizin Apps ein Sicherheitsrisiko dar? 04.06.2013 Medical Apps 2013 Kathrin Schürmann, Rechtsanwältin 1 2013 ISiCO Datenschutz GmbH All rights reserved 2 1 Chancen und Risiken
