Kristallstruktur und Mikrostruktur Teil II
|
|
|
- Melanie Albert
- vor 6 Jahren
- Abrufe
Transkript
1 Kristallstruktur und Mikrostruktur Teil II
2 Teil II (Übersicht) 1 Erstarrung/ Grundlagen 2 Erstarrung/ Gefüge (Mikrostruktur) 3 Praktische Aspekte: Schweißen; Thermisches Spritzen 4 Texturanalyse Macherauch
3 Vorlesung 1 Phasendiagramme Phasenübergänge / Klassifikationen Erstarrung Struktur von Schmelzen (ungeordneten Materialien) Keimbildungsvorgänge Homogene Keimbildung Heterogene Keimbildung Literatur 3
4 Definition Phase Eine Phase ist ein Zustand der Materie, in dem sie, bezüglich ihrer chemischen Zusammensetzung und bezüglich ihres physikalischen Zustandes, durch und durch homogen ist. On the Equilibrium of Heterogeneous Substances, Gibbssche Phasenregel P = C F + 2 ( 1) P - Anzahl von Phasen F Anzahl von Freiheitsgraden (Zustandvariablen) C - Anzahl der unabhängigen Teilchensorten J.W. Gibbs
5 Phasendiagramme Ein Phasendiagramm gibt an, welche Phase eines Stoffes bei einer bestimmten Temperatur und bei einem bestimmten Druck stabil ist. Klassifikation nach der Zahl von Teilchensorten (C) Unary (C = 1) Binary (C = 2) Ternary (C = 3) 5
6 Phasendiagramme idealisiertes unary Phasendiagramm Verdampfung (Übergang von flüssig zu gasförmig) Sublimation (Übergang von fest zu gasförmig) Erstarrung (Übergang von flüssig zu fest) Kondensation (Übergang von gasförmig zu flüssig) 6
7 Unary Phasendiagramme - Beispiele Xenon 7
8 Unary Phasendiagramme - Beispiele Wasser (C = 1 H 2 O) Phase Dichte Raumgruppe (g/cm 3 ) Ih 0.92 P6 3 /mmc Ic 0.93 Fd-3m II R -3 VIII I 4 1 /amd 8
9 Binäre Phasendiagramme - Beispiele C = 2 (zwei Komponenten) 2 Elemente 9
10 Binäre Phasendiagramme - Beispiele C = 2 (zwei Komponenten) 2 Verbindungen (Oxide) Na 2 O SiO 2 10
11 Binary Phasendiagramme - Beispiele C = 2 (zwei Komponenten) 1 Element + 1 Verbindung a (Ferrite) bcc g (Austenite) fcc 11
12 Ternäre Phasendiagramme - Beispiel C = 3 Fo Forsterit Mg 2 SiO 4 An Anorthit CaAl 2 Si 2 O 8 12
13 Binäre Phasendiagramme Einfache Klassifikation 1/ Volle Mischbarkeit der Komponenten A und B sowohl im Festzustand als auch in der Schmelze T > Liquidus homohene Schmelze T < Solidus homogener Mischkristall zwischen Si und Ge (a) L L + a S < T < L Zweiphasenfeld L + a a 13
14 2/ Volle Mischbarkeit der Komponenten A und B nur in der Schmelze Typisches Beispiel: Eutektisches Phasendiagramm Binäre Phasendiagramme Einfache Klassifikation Unterhalb der eutektischen Temperatur T E = 183 o C kristalliziert die homogene Schmelze direkt in zwei Mischkritallen a(pb) mit 18.3 at% Sn und b(sn) mit 97.8 at% Sn. T E 14
15 Binäre Phasendiagramme Einfache Klassifikation 3/ Keine Mischbarkeit der Komponenten A und B sowohl in der Schmelze als auch im Festzustand T > 1070 K homogene Schmelze L 2 T < 1070 K flüssige Mischungslücke: 2 Schmelzen mit unterschidlichen Zn Gehalt L 1 L 1 + L 2 T < 590 K 2-Phasen Gebiet: fast rein Pb + fast rein Zn L 1 + Pb praktisch keine Löschligkeit von Pb in Zn und von Zn in Pb! Pb + Zn Keine chemische Affinität zwischen der beiden Komponenten 15
16 Binäre Phasendiagramme Einfache Klassifikation 4/ Phasendiagramme mit Verbindungen (intermetallischen Phasen) Bei einer starken Affinität zwischen der beiden Komponenten ist die Bildung von intermetallischen Phasen bevorzugt. F m -3 m 16
17 Phasenübergänge Die Umwandlung einer Phase eines Stoffes in eine andere Phase ist Phasenübergang (bzw. eine Phasenumwandlung oder Phasentransformation) genannt. Klassifikationen Strukturelle Thermodynamische Kinetische 17
18 Strukturelle Klassifikation von Phasenübergängen Diskontinuierliche Martensitische Kontinuierliche Dizplazive Ordnung-Unordnung Bond-Breaking und Bond-Rekonstruktion der primären chemischen Bindungen Graphit Diamant hcp fcc, fcc hcp Kooperative Bewegung der Atome durch Scherung NiTi Fe-Mn, Fe-Ni, Stahl Bond-Breaking und Bond-Rekonstruktion nur in der zweiten (dritten) Koordinationsspäre ß-Quarz α-quarz AuCu 18
19 Strukturelle Klassifikation von Phasenübergängen Diskontinuierliche P 6 3 /mmc Fd3m Änderung der Koodinationzahl (CN 3 4) 19
20 Strukturelle Klassifikation von Phasenübergängen Displazive Raumgruppe Raumgruppe P P Die ersten Koordinationen von Si und O in der beiden Phasen sind gleiche, nur kleine Rotationen der Tetrahedra (SiO 4 ) findet statt. 20
21 Kinetische Klassifikation von Phasenübergängen Nullte Ordnung Ṙ ist konstant Erste Ordnung Ṙ = f(konzentration einer Ausgangsphase) Zweite Ordnung Ṙ = f (Konzentrationen von zwei Ausgangs- Phasen) Ṙ - Reaktionsrate 21
22 Thermodynamische Klassifikation (Ehrenfest Klassifikation) Gibbssche Energie G = H pv ST (2) S = - G/ T P V = - G/ p T (3a) (3b) C p = T ( S/ T p ) = - T ( 2 G/ T 2 p ) ß = -1/V ( V/ p T ) = 1/V ( 2 G/ p 2 T ) (3c) (3d) Paul Ehrenfest ( ) 22
23 Thermodynamische Klassifikation (Ehrenfest Klassifikation) 1. Ordnung 2. Ordnung Die ersten Ableitungen der Die ersten Ableitungen der Gibbsschen Energie zeigen Gibbsschen Energie zeigen Sprünge. keine Sprünge. Die zweiten Ableitungen zeigen Sprünge. 23
24 Thermodynamische Klassifikation (Ehrenfest Klassifikation) 24
25 Thermodynamische Klassifikation (Ehrenfest Klassifikation) 1. Ordnung 2. Ordnung Beispiele Erstarren (Kristallization) Ferroelektrizität Kondensation Ferromagnetismus Sublimation Supraleitung Martensitische Umwandlungen Merkmale Keimbildung Keimbildung Aktivierungsschwelle für die Keimbildung Latente Wärme L = T(S 1 S 2 ) keine Aktivierungsschwelle für Keimbildung keine latente Wärme Koexistenz der beiden Phasen 25
26 Phasenübergang Flüssig Festzustand Erstarrung Festzustand: Kristalline Stoffe Quasikristalle Nicht-kristall. Festkörper (Gläser) Flüssigzustand: Flüssigkeiten Schmelzen 26
27 Phasenübergang Flüssig Fest Erstarrung Thermodynamische Bedingung für Erstarrung G S < G L bei T < T m (4) Die Triebkraft für die Erstarrung ist die Differenz DG = G L G S ~ DT (Unterkühlung) (5) G G L Welcher Festzusand formiert sich? T DT T m G S T 27
28 Phasenübergang Flüssig Fest Erstarrung Abkühlen Zustand Prozess langsam Kristalle (kristalline Festkörper) Kristallisation schnell Gläser (amorphe Festkörper) Amorphisation 28
29 Phasenselektion/Unterkühlungsgrad Abkühlrate und/oder rasches Abkühlen Unterkühlungsgrad Glas 29
30 Glasübergangstemperatur 1 Unterkühlte Schmelze T g Glasübergangstemperatur T g ist abhängig von dem Abkühlgrad Rössler (2000) Festkörper (Glas oder Kristall) 1 Schmelze 30
31 Glasübergangstemperatur 31
32 Strukturvergleich von kristallinen und amorphen Stoffen Arten räumlicher Ordnung TS Translationssymmetrie LRO Fernordnung MRO Mittelreichweitige Ordnung SRO - Nahreichweitige Ordnung Stoffe TS LRO MRO SRO Kristalline Quasikrist. Amorphe Das Verständnis der Struktur von Schmelzen ist notwendig für die Beschreibung der Keimbildungsvorgängen. 32
33 Struktur von ungeordneten Materialien SRO - MRO - SiO 4 Tetraeder Ringe von SiO 4 Tetraeder 33
34 Paarkorrelationsfunktion g(r) g(r) = N(r)/(r o 4pr 2 dr) (6a) r o = N/V mittlere numerische Dichte des Stoffes N(r) die Zahl von Teilchen zwichen der Schichten mit Radien r und r + dr g(r) hat zentrale Bedeutung für die Beschreibung von Schmelzen, Flüssigkeiten und amorphen Festkörper. 34
35 Experimentelle Bestimmung der Paarkorrelationsfunktion g(r) Beugungsmessung Intensität I(Q); Q = 4p/l sin(q) Am AlZr Dünnschicht Structure Factor S(Q) = I(Q)/<f 2 (Q)> = 1 + (I(Q) - <f 2 (Q)>)/ <f 2 (Q)> (6b) Al 0.67 Zr 0.33 : <f 2 > = 0.67f Al f Zr2 ; I(Q) I(Q) f 2 Paarkorrelationsfunktion (Fourier Transformation) g(r) = 1 + (1/4pr o r)2/p Q [S(Q) 1]sin(Qr)dQ (6c) Q (A -1 ) g(r) R (A) 35
36 Paarkorrelationsfunktion - Beispiele Liquid Ar r g(r) 1 A. Leach (2001) 36
37 Struktur von unterkühlten Schmelzen US untrekühlte Schmelze S - Schmelze US S US S Holland-Moritz (2002) 37
38 Struktur von unterkühlten Schmelzen Na 2 O.4SiO 2 Glas und unterkühlte Schmelzen Neutronenbeugung Zotov (2000) Q = 4p/l sin(q) Struktur der Schmelze Struktur der unterkühlten Schmelze Glasstruktur Die Peaks in g(r) oder S(Q) sind ein Hinweis für die Existenz von SRO Clusters!!! 38
39 Struktur von unterkühlten Schmelzen Dynamische Clusterbildung in metallischen Schmelzen Dynamische Prozesse! Diffusion Bindung von Atomen (b) (c) Atom Attachment/Abtrennung (e) (f) (g) Clusterbildung fcc pentagonale Dipyramide Icosahedron Gerlach et al. (2006) Cluster sind metastabile unterkritische Keime 39
40 Struktur von unterkühlten Schmelzen Clusterbildung in metallischen Schmelzen Verteilung von kugelförmigen Clustern mit Radius r in einer unterkühlten Schmelze n(r) - Anzahl von Clustern mit Radius r; r = r(m); M Anzahl von Atomen im Cluster n Abtrennung bevorzugt Zerfall von Clustern Attachment bevorzugt Bildung von Clustern Anzahl von Atomen im Cluster 40
41 Keimbildung Homogene Keimbildung alle Stellen sind gleichberechtigt Heterogene Keimbildung Keimbildung findet bevorzugt an Grenzflächen (Wände; Rissen, Fremdkörper, etc.) statt. L ß 41
42 Erstarrungsvorgänge Klassifikation nach Konzentrationsänderungen Erstarrung ohne Konzentrationsänderungen (z.b. bei reinen Metallen oder bei kongruent-schmelzenden intermetallischen Verbindungen) Erstarrung mit Konzentrationsunterschied zwischen der Schmelze (a) und der erstarrten Phase (ß) Erstarrung mit der Bildung von zwei Phasen unterschiedlicher Zusammensetzung 42
43 Klassisches Keimbildungsmodel homogene Keimbildung ohne Konzentrationsänderungen Spezifische Gibbs-Energie (per Volumeneinheit) [J/m 3 ] G L = H L TS L (Gibbs-Energie der Schmelze) Bei T = T m sind die Schmelze und der Kristall im Gleichgewicht: G S = H S TS S (Gibbs-Energie des Festkörpers) DG V T m = 0 ( 8a) DG V = G L G S = DH TDS (die Triebrkraft der Erstarrung) DG V = DG V T m + G V / T T m (T-T m ) + DG V T m + DS T m DT ; DT = T m T > 0 (7) oder DS T m = DH/T m (8b) Erstarrung ist ein Phasenübergang 1. Ordnung DH ~ L (Latentwärme) DS T m ~ L/T m (9) (Schmelzentropy) DG V LDT/T m (10) 43
44 Klassisches Keimbildungsmodel Gottstein (2001) Richard s Regel DS T m ~ R (8.3 J/mol.K) 44
45 Klassisches Keimbildungsmodel homogene Keimbildung ohne Konzentrationsänderungen DG hom = -V S DG V + A SL g SL (11) Für kugelförmigen Embryo mit Radius r: Embryos Keime DG hom = -4/3 p r 3 DG v + 4pr 2 g SL (12) g SL - Grenzflächenenergie Solid-Liquid (J/m 2 ) A SL Solid-Liquid Fläche r < r* r > r* DG* instabile Keime (Embryos) stabile Keime kritische Energie für Keimbildung 45
46 Klassisches Keimbildungsmodel homogene Keimbildung ohne Konzentrationsänderungen Die Größe des kritischen Radius r* folgt von der Bedingung: DG/ r = -4pr 2 DG V + 8prg SL = 0 (13a) r* = 2g SL /DG v (13b) r* = (2g SL /L) T m /DT (14) DG* hom = (16 p g SL3 T m2 /3L 2 ) 1/(DT) 2 (15) 46
47 Klassisches Keimbildungsmodel homogene Keimbildung ohne Konzentrationsänderungen Ṅ hom = N o exp(-dg* hom /kt) = Keimbildungsrate = N o exp (- A/(DT) 2 ); A = 16 p g SL3 T m2 /3L 2 kt (16) DT N kritische Unterkühlung für homogene Keimbildung DT N ~ 0.2 T M (die Turnbull-Regel) 47
48 Klassisches Keimbildungsmodel heterogene Keimbildung ohne Konzentrationsänderungen 1 die Minimisierung der gesamten Grenzflächenenergie führt zu Der Winkel (ABC) = 2Q g ML = g SM + g SL cos(q) (17a) (g SL ist isotrop) g ML die Grenzflächenenergie Mould-Schmelze g SM die Grenzflächenenergie Solid-Mould (Gussform) g SL die Grenzflächenenergie Solid-Liquid Q der Benetzungswinkel 2 Änderung der Gibbsschen Energie: DG het = -V S DG V + Grenzflächenbetrag = A 2Q C -V S DG V + A SL g SL + A SM (g SM g ML ) = = -V S DG V + A SL g SL A SM g SL cos(q) (17b) B 48
49 Klassisches Keimbildungsmodel heterogene Keimbildung ohne Konzentrationsänderungen DG het = {-4/3 p r 3 DG v + 4pr 2 g SL } S(Q) = = DG hom S(Q) (18a) V S = (p/3)[2 cos(q) + cos 3 (Q)] A SL = 2p(1-cos(Q)]r 2 ; A SM = p[rsin(q)] 2 ; S(Q) = (2 + cosq)(1 cosq) 2 /4 Q = 10 o S(Q) = 10-4 Q = 30 o S(Q) = 0.02 Q = 90 o S(Q) = 0.5 (18b) DG* het = DG* hom S(Q) (18c) 49
50 Klassisches Keimbildungsmodel heterogene Keimbildung ohne Konzentrationsänderungen Ṅ het = N o exp(-dg* het /kt) = N o exp(-dg* hom S(Q)/kT) (19) Heterogene Keimbildung: kleinere kritische Unterkühlung DT N 50
51 Literatur Hauptquellen K. E. Estarling Introduction to the physical metallurgy of welding, 1992 D.V. Potter, K.E. Easterling, M.Y. Sherif Phase Transitions in Metals and Alloys CRC Press, 2009 G. Gottstein Physikalische Grundlagen der Materialkunde Springer, 2001 E.J.Mittemeijer Fundamental of Material Science,
Kristallstruktur und Mikrostruktur Teil II
 Kristallstruktur und Mikrostruktur Teil II Teil II (Übersicht) 1 Erstarrung/ Grundlagen 2 Erstarrung/ Gefüge (Mikrostruktur) 3 Praktische Aspekte: Schweißen; Thermisches Spritzen 4 Texturanalyse Macherauch
Kristallstruktur und Mikrostruktur Teil II Teil II (Übersicht) 1 Erstarrung/ Grundlagen 2 Erstarrung/ Gefüge (Mikrostruktur) 3 Praktische Aspekte: Schweißen; Thermisches Spritzen 4 Texturanalyse Macherauch
Kristallstruktur und Mikrostruktur Teil II Vorlesung 2
 Kristallstruktur und Mikrostruktur Teil II Vorlesung 2 Teil II 1 Erstarrung/ Grundlagen 2 Erstarrung/ Wachstum/ Gefüge (Mikrostruktur) 3 Praktische Aspekte/ Schweißen; Thermisches Spritzen 4 Texturanalyse
Kristallstruktur und Mikrostruktur Teil II Vorlesung 2 Teil II 1 Erstarrung/ Grundlagen 2 Erstarrung/ Wachstum/ Gefüge (Mikrostruktur) 3 Praktische Aspekte/ Schweißen; Thermisches Spritzen 4 Texturanalyse
4. Strukturänderung durch Phasenübergänge
 4. Strukturänderung durch Phasenübergänge Phasendiagramm einer reinen Substanz Druck Phasenänderung durch Variation des Drucks und/oder der Temperatur Klassifizierung Phasenübergänge 1. Art Phasenübergänge
4. Strukturänderung durch Phasenübergänge Phasendiagramm einer reinen Substanz Druck Phasenänderung durch Variation des Drucks und/oder der Temperatur Klassifizierung Phasenübergänge 1. Art Phasenübergänge
Kristallstruktur und Mikrostruktur Teil II Vorlesung 2
 Kristallstruktur und Mikrostruktur Teil II Vorlesung 2 6/m 2/m 2/m 2 Teil II 1 Erstarrung: Grundlagen 2 Erstarrung: Wachstum und Gefüge 3 Praktische Aspekte: Schweißen; Thermisches Spritzen 4 Texturanalyse
Kristallstruktur und Mikrostruktur Teil II Vorlesung 2 6/m 2/m 2/m 2 Teil II 1 Erstarrung: Grundlagen 2 Erstarrung: Wachstum und Gefüge 3 Praktische Aspekte: Schweißen; Thermisches Spritzen 4 Texturanalyse
3. Mikrostruktur und Phasenübergänge
 3. Mikrostruktur und Phasenübergänge Definition von Mikrostruktur und Gefüge Gefüge bezeichnet die Beschaffenheit der Gesamtheit jener Teilvolumina eines Werkstoffs, von denen jedes hinsichtlich seiner
3. Mikrostruktur und Phasenübergänge Definition von Mikrostruktur und Gefüge Gefüge bezeichnet die Beschaffenheit der Gesamtheit jener Teilvolumina eines Werkstoffs, von denen jedes hinsichtlich seiner
1.1 Wichtige Begriffe und Größen 1.2 Zustand eines Systems 1.3 Zustandsdiagramme eines Systems 1.4 Gibb sche Phasenregel
 Studieneinheit II Grundlegende Begriffe. Wichtige Begriffe und Größen. Zustand eines Systems. Zustandsdiagramme eines Systems.4 Gibb sche Phasenregel Gleichgewichtssysteme. Einstoff-Systeme. Binäre (Zweistoff-)
Studieneinheit II Grundlegende Begriffe. Wichtige Begriffe und Größen. Zustand eines Systems. Zustandsdiagramme eines Systems.4 Gibb sche Phasenregel Gleichgewichtssysteme. Einstoff-Systeme. Binäre (Zweistoff-)
Begriffsdefinitionen Heterogene Gleichgewichte
 Begriffsdefinitionen Heterogene Gleichgewichte Begriff Erklärung Illustration Stoff oder chemisches Element oder Komponente Verbindung Zustand Zustandsvariable Aggregatzustand (fest, flüssig, gasförmig)
Begriffsdefinitionen Heterogene Gleichgewichte Begriff Erklärung Illustration Stoff oder chemisches Element oder Komponente Verbindung Zustand Zustandsvariable Aggregatzustand (fest, flüssig, gasförmig)
Grenzflächenphänomene. Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie. J m. N m. 1. Oberflächenspannung
 Grenzflächenphänomene 1. Oberflächenspannung Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie Grenzflächenphänomene Phase/Phasendiagramm/Phasenübergang Schwerpunkte: Oberflächenspannung
Grenzflächenphänomene 1. Oberflächenspannung Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie Grenzflächenphänomene Phase/Phasendiagramm/Phasenübergang Schwerpunkte: Oberflächenspannung
E.Hornbogen H.Warlimont. Metalle. Struktur und Eigenschaften der Metalle und Legierungen. 5., neu bearbeitete Auflage. Mit 281 Abbildungen.
 E.Hornbogen H.Warlimont Metalle Struktur und Eigenschaften der Metalle und Legierungen 5., neu bearbeitete Auflage Mit 281 Abbildungen ö Springer Inhaltsverzeichnis Vorwort V 1 Allgemeiner Überblick 1
E.Hornbogen H.Warlimont Metalle Struktur und Eigenschaften der Metalle und Legierungen 5., neu bearbeitete Auflage Mit 281 Abbildungen ö Springer Inhaltsverzeichnis Vorwort V 1 Allgemeiner Überblick 1
10. Phasendiagramme 10.1 Definition und Konstruktion
 10. Phasendiagramme 10.1 Definition und Konstruktion Definition: Phasendiagramme geben die Existenzbereiche und Grenzen der Gleichgewichts-Phasenstabilität als Funktion der emperatur und Konzentration
10. Phasendiagramme 10.1 Definition und Konstruktion Definition: Phasendiagramme geben die Existenzbereiche und Grenzen der Gleichgewichts-Phasenstabilität als Funktion der emperatur und Konzentration
Kristallstruktur und Mikrostruktur Zusammenfassung
 Kristallstruktur und Mikrostruktur Zusammenfassung Teil I 1 Koordinatensysteme; Gitter 2 Punktsymmetrieoperationen 3 Translationssymmetrie 4 Raumgruppen Teil II 1 Erstarrung/ Grundlagen 2 Erstarrung/ Gefüge
Kristallstruktur und Mikrostruktur Zusammenfassung Teil I 1 Koordinatensysteme; Gitter 2 Punktsymmetrieoperationen 3 Translationssymmetrie 4 Raumgruppen Teil II 1 Erstarrung/ Grundlagen 2 Erstarrung/ Gefüge
Wie kommt man zu Kristallen?
 Wie kommt man zu Kristallen? Methodenübersicht aus Lehrbuch von Pamplin: Grob-Klassifizierung hier nach Aggregatzustand und Typ der Ausgangsphase, aus der der Kristall entstehen soll. (Natürlich sind auch
Wie kommt man zu Kristallen? Methodenübersicht aus Lehrbuch von Pamplin: Grob-Klassifizierung hier nach Aggregatzustand und Typ der Ausgangsphase, aus der der Kristall entstehen soll. (Natürlich sind auch
Metalle. Struktur und Eigenschaften der Metalle und Legierungen. Bearbeitet von Erhard Hornbogen, Hans Warlimont
 Metalle Struktur und Eigenschaften der Metalle und Legierungen Bearbeitet von Erhard Hornbogen, Hans Warlimont überarbeitet 2006. Buch. xi, 383 S. Hardcover ISBN 978 3 540 34010 2 Format (B x L): 15,5
Metalle Struktur und Eigenschaften der Metalle und Legierungen Bearbeitet von Erhard Hornbogen, Hans Warlimont überarbeitet 2006. Buch. xi, 383 S. Hardcover ISBN 978 3 540 34010 2 Format (B x L): 15,5
Zustandsänderungen Was sollen Sie mitnehmen?
 Was sollen Sie mitnehmen? Wie entstehen Phasen? Welche Zusammensetzungen haben sie? Teil A: Keimbildung und Kristallwachstum. Langsame und rasche Erstarrung Erstarrung von Mischungen Teil B: Zustandsdiagramme
Was sollen Sie mitnehmen? Wie entstehen Phasen? Welche Zusammensetzungen haben sie? Teil A: Keimbildung und Kristallwachstum. Langsame und rasche Erstarrung Erstarrung von Mischungen Teil B: Zustandsdiagramme
5. Amorphe Festkörper
 5. Amorphe Festkörper [ Hunklinger ] WS 2013/14 1 Bisher: kristalline Festkörper mit - Nahordnung und vor allem - Fernordnung in den Anordnungen der atomaren Bausteine Jede dabei auftretende Abweichung
5. Amorphe Festkörper [ Hunklinger ] WS 2013/14 1 Bisher: kristalline Festkörper mit - Nahordnung und vor allem - Fernordnung in den Anordnungen der atomaren Bausteine Jede dabei auftretende Abweichung
Prozesstechnik-Übung Wintersemester Es ist das Phasendiagramm des Systems Naphthalin/Biphenyl durch thermische Analyse zu bestimmen.
 Prozesstechnik-Übung Wintersemester 2008-2009 Thermische Analyse 1 Versuchsziel Es ist das Phasendiagramm des Systems Naphthalin/Biphenyl durch thermische Analyse zu bestimmen. 2 Theoretische Grundlagen
Prozesstechnik-Übung Wintersemester 2008-2009 Thermische Analyse 1 Versuchsziel Es ist das Phasendiagramm des Systems Naphthalin/Biphenyl durch thermische Analyse zu bestimmen. 2 Theoretische Grundlagen
Keimbildung in der Schmelze
 Erstarrung Keimbildung in der Schmelze Die Kristallisation (Kristallwachstum) beginnt mit der Bildung von festen Keimen; dann Wachstum Energetisch: Freie Enthalpie des Kristalls ist kleiner als für die
Erstarrung Keimbildung in der Schmelze Die Kristallisation (Kristallwachstum) beginnt mit der Bildung von festen Keimen; dann Wachstum Energetisch: Freie Enthalpie des Kristalls ist kleiner als für die
Zustandsänderungen Was sollen Sie mitnehmen?
 Was sollen Sie mitnehmen? Wie entstehen Phasen? Welche Zusammensetzungen haben sie? Teil A: Keimbildung und Kristallwachstum. Langsame und rasche Erstarrung Erstarrung von Mischungen Teil B: Zustandsdiagramme
Was sollen Sie mitnehmen? Wie entstehen Phasen? Welche Zusammensetzungen haben sie? Teil A: Keimbildung und Kristallwachstum. Langsame und rasche Erstarrung Erstarrung von Mischungen Teil B: Zustandsdiagramme
Phasendiagramme. Seminar zum Praktikum Modul ACIII
 Phasendiagramme Seminar zum Praktikum Modul ACIII Definition Phase Eine Phase ist ein Zustand der Materie, in dem sie bezüglich ihrer chemischen Zusammensetzung und bezüglich ihres physikalischen Zustandes
Phasendiagramme Seminar zum Praktikum Modul ACIII Definition Phase Eine Phase ist ein Zustand der Materie, in dem sie bezüglich ihrer chemischen Zusammensetzung und bezüglich ihres physikalischen Zustandes
Vorlesung Statistische Mechanik: Ising-Modell
 Phasendiagramme Das Phasendiagramm zeigt die Existenzbereiche der Phasen eines Stoffes in Abhängigkeit von thermodynamischen Parametern. Das einfachste Phasendiagramm erhält man für eine symmetrische binäre
Phasendiagramme Das Phasendiagramm zeigt die Existenzbereiche der Phasen eines Stoffes in Abhängigkeit von thermodynamischen Parametern. Das einfachste Phasendiagramm erhält man für eine symmetrische binäre
Heterogene Keimbildung
 Heterogene Keimbildung - heterogene Keimbildung ist der allgemeinste Fall, da sich der Einfluss von Grenzflächen praktisch nicht ohne weiteres ausschalten lässt. - Voraussetzung: Benetzbarkeit Eigentlicher
Heterogene Keimbildung - heterogene Keimbildung ist der allgemeinste Fall, da sich der Einfluss von Grenzflächen praktisch nicht ohne weiteres ausschalten lässt. - Voraussetzung: Benetzbarkeit Eigentlicher
5.6 Zusammenfassung / Merkpunkte zu Kapitel 5: Thermodynamisches Gleichgewicht
 5.6 Zusammenfassung / Merkpunkte zu Kapitel 5: Thermodynamisches Gleichgewicht Ein Teilchen, oder auch ein ganzes System von Teilchen, befindet sich im Gleichgewicht, falls sich "nichts" mehr ändert. Bei
5.6 Zusammenfassung / Merkpunkte zu Kapitel 5: Thermodynamisches Gleichgewicht Ein Teilchen, oder auch ein ganzes System von Teilchen, befindet sich im Gleichgewicht, falls sich "nichts" mehr ändert. Bei
6. Strukturgleichgewichte 6.1 Phasenumwandlungen (PU) a) PU flüssig-fest: Erstarrung = Kristallisation
 6. Strukturgleichgewichte 6.1 Phasenumwandlungen (PU) a) PU flüssig-fest: Erstarrung = Kristallisation Reines Blei (Pb) bei sehr langsamer Abkühlung 91 Keimzahl Unterkühlung T Homogene Keimbildung = Eigenkeimbildung
6. Strukturgleichgewichte 6.1 Phasenumwandlungen (PU) a) PU flüssig-fest: Erstarrung = Kristallisation Reines Blei (Pb) bei sehr langsamer Abkühlung 91 Keimzahl Unterkühlung T Homogene Keimbildung = Eigenkeimbildung
12. Ordnung-Unordnung 12.1 Überstrukturen
 12. Ordnung-Unordnung 12.1 Überstrukturen B-Atome A-Atome Geordnete L1 Struktur mit A 3 B Überstruktur, z.b. Ni 3 Al Hochtemperaturbeständig, hohe Streckgrenze, resistent gegen Korrosion Schlechte Duktilität
12. Ordnung-Unordnung 12.1 Überstrukturen B-Atome A-Atome Geordnete L1 Struktur mit A 3 B Überstruktur, z.b. Ni 3 Al Hochtemperaturbeständig, hohe Streckgrenze, resistent gegen Korrosion Schlechte Duktilität
3 Erstarrung. 3.1 Einphasige Erstarrung von Legierungen. 3.2 Zweiphasige Erstarrung
 Studieneinheit IV Erstarrung. Einphasige Erstarrung von Legierungen.. Planare Erstarrung Makroseigerung.. Nicht-planare dendritische Erstarrung Mikroseigerung.. Gussstrukturen. Zweiphasige Erstarrung..
Studieneinheit IV Erstarrung. Einphasige Erstarrung von Legierungen.. Planare Erstarrung Makroseigerung.. Nicht-planare dendritische Erstarrung Mikroseigerung.. Gussstrukturen. Zweiphasige Erstarrung..
Vortrag zur Vorlesung `Nanostrukturphysik` Von Kirstin Kochems
 Vortrag zur Vorlesung `Nanostrukturphysik` Von Kirstin Kochems 05.02.2013 Thermodynamische Phasen Einkristalle Quasikristalle Amorphe Festkörper 05.02.2013 Nanostrukturierte Festkörper I 2 05.02.2013 Nanostrukturierte
Vortrag zur Vorlesung `Nanostrukturphysik` Von Kirstin Kochems 05.02.2013 Thermodynamische Phasen Einkristalle Quasikristalle Amorphe Festkörper 05.02.2013 Nanostrukturierte Festkörper I 2 05.02.2013 Nanostrukturierte
1 Einführung. reine Metalle i.a. sehr weich für praktischen Einsatz nur bedingt geeignet verschiedene Möglichkeiten der Festigkeitssteigerung
 1 Einführung reine Metalle i.a. sehr weich für praktischen Einsatz nur bedingt geeignet verschiedene Möglichkeiten der Festigkeitssteigerung eine Möglichkeit = Festigkeitssteigerung durch Teilchen technische
1 Einführung reine Metalle i.a. sehr weich für praktischen Einsatz nur bedingt geeignet verschiedene Möglichkeiten der Festigkeitssteigerung eine Möglichkeit = Festigkeitssteigerung durch Teilchen technische
Institut für Eisen- und Stahl Technologie. Seminar 2 Binäre Systeme Fe-C-Diagramm. www.stahltechnologie.de. Dipl.-Ing. Ch.
 Institut für Eisen- und Stahl Technologie Seminar 2 Binäre Systeme Fe-C-Diagramm Dipl.-Ing. Ch. Schröder 1 Literatur V. Läpple, Wärmebehandlung des Stahls, 2003, ISBN 3-8085-1308-X H. Klemm, Die Gefüge
Institut für Eisen- und Stahl Technologie Seminar 2 Binäre Systeme Fe-C-Diagramm Dipl.-Ing. Ch. Schröder 1 Literatur V. Läpple, Wärmebehandlung des Stahls, 2003, ISBN 3-8085-1308-X H. Klemm, Die Gefüge
Grundlagen der Allgemeinen und Anorganischen Chemie. Atome
 Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Einführung in Werkstoffkunde Phasenumwandlungen
 Einführung in Werkstoffkunde Phasenumwandlungen Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Dr.-Ing. Norbert Hort norbert.hort@gkss.de Inhalte Über mich Einführung Aufbau
Einführung in Werkstoffkunde Phasenumwandlungen Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Dr.-Ing. Norbert Hort norbert.hort@gkss.de Inhalte Über mich Einführung Aufbau
Phasengleichgewicht und Phasenübergänge. Gasförmig
 Phasengleichgewicht und Phasenübergänge Siedetemperatur Flüssig Gasförmig Sublimationstemperatur Schmelztemperatur Fest Aus unserer Erfahrung mit Wasser wissen wir, dass Substanzen ihre Eigenschaften bei
Phasengleichgewicht und Phasenübergänge Siedetemperatur Flüssig Gasförmig Sublimationstemperatur Schmelztemperatur Fest Aus unserer Erfahrung mit Wasser wissen wir, dass Substanzen ihre Eigenschaften bei
HANDOUT. Vorlesung: Glas-Grundlagen. Glasbildung und Glasübergang
 Materialwissenschaft und Werkstofftechnik an der Universität des Saarlandes HANDOU Vorlesung: Glas-Grundlagen Glasbildung und Glasübergang Leitsatz: 27.04.2017 Wenn man davon ausgeht, dass Flüssigkeiten
Materialwissenschaft und Werkstofftechnik an der Universität des Saarlandes HANDOU Vorlesung: Glas-Grundlagen Glasbildung und Glasübergang Leitsatz: 27.04.2017 Wenn man davon ausgeht, dass Flüssigkeiten
1. Systematik der Werkstoffe 10 Punkte
 1. Systematik der Werkstoffe 10 Punkte 1.1 Werkstoffe werden in verschiedene Klassen und die dazugehörigen Untergruppen eingeteilt. Ordnen Sie folgende Werkstoffe in ihre spezifischen Gruppen: Stahl Holz
1. Systematik der Werkstoffe 10 Punkte 1.1 Werkstoffe werden in verschiedene Klassen und die dazugehörigen Untergruppen eingeteilt. Ordnen Sie folgende Werkstoffe in ihre spezifischen Gruppen: Stahl Holz
3 Wahr oder Falsch? = 6.67 % Werkstoffe und Fertigung I, HS 2015 Prof. Dr. K. Wegener. Seminarübung 6 Musterlösung Diffusion, Erstarrung
 3 Wahr oder Falsch? a) Diamant, Graphit und Fullerene sind allotrope Modifikationen des Kohlenstoffatoms. Sie unterschieden jedoch nur in ihrem strukturellem Aufbau. Falsch: Sie unterschieden sich auch
3 Wahr oder Falsch? a) Diamant, Graphit und Fullerene sind allotrope Modifikationen des Kohlenstoffatoms. Sie unterschieden jedoch nur in ihrem strukturellem Aufbau. Falsch: Sie unterschieden sich auch
Anorganische Chemie III
 Seminar zu Vorlesung Anorganische Chemie III Wintersemester 2013/14 Christoph Wölper Universität Duisburg-Essen # Elektronengas # Bändermodell Bindungsmodelle Metallbindung > Bindungsmodelle Elektronengas
Seminar zu Vorlesung Anorganische Chemie III Wintersemester 2013/14 Christoph Wölper Universität Duisburg-Essen # Elektronengas # Bändermodell Bindungsmodelle Metallbindung > Bindungsmodelle Elektronengas
Flussquantisierung
 2.2.2.4 Flussquantisierung supraleitender Ring mit Strom und Magnetfluss: Φ = n Φ 0 ist quantisiert Φ 0 =2,07 10-15 T m² "Flussquant" Experiment: 2.2.2.4 Flussquantisierung Doll + Näbauer 1961 (fast gleichzeitig:
2.2.2.4 Flussquantisierung supraleitender Ring mit Strom und Magnetfluss: Φ = n Φ 0 ist quantisiert Φ 0 =2,07 10-15 T m² "Flussquant" Experiment: 2.2.2.4 Flussquantisierung Doll + Näbauer 1961 (fast gleichzeitig:
Werkstoffe der Elektrotechnik im Studiengang Elektrotechnik
 Werkstoffe der Elektrotechnik im Studiengang Elektrotechnik - Stoffgemische - Prof. Dr. Ulrich Hahn WS 2008/2009 welche Stoffgemische gibt es? technisch relevante Stoffgemische: Lösung Suspension Legierung
Werkstoffe der Elektrotechnik im Studiengang Elektrotechnik - Stoffgemische - Prof. Dr. Ulrich Hahn WS 2008/2009 welche Stoffgemische gibt es? technisch relevante Stoffgemische: Lösung Suspension Legierung
Metallkunde. E. Hornbogen, H. Warlimont. Aufbau und Eigenschaften von Metallen und Legierungen. Mit einem Beitrag von Th. Ricker
 E. Hornbogen, H. Warlimont 2008 AGI-Information Management Consultants May be used for personal purporses only or by libraries associated to dandelon.com network. Metallkunde Aufbau und Eigenschaften von
E. Hornbogen, H. Warlimont 2008 AGI-Information Management Consultants May be used for personal purporses only or by libraries associated to dandelon.com network. Metallkunde Aufbau und Eigenschaften von
2. Thermische Übergänge 2.1 Zustandsbereiche und thermische Umwandlungen
 . Thermische Übergänge.1 Zustandsbereiche und thermische Umwandlungen Zustände eines Einstoffsystems (Normaldruck) fest Ordnung flüssig Kristall Tm, TK smektisch anisotropes Glas Tg (Elastomer) Unordnung
. Thermische Übergänge.1 Zustandsbereiche und thermische Umwandlungen Zustände eines Einstoffsystems (Normaldruck) fest Ordnung flüssig Kristall Tm, TK smektisch anisotropes Glas Tg (Elastomer) Unordnung
3 Wahr oder Falsch? = 6.67 % Werkstoffe und Fertigung I, HS 2016 Prof. Dr. K. Wegener. Seminarübung 6 Musterlösung Diffusion, Erstarrung
 3 Wahr oder Falsch? a) Diamant, Graphit und Fullerene sind allotrope Modifikationen des Kohlenstoffatoms. Sie unterscheiden jedoch nur in ihrem strukturellem Aufbau. Falsch: Sie unterschieden sich auch
3 Wahr oder Falsch? a) Diamant, Graphit und Fullerene sind allotrope Modifikationen des Kohlenstoffatoms. Sie unterscheiden jedoch nur in ihrem strukturellem Aufbau. Falsch: Sie unterschieden sich auch
11. Der Phasenübergang
 11. Der Phasenübergang - Phasendiagramme, Kritischer Punkt und ripelpunkt - Gibbssche Phasenregel - Phasenübergänge 1. und 2. Ordnung - Das Phasengleichgewicht - Clausius-Clapeyron-Gleichung - Pictet-routon-Regel,
11. Der Phasenübergang - Phasendiagramme, Kritischer Punkt und ripelpunkt - Gibbssche Phasenregel - Phasenübergänge 1. und 2. Ordnung - Das Phasengleichgewicht - Clausius-Clapeyron-Gleichung - Pictet-routon-Regel,
9. Festkörperreaktionen
 9. Festkörperreaktionen Wir hatten bereits bei der Diskussion von Diffusionsvorgängen gesehen, dass auch im festen Zustand Atome ständig ihre Plätze tauschen und so chemische Reaktionen in fester Materie
9. Festkörperreaktionen Wir hatten bereits bei der Diskussion von Diffusionsvorgängen gesehen, dass auch im festen Zustand Atome ständig ihre Plätze tauschen und so chemische Reaktionen in fester Materie
6.2 Zweiter HS der Thermodynamik
 Die Änderung des Energieinhaltes eines Systems ohne Stoffaustausch kann durch Zu-/Abfuhr von Wärme Q bzw. mechanischer Arbeit W erfolgen Wird die Arbeit reversibel geleistet (Volumenarbeit), so gilt W
Die Änderung des Energieinhaltes eines Systems ohne Stoffaustausch kann durch Zu-/Abfuhr von Wärme Q bzw. mechanischer Arbeit W erfolgen Wird die Arbeit reversibel geleistet (Volumenarbeit), so gilt W
Ausscheidungsvorgänge
 9 Ausscheidungsvorgänge Die Kristallstruktur von Metallen kann sich auch im festen Zustand ändern. Sie muß nicht notwendigerweise unterhalb der Schmelztemperatur bei allen Temperaturen stabil sein. Diejenige
9 Ausscheidungsvorgänge Die Kristallstruktur von Metallen kann sich auch im festen Zustand ändern. Sie muß nicht notwendigerweise unterhalb der Schmelztemperatur bei allen Temperaturen stabil sein. Diejenige
9. Thermodynamik. 9.1 Temperatur und thermisches Gleichgewicht 9.2 Thermometer und Temperaturskala. 9.4 Wärmekapazität
 9. Thermodynamik 9.1 Temperatur und thermisches Gleichgewicht 9.2 Thermometer und Temperaturskala 93 9.3 Thermische h Ausdehnung 9.4 Wärmekapazität 9. Thermodynamik Aufgabe: - Temperaturverhalten von Gasen,
9. Thermodynamik 9.1 Temperatur und thermisches Gleichgewicht 9.2 Thermometer und Temperaturskala 93 9.3 Thermische h Ausdehnung 9.4 Wärmekapazität 9. Thermodynamik Aufgabe: - Temperaturverhalten von Gasen,
1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen
 IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
Phasendiagramm. Praktikum I, Teil Werkstoffe HS 2008/09 Versuch 6; Verfasser: Philippe Knüsel
 Praktikum I, Teil Werkstoffe HS 2008/09 Versuch 6; 19.11.2008 Phasendiagramm Verfasser: Philippe Knüsel (pknuesel@student.ethz.ch) Versuchsdurchführung: Claudio Zihlmann und Philippe Knüsel Assistenz:
Praktikum I, Teil Werkstoffe HS 2008/09 Versuch 6; 19.11.2008 Phasendiagramm Verfasser: Philippe Knüsel (pknuesel@student.ethz.ch) Versuchsdurchführung: Claudio Zihlmann und Philippe Knüsel Assistenz:
Zusammenfassung 118 tet, konnte den Verlauf der experimentellen Daten wiedergeben. Das Wachstum der festen Phase aus der unterkühlten Schmelze wurde m
 Zusammenfassung In dieser Arbeit wurde die elektrostatische Levitation aufbauend auf der Arbeit von Meister [93] und Lohöfer weiterentwickelt und erfolgreich zum Einsatz gebracht. Die elektrostatische
Zusammenfassung In dieser Arbeit wurde die elektrostatische Levitation aufbauend auf der Arbeit von Meister [93] und Lohöfer weiterentwickelt und erfolgreich zum Einsatz gebracht. Die elektrostatische
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen!
 1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
Prinzipien des Kristallbaus
 Zirkon Prinzipien des Kristallbaus 1. Pauling sche Regel: Kationen umgeben sich mit Anionen, wobei Anionen annähernd regelmässige Polyeder bilden. Die Koordinationszahl der Kationen, d.h. die Anzahl Anionen
Zirkon Prinzipien des Kristallbaus 1. Pauling sche Regel: Kationen umgeben sich mit Anionen, wobei Anionen annähernd regelmässige Polyeder bilden. Die Koordinationszahl der Kationen, d.h. die Anzahl Anionen
Azeotrope. Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch
 Azeotrope B A Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch zahl- reiche wichtige Systeme weichen davon ab. Ein solches Verhalten kann auftreten, a wenn die Wechselwirkungen
Azeotrope B A Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch zahl- reiche wichtige Systeme weichen davon ab. Ein solches Verhalten kann auftreten, a wenn die Wechselwirkungen
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Physikalische Umwandlungen reiner Stoffe
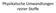 Physikalische Umwandlungen reiner Stoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagramme Phasenübergänge, die D Gleichgewichtkriterien Die Abhängigkeit der
Physikalische Umwandlungen reiner Stoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagramme Phasenübergänge, die D Gleichgewichtkriterien Die Abhängigkeit der
Austenitbildung und -stabilität in 9-12% Chromstählen ein Anwendungsbeispiel für ThermoCalc
 Austenitbildung und -stabilität in 9-12% Chromstählen ein Anwendungsbeispiel für ThermoCalc Ulrich E. Klotz EMPA Eidgenössische Materialprüfungs- und Forschungsanstalt Dübendorf, Schweiz TCC Anwendertreffen
Austenitbildung und -stabilität in 9-12% Chromstählen ein Anwendungsbeispiel für ThermoCalc Ulrich E. Klotz EMPA Eidgenössische Materialprüfungs- und Forschungsanstalt Dübendorf, Schweiz TCC Anwendertreffen
Kristallstruktur und Mikrostruktur Teil II Vorlesung 3
 Kristallstruktur und Mikrostruktur Teil II Vorlesung 3 Teil II 1 Erstarrung - Grundlagen 2 Erstarrung/ - Wachstum/ Gefüge (Mikrostruktur) 3 Praktische Beispiele: das Schweißen und das thermische Spritzen
Kristallstruktur und Mikrostruktur Teil II Vorlesung 3 Teil II 1 Erstarrung - Grundlagen 2 Erstarrung/ - Wachstum/ Gefüge (Mikrostruktur) 3 Praktische Beispiele: das Schweißen und das thermische Spritzen
PhysikalischeUmwandlungen
 PhysikalischeUmwandlungen reinerstoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagramme Phasenübergänge, die D Gleichgewichtkriterien Die Abhängigkeit der Stabilität
PhysikalischeUmwandlungen reinerstoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagramme Phasenübergänge, die D Gleichgewichtkriterien Die Abhängigkeit der Stabilität
PC V: Physikalische Chemie der Festkörper WS 2009/10 1. Einführung Kristallsymmetrie und physikalische Eigenschaften, Neumannsches Prinzip
 PC V: Physikalische Chemie der Festkörper WS 2009/10 1. Einführung Kristallsymmeie und physikalische Eigenschaften, Neumannsches Prinzip 2. Thermodynamik fester Körper Phänomenologische Thermodynamik (Potentiale,
PC V: Physikalische Chemie der Festkörper WS 2009/10 1. Einführung Kristallsymmeie und physikalische Eigenschaften, Neumannsches Prinzip 2. Thermodynamik fester Körper Phänomenologische Thermodynamik (Potentiale,
I Mikroskopische Struktur amorpher Festkörper
 I.4.2 Amorphe Festkörper und Gläser I.4.2.1 Mikroskopische Struktur amorpher Festkörper Während das makroskopische mechanische Verhalten eines amorphen Festkörpers bei tiefen Temperturen dem eines kristallinen
I.4.2 Amorphe Festkörper und Gläser I.4.2.1 Mikroskopische Struktur amorpher Festkörper Während das makroskopische mechanische Verhalten eines amorphen Festkörpers bei tiefen Temperturen dem eines kristallinen
E2: Wärmelehre und Elektromagnetismus 6. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 6. Vorlesung 26.04.2018 Heute: - Kondensationskerne - Van der Waals-Gas - 2. Hauptsatz https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 26.04.2018 Prof.
E2: Wärmelehre und Elektromagnetismus 6. Vorlesung 26.04.2018 Heute: - Kondensationskerne - Van der Waals-Gas - 2. Hauptsatz https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 26.04.2018 Prof.
Zustandsbeschreibungen
 Aggregatzustände fest Kristall, geordnet Modifikationen Fernordnung flüssig teilgeordnet Fluktuationen Nahordnung gasförmig regellose Bewegung Unabhängigkeit ngigkeit (ideales Gas) Zustandsbeschreibung
Aggregatzustände fest Kristall, geordnet Modifikationen Fernordnung flüssig teilgeordnet Fluktuationen Nahordnung gasförmig regellose Bewegung Unabhängigkeit ngigkeit (ideales Gas) Zustandsbeschreibung
E2: Wärmelehre und Elektromagnetismus 6. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 6. Vorlesung 26.04.2018 Heute: - Kondensationskerne - Van der Waals-Gas - 2. Hauptsatz https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 26.04.2018 Prof.
E2: Wärmelehre und Elektromagnetismus 6. Vorlesung 26.04.2018 Heute: - Kondensationskerne - Van der Waals-Gas - 2. Hauptsatz https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 26.04.2018 Prof.
1 Theorie: Reales Zustandsdiagramm. 1.1 Fe 3 C-Diagramm. Seminarübung 5 Eisen-Kohlenstoff. Werkstoffe und Fertigung I, HS 2015 Prof. Dr. K.
 1 Theorie: Reales Zustandsdiagramm 1.1 Fe 3 C-Diagramm Eisenwerkstoffe in der Form von Stahl und Gusseisen sind für den Ingenieur besonders wichtig. Stahl ist der mit Abstand meistverwendete Rohstoff und
1 Theorie: Reales Zustandsdiagramm 1.1 Fe 3 C-Diagramm Eisenwerkstoffe in der Form von Stahl und Gusseisen sind für den Ingenieur besonders wichtig. Stahl ist der mit Abstand meistverwendete Rohstoff und
VL 3: EKD (Eisen-Kohlenstoff- Diagramm)
 1 VL 3: (Eisen-Kohlenstoff- Diagramm) 1. Grundlagen (Polymorphie des Fe) 2. Aufbau (Stahlseite, Gusseisenseite, stabiles System, metastabiles System) 3. Gefüge- und Phasendiagramm verschiedene Darstellungen
1 VL 3: (Eisen-Kohlenstoff- Diagramm) 1. Grundlagen (Polymorphie des Fe) 2. Aufbau (Stahlseite, Gusseisenseite, stabiles System, metastabiles System) 3. Gefüge- und Phasendiagramm verschiedene Darstellungen
4.Legierungen. 4.Legierungen
 a) Systeme mit völliger Unlöslichkeit in Schmelze und Festkörper (Unlöslichkeit = Insolubility) - keinerlei Mischung im atomaren Bereich - Monotektisches Zustandsdiagramm - Beispiele: Cu-Pb, Fe-Pb, Cu-W
a) Systeme mit völliger Unlöslichkeit in Schmelze und Festkörper (Unlöslichkeit = Insolubility) - keinerlei Mischung im atomaren Bereich - Monotektisches Zustandsdiagramm - Beispiele: Cu-Pb, Fe-Pb, Cu-W
Kristallstruktur und Mikrostruktur Teil II Vorlesung 3
 Kristallstruktur und Mikrostruktur Teil II Vorlesung 3 Teil II 1 Erstarrung - Grundlagen 2 Erstarrung/ - Wachstum/ Gefüge (Mikrostruktur) 3 Praktische Beispiele: Schweißen und thermisches Spritzen 4 Texturanalyse
Kristallstruktur und Mikrostruktur Teil II Vorlesung 3 Teil II 1 Erstarrung - Grundlagen 2 Erstarrung/ - Wachstum/ Gefüge (Mikrostruktur) 3 Praktische Beispiele: Schweißen und thermisches Spritzen 4 Texturanalyse
Kristallisationsgeschwindigkeit
 Kristallisationsgeschwindigkeit 1. Versuchsplatz Komponenten: - U-Rohr mit Versuchssubstanz - Thermometer - Bechergläser - Bunsenbrenner 2. Allgemeines zum Versuch Viele Werkstoffe sind kristallin (Metalle,
Kristallisationsgeschwindigkeit 1. Versuchsplatz Komponenten: - U-Rohr mit Versuchssubstanz - Thermometer - Bechergläser - Bunsenbrenner 2. Allgemeines zum Versuch Viele Werkstoffe sind kristallin (Metalle,
2 Gleichgewichtssysteme
 Studieneinheit III Gleichgewichtssysteme. Einstoff-Systeme. Binäre (Zweistoff-) Systeme.. Grundlagen.. Systeme mit vollständiger Mischbarkeit.. Systeme mit unvollständiger Mischbarkeit..4 Systeme mit Dreiphasenreaktionen..4.
Studieneinheit III Gleichgewichtssysteme. Einstoff-Systeme. Binäre (Zweistoff-) Systeme.. Grundlagen.. Systeme mit vollständiger Mischbarkeit.. Systeme mit unvollständiger Mischbarkeit..4 Systeme mit Dreiphasenreaktionen..4.
Anorganische Chemie III - Festkörperchemie
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Festkörperchemie
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Festkörperchemie
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
Zintl-Anionen: Genese und synthetisches Potential. Teil 1
 Teil 1 19. November 2009 Historisches Darstellung und Untersuchung salzartiger intermetallischer Verbindungen durch Eduard Zintl (1898-1941) Vorhergende Forschungsaktivitäten: Atommassenbestimmungen Potentiometrische
Teil 1 19. November 2009 Historisches Darstellung und Untersuchung salzartiger intermetallischer Verbindungen durch Eduard Zintl (1898-1941) Vorhergende Forschungsaktivitäten: Atommassenbestimmungen Potentiometrische
Die innere Energie and die Entropie
 Die innere Energie and die Entropie Aber fangen wir mit der Entropie an... Stellen Sie sich ein System vor, das durch die Entropie S, das Volumen V und die Stoffmenge n beschrieben wird. U ' U(S,V,n) Wir
Die innere Energie and die Entropie Aber fangen wir mit der Entropie an... Stellen Sie sich ein System vor, das durch die Entropie S, das Volumen V und die Stoffmenge n beschrieben wird. U ' U(S,V,n) Wir
TD 4: Schmelzdigramme
 TD 4: Schmelzdigramme Einleitung Wenn ein Stoff vom festen in den flüssigen Aggregatzustand übergeht, wird die Temperatur des Übergangs als Schmelztemperatur bezeichnet. Reine Stoffe besitzen in der Regel
TD 4: Schmelzdigramme Einleitung Wenn ein Stoff vom festen in den flüssigen Aggregatzustand übergeht, wird die Temperatur des Übergangs als Schmelztemperatur bezeichnet. Reine Stoffe besitzen in der Regel
5.Thermisch aktivierbare Prozesse. 5.Thermisch aktivierbare Prozesse
 5.1. Thermodynamische Betrachtung Zustand eines Systems Der Zustand eines Systems wird durch ihre Freie Energie G charakterisiert Zustandsänderungen im Festkörper laufen ab, um dessen Freie Energie G herabzusetzen
5.1. Thermodynamische Betrachtung Zustand eines Systems Der Zustand eines Systems wird durch ihre Freie Energie G charakterisiert Zustandsänderungen im Festkörper laufen ab, um dessen Freie Energie G herabzusetzen
E2: Wärmelehre und Elektromagnetismus 5. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 5. Vorlesung 23.04.2018 Heute: - Phasenübergänge - van der Waals-Gas https://xkcd.com/1561/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 23.04.2018 Prof. Dr. Jan Lipfert
E2: Wärmelehre und Elektromagnetismus 5. Vorlesung 23.04.2018 Heute: - Phasenübergänge - van der Waals-Gas https://xkcd.com/1561/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 23.04.2018 Prof. Dr. Jan Lipfert
1 Kristallgitter und Kristallbaufehler 10 Punkte
 1 Kristallgitter und Kristallbaufehler 10 Punkte 1.1 Es gibt 7 Kristallsysteme, aus denen sich 14 Bravais-Typen ableiten lassen. Charakterisieren Sie die kubische, tetragonale, hexagonale und orthorhombische
1 Kristallgitter und Kristallbaufehler 10 Punkte 1.1 Es gibt 7 Kristallsysteme, aus denen sich 14 Bravais-Typen ableiten lassen. Charakterisieren Sie die kubische, tetragonale, hexagonale und orthorhombische
Bekannter Stoff aus dem 1. Semester:
 Bekannter Stoff aus dem 1. Semester: Atombau! Arten der Teilchen! Elemente/Isotope! Kernchemie! Elektronenhülle/Quantenzahlen Chemische Bindung! Zustände der Materie! Ionenbindung! Atombindung! Metallbindung
Bekannter Stoff aus dem 1. Semester: Atombau! Arten der Teilchen! Elemente/Isotope! Kernchemie! Elektronenhülle/Quantenzahlen Chemische Bindung! Zustände der Materie! Ionenbindung! Atombindung! Metallbindung
Physikalische Umwandlungen reiner Stoffe
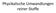 Physikalische Umwandlungen reiner Stoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagrame Phasenübergänge, die D Gleichgewichtkriterium Die Abhängigkeit der
Physikalische Umwandlungen reiner Stoffe Lernziele: Phasendiagramme, die Stabilität von Phasen Phasengrenzen, typische Phasendiagrame Phasenübergänge, die D Gleichgewichtkriterium Die Abhängigkeit der
2.4 Metallische Bindung und Metallkristalle. Unterteilung in Metalle, Halbmetalle, Nicht metalle. Li Be B C N O F. Na Mg Al Si P S Cl
 2.4 Metallische Bindung und Metallkristalle Li Be B C N O F Na Mg Al Si P S Cl K Ca Ga Ge As Se Br Rb Sr In Sn Sb Te I Cs Ba Tl Pb Bi Po At Unterteilung in Metalle, Halbmetalle, Nicht metalle Metalle etwa
2.4 Metallische Bindung und Metallkristalle Li Be B C N O F Na Mg Al Si P S Cl K Ca Ga Ge As Se Br Rb Sr In Sn Sb Te I Cs Ba Tl Pb Bi Po At Unterteilung in Metalle, Halbmetalle, Nicht metalle Metalle etwa
Neuartige Mo-Si-B-Ti Legierungen für den Hochtemperatureinsatz
 Neuartige Mo-Si-B-Ti Legierungen für den Hochtemperatureinsatz D. Schliephake 1, M. Heilmaier 1, M. Azim 2, B. Gorr 2, H.-J. Christ 2 1 Institut für Angewandte Materialien, Karlsruher Institut für Technologie
Neuartige Mo-Si-B-Ti Legierungen für den Hochtemperatureinsatz D. Schliephake 1, M. Heilmaier 1, M. Azim 2, B. Gorr 2, H.-J. Christ 2 1 Institut für Angewandte Materialien, Karlsruher Institut für Technologie
Thermodynamik. Christian Britz
 Hauptsätze der Klassische nanoskaliger Systeme 04.02.2013 Inhalt Einleitung Hauptsätze der Klassische nanoskaliger Systeme 1 Einleitung 2 Hauptsätze der 3 4 Klassische 5 6 7 nanoskaliger Systeme 8 Hauptsätze
Hauptsätze der Klassische nanoskaliger Systeme 04.02.2013 Inhalt Einleitung Hauptsätze der Klassische nanoskaliger Systeme 1 Einleitung 2 Hauptsätze der 3 4 Klassische 5 6 7 nanoskaliger Systeme 8 Hauptsätze
Physikalische Chemie 1 Struktur und Materie Wintersemester 2015/16
 Vorlesung: Kontakt: Physikalische Chemie 1 Struktur und Materie Wintersemester 2015/16 5., 7., 12., 19., 21., 28. Oktober und 4., 11., 13., 18. November Hörsaal 10.01 Daran anschließend Physikalische Chemie
Vorlesung: Kontakt: Physikalische Chemie 1 Struktur und Materie Wintersemester 2015/16 5., 7., 12., 19., 21., 28. Oktober und 4., 11., 13., 18. November Hörsaal 10.01 Daran anschließend Physikalische Chemie
(VIII) Wärmlehre. Wärmelehre Karim Kouz WS 2014/ Semester Biophysik
 Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Lernziele: Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme,
 Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
werkstoffprüfer-blog.de Fragenkatalog Werkstoffwissenschaft I
 1 1. Nennen Sie die ungefähren Zeitangaben 3 Zeitalter der kulturellen Entwicklung des Menschen, die nach ihren Leitwerkstoffen benannt sind. 2. Welche Werkstoffe/Werkstoffgruppen könnte man in der heutigen
1 1. Nennen Sie die ungefähren Zeitangaben 3 Zeitalter der kulturellen Entwicklung des Menschen, die nach ihren Leitwerkstoffen benannt sind. 2. Welche Werkstoffe/Werkstoffgruppen könnte man in der heutigen
Phasentransformation: (fest-fest) Von Marcus Bauer und Henrik Petersen
 Von Marcus Bauer und Henrik Petersen 1. Arten von Phasenumwandlungen - Reine Metalle - Legierungen 2. Martensitische Phasenumwandlung am Beispiel von Fe-C 3. Formgedächtnislegierungen - Allgemeine Betrachtung
Von Marcus Bauer und Henrik Petersen 1. Arten von Phasenumwandlungen - Reine Metalle - Legierungen 2. Martensitische Phasenumwandlung am Beispiel von Fe-C 3. Formgedächtnislegierungen - Allgemeine Betrachtung
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Nachbesprechung. Übung 6
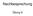 Nachbesprechung Übung 6 Mischungsdreieck Alamandin (Fe) X möglich Pyrop (Mg) X nicht möglich Spessartin (Mn) Phasendiagramm V (Andalusit) > V (Sillimanit) > V (Kyanit) S (Sillimanit) > S (Andalusit) >
Nachbesprechung Übung 6 Mischungsdreieck Alamandin (Fe) X möglich Pyrop (Mg) X nicht möglich Spessartin (Mn) Phasendiagramm V (Andalusit) > V (Sillimanit) > V (Kyanit) S (Sillimanit) > S (Andalusit) >
Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I
 Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Kristallchemie. Atome Ionen Moleküle Chemische Bindungen
 Kristallchemie Atome Ionen Moleküle Chemische Bindungen Metalle, Metalloide, Nichtmetalle Metalle: E-neg < 1.9 - e - Abgabe Kationen Nichtmetalle: E-neg > 2.1 - e - Aufnahme Anionen Metalloide: B, Si,
Kristallchemie Atome Ionen Moleküle Chemische Bindungen Metalle, Metalloide, Nichtmetalle Metalle: E-neg < 1.9 - e - Abgabe Kationen Nichtmetalle: E-neg > 2.1 - e - Aufnahme Anionen Metalloide: B, Si,
Crystallisation kinetics in synthetic magma chambers
 Crystallisation kinetics in synthetic magma chambers H. Strauß, M. Nowak, F. Holtz Wolfersdorf, August 2006 Institut für Mineralogie 1. Einführung nordatlantische Eruptivprovinz sibirische Trapps Columbia-RiverBasalt
Crystallisation kinetics in synthetic magma chambers H. Strauß, M. Nowak, F. Holtz Wolfersdorf, August 2006 Institut für Mineralogie 1. Einführung nordatlantische Eruptivprovinz sibirische Trapps Columbia-RiverBasalt
E2: Wärmelehre und Elektromagnetismus 7. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 7. Vorlesung 30.04.2018 Heute: - 2. Hauptsatz - Boltzmann-Verteilung https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 30.04.2018 Prof. Dr. Jan Lipfert
E2: Wärmelehre und Elektromagnetismus 7. Vorlesung 30.04.2018 Heute: - 2. Hauptsatz - Boltzmann-Verteilung https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 30.04.2018 Prof. Dr. Jan Lipfert
4. Freie Energie/Enthalpie & Gibbs Gleichungen
 4. Freie Energie/Enthalpie & Gibbs Gleichungen 1. Eigenschaften der Materie in der Gasphase 2. Erster Hauptsatz: Arbeit und Wärme 3. Entropie und Zweiter Hauptsatz der hermodynamik 4. Freie Enthalpie G,
4. Freie Energie/Enthalpie & Gibbs Gleichungen 1. Eigenschaften der Materie in der Gasphase 2. Erster Hauptsatz: Arbeit und Wärme 3. Entropie und Zweiter Hauptsatz der hermodynamik 4. Freie Enthalpie G,
13. Keimbildung 13.1 Keimbildung und Unterkühlung
 13. Keimbildung 13.1 Keimbildung und Unterkühlung Erstarrung von Flüssigkeiten: Phasenübergang 1. Ordnung Latente Wärme H f, Keimbildung Thermodynamische Variable: p,t Thermodynamisches Potential: G(p,T)
13. Keimbildung 13.1 Keimbildung und Unterkühlung Erstarrung von Flüssigkeiten: Phasenübergang 1. Ordnung Latente Wärme H f, Keimbildung Thermodynamische Variable: p,t Thermodynamisches Potential: G(p,T)
1 Die elastischen Konstanten 10 Punkte
 1 Die elastischen Konstanten 10 Punkte 1.1 Ein Würfel wird einachsig unter Zug belastet. a) Definieren Sie durch Verwendung einer Skizze den Begriff der Spannung und der Dehnung. b) Der Würfel werde im
1 Die elastischen Konstanten 10 Punkte 1.1 Ein Würfel wird einachsig unter Zug belastet. a) Definieren Sie durch Verwendung einer Skizze den Begriff der Spannung und der Dehnung. b) Der Würfel werde im
Physik 4: Skalen und Strukturen
 Physik 4: Skalen und Strukturen Kapitel : Festkörperphysik.1 Aggregatszustände. Kristallstrukturen.3 Chemische Bindung.4 Gitterschwingungen.5 Elektronen im Festkörper Phasendiagramm von CO Klassisches
Physik 4: Skalen und Strukturen Kapitel : Festkörperphysik.1 Aggregatszustände. Kristallstrukturen.3 Chemische Bindung.4 Gitterschwingungen.5 Elektronen im Festkörper Phasendiagramm von CO Klassisches
Gibbssche Phasenregel und Einführung in Phasendiagramme F = C P + 2
 Petrologie der Magmatite und Metamorphite: Teil Metamorphite - Vorlesung 3 1/6 Gibbssche Phasenregel und Einführung in Phasendiagramme Bei Vorliegen eines thermodynamischen Gleichgewichts (thermodynamic
Petrologie der Magmatite und Metamorphite: Teil Metamorphite - Vorlesung 3 1/6 Gibbssche Phasenregel und Einführung in Phasendiagramme Bei Vorliegen eines thermodynamischen Gleichgewichts (thermodynamic
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern?
 An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Temperatur Der nullte Hauptsatz der Thermodynamik: Thermoskop und Thermometer Kelvin, Celsius- und der Fahrenheit-Skala Wärmeausdehnung
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Temperatur Der nullte Hauptsatz der Thermodynamik: Thermoskop und Thermometer Kelvin, Celsius- und der Fahrenheit-Skala Wärmeausdehnung
Thermodynamik un Statistische Mechanik
 Theoretische Physik Band 9 Walter Greiner Ludwig Neise Horst Stöcker Thermodynamik un Statistische Mechanik Ein Lehr- und Übungsbuch Mit zahlreichen Abbildungen, Beispiele n und Aufgaben mit ausführlichen
Theoretische Physik Band 9 Walter Greiner Ludwig Neise Horst Stöcker Thermodynamik un Statistische Mechanik Ein Lehr- und Übungsbuch Mit zahlreichen Abbildungen, Beispiele n und Aufgaben mit ausführlichen
Physikalisch-chemische Grundlagen der thermischen Verfahrenstechnik
 Lüdecke Lüdecke Thermodynamik Physikalisch-chemische Grundlagen der thermischen Verfahrenstechnik Grundlagen der Thermodynamik Grundbegriffe Nullter und erster Hauptsatz der Thermodynamik Das ideale Gas
Lüdecke Lüdecke Thermodynamik Physikalisch-chemische Grundlagen der thermischen Verfahrenstechnik Grundlagen der Thermodynamik Grundbegriffe Nullter und erster Hauptsatz der Thermodynamik Das ideale Gas
