FACHINFORMATION. 4.3 Gegenanzeigen Überempfindlichkeit gegen die Wirkstoffe oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
|
|
|
- Siegfried Fiedler
- vor 8 Jahren
- Abrufe
Transkript
1 1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-GruppenA,C,W-135und Y-Konjugatimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Nach Rekonstitution enthält 1 Dosis (0,5 ml): Neisseria meningitidis-gruppe A- Neisseria meningitidis-gruppe C- Neisseria meningitidis-gruppe W-135- Neisseria meningitidis-gruppe Y- 1 konjugiert an Tetanustoxoid- Trägerprotein 44 Mikrogramm Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt DARREICHUNGSFORM Pulver und Lösungsmittel zur Herstellung einer Injektionslösung. Das Pulver ist weiß. Das Lösungsmittel ist klar und farblos. 4. KLINISCHE ANGABEN 4.1 Anwendungsgebiete Nimenrix ist indiziert zur aktiven Immunisierung von Personen ab dem Alter von 12 Monaten gegen invasive Meningokokkenerkrankungen, verursacht durch Neisseria meningitidis dergruppena,c,w-135undy. 4.2 Dosierung und Art der Anwendung Dosierung Die Anwendung von Nimenrix sollte gemäß offiziellenempfehlungenerfolgen. Grundimmunisierung: Für die Immunisierung wird eine 0,5 ml Einzeldosis des rekonstituierten Impfstoffes verwendet. Auffrischimpfung: Nimenrix kann als Auffrischimpfung an Personen verabreicht werden, die früher mit einem einfachen Polysaccharid-Meningokokken-Impfstoff geimpft worden waren (siehe Abschnitte 4.4 und 5.1). Die Notwendigkeit einer Auffrischimpfung bei Personen, die mit Nimenrix grundimmunisiert wurden, wurde bisher noch nicht untersucht (siehe Abschnitte 4.4 und 5.1). Kinder und Jugendliche Die Sicherheit und Wirksamkeit von Nimenrix bei Kindern im Alter von unter 12 Monaten ist bisher noch nicht erwiesen. Es liegen keine Daten vor. Ältere Personen Es liegen keine Daten für Personen im Alter von über 55 Jahren vor. Art der Anwendung Nimenrix ist ausschließlich intramuskulär zu injizieren, vorzugsweise in den M. deltoideus. Bei Kindern im Alter von 12 bis 23 Monaten kann der Impfstoff auch in den anterolateralen Bereich des Oberschenkels verabreicht werden (siehe Abschnitte 4.4 und 4.5). Hinweise zur Rekonstitution des Arzneimittels vor der Anwendung, siehe Abschnitt Gegenanzeigen Überempfindlichkeit gegen die Wirkstoffe oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile. 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Nimenrix darf unter keinen Umständen intravasal, intradermal oder subkutan verabreicht werden. Der Impfung sollten eine Anamneseerhebung (unter besonderer Berücksichtigung früherer Impfungen und eventuell aufgetretener Nebenwirkungen) sowie eine klinische Untersuchung vorausgehen. Für den seltenen Fall einer anaphylaktischen Reaktion nach Verabreichung des Impfstoffes sollten stets entsprechende medizinische Behandlungs- und Überwachungsmöglichkeiten sofort verfügbar sein. Die Impfung mit Nimenrix sollte bei Personen, die an einer akuten, schweren, mit Fieber einhergehenden Erkrankung leiden, auf einen späteren Zeitpunkt verschoben werden. Ein banaler Infekt (wie z. B. eine Erkältung) stellt jedoch keine Kontraindikation für eine Impfung dar. Besonders bei Jugendlichen kann es als psychogene Reaktion auf die Nadelinjektion nach oder sogar vor einer Impfung zu einer Synkope (Ohnmacht) kommen. Diese kann während der Erholungsphase von verschiedenen neurologischen Symptomen wie vorübergehende Sehstörung, Parästhesie und tonisch-klonische Bewegungen der Gliedmaßen begleitet sein. Es ist wichtig, Maßnahmen zu ergreifen, um Verletzungen durch dieohnmachtzuverhindern. Bei Personen mit Thrombozytopenie oder einer Blutgerinnungsstörung ist Nimenrix mit Vorsicht zu verabreichen, da es bei diesen Personen nach intramuskulärer Injektion zu Blutungen kommen kann. Nimenrix wird nur einen Schutz vor Neisseria meningitidis dergruppena,c,w-135 und Y verleihen. Der Impfstoff wird nicht vor anderen Neisseria meningitidis-gruppen schützen. Es wird möglicherweise nicht bei allen Geimpften eine schützende Immunantwort erzielt. Es wird möglicherweise bei Patienten unter immunsuppressiver Therapie oder mit geschwächtem Immunsystem keine ausreichende Immunantwort erzielt. Bei Patienten mit erhöhter Anfälligkeit für eine Meningokokkeninfektion wie bei terminalen Komplementdefekten und anatomischer oder funktioneller Asplenie wurde die Sicherheit und Immunogenität nicht untersucht. Bei diesen Patienten wird möglicherweise keine ausreichende Immunantwort erzielt. Personen, die früher schon einmal eine Impfung mit einem einfachen Polysaccharid-Meningokokken-Impfstoff erhalten haben und 30 bis 42 Monate später mit Nimenrix geimpft wurden, hatten niedrigere geometrische Mitteltiter (s, gemessen mit einem Test auf bakterizide Antikörper im Serum unter Verwendung von Kaninchen-Komplement [rsba]) als Personen, die in den vergangenen 10 Jahren keinen Meningokokken-Impfstoff erhalten haben (siehe Abschnitt 5.1). Die klinische Relevanz dieser Beobachtung ist nicht bekannt. Auswirkung von vor der Impfung vorhandenen Anti-Tetanus-Antikörpern Die Sicherheit und Immunogenität von Nimenrix wurde bei aufeinanderfolgender oder gleichzeitiger Verabreichung eines DTPa-HBV-IPV/Hib-Impfstoffes im zweiten Lebensjahr untersucht. Die Verabreichung von Nimenrix einen Monat nach der DTPa- HBV-IPV/Hib-Impfung resultierte in niedrigeren MenA, MenC und MenW-135 rsba- s (siehe Abschnitt 4.5). Die klinische Relevanz dieser Beobachtung ist nicht bekannt. Die Reaktogenität, die bei gleichzeitiger oder aufeinanderfolgender Verabreichung beobachtet wurde, war vergleichbar mitderreaktogenitätnacheinerauffrischimpfung mit einem DTPa-HBV-IPV/Hib-Impfstoff im zweiten Lebensjahr. Auswirkung von Nimenrix auf Anti-Tetanus- Antikörperkonzentrationen Obwohl nach einer Impfung mit Nimenrix ein Anstieg der Anti-Tetanustoxoid (TT)-Antikörperkonzentrationen beobachtet wurde, ersetzt Nimenrix nicht eine Immunisierung gegen Tetanus. Die Verabreichung von Nimenrix im zweiten Lebensjahr gleichzeitig mit oder einen Monat vor einem Tetanustoxoid-haltigen Impfstoff beeinträchtigt weder die Immunantwort auf Tetanustoxoid noch wird die Sicherheit signifikant beeinflusst. Es liegen keine Daten bei Personen über 2 Jahren vor. Persistenz der bakteriziden Serum-Antikörpertiter gegen MenA Studien mit Nimenrix unter Verwendung von humanem Komplement (hsba) haben eine rasche Abnahme (hier ab 12 Monate nach Verabreichung der Dosis gemessen) der bakteriziden Serum-Antikörpertiter gegen MenA gezeigt (siehe Abschnitt 5.1). DieklinischeRelevanzderraschenAbnahme der hsba-mena-antikörpertiter ist nicht bekannt. Wenn jedoch für eine Person ein besonderes Risiko für eine MenA-Exposition zu erwarten ist und eine erste Dosis Nimenrixvormehralsca.einemJahrverabreicht wurde, kann die Verabreichung einer zweiten Dosis Nimenrix in Betracht gezogen werden. Die zur Verfügung stehenden Daten deuten darauf hin, dass durch eine zweite Dosis eine anamnestische Immunantwort auf alle vier im Impfstoff enthaltenen Meningokokkentypen erzielt wird. Derzeit sind sehr wenige Daten zur Sicherheit einer zweiten Dosis verfügbar. 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Nimenrix kann gleichzeitig mit jedem der folgenden Impfstoffe verabreicht werden: E753 Nimenrix n 1
2 Hepatitis A (HAV)- und Hepatitis B (HBV)- Impfstoffe, Masern-Mumps-Röteln (MMR)- Impfstoff, Masern-Mumps-Röteln-Varizellen (MMRV)-Impfstoff, 10-valenter Pneumokokken-Konjugatimpfstoff oder nicht-adjuvantierter saisonaler Influenzaimpfstoff. Nimenrix kann im zweiten Lebensjahr auch gleichzeitig mit kombinierten Diphtherie-Tetanus-azellulären Pertussis (DTPa)-Impfstoffen verabreicht werden, einschließlich kombinierten DTPa-Impfstoffen mit Hepatitis B, Polio inaktiviert oder Haemophilus influenzae Typ b, wie zum Beispiel einem DTPa- HBV-IPV/Hib-Impfstoff. Wann immer möglich sollten Nimenrix und ein TT-haltiger Impfstoff, wie zum Beispiel ein DTPa-HBV-IPV/Hib-Impfstoff, gleichzeitig oder mindestens einen Monat vor dem TT-haltigen Impfstoff verabreicht werden. Die aufeinanderfolgende Verabreichung von Nimenrix einen Monat nach einem DTPa- HBV-IPV/Hib-Impfstoff resultierte in niedrigeren MenA, MenC und MenW-135 s. Die klinische Relevanz dieser Beobachtung ist nicht bekannt, da mindestens 99,4 % der Personen (N=178) einen rsba-titer von 8 für jede Gruppe (A, C, W-135, Y) aufwiesen (siehe Abschnitt 4.4). Einen Monat nach der gleichzeitigen Verabreichung eines 10-valenten Pneumokokken-Konjugatimpfstoffes wurden niedrigere mittlere geometrische Antikörperkonzentrationen (GMCs) und Opsonophagozytose- Test (OPA)-Antikörper-s für einen Pneumokokken-Serotyp (18C, konjugiert an Tetanustoxoid-Trägerprotein) beobachtet. Die klinische Relevanz dieser Beobachtung ist nicht bekannt. Die gleichzeitige Verabreichung hatte keine Auswirkungen auf die anderenneunpneumokokken-serotypen. Falls Nimenrix gleichzeitig mit anderen injizierbaren Impfstoffen verabreicht wird, sollten die Impfstoffe immer in verschiedene Gliedmaßen injiziert werden. Es wird möglicherweise bei Patienten unter immunsuppressiver Therapie keine ausreichende Immunantwort erzielt. FACHINFORMATION Vorteile die potentiellen Risiken überwiegen. Fertilität Tierexperimentelle Studien ergaben keine Hinweise auf direkte oder indirekte gesundheitsschädliche Wirkungen in Bezug auf die Fertilität. 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und das Bedienen von Maschinen durchgeführt. Einige der im Abschnitt 4.8 genannten Nebenwirkungen können jedoch die Verkehrstüchtigkeit oder die Fähigkeit zum Bedienen von Maschinen beeinflussen. 4.8 Nebenwirkungen Zusammenfassung des Nebenwirkungsprofils Das unten aufgezeigte Nebenwirkungsprofil basiert auf Daten aus einer gepoolten Analyse von Personen, die in klinischen Studien mit einer Dosis Nimenrix geimpft wurden. Diese gepoolte Analyse enthält Daten von Kleinkindern (12 bis 23 Monate),1.809Kindern(2bis10Jahre),2.011 Jugendlichen (11 bis 17 Jahre) und Erwachsenen ( 18 Jahre). In allen Altersgruppen waren die am häufigsten berichteten lokalen Nebenwirkungen nach der Impfung Schmerzen (24,1 % bis 39,9 %), Rötung (14,3 % bis 33,0 %) und Schwellung (11,2 % bis 17,9 %). In den Altersgruppen von Monaten und 2 5 Jahren waren die am häufigsten berichteten allgemeinen Nebenwirkungen nach der Impfung Reizbarkeit (36,2 % bzw. 7,5 %), Schläfrigkeit (27,8 % bzw. 8,8 %), Appetitlosigkeit (20,7 % bzw. 6,3 %) und Fieber (17,6 % bzw. 6,5 %). In den Altersgruppen von 6 10 Jahren, Jahren und 18 Jahren waren die am häufigsten berichteten allgemeinen Nebenwirkungen nach der Impfung Kopfschmerzen (13,3 % bzw. 16,1 % bzw. 17,6 %), Müdigkeit (13,8 % bzw. 16,3 % bzw. 16,4 %), gastrointestinale Beschwerden (7,5 % bzw. 6,4 % bzw. 6,3 %) und Fieber(7,5%bzw.4,1%bzw.4,0%). Tabellarische Liste von Nebenwirkungen In den klinischen Studien, die in der gepoolten Sicherheitsanalyse enthalten waren, wurden die Nebenwirkungen wie in der untenstehenden Tabelle aufgeführt, beobachtet. Die Häufigkeit der berichteten Nebenwirkungen ist in folgende Kategorien eingeteilt: Sehr häufig: ( 1/10) Häufig: ( 1/100 bis <1/10) Gelegentlich: ( 1/1.000 bis <1/100) Selten: ( 1/ bis <1/1.000) Sehr selten: (<1/10.000) 4.9 Überdosierung Es wurden keine Fälle von Überdosierung berichtet. 5. PHARMAKOLOGISCHE EIGEN- SCHAFTEN 5.1 Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe: Impfstoffe, Meningokokken-Impfstoffe, ATC-Code: J07AH08 Wirkmechanismus Antikapsuläre Meningokokken-Antikörper schützen vor Meningokokkenerkrankungen durch Komplement-vermittelte bakterizide Aktivität. Nimenrix induziert die Produktion von bakteriziden Antikörpern gegen Kapsel- Polysaccharide der Gruppen A, C, W-135 und Y, gemessen mit Testsystemen, bei denen entweder Kaninchen-Komplement (rsba) oder humanes Komplement (hsba) verwendet wird. Pharmakodynamische Wirkungen Das klinische Entwicklungsprogramm von Nimenrix umfasste 17 klinische Studien, 4.6 Fertilität, Schwangerschaft und Stillzeit Schwangerschaft Bisher liegen nur begrenzte Erfahrungen mit der Anwendung von Nimenrix bei Schwangeren vor. Tierexperimentelle Studien ergaben keine Hinweise auf direkte oder indirekte gesundheitsschädliche Wirkungen in Bezug auf die Schwangerschaft, embryonale/fetale Entwicklung, Geburt oder postnatale Entwicklung (siehe Abschnitt 5.3). Nimenrix sollte während der Schwangerschaft nur angewendet werden, wenn dies unbedingt notwendig ist und die möglichen Vorteile die potentiellen Risiken für den Fötus überwiegen. Stillzeit Es ist nicht bekannt, ob Nimenrix in die Muttermilch übergeht. Nimenrix sollte während der Stillzeit nur verabreicht werden, wenn die möglichen Systemorganklassen Häufigkeit Nebenwirkungen Stoffwechsel- und Ernährungsstörungen Sehr häufig Appetitlosigkeit Psychiatrische Erkrankungen Sehr häufig Reizbarkeit Gelegentlich Schlaflosigkeit, Schreien Erkrankungen des Nervensystems Sehr häufig Schläfrigkeit, Kopfschmerzen Gelegentlich Hypästhesien, Schwindel Erkrankungen des Gastrointestinaltrakts Erkrankungen der Haut und des Unterhautzellgewebes Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Häufig Gelegentlich Gelegentlich Sehr häufig Häufig Gelegentlich Gastrointestinale Beschwerden (einschließlich Durchfall, Erbrechen und Übelkeit) Pruritus, Hautausschlag Myalgie, Schmerzen in den Extremitäten Fieber, Schwellung, Schmerzen und Rötung an der Injektionsstelle, Müdigkeit Hämatom an der Injektionsstelle Unwohlsein, Reaktionen an der Injektionsstelle (einschließlich Verhärtung, Pruritus, Wärme, Schmerzunempfindlichkeit) E753 Nimenrix n
3 Tabelle 1: Bakterizide Antikörperantworten (rsba) bei Kleinkindern im Alter von Monaten Antwort auf Studie MenACWY-TT-039 rsba (1) A Nimenrix ,7 % (98,4; 100) C Nimenrix ,7 % (98,4; 100) In der Studie MenACWY-TT-081 wurde für Nimenrix die Nicht-Unterlegenheit gegenüber einem anderen zugelassenen MenC- MenC-CRM- Impfstoff ,5% (92,9; 99,5) W-135 Nimenrix % (99,0; 100) Y Nimenrix % (99,0; 100) 2205,0 (2007,8; 2421,6) 477,6 (437,3; 521,6) 212,3 (170,0; 265,2) 2681,7 (2453,1; 2931,6) 2729,4 (2472,7; 3012,8) Studie MenACWY-TT-040 rsba (2) ,4 % (95,3; 99,7) ,3 % (93,7; 99,1) ,2 % (93,8; 99,8) ,4 % (95,4; 99,7) ,3 % (93,8; 99,1) Die Immunogenitätsanalyse wurde in den gemäß Studienprotokoll behandelten (ATP) Kohorten für Immunogenität durchgeführt. (1) Entnahme der Blutproben 42 bis 56 Tage nach der Impfung (2) Entnahme der Blutproben 30 bis 42 Tage nach der Impfung 3169,9 (2577,2; 3898,8) 828,7 (672,4; 1021,4) 691,4 (520,8; 917,9) 4022,3 (3269,2; 4948,8) 3167,7 (2521,9; 3978,9) die in 17 Ländern weltweit durchgeführt wurden. Auf die Wirksamkeit des Impfstoffes wurde durch den Beweis der immunologischen Nicht-Unterlegenheit (hauptsächlich basierend auf dem Vergleich des Anteils an Probanden mit einem rsba-titer von mindestens 1 : 8) gegenüber zugelassenen Meningokokken-Impfstoffen geschlossen. Die Immunogenität wurde anhand von rsba oder hsba gemessen, welche Biomarker für eine Schutzwirkung gegen Meningokokken-Gruppen A, C, W-135 und Y sind. Immunogenität bei Kleinkindern im Alter von Monaten In den klinischen Studien MenACWY-TT- 039 und MenAWY-TT-040 wurde die Immunantwort nach Impfung mit Nimenrix oder einem zugelassenen Meningokokken C- CRM 197 -Konjugatimpfstoff (MenC-CRM) untersucht. Nimenrix löste eine bakterizide Antikörperantwort gegen die vier n aus, wobei die Antwort auf die Gruppe C hinsichtlich der rsba-titer von 8vergleichbar mit derjenigen des zugelassenen MenC- CRM-Impfstoffes war (Tabelle 1). In der Studie MenACWY-TT-039 wurde als sekundärer Endpunkt auch die bakterizide Aktivität im Serum, unter Verwendung von humanem Serum als Quelle für das Komplement (hsba), gemessen (Tabelle 2). Immunogenität bei Kindern im Alter von 2 10 Jahren In zwei Vergleichsstudien, die an Probanden im Alter von 2 10 Jahren durchgeführt wurden, erhielt eine Gruppe der Probanden einedosisnimenrixunddiezweitegruppe entweder eine Dosis eines zugelassenen MenC-CRM-Impfstoffes (Studie MenAC- WY-TT-081) oder eine Dosis des zugelassenen einfachen Polysaccharid-Meningokokken-Impfstoffes der Gruppe A, C, W-135,Y (ACWY-PS) von GlaxoSmithKline Biologicals (Studie MenACWY-TT-038) als Vergleichspräparat. In der Studie MenACWY-TT-038 wurde für Nimenrix die Nicht-Unterlegenheit gegenüber dem zugelassenen ACWY-PS-Impfstoff hinsichtlich der Immunantwort auf die vier n (A, C, W-135 und Y) gezeigt (siehe Tabelle 3). Die Immunantwort wurde definiert als Anteil an Probanden mit: einem rsba-titer von 32 für zu Beginn seronegative Probanden (d. h. rsba-titer <8 vor der Impfung) mindestens 4-fachem Anstieg der rsba- TiternachderImpfungimVergleichzu vor der Impfung für zu Beginn seropositive Probanden (d. h. rsba-titer 8vor der Impfung) Tabelle 2: Bakterizide Antikörperantworten (hsba) bei Kleinkindern im Alter von Monaten Antwort auf N Studie MenACWY-TT-039 hsba (1) 8 A Nimenrix ,2 % (72,4; 81,6) C Nimenrix ,5 % (96,6; 99,5) MenC-CRM- Impfstoff ,9 % (73,7; 88,4) W-135 Nimenrix ,5 % (83,5 ; 90,8) Y Nimenrix ,3 % (74,5; 83,6) 19,0 (16,4; 22,1) 196,0 (175,4; 219,0) 40,3 (29,5; 55,1) 48,9 (41,2; 58,0) 30,9 (25,8; 37,1) Die Immunogenitätsanalyse wurde in den ATP-Kohorten für Immunogenität durchgeführt. (1) Entnahme der Blutproben 42 bis 56 Tage nach der Impfung Tabelle 3: Bakterizide Antikörperantworten (rsba) auf Nimenrix und auf den ACWY- PS-Impfstoff bei Kindern im Alter von 2 10 Jahren einen Monat nach der Impfung (Studie MenACWY-TT-038) N Nimenrix Immunantwort A ,6 % (85,8; 90,9) C ,9 % (94,2; 97,2) W ,4 % (96,0; 98,4) Y ,5 % (90,4; 94,2) 6309,7 (5979,0; 6658,8) 4983,6 (4514,1; 5502,0) 11569,8 (10910,7; 12268,7) 10886,6 (10310,7; 11494,5) N ACWY-PS-Impfstoff Immunantwort ,5 % (58,6; 72,0) ,6 % (85,2; 93,1) ,5 % (77,3; 87,0) ,6 % (62,6; 74,2) 2309,4 (2055,8; 2594,3) 1386,8 (1108,9; 1734,4) 2150,6 (1823,9; 2535,8) 2544,7 (2178,2; 2972,9) Die Immunogenitätsanalyse wurde in der ATP-Kohorte für Immunogenität durchgeführt E753 Nimenrix n 3
4 FACHINFORMATION CRM-Impfstoff hinsichtlich der Immunantwort auf die MenC-Gruppe gezeigt [94,8 % (95 % KI:91,4; 97,1) bzw. 95,7 % (95 % KI: 89,2; 98,8)]; die s waren für die Nimenrix-Gruppe [2794,8 (95 % KI: 2393,5; 3263,3)] im Vergleich zum MenC-CRM-Impfstoff [5291,6 (95 % KI: 3814,6; 7340,5)] niedriger. Immunogenität bei Jugendlichen im Alter von Jahren und Erwachsenen im Alter von 18 Jahren In zwei klinischen Studien, die mit Jugendlichen im Alter von Jahren (Studie MenACWY-TT-036) und Erwachsenen im Alter von Jahren (Studie MenAC- WY-TT-035) durchgeführt worden waren, wurde entweder eine Dosis Nimenrix oder eine Dosis des ACWY-PS-Impfstoffes verabreicht. Sowohl bei Jugendlichen als auch bei Erwachsenen wurde für Nimenrix die immunologische Nicht-Unterlegenheit gegenüber dem ACWY-PS-Impfstoff hinsichtlich der oben definierten Immunantwort (Tabelle 4) gezeigt. Die Antwort auf die vier Meningokokken-Gruppen, die durch Nimenrix hervorgerufen wurde, war entweder ähnlich oder höher als die durch den ACWY-PS- Impfstoff ausgelöste Immunantwort. Persistenz der Immunantwort Die Persistenz der durch Nimenrix hervorgerufenen Immunantwort wurde 12 bis 42 Monate nach der Impfung von Probanden im Alter von 12 Monaten bis 55 Jahren untersucht. In allen Altersgruppen waren die zum Zeitpunkt der Persistenzbestimmung beobachteten rsba-s für alle vier n höher als vor der Impfung. Für alle n (A, C, W-135, Y) war die Antikörper-Persistenz bei Nimenrix ähnlich oder höher als bei den zugelassenen Meningokokken-Impfstoffen (d. h. MenC- CRM-Impfstoff bei Probanden im Alter von Monaten und ACWY-PS-Impfstoff bei Probanden über 2 Jahren). Persistenz der Immunantwort bei Kleinkindern In der Studie MenACWY-TT-048 wurde die Persistenz der Immunantwort bei Kleinkindern, die in der Studie MenACWY-TT-039 grundimmunisiert worden waren, anhand von rsba und hsba zwei Jahre nach der Impfung untersucht (Tabelle 5). Im Gegensatz zur beobachteten rsba-mena-persistenz, fand eine rasche Abnahme der hsba-mena-antikörper statt (siehe Abschnitt 4.4). Persistenz der Immunantwort bei Kindern im Alter von 6 10 Jahren In der Studie MenACWY-TT-028 wurde die Persistenz der Immunantwort anhand von hsba ein Jahr nach der Impfung von Kindern im Alter von 6 10 Jahren untersucht, dieinderstudiemenacwy-tt-027grundimmunisiert worden waren (Tabelle 6 auf Seite 5) (siehe Abschnitt 4.4). Persistenz der Immunantwort bei Jugendlichen In der Studie MenACWY-TT-043 wurde die Persistenz der Immunantwort bei Jugendlichen, die in der Studie MenACWY-TT-036 grundimmunisiert worden waren, zwei Jahre nach der Impfung untersucht (Tabelle 7 auf Seite 5). Für die Hauptergebnisse dieser Studie, siehe bitte Tabelle 4. Tabelle 4: Bakterizide Antikörperantworten (rsba) auf Nimenrix und auf den ACWY-PS-Impfstoff bei Jugendlichen im Alter von Jahren und Erwachsenen 18 Jahren einen Monat nach der Impfung Studie (Altersgruppe) Studie MenACWY- TT-036 (11 17 Jahre) Studie MenACWY- TT-035 (18 55 Jahre) Nimenrix ACWY-PS-Impfstoff N Immunantwort N Immunantwort A ,4 % (82,3; 88,1) C ,1 % (95,6; 98,2) W ,5 % (94,9; 97,7) Y ,1 % (91,0; 94,8) A ,1 % (77,0; 82,9) C ,5 % (89,4; 93,3) W ,2 % (88,1; 92,1) Y ,0 % (84,6; 89,2) 6106,8 (5739,5; 6497,6) 12645,5 (11531,8; 13866,7) 8390,1 (7777,8; 9050,7) 13865,2 (12968,1; 14824,4) 3624,7 (3371,7; 3896,8) 8865,9 (8011,0; 9812,0) 5136,2 (4698,8; 5614,3) 7710,7 (7100,1; 8373,8) Die Immunogenitätsanalyse wurde in den ATP-Kohorten für Immunogenität durchgeführt ,5 % (73,5; 84,7) ,6 % (93,5; 98,5) ,0 % (83,2; 91,8) ,0 % (72,3; 83,1) ,8 % (63,8; 75,4) ,0 % (88,3; 94,9) ,5 % (80,9; 89,4) ,8 % (73,6; 83,4) Tabelle 5: 2-Jahres-Persistenzdaten bei Kleinkindern im Alter von Monaten zum Zeitpunkt der Impfung 3203,0 (2854,1; 3594,6) 8271,6 (6937,3; 9862,4) 2679,3 (2363,7; 3037,2) 5245,3 (4644,2; 5924,1) 2127,2 (1909,2; 2370,1) 7371,2 (6297,4; 8628,2) 2461,3 (2081,0; 2911,0) 4314,3 (3782,1; 4921,5) Antwort auf rsba hsba A Nimenrix ,8 % (94,4; 99,4) C Nimenrix ,2 % (82,6; 92,4) MenC-CRM- Impfstoff 29 69,0 % (49,2; 84,7) W-135 Nimenrix ,9 % (96,2; 99,9) Y Nimenrix ,9 % (94,6; 99,4) 420,3 (356,1; 495,9) 98,1 (77,7; 123,8) 53,5 (25,5; 112,0) 369,9 (342,0; 460,5) 396,6 (324,0; 485,5) ,0 % (17,1; 29,7) ,9 % (80,9; 91,5) 19 52,6 % (28,9; 75,6) ,1 % (86,0; 94,8) ,0 % (80,7; 91,9) 3,8 (3,2; 4,5) 50,2 (38,7; 65,1) 10,4 (4,4; 22,8) 77,7 (61,8; 97,6) 58,1 (44,5; 75,8) E753 Nimenrix n
5 Tabelle6: PersistenzdatenbeiKindernimAltervon6 10JahreneinenMonatundeinJahrnachderImpfung Antwort auf 1 Monat nach Impfung 1-Jahres-Persistenz A Nimenrix ,0 % (71,1; 87,2) ACWY-PS 35 25,7% (12,5; 43,3) C Nimenrix ,1% (81,3; 94,4) ACWY-PS 38 39,5% (24,0; 56,6) W-135 Nimenrix ,1% (89,0; 98,4) ACWY-PS 35 34,3% (19,1; 52,2) Y Nimenrix 89 83,1% (73,7; 90,2) ACWY-PS 32 43,8% (26,4; 62,3) 53,4 (37,3; 76,2) 4,1 (2,6; 6,5) 155,8 (99,3; 244,3) 13,1 (5,4; 32,0) 133,5 (99,9; 178,4) 5,8 (3,3; 9,9) 95,1 (62,4; 145,1) 12,5 (5,6; 27,7) ,3% (9,8; 24,9) 35 5,7% (0,7; 19,2) ,2% (89,2; 98,4) 31 32,3% (16,7; 51,4) % (96,5; 100) 31 12,9% (3,6; 29,8) ,1% (94,9; 100) 36 33,3% (18,6; 51,0) 3,5 (2,7; 4,4) 2,5 (1,9; 3,3) 129,5 (95,4; 175,9) 7,7 (3,5; 17,3) 256,7 (218,2; 301,9) 3,4 (2,0; 5,8) 265,0 (213,0; 329,6) 9,3 (4,3; 19,9) Persistenz der Immunantwort bei Jugendlichen und Erwachsenen im Alter von Jahren In der Studie MenACWY-TT-059 wurde die Persistenz der Immunantwort anhand von hsba ein Jahr nach der Impfung von Jugendlichen und Erwachsenen im Alter von Jahren untersucht, die in der Studie MenACWY-TT-052 grundimmunisiert worden waren (Tabelle 8) (siehe Abschnitt 4.4). Immungedächtnis In der Studie MenACWY-TT-014 wurde die Induktion des Immungedächtnisses einen Monat nach der Verabreichung eines Fünftels einer Dosis des ACWY-PS-Impfstoffes (10 μg je Polysaccharid) bei Kindern im dritten Lebensjahr untersucht, die vorher in der Studie MenACWY-TT-013 mit Nimenrix oder mit dem zugelassenen MenC-CRM-Impfstoff im Alter von 12 bis 14 Monaten grundimmunisiert worden waren. Tabelle 7: 2-Jahres-Persistenzdaten (rsba) bei Jugendlichen im Alter von Jahren zum Zeitpunkt der Impfung Nimenrix A ,8 % (98,8; 100) C ,3 % (98,1; 99,9) W ,6 % (98,4; 99,9) Y % (99,2; 100) 1517,4 (1399,7; 1645,1) 1121,9 (996,9; 1262,6) 2070,6 (1869,6; 2293,0) 3715,9 (3409,3; 4049,9) ACWY-PS-Impfstoff % (97,5; 100) ,6 % (95,1; 99,8) ,1 % (90,2; 98,0) ,2 % (92,9; 99,2) 810,6 (695,9; 944,3) 1499,0 (1119,6; 2006,8) 442,6 (341,8; 573,0) 1090,3 (857,7; 1386,1) Tabelle 8: Persistenzdaten bei Jugendlichen und Erwachsenen im Alter von Jahren einen Monat und ein Jahr nach der Impfung Die Europäische Arzneimittel-Agentur hat eine Zurückstellung von der Verpflichtung zur Vorlage von Ergebnissen aus Studien zu Nimenrix zur Prävention von Meningokokkenerkrankungen, die durch Neisseria meningitidis der Gruppen A, C, W-135 und Y verursacht werden, in einer oder mehreren pädiatrischen Altersklassen gewährt (siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen). 1 Monat nach Impfung 1-Jahres-Persistenz A ,0% (77,6; 85,9) C ,1% (93,5; 97,9) W ,0% (87,4; 93,9) Y ,1% (92,3; 97,0) 58,7 (48,6; 70,9) 532,0 (423,8; 667,8) 116,8 (96,8; 141,0) 246,0 (207,7; 291,4) ,1% (24,4; 34,2) ,9% (92,0; 97,0) ,5% (96,5; 99,5) ,8% (95,6; 99,0) 5,4 (4,5; 6,4) 172,0 (142,5; 207,4) 197,5 (173,0; 225,5) 271,8 (237,5: 311,2) Einen Monat nach dieser erneuten Provokationsdosis (Challenge-Dosis) stiegen die s, die bei den mit Nimenrix grundimmunisierten Probanden hervorgerufen wurden, für die n A, C, W-135 und Y 6,5 bis 8fach an. Dies zeigt, dass Nimenrix ein Immungedächtniss für die Gruppen A, W-135 und Y induziert. In beiden Studiengruppen war der rsba-menc- nach der Provokationsdosis vergleichbar und zeigt an, dass Nimenrix ein zum zugelassenen MenC-CRM-Impfstoff analoges Immungedächtnis für die C induziert (Tabelle 9 auf Seite 6). Probanden, die früher mit einem einfachen Polysaccharid-Impfstoff gegen Neisseria meningitidis geimpft wurden In der bei Probanden im Alter von 4,5 34 Jahren durchgeführten Studie MenACWY- TT-021 wurde die Immunogenität einer Impfung mit Nimenrix, die zwischen 30 und 42 Monaten nach der Impfung mit einem ACWY-PS-Impfstoff vorgenommen wurde, mitderimmunogenitätvonprobandenim gleichen Alter verglichen, die in den vergangenen zehn Jahren keinen Meningokokken-Impfstoff erhalten haben. Bei allen Probanden wurde, unabhängig vom Meningokokken-Impfstatus, eine Immunantwort (rsba-titer 8) auf alle Gruppen (A, C, W-135, Y) beobachtet. Bei Personen, die Monate vor Nimenrix eine Dosis des ACWY-PS-Impfstoffes erhielten, waren die rsba-s signifikant niedriger (Tabelle 10 auf Seite 6) (siehe Abschnitt 4.4) E753 Nimenrix n 5
6 FACHINFORMATION Tabelle 9: Immunantwort (rsba) einen Monat nach der Provokationsdosis bei Probanden, die mit Nimenrix oder einem MenC-CRM-Impfstoff im Alter von 12 bis 14 Monaten grundimmunisiert worden waren Antwort auf Vor der Provokationsdosis N A Nimenrix ,0 (325,0; 910,7) C Nimenrix ,0 (104,8; 288,9) Meningitec 28 34,4 (15,8; 75,3) W-135 Nimenrix ,8 (394,1; 1051,8) Y Nimenrix ,8 (274,0; 705,9) Nach der Provokationsdosis N ,9 (2294,2; 4810,0) ,7 (4128,4; 8620,7) ,2 (3437,3; 8065,1) ,1 (8587,2; 14239,9) ,6 (4215,9; 7806,0) Die Immunogenitätsanalyse wurde in der ATP-Kohorte für Immunogenität durchgeführt. 6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung Anleitung für die Rekonstitution des Impfstoffes mit dem Lösungsmittel in einer Fertigspritze Nimenrix wird rekonstituiert, indem man der Durchstechflasche mit dem darin enthaltenen Pulver den gesamten Inhalt der Fertigspritze zusetzt. Um die Nadel an der Spritze zu befestigen, siehe bitte untenstehendes Bild. Die mit Nimenrix zur Verfügung gestellte Spritze kann sich jedoch etwas von der im Bild beschriebenen Spritze unterscheiden (ohne Schraubgewinde). In diesem Fall sollte die Nadel ohne Verschrauben befestigt werden. 1. Halten Sie den Spritzenzylinder in einer Hand (vermeiden Sie, die Spritze am Kolben zu halten), drehen Sie die Spritzenkappe entgegen dem Uhrzeigersinn ab. Tabelle 10: Immunantwort (rsba) einen Monat nach einer Nimenrix-Impfung gemäß des Meningokokken-Impfstatus der Probanden Probanden, die 30 bis 42 Monate vorher mit ACWY-PS geimpft worden waren A % (97,5; 100) C % (97,8; 100) W % (97,8; 100) Y % (97,8; 100) 5.2 Pharmakokinetische Eigenschaften Nicht zutreffend. 5.3 Präklinische Daten zur Sicherheit Basierend auf den Studien zur lokalen Verträglichkeit, akuten Toxizität, Toxizität bei wiederholter Gabe, Entwicklungs-/Reproduktionstoxizität und Fertilität lassen die präklinischen Daten keine besonderen Gefahren für den Menschen erkennen. 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile Pulver: Saccharose Trometamol Lösungsmittel: Natriumchlorid Wasser für Injektionszwecke 6868,8 (6044,9; 7805,0) 1945,8 (1583,3; 2391,1) 4635,7 (3942,5; 5450,7) 7799,9 (6682,8; 9103,6) 6.2 Inkompatibilitäten Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieses Arzneimittel nicht mit anderen Arzneimitteln gemischt werden 6.3 Dauer der Haltbarkeit 3Jahre Nach Rekonstitution: Nach dem Auflösen sollte der Impfstoff sofort verwendet werden. Jedoch konnte Probanden, die keinen Meningokokken-Impfstoff in den vergangenen 10 Jahren erhalten hatten % (94,8; 100) % (95,2; 100) % (95,2; 100) % (95,2; 100) 13014,9 (10722,2; 15798,0) 5494,6 (4266,3; 7076,5) 9078,0 (7087,7; 11627,1) 13895,5 (11186,2; 17260,9) Die Immunogenitätsanalyse wurde in der ATP-Kohorte für Immunogenität durchgeführt. für den gelösten Impfstoff chemische und physikalische Stabilität für 24 Stunden bei 30 C gezeigt werden. 6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung Im Kühlschrank lagern (2 C 8 C). Nicht einfrieren. In der Originalverpackung aufbewahren, um den Inhalt vor Licht zu schützen. Aufbewahrungsbedingungen nach Rekonstitution des Arzneimittels, siehe Abschnitt Art und Inhalt des Behältnisses Pulver in einer Durchstechflasche (Glas Typ I) mit einem Stopfen (Butylgummi) und Lösungsmittel in einer Fertigspritze mit einem Stopfen (Butylgummi). Packungsgrößen zu 1 und 10 mit oder ohne Nadeln/Kanülen. Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht. 2. Um die Nadel an der Spritze anzubringen, drehen Sie die Nadel im Uhrzeigersinn in die Spritze bis sie fest sitzt (siehe Bild). 3. Entfernen Sie den Nadelschutz, der gelegentlich ein wenig fest sitzen kann. 4. Geben Sie das Lösungsmittel zu dem Pulver. Die Mischung ist gründlich zu schütteln bis das Pulver vollständig gelöst ist. Der rekonstituierte Impfstoff ist eine klare, farblose Lösung. Der rekonstituierte Impfstoff ist vor der Verabreichung per Augenschein auf Fremdpartikel und/oder physikalische Veränderungen zu untersuchen. Falls solche beobachtet werden, ist der Impfstoff zu verwerfen. Der Impfstoff sollte nach Rekonstitution unverzüglich verabreicht werden. Zur Verabreichung des Impfstoffes sollte eine neue Nadel/Kanüle verwendet werden. Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen. 7. INHABER DER ZULASSUNG GlaxoSmithKline Biologicals S.A. Ruedel Institut89 B-1330 Rixensart Belgien 8. ZULASSUNGSNUMMER(N) EU/1/12/767/001 EU/1/12/767/ E753 Nimenrix n
7 9. DATUM DER ERTEILUNG DER ZU- LASSUNG/VERLÄNGERUNG DER ZULASSUNG Datum der Erteilung der Zulassung: STAND DER INFORMATION April 2012 Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur verfügbar. 11. VERKAUFSABGRENZUNG Verschreibungspflichtig 12. KONTAKTADRESSE IN DEUTSCH- LAND GlaxoSmithKline GmbH & Co. KG München Service Tel.: ServiceFax: produkt.info@gsk.com IN DEUTSCHLAND VERFÜGBARE PACKUNGSGRÖSSEN EU/1/12/767/001 1 Durchstechflasche mit 1 Fertigspritze (ohne Nadel) EU/1/12/767/ Durchstechflaschen mit 10 Fertigspritzen (ohne Nadeln) PAE Zentrale Anforderung an: Rote Liste Service GmbH FachInfo-Service Postfach Berlin E753 Nimenrix n 7
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 AHAG I ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit.
AHAG I ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit.
Hepatyrix Injektionssuspension Hepatitis-A-(inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) ab dem vollendeten 15.
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER 22.07.2009 Hepatyrix Injektionssuspension Hepatitis-A-(inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) ab dem vollendeten 15. Lebensjahr
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER 22.07.2009 Hepatyrix Injektionssuspension Hepatitis-A-(inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) ab dem vollendeten 15. Lebensjahr
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 AHAG I ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1 1. BEZEICHUG DES ARZEIMITTELS imenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen
AHAG I ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1 1. BEZEICHUG DES ARZEIMITTELS imenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen
EINVERSTÄNDISERKLÄRUNG ZUR SCHUTZIMPFUNG
 EINVERSTÄNDISERKLÄRUNG ZUR SCHUTZIMPFUNG Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff BITTE
EINVERSTÄNDISERKLÄRUNG ZUR SCHUTZIMPFUNG Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff BITTE
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Legalon SIL - Trockensubstanz zur Infusionsbereitung
 PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Viscosan - Augentropfen Wirkstoff: Hypromellose
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A, C, Y und W 135 -Impfstoff 2.
1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A, C, Y und W 135 -Impfstoff 2.
Gebrauchsinformation: Information für Anwender. LOMUSOL Augentropfen. Wirkstoff: Dinatriumcromoglicat
 Gebrauchsinformation: Information für Anwender LOMUSOL Augentropfen Wirkstoff: Dinatriumcromoglicat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für Anwender LOMUSOL Augentropfen Wirkstoff: Dinatriumcromoglicat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
 Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
WAS finde ich WO im Beipackzettel
 WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
Sonstige Bestandteile: Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 1. BEZEICHNUNG DES ARZNEIMITTELS MUTAGRIP Kinder 2014/2015 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis
1. BEZEICHNUNG DES ARZNEIMITTELS MUTAGRIP Kinder 2014/2015 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis
Packungsbeilage CORSODYL Mundspüllösung / Spray 03-2012 Seite 1/5 BE106802 / BE191764 Belgien GEBRAUCHINFORMATION: INFORMATION FÜR DEN ANWENDER
 Seite 1/5 BE106802 / BE191764 Belgien GEBRAUCHINFORMATION: INFORMATION FÜR DEN ANWENDER CORSODYL 200mg/100ml mundwasser CORSODYL 200mg/100ml spray zur Anwendung in der Mundhöhle Chlorhexidindigluconat
Seite 1/5 BE106802 / BE191764 Belgien GEBRAUCHINFORMATION: INFORMATION FÜR DEN ANWENDER CORSODYL 200mg/100ml mundwasser CORSODYL 200mg/100ml spray zur Anwendung in der Mundhöhle Chlorhexidindigluconat
FACHINFORMATION. 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen
 FACHINFORMATION Mencevax ACWY März 2014 493134PD502J 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A,
FACHINFORMATION Mencevax ACWY März 2014 493134PD502J 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A,
AUFKLÄRUNGSBLATT* ZUR IMPFUNG GEGEN DIE FSME (Frühsommer-Meningoenzephalitis) *(Auszug aus den jeweiligen Packungsinformationen)
 AUFKLÄRUNGSBLATT* ZUR IMPFUNG GEGEN DIE FSME (Frühsommer-Meningoenzephalitis) *(Auszug aus den jeweiligen Packungsinformationen) Lesen Sie die gesamte Information sorgfältig durch, bevor Sie sich bzw.
AUFKLÄRUNGSBLATT* ZUR IMPFUNG GEGEN DIE FSME (Frühsommer-Meningoenzephalitis) *(Auszug aus den jeweiligen Packungsinformationen) Lesen Sie die gesamte Information sorgfältig durch, bevor Sie sich bzw.
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Protagent-Einmalaugentropfen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Lösung (= ca. 30 Tropfen) enthält 20 mg
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Protagent-Einmalaugentropfen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Lösung (= ca. 30 Tropfen) enthält 20 mg
Nasa Rhinathiol 0,1 %ige Nasenspray, Lösung Xylometazolinhydrochlorid
 Seite 1/5 Packungsbeilage Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mir der Anwendung dieses Arzneimittels beginnen. Sie enthält wichtige Informationen für Ihre Behandlung. Wenn
Seite 1/5 Packungsbeilage Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mir der Anwendung dieses Arzneimittels beginnen. Sie enthält wichtige Informationen für Ihre Behandlung. Wenn
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen
 Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
1. Was ist Priorix Tetra und wofür wird es angewendet?
 Gebrauchsinformation: Information für Anwender PRIORIX TETRA, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Impfstoff gegen Masern, Mumps, Röteln und Windpocken (lebend) Lesen Sie die
Gebrauchsinformation: Information für Anwender PRIORIX TETRA, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Impfstoff gegen Masern, Mumps, Röteln und Windpocken (lebend) Lesen Sie die
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. PROGESTOGEL 1 % Gel. Progesteron
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER PROGESTOGEL 1 % Gel Progesteron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER PROGESTOGEL 1 % Gel Progesteron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Heumann s Blasen- und Nierentee Solubitrat Wirkstoffe: Dickextrakt aus Birkenblättern, Dickextrakt aus Riesengoldrutenkraut Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Heumann s Blasen- und Nierentee Solubitrat Wirkstoffe: Dickextrakt aus Birkenblättern, Dickextrakt aus Riesengoldrutenkraut Lesen Sie die gesamte Packungsbeilage
Anleitung zur Handhabung von Durchstechflasche und Einmalspritze (für Patienten, Ärzte, Diabetesberater und Apotheker)
 Anleitung zur Handhabung von Durchstechflasche und Einmalspritze (für Patienten, Ärzte, Diabetesberater und Apotheker) EIN LEITFADEN ZUR ERSTEN VERWENDUNG VON APIDRA in 10ml- DURCHSTECHFLASCHEN Apidra
Anleitung zur Handhabung von Durchstechflasche und Einmalspritze (für Patienten, Ärzte, Diabetesberater und Apotheker) EIN LEITFADEN ZUR ERSTEN VERWENDUNG VON APIDRA in 10ml- DURCHSTECHFLASCHEN Apidra
Bijsluiter DE versie Imaverol 100 mg (glas) B. PACKUNGSBEILAGE 1
 B. PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION Imaverol 100 mg, Konzentrat zur örtlichen Anwendung 1.NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
B. PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION Imaverol 100 mg, Konzentrat zur örtlichen Anwendung 1.NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Gebrauchsinformation: Information für Patienten und Anwender
 Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
1. Was sind Dorithricin Halstabletten und wofür werden sie angewendet?
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Dorithricin - Halstabletten Wirkstoffe: Tyrothricin, Benzalkoniumchlorid, Benzocain Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Dorithricin - Halstabletten Wirkstoffe: Tyrothricin, Benzalkoniumchlorid, Benzocain Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
Cytomegalie & Co. Häufige Virusinfektionen in der Schwangerschaft. Deutsches Grünes Kreuz e.v.
 Cytomegalie & Co Häufige Virusinfektionen in der Schwangerschaft Schwangerschaft Eine ganz besondere Zeit der Vorfreude Verantwortung Sorge Die werdenden Eltern möchten alles richtig machen für das Wohl
Cytomegalie & Co Häufige Virusinfektionen in der Schwangerschaft Schwangerschaft Eine ganz besondere Zeit der Vorfreude Verantwortung Sorge Die werdenden Eltern möchten alles richtig machen für das Wohl
FACHINFORMATION/ ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 imenrix FACHIFORMATIO/ ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die
imenrix FACHIFORMATIO/ ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 AHAG I ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1 1. BEZEICHUG DES ARZEIMITTELS - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135
AHAG I ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1 1. BEZEICHUG DES ARZEIMITTELS - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135
10.000 10.000. an Masern erkrankt. an Mumps erkrankt. mit Röteln infiziert
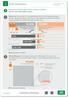 Nutzen: Bei Viruskontakt ist mein geimpftes Kind auch künftig besser gegen Masern, Mumps und Röteln geschützt. Je mehr Menschen geimpft sind, desto unwahrscheinlicher werden Kontakte mit dem Virus. ohne
Nutzen: Bei Viruskontakt ist mein geimpftes Kind auch künftig besser gegen Masern, Mumps und Röteln geschützt. Je mehr Menschen geimpft sind, desto unwahrscheinlicher werden Kontakte mit dem Virus. ohne
Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva
 Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva Darmstadt (19. Februar 2009) Die Merck KGaA hat heute bekannt gegeben, dass die europäische Arzneimittelbehörde EMEA
Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva Darmstadt (19. Februar 2009) Die Merck KGaA hat heute bekannt gegeben, dass die europäische Arzneimittelbehörde EMEA
Fragebogen Kopfschmerzen
 Fragebogen Kopfschmerzen Fragen an Dich Fragen an Dich Fragen an die Eltern Bei diesen Fragen geht es um Deine Kopfschmerzen. Es wäre schön, wenn Du darüber etwas sagst. Deine Antworten helfen, für Deine
Fragebogen Kopfschmerzen Fragen an Dich Fragen an Dich Fragen an die Eltern Bei diesen Fragen geht es um Deine Kopfschmerzen. Es wäre schön, wenn Du darüber etwas sagst. Deine Antworten helfen, für Deine
aktive / passive Immunisierung
 FS 2010 aktive / passive Immunisierung DTP-Impfstoff Michelle, Andrea 3Ma Überblick Wo befinden wir uns eigentlich? 10 000 Mia. Zellen Nerven-, Muskel-, Bindegewebsoder Blutzellen weißes BK (Leukozyt)
FS 2010 aktive / passive Immunisierung DTP-Impfstoff Michelle, Andrea 3Ma Überblick Wo befinden wir uns eigentlich? 10 000 Mia. Zellen Nerven-, Muskel-, Bindegewebsoder Blutzellen weißes BK (Leukozyt)
Meningitec 0,5 ml Injektionssuspension in einer Fertigspritze Meningokokken Serogruppe C Oligosaccharid Konjugatimpfstoff (adsorbiert) 2.
 Meningitec 0,5 ml Injektionssuspension in einer Fertigspritze Meningokokken Serogruppe C Oligosaccharid Konjugatimpfstoff (adsorbiert) 2. Qualitative und quantitative Zusammensetzung Eine Dosis (0,5 ml)
Meningitec 0,5 ml Injektionssuspension in einer Fertigspritze Meningokokken Serogruppe C Oligosaccharid Konjugatimpfstoff (adsorbiert) 2. Qualitative und quantitative Zusammensetzung Eine Dosis (0,5 ml)
APOTHEKIA SPECIAL DIE PILLE DANACH
 APOTHEKIA SPECIAL DIE PILLE DANACH Die zwei Pillen danach In Deutschland sind aktuell zwei Wirkstoffe für die Pille danach zugelassen, Ulipristalacetat (Handelsname ellaone) und Levonorgestrel (Handelsname
APOTHEKIA SPECIAL DIE PILLE DANACH Die zwei Pillen danach In Deutschland sind aktuell zwei Wirkstoffe für die Pille danach zugelassen, Ulipristalacetat (Handelsname ellaone) und Levonorgestrel (Handelsname
Krank durch Schlafstörungen
 Seite 1 von 6 I n f o r m a t i o n s m a t e r i a l v o m 1 2. 0 1. 2 0 1 2 Krank durch Schlafstörungen "Die meisten Menschen sterben an ihren Medikamenten und nicht an ihren Krankheiten", meinte der
Seite 1 von 6 I n f o r m a t i o n s m a t e r i a l v o m 1 2. 0 1. 2 0 1 2 Krank durch Schlafstörungen "Die meisten Menschen sterben an ihren Medikamenten und nicht an ihren Krankheiten", meinte der
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Meningitec-Injektionssuspension in Fertigspritze Konjugierter Oligosaccharid-Impfstoff gegen Meningokokken der Serogruppe C (adsorbiert) Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Meningitec-Injektionssuspension in Fertigspritze Konjugierter Oligosaccharid-Impfstoff gegen Meningokokken der Serogruppe C (adsorbiert) Lesen Sie die gesamte
Verschreibungsfreie Arzneimittel wieder in der Erstattung
 Satzungsleistungen Verschreibungsfreie Arzneimittel wieder in der Erstattung Was sind Satzungsleistungen? Der Rahmen für die Leistungen der gesetzlichen Krankenversicherung wird im Fünften Sozialgesetzbuch
Satzungsleistungen Verschreibungsfreie Arzneimittel wieder in der Erstattung Was sind Satzungsleistungen? Der Rahmen für die Leistungen der gesetzlichen Krankenversicherung wird im Fünften Sozialgesetzbuch
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Kamillosan -Mundspray. Kamillenblütenauszug Pfefferminzöl Anisöl
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Kamillosan -Mundspray Kamillenblütenauszug Pfefferminzöl Anisöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Kamillosan -Mundspray Kamillenblütenauszug Pfefferminzöl Anisöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
Deutsches Rotes Kreuz. Kopfschmerztagebuch von:
 Deutsches Rotes Kreuz Kopfschmerztagebuch Kopfschmerztagebuch von: Hallo, heute hast Du von uns dieses Kopfschmerztagebuch bekommen. Mit dem Ausfüllen des Tagebuches kannst Du mehr über Deine Kopfschmerzen
Deutsches Rotes Kreuz Kopfschmerztagebuch Kopfschmerztagebuch von: Hallo, heute hast Du von uns dieses Kopfschmerztagebuch bekommen. Mit dem Ausfüllen des Tagebuches kannst Du mehr über Deine Kopfschmerzen
Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis Polysaccharid-Impfstoff
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis Polysaccharid-Impfstoff
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren
 Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
1. WAS IST DAFALGAN Zäpfchen UND WOFÜR WIRD ES ANGEWENDET?
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DAFALGAN Säuglinge 80 mg Zäpfchen DAFALGAN Kleinkinder 150 mg Zäpfchen DAFALGAN große Kinder 300 mg Zäpfchen Paracetamol Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DAFALGAN Säuglinge 80 mg Zäpfchen DAFALGAN Kleinkinder 150 mg Zäpfchen DAFALGAN große Kinder 300 mg Zäpfchen Paracetamol Lesen Sie die gesamte Packungsbeilage
Zulassung nach MID (Measurement Instruments Directive)
 Anwender - I n f o MID-Zulassung H 00.01 / 12.08 Zulassung nach MID (Measurement Instruments Directive) Inhaltsverzeichnis 1. Hinweis 2. Gesetzesgrundlage 3. Inhalte 4. Zählerkennzeichnung/Zulassungszeichen
Anwender - I n f o MID-Zulassung H 00.01 / 12.08 Zulassung nach MID (Measurement Instruments Directive) Inhaltsverzeichnis 1. Hinweis 2. Gesetzesgrundlage 3. Inhalte 4. Zählerkennzeichnung/Zulassungszeichen
Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU - Kombination mit Sulfonylharnstoff n
 Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU Kombination mit Sulfonylharnstoff nun ebenfalls zugelassen Haar (März 2008) - Die europäische Arzneimittelbehörde EMEA hat JANUVIA für
Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU Kombination mit Sulfonylharnstoff nun ebenfalls zugelassen Haar (März 2008) - Die europäische Arzneimittelbehörde EMEA hat JANUVIA für
LANSOYL Paraffine Gel zum Einnehmenv3.0_B2.0 1/5
 PIL September 2015 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER LANSOYL PARAFFINE 78,230 g/100 g Gel zum Einnehmen Paraffinöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
PIL September 2015 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER LANSOYL PARAFFINE 78,230 g/100 g Gel zum Einnehmen Paraffinöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
RSV. RSV kennen. Das Virus, das Eltern kennen sollten. Informationen. Kinder schützen
 RSV kennen Kinder schützen RSV Das Virus, das Eltern kennen sollten. Informationen zu einem wenig bekannten Virus sowie praktische Ratschläge, wie Sie das Risiko einer RSV-Infektion verringern können.
RSV kennen Kinder schützen RSV Das Virus, das Eltern kennen sollten. Informationen zu einem wenig bekannten Virus sowie praktische Ratschläge, wie Sie das Risiko einer RSV-Infektion verringern können.
Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Einzeldosisbehältnis
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Einzeldosisbehältnis Polysaccharid-Impfstoff gegen
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Einzeldosisbehältnis Polysaccharid-Impfstoff gegen
BAnz AT 04.04.2014 B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
PACKUNGSBEILAGE. CORSODYL Zahngel, 10 mg Chlorhexidin digluconat pro g Zahngel
 Seite 1/5 981 IS 153 F7 Belgien PACKUNGSBEILAGE Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Wenn Sie weitere Fragen haben, wenden Sie sich an
Seite 1/5 981 IS 153 F7 Belgien PACKUNGSBEILAGE Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Wenn Sie weitere Fragen haben, wenden Sie sich an
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 AHAG I ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1 1. BEZEICHUG DES ARZEIMITTELS - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135
AHAG I ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1 1. BEZEICHUG DES ARZEIMITTELS - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135
Meinungen der Bürgerinnen und Bürger in Hamburg und Berlin zu einer Bewerbung um die Austragung der Olympischen Spiele
 Meinungen der Bürgerinnen und Bürger in Hamburg und Berlin zu einer Bewerbung um die Austragung der Olympischen Spiele 4. März 2015 q5337/31319 Le forsa Politik- und Sozialforschung GmbH Büro Berlin Schreiberhauer
Meinungen der Bürgerinnen und Bürger in Hamburg und Berlin zu einer Bewerbung um die Austragung der Olympischen Spiele 4. März 2015 q5337/31319 Le forsa Politik- und Sozialforschung GmbH Büro Berlin Schreiberhauer
Osteoporose. Ein echtes Volksleiden. Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen
 Osteoporose Osteoporose 9 Osteoporose Ein echtes Volksleiden Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen in den entwickelten Ländern zu den häufigsten Erkrankungen
Osteoporose Osteoporose 9 Osteoporose Ein echtes Volksleiden Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen in den entwickelten Ländern zu den häufigsten Erkrankungen
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Technical Note Nr. 101
 Seite 1 von 6 DMS und Schleifringübertrager-Schaltungstechnik Über Schleifringübertrager können DMS-Signale in exzellenter Qualität übertragen werden. Hierbei haben sowohl die physikalischen Eigenschaften
Seite 1 von 6 DMS und Schleifringübertrager-Schaltungstechnik Über Schleifringübertrager können DMS-Signale in exzellenter Qualität übertragen werden. Hierbei haben sowohl die physikalischen Eigenschaften
1.1. Aufschriften auf der Außenseite von ME-Geräten oder ME-Geräte-Teilen
 1. Bezeichnung, Aufschriften und Begleitpapiere 1.1. Aufschriften auf der Außenseite von ME-Geräten oder ME-Geräte-Teilen 1.1.1. Aufschriften auf der Außenseite von ME-Geräten oder ME-Geräte-Teilen, die
1. Bezeichnung, Aufschriften und Begleitpapiere 1.1. Aufschriften auf der Außenseite von ME-Geräten oder ME-Geräte-Teilen 1.1.1. Aufschriften auf der Außenseite von ME-Geräten oder ME-Geräte-Teilen, die
Durchfall in der Pflege. Der kleine Ratgeber von Aplona
 Durchfallerkrankungen Durchfall in der Pflege Der kleine von Aplona Der kleine von Aplona 3 Fotos: Titel, Seite 2, 3 und 4: Fotolia.com Durchfall in der Pflege Akute Durchfallerkrankungen stellen eine
Durchfallerkrankungen Durchfall in der Pflege Der kleine von Aplona Der kleine von Aplona 3 Fotos: Titel, Seite 2, 3 und 4: Fotolia.com Durchfall in der Pflege Akute Durchfallerkrankungen stellen eine
10 Antworten zum Thema Generika
 10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
MS und Impfungen. DAS KLEINE IMPF-1x1. DAS KLEINE IMPF-1x1. Christian Lampl. Abteilung für Allgemeine Neurologie und Schmerzmedizin
 MS und Impfungen Christian Lampl Abteilung für Allgemeine Neurologie und Schmerzmedizin DAS KLEINE IMPF-1x1 Impfungen stellen sehr wirksame und wichtige präventivmedizinische Maßnahmen dar. Das unmittelbare
MS und Impfungen Christian Lampl Abteilung für Allgemeine Neurologie und Schmerzmedizin DAS KLEINE IMPF-1x1 Impfungen stellen sehr wirksame und wichtige präventivmedizinische Maßnahmen dar. Das unmittelbare
Packungsbeilage GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung. Xylometazolinhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
Glaube an die Existenz von Regeln für Vergleiche und Kenntnis der Regeln
 Glaube an die Existenz von Regeln für Vergleiche und Kenntnis der Regeln Regeln ja Regeln nein Kenntnis Regeln ja Kenntnis Regeln nein 0 % 10 % 20 % 30 % 40 % 50 % 60 % 70 % 80 % 90 % Glauben Sie, dass
Glaube an die Existenz von Regeln für Vergleiche und Kenntnis der Regeln Regeln ja Regeln nein Kenntnis Regeln ja Kenntnis Regeln nein 0 % 10 % 20 % 30 % 40 % 50 % 60 % 70 % 80 % 90 % Glauben Sie, dass
Vi-Polysaccharid von Salmonella typhi (Ty2 Stamm)
 Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff 2. Qualitative und quantitative Zusammensetzung
Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff 2. Qualitative und quantitative Zusammensetzung
Gesundheitsvorsorge in der Schule
 Kanton Zürich Bildungsdirektion Volksschulamt Gesundheitsvorsorge in der Schule Elterninformation Liebe Eltern Die Gesundheit Ihres Kindes liegt auch der Schule am Herzen. Gut sehen und hören sind zum
Kanton Zürich Bildungsdirektion Volksschulamt Gesundheitsvorsorge in der Schule Elterninformation Liebe Eltern Die Gesundheit Ihres Kindes liegt auch der Schule am Herzen. Gut sehen und hören sind zum
Ein neues System für die Allokation von Spenderlungen. LAS Information für Patienten in Deutschland
 Ein neues System für die Allokation von Spenderlungen LAS Information für Patienten in Deutschland Ein neues System für die Allokation von Spenderlungen Aufgrund des immensen Mangels an Spenderorganen
Ein neues System für die Allokation von Spenderlungen LAS Information für Patienten in Deutschland Ein neues System für die Allokation von Spenderlungen Aufgrund des immensen Mangels an Spenderorganen
InVo. Information zu Verordnungen in der GKV. Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen. Stand: Februar 2010
 Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
FACHINFORMATION/ ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 FACHIFORMATIO/ ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1. BEZEICHUG DES ARZEIMITTELS - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-n A, C, W-135
FACHIFORMATIO/ ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1. BEZEICHUG DES ARZEIMITTELS - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-n A, C, W-135
Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU
 Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU 2 DIE MEDIZINISCH-PSYCHOLOGISCHE UNTERSUCHUNG (MPU) IST HOCH ANGESEHEN Das Image der Medizinisch-Psychologischen Untersuchung (MPU) ist zwiespältig: Das ist
Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU 2 DIE MEDIZINISCH-PSYCHOLOGISCHE UNTERSUCHUNG (MPU) IST HOCH ANGESEHEN Das Image der Medizinisch-Psychologischen Untersuchung (MPU) ist zwiespältig: Das ist
q Von der STIKO generell empfohlene Impfungen q Impfungen bei erhöhtem individuellen Risiko bezüglich Exposition,
 ifi-card Impfungen Allgemeines zu Impfungen Standardimpfungen Indikationsimpfungen Injektion Dokumentation Schwangerschaft Immunschwäche q Von der STIKO generell empfohlene Impfungen q Impfungen bei erhöhtem
ifi-card Impfungen Allgemeines zu Impfungen Standardimpfungen Indikationsimpfungen Injektion Dokumentation Schwangerschaft Immunschwäche q Von der STIKO generell empfohlene Impfungen q Impfungen bei erhöhtem
Dipl.-Ing. Herbert Schmolke, VdS Schadenverhütung
 1. Problembeschreibung a) Ein Elektromonteur versetzt in einer überwachungsbedürftigen Anlage eine Leuchte von A nach B. b) Ein Elektromonteur verlegt eine zusätzliche Steckdose in einer überwachungsbedürftigen
1. Problembeschreibung a) Ein Elektromonteur versetzt in einer überwachungsbedürftigen Anlage eine Leuchte von A nach B. b) Ein Elektromonteur verlegt eine zusätzliche Steckdose in einer überwachungsbedürftigen
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tebofortan 40 mg - Filmtabletten. Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tebofortan 40 mg - Filmtabletten Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tebofortan 40 mg - Filmtabletten Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
Auswirkung von vor der Impfung vorhandenen Anti-Tetanus-Antikörpern Auswirkung von Nimenrix auf Anti-Tetanus-Antikörperkonzentrationen
 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert,
Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert,
Labortests für Ihre Gesundheit. Vorsorge-Impfungen bei Kindern 29
 Labortests für Ihre Gesundheit Vorsorge-Impfungen bei Kindern 29 01IPF Labortests für Ihre Gesundheit Vorsorge-Impfungen bei Kindern Schutz von Anfang an Kinder: Wenn sie das Licht der Welt erblicken,
Labortests für Ihre Gesundheit Vorsorge-Impfungen bei Kindern 29 01IPF Labortests für Ihre Gesundheit Vorsorge-Impfungen bei Kindern Schutz von Anfang an Kinder: Wenn sie das Licht der Welt erblicken,
Mobile Intranet in Unternehmen
 Mobile Intranet in Unternehmen Ergebnisse einer Umfrage unter Intranet Verantwortlichen aexea GmbH - communication. content. consulting Augustenstraße 15 70178 Stuttgart Tel: 0711 87035490 Mobile Intranet
Mobile Intranet in Unternehmen Ergebnisse einer Umfrage unter Intranet Verantwortlichen aexea GmbH - communication. content. consulting Augustenstraße 15 70178 Stuttgart Tel: 0711 87035490 Mobile Intranet
Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen.
 Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen. Levobunolol ist ein Beta-Blocker, der den Druck im Inneren des Auges reduziert. Levobunolol Augen (Auge) ist für die Behandlung
Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen. Levobunolol ist ein Beta-Blocker, der den Druck im Inneren des Auges reduziert. Levobunolol Augen (Auge) ist für die Behandlung
Erfahrungen mit Hartz IV- Empfängern
 Erfahrungen mit Hartz IV- Empfängern Ausgewählte Ergebnisse einer Befragung von Unternehmen aus den Branchen Gastronomie, Pflege und Handwerk Pressegespräch der Bundesagentur für Arbeit am 12. November
Erfahrungen mit Hartz IV- Empfängern Ausgewählte Ergebnisse einer Befragung von Unternehmen aus den Branchen Gastronomie, Pflege und Handwerk Pressegespräch der Bundesagentur für Arbeit am 12. November
Downloadfehler in DEHSt-VPSMail. Workaround zum Umgang mit einem Downloadfehler
 Downloadfehler in DEHSt-VPSMail Workaround zum Umgang mit einem Downloadfehler Downloadfehler bremen online services GmbH & Co. KG Seite 2 Inhaltsverzeichnis Vorwort...3 1 Fehlermeldung...4 2 Fehlerbeseitigung...5
Downloadfehler in DEHSt-VPSMail Workaround zum Umgang mit einem Downloadfehler Downloadfehler bremen online services GmbH & Co. KG Seite 2 Inhaltsverzeichnis Vorwort...3 1 Fehlermeldung...4 2 Fehlerbeseitigung...5
Hilfedatei der Oden$-Börse Stand Juni 2014
 Hilfedatei der Oden$-Börse Stand Juni 2014 Inhalt 1. Einleitung... 2 2. Die Anmeldung... 2 2.1 Die Erstregistrierung... 3 2.2 Die Mitgliedsnummer anfordern... 4 3. Die Funktionen für Nutzer... 5 3.1 Arbeiten
Hilfedatei der Oden$-Börse Stand Juni 2014 Inhalt 1. Einleitung... 2 2. Die Anmeldung... 2 2.1 Die Erstregistrierung... 3 2.2 Die Mitgliedsnummer anfordern... 4 3. Die Funktionen für Nutzer... 5 3.1 Arbeiten
Wirkstoffe: Trockenextrakt aus Birkenblättern, Trockenextrakt aus Goldrutenkraut
 Gebrauchsinformation: Information für Anwender HEUMANN Blasen- und Nierentee SOLUBITRAT uro Teeaufgusspulver Wirkstoffe: Trockenextrakt aus Birkenblättern, Trockenextrakt aus Goldrutenkraut Lesen Sie die
Gebrauchsinformation: Information für Anwender HEUMANN Blasen- und Nierentee SOLUBITRAT uro Teeaufgusspulver Wirkstoffe: Trockenextrakt aus Birkenblättern, Trockenextrakt aus Goldrutenkraut Lesen Sie die
Nichtmedikamentöse Kopfschmerztherapie bei Kindern und. Folie 1. Psychotherapeuten bei der Kopfschmerztherapie? Folie 2
 Essen, den 10.Dezember 2009, Audi Max UKE Nichtmedikamentöse Kopfschmerztherapie bei Kindern und Jugendlichen Folie 1 Was sind die Aufgaben eines Kinderpsychiaters und Psychotherapeuten bei der Kopfschmerztherapie?
Essen, den 10.Dezember 2009, Audi Max UKE Nichtmedikamentöse Kopfschmerztherapie bei Kindern und Jugendlichen Folie 1 Was sind die Aufgaben eines Kinderpsychiaters und Psychotherapeuten bei der Kopfschmerztherapie?
Feiertage in Marvin hinterlegen
 von 6 Goecom GmbH & Co KG Marvin How to's Feiertage in Marvin hinterlegen Feiertage spielen in Marvin an einer Reihe von Stellen eine nicht unerhebliche Rolle. Daher ist es wichtig, zum Einen zu hinterlegen,
von 6 Goecom GmbH & Co KG Marvin How to's Feiertage in Marvin hinterlegen Feiertage spielen in Marvin an einer Reihe von Stellen eine nicht unerhebliche Rolle. Daher ist es wichtig, zum Einen zu hinterlegen,
FAQ 04/2015. Auswirkung der ISO 14119 auf 3SE53/3SF13 Positionsschalter. https://support.industry.siemens.com/cs/ww/de/view/109475921
 FAQ 04/2015 Auswirkung der ISO 14119 auf 3SE53/3SF13 Positionsschalter mit https://support.industry.siemens.com/cs/ww/de/view/109475921 Dieser Beitrag stammt aus dem Siemens Industry Online Support. Es
FAQ 04/2015 Auswirkung der ISO 14119 auf 3SE53/3SF13 Positionsschalter mit https://support.industry.siemens.com/cs/ww/de/view/109475921 Dieser Beitrag stammt aus dem Siemens Industry Online Support. Es
Atronase 0,3 mg/ml Nasenspray, Lösung (Ipratropiumbromid)
 GEBRAUCHSINFORMATION ATRONASE 0,3 MG/ML NASENSPRAY, LÖSUNG Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
GEBRAUCHSINFORMATION ATRONASE 0,3 MG/ML NASENSPRAY, LÖSUNG Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
AGROPLUS Buchhaltung. Daten-Server und Sicherheitskopie. Version vom 21.10.2013b
 AGROPLUS Buchhaltung Daten-Server und Sicherheitskopie Version vom 21.10.2013b 3a) Der Daten-Server Modus und der Tresor Der Daten-Server ist eine Betriebsart welche dem Nutzer eine grosse Flexibilität
AGROPLUS Buchhaltung Daten-Server und Sicherheitskopie Version vom 21.10.2013b 3a) Der Daten-Server Modus und der Tresor Der Daten-Server ist eine Betriebsart welche dem Nutzer eine grosse Flexibilität
Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6
 Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6 Trotz sorgfältiger Erstellung des Buchs Benkert, Pocket Guide, Psychopharmaka
Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6 Trotz sorgfältiger Erstellung des Buchs Benkert, Pocket Guide, Psychopharmaka
Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit
 Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit politische Lage verlassen sich auf Familie persönliche, finanzielle Lage meinen, sich Vorsorge leisten zu können meinen, sie seien zu alt nicht mit
Gründe für fehlende Vorsorgemaßnahmen gegen Krankheit politische Lage verlassen sich auf Familie persönliche, finanzielle Lage meinen, sich Vorsorge leisten zu können meinen, sie seien zu alt nicht mit
LEGIONELLEN in Trinkwasser-Installationen
 Wärmetechnik... weil Energie wertvoll ist! LEGIONELLEN in Trinkwasser-Installationen Verbraucherinformation Was sind Legionellen? Legionellen sind eine Gattung stäbchenförmiger Bakterien aus der Familie
Wärmetechnik... weil Energie wertvoll ist! LEGIONELLEN in Trinkwasser-Installationen Verbraucherinformation Was sind Legionellen? Legionellen sind eine Gattung stäbchenförmiger Bakterien aus der Familie
Gebrauchsinformation: Information für Patienten. Desloratadin Genericon 5 mg Filmtabletten. Wirkstoff: Desloratadin
 Gebrauchsinformation: Information für Patienten Desloratadin Genericon 5 mg Filmtabletten Wirkstoff: Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten Desloratadin Genericon 5 mg Filmtabletten Wirkstoff: Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Elternzeit Was ist das?
 Elternzeit Was ist das? Wenn Eltern sich nach der Geburt ihres Kindes ausschließlich um ihr Kind kümmern möchten, können sie bei ihrem Arbeitgeber Elternzeit beantragen. Während der Elternzeit ruht das
Elternzeit Was ist das? Wenn Eltern sich nach der Geburt ihres Kindes ausschließlich um ihr Kind kümmern möchten, können sie bei ihrem Arbeitgeber Elternzeit beantragen. Während der Elternzeit ruht das
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Vitagutt Vitamin E 670 mg, Weichkapsel Zur Anwendung bei Erwachsenen Wirkstoff: 1000 mg all-rac-alpha-tocopherolacetat (entsprechend 670 mg RRR-alpha- Tocopherol-Äquivalente).
Gebrauchsinformation: Information für Anwender Vitagutt Vitamin E 670 mg, Weichkapsel Zur Anwendung bei Erwachsenen Wirkstoff: 1000 mg all-rac-alpha-tocopherolacetat (entsprechend 670 mg RRR-alpha- Tocopherol-Äquivalente).
TOP 3: Loperamid (flüssige Darreichungsformen)
 TOP 3: Loperamid (flüssige Darreichungsformen) Antrag auf Ausweitung der Ausnahme von der Verschreibungspflicht auch für flüssige Darreichungsformen 1 Historie und aktuell: Seit 1993 D. h. folgende Darreichungsformen
TOP 3: Loperamid (flüssige Darreichungsformen) Antrag auf Ausweitung der Ausnahme von der Verschreibungspflicht auch für flüssige Darreichungsformen 1 Historie und aktuell: Seit 1993 D. h. folgende Darreichungsformen
Sidroga Blasentee akut Wirkstoffe: Bärentraubenblätter, Birkenblätter, Goldrutenkraut, Orthosiphonblätter
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Sidroga Blasentee akut Wirkstoffe: Bärentraubenblätter, Birkenblätter, Goldrutenkraut, Orthosiphonblätter Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Sidroga Blasentee akut Wirkstoffe: Bärentraubenblätter, Birkenblätter, Goldrutenkraut, Orthosiphonblätter Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Magnevist 2 mmol/l Injektionslösung. Gadopentetsäure, Dimeglumin
 1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Magnevist 2 mmol/l Injektionslösung Gadopentetsäure, Dimeglumin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei
1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Magnevist 2 mmol/l Injektionslösung Gadopentetsäure, Dimeglumin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. ENCEPUR Erwachsene Suspension zur Injektion in einer Fertigspritze FSME-Adsorbat-Impfstoff
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ENCEPUR Erwachsene Suspension zur Injektion in einer Fertigspritze FSME-Adsorbat-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ENCEPUR Erwachsene Suspension zur Injektion in einer Fertigspritze FSME-Adsorbat-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
FRAGEBOGEN FÜR KINDER UND JUGENDLICHE
 Meinung in Bezug auf die Anwendung von Medikamenten Warum fragen wir? Der Pädiatrische Ausschuss (Paediatric Committee (PDCO)) arbeitet zusammen mit der Europäischen Arzneimittelagentur. Dieser Ausschuss
Meinung in Bezug auf die Anwendung von Medikamenten Warum fragen wir? Der Pädiatrische Ausschuss (Paediatric Committee (PDCO)) arbeitet zusammen mit der Europäischen Arzneimittelagentur. Dieser Ausschuss
Pädagogik. Melanie Schewtschenko. Eingewöhnung und Übergang in die Kinderkrippe. Warum ist die Beteiligung der Eltern so wichtig?
 Pädagogik Melanie Schewtschenko Eingewöhnung und Übergang in die Kinderkrippe Warum ist die Beteiligung der Eltern so wichtig? Studienarbeit Inhaltsverzeichnis 1. Einleitung.2 2. Warum ist Eingewöhnung
Pädagogik Melanie Schewtschenko Eingewöhnung und Übergang in die Kinderkrippe Warum ist die Beteiligung der Eltern so wichtig? Studienarbeit Inhaltsverzeichnis 1. Einleitung.2 2. Warum ist Eingewöhnung
Subkutane spezifische Immuntherapie. Eine Information für Patienten
 Subkutane spezifische Immuntherapie Eine Information für Patienten Spezifische Immuntherapie Die Allergietestung durch Ihren Arzt hat ergeben, dass Sie (oder Ihr Kind) an einer Allergie leiden. Allergische
Subkutane spezifische Immuntherapie Eine Information für Patienten Spezifische Immuntherapie Die Allergietestung durch Ihren Arzt hat ergeben, dass Sie (oder Ihr Kind) an einer Allergie leiden. Allergische
Diabetes mellitus : Folgeschäden
 Diabetes mellitus : Folgeschäden Warum ist der Diabetes mellitus eine wichtige Erkrankung? a. Akute Probleme: Hypoglykämie Hyperglykämie Ketoazidose b. Chronische Probleme: Folgeschäden: Typische Schäden:
Diabetes mellitus : Folgeschäden Warum ist der Diabetes mellitus eine wichtige Erkrankung? a. Akute Probleme: Hypoglykämie Hyperglykämie Ketoazidose b. Chronische Probleme: Folgeschäden: Typische Schäden:
