InVo. Information zu Verordnungen in der GKV. Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen. Stand: Februar 2010
|
|
|
- Hannah Steinmann
- vor 8 Jahren
- Abrufe
Transkript
1 Nr InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B. Dermatika oder individuelle Allergietests) selbst herstellen und persönlich anwenden soweit dies unter Ihrer unmittelbaren fachlichen Verantwortung erfolgte ohne dass diese Arzneimittelherstellung von den Bestimmungen des Arzneimittelgesetzes (AMG) erfasst wurde. Durch das Inkrafttreten der 15. AMG-Novelle am hat sich die Rechtsgrundlage für von Ärzten hergestellte Arzneimittel im Arzneimittelgesetz (AMG) maßgeblich geändert. Das AMG definiert das Herstellen als das Gewinnen, das Anfertigen, das Zubereiten, das Be- oder Verarbeiten, das Umfüllen einschließlich Abfüllen, das Abpacken, das Kennzeichnen und die Freigabe. Sie können so in der täglichen Praxis zum Hersteller von Arzneimitteln werden, die gegenüber den zuständigen Behörden, in NRW den Bezirksregierungen, anzeigepflichtig sind. Die Landesbehörden haben in den verschiedenen Bundesländern die Ärzteschaft sehr verspätet oder noch gar nicht über den neuen Sachverhalt und die Anzeigepflicht nach 67 AMG informiert. Eine im Gesetz vorgegebene Übergangsfrist zur Anzeige bei den zuständigen Regierungen für Personen, die bereits am Arzneimittel im Sinne des Gesetzes hergestellt haben, ist mit dem verstrichen. Dies zieht keine Maßnahmen nach sich, doch sollten Sie die erforderlichen Anzeigen bei den zuständigen Bezirksregierungen möglichst bald machen. Die Anzeige kann formlos erfolgen. Bitte prüfen Sie, ob Sie in Ihrer ärztlichen Tätigkeit von den Neuregelungen betroffen sind. Sie finden dazu im Folgenden weitere Informationen zum Sachverhalt und zur Meldung bei den zuständigen Bezirksregierungen. Keine Anzeigepflicht bei alleiniger Rekonstitution eines Arzneimittels Anzeigepflichtige Herstellung von Arzneimitteln Erlaubnisfreie und erlaubnispflichtige Herstellung Hinweise zur Anzeige bei den zuständigen Bezirksregierungen Geschäftsbereich Verordnungsmanagement Telefon: verordnungsmanagement@kvwl.de
2 Keine Anzeigepflicht bei alleiniger Rekonstitution eines Arzneimittels Durch die neue Rechtslage gelten für die Herstellung von Arzneimitteln durch Ärzte oder andere Personen, die zur Ausübung der Heilkunde befugt sind, nunmehr auch die Vorgaben des AMG zur Überwachung bzw. Anzeigepflicht. Das AMG definiert Herstellen als das Gewinnen, das Anfertigen, das Zubereiten, das Be- oder Verarbeiten, das Umfüllen einschließlich Abfüllen, das Abpacken, das Kennzeichnen und die Freigabe. Für die häufig vorkommende Rekonstitution wurden Sonderregelungen getroffen. Rekonstitution ist dabei die Überführung eines Fertigarzneimittels in seiner anwendungsfähigen Form unmittelbar vor seiner Anwendung gemäß den Angaben der Packungsbeilage (oder im Rahmen der klinischen Prüfung nach Maßgabe des Prüfplans). Wenn Sie in Ihrer Praxis Arzneimittel nur gebrauchsfertig machen, ist somit keine Anzeige bei der Bezirksregierung notwendig. Dies gilt allerdings nicht für Arzneimittelanwendungen im Rahmen von klinischen Prüfungen.
3 Anzeigepflichtige Herstellung von Arzneimitteln Verändern Sie die Anfertigung oder Zubereitung, gehen Sie also über die reine Rekonstitution eines Arzneimittels gemäß Packungsbeilage hinaus, ist dies nach 4 Nr. 14 AMG die Herstellung eines neuen Arzneimittels. Hier noch einige Beispiele für Arbeitsschritte, die der Herstellung eines Arzneimittels entsprechen: Mischung mehrerer Arzneimittel zur Anwendung, z. B. zur Injektion oder Infusion Herstellung von Testlösungen für die Allergie-Testung ( Pricktest) Lösen einer Trockensubstanz in einem nicht in der Fachinformation/Packungsbeilage genannten Lösungsmittel Verdünnung eines Konzentrates mit einem nicht in der Fachinformation/Packungsbeilage genannten Lösungsmittel Gewebe oder Gewebezubereitungen Blut und Blutprodukte sowie Anreicherung von Eigenblut Eine Anzeige sollte auch dann gemacht werden, wenn Unklarheiten oder Zweifel über die Anzeigepflicht bestehen, damit die zuständige Bezirksregierung den Sachverhalt prüfen kann. Hinweise zur Anzeige bei den zuständigen Bezirksregierungen Über die Anzeigepflicht hinaus kann auch das Vorliegen einer arzneimittelrechtlichen Erlaubnis Voraussetzung für die Herstellung sein. Das neue AMG unterscheidet dabei je nach Vorliegen folgender Voraussetzungen in: Erlaubnisfreie und erlaubnispflichtige Herstellung
4 Erlaubnisfreie und erlaubnispflichtige Herstellung Erlaubnisfreie Herstellung gem. 13 Abs. 2b AMG Eine Person, die Arzt ist oder sonst zur Ausübung der Heilkunde beim Menschen befugt ist, bedarf keiner Herstellungserlaubnis nach 13 Abs. 1 AMG, soweit die Arzneimittel unter ihrer unmittelbaren fachlichen Verantwortung zum Zweck der persönlichen Anwendung bei einem bestimmten Patienten hergestellt werden und es sich nicht um bestimmte Arzneimittel ( s. erlaubnispflichtige Herstellung) handelt. In diesem Fall ist eine Anzeige nach 67 AMG bis spätestens erforderlich. Dabei ist auch die Bezeichnung und Zusammensetzung der Arzneimittel anzugeben. Bei der Herstellung sind die anerkannten pharmazeutischen Regeln zu beachten (vgl. 55 Abs. 8 AMG). Erlaubnisfreie Herstellung von zur Verwendung bei Menschen bestimmten menschlichen Geweben und Gewebezubereitungen gem. 20d AMG Einer Erlaubnis nach 20b Abs. 1 und 20c Abs. 1 AMG bedarf eine Person nicht, die Arzt ist oder sonst zur Ausübung der Heilkunde bei Menschen befugt ist und die dort genannten Tätigkeiten mit Ausnahme des Inverkehrbringens ausübt, um das Gewebe oder die Gewebezubereitung persönlich bei ihren Patienten anzuwenden. Dies gilt nicht für Arzneimittel, die zur klinischen Prüfung bestimmt sind. In diesem Fall ist ebenfalls eine Anzeige nach 67 AMG bis spätestens erforderlich. Bezeichnung und Zusammensetzung der Gewebe oder Gewebezubereitungen sollten im Zusammenhang mit der Anzeige angegeben und das Herstellungsverfahren kurz beschrieben werden. Erlaubnispflichtige Herstellung/Tätigkeiten Die Herstellung bestimmter Arzneimittel erfordert in den im Folgenden genannten Fällen auch dann eine Herstellungserlaubnis nach 13 AMG, wenn die Herstellung unter der unmittelbaren fachlichen Verantwortung des Arztes oder der zur Ausübung der Heilkunde berechtigten Person zum Zwecke der persönlichen Anwendung bei einem bestimmten Patienten erfolgt. Hierzu gehört die Herstellung von: Arzneimitteln für neuartige Therapien (Gentherapeutika, somatische Zelltherapeutika, biotechnologisch bearbeitete Gewebeprodukte) und xenogene Arzneimittel, soweit diese genetisch modifizierte oder durch andere Verfahren in ihren biologischen Eigenschaften veränderte lebende Körperzellen sind oder enthalten, Arzneimitteln, die zur klinischen Prüfung bestimmt sind, soweit es sich nicht nur um eine Rekonstitution handelt. Sofern die Voraussetzungen zur erlaubnisfreien Herstellung gem. 20d AMG nicht vorliegen, erfordert die Ausführung folgender Tätigkeiten eine Herstellungserlaubnis nach 20b und/oder 20c AMG:
5 Die Gewinnung von Gewebe oder die für die Gewinnung erforderlichen Laboruntersuchungen ( vgl. 20b AMG) Die Be- und Verarbeitung, Konservierung, Prüfung, Lagerung oder das Inverkehrbringen von Geweben oder Gewebezubereitungen (vgl. 20c AMG). Kassenärztliche Vereinigung In diesen Fällen ist ergänzend zur o.g. Anzeige nach 67 AMG ein Erlaubnisantrag zu stellen. Für Personen, die bereits am eine dieser Tätigkeiten nach ehemals 4a Satz 1 Nr. 3 AMG ausgeübt haben, besteht eine Übergangsfrist zur Beantragung der Erlaubnis bis zum
6 Hinweise zur Anzeige bei den zuständigen Bezirksregierungen Im Falle einer erlaubnisfreien Herstellung von Arzneimitteln können Sie dies der zuständigen Bezirksregierung formlos anzeigen. Anzugeben sind auf jeden Fall: Wer stellt her? Ihr Name als Hersteller Betriebsstätte Ihre Praxis mit Anschrift usw. Was hergestellt wird: genaue Angabe oder Beschreibung des Herstellungsprozesses Nur die reine Rekonstitution eines Arzneimittels ist von der Anzeigepflicht nach 4 Nr. 14 AMG ausgenommen. Eine Anzeige sollte auch dann gemacht werden, wenn Unklarheiten oder Zweifel über die Anzeigepflicht bestehen, damit die zuständige Bezirksregierung den Sachverhalt prüfen kann. Unter dem folgenden Link zu Arzneimittelüberwachung und -untersuchung NRW können Sie die notwendigen Informationen, die wichtigsten Ansprechpartner, Anschriften, Telefon- und Faxnummern der zuständigen Landes- und Bezirksregierungen finden. Sie können Ihre Anzeigen auch über die angegebenen Faxnummern vornehmen:
AMK-AMG-Herstell-Anz Seite 1 von 6
 AMK-AMG-Herstell-Anz-2010-01-25 Seite 1 von 6 Information der Arzneimittelkommission der deutschen Heilpraktiker bezüglich der arzneimittelrechtlichen Änderungen zur Anzeigepflicht der Herstellung von
AMK-AMG-Herstell-Anz-2010-01-25 Seite 1 von 6 Information der Arzneimittelkommission der deutschen Heilpraktiker bezüglich der arzneimittelrechtlichen Änderungen zur Anzeigepflicht der Herstellung von
AMK-AMG-Herstell-Anz-2010-01-25 Seite 1 von 6
 AMK-AMG-Herstell-Anz-2010-01-25 Seite 1 von 6 Information der Arzneimittelkommission der deutschen Heilpraktiker bezüglich der arzneimittelrechtlichen Änderungen zur Anzeigepflicht der Herstellung von
AMK-AMG-Herstell-Anz-2010-01-25 Seite 1 von 6 Information der Arzneimittelkommission der deutschen Heilpraktiker bezüglich der arzneimittelrechtlichen Änderungen zur Anzeigepflicht der Herstellung von
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren
 Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV)
 05.07.2005 Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 13. Februar 2004 (BGBl. I S. 216)
05.07.2005 Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 13. Februar 2004 (BGBl. I S. 216)
Langfristige Genehmigungen
 MB 14 b AV 04/13 Merkblatt zum Thema Langfristige Genehmigungen Einleitung Seit der neuen Heilmittel-Richtlinie (HMR) vom 01.07.2011 können Menschen mit schweren und langfristigen funktionellen/strukturellen
MB 14 b AV 04/13 Merkblatt zum Thema Langfristige Genehmigungen Einleitung Seit der neuen Heilmittel-Richtlinie (HMR) vom 01.07.2011 können Menschen mit schweren und langfristigen funktionellen/strukturellen
Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV)
 Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) Vom 20. Dezember 2001, BGBl. I S. 3854 geändert am 4. Dezember 2002, BGBl I S. 4456 zuletzt geändert am 13. Februar 2004, BGBl I S. 216
Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) Vom 20. Dezember 2001, BGBl. I S. 3854 geändert am 4. Dezember 2002, BGBl I S. 4456 zuletzt geändert am 13. Februar 2004, BGBl I S. 216
GPA-Mitteilung Bau 5/2002
 GPA-Mitteilung Bau 5/2002 Az. 600.513 01.07.2002 Verjährung der Vergütungs-/Honoraransprüche bei Bau-, Architektenund Ingenieurverträgen (Werkverträgen) Durch Art. 1 des Gesetzes zur Modernisierung des
GPA-Mitteilung Bau 5/2002 Az. 600.513 01.07.2002 Verjährung der Vergütungs-/Honoraransprüche bei Bau-, Architektenund Ingenieurverträgen (Werkverträgen) Durch Art. 1 des Gesetzes zur Modernisierung des
Was ist das Budget für Arbeit?
 1 Was ist das Budget für Arbeit? Das Budget für Arbeit ist ein Persönliches Geld für Arbeit wenn Sie arbeiten möchten aber nicht mehr in einer Werkstatt. Das gibt es bisher nur in Nieder-Sachsen. Und in
1 Was ist das Budget für Arbeit? Das Budget für Arbeit ist ein Persönliches Geld für Arbeit wenn Sie arbeiten möchten aber nicht mehr in einer Werkstatt. Das gibt es bisher nur in Nieder-Sachsen. Und in
Installation OMNIKEY 3121 USB
 Installation OMNIKEY 3121 USB Vorbereitungen Installation PC/SC Treiber CT-API Treiber Einstellungen in Starke Praxis Testen des Kartenlesegeräts Vorbereitungen Bevor Sie Änderungen am System vornehmen,
Installation OMNIKEY 3121 USB Vorbereitungen Installation PC/SC Treiber CT-API Treiber Einstellungen in Starke Praxis Testen des Kartenlesegeräts Vorbereitungen Bevor Sie Änderungen am System vornehmen,
10 IDG (Gesetz über die Information und den Datenschutz, LS 170.4) 24 IDV (Verordnung über die Information und den Datenschutz, LS 170.
 M erkblatt Vorabkontrolle 1 Einleitung Öffentliche Organe des Kantons Zürich müssen Projekte und Vorhaben dem Datenschutzbeauftragten zur Prüfung unterbreiten, wenn diese Datenbearbeitungen beinhalten,
M erkblatt Vorabkontrolle 1 Einleitung Öffentliche Organe des Kantons Zürich müssen Projekte und Vorhaben dem Datenschutzbeauftragten zur Prüfung unterbreiten, wenn diese Datenbearbeitungen beinhalten,
Persönliche Zukunftsplanung mit Menschen, denen nicht zugetraut wird, dass sie für sich selbst sprechen können Von Susanne Göbel und Josef Ströbl
 Persönliche Zukunftsplanung mit Menschen, denen nicht zugetraut Von Susanne Göbel und Josef Ströbl Die Ideen der Persönlichen Zukunftsplanung stammen aus Nordamerika. Dort werden Zukunftsplanungen schon
Persönliche Zukunftsplanung mit Menschen, denen nicht zugetraut Von Susanne Göbel und Josef Ströbl Die Ideen der Persönlichen Zukunftsplanung stammen aus Nordamerika. Dort werden Zukunftsplanungen schon
AGROPLUS Buchhaltung. Daten-Server und Sicherheitskopie. Version vom 21.10.2013b
 AGROPLUS Buchhaltung Daten-Server und Sicherheitskopie Version vom 21.10.2013b 3a) Der Daten-Server Modus und der Tresor Der Daten-Server ist eine Betriebsart welche dem Nutzer eine grosse Flexibilität
AGROPLUS Buchhaltung Daten-Server und Sicherheitskopie Version vom 21.10.2013b 3a) Der Daten-Server Modus und der Tresor Der Daten-Server ist eine Betriebsart welche dem Nutzer eine grosse Flexibilität
Welche Bereiche gibt es auf der Internetseite vom Bundes-Aufsichtsamt für Flugsicherung?
 Welche Bereiche gibt es auf der Internetseite vom Bundes-Aufsichtsamt für Flugsicherung? BAF ist die Abkürzung von Bundes-Aufsichtsamt für Flugsicherung. Auf der Internetseite gibt es 4 Haupt-Bereiche:
Welche Bereiche gibt es auf der Internetseite vom Bundes-Aufsichtsamt für Flugsicherung? BAF ist die Abkürzung von Bundes-Aufsichtsamt für Flugsicherung. Auf der Internetseite gibt es 4 Haupt-Bereiche:
Befragung zum Migrationshintergrund
 Befragung zum Migrationshintergrund Ziel der Befragung ist es, Statistiken zum Arbeitsmarkt und zur Grundsicherung für Personen mit und ohne Migrationshintergrund darzustellen. Hierfür bitten wir um Ihre
Befragung zum Migrationshintergrund Ziel der Befragung ist es, Statistiken zum Arbeitsmarkt und zur Grundsicherung für Personen mit und ohne Migrationshintergrund darzustellen. Hierfür bitten wir um Ihre
Sichere E-Mail Anleitung Zertifikate / Schlüssel für Kunden der Sparkasse Germersheim-Kandel. Sichere E-Mail. der
 Sichere E-Mail der Nutzung von Zertifikaten / Schlüsseln zur sicheren Kommunikation per E-Mail mit der Sparkasse Germersheim-Kandel Inhalt: 1. Voraussetzungen... 2 2. Registrierungsprozess... 2 3. Empfang
Sichere E-Mail der Nutzung von Zertifikaten / Schlüsseln zur sicheren Kommunikation per E-Mail mit der Sparkasse Germersheim-Kandel Inhalt: 1. Voraussetzungen... 2 2. Registrierungsprozess... 2 3. Empfang
Die Post hat eine Umfrage gemacht
 Die Post hat eine Umfrage gemacht Bei der Umfrage ging es um das Thema: Inklusion Die Post hat Menschen mit Behinderung und Menschen ohne Behinderung gefragt: Wie zufrieden sie in dieser Gesellschaft sind.
Die Post hat eine Umfrage gemacht Bei der Umfrage ging es um das Thema: Inklusion Die Post hat Menschen mit Behinderung und Menschen ohne Behinderung gefragt: Wie zufrieden sie in dieser Gesellschaft sind.
BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH. Jahrgang 2004 Ausgegeben am 28. Jänner 2004 Teil II
 1 von 5 BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH Jahrgang 2004 Ausgegeben am 28. Jänner 2004 Teil II 57. Verordnung: Konformitätsbewertung von Medizinprodukten [CELEX-Nr.: 32000L0070, 32001L0104,
1 von 5 BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH Jahrgang 2004 Ausgegeben am 28. Jänner 2004 Teil II 57. Verordnung: Konformitätsbewertung von Medizinprodukten [CELEX-Nr.: 32000L0070, 32001L0104,
Was meinen die Leute eigentlich mit: Grexit?
 Was meinen die Leute eigentlich mit: Grexit? Grexit sind eigentlich 2 Wörter. 1. Griechenland 2. Exit Exit ist ein englisches Wort. Es bedeutet: Ausgang. Aber was haben diese 2 Sachen mit-einander zu tun?
Was meinen die Leute eigentlich mit: Grexit? Grexit sind eigentlich 2 Wörter. 1. Griechenland 2. Exit Exit ist ein englisches Wort. Es bedeutet: Ausgang. Aber was haben diese 2 Sachen mit-einander zu tun?
Drei Fragen zum Datenschutz im. Nico Reiners
 Drei Fragen zum Datenschutz im Geoinformationswesen Nico Reiners 1. Frage Welche Geoinformationen sind personenbezogen? Personenbezug? Personenbezogene Daten sind Einzelangaben über persönliche oder sachliche
Drei Fragen zum Datenschutz im Geoinformationswesen Nico Reiners 1. Frage Welche Geoinformationen sind personenbezogen? Personenbezug? Personenbezogene Daten sind Einzelangaben über persönliche oder sachliche
Transaktionsempfehlungen im ebase Online nutzen
 Transaktionsempfehlungen im ebase Online nutzen Anleitung ebase Inhalt 1. Einführung und Voraussetzungen 2. Transaktionsempfehlung für einen Kunden erstellen 3. Möglichkeiten des Kunden 4. Verwaltung von
Transaktionsempfehlungen im ebase Online nutzen Anleitung ebase Inhalt 1. Einführung und Voraussetzungen 2. Transaktionsempfehlung für einen Kunden erstellen 3. Möglichkeiten des Kunden 4. Verwaltung von
WinVetpro im Betriebsmodus Laptop
 WinVetpro im Betriebsmodus Laptop Um Unterwegs Daten auf einem mobilen Gerät mit WinVetpro zu erfassen, ohne den Betrieb in der Praxis während dieser Zeit zu unterbrechen und ohne eine ständige Online
WinVetpro im Betriebsmodus Laptop Um Unterwegs Daten auf einem mobilen Gerät mit WinVetpro zu erfassen, ohne den Betrieb in der Praxis während dieser Zeit zu unterbrechen und ohne eine ständige Online
Abschnitt 1 Anwendungsbereich und Allgemeine Anforderungen an die Konformitätsbewertung 1 Anwendungsbereich
 13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
Geld Verdienen im Internet leicht gemacht
 Geld Verdienen im Internet leicht gemacht Hallo, Sie haben sich dieses E-book wahrscheinlich herunter geladen, weil Sie gerne lernen würden wie sie im Internet Geld verdienen können, oder? Denn genau das
Geld Verdienen im Internet leicht gemacht Hallo, Sie haben sich dieses E-book wahrscheinlich herunter geladen, weil Sie gerne lernen würden wie sie im Internet Geld verdienen können, oder? Denn genau das
Wir machen neue Politik für Baden-Württemberg
 Wir machen neue Politik für Baden-Württemberg Am 27. März 2011 haben die Menschen in Baden-Württemberg gewählt. Sie wollten eine andere Politik als vorher. Die Menschen haben die GRÜNEN und die SPD in
Wir machen neue Politik für Baden-Württemberg Am 27. März 2011 haben die Menschen in Baden-Württemberg gewählt. Sie wollten eine andere Politik als vorher. Die Menschen haben die GRÜNEN und die SPD in
Serienbrieferstellung in Word mit Kunden-Datenimport aus Excel
 Sehr vielen Mitarbeitern fällt es schwer, Serienbriefe an Kunden zu verschicken, wenn sie die Serienbrieffunktion von Word nicht beherrschen. Wenn die Kunden mit Excel verwaltet werden, genügen nur ein
Sehr vielen Mitarbeitern fällt es schwer, Serienbriefe an Kunden zu verschicken, wenn sie die Serienbrieffunktion von Word nicht beherrschen. Wenn die Kunden mit Excel verwaltet werden, genügen nur ein
Qualität und Verlässlichkeit Das verstehen die Deutschen unter Geschäftsmoral!
 Beitrag: 1:43 Minuten Anmoderationsvorschlag: Unseriöse Internetanbieter, falsch deklarierte Lebensmittel oder die jüngsten ADAC-Skandale. Solche Fälle mit einer doch eher fragwürdigen Geschäftsmoral gibt
Beitrag: 1:43 Minuten Anmoderationsvorschlag: Unseriöse Internetanbieter, falsch deklarierte Lebensmittel oder die jüngsten ADAC-Skandale. Solche Fälle mit einer doch eher fragwürdigen Geschäftsmoral gibt
Zwischenablage (Bilder, Texte,...)
 Zwischenablage was ist das? Informationen über. die Bedeutung der Windows-Zwischenablage Kopieren und Einfügen mit der Zwischenablage Vermeiden von Fehlern beim Arbeiten mit der Zwischenablage Bei diesen
Zwischenablage was ist das? Informationen über. die Bedeutung der Windows-Zwischenablage Kopieren und Einfügen mit der Zwischenablage Vermeiden von Fehlern beim Arbeiten mit der Zwischenablage Bei diesen
Dann zahlt die Regierung einen Teil der Kosten oder alle Kosten für den Dolmetscher.
 Erläuterung der Förder-Richtlinie zur Unterstützung der Teilhabe hör- oder sprachbehinderter Eltern und Sorge-Berechtigter an schulischen Veranstaltungen in Leichter Sprache In Rheinland-Pfalz gibt es
Erläuterung der Förder-Richtlinie zur Unterstützung der Teilhabe hör- oder sprachbehinderter Eltern und Sorge-Berechtigter an schulischen Veranstaltungen in Leichter Sprache In Rheinland-Pfalz gibt es
M e r k b l a t t. Neues Verbrauchervertragsrecht 2014: Beispiele für Widerrufsbelehrungen
 Stand: Januar 2016 M e r k b l a t t Neues Verbrauchervertragsrecht 2014: Beispiele für Widerrufsbelehrungen Sie haben Interesse an aktuellen Meldungen aus dem Arbeits-, Gesellschafts-, Wettbewerbsund
Stand: Januar 2016 M e r k b l a t t Neues Verbrauchervertragsrecht 2014: Beispiele für Widerrufsbelehrungen Sie haben Interesse an aktuellen Meldungen aus dem Arbeits-, Gesellschafts-, Wettbewerbsund
Säuglingsanfangsnahrung und Folgenahrung Was ändert sich? Was bleibt?
 Säuglingsanfangsnahrung und Folgenahrung Was ändert sich? Was bleibt? Begleitinformationen: Handout für das Verkaufspersonal im Handel Bei Rückfragen sprechen Sie uns bitte gerne an: DIÄTVERBAND e. V.
Säuglingsanfangsnahrung und Folgenahrung Was ändert sich? Was bleibt? Begleitinformationen: Handout für das Verkaufspersonal im Handel Bei Rückfragen sprechen Sie uns bitte gerne an: DIÄTVERBAND e. V.
Handbuch ECDL 2003 Modul 2: Computermanagement und Dateiverwaltung Der Task-Manager
 Handbuch ECDL 2003 Modul 2: Computermanagement und Dateiverwaltung Der Task-Manager Dateiname: ecdl2_03_05_documentation Speicherdatum: 22.11.2004 ECDL 2003 Modul 2 Computermanagement und Dateiverwaltung
Handbuch ECDL 2003 Modul 2: Computermanagement und Dateiverwaltung Der Task-Manager Dateiname: ecdl2_03_05_documentation Speicherdatum: 22.11.2004 ECDL 2003 Modul 2 Computermanagement und Dateiverwaltung
Vorab per E-Mail. Oberste Finanzbehörden der Länder
 Postanschrift Berlin: Bundesministeriu m der Finanzen, 11016 Berlin Christoph Weiser Unterabteilungsleiter IV C POSTANSCHRIFT Bundesministerium der Finanzen, 11016 Berlin Vorab per E-Mail Oberste Finanzbehörden
Postanschrift Berlin: Bundesministeriu m der Finanzen, 11016 Berlin Christoph Weiser Unterabteilungsleiter IV C POSTANSCHRIFT Bundesministerium der Finanzen, 11016 Berlin Vorab per E-Mail Oberste Finanzbehörden
6 Schulungsmodul: Probenahme im Betrieb
 6 Schulungsmodul: Probenahme im Betrieb WIEDNER Wie schon im Kapitel VI erwähnt, ist die Probenahme in Betrieben, die Produkte nach dem Lebensmittel- und Futtermittelgesetzbuch herstellen oder in den Verkehr
6 Schulungsmodul: Probenahme im Betrieb WIEDNER Wie schon im Kapitel VI erwähnt, ist die Probenahme in Betrieben, die Produkte nach dem Lebensmittel- und Futtermittelgesetzbuch herstellen oder in den Verkehr
1. Adressen für den Serienversand (Briefe Katalogdruck Werbung/Anfrage ) auswählen. Die Auswahl kann gespeichert werden.
 Der Serienversand Was kann man mit der Maske Serienversand machen? 1. Adressen für den Serienversand (Briefe Katalogdruck Werbung/Anfrage ) auswählen. Die Auswahl kann gespeichert werden. 2. Adressen auswählen,
Der Serienversand Was kann man mit der Maske Serienversand machen? 1. Adressen für den Serienversand (Briefe Katalogdruck Werbung/Anfrage ) auswählen. Die Auswahl kann gespeichert werden. 2. Adressen auswählen,
Ihr Zeichen, Ihre Nachricht vom Unser Zeichen (Bei Antwort angeben) Durchwahl (0511) 120- Hannover NDS EU-DLR 20.09.2012
 Landesbetrieb für Statistik und Kommunikationstechnologie Niedersachsen LSKN Postfach 91 04 55 30424 Hannover Bearbeitet von: VPS-Team E-Mail: VPS-Admin(at)lskn.niedersachsen.de Ihr Zeichen, Ihre Nachricht
Landesbetrieb für Statistik und Kommunikationstechnologie Niedersachsen LSKN Postfach 91 04 55 30424 Hannover Bearbeitet von: VPS-Team E-Mail: VPS-Admin(at)lskn.niedersachsen.de Ihr Zeichen, Ihre Nachricht
Eingangsseite Umwelt-online
 Mit dem Erwerb einer Lizenz haben Sie die Möglichkeit, sich ein auf Ihre Bedürfnisse abgestimmtes Kataster zu erstellen. Die Funktionen dieses Rechtskataster wird nachstehend erläutert. Eingangsseite Umwelt-online
Mit dem Erwerb einer Lizenz haben Sie die Möglichkeit, sich ein auf Ihre Bedürfnisse abgestimmtes Kataster zu erstellen. Die Funktionen dieses Rechtskataster wird nachstehend erläutert. Eingangsseite Umwelt-online
Umzug der abfallwirtschaftlichen Nummern /Kündigung
 Umzug der abfallwirtschaftlichen Nummern /Kündigung Um sich bei ebegleitschein abzumelden/ zu kündigen sind folgende Schritte notwendig: Schritt 1: Sie erteilen bifa Umweltinstitut GmbH den Auftrag, Ihre
Umzug der abfallwirtschaftlichen Nummern /Kündigung Um sich bei ebegleitschein abzumelden/ zu kündigen sind folgende Schritte notwendig: Schritt 1: Sie erteilen bifa Umweltinstitut GmbH den Auftrag, Ihre
Mit dem Tool Stundenverwaltung von Hanno Kniebel erhalten Sie die Möglichkeit zur effizienten Verwaltung von Montagezeiten Ihrer Mitarbeiter.
 Stundenverwaltung Mit dem Tool Stundenverwaltung von Hanno Kniebel erhalten Sie die Möglichkeit zur effizienten Verwaltung von Montagezeiten Ihrer Mitarbeiter. Dieses Programm zeichnet sich aus durch einfachste
Stundenverwaltung Mit dem Tool Stundenverwaltung von Hanno Kniebel erhalten Sie die Möglichkeit zur effizienten Verwaltung von Montagezeiten Ihrer Mitarbeiter. Dieses Programm zeichnet sich aus durch einfachste
Zur Wahrung der Widerrufsfrist reicht es aus, dass Sie die Mitteilung über die Ausübung des Widerrufsrechts vor Ablauf der Widerrufsfrist absenden.
 Widerrufsbelehrung der Firma Widerrufsbelehrung - Verträge für die Lieferung von Waren Ist der Kunde Unternehmer ( 14 BGB), so hat er kein Widerrufs- und Rückgaberecht gem. 312g BGB i. V. m. 355 BGB. Das
Widerrufsbelehrung der Firma Widerrufsbelehrung - Verträge für die Lieferung von Waren Ist der Kunde Unternehmer ( 14 BGB), so hat er kein Widerrufs- und Rückgaberecht gem. 312g BGB i. V. m. 355 BGB. Das
DAS GRÜNE REZEPT. Für eine sichere Medikation mit rezeptfreien Arzneimitteln
 DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
Kurzanleitung LFB-Online für Schulen
 1. Anmeldung bei LFB-Online für Schulen Rufen Sie im Browser an einem KISS-Rechner die Adresse: http://kv2las2.kultus.bwl.de:7778/ auf. Klicken Sie dort auf Start LFB-Online für Schulen und melden sich
1. Anmeldung bei LFB-Online für Schulen Rufen Sie im Browser an einem KISS-Rechner die Adresse: http://kv2las2.kultus.bwl.de:7778/ auf. Klicken Sie dort auf Start LFB-Online für Schulen und melden sich
Hinweise in Leichter Sprache zum Vertrag über das Betreute Wohnen
 Hinweise in Leichter Sprache zum Vertrag über das Betreute Wohnen Sie möchten im Betreuten Wohnen leben. Dafür müssen Sie einen Vertrag abschließen. Und Sie müssen den Vertrag unterschreiben. Das steht
Hinweise in Leichter Sprache zum Vertrag über das Betreute Wohnen Sie möchten im Betreuten Wohnen leben. Dafür müssen Sie einen Vertrag abschließen. Und Sie müssen den Vertrag unterschreiben. Das steht
Widerrufsbelehrung der redcoon GmbH
 Widerrufsbelehrung der redcoon GmbH Stand: September 2015 www.redcoon.de Inhaltsverzeichnis Widerrufsbelehrung Verträge für die Lieferung von Waren Seite 3 Muster-Widerrufsformular Seite 5 Widerrufsbelehrung
Widerrufsbelehrung der redcoon GmbH Stand: September 2015 www.redcoon.de Inhaltsverzeichnis Widerrufsbelehrung Verträge für die Lieferung von Waren Seite 3 Muster-Widerrufsformular Seite 5 Widerrufsbelehrung
Elternzeit Was ist das?
 Elternzeit Was ist das? Wenn Eltern sich nach der Geburt ihres Kindes ausschließlich um ihr Kind kümmern möchten, können sie bei ihrem Arbeitgeber Elternzeit beantragen. Während der Elternzeit ruht das
Elternzeit Was ist das? Wenn Eltern sich nach der Geburt ihres Kindes ausschließlich um ihr Kind kümmern möchten, können sie bei ihrem Arbeitgeber Elternzeit beantragen. Während der Elternzeit ruht das
Anleitung zum neuen Überaumbuchungssystem der Hochschule für Musik und Tanz Köln
 Anleitung zum neuen Überaumbuchungssystem der Hochschule für Musik und Tanz Köln Dieses System wird im Sommersemester 2015 getestet und gilt nur für das Übehaus. Das Üben in Räumen des Haupthauses wird
Anleitung zum neuen Überaumbuchungssystem der Hochschule für Musik und Tanz Köln Dieses System wird im Sommersemester 2015 getestet und gilt nur für das Übehaus. Das Üben in Räumen des Haupthauses wird
Datenexport aus JS - Software
 Datenexport aus JS - Software Diese Programm-Option benötigen Sie um Kundendaten aus der JS-Software in andere Programme wie Word, Works oder Excel zu exportieren. Wählen Sie aus dem Programm-Menu unter
Datenexport aus JS - Software Diese Programm-Option benötigen Sie um Kundendaten aus der JS-Software in andere Programme wie Word, Works oder Excel zu exportieren. Wählen Sie aus dem Programm-Menu unter
Glaube an die Existenz von Regeln für Vergleiche und Kenntnis der Regeln
 Glaube an die Existenz von Regeln für Vergleiche und Kenntnis der Regeln Regeln ja Regeln nein Kenntnis Regeln ja Kenntnis Regeln nein 0 % 10 % 20 % 30 % 40 % 50 % 60 % 70 % 80 % 90 % Glauben Sie, dass
Glaube an die Existenz von Regeln für Vergleiche und Kenntnis der Regeln Regeln ja Regeln nein Kenntnis Regeln ja Kenntnis Regeln nein 0 % 10 % 20 % 30 % 40 % 50 % 60 % 70 % 80 % 90 % Glauben Sie, dass
EÜR contra Bilanzierung
 Mandanten-Info Eine Dienstleistung Ihres steuerlichen Beraters EÜR contra Bilanzierung Erleichterungen für Kleinunternehmer durch das BilMoG? In enger Zusammenarbeit mit Inhalt 1. Einführung...1 2. Wer
Mandanten-Info Eine Dienstleistung Ihres steuerlichen Beraters EÜR contra Bilanzierung Erleichterungen für Kleinunternehmer durch das BilMoG? In enger Zusammenarbeit mit Inhalt 1. Einführung...1 2. Wer
SMS/ MMS Multimedia Center
 SMS/ MMS Multimedia Center der BEYOND THE NET GmbH BEYOND THE NET GmbH Seite 1 Unser Multimedia Center ist eine WEB basierende Anwendung, die es ermöglicht von einer Zentrale aus, viele Mitarbeiter zu
SMS/ MMS Multimedia Center der BEYOND THE NET GmbH BEYOND THE NET GmbH Seite 1 Unser Multimedia Center ist eine WEB basierende Anwendung, die es ermöglicht von einer Zentrale aus, viele Mitarbeiter zu
Änderung des IFRS 2 Anteilsbasierte Vergütung
 Änderung IFRS 2 Änderung des IFRS 2 Anteilsbasierte Vergütung Anwendungsbereich Paragraph 2 wird geändert, Paragraph 3 gestrichen und Paragraph 3A angefügt. 2 Dieser IFRS ist bei der Bilanzierung aller
Änderung IFRS 2 Änderung des IFRS 2 Anteilsbasierte Vergütung Anwendungsbereich Paragraph 2 wird geändert, Paragraph 3 gestrichen und Paragraph 3A angefügt. 2 Dieser IFRS ist bei der Bilanzierung aller
Verschreibungsfreie Arzneimittel wieder in der Erstattung
 Satzungsleistungen Verschreibungsfreie Arzneimittel wieder in der Erstattung Was sind Satzungsleistungen? Der Rahmen für die Leistungen der gesetzlichen Krankenversicherung wird im Fünften Sozialgesetzbuch
Satzungsleistungen Verschreibungsfreie Arzneimittel wieder in der Erstattung Was sind Satzungsleistungen? Der Rahmen für die Leistungen der gesetzlichen Krankenversicherung wird im Fünften Sozialgesetzbuch
MERKBLATT ZUR RUNDFUNKGEBÜHRENPFLICHT (GEZ) insbesondere für internetfähige PCs ab dem 01.01.2007
 Wozu dieses Merkblatt? In den vergangenen Monaten ist sowohl beim Verband der Diözesen Deutschlands als auch bei den Rundfunkanstalten und der GEZ eine Vielzahl an Anfragen aus dem kirchlichen Bereich
Wozu dieses Merkblatt? In den vergangenen Monaten ist sowohl beim Verband der Diözesen Deutschlands als auch bei den Rundfunkanstalten und der GEZ eine Vielzahl an Anfragen aus dem kirchlichen Bereich
Widerrufsbelehrung der Free-Linked GmbH. Stand: Juni 2014
 Widerrufsbelehrung der Stand: Juni 2014 www.free-linked.de www.buddy-watcher.de Inhaltsverzeichnis Widerrufsbelehrung Verträge für die Lieferung von Waren... 3 Muster-Widerrufsformular... 5 2 Widerrufsbelehrung
Widerrufsbelehrung der Stand: Juni 2014 www.free-linked.de www.buddy-watcher.de Inhaltsverzeichnis Widerrufsbelehrung Verträge für die Lieferung von Waren... 3 Muster-Widerrufsformular... 5 2 Widerrufsbelehrung
DNotI. Fax - Abfrage. GrEStG 1 Abs. 3 Anteilsvereinigung bei Treuhandverhältnissen. I. Sachverhalt:
 DNotI Deutsches Notarinstitut Fax - Abfrage Gutachten des Deutschen Notarinstitut Dokumentnummer: 1368# letzte Aktualisierung: 14. Juni 2004 GrEStG 1 Abs. 3 Anteilsvereinigung bei Treuhandverhältnissen
DNotI Deutsches Notarinstitut Fax - Abfrage Gutachten des Deutschen Notarinstitut Dokumentnummer: 1368# letzte Aktualisierung: 14. Juni 2004 GrEStG 1 Abs. 3 Anteilsvereinigung bei Treuhandverhältnissen
Anleitung über den Umgang mit Schildern
 Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
Dokumentenverwaltung im Internet
 Dokumentenverwaltung im Internet WS 09/10 mit: Thema: Workflow und Rollenverteilung im Backend Gruppe: DVI 10 Patrick Plaum und Kay Hofmann Inhalt 1. Benutzer und Benutzergruppen erstellen...2 1.1. Benutzergruppen...2
Dokumentenverwaltung im Internet WS 09/10 mit: Thema: Workflow und Rollenverteilung im Backend Gruppe: DVI 10 Patrick Plaum und Kay Hofmann Inhalt 1. Benutzer und Benutzergruppen erstellen...2 1.1. Benutzergruppen...2
Das Bildungspaket: Mitmachen möglich machen
 Anita Schäfer Mitglied des Deutschen Bundestages Das Bildungspaket: Mitmachen möglich machen Das Bundesministerium für Arbeit und Soziales informiert über die Einzelheiten: Ab 2011 haben bedürftige Kinder
Anita Schäfer Mitglied des Deutschen Bundestages Das Bildungspaket: Mitmachen möglich machen Das Bundesministerium für Arbeit und Soziales informiert über die Einzelheiten: Ab 2011 haben bedürftige Kinder
10.3.1.8 Übung - Konfigurieren einer Windows 7-Firewall
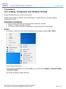 5.0 10.3.1.8 Übung - Konfigurieren einer Windows 7-Firewall Drucken Sie diese Übung aus und führen Sie sie durch. In dieser Übung werden Sie erfahren, wie man die Windows 7-Firewall konfiguriert und einige
5.0 10.3.1.8 Übung - Konfigurieren einer Windows 7-Firewall Drucken Sie diese Übung aus und führen Sie sie durch. In dieser Übung werden Sie erfahren, wie man die Windows 7-Firewall konfiguriert und einige
Arbeitshilfen Messecontrolling Wie geht denn das?
 Messecontrolling Wie geht denn das? In meiner Praxis als Unternehmensberater für Marketing und Vertrieb hat sich über viele Jahre gezeigt, dass die Kunden oftmals Schwierigkeiten haben, ein eigenes Messecontrolling
Messecontrolling Wie geht denn das? In meiner Praxis als Unternehmensberater für Marketing und Vertrieb hat sich über viele Jahre gezeigt, dass die Kunden oftmals Schwierigkeiten haben, ein eigenes Messecontrolling
BERECHNUNG DER FRIST ZUR STELLUNGNAHME DES BETRIEBSRATES BEI KÜNDIGUNG
 Frist berechnen BERECHNUNG DER FRIST ZUR STELLUNGNAHME DES BETRIEBSRATES BEI KÜNDIGUNG Sie erwägen die Kündigung eines Mitarbeiters und Ihr Unternehmen hat einen Betriebsrat? Dann müssen Sie die Kündigung
Frist berechnen BERECHNUNG DER FRIST ZUR STELLUNGNAHME DES BETRIEBSRATES BEI KÜNDIGUNG Sie erwägen die Kündigung eines Mitarbeiters und Ihr Unternehmen hat einen Betriebsrat? Dann müssen Sie die Kündigung
Anleitung zum Computercheck So aktualisieren Sie Ihr Microsoft-Betriebssystem
 Anleitung zum Computercheck So aktualisieren Sie Ihr Microsoft-Betriebssystem Information Wichtiger Hinweis: Microsoft hat am 8. April 2014 den Support für Windows XP eingestellt. Neue Sicherheitsaktualisierungen
Anleitung zum Computercheck So aktualisieren Sie Ihr Microsoft-Betriebssystem Information Wichtiger Hinweis: Microsoft hat am 8. April 2014 den Support für Windows XP eingestellt. Neue Sicherheitsaktualisierungen
1 Abs. 1 a Satz 2 Nr. 1 a KWG definiert die Anlageberatung als die
 Die gesetzliche Definition der Anlageberatung 1 Abs. 1 a Satz 2 Nr. 1 a KWG definiert die Anlageberatung als die Abgabe von persönlichen Empfehlungen an Kunden oder deren Vertreter, die sich auf Geschäfte
Die gesetzliche Definition der Anlageberatung 1 Abs. 1 a Satz 2 Nr. 1 a KWG definiert die Anlageberatung als die Abgabe von persönlichen Empfehlungen an Kunden oder deren Vertreter, die sich auf Geschäfte
Liechtensteinisches Landesgesetzblatt
 Liechtensteinisches Landesgesetzblatt 952.11 Jahrgang 2015 Nr. 250 ausgegeben am 25. September 2015 Verordnung vom 22. September 2015 über die Abänderung der Sorgfaltspflichtverordnung Aufgrund von Art.
Liechtensteinisches Landesgesetzblatt 952.11 Jahrgang 2015 Nr. 250 ausgegeben am 25. September 2015 Verordnung vom 22. September 2015 über die Abänderung der Sorgfaltspflichtverordnung Aufgrund von Art.
Im Folgenden werden einige typische Fallkonstellationen beschrieben, in denen das Gesetz den Betroffenen in der GKV hilft:
 Im Folgenden werden einige typische Fallkonstellationen beschrieben, in denen das Gesetz den Betroffenen in der GKV hilft: Hinweis: Die im Folgenden dargestellten Fallkonstellationen beziehen sich auf
Im Folgenden werden einige typische Fallkonstellationen beschrieben, in denen das Gesetz den Betroffenen in der GKV hilft: Hinweis: Die im Folgenden dargestellten Fallkonstellationen beziehen sich auf
6 Informationsermittlung und Gefährdungsbeurteilung
 Verordnung zum Schutz vor Gefahrstoffen TK Lexikon Arbeitsrecht 6 Informationsermittlung und Gefährdungsbeurteilung HI2516431 (1) 1 Im Rahmen einer Gefährdungsbeurteilung als Bestandteil der Beurteilung
Verordnung zum Schutz vor Gefahrstoffen TK Lexikon Arbeitsrecht 6 Informationsermittlung und Gefährdungsbeurteilung HI2516431 (1) 1 Im Rahmen einer Gefährdungsbeurteilung als Bestandteil der Beurteilung
Selbstständig als Immobilienmakler interna
 Selbstständig als Immobilienmakler interna Ihr persönlicher Experte Inhalt Vorwort... 7 Persönliche Voraussetzungen... 8 Berufsbild... 9 Ausbildung... 10 Voraussetzung für die Tätigkeit als Immobilienmakler...
Selbstständig als Immobilienmakler interna Ihr persönlicher Experte Inhalt Vorwort... 7 Persönliche Voraussetzungen... 8 Berufsbild... 9 Ausbildung... 10 Voraussetzung für die Tätigkeit als Immobilienmakler...
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Legalon SIL - Trockensubstanz zur Infusionsbereitung
 PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
IHR PATIENTENDOSSIER IHRE RECHTE
 IHR PATIENTENDOSSIER IHRE RECHTE Im Spital, in der Klinik bestimmen Sie, wie Sie über Ihre Krankheit und deren Behandlung informiert werden wollen und wer informiert werden darf Information Patientendossier
IHR PATIENTENDOSSIER IHRE RECHTE Im Spital, in der Klinik bestimmen Sie, wie Sie über Ihre Krankheit und deren Behandlung informiert werden wollen und wer informiert werden darf Information Patientendossier
www.computeria-olten.ch Monatstreff für Menschen ab 50 Temporäre Dateien / Browserverlauf löschen / Cookies
 www.computeria-olten.ch Monatstreff für Menschen ab 50 Merkblatt 42 Temporäre Dateien / Browserverlauf löschen / Cookies Im Internet-Explorer Extras / Browserverlauf löschen Jetzt entscheiden, was man
www.computeria-olten.ch Monatstreff für Menschen ab 50 Merkblatt 42 Temporäre Dateien / Browserverlauf löschen / Cookies Im Internet-Explorer Extras / Browserverlauf löschen Jetzt entscheiden, was man
Stand: 28.11.2012. Adressnummern ändern Modulbeschreibung
 Seite 1 Inhalt Allgemein...3 Installation...3 manuelle Eingabe von alten und neuen Adressnummern...4 Vorbereiten von Adressnummern-Änderungen in Tabellen...5 Seite 2 Allgemein Das INKS-Modul ermöglicht
Seite 1 Inhalt Allgemein...3 Installation...3 manuelle Eingabe von alten und neuen Adressnummern...4 Vorbereiten von Adressnummern-Änderungen in Tabellen...5 Seite 2 Allgemein Das INKS-Modul ermöglicht
Bei der Anlage von Pauschalen ist folgendes zu beachten!!!!!!!!
 Bei der Anlage von Pauschalen ist folgendes zu beachten!!!!!!!! Vorgaben für Pauschen: Die Pauschale wird in der Homepage mit 3 Punkten dargestellt Titel ist der Produkttitel Pro Punkt jeweils maximal
Bei der Anlage von Pauschalen ist folgendes zu beachten!!!!!!!! Vorgaben für Pauschen: Die Pauschale wird in der Homepage mit 3 Punkten dargestellt Titel ist der Produkttitel Pro Punkt jeweils maximal
Downloadfehler in DEHSt-VPSMail. Workaround zum Umgang mit einem Downloadfehler
 Downloadfehler in DEHSt-VPSMail Workaround zum Umgang mit einem Downloadfehler Downloadfehler bremen online services GmbH & Co. KG Seite 2 Inhaltsverzeichnis Vorwort...3 1 Fehlermeldung...4 2 Fehlerbeseitigung...5
Downloadfehler in DEHSt-VPSMail Workaround zum Umgang mit einem Downloadfehler Downloadfehler bremen online services GmbH & Co. KG Seite 2 Inhaltsverzeichnis Vorwort...3 1 Fehlermeldung...4 2 Fehlerbeseitigung...5
Merkblatt. Häufige Fragen hinsichtlich der Anforderungen für Hersteller bzw. Inverkehrbringer von Lebensmittelbedarfsgegenständen aus Keramik
 Merkblatt Häufige Fragen hinsichtlich der Anforderungen für Hersteller bzw. Inverkehrbringer von Lebensmittelbedarfsgegenständen aus Keramik Was sind Lebensmittelbedarfsgegenstände? Lebensmittelbedarfsgegenstände
Merkblatt Häufige Fragen hinsichtlich der Anforderungen für Hersteller bzw. Inverkehrbringer von Lebensmittelbedarfsgegenständen aus Keramik Was sind Lebensmittelbedarfsgegenstände? Lebensmittelbedarfsgegenstände
Ist Fernsehen schädlich für die eigene Meinung oder fördert es unabhängig zu denken?
 UErörterung zu dem Thema Ist Fernsehen schädlich für die eigene Meinung oder fördert es unabhängig zu denken? 2000 by christoph hoffmann Seite I Gliederung 1. In zu großen Mengen ist alles schädlich. 2.
UErörterung zu dem Thema Ist Fernsehen schädlich für die eigene Meinung oder fördert es unabhängig zu denken? 2000 by christoph hoffmann Seite I Gliederung 1. In zu großen Mengen ist alles schädlich. 2.
Informationen zum Begleiteten Fahren ab 17
 Informationen zum Begleiteten Fahren ab 17 Ausbildung Darf auch ein Bewerber ausgebildet werden, der in einem Bundesland seinen ersten Wohnsitz hat, wenn dieses Bundesland das Begleitete Fahren nicht eingeführt
Informationen zum Begleiteten Fahren ab 17 Ausbildung Darf auch ein Bewerber ausgebildet werden, der in einem Bundesland seinen ersten Wohnsitz hat, wenn dieses Bundesland das Begleitete Fahren nicht eingeführt
Shopz Zugang Neuanmeldung
 Web Sales, IBM Deutschland Shopz Zugang Neuanmeldung IBM ID einrichten Shopz-Zugang anmelden Shopz Login User ID Management IBM ID und Shopz Zugang im Überblick Überblick ibm.com/software/de/websolutions/
Web Sales, IBM Deutschland Shopz Zugang Neuanmeldung IBM ID einrichten Shopz-Zugang anmelden Shopz Login User ID Management IBM ID und Shopz Zugang im Überblick Überblick ibm.com/software/de/websolutions/
Webseiten mit fragwürdigen Aufrufen von "spy & track" - Unternehmen
 Webseiten mit fragwürdigen Aufrufen von "spy & track" - Unternehmen Die vorliegende Dokumentation umfasst eine kleine Auswahl von Webseiten, bei denen automatisch (ohne Benutzer vorab zu informieren oder
Webseiten mit fragwürdigen Aufrufen von "spy & track" - Unternehmen Die vorliegende Dokumentation umfasst eine kleine Auswahl von Webseiten, bei denen automatisch (ohne Benutzer vorab zu informieren oder
Information zum Projekt. Mitwirkung von Menschen mit Demenz in ihrem Stadtteil oder Quartier
 Information zum Projekt Mitwirkung von Menschen mit Demenz in ihrem Stadtteil oder Quartier Sehr geehrte Dame, sehr geehrter Herr Wir führen ein Projekt durch zur Mitwirkung von Menschen mit Demenz in
Information zum Projekt Mitwirkung von Menschen mit Demenz in ihrem Stadtteil oder Quartier Sehr geehrte Dame, sehr geehrter Herr Wir führen ein Projekt durch zur Mitwirkung von Menschen mit Demenz in
Privatinsolvenz anmelden oder vielleicht sogar vermeiden. Tipps und Hinweise für die Anmeldung der Privatinsolvenz
 Privatinsolvenz anmelden oder vielleicht sogar vermeiden Tipps und Hinweise für die Anmeldung der Privatinsolvenz Privatinsolvenz anmelden oder vielleicht sogar vermeiden Überschuldet Was nun? Derzeit
Privatinsolvenz anmelden oder vielleicht sogar vermeiden Tipps und Hinweise für die Anmeldung der Privatinsolvenz Privatinsolvenz anmelden oder vielleicht sogar vermeiden Überschuldet Was nun? Derzeit
Bericht für Menschen mit Hörbehinderung und gehörlose Menschen
 Bericht für Menschen mit Hörbehinderung und gehörlose Menschen Barrierefreiheit geprüft Bericht St. Michaelis 1/5 Abbildung 1: Außenansicht der Kirche St. Michaelis Anschrift St. Michaelis Turm GmbH Englische
Bericht für Menschen mit Hörbehinderung und gehörlose Menschen Barrierefreiheit geprüft Bericht St. Michaelis 1/5 Abbildung 1: Außenansicht der Kirche St. Michaelis Anschrift St. Michaelis Turm GmbH Englische
Statuten in leichter Sprache
 Statuten in leichter Sprache Zweck vom Verein Artikel 1: Zivil-Gesetz-Buch Es gibt einen Verein der selbstbestimmung.ch heisst. Der Verein ist so aufgebaut, wie es im Zivil-Gesetz-Buch steht. Im Zivil-Gesetz-Buch
Statuten in leichter Sprache Zweck vom Verein Artikel 1: Zivil-Gesetz-Buch Es gibt einen Verein der selbstbestimmung.ch heisst. Der Verein ist so aufgebaut, wie es im Zivil-Gesetz-Buch steht. Im Zivil-Gesetz-Buch
HANDBUCH PHOENIX II - DOKUMENTENVERWALTUNG
 it4sport GmbH HANDBUCH PHOENIX II - DOKUMENTENVERWALTUNG Stand 10.07.2014 Version 2.0 1. INHALTSVERZEICHNIS 2. Abbildungsverzeichnis... 3 3. Dokumentenumfang... 4 4. Dokumente anzeigen... 5 4.1 Dokumente
it4sport GmbH HANDBUCH PHOENIX II - DOKUMENTENVERWALTUNG Stand 10.07.2014 Version 2.0 1. INHALTSVERZEICHNIS 2. Abbildungsverzeichnis... 3 3. Dokumentenumfang... 4 4. Dokumente anzeigen... 5 4.1 Dokumente
WinWerk. Prozess 6a Rabatt gemäss Vorjahresverbrauch. KMU Ratgeber AG. Inhaltsverzeichnis. Im Ifang 16 8307 Effretikon
 WinWerk Prozess 6a Rabatt gemäss Vorjahresverbrauch 8307 Effretikon Telefon: 052-740 11 11 Telefax: 052-740 11 71 E-Mail info@kmuratgeber.ch Internet: www.winwerk.ch Inhaltsverzeichnis 1 Ablauf der Rabattverarbeitung...
WinWerk Prozess 6a Rabatt gemäss Vorjahresverbrauch 8307 Effretikon Telefon: 052-740 11 11 Telefax: 052-740 11 71 E-Mail info@kmuratgeber.ch Internet: www.winwerk.ch Inhaltsverzeichnis 1 Ablauf der Rabattverarbeitung...
Regulatorischer Rahmen. Klassifizierung
 Regulatorischer Rahmen Erkenntnisgewinn zu Regenerations- und Reparaturprozessen des menschlichen Körpers führen zu neuen Arten innovativer und komplexer Produkte. Unter Regenerativer Medizin (kurz: RegMed)
Regulatorischer Rahmen Erkenntnisgewinn zu Regenerations- und Reparaturprozessen des menschlichen Körpers führen zu neuen Arten innovativer und komplexer Produkte. Unter Regenerativer Medizin (kurz: RegMed)
Bereich METIS (Texte im Internet) Zählmarkenrecherche
 Bereich METIS (Texte im Internet) Zählmarkenrecherche Über die Zählmarkenrecherche kann man nach der Eingabe des Privaten Identifikationscodes einer bestimmten Zählmarke, 1. Informationen zu dieser Zählmarke
Bereich METIS (Texte im Internet) Zählmarkenrecherche Über die Zählmarkenrecherche kann man nach der Eingabe des Privaten Identifikationscodes einer bestimmten Zählmarke, 1. Informationen zu dieser Zählmarke
Gemeinsame Erklärung zur inter-kulturellen Öffnung und zur kultur-sensiblen Arbeit für und mit Menschen mit Behinderung und Migrations-Hintergrund.
 Gemeinsame Erklärung zur inter-kulturellen Öffnung und zur kultur-sensiblen Arbeit für und mit Menschen mit Behinderung und Migrations-Hintergrund. Das ist eine Erklärung in Leichter Sprache. In einer
Gemeinsame Erklärung zur inter-kulturellen Öffnung und zur kultur-sensiblen Arbeit für und mit Menschen mit Behinderung und Migrations-Hintergrund. Das ist eine Erklärung in Leichter Sprache. In einer
GmbH. Feuer im Herzen. Werbung im Blut.
 GmbH Feuer im Herzen. Werbung im Blut. feuer im herzen. werbung im blut. professionell im dialog in.signo ist eine inhabergeführte Agentur für Design und Kommunikation mit Sitz in Hamburg. Die Größe einer
GmbH Feuer im Herzen. Werbung im Blut. feuer im herzen. werbung im blut. professionell im dialog in.signo ist eine inhabergeführte Agentur für Design und Kommunikation mit Sitz in Hamburg. Die Größe einer
Aufbereitung von Medizinprodukten
 R K I - R I C H T L I N I E N Aufbereitung von Medizinprodukten Erläuterungen zu der Übersicht Nachfolgend veröffentlichen wir eine Übersicht zur Aufbereitung von Medizinprodukten der Gruppen semikritisch
R K I - R I C H T L I N I E N Aufbereitung von Medizinprodukten Erläuterungen zu der Übersicht Nachfolgend veröffentlichen wir eine Übersicht zur Aufbereitung von Medizinprodukten der Gruppen semikritisch
Rückverfolgbarkeit von Lebensmitteln Erfahrungen aus den Ländern
 Rückverfolgbarkeit von Lebensmitteln Erfahrungen aus den Ländern Untersuchung und Erfassung lebensmittelbedingter Ausbrüche Informationsveranstaltung des Bundesinstituts für Risikobewertung am 25. Januar
Rückverfolgbarkeit von Lebensmitteln Erfahrungen aus den Ländern Untersuchung und Erfassung lebensmittelbedingter Ausbrüche Informationsveranstaltung des Bundesinstituts für Risikobewertung am 25. Januar
Buchhaltung mit WISO EÜR & Kasse 2011
 Vorbemerkung... 1 1. Erste Schritte...Fehler! Textmarke nicht definiert.3 2. Einrichten des Programms... 5 3. Buchungen... 22 1. Anfangsbestand buchen... 22 2. Privateinlage in die Kasse... 26 4. Buchungen
Vorbemerkung... 1 1. Erste Schritte...Fehler! Textmarke nicht definiert.3 2. Einrichten des Programms... 5 3. Buchungen... 22 1. Anfangsbestand buchen... 22 2. Privateinlage in die Kasse... 26 4. Buchungen
Erstellen und Bearbeiten von Inhalten (Assets)
 Wichtig! Beachten Sie die Designrichtlinien im Kapitel Darstellung und Vorgaben zur Erstellung der Inhalte Ein Linkset erstellen Sie, wenn Sie mehrere Links gruppiert ausgeben möchten. Sie sollten diesem
Wichtig! Beachten Sie die Designrichtlinien im Kapitel Darstellung und Vorgaben zur Erstellung der Inhalte Ein Linkset erstellen Sie, wenn Sie mehrere Links gruppiert ausgeben möchten. Sie sollten diesem
Bericht für Menschen mit Gehbehinderung und Rollstuhlfahrer
 Bericht Restaurant Alfsee Piazza 1/8 Bericht für Menschen mit Gehbehinderung und Rollstuhlfahrer Innenansicht des Restaurants Restaurant Alfsee Piazza Anschrift Alfsee GmbH Am Campingpark 10 49597 Rieste
Bericht Restaurant Alfsee Piazza 1/8 Bericht für Menschen mit Gehbehinderung und Rollstuhlfahrer Innenansicht des Restaurants Restaurant Alfsee Piazza Anschrift Alfsee GmbH Am Campingpark 10 49597 Rieste
Informationen zur Prüfung Geprüfter Handelsfachwirt (IHK)/Geprüfte Handelsfachwirtin (IHK)
 Informationen zur Prüfung Geprüfter Handelsfachwirt (IHK)/Geprüfte Handelsfachwirtin (IHK) Die Prüfung zum Geprüften Handelsfachwirt (IHK)/zur Geprüften Handelsfachwirtin (IHK) ist eine öffentlich-rechtliche
Informationen zur Prüfung Geprüfter Handelsfachwirt (IHK)/Geprüfte Handelsfachwirtin (IHK) Die Prüfung zum Geprüften Handelsfachwirt (IHK)/zur Geprüften Handelsfachwirtin (IHK) ist eine öffentlich-rechtliche
Webalizer HOWTO. Stand: 18.06.2012
 Webalizer HOWTO Stand: 18.06.2012 Copyright 2003 by manitu. Alle Rechte vorbehalten. Alle verwendeten Bezeichnungen dienen lediglich der Kennzeichnung und können z.t. eingetragene Warenzeichen sein, ohne
Webalizer HOWTO Stand: 18.06.2012 Copyright 2003 by manitu. Alle Rechte vorbehalten. Alle verwendeten Bezeichnungen dienen lediglich der Kennzeichnung und können z.t. eingetragene Warenzeichen sein, ohne
Papierverbrauch im Jahr 2000
 Hier findest du Forschertipps. Du kannst sie allein oder in der kleinen Gruppe mit anderen Kindern bearbeiten! Gestaltet ein leeres Blatt, schreibt Berichte oder entwerft ein Plakat. Sprecht euch in der
Hier findest du Forschertipps. Du kannst sie allein oder in der kleinen Gruppe mit anderen Kindern bearbeiten! Gestaltet ein leeres Blatt, schreibt Berichte oder entwerft ein Plakat. Sprecht euch in der
Der BeB und die Diakonie Deutschland fordern: Gesundheit und Reha müssen besser werden. So ist es jetzt:
 Der BeB und die Diakonie Deutschland fordern: Gesundheit und Reha müssen besser werden So ist es jetzt: Valuing people Menschen mit Behinderung müssen öfter zum Arzt gehen als Menschen ohne Behinderung.
Der BeB und die Diakonie Deutschland fordern: Gesundheit und Reha müssen besser werden So ist es jetzt: Valuing people Menschen mit Behinderung müssen öfter zum Arzt gehen als Menschen ohne Behinderung.
25. November 2009. Umsatzsteuer: Neuregelung des Orts der Sonstigen Leistung. Sehr geehrte Mandanten,
 25. November 2009 Umsatzsteuer: Neuregelung des Orts der Sonstigen Leistung Sehr geehrte Mandanten, durch das Jahressteuergesetz 2009 ergeben sich weit reichende Änderungen für Unternehmer, die Dienstleistungen
25. November 2009 Umsatzsteuer: Neuregelung des Orts der Sonstigen Leistung Sehr geehrte Mandanten, durch das Jahressteuergesetz 2009 ergeben sich weit reichende Änderungen für Unternehmer, die Dienstleistungen
Vertrag zwischen. der AOK Berlin - Die Gesundheitskasse - und der Kassenärztlichen Vereinigung Berlin (KV)
 Vertrag zwischen der AOK Berlin - Die Gesundheitskasse - und der Kassenärztlichen Vereinigung Berlin (KV) über die Abgrenzung, Vergütung und Abrechnung der stationären vertragsärztlichen Tätigkeit 1) Dem
Vertrag zwischen der AOK Berlin - Die Gesundheitskasse - und der Kassenärztlichen Vereinigung Berlin (KV) über die Abgrenzung, Vergütung und Abrechnung der stationären vertragsärztlichen Tätigkeit 1) Dem
