Physik Organischer Halbleiter:
|
|
|
- Guido Egger
- vor 7 Jahren
- Abrufe
Transkript
1 Physik Organischer albleiter: Opto- und Mikroelektronik, Photovoltaik, Sensorik Vladimir Dyakonov Experimental Physics VI, Julius-Maximilians-University of Würzburg und Bayerisches Zentrum für Angewandte Energieforschung e.v. (ZAE Bayern)
2 Inhalte Einführung und Motivation 1. Elektronische Struktur: von Atomorbitalen zu Molekülorbitalen 2. Spezialbeispiel: Polyacethylen 3. Ladungsträger in organischen albleiter 4. Optische Eigenschaften 5. Grundlagen des Ladungstransports 6. Metall-albleiter Kontakt, Injektion von Ladungsträger 7. Bauelementtechnologie 8. Leuchtdioden (OLED) 9. Solarzellen (OSZ) 10. Andere Anwendungen: Transistoren (OFET), organische Laser, Sensoren 11. Zusammenfassung: Vergleich organischer und anorganischer albleiter 2
3 Allgemeine Anmerkungen Übungen Do. 13:45-14:30 sind für die Übungen vorgesehen Folien zur Vorlesung sind unter: zu finden. 3
4 Allgemeine Anmerkungen Literatur M. Schwoerer,. C. Wolf, Organische Molekulare Festkörper, WILEY-VC, Weinheim, 2005 agen Klauk (Ed.), Organic Electronics: Materials, Manufacturing and Applications, Wiley-VC, Winheim, 2006 M. Pope, C. E. Swenberg, Electronic Processes in Organic Crystals and Polymers, Oxford University Press, New York, 1999 J. Simon and J.-J. Andre, Molecular Semiconductors, Springer Verlag, Berlin, eidelberg, New York, Tokyo 1985 Physik Journal, Schwerpunkt Organische Elektronik, Mai 2008 (erhältlich beim Veranstalter) 4
5 Allgemeine Anmerkungen In dieser VL werden physikalischen Eigenschaften von organischen albleitern und ihre zukunftsträchtigen, multimediafähigen Anwendungen vorgestellt Wir werden uns mit ELEKTRONISCEN PROZESSEN in organischen Systemen beschäftigen, nicht mit IONISCEN 90% alle Stoffe sind organisch, d.h. enthalten Kohlenstoff, aber nicht alle sind albleiter Konjugierte Systeme, oder aromatische Kohlenwasserstoffe, sind für uns interessant 5
6 Einführung Was hält Atome in Polymeren und Molekülen zusammen? Chemische Bindung 1. Die ionische Bindung 2. Die kovalente Bindung (reine QM nach eitler-london) 3. Van-der-Waals-Bindung: Elektrostatische Dipol-Dipol Wechselwirkung (induziert oder permanent) 4. Metallische Bindung: kovalent, aber Bindungselektronen über gesamten Kristall verteilt (delokalisiert) 5. Wasserstoffbrückenbindung 6
7 Einführung 1. Ionische Bindung heteropolar, klassisch zu verstehen Molekül aus Ionen (geladenen Atomen) Atome mit 1 oder 2 Elektronen zu viel oder zu wenig als Edelgas-Konfiguration Ionisation energetisch günstig positive und negative Ionen ziehen sich an (Coulomb-Kräfte) => chemische Bindung! Bei kleinem Abstand: großer Überlapp der Elektronen-Orbitale => Pauli-Abstoßung Doch nicht ganz klassisch... 7
8 Einführung 2. Kovalente Bindung homöopolare Bindung zwischen neutralen Atomen durch Austausch gemeinsamer Elektronen Umordnung der Dichteverteilung zwischen den Kernen Bindungsenergie nur quantenmechanisch zu verstehen großer Einfluss von Pauli-Prinzip und Austausch es existieren Mischformen kovalent-ionisch: schwach ionischer Charakter Atome nicht vollständig ionisiert Beispiel: 2 -Molekül 8
9 Einführung ung neutraler Atome und... W. eitler and F. London: Wechselwirkung neutraler Atome und Kovalente Bindung (eitler-london) W. eitler F. London F. London "Wechselwirkung neutraler Atome und homöopolare Bindung nach der Quantenmechanik", W. eitler and Zeitschrift F. London, für Physik, "Wechselwirkung 44, neutraler (1927). Atome und homöopolare B on, "Wechselwirkung nach neutraler der Quantenmechanik", Atome und homöopolare Bindung hanik", Zeitschrift für Physik, 44, (1927). 9 4, (1927).
10 Einführung eitler and F. London: Wechselwirkung neutraler Atome und... "Wechselwirkung neutraler Atome und homöopolare Bindung nach der Quantenmechanik", Zeitschrift für Physik, 44, (1927). 10
11 Einführung "Wechselwirkung neutraler Atome und homöopolare Bindung nach der Quantenmechanik", Zeitschrift für Physik, 44, (1927). 11
12 Einführung 2. Kovalente Bindung Molekülorbitale konstruieren aus Atomorbitalen im 1s-Grundzustand Gesamtwellenfunktion (Bahnbewegung und Spin) des Elektrons im Grundzustand des -Atoms: Ψ ges =ψ(r) ϕmuss antisymmetrisch bezüglich Vertauschung der beiden Elektronen sein. (Pauli-Prinzip) 12
13 Einführung 3. Van-der-Waals-Bindung Elektrostatische Dipol-Dipol-Wechselwirkung a) permanent wie, z.b. 2O-Molekül b) induziert Elektronen sind nicht fixiert, d.h. es gibt Verteilungsschwankungen temporäres Dipolmoment, zeitlicher Mittelwert = 0 VdW-Bindung ist schwach und kurzreichweitig und fällt mit 1/R 6 ab Bemerkung: VdW-Kräfte = London-Kräfte 13
14 Einführung 4. Metallische Bindung kovalent, aber Bindungselektronen über gesamten Kristall verteilt (delokalisiert, oder frei ) im Feld der Gitterionen können sich die Valenzelektronen quasifrei bewegen (Elektronengas) Elektronengas + Gitter aus positiven Rumpfionen QM liefert die Erklärung für die metallische Bindung Ungefähr ein Elektron pro Atom für alle Metalle ( halbgefülltes Band ) Bemerkung: Elektronengas = Valenzelektronen 14
15 Einführung 5. Wasserstoffbrückenbindung ( sharing of a proton ) Tritt bei mehratomigen Molekülen (z.b. DNA) auf Anziehung zwischen zwei Atomen wird durch ein + -Ion vermittelt Das Proton polarisiert beide Atome = anziehende Kraft; ähnlich wie das Elektron Am häufigsten zwischen 2 Sauerstoffatomen F F F 2 - Molekülion + O O 2 O-Dimer 15
16 Einführung Vergleich Bindung Bindungsenergie Ionenbindung (heteropolare Bindung) -1 ev ev Kovalente Bindung (homöopolare Bindung) -1 ev ev Van der Waals Bindung -0,01 ev.. -0,1 ev Wasserstoffbrückenbindung bis -0,5 ev Metallische Bindung -1eV ev Bindungsenergie ist negativ: bei der Molekülbindung wird diese Bindungsenergie freigesetzt (der stabilste Zustand ist der Zustand mit der minimalsten Energie) Ionenbindung und kovalente Bindung sind nichtreale Grenzfälle der chemischen Bindung (d.h. es gibt keine rein ionische oder rein kovalente Bindung!) 16
17 Motivation Kohlenstoff Kohlenstoff hat 4 Valenzelektronen: C C Diamant Graphit Zwei Formen der räumlichen Anordnung von kovalenten Bindungen! 17
18 Motivation Diamant Vier Bindungen Isolator transparent extrem hart teuer 18
19 Motivation Diamant Vier Bindungen 19
20 Motivation Polyethylen Vier Bindungen + je zwei Wasserstoff Atome Isolator transparent thermoplastisch billig klassisches Plastik 20
21 Motivation Graphit Drei Bindungen + ein freies Elektron elektrischer Leiter grau-metallisch schmierend Bleistift 21
22 Motivation Graphit Drei Bindungen + ein freies Elektron 22
23 Motivation Polyacethylen Drei Bindungen + ein freies Elektron + je ein Wasserstoff albleiter silbern-metallisch Polymer (Kunststoff) Nobel-Preis 23
24 Motivation Neue Materialklasse Nobel-Preis für Chemie 2000 "for the discovery and development of conductive polymers" für die Entdeckung und die Entwicklung leitfähiger Polymere Alan J. eeger Alan G. MacDiarmid ideki Shirakawa 1/3 of the prize 1/3 of the prize 1/3 of the prize USA University of California Santa Barbara, CA, USA USA and New Zealand University of Pennsylvania Philadelphia, PA, USA Japan University of Tsukuba Tokyo, Japan b b (in Masterton, New Zealand) b
25 Zurück zum Graphit 0.67 nm Professor Dr. Vladimir Dyakonov, Experimentelle Physik VI
26 Graphit diamond graphite GRAPENE nanotubes fullerenes Lücke zwischen Graphit und Nanorohr Professor Dr. Vladimir Dyakonov, Experimentelle Physik VI
27 Nobelpreis für Physik 2010 "for groundbreaking experiments regarding the two-dimensional material graphene" A. Geim K. Novoselov Professor Dr. Vladimir Dyakonov, Experimentelle Physik VI
28 Nobelpreis für Physik Tesafilm lösen Professor Dr. Vladimir Dyakonov, Experimentelle Physik VI
29 Graphene Superlatives Professor Dr. Vladimir Dyakonov, Experimentelle Physik VI
30 Einführung Lehrbuch: K. Seeger, 4. Auflage, Springer-Verlag Some aromatic hydrocarbons were found to be semiconductors. No practical application has as yet been found for organic semiconductors. Raising the conductivity in these compounds by heating is limited by thermal decomposition but in some polymers it can be raised by doping up to metallic conductivity values of both n- and p-type. Ziel dieser Vorlesung ist das Gegenteil zu beweisen... 30
31 Inhalte das nächste Mal Einführung und Motivation 1. Elektronische Struktur: von Atomorbitalen zu Molekülorbitalen 2. Spezialbeispiel: Polyacethylen 3. Ladungsträger in organischen albleiter 4. Optische Eigenschaften 5. Grundlagen des Ladungstransports 6. Metall-albleiter Kontakt, Injektion von Ladungsträger 7. Bauelementtechnologie 8. Leuchtdioden (OLED) 9. Solarzellen (OSZ) 10. Andere Anwendungen: Transistoren (OFET), organische Laser, Sensoren 11. Zusammenfassung: Vergleich organischer und anorganischer albleiter 31
Mechanisch-thermische. Materialeigenschaften VL # 2
 Mechanisch-thermische Materialeigenschaften VL # 2 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und Bayerisches Zentrum für Angewandte
Mechanisch-thermische Materialeigenschaften VL # 2 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und Bayerisches Zentrum für Angewandte
Physik Organischer Halbleiter:
 Physik Organischer Halbleiter: Opto- und Mikroelektronik, Photovoltaik, ensorik Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und
Physik Organischer Halbleiter: Opto- und Mikroelektronik, Photovoltaik, ensorik Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und
Kristallchemie. Atome Ionen Moleküle Chemische Bindungen
 Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
Opto-elektronische. Materialeigenschaften VL # 10
 Opto-elektronische Materialeigenschaften VL # 10 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und Bayerisches Zentrum für Angewandte
Opto-elektronische Materialeigenschaften VL # 10 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und Bayerisches Zentrum für Angewandte
Atom-, Molekül- und Festkörperphysik
 Atom-, Molekül- und Festkörperphysik für LAK, SS 2014 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 4. Vorlesung, 27. 3. 2014 Molekülbindung, H2+ - Molekülion, Hybridisierung, Kohlenstoffverbindungen
Atom-, Molekül- und Festkörperphysik für LAK, SS 2014 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 4. Vorlesung, 27. 3. 2014 Molekülbindung, H2+ - Molekülion, Hybridisierung, Kohlenstoffverbindungen
Norbert Koch. Polymer gegen Silizium: Wer wird in der Elektronik gewinnen?
 Polymer gegen Silizium: Wer wird in der Elektronik gewinnen? Norbert Koch Humboldt Universität zu Berlin, Institut für Physik & IRIS Adlershof Helmholtz Zentrum Berlin für Materialien und Energie GmbH
Polymer gegen Silizium: Wer wird in der Elektronik gewinnen? Norbert Koch Humboldt Universität zu Berlin, Institut für Physik & IRIS Adlershof Helmholtz Zentrum Berlin für Materialien und Energie GmbH
Mehratomige Molek ule
 Wir wollen jetzt eine sehr einfache Theorie entwickeln, um die Bindung in Molekülen mit mehr als zwei Atomen zu verstehen Dazu müssen wir den Aufbau von komplexeren n wie π oder δ-n verstehen Wir wissen
Wir wollen jetzt eine sehr einfache Theorie entwickeln, um die Bindung in Molekülen mit mehr als zwei Atomen zu verstehen Dazu müssen wir den Aufbau von komplexeren n wie π oder δ-n verstehen Wir wissen
Graphene. L. Holtmeier. Proseminar Physik, 2013. L. Holtmeier (University of Bielefeld) Graphene 2013 1 / 18
 Graphene L. Holtmeier Proseminar Physik, 2013 L. Holtmeier (University of Bielefeld) Graphene 2013 1 / 18 Gliederung 1 Motivation und Einleitung 2 Entdeckung, Herstellung und Identifikation 3 Eigenschaften
Graphene L. Holtmeier Proseminar Physik, 2013 L. Holtmeier (University of Bielefeld) Graphene 2013 1 / 18 Gliederung 1 Motivation und Einleitung 2 Entdeckung, Herstellung und Identifikation 3 Eigenschaften
Atome und Bindungen. Was sollen Sie mitnehmen?
 Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
08.12.2013. Wichtige Stoffgruppen. Stoffgruppe. Atomverband. Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Metall Metall:
 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter) - Salze Nichtmetall Nichtmetall:
1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter) - Salze Nichtmetall Nichtmetall:
Atome und Bindungen. Was sollen Sie mitnehmen?
 Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Bohrsches Atommodell
 Atome und ihre Bindungen Atomaufbau Im Atomkern befinden sich die Protonen (positiv geladen) und die Neutronen (neutral). P und N sind ungefähr gleich schwer und machen 99% der Atommasse aus. Um den Kern
Atome und ihre Bindungen Atomaufbau Im Atomkern befinden sich die Protonen (positiv geladen) und die Neutronen (neutral). P und N sind ungefähr gleich schwer und machen 99% der Atommasse aus. Um den Kern
30. Lektion. Moleküle. Molekülbindung
 30. Lektion Moleküle Molekülbindung Lernziel: Moleküle entstehen aus Atomen falls ihre Wellenfunktionen sich derart überlappen, daß die Gesamtenergie abgesenkt wird. Begriffe Begriffe: Kovalente Bindung
30. Lektion Moleküle Molekülbindung Lernziel: Moleküle entstehen aus Atomen falls ihre Wellenfunktionen sich derart überlappen, daß die Gesamtenergie abgesenkt wird. Begriffe Begriffe: Kovalente Bindung
HÖHERE PHYSIK SKRIPTUM VORLESUNGBLATT XI
 Prof. Dr. F. Koch Dr. H. E. Porteanu fkoch@ph.tum.de porteanu@ph.tum.de WS 4-5 HÖHEE PHYSIK SKIPTUM VOLESUNGBLATT XI 4..5 Molekülphysik Atome binden zu Molekülen und Festkörpern durch interatomare Kräfte
Prof. Dr. F. Koch Dr. H. E. Porteanu fkoch@ph.tum.de porteanu@ph.tum.de WS 4-5 HÖHEE PHYSIK SKIPTUM VOLESUNGBLATT XI 4..5 Molekülphysik Atome binden zu Molekülen und Festkörpern durch interatomare Kräfte
22. Chemische Bindungen
 .05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
.05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
Allotrope Modifikationen des Kohlenstoffs. Ein Vortrag von Julian Franzgrote, Thorben Hagedorn und Niklas Weitkemper
 Allotrope Modifikationen des Kohlenstoffs Ein Vortrag von Julian Franzgrote, Thorben Hagedorn und Niklas Weitkemper 1 Inhaltsverzeichnis Allotropie Übersicht Diamant Graphit Graphen Fullerene Carbon Nanotubes
Allotrope Modifikationen des Kohlenstoffs Ein Vortrag von Julian Franzgrote, Thorben Hagedorn und Niklas Weitkemper 1 Inhaltsverzeichnis Allotropie Übersicht Diamant Graphit Graphen Fullerene Carbon Nanotubes
Physik 4: Skalen und Strukturen
 Physik 4: Skalen und Strukturen.5: Kleine Skalen Chemische Bindung Aggregatszustände Kristallstrukturen und Streuung Bildung des Lebens Kovalente Molekülbindungen Ladungsdichteverteilungen: CH 4 NH 3 H
Physik 4: Skalen und Strukturen.5: Kleine Skalen Chemische Bindung Aggregatszustände Kristallstrukturen und Streuung Bildung des Lebens Kovalente Molekülbindungen Ladungsdichteverteilungen: CH 4 NH 3 H
VL 22 VL Periodensystem VL Röntgenstrahlung VL Homonukleare Moleküle VL Heteronukleare Moleküle
 VL 22 VL 20 20.1. Periodensystem VL 21 21.1. Röntgenstrahlung VL 22 22.1. Homonukleare Moleküle VL 23 23.1. Heteronukleare Moleküle Wim de Boer, Karlsruhe Atome und Moleküle, 10.07.2012 1 Vorlesung 22:
VL 22 VL 20 20.1. Periodensystem VL 21 21.1. Röntgenstrahlung VL 22 22.1. Homonukleare Moleküle VL 23 23.1. Heteronukleare Moleküle Wim de Boer, Karlsruhe Atome und Moleküle, 10.07.2012 1 Vorlesung 22:
Die Anzahl der Protonen und Neutronen entspricht der Atommassenzahl.
 Atom Der Begriff Atom leitet sich von atomos her, was unteilbar heisst. Diese Definition ist alt, da man heutzutage fähig ist, Atome zu teilen. Atommassenzahl Die Anzahl der Protonen und Neutronen entspricht
Atom Der Begriff Atom leitet sich von atomos her, was unteilbar heisst. Diese Definition ist alt, da man heutzutage fähig ist, Atome zu teilen. Atommassenzahl Die Anzahl der Protonen und Neutronen entspricht
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 5: )
 Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Ionenbindungen. Chemie. Library
 Chemie Ionenbindungen Library IONENBINDUNGEN Begriffserklärung 1 Formeltabelle 1 Ladungsermittlung 2 Formale Ladung 3 Hydrogen-Ionen 3 Verhältnisformeln 4 Nomenklatur 4 Gitterenthalpie 4 Eigenschaften
Chemie Ionenbindungen Library IONENBINDUNGEN Begriffserklärung 1 Formeltabelle 1 Ladungsermittlung 2 Formale Ladung 3 Hydrogen-Ionen 3 Verhältnisformeln 4 Nomenklatur 4 Gitterenthalpie 4 Eigenschaften
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie
 Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Besetzung der Orbitale
 Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Übungsaufgaben zur Kristallographie Serie 9 LÖSUNG
 Chemische Bindung - Struktur - Physikalische Eigenschaften Für diese Aufgabe benötigen Sie das Programm VESTA. Sie finden es im Internet unter http://jp-minerals.org/vesta. Laden Sie die Kristallstrukturen
Chemische Bindung - Struktur - Physikalische Eigenschaften Für diese Aufgabe benötigen Sie das Programm VESTA. Sie finden es im Internet unter http://jp-minerals.org/vesta. Laden Sie die Kristallstrukturen
Darstellungstheorie Näherungsverfahren Messprozess Streutheorie Dirac-Glg.
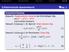 5 Relativistische Quantentheorie Kap. 5 Zusammenfassung Gesucht: Relativistische Variante der Schrödinger-Glg. mit E 2 = p 2 c 2 + m 2 c 4 und Lorentz-Invarianz Versuch 2 (Lösung 1, für Spin-0: Klein-Gordon-Glg.
5 Relativistische Quantentheorie Kap. 5 Zusammenfassung Gesucht: Relativistische Variante der Schrödinger-Glg. mit E 2 = p 2 c 2 + m 2 c 4 und Lorentz-Invarianz Versuch 2 (Lösung 1, für Spin-0: Klein-Gordon-Glg.
Mit seinen vier Valenzelektronen ist das Kohlenstoffatom in der Lage, Einfach-, Doppel- und Dreifachbindungen auszubilden:
 KOLENSTOFF-MODIFIKATIONEN - 1 - Der Kohlenstoff Mit seinen vier Valenzelektronen ist das Kohlenstoffatom in der Lage, Einfach-, Doppel- und Dreifachbindungen auszubilden: 6 4 2 Ein abgeschlossenes Kohlenstoffmolekül
KOLENSTOFF-MODIFIKATIONEN - 1 - Der Kohlenstoff Mit seinen vier Valenzelektronen ist das Kohlenstoffatom in der Lage, Einfach-, Doppel- und Dreifachbindungen auszubilden: 6 4 2 Ein abgeschlossenes Kohlenstoffmolekül
VL 21 VL Periodensystem VL Röntgenstrahlung VL Homonukleare Moleküle VL Heteronukleare Moleküle
 VL 21 VL 19 20.1. Periodensystem VL 20 21.1. Röntgenstrahlung VL 21 22.1. Homonukleare Moleküle VL 22 23.1. Heteronukleare Moleküle Wim de Boer, Karlsruhe Atome und Moleküle, 02.07.2013 1 Vorlesung 22:
VL 21 VL 19 20.1. Periodensystem VL 20 21.1. Röntgenstrahlung VL 21 22.1. Homonukleare Moleküle VL 22 23.1. Heteronukleare Moleküle Wim de Boer, Karlsruhe Atome und Moleküle, 02.07.2013 1 Vorlesung 22:
Grundpraktikum für Biologen 2016
 Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
F Das Periodensystem. Allgemeine Chemie 26
 Allgemeine Chemie 6 F Das Periodensystem Aufgestellt von Mendelejew und Meyer 1869 (rein empirisch!) Perioden in Zeilen: mit jeder Periode erhöht sich die auptquantenzahl der äußeren Schale (s-rbital)
Allgemeine Chemie 6 F Das Periodensystem Aufgestellt von Mendelejew und Meyer 1869 (rein empirisch!) Perioden in Zeilen: mit jeder Periode erhöht sich die auptquantenzahl der äußeren Schale (s-rbital)
Graphen. Kristin Kliemt, Carsten Neumann
 Graphen Kristin Kliemt, Carsten Neumann 18.01.2012 1 Gliederung Kohlenstoffmodifikationen (Diamant, Graphit, Graphen) Stabilität und Struktur Dispersionsrelation Eigenschaften und Herstellung von Graphen
Graphen Kristin Kliemt, Carsten Neumann 18.01.2012 1 Gliederung Kohlenstoffmodifikationen (Diamant, Graphit, Graphen) Stabilität und Struktur Dispersionsrelation Eigenschaften und Herstellung von Graphen
3. Wieviel bindig sind folgende Elemente in kovalenten Bindungen? Einige Elemente können auch verschiedene Bindigkeiten zeigen
 Übungen zur VL Chemie für Biologen und umanbiologen 26. 11.2010 1. ennen Sie mindestens 2 Arten der chemischen Bindungen und geben Sie je 2 Beispielverbindungen dafür an (Strukturformel). 1) Ionische Bindung:
Übungen zur VL Chemie für Biologen und umanbiologen 26. 11.2010 1. ennen Sie mindestens 2 Arten der chemischen Bindungen und geben Sie je 2 Beispielverbindungen dafür an (Strukturformel). 1) Ionische Bindung:
Theoretical Biophysics - Quantum Theory and Molecular Dynamics. 10. Vorlesung. Pawel Romanczuk WS 2016/17
 Theoretical Biophysics - Quantum Theory and Molecular Dynamics 10. Vorlesung Pawel Romanczuk WS 2016/17 http://lab.romanczuk.de/teaching Zusammenfassung letzte VL Der Spin Grundlegende Eigenschaften Spin
Theoretical Biophysics - Quantum Theory and Molecular Dynamics 10. Vorlesung Pawel Romanczuk WS 2016/17 http://lab.romanczuk.de/teaching Zusammenfassung letzte VL Der Spin Grundlegende Eigenschaften Spin
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen V Molkülorbitaltheorie I
 Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen V Molkülorbitaltheorie I MO-Theorie: Molekülorbitale durch Linearkombinationen von Atomorbitalen (LCAO-Methode: Linear Combination
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen V Molkülorbitaltheorie I MO-Theorie: Molekülorbitale durch Linearkombinationen von Atomorbitalen (LCAO-Methode: Linear Combination
(2.65 ev), da sich die beiden Elektronen gegenseitig abstossen.
 phys4.026 Page 1 13.8 Das Wasserstoff-Molekül Wie im Fall des H2 + Moleküls führen im H2 Molekül symmetrische Wellenfunktionen zu bindenden Zuständen, wohingegen anti-symmetrische Wellenfunktionen zu anti-bindenden
phys4.026 Page 1 13.8 Das Wasserstoff-Molekül Wie im Fall des H2 + Moleküls führen im H2 Molekül symmetrische Wellenfunktionen zu bindenden Zuständen, wohingegen anti-symmetrische Wellenfunktionen zu anti-bindenden
Grundwissen Chemie 8. Klasse NTG
 Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
Chemie-Grundwissen der 9.Klasse
 Chemie-Grundwissen der 9.Klasse Stoffebene = Makroskopische (sichtbare) Ebene Betrachtung einer Stoffportion mit den erkennbaren und messbaren Eigenschaften Teilchenebene = Submikroskopische Ebene Betrachtung
Chemie-Grundwissen der 9.Klasse Stoffebene = Makroskopische (sichtbare) Ebene Betrachtung einer Stoffportion mit den erkennbaren und messbaren Eigenschaften Teilchenebene = Submikroskopische Ebene Betrachtung
Zeitaufgelöste Abbildung der Kern- und Elektronenbewegung auf der Femto- und Attosekundenskala
 Zeitaufgelöste Abbildung der Kern- und Elektronenbewegung auf der Femto- und Attosekundenskala Simon Birkholz 26. Mai 2010 S. Birkholz 1 / 25 Inhalt 1 Einführung und Motivation 2 High-Harmonic Generation
Zeitaufgelöste Abbildung der Kern- und Elektronenbewegung auf der Femto- und Attosekundenskala Simon Birkholz 26. Mai 2010 S. Birkholz 1 / 25 Inhalt 1 Einführung und Motivation 2 High-Harmonic Generation
Physik 4: Skalen und Strukturen
 Physik 4: Skalen und Strukturen Kapitel : Festkörperphysik.1 Aggregatszustände. Kristallstrukturen.3 Chemische Bindung.4 Gitterschwingungen.5 Elektronen im Festkörper Phasendiagramm von CO Klassisches
Physik 4: Skalen und Strukturen Kapitel : Festkörperphysik.1 Aggregatszustände. Kristallstrukturen.3 Chemische Bindung.4 Gitterschwingungen.5 Elektronen im Festkörper Phasendiagramm von CO Klassisches
VL 22 VL Homonukleare Moleküle VL Heteronukleare Moleküle VL Molekülschwingungen
 VL 22 VL 21 21.1. Homonukleare Moleküle VL 22 22.1. Heteronukleare Moleküle VL 23 23.1. Molekülschwingungen Wim de Boer, Karlsruhe Atome und Moleküle, 04.07.2013 1 Zum Mitnehmen Moleküle: Wellenfunktion
VL 22 VL 21 21.1. Homonukleare Moleküle VL 22 22.1. Heteronukleare Moleküle VL 23 23.1. Molekülschwingungen Wim de Boer, Karlsruhe Atome und Moleküle, 04.07.2013 1 Zum Mitnehmen Moleküle: Wellenfunktion
1 Einleitung. Einleitung 1
 Einleitung 1 1 Einleitung Die Supramolekulare Chemie ist die Chemie der intermolekularen Bindung. Sie beschäftigt sich mit Strukturen und Funktionen von Einheiten, die durch Assoziation zweier oder mehrerer
Einleitung 1 1 Einleitung Die Supramolekulare Chemie ist die Chemie der intermolekularen Bindung. Sie beschäftigt sich mit Strukturen und Funktionen von Einheiten, die durch Assoziation zweier oder mehrerer
Atomaufbau. Elektronen e (-) Atomhülle
 Atomaufbau Institut für Elementarteilchen Nukleonen Protonen p (+) Neutronen n (o) Elektronen e (-) Atomkern Atomhülle Atom WIBA-NET 2005 Prof. Setzer 1 Elementarteilchen Institut für Name Symbol Masse
Atomaufbau Institut für Elementarteilchen Nukleonen Protonen p (+) Neutronen n (o) Elektronen e (-) Atomkern Atomhülle Atom WIBA-NET 2005 Prof. Setzer 1 Elementarteilchen Institut für Name Symbol Masse
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie Das komplette Material finden Sie hier: Download bei School-Scout.de B201 LÖSUNG:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie Das komplette Material finden Sie hier: Download bei School-Scout.de B201 LÖSUNG:
E4 - Physik kondensierter Materie Mitschrift zur Vorlesung von Prof. Bogdan Sepiol und Prof. Gero Vogl
 E4 - Physik kondensierter Materie Mitschrift zur Vorlesung von Prof. Bogdan Sepiol und Prof. Gero Vogl Markus Drapalik und Bernhard Reiter Version vom 14.03.2006 Einleitung Literatur: Kittel, Charles:...,
E4 - Physik kondensierter Materie Mitschrift zur Vorlesung von Prof. Bogdan Sepiol und Prof. Gero Vogl Markus Drapalik und Bernhard Reiter Version vom 14.03.2006 Einleitung Literatur: Kittel, Charles:...,
Opto-elektronische. Materialeigenschaften VL # 3
 Opto-elektronische Materialeigenschaften VL # 3 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und Bayerisches Zentrum für Angewandte
Opto-elektronische Materialeigenschaften VL # 3 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und Bayerisches Zentrum für Angewandte
Grundwissenkarten Hans-Carossa-Gymnasium. 9. Klasse. Chemie SG
 Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
GRUNDWISSEN CHEMIE 8. KLASSE
 GRUDWISSE CEMIE 8. KLASSE (LS Marquartstein September 2013) 2006 Wagner/Gottschalk LS Marquartstein 1 I. Stoffe und Reaktionen: Physikalische Vorgänge sind begleitet von Energieumwandlungen (Wärme- Licht-
GRUDWISSE CEMIE 8. KLASSE (LS Marquartstein September 2013) 2006 Wagner/Gottschalk LS Marquartstein 1 I. Stoffe und Reaktionen: Physikalische Vorgänge sind begleitet von Energieumwandlungen (Wärme- Licht-
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Hier: Beschränkung auf die elektrische Eigenschaften
 IV. Festkörperphysik Hier: Beschränkung auf die elektrische Eigenschaften 3 Aggregatzustände: fest, flüssig, gasförmig: Wechselspiel Anziehungskräfte der Teilchen gegen die thermische Energie kt. Zustand
IV. Festkörperphysik Hier: Beschränkung auf die elektrische Eigenschaften 3 Aggregatzustände: fest, flüssig, gasförmig: Wechselspiel Anziehungskräfte der Teilchen gegen die thermische Energie kt. Zustand
Vorlesung 20+21: Folien auf dem Web:
 Vorlesung 20+21: Roter Faden: Mehratomige Moleküle Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: http://www.wmi.badw.de/teaching/lecturenotes/index.html und Alonso-Finn:
Vorlesung 20+21: Roter Faden: Mehratomige Moleküle Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: http://www.wmi.badw.de/teaching/lecturenotes/index.html und Alonso-Finn:
Opto-elektronische. Materialeigenschaften VL # 4
 Opto-elektronische Materialeigenschaften VL # 4 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und Bayerisches Zentrum für Angewandte
Opto-elektronische Materialeigenschaften VL # 4 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und Bayerisches Zentrum für Angewandte
CHEMIE KAPITEL 1 AUFBAU DER MATERIE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2014 / 2015
 CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Valenzelektronen und Atomeigenschaften Valenzelektronen (Außenelektronen) bestimmen
CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Valenzelektronen und Atomeigenschaften Valenzelektronen (Außenelektronen) bestimmen
Robert-Koch-Gymnasium Deggendorf. Grundwissen Chemie. 8. Jahrgangsstufe
 Robert-Koch-Gymnasium Deggendorf Grundwissen Chemie 8. Jahrgangsstufe Teilchenmodell und Stoffeigenschaften Teilchenmodell: Alle Stoffe bestehen aus kleinsten Teilchen, vereinfacht dargestellt als Kugeln.
Robert-Koch-Gymnasium Deggendorf Grundwissen Chemie 8. Jahrgangsstufe Teilchenmodell und Stoffeigenschaften Teilchenmodell: Alle Stoffe bestehen aus kleinsten Teilchen, vereinfacht dargestellt als Kugeln.
0.6 Einfache Modelle der chemischen Bindung
 0.6 Einfache Modelle der chemischen Bindung Ionenbindung Ionenbindungen entstehen durch Reaktion von ausgeprägt metallischen Elementen (Alkalimetalle und Erdalkalimetalle mit geringer Ionisierungsenergie)
0.6 Einfache Modelle der chemischen Bindung Ionenbindung Ionenbindungen entstehen durch Reaktion von ausgeprägt metallischen Elementen (Alkalimetalle und Erdalkalimetalle mit geringer Ionisierungsenergie)
ElektronischeBandstruktur
 ElektronischeBandstruktur Literatur: C. Kittel Einführungin die Festkörperphysik Kapitel 7,8 Ashcroft & Mermin, Kapitel 7,8 Ziman Principles of the Theory of solids, Kapitel 3 Dispersionsrelation für
ElektronischeBandstruktur Literatur: C. Kittel Einführungin die Festkörperphysik Kapitel 7,8 Ashcroft & Mermin, Kapitel 7,8 Ziman Principles of the Theory of solids, Kapitel 3 Dispersionsrelation für
Vorlesung Anorganische Chemie
 Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 4 Molekülstruktur Ausnahmen von der Oktettregel Hypervalente Verbindungen VSEPR Hybridisierung Molekülorbitale
Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 4 Molekülstruktur Ausnahmen von der Oktettregel Hypervalente Verbindungen VSEPR Hybridisierung Molekülorbitale
Organische Chemie. Kapitel 1. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Organische Verbindungen enthalten Kohlenstoff
 rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
Chemie für Biologen SS Georg Jansen AG Theoretische Organische Chemie Universität Duisburg Essen. (Teil 3: Kovalente Bindungen)
 Chemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische Chemie Universität Duisburg Essen (Teil 3: Kovalente Bindungen) (3) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung
Chemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische Chemie Universität Duisburg Essen (Teil 3: Kovalente Bindungen) (3) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Fortgeschrittene Experimentalphysik für Lehramtsstudierende
 Fortgeschrittene Experimentalphysik für Lehramtsstudierende Teil I Festkörperphysik Elizabeth von Hauff Organic Photovoltaics & Electronics Hochhaus 401 elizabeth.von.hauff@physik.uni-freiburg.de Teil
Fortgeschrittene Experimentalphysik für Lehramtsstudierende Teil I Festkörperphysik Elizabeth von Hauff Organic Photovoltaics & Electronics Hochhaus 401 elizabeth.von.hauff@physik.uni-freiburg.de Teil
Clusterphysik. Moderne Molekülphysik SS 2013
 Clusterphysik Moderne Molekülphysik SS 2013 Michael Martins michael.martins@desy.de Folien werden im WWW bereitgestellt Vorlesung im Diplom und Masterstudiengang Insgesamt 5 LP 2 SWS Vorlesung, Mittwoch
Clusterphysik Moderne Molekülphysik SS 2013 Michael Martins michael.martins@desy.de Folien werden im WWW bereitgestellt Vorlesung im Diplom und Masterstudiengang Insgesamt 5 LP 2 SWS Vorlesung, Mittwoch
Technische Universität Chemnitz
 Leitfähige Nanoskalierte und elektrisch leitende Organika Rudolf Holze Institut für Chemie, Technische Universität Chemnitz, D09107 Chemnitz http://www.tuchemnitz.de/chemie/elchem Westsächsische Hochschule
Leitfähige Nanoskalierte und elektrisch leitende Organika Rudolf Holze Institut für Chemie, Technische Universität Chemnitz, D09107 Chemnitz http://www.tuchemnitz.de/chemie/elchem Westsächsische Hochschule
Grundtypen der Bindung. Grundtypen chemischer Bindung. Oktettregel. A.8.1. Atombindung
 Grundtypen der Bindung Grundtypen chemischer Bindung Oktettregel A.8.1. Atombindung 1 A.8.1 Atombindung Valenz (Zahl der Bindungen) Atombindung auch: kovalente Bindung, ElektronenpaarBindung Zwei Atome
Grundtypen der Bindung Grundtypen chemischer Bindung Oktettregel A.8.1. Atombindung 1 A.8.1 Atombindung Valenz (Zahl der Bindungen) Atombindung auch: kovalente Bindung, ElektronenpaarBindung Zwei Atome
Anorganische Chemie III
 Seminar zu Vorlesung Anorganische Chemie III Wintersemester 01/13 Christoph Wölper Universität Duisburg-Essen Koordinationszahlen Ionenradien # dichteste Packung mit 1 Nachbarn -> in Ionengittern weniger
Seminar zu Vorlesung Anorganische Chemie III Wintersemester 01/13 Christoph Wölper Universität Duisburg-Essen Koordinationszahlen Ionenradien # dichteste Packung mit 1 Nachbarn -> in Ionengittern weniger
Anorganische Chemie III - Festkörperchemie
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Festkörperchemie
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Festkörperchemie
Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch. Reinstoff, Element, Verbindung. Zweiatomige Elemente.
 Einteilung der Stoffe: Stoff Reinstoff Mischen Gemisch Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b. Farbe,
Einteilung der Stoffe: Stoff Reinstoff Mischen Gemisch Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b. Farbe,
Einführung in die Struktur der Materie. Studierende des Lehramtes und des Nebenfachs SS 2013
 Einführung in die Struktur der Materie für Studierende des Lehramtes und des Nebenfachs SS 2013 Michael Martins und Erika Garutti Inhalt Einleitung Teil A (M. Martins): I. Molekülphysik II. Festkörperphysik
Einführung in die Struktur der Materie für Studierende des Lehramtes und des Nebenfachs SS 2013 Michael Martins und Erika Garutti Inhalt Einleitung Teil A (M. Martins): I. Molekülphysik II. Festkörperphysik
Grundwissen C8 NTG. 1. Stoffe und Reaktionen. Reinstoff
 Grundwissen C8 NTG 1. Stoffe und Reaktionen Reinstoff Stoffgemisch - besitzt unter bestimmten Bedingungen (z.b. Temperatur, Druck ) kennzeichnende Eigenschaften, z.b. Farbe, Geruch, Geschmack, Dichte,
Grundwissen C8 NTG 1. Stoffe und Reaktionen Reinstoff Stoffgemisch - besitzt unter bestimmten Bedingungen (z.b. Temperatur, Druck ) kennzeichnende Eigenschaften, z.b. Farbe, Geruch, Geschmack, Dichte,
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Vorlesung 20+21: Folien auf dem Web:
 Vorlesung 20+21: Roter Faden: Mehratomige Moleküle Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: http://www.wmi.badw.de/teaching/lecturenotes/index.html und Alonso-Finn:
Vorlesung 20+21: Roter Faden: Mehratomige Moleküle Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: http://www.wmi.badw.de/teaching/lecturenotes/index.html und Alonso-Finn:
Einführung in die Quantentheorie der Atome und Photonen
 Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Wechselwirkungen zwischen Atomen Was bisher geschah Quantenmechanisches
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Wechselwirkungen zwischen Atomen Was bisher geschah Quantenmechanisches
Lehrseminar B: Kurzpulslaser und Anwendung. Ultraschnelle Prozesse in der FEMTOCHEMIE. von Alexander Kaebe
 Lehrseminar B: Kurzpulslaser und Anwendung Ultraschnelle Prozesse in der FEMTOCHEMIE von Alexander Kaebe Inhalt l Einführung l Experimenteller Aufbau l Ultraschnelle Prozesse in der Femtochemie l Steuerung
Lehrseminar B: Kurzpulslaser und Anwendung Ultraschnelle Prozesse in der FEMTOCHEMIE von Alexander Kaebe Inhalt l Einführung l Experimenteller Aufbau l Ultraschnelle Prozesse in der Femtochemie l Steuerung
Die kovalente Bindung
 Die kovalente Bindung Atome, die keine abgeschlossene Elektronenschale besitzen, können über eine kovalente Bindung dieses Ziel erreichen. Beispiel: 4 H H + C H H C H H Die Wasserstoffatome erreichen damit
Die kovalente Bindung Atome, die keine abgeschlossene Elektronenschale besitzen, können über eine kovalente Bindung dieses Ziel erreichen. Beispiel: 4 H H + C H H C H H Die Wasserstoffatome erreichen damit
Tabelle: Kristalle - Übesicht und Klassifikation
 Tabelle: Kristalle - Übesicht und Klassifikation Kristall- / Bindungstypen A-A Beispiele A-B Wechselwirkung (attraktive Terme) attraktives Potential E bin (ev) R 0 (Å) T schm (K) 1) Edelgaskristall, Molekülkristall
Tabelle: Kristalle - Übesicht und Klassifikation Kristall- / Bindungstypen A-A Beispiele A-B Wechselwirkung (attraktive Terme) attraktives Potential E bin (ev) R 0 (Å) T schm (K) 1) Edelgaskristall, Molekülkristall
Chemie Zusammenfassung III
 Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Physik Organischer Halbleiter:
 Physik Organischer Halbleiter: Opto- und Mikroelektronik, Photovoltaik, Sensorik Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und
Physik Organischer Halbleiter: Opto- und Mikroelektronik, Photovoltaik, Sensorik Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und
Physik Organischer Halbleiter:
 Physik Organischer Halbleiter: Opto- und Mikroelektronik, Photovoltaik, Sensorik Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und
Physik Organischer Halbleiter: Opto- und Mikroelektronik, Photovoltaik, Sensorik Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Experimental Physics VI, Julius-Maximilians-University of Würzburg und
Allotrope Kohlenstoffmodifikationen. Ein Vortrag von Patrick Knicknie. Datum: 04.05.06 Raum:112
 Allotrope Kohlenstoffmodifikationen Ein Vortrag von Patrick Knicknie Datum: 04.05.06 Raum:112 Themen: 1. Was ist Allotrop? 2. Unterschiedliche Kohlenstoffmodifikationen 3. Der Graphit 4. Der Diamant 5.
Allotrope Kohlenstoffmodifikationen Ein Vortrag von Patrick Knicknie Datum: 04.05.06 Raum:112 Themen: 1. Was ist Allotrop? 2. Unterschiedliche Kohlenstoffmodifikationen 3. Der Graphit 4. Der Diamant 5.
Learn4Med. Es gibt in der Chemie drei verschiedene Arten von Bindungen: Metallische Bindung: zwischen zwei Metallen, es entsteht ein Metall
 6. Chemische Bindung Es gibt in der Chemie drei verschiedene Arten von Bindungen: Metallische Bindung: zwischen zwei Metallen, es entsteht ein Metall Atombindung: zwischen zwei Nichtmetallen, es entsteht
6. Chemische Bindung Es gibt in der Chemie drei verschiedene Arten von Bindungen: Metallische Bindung: zwischen zwei Metallen, es entsteht ein Metall Atombindung: zwischen zwei Nichtmetallen, es entsteht
4.Teil Kovalente Bindung
 4.Teil Kovalente Bindung Lewis-Konzept, Valenstrichformel, Oktettregel Polare Elektronenpaarbindung und Elektronegativität Gebrochene Bindungsordnung und Mesomerie Valenzschalen-Elektronenpaar-Abstoßungsmodell
4.Teil Kovalente Bindung Lewis-Konzept, Valenstrichformel, Oktettregel Polare Elektronenpaarbindung und Elektronegativität Gebrochene Bindungsordnung und Mesomerie Valenzschalen-Elektronenpaar-Abstoßungsmodell
Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten oder in Festkörpern vor.
 phys4.025 Page 1 13. Moleküle Nur eine kleine Anzahl von Elementen kommt natürlich in Form von einzelnen Atomen vor. Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten
phys4.025 Page 1 13. Moleküle Nur eine kleine Anzahl von Elementen kommt natürlich in Form von einzelnen Atomen vor. Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
1. Bedeutung der Oxidationszahlen
 1. Bedeutung der Oxidationszahlen Unterschiedliche Atome geben eine unterschiedliche Zahl an Elektronen ab: Dann hat das Atom eine positive Oxidationsstufe; das Atom ist mit weniger Elektronen als Protonen
1. Bedeutung der Oxidationszahlen Unterschiedliche Atome geben eine unterschiedliche Zahl an Elektronen ab: Dann hat das Atom eine positive Oxidationsstufe; das Atom ist mit weniger Elektronen als Protonen
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Chemische Bindungen, starke, schwache Bindungen, Elektronenpaarbindung, bindende und freie Elektronenpaare, Oktettregel, Edelgaskonfiguration, Lewis-Formeln,
Wiederholung der letzten Vorlesungsstunde: Chemische Bindungen, starke, schwache Bindungen, Elektronenpaarbindung, bindende und freie Elektronenpaare, Oktettregel, Edelgaskonfiguration, Lewis-Formeln,
Thema heute: Chemische Bindungen, Teil I
 Wiederholung der letzten Vorlesungsstunde: Periodensystem, Anordnung der Elemente nach steigender Ordnungszahl, Hauptgruppen, Nebengruppen, Lanthanoide + Actinoide, Perioden, Döbereiner, Meyer, Medelejew
Wiederholung der letzten Vorlesungsstunde: Periodensystem, Anordnung der Elemente nach steigender Ordnungszahl, Hauptgruppen, Nebengruppen, Lanthanoide + Actinoide, Perioden, Döbereiner, Meyer, Medelejew
Allotrope Kohlenstoffmodifikationen
 Übersicht Was ist Allotropie? Graphit Diamant Lonsdaleit Fullerene Carbon Nanotubes 2 Allotropie unterschiedliche Modifikationen eines Elements unterschiedliche physikalische und chemische Eigenschaften
Übersicht Was ist Allotropie? Graphit Diamant Lonsdaleit Fullerene Carbon Nanotubes 2 Allotropie unterschiedliche Modifikationen eines Elements unterschiedliche physikalische und chemische Eigenschaften
Photonische Materialien 10. Vorlesung
 Photonische Materialien 10. Vorlesung Einführung in quantenmechanische Aspekte und experimentelle Verfahren (1) Lumineszenz-Label (1) Supramolekulare und biologische Systeme (1) Halbleiter Nanopartikel
Photonische Materialien 10. Vorlesung Einführung in quantenmechanische Aspekte und experimentelle Verfahren (1) Lumineszenz-Label (1) Supramolekulare und biologische Systeme (1) Halbleiter Nanopartikel
Kristallchemie. Atome Ionen Moleküle Chemische Bindungen
 Kristallchemie Atome Ionen Moleküle Chemische Bindungen Metalle, Metalloide, Nichtmetalle Metalle: E-neg < 1.9 - e - Abgabe Kationen Nichtmetalle: E-neg > 2.1 - e - Aufnahme Anionen Metalloide: B, Si,
Kristallchemie Atome Ionen Moleküle Chemische Bindungen Metalle, Metalloide, Nichtmetalle Metalle: E-neg < 1.9 - e - Abgabe Kationen Nichtmetalle: E-neg > 2.1 - e - Aufnahme Anionen Metalloide: B, Si,
Festkörper. Festkörper
 Festkörper Einteilung der Materie in drei Aggregatszustände: fest, flüssig, gasförmig Unterscheidung Festkörper behält seine Form Nachteil: Ungenaue Abgrenzung Beispiel: Ist Butter Festkörper oder Flüssigkeit
Festkörper Einteilung der Materie in drei Aggregatszustände: fest, flüssig, gasförmig Unterscheidung Festkörper behält seine Form Nachteil: Ungenaue Abgrenzung Beispiel: Ist Butter Festkörper oder Flüssigkeit
PHYSIK. Studienbrief Moleküle. AUTOR: Dr. Johannes Bernardi
 PHYSIK AUTOR: Dr. Johannes Bernardi Inhalt: 1 Einführung...3 2 Ionenbindung (heteropolare Bindung): A + B...4 3 Kovalente Bindung (chemische Bindung): AB...6 4 Van der Waals Bindung...7 5 Wasserstoffbindung...8
PHYSIK AUTOR: Dr. Johannes Bernardi Inhalt: 1 Einführung...3 2 Ionenbindung (heteropolare Bindung): A + B...4 3 Kovalente Bindung (chemische Bindung): AB...6 4 Van der Waals Bindung...7 5 Wasserstoffbindung...8
Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt
 Atom- und Molekülbau Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt Von Peter C. Schmidt und Konrad G. Weil 147 Abbildungen, 19 Tabellen Georg Thieme Verlag Stuttgart New York 1982 Vorwort
Atom- und Molekülbau Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt Von Peter C. Schmidt und Konrad G. Weil 147 Abbildungen, 19 Tabellen Georg Thieme Verlag Stuttgart New York 1982 Vorwort
Übungen zur Vorlesung Physikalische Chemie II Lösungsvorschlag zu Blatt 5
 Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Keine Welt ohne explodierende Sterne. Bruno Leibundgut Europäische Südsternwarte (ESO)
 Keine Welt ohne explodierende Sterne Bruno Leibundgut Europäische Südsternwarte (ESO) Alter der Alpen Entstanden vor etwa 30 bis 35 Millionen Jahren Dinosaurier haben die Alpen nie gekannt! (vor 65 Millionen
Keine Welt ohne explodierende Sterne Bruno Leibundgut Europäische Südsternwarte (ESO) Alter der Alpen Entstanden vor etwa 30 bis 35 Millionen Jahren Dinosaurier haben die Alpen nie gekannt! (vor 65 Millionen
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle
 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
2.4. Atome mit mehreren Elektronen
 2.4. Atome mit mehreren Elektronen 2.4.1. Das Heliumatom Wellenfunktion für das Heliumatom Nach dem Wasserstoffatom ist das Heliumatom das nächst einfachere Atom. Das Heliumatom besitzt einen Kern der
2.4. Atome mit mehreren Elektronen 2.4.1. Das Heliumatom Wellenfunktion für das Heliumatom Nach dem Wasserstoffatom ist das Heliumatom das nächst einfachere Atom. Das Heliumatom besitzt einen Kern der
