STICKSTOFF-STOFFWECHSEL
|
|
|
- Gerhard Reuter
- vor 7 Jahren
- Abrufe
Transkript
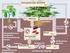
1 5 STICKSTOFF-STOFFWECHSEL BIOCHEMISCHE GRUNDLAGEN HARNSTOFFZYKLUS Beim Abbau von Aminosäuren und anderen stickstoffhaltigen Verbindungen entsteht Ammoniak. Ammoniak in höheren Konzentrationen (>50 µmol/l) ist eine äußerst toxische Substanz. Soweit das entstehende Ammoniak nicht für die Biosynthese anderer stickstoffhaltiger Verbindungen gebraucht wird, erfolgt Einbau von Ammoniak in Harnstoff. Auf diese Weise wird Ammoniak in eine nichttoxische Verbindung überführt. Nur die Leber besitzt eine enzymatische Ausstattung für eine vollständige und bedeutsame Bildung von Harnstoff. Ammoniak kann auch unverändert über die Niere ausgeschieden werden. Bei der Bildung von Harnstoff handelt es sich um eine zyklische Reaktionsfolge, die als Harnstoffzyklus bezeichnet wird. Im Verlauf des Harnstoffzyklus wird Harnstoff aus einem Molekül Ammoniak und Bicarbonat sowie aus dem -Aminostickstoff von Aspartat zusammengesetzt. Eine der Reaktionen, bei welcher in der Leber ein erheblicher Anteil an Ammoniak entsteht, ist die NAD + -abhängige oxydative Desaminierung von Glutamat. Das Enzym Carbamylphosphat-Synthetase (in Gegenwart von N-Acetylglutamat als allosterischem Aktivator) katalysiert die Bildung von Carbamylphosphat aus Ammoniak und Bicarbonat unter Verbrauch von zwei Molekülen ATP (Abb. 1). Diese Reaktion läuft in den Mitochondrien der Hepatozyten ab. Vom Carbamylphosphat wird die Carbamyl-Gruppe auf Ornithin unter Bildung von Citrullin und Freisetzung von Phosphat übertragen. Diese Reaktion wird durch das Enzym Ornithin-Transcarbamylase katalysiert. Citrullin wird aus den Mitochondrien in das Zytosol transportiert. Eine zweite Aminogruppe wird durch Aspartat in den Zyklus eingeschleust. Die Aminogruppe von Asparatat kondensiert mit der Carbonylgruppe des Citrullins, wobei Argininosuccinat entsteht. Diese Reaktion erfordert ein Molekül ATP und als Enzym Argininosuccinat-Synthetase. Argininosuccinat wird durch Argininosuccinatlyase in Fumarsäure und Arginin gespalten. Harnstoffausscheidende Organismen besitzen eine hohe Aktivität des Enzyms Arginase, durch dessen Wirkung Arginin hydrolytisch in Harnstoff und Ornithin gespalten wird; das Gleichgewicht liegt weit auf der Seite von Harnstoff und Ornithin. Der Harnstoff wird ausgeschieden, während das Ornithin wieder in die Mitochondrien transportiert wird.
2 6 Die Biosynthese eines Moleküls Harnstoff nach der Gleichung 2 NH 3 + HCO ATP CO(NH 2 ) ADP + AMP + 4 P i erfordert 3 Moleküle ATP bzw. die Spaltung von vier energiereichen Bindungen. Dabei sind die Energetik der Biosynthese des Aspartats aus Fumarat und die Transportvorgänge durch die Mitochondrienmembran noch nicht berücksichtigt. In folgenden Versuchen wird die Harnstoffsynthese in Leberextrakten untersucht. Ausgehend von verschiedenen Zwischen- und Vorprodukten des Kreisprozesses wird die Bildung von Harnstoff nachgewiesen. Dieser wird quantitativ bestimmt. Daraus wird die spezifische enzymatische Aktivität errechnet. Abb. 1: Harnstoffbiosynthese Enzyme: 1 = Carbamylphosphat-Synthetase I 2 = Ornithin-Carbamyl-Transferase 3 = Argininosuccinat-Synthetase 4 = Argininosuccinat-Lyase 5 = Arginase
3 7 AMINOTRANSFERASEN (TRANSAMINASEN) Für die Einschleusung von Aminogruppen in den Harnstoffzyklus müssen diese entweder in Form von Aspartat zugeführt werden oder aber als Ammoniak aus Aminosäuren abgespalten werden (z.b. durch die Glutamatdehydrogenase-Reaktion aus Glutamat). Damit haben Aminotransferasen, die zur Bildung von Glutamat führen, eine besondere Bedeutung im Stoffwechsel (Abb. 2). (Transaminasen ist eine ältere aber immer noch verwendete Bezeichnung für Aminotransferasen). Aminotransferasen übertragen mit Hilfe von Pyridoxalphosphat als Coenzym reversibel die Aminogruppe einer Aminosäure 1 auf eine -Ketosäure 2 unter Bildung der -Ketosäure 1 und der Aminosäure 2 (Mechanismus siehe Lehrbücher). Aminosäure 1 + -Ketosäure 2 -Ketosäure 1 + Aminosäure 2 Eines dieser Enzyme ist die Alanin-Aminotransferase ALT (frühere Bezeichnung Glutamat- Pyruvat-Transaminase GPT). Sie übernimmt den Aminogruppentransfer von Alanin auf - Ketoglutarat unter Bildung von Pyruvat und Glutamat. Eine zweite wichtige Aminotransferase ist die Aspartat-Aminotransferase AST (früher Glutamat-Oxalacetat-Transaminase GOT). Sie benutzt Glutamat und Oxalacetat als Substrate und führt zur Bereitstellung von -Ketoglutarat und Aspartat. Dieses kann dann zur Harnstoffsynthese verwendet werden. Bestimmung von ALT und AST (GPT und GOT) hat im klinisch-chemischen Labor eine praktische Bedeutung. Erhöhte Aktivitäten dieser Enzyme im Serum deuten auf Organschädigungen, wie Herzinfarkt oder Erkrankungen der Leber (Leberzirrhose, Hepatitis) hin. Aus dem Verhältnis der enzymatischen Aktivitäten von AST (GOT) und ALT (GPT) im Serum kann auf das geschädigte Organ geschlossen werden: In der Leber findet sich hauptsächlich ALT, während im Herzmuskel und Skelettmuskel AST und ALT in annähernd gleich hohen Aktivitäten vorkommen. Abb. 2 Aminotransferasen im Stoffwechsel
4 8
5 9 ALLGEMEINE FRAGESTELLUNGEN Welche energiereichen (Ver)bindungen kommen im Harnstoffzyklus vor? Um welchen chemischen Bindungstyp handelt es sich dabei? Für welche Biosynthese wird sonst noch Carbamylphosphat benötigt? Durch welche Reaktionen werden Aminogruppen aus Aminosäuren als Ammoniak abgespalten? Durch welche Reaktionen im Stoffwechsel wird Ammoniak gebunden? Kommen die Aminosäuren Ornithin, Citrullin und Arginin in Proteinen vor? Worin besteht eine Wechselbeziehung zwischen Harnstoffzyklus und Citratzyklus? Welche klinischen Symptome beobachtet man bei Enzymdefekten des Harnstoffzyklus (genetisch bedingt oder erworben)? Wie lassen sich diese Erkrankungen behandeln? Aus welchen Gründen ist die Harnstoffbestimmung im Serum von klinischer Bedeutung? Welches Coenzym wird von Aminotransferasen benötigt? Von welchen Enzymen wird dieses Coenzym ebenfalls benötigt? Welche Stoffwechselstörungen beim Abbau der Aminosäuren kennen Sie? Welche Bedeutung hat die Bestimmung von Aminosäuren? In welchen Körperflüssigkeiten sind diese Bestimmungen sinnvoll?
6 10 ZIELSETZUNG DER EXPERIMENTE Harnstoffzyklus: Bestimmung von Harnstoff Im Leberrohextrakt soll die Entstehung von Harnstoff unter unterschiedlichen Bedingungen verfolgt werden, und anschließend soll die entstandene Menge an Harnstoff pro Stunde und per mg Protein im Leberextrakt berechnet werden. Harnstoff bildet mit -Isonitrosopropiophenon einen Farbstoff, dessen Extinktion im Photometer bestimmt werden kann. PROTEINBESTIMMUNG (BIURETREAKTION) Proteine bilden mit Kupfer-II-Ionen in alkalischer Lösung violette Komplexverbindungen, die sich vom blauen Kupfer-Tartrat-Komplex, wie er im Biuretreagenz enthalten ist, eindeutig unterscheiden. Diese auf der Bildung von Protein-Kupfer-Komplexen beruhende Proteinbestimmungsmethode wird als Biuretreaktion bezeichnet, da die Verbindung Biuret H 2 N-CO-NH-CO-NH 2 (Säureamidbindung!) mit Biuretreagenz (alkalische Kupfer-Tartrat-Lösung) eine Färbung ergibt, die der Farbe der Protein-Kupfer-Komplexe ähnelt. Die Absorptionsspektren der meisten Protein-Kupfer- Komplexe sind sehr ähnlich, so dass man eine Serumalbuminlösung als Proteinstandard verwenden und auf Korrekturfaktoren in der Regel verzichten kann.
7 11 AMINOTRANSFERASEN Qualitativer Nachweis der Alaninaminotransferase Die Übertragung der Aminogruppe von Glutamat auf Pyruvat unter Bildung von Alanin und -Ketoglutarat sowie die Umkehrung dieser Reaktion sollen nachgewiesen werden. Dazu werden Substrate und Produkte der Reaktion durch Dünnschichtchromatografie voneinander getrennt. Auf den Chromatogrammen werden die Aminosäuren Alanin und Glutamat durch Reaktion mit Ninhydrin nachgewiesen. Ninhydrin bildet beim Erhitzen mit Aminosäuren einen blauvioletten Farbstoff. VERSUCHSDURCHFÜHRUNG UND VERSUCHSPROTOKOLL Harnstoffzyklus Mitbringliste: Kittel, Lineal, Taschenrechner ENZYMATISCHE REAKTION Nach dem Pipettierplan 1 werden die Lösungen in die Eppendorf Cups 1-10 gegeben. Als letztes wird Leberextrakt zupipettiert, wodurch die Reaktion gestartet wird. Nach der Zugabe von Leberextrakt werden die Ansätze gemischt und die Reaktionsgefäße dann 30 min bei 37 C inkubiert. Puffer und Salze enthalten: 0,1 mol/l, Kaliumphosphatpuffer (ph 7.8), 0.02 mol/l L-Asparatat, 0,0075 mol/l MgSO 4 und 0,003 mol/l ATP zusammen mit den Enzymen Glycerat-3-phosphat-Mutase, Enolase und Pyruvatkinase, die ebenfalls im Enzymextrakt enthalten sind, als ATP- Quelle.)
8 12 Pipettierplan 1 (Angaben in Mikrolitern µl) Eppendorfcup Nr Reagenzien µl Puffer und Salze µl L-Citrullin (0,1 mol/l) 25 µl L-Arginin (0,1 mol/l) µl L-Ornithin (0,1 mol/l) µl Carbamylphosphat (0,06 mol/l) µl NH 4 HCO 3 (0,2 mol/l) µl N-Acetylglutamat (0,05 mol/l) 25 µl H 2 O dest µl Leberextrakt Am Ende der Inkubationszeit werden die Reaktionen durch Zugabe von je 100 µl 50 %iger Phosphorsäure zu allen Ansätzen gestoppt. Die Proben werden gut durchgemischt (Eppendorf Cups verschließen, mehrfach umdrehen, nicht heftig schütteln!) und 5 min zentrifugiert. Der Überstand wird zur Harnstoffbestimmung verwendet. Schutzbrille tragen!
9 13 PHOTOMETRISCHE HARNSTOFFBESTIMMUNG Während der Inkubation der Enzymansätze werden die Reagenzgläser für die Bestimmung des in der Enzymreaktion gebildeten Harnstoffs vorbereitet. Die Reagenzgläser werden mit wasserfestem Stift beschriftet. Gemäß Pipettierplan 2 werden in jedes Reagenzglas 0,2 ml -Isonitrosopropiophenon pipettiert. Anschließend werden die Überstände zugegeben. Zuletzt wird die Säuremischung aus einem Dispenser zugemischt. Die Säuremischung sollte zum Schluss zugegeben werden, weil dadurch eine bessere Durchmischung der Lösungen erreicht wird. Schutzbrille tragen! Pipettierplan 2 (Angaben in Mikrolitern µl, bzw. Millilitern ml) Reagenzien Reagenzglas Nr. Lw 1-10 Isonitrosopropiophenon *) 200 µl je 200 µl H 2 O dest. 400 µl - Überstand - je 400 µl Säuremischung **) 5 ml je 5 ml Lw = Leerwert *) 4% ige ethanolische Lösung **) Die Säuremischung enthält konz. H 2 SO 4, konz. H 3 PO 4 und H 2 O im Verhältnis 1 : 3 : 6. Sie wird mit einem Dispenser (automatische Pipette) zugegeben. Die Reagenzgläser werden 45 min im Thermoblock bei 100 C inkubiert. Nach 45 min werden die Gläser aus dem Thermoblock genommen. Man lässt sie kurz abkühlen. (Bei längerem Abkühlen entsteht ein Niederschlag, der die Messungen stört). Anschließend werden die Extinktionen der Proben bei 540 nm im Photometer gegen den Leerwert gemessen. Schutzbrille tragen!
10 14 QUANTITATIVE PROTEINBESTIMMUNG MIT DER BIURETREAKTION Schutzbrille tragen! Pipettierplan 3 (Angaben in Millilitern ml) Reagenzglas Nr. Lw ml NaCl (0,9%) 5 4,9 4,9 4,8 ml Standardserumalbumin (50 mg/ml) 0,1 ml Leberextrakt - - 0,1 0,2 ml Biuretreagenz * * 1 Liter Biuretreagenz enthält: 45 g Kalium-Natrium-Tartrat, 5 g Kupfersulfat und 5 g Kaliumjodid gelöst in Natronlauge (0,2 mol/l) Die Ansätze werden sorgfältig gemischt und dann mindestens 30 min bei Zimmertemperatur stehen gelassen. Danach wird die Extinktion bei 540 nm gegen den Leerwert gemessen.
11 15 AMINOTRANSFERASEN a) Lösungen 10 mmol/l Natriumphosphatpuffer ph 7,6 100 mmol/l Glutamat 100 mmol/l Pyruvat 100 mmol/l Alanin 100 mmol/l -Ketoglutarat Alanin-Aminotransferase aus Schweineherz b) Pipettierplan Probe 1 Probe 2 Probe 3 Probe 4 Phosphatpuffer 150 µl 150 µl 150 µl 150 µl Glutamat 50 µl 50 µl - - Pyruvat 50 µl 50 µl - - Alanin µl 50 µl -Ketoglutarat µl 50 µl Die angegebenen Lösungen in Eppendorf Gefäße pipettieren und gut mischen. Dann die Reaktion durch Zugabe von Alanin µl - 50 µl Aminotransferase H 2 O 50 µl - 50 µl - starten (gut mischen) und die Proben in einem 37 o C Wasserbad mindestens 45 min. inkubieren. Anschließend werden die Proben auf Cellulosefolie aufgetragen. c) Dünnschichtchromatographie der Aminosäuren Für die Trennung und den Nachweis der Aminosäuren werden folgende Lösungen einzeln auf eine Cellulosefolie aufgetragen: 1) Glutamatstandard 2) Alaninstandard 3) Probe 1 4) Probe 2 5) Probe 3 6) Probe 4 Dafür wird die Cellulosefolie mit der breiten Seite in die Auftragschablone gelegt. Mit Kapillaren werden die Lösungen in den Kerben der Schablone solange aufgetragen, bis circa 3 mm große Flecken entstanden sind (Abb. 3). Die rechte untere Ecke der Folie wird mit einem weichen Bleistift markiert, damit später klar ist, an welcher Kante die Proben aufgetragen worden sind (Abb. 4). Die Folie wird unter dem Fön getrocknet und anschlie-
12 16 ßend so in die große Kammer der Chromatografiekammer gelegt, dass die Kante mit den Proben die poröse Platte berührt (Abb. 4). In die kleine Kammer werden 1,5 ml Laufmittel (1- Propanol / 34% Ammoniaklösung 7 : 3) gefüllt. Die Chromatografiekammer wird sofort mit der Glasplatte verschlossen. Abb.3: Auftragschablone mit 6 Kerben Große Kammer mit Cellulosefolie Markierung Poröse Platte Kleine Kammer (1.5 ml Laufmittel einfüllen) Abb.4: Chromatografiekammer
13 17 Sobald die Laufmittelfront ca. 0,5 cm vom oberen Rand der Folie entfernt ist, wird die Folie herausgenommen. Dann wird die Folie unter dem Fön getrocknet und mit Ninhydrinreagenz (0,2% Ninhydrin in Aceton) besprüht. Nach erneutem Trocknen an der Luft wird das Chromatogramm vorsichtig auf der Heizplatte bis zum Erscheinen der violetten Flecken erhitzt. AUSWERTUNG UND FEHLERDISKUSSION Jeder Praktikumsteilnehmer erstellt ein schriftliches Protokoll in Form der Tabelle auf der übernächsten Seite. Berechnung der spezifischen enzymatischen Aktivität: Spezifische Enzymatische Aktivität: Die Menge an Substrat (µmol Harnstoff) die innerhalb einer bestimmten Zeit (Stunde) durch eine definierte Menge Protein (mg Protein) umgesetzt wird. Demnach benötigt man: a. Die Menge an Protein, die in 1ml Ansatz vorlag (1) b. Die Menge an Harnstoff, die in 1ml Ansatz entstanden ist Menge an Protein: 1) Hierfür benötigt man die Extinktion der Proteinbestimmung mit der Biuret-Reaktion Reaktionsansätze nach Pipettierplan 3 2) Es gilt: Die Extinktion (Ext) steigt proportional zur Proteinkonzentration (c). Durch den Vergleich der Probe unbekannter Konzentration mit einer bekannten standardisierten Probe kann die Proteinkonzentration errechnet werden. Die Konzentration an Standardserumalbumin (als Referenzprotein) ist im Skript nachzulesen. C Probe / Ext Probe = C Standard / Ext Standard C Probe = Ext Probe x C Standard / Ext Standard 3) Es wurde eine Doppelbestimmung durchgeführt, wobei bei der einen Probe die doppelte Menge Leberextrakt eingesetzt wurde. Das muss bei der Berechnung eines Mittelwerts beachtet werden. Die Menge an Protein in 1ml Ansatz beträgt: 0.45 ml x C Probe = mg Protein
14 18 Harnstoffmenge: Aus den Extinktionen der photometrischen Harnstoffbestimmung (Pipettierplan 2) wird mittels der hier gegebenen Eichkurve die Menge an Harnstoff, bezogen auf 1 ml Ansatz, bestimmt. Beachten Sie, dass die Eichkurve im Bereich der Extinktionen, die in diesem Versuch gemessen werden, nahezu linear verläuft. Deshalb gilt: mg Harnstoff = Extinktion x Ansatz
15 19 Tabelle zur Berechnung der spezifischen enzymatischen Aktivität Reaktionsgefäß Nummer zugesetzte Substrate gemessene Extinktion nach Pipettierplan 2 = X1 L Arginin/ Leberextrakt Carbamylphosphat/ Leberextrakt L Arginin/ + Leberextrakt L Citrullin/ + Leberextrakt L Ornithin/ Carbamylphosphat/ + Leberextrakt L Ornithin/ + Leberextrakt Carbamylphosphat/ + Leberextrakt L Ornithin/ Ammoniumhydrogencarbonat/ N Acetylglutamat/ + Leberextrakt L Ornithin/ Ammonium+ hydrogencarbonat/ + Leberextrakt + Leberextrakt Harnstoff (mg) bezogen auf 1 ml Ansatz X1 x 0,125= X2 Harnstoff in mol: 1mol Harnstoff wiegt 60 g X2 x 1000/60 = X3 Harnstoff produziert pro Stunde: X3/0.5 hr = X4 Harnstoff pro Stunde pro mg Protein: X4/ Menge an Protein in 1ml Ansatz
16 20 AMINOTRANSFERASEN Liegen in Proben 2 und 4 die Aminosäuren Glutamat und Alanin in Gleichgewichtskonzentrationen vor? Welche Aussagen kann man über das Gleichgewicht der Reaktion machen? Welche Bedeutung hat dies für den Stoffwechsel? SCHLUSSFOLGERUNGEN
1 PROTEINE und ENZYME
 1 PROTEINE und ENZYME 1.1 Elektrophoretische Trennung der LDH-Isoenzyme im Agarosegel Das Enzym Lactatdehydrogenase (LDH) ist Bestandteil der anaeroben Glykolyse und katalysiert die folgende Reaktion:
1 PROTEINE und ENZYME 1.1 Elektrophoretische Trennung der LDH-Isoenzyme im Agarosegel Das Enzym Lactatdehydrogenase (LDH) ist Bestandteil der anaeroben Glykolyse und katalysiert die folgende Reaktion:
Versuch 03: Enzyme. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
 Versuch 03: Enzyme Lactatdehydrogenase I. Der optische Test: Bestimmung von Pyruvat Acetylcholinesterase II. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
Versuch 03: Enzyme Lactatdehydrogenase I. Der optische Test: Bestimmung von Pyruvat Acetylcholinesterase II. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
Versuchsprotokoll: Aminosäure- und Proteinbestimmung
 Versuchsprotokoll: Aminosäure- und Proteinbestimmung a) Proteinbestimmung mit Biuret-Reagenz 1.1. Einleitung Das Ziel des Versuchs ist es nach Aufstellen einer Eichgerade mit gegeben Konzentrationen, die
Versuchsprotokoll: Aminosäure- und Proteinbestimmung a) Proteinbestimmung mit Biuret-Reagenz 1.1. Einleitung Das Ziel des Versuchs ist es nach Aufstellen einer Eichgerade mit gegeben Konzentrationen, die
spaltet. Der Sauerstoff entflammt den Glimmspan. Bei der katalytischen Substanz handelt es sich um das Enzym Katalase.
 ENZYMATIK 1. Vorversuch Versuch Spaltung von Wasserstoffperoxid (H 2 O 2 ) Material: Bäckerhefe, Braunstein (MnO 2 ), Wasserstoffperoxid, Rundkolben, Stativ, Brenner, Glimmspan Durchführung 1: 5ml Wasserstoffperoxid
ENZYMATIK 1. Vorversuch Versuch Spaltung von Wasserstoffperoxid (H 2 O 2 ) Material: Bäckerhefe, Braunstein (MnO 2 ), Wasserstoffperoxid, Rundkolben, Stativ, Brenner, Glimmspan Durchführung 1: 5ml Wasserstoffperoxid
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
GEBRAUCHSANLEITUNG. Lowry Assay Kit. Kit für die Proteinkonzentrationsbestimmung. (Kat.-Nr )
 GEBRAUCHSANLEITUNG Lowry Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39236) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG Lowry Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39236) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
Proteinstoffwechsel. Bildung der Aminosäuren. Protein-Abbau der Körperproteine. Protein-Abbau der Nahrungsproteine. Verwertung der Aminosäuren
 Bildung der Aminosäuren Körperproteine 10000 g Nahrungsproteine Proteinstoffwechsel Proteolyse (300 400 g/d) AminosäurePool Verdauung (50 100 g/d) 100 g Vortragender: Dr. W. Helliger Neusynthese aus z.b.
Bildung der Aminosäuren Körperproteine 10000 g Nahrungsproteine Proteinstoffwechsel Proteolyse (300 400 g/d) AminosäurePool Verdauung (50 100 g/d) 100 g Vortragender: Dr. W. Helliger Neusynthese aus z.b.
Enzymologie 10. Kurs
 Arbeitsgruppe D Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs : Enzymologie Einleitung Enzyme ermöglichen durch ihre katalytische Wirkung viele Reaktionen im Stoffwechsel von Lebewesen.
Arbeitsgruppe D Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs : Enzymologie Einleitung Enzyme ermöglichen durch ihre katalytische Wirkung viele Reaktionen im Stoffwechsel von Lebewesen.
GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN
 45 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN A. BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu
45 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN A. BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu
Biochemische UE Alkaline Phosphatase.
 Biochemische UE Alkaline Phosphatase peter.hammerl@sbg.ac.at Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
Biochemische UE Alkaline Phosphatase peter.hammerl@sbg.ac.at Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
PROTEINBESTIMMUNG. Vergleich Bradford und BCA
 PROTEINBESTIMMUNG Vergleich Bradford und BCA ÜBERSICHT Einleitung Theorie Durchführung Resultate und Diskussion Fragen EINLEITUNG Aufgabenstellung: Vergleich der Methoden zur quantitativen Proteinbestimmung
PROTEINBESTIMMUNG Vergleich Bradford und BCA ÜBERSICHT Einleitung Theorie Durchführung Resultate und Diskussion Fragen EINLEITUNG Aufgabenstellung: Vergleich der Methoden zur quantitativen Proteinbestimmung
Versuch 5. Isocitrat-Dehydrogenase
 Versuch 5 Isocitrat-Dehydrogenase Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X PD Dr. Gimpl Einleitung Ziel des Versuches ist es, die Abhängigkeit
Versuch 5 Isocitrat-Dehydrogenase Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X PD Dr. Gimpl Einleitung Ziel des Versuches ist es, die Abhängigkeit
Versuch 3. Elektrophorese
 Versuch 3 Elektrophorese Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Prof. Dr. Schäfer Wird benotet?: 1. Einleitung Ziel des ersten Versuches
Versuch 3 Elektrophorese Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Prof. Dr. Schäfer Wird benotet?: 1. Einleitung Ziel des ersten Versuches
Versuchsprotokoll: Leitenzyme
 Versuchsprotokoll: Leitenzyme Aufschluss von Lebergewebe / Fraktionierte Zentrifugation / Aufschluss von Mitochondrien / Nachweis von Leitenzymen im Cytosol und 1.1. Einleitung Für die Trennung der Organellen
Versuchsprotokoll: Leitenzyme Aufschluss von Lebergewebe / Fraktionierte Zentrifugation / Aufschluss von Mitochondrien / Nachweis von Leitenzymen im Cytosol und 1.1. Einleitung Für die Trennung der Organellen
Aminosäuren & Ketosäuren BIOGENE AMINE
 BIOGENE AMINE Von Mohammed Jaber BIOGENE AMINE: Biogene Amine sind AS ohne COOH-Gruppe! Und warum sind sie so wichtig? Von Mohammed Jaber und Proteine BIOGENE AMINE: Durch die Abspaltung der COOH- Gruppe
BIOGENE AMINE Von Mohammed Jaber BIOGENE AMINE: Biogene Amine sind AS ohne COOH-Gruppe! Und warum sind sie so wichtig? Von Mohammed Jaber und Proteine BIOGENE AMINE: Durch die Abspaltung der COOH- Gruppe
Biomasse: Bestimmung, Abhängigkeiten
 Protokoll zum Praktikum Aufbaumodul Ökologie: WS 2005/06 Biomasse: Bestimmung, Abhängigkeiten Protokollanten Jörg Mönnich Silke Ammerschubert Anton Friesen - Veranstalter Christian Fuchs Versuchstag 26.01.05
Protokoll zum Praktikum Aufbaumodul Ökologie: WS 2005/06 Biomasse: Bestimmung, Abhängigkeiten Protokollanten Jörg Mönnich Silke Ammerschubert Anton Friesen - Veranstalter Christian Fuchs Versuchstag 26.01.05
Was ist denn NAD / NADP??
 Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Die Pyrimidinsynthese
 Die Pyrimidinsynthese Bei der Pyrimidinsynthese wird zunächst der 6-Ring, also die Base zusammengefügt. Erst anschließend kommt es zum Anknüpfen der Ribose. Lokalisation: Zytoplasma Der Ausgang, der
Die Pyrimidinsynthese Bei der Pyrimidinsynthese wird zunächst der 6-Ring, also die Base zusammengefügt. Erst anschließend kommt es zum Anknüpfen der Ribose. Lokalisation: Zytoplasma Der Ausgang, der
GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN
 53 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu gehören
53 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu gehören
6. Fragentyp A Wie berechnet man die ph-werte wässriger Lösungen starker Basen? A) ph = pks - log [HA] / 2 B) ph = 14 + log [OH-] C) ph = 7+ 1/2 pkb +
![6. Fragentyp A Wie berechnet man die ph-werte wässriger Lösungen starker Basen? A) ph = pks - log [HA] / 2 B) ph = 14 + log [OH-] C) ph = 7+ 1/2 pkb + 6. Fragentyp A Wie berechnet man die ph-werte wässriger Lösungen starker Basen? A) ph = pks - log [HA] / 2 B) ph = 14 + log [OH-] C) ph = 7+ 1/2 pkb +](/thumbs/77/74984433.jpg) 1. Fragentyp D Welche der folgenden Einheiten für den molaren Extinktionskoeffizienten ist/sind korrekt? 1) liter I mol x cm 2) liter I mol 3) cm2 / mmol 4) cm2 / mmol x m1 2. Wie lautet die Henderson-Hasselbalch-Gleichung?
1. Fragentyp D Welche der folgenden Einheiten für den molaren Extinktionskoeffizienten ist/sind korrekt? 1) liter I mol x cm 2) liter I mol 3) cm2 / mmol 4) cm2 / mmol x m1 2. Wie lautet die Henderson-Hasselbalch-Gleichung?
Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker
 Name: Datum: Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter Materialien Lebensmittel: Glucose,
Name: Datum: Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter Materialien Lebensmittel: Glucose,
Enzymatischer Eiweiß-Verdau Best.- Nr
 Enzymatischer Eiweiß-Verdau Best.- Nr. 200.9547 I. Materialzusammenstellung Die folgende Auflistung ermöglicht Ihnen die Vollständigkeit des erhaltenen Materials zu überprüfen oder zu kontrollieren, ob
Enzymatischer Eiweiß-Verdau Best.- Nr. 200.9547 I. Materialzusammenstellung Die folgende Auflistung ermöglicht Ihnen die Vollständigkeit des erhaltenen Materials zu überprüfen oder zu kontrollieren, ob
Was ist drin in der Cola?
 Was ist drin in der Cola? - Nachweisreaktionen für Anionen, Kationen und Zucker - Ein Nachweis ist eine Methode der Analytischen Chemie, die dazu dient, eine Stoffprobe zu untersuchen. Nachweisreaktionen
Was ist drin in der Cola? - Nachweisreaktionen für Anionen, Kationen und Zucker - Ein Nachweis ist eine Methode der Analytischen Chemie, die dazu dient, eine Stoffprobe zu untersuchen. Nachweisreaktionen
Kurstag 3. Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers
 Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie
 Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
1. Fragentyp A Welche der folgenden Aminosäuren ergibt beim Abbau Propionyl-CoA? A) Isoleucin B) Tyrosin C) Glutaminsäure D) Glycin E) Asparaginsäure
 1. Fragentyp A Welche der folgenden Aminosäuren ergibt beim Abbau Propionyl-CoA? A) Isoleucin B) Tyrosin C) Glutaminsäure D) Glycin E) Asparaginsäure 2. Fragentyp D Welche der folgenden Aussagen ist (sind)
1. Fragentyp A Welche der folgenden Aminosäuren ergibt beim Abbau Propionyl-CoA? A) Isoleucin B) Tyrosin C) Glutaminsäure D) Glycin E) Asparaginsäure 2. Fragentyp D Welche der folgenden Aussagen ist (sind)
5 BIOLOGISCHE OXIDATION
 5 BIOLOGISCHE OXIDATION Oxidations-Reduktions-Reaktionen sind im lebenden Organismus die Hauptquelle für chemisch verwertbare Energie. Unter aeroben Bedingungen (in Anwesenheit von O 2 ) werden die Kohlenstoffatome
5 BIOLOGISCHE OXIDATION Oxidations-Reduktions-Reaktionen sind im lebenden Organismus die Hauptquelle für chemisch verwertbare Energie. Unter aeroben Bedingungen (in Anwesenheit von O 2 ) werden die Kohlenstoffatome
Zellulärer Abbau von Proteinen in Aminosäuren:! Proteine werden in Zellen durch Proteasom-Komplexe in! einzelne Aminosäuren abgebaut.!
 Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Energie aus Aminosäuren - Wundermittel Protein?
 Jeder von uns kennt die Versprechen der Eiweißshakes: Mehr Proteine machen dich schlank, jung und wunderschön. Aber was haben Proteine an sich, das diese Versprechen rechtfertigt? Dies ist der vierte Teil
Jeder von uns kennt die Versprechen der Eiweißshakes: Mehr Proteine machen dich schlank, jung und wunderschön. Aber was haben Proteine an sich, das diese Versprechen rechtfertigt? Dies ist der vierte Teil
Übungsaufgabe 1. Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz
 Übungsaufgabe 1 Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz Versuchsbeschreibung: 20 ml der erhaltenen Probelösung werden in ein 150 ml Becherglas
Übungsaufgabe 1 Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz Versuchsbeschreibung: 20 ml der erhaltenen Probelösung werden in ein 150 ml Becherglas
Chemie (in) der Extra-Klasse: Bausteine des Lebens - eine Einführung in die Biochemie der Proteine
 Unterrichts- und Lernmaterialien geprüft vom PARSEL-Konsortium im Rahmen des EC FP6 geförderten Projekts: SAS6-CT-2006-042922-PARSEL Kooperierende Institutionen und Universitäten des PARSEL-Projekts: Anregungen
Unterrichts- und Lernmaterialien geprüft vom PARSEL-Konsortium im Rahmen des EC FP6 geförderten Projekts: SAS6-CT-2006-042922-PARSEL Kooperierende Institutionen und Universitäten des PARSEL-Projekts: Anregungen
Versuch 1. Aminosäure- und Proteinbestimmungen
 Versuch 1 Aminosäure- und Proteinbestimmungen Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de Chemie X X Prof. Dr. Schäfer Aminosäure und Proteinbestimmungen
Versuch 1 Aminosäure- und Proteinbestimmungen Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de Chemie X X Prof. Dr. Schäfer Aminosäure und Proteinbestimmungen
Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2
 Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2 Diese Präsentation befindet sich auf der Lehr-Inhalts Seite des Inst f. unter www.meduniwien.ac.at/hp/medizinische-genetik/lehre Helmut Dolznig Inst.
Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2 Diese Präsentation befindet sich auf der Lehr-Inhalts Seite des Inst f. unter www.meduniwien.ac.at/hp/medizinische-genetik/lehre Helmut Dolznig Inst.
Pflanzenphysiologie. Versuch Stickstoffmetabolismus - Induktion der Nitratreduktase
 Georg-August-Universität Göttingen Fakultät für Biologie und Psychologie Pflanzenphysiologie Versuch Stickstoffmetabolismus - Induktion der Nitratreduktase Mitarbeiter: Brill, Martin Mai, Oliver Schoof,
Georg-August-Universität Göttingen Fakultät für Biologie und Psychologie Pflanzenphysiologie Versuch Stickstoffmetabolismus - Induktion der Nitratreduktase Mitarbeiter: Brill, Martin Mai, Oliver Schoof,
3.1 Isolierung von Glykogen aus Leber-Säurehydrolysat und Nachweis der Glukose
 3 KOHLENHYDRATE 3.1 Isolierung von Glykogen aus Leber-Säurehydrolysat und Nachweis der Glukose Glykogen ist das hochmolekulare Reservekohlenhydrat tierischer Zellen. Bei hohem Kohlenhydratangebot in der
3 KOHLENHYDRATE 3.1 Isolierung von Glykogen aus Leber-Säurehydrolysat und Nachweis der Glukose Glykogen ist das hochmolekulare Reservekohlenhydrat tierischer Zellen. Bei hohem Kohlenhydratangebot in der
SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen
 GEBRAUCHSANLEITUNG SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen (Kat.-Nr. 42177) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
GEBRAUCHSANLEITUNG SERVA Streptavidin Agarose Resin Agarosematrix zur Affinitätsreinigung von biotinylierten Biomolekülen (Kat.-Nr. 42177) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg
Mustervorschrift Versuch
 Mustervorschrift Versuch 10.2.3 N-Acetylierung von D-/L- Methionin (1.Stufe) 5.20 g (34.86 mmol) D-/L- Methionin (racemisch) werden in 51.13 g (48.80 ml, 349 mmol) reiner Essigsäure (Eisessig) gelöst 1.
Mustervorschrift Versuch 10.2.3 N-Acetylierung von D-/L- Methionin (1.Stufe) 5.20 g (34.86 mmol) D-/L- Methionin (racemisch) werden in 51.13 g (48.80 ml, 349 mmol) reiner Essigsäure (Eisessig) gelöst 1.
3 150 ml-bechergläser als Wasserbäder Thermometer 2 ml-plastikpipetten Parafilm
 Nachweis der Enzymaktivität und Enzymhemmung Chemikalien: Harnstofflösung (10% w/v) Phenolphtalein-Lösung Urease rohe Kartoffel Wasserstoffperoxid-Lösung (30 % w/v) Bäckerhefe verdünnte Lösung von Methylenblau
Nachweis der Enzymaktivität und Enzymhemmung Chemikalien: Harnstofflösung (10% w/v) Phenolphtalein-Lösung Urease rohe Kartoffel Wasserstoffperoxid-Lösung (30 % w/v) Bäckerhefe verdünnte Lösung von Methylenblau
Biochemisches Grundpraktikum
 Biochemisches Grundpraktikum Versuch Nummer G-01 01: Potentiometrische und spektrophotometrische Bestim- mung von Ionisationskonstanten Gliederung: I. Titrationskurve von Histidin und Bestimmung der pk-werte...
Biochemisches Grundpraktikum Versuch Nummer G-01 01: Potentiometrische und spektrophotometrische Bestim- mung von Ionisationskonstanten Gliederung: I. Titrationskurve von Histidin und Bestimmung der pk-werte...
1.1. Grundlage aller enzymkinetischen Untersuchungen ist die Michaelis-Menten- Gleichung: V 0 = V max x [S] K m + [S]
![1.1. Grundlage aller enzymkinetischen Untersuchungen ist die Michaelis-Menten- Gleichung: V 0 = V max x [S] K m + [S] 1.1. Grundlage aller enzymkinetischen Untersuchungen ist die Michaelis-Menten- Gleichung: V 0 = V max x [S] K m + [S]](/thumbs/58/42178387.jpg) 1.1 ABSHNITT 1: ENZYME Einführung Enzyme sind informationelle Makromoleküle und als solche Instrumente gezielter Prozeßsteuerung. Sie haben eine katalytische und eine kognitive Funktion. Die katalytische
1.1 ABSHNITT 1: ENZYME Einführung Enzyme sind informationelle Makromoleküle und als solche Instrumente gezielter Prozeßsteuerung. Sie haben eine katalytische und eine kognitive Funktion. Die katalytische
Kohlenhydrate in Lebensmitteln Schokolade ist nicht gleich Schokolade!
 Kohlenhydrate in Lebensmitteln ist nicht gleich! Einführung Sicher hast du schon davon gehört, dass es verschiedene Zuckerarten gibt. So gibt es Traubenzucker (Glucose), Fruchtzucker (Fructose) und natürlich
Kohlenhydrate in Lebensmitteln ist nicht gleich! Einführung Sicher hast du schon davon gehört, dass es verschiedene Zuckerarten gibt. So gibt es Traubenzucker (Glucose), Fruchtzucker (Fructose) und natürlich
Versuch 6. Leitenzyme
 Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
3.2. Aufgaben zu Säure-Base-Gleichgewichten
 .. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
.. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
Standardabweichung und Variationskoeffizient. Themen. Prinzip. Material TEAS Qualitätskontrolle, Standardabweichung, Variationskoeffizient.
 Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Tatort Küche. Versuch 1: Rotkohl. Aufgabe: Geräte und Chemikalien: Versuchsdurchführung: Beobachtungen: Auswertung:
 Tatort Küche Aufgabe: Es muss anhand von chemischen Versuchen herausgefunden werden, welcher von drei sehr ähnlich aussehenden Feststoffen Zucker, welcher Kochsalz und welcher Zitronensäure ist. Das Kosten
Tatort Küche Aufgabe: Es muss anhand von chemischen Versuchen herausgefunden werden, welcher von drei sehr ähnlich aussehenden Feststoffen Zucker, welcher Kochsalz und welcher Zitronensäure ist. Das Kosten
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Aminosäurestoffwechsel I. Grundlagen und Ammoniak-Stoffwechsel COO- +H 3 C R. Johannes Schmidt; Matthias Schnepper
 Aminosäurestoffwechsel I Grundlagen und Ammoniak-Stoffwechsel OO- 3 N R Johannes Schmidt; Matthias Schnepper Einführung Gliederung: Struktur und Einteilung der Aminosäuren Grundzüge des Aminosäurestoffwechsels
Aminosäurestoffwechsel I Grundlagen und Ammoniak-Stoffwechsel OO- 3 N R Johannes Schmidt; Matthias Schnepper Einführung Gliederung: Struktur und Einteilung der Aminosäuren Grundzüge des Aminosäurestoffwechsels
Vorlesung Leber / Plasmaproteine
 Vorlesung Leber / Plasmaproteine Wintersemester 2016 / 2017 Universitätsklinikum Düsseldorf Institut für Laboratoriumsdiagnostik / Zentrallabor Das Organ Leber Funktionen Elimination / Entgiftung Syntheseleistung
Vorlesung Leber / Plasmaproteine Wintersemester 2016 / 2017 Universitätsklinikum Düsseldorf Institut für Laboratoriumsdiagnostik / Zentrallabor Das Organ Leber Funktionen Elimination / Entgiftung Syntheseleistung
Wasserchemie und Wasseranalytik SS 2015
 Wasserchemie und Wasseranalytik SS 015 Übung zum Vorlesungsblock II Wasserchemie Dr.-Ing. Katrin Bauerfeld 5,5 6,5 7,5 8,5 9,5 10,5 11,5 1,5 13,5 Anteile [%] Übungsaufgaben zu Block II Wasserchemie 1.
Wasserchemie und Wasseranalytik SS 015 Übung zum Vorlesungsblock II Wasserchemie Dr.-Ing. Katrin Bauerfeld 5,5 6,5 7,5 8,5 9,5 10,5 11,5 1,5 13,5 Anteile [%] Übungsaufgaben zu Block II Wasserchemie 1.
Methoden zur Untersuchung von Papier, Karton und Pappe für Lebensmittelverpackungen und sonstige Bedarfsgegenstände
 Methoden zur Untersuchung von Papier, Karton und Pappe für Lebensmittelverpackungen und sonstige Bedarfsgegenstände 5. Bestimmung von Einzelsubstanzen 5.19 Levanase 1. Allgemeine Angaben Bezeichnung in
Methoden zur Untersuchung von Papier, Karton und Pappe für Lebensmittelverpackungen und sonstige Bedarfsgegenstände 5. Bestimmung von Einzelsubstanzen 5.19 Levanase 1. Allgemeine Angaben Bezeichnung in
Harnstoffsynthese und Harnstoffzyklusenzyme. in der Rattenleber bei akuter und chronischer Urämie FORSCHUNGSBERICHT DES LANDES NORDRHEIN-WESTFALEN
 FORSCHUNGSBERICHT DES LANDES NORDRHEIN-WESTFALEN Nr. 2869/Fachgruppe Medizin Herausgegeben vom Minister für Wissenschaft und Forschung Priv. - Doz. Dr. med. Martin Vlaho Prof. Dr. med. Heinz-Günter Sieberth
FORSCHUNGSBERICHT DES LANDES NORDRHEIN-WESTFALEN Nr. 2869/Fachgruppe Medizin Herausgegeben vom Minister für Wissenschaft und Forschung Priv. - Doz. Dr. med. Martin Vlaho Prof. Dr. med. Heinz-Günter Sieberth
Nichtessentielle Aminosäuren. Stoffwechsel Nahrungskarenz
 Nichtessentielle Aminosäuren Stoffwechsel Nahrungskarenz Einleitung 11 nichtessentielle AS Können von Säugetierzellen selbstsynthetisiert werden. Im Vergleich zu essentiellen AS einfache Synthesewege Nichtessentiell
Nichtessentielle Aminosäuren Stoffwechsel Nahrungskarenz Einleitung 11 nichtessentielle AS Können von Säugetierzellen selbstsynthetisiert werden. Im Vergleich zu essentiellen AS einfache Synthesewege Nichtessentiell
Technische Universität Chemnitz Chemisches Grundpraktikum
 Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP5 - Massanalytische Bestimmungsverfahren (Volumetrie)» Martin Wolf Betreuerin: Frau Sachse Datum:
Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP5 - Massanalytische Bestimmungsverfahren (Volumetrie)» Martin Wolf Betreuerin: Frau Sachse Datum:
Biochemie-Praktikum: Programm E
 Gruppe Nr. 0 Tübingen, den XXIX. Mai Anno Domini 00 Gero Schwenk, Forian Waker Biochemie-Praktikum: Programm E Versuch : Lactatkonzentration im Serum Enzyme Decies repetita pacebit. Aufgabensteung: Mit
Gruppe Nr. 0 Tübingen, den XXIX. Mai Anno Domini 00 Gero Schwenk, Forian Waker Biochemie-Praktikum: Programm E Versuch : Lactatkonzentration im Serum Enzyme Decies repetita pacebit. Aufgabensteung: Mit
Carbonat, Hydrogencarbonat
 Chlorid a) Die Lösung die einer Menge Substanz, die etwa 2 mg Chlorid entspricht, in 2 ml Wasser R oder 2 ml der vorgeschrieben Lösung werden verwendet. Diese Lösung wird mit verdünnter Salpetersäure R
Chlorid a) Die Lösung die einer Menge Substanz, die etwa 2 mg Chlorid entspricht, in 2 ml Wasser R oder 2 ml der vorgeschrieben Lösung werden verwendet. Diese Lösung wird mit verdünnter Salpetersäure R
Reaktionskinetik. bimolekularen Reaktion. Für die Konzentraton des Dinitrochlorbenzols [a] gilt: = k
![Reaktionskinetik. bimolekularen Reaktion. Für die Konzentraton des Dinitrochlorbenzols [a] gilt: = k Reaktionskinetik. bimolekularen Reaktion. Für die Konzentraton des Dinitrochlorbenzols [a] gilt: = k](/thumbs/42/22840880.jpg) Versuche des Kapitel 7 Reaktionskinetik Einleitung Die Reaktion von Piperidin mit Dinitrochlorbenzol zum gelben Dinitrophenylpiperidin soll auf die Geschwindigkeitskonstante und die Arrheniusparameter
Versuche des Kapitel 7 Reaktionskinetik Einleitung Die Reaktion von Piperidin mit Dinitrochlorbenzol zum gelben Dinitrophenylpiperidin soll auf die Geschwindigkeitskonstante und die Arrheniusparameter
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Kreatinin-Bestimmung
 Kreatinin-Bestimmung TEAS Themen Kreatinin, Clearance, Nierenfunktion, Photometrie, Jaffe-Reaktion Prinzip Kreatinin entsteht als Metabolit des Muskelstoffwechsels in Relation zur Muskelmasse und wird
Kreatinin-Bestimmung TEAS Themen Kreatinin, Clearance, Nierenfunktion, Photometrie, Jaffe-Reaktion Prinzip Kreatinin entsteht als Metabolit des Muskelstoffwechsels in Relation zur Muskelmasse und wird
Praktische Übungen Chemie. Versuch 6
 Bauhaus-Universität Weimar Professur Bauchemie Prof. Dr. rer. nat. habil. Christian Kaps Praktische Übungen Chemie Versuch 6 Bestimmung der Wasserhärte Stand: April 2008 1. Grundlagen und Zielstellung
Bauhaus-Universität Weimar Professur Bauchemie Prof. Dr. rer. nat. habil. Christian Kaps Praktische Übungen Chemie Versuch 6 Bestimmung der Wasserhärte Stand: April 2008 1. Grundlagen und Zielstellung
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Kohlenstoffdioxid wird in lichtabhängigen Reaktion freigesetzt Sauerstoff wird wie in der Atmung verbraucht. Lichtatmung
 1. Kompartimentierung bei der Photorespiration Kohlenstoffdioxid wird in lichtabhängigen Reaktion freigesetzt Sauerstoff wird wie in der Atmung verbraucht. Lichtatmung Kosten: o Energie, da ATP verbraucht
1. Kompartimentierung bei der Photorespiration Kohlenstoffdioxid wird in lichtabhängigen Reaktion freigesetzt Sauerstoff wird wie in der Atmung verbraucht. Lichtatmung Kosten: o Energie, da ATP verbraucht
Kohlenhydrate in Lebensmitteln - Nachweis von Zucker
 Name: Datum: Kohlenhydrate in Lebensmitteln - Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter, schwarzer Stift Materialien Glucose,
Name: Datum: Kohlenhydrate in Lebensmitteln - Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter, schwarzer Stift Materialien Glucose,
Aminosäuren. Versuch 1 Identifizierung von Aminosäuren durch DC und Farbreaktionen
 Aminosäuren, Seite 1 Aminosäuren Einführung Aminosäuren (AS) spielen in allen Zellen eine herausragende Rolle als Strukturbestandteile von komplexen Molekülen, Ausgangsstoffe von Synthesen und zum Teil
Aminosäuren, Seite 1 Aminosäuren Einführung Aminosäuren (AS) spielen in allen Zellen eine herausragende Rolle als Strukturbestandteile von komplexen Molekülen, Ausgangsstoffe von Synthesen und zum Teil
Laborführerschein. Dieses Skript gehört:
 Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Versuch 4. Enzymkinetik
 Versuch 4 Enzymkinetik Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Dr. Postina Wird benotet?: Aufgabenstellung Ermittlung der maximalen Reaktionsgeschwindigkeit
Versuch 4 Enzymkinetik Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Dr. Postina Wird benotet?: Aufgabenstellung Ermittlung der maximalen Reaktionsgeschwindigkeit
Präsentation STOFFWECHSEL STOFFWECHSEL. Fettstoffwechsel im Sport. Biologische Oxidation Zitratzyklus und Atmungskette
 STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
Hämoglobinbestimmung
 Hämoglobinbestimmung TEAS Themen Erythrozyten, Photometrie, Hämoglobin, Cyanhämoglobin, Oxyhämoglobin, Carboxyhämoglobin, Methämoglobin, Anämie. Prinzip Eine quantitative Hämoglobinbestimmung ist unerlässlich,
Hämoglobinbestimmung TEAS Themen Erythrozyten, Photometrie, Hämoglobin, Cyanhämoglobin, Oxyhämoglobin, Carboxyhämoglobin, Methämoglobin, Anämie. Prinzip Eine quantitative Hämoglobinbestimmung ist unerlässlich,
Kapitel 2.2 Kardiopulmonale Homöostase. Kohlendioxid
 Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Aminosäuren und Proteine
 Aminosäuren und Proteine Von Mohammed Jaber Aminosäuren und Proteine Kleinigkeit: 23 proteinogene AS 250 nicht-proteinogene AS (Anzahl synthetisch erzeugten erheblich größer) Aminosäuren und Proteine Kleinigkeit:
Aminosäuren und Proteine Von Mohammed Jaber Aminosäuren und Proteine Kleinigkeit: 23 proteinogene AS 250 nicht-proteinogene AS (Anzahl synthetisch erzeugten erheblich größer) Aminosäuren und Proteine Kleinigkeit:
6. Induktion der Galactosidase von Escherichia coli
 Johannes Gutenberg-Universität Mainz Institut für Mikrobiologie und Weinforschung FI-Übung: Identifizierung, Wachstum und Regulation (WS 2004/05) Sebastian Lux Datum: 19.1.2005 6. Induktion der Galactosidase
Johannes Gutenberg-Universität Mainz Institut für Mikrobiologie und Weinforschung FI-Übung: Identifizierung, Wachstum und Regulation (WS 2004/05) Sebastian Lux Datum: 19.1.2005 6. Induktion der Galactosidase
Inhalt SEMINAR 1: mit zu bringen ist: 1. DC von Aminosäuren. 2. Pipettierübung (Präzisionskontrolle) 3. Gelfiltration
 SEMINAR 1: mit zu bringen ist: Arbeitsmantel Skriptum Rechner, Bleistift, Lineal... Protokollheft Und darin eingeklebt das Anwesenheitsblatt 1 Inhalt 1. DC von Aminosäuren 2. Pipettierübung (Präzisionskontrolle)
SEMINAR 1: mit zu bringen ist: Arbeitsmantel Skriptum Rechner, Bleistift, Lineal... Protokollheft Und darin eingeklebt das Anwesenheitsblatt 1 Inhalt 1. DC von Aminosäuren 2. Pipettierübung (Präzisionskontrolle)
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Versuche zum Thema Aminosäuren
 Versuche zum Thema Aminosäuren und Proteine 1/5 Versuche zum Thema Aminosäuren ❶ ph-abhängigkeit der Löslichkeit von Tyrosin 1) In zwei Reagenzgläser gibt man je eine Spatelspitze Tyrosin und etwa 2 cm
Versuche zum Thema Aminosäuren und Proteine 1/5 Versuche zum Thema Aminosäuren ❶ ph-abhängigkeit der Löslichkeit von Tyrosin 1) In zwei Reagenzgläser gibt man je eine Spatelspitze Tyrosin und etwa 2 cm
Kapitel 5: 1. Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D.
 Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
QUALITATIVE UNTERSUCHUNGEN
 QUALITATIVE UNTERSUCHUNGEN Allgemeiner Alkaloid-Nachweis Cinchonae cortex 0.5 g gepulverte Droge werden mit 10 ml 0.2 M Schwefelsäure geschüttelt und abfiltriert. 2 ml aus den Extrakten werden in Reagenzgläser
QUALITATIVE UNTERSUCHUNGEN Allgemeiner Alkaloid-Nachweis Cinchonae cortex 0.5 g gepulverte Droge werden mit 10 ml 0.2 M Schwefelsäure geschüttelt und abfiltriert. 2 ml aus den Extrakten werden in Reagenzgläser
Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat
 Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
CHEMIE-PRAKTIKUM FÜR MEDIZINER WS 2010/2011
 Universität Duisburg-Essen - Institut für Organische Chemie 1 CHEMIE-PRAKTIKUM FÜR MEDIZINER WS 2010/2011 1. Tag: Maßanalyse I Datum: Name: Kurs: Saal: Platz Nr. Theoret. Grundlagen: 1. Aufgabe: Titerstellung
Universität Duisburg-Essen - Institut für Organische Chemie 1 CHEMIE-PRAKTIKUM FÜR MEDIZINER WS 2010/2011 1. Tag: Maßanalyse I Datum: Name: Kurs: Saal: Platz Nr. Theoret. Grundlagen: 1. Aufgabe: Titerstellung
Abhängigkeit der Reaktionsgeschwindigkeit (RG) von der Konzentration: Kalk (CaCO 3 ) + Salzsäure (HCl)
 Abhängigkeit der Reaktionsgeschwindigkeit Abhängigkeit der Reaktionsgeschwindigkeit (RG) von der Konzentration: Kalk (CaCO 3 ) + Salzsäure (HCl) Beim Lösen von Kalk in Salzsäure bildet sich ein gut wasserlösliches
Abhängigkeit der Reaktionsgeschwindigkeit Abhängigkeit der Reaktionsgeschwindigkeit (RG) von der Konzentration: Kalk (CaCO 3 ) + Salzsäure (HCl) Beim Lösen von Kalk in Salzsäure bildet sich ein gut wasserlösliches
2. Woche. Anorganische Analysenmethodik
 2. Woche Anorganische Analysenmethodik Die analytische Chemie befasst sich mit den Methoden zur Ermittlung der stofflichen Zusammensetzung. Durch eine qualitative Analyse wird festgestellt, welche Atome
2. Woche Anorganische Analysenmethodik Die analytische Chemie befasst sich mit den Methoden zur Ermittlung der stofflichen Zusammensetzung. Durch eine qualitative Analyse wird festgestellt, welche Atome
Gesamteiweiß-Bestimmung
 Gesamteiweiß-Bestimmung TEAS Themen Proteine, Aminosäuren, Peptide, Photometrie, Biuret-Reaktion, Hypo- und Hyperproteinämien Prinzip Die Gesamteiweiß-Bestimmung aus Plasma, Serum, Urin oder Liquor erfolgt
Gesamteiweiß-Bestimmung TEAS Themen Proteine, Aminosäuren, Peptide, Photometrie, Biuret-Reaktion, Hypo- und Hyperproteinämien Prinzip Die Gesamteiweiß-Bestimmung aus Plasma, Serum, Urin oder Liquor erfolgt
SOP_018_Glucosebestimmung
 SOP_018_Glucosebestimmung Inhalt Version erstellt am erstellt durch freigegeben durch D Glucosebestimmung in Fermentationsproben 001 11.08.11 Laborpraxis Frank Eiden mittels UV - Test Einsatzgebiet: UV
SOP_018_Glucosebestimmung Inhalt Version erstellt am erstellt durch freigegeben durch D Glucosebestimmung in Fermentationsproben 001 11.08.11 Laborpraxis Frank Eiden mittels UV - Test Einsatzgebiet: UV
ENZYMKINETIK, ENZYMIMMUNTEST EINES HORMONS
 100 PLATZ 9: ENZYMKINETIK, ENZYMIMMUNTEST EINES HORMONS Die Messung der Enzymaktivität, wie sie im Experiment 1.6 und 1.8 vorgenommen wird, liefert Information über die Geschwindigkeit einer Enzymreaktion
100 PLATZ 9: ENZYMKINETIK, ENZYMIMMUNTEST EINES HORMONS Die Messung der Enzymaktivität, wie sie im Experiment 1.6 und 1.8 vorgenommen wird, liefert Information über die Geschwindigkeit einer Enzymreaktion
Versuchsprotokoll 1.3. Sequenzbestimmung von Proteinen
 Versuchsprotokoll 1.3. Sequenzbestimmung von Proteinen Einleitung Um die Anfangssequenz aus drei Aminosäuren eines Proteins zu bestimmen, benutzen wir eine Methode, bei der schrittweise vom N-terminalen
Versuchsprotokoll 1.3. Sequenzbestimmung von Proteinen Einleitung Um die Anfangssequenz aus drei Aminosäuren eines Proteins zu bestimmen, benutzen wir eine Methode, bei der schrittweise vom N-terminalen
Stoffwechsel der essentiellen Aminosäuren
 Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Die Substratspezifität der Enzyme Trypsin und Chymotrypsin
 Die Substratspezifität der Enzyme Trypsin und Chymotrypsin Einleitung Die Proteine Trypsin und Chymotrypsin sind Enzyme, die im Magen von Säugetieren vorkommen und die Hydrolyse von Peptidbindungen katalysieren.
Die Substratspezifität der Enzyme Trypsin und Chymotrypsin Einleitung Die Proteine Trypsin und Chymotrypsin sind Enzyme, die im Magen von Säugetieren vorkommen und die Hydrolyse von Peptidbindungen katalysieren.
Die Stickstoff-Fixierung: Enzymatik
 Die Stickstoff-Fixierung: Enzymatik Präsentation von Philipp Schumann Stephan Christel Die Stickstoff-Fixierung Stickstoff ist das vierthäufigste Element in Zellen Er liegt in reduzierter Form in Aminosäuren,
Die Stickstoff-Fixierung: Enzymatik Präsentation von Philipp Schumann Stephan Christel Die Stickstoff-Fixierung Stickstoff ist das vierthäufigste Element in Zellen Er liegt in reduzierter Form in Aminosäuren,
52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat
 2. Testat Biochemie 93/94 - Teil B (Leider ist dies nur ein Teil der Fragen!) 52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat 3) Biotin 2)
2. Testat Biochemie 93/94 - Teil B (Leider ist dies nur ein Teil der Fragen!) 52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat 3) Biotin 2)
5 NUKLEINSÄUREN. In diesem Versuch wird ein kommerzielles Plasmid (plitmus38, Firma: NEB, siehe Abbildung) eingesetzt.
 5 NUKLEINSÄUREN Nukleinsäuren sind Polynukleotide, wobei jedes Nukleotid sich aus einem Phosphat, einer Ribose (RNA) oder Desoxyribose (DNA) und einer Purin- oder Pyrimidin-Base zusammensetzt. Die einzelnen
5 NUKLEINSÄUREN Nukleinsäuren sind Polynukleotide, wobei jedes Nukleotid sich aus einem Phosphat, einer Ribose (RNA) oder Desoxyribose (DNA) und einer Purin- oder Pyrimidin-Base zusammensetzt. Die einzelnen
Handbuch zum Chemischen Praktikum für Studierende der Human- und Zahnmedizin. Steffen Blaurock Thomas Zimmermann
 Handbuch zum Chemischen Praktikum für Studierende der Human- und Zahnmedizin Steffen Blaurock Thomas Zimmermann 1.1 Einleitung Titrationen werden in der chemischen Analytik durchgeführt, um die Stoffmenge
Handbuch zum Chemischen Praktikum für Studierende der Human- und Zahnmedizin Steffen Blaurock Thomas Zimmermann 1.1 Einleitung Titrationen werden in der chemischen Analytik durchgeführt, um die Stoffmenge
Versuchsprotokoll. 1.) Versuch 2a: Quantitative Bestimmung der Atmung
 Versuchsprotokoll 1.) Versuch 2a: Quantitative Bestimmung der Atmung 1.1. Einleitung: Bei der aeroben Atmung, also dem oxidativen Abbau der Kohlenhydrate, entsteht im Citratzyklus und bei der oxidativen
Versuchsprotokoll 1.) Versuch 2a: Quantitative Bestimmung der Atmung 1.1. Einleitung: Bei der aeroben Atmung, also dem oxidativen Abbau der Kohlenhydrate, entsteht im Citratzyklus und bei der oxidativen
