1834 Mitscherlich Benzoesäure liefert beim erhitzen den selben Kohlenwasserstoff C 6 H 6
|
|
|
- Rudolph Rudolf Busch
- vor 7 Jahren
- Abrufe
Transkript
1 104 Aromatische Kohlenwasserstoffe Aromatizität Das Benzolproblem 1825 Faraday Im Gasöl: Kohlenwasserstoff C 6 6, Sdp. 80 C, Schmp. 5.5 C 1834 Mitscherlich Benzoesäure liefert beim erhitzen den selben Kohlenwasserstoff C 6 6 Welche Strukturisomere kommen in Frage? rg09_6a.cw2
2 105 istorisch folgende Vorschläge: Kekulé Dewar Baeyer/Armstrong Ladenburg Formeln in vieler insicht unbefriedigend, da Benzol keinen olefinischen Charakter und keine ingspannung aufweist Br 2 Br 2,FeBr 3 C 6 5 Br Br C 6 6 Br KMn 4 Kekulé Armstrong/Baeyer szillation innere Absättigung Die rklärung liefert erst die moderne lektronentheorie rwartung: lang kurz lang kurz lang ealität: In der Kristallstrukturanalyse alle Bindungen gleich lang: 1.39 A Wie erklärt man das? kurz
3 106 esonanzenergie Benzol: symmetrisch Messung: Ar C C C C C C 1.39 Å 1.54 Å 1.34 Å esonanz bedeutet immer nergiegewinn: hypothetisches Trien esonanz-nergie Messung Abschätz ung
4 107 = = 8 kj/mol Methode ydrierwärme = -126 kj/mol Grenzen der esonanztheorie: Willstätter Stufen C 3 Pseudopelletierin gelb / lefin Synthese von CT heute? esonanztheorie keine rklärung für Unterschied zu Benzol rklärung durch M-Theorie, ückel-egel ückel (Anerkennung erst nach 2. Weltkrieg)
5 108 xp-rbitale n π-lektronen ückel-egel cyclische, planare, durchgehend konjugierte π-systeme (4n2) π-lektronen: aromatisch stabilisiert 4n π-lektronen: olefinisch oder destabilisiert n = 0,1,2 aromatisch: 6 π-l. 6 π-l. 2 π-l. Ph Ph Ph planar Tropyliumion Cyclopropenyliumion C leeresp nicht aromatisch: 4 π- lektronen 8 π-lektronen nicht planar 4 π- lektronen nicht durchgehend konjugiert
6 109 Weitere aromatische Verbindungen Mehrkernige aromatische Kohlenwasserstoffe Benzol aphthalin Anthracen Phenanthren Pyren Chrysen Benzpyren Perylen Cyclopentadienyl-Anion pk s =15 C -... Aromatische eterocyclen Pyridin basisch Pyrrol nicht basisch Chinolin basisch Furan S Thiophen
7 110 Pyrazol (1,2-Diazol) Imidazol (1,3-Diazol) Pyridin (Pyrazin) Pyrimidin (1,3-Diazin) Pyrazin (1,4-Diazin) Indol Chinolin Purin
8 111 rdöl und Kohle rdöl auptsächlich aliphatische Verbindungen a) ntstehung Durch Absterben von rganismen in küstennahen egionen, reduzierende Zersetzung: rganische Materie C Druck, eduktion, Mikroorganismen rdöl rdgas Biologischer Ursprung abgesichert (Porphyrine und Steroide) auptfundorte, Bedeutung siehe erstes Kapitel b) Zusammensetzung Je nach Fundort sehr verschieden % C, %, 0-7 %, 0-7 % S, wenig Alkane egelfall Cycloalkane (aphthene) ehemalige UDSS, umänien bis 80% Cyclopentan, Cyclohexan Alkene Aromaten - Indonesien bis 40 % Aromaten
9 112 c) Verarbeitung Auftrennung durch Destillation, siehe Beginn Fraktionen aus rdöl Fraktion Siedepunkt [ C] Ausbeute [%] Fraktion Siedepunkt [ C] rdgas (C 1 -C 4 ) Petrolether ohbezin < Destillation Benzin Leuchtöl Gasöl Ligroin Schmieröl / Paraffine > Schwerbenzin ückstand (Asphalt / Pech) d) Treibstoffe Zwei Probleme: - Direkte Fraktionierung rdöl zu wenig - Klopfen Was ist Klopfen? n-alkane haben schlechte Verbrennungseigenschaften, zünden im Motor schon bei Kompression von Gas/Luft-Gemisch bevor Zündfunke kommt. Verzweigte Alkane und Aromaten sind besser. Qualitätsmaß für Treibstoff: ctanzahl (Z) C 3 3 C(C 2 ) 6 C 3 3 C C C 2 C 3 n-eptan Isooctan Z = 0 Z = 100 C 3 C C 3 2
10 113 Bestimmung der ktanzahl durch Verbrennung in orm-tto- Motor und Vergleich mit Isooctan/eptan-Gemischen. Z = %- Gehalt von Isooctan in Vergleichsgemisch mit gleichen Klopfeigenschaften. Lösung beider Probleme erfordert - Umwandlung linearer in verzweigter Alkane und Aromaten - Umwandlung hochsiedende Fraktionen in niedrig-siedende Cracken Im Prinzip brutales rhitzen unter eventuellem Zusatz von Katalysatoren: C n 2n C 1-80 bar eventuell Kat. C m 2m2 C r 2r hochsiedend niedrigsiedend (rm=n) Mechanismus: 1 -C 2 -C 2 -C 2 -C 2-2 Δ 1 C C C C 2 1 -C 2 -C 2-2 C=C 2 Je nach Katalysator verschiednen Varianten wichtig eforming / Platforming Schwerbenzin Sdp C Pt oder Pt/h auf Al 2 3 Spaltung / Isomeris. ingbildung 500 C / 50 atm 2 Aromatisierung Dest.
11 114 Z. B. aus z. B. aus Aus Crackprozessen hauptsächlich Benzol, Toluol, ylole Andere Aromaten vorwiegend aus 2 Kohle Kohle entstand aus Pflanzen unter hohem Druck und hoher Temperatur unter Mitwirkung von Mikroorganismen durch eduktion: >90% C, daneben viel S, manchmal P! Insgesamt viel mehr Kohle als rdöl vorhanden! Kohle entweder direkt verbrannt oder Kohle > 1000 C Koks Teer C 4 2 C Kohlenstoff aromatische Kohlenwasserstoffe Für chemische Industrie Teer wichtig: fraktionierte Destillation und dann andere Trennprozesse
12 115 Fraktion Siedepunkt [ C] Ausbeute [%] Strukturen Leichtöl Produkt Ausbeute [%] Koks Kokereigas ( 2,C 4,C) Teer Destillation Mittelöl Benzol 1 Ammoniak Schwefelwasserstoff Schweröl Wasser, Sonstiges 8.5 Anthracenöl ückstand (Teerpech) lektrophile aromatische Substitution Substitution am Benzol a) Bromierung und Chlorierung Br 2 aumtemperatur Bruttoreaktion: Br Br 2 (FeBr 3 ) Kat Br Chlorierung analog mit Cl 2 /AlCl 3
13 116 Mechanismus: rzeugung lektrophil δ δ- Br Br FeBr 3 Br Br FeBr 3 eaktion via σ-komplex - Br Br FeBr 3 δ δ- Br Br FeBr 3 Br Br Br Br Br FeBr 3 eaktionsprofil nergie aromatisch Zwischenstufe: nicht aromatisch a 1 geschwindigkeitsbestimmender Schritt a 2 kleine Aktivierung notwendig => schneller Schritt aromatisch
14 117 regeneratives Verhalten des π-systems, die ückbildung eines aromatischen Systems ist energetisch günstiger als die Addition zum Sechsring mit zwei Doppelbindungen => Substitution am planaren sp 2 -Kohlenstoffatom nach einem Additions-liminierungs-Mechanismus über eine Zwischenstufe mit tetraedrischem, sp 3 -hybridisiertem Kohlenstoffatom b) itrierung 3 konz./ 2 S 4 konz. 2 Zn / 10 C itrobenzol Anilin Bezeichnungen: 2 itrogruppe ; 2 Aminogruppe Zum Mechanismus: 2 Typen von eaktionen werden unterschieden rzeugung lektrophil: rzeugung lektrophil: itronium-ion S 4 rasch langsam S 4 S 4 Aromatische Substitution: weiter analog Bromierung
15 118 c) Sulfonierung 2 S 4 10% S 3 35 C 30 min S 3 Gemisch aus 2 S 4 und S 3 = leum lektrophil: S S Wichtig Sulfonierung ist reversibel: deshalb Sulfonylgruppe abspaltbar mit starker Säure ( ). S S S 3 Wegen eversibilität ist S 3 -Gruppe abspaltbar mit, kann also als dirigierender ilfs-substituent verwendet werden! in der Medizin werden antibakterielle Sulfonamide verwendet: S ' z.b. Sulfadiazin (gegen Malaria) 2 S
16 119 Besonders interessanter Fall ist aphthalin S 3 2 S 4 80 C kinetische Kontrolle 2 S C S 3 ther modynamische Kontrolle eaktionsprofil:
17 120 Zweitsubstitution in Benzolderivat kann in der egel nochmals substituiert werden. Dies bringt zwei Probleme mit sich: eaktivität egioselektivität Wo greift das lektrophil an? ipso ortho meta völlig andere Verbindung, kein Isomer!! para Konstitutionsisomere
18 121 Isomerie von Benzolderivaten mit gleichen Substituenten ortho (o) meta (m) para (p) vicinal (vic.) asymmetrisch (asym.) symmetrisch (sym.)
19 122 Vergleich Benzol, Toluol und itrobenzol: 2 S 4 10% S 3 35 C 30 min S 3 Toluol reagiert rascher als Benzol: C 3 2 S 4 C 3 C 3 C 3 (10% S 3 ) 35 C, 5 min S 3 S 3 S 3 32% 62% 6% itrobenzol reagiert viel langsamer als Benzol: S 4 (25% S 3 ) S 3 70 C, 360 min S 3 S 3 1% 2% 97% Dagegen nur wenige Beispiele für eine ipso-substitution: δ SiMe 3 δ metallorganische Verbindung: eine rganosilizium-verbindung
20 123 Allgemein: Substituenten 1. rdnung dirigieren o/p aktivieren 2 Alkyl Aryl Substituenten 2. rdnung dirigieren m 2 (C=) 3 S 3 desaktivieren Substituenteneffekte in Substituent wirkt auf ein C-Gerüst über das σ- und das π- System und über den aum direkt. Die Anteile unterscheidet man als I- und M-ffekt sowie sterischen ffekt. Zwei Grundsysteme analog I σ-donor M π-donor -I σ-akzeptor -M π-akzeptor
21 124 Zweitsubstitution Die egioselektivität der Zweitsubstitution wird durch die Substituenteneffekte des rstsubstituenten im σ-komplex bestimmt: Donor: günstig Akzeptor: ungünstig unwichtig Donor: günstig Akzeptor: ungünstig σ-komplex Konsequenz: M/I = 1/3 Stabilisierung der positiven Ladung im σ-komplex, wenn Substituent relativ zu in o/p-stellung o/p-dirigierend, aktivierend -M/-I stark destabilisierend in der o/p-stellung, schwächer in der m-stellung m-dirigierend, desaktivierend Antagonismus: Sonderfall M/-I, z.b. bei und 2 dominiert M, aber alogene: egioselektivität o/p (wg. M), aber desaktivierend (wg. -I)
22 125 Substituenteneffekte Sterischer ffekt Induktiver ffekt ( od -I-ffekt) Mesomerer ffekt ( oder -M-ffekt) Wirkt nach Maßgabe der Größe (sterischen aumerfüllung) lektronenab- oder -aufnahme über σ-system lektronenab- oder -aufnahme über π-system grund09.doc I Substituenten mit einer lektronegativität () kleiner als 2.5 (C) geben an das C-Gerüst lektronen ab; wichtig insbesondere für ( = 2.1) C 3 < C 2 C 3 < C(C 3 ) 2 < C(C 3 ) 3 Grund: C C - I Substituenen mit > 2.5 des anliegenden Atoms ziehen vom C-Gerüst lektronen ab: 2 < Br < = Cl < 2 < 3 M Substituenten mit einem nichtbindenden lektronenpaar am anliegenden Atom geben über das π-system lektronen an das C-Gerüst ab: al < < 2 ffekt um so größer, je kleiner von anliegendem Atom und, in der gleichen Gruppe, je höher im Periodensystem - M Ungesättigte Substituenten mit Fähigkeit zur Stabilisierung einer negativen Ladung: 2, C,C(=)
23 126 2 Alkylreste etc. Do (Cl, Br) ortho- Angriff Do Do Do Do Do Do Do meta- Angriff para- Angriff Do Do Do Do 2 CF 3 S 3 C Ketone, Aldehyde, ster Ak ortho- Angriff AK Ak Ak meta- Angriff para- Angriff Ak Ak Ak Ak Ak Ak
24 127 Alkylaromaten, Friedel-Crafts-eaktion Äußerst wichtige Verbindungen, vor allem als Lösungsmittel und sog. Zwischenprodukte. Aus Crack-Verfahren billig anfallend. Wichtige Methylderivate des Benzols Sdp. [ C] Schmp. [ C] Benzol 80 6 C 3 Toluol C 3 C 3 ortho-ylol C 3 C 3 meta-ylol C 3 C 3 para-ylol
25 128 erstellung der Alkylaromaten a) Friedel-Crafts-Alkylierung Cl 3 C Cl AlCl 3 C3 AlCl 4 C 3 rascher als Benzol! C3 AlCl 4 C 3 Katalysecyclus ylole Toluol reagiert rascher als Benzol. Ferner alle eaktionen reversibel, deshalb Gemische, die durch Destillation aufgetrennt werden. Allgemein: Lewis-Säure = Friedel-Crafts-Katalysator: AlCl 3, FeBr 3, BF 3 t 2, TiCl 4 eaktion auch mehrfach möglich: 3 AlCl 3 CCl 4-3Cl C Cl Triphenylchlormethan "Tritylchlorid"
26 129 Beispiel für eine elektrophile aromatische Alkylierung: Cumol [ ] -[ ] Cumol b) Friedel-Crafts-Acylierung Präparativ sauberer als Alkylierung, da Produkt deaktiviert. Cl AlCl 3 Zn/ g Cl Clemmenson- eduktion Clemmensen-eduktion besonders gut mit Arylketonen! "Katalysator" AlCl 3 wird in der egel in molarer Menge benötigt, wegen Produktinhibition: Cl AlCl 3 Ar Cl Ar AlCl 3
27 130 eaktionen, Benzyl-esonanz Toluol reagiert mit lektrophilen schneller als Benzol. 3 2 S 4 Gemisch aus o-, p-itrotoluol 2 2 alogenierung zeigt interessante Besoderheiten: C 3 KKK C 3 C 3 C 3 Cl 2 /AlCl 3 Cl 0 C Cl 2 /hv C 2 Cl Cl SSS Siedehitze -Cl Grund adikalkettenreaktion: Start Cl 2 h. ν 2Cl Kette ArC 3 Cl ArC 2 Cl ArC 4 Cl 2 ArC 2 Cl Cl Abbruch 2ArC 2 Ar 2 C C 2 Ar Dibenzyl
28 131 Allgemein: adikal in benzylischer oder allylischer Stellung besonders stabilisiert: Ph-C 2 Benzyl 2 C=C-C 2 Allyl = 50 KJ/mol Das Triphenylmethyl-adikal Versuch Mit drei Phenylgruppen besonders große Stabilisierung (Gomberg 1900) 2 C Cl Zn -ZnCl 2 C gelb-orange langlebiges adikal (10 Grenzstrukturen) 2 C C C Peroxid farblos früher exaphenyläthan
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2016
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2016 Gruppe A
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2016 Gruppe A
1. a) Geben sie den Reaktionsmechanismus für die Nitrierung und die Sulfonierung von Benzol an. Beginnen sie mit der Erzeugung des Elektrophils.
 Übungsblatt 05 - C I - SoSe 2014 (Prof. Bunz) 1. a) Geben sie den Reaktionsmechanismus für die itrierung und die Sulfonierung von Benzol an. Beginnen sie mit der rzeugung des lektrophils. I) rzeugung lektrophil:
Übungsblatt 05 - C I - SoSe 2014 (Prof. Bunz) 1. a) Geben sie den Reaktionsmechanismus für die itrierung und die Sulfonierung von Benzol an. Beginnen sie mit der rzeugung des lektrophils. I) rzeugung lektrophil:
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2018
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
Seminar zum Organisch-Chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016. Aromatische Substitution. Dr. Florian Achrainer AK Zipse
 Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Aromatische Kohlenwasserstoffe.
 Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Arene (Benzolderivate)
 Arene (Benzolderivate) Im Verlauf der Vorlesung haben wir bereits einige kennengelernt: DDT, DIXI, Cumol... hier nun weitere wichtige Vertreter: Acetylsalicylsäure (Aspirin) Synthese über die Kolbe-Schmitt-Synthese
Arene (Benzolderivate) Im Verlauf der Vorlesung haben wir bereits einige kennengelernt: DDT, DIXI, Cumol... hier nun weitere wichtige Vertreter: Acetylsalicylsäure (Aspirin) Synthese über die Kolbe-Schmitt-Synthese
Inhaltsverzeichnis zu Kapitel 6. Aromaten
 Inhaltsverzeichnis zu Kapitel 6. Aromaten 6. Aromaten 6.1 Aromatizität 73 6.2 omenklatur 75 6.3 Darstellung 76 6.4 lektrophile Substitution am Aromaten 76 6.5 Beispiele für S -Reaktionen (was ist?) 77
Inhaltsverzeichnis zu Kapitel 6. Aromaten 6. Aromaten 6.1 Aromatizität 73 6.2 omenklatur 75 6.3 Darstellung 76 6.4 lektrophile Substitution am Aromaten 76 6.5 Beispiele für S -Reaktionen (was ist?) 77
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
3. Gruppe: Aromatische Substitution
 1 1) Zum chanismus der elektrophilen aromatischen Substitution Aromatischer Charakter Antiaromatischer Charakter (4 n 2)π-lektronen 4 nπ e 3 C C 3 2 C C 2 1.48Å 1.54Å 1.34Å 1.39Å ingstrom-ffekte δ = 5
1 1) Zum chanismus der elektrophilen aromatischen Substitution Aromatischer Charakter Antiaromatischer Charakter (4 n 2)π-lektronen 4 nπ e 3 C C 3 2 C C 2 1.48Å 1.54Å 1.34Å 1.39Å ingstrom-ffekte δ = 5
1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden!
 Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
(Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.)
 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
Organische Chemie für MST 5. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
3. Aromatische Verbindungen Benzol(en)
 3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
Konkurrenz zwischen Kern- und Seitenketten-Halogenierung bei Alkylbenzolen (Vollhardt, 3. Aufl., S , 4. Aufl., S.
 Vorlesung 28 Konkurrenz zwischen Kern und Seitenkettenalogenierung bei Alkylbenzolen (Vollhardt, 3. Aufl., S. 10761077, 4. Aufl., S. 11511153) 3 3 3 3 Br 2 [FeBr 3 ] Br KKKegel: Katalysator, Kälte, Kern
Vorlesung 28 Konkurrenz zwischen Kern und Seitenkettenalogenierung bei Alkylbenzolen (Vollhardt, 3. Aufl., S. 10761077, 4. Aufl., S. 11511153) 3 3 3 3 Br 2 [FeBr 3 ] Br KKKegel: Katalysator, Kälte, Kern
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
Aromatische Kohlenwasserstoffe
 Benzol: 6 6 (Faraday 1825) Aromatische Kohlenwasserstoffe OI_folie201 Vorgeschlagene Konstitutionen von Benzol 1,3,5-yclohexatrien-Struktur 1858 Kekulé Erklärt nicht, warum es nur drei regioisomere disubstituierte
Benzol: 6 6 (Faraday 1825) Aromatische Kohlenwasserstoffe OI_folie201 Vorgeschlagene Konstitutionen von Benzol 1,3,5-yclohexatrien-Struktur 1858 Kekulé Erklärt nicht, warum es nur drei regioisomere disubstituierte
σ-bindung beide Kohlenstoffatome sp-hybridisiert => Bindungswinkel 180 eine lineare Struktur
 VIII. Alkine Die C/C-Dreifachbindung als funktionelle Gruppe erste π-bindung σ-bindung zweite π-bindung orthogonal zur ersten beide Kohlenstoffatome sp-hybridisiert => Bindungswinkel 180 eine lineare Struktur
VIII. Alkine Die C/C-Dreifachbindung als funktionelle Gruppe erste π-bindung σ-bindung zweite π-bindung orthogonal zur ersten beide Kohlenstoffatome sp-hybridisiert => Bindungswinkel 180 eine lineare Struktur
5 Chemie aromatischer Verbindungen
 5 hemie aromatischer Verbindungen Benzol wurde 1825 von Faraday entdeckt. bwohl das Verhältnis : = 1:1 stark ungesättigten harakter anzeigte, reagierte es weder mit Br 2 noch mit KMn 4 wie gewöhnliche
5 hemie aromatischer Verbindungen Benzol wurde 1825 von Faraday entdeckt. bwohl das Verhältnis : = 1:1 stark ungesättigten harakter anzeigte, reagierte es weder mit Br 2 noch mit KMn 4 wie gewöhnliche
Lösungen 3. Übungsblatt SS 2002
 Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Wir werden hier nur Benzol-Derivate betrachten, und nicht aromatische Ringe, die ein Heteroatom enthalten (Kapitel-6), z.b. N, O oder S.
 5. Aromatische Kohlenwasserstoffe 36 Aufgrund der starken Aromas, das viele Benzolderivate ausströmen, nennt man sie aromatische Verbindungen. Deshalb gilt Benzol als Stammverbindung der Aromaten. Aromatische
5. Aromatische Kohlenwasserstoffe 36 Aufgrund der starken Aromas, das viele Benzolderivate ausströmen, nennt man sie aromatische Verbindungen. Deshalb gilt Benzol als Stammverbindung der Aromaten. Aromatische
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 C 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr.. Landau und Prof. Dr. J. A. Robinson 5. Aromatische Kohlenwasserstoffe Aufgrund des starken Aromas, das viele Benzolderivate ausströmen, nennt
C 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr.. Landau und Prof. Dr. J. A. Robinson 5. Aromatische Kohlenwasserstoffe Aufgrund des starken Aromas, das viele Benzolderivate ausströmen, nennt
Reaktionsmechanismen nach dem gleichnahmigen Buch von R. Brückner
 Reaktionsmechanismen nach dem gleichnahmigen Buch von R. ückner Kap. 5 Substitutionsreaktionen am Aromaten Dr. ermann A. Wegner hermann.wegner@unibas.ch lektrophile aromatische Substitution Wheland-Komplex
Reaktionsmechanismen nach dem gleichnahmigen Buch von R. ückner Kap. 5 Substitutionsreaktionen am Aromaten Dr. ermann A. Wegner hermann.wegner@unibas.ch lektrophile aromatische Substitution Wheland-Komplex
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 CE 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 6. eterocyclische Verbindungen Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen
CE 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 6. eterocyclische Verbindungen Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen
Chemie für Biologen SS Georg Jansen AG Theoretische Organische Chemie Universität Duisburg Essen. (Teil 11: Alkine / Polyene / Aromaten)
 hemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische hemie Universität Duisburg Essen (Teil 11: Alkine / Polyene / Aromaten) Bindungen mit sp ybridobitalen Bindungen mit sp ybridorbitalen
hemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische hemie Universität Duisburg Essen (Teil 11: Alkine / Polyene / Aromaten) Bindungen mit sp ybridobitalen Bindungen mit sp ybridorbitalen
N N. Chinolin. Pyridin. Imidazol
 6. eterocyclische Verbindungen 51 Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen aufgebaut sind. In den sogenannten eterocyclen ist mindestens ein Kohlenstoff des ings
6. eterocyclische Verbindungen 51 Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen aufgebaut sind. In den sogenannten eterocyclen ist mindestens ein Kohlenstoff des ings
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Übungen zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe. 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit
 O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
Prof. Christoffers, Vorlesung Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 6. Aromaten 6.1 Aromatizität Benzol ist eine Verbindung mit der Summenformel
Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 6. Aromaten 6.1 Aromatizität Benzol ist eine Verbindung mit der Summenformel
Moderne Methoden in der Organischen Chemie
 oderne ethoden in der rganischen Chemie 0 Allgemeines: Wichtig für alle chemischen eaktionen: elektivität Chemoselektivität: egioselektivität: + tereoselektivät: - nantioselektivität: -Diastereosektivität:
oderne ethoden in der rganischen Chemie 0 Allgemeines: Wichtig für alle chemischen eaktionen: elektivität Chemoselektivität: egioselektivität: + tereoselektivät: - nantioselektivität: -Diastereosektivität:
Aromaten, Fette und Tenside Seminar zu chem2010 Stephan Bernt
 , Fette und Tenside 12.05.2010 Seminar zu chem2010 Stephan Bernt Kriterien für Aromatizität: cyclisch planar vollständig konjugiertes π-elektronensystem Hückel-Regel: 4n+2 π-elektronen Prototyp des Aromaten:
, Fette und Tenside 12.05.2010 Seminar zu chem2010 Stephan Bernt Kriterien für Aromatizität: cyclisch planar vollständig konjugiertes π-elektronensystem Hückel-Regel: 4n+2 π-elektronen Prototyp des Aromaten:
Organische Chemie im Überblick
 Evelyne Chelain Nadeqe Lubin-Germain Jacques Uziel Organische Chemie im Überblick Grundwissen in Lerneinheiten Aus dem Französischen übersetzt von Karin Beifuss ~ Springer Spektrum Inhaltsverzeichnis 1
Evelyne Chelain Nadeqe Lubin-Germain Jacques Uziel Organische Chemie im Überblick Grundwissen in Lerneinheiten Aus dem Französischen übersetzt von Karin Beifuss ~ Springer Spektrum Inhaltsverzeichnis 1
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
Energie. 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital
 sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und Herstellung
 6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang
 Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Substituenten-Effekt auf die Orientierung der Zweitsubstituenten Orientierung bei der Toluolsubstitution
 Substituenten-Effekt auf die rientierung der Zweitsubstituenten rientierung bei der Toluolsubstitution I_folie215 3 3 3 3 meta para 58 % Nitrierung 4 % 38 % = N 2 N 3 / 2 S 4 Sulfonierung 32 % 6 % 62 %
Substituenten-Effekt auf die rientierung der Zweitsubstituenten rientierung bei der Toluolsubstitution I_folie215 3 3 3 3 meta para 58 % Nitrierung 4 % 38 % = N 2 N 3 / 2 S 4 Sulfonierung 32 % 6 % 62 %
Radikalische Substitution von Alkanen
 adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
Bundesrealgymnasium Imst. Chemie Klasse 8. Aromaten und deren Reaktionen
 Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
2. Elektroneneffekte in den organischen Molekülen
 2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
Reaktionstypen der Aromate
 Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Reaktionen der Alkene
 Addition an die π-bindung eaktionen der Alkene CI_folie144 C C X Y C C X Y 1) Katalytische ydrierung von Alkenen Beispiele: Katalysator C C Pt C C C C C C C C C C C C, 5 C C -Methyl--hexen (Lösungsmittel)
Addition an die π-bindung eaktionen der Alkene CI_folie144 C C X Y C C X Y 1) Katalytische ydrierung von Alkenen Beispiele: Katalysator C C Pt C C C C C C C C C C C C, 5 C C -Methyl--hexen (Lösungsmittel)
8 Carbonsäuren und Derivate
 8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
3. Klausur zum Praktikum Organische Chemie I für Studierende der Chemie und der Biochemie im SS 2000
 Prof. Dr. B. König Prof. Dr. Th. Troll 3. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Donnerstag, dem 27. Juli 2000 ame: Mustermann...Vorname: Max...
Prof. Dr. B. König Prof. Dr. Th. Troll 3. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Donnerstag, dem 27. Juli 2000 ame: Mustermann...Vorname: Max...
Name, Vorname: Matrikelnummer: Studienrichtung: Fragen auf den folgenden Seiten: Musterlösung zur Klausur zur Experimentalvorlesung Organische Chemie
 rganisch-chemisches nstitut Fakultät für Chemie und Geowissenschaften Universität eidelberg 23. Juni 2015 Musterlösung zur Klausur zur Experimentalvorlesung rganische Chemie von Prof. Stephen ashmi Name,
rganisch-chemisches nstitut Fakultät für Chemie und Geowissenschaften Universität eidelberg 23. Juni 2015 Musterlösung zur Klausur zur Experimentalvorlesung rganische Chemie von Prof. Stephen ashmi Name,
Aromaten H H H C C C C C C C C H C H. Naphthalin: C 10 H 8. Benzol: C 6 H 6. Anthracen: C 14 H 10. Phenanthren: C 14 H 10.
 Aromaten Folie30 C C C C C C Benzol: C 6 6 C C C C C C C C C C aphthalin: C 10 8 7 6 8 8a 5 4a 1 4 3 7 6 8 8a 9 9a 5 10a 10 4a 1 4 3 Anthracen: C 14 10 1 10 9 3 8 4 5 7 6 Phenanthren: C 14 10 Benzpyren:
Aromaten Folie30 C C C C C C Benzol: C 6 6 C C C C C C C C C C aphthalin: C 10 8 7 6 8 8a 5 4a 1 4 3 7 6 8 8a 9 9a 5 10a 10 4a 1 4 3 Anthracen: C 14 10 1 10 9 3 8 4 5 7 6 Phenanthren: C 14 10 Benzpyren:
Aromatische Verbindungen (Vollhardt, 3. Aufl., S. 671 ff, 4. Aufl., S. 749 ff; Hart, S. 137ff; Buddrus, S. 333 ff)
 Vorlesung 27 Aromatische Verbindungen (Vollhardt, 3. Aufl., S. 671 ff, 4. Aufl., S. 749 ff; art, S. 137ff; Buddrus, S. 333 ff) ntdeckung von Benzol durch M. Faraday 1825 im Rückstand von Leuchtgas, das
Vorlesung 27 Aromatische Verbindungen (Vollhardt, 3. Aufl., S. 671 ff, 4. Aufl., S. 749 ff; art, S. 137ff; Buddrus, S. 333 ff) ntdeckung von Benzol durch M. Faraday 1825 im Rückstand von Leuchtgas, das
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag)
 Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Arene Arene sind cyclisch konjugierte
Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Arene Arene sind cyclisch konjugierte
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
ORGANISCHE CHEMIE. Heterocyclen
 RGAISCE CEMIE eterocyclen eterocyclen Ringförmige Verbindungen, in denen ein oder mehrere C-Atome durch andere Elemente (eteroatome) ersetzt sind. Wichtigste eteroatome:,, S, wichtigste Ringgrößen: 5 und
RGAISCE CEMIE eterocyclen eterocyclen Ringförmige Verbindungen, in denen ein oder mehrere C-Atome durch andere Elemente (eteroatome) ersetzt sind. Wichtigste eteroatome:,, S, wichtigste Ringgrößen: 5 und
Übergangsmetall-π-Komplexe
 Übergangsmetall-π-Komplexe ausschließlich π-wechselwirkungen von Liganden- mit etallorbitalen Alken od. Olefin Diolefin Alkenkomplexe Alkin od. Acetylen Allyl yclopentadienyl sehr häufig, Beispiele mit
Übergangsmetall-π-Komplexe ausschließlich π-wechselwirkungen von Liganden- mit etallorbitalen Alken od. Olefin Diolefin Alkenkomplexe Alkin od. Acetylen Allyl yclopentadienyl sehr häufig, Beispiele mit
Br 1. Auch bei der folgenden Kombination, sind die Strukturen nicht identisch, sie lassen sich durch Drehung nicht ineinander überführen.
 Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME Drill&Practice: Arene. Sind folgende Strukturpaare zueinander identisch? Die Frage ist möglicherweise nicht so simpel, wie sie sich anhört. Gemeint
Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME Drill&Practice: Arene. Sind folgende Strukturpaare zueinander identisch? Die Frage ist möglicherweise nicht so simpel, wie sie sich anhört. Gemeint
Übung: Alkene & Alkohole HS-07
 kt. 007, r.marti / Synthese und eaktionsmechanismen Übung: Alkene & Alkohole S-07 = C 6 7 8 CMe 9 0 Fragen: - Wie können die Intermediate - hergestellt werden, auf was ist zu achten bzgl. eaktivitäten/eagenzien
kt. 007, r.marti / Synthese und eaktionsmechanismen Übung: Alkene & Alkohole S-07 = C 6 7 8 CMe 9 0 Fragen: - Wie können die Intermediate - hergestellt werden, auf was ist zu achten bzgl. eaktivitäten/eagenzien
5. Aromatische Kohlenwasserstoffe
 Inhalt Index 5. Aromatische Kohlenwasserstoffe Aufgrund der starken Aromas, das viele Benzolderivate ausströmen, nennt man sie aromatische Verbindungen. Deshalb gilt Benzol als Stammverbindung der Aromaten.
Inhalt Index 5. Aromatische Kohlenwasserstoffe Aufgrund der starken Aromas, das viele Benzolderivate ausströmen, nennt man sie aromatische Verbindungen. Deshalb gilt Benzol als Stammverbindung der Aromaten.
1.2 Vergleichen Sie die Reaktionsbedingungen für die Bromierung von A und B und begründen Sie unter Mitverwendung von Grenzformeln den Unterschied!
 Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Palladiumkatalysierte C-C-Bindungsknüpfungsreaktionen:
 Palladiumkatalysierte C-C-Bindungsknüpfungsreaktionen: Palladium (Pd) hat die Elektronenkonfiguration [Kr] 4d 10 Gruppe VIIIc, spätes Übergangsmetall, xidationsstufen 0 und 2 typische Verwendung: wegen
Palladiumkatalysierte C-C-Bindungsknüpfungsreaktionen: Palladium (Pd) hat die Elektronenkonfiguration [Kr] 4d 10 Gruppe VIIIc, spätes Übergangsmetall, xidationsstufen 0 und 2 typische Verwendung: wegen
Übergangsmetall-π-Komplexe
 Übergangsmetall-π-Komplexe ausschließlich π-wechselwirkungen von Liganden- mit etallorbitalen Alken od. Olefin Diolefin Alkenkomplexe Alkin od. Acetylen Allyl yclopentadienyl sehr häufig, Beispiele mit
Übergangsmetall-π-Komplexe ausschließlich π-wechselwirkungen von Liganden- mit etallorbitalen Alken od. Olefin Diolefin Alkenkomplexe Alkin od. Acetylen Allyl yclopentadienyl sehr häufig, Beispiele mit
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Gruppe 4 Pflichtversuch. Bromierung des Kerns von Toluol 40 % Menge R-Sätze S-Sätze Gefahrensymbole. 2 ml /
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 Pflichtversuch omierung des Kerns von Toluol
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 Pflichtversuch omierung des Kerns von Toluol
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte
 Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Zusammenfassung 2. Teil
 Zusammenfassung 2. Teil Aromaten Wichtigste Vertreter: C 3 Vorkommen und Isolation: rdöl Verwendung: Lösungsmittel, Ausgangsmaterial für Synthesen Benzol (krebserregend) Toluol Bestandteil im Benzin, Benzolfreie
Zusammenfassung 2. Teil Aromaten Wichtigste Vertreter: C 3 Vorkommen und Isolation: rdöl Verwendung: Lösungsmittel, Ausgangsmaterial für Synthesen Benzol (krebserregend) Toluol Bestandteil im Benzin, Benzolfreie
Diene: C n H 2n-2 : 2 Doppelbindungen
 Diene: n 2n-2 : 2 Doppelbindungen I_folie63 ) Isolierte Diene: Die beiden Doppelbindungen sind durch ein oder mehrere sp 3 -hybridisierte - Atome getrennt. 2 2 3 2 4 5 2,4-Pentadien sp 3 2) Kumulierte
Diene: n 2n-2 : 2 Doppelbindungen I_folie63 ) Isolierte Diene: Die beiden Doppelbindungen sind durch ein oder mehrere sp 3 -hybridisierte - Atome getrennt. 2 2 3 2 4 5 2,4-Pentadien sp 3 2) Kumulierte
Prof. Dr. P. Rademacher Organische Chemie IV OCIV-SS2005-Teil3. zumeist planar trigonal. planar bis pyramidal, starr oder flexibel (Zwischenstellung)
 adikale Prof Dr P ademacher rganische Chemie IV CIV-SS2005-Teil3 4 Struktur von adikalen C (+) Carbenium-Ion C C (-) adikal Carbanion zumeist planar trigonal planar bis pyramidal, starr oder flexibel (Zwischenstellung)
adikale Prof Dr P ademacher rganische Chemie IV CIV-SS2005-Teil3 4 Struktur von adikalen C (+) Carbenium-Ion C C (-) adikal Carbanion zumeist planar trigonal planar bis pyramidal, starr oder flexibel (Zwischenstellung)
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
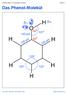 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
UNIVERSITÄT FÜR CHEMISCHE TECHNOLOGIE UND METALLURGIE FAKULTÄT FÜR CHEMIE UND VERFAHRENSTECHNIK
 UNIVERSITÄT FÜR CHEMISCHE TECHNOLOGIE UND METALLURGIE FAKULTÄT FÜR CHEMIE UND VERFAHRENSTECHNIK Genehmigt: Dozent Dr. M. Matschkova Direktor des DCh Bestätigt: Dekan: Prof. Dr. P. Dschambov STUDIENPROGRAMM
UNIVERSITÄT FÜR CHEMISCHE TECHNOLOGIE UND METALLURGIE FAKULTÄT FÜR CHEMIE UND VERFAHRENSTECHNIK Genehmigt: Dozent Dr. M. Matschkova Direktor des DCh Bestätigt: Dekan: Prof. Dr. P. Dschambov STUDIENPROGRAMM
Zweite Klausur zum Organisch-Chemischen Grundpraktikum
 Prof. Dr. Jens Christoffers 12. Juni 2006 Universität ldenburg Zweite Klausur zum rganisch-chemischen Grundpraktikum Vorname: Name: Matrikelnummer: Studiengang: Falls Sie zusätzliche Seiten verwenden,
Prof. Dr. Jens Christoffers 12. Juni 2006 Universität ldenburg Zweite Klausur zum rganisch-chemischen Grundpraktikum Vorname: Name: Matrikelnummer: Studiengang: Falls Sie zusätzliche Seiten verwenden,
Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231
 Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231 Fachhochschule Aachen, Campus Jülich Fachprüfung 32330/32231 Organische Chemie für Biotechnologen II Prüfungsdatum: 10.07.2013 Prüfungsdauer:
Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231 Fachhochschule Aachen, Campus Jülich Fachprüfung 32330/32231 Organische Chemie für Biotechnologen II Prüfungsdatum: 10.07.2013 Prüfungsdauer:
Drill&Practice: Alkene und Alkine
 Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME 1 Drill&Practice: Alkene und Alkine 1. Orbitalzeichnungen sind sehr aufwändig. Zeichnen Sie in die folgenden Strukturen mit rot die π -Bindungen und
Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME 1 Drill&Practice: Alkene und Alkine 1. Orbitalzeichnungen sind sehr aufwändig. Zeichnen Sie in die folgenden Strukturen mit rot die π -Bindungen und
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Ableitung wieder aus einer einfachen anorganischen Verbindung, NH 3 :
 168 X. Amine 1. Übersicht Ableitung wieder aus einer einfachen anorganischen Verbindung, 3 : primär sekündär tertiär Achtung: Ausdrücke primär, sekundär und tertiär beziehen sich auf, nicht auf wie bei
168 X. Amine 1. Übersicht Ableitung wieder aus einer einfachen anorganischen Verbindung, 3 : primär sekündär tertiär Achtung: Ausdrücke primär, sekundär und tertiär beziehen sich auf, nicht auf wie bei
Versuchsprotokoll. Kernbromierung und Seitenkettenbromierung von Xylol. Gruppe 4, Typ: Assiversuch KKK SSS
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Kernbromierung und Seitenkettenbromierung
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Kernbromierung und Seitenkettenbromierung
9 Aromaten. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
 Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
4-Butyl-2,5-dimethylheptan 5-Ethyl-4,8-dimethylundecan
 Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Fossile Rohstoffe. Erdöl
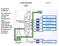 Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
4. Alkene und Alkine : Reaktionen und Darstellung
 Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 Carbonylgruppen und eine C=C Doppelbindung.
 rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
s- und p-orbitale MO-Schema des Wasserstoffmoleküls H 2 y z z x p x p y p z antibindendes MO bindendes MO
 s- und p-rbitale y y z z x x s p x p y p z M-Schema des Wasserstoffmoleküls 2 antibindendes M 1s 1s bindendes M Merkmale wichtiger ybridorbitale sp 3 -ybridisierung: Tetraedrische Ausrichtung der ybridorbitale,
s- und p-rbitale y y z z x x s p x p y p z M-Schema des Wasserstoffmoleküls 2 antibindendes M 1s 1s bindendes M Merkmale wichtiger ybridorbitale sp 3 -ybridisierung: Tetraedrische Ausrichtung der ybridorbitale,
Organische Experimentalchemie
 PD Dr. Alexander Breder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und
PD Dr. Alexander Breder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1
 Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
2 Nucleophile Substitutionen am gesättigten Kohlenstoff
 2 ucleophile Substitutionen am gesättigten Kohlenstoff 21 Allgemeiner eaktionsablauf X Y: Y X: allgemeiner: Substrat ucleophil Produkt ucleofug Elektrophil ucleophil Elektrophil ucleophil ucleophile: Anionen
2 ucleophile Substitutionen am gesättigten Kohlenstoff 21 Allgemeiner eaktionsablauf X Y: Y X: allgemeiner: Substrat ucleophil Produkt ucleofug Elektrophil ucleophil Elektrophil ucleophil ucleophile: Anionen
Konstitutionsisomerie nicht einzige Art der Isomerie, daneben sind auch Stereoisomerie wichtig
 26 sisomerie (Stereoisomerie I) Konstitutionsisomerie nicht einzige Art der Isomerie, daneben sind auch Stereoisomerie wichtig Isomerie II: sisomere: sisomere (bzw. Konformere) sind Isomere, die sich durch
26 sisomerie (Stereoisomerie I) Konstitutionsisomerie nicht einzige Art der Isomerie, daneben sind auch Stereoisomerie wichtig Isomerie II: sisomere: sisomere (bzw. Konformere) sind Isomere, die sich durch
Übungen Kapitel 1 Alkane- Radikalische Substitution
 Übungen Kapitel 1 Alkane- Radikalische Substitution 1. Ein Gemisch aus Halogen und Alkan reagiert bei Bestrahlung mit UV- Licht oder höheren Temperaturen (Bsp. die Gase Methan und Chlor erst bei 250-400
Übungen Kapitel 1 Alkane- Radikalische Substitution 1. Ein Gemisch aus Halogen und Alkan reagiert bei Bestrahlung mit UV- Licht oder höheren Temperaturen (Bsp. die Gase Methan und Chlor erst bei 250-400
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Inhaltsverzeichnis. Teil I Volle Kraft voraus: Die Chemie des Kohlenstoffs 23. Einführung 17. Kapitel 1 Die wundervolle Welt der organischen Chemie 25
 Inhaltsverzeichnis Inhaltsverzeichnis Über den Autor 7 Einführung 17 Über dieses Buch 18 Konventionen in diesem Buch 19 Törichte Annahmen über den Leser 19 Wie dieses Buch aufgebaut ist 20 Teil I: Es war
Inhaltsverzeichnis Inhaltsverzeichnis Über den Autor 7 Einführung 17 Über dieses Buch 18 Konventionen in diesem Buch 19 Törichte Annahmen über den Leser 19 Wie dieses Buch aufgebaut ist 20 Teil I: Es war
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2018
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Carbonsäuren und Derivate Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser/Dr. Martin Sumser September
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Carbonsäuren und Derivate Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser/Dr. Martin Sumser September
Spezielle Methoden der pharmazeutischen Chemie 1
 Spezielle thoden der pharmazeutischen Chemie 1 andhabung von tallorganika (für Diplomanden und Dissertanten im Fach armazeutischen Chemie/Synthese) Kapiteleinteilung: 1. Geräte und Arbeitstechniken 2.
Spezielle thoden der pharmazeutischen Chemie 1 andhabung von tallorganika (für Diplomanden und Dissertanten im Fach armazeutischen Chemie/Synthese) Kapiteleinteilung: 1. Geräte und Arbeitstechniken 2.
Michaeladditionen an auxiliargeschützten cyclischen Enoaten
 Michaeladditionen an auxiliargeschützten cyclischen Enoaten auxiliargeschützte Cyclopentenoncarboxylate auxiliargeschützte Cyclohexenoncarboxylate N S2 Ph N S2 Ph N S2 Ph 1n 6n 16n N S2 Ph N S 2 Ph N S
Michaeladditionen an auxiliargeschützten cyclischen Enoaten auxiliargeschützte Cyclopentenoncarboxylate auxiliargeschützte Cyclohexenoncarboxylate N S2 Ph N S2 Ph N S2 Ph 1n 6n 16n N S2 Ph N S 2 Ph N S
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundlagen der organischen Chfemie
 Dr. sc. nat. Hans Rudolf Christen 'BHiGil.'liÜ ' \ Grundlagen der organischen Chfemie Verlag Sauerländer, Aarau Diesterweg Salle, Frankfurt am Main 9 Inhaltsverzeichnis Vorwort 7 I.Teil: Überblick über
Dr. sc. nat. Hans Rudolf Christen 'BHiGil.'liÜ ' \ Grundlagen der organischen Chfemie Verlag Sauerländer, Aarau Diesterweg Salle, Frankfurt am Main 9 Inhaltsverzeichnis Vorwort 7 I.Teil: Überblick über
Seminar zum Organisch-Chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016. Aliphatische Substitutionen
 Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aliphatische Substitutionen Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aliphatische Substitutionen Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
4. Alkene und Alkine : Reaktionen und Darstellung
 Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
5. Spezielle 5-Ring Heterocyclen 5.1 Pyrrol, Furan, Thiophen
 Vorlesung C2a (eterocyclen) erstmals gehalten im 2011 Th. Ziegler eite 73 5. pezielle 5-ing eterocyclen 5.1 Pyrrol, Furan, Thiophen Eigenschaften: elektronenreiche Aromaten Pyrrol hat auch Diencharakter
Vorlesung C2a (eterocyclen) erstmals gehalten im 2011 Th. Ziegler eite 73 5. pezielle 5-ing eterocyclen 5.1 Pyrrol, Furan, Thiophen Eigenschaften: elektronenreiche Aromaten Pyrrol hat auch Diencharakter
