Gruppenpräparat im Organisch-Chemischen Praktikum II WS 2006/07. Versuch
|
|
|
- Hannah Holst
- vor 7 Jahren
- Abrufe
Transkript
1 Gruppenpräparat im Organisch-Chemischen Praktikum II WS 2006/07 Versuch Patricia Stadtmüller Frank Güthlein Julian Mager Sabin Suraru Martin Schmid Prisca Eckert
2 Inhaltsverzeichnis 1. Einleitung 2 2. Theoretische Grundlagen Gaschromatographie (GC) Hochdruckflüssigkeitschromatographie(HPLC) 4 3. Durchführung 4 4. Experimental-Teil Darstellung von (S)-3-Hydroxybutansäureethylester Derivatisierung mit (S)-Phenylethylsiocyanat Aktivierung von Raney-Nickel Synthese von rac-3-hydroxybutansäureethylester 6 5. Auswertung und Diskussion der Spektren Gaschromatographien HPLC-Spektren NMR-Spektren Perspektiven Gesamtdiskussion Literatur 12 1
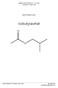
3 1. Einleitung Aus wirtschaftlicher Perspektive haben Hefen eine große Bedeutung, vor allem zur Herstellung von Nahrungs- und Genussmitteln. Aber auch in der präparativen organischen Chemie kann man Hefen zur Synthese nutzen, da diese häufig einen hohen Grad an Stereoselektivität aufweisen. Im Rahmen des organisch-chemischen Praktikums war es Aufgabe unserer Gruppe die Reduktion von Acetessigsäureethylester mittels Hefekulturen näher zu untersuchen. In der Literatur 1 wurde über eine derartige Synthese berichtet, wobei das (S) - Enantiomer zu 93% erhalten wurde. Um dieses Verhältnis zu bestimmen, wurde eine Derivatisierung mit (S) Phenylethylisocyanat durchgeführt. Die erfolgreiche Umsetzung wurde NMRspektroskopisch belegt und die dabei entstandenen Diastereomere mittels GC und HPLC untersucht. OH O O O (R) Hefe, Zucker OEt ca. 7% OEt H 2 O, 145h, RT OH O (S) OEt ca. 93% Me OCN (S) Toluol, N 2 48h, 90 C O Me O O N H (S) EtO (S) 2
4 2. Theoretische Grundlagen Grundsätzlich wird bei allen chromatographischen Untersuchungen die zu untersuchende Substanz mit Hilfe eines Laufmittels (mobile Phase) über eine stationäre Phase geleitet. Die mobile Phase ist flüssig oder gasförmig, die stationäre ist meist fest, kann aber auch flüssig sein. Aufgrund der unterschiedlichen Polarität der Komponenten des zu trennenden Gemisches absorbieren diese verschieden stark an der stationären Phase. Dementsprechend variiert ihre Laufgeschwindigkeit und man erreicht eine gute Auftrennung am Ende der Säule. Der Vorteil dieser Methode ist, dass ein Gemisch aufgetrennt und analysiert werden kann, ohne dass die einzelnen Substanzen dabei verändert oder zerstört werden. Der Grad der Auftrennung lässt sich durch geeignete Wahl der mobilen Phase variieren. Die Auftrennung von sehr kleinen Produktmengen, bei der vor allem die Analyse und weniger die Weiterverarbeitung im Vordergrund steht, lässt sich sehr gut mittels Gaschromatographie (GC) oder Hochdruckflüssigkeitschromatographie (high pressure liquid chromatography, HPLC) realisieren. 2.1 Gaschromatographie (GC) Bei der GC wird die zu untersuchende Probe in den gasförmigen Zustand gebracht. Wichtig ist, dass sie sich dabei nicht zersetzt. Bild 1 zeigt den schematischen Aufbau eines Gaschromatographen. Bild1: Schematischer Aufbau eines Gaschromatographen Die zu untersuchende Probe wird nach der Injektion verdampft und mit Hilfe eines inerten Trägergases (Helium, Wasserstoff oder Stickstoff) über eine heiße Säule geleitet. Ein Detektor misst am Ende der Säule die Veränderung der Wärmeleitfähigkeit oder Flammenionisation und errechnet daraus ein Spektrum. 3
5 Dieses kann am Computer ausgewertet werden. Die Laufzeit lässt qualitative Aussagen zu, während man über die Integration der erhaltenen Peaks Aussagen über die Menge und Mengenverteilung machen kann. Als stationäre Phase werden aufgerollte Kapillarsäulen zum Beispiel aus Kieselgel verwendet. Da diese beim Gaschromatographen aus finanziellen Gründen nicht beliebig oft ausgetauscht werden kann, muss sie sorgfältig ausgesucht und behandelt werden. Aufgrund dieser Tatsache kann man bei einer GC meistens nur wenige Parameter verändern, da normalerweise nur eine einzige Säule pro Gaschromatograph zur Verfügung steht. Im Labor werden normalerweise nur die Heizrate, die Start- und die Endtemperatur verändert. Allgemein lassen sich fast alle chromatographischen Arbeitsgeräte mit einer Vielzahl an Analysatoren koppeln. Eine interessante Möglichkeit ergibt sich durch die Kopplung der GC mit einem Massenspektrometer (MS). Bei der GC-MS werden die einzelnen Substanzen am Ende der Säule massenspektrometrisch untersucht, so dass dadurch eindeutige Aussagen über die Substanzen, die die einzelnen Peaks darstellen gemacht werden können Hochdruckflüssigkeitschromatographie(HPLC) Der Aufbau der HPLC entspricht im Wesentlichen dem der GC. Hier ist die mobile Phase jedoch flüssig. Dadurch wird eine einfache Variation des Laufmittels oder des Laufmittelgemisches möglich. Statt der Temperatur kann bei der HPLC der Druck verändert werden. Die qualitative und quantitative Analyse entspricht der der GC. Allerdings gibt es eine größere Auswahl an Detektoren, zum Beispiel der UV/VIS-, der IR-, der Refraktometer- und der Polarimeterdetektor. Theoretisch ist auch bei der HPLC eine Kopplung mit MS möglich. 3. Durchführung Zunächst wurde nach der Anleitung (S)-3-Hydroxybutansäureethylester dargestellt und anschließend eine Derivatisierung mit (S)-Phenylethylisocyanat durchgeführt. Das erhaltene Produkt wurde mittels GC- und dann mittels HPLC-Messungen untersucht. Zum Vergleich wurde mit Raney-Nickel ein racemisches Gemisch an 3- Hydroxybutansäureethylester hergestellt und derivatisiert. Anschließend wurde nach 4
6 der ersten Vorschrift ein großer Ansatz an Produkt synthetisiert, so weit wie möglich aufgereinigt, und von diesem zur Überprüfung der Reinheit und der qualitativen Analyse ein NMR-Spektrum aufgenommen. 4. Experimentalteil 4.1 Darstellung von (S)-3-Hydroxybutansäureethylester Die Optimierung der Synthese von (S)-3-Hydroxybutansäureethylester mit Hilfe von Hefe war bereits Thema des OPII-Gruppenpräparats von H. Bürckstümmer, Y. Hemberger und J. Köhler im SS2006. Die dabei durchgeführten Versuche zeigten, dass eine Reduzierung der Ansatzgröße zum Teil zu drastischen Ausbeuteverlusten führte. Zur Herstellung von (S)-3-Hydroxybutansäureethylester wurde die hier optimierte Versuchsanleitung übernommen, mit der Ausnahme, dass die gesamte Umsetzung bei Raumtemperatur durchgeführt wurde. Die Synthese wurde in einem 3L-Rundkolben mit großem Rührfisch durchgeführt. Es wurden 300g Haushaltszucker in 1.6 L Wasser aufgelöst und 200 g Backhefe zugegeben. Nach einer Stunde wurden 20 g (0.15 mol) frisch destillierter Acetessigsäureethylester zugegeben. Nach 24 Stunden Rühren wurde ein Liter Zuckerlösung (200 g Zucker in 1 L Wasser) und nach einer Stunde weitere 20 g (0.15 mol) des Acetessigsäureethylesters zur Reaktionsmischung gegeben. Diese wurde weitere 120 Stunden in einem Wasserbad gerührt. Nach wiederholter Zugabe von 200 g Zucker wurde über Nacht weitergerührt. Eine DC-Kontrolle (Petrolether: Diethylether 1:1, KMnO 4 ) wies auf die vollständige Umsetzung des Acetessigsäureethylester hin. Zur Aufreinigung des Produkts wurden 80 g Celite zugegeben und die Hefe abfiltriert. Das Filtrat wurde mit Kochsalz gesättigt und fünfmal mit Diethylether extrahiert. Die organischen Phasen wurden vereinigt und das Lösungsmittel entfernt. Destillation des Rückstands ergab g eines farblosen Öls (58 C, 7 hpa, 14.2 mmol, 48%). 3 Charakterisierung: 1. Fraktion: m = g n 20 D = C 2. Fraktion: m = g n 20 D = C (60 hpa) 5
7 IR-Spektrum: Acetessigester: υ(c=o) = 1710cm -1, υ(cooet) = 1730cm -1 Hydroxybutansäureethylester: υ(oh) = 3450 cm -1 (breit), υ(cooet) = 1730cm -1, Sowohl der Siedepunkt als auch der Brechungsindex stimmen mit den Werten überein, die im Gruppenpräparat 2006 erhalten wurden. 4.2 Derivatisierung mit (S)-Phenylethylisocyanat 10 μl (77 μmol) (S)-3-Hydroxybutansäureethylester wurden in 5 ml absolutiertem Toluol unter Stickstoffatmosphäre mit 10 μl (71 μmol) (S)-Phenylethylisocyanat versetzt und 48 Stunden auf 90 C erhitzt. Das erhaltene Produkt wurde GC- bzw. HPLC analytisch untersucht. Die Synthese wurde mit einem großen Ansatz wiederholt. Hierbei wurden 2.7 ml (21 mmol) (S)-3-Hydroxybutansäureethylester und 3.0 ml (3,13g, 21 mmol) (S)- Phenylethylisocyanat in 500 ml Toluol verwendet Aktivierung von Raney-Nickel In einem 1L-Dreihalskolben wurden 600 ml einer 10%igen Natriumhydroxid-Lösung vorgelegt und über einen Zeitraum von 70 Minuten 40.0g (682 mmol) einer Nickel- Aluminium Legierung (50%) hinzugegeben. Es wurde noch 30 Minuten lang weiter gerührt und anschließend die Lösung abdekantiert. Der Rückstand wurde fünfmal mit je 200 ml Wasser und fünfmal mit je 50 ml Ethanol so gewaschen, dass der Feststoff ständig von Flüssigkeit bedeckt war. Bis zur weiteren Verwendung wurde das auf diese Weise aktivierte Raney-Nickel unter Ethanol aufbewahrt Synthese von rac-3-hydroxybutansäureethylester O O OEt Raney-Nickel EtOH, ΔT, 5h OH O OEt rac Es wurden 4.00g (3.93 ml, 30.7 mmol) Acetessigester zu einer Suspension von 20g Raney-Nickel in 100 ml Ethanol hinzugegeben und 5 Stunden lang unter Rückfluss 6
8 erhitzt. Nach dem Abkühlen wurde die Suspension filtriert und der Rückstand noch dreimal mit je 50 ml Ethanol gewaschen. Von den vereinigten Filtraten wurde im Vakuum das Lösungsmittel entfernt und der Rückstand fraktionierend destilliert. Destillation des Rückstands ergab 3.35g g eines farblosen Öls (25.3 mmol, 82%; Lit: 96%) 6 Charakterisierung: 1. Fraktion: m = 0.27 g n 20 D = nicht ermittelt C 2. Fraktion: m = 3.35 g n 20 D = C (60 hpa) IR-Spektrum: Acetessigester: υ(c=o) = 1710cm -1, υ(cooet) = 1730cm -1 Hydroxybutansäureethylester: υ(oh) = 3450 cm -1 (breit), υ(cooet) = 1730cm -1, 5. Auswertung und Diskussion der Spektren 5.1 Gaschromatographien Die Ausarbeitung einer Analytik mittels Gaschromatographie war die eigentliche Aufgabe des Gruppenpräparats. Nach Aufnahme des Übersichtsspektrums wurde versucht, durch Messungen der Einzelsubstanzen mit Hilfe des Ausschlussverfahrens die Substanzen den im Übersichtsspektrum enthaltenen Peaks zuzuordnen. Substanz Retentionszeit Derivat - (S)-3-Hydroxybutansäureethylester 2.92 min Toluol 2.54 min (S)-Phenylethylisocyanat 3.58 min Die Ausarbeitung einer GC-Analytik gestaltete sich im Praktikum auf Grund der gegebenen technischen Limitationen schwierig, da sich die in der Literatur vorgegebenen Bedingungen nicht realisieren ließen (Trägergas, Säule). Zudem ließ die Auflösung des Ausgabegeräts zu wünschen übrig. Die aufgenommenen Spektren 7
9 sind wenig aussagekräftig, insbesondere der eigentlich zu untersuchenden Substanz lässt sich auf keinem der aufgenommenen Spektren eindeutig ein Peak zuordnen. Auf Grund dieser Umstände erfolgte die weitere Analyse des Reaktionsgemischs mittels HPLC. 5.2 HPLC-Spektren Als Alternativmöglichkeit zur Gaschromatographie stand HPLC zur Verfügung. Hier konnten auf Grund der gegebenen Variationsmöglichkeiten in der Wahl des Eluenten, der größeren Auflösung des Ausgabegeräts und der schnelleren Durchführbarkeit deutlichbessere Ergebnisse erhalten werden. Um das Produkt zu identifizieren wurden vier Messreihen durchgeführt. 1. Messreihe Alle Spektren der 1. Messreihe wurden mit einem Laufmittel von 100 % frisch destilliertem Methanol durchgeführt. Zuerst wurde ein Spektrum des Derivats in Toluol angefertigt (Spektrum 1). Im Folgenden wurde, wie auch bei den gaschromatographischen Untersuchungen versucht, durch Einzelmessungen (Spektrum 2-4) und Abgleich der Retentionszeiten die einzelnen Substanzen zu identifizieren und den ensprechenden Peaks zuzuordnen. Folgende Ergebnisse wurden erhalten: Substanz Retentionszeit Derivat - (S)-3-Hydroxybutansäureethylester 3.47 min Toluol min (S)-Phenylethylisocyanat 2.33 min Da die Retentionszeiten der einzelnen Substanzen sehr nah beieinander lagen, kann man den vorliegenden Daten der ersten Messreihe nur wenig Aussagekraft zuordnen. Vor allem konnte kein Peak dem gewünschten Produkt eindeutig zugeordnet werden. Im Gegensatz zur Gaschromatographie, bei der eine Änderung des Eluenten nur umständlich möglich ist, bot HPLC hier eine einfache und schnelle Möglichkeit, durch Variation des Laufmittels eine bessere Trennleistung zu erzielen. 8
10 2. Messreihe Im Verlauf der zweiten Messreihe wurde ein Laufmittelgemisch von 60 % frisch destilliertem Methanol und 40 % HPLC-Wasser verwendet. Die Vorgehensweise deckt sich mit dem der ersten Messreihe. Substanz Retentionszeit Derivat 8.38 (S)-3-Hydroxybutansäureethylester 1.83 Toluol 10 (S)-Phenylethylisocyanat Hier konnte man im Übersichtsspektrum (Spektrum 1) deutlich einen Peak erkennen, der in keinem der Vergleichsspektren auftauchte (Substanz 012). Bei diesem Peak handelte es mit großer Wahrscheinlichkeit um das synthetisierte Derivat. Auffällig war, dass (S)-Phenylethylisocyanat einen Doppelpeak lieferte. Dieser Sachverhalt konnte auch im Rahmen der weiteren Untersuchungen nicht eindeutig geklärt werden, und es wird angenommen, dass es sich dabei um ein Zersetzungsprodukt des enantiomerenreinen Reagenzes auf der Säule handelt. Um die Reinheit von (S)- Phenylethylisocyanat sicherzustellen, wurde diese Substanz NMR-spektroskopisch untersucht. 3. Messreihe Da das in der zweiten Messreihe verwendete Laufmittelgemisch gute Ergebnisse lieferte, wurde auch in der dritten Messreihe damit gearbeitet. Diese Messreihe zielte darauf ab, die Ergebnisse aus der zweiten Messreihe zu bestätigen, und die eigentliche Aufgabe, nämlich die Bestimmung des Diastereomerenverhältnises zu lösen. Dazu wurden die Messungen mit einem aufgereinigten, größeren Ansatz der Substanz durchgeführt, der nur noch wenig Toluol enthielt. Substanz Retentionszeit Derivat 7.57 (S)-3-Hydroxybutansäureethylester 1.97 Toluol 10 (S)-Phenylethylisocyanat 3.38 Die Ergebnisse der zweiten Messreihe konnten größtenteils bestätigt werden, die Schwankungen der Retentionszeiten liegen im Toleranzbereich. Schön zu sehen ist, dass es sich beim Produkt eindeutig um zwei Substanzen mit unterschiedlichen 9
11 physikalischen Eigenschaften handelt. Leider konnten die beiden Peaks auf Grund der Überlagerung nicht getrennt voneinander integriert werden. 4. Messreihe Um die Ergebnisse der dritten Messreihe zu untermauern, wurde der Alkohol mit Hilfe von Raney-Nickel racemisch hergestellt und dann mit (S)-Phenylethylisocyanat umgesetzt. Wie erwartet fanden sich an der entsprechenden Stelle zwei annähernd gleich große Peaks, wodurch die Retentionszeiten aus der dritten Messreihe untermauert werden konnten. Substanz Derivat Retentionszeit min 5.3 NMR-Spektren Da zum gewünschten Produkt keine Vergleichsretentionszeiten auf der verwendeten Säule in der Literatur bekannt sind, musste zusätzlich zur HPLC noch eine qualitative Analyse der erhaltenen Substanz durchgeführt werden. Die NMR-Spektroskopie bietet ein einfaches, schnelles und trotzdem genaues Verfahren zur Analyse von unbekannten Substanzen, sowie zur Überprüfung ihrer Reinheit (S) Phenylethylisocyanat 1 H-NMR (250,13 MHz, gemessen in CDCl 3 ) δ=1,57 (d,3h) δ=4.78 (q,1h) δ=7.4 (s,5h) Von (S) Phenylethylisocyanat wurde zur Überprüfung der Reinheit ein NMR- Spektrum gemessen (s. HPLC Teil 3.3). Das Spektrum beweist, dass die Substanz sauber und frei von Verunreinigungen ist. 10
12 5.3.2 Derivat 1 H-NMR (250,13 MHz, gemessen in CDCl 3 ) O B O N H E Ph H A G F CO 2 D C δ= (m,6h) Protonen A,B δ= (d,3h) Protonen C δ= (m, 2H) Protonen F (diasterotop) δ= (m,2h) Protonen D δ=4.80 (m,1h) * δ= (m,1h) Proton E δ= (m,1h) Proton G δ= (m,5h) Protonen H * Dieses Signal konnte keinem Proton zugeordnet werden, entweder handelt es sich um eine Verunreinigung oder es gehört zu dem anderen entstandenen Diastereomer. Ansonsten erscheint das Produkt im Spektrum diastereomerenrein, mit einer leichten Verunreinigung durch Toluol, wobei natürlich berücksichtigt werden muss, dass in der Produktverteilung ein Diastereomer stark überwiegt. Es ist nicht ausgeschlossen, dass unter diesen Peaks die Signale des anderen Diastereomers liegen. Das Spektrum kann dahingehend gedeutet werden, dass der größte Teil von Reagenz und Edukt zum Produkt umgesetzt werden konnte. Eine Bestimmung des Diastereomerenverhältnisses ist aber anhand dieses Spektrums nicht möglich. 11
13 5.4 Perspektiven Der nächste logische Schritt zur weiteren Untersuchung wäre die Untersuchung der Substanz mittels GC-MS gewesen, was im Rahmen des Praktikums leider nicht mehr möglich war. Ein anderer angedachter Ansatz war die Trennung des reduzierten Zwischenprodukts mit chiraler Säule und anschließender Derivatisierung und HPLC- Analyse. Auch dieser Weg konnte aus Zeitmangel nicht mehr verfolgt werden. Eine weitere Verbesserung könnte auch mit Acetonitril als Laufmittel erreicht werden. Die Aufspaltung könnte hier noch besser werden. Durch die Ermittlung der Retentionszeiten auf der zur Verfügung stehenden Säule können die Substanzen jetzt ohne Schwierigkeiten mittels HPLC-Untersuchung charakterisiert werden. 6. Gesamtdiskussion Die ursprüngliche Aufgabe, das Bestimmen des Diastereomerenverhältnisses mittels GC-Analytik ließ sich mit der im Praktikum vorhandenen Ausrüstung nicht erfolgreich durchführen, weswegen die Analyse mittels HPLC durchgeführt wurde. Trotz einiger Unstimmigkeiten, die in der vorgegebenen Zeit nicht komplett ausgeräumt werden konnten konnte mittels HPLC-Analyse eine Retentionszeit für die im Praktikum vorhandene Säule ermittelt werden. Zudem wurde das Produkt mit Hilfe von NMR erstmals eindeutig charakterisiert, so dass eine Vergleichssubstanz für zukünftige Analysen zur Verfügung steht. 7. Literatur 1 D. Seebach, M. A. Sutter, R. H. Weber, M. F. Züger, Org. Synth, Col Vol. 1990, B.Kolb, Gaschromatographie in Bildern, 2. Aufl., Wiley-VCH, Org. Synth. Coll. Vol , Org. Synth. Coll. Vol , X. A. Dominguez, I. C. Lopez, R. Franco, J. Org. Chem. 1961, 26, R. Monzingo, C.Spencer, K. Folkers, J. Am. Chem. Soc. 1944, 66,
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol
 4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol OH
 4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester
 NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol
 4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
2. Herstellung der α,β-ungesättigten Kupplungskomponenten C H 3 H 33. Br 22 25
 2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 rganisch-chemisches Praktikum II WS 2008/2009 Gruppenpräparat Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Felix Bergler Benjamin Fröhlich Franziska Witterauf Inhaltsverzeichnis 1. Aufgabenstellung.
rganisch-chemisches Praktikum II WS 2008/2009 Gruppenpräparat Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Felix Bergler Benjamin Fröhlich Franziska Witterauf Inhaltsverzeichnis 1. Aufgabenstellung.
Betreuer: Tobias Olbrich Literatur: Nach Organic Syntheses Coll. Vol. 10 (2004), 96.
 rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
3021 Oxidation von Anthracen zu Anthrachinon
 xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
4006 Synthese von 2-(3-Oxobutyl)cyclopentanon-2- carbonsäureethylester
 4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus
 NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester
 NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
5 HPLC-Methodenentwicklung zur Isomerentrennung
 HPLC-Untersuchungen 5 HPLC-Untersuchungen 65 5 HPLC-Methodenentwicklung zur Isomerentrennung Die bei der -Substitution des Benzimidazolgrundgerüstes entstehenden Isomere machen eine nachfolgende Trennung
HPLC-Untersuchungen 5 HPLC-Untersuchungen 65 5 HPLC-Methodenentwicklung zur Isomerentrennung Die bei der -Substitution des Benzimidazolgrundgerüstes entstehenden Isomere machen eine nachfolgende Trennung
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen
 3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
4010 Synthese von p-methoxyacetophenon aus Anisol
 4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
NO 2 Rühren mit Magnetrührer, Extrahieren, Ausschütteln, Abrotieren, Umkristallisieren, Abfiltrieren,
 1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol
 3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester
 NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
3012 Synthese von Adamantylidenadamantan aus Adamantanon
 Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon)
 1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
4002 Synthese von Benzil aus Benzoin
 4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
Protokoll zum Gruppenpra parat
 Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol
 4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
1035 Synthese von p-methoxyacetophenon aus Anisol
 NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid
 1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
Organisch chemisches Praktikum II
 18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
Mustervorschrift 2.3.1
 Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:
![Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer: Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:](/thumbs/55/37246535.jpg) Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
3011 Synthese von erythro-9,10-dihydroxystearinsäure aus Ölsäure
 311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
Synthese von 1-(p-Tolyl)butan-1,4-diol
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1-(p-Tolyl)butan-1,4-diol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 07. April
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1-(p-Tolyl)butan-1,4-diol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 07. April
Schriftliche Prüfung BSc Herbst 2007
 Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
3016 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure
 6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b).
 2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
Organisches Praktikum I - SS 2006 Assistentin: Gabi Marti. Synthese von. Isobutylacetat. Zürich, Balzers & Eschen, Mai 2005
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion)
 4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol
 Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
2-Methylcyclohexanon
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
2017 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid
 217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol
 7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
!!! NEUE ÖAB-MONOGRAPHIE!!!
 !!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2008
!!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2008
Organisch Chemisches Praktikum II. Gruppenpräparat: Darstellung von Z Crotonsäure
 Organisch Chemisches Praktikum II Gruppenpräparat: 5.3.1.1 Darstellung von Z Crotonsäure Gruppe 5: Andreas Kraft Thomas Kramer Johannes Landmann Datum: 3.10.2009 Aufgabenstellung: Die Aufgabe bestand darin,
Organisch Chemisches Praktikum II Gruppenpräparat: 5.3.1.1 Darstellung von Z Crotonsäure Gruppe 5: Andreas Kraft Thomas Kramer Johannes Landmann Datum: 3.10.2009 Aufgabenstellung: Die Aufgabe bestand darin,
Protokoll zur Übung Ölanalyse
 Protokoll zur Übung Ölanalyse im Rahmen des Praktikums Betreuender Assistent Univ.Ass. Dipl.-Ing. Martin Schwentenwein Verfasser des Protokolls: Daniel Bomze 0726183 1 Theoretischer Hintergrund 1.1 Aufgabenstellung
Protokoll zur Übung Ölanalyse im Rahmen des Praktikums Betreuender Assistent Univ.Ass. Dipl.-Ing. Martin Schwentenwein Verfasser des Protokolls: Daniel Bomze 0726183 1 Theoretischer Hintergrund 1.1 Aufgabenstellung
Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2004
 Prüfungen Analytische Chemie Dienstag, 1. September 4 Schriftliche Prüfung. Vordiplom / BSc erbst 4 D CAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Dienstag, 1. September 4 Schriftliche Prüfung. Vordiplom / BSc erbst 4 D CAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Organisch-chemisches Praktikum Wintersemester 2005/06. 1-Phenyl-propan-1-ol. Stephan Steinmann
 Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Original oder Fälschung?
 Original oder Fälschung? Eine Analyse von Medikamenten Schlussbericht Studienwoche 15 Schweizer Jugend forscht Autor: Gian Fadri Beeli, Kantonsschule Chur Betreuungspersonen: Dr. Christian Guenat, Novartis
Original oder Fälschung? Eine Analyse von Medikamenten Schlussbericht Studienwoche 15 Schweizer Jugend forscht Autor: Gian Fadri Beeli, Kantonsschule Chur Betreuungspersonen: Dr. Christian Guenat, Novartis
1005 Bromierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol
 1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
1024 Eliminierung von Wasser aus 4-Hydroxy-4-methyl-2- pentanon
 0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
Schriftliche Prüfung BSc Frühling 2008
 Prüfungen Analytische Chemie Samstag, 9. Februar 2008 Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Samstag, 9. Februar 2008 Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Schriftliche Prüfung BSc Frühling 2010
 Prüfungen Analytische Chemie Donnerstag, 11. Februar 2010 Schriftliche Prüfung BSc Frühling 2010 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Donnerstag, 11. Februar 2010 Schriftliche Prüfung BSc Frühling 2010 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Analytische Chemie (für Biol. / Pharm. Wiss.)
 Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst Laboratory of Organic Chemistry HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/
Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst Laboratory of Organic Chemistry HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/
Gruppenpräparat im Rahmen des organisch-chemischen Praktikums II im Wintersemester 2006/2007 an der Universität Würzburg
 Gruppenpräparat im Rahmen des organisch-chemischen raktikums II im Wintersemester 2006/2007 an der Universität Würzburg Versuch 10.1.1: Trennung eines racemischen Gemisches aus (M)- und ()-2,2 -Dihydroxy-1,1
Gruppenpräparat im Rahmen des organisch-chemischen raktikums II im Wintersemester 2006/2007 an der Universität Würzburg Versuch 10.1.1: Trennung eines racemischen Gemisches aus (M)- und ()-2,2 -Dihydroxy-1,1
Titanocendichlorid. AC-F Praktikum Wintersemester 2012/13. Iman Errouihi 12.12.2012. Inhaltsverzeichnis
 AC-F Praktikum Wintersemester 2012/13 Titanocendichlorid Iman Errouihi 12.12.2012 Inhaltsverzeichnis 1 Das Experiment Titanocendichlorid 2 1.1 Reaktionsgleichung............................... 2 1.2 Ansatz......................................
AC-F Praktikum Wintersemester 2012/13 Titanocendichlorid Iman Errouihi 12.12.2012 Inhaltsverzeichnis 1 Das Experiment Titanocendichlorid 2 1.1 Reaktionsgleichung............................... 2 1.2 Ansatz......................................
Synthese von Benzalacetophenon
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von Benzalacetophenon Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 10. März 2008 page
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von Benzalacetophenon Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 10. März 2008 page
2023 Reduktion von D-(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b).
 23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
2008 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester
 28 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester H 3 C H 4-Toluolsulfonsäure + Cyclohexan H 3 C H CH 3 + CH 3 H 2 C 3 H 6 2 (74.1) C 4 H 1 (74.1) C 7 H 8 3 S
28 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester H 3 C H 4-Toluolsulfonsäure + Cyclohexan H 3 C H CH 3 + CH 3 H 2 C 3 H 6 2 (74.1) C 4 H 1 (74.1) C 7 H 8 3 S
Synthese von Acetessigsäureethylester
 Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
1007 Synthese von 2,4,6-Tribromanilin aus 4-Bromacetanilid
 1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon
 Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
170 C C 2 H C C 11 H 10 (174.2) Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien
 3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
2002 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan
 22 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan 2 H 5 + H H Montmorillonit K 1 yclohexan 2 H 5 + H 2 6 H 1 3 (13.1) 2 H 6 2 (62.1) 8 H 14 4 (174.2)
22 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan 2 H 5 + H H Montmorillonit K 1 yclohexan 2 H 5 + H 2 6 H 1 3 (13.1) 2 H 6 2 (62.1) 8 H 14 4 (174.2)
Schriftliche Prüfung BSc Herbst 2013
 Prüfungen Analytische Chemie Dienstag, 13. August 2013 Schriftliche Prüfung BSc Herbst 2013 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Dienstag, 13. August 2013 Schriftliche Prüfung BSc Herbst 2013 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
SALICYLAMID. Salicylamidum Salicylsäureamid. 2-Hydroxybenzamid Gehalt: 99,0 bis 101,0% Salicylamid (getrocknete Substanz)
 SALICYLAMID Salicylamidum Salicylsäureamid C7H7NO2 Mr = 137,1 CAS Nr. 65-45-2 Definition 2-Hydroxybenzamid Gehalt: 99,0 bis 101,0% Salicylamid (getrocknete Substanz) Eigenschaften: Aussehen: weißes bis
SALICYLAMID Salicylamidum Salicylsäureamid C7H7NO2 Mr = 137,1 CAS Nr. 65-45-2 Definition 2-Hydroxybenzamid Gehalt: 99,0 bis 101,0% Salicylamid (getrocknete Substanz) Eigenschaften: Aussehen: weißes bis
Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse
 Michael Seitz (aum 33.1.23, Tel.: 943-4647) Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse Durchzuführende eaktionen: 1. NaH, DMS 2. MeI MeS NH 2 K 2 C 3 Glycerin / Ethylenglykol
Michael Seitz (aum 33.1.23, Tel.: 943-4647) Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse Durchzuführende eaktionen: 1. NaH, DMS 2. MeI MeS NH 2 K 2 C 3 Glycerin / Ethylenglykol
Ein Gemisch aus 13,2 g (0,1mol) 2,5-Dimethoxyterahydrofuran und 80ml 0,6 N Salzsäure werden erhitzt bis vollständige Lösung eintritt.
 1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol
 1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
Tris(acetylacetonato)cobalt(III)
 Tris(acetylacetonato)cobalt(III) [Co(C5H7)3] Cobalt(III)acetylacetonat Zürich, 7. November 004 Raphael Aardoom, ACP 1 Synthese 1.1 Methode [1] Cobalt(II)carbonat reagiert mit Acetylaceton in Gegenwart
Tris(acetylacetonato)cobalt(III) [Co(C5H7)3] Cobalt(III)acetylacetonat Zürich, 7. November 004 Raphael Aardoom, ACP 1 Synthese 1.1 Methode [1] Cobalt(II)carbonat reagiert mit Acetylaceton in Gegenwart
5026 Oxidation von Anthracen zu Anthrachinon
 NP 506 xidation von Anthracen zu Anthrachinon KMn /Al C H 0 KMn C H 8 (78.) (58.0) (08.) Literatur Nüchter, M., ndruschka, B., Trotzki, R., J. Prakt. Chem. 000,, No. 7 Klassifizierung Reaktionstypen und
NP 506 xidation von Anthracen zu Anthrachinon KMn /Al C H 0 KMn C H 8 (78.) (58.0) (08.) Literatur Nüchter, M., ndruschka, B., Trotzki, R., J. Prakt. Chem. 000,, No. 7 Klassifizierung Reaktionstypen und
1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid
 NP 1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid KBr 3, HBr Essigsäure Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Literatur P.F. Schatz, J. chem.
NP 1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid KBr 3, HBr Essigsäure Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Literatur P.F. Schatz, J. chem.
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien
 3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
SKRIPT ZUM INTEGRIERTEN SYNTHESEPRAKTIKUM
 Integriertes Synthesepraktikum 2016 rganische Chemie SKRIPT ZUM ITEGRIERTE SYTHESEPRAKTIKUM Woche 1 und 2 (rganische Chemie) 1. Herstellung eines Alkens über die lefinierung eines Aldehyds nach Wittig
Integriertes Synthesepraktikum 2016 rganische Chemie SKRIPT ZUM ITEGRIERTE SYTHESEPRAKTIKUM Woche 1 und 2 (rganische Chemie) 1. Herstellung eines Alkens über die lefinierung eines Aldehyds nach Wittig
Analytische Methoden zum Nachweis der Reinheit von Enantiomeren und Diastereomeren :
 Analytische Methoden zum Nachweis der Reinheit von Enantiomeren und Diastereomeren : durch Polarimetrie durch NMR-Spektroskopie - NMR-Spektroskopie mit chiralen shift-reagenzien - NMR-Spektroskopie diastereomerer
Analytische Methoden zum Nachweis der Reinheit von Enantiomeren und Diastereomeren : durch Polarimetrie durch NMR-Spektroskopie - NMR-Spektroskopie mit chiralen shift-reagenzien - NMR-Spektroskopie diastereomerer
Gruppenpräparat 8.5. Darstellung von 2,4,6 Triphenyl N (3,5 di tert. butyl 4 hydroxyphenyl) pyridinium tetrafluoroborat und entsprechendes Betain
 Gruppenpräparat 8.5 Darstellung von 2,4,6 Triphenyl N (3,5 di tert. butyl 4 hydroxyphenyl) pyridinium tetrafluoroborat und entsprechendes Betain NaN 2,5nHCl H N Zn/HCl Cl NH 3 t-bu t-bu H C 14 H 22 206.33
Gruppenpräparat 8.5 Darstellung von 2,4,6 Triphenyl N (3,5 di tert. butyl 4 hydroxyphenyl) pyridinium tetrafluoroborat und entsprechendes Betain NaN 2,5nHCl H N Zn/HCl Cl NH 3 t-bu t-bu H C 14 H 22 206.33
Schriftliche Prüfung BSc Frühling 2014
 Prüfungen Analytische Chemie Samstag, 1. Februar 2014 Schriftliche Prüfung BSc Frühling 2014 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Samstag, 1. Februar 2014 Schriftliche Prüfung BSc Frühling 2014 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Chloro(salen*)mangan(III)
 Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Chemiepraktikum für Biologen. Versuchsprotokoll. Einzelanalyse Trennung, Reinigung, Nachweis von 3 Reinsubstanzen
 Johannes Gutenberg Universität Fachbereich Biologie hemiepraktikum für Biologen SS 2002 Versuchsprotokoll zum Thema Einzelanalyse Trennung, Reinigung, achweis von 3 Reinsubstanzen von Ausgangslösung: Die
Johannes Gutenberg Universität Fachbereich Biologie hemiepraktikum für Biologen SS 2002 Versuchsprotokoll zum Thema Einzelanalyse Trennung, Reinigung, achweis von 3 Reinsubstanzen von Ausgangslösung: Die
Gruppenpräparat: Versuch Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)- ethanon
 P II Praktikum im WS 2008/2009 Gruppenpräparat: Versuch 7.4.1.1 Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)- ethanon 1.Gruppe: Christoph Mann Marco Schott 2.Gruppe: Tim Walter Holger Hartleb Stefan
P II Praktikum im WS 2008/2009 Gruppenpräparat: Versuch 7.4.1.1 Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)- ethanon 1.Gruppe: Christoph Mann Marco Schott 2.Gruppe: Tim Walter Holger Hartleb Stefan
Synthese von cis- und trans-stilben
 28. April 2008 eifer Manuel raktikum in Organischer Chemie (OC 1) Frühjahrssemester 2008 529-0230-00L eifer Manuel Synthese von cis- und trans-stilben Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich
28. April 2008 eifer Manuel raktikum in Organischer Chemie (OC 1) Frühjahrssemester 2008 529-0230-00L eifer Manuel Synthese von cis- und trans-stilben Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich
Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich,
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich,
Schriftliche Prüfung BSc Herbst 2010
 Prüfungen Analytische Chemie Dienstag, 24. August 2010 Schriftliche Prüfung BSc Herbst 2010 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Dienstag, 24. August 2010 Schriftliche Prüfung BSc Herbst 2010 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Analytische Chemie (für Biol. / Pharm. Wiss.)
 Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst Laboratory of Organic Chemistry HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/
Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst Laboratory of Organic Chemistry HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/
Schriftliche Prüfung BSc Herbst 2014
 Prüfungen Analytische Chemie Montag, 25. August 2014 Schriftliche Prüfung BSc Herbst 2014 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt 36.
Prüfungen Analytische Chemie Montag, 25. August 2014 Schriftliche Prüfung BSc Herbst 2014 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt 36.
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b
 3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
5001 Nitrierung von Phenol zu 2-Nitrophenol und 4-Nitrophenol
 00 Nitrierung von Phenol zu -Nitrophenol und -Nitrophenol KNO, H SO NO + NO C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile Substitution an Aromaten,
00 Nitrierung von Phenol zu -Nitrophenol und -Nitrophenol KNO, H SO NO + NO C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile Substitution an Aromaten,
1017 Azokupplung von Benzoldiazoniumchlorid mit 2-Naphthol zu 1-Phenylazo-2-naphthol
 OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
Gruppenpräparat im Organisch-Chemischen Praktikum II
 Gruppenpräparat im rganisch-chemischen Praktikum II WS 2007/2008 Versuch 6.2.3 Philipp Bissinger Alexander Damme Yvonne Göbel Inhaltsverzeichnis 1. Einleitung 2. Darstellungsmethoden 2.1 Darstellung von
Gruppenpräparat im rganisch-chemischen Praktikum II WS 2007/2008 Versuch 6.2.3 Philipp Bissinger Alexander Damme Yvonne Göbel Inhaltsverzeichnis 1. Einleitung 2. Darstellungsmethoden 2.1 Darstellung von
3002 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure
 32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
2028 Reaktion von Cyclohexylmagnesiumbromid mit Kohlendioxid zu Cyclohexancarbonsäure
 28 Reaktion von Cyclohexylmagnesiumbromid mit Kohlendioxid zu Cyclohexancarbonsäure Br + Mg Diethylether MgBr 1. CO 2 2. H 3 O O OH C 6 H 11 Br CO 2 (163.1) (24.3) (44.) C 7 H 12 O 2 (128.2) Klassifizierung
28 Reaktion von Cyclohexylmagnesiumbromid mit Kohlendioxid zu Cyclohexancarbonsäure Br + Mg Diethylether MgBr 1. CO 2 2. H 3 O O OH C 6 H 11 Br CO 2 (163.1) (24.3) (44.) C 7 H 12 O 2 (128.2) Klassifizierung
Versuch 2.3.1: Darstellung von 1,2- Bis(trimethylsilyloxy)cyclohex-1-en (Gruppenpräparat)
 Institut für Organische Chemie Würzburg 13.04.2012 Versuch 2.3.1: Darstellung von 1,2- Bis(trimethylsilyloxy)cyclohex-1-en (Gruppenpräparat) Christoph Böhm und Thorsten Scherpf Philipp Hennig und Junwen
Institut für Organische Chemie Würzburg 13.04.2012 Versuch 2.3.1: Darstellung von 1,2- Bis(trimethylsilyloxy)cyclohex-1-en (Gruppenpräparat) Christoph Böhm und Thorsten Scherpf Philipp Hennig und Junwen
Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006
 Prüfungen Analytische Chemie Mittwoch, 27. September 2006 Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Prüfungen Analytische Chemie Mittwoch, 27. September 2006 Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Schriftliche Prüfung 2. Vordiplom Herbst 2003
 Prüfungen Analytische hemie Mittwoch, 1. ktober 2003 Schriftliche Prüfung 2. Vordiplom erbst 2003 D AB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische hemie Mittwoch, 1. ktober 2003 Schriftliche Prüfung 2. Vordiplom erbst 2003 D AB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Extraktion von Hesperidin aus Mandarinenschalen
 Extraktion von Hesperidin aus Mandarinenschalen Diese Arbeitsvorschrift für Sie ist eine Weiterentwicklung derjenigen aus Lit. [1]! HO H3 C HO 4 ''' 6 ''' 5 ''' 3 ''' O OH 2 ''' 1'' ' O OCH 2 3 6 '' '
Extraktion von Hesperidin aus Mandarinenschalen Diese Arbeitsvorschrift für Sie ist eine Weiterentwicklung derjenigen aus Lit. [1]! HO H3 C HO 4 ''' 6 ''' 5 ''' 3 ''' O OH 2 ''' 1'' ' O OCH 2 3 6 '' '
Oxidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) CO 2
 6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
4009 Synthese von Adipinsäure aus Cyclohexen
 4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
Darstellung von Chelidamsäure (gekürzte Version)
 CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren Brombutanen
 1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
Endersch, Jonas 09./
 Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
1. Darstellung von 2-Chlor-2-methylpropan Trivialname: tert. Butylchlorid
 1. Darstellung von 2-Chlor-2-methylpropan Trivialname: tert. Butylchlorid Theorie Nucleophile Substitution 1. Ordnung am gesättigten Kohlenstoffatom. Darstellung tertiärer Alkylhalogenide durch Umsetzung
1. Darstellung von 2-Chlor-2-methylpropan Trivialname: tert. Butylchlorid Theorie Nucleophile Substitution 1. Ordnung am gesättigten Kohlenstoffatom. Darstellung tertiärer Alkylhalogenide durch Umsetzung
Synthese 1 Herstellung von. Cyclohex-3-en-1,1-diyldimethanol
 Organisch-Chemisches Praktikum 1 (OCP 1) HS 10/11 Assistenten: Daniel Fankhauser, Lorenz Urner Synthese 1 Herstellung von Cyclohex-3-en-1,1-diyldimethanol Bastian Vögeli Versuch: 21./22. Oktober 2010 1
Organisch-Chemisches Praktikum 1 (OCP 1) HS 10/11 Assistenten: Daniel Fankhauser, Lorenz Urner Synthese 1 Herstellung von Cyclohex-3-en-1,1-diyldimethanol Bastian Vögeli Versuch: 21./22. Oktober 2010 1
Synthese von 3-Menthen
 Synthese von 3-Menthen Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 22/29.11.25 Rémy Denzler, D-Biol 1 1. Methode (-)-Menthol wird in einer säurekatalysierten E1-Eliminierungsreaktion
Synthese von 3-Menthen Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 22/29.11.25 Rémy Denzler, D-Biol 1 1. Methode (-)-Menthol wird in einer säurekatalysierten E1-Eliminierungsreaktion
Gruppenpräparat zu V Cis-9-Methyl-2-decalon
 rganisch-chemisches-praktikum II WS 2007/2008 Gruppenpräparat zu V 6.2.2 Cis-9-Methyl-2-decalon Gruppe: E / F Jürgen Bauer Nadja Bertleff Daniel Ertler Johannes Klein Eva Siedler Johannes Wahler 1 Inhaltsverzeichnis:
rganisch-chemisches-praktikum II WS 2007/2008 Gruppenpräparat zu V 6.2.2 Cis-9-Methyl-2-decalon Gruppe: E / F Jürgen Bauer Nadja Bertleff Daniel Ertler Johannes Klein Eva Siedler Johannes Wahler 1 Inhaltsverzeichnis:
