Serinpeptidasen.
|
|
|
- Jörg Friedrich
- vor 7 Jahren
- Abrufe
Transkript
1 Serinpeptidasen 1
2 Klassifizierung der Peptidasen Peptidasen (alt, Proteasen) Endopeptidasen (Proteinasen) Exopeptidasen Endopeptidasen H 2 N CH H 2 N Exopeptidasen CH 2
3 Endopeptidasen: 5 Untergruppen Einteilung nach katalytischem Mechanismus Serin-Endopeptidasen EC Cystein- Endopeptidasen EC Aspartat- Endopeptidasen EC Metallo- Endopeptidasen EC Threonin- Endopeptidasen EC Adressen über Peptidasen: 3
4 Spezifitätsstellen bei Endopeptidasen nach Schechter & Berger, 1967 Hydrolyse Substrat H 2 N P 4 P 3 P 2 P 1 P 1 ' P 2 ' P 3 ' P 4 ' CH Enzym S 4 S 3 S 2 S 1 S 1 ' S 2 ' S 3 ' S 4 ' Aspartat-Endopeptidase 4
5 Die Serinpeptidasen 180+ bekannte Enzyme Gliederung in Clans und Familien Katalyse: Ser, His, Asp (katalytische Triade) Serin: nucleophiler Angriff 5
6 Chymotrypsin Die gefaltete Struktur ist für die Aktivität notwendig (gilt für alle Enzyme) 6
7 Chymotrypsin Eglin c Hemmer 7
8 Die katalytische Triade Die Nummerierung (57, 102 und 195), die z. B. für Trypsin, Chymotrypsin und Elastase gilt, entspricht der Primärstruktur des Rinder-Chymotrypsinogens. 8
9 Chymotrypsin: Mechanismus (1) S1 N-Terminus CH 2 Ser 195 CH 2 H N C HN CH Hydrolyse Enzym-Substrat Komplex His 57 N H C Säure-Base Katalyse (His 57 ) elektrostatische Katalyse (Asp 102 begraben) Asp 102 C-Terminus 9
10 Chymotrypsin: Mechanismus (2) S1 Nucleophiler Angriff des Ser im aktiven Zentrum auf das Carbonyl C-Atom der zu spaltenden Bindung des tetrahedrischen Überganszustands Ser 195 CH 2 N NH CH 2 CH C NH N-Terminus Erstes tetraedrisches Zwischenprodukt (ähnelt dem Übergangszustand) His 57 Säurekatalyse durch das von Asp polarisierte His im aktiven Zentrum H C Kovalente Katalyse Asp 102 C-Terminus 10
11 Chymotrypsin: Mechanismus (3) S1 N-Terminus CH 2 Ser 195 CH 2 N CH C HNH Acyl-Enzym Intermediat (kovalent) N His 57 H Säurekatalyse durch das von Asp polarisierte His im aktiven Zentrum, gefolgt vom Abgang des Produkts (Cterminales Segment) C Asp 102 C-Terminus 11
12 Chymotrypsin: Mechanismus (4) S1 N-Terminus CH 2 Ser 195 CH 2 C CH N H H Acyl-Enzym-H 2 Komplex N His 57 H Säurekatalyse durch das von Asp polarisierte His im aktiven Zentrum, gefolgt vom Abgang des Produkts (Cterminales Segment) und dessen Ersatz durch ein Wassermolekül. C Asp
13 Chymotrypsin: Mechanismus (5) S1 N-Terminus CH 2 Ser 195 CH 2 C CH H NH Zweites tetraedrisches Zwischenprodukt His 57 H N C Asp
14 Chymotrypsin: Mechanismus (6) S1 N-Terminus Ser 195 CH 2 H N C CH 2 CH His 57 H N H C Freies Enzym Asp
15 Katalytischer Mechanismus (7) Mischung von kovalenter und Säure-Base Katalyse Asp 102 : orientiert His 57 His 57 : Säure-Base Funktion Ser 195 : kovalente Bindung mit Peptid (nucleophiler Angriff auf Carbonyl-Sauerstoff der Peptidbindung) Bildung eines tetrahedrischen Zwischenprodukts und seine Stabilisierung im xyanion-loch durch NHs von Gly 193 und Ser
16 Stabilisierung des Übergangszustandes (8) xyanion-loch Trigonales Carbonyl-C-Atom noch nicht in der richtigen Konformation für die Bindung im xyanion-loch Tetrahedrisches Carbonyl-C-Atom bindet im xyanion-loch 16
17 Acyl-Enzym-Zwischenprodukt (9) Die Kinetik der prästationären Phase liefert den Hinweis auf ein Acyl-Enzym- Zwischenprodukt. Die Hydrolyse von p-nitrophenylacetat durch Chymotrypsin wird anhand der Freisetzung von p-nitrophenol (ein farbiges Produkt) gemessen. Gleich zu Beginn der Reaktion kommt es zu einer raschen Freisetzung von p-nitrophenol; die freigesetzte Menge ist nahezu stöchiometrisch mit der Menge an vorhandenem Enzym. Dies spiegelt die schnelle Acylierungsphase der Reaktion wider. Anschließend verläuft die Reaktion langsamer, weil der Enzymumsatz durch die geringere Geschwindigkeit der Deacylierungsphase begrenzt wird. (Abbildung 6-19 im Lehningers Biochemie Buch). 17
18 Hemmung der Serinpeptidasen durch DIFP CH(CH 3 ) 2 CH(CH 3 ) 2 Enzym-Ser CH 2 H + F P Enzym-Ser CH 2 P + HF CH(CH 3 ) 2 kovalent CH(CH 3 ) 2 Diisopropylfluorophosphat (DIFP) Gefährlich: Nervengift, inaktiviert die Acetylcholinesterase 18
19 Acetylcholinesterase (EC ) (CH 3 ) 3 N CH 2 CH 2 C Acetylcholin (Neurotransmitter) CH 3 Acetylcholinestarase e H 2 (CH 3 ) 3 N CH 2 CH 2 H + C CH + H + 3 Cholin Die Aktivität der Acetylcholinesterase ist, wie bei Chymotrypsin, von einem katalytischen Serinrest abhängig. Acetylcholin wirkt als Neurotransmitter und vermittelt Nervenimpulse durch Synapsen. Acetylcholinesterase baut schnell Acetylcholin ab und somit dauern die Nervenimpulse nur etwa eine Millisekunde. 19
20 Affinitätsmarkierung der Serinpeptidasen Peptidase Peptidase CH 2 CH 2 H Cl N HCl CH 2 N N C N R Chloromethylketon CH 2 Kovalente Bindung mit Histidin im aktiven Zentrum C R 20
21 Spezifische Affinitätsmarkierung Tosyl-Phe-Chloromethylketon Spezifisch für Chymotrypsin H 3 C S CH 2 NH CH C CH 2 Cl NH 3 (CH 2 ) 4 Tosyl-Lys-Chloromethylketon Spezifisch für Trypsin H 3 C S NH CH C CH 2 Cl 21
22 Inhibitor für Serinpeptidasen Ser Cl CCl His Cl Cl 3,4-Dichlorisocoumarin (DCI) Allg. Mechanismbasierte Serinpeptidase Inhibitor C Ser His Cl 22
23 Evolutionäre Verwandtschaft (1) Trypsin, Chymotrypsin und Elastase 40 % Sequenzhomologie Reihenfolge der katalytischen Triade H 2 N His Asp Ser CH 'Ur'-Enzym Genduplikation Divergente Evolution 23
24 Evolutionäre Verwandtschaft (2) H 2 N Subtilisin (Bacillus subtilis) Asp His Ser CH H 2 N Chymotrypsin (Säugetiere) His Asp Ser CH H 2 N Serin Carboxypeptidase II (Weizen) Ser Asp His CH Keine Sequenzhomologie Konvergente Evolution Gleicher katalytischer Mechanismus auf drei unterschiedlichen Wegen gefunden 24
25 Die pankreatischen Serinpeptidasen Trypsin Chymotrypsin Elastase Ser Spezifisch für: Asp Arg, Lys Phe, Trp, Tyr Ala, Val elektrostatische WW van der Waals WW 25
26 Leber Bauchspeicheldrüse = Pankreas Milz Gallenblase Zwölffingerdarm (Duodenum) Aktive Enzyme Bauchspeicheldrüse (Pankreas) Inaktive Enzymvorstufen 26
27 Die Zymogene Inaktive Vorstufen = Zymogene (zum Schutz vor frühzeitiger Proteolyse) Limitierte Proteolyse Aktive Enzyme (die Aktivierung findet erst am Zielort statt) 27
28 Zymogene der pankreatischen Peptidasen Trypsinogen Chymotrypsinogen Proelastase Procarboxypeptidase A Procarboxypeptidase B Im Pankreas als inaktive Zymogene (Schutz vor Selbstverdauung). Die Aktivierung findet im Duodenum statt. 28
29 Warum sind Zymogene inaktiv? Inaktiv wegen Verzerrung des aktiven Zentrums Schutz des aktiven Zentrums durch Peptid Abspaltung eines Peptids Das aktive Zentrum wird frei Konformationsänderungen Ausbildung der Substratbindungstasche 29
30 Aktivierung eines Asp-Endopeptidases Anfang Intermediat Ende 30
31 Aktivierung des Trypsinogens Trypsinogen (inaktiv) Trypsin (aktiv) Enteropeptidase Im Duodenum Trypsinogen (inaktiv) Trypsin (autokatalytisch) Trypsin (aktiv) 31
32 Aktivierung der anderen Zymogene Trypsin Chymotrypsinogen Chymotrypsin Proelastase Elastase Procarboxypeptidase A Procarboxypeptidase B Carboxypeptidase A Carboxypeptidase B 32
33 Aktivierung des Chymotrypsinogens Chymotrypsinogen (inaktiv) S S S S -Chymotrypsin (aktiv) Trypsin Im Duodenum S S S S -Chymotrypsin -Chymotrypsin (aktiv) + S S S S 33
34 Schutzmechanismen BPTI (bovine pancreatic trypsin inhibitor) Elektrostatische Abstossung mit Asp 189 in S 1 Trypsinogen: Val-(Asp) 4 -Lys-Ile-Val-(.) Zymogengranula: Pankreatische Zymogene sind in intrazellulären Vesikeln gespeichert 34
35 Intravaskuläres System Kininogen, Kallikrein Faktor XII XII a Faktor XI Blutgerinnungskaskade Die Blutgerinnungskaskade Extravaskuläres System Gefässverletzung XI a Gewebefaktor Faktor IX IX a Faktor VIII VIII a VII a - Gewebefaktor Faktor VII- Gewebefaktor Faktor X X a Faktor X Faktor V V a Gemeinsamer Weg Prothrombin Thrombin Fibrinogen Fibrin XIII a Faktor XIII Quervernetztes Fibringerinnsel 35
36 Regulatorische Kaskadenverstärkung Signal (Hormon, Peptid, ) Verstärkung Inaktives Enzym A 10x Aktives Enzym A 10x Inaktives Enzym B 10x Aktives Enzym B 100x Inaktives Enzym C 10x Aktives Enzym C 1000x Substrat Produkt 36
37 Aktuelle Forschung (Exkurs 1) 37
38 Aspartat-Endopeptidase (Exkurs 2) 38
39 Aspartat-Endopeptidase (Exkurs 2) 39
40 Serin-Endopeptidase (Exkurs 3) 40
41 Tyrosin Kinase (Exkurs 4) 41
Hemmung der Enzym-Aktivität
 Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Peptide Proteine. 1. Aminosäuren. Alle optisch aktiven proteinogenen Aminosäuren gehören der L-Reihe an: 1.1 Struktur der Aminosäuren
 1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
Praktikum Biochemie B.Sc. Water Science WS Enzymregulation. Marinja Niggemann, Denise Schäfer
 Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
4. Hydrolytisch aktive Enzyme und Gruppentransfer-Reaktionen
 4. Hydrolytisch aktive Enzyme und Gruppentransfer-Reaktionen In der Natur gibt es prinzipiell drei Arten von Hydrolasen (hydrolytisch aktiven Enzymen), die die unterschiedlichen in der Natur vorhandenen
4. Hydrolytisch aktive Enzyme und Gruppentransfer-Reaktionen In der Natur gibt es prinzipiell drei Arten von Hydrolasen (hydrolytisch aktiven Enzymen), die die unterschiedlichen in der Natur vorhandenen
Hemmung der Enzym-Aktivität
 Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Aminosäurenanalytik. Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE
 Aminosäurenanalytik Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE Proteinfällung 2 Proteinfällung 3 Proteinfällung 4 Proteinfällung 5 Proteinfällung
Aminosäurenanalytik Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE Proteinfällung 2 Proteinfällung 3 Proteinfällung 4 Proteinfällung 5 Proteinfällung
Enzyme. Prof. Dr. Albert Duschl
 Enzyme Prof. Dr. Albert Duschl Katalyse Reaktionen laufen normalerweise nicht spontan ab, auch wenn insgesamt dabei Energie gewonnen werden sollte. Es muß zunächst eine Aktivierungsenergie aufgebracht
Enzyme Prof. Dr. Albert Duschl Katalyse Reaktionen laufen normalerweise nicht spontan ab, auch wenn insgesamt dabei Energie gewonnen werden sollte. Es muß zunächst eine Aktivierungsenergie aufgebracht
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Enzyme. Fermente = chemische Substanzen En - zym = in Hefe/Sauerteig ; Trypsin Buchner (1897) zellfreier Hefeextrakt produziert Alkohol
 Enzyme Pasteur (1850) force vitale Liebig (1850) Fermente = chemische Substanzen Kühne (1878) En - zym = in efe/sauerteig ; Trypsin Buchner (1897) zellfreier efeextrakt produziert Alkohol Fischer (1894)
Enzyme Pasteur (1850) force vitale Liebig (1850) Fermente = chemische Substanzen Kühne (1878) En - zym = in efe/sauerteig ; Trypsin Buchner (1897) zellfreier efeextrakt produziert Alkohol Fischer (1894)
Stäbchen und Kügelchen symbolisieren Teile der essentiellen Serin- und Histidin- Reste des aktiven Zentrums, während sich die essentiellen Aspartat
 1 Enzym-Mechanismen (Abb. 1) Bei den letzten Vorlesungen haben wir uns mit einigen allgemeinen Prinzipien bezüglich Enzymwirkungsweise und Enzymkinetik befasst. Im Folgenden werden wir uns mit drei wichtigen
1 Enzym-Mechanismen (Abb. 1) Bei den letzten Vorlesungen haben wir uns mit einigen allgemeinen Prinzipien bezüglich Enzymwirkungsweise und Enzymkinetik befasst. Im Folgenden werden wir uns mit drei wichtigen
Hydrolytisch aktive Enzyme und Gruppentransfer-Reaktionen
 Hydrolytisch aktive Enzyme und Gruppentransfer-Reaktionen (Die Koenzyme Acyl-CoA, ATP, SAM und die Folate) In der Natur gibt es prinzipiell drei Sorten von hydrolytisch aktiven Enyzmen. Diese bauen die
Hydrolytisch aktive Enzyme und Gruppentransfer-Reaktionen (Die Koenzyme Acyl-CoA, ATP, SAM und die Folate) In der Natur gibt es prinzipiell drei Sorten von hydrolytisch aktiven Enyzmen. Diese bauen die
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail. Mag. Gerald Trutschl
 Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Bioorganische Chemie Enzymatische Katalyse 2011
 Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Proteinstoffwechsel. Bildung der Aminosäuren. Protein-Abbau der Körperproteine. Protein-Abbau der Nahrungsproteine. Verwertung der Aminosäuren
 Bildung der Aminosäuren Körperproteine 10000 g Nahrungsproteine Proteinstoffwechsel Proteolyse (300 400 g/d) AminosäurePool Verdauung (50 100 g/d) 100 g Vortragender: Dr. W. Helliger Neusynthese aus z.b.
Bildung der Aminosäuren Körperproteine 10000 g Nahrungsproteine Proteinstoffwechsel Proteolyse (300 400 g/d) AminosäurePool Verdauung (50 100 g/d) 100 g Vortragender: Dr. W. Helliger Neusynthese aus z.b.
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Die Substratspezifität der Enzyme Trypsin und Chymotrypsin
 Die Substratspezifität der Enzyme Trypsin und Chymotrypsin Einleitung Die Proteine Trypsin und Chymotrypsin sind Enzyme, die im Magen von Säugetieren vorkommen und die Hydrolyse von Peptidbindungen katalysieren.
Die Substratspezifität der Enzyme Trypsin und Chymotrypsin Einleitung Die Proteine Trypsin und Chymotrypsin sind Enzyme, die im Magen von Säugetieren vorkommen und die Hydrolyse von Peptidbindungen katalysieren.
Literatur: Enzyme Mechanismen und Kinetik. Enzymes Mechanisms and Kinetics. Biochemie II LVA (WS 2015)
 Biochemie II LVA 166.163 (WS 2015) Vortragender: Ao.Univ.Prof. Dr. Ewald Srebotnik ewald.srebotnik@tuwien.ac.at Einheit 15: und Kinetik Enzymes Mechanisms and Kinetics Literatur: Lehrbuch der Biochemie
Biochemie II LVA 166.163 (WS 2015) Vortragender: Ao.Univ.Prof. Dr. Ewald Srebotnik ewald.srebotnik@tuwien.ac.at Einheit 15: und Kinetik Enzymes Mechanisms and Kinetics Literatur: Lehrbuch der Biochemie
Mathematik und Naturwissenschaften, Biologie, Biochemie. Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Aufgabe 2: (Aminosäuren)
 Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Enzym-Regulation (Abb. 1) Heute werde ich mich mit dem Thema Enzym-Regulation auseinandersetzen. Im Stoffwechsel von lebenden Zellen arbeiten Gruppen
 1 Enzym-Regulation (Abb. 1) Heute werde ich mich mit dem Thema Enzym-Regulation auseinandersetzen. Im Stoffwechsel von lebenden Zellen arbeiten Gruppen von Enzymen nacheinander in dem Sinne, dass das Produkt
1 Enzym-Regulation (Abb. 1) Heute werde ich mich mit dem Thema Enzym-Regulation auseinandersetzen. Im Stoffwechsel von lebenden Zellen arbeiten Gruppen von Enzymen nacheinander in dem Sinne, dass das Produkt
Aminosäuren. Seitenkette. -Kohlenstoffatom. Karboxilgruppe. Aminogruppe
 Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine Bildung der Disulfidbrücke
Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine Bildung der Disulfidbrücke
- Biochemieklausur Name: Matrikelnr.:
 07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
10 BIOGENE-AMINE 4 NICHT-PROTEINOGENE- AS. 20 PROTEINOGENE AS glucoplastisch/ketoplastisch 8 ESSENTIELLE AS
 Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
Mechanismus der Enzymkatalyse
 Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Röntgenstrukturanalyse der humanen Serinprotease DESC-1 und der Zink-Aminopeptidase F3 aus Thermoplasma acidophilum
 Röntgenstrukturanalyse der humanen Serinprotease DESC-1 und der Zink-Aminopeptidase F3 aus Thermoplasma acidophilum tto Kyrieleis Max-Planck-Institut für Biochemie Abteilung Strukturforschung 82152 Martinsried
Röntgenstrukturanalyse der humanen Serinprotease DESC-1 und der Zink-Aminopeptidase F3 aus Thermoplasma acidophilum tto Kyrieleis Max-Planck-Institut für Biochemie Abteilung Strukturforschung 82152 Martinsried
Vertiefendes Seminar zur Vorlesung Biochemie I Bearbeitung Übungsblatt 5
 Vertiefendes Seminar zur Vorlesung Biochemie I 27.11.2015 Bearbeitung Übungsblatt 5 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Vertiefendes Seminar zur Vorlesung Biochemie I 27.11.2015 Bearbeitung Übungsblatt 5 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
manfred kionke Experimentalvortrag im Fachbereich Chemie (Lehramtsstudiengang)
 Thema: Proteasen I Definition und Nachweis Die historisch gewachsene Definition Proteasen sind Enzyme, die Proteine spalten ist heute in dieser Form nicht mehr haltbar, dennoch wird der Begriff weiter
Thema: Proteasen I Definition und Nachweis Die historisch gewachsene Definition Proteasen sind Enzyme, die Proteine spalten ist heute in dieser Form nicht mehr haltbar, dennoch wird der Begriff weiter
Genetische Grundlagen, neue Erkenntnisse der Forschung und Besonderheiten des Krankheitsverlaufs
 Viszeralmedizin 2015 16.-19. September Leipzig Genetische Grundlagen, neue Erkenntnisse der Forschung und Besonderheiten des Krankheitsverlaufs J. Rosendahl Universitätsklinik für Innere Medizin I Universitätsklinikum
Viszeralmedizin 2015 16.-19. September Leipzig Genetische Grundlagen, neue Erkenntnisse der Forschung und Besonderheiten des Krankheitsverlaufs J. Rosendahl Universitätsklinik für Innere Medizin I Universitätsklinikum
BLUUUUT!!!!! BLUTGERINNUNG
 BLUTGERINNUNG BLUTGERINNUNG PRINZIP: PROTHROMBIN ETRINSIC INTRINSIC SYSTEM FIBRINOGEN FIBRIN BLUTGERINNUNG PRINZIP: ETRINSIC INTRINSIC SYSTEM PROTHROMBIN PROTEOLYSE THROMBIN (=ENDOPEPTIDASE) FIBRINOGEN
BLUTGERINNUNG BLUTGERINNUNG PRINZIP: PROTHROMBIN ETRINSIC INTRINSIC SYSTEM FIBRINOGEN FIBRIN BLUTGERINNUNG PRINZIP: ETRINSIC INTRINSIC SYSTEM PROTHROMBIN PROTEOLYSE THROMBIN (=ENDOPEPTIDASE) FIBRINOGEN
Aminosäuren - Proteine
 Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Aminosäuren. Seitenkette. -Kohlenstoffatom. Karboxilgruppe. Aminogruppe
 Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine 18 Primär Struktur Aminosäuer
Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine 18 Primär Struktur Aminosäuer
Enzyme: Grundlegende Konzepte und Kinetik
 Enzyme: Grundlegende Konzepte und Kinetik Enzyme sind Katalysatoren biologischer Systeme Wichtigste Eigenschaften: katalytische Stärke und Spezifität Nahezu alle bekannten Enzyme sind Proteine, es gibt
Enzyme: Grundlegende Konzepte und Kinetik Enzyme sind Katalysatoren biologischer Systeme Wichtigste Eigenschaften: katalytische Stärke und Spezifität Nahezu alle bekannten Enzyme sind Proteine, es gibt
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
15. Aminosäuren, Peptide und Proteine
 15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
BIOINF1110 Einführung in die Bioinforma7k. 5. Molekulare Maschinen Proteinstrukturen und ihre Funk/on
 BIOINF1110 Einführung in die Bioinforma7k 5. Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Zentrum für Bioinforma7k Tübingen Proteine Zentrales Dogma DNA Transkription mrna
BIOINF1110 Einführung in die Bioinforma7k 5. Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Zentrum für Bioinforma7k Tübingen Proteine Zentrales Dogma DNA Transkription mrna
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler
 Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
BIOINF1110 Einführung in die Bioinforma7k. Molekulare Maschinen Proteinstrukturen und ihre Funk/on
 BIOINF1110 Einführung in die Bioinforma7k Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Angewandte Bioinforma0k Zentrum für Bioinforma0k Tübingen Proteine 2 Zentrales Dogma
BIOINF1110 Einführung in die Bioinforma7k Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Angewandte Bioinforma0k Zentrum für Bioinforma0k Tübingen Proteine 2 Zentrales Dogma
Biochemie-Klausur
 Biochemie-Klausur 27.06.03 1) 2) Worauf deutet das? ph 7,36 Pco 2 65 BÜ +9 (normal, gibt s nicht, nicht/kompensierte ph 7,38 Pco 2 25 BÜ 6,2 metabolische/respiratorische Acidose) ph 7,26 Pco2 23 BÜ +9
Biochemie-Klausur 27.06.03 1) 2) Worauf deutet das? ph 7,36 Pco 2 65 BÜ +9 (normal, gibt s nicht, nicht/kompensierte ph 7,38 Pco 2 25 BÜ 6,2 metabolische/respiratorische Acidose) ph 7,26 Pco2 23 BÜ +9
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
1 Einleitung 8. 1 Einleitung
 1 Einleitung 8 1 Einleitung Proteine sind neben der Erbsubstanz DNA die am häufigsten vorkommenden Biopolymere. Ihr Name leitet sich vom griechischen Wort προτεος ab und bedeutet der Erste, der Beste.
1 Einleitung 8 1 Einleitung Proteine sind neben der Erbsubstanz DNA die am häufigsten vorkommenden Biopolymere. Ihr Name leitet sich vom griechischen Wort προτεος ab und bedeutet der Erste, der Beste.
Klausur zur Vorlesung Biochemie I im WS 1993/1994. am 18. Februar Nachklausur zur Vorlesung Biochemie I im WS 1993/1994. am 30. Mai 1994.
 Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Kapitel 3. Nucleophile Substitution
 Kapitel 3. Nucleophile Substitution Reaktionsmechanismen - S N 1-Reaktion: Reaktionskoordinate-Energie-Diagramm; Kinetik, Struktur-Reaktivitätsbeziehungen (stabiles Carbokation, schwaches Nucleophil, gute
Kapitel 3. Nucleophile Substitution Reaktionsmechanismen - S N 1-Reaktion: Reaktionskoordinate-Energie-Diagramm; Kinetik, Struktur-Reaktivitätsbeziehungen (stabiles Carbokation, schwaches Nucleophil, gute
Pharmazeutische Biologie Grundlagen der Biochemie
 Pharmazeutische Biologie Grundlagen der Biochemie Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Aminosäure... chirale Moleküle
Pharmazeutische Biologie Grundlagen der Biochemie Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Aminosäure... chirale Moleküle
4.1. Eigenschaften von Enzymen
 4. Enzyme 106 107 4.1. Eigenschaften von Enzymen Enzyme sind Proteine, die chemische Reaktionen beschleunigen (Biokatalysatoren) Herausragende Merkmale verglichen mit anderen Katalysatoren: drastische
4. Enzyme 106 107 4.1. Eigenschaften von Enzymen Enzyme sind Proteine, die chemische Reaktionen beschleunigen (Biokatalysatoren) Herausragende Merkmale verglichen mit anderen Katalysatoren: drastische
C R H H O H H O. Peptide
 Peptide Peptide: Ketten aus Aminosäuren Enzymatische Prozesse vermögen Aminosäuren im rganismus zu größeren Molekülen, den Peptiden, zu verknüpfen 1. Diese erfüllen vielfältige physiologische Aufgaben,
Peptide Peptide: Ketten aus Aminosäuren Enzymatische Prozesse vermögen Aminosäuren im rganismus zu größeren Molekülen, den Peptiden, zu verknüpfen 1. Diese erfüllen vielfältige physiologische Aufgaben,
Aliphatische Aminosäuren. Aromatische Aminosäuren
 Prof. Dr..-U. eißig rganische Chemie I 17.1 Aliphatische Aminosäuren systematischer ame (Trivialname) truktur Vorkommen, Bedeutung 2-Aminoethansäure (α-aminoessigsäure, Glycin) 3 C 2 C 2 α Proteine, Peptide
Prof. Dr..-U. eißig rganische Chemie I 17.1 Aliphatische Aminosäuren systematischer ame (Trivialname) truktur Vorkommen, Bedeutung 2-Aminoethansäure (α-aminoessigsäure, Glycin) 3 C 2 C 2 α Proteine, Peptide
Was ist denn NAD / NADP??
 Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
WIRKUNGSMECHANISMUS UND SPEZIFITÄT VON ENZYMEN
 155 PLATZ 10: WIRKUNGSMECHANISMUS UND SPEZIFITÄT VON ENZYMEN Einblick in den Mechanismus einer Enzymreaktion gewinnt man aus der Abhängigkeit der Reaktionsgeschwindigkeit v von der Substratkonzentration
155 PLATZ 10: WIRKUNGSMECHANISMUS UND SPEZIFITÄT VON ENZYMEN Einblick in den Mechanismus einer Enzymreaktion gewinnt man aus der Abhängigkeit der Reaktionsgeschwindigkeit v von der Substratkonzentration
Mikrokalorimetrische Studien zum Verständnis der thermodynamischen und strukturellen Eigenschaften von Inhibitoren der Blutgerinnungskaskade
 Mikrokalorimetrische Studien zum Verständnis der thermodynamischen und strukturellen Eigenschaften von Inhibitoren der Blutgerinnungskaskade Dissertation zur Erlangung des Doktorgrades der aturwissenschaften
Mikrokalorimetrische Studien zum Verständnis der thermodynamischen und strukturellen Eigenschaften von Inhibitoren der Blutgerinnungskaskade Dissertation zur Erlangung des Doktorgrades der aturwissenschaften
WIRKUNGSMECHANISMUS UND SPEZIFITÄT VON ENZYMEN
 108 PLATZ 10: WIRKUNGSMECHANISMUS UND SPEZIFITÄT VON ENZYMEN Reaktionsmechanismus von Chymotrypsin: Chymotrypsin ist eine Protease, die unter der Einwirkung von Trypsin aus der im exokrinen Pankreas synthetisierten
108 PLATZ 10: WIRKUNGSMECHANISMUS UND SPEZIFITÄT VON ENZYMEN Reaktionsmechanismus von Chymotrypsin: Chymotrypsin ist eine Protease, die unter der Einwirkung von Trypsin aus der im exokrinen Pankreas synthetisierten
Proteasen. (Peptidasen = Peptidbindungshydrolasen = Proteasen = Proteinasen = proteolytische Enzyme ) Retropepsin. Caspase. Omptin
 Retropepsin Proteasen (Peptidasen = Peptidbindungshydrolasen = Proteasen = Proteinasen = proteolytische Enzyme ) Caspase Anthrax lethal factor Omptin Wozu Proteolyse? Proteolysis is used by the cell for
Retropepsin Proteasen (Peptidasen = Peptidbindungshydrolasen = Proteasen = Proteinasen = proteolytische Enzyme ) Caspase Anthrax lethal factor Omptin Wozu Proteolyse? Proteolysis is used by the cell for
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Nach Terpenen und Kohlenhydraten nun eine weitere große Klasse an Naturstoffen
 260 17. Aminosäuren, Peptide ach Terpenen und Kohlenhydraten nun eine weitere große Klasse an aturstoffen 17.1 Übersicht Analog zu ydroxycarbonsäuren α-, β-, γ- Aminocarbonsäuren möglich: 2 3 2 2 α-amino-essigsäure
260 17. Aminosäuren, Peptide ach Terpenen und Kohlenhydraten nun eine weitere große Klasse an aturstoffen 17.1 Übersicht Analog zu ydroxycarbonsäuren α-, β-, γ- Aminocarbonsäuren möglich: 2 3 2 2 α-amino-essigsäure
Punkte 1. a) Erklären Sie wieso das Wassermolekül ein Dipol ist (gerne mit Zeichnung).
 -Klausur Biochemie - 20.07.6 Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
-Klausur Biochemie - 20.07.6 Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Inhaltsverzeichnis. Vorwort. xvii. Kapitel 1 Aufbau der Materie 1. Kapitel 2 Die chemische Bindung 39
 Vorwort xvii Kapitel 1 Aufbau der Materie 1 1.1 MateriebestehtausAtomen... 3 1.2 Elementarteilchen... 3 1.3 AufbaueinesAtoms... 4 1.4 AtommassenundStoffmengen... 5 1.5 Isotope... 7 1.6 Radioaktivität und
Vorwort xvii Kapitel 1 Aufbau der Materie 1 1.1 MateriebestehtausAtomen... 3 1.2 Elementarteilchen... 3 1.3 AufbaueinesAtoms... 4 1.4 AtommassenundStoffmengen... 5 1.5 Isotope... 7 1.6 Radioaktivität und
Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte)
 Datum: 06.12.2010 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte) Modulnr.: FMI-BI0027 iermit bestätige ich meine Prüfungstauglichkeit.
Datum: 06.12.2010 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte) Modulnr.: FMI-BI0027 iermit bestätige ich meine Prüfungstauglichkeit.
ENZYME. Teil 1: Grundlagen und Substratbestimmungen
 ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
Entropie ist ein Maß für den Ordnungszustand eines thermodynamischen Systems (chem. Reaktion in einem geschlossenen System); kann auch als Maß für
 Entropie ist ein Maß für den Ordnungszustand eines thermodynamischen Systems (chem. Reaktion in einem geschlossenen System); kann auch als Maß für die Nichtumkehrbarkeit (Irreversibilität) eines Vorganges
Entropie ist ein Maß für den Ordnungszustand eines thermodynamischen Systems (chem. Reaktion in einem geschlossenen System); kann auch als Maß für die Nichtumkehrbarkeit (Irreversibilität) eines Vorganges
-Klausur Biochemie Name: Matrikelnr.:
 25.07.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
25.07.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
2. Theoretischer Teil Grundlagen der Protease-Katalyse Katalysemechanismus von Serinproteasen
 2. Theoretischer Teil 9 Rückschlüsse auf die Amidaseaktivität der Proteasen, die idealer Weise fehlen sollte, zuließen (vgl. Abb. 2). Weiterführend sollte das synthetische Potential der im Hinblick auf
2. Theoretischer Teil 9 Rückschlüsse auf die Amidaseaktivität der Proteasen, die idealer Weise fehlen sollte, zuließen (vgl. Abb. 2). Weiterführend sollte das synthetische Potential der im Hinblick auf
Aminosäurebestimmung im Kochschinken
 1. Gegenstand der Untersuchung Es wurden 4 verschiedene Kochschinken eines Discounters hinsichtlich deren Gehalt an freien und NPN-gebundenen sowie möglichen Zusätzen untersucht. Darüber hinaus dienen
1. Gegenstand der Untersuchung Es wurden 4 verschiedene Kochschinken eines Discounters hinsichtlich deren Gehalt an freien und NPN-gebundenen sowie möglichen Zusätzen untersucht. Darüber hinaus dienen
8. Aminosäuren - (Proteine) Eiweiß
 8. Aminosäuren - (Proteine) Eiweiß Proteine sind aus Aminosäuren aufgebaut. Aminosäuren bilden die Grundlage der belebten Welt. 8.1 Struktur der Aminosäuren Aminosäuren sind organische Moleküle, die mindestens
8. Aminosäuren - (Proteine) Eiweiß Proteine sind aus Aminosäuren aufgebaut. Aminosäuren bilden die Grundlage der belebten Welt. 8.1 Struktur der Aminosäuren Aminosäuren sind organische Moleküle, die mindestens
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
ORGANISCHE CHEMIE. Aminosäuren und Proteine
 RGAISE EMIE Aminosäuren und Proteine Aminosäuren (AS) R 2 arbonsäuren mit einer Aminogruppe Die (etwa) 20 proteinogenen Aminosäuren sind alle α-aminosäuren (Aminogruppe an -2), unterscheiden sich durch
RGAISE EMIE Aminosäuren und Proteine Aminosäuren (AS) R 2 arbonsäuren mit einer Aminogruppe Die (etwa) 20 proteinogenen Aminosäuren sind alle α-aminosäuren (Aminogruppe an -2), unterscheiden sich durch
-Klausur Biochemie Name: Matrikelnr.: 1. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist.
 4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
Nucleophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte
 Nucleophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Nucleophile Reak:onen Signale: Das organischen Molekül besitzt ein posi:v polarisiertes C- Atom in der KohlenstoKeLe.
Nucleophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Nucleophile Reak:onen Signale: Das organischen Molekül besitzt ein posi:v polarisiertes C- Atom in der KohlenstoKeLe.
Katalyse. höhere Reaktionsgeschwindigkeit bei derselben Temperatur! Achtung: Gleichgewicht der chemischen Reaktion wird nicht verschoben
 Katalyse Ein Katalysator setzt Aktivierungsenergie einer Reaktion herab, indem er einen anderen Reaktionsweg ermöglicht, so dass der geschwindigkeitsbestimmende Schritt der nicht-katalysierten Reaktion
Katalyse Ein Katalysator setzt Aktivierungsenergie einer Reaktion herab, indem er einen anderen Reaktionsweg ermöglicht, so dass der geschwindigkeitsbestimmende Schritt der nicht-katalysierten Reaktion
Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen. c(a) t. v = -
 REAKTIONSKINETIK 1 Reaktionskinetik Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen Anwendung: - Vorgänge in den lebenden Organismen
REAKTIONSKINETIK 1 Reaktionskinetik Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen Anwendung: - Vorgänge in den lebenden Organismen
2. Zeichnen Sie die Betain-Struktur und schätzen Sie die pi-werte der Peptide:
 1. Berechnen Sie den ph-wert von isoelektrischem Alanin! 2. Zeichnen Sie die Betain-Struktur und schätzen Sie die pi-werte der Peptide: a) Ser-Ala-Phe-Lys-Glu b) Leu-Arg-His-Gly- Asp 3. Die Jodzahl (g(jod)/100g
1. Berechnen Sie den ph-wert von isoelektrischem Alanin! 2. Zeichnen Sie die Betain-Struktur und schätzen Sie die pi-werte der Peptide: a) Ser-Ala-Phe-Lys-Glu b) Leu-Arg-His-Gly- Asp 3. Die Jodzahl (g(jod)/100g
Allgemeine und Anorganische Chemie
 Allgemeine und Anorganische Chemie Ein Leitfaden fur Studierende der Biologie, Biochemie und Pharmazie Wolfgang Jabs ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum 1. Einfiihrung 1 2. Chemische Grundbegriffe
Allgemeine und Anorganische Chemie Ein Leitfaden fur Studierende der Biologie, Biochemie und Pharmazie Wolfgang Jabs ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum 1. Einfiihrung 1 2. Chemische Grundbegriffe
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie) Maximale Punktezahl: 20
 Lösungen Übungsklausur vom 17.01.2012 Teil 1 Aufgaben zum Stoff der Vorlesung C1a (Grundvorlesung rganische Chemie) Maximale Punktezahl: 20 Aufgabe 1.1 (5 Punkte) Zeichnen Sie die Strukturformeln der folgenden
Lösungen Übungsklausur vom 17.01.2012 Teil 1 Aufgaben zum Stoff der Vorlesung C1a (Grundvorlesung rganische Chemie) Maximale Punktezahl: 20 Aufgabe 1.1 (5 Punkte) Zeichnen Sie die Strukturformeln der folgenden
Beispiele für Prüfungsfragen zu den Einheiten. 2, 3, 5, 9-12, 15, 16, und 21 (Hartig)
 Beispiele für Prüfungsfragen zu den Einheiten 2, 3, 5, 9-12, 15, 16, und 21 (Hartig) Untenstehendes Molekül ist ein Peptidhormon. Wieviele Peptidbindungen besitzt dieses Molekül (zeichnen Sie diese ein)?
Beispiele für Prüfungsfragen zu den Einheiten 2, 3, 5, 9-12, 15, 16, und 21 (Hartig) Untenstehendes Molekül ist ein Peptidhormon. Wieviele Peptidbindungen besitzt dieses Molekül (zeichnen Sie diese ein)?
Cell Biology Gravitational Biology
 Biologie im Nebenfach Informationen für Nebenfächler-Informatik Dr. Peter Richter Department Biologie Lehrstuhl für Zellbiologie AG für Gravitationsbiologie Staudtstr. 5, 90158 Erlangen, Deutschland Tel.
Biologie im Nebenfach Informationen für Nebenfächler-Informatik Dr. Peter Richter Department Biologie Lehrstuhl für Zellbiologie AG für Gravitationsbiologie Staudtstr. 5, 90158 Erlangen, Deutschland Tel.
Formeln. Darstellungen von Molekülen C 6 H 14 O. respektive
 Formeln respektive Darstellungen von Molekülen C 6 H 14 O Wählen Sie einen Stoff Chlorgas Chlorgas ist die elementare Form Chlor. Es hat die Gefahrenkennzeichen brandfördernd, giftig und umweltschädlich,
Formeln respektive Darstellungen von Molekülen C 6 H 14 O Wählen Sie einen Stoff Chlorgas Chlorgas ist die elementare Form Chlor. Es hat die Gefahrenkennzeichen brandfördernd, giftig und umweltschädlich,
- Biochemieklausur Name: Matrikelnr.:
 08.07.20 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
08.07.20 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Modul 8: Bioinformatik A. Von der DNA zum Protein Proteinsynthese in silicio
 Modul 8: Bioinformatik A. Von der DNA zum Protein Proteinsynthese in silicio Ein Wissenschaftler erhält nach einer Sequenzierung folgenden Ausschnitt aus einer DNA-Sequenz: 5 ctaccatcaa tccggtaggt tttccggctg
Modul 8: Bioinformatik A. Von der DNA zum Protein Proteinsynthese in silicio Ein Wissenschaftler erhält nach einer Sequenzierung folgenden Ausschnitt aus einer DNA-Sequenz: 5 ctaccatcaa tccggtaggt tttccggctg
Stoffklasse: LIPIDE Funktionen in der Zelle
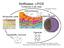 Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
2. Prinzipien der Pflanzenstärkung durch Blattanwendung von L Aminosäuren
 Aminosäuren und Peptide für die Pflanzenstärkung von Dr. Helmut Wolf, Protan AG 1. Einführung 2. Prinzipien der Pflanzenstärkung durch Blattanwendung von L Aminosäuren 3. Wirtschaftlichkeit der Blattanwendung
Aminosäuren und Peptide für die Pflanzenstärkung von Dr. Helmut Wolf, Protan AG 1. Einführung 2. Prinzipien der Pflanzenstärkung durch Blattanwendung von L Aminosäuren 3. Wirtschaftlichkeit der Blattanwendung
Campherchinon (teuer)
 chiral pool alle chiralen, nicht racemischen Verbindungen aturstoffe - müssen enantiomerenrein verfügbar sein - müssen leicht und rein isolierbar sein dann sind diese billig im andel verfügbar alle Verbindungen,
chiral pool alle chiralen, nicht racemischen Verbindungen aturstoffe - müssen enantiomerenrein verfügbar sein - müssen leicht und rein isolierbar sein dann sind diese billig im andel verfügbar alle Verbindungen,
Entwicklung von DegS-Inhibitoren
 Entwicklung von DegS-Inhibitoren Dissertation zur Erlangung des akademischen Grades eines Doktors der Naturwissenschaften Dr. rer. nat. vorgelegt von Anna Laura Schmitz geboren in Dorsten Fakultät für
Entwicklung von DegS-Inhibitoren Dissertation zur Erlangung des akademischen Grades eines Doktors der Naturwissenschaften Dr. rer. nat. vorgelegt von Anna Laura Schmitz geboren in Dorsten Fakultät für
Spezielle Pathologie Exokrines Pankreas. 1. Teil
 Spezielle Pathologie Exokrines Pankreas 1. Teil Anatomie (1): da sich das Pankreas embryologisch aus mehreren Anlagen entwickelt, die dann tierartlich unterschiedlich aus- bzw. rückgebildet werden, kommt
Spezielle Pathologie Exokrines Pankreas 1. Teil Anatomie (1): da sich das Pankreas embryologisch aus mehreren Anlagen entwickelt, die dann tierartlich unterschiedlich aus- bzw. rückgebildet werden, kommt
Arten zellulärer Signalübertragung
 Arten zellulärer Signalübertragung Hormone SignalZelle Synapse Transmittermoleküle RezeptorLigand vermittelter Zell-Zell Kontakt Hormone als Signalmoleküle Adrenalin: Cortisol: Östradiol: Glucagon: Insulin:
Arten zellulärer Signalübertragung Hormone SignalZelle Synapse Transmittermoleküle RezeptorLigand vermittelter Zell-Zell Kontakt Hormone als Signalmoleküle Adrenalin: Cortisol: Östradiol: Glucagon: Insulin:
Einleitung 1 1 EINLEITUNG
 Einleitung 1 1 EINLEITUNG Proteasen haben die Eigenschaft, die Hydrolyse von Amidbindungen zu katalysieren. Obwohl Proteine vielen reversiblen posttranslatorischen Modifizierungen während ihrer Lebensdauer
Einleitung 1 1 EINLEITUNG Proteasen haben die Eigenschaft, die Hydrolyse von Amidbindungen zu katalysieren. Obwohl Proteine vielen reversiblen posttranslatorischen Modifizierungen während ihrer Lebensdauer
-Klausur Biochemie Name:
 -Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
-Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
mrna S/D UTR: untranslated region orf: open reading frame S/D: Shine-Dalgarno Sequenz
 1. Nennen Sie die verschiedenen RNA-Typen, die bei der Translation wichtig sind. Erklären Sie die Funktion der verschiedenen RNA-Typen. Skizzieren Sie die Struktur der verschiedenen RNA-Typen und bezeichnen
1. Nennen Sie die verschiedenen RNA-Typen, die bei der Translation wichtig sind. Erklären Sie die Funktion der verschiedenen RNA-Typen. Skizzieren Sie die Struktur der verschiedenen RNA-Typen und bezeichnen
Strukturelle und physikochemische Charakterisierung der Protein-Ligand-Wechselwirkung am Beispiel der Serinproteasen Thrombin und Trypsin
 Strukturelle und physikochemische Charakterisierung der Protein-Ligand-Wechselwirkung am Beispiel der Serinproteasen Thrombin und Trypsin Dissertation zur Erlangung des Doktorgrades der aturwissenschaften
Strukturelle und physikochemische Charakterisierung der Protein-Ligand-Wechselwirkung am Beispiel der Serinproteasen Thrombin und Trypsin Dissertation zur Erlangung des Doktorgrades der aturwissenschaften
Application Notes. Aracus
 Application Notes Aracus membrapure GmbH Wolfgang Küntscher Str. 14 16761 Hennigsdorf / Berlin Mail: info@membrapure.de Tel.: 03302 / 201 20 0 Fax: 03302 / 201 20 21 Index Physiological Extended 54 amino
Application Notes Aracus membrapure GmbH Wolfgang Küntscher Str. 14 16761 Hennigsdorf / Berlin Mail: info@membrapure.de Tel.: 03302 / 201 20 0 Fax: 03302 / 201 20 21 Index Physiological Extended 54 amino
Grundlagen der Zellulären Biochemie
 Grundlagen der Zellulären Biochemie Wasser das Medium des Lebens, Aminosäuren Vorlesung zum Modul BCB P07 im Bachelor-Studiengang Biochemie Hannover Prof. J. Alves, Institut für Biophysikalische Chemie,
Grundlagen der Zellulären Biochemie Wasser das Medium des Lebens, Aminosäuren Vorlesung zum Modul BCB P07 im Bachelor-Studiengang Biochemie Hannover Prof. J. Alves, Institut für Biophysikalische Chemie,
Vertiefendes Seminar zur Vorlesung Biochemie I. Bearbeitung Übungsblatt 6
 Vertiefendes Seminar zur Vorlesung Biochemie I 04.12.2015 Bearbeitung Übungsblatt 6 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Vertiefendes Seminar zur Vorlesung Biochemie I 04.12.2015 Bearbeitung Übungsblatt 6 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Aufgabe 1: 6 Punkte In English:
 Seite 1/36 Aufgabe 1: 6 Punkte Wie können Sie die folgende Verbindung mit einer Tandemreaktion analog einer Robinson-Anellierung herstellen? Geben Sie die Synthesebausteine, Reagenzien sowie den Reaktionsmechanismus
Seite 1/36 Aufgabe 1: 6 Punkte Wie können Sie die folgende Verbindung mit einer Tandemreaktion analog einer Robinson-Anellierung herstellen? Geben Sie die Synthesebausteine, Reagenzien sowie den Reaktionsmechanismus
TEV Protease, rekombinant (Kat.-Nr )
 GEBRAUCHSANLEITUNG TEV Protease, rekombinant (Kat.-Nr. 36403) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010 e-mail: info@serva.de -http://www.serva.de
GEBRAUCHSANLEITUNG TEV Protease, rekombinant (Kat.-Nr. 36403) SERVA Electrophoresis GmbH - Carl-Benz-Str. 7-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010 e-mail: info@serva.de -http://www.serva.de
Mathematik und Naturwissenschaften, Biologie, Biochemie. Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 12.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 12.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Reaktionskinetik. Katalyse
 Reaktionskinetik Katalyse Katalysatoren beshleunigen hemishe Reaktionen, ohne das Gleihgewiht zu beeinflussen. Sie beeinflussen nur die Aktiierungsenergie Katalyse Katalysatoren beeinflussen den Reaktionsweg
Reaktionskinetik Katalyse Katalysatoren beshleunigen hemishe Reaktionen, ohne das Gleihgewiht zu beeinflussen. Sie beeinflussen nur die Aktiierungsenergie Katalyse Katalysatoren beeinflussen den Reaktionsweg
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
Linagliptin (Trajenta )
 Linagliptin (Trajenta ) Die Arzneistoffklasse der Dipeptidyl-Peptidase-4-Inhibitoren (DPP-4- Inhibitoren) ist noch relativ jung. Sitagliptin (Januvia, Xelevia ) war 2007 das erste Gliptin, das zugelassen
Linagliptin (Trajenta ) Die Arzneistoffklasse der Dipeptidyl-Peptidase-4-Inhibitoren (DPP-4- Inhibitoren) ist noch relativ jung. Sitagliptin (Januvia, Xelevia ) war 2007 das erste Gliptin, das zugelassen
