9. ZUSAMMENFASSUNG DER UNTERSUCHUNGEN ZU KOLLAGEN IV
|
|
|
- Willi Maus
- vor 7 Jahren
- Abrufe
Transkript
1 9. ZUSAMMENFASSUNG DER UNTERSUCHUNGEN ZU KOLLAGEN IV 9.1. Struktur und Faltung von Kollagen Kollagene sind Proteine eukaryontischer Organismen, die aus drei Polypeptidketten aufgebaut sind. Sie werden in verschiedene Typen eingeteilt, die in unterschiedlichen Geweben und Organen vorkommen (Kielty et al., 1993). Die Primärstruktur dieser Ketten ist eine Folge von Tripletts der Form [Gly-Pro-Hyp] n -. Eine einzelne Kollagenkette bildet eine linksgängige Polyprolin-II Helix (Sekundärstruktur). Drei Kollagenketten bilden als Tertiärstruktur eine Kollagentripelhelix, die eine rechtsgängige Schraube mit einer Ganghöhe (pitch) von 8 nm darstellt. Die Seitenketten der Aminosäuren X und Y auf der Oberfläche der Tripelhelix (Zylindermantel) bilden wiederum eine linksgängige Schraube mit einem Durchmesser von 1,5 nm und einer Ganghöhe von 0,9 nm (Eble, 1994; Traub & Piez, 1971). Die Struktur der Tripelhelix wurde von RICH und CRICK 1955 vorgeschlagen (Rich & Crick, 1955). Die Analyse der Kristallstruktur eines kollagenen Peptides (Auflösung 1,9 Å) durch die Gruppe um Helen BERMAN bestätigte 1994 eindrucksvoll die originalen Koordinaten (Bella et al., 1994). Die Tripelhelix von Kollagenen zeigt einen charakteristischen Circulardichroismus im Fern-UV mit einem positiven Extremum bei 221 nm (Engel, 1987). Nach thermischer Denaturierung von Kollagen wird eine Inversion des Signals gemessen, so daß die Faltung durch Messung des Circulardichroismus bei dieser Wellenlänge analysiert werden kann (R12). Die Seitenketten der Tripelhelix sind stark zum Lösungsmittel exponiert. Der Modus der Stabilisierung der Tripelhelix ist bis heute noch nicht vollständig verstanden. Es werden Wasserstoffbrückenbindungen zwischen Gly der einen Kette und Pro in der X-Position der angrenzenden Ketten, Stabilisierungen durch hochgeordnete Wasserbrücken (water bridges) und induktive Effekte der Hydroxylgruppen der Hydroxyproline vorgeschlagen (Stetefeld et al., 2003). Das crosslinking der selektierten Kollagenketten durch trimere Oligomerisierungsdomänen (NC-Domänen, nicht-kollagene Domänen) (Engel, 2004; Engel & Kammerer, 2000) oder Disulfidbrücken (Barth et al., 2003a; Barth et al., 2003b) begünstigt deren Stabilisierung und die Einstellung des Kettenregisters. Allgemein beginnt die Faltung der Tripelhelix mit einer durch die Oligomerisierungsdomänen begünstigten Nukleation (trimolekulare Reaktion), was eine sehr hohe effektive Konzentration der Ketten bedingt (Boudko et al., 2002). Die 72
2 Geschwindigkeit der Faltung von Kollagen ist durch die cis trans -Isomerisierung der Prolylbindungen bestimmt, da in der intakten Tertiärstruktur nur die trans Konformation vorliegt (Bächinger et al., 1980). Die hohe Lösungsmittelzugänglichkeit der Seitenketten der Prolinreste ließ eine Beschleunigung der Kollagenfaltung durch PPIasen (Cyp18) erwarten (Bächinger, 1987). Aus Experimenten zur limitierten Proteolyse faltender Kollagenketten konnte gezeigt werden, daß die Faltung der Tripelhelix vom C- zum N-Terminus verläuft, wobei Nukleationen auch an beiden Termini auftreten können (Frank et al., 2003). Von PROCKOP und ENGEL wurde ein Reißverschlußmodell der Kollagenfaltung (zipper-like model) vorgeschlagen (Engel & Prockop, 1991). Transitionskurven der thermischen und chemischen Entfaltung von Kollagen und kollagenen Peptiden zeigten, daß dieser Prozeß kooperativ und meist reversibel ist (Ausnahme zum Beispiel Col2 von Kollagen XIV, R13). Die Transitionskurven der Entfaltung und Faltung zeigen jedoch eine Hysterese. Aus systematischen Untersuchungen der Faltung von Kollagen III und daraus hergestellten tryptischen kollagenen Peptiden verschiedener Kettenlänge zeigten ENGEL und BÄCHNIGER, daß der langsame Prozeß der Nukleation (annealing) und die Hysterese auf sehr langsame Schritte der Umlagerung / Umorientierung mißgefalteter Regionen des Moleküls zurückzuführen sind. Mit kürzerer Kettenlänge der Fragmente nimmt die Hysterese ab (Engel & Bächinger, 2000) Kollagen IV als Bestandteil der Basalmembran Die Basalmembran ist eine spezielle schichtartige Struktur der extrazellulären Matrix und trennt in allen Organen den Parenchymanteil (Epithel- und Endothelzellen, Muskelzellen und Muskelfasern, Nervengewebe) vom organspezifischen Bindegewebe (Stroma) ab. Hauptbestandteile der Basalmembran sind Kollagen IV, Laminin, Nidogen / Entaktin und Perlecan. Kollagen IV hat eine Länge von ca. 400 nm und ist ein Glykoprotein. Die heteromere Tripelhelix wird aus zwei 1-Ketten und einer 2-Kette gebildet, wobei auch andere Isoformen bekannt sind. Die einzige N-glykosidisch verknüpfte Kohlenhydratkette befindet sich in der N- terminalen 7S-Domäne. Die Tripelhelix von Kollagen IV besitzt einen sehr hohen Glykosylierungsgrad, wobei -D-Glucopyranosyl-( 1 2)-D-galactopyranosyl-Reste O-glykosidisch an 5-Hydroxylysinreste gebunden sind. Lysinreste in Y-Stellung 73
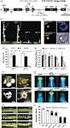
3 werden zu 95 % von Lysin-5-hydroxylase hydroxyliert, von denen % glykosyliert werden (Eble, 1994; Kielty et al., 1993). Kollagen IV unterscheidet sich von interstitiellen Kollagenen durch die Ausbildung netzartiger Strukturen. Am N-Terminus werden in der 30 nm langen 7S-Domäne vier Tripelhelices durch intermolekulare Disulfidbrücken kovalent vernetzt. Diese Verknüpfungen werden durch intermolekulare Aldolvernetzungsprodukte ergänzt, die aus Lysin- und 5-Hydroxylysinresten nach deren Oxidation durch Lysyloxidase entstehen. Die Tripelhelix von Kollagen IV hat eine Länge von 360 nm. Am C- Terminus befindet sich die NC1-Domäne, die aus zwei NC1 1-Untereinheiten und einer NC1 2-Untereinheit aufgebaut ist (Eble, 1994; Kielty et al., 1993). Die Struktur dieser Domäne wurde 2002 aufgeklärt (Than et al., 2002). Die NC1-Domänen zweier Tripelhelices können kovalent über eine ungewöhnliche Met-Lys-Brücke verbunden werden und bilden ein sogenanntes Dimer. Ferner können die Tripelhelices von Kollagen IV lateral assoziieren (Eble, 1994). Das aus diesen Möglichkeiten der Verknüpfung der Ketten resultierende Netzwerk von Kollagen IV bildet das Grundgerüst der Lamina densa der Basalmembran Untersuchungen zur thermischen Stabilität des Bindungsbereiches des Integrins 1 1 (VLA1) an Kollagen IV Integrine sind membranständige Zelladhäsionsmoleküle, die Zell-Matrix-Kontakte gewährleisten und bestehen aus einer - und einer -Untereinheit (Eble, 1994; Humphries et al., 2003). Das Integrin 1 1 (VLA1) bindet an Kollagen IV (Vandenberg et al., 1991). Untersuchungen der Bindung dieses Integrins an durch limitierte Proteolyse hergestellte Fragmente von Kollagen IV (F1, F2, F3, F4 und TL1) zeigten, daß diese Wechselwirkung durch die Aminosäuren Asp461 der beiden 1 und Arg461 der 2-Kette essentiell bestimmt wird (R14). Der Bindungsbereich des Integrins 1 1 (VLA1) an Kollagen IV liegt daher im N-terminalen Teil des Moleküls zwischen zwei Disulfidknoten [Disulfidknoten I der 1-Ketten (Cys454), Disulfidknoten II der 1-Ketten (Cys487, Cys490) und 2-Ketten (Cys486, Cys488)]. Die Untersuchung der thermischen Stabiltät der proteolytischen Fragmente F1, F4 und TL1 wurde mittels Fern-UV Circulardichroismus untersucht (R14). Das Fragment F1 zeigte zwei Transitionen des Entfaltungsprozesses mit T 1 m = 37 C und T m 2 = 49 C. Die Faltung des thermisch denaturierten Fragmentes F1 zeigte 74
4 ebenfalls zwei Transitionen, wobei eine Hysterese zur Entfaltung nur für den ersten Transitionsbereich gemessen wurde. Das Fragment F4 entspricht dem tripelhelikalen Teil zwischen den beiden Disulfidknoten und zeigt bei der thermischen Entfaltung nur noch die Transition mit T m = 51 C. Somit konnten erstmals stabilere lokale Bereiche der Tripelhelix von Kollagen IV nachgewiesen werden, die keine Hysterese der Faltung im Vergleich zur Entfaltung aufweisen. Das Fragment TL1 entspricht der C-terminalen Hälfte des Fragmentes F4. Trotz tripelhelikaler Struktur besitzt es eine geringere thermische Stabilität. Untersuchungen der thermischen Stabilität von Modellpeptiden von Kollagen IV, die auf der Grundlage der Struktur der Bindungsstelle der Integrine synthetisiert wurden, konnten die Messungen und Interpretationen der Ergebnisse der natürlichen Präparate bestätigen (Sacca et al., 2002a) Bestimmung des Rasters der Kollagenketten im Bereich der Bindungsstelle des Integrins 1 1 (VLA1) mittels Fluoreszenzresonanzenergietransfer (FRET) (R15) Für die Synthese von Modellpeptiden zur Inhibition der Bindung von Integrinen an Kollagen IV war es von Interesse, den Raster der drei Einzelketten der Tripelhelix im Bereich des Disulfidknotens zu bestimmen. Kollagen IV besitzt zwischen den Disulfidknoten der Integrinbindungstelle nur einen Tryptophanrest in der 2-Kette in Position 479. Aus Betrachtungen der Primärstruktur und bekannten Daten zum FRET zwischen den intrinsischen Fluorophoren von Proteinen wurden die Phe461 der beiden 1-Ketten als Donormoleküle und Trp479 der 2-Kette als Akzeptormolekül für einen FRET im Fragment F2 in Betracht gezogen. Kollagen ist ein relativ starres Molekül. Es konnte gezeigt werden, daß zwischen den im Fragment F2 vorhandenen Tyrosinresten und Trp479 kein FRET besteht. Die vorhandenen Tyrosinreste wurden nitriert um eine optische Perturbation einzuschränken. Der mittlere Abstand zwischen den beiden Donoren und dem Akzeptor wurde nach Messung der Energietransfereffizienz nach FÖRSTER bestimmt (Förster, 1948). Aus dem Modell der Tripelhelix von Kollagen und den Übergangsmomenten der Aromaten konnte der Orientierungsfaktor der Förster schen Gleichung spezifiziert werden, was eine genauere Abschätzung der Abstände der FRET-Paare erlaubte und die konformative Anordnung favorisierte. Die Anordnung konnte definitiv ausgeschlossen werden. Die Anordnung ähnelt konformativ der Anordnung
5 Neuere Studien der Bestimmung des Kettenregisters mit Modellpeptiden konnten diese Messungen im wesentlichen bestätigen (Sacca et al., 2002a). Die Tripelhelix der Modellpeptide mit dem Register zeigte eine geringere Thermostabilität. Damit wurde eine wesentliche Grundlage zum rationalen Wirkstoffdesign der Integrinbindung an Kollagen IV mit Relevanz zu medizinischen Aspekten der Wundheilung und Tumorinvasion geschaffen (Sacca et al., 2002b). 76
Circulardichroismus (CD) und Fluoreszenz - Anwendungen in der Proteinchemie -
 Circulardichroismus (CD) und Fluoreszenz - Anwendungen in der Proteinchemie - Circulardichroismus (CD) - Einführung Circulardichroismus (CD) - Prinzip Circulardichroismus (CD) - Formel Meßsignal beruht
Circulardichroismus (CD) und Fluoreszenz - Anwendungen in der Proteinchemie - Circulardichroismus (CD) - Einführung Circulardichroismus (CD) - Prinzip Circulardichroismus (CD) - Formel Meßsignal beruht
und Reinstruktur Die Sekundärstruktur ist die Anordnung der Aminosäurenkette, wobei man in zwei Arten unterscheidet: o Faltblatt- oder β- Struktur
 Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
Unter der Kollagensynthese versteht man die intrazellulär und extrazellulär. stattfindende Synthese von Kollagen.
 KOLLAGENSYNTHESE!! Unter der Kollagensynthese versteht man die intrazellulär und extrazellulär stattfindende Synthese von Kollagen. Das Kollagen ist im menschlichen Körper Bestandteil aller Binde. - und
KOLLAGENSYNTHESE!! Unter der Kollagensynthese versteht man die intrazellulär und extrazellulär stattfindende Synthese von Kollagen. Das Kollagen ist im menschlichen Körper Bestandteil aller Binde. - und
1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur
 Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur - Eigenschaften eines Proteins werden durch
Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur - Eigenschaften eines Proteins werden durch
Aufgabe 5 (Supersekundärstruktur)
 Aufgabe 5 (Supersekundärstruktur) Fragestellung Bei der Untereinheit des Arthropodenhämocyanins aus Limulus polyphemus werden folgende Fragestellungen untersucht: - Welche Supersekundärstrukturen gibt
Aufgabe 5 (Supersekundärstruktur) Fragestellung Bei der Untereinheit des Arthropodenhämocyanins aus Limulus polyphemus werden folgende Fragestellungen untersucht: - Welche Supersekundärstrukturen gibt
Aufgabe 6 (Quartärstruktur)
 Aufgabe 6 (Quartärstruktur) Fragestellung Folgende Fragestellungen sollen beim Hämocyanin-Hexamer von Limulus polyphemus (1lla_Hexamer.pdb) untersucht werden: - Welche Symmetrien sind erkennbar? - Wenn
Aufgabe 6 (Quartärstruktur) Fragestellung Folgende Fragestellungen sollen beim Hämocyanin-Hexamer von Limulus polyphemus (1lla_Hexamer.pdb) untersucht werden: - Welche Symmetrien sind erkennbar? - Wenn
Aminosäuren. Seitenkette. -Kohlenstoffatom. Karboxilgruppe. Aminogruppe
 Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine 18 Primär Struktur Aminosäuer
Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine 18 Primär Struktur Aminosäuer
Signaltransduktion durch Zell-Zell und Zell-Matrix Kontakte
 Signaltransduktion durch Zell-Zell und Zell-Matrix Kontakte - Integrine als zentrale Adhäsionsrezeptoren - - Focal Adhesion Kinase (FAK) als zentrales Signalmolekül - Regulation von Zellfunktionen durch
Signaltransduktion durch Zell-Zell und Zell-Matrix Kontakte - Integrine als zentrale Adhäsionsrezeptoren - - Focal Adhesion Kinase (FAK) als zentrales Signalmolekül - Regulation von Zellfunktionen durch
Aufgabe 4 (Sekundärstruktur)
 Aufgabe 4 (Sekundärstruktur) Fragestellung - Durch welche Eigenschaften zeichnen sich α-helices und β-faltblätter aus? Belegen Sie Ihre Antwort mit den entsprechenden Daten. (phi/psi-winkel). - Wodurch
Aufgabe 4 (Sekundärstruktur) Fragestellung - Durch welche Eigenschaften zeichnen sich α-helices und β-faltblätter aus? Belegen Sie Ihre Antwort mit den entsprechenden Daten. (phi/psi-winkel). - Wodurch
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion. Mag. Gerald Trutschl
 Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Aufbau und Konformation von Polypeptiden
 1 Aufbau und Konformation von Polypeptiden Peter Güntert, Sommersemester 2009 Hierarchie von Proteinstrukturen Primärstruktur: Aminosäuresequenz Sekundärstruktur: Helices, Faltblätter, Turns, Loops Tertiärstruktur:
1 Aufbau und Konformation von Polypeptiden Peter Güntert, Sommersemester 2009 Hierarchie von Proteinstrukturen Primärstruktur: Aminosäuresequenz Sekundärstruktur: Helices, Faltblätter, Turns, Loops Tertiärstruktur:
1 Einleitung. 1.1 Die extrazelluläre Matrix
 3 1 Einleitung 1.1 Die extrazelluläre Matrix Als extrazelluläre Matrix (EZM) bezeichnet man die Strukturen, die den Raum zwischen den Zellen der verschiedenen Gewebe ausfüllen und für deren Integrität
3 1 Einleitung 1.1 Die extrazelluläre Matrix Als extrazelluläre Matrix (EZM) bezeichnet man die Strukturen, die den Raum zwischen den Zellen der verschiedenen Gewebe ausfüllen und für deren Integrität
Protokoll Versuch B1 Modellbau, Elektronendichtekarten und Symmetrie
 Protokoll Versuch B1 Modellbau, Elektronendichtekarten und Symmetrie Gruppe 8 Susanne Duncker und Friedrich Hahn Gruppe 8 Susanne Duncker Friedrich Hahn Versuch B1: Modellbau, Elektronendichtekarten und
Protokoll Versuch B1 Modellbau, Elektronendichtekarten und Symmetrie Gruppe 8 Susanne Duncker und Friedrich Hahn Gruppe 8 Susanne Duncker Friedrich Hahn Versuch B1: Modellbau, Elektronendichtekarten und
2 Coulomb-Kraft Elektrisches Potential... 9
 Inhaltsverzeichnis I Strukturprinzipien 7 1 Konservative Kraft / Potential 7 2 Coulomb-Kraft 8 2.1 Elektrisches Potential....................... 9 3 Abstoßendes Potential 10 4 Bindungsarten 10 4.1 Ionische
Inhaltsverzeichnis I Strukturprinzipien 7 1 Konservative Kraft / Potential 7 2 Coulomb-Kraft 8 2.1 Elektrisches Potential....................... 9 3 Abstoßendes Potential 10 4 Bindungsarten 10 4.1 Ionische
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Aminosäuren - Proteine
 Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne
 Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler
 Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Peptide Proteine. 1. Aminosäuren. Alle optisch aktiven proteinogenen Aminosäuren gehören der L-Reihe an: 1.1 Struktur der Aminosäuren
 1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
MM Biopolymere. Michael Meyer. Vorlesung XV
 Biopolymere Vorlesung XV Simulation von Biomolekülen Modellierung von Proteinen Identifizierung und/oder Verwandtschaft mit anderen Proteinen Funktion eines Proteins oder Sequenzfragmentes Modellierung
Biopolymere Vorlesung XV Simulation von Biomolekülen Modellierung von Proteinen Identifizierung und/oder Verwandtschaft mit anderen Proteinen Funktion eines Proteins oder Sequenzfragmentes Modellierung
1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur
 Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 4. Protein-Stabilisierung Proteine sind
Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 4. Protein-Stabilisierung Proteine sind
2.2. Peptide. Peptide entstehen durch Kondensation der a-carboxylgruppe einer Aminosäure mit der a-aminogruppe einer anderen Aminosäure
 2.2. Peptide Peptide entstehen durch Kondensation der a-carboxylgruppe einer Aminosäure mit der a-aminogruppe einer anderen Aminosäure Peptid: bis zu ~30 linear über Peptidbindung verknüpfte Aminosäuren
2.2. Peptide Peptide entstehen durch Kondensation der a-carboxylgruppe einer Aminosäure mit der a-aminogruppe einer anderen Aminosäure Peptid: bis zu ~30 linear über Peptidbindung verknüpfte Aminosäuren
15. Aminosäuren, Peptide und Proteine
 15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
Vertiefendes Seminar zur Vorlesung Biochemie I Bearbeitung Übungsblatt 4
 Vertiefendes Seminar zur Vorlesung Biochemie I 20.11.2015 Bearbeitung Übungsblatt 4 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Vertiefendes Seminar zur Vorlesung Biochemie I 20.11.2015 Bearbeitung Übungsblatt 4 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
1. Peptide und Proteine
 1. Peptide und Proteine 1.1 Einleitung Peptide und Proteine sind ubiquitär in allen Organismen vorhanden. Sie sind die Moleküle des Lebens. Sie sind die Funktionsreagenzien in den Zellen und verantwortlich
1. Peptide und Proteine 1.1 Einleitung Peptide und Proteine sind ubiquitär in allen Organismen vorhanden. Sie sind die Moleküle des Lebens. Sie sind die Funktionsreagenzien in den Zellen und verantwortlich
Aminosäurenanalytik. Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE
 Aminosäurenanalytik Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE Proteinfällung 2 Proteinfällung 3 Proteinfällung 4 Proteinfällung 5 Proteinfällung
Aminosäurenanalytik Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE Proteinfällung 2 Proteinfällung 3 Proteinfällung 4 Proteinfällung 5 Proteinfällung
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
DNA: Aufbau, Struktur und Replikation
 DNA: Aufbau, Struktur und Replikation Biochemie Die DNA als Träger der Erbinformation Im Genom sind sämtliche Informationen in Form von DNA gespeichert. Die Information des Genoms ist statisch, d. h. in
DNA: Aufbau, Struktur und Replikation Biochemie Die DNA als Träger der Erbinformation Im Genom sind sämtliche Informationen in Form von DNA gespeichert. Die Information des Genoms ist statisch, d. h. in
Übungsaufgaben zu Aminosäuren, Peptiden, Proteinen und DNA
 Übungsaufgaben zu Aminosäuren, Peptiden, Proteinen und DNA 1. Aminosäuren a) Benennen Sie die folgenden Aminosäuren nach den Regeln der IUPAC: Ala, Gly, Ile, Thr b) Die Aminosäuren in Proteinen sind α-aminocarbonsäuren
Übungsaufgaben zu Aminosäuren, Peptiden, Proteinen und DNA 1. Aminosäuren a) Benennen Sie die folgenden Aminosäuren nach den Regeln der IUPAC: Ala, Gly, Ile, Thr b) Die Aminosäuren in Proteinen sind α-aminocarbonsäuren
Glykogen. 1,6-glykosidisch verbunden sind. Die Verzweigungen dienen dazu das Molekül an vielen Stellen gleichzeitig ab- oder aufzubauen.
 Glykogen Glykogen stellt die Speicherform der Glucose dar. Der menschliche Körper kann Glucose nicht speichern (Osmose). Es können ca. 400g Glucose als Glykogen aufbewahrt werden. Chemischer Aufbau: Glykogen
Glykogen Glykogen stellt die Speicherform der Glucose dar. Der menschliche Körper kann Glucose nicht speichern (Osmose). Es können ca. 400g Glucose als Glykogen aufbewahrt werden. Chemischer Aufbau: Glykogen
Aufgabe 2: (Aminosäuren)
 Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur
 Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 2. Faserproteine - lange Moleküle deren
Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 2. Faserproteine - lange Moleküle deren
Falschfaltung von Proteinen
 Falschfaltung von Proteinen - Aggregation - domain swapping - amyloidogene Strukturen Was determiniert die Faltung von Proteinen? Einfachstes System: Zwei-Zustandsmodell N U Energie U dg ÜS dg* N Molekulare
Falschfaltung von Proteinen - Aggregation - domain swapping - amyloidogene Strukturen Was determiniert die Faltung von Proteinen? Einfachstes System: Zwei-Zustandsmodell N U Energie U dg ÜS dg* N Molekulare
Versuch: Denaturierung von Eiweiß
 Philipps-Universität Marburg 29.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Denaturierung
Philipps-Universität Marburg 29.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Denaturierung
6. FALTUNG UND STABILITÄT GLOBULÄRER EINDOMÄNENPROTEINE
 6. FALTUNG UND STABILITÄT GLOBULÄRER EINDOMÄNENPROTEINE 6.1. Allgemeine Erkenntnisse Die Aufklärung des Faltungsweges eines Proteins umfaßt die komplette Beschreibung des Ausgangs- (entfaltet) und Endzustandes
6. FALTUNG UND STABILITÄT GLOBULÄRER EINDOMÄNENPROTEINE 6.1. Allgemeine Erkenntnisse Die Aufklärung des Faltungsweges eines Proteins umfaßt die komplette Beschreibung des Ausgangs- (entfaltet) und Endzustandes
Die Persistenzlänge ist sequenzabhängig, für Poly-Serin etwa 5 AS. Der entfaltete Zustand ist Gegenstand intensiver Untersuchungen
 Die Bildung von Quartärstruktur ermöglicht den Bau großer, aber auch multifunktionaler Proteine 9.2 Proteinfaltung Proteine können unter bestimmten Bedingungen denaturiert (entfaltet) werden, das heißt,
Die Bildung von Quartärstruktur ermöglicht den Bau großer, aber auch multifunktionaler Proteine 9.2 Proteinfaltung Proteine können unter bestimmten Bedingungen denaturiert (entfaltet) werden, das heißt,
UAufgabe 12: (evolutiv konservierte Aminosäuren)
 UAufgabe 12: (evolutiv konservierte Aminosäuren) Aufgabenstellung Wählen Sie zur Darstellung evolutiv konservierter Aminosäure-Positionen in "1lla" eine ihnen sinnvoll erscheinende Anfärbung. Exportieren
UAufgabe 12: (evolutiv konservierte Aminosäuren) Aufgabenstellung Wählen Sie zur Darstellung evolutiv konservierter Aminosäure-Positionen in "1lla" eine ihnen sinnvoll erscheinende Anfärbung. Exportieren
KV: DNA Michael Altmann
 Institut für Biochemie und Molekulare Medizin KV: DNA Michael Altmann Herbstsemester 2008/2009 Übersicht VL DNA 1.) Lernmittel 1-3 2.) Struktur der Doppelhelix 3.) Die 4 Bausteine der DNA 4.) Bildung eines
Institut für Biochemie und Molekulare Medizin KV: DNA Michael Altmann Herbstsemester 2008/2009 Übersicht VL DNA 1.) Lernmittel 1-3 2.) Struktur der Doppelhelix 3.) Die 4 Bausteine der DNA 4.) Bildung eines
Referat : Aufbau v. Proteinen u. ihre Raumstruktur
 Referat : Aufbau v. Proteinen u. ihre Raumstruktur 1. Einleitung Unsere Körperzellen enthalten einige Tausend verschiedene Proteine wobei man schätzt, das insgesamt über 50 000 verschiedene Eiweißstoffe
Referat : Aufbau v. Proteinen u. ihre Raumstruktur 1. Einleitung Unsere Körperzellen enthalten einige Tausend verschiedene Proteine wobei man schätzt, das insgesamt über 50 000 verschiedene Eiweißstoffe
Verfahren zu Strukturvorhersagen in vereinfachten Modellen. Tobias Voigt Sommerakademie 2002 St. Johann
 Verfahren zu Strukturvorhersagen in vereinfachten Modellen Tobias Voigt Sommerakademie 2002 St. Johann Einführung! Sequenzierung von Proteinen und Nukleinsäuren ist heute Routine! Die räumliche Struktur
Verfahren zu Strukturvorhersagen in vereinfachten Modellen Tobias Voigt Sommerakademie 2002 St. Johann Einführung! Sequenzierung von Proteinen und Nukleinsäuren ist heute Routine! Die räumliche Struktur
Aromatische Diazoniumionen
 Aromatische Diazoniumionen Wichtige Reaktive Zwischenstufe Aromatische Diazoniumionen Aromatische Diazoniumionen Azofarbstoffe Organische Chemie für MST 7 Lienkamp/ Prucker/ Rühe 7 Inhalt Amine Nomenklatur,
Aromatische Diazoniumionen Wichtige Reaktive Zwischenstufe Aromatische Diazoniumionen Aromatische Diazoniumionen Azofarbstoffe Organische Chemie für MST 7 Lienkamp/ Prucker/ Rühe 7 Inhalt Amine Nomenklatur,
Das Komplementsystem. Membranangriffskomplex Regulation Komplementrezeptoren kleine C-Fragmente
 Das Komplementsystem Membranangriffskomplex Regulation Komplementrezeptoren kleine C-Fragmente Der Membranangriffskomplex C5 Konvertase alle 3 Aktivierungswege mit einem Ziel: Bildung einer C3-Konvertase
Das Komplementsystem Membranangriffskomplex Regulation Komplementrezeptoren kleine C-Fragmente Der Membranangriffskomplex C5 Konvertase alle 3 Aktivierungswege mit einem Ziel: Bildung einer C3-Konvertase
10 BIOGENE-AMINE 4 NICHT-PROTEINOGENE- AS. 20 PROTEINOGENE AS glucoplastisch/ketoplastisch 8 ESSENTIELLE AS
 Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen. Abb. aus Stryer (5th Ed.)
 Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen Die verschiedenen Ribosomen-Komplexe können im Elektronenmikroskop beobachtet werden Durch Röntgenkristallographie wurden
Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen Die verschiedenen Ribosomen-Komplexe können im Elektronenmikroskop beobachtet werden Durch Röntgenkristallographie wurden
Hemmung der Enzym-Aktivität
 Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Was ist der Promotor? Antwort: Eine spezielle Nucleotidsequenz auf der DNA, an der die RNA-Polymerase bindet um die Transkription zu starten.
 Was ist der Promotor? Antwort: Eine spezielle Nucleotidsequenz auf der DNA, an der die RNA-Polymerase bindet um die Transkription zu starten. Wie bezeichnet man den Strang der DNA- Doppelhelix, der die
Was ist der Promotor? Antwort: Eine spezielle Nucleotidsequenz auf der DNA, an der die RNA-Polymerase bindet um die Transkription zu starten. Wie bezeichnet man den Strang der DNA- Doppelhelix, der die
Immunbiologie. Teil 3
 Teil 3 Haupthistokompatibilitätskomplex (1): - es gibt einen grundlegenden Unterschied, wie B-Lymphozyten und T-Lymphozyten ihr relevantes Antigen erkennen - B-Lymphozyten binden direkt an das komplette
Teil 3 Haupthistokompatibilitätskomplex (1): - es gibt einen grundlegenden Unterschied, wie B-Lymphozyten und T-Lymphozyten ihr relevantes Antigen erkennen - B-Lymphozyten binden direkt an das komplette
Posttranskriptionale RNA-Prozessierung
 Posttranskriptionale RNA-Prozessierung Spaltung + Modifikation G Q Spleissen + Editing U UUU Prozessierung einer prä-trna Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende
Posttranskriptionale RNA-Prozessierung Spaltung + Modifikation G Q Spleissen + Editing U UUU Prozessierung einer prä-trna Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende
Zusammensetzung und Struktur der Proteine. Stryer (6. Auflage) Kapitel 2
 Zusammensetzung und Struktur der Proteine Stryer (6. Auflage) Kapitel 2 Vielfalt der Proteine Wie kommt diese Vielfalt an Proteinen zustande? 1. Peptide und Polypeptide sind Ketten aus 20 verschiedenen
Zusammensetzung und Struktur der Proteine Stryer (6. Auflage) Kapitel 2 Vielfalt der Proteine Wie kommt diese Vielfalt an Proteinen zustande? 1. Peptide und Polypeptide sind Ketten aus 20 verschiedenen
Kohlenhydrate Aminosäuren Peptide
 Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Nanotechnologie der Biomoleküle. Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie. Aufbau Struktur Funktion
 anotechnologie der Biomoleküle Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie Aufbau Struktur Funktion Zentrum für Mikro- und anotechnologien Das Miller-Urey-Experiment (auch
anotechnologie der Biomoleküle Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie Aufbau Struktur Funktion Zentrum für Mikro- und anotechnologien Das Miller-Urey-Experiment (auch
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine
 4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
Primärstruktur Proteinsequenzierung
 Proteinanalytik II Primärstruktur Proteinsequenzierung Hydrolyse der Peptidbindung Aminosäurenachweis Ninhydrin Aminosäurenachweis Fluorescamin Proteinhydrolysat Ionenaustauschchromatographie Polypeptidstruktur
Proteinanalytik II Primärstruktur Proteinsequenzierung Hydrolyse der Peptidbindung Aminosäurenachweis Ninhydrin Aminosäurenachweis Fluorescamin Proteinhydrolysat Ionenaustauschchromatographie Polypeptidstruktur
Aliphatische Aminosäuren. Aromatische Aminosäuren
 Prof. Dr..-U. eißig rganische Chemie I 17.1 Aliphatische Aminosäuren systematischer ame (Trivialname) truktur Vorkommen, Bedeutung 2-Aminoethansäure (α-aminoessigsäure, Glycin) 3 C 2 C 2 α Proteine, Peptide
Prof. Dr..-U. eißig rganische Chemie I 17.1 Aliphatische Aminosäuren systematischer ame (Trivialname) truktur Vorkommen, Bedeutung 2-Aminoethansäure (α-aminoessigsäure, Glycin) 3 C 2 C 2 α Proteine, Peptide
MM Proteinmodelling. Michael Meyer. Vorlesung XVII
 Proteinmodelling Vorlesung XVII Proteinstrukturen Es besteht ein sehr großer Bedarf an Proteinstrukturen: Die Kenntnis der 3D-Struktur hat große Vorteile für das Design neuer Wirkstoffe. Experimentelle
Proteinmodelling Vorlesung XVII Proteinstrukturen Es besteht ein sehr großer Bedarf an Proteinstrukturen: Die Kenntnis der 3D-Struktur hat große Vorteile für das Design neuer Wirkstoffe. Experimentelle
7. Zusammenfassung und Ausblick
 7. Zusammenfassung und Ausblick 7.1 Die Mitglieder der Rag-Familie Die verschiedenen Isoformen der Rag-Familie lagen, sofern sie rekombinant löslich isoliert wurden, als Dimer oder höhere Oligomere vor.
7. Zusammenfassung und Ausblick 7.1 Die Mitglieder der Rag-Familie Die verschiedenen Isoformen der Rag-Familie lagen, sofern sie rekombinant löslich isoliert wurden, als Dimer oder höhere Oligomere vor.
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
4. CIS / TRANS -ISOMERISIERUNG VON PEPTIDYL-PROLYL-BINDUNGEN
 4. CIS / TRANS -ISOMERISIERUNG VON PEPTIDYL-PROLYL-BINDUNGEN ALS LANGSAME KONFORMATIONSÄNDERUNGEN UND DEREN KATALYSE DURCH PEPTIDYL-PROLYL-CIS / TRANS -ISOMERASEN 4.1. Eigenschaften von Peptidyl-prolyl-bindungen
4. CIS / TRANS -ISOMERISIERUNG VON PEPTIDYL-PROLYL-BINDUNGEN ALS LANGSAME KONFORMATIONSÄNDERUNGEN UND DEREN KATALYSE DURCH PEPTIDYL-PROLYL-CIS / TRANS -ISOMERASEN 4.1. Eigenschaften von Peptidyl-prolyl-bindungen
Aufgabe 1. Bakterien als Untersuchungsgegenstand!
 Genetik I Aufgabe 1. Bakterien als Untersuchungsgegenstand 1. Beschriften Sie die Abbildung zu den Bakterien. 2. Nennen Sie Vorteile, die Bakterien wie Escherichia coli so wertvoll für die genetische Forschung
Genetik I Aufgabe 1. Bakterien als Untersuchungsgegenstand 1. Beschriften Sie die Abbildung zu den Bakterien. 2. Nennen Sie Vorteile, die Bakterien wie Escherichia coli so wertvoll für die genetische Forschung
Intelligente Polymere. Anne Oestreicher
 Intelligente Polymere Anne Oestreicher 09.12.2014 2 Intelligente Polymere 1. Einleitung 2. Stimuli-responsive Polymere 3. Thermoresponsive Polymere a. Kritische Entmischungstemperaturen b. Thermodynamik
Intelligente Polymere Anne Oestreicher 09.12.2014 2 Intelligente Polymere 1. Einleitung 2. Stimuli-responsive Polymere 3. Thermoresponsive Polymere a. Kritische Entmischungstemperaturen b. Thermodynamik
Aneliya Petrova 1, Günter Westphal 1, Rafael Valbuena 1 und Jochen Ringe 2
 LIFIS ONLINE [13.09.11] ISSN 1864-6972 Aneliya Petrova 1, Günter Westphal 1, Rafael Valbuena 1 und Jochen Ringe 2 Struktur und technofunktionelle Eigenschaften von Kollagenen tierischen Ursprungs Kollagenhaltiges
LIFIS ONLINE [13.09.11] ISSN 1864-6972 Aneliya Petrova 1, Günter Westphal 1, Rafael Valbuena 1 und Jochen Ringe 2 Struktur und technofunktionelle Eigenschaften von Kollagenen tierischen Ursprungs Kollagenhaltiges
Hypothetisches Modell
 Hypothetisches Modell Das Heutige Paper Inhalt: SCF bindet Auxin direkt TIR1 ist ein Auxin Rezeptor Auxin bindet direkt an TIR1, es sind keine zusätzlichen Komponenten nötig Methode Normales Pull down
Hypothetisches Modell Das Heutige Paper Inhalt: SCF bindet Auxin direkt TIR1 ist ein Auxin Rezeptor Auxin bindet direkt an TIR1, es sind keine zusätzlichen Komponenten nötig Methode Normales Pull down
Synthese von Teroxazolen als Peptidmimetika
 Synthese von Teroxazolen als Peptidmimetika Dissertation zur Erlangung des Doktorgrades der Naturwissenschaften vorgelegt beim Fachbereich Biochemie, Chemie und Pharmazie der Johann Wolfgang Goethe-Universität
Synthese von Teroxazolen als Peptidmimetika Dissertation zur Erlangung des Doktorgrades der Naturwissenschaften vorgelegt beim Fachbereich Biochemie, Chemie und Pharmazie der Johann Wolfgang Goethe-Universität
...-Arg-Met-Phe-Ala-Asn-His-Lys-Ser-Val-Gly-...
 1. Im Enzym Xase, das aus einer Polypeptidkette aus 300 Aminosäuren besteht, findet sich in der Region der Aminosäuren 40-50 die folgende Aminosäurensequenz:...-Arg-Met-Phe-Ala-Asn-His-Lys-Ser-Val-Gly-...
1. Im Enzym Xase, das aus einer Polypeptidkette aus 300 Aminosäuren besteht, findet sich in der Region der Aminosäuren 40-50 die folgende Aminosäurensequenz:...-Arg-Met-Phe-Ala-Asn-His-Lys-Ser-Val-Gly-...
Eukaryotische messenger-rna
 Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende u.u. nicht-codierende Bereiche (Introns) Spleißen von prä-mrna Viele Protein-codierende Gene in Eukaryoten sind durch nicht-codierende
Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende u.u. nicht-codierende Bereiche (Introns) Spleißen von prä-mrna Viele Protein-codierende Gene in Eukaryoten sind durch nicht-codierende
Grundlagen der Zellulären Biochemie
 Grundlagen der Zellulären Biochemie Proteinstruktur Vorlesung zum Modul BCB P07 im Bachelor-Studiengang Biochemie Hannover Prof. J. Alves, Institut für Biophysikalische Chemie, MHH Damit liegen die fünf
Grundlagen der Zellulären Biochemie Proteinstruktur Vorlesung zum Modul BCB P07 im Bachelor-Studiengang Biochemie Hannover Prof. J. Alves, Institut für Biophysikalische Chemie, MHH Damit liegen die fünf
Das Zytoskelett (Gastvorlesung R. Brandt, Neurobiologie)
 Das Zytoskelett (Gastvorlesung R. Brandt, Neurobiologie) Inhalt: 1. Struktur und Dynamik der zytoskeletalen Filamentsysteme 2. Regulation der zytoskeletalen Komponenten 3. Molekulare Motoren 4. Zytoskelett
Das Zytoskelett (Gastvorlesung R. Brandt, Neurobiologie) Inhalt: 1. Struktur und Dynamik der zytoskeletalen Filamentsysteme 2. Regulation der zytoskeletalen Komponenten 3. Molekulare Motoren 4. Zytoskelett
8. Aminosäuren - (Proteine) Eiweiß
 8. Aminosäuren - (Proteine) Eiweiß Proteine sind aus Aminosäuren aufgebaut. Aminosäuren bilden die Grundlage der belebten Welt. 8.1 Struktur der Aminosäuren Aminosäuren sind organische Moleküle, die mindestens
8. Aminosäuren - (Proteine) Eiweiß Proteine sind aus Aminosäuren aufgebaut. Aminosäuren bilden die Grundlage der belebten Welt. 8.1 Struktur der Aminosäuren Aminosäuren sind organische Moleküle, die mindestens
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit
 In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
CELLCOAT Proteinbeschichtete Zellkultur Gefäße
 1 Zell und 2 HTS CELLCOAT Protein Gefäße CELLCOAT Proteinbeschichtete Zellkultur Gefäße Die Greiner BioOne Produktlinie CELLCOAT beinhaltet Zellkulturgefäße, die mit Proteinen der extrazellulären Matrix
1 Zell und 2 HTS CELLCOAT Protein Gefäße CELLCOAT Proteinbeschichtete Zellkultur Gefäße Die Greiner BioOne Produktlinie CELLCOAT beinhaltet Zellkulturgefäße, die mit Proteinen der extrazellulären Matrix
Der Haupthistokompatibilitätskomplex (MHC) AG-Erkennung von Ly. Doppelspezifität der T-Ly: AG-Spezifität und MHC-Spezifität
 Der Haupthistokompatibilitätskomplex (MHC) Major Histocompatibility Complex AG-Erkennung von Ly B-Ly: Erkennung unmittelbar der Determinanten von intakten AG T-Ly: in Komplex mit eigenen MHC- Molekülen
Der Haupthistokompatibilitätskomplex (MHC) Major Histocompatibility Complex AG-Erkennung von Ly B-Ly: Erkennung unmittelbar der Determinanten von intakten AG T-Ly: in Komplex mit eigenen MHC- Molekülen
COOH. Die Aminosäuren tragen laborübliche Abkürzungen, so stehen z. B. Gly für Glycin oder Phe für Phenylalanin.
 Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Faltung, Dynamik und strukturelle Evolution der Proteine (Voet Kapitel 8)
 Faltung, Dynamik und strukturelle Evolution der Proteine (Voet Kapitel 8) 1. Proteinfaltung: Theorie und Experiment 2. Proteindynamik 3. Strukturelle Evolution A. Protein-Renaturierung Denaturierung in
Faltung, Dynamik und strukturelle Evolution der Proteine (Voet Kapitel 8) 1. Proteinfaltung: Theorie und Experiment 2. Proteindynamik 3. Strukturelle Evolution A. Protein-Renaturierung Denaturierung in
Proteine: Dreidimensionale Struktur
 Proteine: Dreidimensionale Struktur 1. Sekundärstruktur A. Die Peptidgruppe B. Reguläre Sekundärstrukktur: α-helix und β-faltblatt C. Faserproteine D. Nichtrepetitive Proteinstruktur 2. Tertiärstruktur
Proteine: Dreidimensionale Struktur 1. Sekundärstruktur A. Die Peptidgruppe B. Reguläre Sekundärstrukktur: α-helix und β-faltblatt C. Faserproteine D. Nichtrepetitive Proteinstruktur 2. Tertiärstruktur
Charakterisierung von Einzelbindungs-Konformationsänderungen in Polypeptiden durch chemische Modifikation und Enzymkatalyse. 1.
 harakterisierung von Einzelbindungs-Konformationsänderungen in Polypeptiden durch chemische Modifikation und Enzymkatalyse 1. Einleitung Peptide sind u. a. in Form von ormonen, Transmittern und Modulatoren
harakterisierung von Einzelbindungs-Konformationsänderungen in Polypeptiden durch chemische Modifikation und Enzymkatalyse 1. Einleitung Peptide sind u. a. in Form von ormonen, Transmittern und Modulatoren
3.2 Posttranslationelle Modifikation von Wt1 durch Phosphorylierung
 3.2 Posttranslationelle Modifikation von Wt1 durch Phosphorylierung Transkriptionsfaktoren erfahren oft eine posttranslationelle Modifikation in Form von Phosphorylierung und werden dadurch in ihrer Aktivität
3.2 Posttranslationelle Modifikation von Wt1 durch Phosphorylierung Transkriptionsfaktoren erfahren oft eine posttranslationelle Modifikation in Form von Phosphorylierung und werden dadurch in ihrer Aktivität
Organische Experimentalchemie
 PD Dr. Alexander Breder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 rganische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und Biologie
PD Dr. Alexander Breder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 rganische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und Biologie
Praktikum Biochemie B.Sc. Water Science WS Enzymregulation. Marinja Niggemann, Denise Schäfer
 Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Dieser Anteil ist oft experimentell zumindest näherungsweise zugänglich, zum Beispiel durch optische Messungen
 Dieser Anteil ist oft experimentell zumindest näherungsweise zugänglich, zum Beispiel durch optische Messungen Die Kooperativität zeigt sich in einem sigmoidalen Verlauf des Ordnungsparameters bei Änderung
Dieser Anteil ist oft experimentell zumindest näherungsweise zugänglich, zum Beispiel durch optische Messungen Die Kooperativität zeigt sich in einem sigmoidalen Verlauf des Ordnungsparameters bei Änderung
Grundlagen zum Verständnis chemischer Reaktionen = Handwerkszeug
 Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Denaturierung von Proteinen
 Denaturierung von Proteinen = Auflösen der konformationsstabilisierenden Wechselwirkungen, wodurch die Konformation reversibel oder irreversibel zerstört wird durch Erhitzen, Einwirkung von Scherkräften,
Denaturierung von Proteinen = Auflösen der konformationsstabilisierenden Wechselwirkungen, wodurch die Konformation reversibel oder irreversibel zerstört wird durch Erhitzen, Einwirkung von Scherkräften,
Invasionsmechanismen und Metastasierung des Urothelkarzinoms. Dr. med. Karl-Ernst Ambs, Facharzt für Urologie, Parkstr.
 Invasionsmechanismen und Metastasierung des Urothelkarzinoms Dr. med. Karl-Ernst Ambs, Facharzt für Urologie, Parkstr. 6 65812 Bad Soden Allgemeines Hauptursachen der krebsspezifischen Mortalität sind
Invasionsmechanismen und Metastasierung des Urothelkarzinoms Dr. med. Karl-Ernst Ambs, Facharzt für Urologie, Parkstr. 6 65812 Bad Soden Allgemeines Hauptursachen der krebsspezifischen Mortalität sind
Zusammenfassung. 10 Zusammenfassung
 10 Zusammenfassung Im Rahmen dieser Arbeit wurden neuartige Ir III und Rh III Organometallkomplexe der Verbindungsklassen [(η 5 -Cp*)ML(XX )] n+, [(η 5 -Cp*)M(XX X )] n+ und fac-[ircl 3 (DMSO)(pp)] synthetisiert
10 Zusammenfassung Im Rahmen dieser Arbeit wurden neuartige Ir III und Rh III Organometallkomplexe der Verbindungsklassen [(η 5 -Cp*)ML(XX )] n+, [(η 5 -Cp*)M(XX X )] n+ und fac-[ircl 3 (DMSO)(pp)] synthetisiert
Zucker und Polysaccharide (Voet Kapitel 10)
 Zucker und Polysaccharide (Voet Kapitel 10) 1. Monosaccharide 2. Polysaccharide 3. Glycoproteine Kohlenhydrate oder Saccharide = essentielle Bestandteile der Organismen = Hydrate des Kohlenstoffs Grundbaustein
Zucker und Polysaccharide (Voet Kapitel 10) 1. Monosaccharide 2. Polysaccharide 3. Glycoproteine Kohlenhydrate oder Saccharide = essentielle Bestandteile der Organismen = Hydrate des Kohlenstoffs Grundbaustein
Chemie für Mediziner. Norbert Sträter
 Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
Vertiefendes Seminar zur Vorlesung Biochemie
 Vertiefendes Seminar zur Vorlesung Biochemie 31.10.2014 Proteine: Struktur Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Vertiefendes Seminar zur Vorlesung Biochemie 31.10.2014 Proteine: Struktur Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Fragen zur Vorlesung Grundlagen der Biologie (I) Teil 1: Biomoleküle (B. Moerschbacher)
 Fragen zur Vorlesung Grundlagen der Biologie (I) Teil 1: Biomoleküle (B. Moerschbacher) Wieviele Elektronen, Protonen und Neutronen besitzt ein Kohlenstoffatom? Wie unterscheiden sich die Kohlenstoffisotope
Fragen zur Vorlesung Grundlagen der Biologie (I) Teil 1: Biomoleküle (B. Moerschbacher) Wieviele Elektronen, Protonen und Neutronen besitzt ein Kohlenstoffatom? Wie unterscheiden sich die Kohlenstoffisotope
t-rna Ribosom (adapted from the handouts of Prof. Beck-Sickinger, Universität Leipzig)
 ukleinsäuren speichern die Erbinformation. Das menschliche Genom ist in jeder Zelle aus 3900 Millionen Basenpaare (Mbp) aufgebaut und hat eine Gesamtlänge von 99 cm. t-ra Ribosom (adapted from the handouts
ukleinsäuren speichern die Erbinformation. Das menschliche Genom ist in jeder Zelle aus 3900 Millionen Basenpaare (Mbp) aufgebaut und hat eine Gesamtlänge von 99 cm. t-ra Ribosom (adapted from the handouts
Stützgewebe 1/3. Knorpel
 Stützgewebe 1/3 Knorpel Knorpel Knorpelzellen Matrix Chondroblasten Chondrozyten Wasser (80%) Kollagen Typ II (Hauptanteil) Kollagen Typ IX (verbindet Typ II Fibrillen) Kollagen Typ X Kollagen Typ XI (Teil
Stützgewebe 1/3 Knorpel Knorpel Knorpelzellen Matrix Chondroblasten Chondrozyten Wasser (80%) Kollagen Typ II (Hauptanteil) Kollagen Typ IX (verbindet Typ II Fibrillen) Kollagen Typ X Kollagen Typ XI (Teil
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Funktion von Proteinen:
 Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail. Mag. Gerald Trutschl
 Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Vortrag Nanostrukturphysik II: Nanoskalige Biomoleküle. Kai Sauer
 Vortrag Nanostrukturphysik II: Nanoskalige Biomoleküle Kai Sauer Gliederung Definition Grundlagen Funktionen im Körper Proteine Proteinfaltungen Protein-Protein-Wechselwirkung Interprotein-Wechselwirkung
Vortrag Nanostrukturphysik II: Nanoskalige Biomoleküle Kai Sauer Gliederung Definition Grundlagen Funktionen im Körper Proteine Proteinfaltungen Protein-Protein-Wechselwirkung Interprotein-Wechselwirkung
Proteinstrukturklassen α-helikale Proteine
 Proteinstrukturklassen α-helikale Proteine Wintersemester 2011/12 Peter Güntert Domäne Modul Faltung Domäne (domain): Polypeptidkette (oder Teil davon), die unabhängig in eine stabile, kompakte Tertiärstruktur
Proteinstrukturklassen α-helikale Proteine Wintersemester 2011/12 Peter Güntert Domäne Modul Faltung Domäne (domain): Polypeptidkette (oder Teil davon), die unabhängig in eine stabile, kompakte Tertiärstruktur
Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine
 Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka Übungen zur Vorlesung Aminosäuren, Peptide, Proteine Dr. Katja
Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka Übungen zur Vorlesung Aminosäuren, Peptide, Proteine Dr. Katja
Proteinbestimmung. Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der Proteinbestimmung mit den folgenden Lehrzielen:
 Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der mit den folgenden Lehrzielen: Verständnis der Prinzipien der sowie deren praktischer Durchführung Unterscheidung zwischen
Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der mit den folgenden Lehrzielen: Verständnis der Prinzipien der sowie deren praktischer Durchführung Unterscheidung zwischen
1.1 Die zellulare Eisenaufnahme bei Vertebraten
 1 Einleitung 1.1 Die zellulare Eisenaufnahme bei Vertebraten Mit Ausnahme einiger Bakterienarten benötigen nahezu alle Organismen Eisen für ihren Metabolismus. Eisen ist daher ein zentrales Element, dessen
1 Einleitung 1.1 Die zellulare Eisenaufnahme bei Vertebraten Mit Ausnahme einiger Bakterienarten benötigen nahezu alle Organismen Eisen für ihren Metabolismus. Eisen ist daher ein zentrales Element, dessen
Dipolmomente + - a ohne Feld b mit Feld. δ + δ- δ + δ - δ + δ - δ + δ - δ + δ - δ + Dipolmoment: µ = q * d
 CI_folie29 Dipolmomente δ- + - a ohne Feld b mit Feld + + + + + + - - - - - - Effekt eines elektrostatischen Feldes auf die rientierung polarer Moleküle. Dipolmoment: µ = q * d d: Abstand zwischen den
CI_folie29 Dipolmomente δ- + - a ohne Feld b mit Feld + + + + + + - - - - - - Effekt eines elektrostatischen Feldes auf die rientierung polarer Moleküle. Dipolmoment: µ = q * d d: Abstand zwischen den
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
