Einfluss verschiedener Antioxidantien auf den oxidativen Stress und die körperliche Leistungsfähigkeit im Hochleistungssport
|
|
|
- Karsten Giese
- vor 6 Jahren
- Abrufe
Transkript
1 Aus dem Institut für Kreislaufforschung und Sportmedizin der Deutschen Sporthochschule Köln Abteilung für präventive und rehabilitative Sport- und Leistungsmedizin Leiter: Universitätsprofessor Dr. med H.-G. Predel Einfluss verschiedener Antioxidantien auf den oxidativen Stress und die körperliche Leistungsfähigkeit im Hochleistungssport Inaugural-Dissertation zur Erlangung der Doktorwürde der Hohen Medizinischen Fakultät der Universität zu Köln vorgelegt von Kerstin Schäfer aus Köln Promoviert am 28. September 2011
2 Dekan: Universitätsprofessor Dr. med. Dr. h.c. Th. Krieg 1. Berichterstatter: Universitätsprofessor Dr. med W. Bloch 2. Berichterstatter: Universitätsprofessor Dr. med H.-G. Predel Erklärung Ich erkläre hiermit, dass ich die vorliegende Dissertationsschrift ohne unzulässige Hilfe Dritter und ohne Benutzung anderer als der angegebenen Hilfsmittel angefertigt habe; die aus fremden Quellen direkt oder indirekt übernommenen Gedanken sind als solche kenntlich gemacht. Bei der Auswahl und Auswertung des Materials sowie bei der Herstellung des Manuskriptes habe ich Unterstützungsleistungen von folgenden Personen erhalten: Universitätsprofessor Dr. med. W. Bloch Universitätsprofessor Dr. med. H.-G. Predel Mitarbeiter des Instituts für Medizinische Statistik, Informatik und Epidemiologie der Universität zu Köln Weitere Personen waren an der geistigen Herstellung der vorliegenden Arbeit nicht beteiligt. Insbesondere habe ich nicht die Hilfe einer Promotionsberaterin/ eines Promotionsberaters in Anspruch genommen. Dritte haben von mir weder unmittelbar noch mittelbar geldwerte Leistungen für Arbeiten erhalten, die im Zusammenhang mit dem Inhalt der vorgelegten Dissertationsschrift stehen. Die Dissertationsschrift wurde von mir bisher weder im Inland noch im Ausland in gleicher oder ähnlicher Form einer anderen Prüfungsbehörde vorgelegt. Köln, (Kerstin Schäfer)
3 Die dieser Arbeit zugrunde liegenden Experimente sind von mir mit Unterstützung von Herrn Dr. A. Vassiliadis durchgeführt worden.
4 Danksagung Zuerst möchte ich mich bei Universitätsprofessor Dr. med H.-G. Predel bedanken, der mir die Möglichkeit gab, meine Dissertation in seiner Abteilung zu erstellen und mich dabei unterstützte. Ich habe die freundliche Arbeitsatmosphäre im Institut sehr genossen. Universitätsprofessor Dr. med Wilhelm Bloch danke ich dafür, dass er sich meiner Arbeit annahm und immer Zeit für mich fand. Außerdem bedanke ich mich für die freundliche Unterstützung, konstruktive Kritik, fachliche Orientierungshilfe und die raschen Rückmeldungen. Mein besonderer Dank gilt Dr. sportwiss. A. Vassiliadis, der mir den Kontakt zu den Sportlern vermittelte, mich bei der Durchführung der Untersuchungen tatkräftig unterstützte, wegen mir unzählige Überstunden ableistete und ohne den diese Studie niemals stattgefunden hätte. Es hat mir großen Spaß gemacht, mit ihm zusammenzuarbeiten. Ein besonderer Dank gilt den Probanden, die einige blaue Flecken davontrugen und dennoch zu jedem Untersuchungstermin gut gelaunt und pünktlich den Weg ins Institut zurückfanden. Hierbei danke ich insbesondere Christoph, Christopher, Martin und Miguel für ihre Zuverlässigkeit und Geduld. Es hat mir großen Spaß bereitet mit euch zusammenzuarbeiten und dem ein oder anderen im Laufe der Zeit auch eine Blutabnahme beizubringen! Einen großen Anteil am Gelingen hatten auch Anke Schmitz, Astrid Hofrichter und Anna Dinter. Eure Herzlichkeit und Hilfe war einfach wundervoll. Vielen Dank auch Frau Bauer, Frau Bickenbach und Frau von Holtey, die sich stets bemühten, mir einen Termin im überfüllten Terminkalender von Professor Predel zu sichern. Ich danke meinen Freunden, die sich geduldig mein Leid angehört haben, mich immer wieder motivieren konnten weiterzumachen und für den nötigen Freizeitausgleich sorgten. Des Weiteren danke ich meiner Familie, die mir das Studium ermöglichten und insbesondere meinem Bruder Jens, der mir half diverse Computerprogramme richtig zu nutzen.
5 Meiner Familie und meinen Freunden
6 Inhaltsverzeichnis Abkürzungsverzeichnis 1 Einleitung Definition reaktiver Sauerstoffderivate Superoxidanion-Radikal Wasserstoffperoxid Hydroxyl-Radikal Organische Hydroperoxide Biochemische Mechanismen der Entstehung reaktiver Sauerstoffderivate Radikalbildung in den Mitochondrien Xanthinoxidase Respiratory Burst und NADPH-Oxidase-Komplexe (NOX) Weitere Entstehungsmechanismen von Sauerstoffradikalen Oxidativer Stress und Auswirkungen auf den Körper Lipidperoxidation Proteinmodifikation DNA-Modifikation Physiologische Reaktionen von ROS Antioxidative Schutzmechanismen Enzymatische Antioxidantien Nicht-enzymatische Antioxidantien Auswirkungen körperlicher Belastung auf die antioxidativen Enzyme Fragestellungen Methodik Probandenkollektiv Untersuchungsgang Laborbestimmungen... 27
7 2.4 Apparaturbesprechung und analytische Methoden Nahrungsergänzungsmittel Statistische Auswertung Untersuchungsergebnisse Untersuchungsreihe frubiase SPORT Ausdauer Leistungsdiagnostische Parameter der Stufentests Herzfrequenz Blutlaktat Sauerstoffaufnahme Atemäquivalent Respiratorischer Quotient Parameter des oxidativen Stresses drom BAP Untersuchungsreihe Injektion Leistungsdiagnostische Parameter der Stufentests Herzfrequenz Blutlaktat Sauerstoffaufnahme Atemäquivalent Respiratorischer Quotient Parameter des oxidativen Stresses drom BAP Diskussion Methodische Probleme Freie Sauerstoffradikale (drom) Untersuchungsreihe frubiase SPORT Ausdauer... 64
8 4.2.2 Untersuchungsreihe Injektion Biologisch antioxidatives Potential (BAP) Untersuchungsreihe frubiase SPORT Ausdauer Untersuchungsreihe Injektion Supplementierung mit Antioxidantien Einfluss von frubiase SPORT Ausdauer auf drom und BAP Einfluss der Injektionen auf drom und BAP Einfluss der Antioxidantien auf die Leistungsfähigkeit Untersuchungsreihe frubiase SPORT Ausdauer Untersuchungsreihe Injektion Zusammenfassung Literaturverzeichnis Anhang Untersuchungsreihe frubiase SPORT Ausdauer Untersuchungsreihe Injektion Lebenslauf
9 Abkürzungsverzeichnis Abkürzungsverzeichnis µ Mikro ADP AMP AMV ATP BAP BMI BZ CO 2 CRP Cu DNA drom Adenosindiphosphat Adenosinmonophosphat Atemminutenvolumen Adenosintriphosphat biologisch antioxidatives Potential Body Mass Index Blutzucker Kohlenstoffdioxid C- reaktives Protein Kupfer Desoxyribonucleinsäure reactive oxygen metabolites (freie Sauerstoffradikale) E-BAP Einheit BAP: µmol reduziertes Fe 3+ /l Blutplasma Erys FRAP-Assay Frubiase GPX GSH GSSG h H + H 2 O 2 Hb HF HKT HOCl Erythrozyten ferric reducing antioxidant power frubiase SPORT Ausdauer Glutathionperoxidase reduziertes Glutathion oxidiertes Glutathion Stunde Wasserstoff Wasserstoffperoxid Hämoglobin Herzfrequenz Hämatokrit Hypochlorsäure
10 Abkürzungsverzeichnis IL 6 Interleukin 6 KAT Leukos MDA mmol Mn ms n NaCL NADPH Nm NO NOS NOX - O 2 O 2 OH p Plt Katalase Leukozyten Malondialdehyd Millimol Mangan Millisekunden Zahl der Beobachtungen Kochsalz Nicotinamid Adenin- Dinucleotid- Phosphat Nanometer Stickstoffmonoxid NO-Synthase NADP(H)-Oxidase Superoxidanion-Radikal Sauerstoff Hydroxyl-Radikal (Irrtums-) Wahrscheinlichkeit Thrombozyten RDA Recommended daily allowance ( empfohlene Tagesdosis ) RNA RNS ROS RQ SD S/min SOD TAC TBA- Assay Ribonucleinsäure reaktive Stickstoffspezies reaktive Sauerstoffspezies Respiratorischer Quotient Standardabweichung Schläge pro Minute Superoxiddismutase total antioxidant capacity Thiobarbiturat- Assay
11 Abkürzungsverzeichnis TEAC TNFα trolox-equivalent antioxidant capacity Tumornekrosefaktor α VO 2 Flussvolumen Sauerstoff (V O 2 ) V O 2max Zn μmol maximale Sauerstoffaufnahme Zink Mikromol Mittelwert
12 Einleitung 1 Einleitung 1.1 Definition reaktiver Sauerstoffderivate Als Freie Radikale (RONS) werden Atome oder Moleküle bezeichnet, die ein oder mehrere ungepaarte Elektronen im äußeren Orbital aufweisen und infolgedessen eine ausgeprägte chemische Reaktivität besitzen [8;90]. Durch Oxidation anderer Moleküle versuchen sie ihre äußere Elektronenschale aufzufüllen. Man kann die Freien Radikale in reaktive Sauerstoff- (reactive oxygen species, ROS) oder Stickstoffverbindungen (reactive nitrogen species, RNS) unterteilen [90]. Nicht radikalische ROS (H 2 O 2, O 3, Singulett-Sauerstoff, und HOCL) können leicht in Radikale überführt werden [93]. Als Zwischenprodukte des Stoffwechsels entstehen ständig Freie Radikale bei physiologischen sowie pathophysiologischen Vorgängen in jeder Zelle unseres Körpers. Dies geschieht durch Reduktion von molekularem Sauerstoff zu Wasser [109]. Diese Reduktion kann in Ein- oder Zweielektronenschritten erfolgen, wobei die Reduktion des Sauerstoffs mit nur einem Elektron reaktive Sauerstoffspezies entstehen lässt. Sauerstoff ist ein universeller Elektronenakzeptor, der es ermöglicht Energie aus Kohlenhydraten, Fetten und Proteinen zu gewinnen [8]. Freie Radikale sind sehr kurzlebig (Halbwertszeit im Bereich von µs-ms) und haben eine hohe Diffusionsfähigkeit in Zellen und Geweben, jedoch mit einer geringen Halbwertstiefe (weniger als 1mm) [8]. Des Weiteren besitzen sie oxidative Eigenschaften und können in der Umgebung, in der sie gebildet werden, mit einer ganzen Reihe biologischer Substrate (Lipide, Proteine, Zucker, Nukleinsäuren, Extrazellulärmatrixbestandteile) reagieren und so deren biologische Eigenschaften ungünstig verändern [33]. Daraus kann sich eine Schädigung von Zellen und Extrazellulärmatrix ergeben, wodurch Freie Radikale für die Pathogenese von vielen Erkrankungen mitverantwortlich gemacht werden können [8;65;93]. Gleichung 1 zeigt die in vier Teilschritten ablaufende Reduktion von Sauerstoff zu Wasser. Hierbei entstehen Zwischenstufen, die als reaktive Sauerstoffderivate bezeichnet werden. Im Einzelnen sind dies das Superoxidanion-Radikal (O - 2 ), Wasserstoffperoxid (H 2 O 2 ) und das Hydroxyl-Radikal (OH ) [8;42;93]. 1
13 Einleitung O 2 H 2 O 2 OH H 2 O Gl. 1: Reduktion von Sauerstoff (O 2 ) zu Wasser (H 2 O) Die in den Zwischenschritten entstehenden Sauerstoffderivate werden im folgendem kurz vorgestellt: Superoxidanion-Radikal Das Superoxidanion-Radikal entsteht als erstes Zwischenprodukt durch einen reduktiven 1-Elektronen-Übergang bei der Reaktion von molekularem Sauerstoff zu Wasser (Gl. 2): O 2 O 2 - Gl. 2: Bildung eines Superoxidanion-Radikals (O 2 - ) Seine Bildung erfolgt vor allem als Nebenprodukt der mitochondrialen Atmungskette. Die Halbwertszeit ist ph- und lösungsmittelabhängig, wobei Superoxidanion-Radikale in saurer wässriger Umgebung spontan zu Wasserstoffperoxid und Sauerstoff dissoziieren [37]. Zellschädigend wirken vor allem Oxidationsreaktionen des Superoxidanion-Radikals mit anderen Substanzen wie Struktur- und Enzymproteinen, Reduktion der oxidierten Form des Cytochroms C sowie Oxidationen und Abbau von SH-Gruppen [93] Wasserstoffperoxid Das Superoxidanion wird mit Hilfe einer Superoxiddismutase (SOD), welche erstmalig von McCord und Fridovich (1969) beschrieben wurde, in das toxische Metabolit Wasserstoffperoxid (H 2 O 2 ) umgewandelt [87]. Die Superoxiddismutase liegt einmal als CuZn-SOD im Zytoplasma und einmal als Mn-SOD in den Mitochondrien vor [8]. - 2 O SOD 2 H 2 O g O 2 Gl. 3: Bildung von Wasserstoffperoxid (H 2 O 2 ), SOD- katalysiert 2
14 Einleitung H 2 O 2 ist kein Radikal, da es kein ungepaartes Elektron in der äußeren Schale enthält [42]. Eine besondere Gefahr birgt neben der substanzeigenen Toxizität des H 2 O 2 und die Fähigkeit Lipidmembranen zu passieren, die auf unterschiedlichen Wegen mögliche Bildung von Hydroxyl-Radikalen. Diese Bildung kann nur durch die direkte enzymatische Reaktion von Wasserstoffperoxid zu Wasser über die Katalase (CAT; vorwiegend in Peroxisomen) oder über die Gluathion-Peroxidase (GPX, in höheren Konzentrationen in Mitochondrien) verhindert werden (Gl. 4 u. 5) [64]. 2 H 2 O 2 CAT O H 2 O 2 H 2 O GSH GPX GSSG + 2H 2 O Gl. 4 und 5: Mögliche Reaktionswege zur Bildung von H 2 O Hydroxyl-Radikal Diese Zwischenstufe ist das bei weitem reaktivste und destruktivste Sauerstoffderivat. Es greift eine Vielzahl biologischer Strukturen an. Durch seine extrem kurze Halbwertszeit kann es nur da Schäden anrichten, wo es entsteht. Bisher ist kein wirksames Antioxidanz gegen das Hydroxyl-Radikal bekannt. Besonders gefährlich ist daher dessen Bildung in unmittelbarer Nähe von DNA- oder RNA-Molekülen, an denen es Einzel- und Doppelstrangbrüche, Basenverluste und mutationen bewirken kann. Besonders gerne reagiert es auch mit den mehrfach ungesättigten Fettsäuren der Lipidmembranen und diversen Enzymen [77;93]. Die Bildungsreaktionen von Hydroxyl-Radikalen (OH ) können sowohl mit Hilfe von Semiquinonen in der Mitochondrienmembran bei einer hohen Konzentration von H + - Ionen (Gl. 6), als auch mit Hilfe der Haber-Weiß und der Fenton-Reaktion im Cytosol erfolgen (Gl. 7) [65,93]. H 2 O 2 + SQ + H + Quinon + OH + H 2 O H 2 O 2 + Fe 2+ Fe 3+ + OH - + OH Gl. 6 und 7: Mögliche Reaktionswege zur Bildung von OH 3
15 Einleitung Organische Hydroperoxide Die bei der Lipidoxidation auftretenden Produkte werden als Hydroperoxide (ROOH) bezeichnet (Abb. 1). Diese Fettsäurederivate sind chemisch instabil und zerfallen in Aldehyde, wie zum Beispiel das Malondialdehyd. Dabei werden vor allem mehrfach ungesättigte Fettsäuren, wie Linolsäuren und Arachidonsäuren angegriffen, denn mit der Zahl der Doppelbindungen steigt auch die Oxidationsempfindlichkeit gegenüber Sauerstoff. Diese Säuren haben jedoch entscheidenden Einfluss auf die Fluidität und Integrität von Zellmembranen [71]. Abb. 1: Schema der Lipidperoxidation. I ist das die Radikalreaktion initiierende Radikal, LH ist eine weitere Fettsäure, die durch die Reaktion mit dem Peroxyl-Radikal selbst wieder zu einem Radikal (L ) wird, das die Kettenreaktion weiter antreibt [95] 4
16 Einleitung 1.2 Biochemische Mechanismen der Entstehung reaktiver Sauerstoffderivate Radikalbildung in den Mitochondrien Eine der wichtigsten Quellen für die Entstehung Freier Radikale während körperlicher Belastung stellt die mitochondriale Atmungskette dar, die vor allem über den Cytochromoxidase-Regulationsweg Freie Radikale produziert [30;63]. Unter normalen physiologischen Bedingungen entstehen 90 % der ROS während der in den Mitochondrien ablaufenden oxidativen Phosphorylierung. Zwei bis fünf Prozent des gesamten Sauerstoffs werden hier zum Superoxidradikal umgewandelt [4;8;42;118]. Dies legt nahe, dass unter körperlicher Belastung, die mit einer Steigerung der Sauerstoffaufnahme im Muskel um den Faktor und einem erhöhten Elektronenfluss einhergehen kann, auch verstärkt Superoxide gebildet werden [66]. Der Sauerstoffverbrauch des gesamten Körpers steigt um den Faktor 20 an [6]. Studien belegen, dass aerobe körperliche Belastung zu einer erhöhten Freisetzung von Superoxidradikalen aus Muskelzellen führen [63]. Durch direkte Messung mittels Elektronenspinresonanzspektroskopie konnte ein Anstieg Freier Radikale nach körperlicher Belastung gezeigt werden [6]. NADH-Ubichinon Reduktase (Komplex 1) und Ubichinon-Cytochrom C-Reduktase (Komplex 3) sind bekannt für die Bildung von O 2 und H 2 O 2 [66]. Besonders kritisch ist hierbei das Coenzym Q, das zur Produktion von Sauerstoffradikalen beiträgt. Ubichinon ist ein beweglicher Wasserstoffüberträger, der Wasserstoff unter anderem von Komplex 1 und Komplex 2 auf Komplex 3 überträgt. Dabei nimmt Ubichinon erst ein Elektron auf, wodurch es zum Semichinon-Radikal reduziert wird, um dann in einem zweiten Schritt vollständig zum Ubichinol reduziert zu werden. Das Semichinon ist lipophil und daher in der Membran sehr gut beweglich, wodurch der Kontakt zu Sauerstoffmolekülen schnell hergestellt werden kann. Es kommt zur Bildung von Sauerstoffradikalen [42;63;65]. Wie Gleichung 8 verdeutlicht, geschieht dies besonders günstig in saurer Umgebung, wie sie im anaeroben Stoffwechsel vorkommt [65]: H 2 O 2 + SQ + H + Quinon + OH + H 2 O Gl. 8: Möglicher Reaktionsweg zur Bildung von OH 5
17 Einleitung Des Weiteren wird die Aktivität der Cytochromoxidase, die den letzten Schritt, die Reduktion von molekularem Sauerstoff zu Wasser katalysiert, durch eine erhöhte H + - Konzentration gehemmt. Gleichzeitig nimmt jedoch die Elektronenflussrate aufgrund des erhöhten Energiebedarfs zu, wodurch sich Elektronen anstauen. Dies sind optimale Voraussetzungen für eine vorzeitige Reduktion des Sauerstoffs an der Mitochondrienmembran [53]. Doch haben die Mitochondrien auch sehr gut entwickelte Schutzmechanismen, die dem schädigenden Einfluss Freier Radikale entgegenwirken: Hierfür existiert eine spezifische mitochondriale Superoxiddismutase, die das Superoxid in Wasserstoffperoxid umwandelt. Da einige andere Studien keine erhöhte Radikalbildung in Mitochondrien nachweisen konnten, muss es auch extramitochondriale Entstehungsmechanismen Freier Radikalen geben [66;118]. Während körperlicher Belastung spielen dabei folgende Stoffwechselwege ebenfalls eine bedeutsame Rolle in der Generierung Freier Radikale: Xanthinoxidase Einige Untersuchungen stützen die These einer Analogie zwischen einer Gewebeschädigung während der Reperfusion nach einem Ischämiezustand und den Gewebsläsionen nach körperlicher Belastung [112]. Unter Ruhebedingungen katalysiert die Xanthindehydrogenase die Oxidation von Hypoxanthin über Xanthin zu Harnsäure [8]. Während des Zustands der Ischämie wird die Xanthindehydrogenase durch Aktivierung einer Calcium-abhängigen Protease zur Xanthinoxidase umgewandelt [10]. Wenn das Sauerstoffangebot zu gering ist, erfolgt die Regeneration von 1 ATP aus 2 ADP, katalysiert durch die Adenylatkinase. Bei intensiver körperlicher Belastung kommt es einerseits zu einem verstärkten Abbau des ATP zu AMP, andererseits zu einer gesteigerten Bildung von ATP aus 2 ADP, so dass vermehrt AMP anfällt. AMP wandelt sich nachfolgend zu IMP, Inosin und schließlich zu Hypoxanthin um (Abb. 2). - Hypoxanthin wird schließlich über die Xanthinoxidase zu Xanthin, Harnsäure und O 2 abgebaut [125]. 6
18 Einleitung Abb. 2: Regeneration von ATP aus ADP und Abbau von AMP Dabei nutzt die Xanthinoxidase molekularen Sauerstoff als Elektronenakzeptor. Als Nebenprodukt entsteht jedes Mal ein Superoxidradikal (Gl. 9). XOD Hypoxanthin + 2 H 2 O+ 2O 2 Xanthin+ Harnsäure+ 4H + + 4O 2 Gl. 9: Oxidation von Hypoxanthin zu Harnsäure, katalysiert durch Xanthinoxidase - Westing et al. (1989) fanden eine gesteigerte Adenylatkinaseaktivität unter körperlicher Belastung, so dass auch eine größere Menge an Hypoxanthin anfällt und somit eine gesteigerte Produktion an Sauerstoffradikalen gebildet durch die Xanthinoxidase vorliegt [121]. Ca ++ Abb. 3: Xanthinoxidasereaktion bei Ischämie und Reperfusion. ATP= Adenosintriphosphat, ADP= Adenosindiphosphat, 0 2 = Sauerstoff, 0-2 = Superoxid, Ca 2+ = Calcium, modifiziert nach [114] 7
19 Einleitung Um die Xanthindehydrogenase in Xanthinoxidase umwandeln zu können, müssen einige Bedingungen erfüllt sein: Xanthindehydrogenase/-oxidase müssen im Skelettmuskel vorhanden sein (vor allem in kapillären Endothelzellen des Muskels) Gesteigerte intrazelluläre Calciumkonzentration Ausreichende Menge an Hypoxanthin und Xanthin aus AMP verfügbar [54] Die Rolle der Entstehung von Sauerstoffradikalen durch die Xanthinoxidase wird zunehmend diskutiert, da der Skelettmuskel nur eine geringe Anzahl dieses Enzyms enthält [8;42]. Viňa et al. (2000) hingegen konnten zeigen, dass die Hemmung der Xanthinoxidase durch Allopurinol eine geringere Bildung von GSSG zur Folge hatte [118]. Darmtrakt und Niere des Menschen enthalten dagegen eine deutlich nachweisbare Xanthinoxidase-Aktivität. Diese Areale werden während körperlicher Belastung vermindert durchblutet, so dass sich hier eine hypoxische Situation ergibt. So ist es denkbar, dass nach Belastungsende eine Reperfusion mit verstärkter Radikalbildung erfolgt [42;52] Respiratory Burst und NADPH-Oxidase-Komplexe (NOX) Als weiterer wesentlicher Bildungsort reaktiver Sauerstoffderivate beim Sport werden Granulozyten und Makrophagen diskutiert [63]. Unter physiologischen Bedingungen bilden Granulozyten und Makrophagen Sauerstoffradikale, mit deren Hilfe sie Antigene abtöten (Gl. 10 und 11). 2 O 2 + NADPH NADPH Oxidase 2 O NADP + + H O H + H 2 O 2 + O 2 - Gl. 10 und 11: Bildung von O 2 und H 2 O 2 in neutrophilen Granulozyten Das Superoxidanion-Radikal kann durch SOD in Wasserstoffperoxid umgewandelt werden. Wasserstoffperoxid kann nun wiederum zu einem Hydroxyl-Radikal reagieren, oder über die Myeloperoxidase zur Hypochlorsäure reduziert werden, die eine hochreaktive Substanz zur Abtötung von Viren und Bakterien darstellt (Gl. 12): 8
20 Einleitung H 2 O 2 + Cl - + H + H 2 O + HOCl Gl.12: Bildung unterchloriger Säure Eine Verletzung von Muskelfasern infolge von mechanischer Belastung wie sie bei körperlicher Belastung vorkommt, führt zur Freisetzung von TNF-α, Interleukin-1 und Interleukin-6 und somit zur Einwanderung von Makrophagen und neutrophilen Granulozyten [6]. Diese produzieren im respiratory burst Superoxidradikale, Wasserstoffperoxid und Hypochlorsäure, die wiederum weitere Schäden am Muskel anrichten können und zur weiteren Einwanderung von Phagozyten führen. Der respiratory burst, induziert durch körperliche Aktivität, führt vor allem in der Nachbelastungsphase zu einer Freisetzung von Sauerstoffradikalen [30]. Neben der NADPH-Oxidase in Abwehrzellen, in denen sie im Rahmen des respiratory burst die Generierung von Superoxidanionen katalysiert, wurden vor mehr als zehn Jahren in vaskulären Zellen erstmals funktionelle NADPH-Oxidase- Komplexe nachgewiesen [46;67]. In den letzen Jahren wurden eine Reihe von Enzymen auf molekularer Ebene identifiziert, die für die Bildung von reaktiven Sauerstoffspezies in verschiedenen Geweben verantwortlich sind. Diese Enzyme zeigen einen hohen Grad an Homologie zur gp91 phox -Untereinheit der klassischen NAD(P)H-Oxidase in phagozytierenden Zellen [72]. Daraufhin wurde eine einheitliche Nomenklatur eingeführt, wonach die Isoformen NOX 1-NOX 5, DUOX 1 und DUOX 2 zu unterscheiden sind. Alle diese Isoformen zeigen strukturelle Ähnlichkeiten auf, doch finden sich signifikante Unterschiede hinsichtlich Gewebeverteilung, Kofaktoren, Aktivierungsmodi, Menge der Superoxidproduktion und Funktion [26]. Tab. 1 zeigt das Vorkommen der einzelnen Formen in den unterschiedlichen Geweben an [74]. 9
21 Einleitung Tab. 1: Vorkommen und Funktion der einzelnen NOX Isoform Vorkommen Funktion NOX 1 Kolon, Niere, Muskelzelle, Uterus Blutdruckregulation, Immunabwehr NOX 2 Phagozyten Immunabwehr NOX 3 NOX 4 Innenohr, fetales Gewebe Niere, Endothel, Osteoklasten, Skelettmuskulatur Regulation EPO, Sauerstoffsensor, Vasoregulation NOX 5 Lymphknoten, Milz, Testis Spermatogenese, Lymphozytenregulierung DUOX ½ Schilddrüse, Lunge, Gastrointestinaltrakt Thyroid-Hormonsynthese Die NADPH-Oxidase ist als einzige Enzymfamilie bekannt, deren alleinige Aufgabe es ist Freie Radikale zu generieren. Andere Enzyme, die bei der Bildung von ROS eine Rolle spielen haben primär biochemisch andere Funktionen und bilden die Freien Radikale nur als Nebenprodukt [124]. Für uns relevant ist dabei vor allem der intrazelluläre NOX 4-haltige NADPH- Oxidase-Komplex, der für die Radikalbildung in Endothelzellen vorwiegend verantwortlich ist. Sowohl NOX 1 als auch NOX 4 werden durch Angiotensin II induziert [1]. Die gebildeten Radikale inaktivieren Stickstoffmonoxid (nitric oxide, NO) in einer direkten Reaktion, schädigen das NO-bildende Enzym NOS (NO-Synthase) in Endothelzellen und schädigen den NO-Rezeptor. Stickstoffmonoxid vermittelt jedoch gefäßschützende Effekte: Es führt zur Vasodilatation, hemmt die Thrombozytenaggregation sowie das Wachstum glatter Muskelzellen. Des Weiteren sind die gebildeten Freien Radikale in der Lage die Xanthinoxidase hoch zu regulieren und die endotheliale NO-Synthase (enos) zu entkoppeln, was wiederum zu einer erhöhten Radikalproduktion führt [124]. Somit spielt NOX-4 im Gefäßsystem eine wesentliche Rolle bei der Entstehung der endothelialen Dysfunktion und den damit einhergehenden Herz-Kreislauf-Erkrankungen [74]. Aber auch bei körperlicher Aktivität kommt der Freisetzung von NO durch eine Scherkraft- oder Rezeptorabhängigen Aktivierung der enos zur Verbesserung der Durchblutung eine zentrale Bedeutung zu. Wird dieser Mechanismus durch die Freien Radikale gestört, kann die 10
22 Einleitung notwendige Gefäßanpassung nicht erfolgen und somit die erhöhte Sauerstoffversorgung nicht gewährleistet werden [19] Weitere Entstehungsmechanismen von Sauerstoffradikalen Peroxisomen Peroxisomen sind an dem oxidativem Abbau von Fettsäuren sowie D-Aminosäuren beteiligt, wobei als Nebenprodukt H 2 O 2 entsteht. Da bei längerer körperlicher Betätigung vor allem Fettsäuren als Energielieferant für Herz- und Skelettmuskel dienen, könnte dieser Weg eine bedeutende Rolle bei der ROS-Produktion spielen. Jedoch fehlen hierzu noch Studien [66]. Katecholamine Diese werden bei körperlicher Belastung vermehrt ausgeschüttet und können über eine Autoxidation von Epinephrin zu Adrenochrom oder eine Metallionen-katalysierte Oxidation zur Freien Radikalbildung führen [63;111]. Prostaglandinmetabolismus Während des Umbaus von Arachidonsäure zu Prostaglandinen entstehen als Zwischenstufen Freie Radikale. Da es im Skelettmuskel keine Lipoxygenase gibt, spielt hier vor allem der Umbau über die Cyclooxygenase eine Rolle. Allerdings ist die Bedeutung der Entstehung von Freien Radikalen während körperlicher Belastung über oben genannten Mechanismus noch nicht genau geklärt [63]. Cytochrom P 450 Des Weiteren entstehen ROS auch im Fremdstoffmetabolismus über das Cytochrom P 450-System [63]. Laktatmetabolismus Eine vermehrte Produktion von Laktat, das die reaktionsträgeren Superoxide in die gefährlicheren Hydroxyl-Radikale umwandeln kann, kann ebenfalls zur Bildung von oxidativem Stress beitragen. [29;42]. 11
23 Einleitung Mechanische Hämolyse- Fentonreaktion Die Bildung der aggressiven Hydroxyl-Radikale aus Wasserstoffperoxid wird in Anwesenheit von Eisenionen im Rahmen der Fentonreaktion stark beschleunigt (Gl. 13) [63]. H 2 O 2 + Fe 2+ Fe 3+ + OH + OH Gl.13: Fenton- Reaktion - Man kann davon ausgehen, dass für diese Reaktion nur Hämoglobin oder Hämoglobinabbauprodukte zur Verfügung stehen, nicht aber an Transferrin gebundenes Eisen. Daraus kann man schließen, dass auch eine mechanische Hämolyse, wie sie bei Laufbelastung auftritt, zum oxidativen Stress beiträgt [63]. Fenton-ähnliche Reaktionen können auch unter Beteiligung anderer niedervalenter Metallkomplexe wie Cu(II), Ti(III), Cr(II) oder Co(II) stattfinden. Die Fenton-Reaktion wird als eine der wesentlichen Quellen der Generierung reaktiver Sauerstoffspezies in der Zelle angesehen [93]. Autoxidation von Oxyhämoglobin und Oxymyoglobin 3 % des Gesamthämoglobins werden autooxidiert, bei körperlicher Arbeit steigt der Prozentsatz an. Es werden Methämoglobin und 0 2 gebildet. Myoglobin kann ebenfalls autooxidiert werden. Interaktionen von H 2 O 2 mit Myoglobin können andere Radikale wie Eisen- und Peroxylradikale bilden [29;42]. Cyclooxygenase, Lipooxygenase, Stickstoffmonoxidsynthase Als letztes wären noch die Enzyme Cyclooxygenase, Lipooxygenase und Stickstoffmonoxidsynthase zu erwähnen, die zur Generierung von Freien Radikalen beitragen [63;90]. Exogene Quellen An dieser Stelle sollte auch erwähnt werden, dass es eine relativ große Anzahl exogener Quellen für ROS gibt: photochemischer Smog, Stickoxide, Ozon, 12
24 Einleitung Elektrosmog, toxische Schwermetalle, diverse Umweltchemikalien, halogenierte Kohlenwasserstoffe, organische Lösungsmittel, Teerabkömmlinge, Kunststoffe, Xenobiotika im weitesten Sinne, UV-Strahlung und ionisierende Strahlen und künstliche radioaktive Nuklide [93]. Freie Radikale Antioxidative Abwehr Abb. 4: Die wichtigsten Freien Radikale und ihre Gegenspieler. Bei einem Überwiegen der Freien Radikale kommt es zu Gewebeschäden bis hin zum Zelltod 1.3 Oxidativer Stress und Auswirkungen auf den Körper Bildung und Beseitigung der ROS bilden in gesunden Zellen ein Gleichgewicht. Erst wenn vermehrt Freie Radikale gebildet werden oder deren Entfernung nicht mehr funktioniert, spricht man von oxidativem Stress [48]. Reaktive Sauerstoffderivate können in gesunden Zellen Apoptose induzieren, Entzündungsreaktionen hervorrufen oder die zellulären Funktionen verändern. Es ist bekannt, dass oxidativer Stress zu Zellschädigungen führen kann und mit der Pathogenese verschiedener Erkrankungen in Zusammenhang gebracht wird: Katarakt, Herzkreislauferkrankungen, Lungenerkrankungen, Artherosklerose, Diabetes, Tumorentstehung, Osteoporose, erektile Dysfunktion, Alzheimer und Parkinson sind nur einige Beispiele von Erkrankungen, die direkt oder indirekt mit der 13
25 Einleitung Wirkung von Freien Radikalen in Verbindung gebracht werden. Des Weiteren spielen Freie Radikale neben den Genen und der neuroendokrinen Theorie- Hormonrezeptoren werden im Laufe der Zeit desensibilisiert- eine erhebliche Rolle im Alterungsprozess. So besagt die Freie Radikalentheorie des Alterns, dass eine inverse Korrelation zwischen der Menge an produzierten Freien Radikalen und der Lebensdauer bestehe. Freie Radikale können fast alle Biomoleküle wie DNA, Lipide, Proteine und Zucker schädigen. Können diese Schäden durch spezifische Reparaturmechanismen nicht beseitigt werden, akkumulieren sie über die Lebenszeit und führen zu zellulären Schäden mit Dysfunktion und Zelltod [50]. Eine entscheidende Rolle spielen im Zusammenhang mit dem Alterungsprozess die Freien Radikale auch bei der Faltenbildung Lipidperoxidation Die Reduktion von Seitenketten mehrfach ungesättigter Fettsäuren durch Freie Radikale stellt die Startreaktion der Lipidperoxidation dar. Die Lipidperoxidation findet in Zellmembranen statt, was zu einer reduzierten Fluidität der Zellmembran, der Unfähigkeit Ionengradienten aufrecht zu erhalten, einer Zellschwellung und Gewebsentzündung führt [5;6:42]. Die Zellmembranen können undicht werden, wodurch intrazelluläre Enzyme verloren gehen. Die bei der Lipidperoxidation entstehenden oxidierten Membranfragmente werden als Hydroperoxide bezeichnet. Hydroperoxide kommen in verschiedenen Verbindungen vor, deren wichtigster Vertreter das Malondialdehyd (MDA) ist [32]. Lipidperoxide können von ihrer Bildungsstätte wegdiffundieren und an einer anderen Stelle in der Zellmembran Schäden anrichten. MDA wird häufig als Indikator für das Ausmaß an oxidativen Stress im Körper gewertet. Allerdings kann MDA auch aus dem Arachidonsäure- Stoffwechsel durch Cyclooxygenase gebildet werden [5] Proteinmodifikation Des Weiteren können Proteine durch Oxidation der Seitenketten der Aminosäuren oder intra- und intermolekularer Vernetzung der Aminosäureketten modifiziert werden, was zu einer Strukturänderung und somit unter anderem zu einer Störung der Enzymfunktionen führen kann. 14
26 Einleitung Die Enzymfunktionen können allerdings auch durch die Lipidperoxidation verändert werden: Zum Beispiel werden die Succinat-Dehydrogenase und N-Hydroxybutyrat- Dehydrogenase dadurch inaktiviert, dass Phospholipide in ihrer Umgebung entfernt werden [11] DNA-Modifikation Auch sind ROS, insbesondere Hydroxyl-Radikale, dafür bekannt Einzel- und Doppelstrangbrüche in DNA und RNA vorzunehmen [8]. Oxidation der Desoxyribose und Hydroxylierung der Basen können zu Basenfehlpaarungen und DNA- Strangbrüchen führen, was entscheidend zur Tumorentstehung und Zellalterung beiträgt Physiologische Reaktionen von ROS Doch haben ROS nicht nur schädigende Wirkungen auf den Organismus. So sind Freie Radikale zum Beispiel an der Synthese mancher Hormone beteiligt, während Leukozyten und Makrophagen im Rahmen des respiratory burst die Produktion von Freien Radikalen nutzen, um Bakterien und Viren zu töten. Andere Freie Radikale, wie Stickstoffmonoxid (NO), sind fundamental für die Homöostase des Körpers und modulieren wichtige Funktionen einschließlich des Gefäßtonus, der Thrombozyten- Aggregation und der Zelladhäsion. Eine moderate Zunahme des myozellulären ROS-Gehaltes führt zu einer Optimierung der Kontraktilität des Muskels [90]. Ein übermäßiger Anstieg Freier Radikale ist allerdings mit Muskelermüdung und Muskelschädigung verbunden [9;34]. Des Weiteren rückte in den letzten Jahren auch ihre Rolle als Signal- und Modulatormolekül sowie ihre Funktion in der Transkriptionsregulation in den Vordergrund [90]. 15
27 Einleitung Abb. 5: Entstehung, Entgiftung und Folgen von oxidativem Stress. Endogene und exogene Faktoren führen zur Bildung von hoch reaktiven Superoxidanionen; nach [36] 1.4 Antioxidative Schutzmechanismen Das antioxidative System, welches zum Schutz des Körpers vor oxidativen Stress angelegt wurde, besteht aus einem enzymatischen und einem nicht-enzymatischen System Enzymatische Antioxidantien Superoxiddismutase (SOD) Dieses Enzym stellt die primäre Abwehr gegenüber O 2 dar [42]. Die Superoxiddismutase wandelt das Superoxidanion in Wasserstoffperoxid (H 2 O 2 ) um (Gl. 14). Dieses Enzym benötigt als Kofaktor Kupfer und Zink (SOD im Zytosol der Eukaryoten) oder Mangan (SOD in Mitochondrien der Eukaryoten) [110]. 2 O H + SOD H 2 O 2 + O 2 Gl. 14: Bildung von Wasserstoffperoxid 16
28 Einleitung Katalase Dieses Enzym (CAT) zeigt die höchste Aktivität in Peroxisomen, kommt aber auch in Mitochondrien und Zytosol aller Zellen vor und benötigt als Kofaktor Eisen. Durch dieses Enzym wird das toxische Wasserstoffperoxid zu Wasser und Sauerstoff abgebaut (Gl. 15) [42]. 2 H 2 O 2 CAT 2H 2 O + O 2 Gl. 15: Entgiftung von Wasserstoffperoxid Glutathion-Peroxidase Wie oben bereits beschrieben kann Wasserstoffperoxid selbst zelltoxisch wirken, eine besonders große Gefahr stellt aber auch dessen Umwandlung in das außerordentlich reaktive Hydroxyl-Radikal dar. Um diese Reaktionen zu verhindern, existiert die Glutathion-Peroxidase (GPX). Die GPX kommt sowohl im Zytosol als auch in den Mitochondrien der Zellen vor. Um enzymatisch arbeiten zu können, braucht es als Kofaktor Selen. Die GPX wandelt GSH (reduziertes Glutathion) zu GSSG (oxidiertes Glutathion) unter Verbrauch von H 2 O 2 um (Gl. 16). Dadurch wird das Wasserstoffperoxid zu Wasser neutralisiert [42]. H 2 O GSH GPX H 2 O+ GSSG Gl. 16: Entgiftung von Wasserstoffperoxid Reduziertes Glutathion dient hierbei als Elektronendonator und wird dabei in seine oxidierte Form (GSSG) überführt. Glutathion-Reduktase Dieses Enzym ist dafür zuständig in einem Recyclingprozess einen hohen Spiegel von reduziertem Glutathion aufrecht zu erhalten. Mittels NADPH kann die Glutathion- Reduktase die Disulfidbrücke des oxidierten Glutathions (GSSG) wieder zu Schwefelwasserstoff (HS-Gruppen) reduzieren (Gl. 17). 17
29 Einleitung GSSG + NADPH + H + Glutathion Reduktase 2GSH + NADP Gl. 17: Umwandlung von oxidiertem zu reduziertem Glutathion + Die Glutathion-Reduktase arbeitet flavinabhängig und schützt den Körper durch die Produktion von GSH indirekt vor reaktiven Substanzen [93] Nicht-enzymatische Antioxidantien Glutathionsystem Glutathion ist ein cysteinhaltiges Tripeptid (Glycin, Cystein, Glutaminsäure), das in jeder Zelle unseres Körpers vorkommt. Dadurch, dass die Aminosäure Cystein eine Thiolgruppe aufweist, kann Glutathion mit einem weiteren Molekül unter Abgabe von zwei Wasserstoffatomen eine Disulfidbrücke eingehen und Glutathiondisulfid bilden. Dabei präsentiert Glutathiondisulfid den oxidierten Zustand des Glutathions. Die Konzentration von Glutathion im Gewebe kann als Anhalt für das Gleichgewicht von GSH zu GSSG genommen werden. Normalerweise ist die Glutathionkonzentration im Erythrozyten viel höher als die Glutathiondisulfidkonzentration. Neben den oben genannten Reaktionen kann Glutathion oxidiertes α-tocopherol wieder reduzieren. Auch kann es zur Entgiftung von Xenobiotika oder als direkter Radikalfänger dienen [65;66]. Vitamine Besonders die Vitamine A, C und E sowie ß- Karotin gelten als Radikalfänger [27;65]. Vitamin E (ArOH) ist fettlöslich und von den acht natürlich vorkommenden Vitamin E- Derivaten ist α-tocopherol als sein wichtigster Vertreter das stärkste Antioxidanz in Zellmembranen. Vitamin E ist aufgrund seiner Beziehung zur Zellmembran als das wichtigste Antioxidanz überhaupt im biologischen System mit der bedeutendsten Eigenschaft Freie Radikale zu neutralisieren anzusehen [14;38]. Es schützt vor Lipidperoxidation durch direkte Reaktion mit einigen Radikalen, wie den 18
30 Einleitung Superoxidradikalen und Peroxylradikalen. Außerhalb der Zellmembran neutralisiert es Singulett-Sauerstoff über die Bildung verschiedener Oxidationsprodukte. Dabei wird ein relativ reaktionsträges Tocopherol-Radikal gebildet [39]. Die antioxidativen Eigenschaften des Vitamin E hängen mit seinem chemischen Aufbau zusammen: Das fettlösliche Ende ist in der Zellmembran verankert, der Chromanolring ist für das antioxidative Wirkungspotential verantwortlich und ist der Membranaußenseite zugewandt. Vitamin E ist essentiell für die Erhaltung der Funktion der Zelle während körperlicher Belastung. Ratten mit Vitamin E-Mangel zeigten eine deutlich höhere Produktion an Freien Radikalen in Leber- und Muskelgewebe und eine gesteigerte Lipidperoxidation sowie mitochondriale Dysfunktion nach erschöpfender Belastung verglichen mit Ratten, die einen normalen Vitamin E-Spiegel aufwiesen [30]. β-carotin (Provitamin A) Der lipophile Vorläufer vom Vitamin A ist ein hervorragendes Molekül zur Abwehr von Singulett-Sauerstoff (Gl.18 u. 19): O 2 + ß-Karotin O 2 + ß-Karotin ß-Karotin ß-Karotin + Wärme Gl. 18 u. 19: Abwehr von Singulett-Sauerstoff durch ß-Karotin Des Weiteren reagiert es auch mit Alkoxyl- und Peroxylradikalen. Das dabei entstehende stabile und reaktionsträge ß-Karotin-Radikal besitzt noch antioxidative Funktionen [93]. Vitamin C ist hydrophil und gilt als einer der effektivsten Radikalfänger im Plasma. Es entschärft toxische Formen des Sauerstoffs, Superoxidanionen, Singulett- Sauerstoffe und Hydroxyl-Radikale [42]. Des Weiteren dient es zur Regeneration von α-tocopherol und Glutathion in ihre reduzierte, aktive Form (Abb. 6). Vitamin C wird dabei durch Enzyme (Semidehydroascorbatreduktase und Dehydroascorbatreduktase) wieder in seine reduzierte Form überführt. Darüber hinaus spielt Vitamin C als Kofaktor für mehrere enzymatische Reaktionen eine große Rolle [98]. Da Vitamin C in zu hohen Dosen verabreicht gastrointestinale Beschwerden auslösen kann sowie eine erhöhte Wahrscheinlichkeit für die Entstehung von Nierensteinen, Thrombozytosen und eine herabgesetzte 19
31 Einleitung Koagulationszeit besteht, sollte es nicht überdosiert werden. Ebenfalls wurde in einer Studie gezeigt, dass Vitamin C in Anwesenheit von Eisen prooxdierend wirken kann [57;58]. Des Weiteren spielt Vitamin C eine Rolle bei der Synthese von Kollagen, Hormonen und Neurotransmittern. Kupfer und Zink sind essentiell für die zytosolische Superoxiddismutase, wohingegen die mitochondriale Superoxiddismutase nicht ohne Mangan funktioniert. Eisen ist ein wichtiger Bestandteil der Katalase und Selenium von der Glutathionperoxidase, was in Tab. 2 noch einmal dargestellt wird. Alle diese Mineralien können bei körperlicher Belastung abnehmen. Tab. 2: Notwendige Kofaktoren für die einzelnen antioxidativ wirkenden Enzyme Cytosolische Superoxiddismutase Kupfer, Zink Mitochondriale Superoxiddismutase Glutathionperoxidase Katalase Mangan Selenium Eisen Weitere wasserlösliche Antioxidantien sind Harnsäure, Cystin, Glutathion, Melatonin, Ubiquinon, Bilirubin, Flavonoide und Polyphenole und Carotenoide. Vitamin E, ß- Karotin und Ubiquinon sind lipidlöslich, wobei Harnsäure, GSH und Bilirubin hydrophil sind [65;98]. Harnsäure ist ein Endprodukt des Purinmetabolismus, so dass durch körperliche Belastung einhergehend mit einem gesteigerten Abbau von ATP, die Konzentration von Harnsäure im Plasma ansteigt. Harnsäure diffundiert dann in Muskelgewebe um dieses vor den Angriffen Freier Radikale zu bewahren [55]. Des Weiteren hat Harnsäure auch direkte Effekte auf Singulett-Sauerstoff, HOCL, Peroxylradikale, Peroxynitrit und Ozon und hilft Erythrozyten, Zellmembranen, Hyaluronsäure und DNA sich vor Oxidationen durch Freie Radikale zu schützen. Einige Studien konnten nachweisen, dass Harnsäure einen großen Anteil ( 50%) der plasmatischen antioxidativen Kapazität ausmacht [120]. In vivo kann man Allantoin, Produkt der Oxidation von Harnsäure, messen [56]. 20
32 Einleitung Abb. 6: Wechselwirkung zwischen ausgewählten Parametern des antioxidativen Systems nach Vafa 2007 [116] 1.5 Auswirkungen körperlicher Belastung auf die antioxidativen Enzyme Durch körperliche Belastung wird nicht nur oxidativer Stress generiert, sondern das antioxidative System kann sich durch regelmäßiges Training der erhöhten Radikalbelastung anpassen [98]. In tierexperimentellen Modellen konnte gezeigt werden, dass Ausdauertraining zu einer Aktivitätssteigerung von antioxidativen Enzymen wie der Glutathionperoxidase und der Superoxiddismutase sowie dem Gehalt von antioxidativem Glutathion führt [78;96;97;98]. Die trainingsinduzierte Anpassung beschränkt sich jedoch nicht alleine auf eine Zunahme der Aktivität antioxidativer Enzyme, vielmehr kann Training auch zu einer erhöhten Expression dieser Enzyme führen, so wie etwa für die Superoxiddismutase-1, die Glutathionperoxidase und die Katalase gezeigt wurde [15;123]. Der trainingsinduzierte Anstieg der Superoxiddismutase ist dabei abhängig von der täglichen Trainingsdauer und Intensität, wobei die Aktivitätszunahme bei langer Trainingsdauer mit hoher Intensität am ausgeprägtesten ist [96;98]. Oh-Ishi et al konnten in einer Tierstudie zeigen, dass durch Ausdauertraining sowohl die MnSOD als auch die CuZnSOD im Diaphragma der Ratten anstiegen [92]. Die Literatur bezüglich des Anstiegs der Aktivität der Glutathionperoxidase (GPX) ist weitgehend einheitlich: Hierbei hat lang anhaltende körperliche Aktivität einen 21
33 Einleitung größeren Effekt auf die Aktivitätszunahme der GPX als kurz dauerndes Training [96;98]. Die Hochregulation der GPX-Aktivität ist dabei vor allem in den oxidativen Fasertypen zu erkennen (Typ 1 und 2a Fasern). Des Weiteren konnte gezeigt werden, dass sowohl die cytosolische als auch die mitochondriale GPX-Aktivität ansteigt, mit vermehrter Zunahme der mitochondrialen GPX- Aktivität [98]. Der Glutathiongehalt des Muskels erhöht sich ebenfalls durch Ausdauertraining [98]. Es gibt nur wenige Studien, die sich mit dem Einfluss von Ausdauertraining auf nichtenzymatische Antioxidantien beschäftigt haben. Hierbei wurde vor allem die Veränderung des Gewebegehaltes von Vitamin E betrachtet. Die Ergebnisse hierzu sind uneinheitlich: So konnte in einigen Studien eine Abnahme des Vitamin E-Levels unter Belastung nachgewiesen werden, wohingegen andere Studien keine Veränderungen erkennen konnten [98]. 1.6 Fragestellungen Hinsichtlich der pathophysiologischen Wirkungen ist das medizinische Interesse an den Entstehungs- und Regelmechanismen von Freien Radikalen sowie des oxidativen Stresses und dessen negativen Auswirkungen dementsprechend groß. Im Detail lauten die Fragestellungen der folgenden Untersuchung wie folgt: Welche Auswirkung hat eine akute maximal erschöpfende Belastung auf das antioxidative System und den oxidativen Stress bei Hochleistungssportlern? Welchen Einfluss hat die zusätzliche Einnahme von Nahrungsergänzungsmitteln (frubiase SPORT Ausdauer vs. Injektion bestehend aus Vitamin B12, Folsäure und Vitamin C) auf die Bildung Freier Radikale und auf das antioxidative System? Welchen Einfluss hat die Gabe der Nahrungsergänzungsmittel auf die körperliche Leistungsfähigkeit? 22
34 Methodik 2 Methodik In zwei Untersuchungsreihen mit jeweils 10 Leistungssportlern wurde der Einfluss von Nahrungsergänzungsmitteln auf die Bildung Freier Sauerstoffradikale, das biologisch antioxidative Potenzial und die leistungsdiagnostischen Parameter unter einer maximal erschöpfenden Laufbandbelastung überprüft. In der ersten Untersuchungsreihe Injektion absolvierten die Probanden zunächst eine Laufbandergometrie, erhielten in der darauffolgenden Woche drei Injektionen mit jeweils 48 Stunden Pause und wiederholten nach fünf Tagen die Laufbandbelastung nach dem gleichen Belastungsprotokoll. In der zweiten Untersuchungsreihe absolvierten die Probanden zu Beginn ebenfalls eine Laufbandergometrie, nahmen dann über einen Zeitraum von 35 Tagen das Nahrungsergänzungsmittel frubiase SPORT Ausdauer ( Frubiase ) ein und wiederholten nach Beendigung der Einnahme die Laufbandbelastung mit der gleichen Belastungsintensität. Beide Untersuchungsreihen fanden in der Vorwettkampfphase der Sportler statt. Die Laufbandbelastungen wurden routinemäßig im Rahmen der Untersuchungen des Olympiastützpunkts durchgeführt. 2.1 Probandenkollektiv Die Untersuchungsreihe Injektion wurde an 10 männlichen, gesunden Probanden im Alter von Jahren mit einer durchschnittlichen Körpergröße von 185,8 cm und einem durchschnittlichen Körpergewicht von 76,1 kg durchgeführt. Die Untersuchungsreihe Frubiase wurde ebenfalls an 10 männlichen, gesunden Probanden im Alter von Jahren mit einer durchschnittlichen Körpergröße von 184,9 cm und einem mittleren Körpergewicht von 78,5 kg durchgeführt. Alle Probanden betrieben Leistungssport Leichtathletik mit durchschnittlich Trainingsstunden pro Woche, wobei die Hauptdisziplinen bei den Probanden der ersten Untersuchungsreihe zwischen Sprint- (100 m und 200 m) und Mittelstrecke (400 m/800 m/1500 m) variierten. Sämtliche Probanden der Untersuchungsreihe Frubiase hatten als Hauptdisziplin eine Sprintstrecke und gehörten der gleichen 23
35 Methodik Trainingsgruppe an. Des Weiteren waren alle Teilnehmer Nichtraucher. Die anthropometrischen Daten der Probanden sind in Tab. 3 und Tab. 4 dargestellt. Die Anamnese vor Beginn der Studie ergab, dass alle Probanden gesund und nicht unter Einfluss von Medikamenten und Nahrungsergänzungsmittel standen. Des Weiteren waren sie zum Zeitpunkt aller Untersuchungen bezüglich ihrer Ernährung und ihrer Gesundheit unauffällig und ohne wesentliche körperliche Vorbelastung. Die Probanden wurden vor Beginn der Studie über Zweck, Ablauf und Risiken der Untersuchung informiert. Zudem wurden sie dazu aufgefordert, die Ernährungsvorgaben einzuhalten, am Vortag keinen Alkohol zu trinken und keine zusätzlichen Nahrungsergänzungsmittel einzunehmen. Tab. 3: Anthropometrische Daten (Alter, Größe, Gewicht, BMI) und Hauptdisziplin der Versuchspersonen der Untersuchungsreihe Injektion, Einzel- und Mittelwerte ( ), Standardabweichungen (SD) der Gesamtgruppe (n=10) Proband Alter Größe Gewicht BMI Disziplin (Jahre) (cm) (kg) (kg/m²) A Sprint B ,5 24,1 Sprint C ,7 23,5 Sprint D ,7 Sprint E ,6 Sprint F ,5 22,6 Mittelstrecke G ,9 Mittelstrecke H ,6 19,5 Mittelstrecke I ,6 21,1 Mittelstrecke J ,5 22,1 Mittelstrecke 22,9 185,8 76,14 22,01 SD 2,28 6,66 9,70 1,90 24
36 Methodik Tab. 4: Anthropometrische Daten (Alter, Größe, Gewicht, BMI) und Hauptdisziplin der Versuchspersonen der Untersuchungsreihe Frubiase, Einzel- und Mittelwerte ( ), Standardabweichungen (SD) der Gesamtgruppe (n=10) Proband Alter Größe Gewicht BMI Disziplin (Jahre) (cm) (kg) (kg/m²) ,2 21,9 Sprint ,7 Sprint ,7 Sprint ,6 Sprint ,5 23,9 Sprint ,2 Sprint ,8 Sprint ,5 23,1 Sprint ,5 20,5 Sprint Sprint ,9 78,47 22,94 SD 4,00 4,63 6,15 1, Untersuchungsgang Sämtliche Tests fanden im Institut für Kreislaufforschung und Sportmedizin der Deutschen Sporthochschule Köln statt. Die Studie wurde in zwei Untersuchungsreihen unterteilt und lief wie folgt ab: Jeweils zu Beginn und zum Abschluss einer Untersuchungsreihe unterzogen sich alle Probanden einem Laufbandstufentest, wobei vor jeder Belastung venöse Blutabnahmen im Sitzen aus der Vena cubitalis zur Bestimmung des großen Blutbildes erfolgten. Des Weiteren wurde Kapillarblut aus dem Ohrläppchen zur Bestimmung des biologisch antioxidativen Potenzials (BAP) und oxidativen Stresses (drom) sowohl vor als auch unmittelbar nach körperlicher Belastung entnommen. Die Belastung wurde als Spiroergometrie auf dem Laufband nach folgendem Belastungsprotokoll bis zur maximalen Belastungsgrenze durchgeführt: 25
37 Methodik Beginn der Belastung Stufenerhöhung Stufendauer Pausendauer maximal 2,5 m/s (3m/s) 0,5 m/s 5 Minuten 30 Sekunden Während der Belastungstests wurden zudem spirometrische Daten und die Laktatleistungskurve ermittelt. Untersuchungsreihe: Injektion (Vitamin C, Folsäure, Vitamin B12) Nach der Eingangsuntersuchung inklusive venöser Blutabnahme und Laufbandstufentest erhielten alle Probanden drei Injektionen (jeweils bestehend aus Vitamin C, Folsäure, Vitamin B12) über eine Woche verteilt (Montag, Mittwoch, Freitag). Nach Verabreichung der letzten Injektion unterzogen sich die Probanden erneut einer Spiroergometrie auf dem Laufband mit maximaler Ausbelastung und Bestimmung der Stressparameter sowohl vor, als auch unmittelbar nach Belastung. Dabei lag der zeitliche Abstand zwischen Verabreichung der letzten Injektion und Beginn der Laufbandbelastung bei circa Minuten. Abb. 7 stellt den Untersuchungsablauf noch einmal schematisch dar. Woche A Laufbandstufentest Parameter: großes Blutbild, BAP, drom, HF, Laktat, VO 2, RQ Woche B Tag 1, 3, 5: Verabreichung der Injektionen, bestehend aus Vitamin C, Folsäure, Vitamin B12 Woche B, Tag 5 Laufbandstufentest Parameter: großes Blutbild, BAP, drom, HF, Laktat, VO 2, RQ Abb. 7: Schematische Darstellung des Versuchsablaufs der Untersuchungsreihe Injektion 26
38 Methodik Untersuchungsreihe: frubiase SPORT Ausdauer Bei der zweiten Untersuchungsreihe gingen wir nach dem gleichen Schema vor. Hier betrug die Studiendauer jedoch fünf Wochen. Nach einer Eingangsuntersuchung mit venöser Blutabnahme wurden die Probanden auf dem Laufband nach obenstehendem Schema ausbelastet. Daraufhin erhielten alle Teilnehmer das Produkt frubiase SPORT Ausdauer und wurden dazu angehalten dieses täglich (40 g frubiase SPORT Ausdauer in pulverform, aufgelöst in 500 ml Wasser) einzunehmen. Nach 35 Tagen unterzogen sich die Probanden erneut einer Spiroergometrie auf dem Laufband mit Bestimmung der Stressparameter sowohl vor, als auch unmittelbar nach Belastung. Abb. 8 stellt den Untersuchungsablauf noch einmal schematisch dar. Tag 1 Laufbandstufentest Parameter: großes Blutbild, BAP, drom, HF, Laktat, VO 2, RQ Tag 2-36 Einnahme von 40 mg frubiase SPORT Ausdauer täglich Tag 37 Laufbandstufentest Parameter: großes Blutbild, BAP, drom, HF, Laktat, VO 2, RQ Abb. 8: Schematische Darstellung des Versuchsablaufs der Untersuchungsreihe Frubiase 2.3 Laborbestimmungen Blutlaktat Für die Blutlaktatbestimmung wurden mit geeichten Na + -Heparin- Glaskapillarpipetten der Firma Hirschmann Laborgeräte 20 µl arterialisiertes Kapillarblut aus dem Ohrläppchen abgenommen und in ein mit 0,2 ml 0,6 N- Perchlorsäure gefülltes Eppendorf Reaktionsgefäß (EKF-diagnostic GmbH, Barleben/ Marburg) gegeben und vermischt. Die Perchlorsäure bewirkte die Enteiweißung des Blutes. Nach der Laufbandergometrie wurden die Proben dann bis spätestens zwölf 27
39 Methodik Stunden nach Untersuchungsende mit dem Epos Analyser 5060 (Fa. EPPENDORF) analysiert. Der Test basiert auf folgendem Prinzip: L-Laktat + NAD + LDH Pyruvat + NADH + H + Das Enzym Laktatdehydrogenase (LDH) oxidiert Laktat zu Pyruvat, wobei NAD + zu NADH+ H + reduziert wird. Das während der Reaktion gebildete NADH+H + ist der Laktatkonzentration direkt proportional und kann bei 334 nm oder bei 365 nm photometrisch gemessen werden. Die venösen Blutentnahmen erfolgten jeweils vor der körperlichen Belastung zu Beginn und am Ende jeder Untersuchungsreihe zu gleichen Tageszeiten ( ), nicht nüchtern und im Sitzen. Mit Hilfe des Vacuette -Blutentnahmesystems der Firma Greiner bio-one (Flügelkanüle) wurde Blut aus einer Unterarmvene entnommen. EDTA Blut wurde zur Bestimmung des Blutbildes verwendet. drom und BAP Zur Bestimmung der Freien Sauerstoffradikale (drom) und des biologisch antioxidativen Potenzials (BAP) wurde das Ohrläppchen mit einer Hämostilette angestochen. Für die Messung der droms wurden 20 µl Kapillarblut in eine Kapillare gefüllt, für die Bestimmung von BAP benötigte man 400 µl Kapillarblut, das in eine heparinisierte Microvette gefüllt wurde. Diese Parameter wurden sowohl vor, als auch unmittelbar nach körperlicher Belastung bestimmt. 2.4 Apparaturbesprechung und analytische Methoden Für die Belastungsuntersuchungen wurden folgende Apparaturen eingesetzt: Laufbandergometer Alle Tests wurden auf dem Laufbandergometer der Fa. WOODWAY, Lörrach durchgeführt. Die technischen Daten des Laufbandes lauten: maximale Geschwindigkeit 7,15 m/s, Anstiegswinkel bis 20,5 und eine Lauffläche von 0,7x2,70 m. Die Lauffläche bestand aus einem Lamellengummibelag von 7 mm Stärke, 30 28
40 Methodik Schore Härte und einer Lamellenbreite von 6 cm. Das Laufband war auf vier Schwingungsdämpfern federnd gelagert. Seitlich des Laufbandes waren am Geländer Haltevorrichtungen für Schläuche und Atemmaske vorhanden. Während des Laufbandtests waren die Probanden mit einem Taillengurt gesichert, der über ein Seil mit einem Notstop verbunden war. Der Steigungswinkel betrug bei jedem Test 1 %, um den Energieverbrauch gegenüber Feldbedingungen auszugleichen. Stufentest Als Belastungsschema zur Beurteilung der Ausdauerleistungsfähigkeit wie auch der Vita maxima haben sich stufenförmige Belastungsverfahren sowohl auf dem Fahrradergometer als auch auf dem Laufband durchgesetzt [61]. Die Anfangsgeschwindigkeit des Stufentests betrug 2,5 m/s und wurde alle fünf Minuten stufenweise um 0,5 m/s bis zur Erschöpfung des Probanden gesteigert. Eine Ausnahme machten wir bei fünf Probanden der Untersuchungsreihe Injektion. Vier der fünf Mittelstreckler starteten die Ergometrie bei 3 m/s, einer der Sportler erst bei 3,5 m/s um eine vergleichbare Belastungszeit zu erhalten. Zu Beginn und danach alle fünf Minuten wurde während einer 30- sekündigen Pause kapilläres Blut aus dem Ohrläppchen zur Blutlaktatbestimmung entnommen. Während der letzten 15 Sekunden jeder Belastungsstufe wurde die Pulsfrequenz gemessen. Die Belastungsabbruchkriterien setzten sich aus der subjektiven Meinung der Sportler und objektiven Parameter wie Herzfrequenz und Respiratorischer Quotient zusammen. Im Untersuchungslabor herrschte eine durchschnittliche Raumtemperatur von 20 C, (Schwankungen von 19 C 23 C) und eine relative Luftfeuchtigkeit von 50%, was den Empfehlungen der ICSPE (International Council of Sport and Physical Education) entsprach [81]. Herzfrequenzmessgerät Die Pulsfrequenzmessung erfolgte telemetrisch durch den Sporttester PE 3000 (Fa. Unilife), der aus einem Elektrodengurt mit abnehmbarem Sender und einer Armbanduhr mit eingebautem Empfänger bestand. Der Gurt wurde im Thoraxbereich unter dem Pektoralmuskel angelegt. Er beinhaltete sowohl die Sendeelektronik als auch die Energieversorgung. Die Uhr wurde am Handgelenk getragen, um Signale 29
41 Methodik zu empfangen. Sie zeigte kontinuierlich die Pulsfrequenz an und speicherte diese elektronisch. Spiroergometriesystem Zur Registrierung und Speicherung der respiratorischen Parameter kam das offene Spirometriesystem ZAN Firma Ing. Wilhelm Horst ZAN Austria Medizintechnik (Bad Hall) zum Einsatz. Aus den registrierten Werten (AMV, CO 2 - und O 2 -Konzentrationen) erfolgte die Berechnung der relativen und absoluten V O 2, des Respiratorischen Quotienten (RQ), des Atemäquivalents und anderer Werte. Für die Blutparameterbestimmungen setzten wir folgende Apparaturen ein: Laktatmessgerät Die Laktatmessung erfolgte mit dem Gerät BIOSEN C_line der Firma EKF diagnostics Sales GmbH (Barleben/ Magdeburg). Die Bestimmung des Laktats erfolgte nach dem enzymatisch- ampèrometrischen Messprinzip mit Hilfe von Chip- Sensoren. Free Radical Analytical System Die Freien Sauerstoffradikale (drom) und das biologisch antioxidative Potential (BAP) wurden photometrisch mittels des F.R.A.S. 4 (Free Radical Analytical System) der Firma H&D srl (Parma, Italia) gemessen. Freie Sauerstoffradikale (drom) Mit Hilfe einer Glaskapillarpipette wurden 20 µl Kapillarblut aus dem Ohrläppchen abgenommen und in eine mit einem Puffer (ph 4,8) versehene Microvette gegeben und manuell durchmischt. Das Gemisch aus der Microvette wurde anschließend ohne die Glaskapillarpipette in eine Küvette gefüllt, die das kondensierte Chromogengemisch (N, N- Diethyl-para-phenylendiamin) enthielt. Zur Lösung des Chromogengemisches wurde die Küvette 10 Sekunden manuell geschwenkt und dann 60 Sekunden zentrifugiert. Danach wurde die Küvette zur Auswertung im Ableseschlitz platziert. Da es sich um eine kinetikgestützte Reaktion handelte, wurde 30
42 Methodik diese Aluminium- Messzelle automatisch auf 37 C erwärmt. Das Ergebnis wurde angezeigt und ausgedruckt. Alle Materialen waren von der Firma H&D srl (Parma, Italia) Der drom-test misst den Gehalt an Hydroperoxiden, wobei er auf einer Entdeckung von Fenton, vervollständigt von Haber und Weiss basiert. Der Test basiert auf dem Konzept, dass der Gehalt an organischen Hydroperoxiden im Serum mit der Anzahl der Freien Radikalen korreliert, aus denen diese gebildet wurden [3;22]. Die Verdünnung von 20 µl Kapillarblut in einer sauren Pufferlösung (ph 4,8) leitet eine Mikroazidose ein. Die von den Proteinen der sauren Pufferlösung freigesetzten Eisenionen, katalysieren die Reaktion von im Blut enthaltenen Hydroperoxiden zu Alkoxy- und Peroxy-Radikalen. Durch Zugabe eines farblosen, oxidierbaren Chromogengemisches (N,N-Diethyl-para-phenylendiamin) zu der Lösung, werden diese aromatischen Amine durch Elektronenabgabe an die neu gebildeten Radikale zu farblich veränderten radikalischen Kationen. Deren optische Dichte kann photometrisch bei 505 nm gemessen werden. Dabei ist die Konzentration an radikalischen Kationen nach dem Lambert-Beerschen-Gesetz direkt proportional zur Konzentration Freier Radikale und somit auch proportional zu der ursprünglichen Konzentration an Hydroperoxiden in der Probe. R-OOH + Fe 2+ R-O* + Fe 3+ + OH - R-OOH + Fe 3+ ROO * + Fe 2+ + H + R-O* + A-NH 2 RO - + [A-NH 2 *] + Chemische Reaktionen des drom-tests ROOH: Hydroperoxid, R-O*: Radikal aus Hydroperoxid generiert, A-NH 2 : N,N-Diethyl- Paraphenylendiamin (Chromogen), [A-NH 2 *] + : gefärbtes radikalisches Kation des Chromogens Die Messeinheit des drom-tests wird in Caratelli Units angegeben, nach dem italienischen Erfinder Mauro Caratelli. Ein UCarr ist äquivalent zu 0,08 mg/dl H 2 O 2. Nach Alberti et al. (2000) liegt der Normwert zwischen UCarr [3]. Tab. 5 zeigt die vom Hersteller definierte Zuordnung der drom-werte zur Höhe des oxidativen Stresses. 31
43 Methodik Tab. 5: Zuordnung der drom-werte UCarr: Normalwerte UCarr: Grenzbereich UCarr: niedriger oxidativer Stress UCarr: mittlerer oxidativer Stress UCarr: hoher oxidativer Stress >500U Carr: sehr hoher oxidativer Stress Biologisch Antioxidatives Potenzial (BAP) Auch der Test zum Nachweis des biologisch antioxidativen Potenzials ist ein photometrischer Test, wobei er auf folgendem Vorgang basiert: Bei diesem Test werden die Blutkonzentrationen von antioxidativen Reagenzien, die in der Lage sind Eisen (III)-Ionen (Fe 3+ ) zu Eisen (II)-Ionen (Fe 2+ ) zu reduzieren, gemessen. Zuerst wird zu dem in der Küvette bereits enthaltenen Reagenz R1 (Chromogen; Thiocyanat- Derivat) ein Tropfen des Reagenz R2 (Eisenchlorid; FeCl 3 ) zugegeben. Anschließend wird die Absorption der gefärbten Lösung bei 505 nm gemessen. Parallel dazu wird die Microvette mit dem aus dem Ohrläppchen abgenommenen Kapillarblut für 90 Sekunden bei 37 C zentrifugiert. Anschließend werden 10µl Plasma abpipettiert und zu dem oben genannten Gemisch hinzugegeben. Nach Zugabe des Plasmas und einer Inkubationszeit von fünf Minuten tritt durch die Reduktion von Fe 3+ zu Fe 2+ eine Entfärbung ein, die photometrisch als Absorptionsänderung bei 505 nm detektiert wird und direkt proportional zu der Konzentration aller Substanzen ist, die in der Lage sind, das Eisen von Fe 3+ zu Fe 2+ zu reduzieren, welche das biologisch antioxidative Potential der Plasmaprobe darstellen. Der BAP-Test liefert eine globale Messung zahlreicher Antioxidantien, einschließlich Harnsäure, Ascorbinsäure, Proteine, α- Tocopherole und Bilirubin. Er gibt keine Information über die Konzentration einzelner Antioxidantien sondern versucht vielmehr die gesamte antioxidative Kapazität zu erfassen. 32
44 Methodik Der BAP-Test ist eine vereinfachte Variante des verbreiteten und bekannten FRAP- Assays (ferric reducing antioxidant power), das heißt der Bestimmung der eisenreduzierenden Aktivität von Plasma. Gemessen wird in µmol reduziertes Fe 3+ /l Blutplasma, wobei die in Tab. 6 aufgelisteten Zuordnungen gelten. Nachfolgend wird anstatt der Einheit µmol red. Fe 3+ / l Blutplasma die Abkürzung E-BAP verwendet. µmol red. Fe 3+ / l Blutplasma Tab. 6: Zuordnung der BAP-Werte Verlust der antioxidativen Barriere > <1400 Optimaler Wert Grenzwert Leichter Mangel Moderater Mangel Erheblicher Mangel Sehr starker Mangel 33
45 Methodik 2.5 Nahrungsergänzungsmittel Für die Injektionslösung aus der ersten Untersuchungsreihe zogen wir eine Ampulle Vitamin B12-Hevert und eine Ampulle Folsäure-Hevert (Hevert-Arzneimittel GmbH & Co. KG, Nussbaum) auf 10 ml verdünnt mit NaCl (physiologische Kochsalzlösung) auf und injizierten das Gemisch intravenös über ein Butterflysystem in die Unterarmvene. Die Injektionslösung wird den Sportlern routinemäßig zur Infektprophylaxe verabreicht um saisonal gehäuft auftretende Infekte zu verhindern. Zusammensetzung: 1 Ampulle Vitamin B12-Hevert zu 2 ml enthält: Arzneilich wirksame Bestandteile: Cyanocobalamin 3mg Sonstige Bestandteile: Ammoniumsulfat, Natriumchlorid, Salzsäure 25 % (m/m), Wasser für Injektionszwecke 1 Ampulle Folsäure-Hevert zu 2 ml enthält: Arzneilich wirksame Bestandteile: Folsäure 20 mg Sonstige Bestandteile: Natriumchlorid, Natriumhydroxidlösung 25 % (m/v), Wasser für Injektionszwecke Eine zweite 10 ml Spritze wurde mit einer Ampulle zu 5 ml Injektionslösung Vitamin C 1000 mg (Wörwag Pharma GmbH & Co. KG, Böblingen) und 5 ml physiologische Kochsalzlösung aufgezogen und ebenfalls intravenös nach Gabe der ersten Spritze über das Butterflysytem injiziert. Dabei enthielt eine Ampulle 1000 mg Ascorbinsäure. Für die zweite Untersuchungsreihe erhielten die Probanden frubiase SPORT Ausdauer (Boehringer Ingelheim Pharma GmbH&Co. KG). Dabei sollten die Sportler einmal täglich 40 g des Pulvers in 500 ml Wasser auflösen und das Getränk vor oder während des Trainings trinken. 34
46 Methodik Inhaltsstoffe [129]: Nährwerte In 100 g Pro Portion (40 g) Energiewert Kohlenhydrate Davon mehrwertige Natrium Fett Eiweiß Alkohol Broteinheiten 1364 kj = 326 kcal 68,70 g 1,50 g 1,04 g ,14 BE 546 kj = 130 kcal 27,48 g 0,60 g 0,42 g ,46 BE Inhaltsstoffe Pro 100 g Pro Portion (40 g) RDA pro Portion (%) Vitamin D3 12,5 µg 5 µg 100 Vitamin B1 10,5 mg 4,2 mg 380 Vitamin B2 12 mg 4,8 mg 340 Niacin (NE) 135 mg 54 mg 340 Pantothensäure 45 mg 18 mg 300 Vitamin B6 15 mg 6 mg 400 Folsäure 1500 µg 600 µg 300 Biotin 1125 µg 450 µg 900 Vitamin B12 7,5 µg 3 µg 120 Vitamin C 450 mg 180 mg 225 Vitamin E (α-te) 75 mg 30 mg 250 Calcium 1250 mg 500 mg 63 Kalium 1250 mg 500 mg 25 Magnesium 875 mg 350 mg 93 Eisen 12,5 mg 5 mg 36 Zink 12,5 mg 5 mg 50 Jod 225 µg 90 µg 60 35
47 Methodik 2.6 Statistische Auswertung Die in dieser Studie erhobenen Daten wurden in Microsoft Excel verwaltet und mit dem Programm SPSS Statistic Version 17.0 ausgewertet. Bei der Auswertung der Untersuchungsergebnisse kamen folgende Prüfverfahren zur Anwendung: Arithmetisches Mittel ( x) = x/ n Varianz (v) und Standardabweichung (SD) Die Standardabweichung ist definitionsgemäß die Quadratwurzel aus der Varianz. Als Varianz bezeichnet man die Summe der Abweichungsquadrate aller Messwerte einer Verteilung von ihrem arithmetischen Mittel, dividiert durch die um 1 verminderte Anzahl der Messungen. Nach Absprache mit dem Institut für Medizinische Statistik, Informatik und Epidemiologie der Universität zu Köln verwendeten wir als weiteres prüfstatistisches Verfahren den student- t- Test für verbundene Stichproben. Des Weiteren wurden die Ergebnisse des student-t-tests post hoc mit Hilfe der Bonferroni-Methode korrigiert, um die Alphafehler-Kumulierung bei multiplen Paarvergleichen zu neutralisieren. Die Varianzanalyse (General linear model) wurde als zusätzliches prüfstatistisches Verfahren eingesetzt. Signifikanzschranken Folgende Signifikanzschranken gelten für die Irrtumswahrscheinlichkeit p: p > 0.05 nicht signifikant (-) p 0.05 schwach signifikant (*) p 0.01 hoch signifikant (**) 36
48 Untersuchungsergebnisse 3 Untersuchungsergebnisse 3.1 Untersuchungsreihe frubiase SPORT Ausdauer Leistungsdiagnostische Parameter der Stufentests In Tab. 7 sind die Mittelwerte ( ) und Standardabweichungen (SD) ausgewählter leistungsdiagnostischer Parameter des Stufentests dargestellt. Es werden die Ruhewerte, die Werte der einzelnen Geschwindigkeitsstufen des Stufentests sowie die Werte nach der Erholungsphase von 3 Minuten (3E) angegeben. Die Tabelle ist unterteilt in die Ergebnisse des Stufentests vor Einnahme von Frubiase (Vortest) und nach 35-tägiger Einnahme von Frubiase (Nachtest). Bei dieser Untersuchungsreihe starteten alle 10 Probanden die Ergometrie bei einer Geschwindigkeit von 2,5 m/s, zwei Probanden beendeten die Belastung nach der Stufe von 3.5 m/s, fünf Probanden beendeten die Laufbandbelastung nach der Geschwindigkeitsstufe von 4 m/s und drei Probanden waren erst nach der Geschwindigkeitsstufe von 4,5 m/s ausbelastet. 37
49 Untersuchungsergebnisse Tab. 7: Mittelwerte und Standardabweichungen der leistungsdiagnostischen Parameter Herzfrequenz (HF), Laktat, absolute Sauerstoffaufnahme(V O 2 ), Atemäquivalent (V E/ V O 2 ) und Respiratorischer Quotient (RQ) der beiden Laufbandstufentests der Frubiase-Untersuchungsreihe Parameter Ruhe 2,5 m/s 3 m/s 3,5 m/s 4 m/s 4,5 m/s 3E Vortest HF 78,2 145,4 161, ,88 193,67 - (S/min) ±8,59 ±10,73 ±10,06 ±8,64 ±6,81 ±8,50 Laktat 1,49 2,64 3,54 5,4 7, ,56 (mmol/l) ±0,22 ±0,98 ±1,57 ±2,51 ±1,37 ±1,25 ±1,87 V O 2 708,9 2856, , (ml/min) ±136,50 ±555,54 ±632,87 ±814,29 ±503,79 ±66,64 V E/ V O 2 29,55 23,8 25,56 29,27 30,77 32,75 - ±3,60 ±2,62 ±4,55 ±6,59 ±4,06 ±3,98 RQ 0,82 0,88 0,92 0,98 1,02 1,04 - ±0,10 ±0,04 ±0,05 ±0,06 ±0,05 ±0,04 Nachtest HF 68, ,8 171,5 183, (S/min) ±7,58 ±7,39 ±7,54 ±5,34 ±6,71 ±5,57 Laktat 1 2,19 2,69 4,33 6,3 9,03 7,18 (mmol/l) ±0,25 ±0,63 ±0,98 ±1,81 ±1,01 ±1,60 ±1,44 V O 2 739, ,5 3880,9 4449, ,33 - (l/min) ±126,61 ±592,26 ±624,41 ±517,38 ±401,92 ±407,52 V E/ V O 2 29,7 23,91 24,36 26,22 28,6 30,18 - ±6,24 ±2,73 ±2,51 ±2,40 ±3,37 ±4,92 RQ 0,82 0,89 0,93 0,98 1,02 1,02 - ±0,09 ±0,03 ±0,05 ±0,08 ±0,04 ±0,01 38
50 Untersuchungsergebnisse Herzfrequenz Abb. 9 zeigt den Verlauf der mittleren Herzfrequenz (HF) mit Standardabweichung in Ruhe und während der jeweiligen Belastungsstufen (2,5 m/s; 3 m/s; 3,5 m/s; 4m/s; 4,5 m/s) bis zum Abbruch der Ergometrie von Vortest und Nachtest im Vergleich. Bei den Geschwindigkeitsstufen 3 m/s und 3,5 m/s zeigten sich signifikante Unterschiede zwischen der Laufbandbelastung vor Einnahme von Frubiase und nach 35-tägiger Einnahme des Präparats (p=0,013 und p=0,014). Führte man post hoc jedoch die Bonferroni-Korrektur durch, verschwanden diese Signifikanzen und es zeigten sich nur noch Tendenzen (für beide Stufen p=0,09) Herzfrequenz (S/min) n=10 n=10 n=10 n=8 n= n=10 Ruhe 2,5 3 3,5 4 4,5 Geschwindigkeit (m/s) vor Frubiaseeinnahme nach Frubiaseeinnahme Abb. 9: Verlauf der mittleren Herzfrequenz mit Standardfehlern in Ruhe und im Laufe der Ergometrie vor und nach 35-tägiger Frubiaseeinnahme. n= Anzahl der Probanden, die die jeweilige Stufe gelaufen sind 39
51 Untersuchungsergebnisse Blutlaktat Abb. 10 zeigt den Verlauf der mittleren Blutlaktatkonzentration mit Standardabweichung in Ruhe, während der jeweiligen Belastungsstufen (2,5 m/s; 3 m/s; 3,5 m/s; 4 m/s; 4,5 m/s) bis zum Abbruch der Ergometrie und nach einer Erholungsphase von 3 Minuten (3E) von Vortest und Nachtest im Vergleich. Bis auf die Geschwindigkeitsstufe von 2,5 m/s, 3,5 m/s und 4,5 m/s unterschieden sich die Blutlaktatkonzentrationen zwischen Vortest und Nachtest bei den jeweiligen Belastungsstufen signifikant (p 0,05) als auch hochsignifikant (p 0,01). Die einzelnen p-werte, unter Berücksichtigung der post hoc durchgeführten Bonferroni- Korrektur, mit den dazugehörigen Geschwindigkeitsstufen sind in Tab. 8 dargestellt: Tab. 8: p-werte der Blutlaktatkonzentrationen bei den jeweiligen Geschwindigkeitsstufen Geschwindigkeit p-wert (m/s) Ruhe 0,002 2,5 0, ,046 3,5 0, ,028 4,5 0,602 3E 0,035 40
52 Untersuchungsergebnisse 14 Laktat (mmol/l) * ** n=10 n= 10 n=10 * * n=3 n= 8 n = 10 n= 10 Ruhe 2,5 3 3,5 4 4,5 3E Geschwindigkeit (m/s) vor Frubiaseeinnahme nach Frubiaseeinnahme Abb. 10: Verlauf der mittleren Blutlaktatkonzentration mit Standardfehlern in Ruhe, im Laufe der Ergometrie und nach Erholung vor und nach Frubiaseeinnahme. Signifikante Unterschiede (p 0,05) (*) und hochsignifikante Unterschiede (p 0,01) (**) zwischen den Belastungstests bei den jeweiligen Geschwindigkeitsstufen. n= Anzahl der Probanden, die die jeweilige Stufe gelaufen sind Tab. 9 stellt die 2 mmol/l- Laktatschwellenleistung und Tab. 10 die 4 mmol/l- Laktatschwellenleistung der Stufentests vor und nach Frubiaseeinnahme gegenüber. Tab. 9: Mittelwert ( ) und Standardabweichung (SD) der 2 mmol/l- Laktatschwellenleistung (in m/s) vor und nach Frubiaseeinnahme Vortest Nachtest 2,18 2,45 SD 0,31 0,55 Tab. 10: Mittelwert ( ) und Standardabweichung (SD) der 4 mmol/ l- Laktatschwellenleistung (in m/s) vor und nach Frubiaseeinnahme Vortest Nachtest 3,33 3,44 SD 0,24 0,35 41
53 Untersuchungsergebnisse Die Geschwindigkeiten sowohl bei 2 mmol/l Laktat (p=0,02) als auch bei 4 mmol/l Laktat (p=0,01) unterschieden sich vor und nach 35-tägiger Frubiaseeinnahme signifikant voneinander. Betrug die Geschwindigkeit der 2 mmol/l-laktatschwelle beim Vortest 2,18 ± 0,31 m/s, lag sie nach der 35-tägigen Einnahme von Frubiase bei 2,45 ± 0,55 m/s. Die 4 mmol/l-laktatschwelle veränderte sich von 3,33 m/s im Vortest auf 3,44 m/s im Nachtest. Die daraus resultierende Rechtsverschiebung der Laktatleistungskurve ist in Abb. 10 dargestellt Sauerstoffaufnahme Abb. 11 zeigt den Verlauf der mittleren Sauerstoffaufnahme (V O 2 in ml/min) mit Standardabweichung in Ruhe und während der jeweiligen Belastungsstufen (2,5 m/s; 3 m/s; 3,5 m/s; 4m/s; 4,5 m/s) bis zum Abbruch der Ergometrie von Vortest und Nachtest im Vergleich. Die statistische Auswertung zeigte weder in Ruhe noch bei den einzelnen Geschwindigkeitsstufen Unterschiede zwischen den beiden Belastungstests. VO 2 (ml/min) n= 3 n= 8 n= 10 n= 10 n= 10 n= 10 Ruhe 2,5 3 3,5 4 4,5 Geschwindigkeit (m/s) vor Frubiaseeinnahme nach Frubiaseeinnahme Abb. 11: Verlauf der mittleren Sauerstoffaufnahme (V O 2 ) mit Standardfehlern in Ruhe und im Laufe der Ergometrie vor und nach Frubiaseeinnahme. n= Anzahl der Probanden, die die jeweilige Stufe gelaufen sind 42
54 Untersuchungsergebnisse Atemäquivalent Abb. 12 zeigt den Verlauf des mittleren Atemäquivalents (V E/V O 2 ) mit Standardabweichung in Ruhe und während der jeweiligen Belastungsstufen (2,5 m/s; 3 m/s; 3,5 m/s; 4 m/s; 4,5 m/s) bis zum Abbruch der Ergometrie von Vortest und Nachtest im Vergleich. Die statistische Auswertung zeigte weder in Ruhe noch bei den einzelnen Geschwindigkeitsstufen Unterschiede zwischen den beiden Belastungstests. VE/ VO n= 8 n=3 n=10 n= 10 n=10 n=10 Ruhe 2,5 3 3,5 4 4,5 Geschwindigkeit (m/s) vor Frubiaseeinnahme nach Frubiaseeinnahme Abb. 12: Verlauf des mittleren Atemäquivalents (V E/V O 2 ) mit Standardfehlern in Ruhe und im Laufe der Ergometrie vor und nach Frubiaseeinnahme. n= Anzahl der Probanden, die die jeweilige Stufe gelaufen sind 43
55 Untersuchungsergebnisse Respiratorischer Quotient Abb. 13 zeigt den Verlauf des mittleren Respiratorischen Quotienten (RQ) mit Standardabweichung in Ruhe und während der jeweiligen Belastungsstufen (2,5 m/s; 3 m/s; 3,5 m/s; 4 m/s; 4,5 m/s) bis zum Abbruch der Ergometrie von Vortest und Nachtest im Vergleich. Die statistische Auswertung zeigte weder in Ruhe noch bei einer der Geschwindigkeitsstufen Unterschiede zwischen den beiden Belastungstests. RQ 1,1 1,06 1,02 0,98 0,94 0,9 0,86 0,82 0,78 0,74 0,7 n= 3 n= 8 n= 10 n= 10 n= 10 n= 10 Ruhe 2,5 3 3,5 4 4,5 Geschwindigkeit (m/s) Vortest Nachtest Abb. 13: Verlauf des Respiratorischen Quotienten (RQ) mit Standardfehlern in Ruhe und im Laufe der Ergometrie vor und nach Frubiaseeinnahme. n= Anzahl der Probanden, die die jeweilige Stufe gelaufen sind 44
56 Untersuchungsergebnisse Parameter des oxidativen Stresses drom In Tab. 11 sind die Mittelwerte und Standardabweichungen der Freien Sauerstoffradikale (drom) vor und nach Belastung dargestellt. Die Tabelle ist weiter unterteilt in Vortest (vor Frubiaseeinnahme) und Nachtest (nach Frubiaseeinnahme). Abb. 14 stellt diese Werte noch einmal graphisch dar. Bei der Untersuchungsreihe Frubiase konnte weder beim Vortest noch beim Nachtest ein signifikanter Unterschied zwischen den Werten vor Belastung und nach Belastung gefunden werden. So lag die Konzentration der Freien Sauerstoffradikalen beim Vortest vor der Ergometrie bei 224,8 ± 31,22 UCarr und stieg nach der Laufbandbelastung um 9 % auf 245,5 ± 63,74 UCarr (p= 0,26). Beim Nachtest stieg die Konzentration an Freien Sauerstoffradikalen um 8,5% von 229,9 ± 42,02 UCarr auf 249,4 ± 37,72 UCarr (p=0,08). Auch konnten wir keinen signifikanten Unterschied zwischen den beiden Werten Freier Sauerstoffradikale vor Belastung vom Vortest und Nachtest erkennen (p=0,81). Des Weiteren untersuchten wir, ob es einen signifikanten Unterschied zwischen den Anstiegen der Konzentration der Freien Sauerstoffradikale im Laufe der Ergometrie von Vortest und Nachtest gab. Auch hier konnten wir kein signifikantes Ergebnis finden (p=0,95) Tab. 11: Mittelwerte und Standardabweichung der Freien Sauerstoffradikale (drom in UCarr) von Vortest und Nachtest der Untersuchungsreihe Frubiase Test vor Belastung nach Belastung Vortest 224,8 245,5 ±31,22 ±63,74 Nachtest 229,9 249,4 ±42,02 ±37,72 45
57 Untersuchungsergebnisse drom (UCarr) vor Frubiaseeinnahme nach Frubiaseeinnahme Abnahmezeitpunkt vor Belastung nach Belastung Abb. 14: Graphische Darstellung von Mittelwerten und Standardabweichungen der Freien Sauerstoffradikale (drom in UCarr) vor und nach Belastung der beiden Laufbandbelastungen der Untersuchungsreihe Frubiase BAP In Tab. 12 sind die Mittelwerte und Standardabweichungen des biologischen antioxidativen Potenzials (BAP), gemessen in µmol red. Fe 3+ /l Blutplasma vor und nach Belastung der Untersuchungsreihe Frubiase dargestellt. Die Tabelle ist weiter unterteilt in Vortest (vor Frubiaseeinnahme) und Nachtest (nach Frubiaseeinnahme). Abb. 15 stellt diese Werte noch einmal graphisch dar. Die BAP-Einheit µmol red. Fe 3+ /l Blutplasma wird nachfolgend abgekürzt als E-BAP bezeichnet. Tab. 12: Mittelwerte und Standardabweichung des biologisch antioxidativen Potenzials (BAP in E- BAP) von Vortest und Nachtest der Untersuchungsreihe Frubiase Test vor Belastung nach Belastung Vortest 2117,6 2496,3 ±225,78 ±255,41 Nachtest 2177,4 2571,5 ±130,95 ±265,45 46
58 Untersuchungsergebnisse Bei der Untersuchungsreihe Frubiase konnten signifikante Unterschiede sowohl beim Vortest als auch beim Nachtest zwischen den BAP-Werten vor Belastung und nach Belastung gefunden werden. So lag der BAP-Wert beim Vortest bei 2117,6 ± 225,78 E-BAP und stieg um 17,9 % auf 2496,3 ± 255,41 E-BAP nach Belastung an (p= 0,002). Beim Nachtest stieg BAP von 2177,4 ± 130,95 E-BAP um 18,1 % auf 2571,5 ± 265,45 E-BAP nach Belastung an (p=0,00), womit wir einen hochsignifikanten Unterschied nachweisen konnten. Keinen signifikanten Unterschied fanden wir beim Vergleich der beiden Vorbelastungswerte des biologisch antioxidativen Potenzials der beiden Belastungstests (p=0,35). Auch konnten wir keinen signifikanten Unterschied zwischen den Anstiegen der Konzentration der Freien Sauerstoffradikale im Laufe der Ergometrie von Vortest und Nachtest feststellen (p=0,88) ** ** BAP vor Frubiaseeinahme nach Frubiaseeinnahme Abnahmezeitpunkt vor Belastung nach Belastung Abb. 15: Mittelwerte und Standardabweichung des biologisch antioxidativen Potentials (BAP in E- BAP) vor und nach Belastung der beiden Laufbandbelastungen der Untersuchungsreihe Frubiase. Hochsignifikante Unterschiede (**) (p 0,01) zwischen den Werten vor und nach Belastung 47
59 Untersuchungsergebnisse 3.2 Untersuchungsreihe Injektion Leistungsdiagnostische Parameter der Stufentests Im Folgenden werden die leistungsdiagnostischen Ergebnisse der Injektions- Untersuchungsreihe vorgestellt. In Tab. 13 sind die Mittelwerte und Standardabweichungen ausgewählter leistungsdiagnostischer Parameter des Stufentests dargestellt. Es werden die Ruhewerte, die Werte der einzelnen Geschwindigkeitsstufen des Stufentests sowie die Werte nach einer Erholungsphase von 3 Minuten angegeben. Die Tabelle ist unterteilt in die Ergebnisse des Stufentests vor Gabe der Injektionen (Vortest) und nach Verabreichung der drei Injektionen (Nachtest). Bei dieser Untersuchungsreihe starteten fünf Probanden die Ergometrie bei einer Geschwindigkeit von 2,5 m/s, vier Probanden begannen bei der Stufe von 3 m/s und einer bei der Stufe von 3,5 m/s. Von den fünf Probanden, die bereits bei 2,5 m/s starteten beendete einer die Belastung nach der Stufe von 3,5 m/s, die anderen beendeten die Ergometrie nach der 4,5 m/s-belastungsstufe. Von den Probanden, die bei 3 m/s starteten, waren alle nach einer Geschwindigkeitsstufe von 5 m/s ausbelastet. Der Sportler, der die Belastung bei 3,5 m/s begann, lief bis einschließlich der Geschwindigkeitsstufe von 5,5 m/s. Weitere Details sind in den nachfolgenden Diagrammen sichtbar. 48
60 Untersuchungsergebnisse Tab. 13: Mittelwerte und Standardabweichungen der leistungsdiagnostischen Parameter Herzfrequenz (HF), Laktat, Sauerstoffaufnahme (V 0 2 ), Atemäquivalent (V E/V O 2 ) und Respiratorischer Quotient (RQ) der beiden Laufbandstufentests der Injektionsuntersuchungsreihe Parameter Ruhe 2,5 m/s 3m/s 3,5m/s 4m/s 4,5m/s 5m/s 5,5m/s 3E Vortest HF 79,00 146,80 151,67 164,50 177,22 187,33 191,40 189,00 - (S/min) ±10,87 ±10,43 ±19,33 ±19,79 ±17,27 ±15,17 ±12,88 - Laktat 1,12 1,76 1,71 2,37 3,27 6,29 7,90 10,70 8,03 (mmol/l) ±0,25 ±0,27 ±0,76 ±1,56 ±1,91 ±3,50 ±2,24 - ±1,68 V O 2 559, , , , , , , ,00 - (ml/min) ±93,66 ±415,44 ±470,81 ±495,62 ±512,70 ±537,17 ±545,08 - (V E/V O 2 ) 28,03 22,58 22,33 23,70 25,18 27,99 27,88 36,68 - ±2,73 ±1,65 ±2,92 ±2,68 ±3,89 ±4,28 ±3,16 - RQ 0,84 0,94 0,93 0,95 0,98 1,04 1,05 1,09 - ±0,05 ±0,02 ±0,05 ±0,05 ±0,06 ±0,09 ±0,03 - Nachtest HF 73,50 140,40 143,22 155,50 168,22 181,44 183,20 182,00 - (S/min) ±8,34 ±10,85 ±17,06 ±19,36 ±17,64 ±14,22 ±7,01 - Laktat 1,06 1,78 1,57 2,29 2,74 5,04 4,70 7,50 6,56 (mmol/l) ±0,25 ±0,55 ±1,09 ±2,19 ±1,88 ±3,49 ±1,06 - ±2,02 V O 2 576, , , , , , , ,00 - (ml/min) ±41,83 ±187,48 ±552,11 ±698,28 ±592,40 ±659,19 ±508,01 - (V E/V O 2 ) 29,84 21,96 22,73 23,38 24,75 27,85 26,93 36,02 - ±3,43 ±2,10 ±2,82 ±2,73 ±2,77 ±3,78 ±0,93 - RQ 0,82 0,93 0,93 0,96 0,98 1,04 1,04 1,11 - ±0,06 ±0,03 ±0,07 ±0,07 ±0,04 ±0,08 ±0,04-49
61 Untersuchungsergebnisse Herzfrequenz Abb. 16 zeigt den Verlauf der mittleren Herzfrequenz mit Standardabweichung in Ruhe und während der jeweiligen Belastungsstufen (2,5 m/s; 3 m/s; 3,5 m/s; 4m/s; 4,5 m/s, 5m/s; 5,5m/s) bis zum Abbruch der Ergometrie von Vortest und Nachtest der Injektionsuntersuchungsreihe im Vergleich. Unter Berücksichtigung der post hoc durchgeführten Korrektur nach Bonferroni zeigte sich nur noch bei der Geschwindigkeitsstufe von 2,5 m/s ein signifikanter Unterschied zwischen den beiden Belastungstests (p=0,023) Herzfrequenz * n= 5 n= 9 n= 10 n= 9 n= 9 n= 5 n= n= 10 Ruhe 2,5 3 3,5 4 4,5 5 5,5 Geschwindigkeit (m/s) Vortest Nachtest Abb. 16: Verlauf der mittleren Herzfrequenz mit Standardfehlern in Ruhe und im Lauf der Ergometrie vor und nach der Verabreichung der drei Injektionen. Signifikante Unterschiede (p 0,05) (*) zwischen den Belastungstests bei den jeweiligen Geschwindigkeitsstufen. n= Anzahl der Probanden, die die jeweilige Stufe gelaufen sind 50
62 Untersuchungsergebnisse Blutlaktat Abb. 17 zeigt den Verlauf der mittleren Blutlaktatkonzentration mit Standardabweichung in Ruhe, während der jeweiligen Belastungsstufen (2,5 m/s; 3 m/s; 3,5 m/s; 4m/s; 4,5 m/s; 5 m/s, 5,5 m/s) bis zum Abbruch der Ergometrie und nach einer Erholungsphase von drei Minuten (3E) von Vortest und Nachtest der Injektions-Untersuchungsreihe im Vergleich. Bei der Belastungsstufe von 4 m/s (p=0,011) konnten wir signifikante Unterschiede zwischen den Laktatwerten von Vortest und Nachtest beobachten. Tab. 14 stellt die 2 mmol/l-laktatschwellenleistung und Tab. 15 die 4 mmol/l- Laktatschwellenleistung der Stufentests vor und nach Verabreichung der Injektionen gegenüber Laktat (mmol/l) * n= 5 n = 1 n = n= 9 n= 5 n= 10 n= 9 n= 10 n= 9 Ruhe 2,5 3 3,5 4 4,5 5 5,5 3E Geschwindigkeit (m/s) Vortest Nachtest Abb. 17: Verlauf der mittleren Blutlaktatkonzentration mit Standardfehlern in Ruhe, im Lauf der Ergometrie und nach Erholung vor und nach Verabreichung der drei Injektionen. Signifikante Unterschiede (p 0,05) (*) zwischen den Belastungstests bei den jeweiligen Geschwindigkeitsstufen. n= Anzahl der Probanden, die die jeweilige Stufe gelaufen sind 51
63 Untersuchungsergebnisse Tab. 14: Mittelwert ( ) und Standardabweichung (SD) der 2 mmol/l-laktatschwellenleistung (in m/s) vor und nach Gabe der Injektionen Vortest Nachtest 3,47 3,61 SD 0,7 0,94 Tab. 15: Mittelwert ( ) und Standardabweichung (SD) der 4 mmol/l-laktatschwellenleistung (in m/s) vor und nach Gabe der Injektionen Vortest Nachtest 4,1 4,21 SD 0,55 0,68 Bei der Injektionsuntersuchungsreihe konnten wir bei der 4mmol/l- Laktatschwellenleistung einen signifikanten Unterschied zwischen Vortest und Nachtest finden (p=0,037). 52
64 Untersuchungsergebnisse Sauerstoffaufnahme Abb. 18 zeigt den Verlauf der mittleren Sauerstoffaufnahme (V O 2 in ml/min) mit Standardabweichung in Ruhe und während der jeweiligen Belastungsstufen (2,5 m/s; 3 m/s; 3,5 m/s; 4m/s; 4,5 m/s; 5 m/s; 5,5 m/s) bis zum Abbruch der Ergometrie von Vortest und Nachtest im Vergleich. Die statistische Auswertung zeigte weder in Ruhe noch bei den einzelnen Geschwindigkeitsstufen Unterschiede zwischen den beiden Belastungstests VO 2 (ml/min) n= 5 n= 9 n= 10 n= 9 n= 9 n= 5 n= n= 10 Ruhe 2,5 3 3,5 4 4,5 5 5,5 Geschwindigkeit (m/s) Vortest Nachtest Abb. 18: Verlauf der mittleren Sauerstoffaufnahme V O 2 mit Standardfehlern in Ruhe und im Lauf der Ergometrie vor und nach der Gabe der drei Injektionen. n= Anzahl der Probanden, die die jeweilige Stufe gelaufen sind 53
65 Untersuchungsergebnisse Atemäquivalent Abb. 19 zeigt den Verlauf des mittleren Atemäquivalents (V E/V O 2 ) mit Standardabweichung in Ruhe und während der jeweiligen Belastungsstufen (2,5 m/s; 3 m/s; 3,5 m/s; 4m/s; 4,5 m/s; 5 m/s; 5,5 m/s) bis zum Abbruch der Ergometrie von Vortest und Nachtest im Vergleich. Die statistische Auswertung zeigte keine signifikanten Unterschiede zwischen Vortest und Nachtest n= 1 32 VE/VO n= 10 n= 9 n= n= 10 n= 9 n= 5 n=9 Ruhe 2,5 3 3,5 4 4,5 5 5,5 Geschwindigkeit (m/s) vor Injektion nach Injektion Abb. 19: Verlauf des mittleren Atemäquivalents (V E/V O 2 ) mit Standardfehlern in Ruhe und im Lauf der Ergometrie vor und nach Gabe der drei Injektionen. n= Anzahl der Probanden, die die jeweilige Stufe gelaufen sind 54
66 Untersuchungsergebnisse Respiratorischer Quotient Abb. 20 zeigt den Verlauf des mittleren Respiratorischen Quotienten (RQ) mit Standardabweichung in Ruhe und während der jeweiligen Belastungsstufen (2,5 m/s; 3 m/s; 3,5 m/s; 4 m/s; 4,5 m/s; 5 m/s; 5,5 m/s) bis zum Abbruch der Ergometrie von Vortest und Nachtest der Injektionsuntersuchungsreihe im Vergleich. Die statistische Auswertung zeigte weder in Ruhe noch bei einer der Geschwindigkeitsstufen signifikante Unterschiede zwischen den beiden Belastungstests. 1,16 1,12 1,08 1,04 n= 1 1 RQ 0,96 0,92 0,88 0,84 n= 5 n= 9 n= 10 n= 9 n= 9 n= 5 0,8 0,76 0,72 n= 10 Ruhe 2,5 3 3,5 4 4,5 5 5,5 Geschwindigkeit (m/s) Vortest Nachtest Abb. 20: Verlauf des Respiratorischen Quotienten (RQ) mit Standardfehlern in Ruhe und im Lauf der Ergometrie vor und nach der Gabe der 3 Injektionen. n= Anzahl der Probanden, die die jeweilige Stufe gelaufen sind 55
67 Untersuchungsergebnisse Parameter des oxidativen Stresses drom In Tab. 16 sind die Mittelwerte und Standardabweichungen der Freien Sauerstoffradikale (drom) vor und nach Belastung dargestellt. Die Tabelle ist weiter unterteilt in Vortest (vor den Injektionen) und Nachtest (nach den drei Injektionen). Abb. 21 stellt diese Werte noch einmal graphisch dar. Tab. 16: Mittelwerte und Standardabweichung der Freien Sauerstoffradikale (drom in UCarr) von Vortest und Nachtest der Injektions-Untersuchungsreihe Test vor Belastung nach Belastung Vortest 233,7 246,3 ±30,45 ±54,31 Nachtest 246,3 270 ±44,07 ±46,81 Bei der Untersuchungsreihe Injektion konnte beim Nachtest ein signifikanter Unterschied zwischen den Werten vor Belastung und nach Belastung gefunden werden. So lag die Konzentration der Freien Sauerstoffradikale beim Nachtest vor der Ergometrie bei 246,3 ± 44,07 UCarr und stieg nach der Laufbandbelastung um 9,6 % auf 270 ± 46,81 UCarr (p=0,027). Beim Vortest konnten wir keinen signifikanten Unterschied feststellen (p=0,4). Auch konnten wir keinen signifikanten Unterschied zwischen den drom-werten gemessen jeweils vor Belastung von Vortest und Nachtest erkennen (p=0,55). Des Weiteren untersuchten wir, ob es einen signifikanten Unterschied zwischen den Anstiegen der Konzentration der Freien Sauerstoffradikale im Laufe der Ergometrie von Vortest und Nachtest gab. Auch hier konnten wir kein signifikantes Ergebnis finden (p=0,92). 56
68 Untersuchungsergebnisse * drom (UCarr) vor Belastung nach Belastung 150 vor Injektion nach Injektion Abnahmezeitpunkt Abb. 21: Graphische Darstellung von Mittelwerten und Standardabweichungen der Freien Sauerstoffradikale (drom in UCarr) vor und nach Belastung der beiden Laufbandbelastungen der Injektionsuntersuchungsreihe. Signifikante Unterschiede (*) (p 0,05) zwischen den Werten vor und nach Belastung BAP In Tab. 17 sind die Mittelwerte und Standardabweichungen des biologisch antioxidativen Potenzials, gemessen in µmol red. Fe 3+ / l Blutplasma (E-BAP), vor und nach Belastung der Untersuchungsreihe Injektion dargestellt. Die Tabelle ist weiter unterteilt in Vortest (vor den Injektionen) und Nachtest (nach Verabreichung der drei Injektionen). Abb. 22 stellt diese Werte noch einmal graphisch dar. Tab. 17: Mittelwerte und Standardabweichung des biologisch antioxidativen Potenzials (BAP in E- BAP) von Vortest und Nachtest der Injektions-Untersuchungsreihe Test vor Belastung nach Belastung Vortest ,1 ±256,39 ±493,23 Nachtest 2557, ±158,76 ±242,71 57
69 Untersuchungsergebnisse Bei der Untersuchungsreihe Injektion konnten hochsignifikante Unterschiede sowohl beim Vortest als auch beim Nachtest zwischen den BAP-Werten vor Belastung und nach Belastung gefunden werden. So lag der Mittelwert des biologisch antioxidativen Potentials beim Vortest bei 2072 ± 256,39 E-BAP und stieg um 27,5 % auf 2641,1 ± 493,23 E-BAP nach Belastung an (p=0,004). Beim Nachtest stieg der Mittelwert des biologisch antioxidativen Potenzials um 16,8 % von 2557,8 ± 158,76 E-BAP auf 2987 ± 242,71 E-BAP nach Belastung an (p=0,001). Keinen signifikanten Unterschied fanden wir beim Vergleich der Anstiege der Mittelwerte des biologisch antioxidativen Potenzials im Laufe der Ergometrie von Vortest und Nachtest (p=0,504) ** ** BAP vor Belastung nach Belastung vor Injektion Abnahmezeitpunkt nach Injektion Abb. 22: Graphische Darstellung von Mittelwerten und Standardabweichungen des biologisch antioxidativen Potenzials (BAP in E-BAP) vor und nach Belastung der beiden Laufbandbelastungen der Injektions-Untersuchungsreihe. Hochsignifikante Unterschiede (**) (p 0,01) zwischen den Werten vor und nach Belastung Zu Wochenbeginn vor Gabe der ersten Injektion haben wir noch einmal die BAP- und drom-werte gemessen. Wir konnten weder bei der Messung der Freien Sauerstoffradikale (p=0,56) noch bei der Messung des biologisch antioxidativen Potenzials (p=0,17) signifikante Unterschiede zwischen den Werten vor der ersten 58
70 Untersuchungsergebnisse Injektion beziehungsweise nach der letzten Injektion erkennen. In Tab. 18 werden diese Werte noch einmal gegenüber gestellt. Tab. 18: Tabellarische Darstellung der Mittelwerte sowie Standardabweichung von drom (in UCarr) und BAP (in E-BAP) vor der ersten Injektion und nach der letzten der drei Injektionen der Injektionsuntersuchungsreihe Parameter vor erster Injektion nach letzter Injektion drom 253,9 246,3 ±35,48 ±44,07 BAP 2453,2 2557,8 ±180,88 ±158,76 59
71 Diskussion 4 Diskussion Oxidativer Stress entsteht bei einem Ungleichgewicht zwischen der Bildung Freier Radikale und dem Verbrauch des antioxidativen Schutzsystems [48]. Erschöpfende körperliche Belastung ist assoziiert mit einer gesteigerten Bildung Freier Radikale und Entstehung von oxidativem Stress [6;30;69], wodurch die Gesundheit und das Wohlbefinden des Sportlers eingeschränkt werden können. Die verstärkte Bildung Freier Radikale korreliert positiv mit einer erhöhten Muskelschädigung und verstärkten Ermüdbarkeit [9;34]. Normalerweise entstehen bei allen aeroben Stoffwechselprozessen aus zwei bis zehn Prozent des im Mitochondrium umgesetzten Sauerstoffs Freie Radikale [4;12]. Aufgrund des enormen Anstiegs des Sauerstoffverbrauchs während körperlicher Belastung kann somit von einer erhöhten Radikalbelastung des Organismus ausgegangen werden. In unserer Studie stieg die Sauerstoffaufnahme während der Laufbandbelastung im Durchschnitt um das sieben- bis achtfache an, wie in Abb. 23 zu sehen ist VO 2 (ml/min) vor Injektion nach Injektion vor Frubiase nach Frubiase Ruhe Arbeit Abb. 23: Absolute Sauerstoffaufnahme in Ruhe und nach körperlicher Arbeit Der durch körperliche Belastung entstandene oxidative Stress kann nun zur Lipidperoxidation, Protein- und DNA-Schäden führen [6;51] und somit die Integrität der Zelle stören und Gewebeschädigungen herbeiführen. Um dies zu verhindern hat der Organismus zum einen ein antioxidatives Schutzsystem und zum anderen 60
72 Diskussion Mechanismen entwickelt, die die durch Freie Radikale entstandenen Schäden reparieren. Das antioxidative Schutzsystem ist ein komplexes System bestehend aus zahlreichen Enzymen und niedermolekularen Stoffen. Es basiert auf dem Prinzip, dass das antioxidative Schutzsystem die hochreaktiven Freien Radikale in weniger reaktive Moleküle umwandelt. Abb. 24: Sauerstoffradikale und seine Wirkungen im Organismus nach [89] Die Kapazität des antioxidativen Schutzsystems ist sowohl abhängig von einer adäquaten Aufnahme von Vitaminen, Mineralstoffen und Spurenelementen als auch von der körpereigenen Synthese einiger Antioxidantien wie Glutathion. Es wurde angedeutet, dass Athleten, die regelmäßig hoch intensiv trainieren und Wettkämpfe absolvieren, nicht in der Lage sind über die Nahrung eine ausreichende Menge an Vitaminen zu sich zu nehmen [28]. Inwieweit diese Aussage mit unserer Studie übereinstimmt, wird im Laufe der Arbeit diskutiert. Ziel dieser Untersuchung war es zu ermitteln, ob nach einer maximal erschöpfenden Belastung auf dem Laufband bei Hochleistungssportlern oxidativer Stress im Blut zu beobachten ist und welchen Einfluss die Belastung auf das biologisch antioxidative Potential hat. Darüber hinaus interessierte uns der Effekt der zusätzlichen Einnahme von Nahrungsergänzungsmitteln auf das biologisch antioxidative Potential und den 61
Wie funktioniert der FORT Test (Free Oxygen Radicals Test)
 Wie funktioniert der FORT Test (Free Oxygen Radicals Test) mit dem FORM Analysator (Free Oxygen Radicals Monitor)? Einführung zur Thematik der freien Radikale Normalerweise verfügen alle Stoffe über eine
Wie funktioniert der FORT Test (Free Oxygen Radicals Test) mit dem FORM Analysator (Free Oxygen Radicals Monitor)? Einführung zur Thematik der freien Radikale Normalerweise verfügen alle Stoffe über eine
Oxidativer Stress Vitamine
 1 Oxidativer Stress Vitamine 2 Reaktive Sauerstoffspezies (ROS) Reaktive Sauerstoffspezies (ROS) Ein-Elektronenreduktion von Sauerstoff durch Strahlung oder Autooxidation von reduzierten Stoffwechselzwischenprodukten
1 Oxidativer Stress Vitamine 2 Reaktive Sauerstoffspezies (ROS) Reaktive Sauerstoffspezies (ROS) Ein-Elektronenreduktion von Sauerstoff durch Strahlung oder Autooxidation von reduzierten Stoffwechselzwischenprodukten
O 2. Perhydroxyl-Radikal HOO initiiert eine Kettenreaktion mit gebildeten Lipid Peroxyl- Radikalen (LOO )
 Singulett Sauerstoff 1 2 Relativ stabil, aber sehr reaktiv Superoxid-Radikal 2 Mitochondrien sind wichtige Quelle; Signalmolekül, generiert andere RS Hydroxyl-Radikal H Äußerst reaktiv, kurze Halbwertszeit
Singulett Sauerstoff 1 2 Relativ stabil, aber sehr reaktiv Superoxid-Radikal 2 Mitochondrien sind wichtige Quelle; Signalmolekül, generiert andere RS Hydroxyl-Radikal H Äußerst reaktiv, kurze Halbwertszeit
Oxidativer- / Nitrosativer-Stress
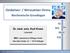 Oxidativer- / Nitrosativer-Stress Biochemische Grundlagen Dr. med. univ. Kurt Kraus Laborarzt Otto-Hahn-Straße 18 76275 Ettlingen 1 Inhalt Was ist oxidativer Stress? Was ist nitrosativer Stress? Was sind
Oxidativer- / Nitrosativer-Stress Biochemische Grundlagen Dr. med. univ. Kurt Kraus Laborarzt Otto-Hahn-Straße 18 76275 Ettlingen 1 Inhalt Was ist oxidativer Stress? Was ist nitrosativer Stress? Was sind
07. März Atherosklerose durch oxidativen Stress?
 07. März 2012 Atherosklerose durch oxidativen Stress? Dr. rer. nat. Katrin Huesker Atherosklerose durch oxidativen Stress? Pathogenese Diagnostik Therapie www.nlm.nih.gov/medlineplus Atherosklerose durch
07. März 2012 Atherosklerose durch oxidativen Stress? Dr. rer. nat. Katrin Huesker Atherosklerose durch oxidativen Stress? Pathogenese Diagnostik Therapie www.nlm.nih.gov/medlineplus Atherosklerose durch
07. März Atherosklerose durch oxidativen Stress?
 07. März 2012 Atherosklerose durch oxidativen Stress? Dr. rer. nat. Katrin Huesker Atherosklerose durch oxidativen Stress? Pathogenese Diagnostik Therapie www.nlm.nih.gov/medlineplus Atherosklerose durch
07. März 2012 Atherosklerose durch oxidativen Stress? Dr. rer. nat. Katrin Huesker Atherosklerose durch oxidativen Stress? Pathogenese Diagnostik Therapie www.nlm.nih.gov/medlineplus Atherosklerose durch
8 Reaktive Sauerstoffspezies
 8 Reaktive Sauerstoffspezies 166 8 Reaktive Sauerstoffspezies Reaktive Sauerstoffspezies (Reactive xygen Species, RS) werden durch normale zelluläre Reaktionen in aeroben rganismen gebildet. Zu den RS
8 Reaktive Sauerstoffspezies 166 8 Reaktive Sauerstoffspezies Reaktive Sauerstoffspezies (Reactive xygen Species, RS) werden durch normale zelluläre Reaktionen in aeroben rganismen gebildet. Zu den RS
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase
 Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Pentosephosphat. hosphatweg
 Pentosephosphat hosphatweg Wie aus dem Namen abzuleiten ist, werden C5-Zucker, einschließlich Ribose, aus Glucose synthetisiert. Das oxidierende Agens ist hierbei NADP + ; es wird zu NADP reduziert, das
Pentosephosphat hosphatweg Wie aus dem Namen abzuleiten ist, werden C5-Zucker, einschließlich Ribose, aus Glucose synthetisiert. Das oxidierende Agens ist hierbei NADP + ; es wird zu NADP reduziert, das
BLUUUUT!!!!! Das Blut ist ein Organ!! Es hat wichtige Funktionen: - O2/ CO2+Vitamine+ Nahrung Stoffwechselendprodukt-Transport - Wärmeabtransport!
 BLUUUUUUT!!!!! Das Blut ist ein Organ!! Es hat wichtige Funktionen: - O2/ COVitamine+ Nahrung Stoffwechselendprodukt-Transport - Wärmeabtransport! - Elektrolyttransport -Osmoregulation - Hormontransport
BLUUUUUUT!!!!! Das Blut ist ein Organ!! Es hat wichtige Funktionen: - O2/ COVitamine+ Nahrung Stoffwechselendprodukt-Transport - Wärmeabtransport! - Elektrolyttransport -Osmoregulation - Hormontransport
"Dexamethason und Selenige Säure als Beispiele für ultraschnell wirksame direkte Radikalfänger: Quantenpharmakologische Untersuchungen"
 "Dexamethason und lenige Säure als Beispiele für ultraschnell wirksame direkte Radikalfänger: Quantenpharmakologische Untersuchungen" Priv.-Doz. Dr. ans-georg Mack (hans-georg.mack@uni-tuebingen.de) Computational
"Dexamethason und lenige Säure als Beispiele für ultraschnell wirksame direkte Radikalfänger: Quantenpharmakologische Untersuchungen" Priv.-Doz. Dr. ans-georg Mack (hans-georg.mack@uni-tuebingen.de) Computational
Fragenkatalog SSM04 Grundlagen der Ernährung, oxidativer Stress und Sport
 Fragenkatalog SSM04 Grundlagen der Ernährung, oxidativer Stress und Sport Bei der Prüfung werden aus den Kapiteln Grundlagen der Ernährung, Chemie der freien Radikale und Antioxidantien, sowie Schädigung
Fragenkatalog SSM04 Grundlagen der Ernährung, oxidativer Stress und Sport Bei der Prüfung werden aus den Kapiteln Grundlagen der Ernährung, Chemie der freien Radikale und Antioxidantien, sowie Schädigung
Vorname: Frage 1. Nennen Sie drei Metalle, die :für den Menschen essentiell sind und als Mengenelemente Körper vorkommen (3 P) Frage 2
 1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
Lipide. Dr. med. Tamás Pándics. Biochemie I. SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie
 Lipide Biochemie I Dr. med. Tamás Pándics SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie Lipide Definition: hydrophobe Biomoleküle Heterogene Gruppe mit abwechslungsreichen Funktionen: Bestandteile
Lipide Biochemie I Dr. med. Tamás Pándics SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie Lipide Definition: hydrophobe Biomoleküle Heterogene Gruppe mit abwechslungsreichen Funktionen: Bestandteile
1 Vom Organismus zum Molekül... 3
 I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
Kraftwerk Körper Energiegewinnung in unseren Zellen
 Was passiert eigentlich, wenn wir etwas essen und dann loslaufen müssen? Wie können unsere Zellen die Stoffen aus der Nahrung zur Energiegewinnung nutzen? Die Antwort auf diese Fragen gibt s in diesem
Was passiert eigentlich, wenn wir etwas essen und dann loslaufen müssen? Wie können unsere Zellen die Stoffen aus der Nahrung zur Energiegewinnung nutzen? Die Antwort auf diese Fragen gibt s in diesem
Trainingslehre - Ausdauer. Ausdauer. Das zentrale Thema der Trainingslehre im Pflichtfach Sport! Folie 1
 Ausdauer Das zentrale Thema der Trainingslehre im Pflichtfach Sport! Folie 1 Ausdauer 1. Lohnt sich Ausdauertraining? 2. Energiebereitstellung in der Muskelzelle und Funktion des Herz-Kreislauf-Systems
Ausdauer Das zentrale Thema der Trainingslehre im Pflichtfach Sport! Folie 1 Ausdauer 1. Lohnt sich Ausdauertraining? 2. Energiebereitstellung in der Muskelzelle und Funktion des Herz-Kreislauf-Systems
Energieverbrauch > 5.000 kcal/woche durch Training = mind. 6 Std. intensives Training!!! Ernährung (Essen + Trinken!) der letzten Hauptmahlzeit vor
 Energieverbrauch > 5.000 kcal/woche durch Training = mind. 6 Std. intensives Training!!! Ernährung (Essen + Trinken!) der letzten Hauptmahlzeit vor der Belastung, unmittelbar vor der Belastung, während
Energieverbrauch > 5.000 kcal/woche durch Training = mind. 6 Std. intensives Training!!! Ernährung (Essen + Trinken!) der letzten Hauptmahlzeit vor der Belastung, unmittelbar vor der Belastung, während
Redoxprozesse. Warum ist Sauerstoff für uns lebensnotwendig?
 Redoxprozesse Diese Lerneinheit befasst sich mit der Knallgasexplosion und Atmungskette - eine biologische Betrachtung von Redoxreaktionen mit den folgenden Lehrzielen: Warum ist Sauerstoff für uns lebensnotwendig?
Redoxprozesse Diese Lerneinheit befasst sich mit der Knallgasexplosion und Atmungskette - eine biologische Betrachtung von Redoxreaktionen mit den folgenden Lehrzielen: Warum ist Sauerstoff für uns lebensnotwendig?
Inhaltsverzeichnis. I Stoffwechsel. 1 Vom Organismus zum Molekül Aminosäuren Peptide und Proteine Enzyme...
 XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
Inhalt 1. Ausdauertraining Regeneration Pause
 Inhalt 1. Ausdauertraining 1.1 Definition 1.2 Energiebereitstellung 1.3 Anaerobe Schwelle 1.4 Formen von Ausdauer 1.5 Methoden des Ausdauertrainings 2. Regeneration 2.1 Definition 2.2 Superkompensation
Inhalt 1. Ausdauertraining 1.1 Definition 1.2 Energiebereitstellung 1.3 Anaerobe Schwelle 1.4 Formen von Ausdauer 1.5 Methoden des Ausdauertrainings 2. Regeneration 2.1 Definition 2.2 Superkompensation
Adiponectin Eine Schlüsselsubstanz im Stoffwechsel
 Adiponectin Eine Schlüsselsubstanz im Stoffwechsel Dr. Harald Fischer, Frankfurt am Main 2015 Adiponectin Grosse Familie der Adipocytokine Über 100 Hormone (-ähnliche) die regulierend in den Stoffwechsel
Adiponectin Eine Schlüsselsubstanz im Stoffwechsel Dr. Harald Fischer, Frankfurt am Main 2015 Adiponectin Grosse Familie der Adipocytokine Über 100 Hormone (-ähnliche) die regulierend in den Stoffwechsel
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Hämatopoese TITAN. Dezember 2005 S.Gärtner
 Hämatopoese Alle reifen Blutzellen stammen von pluripotenten hämatopoetischen Stammzellen ab, die sich von Geburt an im Knochenmark, in der Leber und der Milz befinden. Hämatopoese Die hämapoetischen Stammzelle
Hämatopoese Alle reifen Blutzellen stammen von pluripotenten hämatopoetischen Stammzellen ab, die sich von Geburt an im Knochenmark, in der Leber und der Milz befinden. Hämatopoese Die hämapoetischen Stammzelle
TIENS H-Cup Exzellente Wahl
 TIENS H-Cup Exzellente Wahl Wasser ist unverzichtbar Entwicklung von wasserstoffreichem Wasser 2007 Professor Ohsawavon der medizinischeruniversität in Japan veröffentlichte die These vom Wasserstoff als
TIENS H-Cup Exzellente Wahl Wasser ist unverzichtbar Entwicklung von wasserstoffreichem Wasser 2007 Professor Ohsawavon der medizinischeruniversität in Japan veröffentlichte die These vom Wasserstoff als
Auswirkungen von Ausdauersport auf kardiovaskuläre Veränderungen
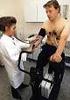 Auswirkungen von Ausdauersport auf kardiovaskuläre Veränderungen Definition von kardiovaskulär Kardiovaskulär bedeutet Herz ( kardio ) und Gefäße ( vaskulär ) betreffend. Da Herz und Gefäße ein System
Auswirkungen von Ausdauersport auf kardiovaskuläre Veränderungen Definition von kardiovaskulär Kardiovaskulär bedeutet Herz ( kardio ) und Gefäße ( vaskulär ) betreffend. Da Herz und Gefäße ein System
SS Thomas Schrader. der Universität Duisburg-Essen. (Teil 8: Redoxprozesse, Elektrochemie)
 Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Diagnostik und Interpretation von Mineralstoffspiegeln. Dr. rer. nat. Katrin Huesker, IMD Berlin
 Diagnostik und Interpretation von Mineralstoffspiegeln Dr. rer. nat. Katrin Huesker, IMD Berlin Einflussgrößen Mineralstoff -status Wirkung Was ist bei der Labordiagnostik wichtig? 1. Heparin- oder EDTA-Vollblut
Diagnostik und Interpretation von Mineralstoffspiegeln Dr. rer. nat. Katrin Huesker, IMD Berlin Einflussgrößen Mineralstoff -status Wirkung Was ist bei der Labordiagnostik wichtig? 1. Heparin- oder EDTA-Vollblut
Energiehaushalt. Cem Ekmekcioglu Valentin Leibetseder. Institut für Physiologie, MUW
 Energiehaushalt Cem Ekmekcioglu Valentin Leibetseder Institut für Physiologie, MUW Vorlesung unter: http://www.meduniwien.ac.at/umweltphysiologie/links.htm Energiehaushalt Die Energie im Organismus wird
Energiehaushalt Cem Ekmekcioglu Valentin Leibetseder Institut für Physiologie, MUW Vorlesung unter: http://www.meduniwien.ac.at/umweltphysiologie/links.htm Energiehaushalt Die Energie im Organismus wird
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Das Spurenelement Chrom III als Komponente des Glucose Toleranz Faktors
 Das Spurenelement Chrom III als Komponente des Glucose Toleranz Faktors Obwohl nicht mehr als etwa 6 mg Chrom im menschlichen Körper vorkommt, spielt es eine wichtige Rolle im Stoffwechsel der Kohlenhydrate.Die
Das Spurenelement Chrom III als Komponente des Glucose Toleranz Faktors Obwohl nicht mehr als etwa 6 mg Chrom im menschlichen Körper vorkommt, spielt es eine wichtige Rolle im Stoffwechsel der Kohlenhydrate.Die
Metallbelastung und oxidativer Stress
 Metallbelastung und oxidativer Stress Dr. rer. nat. Katrin Huesker, IMD Berlin Oxidativer Stress schwächt die Blut-Hirn-Schranke! Barrierefunktion Glukose Zigarettenrauch- Extrakt Prasad et al., 2015 Zigarettenrauch
Metallbelastung und oxidativer Stress Dr. rer. nat. Katrin Huesker, IMD Berlin Oxidativer Stress schwächt die Blut-Hirn-Schranke! Barrierefunktion Glukose Zigarettenrauch- Extrakt Prasad et al., 2015 Zigarettenrauch
TOP-CHECK-UP OXIDATIVER STRESS
 TOP-CHECK-UP TOP-CHECK-UP Für unsere Gesundheit sind wir zu einem grossen Teil selbst verantwortlich. Sie wird hauptsächlich dadurch bestimmt, wie wir uns verhalten, was wir essen und wieviel wir uns bewegen.
TOP-CHECK-UP TOP-CHECK-UP Für unsere Gesundheit sind wir zu einem grossen Teil selbst verantwortlich. Sie wird hauptsächlich dadurch bestimmt, wie wir uns verhalten, was wir essen und wieviel wir uns bewegen.
Oxidative Phosphorylierung
 BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
BIORACING Ergänzungsfuttermittel
 BIORACING Ergänzungsfuttermittel...für Pferde Der natürlich Weg zur optimaler Gesundheit und Leistungsfähigkeit Einführung Was ist BIORACING? Die einzigartige Nahrungsergänzung enthält die Grundbausteine
BIORACING Ergänzungsfuttermittel...für Pferde Der natürlich Weg zur optimaler Gesundheit und Leistungsfähigkeit Einführung Was ist BIORACING? Die einzigartige Nahrungsergänzung enthält die Grundbausteine
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Stoffwechsel. Die Chemie des Lebens ist in Stoffwechselwegen organisiert
 Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
Inhaltsverzeichnis. a. Chemie der Aminosäuren und Peptide
 Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
ESSENTIAL. mit Mangostan, Acai & Aloe Vera 900ml
 ESSENTIAL mit Mangostan, Acai & Aloe Vera 900ml 2/16 3/16 01 MANCHE MENSCHEN BLEIBEN GESÜNDER; LEBEN LÄNGER UND ALTERN LANGSAMER; DA SIE IN IHRER ERNÄHRUNG NÄHRSTOFFMÄNGEL VERMEIDEN: EQ Essential ist die
ESSENTIAL mit Mangostan, Acai & Aloe Vera 900ml 2/16 3/16 01 MANCHE MENSCHEN BLEIBEN GESÜNDER; LEBEN LÄNGER UND ALTERN LANGSAMER; DA SIE IN IHRER ERNÄHRUNG NÄHRSTOFFMÄNGEL VERMEIDEN: EQ Essential ist die
Stoffwechsel der essentiellen Aminosäuren
 Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasse
 Hämoglobin Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasseraustausch im Kapillarbereich Durch die
Hämoglobin Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasseraustausch im Kapillarbereich Durch die
Reaktionen der Zellatmung (1)
 ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
Aus der Klinik für Dermatologie, Venerologie und Allergologie der Medizinischen Fakultät der Charité Universitätsmedizin Berlin DISSERTATION
 Aus der Klinik für Dermatologie, Venerologie und Allergologie der Medizinischen Fakultät der Charité Universitätsmedizin Berlin DISSERTATION Evaluation der Laser-Scan-Mikroskopie, der Laser-Doppler- Blutflussmessung
Aus der Klinik für Dermatologie, Venerologie und Allergologie der Medizinischen Fakultät der Charité Universitätsmedizin Berlin DISSERTATION Evaluation der Laser-Scan-Mikroskopie, der Laser-Doppler- Blutflussmessung
Atmung Respiration 1
 Atmung Respiration 1 Atmung Die oxidative Phosphorylierung ist der letzte Schritt einer Serie von Energieumwandlungen, die insgesamt als Zellatmung oder einfach Atmung (Respiration) bezeichnet werden 2
Atmung Respiration 1 Atmung Die oxidative Phosphorylierung ist der letzte Schritt einer Serie von Energieumwandlungen, die insgesamt als Zellatmung oder einfach Atmung (Respiration) bezeichnet werden 2
Raumfahrtmedizin. darauf hin, dass es auch einen Zusammenhang zwischen Knochenabbau, Bluthochdruck und Kochsalzzufuhr gibt. 64 DLR NACHRICHTEN 113
 Raumfahrtmedizin Gibt es einen Die geringe mechanische Belastung der unteren Extremitäten von Astronauten im All ist eine wesentliche Ursache für den Knochenabbau in Schwerelosigkeit. Gleichzeitig haben
Raumfahrtmedizin Gibt es einen Die geringe mechanische Belastung der unteren Extremitäten von Astronauten im All ist eine wesentliche Ursache für den Knochenabbau in Schwerelosigkeit. Gleichzeitig haben
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Ozon und Vitamin C. von Dr. med. Horst Kief. Gelsenkirchen Oktober 2015
 Ozon und Vitamin C von Dr. med. Horst Kief Gelsenkirchen Oktober 2015 Physiologische Wirkung von Vitamin C Hydroxilierung von Nebennierenrindenhormonen Hydroxilierung von Dopamin zu Noradrenalin und von
Ozon und Vitamin C von Dr. med. Horst Kief Gelsenkirchen Oktober 2015 Physiologische Wirkung von Vitamin C Hydroxilierung von Nebennierenrindenhormonen Hydroxilierung von Dopamin zu Noradrenalin und von
Test über die Veränderung von Laktat und Herzfrequenz unter regelmäßiger Einnahme von fitrabbit Mag. Bernhard Schimpl
 Test über die Veränderung von Laktat und Herzfrequenz unter regelmäßiger Einnahme von fitrabbit Mag. Bernhard Schimpl Testdesign: 6 Hobbyläufer (3 Frauen / 3 Männer) wurden einer Laufbandergometrie unterzogen,
Test über die Veränderung von Laktat und Herzfrequenz unter regelmäßiger Einnahme von fitrabbit Mag. Bernhard Schimpl Testdesign: 6 Hobbyläufer (3 Frauen / 3 Männer) wurden einer Laufbandergometrie unterzogen,
Chemische Evolution. Biologie-GLF von Christian Neukirchen Februar 2007
 Chemische Evolution Biologie-GLF von Christian Neukirchen Februar 2007 Aristoteles lehrte, aus Schlamm entstünden Würmer, und aus Würmern Aale. Omne vivum ex vivo. (Alles Leben entsteht aus Leben.) Pasteur
Chemische Evolution Biologie-GLF von Christian Neukirchen Februar 2007 Aristoteles lehrte, aus Schlamm entstünden Würmer, und aus Würmern Aale. Omne vivum ex vivo. (Alles Leben entsteht aus Leben.) Pasteur
Vitalstoffe zum Schutz vor Strahlung. Dipl.-Päd. Miriam Lauterbach-Paula Vitalstoffberatung
 Vitalstoffe zum Schutz vor Strahlung Dipl.-Päd. Miriam Lauterbach-Paula Vitalstoffberatung Wir sind ständig unterschiedlichen Strahlen ausgesetzt, z.b. Sonnenstrahlen, Höhenstrahlen, Erdstrahlen, Elektrosmog,
Vitalstoffe zum Schutz vor Strahlung Dipl.-Päd. Miriam Lauterbach-Paula Vitalstoffberatung Wir sind ständig unterschiedlichen Strahlen ausgesetzt, z.b. Sonnenstrahlen, Höhenstrahlen, Erdstrahlen, Elektrosmog,
Forschungswerkstatt Herz Kreislauf 2007 Neue Daten zu Aspirin. Von Prof. Dr. Stefanie M. Bode Böger
 Forschungswerkstatt Herz Kreislauf 2007 Neue Daten zu Aspirin Von Prof. Dr. Stefanie M. Bode Böger Köln (15. März 2007) - Das akute Koronarsyndrom (AKS) ist durch Angina pectoris Beschwerden und Ischämie-typische
Forschungswerkstatt Herz Kreislauf 2007 Neue Daten zu Aspirin Von Prof. Dr. Stefanie M. Bode Böger Köln (15. März 2007) - Das akute Koronarsyndrom (AKS) ist durch Angina pectoris Beschwerden und Ischämie-typische
Ei ne P ä r sentati ti on vo n T om D ro t s e, P t e er Haak k und Patrick Schürmann
 Ei P ä tti T D t P t H k d Eine Präsentation von Tom Droste, Peter Haak und Patrick Schürmann Inhaltsverzeichnis Allgemein: Was ist Stickstofffixierung? Welche Arten der Fixierung gibt es? Welchen Zweck
Ei P ä tti T D t P t H k d Eine Präsentation von Tom Droste, Peter Haak und Patrick Schürmann Inhaltsverzeichnis Allgemein: Was ist Stickstofffixierung? Welche Arten der Fixierung gibt es? Welchen Zweck
FIT MIT ROH- & NATURKOST
 FIT MIT ROH- & NATURKOST Keimling Mikroalgen Typische Nährwertanalysen Winfried Holler prüft Bio-Spirulina vor Ort Bio-Spirulina-Farm Spezial-Info Nr. s7000 Stand: 02/2006 Das kleine Nährstofflexikon
FIT MIT ROH- & NATURKOST Keimling Mikroalgen Typische Nährwertanalysen Winfried Holler prüft Bio-Spirulina vor Ort Bio-Spirulina-Farm Spezial-Info Nr. s7000 Stand: 02/2006 Das kleine Nährstofflexikon
Chemie-Tutorien zur Vorbereitung auf das Praktikum
 Seite 1 von 7 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie-Tutorien zur Vorbereitung auf das Praktikum 07.03.-18.03.2017 Dienstag, 07.03.2017 18.00-20.00 Uhr Grundlagen der Chemie I Donnerstag, 09.03.2017
Seite 1 von 7 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie-Tutorien zur Vorbereitung auf das Praktikum 07.03.-18.03.2017 Dienstag, 07.03.2017 18.00-20.00 Uhr Grundlagen der Chemie I Donnerstag, 09.03.2017
WIE HORMONE UNSER GEWICHT BEEINFLUSSEN
 GEWICHTSMANAGEMENT WIE HORMONE UNSER GEWICHT BEEINFLUSSEN Übergewicht ist ein Risikofaktor für viele Krankheiten und ein erstzunehmendes Problem unserer Gesellschaft. Mit zunehmendem Gewicht steigt das
GEWICHTSMANAGEMENT WIE HORMONE UNSER GEWICHT BEEINFLUSSEN Übergewicht ist ein Risikofaktor für viele Krankheiten und ein erstzunehmendes Problem unserer Gesellschaft. Mit zunehmendem Gewicht steigt das
Auch heute wird noch diskutiert, ob Fluor zu den
 Spurenelement. Die höchsten Konzentrationen an Kupfer liegen in Leber und Gehirn sowie Herz und Nieren vor. Auf Knochen und Muskulatur entfallen rund 20 und 40 Prozent des Gesamtgehalts. Nur ein sehr kleiner
Spurenelement. Die höchsten Konzentrationen an Kupfer liegen in Leber und Gehirn sowie Herz und Nieren vor. Auf Knochen und Muskulatur entfallen rund 20 und 40 Prozent des Gesamtgehalts. Nur ein sehr kleiner
1. Teil Stoffwechselphysiologie
 A TIERPHYSIOLOGISCHES PRAKTIKUM Martin-Luther-King-Platz KLAUSUR WS 2011/12 D-20146 Hamburg Name:... Matrikel Nr... (Ausweis vorlegen) 0.02.2012 1. Teil Stoffwechselphysiologie Fachbereich Biologie Biozentrum
A TIERPHYSIOLOGISCHES PRAKTIKUM Martin-Luther-King-Platz KLAUSUR WS 2011/12 D-20146 Hamburg Name:... Matrikel Nr... (Ausweis vorlegen) 0.02.2012 1. Teil Stoffwechselphysiologie Fachbereich Biologie Biozentrum
Thema: Energiebereitstellung (beim Walking)
 Fortbildungsveranstaltung am IfSS der Universität Karlsruhe (TH) Trainingslehre im Neigungsfach Sport Datum: 26.09.2005 Thema: Energiebereitstellung (beim Walking) Faktoren sportlicher Leistung Schnabel
Fortbildungsveranstaltung am IfSS der Universität Karlsruhe (TH) Trainingslehre im Neigungsfach Sport Datum: 26.09.2005 Thema: Energiebereitstellung (beim Walking) Faktoren sportlicher Leistung Schnabel
Taurin. Ursprung. Vorkommen
 Ursprung Taurin oder 2-Aminoethansulfonsäure ist eine organische Säure mit einer Aminogruppe und wird deshalb oft als Aminosäure bezeichnet es handelt sich jedoch um eine Aminosulfonsäure, da es statt
Ursprung Taurin oder 2-Aminoethansulfonsäure ist eine organische Säure mit einer Aminogruppe und wird deshalb oft als Aminosäure bezeichnet es handelt sich jedoch um eine Aminosulfonsäure, da es statt
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt.
 Übung und Lösung zur Übung Aminosäuren 1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt. 2. Das Tripeptid Glutathion ( -Glu-Cys-Gly)
Übung und Lösung zur Übung Aminosäuren 1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt. 2. Das Tripeptid Glutathion ( -Glu-Cys-Gly)
Konditionellen Substanz Ausdauer. Zuchwil, MSL
 Konditionellen Substanz Ausdauer Zuchwil, 24.4.2016 MSL Einordnung im Modell 2 22 Stoffwechsel: Baustoffwechsel Wachstum und Erneuerung durch Zellteilung und mit Eiweissbestandteilen Betriebs- oder Energiestoffwechsel
Konditionellen Substanz Ausdauer Zuchwil, 24.4.2016 MSL Einordnung im Modell 2 22 Stoffwechsel: Baustoffwechsel Wachstum und Erneuerung durch Zellteilung und mit Eiweissbestandteilen Betriebs- oder Energiestoffwechsel
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
σ2p. π2p. σ*2s. σ2s. σ*1s. σ1s. Σ g O 2. Δ g O 2. Σ g+ O 2 *O 2 O 2
 Freie Radikale und Ernährung Was sind Freie Radikale? Freie Radikale sind Atome oder Moleküle mit einem oder mehreren ungepaarten Elektronen im äußersten Orbital wodurch sie sehr reaktiv werden und ihre
Freie Radikale und Ernährung Was sind Freie Radikale? Freie Radikale sind Atome oder Moleküle mit einem oder mehreren ungepaarten Elektronen im äußersten Orbital wodurch sie sehr reaktiv werden und ihre
Adaptation der Muskulatur an Arbeit und Training beim Pferd. Korinna Huber Tierärztliche Hochschule Hannover
 Adaptation der Muskulatur an Arbeit und Training beim Pferd Korinna Huber Tierärztliche Hochschule Hannover Aktivierung körpereigener Systeme bei körperlicher Arbeit Breves/Engelhardt Physiologie der Haustiere
Adaptation der Muskulatur an Arbeit und Training beim Pferd Korinna Huber Tierärztliche Hochschule Hannover Aktivierung körpereigener Systeme bei körperlicher Arbeit Breves/Engelhardt Physiologie der Haustiere
HYPOXIETRAINING WAS VERSTEHT MAN UNTER HYPOXIE? WAS IST IN DER HÖHE ANDERS?
 ???? IMSB-Austria 1 WAS VERSTEHT MAN UNTER? WAS IST IN DER HÖHE ANDERS? IMSB-Austria 2 1 WELCHE VERÄNDERUNGEN SIND ZU ERWARTEN? ARTEN DES S IMSB-Austria 3 ERFAHRUNGEN DISKUSSION IMSB-Austria 4 2 TRAINING
???? IMSB-Austria 1 WAS VERSTEHT MAN UNTER? WAS IST IN DER HÖHE ANDERS? IMSB-Austria 2 1 WELCHE VERÄNDERUNGEN SIND ZU ERWARTEN? ARTEN DES S IMSB-Austria 3 ERFAHRUNGEN DISKUSSION IMSB-Austria 4 2 TRAINING
Oxidativer Stress. Fachinformation 0081
 Oxidativer Stress 2 Oxidativer Stress In einem gesunden Organismus besteht ein Gleichgewicht zwischen prooxidativen Faktoren und antioxidativen Schutzsystemen, bestehend aus Enzymen, Vitaminen, Spurenelementen
Oxidativer Stress 2 Oxidativer Stress In einem gesunden Organismus besteht ein Gleichgewicht zwischen prooxidativen Faktoren und antioxidativen Schutzsystemen, bestehend aus Enzymen, Vitaminen, Spurenelementen
82211 Herrsching. 1 Hintergrund. 2 Produktbeschreibung. Seite 1 (8) Oskar-von-Miller-Straße 10 D Schongau, Germany
 Seite 1 (8) Dartsch Scientific GmbH Oskar-von-Miller-Str. 10 D-86956 Schongau Medizinisches Beratungszentrum GmbH & Co. KG c/o Herrn Michael Schellenberger Seestraße 38 82211 Herrsching Oskar-von-Miller-Straße
Seite 1 (8) Dartsch Scientific GmbH Oskar-von-Miller-Str. 10 D-86956 Schongau Medizinisches Beratungszentrum GmbH & Co. KG c/o Herrn Michael Schellenberger Seestraße 38 82211 Herrsching Oskar-von-Miller-Straße
Mitochondrien und oxidativer Stress
 Neuigkeiten aus der Huntington-Forschung. In einfacher Sprache. Von Wissenschaftlern geschrieben Für die Huntington-Gemeinschaft weltweit. Oxidativer Stress bei der Huntington'schen Krankheit im Visier
Neuigkeiten aus der Huntington-Forschung. In einfacher Sprache. Von Wissenschaftlern geschrieben Für die Huntington-Gemeinschaft weltweit. Oxidativer Stress bei der Huntington'schen Krankheit im Visier
Metabolische Veränderungen und Zelltod in neuralen Zellen. durch Advanced Glycation Endproducts -
 Metabolische Veränderungen und Zelltod in neuralen Zellen durch Advanced Glycation Endproducts - Implikationen für die Pathogenese der Alzheimer schen Demenz Dissertation zur Erlangung des naturwissenschaftlichen
Metabolische Veränderungen und Zelltod in neuralen Zellen durch Advanced Glycation Endproducts - Implikationen für die Pathogenese der Alzheimer schen Demenz Dissertation zur Erlangung des naturwissenschaftlichen
F Ü R S T U D I E R E N D E D E R M E D I Z I N BIOCHEMISCHES INSTITUT DER UNIVERSITÄT ZÜRICH
 B I O C H E M I S C H E S P R A K T I K U M F Ü R S T U D I E R E N D E D E R M E D I Z I N BIOCHEMISCHES INSTITUT DER UNIVERSITÄT ZÜRICH 2003 INHALTSVERZEICHNIS *) Zum Biochemischen Praktikum steht Ihnen
B I O C H E M I S C H E S P R A K T I K U M F Ü R S T U D I E R E N D E D E R M E D I Z I N BIOCHEMISCHES INSTITUT DER UNIVERSITÄT ZÜRICH 2003 INHALTSVERZEICHNIS *) Zum Biochemischen Praktikum steht Ihnen
Trainingslehre für Herzpatienten. H. Brito da Silva Physiotherapeutin FH Ambulante kardiale Rehabilitation
 Trainingslehre für Herzpatienten H. Brito da Silva Physiotherapeutin FH Ambulante kardiale Rehabilitation Inhalt Wieso ist Training bei Herzerkrankungen wichtig? Ziele Physiologie: was passiert im Körper?
Trainingslehre für Herzpatienten H. Brito da Silva Physiotherapeutin FH Ambulante kardiale Rehabilitation Inhalt Wieso ist Training bei Herzerkrankungen wichtig? Ziele Physiologie: was passiert im Körper?
Vitamine und Antioxidantien im Sport. Birgit Wild, UMIT
 Vitamine und Antioxidantien im Sport Birgit Wild, UMIT Inhalte Oxidativer Stress Freie Radikale Hormesis, Bewertung von ROS Antioxidantien Antioxidativer Status AO Supplemente im Sport Bedarf, stateoftheart
Vitamine und Antioxidantien im Sport Birgit Wild, UMIT Inhalte Oxidativer Stress Freie Radikale Hormesis, Bewertung von ROS Antioxidantien Antioxidativer Status AO Supplemente im Sport Bedarf, stateoftheart
Der Stoffwechsel: Konzepte und Grundmuster
 Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Lipide als Funktionelle Lebensmittel
 'ß -.-:-- Schriftenreihe des Bundesministeriums für Verbraucherschutz, Ernährung und Landwirtschaft Reihe A: Angewandte Wissenschaft Heft 495 Lipide als Funktionelle Lebensmittel Wissenschaftliche Koordination
'ß -.-:-- Schriftenreihe des Bundesministeriums für Verbraucherschutz, Ernährung und Landwirtschaft Reihe A: Angewandte Wissenschaft Heft 495 Lipide als Funktionelle Lebensmittel Wissenschaftliche Koordination
Aspekte der Eisenresorption. PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse Binningen
 Aspekte der Eisenresorption PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse 19 4102 Binningen Chemische Eigenschaften Fe-II wird leichter aufgenommen als Fe-III wegen der besseren
Aspekte der Eisenresorption PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse 19 4102 Binningen Chemische Eigenschaften Fe-II wird leichter aufgenommen als Fe-III wegen der besseren
vom Meldenden Personengruppe, die von der Angabe erfasst werden, eingeschränkt auf
 81 Calcium 82 Calcium 83 Calcium 84 Calcium 85 Calcium 86 Calcium 87 Calcium 88 Calcium 89 Calcium 90 Calcium 91 Calcium 92 Calcium Mineralisierung und Knochendichte/- Calcium ist notwendig für normale
81 Calcium 82 Calcium 83 Calcium 84 Calcium 85 Calcium 86 Calcium 87 Calcium 88 Calcium 89 Calcium 90 Calcium 91 Calcium 92 Calcium Mineralisierung und Knochendichte/- Calcium ist notwendig für normale
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Schritt für Schritt Simulation Die Atmungskette
 KENNZEICHEN: KURS - SCHULE - - Schritt für Schritt Simulation Die Atmungskette Inhalt Übersicht über das Mitochondrium und die Mitochondrienmembran S.2 Zeichenerklärung S.3 Stichwortverzeichnis S.4 Leitfaden
KENNZEICHEN: KURS - SCHULE - - Schritt für Schritt Simulation Die Atmungskette Inhalt Übersicht über das Mitochondrium und die Mitochondrienmembran S.2 Zeichenerklärung S.3 Stichwortverzeichnis S.4 Leitfaden
TRAININGSLEHRE Übungsaufgabe zum Thema Ausdauer
 TRAININGSLEHRE Übungsaufgabe zum Thema Ausdauer AUFGABE Der äthiopische Wunderläufer Haile Gebrselassie, der 1989 im Alter von 16 Jahren als weitgehend unbekannter Athlet sowohl über 5000 Meter als auch
TRAININGSLEHRE Übungsaufgabe zum Thema Ausdauer AUFGABE Der äthiopische Wunderläufer Haile Gebrselassie, der 1989 im Alter von 16 Jahren als weitgehend unbekannter Athlet sowohl über 5000 Meter als auch
Von Nadine Ufermann und Marcus Oldekamp
 Von Nadine Ufermann und Marcus Oldekamp Photosynthese: Allgemein und Lichtreaktion Photosysteme: PSI und PSII, Entdeckung und Funktion Mangan und Manganenzyme: Speziell sauerstoffentwickelnder Mn Cluster
Von Nadine Ufermann und Marcus Oldekamp Photosynthese: Allgemein und Lichtreaktion Photosysteme: PSI und PSII, Entdeckung und Funktion Mangan und Manganenzyme: Speziell sauerstoffentwickelnder Mn Cluster
BIOCHEMIE. Teil 2: Aminosäuren, Proteine, Enzyme. Urheberrechtlich geschütztes Material. Lernkarteikarten Veterinärmedizin - BIOCHEMIE
 Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
2. Oxidativer Stress & Ernährung
 2.1 Vitamine & Antioxidantien 2.2 Spurenelemente und Enzyme OXIDATIVER STRESS & ERNÄHRUNG Ernährung : Vitamine und Carotinoide, Fettlösl. Antioxidantien Vitamine &AntioxidantienZVIT Röhrchen mit Trenngel
2.1 Vitamine & Antioxidantien 2.2 Spurenelemente und Enzyme OXIDATIVER STRESS & ERNÄHRUNG Ernährung : Vitamine und Carotinoide, Fettlösl. Antioxidantien Vitamine &AntioxidantienZVIT Röhrchen mit Trenngel
Entstehung und Ursachen einer Übersäuerung
 Entstehung und Ursachen einer Übersäuerung Übersäuerung im Körper normal ph 7,4 (Normbereich ph 7,35 7,45) übersäuert ph 7,35-7,40 (Normbereich zum Sauren verschoben) Verminderte Pufferkapazität im Blut
Entstehung und Ursachen einer Übersäuerung Übersäuerung im Körper normal ph 7,4 (Normbereich ph 7,35 7,45) übersäuert ph 7,35-7,40 (Normbereich zum Sauren verschoben) Verminderte Pufferkapazität im Blut
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Untersuchung des Einflusses von Laktat auf die maximale Sprintleistung mit Hilfe eines modifizierten Feldstufentests
 Sport Jonathan Januschke Untersuchung des Einflusses von Laktat auf die maximale Sprintleistung mit Hilfe eines modifizierten Feldstufentests Diplomarbeit Diplomarbeit im Diplomstudiengang Sportwissenschaft
Sport Jonathan Januschke Untersuchung des Einflusses von Laktat auf die maximale Sprintleistung mit Hilfe eines modifizierten Feldstufentests Diplomarbeit Diplomarbeit im Diplomstudiengang Sportwissenschaft
Untersuchungen zur Zytokinexpression von Patienten mit fortgeschrittenen gynäkologischen Tumoren und Tumoren im Kopf-Hals-Bereich
 Aus der Universitätsklinik und Poliklinik für Strahlentherapie an der Martin-Luther-Universität Halle-Wittenberg (Komm.Direktorin: Frau PD Dr. med. Gabriele Hänsgen) Untersuchungen zur Zytokinexpression
Aus der Universitätsklinik und Poliklinik für Strahlentherapie an der Martin-Luther-Universität Halle-Wittenberg (Komm.Direktorin: Frau PD Dr. med. Gabriele Hänsgen) Untersuchungen zur Zytokinexpression
M 4a 1: Fragen stellen
 M 4a 1: Fragen stellen Wozu? (Sinn, Zweck) Wo? (Ort) Bei Bewegung entsteht mehr Kohlenstoffdioxid. Wodurch? (Ursache) Wie viel? (Menge) Wie? (Art und Weise) M 4a 2: Je mehr man sich bewegt, desto mehr
M 4a 1: Fragen stellen Wozu? (Sinn, Zweck) Wo? (Ort) Bei Bewegung entsteht mehr Kohlenstoffdioxid. Wodurch? (Ursache) Wie viel? (Menge) Wie? (Art und Weise) M 4a 2: Je mehr man sich bewegt, desto mehr
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Mitochondriale Elektronentransportkette (Atmungskette)
 Mitochondriale Elektronentransportkette (Atmungskette) Mitochondriale Elektronentransportkette (Atmungskette) Komplex I und II übetragen Elektronen auf Coenzym Q (Ubichinon) Gekoppelte Elektronen-Protonen
Mitochondriale Elektronentransportkette (Atmungskette) Mitochondriale Elektronentransportkette (Atmungskette) Komplex I und II übetragen Elektronen auf Coenzym Q (Ubichinon) Gekoppelte Elektronen-Protonen
TRAININGSLEHRE. IMSB-Austria 1
 TRAININGSLEHRE KONDITION TECHNIK ERNÄHRUNG KONSTITUTION PSYCHE TAKTIK IMSB-Austria 1 TRAININGSLEHRE AUSDAUER KRAFT BEWEGLICHKEIT SCHNELLIGKEIT IMSB-Austria 2 TRAININGSLEHRE KOORDINATION IMSB-Austria 3
TRAININGSLEHRE KONDITION TECHNIK ERNÄHRUNG KONSTITUTION PSYCHE TAKTIK IMSB-Austria 1 TRAININGSLEHRE AUSDAUER KRAFT BEWEGLICHKEIT SCHNELLIGKEIT IMSB-Austria 2 TRAININGSLEHRE KOORDINATION IMSB-Austria 3
1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P)
 1. Klausur zum Modul 5.3 Biochemie WS 09/10 12.2.2010 1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P) 2) Welche Funktion
1. Klausur zum Modul 5.3 Biochemie WS 09/10 12.2.2010 1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P) 2) Welche Funktion
PURE 365 Sport. Verbesserte Leistung - Schnellere Regeneration
 PURE 365 Sport Verbesserte Leistung - Schnellere Regeneration Reinsubstanzen mit optimaler Bioverfügbarkeit pure encapsulations steht für hochwertige Reinsubstanzen frei von versteckten Zusatzstoffen.
PURE 365 Sport Verbesserte Leistung - Schnellere Regeneration Reinsubstanzen mit optimaler Bioverfügbarkeit pure encapsulations steht für hochwertige Reinsubstanzen frei von versteckten Zusatzstoffen.
1.2 Freie Radikale - Antioxidantien
 12 1.2 Freie Radikale - Antioxidantien Mechanismen, die die Unterbrechung der zellulären Homeostase durch reaktive Stickstoffund Sauerstoffspezies verhindern, werden allgemein unter dem Begriff antioxidative
12 1.2 Freie Radikale - Antioxidantien Mechanismen, die die Unterbrechung der zellulären Homeostase durch reaktive Stickstoffund Sauerstoffspezies verhindern, werden allgemein unter dem Begriff antioxidative
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Wissenschaftlicher Informationsdienst Tee
 Herbst 2001 Wissenschaftlicher Informationsdienst Tee Oxidativer Stress durch Sport Können Antioxidantien aus Tee dem oxidativen Stress entgegenwirken? Prof. Dr. Aloys. Berg 1, Dr. Marco Netsch 2, Dr.
Herbst 2001 Wissenschaftlicher Informationsdienst Tee Oxidativer Stress durch Sport Können Antioxidantien aus Tee dem oxidativen Stress entgegenwirken? Prof. Dr. Aloys. Berg 1, Dr. Marco Netsch 2, Dr.
Primärstoffwechsel. Prof. Dr. Albert Duschl
 Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Oxidativer Stress Monitoring der oxidativen Belastung
 Oxidativer Stress Monitoring der oxidativen Belastung WOLF D. KUHLMANN Radioonkologie, Klinische Kooperationseinheit Strahlentherapie DKFZ Heidelberg Im Neuenheimer Feld 280, D-69120 Heidelberg Ein personenbezogenes
Oxidativer Stress Monitoring der oxidativen Belastung WOLF D. KUHLMANN Radioonkologie, Klinische Kooperationseinheit Strahlentherapie DKFZ Heidelberg Im Neuenheimer Feld 280, D-69120 Heidelberg Ein personenbezogenes
