Label und Off-Label Use von Medikamenten bei Kindern und Jugendlichen in Österreich
|
|
|
- Ingeborg Winter
- vor 6 Jahren
- Abrufe
Transkript
1 Label und Off-Label Use von Medikamenten bei Kindern und Jugendlichen in Österreich AGES Gespräch Dr. Doris Tschabitscher AGES PharmMed, National Contact Point Paediatrics Erkenntnis Kinder sind keine kleinen Erwachsenen und Jugendliche sind keine großen Kinder 3 1
2 Beispiele Quelle: Prof. Dr. John N. van den Anker 4 Mangel an Information Über 80% aller zugelassenen Medikamente geben an entweder für Kinder nicht geeignet zu sein oder es fehlen genaue Dosierungsanleitungen für Kinder Nur 20-30% der von der FDA geprüften Medikamente sind für Kinder zugelassen Nur bei 38% der neu entwickelten und möglicherweise auch für Kinder hilfreichen Medikamente wird eine Zulassung auch für Kinder beantragt FDA statistics 5 Mangel an Information Daraus resultiert der weit verbreitete off-label use in der Pädiatrie Inzidenz: Ordinationen 16-42%, KH 25-46%, NICU 58-75% und Mehr Nebenwirkungen bei off-label use: KH: 3,9% bei Zulassung, 6% bei off-label (p 0,01) Ordination: Relatives Risiko 3,44 (1,6-12,25) Nelson R.M Legislation on Paediatric Drug Evaluation in USA 6 2
3 Situation in Europa Survey of unlicensed and off label drug use in paediatric wards in European countries Conroy S et al; BMJ 2000;320; Prospective study of drugs administered to children in general paediatric wards over 4 weeks in 5 hospitals (UK, Schweden, Deutschland, Italien, Holland) Verschreibungen für 624 Kinder VO (46%) unlicensed (164) oder offlabel (872) Kinder (67%) erhielten unlicensed oder off label ASP 7 Situation in Europa Unlicensed and off label drug use by children in the community: cross sectional study Schirm E et al; BMJ 2002;324; VO für Kinder (0-16a) im Jahr 2000 (Daten von holländischen Apotheken) VO für Kinder (16,6%) unlicensed (22,7%) off label 8 Off-label use Erkenntnisgewinn Der off- label use in seiner nicht systematischen Form ist gegenwärtig eine Veranstaltung zur Vernichtung medizinischer Erkenntnisse. R. Francke et. al: Die Sozialgerichtsbarkeit
4 Gesetzliche Basis Verordnung (EG) Nr. 1901/2006 des Europäischen Parlaments und des Rates vom über Kinderarzneimittel Artikel 42: Die Mitgliedsstaaten tragen die verfügbaren Daten über alle derzeitigen Verwendungen von Arzneimitteln in der pädiatrischen Bevölkerungsgruppe zusammen und übermitteln sie der Agentur bis zum 26. Jänner Erhebung aller verfügbaren Daten (label und off-label use) von Medikamenten, die Kindern und Jugendlichen in Österreich verabreicht werden 11 Erhebung und Evaluierung des Arzneimitteleinsatzes aus dem 1. extramuralen Bereich: Rezeptpflichtige, erstattungsfähige ASP Ausgewählte rezeptpflichtige, nicht erstattungsfähige ASP ausgewählte OTCs 12 4
5 2. intramuralen Bereich: inklusive KH-Apothekeneigene ASP Magistrale Zubereitungen Offizinale Zubereitungen 13 Zusammenführung dieser Ergebnisse mit den Daten über Arzneimittel mit zugelassenen Indikationen und/oder mit Dosierungen für Kinder und Jugendliche 14 Übermittlung des zusammenfassenden Ergebnisberichts (Endbericht) an die European Medicines Agency, EMEA (Art. 42 der Regulation (EC) 1901/2006) Einreichung der Ergebnisse des Endberichts bei einem wissenschaftlichen Fachmedium zur Veröffentlichung 15 5
6 Datenquellen ad 1: aus dem extramuralen Bereich - Rp-pflichtige und erstattungsfähige ASP HVB ASVG 2 Kassen (GKKs + Betriebskrankenkassen) - Rp-pflichtige und nicht erstattungsfähige ASP Ausgewählte Apotheken - OTCs (ausgewählte) IMS-Health 16 Datenquellen ad 2: aus dem intramuralem Bereich - Spitalsapotheken von fünf Krankenhäusern mit großen Kinderabteilungen (AKH Wien, KH St. Pölten, Uni-Klinik Innsbruck, LKH Salzburg, KH Schwaz, KH Lienz) 17 Datenquellen ad 3: Daten, welche ASP für Kinder zugelassen sind bzw. Dosierungsanleitungen für Kinder haben - Zulassungsinhaber 18 6
7 Projektorganisation Projektsteuerungsgruppe Projektleitung Qualitätsmanagement Projektteam Teambesprechungen: Start und bei Bedarf Informationsfluss: Telefon und elektronisch Dokumentenaustausch: Zeitplan: August 2007 Jänner Nutzen des Projekts Eine so weit wie möglich klare Abbildung des realen Medikamentenverbrauchs in der pädiatrischen Bevölkerungsgruppe ist Basis für: Aufdecken der Forschungslücken Arzneimittel, deren Wirksamkeit und Sicherheit in der jeweilige Altersgruppe durch Zulassungsstudien belegt sind 20 Nutzen des Projekts 21 7
AMNOG-Fachtagung des G-BA Besondere Therapiesituationen Bedingte Zulassung, Kinderarzneimittel und Orphan Drugs
 AMNOG-Fachtagung des G-BA Besondere Therapiesituationen Bedingte Zulassung, Kinderarzneimittel und Orphan Drugs Martin Völkl, Director Market Access & Public Affairs, Celgene GmbH Warum forschen Pharmaunternehmen?
AMNOG-Fachtagung des G-BA Besondere Therapiesituationen Bedingte Zulassung, Kinderarzneimittel und Orphan Drugs Martin Völkl, Director Market Access & Public Affairs, Celgene GmbH Warum forschen Pharmaunternehmen?
Kombinationsprodukte im Kontext der Revision der RL 93/42/EWG. Tamara Bauer
 Kombinationsprodukte im Kontext der Revision der RL 93/42/EWG Tamara Bauer Inhalt Definitionen Richtlinien Kombinationsprodukte 2 Fallbeispiele: Medizinprodukt/Arzneimittel Medizinprodukt/Arzneimittel
Kombinationsprodukte im Kontext der Revision der RL 93/42/EWG Tamara Bauer Inhalt Definitionen Richtlinien Kombinationsprodukte 2 Fallbeispiele: Medizinprodukt/Arzneimittel Medizinprodukt/Arzneimittel
Kinder- und Jugend- Gesundheitsbericht 2010 für die Steiermark
 Kinder- und Jugend- Gesundheitsbericht 2010 für die Steiermark Gesundheitsziel: Rahmenbedingungen für ein gesundes Leben schaffen Bewusstsein im Umgang mit Alkohol in der Steiermark fördern Kapitel 17:
Kinder- und Jugend- Gesundheitsbericht 2010 für die Steiermark Gesundheitsziel: Rahmenbedingungen für ein gesundes Leben schaffen Bewusstsein im Umgang mit Alkohol in der Steiermark fördern Kapitel 17:
 Arzneimittel für Kinder Stand November 2009 Viele neue Kindermedikamente in Entwicklung In den letzten vier Jahren wurde viel zugunsten einer besser ausgestatteten Kinderapotheke bewegt. Forschende Pharma-Unternehmen
Arzneimittel für Kinder Stand November 2009 Viele neue Kindermedikamente in Entwicklung In den letzten vier Jahren wurde viel zugunsten einer besser ausgestatteten Kinderapotheke bewegt. Forschende Pharma-Unternehmen
Erstellung einer Anleitung zur Anwendung von Arzneimitteln im Off-label Use für die ICH
 Erstellung einer Anleitung zur Anwendung von Arzneimitteln im Off-label Use für die ICH Exposé zur Erstellung einer Dissertation am Lehrstuhl für Drug Regulatory Affairs der Rheinischen Friedrich-Wilhelms-Universität
Erstellung einer Anleitung zur Anwendung von Arzneimitteln im Off-label Use für die ICH Exposé zur Erstellung einer Dissertation am Lehrstuhl für Drug Regulatory Affairs der Rheinischen Friedrich-Wilhelms-Universität
Kinderarzneimittel im deutschen Gesundheitssystem
 Kinderarzneimittel im deutschen Gesundheitssystem Die Initiative Arzneimittel für Kinder ist ein gemeinnütziger Verein, der von Mitgliedern aus der Arzneimittelindustrie, der Apothekerschaft und der Forschung
Kinderarzneimittel im deutschen Gesundheitssystem Die Initiative Arzneimittel für Kinder ist ein gemeinnütziger Verein, der von Mitgliedern aus der Arzneimittelindustrie, der Apothekerschaft und der Forschung
Frühe Nutzenbewertungen nach AMNOG: Einblicke in die aktuellen Verfahren und mögliche Auswirkungen für Ärzte und Patienten
 Frühe Nutzenbewertungen nach AMNOG: Einblicke in die aktuellen Verfahren und mögliche Auswirkungen für Ärzte und Patienten Arzneimittelmarktneuordnungsgesetz (AMNOG) 35a Bewertung des Nutzens von Arzneimitteln
Frühe Nutzenbewertungen nach AMNOG: Einblicke in die aktuellen Verfahren und mögliche Auswirkungen für Ärzte und Patienten Arzneimittelmarktneuordnungsgesetz (AMNOG) 35a Bewertung des Nutzens von Arzneimitteln
Kinder mit seltenen Erkrankungen in klinischen Prüfungen-was gibt es aus ärztlicher Sicht zu beachten
 Kinder mit seltenen Erkrankungen in klinischen Prüfungen-was gibt es aus ärztlicher Sicht zu beachten Dr. med. Christina Lampe Zentrum für seltene Erkrankungen Helios Horst Schmidt Kliniken, (HSK) Wiesbaden,
Kinder mit seltenen Erkrankungen in klinischen Prüfungen-was gibt es aus ärztlicher Sicht zu beachten Dr. med. Christina Lampe Zentrum für seltene Erkrankungen Helios Horst Schmidt Kliniken, (HSK) Wiesbaden,
Medizinische Versorgung im Kinder- und Jugendalter: Problematik der Kinderarzneimittel
 Medizinische Versorgung im Kinder- und Jugendalter: Problematik der Kinderarzneimittel Univ. Doz. Dr. Ruth Ladenstein, MBA, cpm Leitung des Koordinierungszentrums für Klinische Studien (S²IRP) St. Anna
Medizinische Versorgung im Kinder- und Jugendalter: Problematik der Kinderarzneimittel Univ. Doz. Dr. Ruth Ladenstein, MBA, cpm Leitung des Koordinierungszentrums für Klinische Studien (S²IRP) St. Anna
Der Erhalt der Kinder-Grundversorgung in Europa muss eine Herausforderung der Zukunft sein
 Der Erhalt der Kinder-Grundversorgung in Europa muss eine Herausforderung der Zukunft sein Elke Jäger-Roman, ECPCP European Confederation of Primary Care Paediatricians In Europa gibt es derzeit: 91 Mill
Der Erhalt der Kinder-Grundversorgung in Europa muss eine Herausforderung der Zukunft sein Elke Jäger-Roman, ECPCP European Confederation of Primary Care Paediatricians In Europa gibt es derzeit: 91 Mill
KAI EDV. Titelmasterformat durch Klicken bearbeiten. Arzneimittelversorgung an dem Universitätsklinikum Jena mit RFID-Lösung
 Titelmasterformat durch Klicken bearbeiten KAI EDV Textmasterformate durch Klicken bearbeiten Zweite Ebene Dritte Ebene Vierte Ebene Fünfte Ebene Martin Specht Arzneimittelversorgung an dem Universitätsklinikum
Titelmasterformat durch Klicken bearbeiten KAI EDV Textmasterformate durch Klicken bearbeiten Zweite Ebene Dritte Ebene Vierte Ebene Fünfte Ebene Martin Specht Arzneimittelversorgung an dem Universitätsklinikum
Off label use Umgang in der Klinik
 Off label use Umgang in der Klinik Markus Thalheimer Leiter Medizincontrolling Universitätsklinikum Heidelberg 1 Agenda Definition und Themeneingrenzung Rahmenbedingungen im Krankenhaus Praktisches Vorgehen
Off label use Umgang in der Klinik Markus Thalheimer Leiter Medizincontrolling Universitätsklinikum Heidelberg 1 Agenda Definition und Themeneingrenzung Rahmenbedingungen im Krankenhaus Praktisches Vorgehen
Wirksame und sichere Arzneimittelbehandlung: Gesundheit für unsere Kinder
 Wirksame und sichere Arzneimittelbehandlung: Gesundheit für unsere Kinder Prof. Dr. Fred Zepp, PAED-Net Direktor des Zentrums für Kinder- und Jugendmedizin, 16 Millionen Kinder und Jugendliche unter 18
Wirksame und sichere Arzneimittelbehandlung: Gesundheit für unsere Kinder Prof. Dr. Fred Zepp, PAED-Net Direktor des Zentrums für Kinder- und Jugendmedizin, 16 Millionen Kinder und Jugendliche unter 18
Arzneimittelfälschungen
 39. Gesundheitspolitisches Forum Arzneimittelfälschungen Realitäten zwischen illegalen Machenschaften und hoch regulierter Vertriebskette Sichere Arzneimittel Die österreichischen Apotheken 1300 Apotheken
39. Gesundheitspolitisches Forum Arzneimittelfälschungen Realitäten zwischen illegalen Machenschaften und hoch regulierter Vertriebskette Sichere Arzneimittel Die österreichischen Apotheken 1300 Apotheken
Problematik des off-label use von Medikamenten für Kinder - was darf ich verordnen, wo liegen die Probleme?
 Problematik des off-label use von Medikamenten für Kinder - was darf ich verordnen, wo liegen die Probleme? IQN Fortbildungsveranstaltung für niedergelassene und Krankenhausärzte Düsseldorf am 13. Mai
Problematik des off-label use von Medikamenten für Kinder - was darf ich verordnen, wo liegen die Probleme? IQN Fortbildungsveranstaltung für niedergelassene und Krankenhausärzte Düsseldorf am 13. Mai
Helicobacter pylori. Arbeitsgruppenleiter: Assoc.Prof. Dr. Christoph Steininger
 Helicobacter pylori Erstellt durch Univ. Prof. Dr. Christoph Högenauer, Assoc.Prof. Dr. Christoph Steininger, Prof. Dr. Michael Gschwantler am 22.02.2014 Arbeitsgruppenleiter: Assoc.Prof. Dr. Christoph
Helicobacter pylori Erstellt durch Univ. Prof. Dr. Christoph Högenauer, Assoc.Prof. Dr. Christoph Steininger, Prof. Dr. Michael Gschwantler am 22.02.2014 Arbeitsgruppenleiter: Assoc.Prof. Dr. Christoph
Die frühe Nutzenbewertung und ihre rechtlichen Herausforderungen
 und ihre rechtlichen Herausforderungen Rechtssymposium Die frühe Nutzenbewertung von Arzneimitteln nach AMNOG G-BA, Berlin Referent: Dr. jur. Rainer Hess, G-BA Seite 1 16. November 2010 Rechtssymposium
und ihre rechtlichen Herausforderungen Rechtssymposium Die frühe Nutzenbewertung von Arzneimitteln nach AMNOG G-BA, Berlin Referent: Dr. jur. Rainer Hess, G-BA Seite 1 16. November 2010 Rechtssymposium
BAnz AT B1. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Engagiert Erfahren Erfolgreich. Umfrage Kinderarzneimittel
 Engagiert Erfahren Erfolgreich Umfrage Kinderarzneimittel 1 Methode Feldzeit: 23.02. 26.02.2015 Methodik: Die Untersuchung basiert auf computerunterstützten Telefoninterviews ("computerassistiertes Telefon-Interview"
Engagiert Erfahren Erfolgreich Umfrage Kinderarzneimittel 1 Methode Feldzeit: 23.02. 26.02.2015 Methodik: Die Untersuchung basiert auf computerunterstützten Telefoninterviews ("computerassistiertes Telefon-Interview"
Einleitung und Leseanweisung
 VII Einleitung und Leseanweisung Für wen ist dieses Buch? Der Pocket Guide ist für alle klinisch tätigen Psychiater geschrieben, denen das Kompendium der Psychiatrischen Pharmakotherapie für die Kitteltasche
VII Einleitung und Leseanweisung Für wen ist dieses Buch? Der Pocket Guide ist für alle klinisch tätigen Psychiater geschrieben, denen das Kompendium der Psychiatrischen Pharmakotherapie für die Kitteltasche
Perjeta für die neoadjuvante Therapie zugelassen
 HER2-positives Mammakarzinom Perjeta für die neoadjuvante Therapie zugelassen Grenzach-Wyhlen (31. Juli 2015) - Die Europäische Arzneimittel-Agentur (EMA) hat Perjeta (Pertuzumab) in Kombination mit Herceptin
HER2-positives Mammakarzinom Perjeta für die neoadjuvante Therapie zugelassen Grenzach-Wyhlen (31. Juli 2015) - Die Europäische Arzneimittel-Agentur (EMA) hat Perjeta (Pertuzumab) in Kombination mit Herceptin
Europäische Verfahren
 Europäische Verfahren Zur Zeit existieren 3 verschieden Zulassungsverfahren in der EU: Verfahren der gegenseitigen Anerkennung (MRP) dezentrales Verfahren (DCP) zentrales Verfahren Alle Biotech Produkte
Europäische Verfahren Zur Zeit existieren 3 verschieden Zulassungsverfahren in der EU: Verfahren der gegenseitigen Anerkennung (MRP) dezentrales Verfahren (DCP) zentrales Verfahren Alle Biotech Produkte
077582/EU XXIV. GP. Eingelangt am 29/03/12 RAT DER EUROPÄISCHEN UNION. Brüssel, den 28. März 2012 (29.03) (OR. fr) 8286/12 AGRILEG 48 ENV 250
 077582/EU XXIV. GP Eingelangt am 29/03/12 RAT DER EUROPÄISCHEN UNION Brüssel, den 28. März 2012 (29.03) (OR. fr) 8286/12 AGRILEG 48 ENV 250 ÜBERMITTLUNGSVERMERK Absender: Europäische Kommission Eingangsdatum:
077582/EU XXIV. GP Eingelangt am 29/03/12 RAT DER EUROPÄISCHEN UNION Brüssel, den 28. März 2012 (29.03) (OR. fr) 8286/12 AGRILEG 48 ENV 250 ÜBERMITTLUNGSVERMERK Absender: Europäische Kommission Eingangsdatum:
BAnz AT B5. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Orphan Drugs. Arzneimitteltherapie seltener Krankheiten
 Orphan Drugs Arzneimitteltherapie seltener Krankheiten Seltene Krankheiten 30 Millionen Europäer, davon etwa 4 Millionen Deutsche, leiden an seltenen Krankheiten. Als selten gilt hier eine Krankheit, wenn
Orphan Drugs Arzneimitteltherapie seltener Krankheiten Seltene Krankheiten 30 Millionen Europäer, davon etwa 4 Millionen Deutsche, leiden an seltenen Krankheiten. Als selten gilt hier eine Krankheit, wenn
Patientenübergabe vom Rettungsdienst an die Ambulanz
 Patientenübergabe vom Rettungsdienst an die Ambulanz P R O J E K TG R U P P E : - M a g. D r. G a b r i e l e P o l a n e z k y, M S c ( P f l e g e d i r e k t o r i n B K H - S c h w a z ) - D r. p h
Patientenübergabe vom Rettungsdienst an die Ambulanz P R O J E K TG R U P P E : - M a g. D r. G a b r i e l e P o l a n e z k y, M S c ( P f l e g e d i r e k t o r i n B K H - S c h w a z ) - D r. p h
Gesundheitsbezogene Angaben nach der Health-Claims-Verordnung
 Europäische Hochschulschriften / European University Studies / Publications Universitaires Européennes 5482 Gesundheitsbezogene Angaben nach der Health-Claims-Verordnung Zu den Anforderungen an den wissenschaftlichen
Europäische Hochschulschriften / European University Studies / Publications Universitaires Européennes 5482 Gesundheitsbezogene Angaben nach der Health-Claims-Verordnung Zu den Anforderungen an den wissenschaftlichen
Pressemitteilung der EMEA vom in deutscher Übersetzung:
 Pressemitteilung der EMEA vom 9. 12. 2004 in deutscher Übersetzung: Außerordentliche Sitzung des CHMP zu Paroxetin und anderen selektiven Serotonin-Wiederaufnahmehemmern Der Ausschuss für Humanarzneimittel
Pressemitteilung der EMEA vom 9. 12. 2004 in deutscher Übersetzung: Außerordentliche Sitzung des CHMP zu Paroxetin und anderen selektiven Serotonin-Wiederaufnahmehemmern Der Ausschuss für Humanarzneimittel
Anlage 1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 Anlage 1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER (Name/Phantasiebezeichnung des Arzneimittels Stärke Darreichungsform) 1 (Wirkstoff(e)) 1 Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Anlage 1 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER (Name/Phantasiebezeichnung des Arzneimittels Stärke Darreichungsform) 1 (Wirkstoff(e)) 1 Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
GKV-Modernisierungsgesetz (GMG)
 GKV-Modernisierungsgesetz (GMG) erste Auswirkungen auf den GKV-Arzneimittelmarkt BPI-Pressekonferenz 8. März 2004, Berlin Dagmar Wald-Eßer, IMS HEALTH Überblick Gesundheitspolitische Maßnahmen im Rahmen
GKV-Modernisierungsgesetz (GMG) erste Auswirkungen auf den GKV-Arzneimittelmarkt BPI-Pressekonferenz 8. März 2004, Berlin Dagmar Wald-Eßer, IMS HEALTH Überblick Gesundheitspolitische Maßnahmen im Rahmen
BAnz AT B5. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG)
 Gesetzliche Regelungen für Arzneimittel Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG) 1 Zweck des Gesetzes Es ist der Zweck dieses Gesetzes, im Interesse einer ordnungsgemäßen Arzneimittelversorgung
Gesetzliche Regelungen für Arzneimittel Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG) 1 Zweck des Gesetzes Es ist der Zweck dieses Gesetzes, im Interesse einer ordnungsgemäßen Arzneimittelversorgung
Nationales Cluster für Medizintechnik Medical Valley EMN Gesundheitswirtschaft und Medizintechnik
 Nationales Cluster für Medizintechnik Medical Valley EMN Gesundheitswirtschaft und Medizintechnik Einsatz von CardioMEMS - Abschätzung der Einsparpotentiale im deutschen GKV-System 180 MedTech Unternehmen
Nationales Cluster für Medizintechnik Medical Valley EMN Gesundheitswirtschaft und Medizintechnik Einsatz von CardioMEMS - Abschätzung der Einsparpotentiale im deutschen GKV-System 180 MedTech Unternehmen
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic )
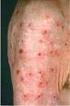 Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
10 Superlativ Begriffe Google s news search. Artikel N=94
 Status quo und zukünftige Anforderungen an wissenschaftliche Erkenntnisse zu Wirksamkeit und Sicherheit bei der Zulassung onkologischer Wirkstoffe im Zeitalter der Präzisionsmedizin Wolf-Dieter Ludwig
Status quo und zukünftige Anforderungen an wissenschaftliche Erkenntnisse zu Wirksamkeit und Sicherheit bei der Zulassung onkologischer Wirkstoffe im Zeitalter der Präzisionsmedizin Wolf-Dieter Ludwig
PILLEN, PULVER, SALBEN PHARMAZIE UND PHARMAKOLOGIE Vom Kräutergarten zur Gentechnologie die Geschichte der Arzneimittel
 Arbeitsblätter mit Lösungen zur DVD 14064 PILLEN, PULVER, SALBEN PHARMAZIE UND PHARMAKOLOGIE Vom Kräutergarten zur Gentechnologie die Geschichte der Arzneimittel Arbeitsblätter mit Lösungen zur DVD 14064
Arbeitsblätter mit Lösungen zur DVD 14064 PILLEN, PULVER, SALBEN PHARMAZIE UND PHARMAKOLOGIE Vom Kräutergarten zur Gentechnologie die Geschichte der Arzneimittel Arbeitsblätter mit Lösungen zur DVD 14064
Meilenstein in der personalisierten Medizin FDA-Zulassung für Pertuzumab beim HER2-positiven metastasierten Mammakarzinom
 Meilenstein in der personalisierten Medizin FDA-Zulassung für Pertuzumab beim HER2-positiven metastasierten Mammakarzinom Frankfurt am Main (15. Juni 2012) - Die US-amerikanische Arzneimittelzulassungsbehörde
Meilenstein in der personalisierten Medizin FDA-Zulassung für Pertuzumab beim HER2-positiven metastasierten Mammakarzinom Frankfurt am Main (15. Juni 2012) - Die US-amerikanische Arzneimittelzulassungsbehörde
Die EU zum Thema Kräuter
 Die EU zum Thema Kräuter Herbert DORFMANN Mitglied des Europäischen Parlaments AGENDA Die Herausforderungen Nationale Agenturen Europäische Arzneimittelagentur Der Gesetzesrahmen Richtlinie zu pflanzlichen
Die EU zum Thema Kräuter Herbert DORFMANN Mitglied des Europäischen Parlaments AGENDA Die Herausforderungen Nationale Agenturen Europäische Arzneimittelagentur Der Gesetzesrahmen Richtlinie zu pflanzlichen
Integration der gesetzlich authorisierten Arzneimittelinformation in rechnergestützte klinische Arbeitsplatzsysteme
 Integration der gesetzlich authorisierten Arzneimittelinformation in rechnergestützte klinische Arbeitsplatzsysteme unter Verwendung der ICD und der Alpha-ID Manfred Criegee-Rieck Ein paar Zahlen: Blick
Integration der gesetzlich authorisierten Arzneimittelinformation in rechnergestützte klinische Arbeitsplatzsysteme unter Verwendung der ICD und der Alpha-ID Manfred Criegee-Rieck Ein paar Zahlen: Blick
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Auswirkungen der 12. AMG- Novelle auf wissenschaftsgesteuerte Studien die Sicht eines Klinikers -
 Auswirkungen der 12. AMG- Novelle auf wissenschaftsgesteuerte Studien die Sicht eines Klinikers - Priv.-Doz. Dr. A. Erhardt Klinik für Gastroenterologie, Hepatologie und Infektiologie Heinrich-Heine-Universität
Auswirkungen der 12. AMG- Novelle auf wissenschaftsgesteuerte Studien die Sicht eines Klinikers - Priv.-Doz. Dr. A. Erhardt Klinik für Gastroenterologie, Hepatologie und Infektiologie Heinrich-Heine-Universität
Arzneimittelforschung für Kinder: Versorgungssituation in der Pädiatrischen Onkologie. A. Eggert Westdeutsches Tumorzentrum
 Arzneimittelforschung für Kinder: Versorgungssituation in der Pädiatrischen Onkologie A. Eggert Westdeutsches Tumorzentrum Arzneimittelforschung in der Versorgung krebskranker Kinder: Problemfelder Off-Label
Arzneimittelforschung für Kinder: Versorgungssituation in der Pädiatrischen Onkologie A. Eggert Westdeutsches Tumorzentrum Arzneimittelforschung in der Versorgung krebskranker Kinder: Problemfelder Off-Label
Einstufung von Änderungen
 Einstufung von Änderungen Mag. Caroline Kleber AGES MEA, Wien AGES-Gespräch, 24. Juni 2014 Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Aufbau und Zusammenhänge Variation Regulation
Einstufung von Änderungen Mag. Caroline Kleber AGES MEA, Wien AGES-Gespräch, 24. Juni 2014 Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Aufbau und Zusammenhänge Variation Regulation
Standardarbeitsanweisung (SOP) zur (Nicht)Einstufung von Studienvorhaben als klinische Prüfung nach AMG
 Standardarbeitsanweisung (SOP) zur (Nicht)Einstufung von Studienvorhaben als klinische Prüfung nach AMG Die folgende SOP basiert auf dem EU-Guidance Dokument vom März 2010 mit seinem Decision Tree (siehe
Standardarbeitsanweisung (SOP) zur (Nicht)Einstufung von Studienvorhaben als klinische Prüfung nach AMG Die folgende SOP basiert auf dem EU-Guidance Dokument vom März 2010 mit seinem Decision Tree (siehe
Die Delegationen erhalten in der Anlage das Kommissionsdokument - D007617/03.
 RAT R EUROPÄISCHEN UNION Brüssel, den 14. Januar 2010 (15.01) (OR. en) 5349/10 NLEG 5 ÜBERMITTLUNGSVERMERK Absender: Europäische Kommission Eingangsdatum: 8. Januar 2010 Empfänger: Generalsekretariat des
RAT R EUROPÄISCHEN UNION Brüssel, den 14. Januar 2010 (15.01) (OR. en) 5349/10 NLEG 5 ÜBERMITTLUNGSVERMERK Absender: Europäische Kommission Eingangsdatum: 8. Januar 2010 Empfänger: Generalsekretariat des
Hohe Variabilität von Diabeteskurven im Krankenhaus
 3. Grazer Risikotag, 30. September 2015 Hohe Variabilität von Diabeteskurven im Krankenhaus Julia Kopanz, BSc 1, Katharina M. Neubauer, BSc, MSc 1, Gerald Sendlhofer, PHD 2,3, Barbara Semlitsch, MSc 1,
3. Grazer Risikotag, 30. September 2015 Hohe Variabilität von Diabeteskurven im Krankenhaus Julia Kopanz, BSc 1, Katharina M. Neubauer, BSc, MSc 1, Gerald Sendlhofer, PHD 2,3, Barbara Semlitsch, MSc 1,
Praxisbeispiel Wirkungsorientierung in der AGES
 Praxisbeispiel Wirkungsorientierung in der AGES Mag. Wolfgang Hermann Geschäftsführer Wirkungsorientierte Steuerung und Wirkungserfassung in der öffentlichen Verwaltung Berlin, 23. Januar 2015 Österreichische
Praxisbeispiel Wirkungsorientierung in der AGES Mag. Wolfgang Hermann Geschäftsführer Wirkungsorientierte Steuerung und Wirkungserfassung in der öffentlichen Verwaltung Berlin, 23. Januar 2015 Österreichische
Reinhard Busse, Prof. Dr. med. MPH
 Reinhard Busse, Prof. Dr. med. MPH FG Management im Gesundheitswesen, Technische Universität Berlin (WHO Collaborating Centre for Health Systems Research and Management) & European Observatory on Health
Reinhard Busse, Prof. Dr. med. MPH FG Management im Gesundheitswesen, Technische Universität Berlin (WHO Collaborating Centre for Health Systems Research and Management) & European Observatory on Health
IQWiG Herbstsymposium / Unterschied zwischen Risiko-Nutzenabwägung (nach AMG) und Nutzen-Schadenabwägung (nach SGB V)
 IQWiG Herbstsymposium 19.11./20.11.2010 Unterschied zwischen Risiko-Nutzenabwägung (nach AMG) und Nutzen-Schadenabwägung (nach SGB V) Referent: Maximilian Grüne, Justiziar Gemeinsamer Bundesausschuss Seite
IQWiG Herbstsymposium 19.11./20.11.2010 Unterschied zwischen Risiko-Nutzenabwägung (nach AMG) und Nutzen-Schadenabwägung (nach SGB V) Referent: Maximilian Grüne, Justiziar Gemeinsamer Bundesausschuss Seite
Arzneimitteltherapiesicherheit in der Kindermedizin
 Arzneimitteltherapiesicherheit in der Kindermedizin 4. ATMS-Expertenworkshop in Erlangen 9./10.11.2012 W. Rascher, A. Neubert Kinder- und Jugendklinik Medikamentöse Therapie als Hochrisikoprozess Besonderheiten
Arzneimitteltherapiesicherheit in der Kindermedizin 4. ATMS-Expertenworkshop in Erlangen 9./10.11.2012 W. Rascher, A. Neubert Kinder- und Jugendklinik Medikamentöse Therapie als Hochrisikoprozess Besonderheiten
Klinische Studien mit Medizinprodukten aus der Sicht des Klinikers
 Klinische Studien mit Medizinprodukten aus der Sicht des Klinikers Prof. Dr. med. Volker A. Coenen Stereotaktische und Funktionelle Neurochirurgie Universitätsklinikum Freiburg volker.coenen@uniklinik-freiburg.de
Klinische Studien mit Medizinprodukten aus der Sicht des Klinikers Prof. Dr. med. Volker A. Coenen Stereotaktische und Funktionelle Neurochirurgie Universitätsklinikum Freiburg volker.coenen@uniklinik-freiburg.de
Stelara ist ein Arzneimittel, das zur Behandlung der folgenden Erkrankungen angewendet wird:
 EMA/636854/2016 EMEA/H/C/000958 Zusammenfassung des EPAR für die Öffentlichkeit Ustekinumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/636854/2016 EMEA/H/C/000958 Zusammenfassung des EPAR für die Öffentlichkeit Ustekinumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
Austrian Energy Agency
 Austrian Energy Agency HARMONAC Workshop: Implementierung von Art. 9 der Gebäuderichtlinie in Österreich Mag. (FH) Christina Spitzbart Austrian Energy Agency 05/02/10 Seite 1 Richtlinie 2002/91/EG des
Austrian Energy Agency HARMONAC Workshop: Implementierung von Art. 9 der Gebäuderichtlinie in Österreich Mag. (FH) Christina Spitzbart Austrian Energy Agency 05/02/10 Seite 1 Richtlinie 2002/91/EG des
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Forderungen der DGHO unter Berücksichtigung der Rolle von Ethik-Kommissionen und des Bundesamts für Strahlenschutz (BfS) bei Klinischen Studien
 Berlin, 17.6.2014: Pressekonferenz: Die neue EU-Verordnung zu klinischen Studien eine Chance für den Forschungsstandort Deutschland Forderungen der DGHO unter Berücksichtigung der Rolle von Ethik-Kommissionen
Berlin, 17.6.2014: Pressekonferenz: Die neue EU-Verordnung zu klinischen Studien eine Chance für den Forschungsstandort Deutschland Forderungen der DGHO unter Berücksichtigung der Rolle von Ethik-Kommissionen
Gemeinsam gegen Arzneimittelfälschungen!
 Gemeinsam gegen Arzneimittelfälschungen! Arzneimittelkauf übers Internet Der Vertrieb illegaler Arzneimittel über das Internet und damit die Gefährdung der öffentlichen Gesundheit wächst laufend. Heute
Gemeinsam gegen Arzneimittelfälschungen! Arzneimittelkauf übers Internet Der Vertrieb illegaler Arzneimittel über das Internet und damit die Gefährdung der öffentlichen Gesundheit wächst laufend. Heute
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um den Wirkstoff Vedolizumab wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen. Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster
 Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster Bayer Werbung um 1900: Heroin, das ideale Sedativum
Die neue Rolle von Kindern im Arzneimittelrecht und ihre praktischen Konsequenzen Was hat mein Kind von der EU? Prof. Dr. med. Joachim Boos, Münster Bayer Werbung um 1900: Heroin, das ideale Sedativum
BAnz AT B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
BAnz AT B1. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Prevenar 13 für Erwachsene von 18 bis 49 Jahren
 Pneumokokken-Schutz jetzt für alle Altersgruppen Europäische Kommission erteilt Zulassung für Prevenar 13 für Erwachsene von 18 bis 49 Jahren Berlin (17. Juli 2013) - Pfizer hat für den 13-valenten Pneumokokken-Konjugatimpfstoff
Pneumokokken-Schutz jetzt für alle Altersgruppen Europäische Kommission erteilt Zulassung für Prevenar 13 für Erwachsene von 18 bis 49 Jahren Berlin (17. Juli 2013) - Pfizer hat für den 13-valenten Pneumokokken-Konjugatimpfstoff
Rechtliche Grundlagen im Pflanzenschutz / Zulassungen von PS-Mitteln. Ute Lachermeier - 12.Juni
 Rechtliche Grundlagen im Pflanzenschutz / Zulassungen von PS-Mitteln Ute Lachermeier - 12.Juni 2013 1 Rechtliche Grundlagen im Pflanzenschutz / Zulassungen von PS-Mitteln 1. Änderungen im neuen Pflanzenschutzgesetz
Rechtliche Grundlagen im Pflanzenschutz / Zulassungen von PS-Mitteln Ute Lachermeier - 12.Juni 2013 1 Rechtliche Grundlagen im Pflanzenschutz / Zulassungen von PS-Mitteln 1. Änderungen im neuen Pflanzenschutzgesetz
Notfallmedikamente sind Fehldosierungen vermeidbar? Dr. Jost Kaufmann
 Notfallmedikamente sind Fehldosierungen vermeidbar? Dr. Jost Kaufmann Kinderkrankenhaus Amsterdamerstraße, Kliniken der Stadt Köln ggmbh Inzidenz allgemein USA 2005: Schätzung des Institute of Medicine
Notfallmedikamente sind Fehldosierungen vermeidbar? Dr. Jost Kaufmann Kinderkrankenhaus Amsterdamerstraße, Kliniken der Stadt Köln ggmbh Inzidenz allgemein USA 2005: Schätzung des Institute of Medicine
Allgemeines Krankenhaus der Stadt Wien Medizinischer Universitätscampus 1090 Wien, Währinger Gürtel 18-20
 Allgemeines Krankenhaus der Stadt Wien Medizinischer Universitätscampus 1090 Wien, Währinger Gürtel 18-20 An: Dr. Robert Pinter Zollhausstraße 6 7022 Schattendorf Univ. Klinik für Innere Medizin III Klin.
Allgemeines Krankenhaus der Stadt Wien Medizinischer Universitätscampus 1090 Wien, Währinger Gürtel 18-20 An: Dr. Robert Pinter Zollhausstraße 6 7022 Schattendorf Univ. Klinik für Innere Medizin III Klin.
Rat der Europäischen Union Brüssel, den 29. März 2016 (OR. en)
 Rat der Europäischen Union Brüssel, den 29. März 2016 (OR. en) 7374/16 DENLEG 23 AGRI 154 SAN 104 ÜBERMITTLUNGSVERMERK Absender: Europäische Kommission Eingangsdatum: 22. März 2016 Empfänger: Nr. Komm.dok.:
Rat der Europäischen Union Brüssel, den 29. März 2016 (OR. en) 7374/16 DENLEG 23 AGRI 154 SAN 104 ÜBERMITTLUNGSVERMERK Absender: Europäische Kommission Eingangsdatum: 22. März 2016 Empfänger: Nr. Komm.dok.:
Arzneimittel als Proxy für eine Diagnose: Methodisch sinnvoll? - Das Beispiel Asthma
 Arzneimittel als Proxy für eine Diagnose: Methodisch sinnvoll? - Das Beispiel Asthma AGENS-Methodenworkshop am 12. und 13. März 2009 im Universitätsklinikum Magdeburg Dr. Falk Hoffmann, MPH Hintergrund
Arzneimittel als Proxy für eine Diagnose: Methodisch sinnvoll? - Das Beispiel Asthma AGENS-Methodenworkshop am 12. und 13. März 2009 im Universitätsklinikum Magdeburg Dr. Falk Hoffmann, MPH Hintergrund
Abgrenzung aus Sicht der Lebensmittelwirtschaft
 Abgrenzung aus Sicht der Lebensmittelwirtschaft Antje Preußker Wissenschaftliche Leitung BfArM im Dialog: Abgrenzung von Arzneimitteln 19. September 2016 Schwerpunkt Nahrungsergänzungsmittel steht für
Abgrenzung aus Sicht der Lebensmittelwirtschaft Antje Preußker Wissenschaftliche Leitung BfArM im Dialog: Abgrenzung von Arzneimitteln 19. September 2016 Schwerpunkt Nahrungsergänzungsmittel steht für
Wie wird grenzüberschreitende Gesundheitsversorgung bezahlt?? Brigitte van der Zanden Healthacross, 14 Dezember 2010
 Wie wird grenzüberschreitende Gesundheitsversorgung bezahlt?? Brigitte van der Zanden Healthacross, 14 Dezember 2010 Einleitung Directive Grenzüberschreitende Strömen Wie wird das bezahlt? Herausforderungen
Wie wird grenzüberschreitende Gesundheitsversorgung bezahlt?? Brigitte van der Zanden Healthacross, 14 Dezember 2010 Einleitung Directive Grenzüberschreitende Strömen Wie wird das bezahlt? Herausforderungen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Wirkstoffe: Thymiantrockenextrakt, Eibischwurzelflüssigextrakt
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER BRONCHOSTOP Thymian Eibisch sine Hustensaft Wirkstoffe: Thymiantrockenextrakt, Eibischwurzelflüssigextrakt Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER BRONCHOSTOP Thymian Eibisch sine Hustensaft Wirkstoffe: Thymiantrockenextrakt, Eibischwurzelflüssigextrakt Lesen Sie die gesamte Packungsbeilage sorgfältig
Der Bundesrat hat ferner die aus der Anlage ersichtliche Entschließung gefasst.
 Bundesrat Drucksache 169/14 (Beschluss) 23.05.14 Beschluss des Bundesrates Verordnung zur Umsetzung der Regelungen der Europäischen Union über die Anerkennung von in anderen Mitgliedstaaten ausgestellten
Bundesrat Drucksache 169/14 (Beschluss) 23.05.14 Beschluss des Bundesrates Verordnung zur Umsetzung der Regelungen der Europäischen Union über die Anerkennung von in anderen Mitgliedstaaten ausgestellten
Bank für Tirol und Vorarlberg Aktiengesellschaft
 Bank für Tirol und Vorarlberg Aktiengesellschaft 1. Nachtrag vom 13.01.2010 gemäß Art. 16 der Richtline 2003/71/EG des Europäischen Parlaments und des Rates vom 4. November 2003 und 6 Kapitalmarktgesetz
Bank für Tirol und Vorarlberg Aktiengesellschaft 1. Nachtrag vom 13.01.2010 gemäß Art. 16 der Richtline 2003/71/EG des Europäischen Parlaments und des Rates vom 4. November 2003 und 6 Kapitalmarktgesetz
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien
 Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Datum: Kontakt: Abteilung: Tel. / Fax: Unser Zeichen: Ihr Zeichen:
 BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 25.06.2015 Mag. pharm. Dr. Ulrike Rehberger REGA +43 (0) 505 55 36258 pv-implementation@ages.at
BASG / AGES Institut LCM Traisengasse 5, A-1200 Wien Datum: Kontakt: Abteilung: Tel. / Fax: E-Mail: Unser Zeichen: Ihr Zeichen: 25.06.2015 Mag. pharm. Dr. Ulrike Rehberger REGA +43 (0) 505 55 36258 pv-implementation@ages.at
Risikokommunikation der Behörden Risiken und Nutzen von Arzneimitteln
 Risikokommunikation der Behörden Risiken und Nutzen von Arzneimitteln Marcus Müllner AGES PharmMed / Bundesamt für Sicherheit im Gesundheitswesen 21.11.2011 www.basg.at Österreichische Agentur für Gesundheit
Risikokommunikation der Behörden Risiken und Nutzen von Arzneimitteln Marcus Müllner AGES PharmMed / Bundesamt für Sicherheit im Gesundheitswesen 21.11.2011 www.basg.at Österreichische Agentur für Gesundheit
BMVZ Regionaltreffen Augsburg 19. Oktober 2011
 QM im Krankenhaus-MVZ am Beispiel der Einführung von EPA: Prozesse & Nutzen Regionaltreffen Süd BMVZ, 19.10.2011 Dr. med. Roland Strasheim Organisatorischer Leiter Seite 1 Seite 2 Seite 1 Agenda 3. Ablauf-
QM im Krankenhaus-MVZ am Beispiel der Einführung von EPA: Prozesse & Nutzen Regionaltreffen Süd BMVZ, 19.10.2011 Dr. med. Roland Strasheim Organisatorischer Leiter Seite 1 Seite 2 Seite 1 Agenda 3. Ablauf-
MEDIKAMENTÖSER SCHWANGERSCHAFTSABBRUCH
 Dr. Christiane Tennhardt Berlin - Lichtenberg Internationale Erfahrungen / besondere Risiken? Legale / Abrechnungstechnische Aspekte Akzeptanz der Klientinnen bei BALANCE Praktische Durchführung Zwischenbilanz
Dr. Christiane Tennhardt Berlin - Lichtenberg Internationale Erfahrungen / besondere Risiken? Legale / Abrechnungstechnische Aspekte Akzeptanz der Klientinnen bei BALANCE Praktische Durchführung Zwischenbilanz
Legalisierung von Cannabis Risiko für den Jugendschutz?
 Legalisierung von Cannabis Risiko für den Jugendschutz? Dr. Dr. med. Armin Claus Station zum Qualifizierten Entzug Das Grüne Haus Klinik für Kinder- und Jugendpsychiatrie und Psychotherapie des Kinderkrankenhauses
Legalisierung von Cannabis Risiko für den Jugendschutz? Dr. Dr. med. Armin Claus Station zum Qualifizierten Entzug Das Grüne Haus Klinik für Kinder- und Jugendpsychiatrie und Psychotherapie des Kinderkrankenhauses
FSME-Impfstoffe für Kinder
 Fortbildungsveranstaltung für den Öffentlichen Gesundheitsdienst FSME-Impfstoffe für Kinder Christoph Conrad, Dr. Michael Pfleiderer Paul-Ehrlich-Institut (PEI), Langen 26. März 2003 Fortbildung ÖGD 1
Fortbildungsveranstaltung für den Öffentlichen Gesundheitsdienst FSME-Impfstoffe für Kinder Christoph Conrad, Dr. Michael Pfleiderer Paul-Ehrlich-Institut (PEI), Langen 26. März 2003 Fortbildung ÖGD 1
Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission
 Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission ass. iur. Jan Paus, LL.M. Rechtsreferent Ethik-Kommission der Ärztekammer Westfalen-Lippe und der Medizinischen Fakultät der WWU Münster
Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission ass. iur. Jan Paus, LL.M. Rechtsreferent Ethik-Kommission der Ärztekammer Westfalen-Lippe und der Medizinischen Fakultät der WWU Münster
Dr. Dietmar Ranftler Medizinisches Controlling LKH Klagenfurt
 Dr. Dietmar Ranftler Medizinisches Controlling LKH Klagenfurt 09.01.2014 HOPE-Evaluierungstreffen - Dr. Dietmar Ranftler, LKH Klagenfurt 1 Gastorganisation Gastorganisation: South West Dorset Primary Care
Dr. Dietmar Ranftler Medizinisches Controlling LKH Klagenfurt 09.01.2014 HOPE-Evaluierungstreffen - Dr. Dietmar Ranftler, LKH Klagenfurt 1 Gastorganisation Gastorganisation: South West Dorset Primary Care
AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie
 AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie Dr. Jutta Wendel-Schrief Direktor Market Access MSD SHARP & DOHME GMBH Was sind Innovationen? Neue
AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie Dr. Jutta Wendel-Schrief Direktor Market Access MSD SHARP & DOHME GMBH Was sind Innovationen? Neue
Polypharmazie - Bringt weniger mehr?
 Polypharmazie - Bringt weniger mehr? Seniorenkongress 14. Oktober 2015 Mag.pharm. Caroline Fritsche Polypharmazie: was ist das? die parallele Einnahme mehrerer verschiedener Medikamente sie können sich
Polypharmazie - Bringt weniger mehr? Seniorenkongress 14. Oktober 2015 Mag.pharm. Caroline Fritsche Polypharmazie: was ist das? die parallele Einnahme mehrerer verschiedener Medikamente sie können sich
ONKOLOGIE C. Düsseldorf
 MDS MDK GKV ONKOLOGIE C Düsseldorf Wiesbaden 09. April 2013 Relevanz klinischer Studien für die Versorgung onkologischer Patienten Sicht des MDK Prof. Dr. med. Axel Heyll Kompetenz Centrum Onkologie der
MDS MDK GKV ONKOLOGIE C Düsseldorf Wiesbaden 09. April 2013 Relevanz klinischer Studien für die Versorgung onkologischer Patienten Sicht des MDK Prof. Dr. med. Axel Heyll Kompetenz Centrum Onkologie der
Qualität der geburtshilflichen Versorgung im europäischen Vergleich. Nicholas Lack
 Qualität der geburtshilflichen Versorgung im europäischen Vergleich Nicholas Lack European Perinatal Health Report (EPHR) 2010 Starke Variation in der Versorgung Im Vergleich zu 2004 Daten aus allen Bundesländern
Qualität der geburtshilflichen Versorgung im europäischen Vergleich Nicholas Lack European Perinatal Health Report (EPHR) 2010 Starke Variation in der Versorgung Im Vergleich zu 2004 Daten aus allen Bundesländern
Änderungsvorschläge zum Entwurf der EU Kommission für eine neue Tierarzneimittelverordnung
 München, 1.6.2015 Landwehrstr. 64a 80336 München Telefon: (089) 30 77 49 0 Telefax: (089) 30 77 49 20 www.umweltinstitut.org Änderungsvorschläge zum Entwurf der EU Kommission für eine neue Tierarzneimittelverordnung
München, 1.6.2015 Landwehrstr. 64a 80336 München Telefon: (089) 30 77 49 0 Telefax: (089) 30 77 49 20 www.umweltinstitut.org Änderungsvorschläge zum Entwurf der EU Kommission für eine neue Tierarzneimittelverordnung
Auf dem Weg zu einem evidenzbasierten. auch in der Onkologie
 Auf dem Weg zu einem evidenzbasierten Gesundheitssystem auch in der Onkologie Reinhard Busse, Prof. Dr. med. MPH FFPH FG Management im Gesundheitswesen, Technische Universität Berlin (WHO Collaborating
Auf dem Weg zu einem evidenzbasierten Gesundheitssystem auch in der Onkologie Reinhard Busse, Prof. Dr. med. MPH FFPH FG Management im Gesundheitswesen, Technische Universität Berlin (WHO Collaborating
VERORDNUNG (EU) Nr. 26/2011 DER KOMMISSION vom 14. Januar 2011 zur Zulassung von Vitamin E als Zusatzstoff in Futtermitteln für alle Tierarten
 2011R0026 DE 02.10.2015 001.001 1 Dieses Dokument ist lediglich eine Dokumentationshilfe, für deren Richtigkeit die Organe der Union keine Gewähr übernehmen B VERORDNUNG (EU) Nr. 26/2011 DER KOMMISSION
2011R0026 DE 02.10.2015 001.001 1 Dieses Dokument ist lediglich eine Dokumentationshilfe, für deren Richtigkeit die Organe der Union keine Gewähr übernehmen B VERORDNUNG (EU) Nr. 26/2011 DER KOMMISSION
W. Beindl, Juli Multimedikation und Parkinson - Risiken minimieren, Effizienz erhöhen -
 W. Beindl, Juli 2016 Multimedikation und Parkinson - Risiken minimieren, Effizienz erhöhen - Stationäre Aufnahmen wegen Arzneimittelunfällen Metaanalyse: Howard RL et al.: Brit.J.Clin.Pharmacol.2007 Studie
W. Beindl, Juli 2016 Multimedikation und Parkinson - Risiken minimieren, Effizienz erhöhen - Stationäre Aufnahmen wegen Arzneimittelunfällen Metaanalyse: Howard RL et al.: Brit.J.Clin.Pharmacol.2007 Studie
Homviotensin. Mischung zum Einnehmen
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Homviotensin Mischung zum Einnehmen Wirkstoffe: Cactus Dil. D1, Viscum album Urtinktur, Rauwolfia Dil. D3, Crataegus Urtinktur Lesen Sie bitte die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Homviotensin Mischung zum Einnehmen Wirkstoffe: Cactus Dil. D1, Viscum album Urtinktur, Rauwolfia Dil. D3, Crataegus Urtinktur Lesen Sie bitte die gesamte
RICHTLINIEN DES DEPARTEMENTES FÜR GESUNDHEIT, SOZIALWESEN UND ENERGIE BETREFFEND DIE ARZNEIMITTELVERSORGUNG IN DEN PFLEGEHEIMEN FÜR BETAGTE
 DER VORSTEHER DES DEPARTEMENTES FÜR, GESUNDHEIT, SOZIALWESEN UND ENERGIE RICHTLINIEN DES DEPARTEMENTES FÜR GESUNDHEIT, SOZIALWESEN UND ENERGIE BETREFFEND DIE ARZNEIMITTELVERSORGUNG IN DEN PFLEGEHEIMEN
DER VORSTEHER DES DEPARTEMENTES FÜR, GESUNDHEIT, SOZIALWESEN UND ENERGIE RICHTLINIEN DES DEPARTEMENTES FÜR GESUNDHEIT, SOZIALWESEN UND ENERGIE BETREFFEND DIE ARZNEIMITTELVERSORGUNG IN DEN PFLEGEHEIMEN
in Deutschland und Europa (und ein bisschen in der Welt)
 Zum aktuellen Cannabiskonsum Institut für Therapieforschung München in Deutschland und Europa (und ein bisschen in der Welt) Tim Pfeiffer-Gerschel IFT Institut für Therapieforschung, München Cannabis -
Zum aktuellen Cannabiskonsum Institut für Therapieforschung München in Deutschland und Europa (und ein bisschen in der Welt) Tim Pfeiffer-Gerschel IFT Institut für Therapieforschung, München Cannabis -
Gebrauchsinformation: Information für Patienten. Essentiale forte-kapseln Wirkstoff: Phospholipide aus Sojabohnen
 Gebrauchsinformation: Information für Patienten Essentiale forte-kapseln Wirkstoff: Phospholipide aus Sojabohnen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten Essentiale forte-kapseln Wirkstoff: Phospholipide aus Sojabohnen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Registrierung von Stoffen Gemeinsame Nutzung von Daten und Vermeidung unnötiger Versuche Informationen in der Lieferkette Nachgeschaltete Anwender
 REACH-VERORDNUNG Verordnung (EG) Nr. 1907/2006 des Europäischen Parlaments und des Rates vom 18. Dezember 2006 zur Registrierung, Bewertung, Zulassung und Beschränkung chemischer Stoffe (REACH) Die REACH-Verordnung
REACH-VERORDNUNG Verordnung (EG) Nr. 1907/2006 des Europäischen Parlaments und des Rates vom 18. Dezember 2006 zur Registrierung, Bewertung, Zulassung und Beschränkung chemischer Stoffe (REACH) Die REACH-Verordnung
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um die Wirkstoffkombination Indacaterol/Glycopyrronium wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Als Krebspatient an einer Studie teilnehmen was sollte man wissen?
 Als Krebspatient an einer Studie teilnehmen was sollte man wissen? Krebsinformationsdienst, Heidelberg Dr. Susanne Weg-Remers Seite 2 Grundlage für evidenzbasiertes medizinisches Wissen sind klinische
Als Krebspatient an einer Studie teilnehmen was sollte man wissen? Krebsinformationsdienst, Heidelberg Dr. Susanne Weg-Remers Seite 2 Grundlage für evidenzbasiertes medizinisches Wissen sind klinische
Nutzer und Nutzung von Gesundheitsinformationen im Internet. Nutzer und Nutzung von Gesundheitsinformationen im Internet
 Nutzer und Nutzung von Gesundheitsinformationen im Internet Nutzer und Nutzung von Gesundheitsinformationen im Internet Agenda Abruf von Gesundheitsinformationen in den Medien Informationsbedürfnis von
Nutzer und Nutzung von Gesundheitsinformationen im Internet Nutzer und Nutzung von Gesundheitsinformationen im Internet Agenda Abruf von Gesundheitsinformationen in den Medien Informationsbedürfnis von
Pflanzliche und traditionelle Arzneimittel
 Pflanzliche und traditionelle Arzneimittel Dr. Friederike Stolte BfArM, Bonn Phytopharmaka Vollantrag (klinische Prüfungen und neue Tests) Bibliographischer Antrag (well-established, 10 Jahre) Mixed application
Pflanzliche und traditionelle Arzneimittel Dr. Friederike Stolte BfArM, Bonn Phytopharmaka Vollantrag (klinische Prüfungen und neue Tests) Bibliographischer Antrag (well-established, 10 Jahre) Mixed application
Neues adaptiertes Zulassungsmodell für AT-CMS Verfahren unter Berücksichtigung des Vermarktungswunsches der Firma
 Neues adaptiertes Zulassungsmodell für AT-CMS Verfahren unter Berücksichtigung des Vermarktungswunsches der Firma DI Dr. Christa Wirthumer-Hoche Leiterin Institut Zulassung & Lifecycle Management AGES
Neues adaptiertes Zulassungsmodell für AT-CMS Verfahren unter Berücksichtigung des Vermarktungswunsches der Firma DI Dr. Christa Wirthumer-Hoche Leiterin Institut Zulassung & Lifecycle Management AGES
