Vierte Verordnung zur Änderung der Apothekenbetriebsordnung. Krankenhausapotheken? Dr. Gabriele Wanninger Regierung von Oberbayern
|
|
|
- Karlheinz Biermann
- vor 6 Jahren
- Abrufe
Transkript
1 Vierte Verordnung zur Änderung der Apothekenbetriebsordnung Was ändert sich für f r die Krankenhausapotheken? Dr. Gabriele Wanninger
2 Begriffsbestimmungen 1a (neu) Begriffsbestimmungen Einführung von 17 Begriffsbestimmungen Krankenhausversorgende Apotheke Pharmazeutisches Personal und pharmazeutische Tätigkeit Patientenindividuelles Stellen bzw. Verblistern Ausgangsstoffe und primäre Verpackungsmaterialien Rezeptur- und Defekturarzneimittel Apothekenübliche Waren und Dienstleistungen Inprozesskontrollen Kritische Ausgangsstoffe Kalibrierung, Qualifizierung, Validierung Herstellung im geschlossenen System 2
3 Qualitätsmanagement 2a (neu) Qualitätsmanagementsystem Betreiben eines QMS entsprechend Art und Umfang der pharmazeutischen Tätigkeiten Festlegung der betrieblichen Abläufe (QM-Handbuch) Herstellung, Prüfung und Lagerung der Arzneimittel nach Stand von Wissenschaft und Technik Vermeidung von Verwechslungen Regelmäßige Selbstinspektionen sowie Teilnahme an externen Qualitätsprüfungen Verantwortung des Apothekenleiters für notwendige Maßnahmen 3
4 Hygiene 4a (neu) Hygienemaßnahmen Hygienemaßnahmen zur Sicherstellung der mikrobiologischen Qualität der Arzneimittel Art der Raumreinigung und Frequenz Häufigkeit der Desinfektion, soweit erforderlich Zu verwendende Mittel und Geräte (Was, wann, wo, wie, womit?) Hygieneplan Dokumentation der Hygienemaßnahmen Hygienisches Verhalten und Schutzkleidung 4
5 Wissenschaftliche Hilfsmittel 5 (geändert) Wissenschaftliche und sonstige Hilfsmittel Keine Forderung weiterer Hilfsmittel neben dem Arzneibuch jedoch müssen notwendige Hilfsmittel vorhanden sein Hilfsmittel können auch in elektronischer Form genutzt werden. 5
6 Herstellung und Prüfung 6 Allgemeine Vorschriften über die Herstellung und Prüfung Prüfung der Arzneimittel außerhalb der Apotheke in einem Betrieb mit Erlaubnis nach 13 AMG in einem Betrieb mit Erlaubnis nach Art. 40 der RiLi 2001/83/EG oder Art. 44 der RiLi 2001/82/EG in einer Apotheke mit Betriebserlaubnis durch einen Sachverständigen nach 65 Abs. 4 AMG Prüfzertifikat des externen Betriebs Freigabe in der Apotheke auf Basis des Prüfzertifikats Mindestens Identitätsprüfung + Dokumentation 6
7 Rezeptur 7 Rezepturarzneimittel Abs. 1a c (neu) Herstellungsanweisung Herstellungstechnik und Geräte; Plausibilitätsprüfung; Verpackung und Kennzeichnung, ggf. Inprozesskontrollen; Vorbereitung des Arbeitsplatzes; Freigabe und Dokumentation Plausibilitätsprüfung Dosierung; Applikationsart; Art, Menge, Kompatibilität und Qualität der Ausgangsstoffe; Haltbarkeit der Rezeptur Herstellungsprotokoll Art/Menge der Ausgangsstoffe mit Ch.-B./Prüf-Nr.; Herstellungsparameter; ggf. IPK, Patient/Kunde; verschreibender Arzt/Zahnarzt, Tierarzt; herstellende Person 7
8 Rezeptur 7 Rezepturarzneimittel Abs. 1b Freigabe Organoleptische Prüfung und Freigabe durch einen Apotheker vor der Abgabe an den Patienten Abs. 1c Analytische Prüfung nicht erforderlich, wenn die Qualität des Rezepturarzneimittels gewährleistet ist durch das Herstellungsverfahren, durch die organoleptische Prüfung und ggf. durch die Ergebnisse der Inprozesskontrollen 8
9 Defektur 8 Defekturarzneimittel Herstellungsanweisung Ausgangsstoffe, Packmaterialien und Geräte; Vermeidung von Kontaminationen und Verwechslungen; Arbeitsschritte und IPK; Kennzeichnung (Herstellungsdatum, Verfalldatum, Nachprüfdatum, ggf. Lagerungsbedingungen); Freigabe. Herstellungsprotokoll Herstellungsdatum und Ch.-B.; Art/Menge der Ausgangsstoffe mit Ch.-B./Prüf-Nr.; IPK; Herstellungsparameter; Gesamtausbeute; Verfalldatum oder Nachtestdatum; Name der herstellenden Person. Freigabe durch einen Apotheker 9
10 Defektur 8 Defekturarzneimittel Prüfanweisung Probenahme Prüfmethoden Akzeptanzkriterien Prüfprotokoll Datum der Prüfung Prüfergebnisse Freigabe durch den verantwortlichen Apotheker Von der analytischen Prüfung der Defekturarzneimittel kann nicht mehr abgesehen werden. 10
11 Großherstellung 9, 10 (Großherstellung) werden aufgehoben Herstellung über den Defekturmaßstab (sog. 100-er- Regel) hinaus erfordert Herstellungserlaubnis gem. 13 AMG Es gilt die AMWHV einschl. EU-GMP-Leitfaden Kommentar zum Entwurf der ApBetrO: Dies ergibt sich auch aus der Resolution des Europarates (CM/ResAP (2011)1 on quality and safety assurance requirements for medicinal products prepared in pharmacies for the special needs of patients), die am 19. Januar 2011 in der Sitzung des Ministerkomitees angenommen wurde. 11
12 Ausgangsstoffe 11 Ausgangsstoffe Prüfzertifikat für Wirkstoffe Bestätigung, dass die Wirkstoffe GMP-konform hergestellt worden sind 12
13 Tätigkeiten im Auftrag 11a (neu) Tätigkeiten im Auftrag Anwendungsbereich Patientenindividuelle Herstellung von Arzneimitteln gem. 21 Abs. 2 Nr. 1b AMG Zytostatikazubereitungen für andere Apotheken gem. 11 Abs. 3 ApG Prüfung von in der Apotheke hergestellten Arzneimitteln und Prüfung von Ausgangsstoffen, sofern die Prüfung über die Identitätsprüfung hinausgeht, weil kein Prüfzertifikat vorliegt. 13
14 Tätigkeiten im Auftrag 11a (neu) Tätigkeiten im Auftrag Schriftlicher Vertrag über die Herstellung von Arzneimitteln nach 21 Abs. 2 Nr. 1b (Zytostatikazubereitungen, parenterale Ernährung, besondere Bedarfsarzneimittel, Verblisterung) aus zugelassenen Fertigarzneimitteln über die Herstellung von Arzneimitteln nach 11 Abs. 3 ApG (Zytostatikazubereitungen für andere Apotheken) und 11 Abs. 4 ApG (Arzneimittel für den Pandemiefall) Beauftragung erst nach Vorliegen der Verschreibung die Qualität des Arzneimittels verantwortet die Apotheke 14
15 Prüfung 12 Prüfung der nicht in der Apotheke hergestellten Fertigarzneimittel und apothekenpflichtigen Medizinprodukte Die stichprobenweise Prüfung ist sowohl für Fertigarzneimittel als auch für apothekenpflichtige Medizinprodukte durchzuführen. Im Fall von Medizinprodukten ist im Prüfprotokoll der Name des Hersteller oder seines Bevollmächtigten anzugeben 15
16 Kennzeichnung 14 Kennzeichnung Kennzeichnung von Rezepturarzneimitteln Redaktionelle Änderungen Gebrauchsanweisung ist grundsätzlich erforderlich Prüfpräparate Kennzeichnung nach 5 GCP-V Kennzeichnung von Defekturarzneimitteln Nach 10 und 11 AMG ggf. mit Ausnahme der Zul.Nr. oder Reg.Nr. mit Ausnahme der Angaben in Blindenschrift 16
17 Lagerung 16 Lagerung Lagerungsvorschriften Gelten auch für Medizinprodukte Eignung der Vorratsbehältnisse für Arzneimittel und Ausgangsstoffe Angabe des Verfall- oder Nachprüfdatums 17
18 Erwerb und Abgabe 17 Erwerb und Abgabe von Arzneimitteln und Medizinprodukten Erwerb von Arzneimitteln und Medizinprodukten Nur von berechtigten Betrieben Abs. 6c (neu): Apotheken dürfen von anderen Apotheken keine Arzneimittel beziehen; Ausnahmen: Im Rahmen des apothekenüblichen Betrieb Filialapotheke Zytostatika, Arzneimittel für den Pandemiefall ( 11 ApG) Nachfolgender Erlaubnisinhaber bei Apothekenschließung In dringenden Fällen 18
19 Einfuhr 18 Einfuhr von Arzneimitteln Einfuhr nach 73 Abs. 3 (Humanarzneimittel) oder 3a (Tierarzneimittel) AMG Zusätzlich Dokumentation der Chargenbezeichnung 19
20 Information und Beratung 20 Information und Beratung QMS soll Information und Beratung sicherstellen Die Verpflichtung zur Information und Beratung über Arzneimittel muss durch Apotheker der Apotheke ausgeübt werden, sie kann durch andere Angehörige des pharmazeutischen Personals der Apotheke übernommen werden, wenn der Apothekenleiter dies zuvor schriftlich festgelegt hat. Dabei hat er auch zu definieren, in welchen Fällen ein Apotheker der Apotheke grundsätzlich hinzuzuziehen ist. 20
21 Leiter der Krankenhausapotheke 27 Leiter der Krankenhausapotheke; Abs. 2: Verantwortung des Leiters der Krankenhausapotheke Bedarfsgerechte Bereitstellung von Arzneimitteln und Medizinprodukten; Arzneimittel für die Akutversorgung müssen unverzüglich zur Verfügung gestellt werden. Regelmäßige Überprüfung der lagernden Arzneimittel und Medizinprodukte (Dokumentation) Beratung des Krankenhauspersonals durch einen Apotheker zur sicheren, zweckmäßigen und wirtschaftlichen Arzneimitteltherapie Beratung der Patienten zur sicheren Anwendung der Arzneimittel (insbesondere bei deren Entlassung) Mitglied der Arzneimittelkommission des KH 21
22 Räume 29 Räume und Einrichtungen der Krankenhausapotheke mit 4 Abs. 1 Satz 3 Betriebsräume Abtrennung durch Wände oder Türen von anderweitig gewerblich oder beruflich genutzten Räumen von öffentlichen Verkehrsflächen und Ladenstraßen Schutz gegen unbefugten Zutritt Ausreichende Beleuchtung, Belüftung und ggf. Klimatisierung Einwandfreier baulicher und hygienischer Zustand Raumeinheit ist nicht gefordert 22
23 Räume 29: 4 Abs. 2b,c,d (neu) gelten entsprechend (2b) Für die Herstellung von nicht zur parenteralen Anwendung bestimmten Arzneimitteln ist ein eigener Arbeitsplatz vorzusehen. Der Arbeitsplatz ist von mindestens drei Seiten raumhoch von anderen Bereichen der Apotheke abzutrennen. Seine Wände und Oberflächen sowie der Fußboden müssen leicht zu reinigen sein, damit das umgebungsbedingte Kontaminationsrisiko für die herzustellenden Arzneimittel minimal ist. 2c) Für die Herstellung von Arzneimitteln, die Drogen oder Drogenmischungen sind oder für die sonstige Verarbeitung von Drogen als Ausgangsstoffe ist ein gesonderter Arbeitsplatz vorzusehen. 2d) Lagerungsräume und bedingungen: Lagerung unter 25 Grad C; Sperrlager; Schutz vor Zugriff Unbefugter 23
24 Geräte 29: 4 Abs. 7 und 8 gelten entsprechend Geräte für folgende Darreichungsformen: Lösungen, Emulsionen, Suspensionen, auch steril, Salben, Cremes, Gele, Pasten, Kapseln, Pulver, Drogenmischungen sowie Zäpfchen und Ovula Wasser für Injektionszwecke Gerät zur Herstellung oder ausreichende Bevorratung Geräte und Prüfmittel Keine Auflistung; Verantwortung des Apothekenleiters 24
25 Vorratshaltung und Abgabe 30 Vorratshaltung in der Krankenhausapotheke Die zur Sicherstellung einer ordnungsgemäßen Arzneimittelversorgung der Patienten des Krankenhauses notwendigen Arzneimittel und apothekenpflichtigen Medizinprodukte müssen in ausreichender Menge vorrätig gehalten werden, die mindestens dem durchschnittlichen Bedarf für zwei Wochen entsprechen muss. Diese Arzneimittel und apothekenpflichtigen Medizinprodukte sind aufzulisten. Für die Abgabe an die Stationen ( 31) gilt Entsprechendes 25
26 Stationsbegehungen 32: Überprüfung der Arzneimittelvorräte und der apothekenpflichtigen Medizinprodukte auf den Stationen Protokoll in vierfacher Ausfertigung für Krankenhausleitung, spätestens nach 4 Wochen, bei schwerwiegenden Mängeln unmittelbar nach der Begehung Arzt Pflegedienstleitung, die für die Arzneimittelversorgung auf der Station zuständig ist Verbleib in der Apotheke 26
27 Stellen und Verblistern 34 (neu) Patientenindividuelles Stellen oder Verblistern von Arzneimitteln Abs. 1: Festlegungen im QMS Ausnahmslos im Geltungsbereich des AMG zugelassene Fertigarzneimittel Auswahl- bzw. Ausschlusskriterien für Arzneimittel Kompatibilität von Arzneimitteln im selben Einzelblister Teilung von Tabletten im Ausnahmefall Zwischenlagerung und Kennzeichnung der entblisterten Arzneimittel Erhalt der Qualität der entblisterten Arzneimittel Kalibrierung, Qualifizierung, Wartung und Reinigung der Blisterautomaten 27
28 Stellen und Verblistern 34 Patientenindividuelles Stellen oder Verblistern von Arzneimitteln Festlegungen im QMS (Fortsetzung) Primäre Verpackungsmaterialien und Qualitätsprüfungen Herstellungsanweisungen und protokolle Hygieneplan Personalhygiene Abs. 2: Qualifikation des Personals und Schulung Siehe auch: Aide-Mémoire Maschinelles patientenindividuelles Verblistern von Arzneimitteln 28
29 Stellen und Verblistern 34 Abs. 3 Räumliche Anforderungen Eigener Raum nur für diesen Verwendungszweck Angemessene Größe und Bereich für die jeweiligen Arbeitsschritte Wände, Böden und Oberflächen leicht zu reinigen Zusätzliche Schleuse für das Einbringen von Materialien beim maschinellen Verblistern Abweichungen sind möglich, wenn das Stellen oder das manuelle Verblistern nur im Einzelfall erfolgt 29
30 Stellen und Verblistern 34 Abs. 4 Kennzeichnung 1. der Name des Patienten, 2. die enthaltenen Arzneimittel und ihre Chargenbezeichnungen, 3. das Verfalldatum des neu zusammengestellten Arzneimittels und seine Chargenbezeichnung, 4. die Einnahmehinweise, 5. eventuelle Lagerungshinweise sowie 6. die abgebende Apotheke und, soweit unterschiedlich, des Herstellers. Dem neu verpackten Arzneimittel sind patientenbezogen die Packungsbeilagen der enthaltenen Fertigarzneimittel gemäß 11 Absatz 7 des Arzneimittelgesetzes beizufügen. 30
31 Herstellung von Parenteralia 35 (neu) Herstellung von Arzneimitteln zur parenteralen Anwendung Festlegungen im QMS Einzusetzende Arzneimittel und primäre Verpackungsmaterialien einschl. deren Prüfung Maßnahmen zu Vermeidung von Kontaminationen, Kreuzkontaminationen und Verwechslungen und Überprüfung ihrer Wirksamkeit Kalibrierung, Qualifizierung, Wartung und Reinigung der Ausrüstung Validierung der Prozesse, Methoden und System einschl. Revalidierung; bei aseptischen Prozessen am Ende jedes Arbeitstages; das Herstellungspersonal ist einzubeziehen 31
32 Herstellung von Parenteralia 35 (neu) Herstellung von Arzneimitteln zur parenteralen Anwendung Festlegungen im QMS (Fortsetzung) kritische Ausrüstungsgegenstände oder Geräte Herstellungsanweisungen und-protokolle Transport Hygienemaßnahmen Hygienisches Verhalten des Personals, Schutzkleidung, Umkleidevorgänge Qualifizierung und regelmäßige Schulung des Personals 32
33 Herstellung von Parenteralia 35 (neu) Abs. 3 Räumliche Anforderungen Separater, nur zu diesem Zweck genutzter Raum mit Schleusen für Personal und Material Belüftungssystem Wände und Oberflächen leicht zu reinigen Nur Personal in erforderlicher Zahl mit Schutzkleidung Reinraumklassen für aseptische Prozesse Klasse A für offene aseptische Arbeitsschritte Umgebung mind. der Klasse B oder mind. Klasse C, wenn die Qualität gewährleistet und das Verfahren validiert ist Klasse D bei Verwendung eines Isolators 33
34 Herstellung von Parenteralia Anforderungen an Reinräume und Ausrüstung Wo sind die Anforderungen definiert? EU-GMP-Leitfaden Annex 1 ISO Ph.Eur Methoden z. Herstellung steriler Zubereitungen PIC/S Guide to good practices for the preparation of medicinal products in healthcare establishments, PE 010-3, Relevante Reinraumklassen A, B, C, D; spezifiziert durch Grenzwerte für Partikelzahl (Größe 0,5µm und 5µm) pro m³ Luft, Luftkeimzahl pro m³, Luftkeimzahl pro Sedimentationsplatte, Keimzahl auf Oberflächen und Handschuhen des herstellenden Personals Qualifizierung und Monitoring 34
35 Herstellung von Parenteralia Welche Tätigkeiten in welchen Reinraumklassen? Aseptische Herstellung: Klasse A Hintergrund Klasse B oder ggf. C, wenn validiert Endsterilisation: Mind. Klasse D für die Herstellung der Lösung, mind. Klasse C für die Abfüllung Reinraumklasse je nach Risiko Bauliche Anforderungen Wände, Decken und Böden glatt und leicht zu reinigen; keine Abflüsse in Klasse A/B; keine Staub fangende Ausstattung RLT-Anlage mit HEPA-Filtern zur Erzeugung laminarer Luftströmung mit definierter Geschwindigkeit und Luftreinheit; Etablierung einer Druckkaskade 35
36 Herstellung von Parenteralia Hygienische Anforderungen Betriebshygiene Reinigungs- und Desinfektionsplan; Qualität der Reinigungsund Desinfektionsmittel Ein- und Ausschleusung von Material Schulung des Reinigungs- und Produktionspersonals Personalhygiene Kleidungsvorschriften für jede Reinraumklasse Vorschriften zur Ein- und Ausschleusung Hygienisches Verhalten Gesundheitsüberwachung Schulung 36
37 Herstellung von Parenteralia Monitoring der Umgebungsbedingungen Parameter Luftpartikel, Luft- und Oberflächenkeimzahl, Druckkaskade, Strömungsgeschwindigkeit, ggf. Temperatur und Feuchte Probenahme Intervalle (ja nach Reinraumklasse) Methode Messstellenplan und Betriebsstatus Akzeptanzkriterien Festlegung von Warn- und Aktionsgrenzen Vorgehen bei Messergebnissen außerhalb der Spezifikation 37
38 Übergangsvorschriften 37 Übergangsvorschriften Übergangsfrist bis 1. Juni 2014 Für die Etablierung eines QM-Systems Separater Raum und Schleuse für die patientenindividuelle Verblisterung für Räume, die zur Herstellung von Parenteralia eingesetzt werden, aber noch nicht über eine Schleuse verfügen. Übergangsfrist bis 1. Juni 2013 Für geeignete Kontrollen der Reinraumbedingungen bei der Herstellung in offenen Systemen; Warn- und Aktionsgrenzen 38
39 Vielen Dank für Ihre Aufmerksamkeit 39
Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Einnahmezeitpunkte
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Stand: 26.11.2014 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Stand: 26.11.2014 Inhaltsverzeichnis
Die neue Apothekenbetriebsordnung
 Die neue Apothekenbetriebsordnung Fortbildungsveranstaltung der Apothekerkammer Nordrhein Dr. Dagmar Krüger Bundesministerium für Gesundheit D. Krüger 2012 1 Verlauf nicht offizieller Arbeitsentwurf 2010
Die neue Apothekenbetriebsordnung Fortbildungsveranstaltung der Apothekerkammer Nordrhein Dr. Dagmar Krüger Bundesministerium für Gesundheit D. Krüger 2012 1 Verlauf nicht offizieller Arbeitsentwurf 2010
Checkliste zur Überprüfung des QMS in der öffentlichen Apotheke
 Landesamt für soziale Dienste Schleswig-Holstein - Abt. Gesundheitsschutz - Checkliste zur Überprüfung des QMS in der öffentlichen Apotheke (ohne Versandhandel, Stellen/Verblistern, Krankenhaus-und Heimbelieferung,
Landesamt für soziale Dienste Schleswig-Holstein - Abt. Gesundheitsschutz - Checkliste zur Überprüfung des QMS in der öffentlichen Apotheke (ohne Versandhandel, Stellen/Verblistern, Krankenhaus-und Heimbelieferung,
Änderung der Apothekenbetriebsordnung Synopse, Stand Geltende Fassung Referentenentwurf BVKA-Stellungnahme Kabinettsvorlage
 Erster Abschnitt Allgemeine Bestimmung Erster Abschnitt Allgemeine Bestimmung 1 Anwendungsbereich 1 Anwendungsbereich (1) Diese Verordnung findet Anwendung auf den Betrieb und die Einrichtung von öffentlichen
Erster Abschnitt Allgemeine Bestimmung Erster Abschnitt Allgemeine Bestimmung 1 Anwendungsbereich 1 Anwendungsbereich (1) Diese Verordnung findet Anwendung auf den Betrieb und die Einrichtung von öffentlichen
Vorblatt. Vierte Verordnung zur Änderung der Apothekenbetriebsordnung
 Vorblatt Vierte Verordnung zur Änderung der Apothekenbetriebsordnung A. Problem und Ziel Die Apothekenbetriebsordnung vom 9. Februar 1987 wurde seit ihrem Inkrafttreten punktuell geändert, sie bedarf nunmehr
Vorblatt Vierte Verordnung zur Änderung der Apothekenbetriebsordnung A. Problem und Ziel Die Apothekenbetriebsordnung vom 9. Februar 1987 wurde seit ihrem Inkrafttreten punktuell geändert, sie bedarf nunmehr
Eckpunkte 1 für die Dokumentation der Apothekenbesichtigung im Sinn der Grundsätze für die Apothekenüberwachung
 Arbeitsgruppe Arzneimittel-, Apotheken-, Transfusions- und Betäubungsmittelwesen (AATB) Stand 14. Februar 2013 Eckpunkte 1 für die Dokumentation der Apothekenbesichtigung im Sinn der Grundsätze für die
Arbeitsgruppe Arzneimittel-, Apotheken-, Transfusions- und Betäubungsmittelwesen (AATB) Stand 14. Februar 2013 Eckpunkte 1 für die Dokumentation der Apothekenbesichtigung im Sinn der Grundsätze für die
Vierte Verordnung zur Änderung der Apothekenbetriebsordnung
 - 1 - Vierte Verordnung zur Änderung der Apothekenbetriebsordnung Auf Grund des Vom... 21 Absatz 1 in Verbindung mit Absatz 2 und 3 des Apothekengesetzes, dessen Absatz 1 zuletzt durch Artikel 34 der Verordnung
- 1 - Vierte Verordnung zur Änderung der Apothekenbetriebsordnung Auf Grund des Vom... 21 Absatz 1 in Verbindung mit Absatz 2 und 3 des Apothekengesetzes, dessen Absatz 1 zuletzt durch Artikel 34 der Verordnung
Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel
 Leitlinie der Bundesapothekerkammer zur Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel Stand der Revision: 25.11.2008 Inhaltsübersicht I II III
Leitlinie der Bundesapothekerkammer zur Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel Stand der Revision: 25.11.2008 Inhaltsübersicht I II III
Niederschrift über die Apothekenbesichtigung gemäß 64 ff. des Arzneimittelgesetzes
 Landesamt für Gesundheit und Soziales 1 Landesamt für Gesundheit und Soziales Berlin Postfach 31 09 29, 10639 Berlin (Postanschrift) Tel.: 90229 2330, 2331 Fax: 90229 2097 Niederschrift über die Apothekenbesichtigung
Landesamt für Gesundheit und Soziales 1 Landesamt für Gesundheit und Soziales Berlin Postfach 31 09 29, 10639 Berlin (Postanschrift) Tel.: 90229 2330, 2331 Fax: 90229 2097 Niederschrift über die Apothekenbesichtigung
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Hygienemanagement
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 25.11.2015 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 25.11.2015 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Erster Abschnitt Allgemeine Bestimmung 1 Anwendungsbereich 1a Begriffsbestimmungen
 Erster Abschnitt Allgemeine Bestimmung 1 Anwendungsbereich Apothekenbetriebsordnung vom 9.2. 1987 Inhaltsübersicht Zweiter Abschnitt Der Betrieb von öffentlichen Apotheken 2 Apothekenleiter 3 Apothekenpersonal
Erster Abschnitt Allgemeine Bestimmung 1 Anwendungsbereich Apothekenbetriebsordnung vom 9.2. 1987 Inhaltsübersicht Zweiter Abschnitt Der Betrieb von öffentlichen Apotheken 2 Apothekenleiter 3 Apothekenpersonal
Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit toxischem Potenzial
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit toxischem Potenzial Stand der Revision: 25.11.2008 Inhaltsübersicht I
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit toxischem Potenzial Stand der Revision: 25.11.2008 Inhaltsübersicht I
Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung - ApBetrO)
 Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung - ApBetrO) ApBetrO Ausfertigungsdatum: 09.02.1987 Vollzitat: "Apothekenbetriebsordnung in der Fassung der Bekanntmachung vom 26. September
Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung - ApBetrO) ApBetrO Ausfertigungsdatum: 09.02.1987 Vollzitat: "Apothekenbetriebsordnung in der Fassung der Bekanntmachung vom 26. September
194 6 Die Apotheke. 6.2 Apothekenbetriebsordnung
 194 6 Die Apotheke CE-Kennzeichnung tragen, auch im Ausland zur Auffüllung der Ausrüstung beschafft werden; diese sind, sofern sie eine fremdsprachige Beschriftung und eine fremdsprachige Packungsbeilage
194 6 Die Apotheke CE-Kennzeichnung tragen, auch im Ausland zur Auffüllung der Ausrüstung beschafft werden; diese sind, sofern sie eine fremdsprachige Beschriftung und eine fremdsprachige Packungsbeilage
Apothekenbetriebsordnung 2012
 Apothekenbetriebsordnung 2012 1 Anwendungsbereich (1) Diese Verordnung findet Anwendung auf den Betrieb und die Einrichtung von öffentlichen Apotheken einschließlich der krankenhausversorgenden Apotheken,
Apothekenbetriebsordnung 2012 1 Anwendungsbereich (1) Diese Verordnung findet Anwendung auf den Betrieb und die Einrichtung von öffentlichen Apotheken einschließlich der krankenhausversorgenden Apotheken,
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Hygienemanagement. Stand der Revision: 13.11.
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 13.11.2013 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 13.11.2013 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
Verordnung zur Änderung der Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung ApBetrO)
 Verordnungsentwurf Bundesministerium für Gesundheit Verordnungsentwurf Bundesministerium für Gesundheit Verordnung zur Änderung der Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung ApBetrO)
Verordnungsentwurf Bundesministerium für Gesundheit Verordnungsentwurf Bundesministerium für Gesundheit Verordnung zur Änderung der Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung ApBetrO)
DOSSIER FÜR DEFEKTURARZNEIMITTEL 1
 Defekturbezeichnung DOSSIER FÜR DEFEKTURARZNEIMITTEL 1 Zu den unten genannten Punkten sind gegeben falls entsprechende Unterlagen im Anhang beigefügt. 1. Mehrwert 2 Herstellung aufgrund wiederkehrender
Defekturbezeichnung DOSSIER FÜR DEFEKTURARZNEIMITTEL 1 Zu den unten genannten Punkten sind gegeben falls entsprechende Unterlagen im Anhang beigefügt. 1. Mehrwert 2 Herstellung aufgrund wiederkehrender
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Prüfung der Fertigarzneimittel und apothekenpflichtigen
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Prüfung der Fertigarzneimittel und apothekenpflichtigen Medizinprodukte Stand der Revision:16.06.2016 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Prüfung der Fertigarzneimittel und apothekenpflichtigen Medizinprodukte Stand der Revision:16.06.2016 Inhaltsverzeichnis
Die neue Apothekenbetriebsordnung. Dr. Valentin Saalfrank Rechtsanwalt und Fachanwalt für Medizinrecht Köln
 Die neue Apothekenbetriebsordnung 1 Neue Regelungen 1a Begriffsbestimmungen 2a Qualitätsmanagementsystem 4a Hygienemaßnahmen 11a Tätigkeiten im Auftrag 34 Patientenindividuelle Verblisterung 35 Patientenindividuelle
Die neue Apothekenbetriebsordnung 1 Neue Regelungen 1a Begriffsbestimmungen 2a Qualitätsmanagementsystem 4a Hygienemaßnahmen 11a Tätigkeiten im Auftrag 34 Patientenindividuelle Verblisterung 35 Patientenindividuelle
Herstellung und Prüfung applikationsfertiger Parenteralia ohne CMR-Eigenschaften der Kategorie 1A oder 1B
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung applikationsfertiger Parenteralia ohne CMR-Eigenschaften der Kategorie 1A oder 1B Stand
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung applikationsfertiger Parenteralia ohne CMR-Eigenschaften der Kategorie 1A oder 1B Stand
Fischer /Schüler. Rezeptur - Qualität in 7 Schritten. Ulrike Fischer, Dresden Katrin Schüler, Dresden. Mit 55 Abbildungen und 101 Tabellen
 Fischer /Schüler Rezeptur - Qualität in 7 Schritten Ulrike Fischer, Dresden Katrin Schüler, Dresden Mit 55 Abbildungen und 101 Tabellen Ä Checklisten, Arbeitsblätter und Fallbeispiele unterwww.online-plusbase.de
Fischer /Schüler Rezeptur - Qualität in 7 Schritten Ulrike Fischer, Dresden Katrin Schüler, Dresden Mit 55 Abbildungen und 101 Tabellen Ä Checklisten, Arbeitsblätter und Fallbeispiele unterwww.online-plusbase.de
ARBEITSBOGEN 5: HERSTELLUNG VON REZEPTURARZNEIMITTELN
 I Hinweis zur Bearbeitung des Arbeitsbogens Stellen Sie ein wirkstoffhaltiges Rezepturarzneimittel her. Verwenden Sie zur Bearbeitung des Arbeitsbogens die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung
I Hinweis zur Bearbeitung des Arbeitsbogens Stellen Sie ein wirkstoffhaltiges Rezepturarzneimittel her. Verwenden Sie zur Bearbeitung des Arbeitsbogens die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung
Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit CMR-Eigenschaften der Kategorie 1A oder 1B
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit CMR-Eigenschaften der Kategorie 1A oder
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit CMR-Eigenschaften der Kategorie 1A oder
Niederschrift über die Apothekenbesichtigung vom... von... bis... Uhr. Abnahme-, Regel-, Kurz-, Nachbesichtigung
 Niederschrift über die Apothekenbesichtigung vom... von... bis... Uhr Apothekenanschrift mit Telefon (Stempel): Abnahme-, Regel-, Kurz-, Nachbesichtigung Teilnehmer:......... Datum der letzten Besichtigung:...
Niederschrift über die Apothekenbesichtigung vom... von... bis... Uhr Apothekenanschrift mit Telefon (Stempel): Abnahme-, Regel-, Kurz-, Nachbesichtigung Teilnehmer:......... Datum der letzten Besichtigung:...
Prüfung der Fertigarzneimittel
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Leitlinie Kommentar Arbeitshilfe. Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Hygienemanagement
 Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 25.11.2015 Die Erläuterungen sind eine Zusammenfassung der Anforderungen pharmazeutischer
Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 25.11.2015 Die Erläuterungen sind eine Zusammenfassung der Anforderungen pharmazeutischer
Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung - ApBetrO)
 Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung - ApBetrO) ApBetrO Ausfertigungsdatum: 09.02.1987 Vollzitat: "Apothekenbetriebsordnung in der Fassung der Bekanntmachung vom 26. September
Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung - ApBetrO) ApBetrO Ausfertigungsdatum: 09.02.1987 Vollzitat: "Apothekenbetriebsordnung in der Fassung der Bekanntmachung vom 26. September
Apotheken Recht Tag Forum Arzneimittel&Recht
 Apotheken Recht Tag Forum Arzneimittel&Recht Offene Fragen zur neuen Apothekenbetriebsordnung 1 Übersicht Anforderungen an die Räume Vertretung des Apothekenleiters Information und Beratung Bezug und Abgabe
Apotheken Recht Tag Forum Arzneimittel&Recht Offene Fragen zur neuen Apothekenbetriebsordnung 1 Übersicht Anforderungen an die Räume Vertretung des Apothekenleiters Information und Beratung Bezug und Abgabe
Initialvorlesung WS 2011 / Schwerpunktthema: Industrielle Arzneimittelherstellung versus Individualherstellung 26. Oktober 2011 in Mainz
 Initialvorlesung WS 2011 / 2012 Schwerpunktthema: Industrielle Arzneimittelherstellung versus Individualherstellung in Mainz Folie 1 Mittelalter bis zum 19. Jahrhundert traditionelle Arzneimittelherstellung
Initialvorlesung WS 2011 / 2012 Schwerpunktthema: Industrielle Arzneimittelherstellung versus Individualherstellung in Mainz Folie 1 Mittelalter bis zum 19. Jahrhundert traditionelle Arzneimittelherstellung
Anforderungen an eine Unit-Dose Versorgung in der Krankenhausapotheke
 Leitlinie Anforderungen an eine Unit-Dose Versorgung in der Krankenhausapotheke Stand der letzten Änderung: 13.10.2014 Inhaltsverzeichnis I II III IV V I Präambel Expertengremium: Michael Baehr, Hamburg,
Leitlinie Anforderungen an eine Unit-Dose Versorgung in der Krankenhausapotheke Stand der letzten Änderung: 13.10.2014 Inhaltsverzeichnis I II III IV V I Präambel Expertengremium: Michael Baehr, Hamburg,
Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 23.11.2016 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 23.11.2016 Inhaltsverzeichnis
Was bringen die Novellen zur Apothekenbetriebsordnung, und zur Pflegeversicherung für die Heimversorgung? Eine erste Bewertung
 Von der Arzneimittelsicherheit zur Patientensicherheit Tagung des Bundesverbandes der klinik- und heimversorgenden Apotheker e.v. Berlin, 06. Februar 2012 Was bringen die Novellen zur Apothekenbetriebsordnung,
Von der Arzneimittelsicherheit zur Patientensicherheit Tagung des Bundesverbandes der klinik- und heimversorgenden Apotheker e.v. Berlin, 06. Februar 2012 Was bringen die Novellen zur Apothekenbetriebsordnung,
Die Prüfung der Ausgangsstoffe. Eine Hilfe zur Umsetzung
 Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung Gesetzliche Vorgaben Apothekenbetriebsordnung (ApBetrO) Arzneimittel, die in der Apotheke hergestellt werden, müssen die nach der pharmazeutischen
Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung Gesetzliche Vorgaben Apothekenbetriebsordnung (ApBetrO) Arzneimittel, die in der Apotheke hergestellt werden, müssen die nach der pharmazeutischen
Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung ApBetrO)
 Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung ApBetrO) in der Fassung der Bekanntmachung vom 26. September 1995 (BGBl. I S. 1195), zuletzt geändert durch Artikel 1 der Vierten Verordnung
Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung ApBetrO) in der Fassung der Bekanntmachung vom 26. September 1995 (BGBl. I S. 1195), zuletzt geändert durch Artikel 1 der Vierten Verordnung
Apothekenbetriebsordnung 2012- Was ist neu für Rezeptur und Defektur? (ohne 35)
 Apothekenbetriebsordnung 2012- Was ist neu für Rezeptur und Defektur? (ohne 35) Ausschuss für Arzneimittelherstellung und Analytik R. Heimke-Brinck Neue Apothekenbetriebsordnung 12.Juni 2012 Ein Jahr später
Apothekenbetriebsordnung 2012- Was ist neu für Rezeptur und Defektur? (ohne 35) Ausschuss für Arzneimittelherstellung und Analytik R. Heimke-Brinck Neue Apothekenbetriebsordnung 12.Juni 2012 Ein Jahr später
Tab. 3.1 Was muss im Einzelnen dokumentiert werden? A Ausgangsstoff/Bezeichnung. B Lieferdatum/Herstellungsdatum. C Lieferant/Hersteller
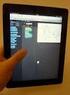 51 3.1 Prüfung von Ausgangsstoffen und Defekturarzneimitteln Tab. 3.1 Was muss im Einzelnen dokumentiert werden? Was Wer Apothekenbetriebsordnung 6 Allgemeine Vorschriften über die Herstellung und Prüfung
51 3.1 Prüfung von Ausgangsstoffen und Defekturarzneimitteln Tab. 3.1 Was muss im Einzelnen dokumentiert werden? Was Wer Apothekenbetriebsordnung 6 Allgemeine Vorschriften über die Herstellung und Prüfung
Fragen- und Antwortkatalog (FAQ) zu 35 ApBetrO eine Richtschnur bei der Apothekenrevision
 Fragen- und Antwortkatalog (FAQ) zu 35 ApBetrO eine Richtschnur bei der Apothekenrevision 1 Überblick Grundsätze des FAQ Risikobewertung PIC/S PE 10 insbesondere Annex 1 Besondere Anforderungen an Qualitätssicherungssystem
Fragen- und Antwortkatalog (FAQ) zu 35 ApBetrO eine Richtschnur bei der Apothekenrevision 1 Überblick Grundsätze des FAQ Risikobewertung PIC/S PE 10 insbesondere Annex 1 Besondere Anforderungen an Qualitätssicherungssystem
Aktueller Stand der Leitlinien, Kommentare und Arbeitshilfen der Bundesapothekerkammer
 Aktueller der Leitlinien, Kommentare und Arbeitshilfen der Bundesapothekerkammer Name des Dokumentes ARZNEIMITTELINFORMATION Arzneimittelinformation in der Apotheke (Leitlinie und Kommentar ) Dokumentationsbogen
Aktueller der Leitlinien, Kommentare und Arbeitshilfen der Bundesapothekerkammer Name des Dokumentes ARZNEIMITTELINFORMATION Arzneimittelinformation in der Apotheke (Leitlinie und Kommentar ) Dokumentationsbogen
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Versand der Arzneimittel aus der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 28.04.2015 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 28.04.2015 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
AMK-AMG-Herstell-Anz Seite 1 von 6
 AMK-AMG-Herstell-Anz-2010-01-25 Seite 1 von 6 Information der Arzneimittelkommission der deutschen Heilpraktiker bezüglich der arzneimittelrechtlichen Änderungen zur Anzeigepflicht der Herstellung von
AMK-AMG-Herstell-Anz-2010-01-25 Seite 1 von 6 Information der Arzneimittelkommission der deutschen Heilpraktiker bezüglich der arzneimittelrechtlichen Änderungen zur Anzeigepflicht der Herstellung von
ARBEITSBOGEN 1: HALTBARKEIT, LAGERUNG UND ENTSORGUNG DER FERTIGARZNEIMITTEL, MEDI- ZINPRODUKTE, APOTHEKENÜBLICHEN WAREN UND AUSGANGSSTOFFE
 I Hinweis zur Bearbeitung des Arbeitsbogens Informieren Sie sich über die Haltbarkeit, Lagerung und Entsorgung der Fertigarzneimittel (FAM), Medizinprodukte (MP), apothekenüblichen Ware und Ausgangsstoffe
I Hinweis zur Bearbeitung des Arbeitsbogens Informieren Sie sich über die Haltbarkeit, Lagerung und Entsorgung der Fertigarzneimittel (FAM), Medizinprodukte (MP), apothekenüblichen Ware und Ausgangsstoffe
Apothekerkammer des Saarlandes
 Niederschrift über die Besichtigung gemäß 64 AMG und der ApBetrO über die: Stempel Regel- Abnahme- Nach- Schwerpunktbesichtigung am: Dauer: Std. letzte Besichtigung am: bei der Besichtigung anwesend: E-Mail:
Niederschrift über die Besichtigung gemäß 64 AMG und der ApBetrO über die: Stempel Regel- Abnahme- Nach- Schwerpunktbesichtigung am: Dauer: Std. letzte Besichtigung am: bei der Besichtigung anwesend: E-Mail:
Jahrestagung der AGRR 2011 Aktuelle Problemstellungen bei der Herstellung von Radiopharmaka
 Jahrestagung der AGRR 2011 Aktuelle Problemstellungen bei der Herstellung von Radiopharmaka Themen Regulatorische Grundlagen und das Gesetz vom 17. Juli 2009 in der Praxis: 13 Abs. 2b AMG Zulassungspflicht;
Jahrestagung der AGRR 2011 Aktuelle Problemstellungen bei der Herstellung von Radiopharmaka Themen Regulatorische Grundlagen und das Gesetz vom 17. Juli 2009 in der Praxis: 13 Abs. 2b AMG Zulassungspflicht;
F r e i e u n d H a n s e s t a d t H a m b u r g Behörde für Gesundheit und Verbraucherschutz
 F r e i e u n d H a n s e s t a d t H a m b u r g Behörde für Gesundheit und Verbraucherschutz Häufig gestellte Fragen zur neuen Apothekenbetriebsordnung Stand: Mai 2015 Seit dem 12.06.2012 ist die neue
F r e i e u n d H a n s e s t a d t H a m b u r g Behörde für Gesundheit und Verbraucherschutz Häufig gestellte Fragen zur neuen Apothekenbetriebsordnung Stand: Mai 2015 Seit dem 12.06.2012 ist die neue
GMP-gerechte Betriebshygiene und mikrobiologisches Monitoring in der Arzneimittel herstellenden Apotheke
 GMP-gerechte Betriebshygiene und mikrobiologisches Monitoring in der Arzneimittel herstellenden Apotheke Referenten: Dr. Klaus Haberer (Compliance Advice and Services in Microbiology GmbH in Köln) Dr.
GMP-gerechte Betriebshygiene und mikrobiologisches Monitoring in der Arzneimittel herstellenden Apotheke Referenten: Dr. Klaus Haberer (Compliance Advice and Services in Microbiology GmbH in Köln) Dr.
Arzneimittelpreisverordnung (AMPreis V) Vom 14. November 1980 (BGBl. I S. 2147) 1 Anwendungsbereich der Verordnung
 Nur die Originaltexte sind rechtsverbindlich! E 1. 2.18 Arzneimittelpreisverordnung (AMPreis V) Vom 14. November 1980 (BGBl. I S. 2147) zuletzt geändert durch: Artikel 24 des Gesetzes vom 14. November
Nur die Originaltexte sind rechtsverbindlich! E 1. 2.18 Arzneimittelpreisverordnung (AMPreis V) Vom 14. November 1980 (BGBl. I S. 2147) zuletzt geändert durch: Artikel 24 des Gesetzes vom 14. November
Reinräume Hintergrund Zum Apothekenbetriebsverordnung (ApBetrO) VOM
 Reinräume Hintergrund Zum Apothekenbetriebsverordnung (ApBetrO) VOM 12.06.2012 Reinräume HINTERGRUND ZUM APOTHEKENBETRIEBSVERORDNUNG (ApBetrO) VOM 12.06.2012 INHALT:- (i) (ii) (iii) (iv) (v) (vi) (vii)
Reinräume Hintergrund Zum Apothekenbetriebsverordnung (ApBetrO) VOM 12.06.2012 Reinräume HINTERGRUND ZUM APOTHEKENBETRIEBSVERORDNUNG (ApBetrO) VOM 12.06.2012 INHALT:- (i) (ii) (iii) (iv) (v) (vi) (vii)
Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen. Referent: Dipl.-Ing. Burkhard Schulze
 Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen Referent: Dipl.-Ing. Burkhard Schulze Definition: Aufbereitung Reinigung, Desinfektion und Sterilisation von bestimmungsgemäß
Gesetzliche Anforderungen an die Aufbereitung von flexiblen thermolabilen Endoskopen Referent: Dipl.-Ing. Burkhard Schulze Definition: Aufbereitung Reinigung, Desinfektion und Sterilisation von bestimmungsgemäß
WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil XI 18. Januar 2012 in Mainz
 WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil XI in Mainz Folie 1 ApBetrO vom 20. Oktober 2011 24 Rezeptsammelstellen OLG München hatte
WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil XI in Mainz Folie 1 ApBetrO vom 20. Oktober 2011 24 Rezeptsammelstellen OLG München hatte
Arzneimittelpreisverordnung (AMPreisV)
 Arzneimittelpreisverordnung (AMPreisV) AMPreisV Ausfertigungsdatum: 14.11.1980 Vollzitat: "Arzneimittelpreisverordnung vom 14. November 1980 (BGBl. I S. 2147), die zuletzt durch Artikel 2b des Gesetzes
Arzneimittelpreisverordnung (AMPreisV) AMPreisV Ausfertigungsdatum: 14.11.1980 Vollzitat: "Arzneimittelpreisverordnung vom 14. November 1980 (BGBl. I S. 2147), die zuletzt durch Artikel 2b des Gesetzes
Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 13.11.2013 Inhaltsübersicht
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 13.11.2013 Inhaltsübersicht
Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel
 Leitlinie Kommentar rbeitshilfe Leitlinie der Bundesapothekerkammer Herstellung und Prüfung der nicht zur parenteralen nwendung bestimmten Rezeptur- Stand der Revision: 25.11.2015 Inhaltsverzeichnis I
Leitlinie Kommentar rbeitshilfe Leitlinie der Bundesapothekerkammer Herstellung und Prüfung der nicht zur parenteralen nwendung bestimmten Rezeptur- Stand der Revision: 25.11.2015 Inhaltsverzeichnis I
BUNDESVERWALTUNGSGERICHT BESCHLUSS
 BUNDESVERWALTUNGSGERICHT BESCHLUSS BVerwG 3 B 15.15 OVG 5 B 2.12 In der Verwaltungsstreitsache hat der 3. Senat des Bundesverwaltungsgerichts am 1. März 2016 durch die Richterin am Bundesverwaltungsgericht
BUNDESVERWALTUNGSGERICHT BESCHLUSS BVerwG 3 B 15.15 OVG 5 B 2.12 In der Verwaltungsstreitsache hat der 3. Senat des Bundesverwaltungsgerichts am 1. März 2016 durch die Richterin am Bundesverwaltungsgericht
Freistaat SACHSEN LANDESDIREKTION SACHSEN HERSTELLUNGSERLAUBNIS. Apotheke des Universitätsklinkums Leipzig AöR
 LANDESDIREKTION SACHSEN Freistaat SACHSEN HERSTELLUNGSERLAUBNIS 1. Nummer der Erlaubnis/Aktenzeichen 2. Name des Erlaubnisinhabers DE_SN_01_MIA_2015_0009/L24-5111/83/1 Universitätsklinikum Leipzig AöR
LANDESDIREKTION SACHSEN Freistaat SACHSEN HERSTELLUNGSERLAUBNIS 1. Nummer der Erlaubnis/Aktenzeichen 2. Name des Erlaubnisinhabers DE_SN_01_MIA_2015_0009/L24-5111/83/1 Universitätsklinikum Leipzig AöR
Bezirksregierung Münster Dezernat 24 Domplatz Münster Fax: +49 (251)
 Bezirksregierungen Münster Anzeige gemäß 67 Abs. 1 u. 2 AMG für die erlaubnisfreie Herstellung von Arzneimitteln durch Ärzte und zur Ausübung der Heilkunde bei Menschen befugten Personen gemäß 13 Abs.
Bezirksregierungen Münster Anzeige gemäß 67 Abs. 1 u. 2 AMG für die erlaubnisfreie Herstellung von Arzneimitteln durch Ärzte und zur Ausübung der Heilkunde bei Menschen befugten Personen gemäß 13 Abs.
Medizinprodukte recht und Apothekenbetriebsordnung
 Medizinprodukte recht und Apothekenbetriebsordnung Rechtstexte mit Einffihrang und Erläuterungen Von Dr. Gert Schorn, Meckenheim/Bonn Regierungsdirektor im Bundesministerium für Gesundheit I &O 1 Deutscher
Medizinprodukte recht und Apothekenbetriebsordnung Rechtstexte mit Einffihrang und Erläuterungen Von Dr. Gert Schorn, Meckenheim/Bonn Regierungsdirektor im Bundesministerium für Gesundheit I &O 1 Deutscher
Stellen von Arzneimitteln für Heimbewohner und erneutes Verblistern
 Stellen von Arzneimitteln für Heimbewohner und erneutes Verblistern Sachstand Rechtliche, organisatorische und technische Probleme Perspektiven Meschede, den 25. Januar 2011 Stellen und Verblistern Lage
Stellen von Arzneimitteln für Heimbewohner und erneutes Verblistern Sachstand Rechtliche, organisatorische und technische Probleme Perspektiven Meschede, den 25. Januar 2011 Stellen und Verblistern Lage
4.1 Anforderungskatalog für die praktische Ausbildung in der Apotheke
 4.1 Anforderungskatalog für die praktische Ausbildung in der Apotheke Ziel der praktischen Ausbildung ist die Erweiterung, Vertiefung und praktische Anwendung der im Studium erworbenen Kenntnisse. Dazu
4.1 Anforderungskatalog für die praktische Ausbildung in der Apotheke Ziel der praktischen Ausbildung ist die Erweiterung, Vertiefung und praktische Anwendung der im Studium erworbenen Kenntnisse. Dazu
GDP-Audit-Checkliste. GMP-Audit-Checkliste. für Lagerung und Transport von Arzneimitteln
 GDP-Audit-Checkliste für Lagerung und Transport von Arzneimitteln Über 700 Fragen mit Referenzen zu GMP-Regelwerken zur Vorbereitung und Durchführung von GDP-Audits PDF Download GMP-Audit-Checkliste Wichtiger
GDP-Audit-Checkliste für Lagerung und Transport von Arzneimitteln Über 700 Fragen mit Referenzen zu GMP-Regelwerken zur Vorbereitung und Durchführung von GDP-Audits PDF Download GMP-Audit-Checkliste Wichtiger
Verordnung über den Betrieb von Apotheken
 Verordnung über den Betrieb von Apotheken Kreis Soest Die Landrätin Arzneimittelüberwachung Soest, den 26. September 2012 Formalien Folie 2 Apothekenbetriebsordnung vom 09. Februar 1987, in der Fassung
Verordnung über den Betrieb von Apotheken Kreis Soest Die Landrätin Arzneimittelüberwachung Soest, den 26. September 2012 Formalien Folie 2 Apothekenbetriebsordnung vom 09. Februar 1987, in der Fassung
WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil II 2. November 2011 in Mainz
 WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil II in Mainz Folie 1 2 Begriffsbestimmungen 3. ist der EG-GMP Leitfaden (BAnz. S. 6887)
WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil II in Mainz Folie 1 2 Begriffsbestimmungen 3. ist der EG-GMP Leitfaden (BAnz. S. 6887)
Seite 1 von 5. Merkblatt. betreffend die
 Seite 1 von 5 Landesuntersuchungsamt Rheinland-Pfalz Institut für Lebensmittelchemie und Arzneimittelprüfung, Mainz Merkblatt betreffend die Kennzeichnung von Arzneimitteln, die in öffentlichen Apotheken
Seite 1 von 5 Landesuntersuchungsamt Rheinland-Pfalz Institut für Lebensmittelchemie und Arzneimittelprüfung, Mainz Merkblatt betreffend die Kennzeichnung von Arzneimitteln, die in öffentlichen Apotheken
Pharmazeutisch-technische/r Assistent/in (PTA) Ausbildung und Tätigkeitsfelder
 Pharmazeutisch-technische/r Assistent/in (PTA) Ausbildung und Tätigkeitsfelder Der PTA-Beruf entsteht Foto: istock Pharmazeutisch-technische/r Assistent/in (PTA) 2 Tätigkeitsbereiche der PTA Insbesondere
Pharmazeutisch-technische/r Assistent/in (PTA) Ausbildung und Tätigkeitsfelder Der PTA-Beruf entsteht Foto: istock Pharmazeutisch-technische/r Assistent/in (PTA) 2 Tätigkeitsbereiche der PTA Insbesondere
Dr. Michael Hörnig Deutsche Arzneimittel Codex Neues Rezeptur Formularium Eschborn
 21. Juni 2016, Berlin DAC Monographie Cannabisblüten Dr. Michael Hörnig Deutsche Arzneimittel Codex Neues Rezeptur Formularium Eschborn Pharmazeutische Qualität Was ist eine Monographie? Das amtliches
21. Juni 2016, Berlin DAC Monographie Cannabisblüten Dr. Michael Hörnig Deutsche Arzneimittel Codex Neues Rezeptur Formularium Eschborn Pharmazeutische Qualität Was ist eine Monographie? Das amtliches
Landesamt für Gesundheit und Soziales
 (mit Änderungen zur Vorversion vom 29.01.2015) Seite 1 von 23 Am 12.06.2012 ist die neue Apothekenbetriebsordnung (ApBetrO) in Kraft getreten. Die für einige Bereiche vorgesehenen Übergangsfristen sind
(mit Änderungen zur Vorversion vom 29.01.2015) Seite 1 von 23 Am 12.06.2012 ist die neue Apothekenbetriebsordnung (ApBetrO) in Kraft getreten. Die für einige Bereiche vorgesehenen Übergangsfristen sind
Führen einer tierärztlichen Hausapotheke in der Kleintierpraxis
 Führen einer tierärztlichen Hausapotheke in der Kleintierpraxis Dr. Anke Litwicki, Dr. Nadine Werth Inhaltsübersicht A Gesetzliche Grundlagen B Allgemeines Verfahren (Ablauf einer Kontrolle) C Schwerpunkte
Führen einer tierärztlichen Hausapotheke in der Kleintierpraxis Dr. Anke Litwicki, Dr. Nadine Werth Inhaltsübersicht A Gesetzliche Grundlagen B Allgemeines Verfahren (Ablauf einer Kontrolle) C Schwerpunkte
Merkblatt für Tierärzte (Stand )
 Merkblatt für Tierärzte (Stand 15.07.2014) Informationen für Tierärzte zu rechtlichen Bestimmungen zum Tierarzneimittelverkehr innerhalb von EU-Mitgliedstaaten bzw. EWR- Vertragsstaaten Grundsatz Verbringungsverbot
Merkblatt für Tierärzte (Stand 15.07.2014) Informationen für Tierärzte zu rechtlichen Bestimmungen zum Tierarzneimittelverkehr innerhalb von EU-Mitgliedstaaten bzw. EWR- Vertragsstaaten Grundsatz Verbringungsverbot
Apothekenbetriebsordnung 2012 Revision QM-System
 Apothekenbetriebsordnung 2012 Revision QM-System in ApoBetrO Detail Regelung im QMS eingearbeitet 2a Qualitätsmanagementsystem Selbstinspektion VA 8.2.4 Interne Audits: Hinweis, dass im Laufe eines Jahres
Apothekenbetriebsordnung 2012 Revision QM-System in ApoBetrO Detail Regelung im QMS eingearbeitet 2a Qualitätsmanagementsystem Selbstinspektion VA 8.2.4 Interne Audits: Hinweis, dass im Laufe eines Jahres
Anforderungen an die Aufbereitung von Medizinprodukten Gesundheitssystem Pflichten Reinigung Desinfektion Sterilisation Haftung
 Positionspapier Anforderungen an die Aufbereitung von Medizinprodukten Pflichten der Hersteller und Pflichten der GesundheitssystemAufbereitun Pflichten Reinigung Desinfektion Sterilisation Haftung Hygiene
Positionspapier Anforderungen an die Aufbereitung von Medizinprodukten Pflichten der Hersteller und Pflichten der GesundheitssystemAufbereitun Pflichten Reinigung Desinfektion Sterilisation Haftung Hygiene
Verordnung über die Bewilligungen im Arzneimittelbereich
 Verordnung über die Bewilligungen im Arzneimittelbereich (Arzneimittel-Bewilligungsverordnung, AMBV) Änderung vom 8. September 2010 Der Schweizerische Bundesrat verordnet: I Die Arzneimittel-Bewilligungsverordnung
Verordnung über die Bewilligungen im Arzneimittelbereich (Arzneimittel-Bewilligungsverordnung, AMBV) Änderung vom 8. September 2010 Der Schweizerische Bundesrat verordnet: I Die Arzneimittel-Bewilligungsverordnung
6. Beschaffenheit, Größe und Einrichtung der Betriebsräume
 Erforderliche Unterlagen für die Antragstellung zur Erteilung einer Großhandelserlaubnis gem. 52 a Arzneimittelgesetz (AMG) im Rahmen einer Apothekenbetriebserlaubnis Dieses Merkblatt bezieht sich auf
Erforderliche Unterlagen für die Antragstellung zur Erteilung einer Großhandelserlaubnis gem. 52 a Arzneimittelgesetz (AMG) im Rahmen einer Apothekenbetriebserlaubnis Dieses Merkblatt bezieht sich auf
WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil XII 25. Januar 2012 in Mainz
 WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil XII in Mainz Folie 1 9 Tätigkeiten im Auftrag (1) Für jede Tätigkeit im Auftrag, insbesondere
WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil XII in Mainz Folie 1 9 Tätigkeiten im Auftrag (1) Für jede Tätigkeit im Auftrag, insbesondere
Krankenhausversorgungsvertrag. ( 14 Apothekengesetz ApoG) Muster
 Krankenhausversorgungsvertrag ( 14 Apothekengesetz ApoG) 2013 Govi-Verlag Pharmazeutischer Verlag GmbH Eschborn Alle Rechte vorbehalten. Ohne ausdrückliche Genehmigung des Verlags ist es nicht gestattet,
Krankenhausversorgungsvertrag ( 14 Apothekengesetz ApoG) 2013 Govi-Verlag Pharmazeutischer Verlag GmbH Eschborn Alle Rechte vorbehalten. Ohne ausdrückliche Genehmigung des Verlags ist es nicht gestattet,
BETRIEBSBESCHREIBUNG FÜR BOR-BEWERTUNG
 Checkliste CL - K 0215.06 Version 6.0 Seite 1 von 5 BETRIEB (Stampiglie des Betriebes) DATUM DER KONTROLLE UHRZEIT (Beginn - Ende) Unterschrift des Anwesenden des Betriebes über die Dauer der Kontrolle
Checkliste CL - K 0215.06 Version 6.0 Seite 1 von 5 BETRIEB (Stampiglie des Betriebes) DATUM DER KONTROLLE UHRZEIT (Beginn - Ende) Unterschrift des Anwesenden des Betriebes über die Dauer der Kontrolle
Die Kontrolle durch die Lebensmittelaufsicht. Die geltende VA - K Steppert Stefan Lebensmittelinspektor
 Die Kontrolle durch die Lebensmittelaufsicht Die geltende VA - K 0211.06 Steppert Stefan Lebensmittelinspektor Lebensmittelkontrolle in NÖ Aufbau der NÖ Lebensmittelaufsicht: Bundesministerium für Gesundheit
Die Kontrolle durch die Lebensmittelaufsicht Die geltende VA - K 0211.06 Steppert Stefan Lebensmittelinspektor Lebensmittelkontrolle in NÖ Aufbau der NÖ Lebensmittelaufsicht: Bundesministerium für Gesundheit
Arbeitshilfe der Bundesapothekerkammer zur Qualitätssicherung. Wasser als Ausgangsstoff zur rezeptur- und defekturmäßigen
 Leitlinie Kommentar Arbeitshilfe Arbeitshilfe der Bundesapothekerkammer zur Qualitätssicherung Wasser als Ausgangsstoff zur rezeptur- und defekturmäßigen Herstellung Anwendungsbeispiel zu den Leitlinien
Leitlinie Kommentar Arbeitshilfe Arbeitshilfe der Bundesapothekerkammer zur Qualitätssicherung Wasser als Ausgangsstoff zur rezeptur- und defekturmäßigen Herstellung Anwendungsbeispiel zu den Leitlinien
AMWHV. Ausfertigungsdatum: Vollzitat:
 Verordnung über die Anwendung der Guten Herstellungspraxis bei der Herstellung von Arzneimitteln und Wirkstoffen und über die Anwendung der Guten fachlichen Praxis bei der Herstellung von Produkten menschlicher
Verordnung über die Anwendung der Guten Herstellungspraxis bei der Herstellung von Arzneimitteln und Wirkstoffen und über die Anwendung der Guten fachlichen Praxis bei der Herstellung von Produkten menschlicher
Umsetzung der Apothekenbetriebsordnung (ApBetrO)
 Arbeitsgruppe Arzneimittel-, Apotheken-, 27. Februar 2014 Transfusions- und Betäubungsmittelwesen (AATB) Umsetzung der Apothekenbetriebsordnung (ApBetrO) (unter Berücksichtigung der durch die 4. Verordnung
Arbeitsgruppe Arzneimittel-, Apotheken-, 27. Februar 2014 Transfusions- und Betäubungsmittelwesen (AATB) Umsetzung der Apothekenbetriebsordnung (ApBetrO) (unter Berücksichtigung der durch die 4. Verordnung
Medizinproduktebuch. Blatt 1. Geräte-Stammdaten Funktionsprüfung Geräteeinweisung... 4
 Medizinproduktebuch Nach 7 MPBetreibV für Medizinprodukte 1 Für das Gerät Inhalt Blatt 1. Geräte-Stammdaten... 2 2. Funktionsprüfung... 3 3. Geräteeinweisung... 4 3.1 Einweisung der vom Betreiber beauftragten
Medizinproduktebuch Nach 7 MPBetreibV für Medizinprodukte 1 Für das Gerät Inhalt Blatt 1. Geräte-Stammdaten... 2 2. Funktionsprüfung... 3 3. Geräteeinweisung... 4 3.1 Einweisung der vom Betreiber beauftragten
Überprüfung der Qualifikation des Personals nach 14, 52a, 63a, 72 Abs. 2 und 74a AMG
 Seite 2 von 5 1 Zweck Diese Verfahrensanweisung regelt das Verfahren zur Feststellung der erforderlichen Qualifikation bei Personen, die eine oder mehrere der folgenden Tätigkeiten auszuüben beabsichtigen:
Seite 2 von 5 1 Zweck Diese Verfahrensanweisung regelt das Verfahren zur Feststellung der erforderlichen Qualifikation bei Personen, die eine oder mehrere der folgenden Tätigkeiten auszuüben beabsichtigen:
Umsetzung der Apothekenbetriebsordnung (ApBetrO)
 Arbeitsgruppe Arzneimittel-, Apotheken-, 14. Februar 2013 Transfusions- und Betäubungsmittelwesen (AATB) Umsetzung der Apothekenbetriebsordnung (ApBetrO) (unter Berücksichtigung der durch die 4. Verordnung
Arbeitsgruppe Arzneimittel-, Apotheken-, 14. Februar 2013 Transfusions- und Betäubungsmittelwesen (AATB) Umsetzung der Apothekenbetriebsordnung (ApBetrO) (unter Berücksichtigung der durch die 4. Verordnung
Betriebsverordnung für pharmazeutische Unternehmer (PharmBetrV)
 Betriebsverordnung für pharmazeutische Unternehmer (PharmBetrV) Anmerkungen: Dieser Text gibt die Betriebsverordnung für pharmazeutische Unternehmer vom 08. März 1985 (BGBl. I S. 546) unter Einarbeitung
Betriebsverordnung für pharmazeutische Unternehmer (PharmBetrV) Anmerkungen: Dieser Text gibt die Betriebsverordnung für pharmazeutische Unternehmer vom 08. März 1985 (BGBl. I S. 546) unter Einarbeitung
Strategische Partnerschaften mit Apotheken in der Onkologie. Die Chancen und Risiken neuer Versorgungskonzepte
 Strategische Partnerschaften mit Apotheken in der Onkologie Die Chancen und Risiken neuer Versorgungskonzepte 11.05.2012 BVDVA - Kongress Die GHD GesundHeits GmbH Deutschland ist das größ ößte ambulante
Strategische Partnerschaften mit Apotheken in der Onkologie Die Chancen und Risiken neuer Versorgungskonzepte 11.05.2012 BVDVA - Kongress Die GHD GesundHeits GmbH Deutschland ist das größ ößte ambulante
Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung
 Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung Dipl.-Kfm. Matthias Klar, IfB Hagenow Tel. 0160 96420022 1 4 Absatz 1 MP BetreibV
Herzlich willkommen zur Veranstaltung: Vorstellung des Kurskonzeptes des BVF zur Umsetzung der MP- Betreiberverordnung Dipl.-Kfm. Matthias Klar, IfB Hagenow Tel. 0160 96420022 1 4 Absatz 1 MP BetreibV
Abnahmeinspektion Begehungsbogen für die aseptische Herstellung von Arzneimitteln in Apotheken
 Abnahmeinspektion Begehungsbogen für die aseptische Herstellung von Arzneimitteln in Apotheken Apotheke Datum: 1. Art und Umfang der Herstellung: 1.1 Herstellung von: Anzahl / hr Zytostatika Antikörperlösungen
Abnahmeinspektion Begehungsbogen für die aseptische Herstellung von Arzneimitteln in Apotheken Apotheke Datum: 1. Art und Umfang der Herstellung: 1.1 Herstellung von: Anzahl / hr Zytostatika Antikörperlösungen
Dokumentationshilfe Einzelhändler - Arzneimittelrecht
 Dokumentationshilfe Einzelhändler - Arzneimittelrecht Besichtigung des Bestandes an Arzneimitteln Fertigarzneimittel Der Einzelhändler bringt nur freiverkäufliche Arzneimittel in den Verkehr ( 43 Abs.
Dokumentationshilfe Einzelhändler - Arzneimittelrecht Besichtigung des Bestandes an Arzneimitteln Fertigarzneimittel Der Einzelhändler bringt nur freiverkäufliche Arzneimittel in den Verkehr ( 43 Abs.
Be- und Verarbeitung von. Anforderungen an Reinräume. Dr. Dr. Jürgen Mählitz, Regierung von von Oberbayern juergen.maehlitz@reg-ob.bayern.
 Be- und Verarbeitung von Gewebe und Gewebezubereitungen gem. 20c AMG; Anforderungen an Reinräume Dr., Regierung von von Oberbayern juergen.maehlitz@reg-ob.bayern.de Rechtliche Rahmenbedingungen (1) Rechtliche
Be- und Verarbeitung von Gewebe und Gewebezubereitungen gem. 20c AMG; Anforderungen an Reinräume Dr., Regierung von von Oberbayern juergen.maehlitz@reg-ob.bayern.de Rechtliche Rahmenbedingungen (1) Rechtliche
Verordnung zur Ablösung der Betriebsverordnung für pharmazeutische Unternehmer
 Bundesgesetzblatt Jahrgang 2006 Teil I Nr. 51, ausgegeben zu Bonn am 9. November 2006 2523 Verordnung zur Ablösung der Betriebsverordnung für pharmazeutische Unternehmer Vom 3. November 2006 Es verordnen
Bundesgesetzblatt Jahrgang 2006 Teil I Nr. 51, ausgegeben zu Bonn am 9. November 2006 2523 Verordnung zur Ablösung der Betriebsverordnung für pharmazeutische Unternehmer Vom 3. November 2006 Es verordnen
Zu Artikel 1 Nummer 1a ( 4 Absatz 18 Satz 2 AMG) (Definition pharmazeutischer Unternehmer)
 Änderungsantrag 1 Zu Artikel 1 Nummer 1a ( 4 Absatz 18 Satz 2 AMG) (Definition pharmazeutischer Unternehmer) In 4 Absatz 18 werden in Satz 2 nach dem Wort Arzneimittel die Wörter im Parallelvertrieb oder
Änderungsantrag 1 Zu Artikel 1 Nummer 1a ( 4 Absatz 18 Satz 2 AMG) (Definition pharmazeutischer Unternehmer) In 4 Absatz 18 werden in Satz 2 nach dem Wort Arzneimittel die Wörter im Parallelvertrieb oder
Änderungskontrolle. Anforderungen / Zitate aus den Rechtsvorschriften
 Änderungskontrolle Anforderungen / Zitate aus den Rechtsvorschriften Definition im Glossar zum Annex 15 (Qualifizierung und Validierung) des EU-GMP-Leitfadens: Die Änderungskontrolle ist ein formales System,
Änderungskontrolle Anforderungen / Zitate aus den Rechtsvorschriften Definition im Glossar zum Annex 15 (Qualifizierung und Validierung) des EU-GMP-Leitfadens: Die Änderungskontrolle ist ein formales System,
Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und Aufbereitungsverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen
 Seite 1 von 8 Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und sverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen Inhalt: Unterscheidung aufgrund von Verwendungszweck und sverfahren Risikobewertung
Seite 1 von 8 Anlage 4 zur Hygiene-VO der ÖÄK Risikobewertung und sverfahren für Medizinprodukte in Ordinationen und Gruppenpraxen Inhalt: Unterscheidung aufgrund von Verwendungszweck und sverfahren Risikobewertung
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Prüfung und Lagerung der Ausgangsstoffe
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 16.06.2016 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 16.06.2016 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Verordnung über das Inverkehrbringen von Arzneimitteln ohne Genehmigung oder ohne Zulassung in Härtefällen (Arzneimittel- Härtefall-Verordnung - AMHV)
 Verordnung über das Inverkehrbringen von Arzneimitteln ohne Genehmigung oder ohne Zulassung in Härtefällen (Arzneimittel- Härtefall-Verordnung - AMHV) AMHV Ausfertigungsdatum: 14.07.2010 Vollzitat: "Arzneimittel-Härtefall-Verordnung
Verordnung über das Inverkehrbringen von Arzneimitteln ohne Genehmigung oder ohne Zulassung in Härtefällen (Arzneimittel- Härtefall-Verordnung - AMHV) AMHV Ausfertigungsdatum: 14.07.2010 Vollzitat: "Arzneimittel-Härtefall-Verordnung
LABORGEMEINSCHAFT FÜR HÄMATOLOGIE UND ONKOLOGIE
 LABORGEMEINSCHAFT FÜR HÄMATOLOGIE UND ONKOLOGIE KOMPETENZ. VERANTWORTUNG. PRÄZISION. UNTERNEHMEN UND PHILOSOPHIE LGHO die Laborgemeinschaft für Hämatologie und Onkologie stellt sterile, flüssige Arzneimittel
LABORGEMEINSCHAFT FÜR HÄMATOLOGIE UND ONKOLOGIE KOMPETENZ. VERANTWORTUNG. PRÄZISION. UNTERNEHMEN UND PHILOSOPHIE LGHO die Laborgemeinschaft für Hämatologie und Onkologie stellt sterile, flüssige Arzneimittel
Workshop on the EU Clinical Trials Directive. GMP für Prüfpräparate und die Rolle der sachkundigen Person
 Workshop on the EU Clinical Trials Directive GMP für Prüfpräparate und die Rolle der sachkundigen Person Dr. Gabriele Wanninger Bayer. Landesamt für Klinische Prüfung von Arzneimitteln Ethikkommission
Workshop on the EU Clinical Trials Directive GMP für Prüfpräparate und die Rolle der sachkundigen Person Dr. Gabriele Wanninger Bayer. Landesamt für Klinische Prüfung von Arzneimitteln Ethikkommission
Sauberkeit und Hygiene
 Sauberkeit und Hygiene Spirig Pharma AG 18.10.2012, C. Laeri Inhalt Rechtliche Grundlagen «Schmutz»-Quellen Massnahmen dagegen Überprüfung der Massnahmen Gesetzliche Grundlagen EU-GMP Leitfaden: Gute Herstellpraxis
Sauberkeit und Hygiene Spirig Pharma AG 18.10.2012, C. Laeri Inhalt Rechtliche Grundlagen «Schmutz»-Quellen Massnahmen dagegen Überprüfung der Massnahmen Gesetzliche Grundlagen EU-GMP Leitfaden: Gute Herstellpraxis
Praxisorganisation. Swissmedic-Richtlinien zur Sterilisation und Arzneimittelaufbewahrung aus Sicht des Kantonsapothekers
 1 Praxisorganisation Swissmedic-Richtlinien zur Sterilisation und Arzneimittelaufbewahrung aus Sicht des Kantonsapothekers 2 1. Führung einer zahnärztlichen Privatapotheke 1.1 Rechtliche Grundsätze Kanton
1 Praxisorganisation Swissmedic-Richtlinien zur Sterilisation und Arzneimittelaufbewahrung aus Sicht des Kantonsapothekers 2 1. Führung einer zahnärztlichen Privatapotheke 1.1 Rechtliche Grundsätze Kanton
Ein dynamisch agierendes Unternehmen mit soliden Werten, die von alle Mitarbeitern im Unternehmen gelebt werden.
 Ein dynamisch agierendes Unternehmen mit soliden Werten, die von alle Mitarbeitern im Unternehmen gelebt werden. Das Unternehmen Seit dem Gründungsjahr 1993 hat sich Euro OTC Pharma zu einem maßgeblichen
Ein dynamisch agierendes Unternehmen mit soliden Werten, die von alle Mitarbeitern im Unternehmen gelebt werden. Das Unternehmen Seit dem Gründungsjahr 1993 hat sich Euro OTC Pharma zu einem maßgeblichen
Fortbildung der LAK Nordrhein in Köln 24. September 2012. Amtsapothekerin Monika Paul
 Fortbildung der LAK Nordrhein in Köln 24. September 2012 Amtsapothekerin Apothekenbetriebsräume Einrichtung und Ausstattung Personal Pharmazeutische Tätigkeiten QMS Hygienemaßnahmen Herstellung Erwerb
Fortbildung der LAK Nordrhein in Köln 24. September 2012 Amtsapothekerin Apothekenbetriebsräume Einrichtung und Ausstattung Personal Pharmazeutische Tätigkeiten QMS Hygienemaßnahmen Herstellung Erwerb
