Carvedilol - 1 A Pharma
|
|
|
- Magdalena Bösch
- vor 8 Jahren
- Abrufe
Transkript
1 Stand: August BEZEICHNUNG DER ARZNEIMITTEL 3,125 mg Tabletten 6,25 mg Tabletten 12,5 mg Tabletten 25 mg Tabletten 50 mg Tabletten 2. QUALITATIVE UND QUANTITATIVE ZU- SAMMENSETZUNG 1 Tablette enthält 3,125 mg/6,25 mg/12,5 mg/ 25 mg/50 mg Carvedilol. Sonstiger Bestandteil mit bekannter Wirkung: Lactose-Monohydrat Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt DARREICHUNGSFORM Tablette Carvedilol - 1 A Pharma 3,125 mg Tabletten Hellrote, runde, konvexe, teilbare Tablette C1. Carvedilol - 1 A Pharma 6,25 mg Tabletten Gelbe, runde, konvexe, teilbare Tablette C2. Carvedilol - 1 A Pharma 12,5 mg Tabletten Altrosa, runde, konvexe, teilbare Tablette C3. Carvedilol - 1 A Pharma 25 mg Tabletten Weiße, runde, konvexe, teilbare Tablette C4. Carvedilol - 1 A Pharma 50 mg Tabletten Weiße, runde, konvexe, teilbare Tablette C5. 4. KLINISCHE ANGABEN 4.1 Anwendungsgebiete Essentielle Hypertonie Chronisch stabile Angina pectoris Zusatzbehandlung bei mäßiger bis schwerer stabiler Herzinsuffizienz 4.2 Dosierung und Art der Anwendung Dosierung Carvedilol ist in 5 Stärken erhältlich: 3,125 mg, 6,25 mg, 12,5 mg, 25 mg und 50 mg. Essentielle Hypertonie Carvedilol kann zur Behandlung der Hypertonie allein oder in Kombination mit anderen Antihypertonika, insbesondere Thiazid-Diuretika, verwendet werden. Eine einmal tägliche Dosierung wird empfohlen, die empfohlene maximale Einzeldosis beträgt jedoch 25 mg und die empfohlene maximale Tagesdosis beträgt 50 mg. Erwachsene: Die empfohlene Initialdosis beträgt einmal täglich 12,5 mg für zwei Tage. Danach wird die Behandlung mit einer Dosis von 25 mg/tag fortgesetzt. Die Dosis kann gegebenenfalls schrittweise in Intervallen von zwei Wochen oder in größeren Abständen weiter erhöht werden. Ältere Patienten: Bei Hypertonie beträgt die empfohlene Initialdosis einmal täglich 12,5 mg. Diese Dosis kann auch für die Weiterbehandlung ausreichend sein. Bei ungenügender Wirkung kann die Dosis jedoch schrittweise in Intervallen von zwei Wochen oder in größeren Abständen erhöht werden. Chronisch stabile Angina pectoris Erwachsene: Die empfohlene Initialdosis beträgt zweimal täglich 12,5 mg für zwei Tage. Danach wird die Behandlung mit einer Dosis von zweimal täglich 25 mg fortgesetzt. Die Dosis kann gegebenenfalls schrittweise in Intervallen von zwei Wochen oder in größeren Abständen weiter erhöht werden. Die empfohlene Tageshöchstdosis beträgt 100 mg, verteilt auf zwei Dosen. Ältere Patienten: Die empfohlene Initialdosis beträgt zweimal täglich 12,5 mg für 2 Tage. Danach wird die Behandlung mit einer Dosis von zweimal täglich 25 mg fortgesetzt, welche auch die empfohlene Tageshöchstdosis ist. Herzinsuffizienz Behandlung einer mäßigen bis schweren Herzinsuffizienz zusätzlich zu einer konventionellen Basistherapie mit Diuretika, ACE-Hemmern, Digitalis und/oder Vasodilatatoren. Der Patient sollte klinisch stabil sein (keine Änderung der NYHA-Klasse, keine Hospitalisierung wegen einer Herzinsuffi zienz) und die Basistherapie muss mindestens 4 Wochen vor Behandlungsbeginn eingestellt worden sein. Außerdem sollte der Patient eine verminderte linksventrikuläre Ejektionsfraktion aufweisen, die Herzfrequenz sollte > 50 Schläge pro Minute betragen und der systolische Blutdruck > 85 mmhg (siehe 4.3. Gegenanzeigen ). Die Initialdosis beträgt zweimal täglich 3,125 mg Carvedilol für zwei Wochen. Wenn die Initialdosis gut vertragen wird, kann die Carvedilol-Dosis in Intervallen von zwei Wochen oder in größeren Abständen zuerst auf zweimal täglich 6,25 mg, dann auf zweimal täglich 12,5 mg und danach auf zweimal täglich 25 mg er- höht werden. Es wird empfohlen, die höchste vom Patienten tolerierte Dosis anzustreben. Die empfohlene Maximaldosis beträgt zweimal täglich 25 mg bei Patienten mit einem Körpergewicht unter 85 kg und zweimal täglich 50 mg bei Patienten mit einem Körpergewicht über 85 kg, vorausgesetzt, dass keine schwere Herzinsuffizienz vorliegt. Eine Dosiserhöhung auf zweimal täglich 50 mg sollte unter engmaschiger ärztlicher Überwachung erfolgen. Zu Therapiebeginn oder aufgrund einer Dosiserhöhung kann eine vorübergehende Verschlechterung der Symptome der Herzinsuffizienz auftreten, insbesondere bei Patienten mit schwerer Herzinsuffi - zienz und/oder hochdosierter Diuretikatherapie. Dies erfordert üblicherweise keinen Abbruch der Behandlung, die Dosis sollte jedoch nicht erhöht werden. Nach Behandlungsbeginn oder Dosiserhöhung sollte der Patient von einem Internisten/ Kardiologen überwacht werden. Vor jeder Erhöhung der Dosis sollte eine Untersuchung im Hinblick auf potentielle Symptome einer Verschlechterung der Herzinsuffizienz oder Symptome einer übermäßigen Vasodilatation (z. B. Nierenfunktion, Körpergewicht, Blutdruck, Herzfrequenz und -rhythmus) stattfinden. Eine Verschlechterung der Herzinsuffizienz oder Flüssigkeitsretention wird durch eine Erhöhung der Diuretika-Dosierung behandelt; die Dosis von Carvedilol sollte erst erhöht werden, wenn der klinische Zustand des Patienten stabil ist. Bei Bradykardie oder Verzögerung der AV-Überleitung sollte zunächst der Digoxinspiegel überprüft werden. Eine Reduktion der Carvedilol-Dosis oder vorübergehendes Absetzen der Behandlung kann gelegentlich notwendig sein. Auch in diesen Fällen kann die Einstellung der Carvedilol-Dosis häufig erfolgreich fortgesetzt werden. Falls die Carvedilol-Therapie länger als zwei Wochen unterbrochen wurde, sollte sie mit zweimal täglich 3,125 mg wieder aufgenommen werden und erneut eine schrittweise Erhöhung - gemäß obiger Empfehlungen - erfolgen. Niereninsuffizienz Die Dosierung muss für jeden Patienten individuell festgelegt werden, es gibt jedoch aufgrund der pharmakokinetischen Parameter keine Hinweise darauf, dass eine Dosisanpassung von Carvedilol bei Patienten mit Herzinsuffizienz erforderlich ist. Mäßige Leberfunktionsstörung Eine Anpassung der Dosis kann erforderlich sein
2 Kinder und Jugendliche (< 18 Jahre) Es liegen nur unzureichende Daten über die Wirksamkeit und Unbedenklichkeit von Carvedilol vor. Ältere Patienten Ältere Patienten können empfindlicher auf Carvedilol reagieren und sollten sorgfältiger überwacht werden. Wie bei anderen Betablockern und insbesondere bei Koronarpatienten sollte Carvedilol schrittweise abgesetzt werden (siehe 4.4. Warnhinweise und Vorsichtsmaßnahmen für die Anwendung ). Art der Anwendung Die Einnahme der Tabletten kann unabhängig von einer Mahlzeit erfolgen. Es wird jedoch Patienten mit Herzinsuffizienz empfohlen, die Tabletten mit Nahrung zu sich zu nehmen, damit Carvedilol langsamer resorbiert und das Risiko einer orthostatischen Hypotonie vermindert wird. 4.3 Gegenanzeigen Überempfi ndlichkeit gegen Carvedilol oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile Instabile/dekompensierte Herzinsuffi - zienz Klinisch manifeste Leberfunktionsstörung Bronchospasmus oder Asthma in der Anamnese AV-Block II. oder III. Grades (sofern kein permanenter Schrittmacher vorhanden) Schwere Bradykardie (< 50 Schläge pro Minute) Kardiogener Schock Sinusknotensyndrom (einschließlich sinuatrialer Block) Schwere Hypotonie (systolischer Blutdruck unter 85 mmhg) 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Chronisch dekompensierte Herzinsuffizienz Bei Patienten mit dekompensierter Herzinsuffizienz kann es während einer Dosiserhöhung von Carvedilol zu einer Verschlechterung der Herzinsuffizienz oder Flüssigkeitsretention kommen. Bei Auftreten solcher Symptome sollten die Diuretika-Dosis erhöht und die Carvedilol-Dosis nicht weiter erhöht werden, bis eine klinische Stabilisierung erfolgt ist. Gelegentlich kann es erforderlich sein, die Carvedilol- Dosis zu senken oder seltenen Fällen die Gabe zu unterbrechen. Derartige Episoden schließen eine erfolgreiche Dosiseinstellung von Carvedilol nicht von vorneherein aus. Carvedilol ist in Kombination mit Digitalisglykosiden mit Vorsicht anzuwenden, da beide Wirkstoffe die AV- Überleitung verzögern. Nierenfunktion bei dekompensierter Herzinsuffizienz Eine reversible Verschlechterung der Nierenfunktion wurde bei Patienten mit chronischer Herzinsuffi zienz und Hypotonie (systolischer Blutdruck <100 mmhg), ischämischer Herzerkrankung und diffuser Gefäßerkrankung und/oder zugrunde liegender Niereninsuffizienz unter Carvedilol-Therapie beobachtet. Linksventrikuläre Dysfunktion nach akutem Myokardinfarkt Vor Einleitung der Behandlung mit Carvedilol muss der Patient klinisch stabil sein und sollte mindestens über die vorangegangenen 48 Stunden einen ACE-Hemmer erhalten haben, wobei die Dosis des ACE-Hemmers mindestens über die vorangegangenen 24 Stunden stabil gewesen sein sollte. Chronisch-obstruktive Lungenerkrankung Carvedilol sollte bei Patienten mit chronisch-obstruktiver Lungenerkrankung (COPD) mit bronchospastischer Komponente, die nicht unter oraler oder inhalativer Medikation stehen, mit Vorsicht und nur dann angewendet werden, wenn der potenzielle Nutzen gegenüber dem potenziellen Risiko überwiegt. Bei Patienten mit einer Neigung zu Bronchospasmus kann es infolge eines möglichen Anstiegs des Atemwegswiderstands zu Atemnot kommen. Die Patienten sind während der Einleitung der Behandlung mit und Auftitrierung von Carvedilol engmaschig zu überwachen, und die Carvedilol-Dosis ist zu senken, falls unter der Behandlung Hinweise auf Bronchospasmus beobachtet werden. Diabetes Bei der Verabreichung von Carvedilol an Patienten mit Diabetes mellitus ist mit Vorsicht vorzugehen, da die frühen Anzeichen und Symptome einer akuten Hypoglykämie maskiert oder abgeschwächt sein können. Bei Diabetikern mit chronischer Herzinsuffi zienz kann die Anwendung von Carvedilol mit einer schlechteren Blutglukoseeinstellung einhergehen. Periphere Gefäßerkrankung Carvedilol ist bei Patienten mit peripherer Gefäßerkrankung mit Vorsicht anzuwenden, da durch Betablocker die Symptome einer Arterieninsuffizienz ausgelöst oder verschlimmert werden können. Raynaud-Phänomen Carvedilol ist bei Patienten mit peripheren Durchblutungsstörungen (z. B. Raynaud- Phänomen) mit Vorsicht anzuwenden, da es zu einer Exazerbation der Symptomatik kommen kann. Hyperthyreose Carvedilol kann die Symptome einer Hyperthyreose maskieren. Anästhesie und große operative Eingriffe Bei Patienten, die sich einem allgemeinchirurgischen Eingriff unterziehen, ist aufgrund der synergistischen negativ inotropen Wirkungen von Carvedilol und Anästhetika mit Vorsicht vorzugehen. Bradykardie Carvedilol kann zu Bradykardie führen. Fällt die Pulsfrequenz des Patienten auf unter 55 Schläge/Minute, ist die Carvedilol-Dosis zu senken. Überempfindlichkeit Bei der Verabreichung von Carvedilol an Patienten mit schweren Überempfindlichkeitsreaktionen in der Anamnese sowie bei Patienten unter Desensibilisierungstherapie ist mit Vorsicht vorzugehen, da Betablocker sowohl die Empfindlichkeit gegenüber Allergenen als auch die Schwere einer anaphylaktischen Reaktion erhöhen können. Psoriasis Patienten mit Psoriasis im Zusammenhang mit einer Betablocker-Therapie in der Anamnese sollten Carvedilol nur nach Abwägung des Nutzen/Risiko-Verhältnisses einnehmen. Gleichzeitige Anwendung von Kalziumantagonisten Bei Patienten, die gleichzeitig mit Kalziumantagonisten des Verapamil- oder Diltiazemtyps oder mit anderen Antiarrhythmika behandelt werden, ist eine sorgfältige Überwachung des EKG und des Blutdrucks erforderlich. Phäochromozytom Bei Patienten mit Phäochromozytom ist vor jeder Anwendung eines Betablockers die Behandlung mit einem Alphablocker einzuleiten. Auch wenn Carvedilol pharmakologisch sowohl alpha- als auch betablockierend wirkt, liegen keine Erfahrungen mit seiner Anwendung bei dieser Erkrankung vor. Daher sollte die Verabreichung von Carvedilol an Patienten mit Verdacht auf Phäochromozytom mit Vorsicht erfolgen. Prinzmetal-Angina Substanzen mit nicht selektiver betablockierender Wirkung können bei Patienten mit Prinzmetal-Angina Brustschmerzen auslösen. Es liegen keine klinischen Erfahrungen mit Carvedilol bei diesen Patienten vor, auch wenn die alphablockierende Wirkung von Carvedilol u. U. das Auftreten derartiger Symptome verhindert. Bei der 2
3 Verabreichung von Carvedilol an Patienten mit Verdacht auf Prinzmetal-Angina ist dennoch mit Vorsicht vorzugehen. Kontaktlinsen Kontaktlinsenträger sollten eine mögliche verminderte Bildung von Tränenflüssigkeit berücksichtigen. Entzugssyndrom Die Behandlung mit Carvedilol darf nicht abrupt abgesetzt werden. Dies gilt insbesondere für Patienten mit ischämischer Herzerkrankung. Carvedilol sollte über einen Zeitraum von zwei Wochen ausgeschlichen werden. Doping Die Anwendung von Carvedilol kann bei Dopingkontrollen zu positiven Ergebnissen führen. Eine missbräuchliche Anwendung des Arzneimittels zu Dopingzwecken kann die Gesundheit gefährden. Lactose Dieses Arzneimittel enthält Lactose. Patienten mit den seltenen vererbbaren Problemen einer Galaktose-Intoleranz, Lapp- Laktasemangel oder Glukose-Galaktose- Malabsorption sollten dieses Medikament nicht einnehmen. 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Pharmakokinetische Wechselwirkungen Carvedilol ist ein Substrat und ein Hemmer von P-Glykoprotein. Daher kann die Bioverfügbarkeit von Wirkstoffen, die über P-Glykoprotein transportiert werden, bei gleichzeitiger Verabreichung mit Carvedilol erhöht sein. Darüber hinaus kann die Bioverfügbarkeit von Carvedilol durch Induktoren oder Inhibitoren von P-Glykoprotein verändert werden. Inhibitoren sowie Induktoren von CYP2D6 und CYP2C9 können die systemische und/oder präsystemische Verstoffwechslung von Carvedilol stereoselektiv modifizieren, was zu erhöhten bzw. verminderten Plasmaspiegeln von R- und S-Carvedilol führt. Einige bei Patienten oder gesunden Probanden beobachteten Beispiele sind im Folgenden aufgelistet, wobei die Aufzählung jedoch nicht erschöpfend ist. Digoxin: Es kommt zu einer Erhöhung der Digoxinspiegel um ca. 15 %, wenn Digoxin und Carvedilol gleichzeitig verabreicht werden. Sowohl Digoxin als auch Carvedilol verzögern die AV-Überleitung. Bei Einleitung, Titrierung oder Absetzen von Carvedilol wird eine verstärkte Überwachung der Digoxinspiegel empfohlen (siehe Abschnitt 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung ). Rifampicin: In einer Studie mit 12 gesunden Probanden führte die Verabreichung von Rifampicin zu einer Senkung des Carvedilol-Plasmaspiegels um ca. 70 %, höchstwahrscheinlich über eine durch die Induktion von P-Glykoprotein bedingte Verminderung der intestinalen Resorption von Carvedilol. Cyclosporin: Zwei Studien mit Patienten nach Nieren- und Herztransplantation, die oral Cyclosporin erhielten, haben einen Anstieg der Cyclosporin-Plasmaspiegel nach Einleitung der Carvedilolbehandlung ergeben. Bei etwa 30 % der Patienten musste die Cyclosporindosis gesenkt werden, um die Cyclosporinspiegel innerhalb des therapeutischen Bereichs zu halten, während bei den übrigen Patienten keine Anpassung erforderlich war. Durchschnittlich wurde die Cyclosporindosis bei rund 20 % dieser Patienten gesenkt. Aufgrund der erheblichen interindividuellen Schwankungen bezüglich der erforderlichen Dosisanpassung ist es empfehlenswert, nach Einleitung der Carvedilolbehandlung den Cyclosporinspiegel engmaschig zu kontrollieren und die Cyclosporindosis gegebenenfalls anzupassen. Amiodaron: Bei Patienten mit Herzinsuffizienz verringerte Amiodaron die Clearance von S-Carvedilol, wahrscheinlich durch Hemmung von CYP2C9. Der mittlere Plasmaspiegel von R-Carvedilol war unverändert. Infolgedessen besteht das potenzielle Risiko einer verstärkten beta- Blockade bedingt durch einen Anstieg der S-Carvedilol-Plasmakonzentration. Fluoxetin: In einer randomisierten Crossover-Studie an 10 Patienten mit Herzinsuffizienz führte die gleichzeitige Anwendung von Fluoxetin, einem starken CYP2D6-Hemmer, zu einer stereoselektiven Hemmung des Carvedilolstoffwechsels mit einem Anstieg der mittleren AUC für das R(+)-Enantiomer um 77 %. Es wurden zwischen den Behandlungsgruppen jedoch keine Unterschiede in Bezug auf unerwünschte Ereignisse, Blutdruck oder Herzfrequenz festgestellt. Pharmakodynamische Wechselwirkungen Insulin oder orale Hypoglykämika: Substanzen mit betablockierenden Eigenschaften können den Blutglukose senkenden Effekt von Insulin und oralen Hypoglykämika verstärken. Die Anzeichen einer Hypoglykämie (insbesondere Tachykardie) können maskiert oder abgeschwächt sein. Bei Patienten unter Insulin oder oralen Hypoglykämika wird daher eine regelmäßige Überwachung der Blutglukosewerte empfohlen. Katecholamin abbauende Substanzen: Patienten, die Substanzen mit betablockie- renden Eigenschaften sowie einen Wirkstoff anwenden, der Katecholamine abbaut (z. B. Reserpin und Monoaminoxidasehemmer), sind engmaschig auf Anzeichen von Hypotonie und/oder schwere Bradykardie zu überwachen. Digoxin: Die kombinierte Anwendung von Betablockern und Digoxin kann zur additiven Verlängerung der atrioventrikulären (AV) Überleitungszeit führen. Verapamil, Diltiazem, Amiodaron oder andere Antiarrhythmika: In Kombination mit Carvedilol können diese Wirkstoffe das Risiko von AV-Überleitungsstörungen erhöhen (siehe Abschnitt 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung ). Clonidin: Durch die gleichzeitige Verabreichung von Clonidin und Wirkstoffen mit betablockierenden Eigenschaften können die Blutdruck und Herzfrequenz senkenden Effekte verstärkt werden. Soll die gleichzeitige Behandlung mit Substanzen mit betablockierenden Eigenschaften und Clonidin beendet werden, ist der betablockierende Wirkstoff als erstes abzusetzen. Die Clonidin-Therapie kann dann einige Tage später durch schrittweise Senkung der Dosis abgesetzt werden. Kalziumantagonisten (siehe Abschnitt 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung ): In Einzelfällen werden bei gleichzeitiger Verabreichung von Carvedilol mit Diltiazem Überleitungsstörungen (selten mit hämodynamischer Beeinträchtigung) beobachtet. Wie bei anderen Substanzen mit betablockierenden Eigenschaften ist bei einer oralen Verabreichung von Carvedilol mit Kalziumantagonisten des Verapamil- oder Diltiazemtyps eine Überwachung von EKG und Blutdruck empfehlenswert. Antihypertonika: Wie andere Substanzen mit betablockierender Wirkung kann auch Carvedilol die Wirkung anderer gleichzeitig verabreichter Arzneimittel, die Blutdruck senkende Eigenschaften besitzen (z. B. alpha 1 -Rezeptorantagonisten) oder bei denen Hypotonie zum Nebenwirkungsprofil gehört, verstärken. Anästhetika: Während der Gabe von Anästhetika wird aufgrund der synergistischen negativ inotropen und hypotonischen Effekte von Carvedilol und Anästhetika eine sorgfältige Überwachung der Vitalzeichen empfohlen (siehe Abschnitt 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung ). NSAR: Die gleichzeitige Anwendung nicht steroidaler Antiphlogistika (NSAR) und beta- 3
4 adrenerger Blocker kann zu Blutdruckanstieg und verschlechterter Blutdruckkontrolle führen. Beta-agonistische Bronchodilatatoren: Nicht kardioselektive Betablocker wirken den bronchodilatierenden Wirkungen betaagonistischer Bronchodilatatoren entgegen. Eine sorgfältige Überwachung der Patienten wird empfohlen. 4.6 Fertilität, Schwangerschaft und Stillzeit Schwangerschaft Es liegen keine ausreichenden klinischen Erfahrungen mit einer Anwendung von Carvedilol in der Schwangerschaft vor. Tierexperimentelle Studien sind in Bezug auf Auswirkungen auf die Schwangerschaft, die embryonale/fetale Entwicklung, die Geburt und die postnatale Entwicklung nicht ausreichend (siehe Abschnitt 5.3). Das potenzielle Risiko für den Menschen ist unbekannt. Carvedilol sollte während der Schwangerschaft nicht angewendet werden, sofern der potenzielle Nutzen nicht gegenüber den potenziellen Risiken überwiegt. Betablocker vermindern die Plazentaperfusion. In der Folge kann es zum intrauterinen Fruchttod des Fetus, zu Fehl- und Frühgeburten kommen. Außerdem können sowohl beim Feten als auch beim Neugeborenen schädigende Nebenwirkungen auftreten (insbesondere Hypoglyk ämie und Bradykardie, Atemdepression und Hypothermie). Für das Neugeborene kann in der postnatalen Phase u. U. ein erhöhtes Risiko hinsichtlich kardialer und pulmonaler Komplikationen bestehen. Tierexperimentelle Studien ergaben keine substanziellen Hinweise auf eine Teratogenität unter Carvedilol (siehe auch Abschnitt 5.3). Stillzeit In tierexperimentellen Studien wurde nachgewiesen, dass Carvedilol bzw. seine Metaboliten in die Muttermilch ausgeschieden werden. Es ist nicht bekannt, ob Carvedilol in die Muttermilch übergeht. Das Stillen während der Behandlung mit Carvedilol wird daher nicht empfohlen. 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Es wurden keine Studien zu den Auswirkungen von Carvedilol auf die Verkehrstüchtigkeit der Patienten und die Fähigkeit zum Bedienen von Maschinen durchgeführt. Aufgrund der individuell unterschiedlich stark ausgeprägten Reaktionen (z. B. Schwindel, Müdigkeit) kann die Verkehrstüchtigkeit, die Fähigkeit zum Bedienen von Maschinen oder das Arbeiten ohne feste Unterstützung eingeschränkt sein. Dies gilt insbesondere für den Beginn der Behandlung, nach einer Dosiserhöhung, bei einer Umstellung auf andere Arzneimittel und in Kombination mit Alkohol. 4.8 Nebenwirkungen (a) Zusammenfassung des Sicherheitsprofils Die Häufigkeit unerwünschter Nebenwirkungen ist mit Ausnahme von Schwindel, anomalem Sehen und Bradykardie - nicht dosisabhängig. (b) Verzeichnis der unerwünschten Wirkungen Das Risiko der meisten im Zusammenhang mit Carvedilol auftretenden unerwünschten Wirkungen ist bei allen Anwendungsgebieten vergleichbar. Ausnahmen werden in Unterabschnitt (c) beschrieben. Folgende Häufi gkeitskategorien werden zugrunde gelegt: Sehr häufig ( 1/10) Häufig ( 1/100 bis < 1/10) Gelegentlich ( 1/1.000 bis < 1/100) Selten ( 1/ bis < 1/1.000) Sehr selten (< 1/10.000) Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar) siehe Tabelle, Seite 5 (c) Beschreibung ausgewählter Nebenwirkungen Schwindel, Synkope, Kopfschmerzen und Asthenie sind in der Regel leicht ausgeprägt und treten mit größerer Wahrscheinlichkeit zu Beginn der Behandlung auf. Bei Patienten mit dekompensierter Herzinsuffizienz kann es unter einer Erhöhung der Carvediloldosis zu einer Verschlechterung der Herzinsuffizienz und Flüssigkeitsretention kommen (siehe Abschnitt 4.4). Herzinsuffizienz ist bei Patienten sowohl unter Placebo als auch unter Carvedilol ein häufig berichtetes unerwünschtes Ereignis (14,5 % bzw. 15,4 % bei Patienten mit linksventrikulärer Dysfunktion nach akutem Myokardinfarkt). Eine reversible Verschlechterung der Nierenfunktion wurde unter Carvediloltherapie bei Patienten mit chronischer Herzinsuffizienz und Hypotonie, ischämischer Herzerkrankung und diffuser Gefäßerkrankung und/oder zugrunde liegender Niereninsuffizienz beobachtet (siehe Abschnitt 4.4). Beta-adrenerge Rezeptorblocker können als Wirkstoffklasse insgesamt zur Manifestation eines latenten Diabetes mellitus führen, manifester Diabetes kann sich verschlechtern, und die Kontrolle der Blutglucose kann beeinträchtigt sein. Carvedilol kann bei Frauen zu Harninkontinenz führen, die bei Absetzen der Behandlung reversibel ist. Meldung des Verdachts auf Nebenwirkungen Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen- Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte Abt. Pharmakovigilanz Kurt-Georg-Kiesinger-Allee 3 D Bonn Website: anzuzeigen. 4.9 Überdosierung Symptome und Anzeichen Bei Überdosierung kann es zu schwerer Hypotonie, Bradykardie, Herzinsuffizienz, kardiogenem Schock und Herzstillstand kommen. Zusätzlich können Atembeschwerden, Bronchospasmen, Erbrechen, Bewusstseinsstörungen und generalisierte Krampfanfälle auftreten. Behandlung Neben allgemeinen unterstützenden Maßnahmen muss unter intensivmedizinischen Bedingungen die Überwachung und gegebenenfalls Korrektur der Vitalparameter erfolgen. Atropin kann bei exzessiver Bradykardie angewendet werden, während zur Unterstützung der Ventrikelfunktion intravenöses Glukagon oder Sympathomimetika (Dobutamin, Isoprenalin) empfohlen werden. Soll eine positiv inotrope Wirkung erzielt werden, sind Phosphodiesterasehemmer (PDE) in Betracht zu ziehen. Ist eine periphere Vasodilatation das beherrschende Symptom des Intoxikationsprofils, sind unter kontinuierlicher Kreislaufüberwachung Norfenephrin oder Noradrenalin zu verabreichen. Bei therapierefraktärer Bradykardie ist eine Schrittmachertherapie einzuleiten. Bei Bronchospasmus sollten Beta-Sympathomimetika (als Aerosol oder intravenös) oder aber Aminophyllin intravenös als langsame Injektion oder Infusion gegeben werden. Bei Krampfanfällen wird die langsame intravenöse Injektion von Diazepam oder Clonazepam empfohlen. Bei schwerer Überdosierung mit Schocksymptomatik muss die unterstützende 4
5 Infektionen und parasitäre Erkrankungen Erkrankungen des Blutes und des Lymphsystems Erkrankungen des Immunsystems Stoffwechsel- und Ernährungsstörungen Psychiatrische Erkrankungen Erkrankungen des Nervensystems Augenerkrankungen Sehr häufig Häufig Gelegentlich Selten Sehr selten Schwindel, Kopfschmerzen Bronchitis, Pneumonie, Infektionen der oberen Atemwege, Infektionen der Harnwege Anämie Thrombozytopenie Leukopenie Gewichtszunahme, Hypercholesterinämie, beeinträchtigte Blutzuckereinstellung (Hyperglykämie, Hypoglykämie) bei Patienten mit vorbestehendem Diabetes Depression, depressive Verstimmung Sehstörungen, verminderte Tränensekretion (trockene Augen), Augenreizung Herzerkrankungen Herzinsuffizienz Bradykardie, Ödeme, Hypervolämie, Überwässerung Gefäßerkrankungen Hypotonie Orthostatische Hypotonie, Störungen der peripheren Durchblutung (kalte Extremitäten, periphere Gefäßerkrankung, intermittierende Claudicatio und Raynaud-Phänomen exazerbiert) Erkrankungen der Atemwege, des Brustraums und des Mediastinums Erkrankungen des Gastrointestinaltrakts Leber- und Gallenerkrankungen Erkrankungen der Haut und des Unterhautzellgewebes Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen Erkrankungen der Nieren und Harnwege Erkrankungen der Geschlechtsorgane und der Brustdrüse Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Asthenie (Müdigkeit) Dyspnoe, Lungenödem, Asthma bei prädisponierten Patienten Übelkeit, Diarrhoe, Erbrechen, Dyspepsie, Abdominalschmerz Schmerzen in den Extremitäten Niereninsuffizienz und Nierenfunktionsstörungen bei Patienten mit diffuser Gefäßerkrankung und/oder zugrunde liegender Niereninsuffizienz, Miktionsstörungen Schmerzen Schlafstörungen Präsynkope, Synkope, Parästhesie Atrioventrikulärer Block, Angina pectoris Hautreaktionen (z. B. allergisches Exanthem, Dermatitis, Urticaria, Pruritus, psoriatische und Lichen-planus-artige Hautläsionen), Alopezie Erektile Dysfunktion Nasenverstopfung Verschlechterung der Nierenfunktion Überempfindlichkeit (allergische Reaktion) Alaninaminotransferase (ALT), Aspartat-Aminotransferase (AST) und Gamma-Glutamyltransferase (GGT) erhöht Schwere dermatologische Nebenwirkungen (z. B. Erythema multiforme, Stevens-Johnson-Syndrom, toxische epidermale Nekrolyse) Harninkontinenz bei Frauen 5
6 Behandlung ausreichend lange fortgesetzt werden, bis sich der Zustand des Patienten stabilisiert hat, da mit einer Verlängerung der Eliminationshalbwertzeit und Rückverteilung von Carvedilol aus tieferen Kompartimenten zu rechnen ist. 5. PHARMAKOLOGISCHE EIGENSCHAFTEN 5.1 Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe: Alphaund Betablocker ATC-Code: C07AG02 Carvedilol ist ein vasodilatierender nichtselektiver Betablocker, der den peripheren Gefäßwiderstand aufgrund einer selektiven alpha 1 -Rezeptorenblockade reduziert und das Renin-Angiotensin-System aufgrund der nicht-selektiven Betablockade unterdrückt. Die Plasma-Renin-Aktivität ist vermindert und eine Flüssigkeitsretention tritt selten auf. Carvedilol besitzt keine intrinsische sympathomimetische Aktivität (ISA). Wie Propanolol hat es membranstabilisierende Eigenschaften. Carvedilol ist ein Razemat aus zwei Stereoisomeren. Im Tiermodell zeigten beide Enantiomere alpha-blockierende Aktivität. Die nicht-selektive beta 1 - und beta 2 -Adrenozeptorblockade ist hauptsächlich dem S(- )-Enantiomer zuzuschreiben. Die antioxidativen Eigenschaften von Carvedilol und seiner Metaboliten wurden in In-vitro- und In-vivo-Experimenten im Tiermodell und in vitro in einer Reihe von menschlichen Zelltypen demonstriert. Bei hypertonen Patienten wird die Blutdrucksenkung nicht von einer gleichzeitigen Erhöhung des peripheren Widerstandes begleitet, wie dies bei reinen Betablockern beobachtet wurde. Die Herzfrequenz wird geringfügig gesenkt. Das Herzschlagvolumen bleibt unverändert. Der renale Blutfluss und die Nierenfunktion bleiben ebenso wie der periphere Blutfluss im normalen Bereich; daher tritt ein bei Betablockern oft beobachtetes Kältegefühl an den Gliedmaßen nur selten auf. Bei Hypertonikern erhöht Carvedilol die Plasmakonzentration von Norepinephrin. In der Langzeitbehandlung von Patienten mit Angina pectoris zeigte Carvedilol antiischämische und antianginöse Effekte. Hämodynamische Studien zeigten eine Verringerung der ventrikulären Vor- und Nachlast. Bei Patienten mit linksventrikulärer Dysfunktion oder Stauungsherzinsuffizienz bewirkt Carvedilol günstige Effekte auf hämodynamische Parameter sowie eine Verbesserung der linksventrikulären Ejektionsfraktion und eine Verringerung der Herzgröße. Bei Patienten mit Herzinsuffizienz wird durch Carvedilol die Sterblichkeit sowie die Notwendigkeit von Hospitalisierungen aus kardiovaskulären Gründen reduziert. Carvedilol hat weder eine negative Auswirkung auf die Serumlipidspiegel noch auf Elektrolyte. Das Verhältnis von HDL (high-density Lipoproteine) und LDL (lowdensity Lipoproteine) bleibt normal. 5.2 Pharmakokinetische Eigenschaften Allgemeine Beschreibung Die absolute Bioverfügbarkeit nach oraler Gabe von Carvedilol beträgt etwa 25 %. Die maximale Plasmakonzentration wird etwa 1 Stunde nach der Gabe erreicht. Es besteht eine lineare Korrelation zwischen Dosis und Plasmaspiegel. Bei Patienten, die eine langsame Hydroxylierung von Debrisoquin aufweisen, erhöhten sich die Plasmakonzentrationen von Carvedilol auf das 2-3-fache im Vergleich zu schnellen Verstoffwechslern von Debrisoquin. Die Bioverfügbarkeit wird durch gleichzeitige Nahrungsaufnahme nicht verändert, nur die maximalen Plasmaspiegel werden verzögert erreicht. Carvedilol ist eine sehr lipophile Verbindung. Es wird zu etwa 98 % bis 99 % an Plasmaproteine gebunden. Das Verteilungsvolumen beträgt etwa 2 l/kg. Der First-pass-Effekt beträgt nach oraler Gabe etwa 60 bis 75 %. Die durchschnittliche Eliminations-Halbwertszeit von Carvedilol beträgt etwa 6 bis 10 Stunden. Die Plasmaclearance liegt bei etwa 590 ml/min. Die Ausscheidung erfolgt überwiegend biliär. Die Hauptausscheidung von Carvedilol erfolgt über die Faeces. Ein geringer Anteil wird in Form von Metaboliten über die Nieren ausgeschieden. Carvedilol wird in hohem Ausmaß zu verschiedenen Metaboliten abgebaut, die hauptsächlich biliär eliminiert werden. Carvedilol wird in der Leber vornehmlich durch Oxidierung des aromatischen Ringes und Glukuronidierung metabolisiert. Durch Demethylierung und Hydroxylierung entstehen am Phenolring drei aktive Metaboliten mit betablockierenden Wirkungen. Im Vergleich zu Carvedilol haben diese drei aktiven Metaboliten eine schwache vasodilatierende Wirkung. Aus präklinischen Studien geht hervor, dass der 4 -Hydroxyphenol-Metabolit eine 13- fach höhere betablockierende Wirkung hat als Carvedilol. Die Konzentrationen des Metaboliten im Menschen sind jedoch etwa 10-fach niedriger als die von Carvedilol. Zwei der Hydroxycarbazol-Metaboliten von Carvedilol sind hochwirksame Antioxidantien mit einer fach höheren Wirkung als Carvedilol. Pharmakokinetische Eigenschaften bei Patienten Die Pharmakokinetik von Carvedilol wird vom Alter beeinflusst; die Carvedilol-Plasmaspiegel sind bei älteren Patienten etwa um 50 % höher als bei jungen Patienten. In einer Studie mit Patienten mit Leberzirrhose war die Bioverfügbarkeit von Carvedilol 4-fach und die Plasmaspiegel 5-fach sowie das Verteilungsvolumen dreifach höher als bei Lebergesunden. Bei einigen Hypertonikern mit mäßiger (Kreatininclearance ml/ min) oder schwerer (Kreatininclearance < 20 ml/min) Niereninsuffizienz wurde im Vergleich zu Nierengesunden ein Anstieg der Plasmakonzentrationen von Carvedilol von etwa % beobachtet. Die Ergebnisse variierten jedoch sehr stark. 5.3 Präklinische Daten zur Sicherheit Studien an Ratten und Mäusen zeigten mit Dosen von 75 mg/kg und 200 mg/kg (das Fache der täglichen Maximaldosis beim Menschen) kein karzinogenes Potential von Carvedilol. In-vitro- oder In-vivo-Studien an Säugetieren oder anderen Tieren zeigten kein mutagenes Potential von Carvedilol. Nach Gabe hoher Dosen Carvedilol an trächtige Ratten (> 200 mg/kg = > das 100-Fache der täglichen Maximaldosis beim Menschen) wurden unerwünschte Nebenwirkungen auf die Schwangerschaft und Fertilität beobachtet. Bei Dosen > 60 mg/kg (> das 30-Fache der täglichen Maximaldosis beim Menschen) waren körperliches Wachstum und Entwicklung der Feten verzögert. Embryotoxizität (erhöhte Sterblichkeit nach Implantation des Embryos) trat auf, es kam jedoch zu keinen Missbildungen bei Ratten oder Kaninchen bei Dosen von 200 mg/ kg und 75 mg/kg (das Fache der täglichen Maximaldosis beim Menschen). 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile Lactose-Monohydrat mikrokristalline Cellulose Crospovidon Povidon K 30 hochdisperses Siliciumdioxid Magnesiumstearat (Ph.Eur.) zusätzlich für Carvedilol - 1 A Pharma 3,125 mg Tabletten: Eisen(III)-oxid (E 172) 6
7 zusätzlich für Carvedilol - 1 A Pharma 6,25mg Tabletten: Eisenoxidhydrat (E 172) zusätzlich für Carvedilol - 1 A Pharma 12,5 mg Tabletten: Eisen(III)-oxid (E 172) Eisenoxidhydrat (E 172) 6.2 Inkompatibilitäten Nicht zutreffend 6.3 Dauer der Haltbarkeit 4 Jahre Datum der letzten Verlängerung der Zulassungen: 11.August STAND DER INFORMATION August VERKAUFSABGRENZUNG Verschreibungspflichtig 6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung Polyethylen(PE-HD)-Behälter und Verschlüsse: In der Originalpackung aufbewahren. Blister (Al/PVC): In der Originalpackung aufbewahren. 6.5 Art und Inhalt des Behältnisses Polyethylen(PE-HD)-Behälter und Verschlüsse: 28, 30, 60, 100, 250 und 500 Tabletten. Blister (Al/PVC): 14, 20, 28, 30, 50, 50x1, 56, 60, 98, 98x1 und 100 Tabletten. Es werden möglicherweise nicht alle Packungsgrößen und Verpackungsmaterialien in den Verkehr gebracht. 6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung Keine besonderen Anforderungen 7. INHABER DER ZULASSUNGEN 1 A Pharma GmbH Keltenring Oberhaching Telefon: 089/ Telefax: 089/ medwiss@1apharma.com 8. ZULASSUNGSNUMMERN Carvedilol - 1 A Pharma 3,125 mg Tabletten Carvedilol - 1 A Pharma 6,25 mg Tabletten Carvedilol - 1 A Pharma 12,5 mg Tabletten Carvedilol - 1 A Pharma 25 mg Tabletten Carvedilol - 1 A Pharma 50 mg Tabletten DATUM DER ERTEILUNG DER ZULAS- SUNGEN/VERLÄNGERUNG DER ZU- LASSUNGEN Datum der Erteilung der Zulassungen: 17.Juni
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Viscosan - Augentropfen Wirkstoff: Hypromellose
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen.
 Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen. Levobunolol ist ein Beta-Blocker, der den Druck im Inneren des Auges reduziert. Levobunolol Augen (Auge) ist für die Behandlung
Wie unsere Augen Erfahren Sie, wie wir sehen, und wie Sie Ihre Vision zu schützen. Levobunolol ist ein Beta-Blocker, der den Druck im Inneren des Auges reduziert. Levobunolol Augen (Auge) ist für die Behandlung
Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6
 Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6 Trotz sorgfältiger Erstellung des Buchs Benkert, Pocket Guide, Psychopharmaka
Erratum Benkert, Pocket Guide, Psychopharmaka von A bis Z. 3.Aufl. ISBN (print): 978-3-642-54766-9/ DOI 10.1007/978-3-642-54767-6 Trotz sorgfältiger Erstellung des Buchs Benkert, Pocket Guide, Psychopharmaka
1. WAS IST DAFALGAN Zäpfchen UND WOFÜR WIRD ES ANGEWENDET?
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DAFALGAN Säuglinge 80 mg Zäpfchen DAFALGAN Kleinkinder 150 mg Zäpfchen DAFALGAN große Kinder 300 mg Zäpfchen Paracetamol Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DAFALGAN Säuglinge 80 mg Zäpfchen DAFALGAN Kleinkinder 150 mg Zäpfchen DAFALGAN große Kinder 300 mg Zäpfchen Paracetamol Lesen Sie die gesamte Packungsbeilage
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen
 Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Anhang III. Ergänzungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Ergänzungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage 20 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS [Der unten genannte Wortlaut
Anhang III Ergänzungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage 20 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS [Der unten genannte Wortlaut
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Protagent-Einmalaugentropfen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Lösung (= ca. 30 Tropfen) enthält 20 mg
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Protagent-Einmalaugentropfen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Lösung (= ca. 30 Tropfen) enthält 20 mg
WAS finde ich WO im Beipackzettel
 WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Legalon SIL - Trockensubstanz zur Infusionsbereitung
 PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Kamillosan -Mundspray. Kamillenblütenauszug Pfefferminzöl Anisöl
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Kamillosan -Mundspray Kamillenblütenauszug Pfefferminzöl Anisöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Kamillosan -Mundspray Kamillenblütenauszug Pfefferminzöl Anisöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
Gebrauchsinformation: Information für Anwender. LOMUSOL Augentropfen. Wirkstoff: Dinatriumcromoglicat
 Gebrauchsinformation: Information für Anwender LOMUSOL Augentropfen Wirkstoff: Dinatriumcromoglicat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für Anwender LOMUSOL Augentropfen Wirkstoff: Dinatriumcromoglicat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Nasa Rhinathiol 0,1 %ige Nasenspray, Lösung Xylometazolinhydrochlorid
 Seite 1/5 Packungsbeilage Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mir der Anwendung dieses Arzneimittels beginnen. Sie enthält wichtige Informationen für Ihre Behandlung. Wenn
Seite 1/5 Packungsbeilage Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mir der Anwendung dieses Arzneimittels beginnen. Sie enthält wichtige Informationen für Ihre Behandlung. Wenn
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tantum Verde 3 mg Pastillen mit Minzgeschmack Wirkstoff: Benzydaminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Faltschachtel. Unverkäufliches Muster (Eindruck auf Linie) Teil einer Klinikpackung, Einzelverkauf unzulässig (Eindruck auf Linie)
 Packmittelmanuskript Nr. 64000/009/94/6 Seite 2 Faltschachtel HEUMANN PHARMA GmbH & Co. Generica KG Südwestpark 50 90449 Nürnberg Urso 400 Heumann Filmtabletten mit 400 mg Ursodeoxycholsäure Zur Auflösung
Packmittelmanuskript Nr. 64000/009/94/6 Seite 2 Faltschachtel HEUMANN PHARMA GmbH & Co. Generica KG Südwestpark 50 90449 Nürnberg Urso 400 Heumann Filmtabletten mit 400 mg Ursodeoxycholsäure Zur Auflösung
Packungsbeilage CORSODYL Mundspüllösung / Spray 03-2012 Seite 1/5 BE106802 / BE191764 Belgien GEBRAUCHINFORMATION: INFORMATION FÜR DEN ANWENDER
 Seite 1/5 BE106802 / BE191764 Belgien GEBRAUCHINFORMATION: INFORMATION FÜR DEN ANWENDER CORSODYL 200mg/100ml mundwasser CORSODYL 200mg/100ml spray zur Anwendung in der Mundhöhle Chlorhexidindigluconat
Seite 1/5 BE106802 / BE191764 Belgien GEBRAUCHINFORMATION: INFORMATION FÜR DEN ANWENDER CORSODYL 200mg/100ml mundwasser CORSODYL 200mg/100ml spray zur Anwendung in der Mundhöhle Chlorhexidindigluconat
1. Was sind Dorithricin Halstabletten und wofür werden sie angewendet?
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Dorithricin - Halstabletten Wirkstoffe: Tyrothricin, Benzalkoniumchlorid, Benzocain Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Dorithricin - Halstabletten Wirkstoffe: Tyrothricin, Benzalkoniumchlorid, Benzocain Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Heumann s Blasen- und Nierentee Solubitrat Wirkstoffe: Dickextrakt aus Birkenblättern, Dickextrakt aus Riesengoldrutenkraut Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Heumann s Blasen- und Nierentee Solubitrat Wirkstoffe: Dickextrakt aus Birkenblättern, Dickextrakt aus Riesengoldrutenkraut Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tebofortan 40 mg - Filmtabletten. Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tebofortan 40 mg - Filmtabletten Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tebofortan 40 mg - Filmtabletten Wirkstoff: Trockenextrakt aus Ginkgo-biloba-Blättern Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
Patienteninformationsbroschüre Valproat
 Patienteninformationsbroschüre Valproat Informationen für Patientinnen Die Informationen in dieser Broschüre sind für Frauen bestimmt, denen Valproat verschrieben wird und die schwanger werden können (Frauen
Patienteninformationsbroschüre Valproat Informationen für Patientinnen Die Informationen in dieser Broschüre sind für Frauen bestimmt, denen Valproat verschrieben wird und die schwanger werden können (Frauen
Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva
 Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva Darmstadt (19. Februar 2009) Die Merck KGaA hat heute bekannt gegeben, dass die europäische Arzneimittelbehörde EMEA
Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva Darmstadt (19. Februar 2009) Die Merck KGaA hat heute bekannt gegeben, dass die europäische Arzneimittelbehörde EMEA
Die östrogenfreie Pille
 Alle wichtigen Infos über Sexualität und Verhütung unter: www.frau-und-pille.de Mit bester Empfehlung Die östrogenfreie Pille Verhütung für Frauen mit besonderem Anspruch. Einscannen und mehr erfahren...
Alle wichtigen Infos über Sexualität und Verhütung unter: www.frau-und-pille.de Mit bester Empfehlung Die östrogenfreie Pille Verhütung für Frauen mit besonderem Anspruch. Einscannen und mehr erfahren...
SGMO - Schweizerische Gesellschaft für medizinische Onkologie
 SGMO - Schweizerische Gesellschaft für medizinische Onkologie Seminar: Neue Medikamente neue Nebenwirkungen Kardiovaskuläre Nebenwirkungen Prof. Thomas M. Suter, Leitender Arzt, Universitätsklink für Kardiologie,
SGMO - Schweizerische Gesellschaft für medizinische Onkologie Seminar: Neue Medikamente neue Nebenwirkungen Kardiovaskuläre Nebenwirkungen Prof. Thomas M. Suter, Leitender Arzt, Universitätsklink für Kardiologie,
Atronase 0,3 mg/ml Nasenspray, Lösung (Ipratropiumbromid)
 GEBRAUCHSINFORMATION ATRONASE 0,3 MG/ML NASENSPRAY, LÖSUNG Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
GEBRAUCHSINFORMATION ATRONASE 0,3 MG/ML NASENSPRAY, LÖSUNG Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel ist auch ohne Verschreibung
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. PROGESTOGEL 1 % Gel. Progesteron
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER PROGESTOGEL 1 % Gel Progesteron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER PROGESTOGEL 1 % Gel Progesteron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
APOTHEKIA SPECIAL DIE PILLE DANACH
 APOTHEKIA SPECIAL DIE PILLE DANACH Die zwei Pillen danach In Deutschland sind aktuell zwei Wirkstoffe für die Pille danach zugelassen, Ulipristalacetat (Handelsname ellaone) und Levonorgestrel (Handelsname
APOTHEKIA SPECIAL DIE PILLE DANACH Die zwei Pillen danach In Deutschland sind aktuell zwei Wirkstoffe für die Pille danach zugelassen, Ulipristalacetat (Handelsname ellaone) und Levonorgestrel (Handelsname
LANSOYL Paraffine Gel zum Einnehmenv3.0_B2.0 1/5
 PIL September 2015 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER LANSOYL PARAFFINE 78,230 g/100 g Gel zum Einnehmen Paraffinöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
PIL September 2015 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER LANSOYL PARAFFINE 78,230 g/100 g Gel zum Einnehmen Paraffinöl Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Labortests für Ihre Gesundheit. Therapie nach Maß 26
 Labortests für Ihre Gesundheit Therapie nach Maß 26 01IPF Labortests für Ihre Gesundheit Therapie nach Maß Die individuelle Dosis finden Jeder Mensch ist einzigartig. Keiner gleicht dem anderen nicht nur
Labortests für Ihre Gesundheit Therapie nach Maß 26 01IPF Labortests für Ihre Gesundheit Therapie nach Maß Die individuelle Dosis finden Jeder Mensch ist einzigartig. Keiner gleicht dem anderen nicht nur
Packungsbeilage GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung. Xylometazolinhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER NUSO-SAN Menthol 1mg/ml Nasenspray, Lösung Xylometazolinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Vitagutt Vitamin E 670 mg, Weichkapsel Zur Anwendung bei Erwachsenen Wirkstoff: 1000 mg all-rac-alpha-tocopherolacetat (entsprechend 670 mg RRR-alpha- Tocopherol-Äquivalente).
Gebrauchsinformation: Information für Anwender Vitagutt Vitamin E 670 mg, Weichkapsel Zur Anwendung bei Erwachsenen Wirkstoff: 1000 mg all-rac-alpha-tocopherolacetat (entsprechend 670 mg RRR-alpha- Tocopherol-Äquivalente).
Durchfall in der Pflege. Der kleine Ratgeber von Aplona
 Durchfallerkrankungen Durchfall in der Pflege Der kleine von Aplona Der kleine von Aplona 3 Fotos: Titel, Seite 2, 3 und 4: Fotolia.com Durchfall in der Pflege Akute Durchfallerkrankungen stellen eine
Durchfallerkrankungen Durchfall in der Pflege Der kleine von Aplona Der kleine von Aplona 3 Fotos: Titel, Seite 2, 3 und 4: Fotolia.com Durchfall in der Pflege Akute Durchfallerkrankungen stellen eine
Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU - Kombination mit Sulfonylharnstoff n
 Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU Kombination mit Sulfonylharnstoff nun ebenfalls zugelassen Haar (März 2008) - Die europäische Arzneimittelbehörde EMEA hat JANUVIA für
Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU Kombination mit Sulfonylharnstoff nun ebenfalls zugelassen Haar (März 2008) - Die europäische Arzneimittelbehörde EMEA hat JANUVIA für
PACKUNGSBEILAGE. CORSODYL Zahngel, 10 mg Chlorhexidin digluconat pro g Zahngel
 Seite 1/5 981 IS 153 F7 Belgien PACKUNGSBEILAGE Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Wenn Sie weitere Fragen haben, wenden Sie sich an
Seite 1/5 981 IS 153 F7 Belgien PACKUNGSBEILAGE Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Wenn Sie weitere Fragen haben, wenden Sie sich an
Diabetes mellitus : Folgeschäden
 Diabetes mellitus : Folgeschäden Warum ist der Diabetes mellitus eine wichtige Erkrankung? a. Akute Probleme: Hypoglykämie Hyperglykämie Ketoazidose b. Chronische Probleme: Folgeschäden: Typische Schäden:
Diabetes mellitus : Folgeschäden Warum ist der Diabetes mellitus eine wichtige Erkrankung? a. Akute Probleme: Hypoglykämie Hyperglykämie Ketoazidose b. Chronische Probleme: Folgeschäden: Typische Schäden:
Patientenleitfaden für das Gespräch mit dem Arzt. Liebe Patientin, lieber Patient!
 Patientenleitfaden für das Gespräch mit dem Arzt Liebe Patientin, lieber Patient! Je besser Sie sich auf das Gespräch mit Ihrem Arzt vorbereiten, desto leichter wird es für sie/ihn sein, eine Diagnose
Patientenleitfaden für das Gespräch mit dem Arzt Liebe Patientin, lieber Patient! Je besser Sie sich auf das Gespräch mit Ihrem Arzt vorbereiten, desto leichter wird es für sie/ihn sein, eine Diagnose
Woran Sie vor und nach Ihrer Linsenaustauschbehandlung (RLE) denken sollten
 Woran Sie vor und nach Ihrer Linsenaustauschbehandlung (RLE) denken sollten Der sichere Weg zu einem Leben ohne Brille und Kontaktlinsen! 2 Herzlichen Glückwunsch! Sie haben sich für eine Linsenaustauschbehandlung
Woran Sie vor und nach Ihrer Linsenaustauschbehandlung (RLE) denken sollten Der sichere Weg zu einem Leben ohne Brille und Kontaktlinsen! 2 Herzlichen Glückwunsch! Sie haben sich für eine Linsenaustauschbehandlung
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Tilidin N Lichtenstein Wirkstoffe: Tilidinhydrochlorid 50 mg in 20 Tropfen Naloxonhydrochlorid 4 mg in 20 Tropfen Für Erwachsene, Kinder ab 2 Jahre Lösung
Gebrauchsinformation: Information für Anwender Tilidin N Lichtenstein Wirkstoffe: Tilidinhydrochlorid 50 mg in 20 Tropfen Naloxonhydrochlorid 4 mg in 20 Tropfen Für Erwachsene, Kinder ab 2 Jahre Lösung
Zusammenfassung der Merkmale des Arzneimittels. Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Virupos 30 mg/g Augensalbe 2. Qualitative und quantitative Zusammensetzung Wirkstoff: 1 g Salbe enthält Aciclovir 30 mg Die
Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Virupos 30 mg/g Augensalbe 2. Qualitative und quantitative Zusammensetzung Wirkstoff: 1 g Salbe enthält Aciclovir 30 mg Die
Krank durch Schlafstörungen
 Seite 1 von 6 I n f o r m a t i o n s m a t e r i a l v o m 1 2. 0 1. 2 0 1 2 Krank durch Schlafstörungen "Die meisten Menschen sterben an ihren Medikamenten und nicht an ihren Krankheiten", meinte der
Seite 1 von 6 I n f o r m a t i o n s m a t e r i a l v o m 1 2. 0 1. 2 0 1 2 Krank durch Schlafstörungen "Die meisten Menschen sterben an ihren Medikamenten und nicht an ihren Krankheiten", meinte der
Künstlicher Hüftgelenksersatz
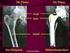 Künstlicher Hüftgelenksersatz Künstlicher Hüftgelenksersatz Was ist eine Hüftgelenk-Arthrose? Das Hüftgelenk ist eine bewegliche Verbindung zwischen dem Becken- und dem Oberschenkelknochen. Die am Gelenk
Künstlicher Hüftgelenksersatz Künstlicher Hüftgelenksersatz Was ist eine Hüftgelenk-Arthrose? Das Hüftgelenk ist eine bewegliche Verbindung zwischen dem Becken- und dem Oberschenkelknochen. Die am Gelenk
Deutsches Rotes Kreuz. Kopfschmerztagebuch von:
 Deutsches Rotes Kreuz Kopfschmerztagebuch Kopfschmerztagebuch von: Hallo, heute hast Du von uns dieses Kopfschmerztagebuch bekommen. Mit dem Ausfüllen des Tagebuches kannst Du mehr über Deine Kopfschmerzen
Deutsches Rotes Kreuz Kopfschmerztagebuch Kopfschmerztagebuch von: Hallo, heute hast Du von uns dieses Kopfschmerztagebuch bekommen. Mit dem Ausfüllen des Tagebuches kannst Du mehr über Deine Kopfschmerzen
Ausfüllanleitung. zum indikationsspezifischen Datensatz. für das strukturierte Behandlungsprogramm. Asthma bronchiale
 Ausfüllanleitung zum indikationsspezifischen Datensatz für das strukturierte Behandlungsprogramm Asthma bronchiale Stand der letzten Bearbeitung: 20.11.2012 Version 4.2 Anamnese- und Befunddaten Häufigkeit
Ausfüllanleitung zum indikationsspezifischen Datensatz für das strukturierte Behandlungsprogramm Asthma bronchiale Stand der letzten Bearbeitung: 20.11.2012 Version 4.2 Anamnese- und Befunddaten Häufigkeit
10 Antworten zum Thema Generika
 10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
Betreff: Citalopram hältige Arzneispezialitäten Änderungen der Fach- und Gebrauchsinformationen
 Datum: 15.11.2011 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43(0)505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-111114-23425-A-PHV Ihr Zeichen: Betreff:
Datum: 15.11.2011 Kontakt: Mag. pharm. Dr. Ulrike Rehberger Abteilung: Tel. / Fax: +43(0)505 55 36258, DW.Fax-36207 E-Mail: ulrike.rehberger@ages.at Unser Zeichen: 16c-111114-23425-A-PHV Ihr Zeichen: Betreff:
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren
 Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
TOP 3: Loperamid (flüssige Darreichungsformen)
 TOP 3: Loperamid (flüssige Darreichungsformen) Antrag auf Ausweitung der Ausnahme von der Verschreibungspflicht auch für flüssige Darreichungsformen 1 Historie und aktuell: Seit 1993 D. h. folgende Darreichungsformen
TOP 3: Loperamid (flüssige Darreichungsformen) Antrag auf Ausweitung der Ausnahme von der Verschreibungspflicht auch für flüssige Darreichungsformen 1 Historie und aktuell: Seit 1993 D. h. folgende Darreichungsformen
!!! Folgeerkrankungen
 Ein zu hoher Blutzuckerspiegel kann Folgen auf Ihr Herzkreislaufsystem haben und zu Erkrankungen wie der Schaufensterkrankheit, einer Angina pectoris, einem Herzinfarkt oder einem Schlaganfall führen.
Ein zu hoher Blutzuckerspiegel kann Folgen auf Ihr Herzkreislaufsystem haben und zu Erkrankungen wie der Schaufensterkrankheit, einer Angina pectoris, einem Herzinfarkt oder einem Schlaganfall führen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Clarityn 10 mg - Brausetabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Clarityn 10 mg - Brausetabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen
!!! Substanzen, die den Blutdruck erhöhen
 Substanzen, die den Blutdruck erhöhen Substanzen, die den Blutdruck erhöhen Es gibt zahlreiche Substanzen, die in verschreibungspflichtigen und nichtverschreibungspflichtige Medikamente, Nahrungsergänzungsmitteln,
Substanzen, die den Blutdruck erhöhen Substanzen, die den Blutdruck erhöhen Es gibt zahlreiche Substanzen, die in verschreibungspflichtigen und nichtverschreibungspflichtige Medikamente, Nahrungsergänzungsmitteln,
DMP - Intensiv Seminar. Lernerfolgskontrolle
 DMP - Intensiv Seminar Lernerfolgskontrolle A DIABETES 1. Für einen 84 jährigen Mann mit Diabetes mellitus Typ 2, Herzinsuffizienz bei Z.n. 2-maligem Myokardinfarkt, art. Hypertonie, M. Parkinson, Kachexie
DMP - Intensiv Seminar Lernerfolgskontrolle A DIABETES 1. Für einen 84 jährigen Mann mit Diabetes mellitus Typ 2, Herzinsuffizienz bei Z.n. 2-maligem Myokardinfarkt, art. Hypertonie, M. Parkinson, Kachexie
Gebrauchsinformation: Information für Patienten. Desloratadin Genericon 5 mg Filmtabletten. Wirkstoff: Desloratadin
 Gebrauchsinformation: Information für Patienten Desloratadin Genericon 5 mg Filmtabletten Wirkstoff: Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten Desloratadin Genericon 5 mg Filmtabletten Wirkstoff: Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER SINUTAB 500/30 mg Tabletten SINUTAB FORTE 500/60 mg Tabletten Paracetamol und Pseudoephedrinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER SINUTAB 500/30 mg Tabletten SINUTAB FORTE 500/60 mg Tabletten Paracetamol und Pseudoephedrinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
Bijsluiter DE versie Imaverol 100 mg (glas) B. PACKUNGSBEILAGE 1
 B. PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION Imaverol 100 mg, Konzentrat zur örtlichen Anwendung 1.NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
B. PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION Imaverol 100 mg, Konzentrat zur örtlichen Anwendung 1.NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
Verschreibungsfreie Arzneimittel wieder in der Erstattung
 Satzungsleistungen Verschreibungsfreie Arzneimittel wieder in der Erstattung Was sind Satzungsleistungen? Der Rahmen für die Leistungen der gesetzlichen Krankenversicherung wird im Fünften Sozialgesetzbuch
Satzungsleistungen Verschreibungsfreie Arzneimittel wieder in der Erstattung Was sind Satzungsleistungen? Der Rahmen für die Leistungen der gesetzlichen Krankenversicherung wird im Fünften Sozialgesetzbuch
Pflichttexte zur Verwendung in der Werbung für Arzneimittel in Deutschland gemäß Heilmittelwerbegesetz (HWG) Endverbraucher
 Cutasept F Pflichttexte Cutasept F: Wirkstoff: Propan-2-ol. Zusammensetzung: 100 g Lösung enthalten: Wirkstoff: Propan-2-ol 63,0 g, entspricht 72 Vol.%. Sonstige Bestandteile: Benzalkoniumchlorid, Gereinigtes
Cutasept F Pflichttexte Cutasept F: Wirkstoff: Propan-2-ol. Zusammensetzung: 100 g Lösung enthalten: Wirkstoff: Propan-2-ol 63,0 g, entspricht 72 Vol.%. Sonstige Bestandteile: Benzalkoniumchlorid, Gereinigtes
Trockenes Auge. Haben Sie Trockene Augen?
 Trockenes Auge Jeder 3 bis 5 Patient, der den Augenarzt besucht, an der Krankheit Trockenes Auge leidet. Ein Trockenes Auge entsteht, wenn der Körper zu wenig Tränenflüssigkeit produziert oder die Zusammensetzung
Trockenes Auge Jeder 3 bis 5 Patient, der den Augenarzt besucht, an der Krankheit Trockenes Auge leidet. Ein Trockenes Auge entsteht, wenn der Körper zu wenig Tränenflüssigkeit produziert oder die Zusammensetzung
SUBSTANZABHÄNGIGKEIT - PROBLEMSTELLUNG IN DER BEURTEILUNG DER FAHRTAUGLICHKEIT
 SUBSTANZABHÄNGIGKEIT - PROBLEMSTELLUNG IN DER BEURTEILUNG DER FAHRTAUGLICHKEIT HR Dr. Wilhelm SAURMA LandespolizeidirekHon Wien Ref. A 1.3 Polizeiärztlicher Dienst Verordnung des Bundesministers für WissenschaT
SUBSTANZABHÄNGIGKEIT - PROBLEMSTELLUNG IN DER BEURTEILUNG DER FAHRTAUGLICHKEIT HR Dr. Wilhelm SAURMA LandespolizeidirekHon Wien Ref. A 1.3 Polizeiärztlicher Dienst Verordnung des Bundesministers für WissenschaT
Fragebogen Kopfschmerzen
 Fragebogen Kopfschmerzen Fragen an Dich Fragen an Dich Fragen an die Eltern Bei diesen Fragen geht es um Deine Kopfschmerzen. Es wäre schön, wenn Du darüber etwas sagst. Deine Antworten helfen, für Deine
Fragebogen Kopfschmerzen Fragen an Dich Fragen an Dich Fragen an die Eltern Bei diesen Fragen geht es um Deine Kopfschmerzen. Es wäre schön, wenn Du darüber etwas sagst. Deine Antworten helfen, für Deine
BLUTHOCHDRUCK UND NIERE
 BLUTHOCHDRUCK UND NIERE Hilfreiche Informationen zu Ihrer Nierengesundheit Bluthochdruck und Niere Die Nieren sind die Organe unseres Körpers, die den Blutdruck regeln. Der Blutdruck ist der Druck, der
BLUTHOCHDRUCK UND NIERE Hilfreiche Informationen zu Ihrer Nierengesundheit Bluthochdruck und Niere Die Nieren sind die Organe unseres Körpers, die den Blutdruck regeln. Der Blutdruck ist der Druck, der
ANWEISUNGSKARTE FÜR DEN PATIENTEN
 Der Plan zur Risikobegrenzung in Belgien, zu dem diese Information gehört, ist eine Maßnahme, die ergriffen wurde, um eine sichere und wirksame Anwendung fon ZypAdhera TM zu garantieren. (RMA modifizierte
Der Plan zur Risikobegrenzung in Belgien, zu dem diese Information gehört, ist eine Maßnahme, die ergriffen wurde, um eine sichere und wirksame Anwendung fon ZypAdhera TM zu garantieren. (RMA modifizierte
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Candesartan Zentiva 16 mg Tabletten Wirkstoff: Candesartancilexetil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender Candesartan Zentiva 16 mg Tabletten Wirkstoff: Candesartancilexetil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Ein neues System für die Allokation von Spenderlungen. LAS Information für Patienten in Deutschland
 Ein neues System für die Allokation von Spenderlungen LAS Information für Patienten in Deutschland Ein neues System für die Allokation von Spenderlungen Aufgrund des immensen Mangels an Spenderorganen
Ein neues System für die Allokation von Spenderlungen LAS Information für Patienten in Deutschland Ein neues System für die Allokation von Spenderlungen Aufgrund des immensen Mangels an Spenderorganen
Gebrauchsinformation: Information für Patienten. Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench)
 Gebrauchsinformation: Information für Patienten Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench) Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Patienten Urgenin Tropfen Tinktur aus Serenoa repens (Bartram Small) ; Saft aus Echinacea purpurea (Moench) Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
InVo. Information zu Verordnungen in der GKV. Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen. Stand: Februar 2010
 Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
Der Medizinkamm fürs Haar Ein Ratgeber bei Haarausfall für Sie und Ihn
 Der Medizinkamm fürs Haar Ein Ratgeber bei Haarausfall für Sie und Ihn Ein Wort zuvor: Etwas Haarverlust ist ganz natürlich Das große Problem: Erblich bedingter Haarausfall as Leben eines Haares dauert
Der Medizinkamm fürs Haar Ein Ratgeber bei Haarausfall für Sie und Ihn Ein Wort zuvor: Etwas Haarverlust ist ganz natürlich Das große Problem: Erblich bedingter Haarausfall as Leben eines Haares dauert
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. AERIUS 5 mg Schmelztabletten Desloratadin
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Schmelztabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Schmelztabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
RSV. RSV kennen. Das Virus, das Eltern kennen sollten. Informationen. Kinder schützen
 RSV kennen Kinder schützen RSV Das Virus, das Eltern kennen sollten. Informationen zu einem wenig bekannten Virus sowie praktische Ratschläge, wie Sie das Risiko einer RSV-Infektion verringern können.
RSV kennen Kinder schützen RSV Das Virus, das Eltern kennen sollten. Informationen zu einem wenig bekannten Virus sowie praktische Ratschläge, wie Sie das Risiko einer RSV-Infektion verringern können.
zur Verfügung gestellt von Gebrauchs.info GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 2,5 mg/g Wirkstoff: Prednicarbat GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
2,5 mg/g Wirkstoff: Prednicarbat GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen. Heben
Gebrauchsinformation: Information für Anwender. Cyprostol - Tabletten Wirkstoff: Misoprostol
 1 Gebrauchsinformation: Information für Anwender Cyprostol - Tabletten Wirkstoff: Misoprostol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
1 Gebrauchsinformation: Information für Anwender Cyprostol - Tabletten Wirkstoff: Misoprostol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
CARTERS PILLEN "NEUE FORMULA" 5 mg magensaftresistente Tabletten
 13.01.2004 1 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittel beginnen. Wenn Sie weitere Fragen haben, wenden Sie sich bitte an Ihren Arzt oder Apotheker.
13.01.2004 1 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittel beginnen. Wenn Sie weitere Fragen haben, wenden Sie sich bitte an Ihren Arzt oder Apotheker.
Was ist ein Grauer Star?
 Was ist ein Grauer Star? 1 Als Grauen Star oder Katarakt bezeichnet man die Eintrübung der ursprünglich klaren Augenlinse. Sie bemerken, dass Sie wie durch einen leichten Schleier sehen, der mit der Zeit
Was ist ein Grauer Star? 1 Als Grauen Star oder Katarakt bezeichnet man die Eintrübung der ursprünglich klaren Augenlinse. Sie bemerken, dass Sie wie durch einen leichten Schleier sehen, der mit der Zeit
Besser leben mit Gicht. Seite 3 Seite 4 Seite 5 Seite 6. Zu starke Schweißbildung. besser natürlich behandeln. Gicht-Telegramm
 Besser leben mit Gicht GT II-2014 Seite 3 Seite 4 Seite 5 Seite 6 Purinrechner jetzt auf i-phone und Android Warnung vor dem Einsatz von NSAR wie Diclofenac Zu starke Schweißbildung besser natürlich behandeln
Besser leben mit Gicht GT II-2014 Seite 3 Seite 4 Seite 5 Seite 6 Purinrechner jetzt auf i-phone und Android Warnung vor dem Einsatz von NSAR wie Diclofenac Zu starke Schweißbildung besser natürlich behandeln
Dontisolon D Mundheilpaste
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER 5 mg/g Paste Wirkstoff: Prednisolonacetat (Ph.Eur.) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER 5 mg/g Paste Wirkstoff: Prednisolonacetat (Ph.Eur.) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gefährlich hohe Blutzuckerwerte
 Gefährlich hohe Blutzuckerwerte In besonderen Situationen kann der Blutzuckerspiegel gefährlich ansteigen Wenn in Ausnahmefällen der Blutzuckerspiegel sehr hoch ansteigt, dann kann das für Sie gefährlich
Gefährlich hohe Blutzuckerwerte In besonderen Situationen kann der Blutzuckerspiegel gefährlich ansteigen Wenn in Ausnahmefällen der Blutzuckerspiegel sehr hoch ansteigt, dann kann das für Sie gefährlich
Diabetische Retinopathie
 Netzhautkomplikationen Diabetische Netzhautkomplikationen sind krankhafte Veränderungen in den Augen, die durch einen Diabetes mellitus verursacht werden können. Es handelt sich um die diabetische Retinopathie
Netzhautkomplikationen Diabetische Netzhautkomplikationen sind krankhafte Veränderungen in den Augen, die durch einen Diabetes mellitus verursacht werden können. Es handelt sich um die diabetische Retinopathie
Gebrauchsinformation: Information für Anwender. LIVOSTIN - Augentropfen Wirkstoff: Levocabastin-Hydrochlorid
 Gebrauchsinformation: Information für Anwender LIVOSTIN - Augentropfen Wirkstoff: Levocabastin-Hydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für Anwender LIVOSTIN - Augentropfen Wirkstoff: Levocabastin-Hydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Sidroga Blasentee akut Wirkstoffe: Bärentraubenblätter, Birkenblätter, Goldrutenkraut, Orthosiphonblätter
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Sidroga Blasentee akut Wirkstoffe: Bärentraubenblätter, Birkenblätter, Goldrutenkraut, Orthosiphonblätter Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Sidroga Blasentee akut Wirkstoffe: Bärentraubenblätter, Birkenblätter, Goldrutenkraut, Orthosiphonblätter Lesen Sie die gesamte Packungsbeilage sorgfältig
DAS GRÜNE REZEPT. Für eine sichere Medikation mit rezeptfreien Arzneimitteln
 DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
Subkutane spezifische Immuntherapie. Eine Information für Patienten
 Subkutane spezifische Immuntherapie Eine Information für Patienten Spezifische Immuntherapie Die Allergietestung durch Ihren Arzt hat ergeben, dass Sie (oder Ihr Kind) an einer Allergie leiden. Allergische
Subkutane spezifische Immuntherapie Eine Information für Patienten Spezifische Immuntherapie Die Allergietestung durch Ihren Arzt hat ergeben, dass Sie (oder Ihr Kind) an einer Allergie leiden. Allergische
GEBRAUCHSINFORMATION. Wirkstoff: Acetylsalicylsäure. Z.Nr.: 3155
 Liebe Patientin, lieber Patient! Bitte lesen Sie diese Gebrauchsinformation aufmerksam, weil sie wichtige Informationen darüber enthält, was Sie bei der Einnahme dieses Arzneimittels beachten sollen. Wenden
Liebe Patientin, lieber Patient! Bitte lesen Sie diese Gebrauchsinformation aufmerksam, weil sie wichtige Informationen darüber enthält, was Sie bei der Einnahme dieses Arzneimittels beachten sollen. Wenden
PACKUNGSBEILAGE. Bisolvon Hustenlöser - Saft Version 4.1 1
 PACKUNGSBEILAGE Bisolvon Hustenlöser - Saft Version 4.1 1 Gebrauchsinformation: Information für Patienten Bisolvon Hustenlöser - Saft Wirkstoff: Bromhexinhydrochlorid Lesen Sie die gesamte Packungsbeilage
PACKUNGSBEILAGE Bisolvon Hustenlöser - Saft Version 4.1 1 Gebrauchsinformation: Information für Patienten Bisolvon Hustenlöser - Saft Wirkstoff: Bromhexinhydrochlorid Lesen Sie die gesamte Packungsbeilage
KOPIE. Diabetes in Kürze. «Schritt um Schritt zu mehr Gesundheit!»
 Diabetes in Kürze «Schritt um Schritt zu mehr Gesundheit!» Schweizerische Diabetes-Gesellschaft Association Suisse du Diabète Associazione Svizzera per il Diabete Was ist Diabetes? Es gibt 2 Typen von
Diabetes in Kürze «Schritt um Schritt zu mehr Gesundheit!» Schweizerische Diabetes-Gesellschaft Association Suisse du Diabète Associazione Svizzera per il Diabete Was ist Diabetes? Es gibt 2 Typen von
Das ICD-Patientenzufriedenheitsbarometer
 Das ICD-Patientenzufriedenheitsbarometer Zu Ihrer Person 1. Geburtshr bzw. Alter Einige Fakten: 1. Das Durchschnittsalter lag bei 66 Jahren. 2. Die Hälfte von Ihnen ist mindestens 69 Jahre alt. 3. Die
Das ICD-Patientenzufriedenheitsbarometer Zu Ihrer Person 1. Geburtshr bzw. Alter Einige Fakten: 1. Das Durchschnittsalter lag bei 66 Jahren. 2. Die Hälfte von Ihnen ist mindestens 69 Jahre alt. 3. Die
BAnz AT 04.04.2014 B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Vor- und Nachteile der Kastration
 Vor- und Nachteile der Kastration Was versteht man unter Kastration? Unter Kastration versteht man die chirugische Entfernung der Keimdrüsen. Bei der Hündin handelt es sich dabei um die Eierstöcke, beim
Vor- und Nachteile der Kastration Was versteht man unter Kastration? Unter Kastration versteht man die chirugische Entfernung der Keimdrüsen. Bei der Hündin handelt es sich dabei um die Eierstöcke, beim
Das NEUE Leistungspaket der Sozialversicherung. Mehr Zahngesundheit für Kinder und Jugendliche bis zum 18. Lebensjahr. Fragen und Antworten
 Das NEUE Leistungspaket der Sozialversicherung Mehr Zahngesundheit für Kinder und Jugendliche bis zum 18. Lebensjahr Fragen und Antworten Stand: Juni 2015 1 Grundsatzfragen zum neuen Leistungspaket 1.1
Das NEUE Leistungspaket der Sozialversicherung Mehr Zahngesundheit für Kinder und Jugendliche bis zum 18. Lebensjahr Fragen und Antworten Stand: Juni 2015 1 Grundsatzfragen zum neuen Leistungspaket 1.1
UND WOFÜR WIRD ES ANGEWENDET?
 Gebrauchsinformation: Information für den Anwender Quadronal comp. gegen Kopfschmerzen 400 mg Paracetamol und 50 mg Coffein, Tablette Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahren Wirkstoffe:
Gebrauchsinformation: Information für den Anwender Quadronal comp. gegen Kopfschmerzen 400 mg Paracetamol und 50 mg Coffein, Tablette Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahren Wirkstoffe:
Soja-Lebensmittel - Quelle von hochwertigem Eiweiß
 Soja-Lebensmittel - Quelle von hochwertigem Eiweiß Thesenpapier des wissenschaftlichen Beirats der ENSA Einleitung Eiweiß ist ein wichtiger Grundnährstoff, der für das Wachstum und die Reparatur aller
Soja-Lebensmittel - Quelle von hochwertigem Eiweiß Thesenpapier des wissenschaftlichen Beirats der ENSA Einleitung Eiweiß ist ein wichtiger Grundnährstoff, der für das Wachstum und die Reparatur aller
Gebrauchsinformation: Information für Anwender. Delphi 0,1 % Creme Triamcinolonacetonid
 Gebrauchsinformation: Information für Anwender Delphi 0,1 % Creme Triamcinolonacetonid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender Delphi 0,1 % Creme Triamcinolonacetonid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. AERIUS 5 mg Filmtabletten Desloratadin
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Filmtabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN AERIUS 5 mg Filmtabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Typ-1-Diabetes und Lebensstil
 Typ-1-Diabetes und Lebensstil Bayer Austria Ges.m.b.H Herbststraße 6-10 1160 Wien 0800/220 110 www.bayerdiabetes.at Diese Informationsbroschüre ist nicht als medizinischer Ratgeber zu betrachten und ist
Typ-1-Diabetes und Lebensstil Bayer Austria Ges.m.b.H Herbststraße 6-10 1160 Wien 0800/220 110 www.bayerdiabetes.at Diese Informationsbroschüre ist nicht als medizinischer Ratgeber zu betrachten und ist
INFORMATIONSBROSCHÜRE FÜR PATIENTEN/BEZUGSPERSONEN. Bitte lies die Packungsbeilage vor der Anwendung des Arzneimittels ABILIFY sorgfältig durch.
 Die Europäischen Gesundheitsbehörden haben die Vermarktung des Arzneimittels ABILIFY an bestimmte Bedingungen geknüpft. Die vorliegenden Informationen sind Teil des obligatorischen Risikomanagementplans
Die Europäischen Gesundheitsbehörden haben die Vermarktung des Arzneimittels ABILIFY an bestimmte Bedingungen geknüpft. Die vorliegenden Informationen sind Teil des obligatorischen Risikomanagementplans
Kopf dicht? Nase zu? Husten?
 Kopf dicht? Nase zu? Husten? Inhalt 2 Inhalt 2-3 Wunderwerk Atemwege 4-7 Kopf dicht, Nase zu, Husten was im Körper passiert 8-11 Wie hilft GeloMyrtol forte? 12-15 Wirksamkeit klinisch bestätigt 16-17 Wie
Kopf dicht? Nase zu? Husten? Inhalt 2 Inhalt 2-3 Wunderwerk Atemwege 4-7 Kopf dicht, Nase zu, Husten was im Körper passiert 8-11 Wie hilft GeloMyrtol forte? 12-15 Wirksamkeit klinisch bestätigt 16-17 Wie
Pädagogik. Melanie Schewtschenko. Eingewöhnung und Übergang in die Kinderkrippe. Warum ist die Beteiligung der Eltern so wichtig?
 Pädagogik Melanie Schewtschenko Eingewöhnung und Übergang in die Kinderkrippe Warum ist die Beteiligung der Eltern so wichtig? Studienarbeit Inhaltsverzeichnis 1. Einleitung.2 2. Warum ist Eingewöhnung
Pädagogik Melanie Schewtschenko Eingewöhnung und Übergang in die Kinderkrippe Warum ist die Beteiligung der Eltern so wichtig? Studienarbeit Inhaltsverzeichnis 1. Einleitung.2 2. Warum ist Eingewöhnung
Versetzungsregeln in Bayern
 Grundschule Schüler der Jahrgangsstufen 1 und 2 rücken ohne besondere Entscheidung vor. Das Vorrücken in den Jahrgangsstufen 3 und 4 soll nur dann versagt werden, wenn der Schüler in seiner Entwicklung
Grundschule Schüler der Jahrgangsstufen 1 und 2 rücken ohne besondere Entscheidung vor. Das Vorrücken in den Jahrgangsstufen 3 und 4 soll nur dann versagt werden, wenn der Schüler in seiner Entwicklung
? Kann ich mit Karotten zu viel Vitamin A
 Schwangere aus sozial schwachen Schichten Schwangere, die alkohol-, drogen- oder nikotinabhängig sind Schwangere, die aufgrund einer chronischen Erkrankung Medikamente einnehmen müssen, welche die Nährstoffverwertung
Schwangere aus sozial schwachen Schichten Schwangere, die alkohol-, drogen- oder nikotinabhängig sind Schwangere, die aufgrund einer chronischen Erkrankung Medikamente einnehmen müssen, welche die Nährstoffverwertung
Reizdarmsyndrom lindern
 MARIA HOLL Reizdarmsyndrom lindern Mit der Maria-Holl-Methode (MHM) Der ganzheitliche Ansatz 18 Wie Sie mit diesem Buch Ihr Ziel erreichen Schritt 1: Formulieren Sie Ihr Ziel Als Erstes notieren Sie Ihr
MARIA HOLL Reizdarmsyndrom lindern Mit der Maria-Holl-Methode (MHM) Der ganzheitliche Ansatz 18 Wie Sie mit diesem Buch Ihr Ziel erreichen Schritt 1: Formulieren Sie Ihr Ziel Als Erstes notieren Sie Ihr
