Analytisches Praktikum: Qualitative Analyse
|
|
|
- Elvira Hase
- vor 6 Jahren
- Abrufe
Transkript
1 Analytisches Praktikum: Qualitative Analyse 2. Auflage Franz Josef Hahn und Günter Haubold VCH Weinheim New York Basel Cambridge Tokyo
2 Inhalt 1 Einleitung 1 2 Theoretische Grundlagen Massen Wirkungsgesetz Löslichkeitsprodukt Arbeits- und Nachweistechniken Geräte und Arbeitsmittel Hinweise auf Arbeitsfehler Probenvorbereitung Arbeitssicherheit und Umweltschutz 14 3 Nachweise der Anionen n 3.1 Theoretische Grundlagen Nachweise aus der Analysensubstanz Nachweis von Acetat-Ionen (CH 3 COO~) Nachweis von Borat-Ionen (BO?") Nachweis von Carbonat-Ionen (COl~) Nachweis von Fluorid-Ionen (F - ) Nachweis von Nitrat-Ionen (NOy) Nachweis von Oxalat-Ionen (C 2 04~) Nachweis von Silikat-Ionen (SiO^-) Nachweis von Sulfit-Ionen (SOf~) Nachweis von Thiosulfat-Ionen (S 2 0^) Nachweise aus dem Natriumcarbonatauszug Herstellung des Natriumcarbonatauszuges Nachweis von Bromid-Ionen (Br~) Nachweis von Chlorid-Ionen (Cl~) Nachweis von Iodid-Ionen (I - ) Nachweis von Chromat-Ionen (CrOj - ) 25
3 VIII Inhalt Nachweis von Nitrat-Ionen (NO^) Nachweis von Nitrit-Ionen (N0 2 ~) Nachweis von Oxalat-Ionen (C ~) Nachweis von Phosphat-Ionen (PO 3, - ) Nachweis von Sulfat-Ionen (SO 2. - ) Nachweis von Sulfid-Ionen (S 2 ~) Nachweis von Sulfit-Ionen (SO 2 ") Wiederholungsfragen 30 4 Nachweise der Kationen Theoretische Grundlagen Nachweis von Aluminium-Ionen (Al 3+ ) Nachweis von Aluminium-Ionen als Aluminiumhydroxid Nachweis von Aluminium-Ionen mit Ammoniumhydroxid-Lösung Nachweis von Aluminium-Ionen als Natriumaluminiumfluorid Nachweis von Aluminium-Ionen als Thenards Blau Nachweis von Aluminium-Ionen mit Aluminon als roter Farblack Nachweis von Aluminium-Ionen mit Alizarin-S Nachweis von Aluminium-Ionen mit Morin Nachweis von Ammonium-Ionen (NHj) Nachweis von Ammonium-Ionen als Ammoniak (NH 3 ) Nachweis von Ammonium-Ionen mit Neßlers Reagenz Nachweis von Antimon-Ionen (Sb 3+, Sb 5+ ) Nachweis von Antimon-Ionen durch Reduktion mit metallischem Eisen Nachweis von Antimon-Ionen als Antimonsulfid Nachweis von Antimon-Ionen durch Marshsche Probe Nachweis von Antimon-Ionen durch Farbreaktion mit Rhodmin B Nachweis von Arsen-Ionen (As 3+, As 5+ ) Nachweis von Arsen-Ionen als Arsen(III)-sulfid Nachweis von Arsen-Ionen als Arsen(V)-sulfid Nachweis von Arsen-Ionen durch Marshsche Probe Nachweis von Arsen-Ionen als Arsen(III)-hydrid aus alkalischer Lösung Nachweis von Barium-Ionen (Ba 2+ ) Nachweis von Barium-Ionen durch Flammenfärbung Nachweis von Barium-Ionen als Bariumsulfat Nachweis von Barium-Ionen als Bariumchromat Nachweis von Barium-Ionen als Bariumcarbonat Nachweis von Barium-Ionen mit Natriumrhodizonat 43
4 Inhalt IX 4.7 Nachweis von Bismut-Ionen (Bi 3+ ) Nachweis von Bismut-Ionen als Bismutsulfid Nachweis von Bismut-Ionen durch Hydrolysereaktion Nachweis von Bismut-Ionen als Bismuthydroxid Nachweis von Bismut-Ionen als elementares Bismut Nachweis von Bismut-Ionen mit Kaliumiodid und 8-Hydroxychinolin Nachweis von Blei-Ionen (Pb 2+ ) Nachweis von Blei-Ionen als Bleichlorid Nachweis von Blei-Ionen als Bleisulfat Nachweis von Blei-Ionen als Bleichromat Nachweis von Blei-Ionen durch Farbreaktion mit Dithizon Nachweis von Blei-Ionen als Bleisulfid Nachweis von Blei-Ionen als Bleiiodid Nachweis von Cadmium-Ionen (Cd 2+ ) Nachweis von Cadmium-Ionen als Cadmiumsulfid Nachweis von Cadmium-Ionen mit Natriumoxalat und Schwefel im Glührohr Nachweis von Calcium-Ionen (Ca 2+ ) Nachweis von Calcium-Ionen durch Flammenfärbung Nachweis von Calcium-Ionen als Calciumcarbonat Nachweis von Calcium-Ionen als Calciumoxalat Nachweis von Calcium-Ionen mit Kaliumhexacyanoferrat(II) Nachweis von Chrom-Ionen (Cr 3+ ) Nachweis von Chrom-Ionen durch Oxidationsschmelze Nachweis von Chrom-Ionen durch Phosphorsalz- oder Boraxperle Nachweis von Chrom-Ionen als Chrom(III)-hydroxid Nachweis von Chrom-Ionen als Bariumchromat Nachweis von Chrom-Ionen als Chrom(VI)-peroxid Nachweis von Cobalt-Ionen (Co 2+ ) Nachweis von Cobalt-Ionen durch Phosphorsalz oder Boraxperle Nachweis von Cobalt-Ionen als Cobalthydroxid Nachweis von Cobalt-Ionen mit Amrnoniumthiocyanat Nachweis von Cobalt-Ionen mit Ammoniumtetrathiocyanatomercurat(II) Nachweis von Eisen-Ionen (Fe 2+, Fe 3+ ) Nachweis von Eisen-Ionen als Eisenhydroxide Nachweis von Eisen-Ionen mit Kaliumhexacyanoferrat(II) Nachweis von Eisen-Ionen mit Dimethylglyoxim Nachweis von Eisen-Ionen mit Amrnoniumthiocyanat Nachweis von Kalium-Ionen (K + ) Nachweis von Kalium-Ionen durch Flammenfärbung Nachweis von Kalium-Ionen mit Perchlorsäure Nachweis von Kalium-Ionen als Kaliumnatriumhexanitrocobaltat(III) Nachweis von Kalium-Ionen als Kaliumtetraphenylborat 61
5 X Inhalt 4.15 Nachweis von Kupfer-Ionen (Cu 2+ ) Nachweis von Kupfer-Ionen durch Flammenfärbung Nachweis von Kupfer-Ionen mit Ammoniumhydroxid-Lösung Nachweis von Kupfer-Ionen mit Kaliumhexacyanoferrat(II) Nachweis von Kupfer-Ionen mit Ammoniumtetrathiocyanatomercurat(II) Nachweis von Magnesium-Ionen (Mg 2+ ) Nachweis von Magnesium-Ionen als Magnesiumammoniumphosphat Nachweis von Magnesium-Ionen mit Magneson als blauer Farblack Nachweis von Magnesium-Ionen mit Titangelb als roter Farblack Nachweis von Magnesium-Ionen mit Chinalizarin als blauer Farblack Nachweis von Mangan-Ionen (Mn 2+ ) Nachweis von Mangan-Ionen durch Oxidationsschmelze Nachweis von Mangan-Ionen durch Phosphorsalz- oder Boraxperle Nachweis von Mangan-Ionen als Mangansulfid Nachweis von Mangan-Ionen mit Ammoniumhydrogenphosphat Nachweis von Mangan-Ionen mit Bleidioxid Nachweis von Mangan-Ionen mit Ammoniumperoxodisulfat Nachweis von Natrium-Ionen (Na + ) Nachweis von Natrium-Ionen durch Flammenfärbung Nachweis von Natrium-Ionen als Natriummagnesiumuranylacetat Nachweis von Natrium-Ionen mit Kaliumhexahydroxoantimonat(V) Nachweis von Nickel-Ionen (Ni 2+ ) Nachweis von Nickel-Ionen mit der Phosphorsalzperle Nachweis von Nickel-Ionen als Nickelhydroxid Nachweis von Nickel-Ionen mit Ammoniumhydroxid-Lösung Nachweis von Nickel-Ionen als Nickeldimethylglyoxim Nachweis von Quecksilber-Ionen (Hg 2+, Hg 2+ ) Nachweis von Quecksilber-Ionen als Kupferamalgam Nachweis von Quecksilber-Ionen als elementares Quecksilber Nachweis von Quecksilber-Ionen als Cobalttetrathiocyanatomercurat Nachweis von Quecksilber-Ionen mit Zinn(II)-chlorid Nachweis von Silber-Ionen (Ag + ) Nachweis von Silber-Ionen als Silberchlorid Nachweis von Silber-Ionen als Silberchromat Nachweis von Strontium-Ionen (Sr 2+ ) Nachweis von Strontium-Ionen durch Flammenfärbung Nachweis von Strontium-Ionen als Strontiumsulfat Nachweis von Strontium-Ionen als Strontiumcarbonat Nachweis von Strontium-Ionen als Strontiumchromat Nachweis von Zink-Ionen (Zn 2+ ) Nachweis von Zink-Ionen als Rinnmanns-Grün Nachweis von Zink-Ionen als Zinksulfid 77
6 Inhalt XI Nachweis von Zink-Ionen als Zinkhexacyanoferrat(III) Nachweis von Zink-Ionen mit Ammoniumtetrathiocyanatomercurat(II) Nachweis von Zink-Ionen mit Dithizon Nachweis von Zinn-Ionen (Sn 2+, Sn 4+ ) Nachweis von Zinn-Ionen durch die Leuchtprobe Nachweis von Zinn-Ionen als Zinn(II)-sulfid oder Zinn(IV)-sulfid Nachweis von Zinn-Ionen als Molybdänblau Wiederholungsfragen 80 5 Identifizierung anorganischer Verbindungen Grundlagen, Verzeichnis der zu identifizierenden Substanzen Aufgaben- und Bearbeitungsvorschlag 83 6 Trennungsgang der Kationen Theoretische Grundlagen Vorproben Allgemeines Flammenfärbung und Spektralanalyse Perlreaktionen Behandlung im Glühröhrchen Lösen der Substanz Identifizierung schwerlöslicher Rückstände Aufschluß schwerlöslicher Rückstände Wiederholungsfragen Salzsäuregruppe Theoretische Grundlagen Arbeitsanweisung Wiederholungsfragen Hydrogensulfid-Gruppe Theoretische Grundlagen Toxikologie und Bereitstellung von Hydrogensulfid Fällung der Sulfide Lithiumhydroxid-Trennung Trennung der Kupfer-Gruppe Trennung der Arsen-Gruppe Arbeitsanweisung Vorbereitung der Probe-Lösung für die Sulfid-Fällung Fällung der Sulfide mit Thioacetamid-Lösung Fällung der Sulfide mit Hydrogensulfid 112
7 XII Inhalt Lithiumhydroxid-Trennung Trennung der Kupfer-Gruppe Trennung der Arsen-Gruppe Wiederholungsfragen Ammoniumsulfid-Gruppe Theoretische Grundlagen Allgemeines Die Hydrolyse-Trennung Die Salzsäure-Hydrogenperoxid-Trennung Arbeitsanweisung Trennung der Ammoniumsulfid-Gruppe durch die Hydrolyse-Trennung Trennung der Ammoniumsulfid-Gruppe durch die Salzsäure-Hydrogenperoxid- Trennung Wiederholungsfragen Ammoniumcarbonat-Gruppe Theoretische Grundlagen Allgemeines Das Chromat-Verfahren Das Ethanol-Verfahren Arbeitsanweisung Fällung der Carbonate Trennung der Carbonate nach dem Chromat-Verfahren Trennung der Carbonate nach dem Ethanol-Verfahren Wiederholungsfragen Lösliche Gruppe (Magnesium-, Alkalimetall- und Ammonium-Ionen) Theoretische Grundlagen Allgemeines Die Gruppentrennung Austreibung oder Zerstörung der Ammoniumsalze Arbeitsanweisung Trennung der löslichen Gruppe, Nachweis von Ammonium-Ionen Wiederholungsfragen Identifizierung organischer Verbindungen Theoretische Grundlagen Vorproben Aussehen und Geruch der Substanz Brenn- und Glühverhalten der Substanz Physikalische Eigenschaften Löslichkeit Nachweis der Elemente (Elementaranalyse) Nachweis von Kohlenstoff und Wasserstoff 141
8 Inhalt XIII Nachweis von Stickstoff Nachweis von Schwefel Nachweis von Halogenen Nachweis von Phosphor Nachweis funktioneller Gruppen Allgemeines Nachweis von Alkenen (Doppelbindung) Nachweis von Alkoholen und Phenolen (Hydroxy-Gruppe) Nachweis von Alkoholen und Phenolen mit Ammoniumcer(IV)-nitrat Unterscheidung primärer, sekundärer und tertiärer wasserlöslicher Alkohole mit dem Lukas-Reagenz Nachweis mit Natrium Nachweis von Aldehyden und Ketonen (Carbonyl-Gruppen) Nachweis von Aldehyden und Ketonen mit Dinitrophenylhydrazin Nachweis von Aldehyden und Ketonen mit Natriumhydrogensulfit Nachweis von Aldehyden mit Fehlingscher Lösung Nachweis von Aldehyden mit fuchsinschwefliger Säure (Schiffsches Reagenz) Nachweis von Methylketonen mit o-nitrobenzaldehyd Nachweis von Carbonsäuren und Carbonsäureestern (Carboxy-Gruppe) Nachweis von Carbonsäuren mit Hydroxylamin Nachweis von Carbonsäuren mit Alkali-Lauge Nachweis von Carbonsäureestern mit Hydroxylamin Nachweis von primären Aminen (Amino-Gruppe) Nachweis von primären Aminen als Alkylisocyanide (Isonitrile) Nachweis von primären Aminen durch Reaktion mit salpetriger Säure Wiederholungsfragen Anhang: Fließbilder zur Vollanalyse Der Trennungsgang in Übersicht Fließbilder zum Trennungsgang Lösen der Substanz Salzsäure-Gruppe Hydrogensulfid-Gruppe Lithiumhydroxid-Trennung Kupfer-Gruppe Arsen-Gruppe Ammoniumsulfid-Gruppe Hydrolyse-Trennung Salzsäure-Hydrogenperoxid-Trennung Ammoniumcarbonat-Gruppe Überblick Chromat-Verfahren 168
9 XIV Inhalt Ethanol-Verfahren Lösliche Gruppe Aufgaben- und Bearbeitungsvorschlag 172 Register 177
Einzelionennachweise des H2S-Trennungsgangs. Natrium Na + Kalium K + Ammonium NH4 + Blei Pb 2+ (für die Laborprüfung , LBT) Stand: 23.9.
 Einzelionennachweise des H2S-Trennungsgangs (für die Laborprüfung 771105, LBT) Stand: 23.9.2011 Natrium Na + gelbe Flammfärbung Kalium K + 1. mit Perchlorsäure im sauren Auszug der Urprobe: K + + ClO -
Einzelionennachweise des H2S-Trennungsgangs (für die Laborprüfung 771105, LBT) Stand: 23.9.2011 Natrium Na + gelbe Flammfärbung Kalium K + 1. mit Perchlorsäure im sauren Auszug der Urprobe: K + + ClO -
Wasserstoff. Helium. Bor. Kohlenstoff. Standort: Name: Ordnungszahl: Standort: Name: Ordnungszahl: 18. Gruppe. Standort: Ordnungszahl: Name:
 H Wasserstoff 1 1. Gruppe 1. Periode He Helium 2 18. Gruppe 1. Periode B Bor 5 13. Gruppe C Kohlenstoff 6 14. Gruppe N Stickstoff 7 15. Gruppe O Sauerstoff 8 16. Gruppe Ne Neon 10 18. Gruppe Na Natrium
H Wasserstoff 1 1. Gruppe 1. Periode He Helium 2 18. Gruppe 1. Periode B Bor 5 13. Gruppe C Kohlenstoff 6 14. Gruppe N Stickstoff 7 15. Gruppe O Sauerstoff 8 16. Gruppe Ne Neon 10 18. Gruppe Na Natrium
EINFÜHRUNG IN DIE QUALITATIVE CHEMISCHE ANALYSE
 EINFÜHRUNG IN DIE QUALITATIVE CHEMISCHE ANALYSE VON PROFESSOR DR. R. FRESENIUS UND DR. PHIL. HABIL. A. GEHRING UNTER MITARBEIT VON DIPL.-CHEM. O. FUCHS UND MARIANNE VULPIUS 3. VERBESSERTE AUFLAGE MIT 5
EINFÜHRUNG IN DIE QUALITATIVE CHEMISCHE ANALYSE VON PROFESSOR DR. R. FRESENIUS UND DR. PHIL. HABIL. A. GEHRING UNTER MITARBEIT VON DIPL.-CHEM. O. FUCHS UND MARIANNE VULPIUS 3. VERBESSERTE AUFLAGE MIT 5
Unwanted. TRITON Error correction sheet ICP-OES V1.1 !!! !!!!!!!! TRITON GmbH Rather Broich Düsseldorf (Germany)
 Unwanted TRITON Error correction sheet ICP-OES V1.1 1 Unerwünschte Schwermetalle Quecksilber zu hoch 4x 15% wöchentlicher Wasserwechsel mit Hg Selen zu hoch 4x 15% wöchentlicher Wasserwechsel mit Se Cadmium
Unwanted TRITON Error correction sheet ICP-OES V1.1 1 Unerwünschte Schwermetalle Quecksilber zu hoch 4x 15% wöchentlicher Wasserwechsel mit Hg Selen zu hoch 4x 15% wöchentlicher Wasserwechsel mit Se Cadmium
Seminar zum Grundpraktikum Anorganische Chemie
 Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 201 Christoph Wölper Universität DuisburgEssen 4 CO Analyse 4 SalzsäureGruppe Ag + Pb 2+ Hg 2 2+ Bi + Cu 2+ Cd 2+ Sb +/5+ Sn 2+/4+ As +/5+
Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 201 Christoph Wölper Universität DuisburgEssen 4 CO Analyse 4 SalzsäureGruppe Ag + Pb 2+ Hg 2 2+ Bi + Cu 2+ Cd 2+ Sb +/5+ Sn 2+/4+ As +/5+
Anorganische-Chemie. Michael Beetz Arbeitskreis Prof. Bein. Grundpraktikum für Biologen 2017
 Michael Beetz Arbeitskreis Prof. Bein Butenandstr. 11, Haus E, E 3.027 michael.beetz@cup.uni-muenchen.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Trennungsgänge und Nachweise # 2 Trennungsgänge
Michael Beetz Arbeitskreis Prof. Bein Butenandstr. 11, Haus E, E 3.027 michael.beetz@cup.uni-muenchen.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Trennungsgänge und Nachweise # 2 Trennungsgänge
Seminar zum Grundpraktikum Anorganische Chemie
 Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2012 Christoph Wölper Universität DuisburgEssen 4 CO Cl Analyse 4 SalzsäureGruppe Ag + Pb 2+ Hg 2 2+ Bi + Cu 2+ Cd 2+ Sb +/5+ Sn 2+/4+ As +/5+
Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2012 Christoph Wölper Universität DuisburgEssen 4 CO Cl Analyse 4 SalzsäureGruppe Ag + Pb 2+ Hg 2 2+ Bi + Cu 2+ Cd 2+ Sb +/5+ Sn 2+/4+ As +/5+
Integration von Schülerinnen und Schülern mit einer Sehschädigung an Regelschulen. Didaktikpool
 Integration von Schülerinnen und Schülern mit einer Sehschädigung an Regelschulen Didaktikpool Periodensystem der Elemente für blinde und hochgradig sehgeschädigte Laptop-Benutzer Reinhard Apelt 2008 Technische
Integration von Schülerinnen und Schülern mit einer Sehschädigung an Regelschulen Didaktikpool Periodensystem der Elemente für blinde und hochgradig sehgeschädigte Laptop-Benutzer Reinhard Apelt 2008 Technische
Übungsaufgaben zu Ionenreaktionen in wässriger Lösung
 Übungsaufgaben zu Ionenreaktionen in wässriger Lösung 1) Berechnen Sie den phwert von folgenden Lösungen: a) 0.01 M HCl b) 3 10 4 M KOH c) 0.1 M NaOH d) 0.1 M CH 3 COOH (*) e) 0.3 M NH 3 f) 10 8 M HCl
Übungsaufgaben zu Ionenreaktionen in wässriger Lösung 1) Berechnen Sie den phwert von folgenden Lösungen: a) 0.01 M HCl b) 3 10 4 M KOH c) 0.1 M NaOH d) 0.1 M CH 3 COOH (*) e) 0.3 M NH 3 f) 10 8 M HCl
H Wasserstoff. O Sauerstoff
 He Helium Ordnungszahl 2 Atommasse 31,8 268,9 269,7 0,126 1,25 H Wasserstoff Ordnungszahl 1 Atommasse 14,1 252,7 259,2 2,1 7,14 1 3,45 1,38 Li Lithium Ordnungszahl 3 Atommasse 13,1 1330 180,5 1,0 0,53
He Helium Ordnungszahl 2 Atommasse 31,8 268,9 269,7 0,126 1,25 H Wasserstoff Ordnungszahl 1 Atommasse 14,1 252,7 259,2 2,1 7,14 1 3,45 1,38 Li Lithium Ordnungszahl 3 Atommasse 13,1 1330 180,5 1,0 0,53
Wasser und Abwasser - Methoden und Preise
 Wasser und Abwasser - Methoden und Preise Inhalt Wasser GSchV / FIV / SLMB / EDI Allgemeine Parameter 1 Chlor-, Phosphor- und Stickstoffverbindungen 1 Elemente, gelöst oder nach Aufschluss 2 Programme
Wasser und Abwasser - Methoden und Preise Inhalt Wasser GSchV / FIV / SLMB / EDI Allgemeine Parameter 1 Chlor-, Phosphor- und Stickstoffverbindungen 1 Elemente, gelöst oder nach Aufschluss 2 Programme
Ausführung qualitativer Analysen
 Ausführung qualitativer Analysen Von Prof. Dr. S. Walter Souci unter Mitwirkung von Prof. Dr. Heinrich Thies Neunte, neu bearbeitete Auflage Springer-Verlag Berlin Heidelberg GmbH 1971 ISBN 978-3-662-40496-6
Ausführung qualitativer Analysen Von Prof. Dr. S. Walter Souci unter Mitwirkung von Prof. Dr. Heinrich Thies Neunte, neu bearbeitete Auflage Springer-Verlag Berlin Heidelberg GmbH 1971 ISBN 978-3-662-40496-6
Quantitative Anorganische Analyse
 Hermann Lux Wolfgang Fichtner Quantitative Anorganische Analyse Leitfadenj ßurn^f fa j$ jkgrn ;. Neunte, neubearbeitete Auflage Mit 50 Abbildungen Springer-Verlag Berlin Heidelberg New York London Paris
Hermann Lux Wolfgang Fichtner Quantitative Anorganische Analyse Leitfadenj ßurn^f fa j$ jkgrn ;. Neunte, neubearbeitete Auflage Mit 50 Abbildungen Springer-Verlag Berlin Heidelberg New York London Paris
6. Seminar. Prof. Dr. Christoph Janiak. Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002
 ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 6. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 6. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
Handbuch für das Eisenhüttenlaboratorium, Band 3, Teil 1 5. Inhaltsübersicht
 Handbuch für das Eisenhüttenlaboratorium, Band 3, Teil 1 5 Inhaltsübersicht Seite Vorwort zur dritten Ausgabe 1 Allgemeine Hinweise 17 Allgemein gebrauchte Reagenzien 22 Die Untersuchung der Erze Die Bestimmung
Handbuch für das Eisenhüttenlaboratorium, Band 3, Teil 1 5 Inhaltsübersicht Seite Vorwort zur dritten Ausgabe 1 Allgemeine Hinweise 17 Allgemein gebrauchte Reagenzien 22 Die Untersuchung der Erze Die Bestimmung
Prüfbericht. Untersuchungsergebnisse der Parameter nach TrinkwV. Anlage 1-4, vom Gladenbach-Rachelshausen
 Betreiber : Messstellen- (HLfU) : 7101 Probenart : U-13 U13 Untersuchungs- (Labor) : B141770/CH140527 TrinkwV. Anlage 1, Teil I Parameter Einheit Prüfergebnis GW 1) BG 2) Verfahren 2. Enterokokken KBE/100ml
Betreiber : Messstellen- (HLfU) : 7101 Probenart : U-13 U13 Untersuchungs- (Labor) : B141770/CH140527 TrinkwV. Anlage 1, Teil I Parameter Einheit Prüfergebnis GW 1) BG 2) Verfahren 2. Enterokokken KBE/100ml
Qualitative Analyse. - Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch,
 - Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch, Löslichkeit - charakteristische Nachweisreaktionen für Einzelionen: - Fällungsreaktionen
- Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch, Löslichkeit - charakteristische Nachweisreaktionen für Einzelionen: - Fällungsreaktionen
Anorganisch-Chemisches Praktika für Studierende der PHYS, GEÖK, AGEW, MWT und TVWL:
 Anorganisch-Chemisches Praktika für Studierende der PHYS, GEÖK, AGEW, MWT und TVWL: Analyse 4: Vollanalyse Dr. Christopher Anson INSTITUT FÜR ANORGANISCHE CHEMIE KIT Universität des Landes Baden-Württemberg
Anorganisch-Chemisches Praktika für Studierende der PHYS, GEÖK, AGEW, MWT und TVWL: Analyse 4: Vollanalyse Dr. Christopher Anson INSTITUT FÜR ANORGANISCHE CHEMIE KIT Universität des Landes Baden-Württemberg
Inhalte der Veranstaltung Chemisches Praktikum für Geologen und Physiker an der TU München
 Inhalte der Veranstaltung Chemisches Praktikum für Geologen und Physiker an der TU München Stand: Herbst 2002 A) Einführung in das chemische Experimentieren (Erläuterung von Laborgeräten, Experimentiertechniken
Inhalte der Veranstaltung Chemisches Praktikum für Geologen und Physiker an der TU München Stand: Herbst 2002 A) Einführung in das chemische Experimentieren (Erläuterung von Laborgeräten, Experimentiertechniken
Reagenzien für Photometer
 Reagenzien für Photometer SERIE HI 937(00)-(00) Artikel : Reagenzien für Photometer, Cyanursäure (100 Tests) HI 93722-01 Parameter : Cyanursäure - Reagenzien für Photometer, Cyanursäure (300 Tests) HI
Reagenzien für Photometer SERIE HI 937(00)-(00) Artikel : Reagenzien für Photometer, Cyanursäure (100 Tests) HI 93722-01 Parameter : Cyanursäure - Reagenzien für Photometer, Cyanursäure (300 Tests) HI
Emder Wasser Trinkwasser-Analysewerte
 Emder Wasser Trinkwasser-Analysewerte Die Lust auf Wasser hat viele Gesichter. An heißen Sommertagen träumen wir von einer erfrischenden Dusche und einem Glas Wasser gegen den Durst. Im Winter verwöhnt
Emder Wasser Trinkwasser-Analysewerte Die Lust auf Wasser hat viele Gesichter. An heißen Sommertagen träumen wir von einer erfrischenden Dusche und einem Glas Wasser gegen den Durst. Im Winter verwöhnt
Analysenservice FM-VEA-AS
 Analysenservice FM-VEA-AS Preisliste 2015 Analytik von Wasser, Abwasser, Böden, Schlämmen, Abfällen, Sonderproben Art der Leistung Probennahme nach Aufwand nach Aufwand Aufbereitung von Feststoffen Brechen
Analysenservice FM-VEA-AS Preisliste 2015 Analytik von Wasser, Abwasser, Böden, Schlämmen, Abfällen, Sonderproben Art der Leistung Probennahme nach Aufwand nach Aufwand Aufbereitung von Feststoffen Brechen
Grenzwerte für die Annahme von Abfällen
 BGBl. II - Ausgegeben am 30. Jänner 2008 - Nr. 39 1 von 11 Allgemeines e für die Annahme von Abfällen Anhang 1 Für die Untersuchung und Beurteilung, ob die e gegebenenfalls nach Maßgabe des 8 eingehalten
BGBl. II - Ausgegeben am 30. Jänner 2008 - Nr. 39 1 von 11 Allgemeines e für die Annahme von Abfällen Anhang 1 Für die Untersuchung und Beurteilung, ob die e gegebenenfalls nach Maßgabe des 8 eingehalten
ANIONENNACHWEISE Vorlesung analytische Chemie SS 2010
 ANIONENNACHWEISE Vorlesung analytische Chemie SS 2010 Übersicht Allgemeines zu Nachweisen Anionentrennungsgang Ausgewählte Einzelnachweise Grenzkonzentration Grenzkonzentration (GK, D): die Konzentration,
ANIONENNACHWEISE Vorlesung analytische Chemie SS 2010 Übersicht Allgemeines zu Nachweisen Anionentrennungsgang Ausgewählte Einzelnachweise Grenzkonzentration Grenzkonzentration (GK, D): die Konzentration,
Nomenklatur einfacher anorganischer Verbindungen
 Nomenklatur einfacher anorganischer Verbindungen chemische Reaktion: Elemente verbinden sich in verschiedenen spezifischen Proportionen 2 H 2 + 2 > 2 H 2 Elementsymbol stöchiometrischer Koeffizient Atomverhältnis
Nomenklatur einfacher anorganischer Verbindungen chemische Reaktion: Elemente verbinden sich in verschiedenen spezifischen Proportionen 2 H 2 + 2 > 2 H 2 Elementsymbol stöchiometrischer Koeffizient Atomverhältnis
Text Anhang 1. Grenzwerte für die Annahme von Abfällen
 Kurztitel Deponieverordnung 2008 Kundmachungsorgan BGBl. II Nr. 39/2008 zuletzt geändert durch BGBl. II Nr. 104/2014 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 01.06.2014 Text Anhang 1 Allgemeines e für
Kurztitel Deponieverordnung 2008 Kundmachungsorgan BGBl. II Nr. 39/2008 zuletzt geändert durch BGBl. II Nr. 104/2014 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 01.06.2014 Text Anhang 1 Allgemeines e für
7. Woche. Gesamtanalyse (Vollanalyse) einfacher Salze. Qualitative Analyse anorganischer Verbindungen
 7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
Trennungsgang. AC-I Seminar, B.
 Trennungsgang http://illumina-chemie.de/mangan-chrom-t2100.html www.chemgapedia.de, www.chemische-experimente.com 1 Trennungsgang auf einen Blick Trennungsgang Reaktionen in wässriger Lösung Fällung und
Trennungsgang http://illumina-chemie.de/mangan-chrom-t2100.html www.chemgapedia.de, www.chemische-experimente.com 1 Trennungsgang auf einen Blick Trennungsgang Reaktionen in wässriger Lösung Fällung und
Grenzwerte für die Annahme von Abfällen auf Deponien
 Anhang 1 e für die Annahme von Abfällen auf Deponien Allgemeines Für die Untersuchung und Beurteilung, ob die e eingehalten werden, sind der Anhang 4 und gegebenenfalls der Anhang 5 anzuwenden. Die Behörde
Anhang 1 e für die Annahme von Abfällen auf Deponien Allgemeines Für die Untersuchung und Beurteilung, ob die e eingehalten werden, sind der Anhang 4 und gegebenenfalls der Anhang 5 anzuwenden. Die Behörde
Johann Wolfgang Goethe-Universität Frankfurt am Main Institut für Pharmazeutische Chemie
 Johann Wolfgang Goethe-Universität Frankfurt am Main Institut für Pharmazeutische Chemie Name: Matrikelnummer: Beurteilung: / Zwischenklausur zum Praktikum QUALITATIVE ANORGANISCHE ANALYSE Termin: 8. November
Johann Wolfgang Goethe-Universität Frankfurt am Main Institut für Pharmazeutische Chemie Name: Matrikelnummer: Beurteilung: / Zwischenklausur zum Praktikum QUALITATIVE ANORGANISCHE ANALYSE Termin: 8. November
Entwurf 6.August Jänner Anhang 1 Grenzwerte für die Annahme von Abfällen auf Deponien
 Entwurf 6.August 2007 9.Jänner 2007 Anhang 1 e für die Annahme von Abfällen auf Deponien Allgemeines Für die Untersuchung und Beurteilung, ob die e eingehalten werden, sind der Anhang 4 und gegebenenfalls
Entwurf 6.August 2007 9.Jänner 2007 Anhang 1 e für die Annahme von Abfällen auf Deponien Allgemeines Für die Untersuchung und Beurteilung, ob die e eingehalten werden, sind der Anhang 4 und gegebenenfalls
Seminar zum Grundpraktikum Anorganische Chemie
 Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2012 Christoph Wölper Universität Duisburg-Essen Analyse 2 (NH 4 ) 2 CO 3 -Gruppe Ba 2+ Sr 2+ Ca 2+ Lösliche Gruppe Na + Mg 2+ NH 4+ Eigenschaften
Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2012 Christoph Wölper Universität Duisburg-Essen Analyse 2 (NH 4 ) 2 CO 3 -Gruppe Ba 2+ Sr 2+ Ca 2+ Lösliche Gruppe Na + Mg 2+ NH 4+ Eigenschaften
Formeln & Namen. Will man ein Kapitel nicht bearbeiten, kann man dessen Aufgabenzahl auf '0' setzen.
 Kategorie Übungen und Tests Kategorien 4 Übungsmodus ja Testmodus ja Schwierigkeitsgrade 2/2 vorwählbare Aufgabenzahl 0-20 Aktueller Notenstand ja Highscore ja Musik zur Belobigung wählbar Spezielle Hilfen:
Kategorie Übungen und Tests Kategorien 4 Übungsmodus ja Testmodus ja Schwierigkeitsgrade 2/2 vorwählbare Aufgabenzahl 0-20 Aktueller Notenstand ja Highscore ja Musik zur Belobigung wählbar Spezielle Hilfen:
3. Seminar. Prof. Dr. Christoph Janiak. Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002
 ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 3. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 3. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
Ausführung potentiometrischer Analysen
 Ausführung potentiometrischer Analysen nebst vollständigen Analysenvorschriften für technische Produkte Von Dr. Werner Hiltner Breslau Einleitung 1 Allgemeiner Teil. A. Grundlagen der potentiometrischen
Ausführung potentiometrischer Analysen nebst vollständigen Analysenvorschriften für technische Produkte Von Dr. Werner Hiltner Breslau Einleitung 1 Allgemeiner Teil. A. Grundlagen der potentiometrischen
Aluminium. Eisen. Gold. Lithium. Platin. Neodym
 Fe Eisen Al Aluminium Li Lithium Au Gold Pt Platin Nd Neodym Zn Zink Sn Zinn Ni Nickel Cr Chrom Mo Molybdän V Vanadium Co Cobalt In Indium Ta Tantal Mg Magnesium Ti Titan Os Osmium Pb Blei Ag Silber
Fe Eisen Al Aluminium Li Lithium Au Gold Pt Platin Nd Neodym Zn Zink Sn Zinn Ni Nickel Cr Chrom Mo Molybdän V Vanadium Co Cobalt In Indium Ta Tantal Mg Magnesium Ti Titan Os Osmium Pb Blei Ag Silber
1. Karte der LAWA-Messstellen... A 1-0
 Anhang I: Inhaltsübersicht Anhang I: Karten und grafische Darstellungen 1. Karte der LAWA-Messstellen... A 1-0 2. Karten zur Wasserbeschaffenheit... A 2-0 Chlorid...A 2-1 Orthophosphat-Phosphor...A 2-2
Anhang I: Inhaltsübersicht Anhang I: Karten und grafische Darstellungen 1. Karte der LAWA-Messstellen... A 1-0 2. Karten zur Wasserbeschaffenheit... A 2-0 Chlorid...A 2-1 Orthophosphat-Phosphor...A 2-2
Seminar zum Grundpraktikum Anorganische Chemie
 Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2015 Christoph Wölper Universität DuisburgEssen Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2015 Christoph Wölper http://www.unidue.de/~adb297b
Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2015 Christoph Wölper Universität DuisburgEssen Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2015 Christoph Wölper http://www.unidue.de/~adb297b
Laborprotokoll Qualitative Analyse Ralph Koitz, Einzelsalz
 1. Einzelsalz Aufgabenstellung: Nasschemische qualitative Analyse eines anorganischen Einzelsalzes. o Farblose, grobkörnige Kristalle o Flammenfärbung: leicht orange, nicht charakteristisch da vermutlich
1. Einzelsalz Aufgabenstellung: Nasschemische qualitative Analyse eines anorganischen Einzelsalzes. o Farblose, grobkörnige Kristalle o Flammenfärbung: leicht orange, nicht charakteristisch da vermutlich
Der Trennungsgang der Qualitativen Analyse liefert zahlreiche Anwendungsbeispiele für...
 Qualitative Analyse Der Trennungsgang der Qualitativen Analyse liefert zahlreiche Anwendungsbeispiele für... Qualitative Analyse Die qualitative Analyse ist der Teil der analytischen Chemie, der sich mit
Qualitative Analyse Der Trennungsgang der Qualitativen Analyse liefert zahlreiche Anwendungsbeispiele für... Qualitative Analyse Die qualitative Analyse ist der Teil der analytischen Chemie, der sich mit
Prüfbericht über Wasseruntersuchungen gemäß TrinkwV 2001
 Zweckverband Wassererversorgung und Abwasserbeseitigung Grimmen Grellenberger Straße 6 1857 Grimmen Tel. ( 38326 ) 63- / Fax ( 38326 ) 63-12 Zweckverband Wasserversorgung und Abwasserbeseitigung Grimmen
Zweckverband Wassererversorgung und Abwasserbeseitigung Grimmen Grellenberger Straße 6 1857 Grimmen Tel. ( 38326 ) 63- / Fax ( 38326 ) 63-12 Zweckverband Wasserversorgung und Abwasserbeseitigung Grimmen
Wasseranalyse - Prüfbericht
 101 Ww.Ausgang H Grenzwert 1,2-Dichlorethan < 0,000100 0,003000 mg/l DIN EN ISO 10301 (F4) 2,6-Dichlorbenzamid < 0,000030 0,003000 mg/l DIN EN ISO 11369 (F12) Aluminium (Al), gesamt < 0,0050 0,2000 mg/l
101 Ww.Ausgang H Grenzwert 1,2-Dichlorethan < 0,000100 0,003000 mg/l DIN EN ISO 10301 (F4) 2,6-Dichlorbenzamid < 0,000030 0,003000 mg/l DIN EN ISO 11369 (F12) Aluminium (Al), gesamt < 0,0050 0,2000 mg/l
Das Formelpuzzle Kopiervorlage
 Das Formelpuzzle Kopiervorlage Die Vorlage wird foliert, die einzelnen Bausteine werden ausgeschnitten. Durch einfaches Aneinanderlegen von Kationen und Anionen können die Formeln von Säuren, Basen und
Das Formelpuzzle Kopiervorlage Die Vorlage wird foliert, die einzelnen Bausteine werden ausgeschnitten. Durch einfaches Aneinanderlegen von Kationen und Anionen können die Formeln von Säuren, Basen und
Umwelthygiene Marburg GmbH & Co KG
 1305431 Umwelthygiene Marburg GmbH & Co KG Rudolf Breitscheidstr. 24, D35037 Marburg Umwelthygiene Marburg GmbH & Co KG Staatlich anerkannte Untersuchungsstelle nach 15 Abs. 4 Amtsgericht Marburg: HRB
1305431 Umwelthygiene Marburg GmbH & Co KG Rudolf Breitscheidstr. 24, D35037 Marburg Umwelthygiene Marburg GmbH & Co KG Staatlich anerkannte Untersuchungsstelle nach 15 Abs. 4 Amtsgericht Marburg: HRB
Analyse 2015 für das Trinkwasser aus dem Wasserwerk Nord
 Analyse 2015 für das Trinkwasser aus dem Wasserwerk Nord Anorganische Spurenelemente Aluminium mg/l 0,2 nicht nachweisbar 0,01 Antimon mg/l 0,005 nicht nachweisbar 0,001 Arsen mg/l 0,01 nicht nachweisbar
Analyse 2015 für das Trinkwasser aus dem Wasserwerk Nord Anorganische Spurenelemente Aluminium mg/l 0,2 nicht nachweisbar 0,01 Antimon mg/l 0,005 nicht nachweisbar 0,001 Arsen mg/l 0,01 nicht nachweisbar
Analytische Chemie. B. Sc. Chemieingenieurwesen. 9. September 2015, Uhr. Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc.
 Analytische Chemie B. Sc. Chemieingenieurwesen 9. September 2015, 13.30 16.30 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Analytische Chemie B. Sc. Chemieingenieurwesen 9. September 2015, 13.30 16.30 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
PRÜFBERICHT 925043-675912
 Tel.: +49 (843) 79, Fax: +49 (843) 724 [@ANALYNR_START=67592] [@BARCODE= R] Dr.Blasy-Dr.Busse Moosstr. 6A, 82279 Eching ZV ZUR WASSERVERSORGUNG ACHENGRUPPE Herr Jürs RATHAUSPLATZ 8 8347 KIRCHANSCHÖRING
Tel.: +49 (843) 79, Fax: +49 (843) 724 [@ANALYNR_START=67592] [@BARCODE= R] Dr.Blasy-Dr.Busse Moosstr. 6A, 82279 Eching ZV ZUR WASSERVERSORGUNG ACHENGRUPPE Herr Jürs RATHAUSPLATZ 8 8347 KIRCHANSCHÖRING
6,
 ph-wert 10,00 9,50 9,00 8,50 8,00 7,50 7,00 6,50 U:\13h\U135009_DGW_Änderung_Planfeststellung\02_Daten\Chemie\Wasser\Analyseberichte_neu\Sickerwasse_v03.xls Seite 1/18 Leitfähigkeit µs/cm 20000 15000 10000
ph-wert 10,00 9,50 9,00 8,50 8,00 7,50 7,00 6,50 U:\13h\U135009_DGW_Änderung_Planfeststellung\02_Daten\Chemie\Wasser\Analyseberichte_neu\Sickerwasse_v03.xls Seite 1/18 Leitfähigkeit µs/cm 20000 15000 10000
Entsäuern und Entgiften mit Body Detox neueste wissenschaftliche Erkenntnisse
 Entsäuern und Entgiften mit Body Detox neueste wissenschaftliche Erkenntnisse Dr.Dr.med. Rainer Zierer Diplom Bio-Chemiker, Betriebsarzt und praktischer Arzt, München Physiko-chemische Schwermetallprovokation
Entsäuern und Entgiften mit Body Detox neueste wissenschaftliche Erkenntnisse Dr.Dr.med. Rainer Zierer Diplom Bio-Chemiker, Betriebsarzt und praktischer Arzt, München Physiko-chemische Schwermetallprovokation
Maßanalyse Theorie und Praxis der Titrationen mit chemischen und physikalischen Indikationen
 Jander Jahr Maßanalyse Theorie und Praxis der Titrationen mit chemischen und physikalischen Indikationen fortgeführt von Gerhard Schulze und Jürgen Simon 15. Auflage! Walter de Gruyter Berlin New York
Jander Jahr Maßanalyse Theorie und Praxis der Titrationen mit chemischen und physikalischen Indikationen fortgeführt von Gerhard Schulze und Jürgen Simon 15. Auflage! Walter de Gruyter Berlin New York
Chemische-technische hygienische Parameter
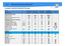 Chemische-technische hygienische Parameter Datum 13.04.2016 15.09.2016 12.04.2017 14.09.2017 Sensorische Prüfungen Färbung (vor Ort) farblos farblos farblos farblos Geruch (vor Ort) ohne ohne ohne ohne
Chemische-technische hygienische Parameter Datum 13.04.2016 15.09.2016 12.04.2017 14.09.2017 Sensorische Prüfungen Färbung (vor Ort) farblos farblos farblos farblos Geruch (vor Ort) ohne ohne ohne ohne
Analytische Chemie. B. Sc. Chemieingenieurwesen. 14. März Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
KRITERIEN UND GRENZWERTE FÜR DIE ZUORDNUNG VON ABFÄLLEN ZU DEPONIETYPEN
 Kurztitel Deponieverordnung Kundmachungsorgan BGBl. Nr. 164/1996 aufgehoben durch BGBl. II Nr. 39/2008 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 24.01.2004 Außerkrafttretensdatum 29.02.2008 Text Anlage
Kurztitel Deponieverordnung Kundmachungsorgan BGBl. Nr. 164/1996 aufgehoben durch BGBl. II Nr. 39/2008 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 24.01.2004 Außerkrafttretensdatum 29.02.2008 Text Anlage
Chemische Nachweise. 30. September 1991
 Chemische Nachweise Uwe Münch 30. September 1991 Im folgenden sind die Nachweise von Kationen (insbesondere Metallkationen), Anionen (Sulfate, Nitrate, Halogenide, etc.) und Elementen zusammengefaßt, die
Chemische Nachweise Uwe Münch 30. September 1991 Im folgenden sind die Nachweise von Kationen (insbesondere Metallkationen), Anionen (Sulfate, Nitrate, Halogenide, etc.) und Elementen zusammengefaßt, die
Trinkwasserbeschaffenheit 2015 zu den Entnahmestellen - Trinkwasser - des Auftraggebers Stadtwerke Schnaudertal - Eigenbetrieb der Stadt Meuselwitz
 colif. Keime E.-coli bakteriologische Untersuchungsparameter Entero kokken Kolonie zahl 22 C organoleptische und andere hygienisch relevante Kolonie zahl 36 C Trübung Färbung Geruch/ Geschmack Geruch (TON)
colif. Keime E.-coli bakteriologische Untersuchungsparameter Entero kokken Kolonie zahl 22 C organoleptische und andere hygienisch relevante Kolonie zahl 36 C Trübung Färbung Geruch/ Geschmack Geruch (TON)
THEORIE UND PRAKTISCHE ANWENDUNG VON KOMPLEXBILDNERN
 THEORIE UND PRAKTISCHE ANWENDUNG VON KOMPLEXBILDNERN VON DR. FRITZ UMLAND PROFESSOR FÜR ANORGANISCH-ANALYTISCHE CHEMIE AN DER UNIVERSITÄT MÜNSTER DR. ANTON JANSSEN UNIVERSITÄT MÜNSTER DR. DETLEF THIERIG
THEORIE UND PRAKTISCHE ANWENDUNG VON KOMPLEXBILDNERN VON DR. FRITZ UMLAND PROFESSOR FÜR ANORGANISCH-ANALYTISCHE CHEMIE AN DER UNIVERSITÄT MÜNSTER DR. ANTON JANSSEN UNIVERSITÄT MÜNSTER DR. DETLEF THIERIG
Kochsalz-Kristalle (Halit) Wichtige Stoffgruppen Atomverband Stoffgruppe Metall Metall: Metallische Stoffe Salzartige Stoffe Metall Nichtmetall:
 Kochsalz-Kristalle (Halit) 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter)
Kochsalz-Kristalle (Halit) 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter)
Ammonium Gasdiffusion / ph-indikator DIN EN ISO (Ammoniak)
 FIA Methodenliste Stand: 24.03.2016 Gesamt- Brenzcatechinviolett APHA 3500 Al modifiziert Aluminium 0,01 mg/l 0,05... 0,5 mg/l Al-T Wasser / Abwasser 0,2... 2 mg/l Al-T Ammonium Gasdiffusion / ph-indikator
FIA Methodenliste Stand: 24.03.2016 Gesamt- Brenzcatechinviolett APHA 3500 Al modifiziert Aluminium 0,01 mg/l 0,05... 0,5 mg/l Al-T Wasser / Abwasser 0,2... 2 mg/l Al-T Ammonium Gasdiffusion / ph-indikator
Einführung in das chemische und. chemisch - analytische Praktikum
 Einführung in das chemische und chemisch - analytische Praktikum Einführung in das chemische und chemisch -analytische Praktikum Von Dr.-ng. F. Martin Privatdozent am chemischen nltil"t d T hni.chu liochsclt.ulc
Einführung in das chemische und chemisch - analytische Praktikum Einführung in das chemische und chemisch -analytische Praktikum Von Dr.-ng. F. Martin Privatdozent am chemischen nltil"t d T hni.chu liochsclt.ulc
Chemie: Nachweisreaktionen
 Chemie: Nachweisreaktionen 1. Nachweis von Elementen und Verbindungen a) Nachweis von Wasserstoff Wasserstoff H2 Nachweis: Knallgasprobe Durchführung: verschlossenes Reagenzglas wird waagerecht mit der
Chemie: Nachweisreaktionen 1. Nachweis von Elementen und Verbindungen a) Nachweis von Wasserstoff Wasserstoff H2 Nachweis: Knallgasprobe Durchführung: verschlossenes Reagenzglas wird waagerecht mit der
Trinkwasser Analysedaten Hamburg
 Trinkwasser Analysedaten Hamburg Bezirk Altona Osdorf Datum 14.07.2009 22549 Kupfer, gesamt 0,0730 mg/l Baursberg 14.07.2009 22549 Cadmium < 0,0000500 mg/l Baursberg 14.07.2009 22549 Blei 0,000170 mg/l
Trinkwasser Analysedaten Hamburg Bezirk Altona Osdorf Datum 14.07.2009 22549 Kupfer, gesamt 0,0730 mg/l Baursberg 14.07.2009 22549 Cadmium < 0,0000500 mg/l Baursberg 14.07.2009 22549 Blei 0,000170 mg/l
festem Boden ab steckte den Strom an und begab mich samt Hund auf einem Erkundungstrip.
 Nachdem mir mein Arzt einige Behandlungen verordnet hat die in Wien recht kostspielig sind deren Wirkung für mich zukunftsmäßig gesehen fraglich erschienen, ein Kuraufenthalt in Österreich von der Kassa
Nachdem mir mein Arzt einige Behandlungen verordnet hat die in Wien recht kostspielig sind deren Wirkung für mich zukunftsmäßig gesehen fraglich erschienen, ein Kuraufenthalt in Österreich von der Kassa
Chemische und Mikrobiologische Untersuchung von mittels YVE-310-Filterkanne aufbereitetem Leitungswasser
 REPORT Chemische und Mikrobiologische Untersuchung von mittels YVE-310-Filterkanne aufbereitetem Leitungswasser DI Otmar Plank Verteiler: 1-3 Fa. YVE & BIO GmbH, Bremen 4 Otmar Plank 5 HET August 2014
REPORT Chemische und Mikrobiologische Untersuchung von mittels YVE-310-Filterkanne aufbereitetem Leitungswasser DI Otmar Plank Verteiler: 1-3 Fa. YVE & BIO GmbH, Bremen 4 Otmar Plank 5 HET August 2014
Johann Wolfgang Goethe-Universität Frankfurt am Main Institut für Pharmazeutische Chemie
 Johann Wolfgang Goethe-Universität Frankfurt am Main Institut für Pharmazeutische Chemie Name: Matrikelnummer: Beurteilung: / Zwischenklausur zum Praktikum QUALITATIVE ANORGANISCHE ANALYSE Termin: 3. Mai
Johann Wolfgang Goethe-Universität Frankfurt am Main Institut für Pharmazeutische Chemie Name: Matrikelnummer: Beurteilung: / Zwischenklausur zum Praktikum QUALITATIVE ANORGANISCHE ANALYSE Termin: 3. Mai
SPEKTRALANALYSE VON MINERALIEN UND GESTEINEN
 SPEKTRALANALYSE VON MINERALIEN UND GESTEINEN EINE ANLEITUNG ZUR EMISSIONS- UND AB SORPTIONS SPEKTROSKOPIE VON DR. RER. NAT. HORST MOENKE WISSENSCHAFTLICHER MITARBEITER IM VEB CARL ZEISS JENA MIT 58 ABBILDUNGEN
SPEKTRALANALYSE VON MINERALIEN UND GESTEINEN EINE ANLEITUNG ZUR EMISSIONS- UND AB SORPTIONS SPEKTROSKOPIE VON DR. RER. NAT. HORST MOENKE WISSENSCHAFTLICHER MITARBEITER IM VEB CARL ZEISS JENA MIT 58 ABBILDUNGEN
CHEMIE-PRAKTIKUM FÜR MEDIZINER WS 2010/2011
 Universität Duisburg-Essen - Institut für Organische Chemie 1 CHEMIE-PRAKTIKUM FÜR MEDIZINER WS 2010/2011 1. Tag: Maßanalyse I Datum: Name: Kurs: Saal: Platz Nr. Theoret. Grundlagen: 1. Aufgabe: Titerstellung
Universität Duisburg-Essen - Institut für Organische Chemie 1 CHEMIE-PRAKTIKUM FÜR MEDIZINER WS 2010/2011 1. Tag: Maßanalyse I Datum: Name: Kurs: Saal: Platz Nr. Theoret. Grundlagen: 1. Aufgabe: Titerstellung
Fällungsreaktionen. Allgemeine Chemie I - Anorgan. Teil
 Fällungsreaktionen Gleichgewicht: Fällen Auflösen G 0 = H 0 T S 0 Fällung und Kristallisation Natrium-Magnesium-Uranylacetat NaMg(UO 2 ) 3 (CH 3 COO) 9 9 H 2 O Ammonium-Molybdato-Phosphat (NH 4 ) 3 [P(Mo
Fällungsreaktionen Gleichgewicht: Fällen Auflösen G 0 = H 0 T S 0 Fällung und Kristallisation Natrium-Magnesium-Uranylacetat NaMg(UO 2 ) 3 (CH 3 COO) 9 9 H 2 O Ammonium-Molybdato-Phosphat (NH 4 ) 3 [P(Mo
5. Seminar. Prof. Dr. Christoph Janiak. Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002
 ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 5. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 5. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
Sehr geehrter Auftraggeber, anbei erhalten Sie den Prüfbericht zu den Proben: Probenummer Entnahmestelle Probenahme
 / S-NA-LB, Wasserversorgung weber@sw-ba.de Besucheranschrift S-NA-LB Gebäude G (Labor) Emmy-Noether-Str. 2 Techn. Leiter: Hr. Dr. Hofmann Ansprechpartner: Hr. Bader Telefon / -Fax 089 / 2361-3474/ -3453
/ S-NA-LB, Wasserversorgung weber@sw-ba.de Besucheranschrift S-NA-LB Gebäude G (Labor) Emmy-Noether-Str. 2 Techn. Leiter: Hr. Dr. Hofmann Ansprechpartner: Hr. Bader Telefon / -Fax 089 / 2361-3474/ -3453
Qualitative anorganische Analyse
 Qualitative anorganische Analyse Grundprinzip: nicht Stoffe (chemische Verbindungen) werden nachgewiesen, sondern die Ionen, aus denen sie aufgebaut sind Ergebnisform: (auf einem A4 oder A5 Blatt mit Namen,
Qualitative anorganische Analyse Grundprinzip: nicht Stoffe (chemische Verbindungen) werden nachgewiesen, sondern die Ionen, aus denen sie aufgebaut sind Ergebnisform: (auf einem A4 oder A5 Blatt mit Namen,
Anleitung zum Praktikum der analytischen Chemie
 Anleitung zum Praktikum der analytischen Chemie in drei Teilen Von Dozent Dr. S. W. Souci unter Mitwirkung von Professor Dr. Dr. F. Fischler und Dr. H. Thies Erster Teil Praktikum der qualitativen Analyse
Anleitung zum Praktikum der analytischen Chemie in drei Teilen Von Dozent Dr. S. W. Souci unter Mitwirkung von Professor Dr. Dr. F. Fischler und Dr. H. Thies Erster Teil Praktikum der qualitativen Analyse
Nitratabbau im Grundwasser Kenntnisstand t aus Messungen
 Nitratabbau im Grundwasser Kenntnisstand t aus Messungen Knut Meyer & Jörg Elbracht Gliederung Das Projekt Natürliche Charakteristik der Grundwasserkörper Datenbestand zur Denitrifikation im Grundwasser
Nitratabbau im Grundwasser Kenntnisstand t aus Messungen Knut Meyer & Jörg Elbracht Gliederung Das Projekt Natürliche Charakteristik der Grundwasserkörper Datenbestand zur Denitrifikation im Grundwasser
Gesamt- Brenzcatechinviolett APHA 3500 Al modifiziert Aluminium
 FIA Methodenliste Stand: 21.03.2012 Gesamt- Brenzcatechinviolett APHA 3500 Al modifiziert Aluminium 0,01 mg/l 0,05... 0,5 mg/l Al-T Wasser / Abwasser / 0,2... 2 mg/l Al-T Bodenextrakt Ammonium Gasdiffusion
FIA Methodenliste Stand: 21.03.2012 Gesamt- Brenzcatechinviolett APHA 3500 Al modifiziert Aluminium 0,01 mg/l 0,05... 0,5 mg/l Al-T Wasser / Abwasser / 0,2... 2 mg/l Al-T Bodenextrakt Ammonium Gasdiffusion
Teilprüfung Anorganische Chemie
 Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Zwischenprüfung Lehramt Chemie Teilprüfung Anorganische Chemie 8.8.2006 Name: Vorname: Matrikel-Nr. Hinweis: Verwenden Sie für die Antworten den hinter den Fragen
Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Zwischenprüfung Lehramt Chemie Teilprüfung Anorganische Chemie 8.8.2006 Name: Vorname: Matrikel-Nr. Hinweis: Verwenden Sie für die Antworten den hinter den Fragen
1.6. Die Ionenbindung
 1.6. Die Ionenbindung 1.6.1. Die Edelgasregel Die Edelgase gehen kaum Verbindungen ein und zeigen in ihrer Periode jeweils die höchsten Ionisierungsenergien. Ihre Elektronenkonfiguration mit jeweils Außenelektronen
1.6. Die Ionenbindung 1.6.1. Die Edelgasregel Die Edelgase gehen kaum Verbindungen ein und zeigen in ihrer Periode jeweils die höchsten Ionisierungsenergien. Ihre Elektronenkonfiguration mit jeweils Außenelektronen
Trinkwasseranalyse Versorgungsgebiet Kernbereich Friedrichsdorf
 Seite 1 von 3 Stadtwerke Friedrichsdorf Färberstraße 13-15 Trinkwasseranalyse Versorgungsgebiet Kernbereich Friedrichsdorf Ergebnisse der Trinkwasseranalysen 2014 und 2015 vom Institut Fresenius, Taunusstein
Seite 1 von 3 Stadtwerke Friedrichsdorf Färberstraße 13-15 Trinkwasseranalyse Versorgungsgebiet Kernbereich Friedrichsdorf Ergebnisse der Trinkwasseranalysen 2014 und 2015 vom Institut Fresenius, Taunusstein
Allgemeine und Anorganische Chemie
 Norbert Kuhn Thomas M. Klapötke Allgemeine und Anorganische Chemie Eine Einführung Unter Mitarbeit von Isabel Walker ^ Springer Spektrum Inhaltsverzeichnis 1 Einleitung 1 2 Definitionen 5 3 Chemische Stoffe
Norbert Kuhn Thomas M. Klapötke Allgemeine und Anorganische Chemie Eine Einführung Unter Mitarbeit von Isabel Walker ^ Springer Spektrum Inhaltsverzeichnis 1 Einleitung 1 2 Definitionen 5 3 Chemische Stoffe
Sehr geehrter Auftraggeber, anbei erhalten Sie den Prüfbericht zu den Proben: Probenummer Entnahmestelle Probenahme
 / S-NA-LB, Wasserwerk schueler@taufkirchen-mucl.de wierer@taufkirchen-mucl.de Besucheranschrift S-NA-LB Gebäude G (Labor) Emmy-Noether-Str. 2 Techn. Leiter: Hr. Dr. Hofmann Ansprechpartner: Hr. Bader Telefon
/ S-NA-LB, Wasserwerk schueler@taufkirchen-mucl.de wierer@taufkirchen-mucl.de Besucheranschrift S-NA-LB Gebäude G (Labor) Emmy-Noether-Str. 2 Techn. Leiter: Hr. Dr. Hofmann Ansprechpartner: Hr. Bader Telefon
Redox - Übungsaufgaben:
 Redox - Übungsaufgaben: Schwierigkeitsgrad I: 1.Magnesium reagiert mit Sauerstoff zu Magnesiumoxid. Ox: Mg Mg 2+ + 2e - /*2 Red: O 2 + 4e - 2 O 2- Redox: 2 Mg + O 2 2 MgO 2.Kalium Reagiert mit Schwefel
Redox - Übungsaufgaben: Schwierigkeitsgrad I: 1.Magnesium reagiert mit Sauerstoff zu Magnesiumoxid. Ox: Mg Mg 2+ + 2e - /*2 Red: O 2 + 4e - 2 O 2- Redox: 2 Mg + O 2 2 MgO 2.Kalium Reagiert mit Schwefel
1 Grundwissenskatalog Chemie G8 SG, Inhalt der 10. Jahrgangsstufe
 1 Grundwissenskatalog Chemie G8 SG, Inhalt der 10. Jahrgangsstufe Grundwissenskatalog Chemie für die 11. bis 12. Jahrgangsstufe G 8 (sprachliches Gymnasium) mit den Inhalten der 10. Jahrgangsstufe Hinweis:
1 Grundwissenskatalog Chemie G8 SG, Inhalt der 10. Jahrgangsstufe Grundwissenskatalog Chemie für die 11. bis 12. Jahrgangsstufe G 8 (sprachliches Gymnasium) mit den Inhalten der 10. Jahrgangsstufe Hinweis:
Analytische Chemie. B. Sc. Chemieingenieurwesen. 19. März Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 19. März 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
Analytische Chemie B. Sc. Chemieingenieurwesen 19. März 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
Kapitel 21: Analytik und Ionennachweise
 Kapitel 21: Analytik und Ionennachweise 1 Kapitel 21: Analytik und Ionennachweise Freies Lehrbuch der anorganischen Chemie von H. Hoffmeister und C. Ziegler (unter GNU Free Documentation License, Version
Kapitel 21: Analytik und Ionennachweise 1 Kapitel 21: Analytik und Ionennachweise Freies Lehrbuch der anorganischen Chemie von H. Hoffmeister und C. Ziegler (unter GNU Free Documentation License, Version
Umwelthygiene Marburg GmbH & Co KG
 1407086 Umwelthygiene Marburg GmbH & Co KG Rudolf Breitscheidstr. 24, D35037 Marburg Umwelthygiene Marburg GmbH & Co KG Staatlich anerkannte Untersuchungsstelle nach 15 Abs. 4 Amtsgericht Marburg: HRB
1407086 Umwelthygiene Marburg GmbH & Co KG Rudolf Breitscheidstr. 24, D35037 Marburg Umwelthygiene Marburg GmbH & Co KG Staatlich anerkannte Untersuchungsstelle nach 15 Abs. 4 Amtsgericht Marburg: HRB
Parameter-Nummer gem. Anlage zum 4 Abwasserverordnung (AbwV)
 Anlage: Parameter nach FM Wasser (Stand 06.04.2005) Labor: Erläuterungen zum Fragebogen: Einteilung der Parameter nach dem Fachmodul Wasser, ergänzt nach der Anlage zum 4 Abwasserverordnung (Mindestparameterumfang
Anlage: Parameter nach FM Wasser (Stand 06.04.2005) Labor: Erläuterungen zum Fragebogen: Einteilung der Parameter nach dem Fachmodul Wasser, ergänzt nach der Anlage zum 4 Abwasserverordnung (Mindestparameterumfang
1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss
 1 Uebungen zur Prüfungsvorbereitung 4.12.14 1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss Die folgenden Tiefenprofile von gelöstem Mangan, Eisen und Sulfid (S 2- ) sowie die
1 Uebungen zur Prüfungsvorbereitung 4.12.14 1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss Die folgenden Tiefenprofile von gelöstem Mangan, Eisen und Sulfid (S 2- ) sowie die
Ganz einfach: Profitieren Sie von über 100 Jahren Erfahrung in der Analytik und verwenden Sie Testsätze und Geräte von Merck Chemicals.
 Wie erhalte ich schnell und sicher zuverlässige Analysenergebnisse? Ganz einfach: Profitieren Sie von über 100 Jahren Erfahrung in der Analytik und verwenden Sie Testsätze und Geräte von Merck Chemicals.
Wie erhalte ich schnell und sicher zuverlässige Analysenergebnisse? Ganz einfach: Profitieren Sie von über 100 Jahren Erfahrung in der Analytik und verwenden Sie Testsätze und Geräte von Merck Chemicals.
Trennungsmöglichkeit
 Trennungsmöglichkeit Erst Fällung mit Urotropin, dann mit (H 4 ) 2 S Was ist Urotropin? (H 2 S im basischen Milieu) 6 H 12 4 + 6 H 2 O 6 H 2 O + 4 H 3 Urotropin Formaldehyd H 2 H 2 H 2 H 2 H 2 H2 Adamantan-Gerüst
Trennungsmöglichkeit Erst Fällung mit Urotropin, dann mit (H 4 ) 2 S Was ist Urotropin? (H 2 S im basischen Milieu) 6 H 12 4 + 6 H 2 O 6 H 2 O + 4 H 3 Urotropin Formaldehyd H 2 H 2 H 2 H 2 H 2 H2 Adamantan-Gerüst
Übungsbogen 4 zum Praktikum/zur Vorlesung Analytische Chemie I
 Übungsbogen 4 zum Praktikum/zur Vorlesung 1. Aufgabe Eine rotbraune, in Wasser schwerlösliche Verbindung zeigt folgende Reaktionen: i) Sie löst sich in NH 3 -Lösung unter Bildung einer gelben Lösung. ii)
Übungsbogen 4 zum Praktikum/zur Vorlesung 1. Aufgabe Eine rotbraune, in Wasser schwerlösliche Verbindung zeigt folgende Reaktionen: i) Sie löst sich in NH 3 -Lösung unter Bildung einer gelben Lösung. ii)
Calcium. Calcium fest. Ordnungszahl. Siedepunkt. Siedepunkt Atommasse Dichte. Kohlenstoff. Carbon fest. Ordnungszahl 3642!
 Al Aluminium Aluminium fest 13 660.32 2519 2.375 5000 74.92160 B Bor Cl Boron fest 5 10.811 2.08 3.515 2076 3927 16,200 Co 58.933195 18,350 Chlorine gasförmig 17 35.453 1.5625-101.5-34.04 206 7.75 Cu 1907
Al Aluminium Aluminium fest 13 660.32 2519 2.375 5000 74.92160 B Bor Cl Boron fest 5 10.811 2.08 3.515 2076 3927 16,200 Co 58.933195 18,350 Chlorine gasförmig 17 35.453 1.5625-101.5-34.04 206 7.75 Cu 1907
ICP Analytik Brandenburger Platz1 24211 Preetz Tel. 04342/858300 Fax 04342/858301. Beschreibung
 n-labor Stand September 2013 Haarmineralanalyse PZN- 0286551 Analyse von 30 Elementen und Auswertung, Lebensmittellisten, en von Nahrungsergänzungs- sowie freiverkäuflichen Arzneimitteln BlutElementAnalyse
n-labor Stand September 2013 Haarmineralanalyse PZN- 0286551 Analyse von 30 Elementen und Auswertung, Lebensmittellisten, en von Nahrungsergänzungs- sowie freiverkäuflichen Arzneimitteln BlutElementAnalyse
EINZELPREISLISTE / UNTERSUCHUNGSPROGRAMME
 EINZELPREISLISTE / UNTERSUCHUNGSPROGRAMME LANDWIRTSCHAFT UND GARTENBAU Boden Seite 1 Analysenprogramme zur Düngeberatung für Obst-, Beerenund Weinbau sowie Gemüsebau Kompost Seite 2 Hofdünger Seite 3 Gärprozess,
EINZELPREISLISTE / UNTERSUCHUNGSPROGRAMME LANDWIRTSCHAFT UND GARTENBAU Boden Seite 1 Analysenprogramme zur Düngeberatung für Obst-, Beerenund Weinbau sowie Gemüsebau Kompost Seite 2 Hofdünger Seite 3 Gärprozess,
LEISTUNGSVERZEICHNIS 2017
 2017 7 Bodenluft Altlasten Deponien Seite: 43 von 71 Stand: 29.03.2017 LV_2017 70010 Bundesbodenschutzverordnung Anhang 2 Abschnitt 1.2 Maßnahmewerte Pfad Boden Mensch Dioxine, Furane (PCDD, PCDF) (Einzelbestimmung)
2017 7 Bodenluft Altlasten Deponien Seite: 43 von 71 Stand: 29.03.2017 LV_2017 70010 Bundesbodenschutzverordnung Anhang 2 Abschnitt 1.2 Maßnahmewerte Pfad Boden Mensch Dioxine, Furane (PCDD, PCDF) (Einzelbestimmung)
Allgemeine und Anorganische Chemie
 Technische Universität München Allgemeine und Anorganische Chemie Vorlesungsinhalte WS 2015/2016 13.10. Chemie Einführung, Geschichte der Chemie Grundbegriffe; Element/Verbindung 20.10. Periodensystem
Technische Universität München Allgemeine und Anorganische Chemie Vorlesungsinhalte WS 2015/2016 13.10. Chemie Einführung, Geschichte der Chemie Grundbegriffe; Element/Verbindung 20.10. Periodensystem
Der qualitative Trennungsgang
 Der qualitative Trennungsgang Vorschriften für das Praktikum im Labor für Anorganische Chemie im Fachbereich Chemieingenieurwesen der FH Münster, Abt. Steinfurt Vorbemerkungen Zunächst sind mit den erhaltenen
Der qualitative Trennungsgang Vorschriften für das Praktikum im Labor für Anorganische Chemie im Fachbereich Chemieingenieurwesen der FH Münster, Abt. Steinfurt Vorbemerkungen Zunächst sind mit den erhaltenen
Allgemeine und anorganische Chemie. Chemie ist die Lehre von den Stoffen und den stofflichen Veränderungen.
 Allgemeine und anorganische Chemie 1. Inhalte und Aufgaben der Chemie - Chemische Grundbegriffe Chemie ist die Lehre von den Stoffen und den stofflichen Veränderungen. Chemische Verbindungen setzen sich
Allgemeine und anorganische Chemie 1. Inhalte und Aufgaben der Chemie - Chemische Grundbegriffe Chemie ist die Lehre von den Stoffen und den stofflichen Veränderungen. Chemische Verbindungen setzen sich
Analyse 3 NO 3 SO 4. Cl - Urotropin-Gruppe. (NH 4 ) 2 S-Gruppe. Ba 2+ Sr 2+ Ca 2+ (NH 4 ) 2 CO 3 -Gruppe. Lösliche Gruppe. TiO 2+ Al 3+ Cr 3+ VO 2+
 Cl Analyse 3 UrotropinGruppe Fe 2+/3+ TiO 2+ Al 3+ Cr 3+ VO 2+ (NH 4 ) 2 SGruppe Mn 2+ Zn 2+ Co 2+ Ni 2+ (NH 4 ) 2 Gruppe Lösliche Gruppe Lösung der Ursubstanz KationenTrennungsgang + HCl SalzsäureGruppe
Cl Analyse 3 UrotropinGruppe Fe 2+/3+ TiO 2+ Al 3+ Cr 3+ VO 2+ (NH 4 ) 2 SGruppe Mn 2+ Zn 2+ Co 2+ Ni 2+ (NH 4 ) 2 Gruppe Lösliche Gruppe Lösung der Ursubstanz KationenTrennungsgang + HCl SalzsäureGruppe
