HUNTER SEHNENIMPLANTATE Dieses Paket enthält die folgenden Sprachen:
|
|
|
- Sigrid Holzmann
- vor 6 Jahren
- Abrufe
Transkript
1 DE HUNTER SEHNENIMPLANTATE Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe (tk) Weitere Sprachen finden Sie auf unserer Website Klicken Sie auf die Option Prescribing Information (Verschreibungsangaben). Weitere Informationen und Übersetzungen erhalten Sie vom Hersteller oder dem zuständigen Vertrieb. M C 0086* P Wright Medical Technology, Inc. Wright Medical UK Ltd 1023 Cherry Road 3rd Avenue Memphis, TN Letchworth U.S.A. Herts, SG6 2JF UK * Die CE-Kennzeichnung gilt für einzelne Katalognummern und befindet sich ggf. auf dem Außenetikett. 1 Oktober 2013 Gedruckt in den USA
2 Zur Beachtung für den Chirurgen WICHTIGE MEDIZINISCHE INFORMATIONEN ÜBERBLICK: I. ALLGEMEINE PRODUKT-HINWEISE A. INDIKATIONEN B. KONTRAINDIKATIONEN C. WARNHINWEISE D. VORSICHTSMASSNAHMEN E. STERILISATIONSVERFAHREN F. AUFBEWAHRUNGSBEDINGUNGEN II. HUNTER SEHNENIMPLANTATE ( ) INFORMATIONEN ZU EINZELNEN PRODUKTEN A. HUNTER SEHNENSTAB- UND PASSIVE SEHNENIMPLANTATE B. HUNTER AKTIVE SEHNENIMPLANTATE C. HUNTER AKTIVES SEHNENIMPLANTAT BC (DOPPELSTRANG) D. HUNTER AKTIVES SEHNENIMPLANTAT DC (DISTALER STRANG) E. HUNTER AKTIVES SEHNENIMPLANTAT PC (PROXIMALER STRANG) DEFINITIONEN Auf dem Versandetikett befinden sich Symbole und Abkürzungen. Die folgende Tabelle enthält die Definitionen dieser Symbole und Abkürzungen. 2
3 Tabelle 1. Definitionen der Symbole und Abkürzungen Symbol g h D Y i H l p N M Definition Chargenbezeichnung Katalognummer Nicht wiederverwenden Vorsicht, Begleitunterlagen beachten Gebrauchsanweisung beachten Verwendbar bis Temperaturbereich Trocken aufbewahren Vor Sonnenlicht schützen Herstellungsdatum Hersteller 3
4 P I K STERILE GAS J Bevollmächtigter in der EG Mit Ethylenoxid sterilisiert Mit Strahlung sterilisiert Mit Gasplasma sterilisiert Mit aseptischen Verarbeitungsmethoden sterilisiert Gebrauch nur auf Rezept Abkürzung Ti Ti6Al4V CoCr SS UHMWPE Material Titan Titanlegierung Kobaltchromlegierung Edelstahl Ultrahochmolekulares Polyethylen 4
5 I. ALLGEMEINE PRODUKT-HINWEISE Die Fortschritte auf dem Gebiet der Gelenk-Teil- und -Totalendoprothesen haben dem Chirurgen die Möglichkeit gegeben, bei vielen Patienten Mobilität wiederherzustellen, Deformierungen zu korrigieren und Schmerzen zu lindern. Obwohl die für diese Zwecke verwendeten Prothesen größtenteils erfolgreich eingesetzt werden, ist zu beachten, dass sie aus Silikon und Metall hergestellt werden. Hinzu kommt, dass das System nicht so stabil, zuverlässig und haltbar ist wie eine natürliche menschliche Sehne. Dem Chirurgen sollte Folgendes bewusst sein: A. Alle Produkte sind aus einem gewobenen Polyesterkern hergestellt, der mit bariumimprägniertem Silikonelastomer bedeckt ist. B. Die Entscheidung des Chirurgen zur Implantation von Silikonelastomerimplantaten umfasst die Abwägung von Risiken und Vorteilen. Zusätzlich zu den Kenntnissen des Chirurgen hinsichtlich der zu erwartenden Ergebnisse und Komplikationen sowie der therapeutischen Alternativen müssen auch die Bedürfnisse und Wünsche des Patienten berücksichtigt werden. Wright Medical Technology, Inc. kann jedem Arzt eine Bibliographie von Artikeln zur Verwendung und zu den Komplikationen von Silikonelastomerimplantaten zur Verfügung stellen. Dazu bitte schriftlich oder telefonisch Kontakt mit Wright aufnehmen. C. Die richtige Auswahl und Größenanpassung des Implantats sind äußerst wichtig. Die Auswahl der richtigen Größe, Form und Ausführung des Implantats erhöht die Chancen eines erfolgreichen Eingriffs. D. Wright empfiehlt keine bestimmte Operationstechnik beim Einsatz des Implantats. Der Mediziner ist dafür verantwortlich, dass geeignete chirurgische Methoden und Techniken angewendet werden. Jeder Chirurg muss die Eignung des Eingriffs auf der Grundlage seiner persönlichen medizinischen Ausbildung und Erfahrung beurteilen. 5
6 E. Eine Umformung des Implantats sollte vermieden werden, da die strukturelle Integrität und Funktionalität des Implantats dadurch beeinträchtigt werden könnte. F. Bei der Auswahl der für eine Sehnenprothese geeigneten Patienten können die folgenden Aspekte für den Langzeiterfolg des Eingriffs entscheidend sein: 1. Beschäftigung bzw. Aktivität des Patienten. Hat der Patient eine Tätigkeit bzw. nimmt er an einer Aktivität teil, bei der er schwer heben muss oder die Muskeln übermäßig beansprucht werden, können die daraus resultierenden Kräfte zum Versagen der Fixierung, des Implantats oder beidem führen. Die Prothese ist nicht in der Lage, die Funktion bis zu dem Grad wiederherzustellen, der von einer normalen, gesunden Sehne erwartet werden kann, und der Patient sollte keine unrealistischen Erwartungen bezüglich dieser Funktion haben. 2. Senilität, Geisteskrankheit oder Alkoholismus. Diese und andere Krankheitsbilder führen ggf. dazu, dass der Patient bestimmte notwendige Einschränkungen und Vorsichtsmaßnahmen beim Gebrauch der Prothese außer Acht lässt, was zu einem Ausfall der Prothese oder anderen Komplikationen führen kann. 3. Empfindlichkeit gegen Fremdkörper. In Fällen, in denen Verdacht auf Empfindlichkeit gegen das verwendete Material besteht, sollten vor der Materialauswahl oder Implantation entsprechende Tests durchgeführt werden. A. INDIKATIONEN Dieses Produkt ist für den Gebrauch in der ersten Stufe des zweistufigen, von Dr. James M. Hunter entwickelten Eingriffs zur Rekonstruktion der Beuge- und Strecksehnen bei Personen mit signifikanten Verletzungen der Handsehnen indiziert. Dieses Produkt ist für die temporäre Implantation vorgesehen, um die Bildung einer Pseudosehnenscheide zu fördern, die später ein autogenes Sehnenimplantat versorgt und schmiert. Informationen zu einzelnen Produkten sind in Abschnitt II aufgeführt. 6
7 B. KONTRAINDIKATIONEN Dieses Produkt ist für keine anderen Verwendungszwecke als die in den Indikationen angegebenen vorgesehen. Eine vorausgehende Restinfektion ist eine Kontraindikation für den Gebrauch dieses Produkts. Durch eine angemessene operative und antimikrobielle Behandlung und nachfolgende Wundheilung kann der Eingriff zu einem späteren Zeitpunkt durchgeführt werden. Ein Finger mit einem vernarbten Sehnenbett, grenzwertiger Versorgung, Nervendefizit und schwerer Gelenksteifheit könnte möglicherweise gerettet werden; dies sollte jedoch wahrscheinlich nur bei Patienten mit ganz speziellen Anforderungen versucht werden. Informationen zu einzelnen Produkten sind in Abschnitt II aufgeführt. C. WARNHINWEISE Für Rekonstruktionseingriffe, die dem HUNTER Sehnenimplantat ähnlich sind, wurden Synovitis, Adhäsion und Wundinfektion als Komplikationen berichtet und man muss deshalb davon ausgehen, dass dies auch potenzielle Komplikationen bei der Verwendung dieses Produkts sind. Bei der Verwendung ähnlicher Vorrichtungen wurde auch von einer Abwanderung der Vorrichtung berichtet; dies gilt bei der Verwendung dieses Produkts jedoch als unwahrscheinlich. Bei jedem chirurgischen Eingriff besteht das Potenzial für Komplikationen. Zu den Risiken und Komplikationen beim Einsatz von Silikonimplantaten gehören: Infektion oder schmerzhafte, geschwollene bzw. entzündete Implantationsstelle Fraktur des Implantats Lockerung oder Dislokation der Prothese, wodurch ein Revisionseingriff erforderlich wird 7
8 Knochenrestoration oder -überproduktion Allergische Reaktion(en) auf das/die Prothesenmaterial(ien) Ungünstige histologische Reaktionen möglicherweise mit Makrophagen und/oder Fibroblasten Migration von Abriebpartikeln mit möglicher körperlicher Reaktion Embolie Ein gewisser Grad an Partikelbildung ist bei allen Implantaten, Silikonelastomer- Implantate eingeschlossen, unvermeidbar. Die anfallende Menge ist von verschiedenen Faktoren abhängig, wie etwa Patientenaktivität, Gelenkstabilität bzw. -instabilität nach der Implantation, Implantatposition und Ausmaß der Unterstützung durch Weichteile. Die biologische Reaktion des Patienten auf diese Partikel ist unterschiedlich, kann jedoch lokale Synovitis und Knochenlyse in angrenzenden Knochen einschließen. Informationen zu einzelnen Produkten sind in Abschnitt II aufgeführt. D. VORSICHTSMASSNAHMEN Bei allen Implantaten kann das Potenzial für Komplikationen oder unerwünschte Reaktionen minimiert werden, indem die der Produktliteratur beiliegende Gebrauchsanweisung befolgt wird. Ein Kontakt dieses Implantats mit unbehandschuhten Fingern oder Textilfasern ist unter allen Umständen zu vermeiden. Silikonelastomere sind stark elektrostatisch und deshalb anfällig für eine Kontamination durch Luft- oder Oberflächenpartikel. Die Anwesenheit solcher Kontaminationsstoffe könnte zu einer unerwünschten Gewebereaktion führen. Im Falle eines Kontakts des Implantats mit solchen Kontaminationsstoffen das Produkt gründlich mit sterilem destilliertem Wasser abspülen. 8
9 Das Produkt ist NUR ZUR EINMALIGEN VERWENDUNG bestimmt. Rückmeldungen und Motivation des Patienten sind wichtig für den Erfolg dieses Eingriffs, da eine besonders aktive Teilnahme des Patienten während des postoperativen Programms zur Handrehabilitation erforderlich ist. Nach US-Recht darf dieses Produkt nur von einem Arzt oder auf dessen Anordnung verkauft werden. Eine Resterilisierung dieses Produkts wird nicht empfohlen, da sich das Produkt dadurch verziehen könnte. Es liegt in der Verantwortlichkeit des einzelnen Chirurgen, der Implantate verwendet, den klinischen und medizinischen Zustand jedes Patienten zu berücksichtigen und über alle Aspekte der Implantation und der eventuell auftretenden potenziellen Komplikationen umfassend informiert zu sein. Der von der Implantationschirurgie abgeleitete Nutzen entspricht möglicherweise nicht den Erwartungen des Patienten bzw. kann sich im Laufe der Zeit verringern und einen Revisionseingriff erforderlich machen, um das Implantat zu ersetzen oder Alternativmaßnahmen durchzuführen. Revisionseingriffe bei Implantaten sind häufig. Der geistige Zustand des Patienten muss ebenfalls berücksichtigt werden. Die Bereitschaft und/oder Fähigkeit zur Befolgung postoperativer Anweisungen kann den Erfolg der Operation ebenfalls beeinflussen. Der Chirurg muss viele Aspekte abwägen, um bei jedem Patienten das beste Ergebnis zu erzielen. Die klinischen Ergebnisse hängen vom Chirurgen und der angewandten Technik, der präoperativen und postoperativen Versorgung, dem Implantat, der Pathologie des Patienten und dessen täglichen Aktivitäten ab. Es ist wichtig, von jedem Patienten vor der Operation eine entsprechende Einwilligung nach fachgerechter Aufklärung einzuholen und potenzielle Komplikationen mit ihm zu besprechen. Dies schließt evtl. auch einen Überblick über Alternativmethoden ohne Einsatz eines Implantats ein, wie etwa eine Rekonstruktion von Weichteilen oder Arthrodese. 9
10 Empfehlungen zu Implantatfragmenten 1. Medizinprodukte stets gemäß den in der Begleitdokumentation angegebenen Indikationen und der Gebrauchsanweisung des jeweiligen Herstellers verwenden, vor allem beim Einführen und Entfernen. 2. Die Produkte müssen vor der Verwendung auf evtl. beim Transport oder bei der Lagerung entstandene Beschädigungen sowie auf Defekte, die die Wahrscheinlichkeit eines Bruches während des Eingriffs erhöhen könnten, untersucht werden. 3. Die Produkte sofort nach der Entfernung aus dem Patienten auf Anzeichen von Bruch oder Fragmentierung untersuchen. 4. Im Fall einer Beschädigung muss das Produkt aufbewahrt werden, damit der Hersteller den Vorfall untersuchen kann. 5. Risiken und Nutzen der Entfernung gegenüber dem Zurücklassen des Fragments im Körper müssen mit dem Patienten ausführlich besprochen werden (wenn möglich). 6. Dabei muss der Patient über die Art und die Sicherheit des im Körper zurückgelassenen Fragments unter Angabe folgender Informationen aufgeklärt werden: a. Die Materialzusammensetzung des Fragments (soweit diese bekannt ist); b. Die Größe des Fragments (soweit diese bekannt ist); c. Die Lage des Fragments; d. Potenzielle Mechanismen, die zur Verletzung führen könnten (z.b. Migration, Infektion); e. Zu vermeidende Eingriffe oder Behandlungen, wie z.b. MRT-Untersuchungen im Fall von Metallfragmenten. Dadurch kann die Möglichkeit einer schweren Verletzung durch das Fragment reduziert werden. 10
11 Verhalten bei Untersuchungen mittels Magnetresonanztomographie Die in dieser Packungsbeilage beschriebenen Produkte wurden nicht auf Sicherheit bei und Verträglichkeit mit MRT-Untersuchungen getestet. Die in dieser Packungsbeilage beschriebenen Produkte wurden nicht auf Erwärmung oder Migration bei MRT- Untersuchungen getestet. Informationen zu einzelnen Produkten sind in Abschnitt II aufgeführt. E. STERILISATIONSVERFAHREN Implantate in sterilen Verpackungen sollten untersucht werden, um sicherzustellen, dass die Verpackung nicht beschädigt ist oder bereits geöffnet wurde. Wenn die innere Verpackung beschädigt ist, müssen vom Hersteller weitere Anweisungen eingeholt werden. Die Implantate sollten aseptisch geöffnet werden; sie sollten erst dann geöffnet werden, wenn die richtige Größe bestimmt wurde. Die Handhabung des Implantats sollte nur mit stumpfen Instrumenten erfolgen, um ein Oberflächentrauma oder eine Kontamination mit Fremdkörpern zu vermeiden. Das Implantat vor dem Einsetzen gründlich mit steriler Kochsalzlösung spülen. Dieses Produkt ist nur zur einmaligen Verwendung vorgesehen. Ein Implantat darf nach Kontakt mit Körpergeweben oder -flüssigkeiten nicht erneut sterilisiert werden. Als Einmalprodukte gekennzeichnete Produkte dürfen unter keinen Umständen wiederverwendet werden. Eine Wiederverwendung dieser Produkte kann die Gesundheit des Patienten potenziell ernsthaft schädigen. Beispiele für die mit einer Wiederverwendung dieser Produkte verbundenen Gefahren sind u.a. deutlich herabgesetzte Produktleistung, Kreuzinfektion und Kontamination. 11
12 F. AUFBEWAHRUNGSBEDINGUNGEN Alle Implantate müssen in einer sauberen trockenen Umgebung aufbewahrt und vor Sonnenlicht und extremen Temperaturen geschützt werden. II. INFORMATIONEN ZU EINZELNEN PRODUKTEN A. HUNTER SEHNENSTAB- UND PASSIVE SEHNENIMPLANTATE BESCHREIBUNG Das HUNTER Sehnenstab-Implantat besteht aus einem gewobenen Polyesterkern, der mit einem (bariumimprägnierten und daher röntgensichtbaren) Silikonelastomer bedeckt ist. Dieses Design bietet die notwendige Kombination aus inerten Eigenschaften, Festigkeit und Flexibilität sowie die glatte Oberfläche, die zur Induzierung der Bildung einer Pseudosehnenscheide, zur leichten Einführung sowie für das Gleiten durch Finger, Handfläche und Unterarm erforderlich ist. Das HUNTER passive Sehnenimplantat besteht hauptsächlich aus einem gewobenen Polyesterkern, der mit einem (bariumimprägnierten und daher röntgensichtbaren) Silikonelastomer bedeckt ist. Am distalen Ende des Implantats befindet sich eine Fixierungskomponente aus Edelstahl Typ 316. In der Fixierungskomponente befindet sich eine Öffnung für eine 2,0 mm große Edelstahl-Knochenschraube (nicht mitgeliefert) zur Befestigung des Implantats an der Phalanx. (Angaben zur Schraube sind in den Informationen zum Eingriff zu finden.) Die HUNTER Sehnenstab-Implantate und HUNTER passiven Sehnenimplantate sind beide in doppelten Beuteln verpackt und STERIL, es sei denn, die innere Verpackung ist geöffnet oder beschädigt. 12
13 WARNHINWEISE Stufe I ist bei Patienten unter 5 Jahren nicht kontraindiziert. Für eine Sehnenrekonstruktion bei Kindern muss jedoch ein 2 bis 4 mm großer verstärkter Sehnenstab ohne distale Fixierungskomponente verwendet werden. B. HUNTER AKTIVE SEHNENIMPLANTATE BESCHREIBUNG Das HUNTER aktive Sehnenimplantat besteht hauptsächlich aus einem gewobenen Polyesterkern, der mit einem (bariumimprägnierten und daher röntgensichtbaren) Silikonelastomer bedeckt ist, der die notwendige Kombination aus inerten Eigenschaften, Festigkeit und Flexibilität sowie die glatte Oberfläche, die zur Induzierung der Bildung einer Pseudosehnenscheide, zur leichten Einführung sowie für das Gleiten durch Finger, Handfläche und Unterarm erforderlich ist, bietet. Am distalen Ende des Implantats befindet sich eine Fixierungskomponente aus Edelstahl Typ 316. In der Fixierungskomponente befindet sich eine Öffnung für eine 2,0 mm große Edelstahl-Knochenschraube (nicht mitgeliefert) zur Befestigung des Implantats am Knochen. Die Öffnung ist abgewinkelt, um die Schraube besser in die Kortikalis lenken zu können. Das proximale Ende endet in einer Schlaufe, die die operative Befestigung der Motorsehne am Implantat ermöglicht. Das HUNTER aktive Sehnenimplantat ist STERIL, es sei denn, die innere Verpackung ist geöffnet oder beschädigt. 13
14 KONTRAINDIKATIONEN Aufgrund der derzeit erhältlichen Implantatgrößen kann es nur bei Erwachsenen mit abgeschlossenem Skelettwachstum eingesetzt werden. Für eine Sehnenrekonstruktion bei Kindern muss ein 2 mm, 3 mm oder 4 mm großer verstärkter Sehnenstab ohne distale Fixierungskomponenten oder proximale Schlaufe verwendet werden. C. HUNTER AKTIVES SEHNENIMPLANTAT BC (DOPPELSTRANG) BESCHREIBUNG Das HUNTER aktive Sehnenimplantat BC besteht aus einem gewobenen Polyesterkern, der mit einem (bariumimprägnierten und daher röntgensichtbaren) Silikonelastomer bedeckt ist. Der Stabteil des Implantats ist 4 mm breit und 2 mm dick und von unterschiedlicher Länge. Am proximalen und distalen Ende des Implantats befinden sich zwei Polyesterstränge, die eine Fortsetzung des Innenkerns des Stabs bilden und eine Flecht-Anastomose zur Motorsehne bzw. die Befestigung an der Phalanx ermöglichen. Die Stränge reichen 15 cm über die Stabenden hinaus. Das HUNTER aktive Sehnenimplantat PC ist in doppelten Beuteln verpackt und STERIL, es sei denn, die innere Verpackung ist geöffnet oder beschädigt. Der Zeitraum zwischen der ersten Stufe (Einbringen des Implantats und Bildung der Pseudo-Sehnenscheide) und der zweiten Stufe (Entfernen des Implantats und Einbringen des autogenen Sehnentransplantats) sollte zwei bis sechs Monate betragen, damit das Sehnenbett soweit ausreifen kann, dass es ein Sehnentransplantat versorgen und schmieren kann. Der Chirurg muss anhand der Befunde in der Hand innerhalb dieses Zeitraums den besten Zeitpunkt für den Beginn der zweiten Stufe des Eingriffs bestimmen. 14
15 INDIKATIONEN Das HUNTER aktive Sehnenimplantat BC ist speziell für Fälle indiziert, in denen eine distale Fixierung mit einer Knochenschraube durch die kleine Größe und schlechte Qualität der Phalanx beeinträchtigt werden könnte. Sie ist auch indiziert für Patienten mit kleinen Trochleae, die keine Einführung eines standardmäßigen HUNTER aktiven Sehnenimplantats erlauben, es sei denn, sie werden operativ geöffnet. WARNHINWEISE Der Patient sollte nach der Operation für die erste Stufe häufig durch klinische Untersuchungen und Röntgenaufnahmen überwacht werden, um den Fortschritt zu bewerten und das Behandlungsprogramm evtl. anzupassen. D. HUNTER AKTIVES SEHNENIMPLANTAT DC (DISTALER STRANG) BESCHREIBUNG Das HUNTER aktive Sehnenimplantat DC besteht aus einem gewobenen Polyesterkern, der mit einem (bariumimprägnierten und daher röntgensichtbaren) Silikonelastomer bedeckt ist. Der Stabteil des Implantats ist 4 mm breit und 2 mm dick und von unterschiedlicher Länge. Das proximale Ende endet in einer Schlaufe, die ebenfalls aus einem Polyesterkern besteht, der mit barium-imprägniertem Silikonelastomer bedeckt ist. Diese Schlaufe ermöglicht die Anastomose der Motorsehne am Implantat. Am distalen Ende des Implantats befinden sich zwei Polyesterstränge, die eine Fortsetzung des Innenkerns des Stabs bilden und die Befestigung an der Phalanx ermöglichen. Die Stränge reichen 15 cm über das distale Stabende hinaus. 15
16 Das HUNTER aktive Sehnenimplantat DC ist in doppelten Beuteln verpackt und STERIL, es sei denn, die innere Verpackung ist geöffnet oder beschädigt. Der Zeitraum zwischen der ersten Stufe (Einbringen des Implantats und Bildung der Pseudo-Sehnenscheide) und der zweiten Stufe (Entfernen des Implantats und Einbringen des autogenen Sehnentransplantats) sollte zwei bis sechs Monate betragen, damit das Sehnenbett soweit ausreifen kann, dass es ein Sehnentransplantat versorgen und schmieren kann. Der Chirurg muss anhand der Befunde in der Hand innerhalb dieses Zeitraums den besten Zeitpunkt für den Beginn der zweiten Stufe des Eingriffs bestimmen. INDIKATIONEN Das HUNTER aktive Sehnenimplantat DC ist speziell für Fälle indiziert, in denen eine distale Fixierung mit einer Knochenschraube durch die kleine Größe und schlechte Qualität der Phalanx beeinträchtigt werden könnte. Es kann nach Ermessen des Chirurgen auch bei Patienten mit kleinen Trochleae verwendet werden, die ohne operative Öffnung keine Einführung eines standardmäßigen HUNTER aktiven Sehnenimplantats erlauben. WARNHINWEISE Der Patient sollte nach der Operation für die erste Stufe häufig durch klinische Untersuchungen und Röntgenaufnahmen überwacht werden, um den Fortschritt zu bewerten und das Behandlungsprogramm evtl. anzupassen. 16
17 E. HUNTER AKTIVES SEHNENIMPLANTAT PC (PROXIMALER STRANG) BESCHREIBUNG Das HUNTER aktive Sehnenimplantat PC besteht aus einem gewobenen Polyesterkern, der mit einem (bariumimprägnierten und daher röntgensichtbaren) Silikonelastomer bedeckt ist. Der Stabteil des Implantats ist 4 mm breit und 2 mm dick und von unterschiedlicher Länge. Am proximalen Ende des Implantats befinden sich zwei Polyesterstränge, die eine Fortsetzung des Innenkerns des Stabs bilden und die eine Flecht-Anastomose an der Motorsehne ermöglichen. Die Stränge reichen 15 cm über das proximale Stabende hinaus. Am distalen Ende des Implantats befindet sich eine Fixierungskomponente aus Edelstahl Typ 316. In der Fixierungskomponente befindet sich eine Öffnung für eine 2,0 mm große Edelstahl-Knochenschraube (nicht mitgeliefert) zur Befestigung des Implantats am Knochen. Die Öffnung ist abgewinkelt, um die Schraube besser in die Kortikalis lenken zu können. Das HUNTER aktive Sehnenimplantat PC ist in doppelten Beuteln verpackt und STERIL, es sei denn, die innere Verpackung ist geöffnet oder beschädigt. Der Zeitraum zwischen der ersten Stufe (Einbringen des Implantats und Bildung der Pseudo-Sehnenscheide) und der zweiten Stufe (Entfernen des Implantats und Einbringen des autogenen Sehnentransplantats) sollte zwei bis sechs Monate betragen, damit das Sehnenbett soweit ausreifen kann, dass es ein Sehnentransplantat versorgen und schmieren kann. Der Chirurg muss anhand der Befunde in der Hand innerhalb dieses Zeitraums den besten Zeitpunkt für den Beginn der zweiten Stufe des Eingriffs bestimmen. 17
18 INDIKATIONEN Das HUNTER aktive Sehnenimplantat PC ist speziell für Fälle indiziert, in denen die proximale Anastomose tief im proximalen Unterarm ausgeführt werden muss. Es kann nach Ermessen des Chirurgen auch bei Patienten mit kleinen Trochleae verwendet werden, die ohne operative Öffnung keine Einführung eines standardmäßigen HUNTER aktiven Sehnenimplantats erlauben. WARNHINWEISE Der Patient sollte nach der Operation für die erste Stufe häufig durch klinische Untersuchungen und Röntgenaufnahmen überwacht werden, um den Fortschritt zu bewerten und das Behandlungsprogramm evtl. anzupassen. Marken und eingetragene Marken sind Eigentum von Wright Medical Technology, Inc. oder werden unter Lizenz verwendet. 18
Dieses Paket enthält die folgenden Sprachen:
 DE OSTEOSET XR KNOCHENHOHLRAUMFÜLLER 150841-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE OSTEOSET XR KNOCHENHOHLRAUMFÜLLER 150841-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DARCO SIMONS PLANTARE PLATTE FÜR LAPIDUS-OPERATION
 DE DARCO SIMONS PLANTARE PLATTE FÜR LAPIDUS-OPERATION 150857-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português
DE DARCO SIMONS PLANTARE PLATTE FÜR LAPIDUS-OPERATION 150857-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português
DARCO MIS VORFUSSSCHRAUBE Dieses Paket enthält die folgenden Sprachen:
 DE DARCO MIS VORFUSSSCHRAUBE 140418-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) - Chinese (sch) Türkçe
DE DARCO MIS VORFUSSSCHRAUBE 140418-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) - Chinese (sch) Türkçe
FuseFORCE -IMPLANTATSYSTEM
 DE FuseFORCE -IMPLANTATSYSTEM 152189-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch)
DE FuseFORCE -IMPLANTATSYSTEM 152189-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch)
Metallimplantate für die interne Fixation Dieses Paket enthält die folgenden Sprachen:
 DE Metallimplantate für die interne Fixation 150848-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 -
DE Metallimplantate für die interne Fixation 150848-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 -
Dieses Paket enthält die folgenden Sprachen:
 DE G-FORCE PEEK-OPTIMA NAHTANKERSYSTEM 144880-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) - Chinese
DE G-FORCE PEEK-OPTIMA NAHTANKERSYSTEM 144880-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) - Chinese
GRAVITY SYNCHFIX
 DE M GRAVITY SYNCHFIX 153516-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) Türkçe (tk) Weitere Sprachen
DE M GRAVITY SYNCHFIX 153516-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) Türkçe (tk) Weitere Sprachen
MIIG INJIZIERBARES Transplantat Dieses Paket enthält die folgenden Sprachen:
 MIIG INJIZIERBARES Transplantat 150816-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch)
MIIG INJIZIERBARES Transplantat 150816-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch)
EXTERNE FIXIERUNGSSYSTEME
 DE EXTERNE FIXIERUNGSSYSTEME 150860-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
DE EXTERNE FIXIERUNGSSYSTEME 150860-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
ORTHOLOC KNOCHENSCHRAUBEN Dieses Paket enthält die folgenden Sprachen:
 DE ORTHOLOC KNOCHENSCHRAUBEN 145245-1 Deutsch (de) Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wmt.com. Klicken Sie auf die Option Prescribing Information
DE ORTHOLOC KNOCHENSCHRAUBEN 145245-1 Deutsch (de) Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wmt.com. Klicken Sie auf die Option Prescribing Information
Mischanleitung für IGNITE
 Mischanleitung für IGNITE 150830-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 -Chinese (sch) Türkçe
Mischanleitung für IGNITE 150830-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 -Chinese (sch) Türkçe
CELLPLEX TCP SYNTHETISCHES SPONGIOSAMATERIAL
 DE CELLPLEX TCP SYNTHETISCHES SPONGIOSAMATERIAL 129257-9 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) -
DE CELLPLEX TCP SYNTHETISCHES SPONGIOSAMATERIAL 129257-9 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) -
ENDO-FUSE INTRAOSSÄRES FUSIONSSYSTEM 150843-0. Dieses Paket enthält die folgenden Sprachen:
 DE ENDO-FUSE INTRAOSSÄRES FUSIONSSYSTEM 150843-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中 文 - Chinese
DE ENDO-FUSE INTRAOSSÄRES FUSIONSSYSTEM 150843-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中 文 - Chinese
PRO-DENSE Knochenersatzmaterial Dieses Paket enthält die folgenden Sprachen:
 DE PRO-DENSE Knochenersatzmaterial 133486-11 Dieses Paket enthält die folgenden Sprachen: Deutsch (de) Weitere Sprachen finden Sie auf unserer Website www.wmt.com Klicken Sie dann auf die Option Prescribing
DE PRO-DENSE Knochenersatzmaterial 133486-11 Dieses Paket enthält die folgenden Sprachen: Deutsch (de) Weitere Sprachen finden Sie auf unserer Website www.wmt.com Klicken Sie dann auf die Option Prescribing
M C 0086* Cherry Road 3rd Avenue. Oktober 2013 Gedruckt in den USA
 DE OSTEOSET Knochentransplantatprodukte 150832-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE OSTEOSET Knochentransplantatprodukte 150832-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
BIOARCH SUBTALAR-IMPLANTATSYSTEM
 DE BIOARCH SUBTALAR-IMPLANTATSYSTEM 150840-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch)
DE BIOARCH SUBTALAR-IMPLANTATSYSTEM 150840-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch)
G-FORCE TENODESESCHRAUBE Dieses Paket enthält die folgenden Sprachen:
 DE G-FORCE TENODESESCHRAUBE 150847-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
DE G-FORCE TENODESESCHRAUBE 150847-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
BIOFOAM SPRUNGGELENK-ABSTANDSBLOCK
 DE BIOFOAM SPRUNGGELENK-ABSTANDSBLOCK 150865-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) - Chinese (sch)
DE BIOFOAM SPRUNGGELENK-ABSTANDSBLOCK 150865-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) - Chinese (sch)
SIDEKICK EZ FRAME EXTERNES FIXATIONSSYSTEM
 DE SIDEKICK EZ FRAME EXTERNES FIXATIONSSYSTEM 150886-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文
DE SIDEKICK EZ FRAME EXTERNES FIXATIONSSYSTEM 150886-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文
ORTHOLOC 3Di PLANTARE LAPIDUS-PLATTE
 DE ORTHOLOC 3Di PLANTARE LAPIDUS-PLATTE 152130-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE ORTHOLOC 3Di PLANTARE LAPIDUS-PLATTE 152130-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
BIOFOAM KNOCHENKEIL
 DE BIOFOAM KNOCHENKEIL 150837-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
DE BIOFOAM KNOCHENKEIL 150837-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
HV-SCHRAUBEN Dieses Paket enthält die folgenden Sprachen:
 DE HV-SCHRAUBEN 153421-0 Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wright.com. Klicken Sie auf den Link Prescribing Information (Verschreibungsangaben).
DE HV-SCHRAUBEN 153421-0 Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wright.com. Klicken Sie auf den Link Prescribing Information (Verschreibungsangaben).
SCHULTER-TOTALENDOPROTHESEN-SYSTEM Dieses Paket enthält die folgenden Sprachen:
 DE SCHULTER-TOTALENDOPROTHESEN-SYSTEM 150813-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE SCHULTER-TOTALENDOPROTHESEN-SYSTEM 150813-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
ORTHOLOC Fersenbein-Plattensystem
 DE ORTHOLOC Fersenbein-Plattensystem 150881-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE ORTHOLOC Fersenbein-Plattensystem 150881-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
MICA SCHRAUBEN
 DE MICA SCHRAUBEN 152580-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe (tk)
DE MICA SCHRAUBEN 152580-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe (tk)
INBONE SPRUNGGELENK- TOTALENDOPROTHESEN-SYSTEM MIT KALKANEALSCHAFT
 DE INBONE SPRUNGGELENK- TOTALENDOPROTHESEN-SYSTEM MIT KALKANEALSCHAFT 142742-2 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano
DE INBONE SPRUNGGELENK- TOTALENDOPROTHESEN-SYSTEM MIT KALKANEALSCHAFT 142742-2 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano
GRAVITY NAHTANKERSYSTEM AUS TITAN
 DE GRAVITY NAHTANKERSYSTEM AUS TITAN 152019-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE GRAVITY NAHTANKERSYSTEM AUS TITAN 152019-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
EVOLVE TRIAD SYSTEM 146884-2
 DE EVOLVE TRIAD SYSTEM 146884-2 Deutsch (de) Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wmt.com Klicken Sie dann auf die Option Verschreibungsinformationen.
DE EVOLVE TRIAD SYSTEM 146884-2 Deutsch (de) Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wmt.com Klicken Sie dann auf die Option Verschreibungsinformationen.
GRAVITY NAHTANKERSYSTEME
 DE GRAVITY NAHTANKERSYSTEME 153202-0 Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wright.com. Klicken Sie auf die Option Prescribing Information (Verschreibungsinformationen).
DE GRAVITY NAHTANKERSYSTEME 153202-0 Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wright.com. Klicken Sie auf die Option Prescribing Information (Verschreibungsinformationen).
KLEINZEHEN-METATARSALKÖPFCHEN-IMPLANTATSYSTEM (LMH-SYSTEM) 152382-0
 DE KLEINZEHEN-METATARSALKÖPFCHEN-IMPLANTATSYSTEM (LMH-SYSTEM) 152382-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português
DE KLEINZEHEN-METATARSALKÖPFCHEN-IMPLANTATSYSTEM (LMH-SYSTEM) 152382-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português
EVOLVE TRIAD BONE SCREWS 146886-1
 DE EVOLVE TRIAD BONE SCREWS 146886-1 Deutsch (de) Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wmt.com Klicken Sie dann auf die Option Verschreibungsinformationen.
DE EVOLVE TRIAD BONE SCREWS 146886-1 Deutsch (de) Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wmt.com Klicken Sie dann auf die Option Verschreibungsinformationen.
HANDHABUNG KUNDENSPEZIFISCH HERGESTELLTER MEDIZINISCHER PROPHECY EINWEG-INSTRUMENTE VON MICROPORT
 DE HANDHABUNG KUNDENSPEZIFISCH HERGESTELLTER MEDIZINISCHER PROPHECY EINWEG-INSTRUMENTE VON MICROPORT 150807-1 Deutsch (de) Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer
DE HANDHABUNG KUNDENSPEZIFISCH HERGESTELLTER MEDIZINISCHER PROPHECY EINWEG-INSTRUMENTE VON MICROPORT 150807-1 Deutsch (de) Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer
ORTHOLOC 3Di FUSSREKONSTRUKTION Dieses Paket enthält die folgenden Sprachen:
 Deutsch (de) ORTHOLOC 3Di FUSSREKONSTRUKTION 147996-0 Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wmt.com Klicken Sie dann auf die Option Prescribing
Deutsch (de) ORTHOLOC 3Di FUSSREKONSTRUKTION 147996-0 Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wmt.com Klicken Sie dann auf die Option Prescribing
ORTHOLOC 3Di FUSSREKONSTRUKTIONSSYSTEM - CROSSCHECK -MODUL
 DE ORTHOLOC 3Di FUSSREKONSTRUKTIONSSYSTEM - CROSSCHECK -MODUL 152914-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português
DE ORTHOLOC 3Di FUSSREKONSTRUKTIONSSYSTEM - CROSSCHECK -MODUL 152914-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português
ORTHOLOC 3Di SPRUNGGELENK-PLATTENSYSTEM
 DE ORTHOLOC 3Di SPRUNGGELENK-PLATTENSYSTEM 150853-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE ORTHOLOC 3Di SPRUNGGELENK-PLATTENSYSTEM 150853-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DARCO KANÜLIERTE SCHRAUBEN MIT KOPF
 DE DARCO KANÜLIERTE SCHRAUBEN MIT KOPF 151677-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE DARCO KANÜLIERTE SCHRAUBEN MIT KOPF 151677-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
PRO-TOE HAMMERZEH-FIXIERUNGSSYSTEM
 DE PRO-TOE HAMMERZEH-FIXIERUNGSSYSTEM 150859-2 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE PRO-TOE HAMMERZEH-FIXIERUNGSSYSTEM 150859-2 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
PRO-TOE VO HAMMERZEH-IMPLANTATSYSTEM
 DE PRO-TOE VO HAMMERZEH-IMPLANTATSYSTEM 144939-4 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE PRO-TOE VO HAMMERZEH-IMPLANTATSYSTEM 144939-4 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
SJO SILICONE IMPLANTS Dieses Paket enthält die folgenden Sprachen:
 DE SJO SILICONE IMPLANTS 150823-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
DE SJO SILICONE IMPLANTS 150823-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
SJO SILICONE IMPLANTS Dieses Paket enthält die folgenden Sprachen:
 DE SJO SILICONE IMPLANTS 150823-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
DE SJO SILICONE IMPLANTS 150823-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
Frakturfixation 150846-0. Dieses Paket enthält die folgenden Sprachen:
 DE Frakturfixation 150846-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中 文 - Chinese (sch) Türkçe (tk)
DE Frakturfixation 150846-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中 文 - Chinese (sch) Türkçe (tk)
Rückruf des ASR XL Acetabulumsystems und ASR Hüftoberflächenersatzsystems von DePuy Patienteninformation
 Rückruf des ASR XL Acetabulumsystems und ASR Hüftoberflächenersatzsystems von DePuy Patienteninformation Bei DePuy haben die Sicherheit und Gesundheit unserer Patienten oberste Priorität. Daher evaluieren
Rückruf des ASR XL Acetabulumsystems und ASR Hüftoberflächenersatzsystems von DePuy Patienteninformation Bei DePuy haben die Sicherheit und Gesundheit unserer Patienten oberste Priorität. Daher evaluieren
PHALINX HAMMERZEH-SYSTEM Dieses Paket enthält die folgenden Sprachen:
 DE PHALINX HAMMERZEH-SYSTEM 151676-2 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) Türkçe (tk) Ελληνικά
DE PHALINX HAMMERZEH-SYSTEM 151676-2 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) Türkçe (tk) Ελληνικά
Injektor zur Implantation von hydrophilen preloaded 1stQ Intraokularlinsen
 Gebrauchsanweisung 1st Inject P2.2 Instrument Injektor zur Implantation von hydrophilen preloaded 1stQ Intraokularlinsen Gebrauchsanweisungen werden auf unserer Webseite bereitgestellt: www.1stq.de Inhalt:
Gebrauchsanweisung 1st Inject P2.2 Instrument Injektor zur Implantation von hydrophilen preloaded 1stQ Intraokularlinsen Gebrauchsanweisungen werden auf unserer Webseite bereitgestellt: www.1stq.de Inhalt:
Gebrauchsanleitung für kieferorthopädische Minischrauben mit Warnhinweisen und Vorsichtsmaßnahmen für medizinische Anwender und Patienten.
 Dual-Top Anchor-Systems Gebrauchsanleitung für kieferorthopädische Minischrauben mit Warnhinweisen und Vorsichtsmaßnahmen für medizinische Anwender und Patienten. Vor der klinischen Anwendung ist diese
Dual-Top Anchor-Systems Gebrauchsanleitung für kieferorthopädische Minischrauben mit Warnhinweisen und Vorsichtsmaßnahmen für medizinische Anwender und Patienten. Vor der klinischen Anwendung ist diese
PHALINX YS-HEZREMMAH STEM
 PHALINX YS-HEZREMMAH STEM 151676-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
PHALINX YS-HEZREMMAH STEM 151676-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese (sch) Türkçe
Pflege der Schraubeneintrittsstelle bei Versorgung mit Fixateur Externe
 PAT I E N T E N I N F O R M AT I O N Pflege der Schraubeneintrittsstelle bei Versorgung mit Fixateur Externe EXTERNE FIXATION Was ist externe Fixation? Bei der Behandlung eines Knochens, um eine Fraktur
PAT I E N T E N I N F O R M AT I O N Pflege der Schraubeneintrittsstelle bei Versorgung mit Fixateur Externe EXTERNE FIXATION Was ist externe Fixation? Bei der Behandlung eines Knochens, um eine Fraktur
INVISION TOTAL ANKLE REVISION SYSTEM Dieses Paket enthält die folgenden Sprachen:
 DE INVISION TOTAL ANKLE REVISION SYSTEM 151678-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 -Chinese
DE INVISION TOTAL ANKLE REVISION SYSTEM 151678-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 -Chinese
KANÜLIERTES SCHRAUBENSYSTEM 137183-1. Dieses Paket enthält die folgenden Sprachen:
 DE KANÜLIERTES SCHRAUBENSYSTEM 137183-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) -Chinese (sch) Türkçe
DE KANÜLIERTES SCHRAUBENSYSTEM 137183-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) -Chinese (sch) Türkçe
Entscheidungshilfe der französischen Behörde Afssaps zu PIP-Brustimplantaten
 Entscheidungshilfe der französischen Behörde Afssaps zu PIP-Brustimplantaten Inoffizielle Übersetzung des BfArM im Zweifelsfall gilt der Text der französischen Originalfassung afssaps Französische Agentur
Entscheidungshilfe der französischen Behörde Afssaps zu PIP-Brustimplantaten Inoffizielle Übersetzung des BfArM im Zweifelsfall gilt der Text der französischen Originalfassung afssaps Französische Agentur
SETZEN SIE IHR VERTRAUEN
 SETZEN SIE IHR VERTRAUEN in die Metallstents von Boston Scientific IN KLINISCHE NACHWEISE IN FORTSCHRITTLICHES DESIGN IN TAUSENDE VON ÄRZTEN WIE IHNEN IN ERFAHRUNG EXZELLENTE PROZEDUREN GESTÜTZT DURCH
SETZEN SIE IHR VERTRAUEN in die Metallstents von Boston Scientific IN KLINISCHE NACHWEISE IN FORTSCHRITTLICHES DESIGN IN TAUSENDE VON ÄRZTEN WIE IHNEN IN ERFAHRUNG EXZELLENTE PROZEDUREN GESTÜTZT DURCH
ORTHOLOC 3Di OSG-ARTHRODESE-PLATTENSYSTEM 150884-0
 DE ORTHOLOC 3Di OSG-ARTHRODESE-PLATTENSYSTEM 150884-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中 文
DE ORTHOLOC 3Di OSG-ARTHRODESE-PLATTENSYSTEM 150884-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中 文
INFINITY SPRUNGGELENK-TOTALENDOPROTHESEN-SYSTEM Dieses Paket enthält die folgenden Sprachen:
 DE Deutsch (de) INFINITY SPRUNGGELENK-TOTALENDOPROTHESEN-SYSTEM 149336-0 Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wmt.com. Klicken Sie dann auf die
DE Deutsch (de) INFINITY SPRUNGGELENK-TOTALENDOPROTHESEN-SYSTEM 149336-0 Dieses Paket enthält die folgenden Sprachen: Weitere Sprachen finden Sie auf unserer Website www.wmt.com. Klicken Sie dann auf die
Entscheidungshilfe der französischen Behörde Afssaps zu PIP-Brustimplantaten
 Entscheidungshilfe der französischen Behörde Afssaps zu PIP-Brustimplantaten Inoffizielle Übersetzung des BfArM im Zweifelsfall gilt der Text der französischen Originalfassung afssaps Französische Agentur
Entscheidungshilfe der französischen Behörde Afssaps zu PIP-Brustimplantaten Inoffizielle Übersetzung des BfArM im Zweifelsfall gilt der Text der französischen Originalfassung afssaps Französische Agentur
Definition. Entsprechend der Anatomie des Oberarms kann der Bruch folgende vier Knochenanteile betreffen: = Schultergelenkanteil des Oberarms
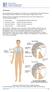 Definition Die proximale Humerusfraktur ist ein Bruch des schulternahen Oberarmknochens, der häufig bei älteren Patienten mit Osteoporose diagnostiziert wird. Entsprechend der Anatomie des Oberarms kann
Definition Die proximale Humerusfraktur ist ein Bruch des schulternahen Oberarmknochens, der häufig bei älteren Patienten mit Osteoporose diagnostiziert wird. Entsprechend der Anatomie des Oberarms kann
INSTRUMENTE Dieses Paket enthält die folgenden Sprachen:
 INSTRUMENTE 137181-1 DE Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) -Chinese (sch) Türkçe (tk) Vertrieb:
INSTRUMENTE 137181-1 DE Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) -Chinese (sch) Türkçe (tk) Vertrieb:
IHR WEG ZUR WIEDERHERSTELLUNG IHRES LÄCHELNS
 Knochen Aufbau: IHR WEG ZUR WIEDERHERSTELLUNG IHRES LÄCHELNS WARUM BENÖTIGE ICH einen KNOCHENaufbau? Ein Knochenaufbau erfolgt in Vorbereitung einer Implantation von Zahnimplantaten, die zum Ersatz eines
Knochen Aufbau: IHR WEG ZUR WIEDERHERSTELLUNG IHRES LÄCHELNS WARUM BENÖTIGE ICH einen KNOCHENaufbau? Ein Knochenaufbau erfolgt in Vorbereitung einer Implantation von Zahnimplantaten, die zum Ersatz eines
SALVATION EXTERNES FIXIERUNGSSYSTEM
 DE SALVATION EXTERNES FIXIERUNGSSYSTEM 151660-2 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) Türkçe (tk)
DE SALVATION EXTERNES FIXIERUNGSSYSTEM 151660-2 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) Türkçe (tk)
INDIKATIONEN Der TITAN-PORT APH ermöglicht einen wiederholten Gefäßzugang zur Apherese.
 INDIKATIONEN Der TITAN-PORT APH ermöglicht einen wiederholten Gefäßzugang zur Apherese. Der Vorteil liegt in der Anwendung eines geschlossenen Systems mit geringerer Infektionsrate und längerer Verweildauermöglichkeit.
INDIKATIONEN Der TITAN-PORT APH ermöglicht einen wiederholten Gefäßzugang zur Apherese. Der Vorteil liegt in der Anwendung eines geschlossenen Systems mit geringerer Infektionsrate und längerer Verweildauermöglichkeit.
Gebrauchsanweisungen BAUTEILE AUS TITAN
 Gebrauchsanweisungen BAUTEILE AUS TITAN Die Techniken, welche zur Durchführung von Prothesen auf Implantate angewandt werden, sind hoch spezialisiert und umfassen besondere Vorgänge, welche durch einen
Gebrauchsanweisungen BAUTEILE AUS TITAN Die Techniken, welche zur Durchführung von Prothesen auf Implantate angewandt werden, sind hoch spezialisiert und umfassen besondere Vorgänge, welche durch einen
129592-11. Dieses Paket enthält die folgenden Sprachen:
 DE Nicht-Silikon-Implantate für die Kleingelenk-Orthopädie 129592-11 Dieses Paket enthält die folgenden Sprachen: Deutsch (de) Weitere Sprachen finden Sie auf unserer Website www.wmt.com. Klicken Sie auf
DE Nicht-Silikon-Implantate für die Kleingelenk-Orthopädie 129592-11 Dieses Paket enthält die folgenden Sprachen: Deutsch (de) Weitere Sprachen finden Sie auf unserer Website www.wmt.com. Klicken Sie auf
Pin-Pflege bei Versorgung mit Fixateur Externe
 PATIENTEN INFORMATION Pin-Pflege bei Versorgung mit Fixateur Externe INHALTSVERZEICHNIS WAS IST EXTERNE FIXATION? 1 WARUM IST DIE PIN-EINTRITTSSTELLE SO WICHTIG? 1 PFLEGE UND REINIGUNG 2 WAS IST ERFORDERLICH?
PATIENTEN INFORMATION Pin-Pflege bei Versorgung mit Fixateur Externe INHALTSVERZEICHNIS WAS IST EXTERNE FIXATION? 1 WARUM IST DIE PIN-EINTRITTSSTELLE SO WICHTIG? 1 PFLEGE UND REINIGUNG 2 WAS IST ERFORDERLICH?
BOHRER Dieses Paket enthält die folgenden Sprachen:
 BOHRER 137182-1 DE Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) -Chinese (sch) Türkçe (tk) Vertrieb: Wright
BOHRER 137182-1 DE Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) -Chinese (sch) Türkçe (tk) Vertrieb: Wright
1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung, max. 200 Zeichen)
 NUB 1/4 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung, max. 200 Zeichen) Magenschrittmacher 1.2 Alternative Bezeichnunge(en) der Methode Enterra 1.3 Beschreibung der Methode Die
NUB 1/4 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung, max. 200 Zeichen) Magenschrittmacher 1.2 Alternative Bezeichnunge(en) der Methode Enterra 1.3 Beschreibung der Methode Die
KYPHON Ballon-Kyphoplastie. Minimal-invasives Verfahren zur Behandlung von Wirbelkörperkompressionsfrakturen
 KYPHON Ballon-Kyphoplastie Minimal-invasives Verfahren zur Behandlung von Wirbelkörperkompressionsfrakturen Zu dieser Broschüre Ihr Arzt hat bei Ihnen eine Wirbelkörperkompressionsfraktur diagnostiziert.
KYPHON Ballon-Kyphoplastie Minimal-invasives Verfahren zur Behandlung von Wirbelkörperkompressionsfrakturen Zu dieser Broschüre Ihr Arzt hat bei Ihnen eine Wirbelkörperkompressionsfraktur diagnostiziert.
Betrifft: DRINGENDER SICHERHEITSHINWEIS FÜR MEDIZINPRODUKTE (RÜCKRUF) CHARGENSPEZIFISCH
 31. Mai 2017 An: Chirurgen Betrifft: DRINGENDER SICHERHEITSHINWEIS FÜR MEDIZINPRODUKTE (RÜCKRUF) CHARGENSPEZIFISCH Betroffenes Produkt: Trauma-Implantate, siehe Anlage 2 Zimmer Biomet leitet einen Rückruf
31. Mai 2017 An: Chirurgen Betrifft: DRINGENDER SICHERHEITSHINWEIS FÜR MEDIZINPRODUKTE (RÜCKRUF) CHARGENSPEZIFISCH Betroffenes Produkt: Trauma-Implantate, siehe Anlage 2 Zimmer Biomet leitet einen Rückruf
SALVATION EXTERNES FIXIERUNGSSYSTEM
 DE SALVATION EXTERNES FIXIERUNGSSYSTEM 151660-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE SALVATION EXTERNES FIXIERUNGSSYSTEM 151660-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DensAccess. Anteriore Kompressionstechnik mit Zugschrauben für die Fixation von Dens- und Transversalfrakturen.
 DensAccess. Anteriore Kompressionstechnik mit Zugschrauben für die Fixation von Dens- und Transversalfrakturen. Operationstechnik Dieses Dokument ist nicht zur Verteilung in den USA bestimmt. Instrumente
DensAccess. Anteriore Kompressionstechnik mit Zugschrauben für die Fixation von Dens- und Transversalfrakturen. Operationstechnik Dieses Dokument ist nicht zur Verteilung in den USA bestimmt. Instrumente
SPRUNGGELENK-TOTALENDOPROTHESENSYSTEME
 DE SPRUNGGELENK-TOTALENDOPROTHESENSYSTEME 150864-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
DE SPRUNGGELENK-TOTALENDOPROTHESENSYSTEME 150864-1 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
OPERATIONSTECHNIK. MCP- / PIP- Implantatsysteme aus Silikon
 OPERATIONSTECHNIK MCP- / PIP- Implantatsysteme aus Silikon MCP- / PIP-Implantatsysteme aus Silikon OPERATIONSTECHNIK INHALT Einführung 1 MCP / PreFlex Operationstechnik 1. Inzision und Freilegung 2 2.
OPERATIONSTECHNIK MCP- / PIP- Implantatsysteme aus Silikon MCP- / PIP-Implantatsysteme aus Silikon OPERATIONSTECHNIK INHALT Einführung 1 MCP / PreFlex Operationstechnik 1. Inzision und Freilegung 2 2.
Gebrauchsanweisung Art.-Nr V04. Analelektrode. Für den ausschliesslich persönlichen Gebrauch durch. Frau/Herr...
 DE Gebrauchsanweisung Art.-Nr.100811-V04 Analelektrode Für den ausschliesslich persönlichen Gebrauch durch Frau/Herr... schwa-medico Gebrauchsanweisung - Analelektrode Zweckbestimmung Diese Analelektrode
DE Gebrauchsanweisung Art.-Nr.100811-V04 Analelektrode Für den ausschliesslich persönlichen Gebrauch durch Frau/Herr... schwa-medico Gebrauchsanweisung - Analelektrode Zweckbestimmung Diese Analelektrode
H A N D, H A N D G E L E N K U N D E L L E N B O G E N Lösungen von Tornier
 H A N D, H A N D G E L E N K U N D E L L E N B O G E N Lösungen von Tornier T o t a l e E l l e n b o g e n p r o t h e s e Wir präsentieren die neueste ENTWICKLUNG der Totale Ellenbogenprothese Latitude
H A N D, H A N D G E L E N K U N D E L L E N B O G E N Lösungen von Tornier T o t a l e E l l e n b o g e n p r o t h e s e Wir präsentieren die neueste ENTWICKLUNG der Totale Ellenbogenprothese Latitude
MICROPORT KNIEGELENKSYSTEME
 DE MICROPORT KNIEGELENKSYSTEME 150806-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) -Chinese (sch) Türkçe
DE MICROPORT KNIEGELENKSYSTEME 150806-0 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) -Chinese (sch) Türkçe
Bedienungsanleitung. MICROPERC -Set steril, zur Einmalverwendung PD-PN-1008
 Bedienungsanleitung MICROPERC -Set steril, zur Einmalverwendung PD-PN-1008 PMT GmbH Im Gewerbegebiet 11 D 66709 Weiskirchen Telefon: +49 (0)6876 9100-0 PD_IFU_MICROPERC-Set-D_A 1 1 Sicherheit 1.1 Vorgesehener
Bedienungsanleitung MICROPERC -Set steril, zur Einmalverwendung PD-PN-1008 PMT GmbH Im Gewerbegebiet 11 D 66709 Weiskirchen Telefon: +49 (0)6876 9100-0 PD_IFU_MICROPERC-Set-D_A 1 1 Sicherheit 1.1 Vorgesehener
Kanülierungsschulung
 Kanülierungsschulung Beachten Sie alle Kontraindikationen, Warn- und Vorsichtshinweise, möglichen unerwünschten Ereignisse sowie alle anderen Hinweise in der Gebrauchsanweisung. 00274 DE Rev F 12Sep2014
Kanülierungsschulung Beachten Sie alle Kontraindikationen, Warn- und Vorsichtshinweise, möglichen unerwünschten Ereignisse sowie alle anderen Hinweise in der Gebrauchsanweisung. 00274 DE Rev F 12Sep2014
Operationstechnik. LCP Distale Tibiaplatte.
 Operationstechnik LCP Distale Tibiaplatte. Inhaltsverzeichnis Indikationen 2 Implantate und Instrumente 3 Operationstechnik 4 Implantate entfernen 9 Bildverstärkerkontrolle Warnung Diese Beschreibung
Operationstechnik LCP Distale Tibiaplatte. Inhaltsverzeichnis Indikationen 2 Implantate und Instrumente 3 Operationstechnik 4 Implantate entfernen 9 Bildverstärkerkontrolle Warnung Diese Beschreibung
HemiCAP kongruente Gelenkrekonstruktion
 HemiCAP kongruente Gelenkrekonstruktion Patello-femorales Gleitlager Hinweise und OP-Anleitung - 1 - Beschreibung Das HemiCAP Implantat zur kongruenten Rekonstruktion des patello-femoralen Gleitlagers
HemiCAP kongruente Gelenkrekonstruktion Patello-femorales Gleitlager Hinweise und OP-Anleitung - 1 - Beschreibung Das HemiCAP Implantat zur kongruenten Rekonstruktion des patello-femoralen Gleitlagers
Verschiedene steril verpackte Hüft- und Trauma-Implantat Schrauben (Siehe Anhang A)
 19. Mai 2016 An: Betreff: Betroffenes Produkt: Risikomanager und Chirurgen DRINGENDE SICHERHEITSINFORMATIONEN - RÜCKRUF Verschiedene steril verpackte Hüft- und Trauma-Implantat Schrauben (Siehe Anhang
19. Mai 2016 An: Betreff: Betroffenes Produkt: Risikomanager und Chirurgen DRINGENDE SICHERHEITSINFORMATIONEN - RÜCKRUF Verschiedene steril verpackte Hüft- und Trauma-Implantat Schrauben (Siehe Anhang
Mandibula-Distraktor Operationstechnik
 Mandibula-Distraktor Operationstechnik 2 Inhaltsverzeichnis Seite Indikationen 4 Distraktor 5 Operationstechnik 6 Set-Inhalt 10 3 Indikationen Indikationen für den Mandibula-Distraktor Der Mandibula-Distraktor
Mandibula-Distraktor Operationstechnik 2 Inhaltsverzeichnis Seite Indikationen 4 Distraktor 5 Operationstechnik 6 Set-Inhalt 10 3 Indikationen Indikationen für den Mandibula-Distraktor Der Mandibula-Distraktor
Die Gelenkspiegelung (=Arthroskopie)
 Die Gelenkspiegelung (=Arthroskopie) Die Funktionsfähigkeit unseres Bewegungsapparates basiert neben der tragenden Fähigkeit unserer Knochen und der Kraft unserer Muskulatur auf der Beweglichkeit unserer
Die Gelenkspiegelung (=Arthroskopie) Die Funktionsfähigkeit unseres Bewegungsapparates basiert neben der tragenden Fähigkeit unserer Knochen und der Kraft unserer Muskulatur auf der Beweglichkeit unserer
Fixationssystem von. AcUMED. AcUMED
 GR_287958_A4.qxd 3/23/06 10:56 AM Page 2 Fixationssystem von AcUMED en Standard Acutrak Mini-Acutrak Repositionsklemme Arthroskopisches Instrumentarium Acutrak 4/5 Acutrak Plus Acutrak Fusion AcUMED 5885
GR_287958_A4.qxd 3/23/06 10:56 AM Page 2 Fixationssystem von AcUMED en Standard Acutrak Mini-Acutrak Repositionsklemme Arthroskopisches Instrumentarium Acutrak 4/5 Acutrak Plus Acutrak Fusion AcUMED 5885
Mini-Fixateur externe.
 Mini-Fixateur externe. Operations- und Montagetechnik Dieses Dokument ist nicht zur Verteilung in den USA bestimmt. Instrumente und Implantate geprüft und freigegeben von der AO Foundation. Bildverstärkerkontrolle
Mini-Fixateur externe. Operations- und Montagetechnik Dieses Dokument ist nicht zur Verteilung in den USA bestimmt. Instrumente und Implantate geprüft und freigegeben von der AO Foundation. Bildverstärkerkontrolle
Operationstechnik MODUS MDO 1.5 Le Fort I Distraktor
 Operationstechnik MODUS MDO 1.5 Le Fort I Distraktor Der MODUS MDO 1.5 Le Fort I Distraktor ist Teil von MODUS MDO 1.5 und besteht aus Adaptionsplatten (M-4978/79), Schrauben, Distraktionszylindern, flexiblen
Operationstechnik MODUS MDO 1.5 Le Fort I Distraktor Der MODUS MDO 1.5 Le Fort I Distraktor ist Teil von MODUS MDO 1.5 und besteht aus Adaptionsplatten (M-4978/79), Schrauben, Distraktionszylindern, flexiblen
AspireSR. Wichtige Informationen zu Ihrem neuen Gerät
 AspireSR Wichtige Informationen zu Ihrem neuen Gerät AspireSR FAQ für Patienten Ihr Arzt empfiehlt das neueste VNS Therapy- Gerät für Ihre Behandlung. Diese Broschüre enthält weitere Informationen zu den
AspireSR Wichtige Informationen zu Ihrem neuen Gerät AspireSR FAQ für Patienten Ihr Arzt empfiehlt das neueste VNS Therapy- Gerät für Ihre Behandlung. Diese Broschüre enthält weitere Informationen zu den
Sprunggelenk-Totalendoprothesensysteme Dieses Paket enthält die folgenden Sprachen:
 DE Sprunggelenk-Totalendoprothesensysteme 150864-2 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) Türkçe
DE Sprunggelenk-Totalendoprothesensysteme 150864-2 Dieses Paket enthält die folgenden Sprachen: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) Türkçe
Klammer Fixationssystem. Implantate Instrumente Applikationen
 Klammer Fixationssystem Implantate Instrumente Applikationen Inhalt Einführung 3 Verwendung der Instrumente Universaleinschläger 4 Verwendung der Instrumente Universalstange 5 Bestellinformation Implantate
Klammer Fixationssystem Implantate Instrumente Applikationen Inhalt Einführung 3 Verwendung der Instrumente Universaleinschläger 4 Verwendung der Instrumente Universalstange 5 Bestellinformation Implantate
Anhang III. Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale
Anhang III Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen der relevanten Abschnitte der Zusammenfassung der Merkmale
Operationstechnik. SynMesh. Wirbelkörperersatz für die zervikale, thorakale und lumbale Wirbelsäule.
 Operationstechnik SynMesh. Wirbelkörperersatz für die zervikale, thorakale und lumbale Wirbelsäule. Inhaltsverzeichnis Indikationen 3 Runde Implantate 4 Ovale Implantate 6 Verschlussschrauben 8 Operationstechnik
Operationstechnik SynMesh. Wirbelkörperersatz für die zervikale, thorakale und lumbale Wirbelsäule. Inhaltsverzeichnis Indikationen 3 Runde Implantate 4 Ovale Implantate 6 Verschlussschrauben 8 Operationstechnik
LCP DF und PLT. Plattensystem für das Distale Femur und die Proximale Laterale Tibia.
 LCP DF und PLT. Plattensystem für das Distale Femur und die Proximale Laterale Tibia. Breite Auswahl anatomisch vorgeformter Platten LCP Kombinationslöcher Winkelstabilität Inhaltsverzeichnis Einführung
LCP DF und PLT. Plattensystem für das Distale Femur und die Proximale Laterale Tibia. Breite Auswahl anatomisch vorgeformter Platten LCP Kombinationslöcher Winkelstabilität Inhaltsverzeichnis Einführung
REAGENZIEN UND MATERIALIEN Positivkontrolle (1) Negativkontrolle (1) Verdünnungslösung (1) Packungsbeilage (1)
 Nur zur Verwendung in der In-vitro-Diagnostik VERWENDUNGSZWECK InflammaDry externe Kontrollen sind nur für die Verwendung mit dem InflammaDry Test. Sie dienen der Überprüfung, ob die Testreagenzien funktionieren
Nur zur Verwendung in der In-vitro-Diagnostik VERWENDUNGSZWECK InflammaDry externe Kontrollen sind nur für die Verwendung mit dem InflammaDry Test. Sie dienen der Überprüfung, ob die Testreagenzien funktionieren
Anhang III. Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale des Arzneimittels, der Etikettierung und
Anhang III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale des Arzneimittels, der Etikettierung und
SEPRAFILM ADHÄSIONSBARRIERE
 SEPRAFILM ADHÄSIONSBARRIERE BESCHREIBUNG Die Seprafilm Adhäsionsbarriere (Seprafilm) ist eine sterile, bioresorbierbare, durchsichtige Membran, die aus zwei chemisch veränderten anionischen Polysacchariden,
SEPRAFILM ADHÄSIONSBARRIERE BESCHREIBUNG Die Seprafilm Adhäsionsbarriere (Seprafilm) ist eine sterile, bioresorbierbare, durchsichtige Membran, die aus zwei chemisch veränderten anionischen Polysacchariden,
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER VENODRIL Tropfen Wirkstoffe: Aesculus hippocastanum Dil. D6, Hamamelis virginiana Dil. D4, Melilotus officinalis Dil. D6, Silybum marianum Dil. D4 Lesen Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER VENODRIL Tropfen Wirkstoffe: Aesculus hippocastanum Dil. D6, Hamamelis virginiana Dil. D4, Melilotus officinalis Dil. D6, Silybum marianum Dil. D4 Lesen Sie
Aufklärungs- und Einwilligungsbogen für die Operation eines Basalioms
 Name: Vorname: Geburtsdatum: Aufklärungs- und Einwilligungsbogen für die Operation eines Basalioms Liebe Patientin, lieber Patient, bei den Untersuchungen wurde ein Basaliom festgestellt. Das Basaliom
Name: Vorname: Geburtsdatum: Aufklärungs- und Einwilligungsbogen für die Operation eines Basalioms Liebe Patientin, lieber Patient, bei den Untersuchungen wurde ein Basaliom festgestellt. Das Basaliom
Gebrauchsanweisung. HCS 1.5. Die versenkbare Kompressionsschraube.
 Gebrauchsanweisung HCS 1.5. Die versenkbare Kompressionsschraube. Inhaltsverzeichnis Einführung HCS 1.5 2 Indikationen 4 Operationstechnik Operationstechnik für HCS 1.5 5 Schraubenextraktion 11 Produktinformation
Gebrauchsanweisung HCS 1.5. Die versenkbare Kompressionsschraube. Inhaltsverzeichnis Einführung HCS 1.5 2 Indikationen 4 Operationstechnik Operationstechnik für HCS 1.5 5 Schraubenextraktion 11 Produktinformation
SERAG BSS I+II. Gebrauchsanweisung SERAG-WIESSNER GmbH & Co. KG Zum Kugelfang Naila / Deutschland
 Gebrauchsanweisung SERAG-WIESSNER GmbH & Co. KG Zum Kugelfang 8-12 95119 Naila / Deutschland SERAG BSS I+II Beschreibung Serag BSS I+II ist eine physiologische, mit Natriumhydrogencarbonat, Glucose und
Gebrauchsanweisung SERAG-WIESSNER GmbH & Co. KG Zum Kugelfang 8-12 95119 Naila / Deutschland SERAG BSS I+II Beschreibung Serag BSS I+II ist eine physiologische, mit Natriumhydrogencarbonat, Glucose und
