Versuch 2. Membranpotentiale
|
|
|
- Carsten Schmitz
- vor 5 Jahren
- Abrufe
Transkript
1 Versuch 2 Membranpotentiale Till Biskup Matrikelnummer: Mai 2000 Einleitung Der vorliegende Versuch demonstrierte vergleichsweise einfach durchführbare Methoden zur Bestimmung von Transmembranpotentialen an lebenden Zellen. Als Versuchsobjekt kamen dabei menschliche Erythrocyten zum Einsatz, die Membranpotentiale wurden über die passive Verteilung kleiner Ladungsträger (Protonen) ermittelt. 1 Aufgaben 1. Eichung des ph Meters und des Schreibers 2. Bestimmung der Zeitkonstanten der Elektrode 3. Bestimmung des Membranpotentials unbehandelter Erythrocyten 4. Bestimmung des K Diffusionspotentials nach Zugabe von A23187 (GARDOS Effekt) 5. Bestimmung der ph Abhängigkeit des DONNAN Potentials 1.1 Eichung von ph Meter und Schreiber Die Messung der Protonen Verteilung erfolgte mittels einer Einstab ph Glaselektrode, die über ein ph Meter an einen y t Schreiber angeschlossen war. Da für die Auswertung ph Wert Differenzen von Interesse sind, mußte zunächst der Schreiber mittels dreier definierter Pufferlösungen kalibriert werden. Durch die Auftragung der Schreiber Einheiten (E s ) des y t Schreibers gegen den ph Wert und sich anschließende lineare Regression konnte eine Eichgerade ermittelt werden, die eine Zuordnung dieser beiden Größen und damit eine Ermittlung des ph Wertes anhand der Meßkurve des Schreibers gestattet. Eichgerade ph E s lineare Regression a u a b u b
2 E S ph Abbildung 1: Eichgerade für ph Meter und Schreiber Stellt man die in Abb. 1 dargestellte, durch lineare Regression errechnete Geradengleichung nach x um, so ergibt sich zur Berechnung des ph Wertes folgende Gleichung: E s b ph a E s Sie erlaubt die Ermittlung der ph Werte für alle weiteren Teilversuche. (1) 1.2 Zeitkonstante der Elektrode Zur Bestimmung der Zeitkonstante wurden 10 ml der gepufferten Versuchslösung (20mM NaCl und Saccharose) verwendet. Nach der Einstellung eine Plateaus wurden 50 ml einer 1 molaren HCl-Lösung hinzugegeben. Es konnte ein deutlicher ph-abfall registriert werden, der sich exponentiell verhielt. Dies läßt sich durch folgende Formel darstellen: ph t ph Ende ph e kt Um jedoch Aussagen über die erhaltenen Punkte machen zu können, wurde die Gleichung logarithmiert und etwas umgeformt: ln ph t ph ph Ende kt (2) 2
3 Zeitkonstante Meßwerte t s E s ph ln ph t ph Ende ph Zeitkonstante Meßwerte t s E s ph ln ph t ph Ende ph Wie aus der Tabelle hervorgeht, sind die Werte bis 105 Sekunden für eine lineare Regression der halblogarithmischen Darstellung brauchbar. Die Zeitkonstante k der Elektrode ergibt sich nun gemäß Gleichung (2) als Steigung aus der durch die erhaltenen Werte gelegten Regressionsgerade. 0.0 ln((ph(t)-ph) / ph) t / s Abbildung 2: Zeitkonstante der Elektrode Auftragung t gegen ln ph t ph Ende ph lineare Regression a u a b u b
4 Somit beträgt die Zeitkonstante k der Elektrode Halbwertszeit t 1 von: s 1. Daraus ergibt sich eine t 1 2 ln2 k s 1.3 Membranpotential unbehandelter Erythrocyten Zur Bestimmung des Membranpotentials wurden 10 ml einer Suspension (Hämatokrit 5) der Lösung I (140 mm NaCl, 5 mm KCl, 2 mm CaCl2) hergestellt. Die Zugabe von 5 µl des protonenspezifischen Ionophors CCCP diente der Permeabilitätserhöhung der Erythrocyten Membran für Protonen und damit der beschleunigten Einstellung der passiven Verteilung der Protonen. Ein erster ph Wert wurde nach Äquilibrierung festgehalten, ein zweiter nach der Hämolyse der Zellen durch Zugabe von 20 µl Triton. Der theoretische Hintergrund dieses Vorgehens ist die Annahme, daß die Pufferwirkung der Erythrocyten stark genug ist, um nach der Hämolyse auch die Lösung auf den zuvor im Erythrocyten vorherrschenden ph Wert zu puffern, so daß auf diese Weise der intrazelluläre ph Wert bestimmt werden kann. Membranpotential E s ph Äquilibrierung Hämolyse Mit Hilfe der NERNST Gleichung (Gl. 3) kann aus der Differenz der beiden ph Werte wie folgt das Transmembranpotential errechnet werden. ψ RT F ph i ph a R Gaskonstante: J K! 1 mol! 1 Temperatur: 298 K F FARADAY Konstante: A s mol! 1 T (3) Für den vorliegenden Versuch ergab sich dabei ein Wert für das Potential ψ von ψ 3 19 mv Dieser unterscheidet sich deutlich vom Literaturwert (-9 mv), hat aber immerhin dieselbe Dimension wie dieser. 1.4 GARDOS Effekt Als GARDOS Effekt bezeichnet man die Ca 2 abhängige Öffnung spezifischer K Kanäle in der Erythrocytenmembran. Diese Öffnung tritt dabei erst bei einem drastischen Anstieg der intrazellulären Ca 2 Konzentration auf. Im Versuch wurde dies durch Zugabe des Ca Ionophors A23187 erreicht, das die Membranpermeabilität für Calcium Ionen stark erhöht bzw. deren Permeieren erst ermöglicht. Die Folge dieser Ca vermittelten Öffnung der Kalium Kanäle ist, daß sich ein K Diffusionspotential einstellt, das im folgenden Versuch experimentell ermittelt wurde. Der Versuch wurde für zwei Lösungen (I und II) durchgeführt und jeweils das Ausgangspotential nach Äquilibrierung sowie die Potentiale nach Zugabe des Ca Ionophors A23187 sowie der Hämolyse gemessen. 4
5 GARDOS Effekt Lösung I E s ph Äquilibrierung A Hämolyse GARDOS Effekt Lösung II E s ph Äquilibrierung A Hämolyse Aus den erhaltenen und hier tabellarisch dargestellten Werten konnten je zwei Potentiale mit Hilfe der NERNST Gleichung (Gl. 3) ermittelt werden: ψ I ψ II RT F ph Äquilibrierung ph A23187 RT F ph Äquilibrierung ph Hämolyse Potentiale in mv Lösung I Lösung II ψ I ψ II Aus den experimentellen Daten geht hervor, daß das Potential zwischen der Äquilibrierung und der Ionophorzugabe in der ersten Lösung relativ stark positiv, in der zweiten Lösung dagegen leicht negativ ist. Das Potential zwischen Äquilibrierung und Hämolyse ist dagegen in beiden Lösungen leicht negativ, in Lösung II sogar ein wenig stärker als in Lösung I. Dieser Sachverhalt läßt sich theoretisch wie folgt erklären: Durch Zugabe des Ca Ionophors A23187 strömte Calcium in die Zelle ein und öffnete dort Kalium Kanäle. Die Kaliumkonzentration des Erythrocyten beträgt etwa 133 mm. Da in der ersten Lösung die K Konzentration wesentlich geringer war als in der Zelle, kam es zu einem starken Kalium Ausstrom, der sich in einer Positivierung der Lösung gegenüber dem Erythrocyten (einem stark positiven Transmembranpotential) bemerkbar machte. In der zweiten Lösung ist die Kaliumkonzentration dagegen etwas höher als in der Zelle. Somit strömt in geringem Maße Kalium durch die geöffneten Kanäle in die Zellen ein, die Lösung wird geringfügig negativ gegenüber dem Erythrocyten geladen, was sich am errechneten Membranpotential direkt ablesen läßt. Das zweite errechnete Potential ψ II entspricht wieder den für unbehandelte Erythocyten ermittelten Potentialen, da die Zellen hämolysiert wurden. Die Ladungsträger konnten sich nun wieder frei verteilen, durch die hohe Pufferkapazität des Hämoglobins wurde der ph Wert der Lösung dem der Erythrocyten angepaßt. 1.5 ph Abhängigkeit des DONNAN Potentials Durch Zugabe von Amphoterizin, einem unspezifischen Kationen Ionophor, wird ein DONNAN Gleichgewicht an der Erythrocyten Membran eingestellt. Im ersten Teil des Versuches wurde wieder der ph Wert vor und nach der Hämolyse gemessen, um daraus das Transmembranpotential zu errechnen. Membranpotential E s ph Äquilibrierung Hämolyse
6 Aus den in der Tabelle angegebenen Werten errechnete sich das Transmembranpotential für diesen Versuchsteil zu mv. Der zweite Versuchsteil, der die Abhängigkeit des DONNAN Potentials vom ph Wert demonstrieren sollte, mißlang durch zu schnelles Zusetzen der 0.1n HCl Lösung. Infolge zu starker Ansäuerung kam es zur Lysis der Zellen, außerdem sank der ph Wert unter den Bereich des y t Schreibers. Zu erwarten wäre gewesen, daß das Potential mit abnehmenden ph-wert größer wird, also von -14,67 mv ansteigt, bei einem ph von etwa 6,5 den Nullpunkt erreicht und dann weiter im positiven Bereich ansteigt. 2 Fehlerbetrachtung Über dir Ursachen der Abweichung des im Versuch 1.3 ermittelten Transmembranpotentials der Erythrocyten vom Literaturwert um den Faktor drei läßt sich nur spekulieren. In Betracht kommen hier in erster Linie das Alter des Blutes sowie Pipettierfehler aufgrund der hohen Viskosität des Blutes. Beim GARDOS Effekt könnten Abweichungen zwischen den beiden Lösungen dadurch erklärt werden, daß jeweils eine neue Verdünnung hergestellt wurde, also auch hier wieder Pipettierfehler möglich waren. 3 Fragen 1. Wie ist eine physiologische Lösung zusammengesetzt, die das extrazelluläre Milieu (Blutplasma) ersetzen soll? Welcher Unterschied besteht zur intrazellulären Lösung (Osmolarität, qualitative Ionenverteilung, ph). 2. Welche Prozesse sind am Zustandekommen des Transmembranpotentials der Erythrocyten beteiligt und wie hoch ist es normalerweise? Welche Rolle spielt das Hämoglobin dabei? 3. Welche Puffersysteme sind an der ph Regulation im Erythrocyten beteiligt? 4. Wie bestimmt man die Zeitkonstante der Elektrode und wofür braucht man sie? 5. Was versteht man unter einer elektrochemischen Meßkette? Was sind Bezugselektroden? 6. Wie kann man mit der Glaselektrode ph Werte messen? 7. Welche Voraussetzungen müssen in diesem Versuch erfüllt sein, damit das Membranpotential mithilfe der NERNST Gleichung bestimmt werden kann? 8. Welche anderen Möglichkeiten, Membranpotentiale zu messen, gibt es? 9. Wie ist das K Diffusionspotential gepolt, wenn der " K # i 133 mm, " K $# a 5 mm betragen? Wie hoch könnte es sein, wenn es nicht zum großen Teil durch die Cl Permeabilität kompensiert würde? Welche Gleichung erlaubt die Berechnung eines Diffusionspotentials? Was würde passieren, wenn " K $# a 140 mm beträgt? 10. Wie entsteht ein DONNAN Potential? Wo kann es auftreten? 1 der Meßgraph zeigte periodische Oszillationen 6
7 3.1 Zusammensetzung einer physiologischen Lösung Die physiologische Lösung, welche das Blutplasma ersetzen soll, ist eine 0,9 NaCl-Lösung in Wasser. Sie besitzt jedoch im Vergleich zur intrazellulären Lösung keine Anteile an K Ionen (In der intrazellulären Lösung liegen K Ionen vor allem innen, Na Ionen dagegen eher außen vor). NaCl ist ein 1 1 wertiges Salz, welches einmal dissoziiert die doppelt so hohe Osmolarität erreicht, als seine Molarität. Man errechne nun die Höhe der Osmolarität: 0,9 bedeuten 9g NaCl in 1kg Wasser. Daraus lässt sich die Molmenge an NaCl berechnen. Sie lautet: 0,154 mol. Da die Rechnung bereits auf einen Liter Wasser bezogen wurde liegt das Endergebnis bereits vor: Die Osmolarität beträgt 0,154 M. 3.2 Transmembranpotential der Erythrocyten Im Unterschied zu den meisten lebenden Zellen ist das Transmembranpotential menschlicher Erythrocyten (ca -9 mv) unter in vivo Bedingungen ein DONNAN Potential, wobei als feste Ladungsträger neben Hämoglobin auch die Kationen K und in geringerem Maße Na gehören. Die Kationen können in gewisser Weise als feste Ladungsträger aufgefaßt werden, da sie vor allem aktiv (d. h. durch Pumpen) transportiert werden und somit eine geringe Permeabilität besitzen. 3.3 Puffersysteme der ph Regulation in Erythrocyten Bikarbonat-Puffer (CO 2 dissoziert in Wasser zu H und HCO3 ) Protein-Puffer (hauptsächlich Imidazolgruppen des Histidins) Haldane-Effekt (desoxygeniertes Blut nimmt H Ionen auf) Carbamino Hb (direkte Bindung von CO 2 an Hämoglobin) H 2 PO4 /HPO2 4 Das im Erythrocyten gebildete Bicarbonat stört das Donnan-Gleichgewicht und wird bis zur Gleichgewichtsherstellung mit Cl Ionen aus Plasma ausgetauscht. 3.4 Zeitkonstante der Elektrode Von der gepufferten Versuchslösung wird die ph Kurve aufgezeichnet, bis sich ein Plateau ergibt. Dann werden 50 ml einer 1M HCl Lösung und der ph Abfall registriert. Es ergibt sich eine exponentielle Kurve, die nach einer Linearisierung ausgewertet werden kann, indem man die aus der Meßkurve entnommen Werte auf halblogarithmisches Papier überträgt und an diesen Werten eine Gerade anlegt. Aus der Steigung der Geraden ergibt sich die Zeitkonstante k der ph Elektrode. Sie ermöglicht eine Aussage darüber, ob die verwendete Elektrode für die Potentialmessung geeignet ist. 3.5 Elektrochemische Meßkette und Bezugselektroden Eine elektrochemische Meßkette ist die elektrisch leitende Verbindung zweier Elektroden zur Messung von Potentialdifferenzen. Eine der beiden Elektroden wird als Bezugselektrode verwendet, in der Regel die Standard Wasserstoffelektrode, deren Potential willkürlich gleich Null gesetzt wird. Die so gemessene Potentialdifferenz entspricht damit direkt dem Elektrodenpotential 7
8 der Meßelektrode. Kommt als Bezugselektrode eine andere Elektrode zum Einsatz, so ist deren Potential bezogen auf die Standard Wasserstoffelektrode bekannt und kann daher in den Berechnungen des Potentials der Meßelektrode berücksichtigt werden. 3.6 ph Wert Messung mit der Glaselektrode Eine Meßkette zur Erfassung des ph Wertes besteht immer aus zwei Komponenten: der Sensorelektrode (Meßelektrode) und der Bezugselektrode. Zwischen diesen beiden wird eine Spannung gemessen, die für den jeweiligen ph Wert typisch ist. Beide Elektroden sind heute zu einer Einstab Glaselektrode zusammengefaßt, die man als ph Sensor bezeichnet. Wird ein ph Sensor in eine wäßrige Lösung eingetaucht, bildet sich am ph sensitiven Membranglas eine Quellschicht. Dies geschieht auch an der Glasmembraninnenseite, die mit einer definierten Pufferlösung (Innenpuffer) in Kontakt steht. Je nach ph Wert der Meßlösung diffundieren die H Ionen aus der Quellschicht heraus oder in sie hinein. Bei alkalischen Lösungen diffundieren die H Ionen nach außen, wobei sich ein negatives Potential an der Quellschichtaußenseite aufbaut. Da die Glasmembran an der Innenseite einen konstanten ph Wert hat, ändert sich das Potential innen während der Messung nicht. Die für den ph Wert der Lösung typische Spannung ergibt sich aus der Potentialdifferenz E zwischen innen und außen nach der NERNSTschen Gleichung: R T E n F ln " H &# i " H # a Für n 1 und mit den eingesetzten Größen für R, T und F sowie unter Berücksichtigung von ln in lg vereinfacht sich die NERNSTsche Gleichung wie folgt: E ' lg" H # i lg" H # a $ ( ph a ph i Der unbekannte ph a Wert kann durch eine einfache Potentialmessung bestimmt werden. Die Potentialdifferenz E wird mittels eines empfindlichen Spannungsmeßgerätes (ph Meter) direkt als ph Wert dargestellt. 3.7 Voraussetzungen für die Bestimmung des Membranpotentials mittels NERNST Gleichung Die Außenlösung muß ungepuffert sein und die Blutzellen müssen hämolysiert werden. Dadurch findet ein Angleich der ph Werte von Außenlösung und Erythrocyten Plasma statt, da letzteres sehr stark gepuffert ist. 3.8 Weitere Möglichkeiten der Messung von Membranpotentialen Als weitere Möglichkeiten der Messung von Membranpotentialen bieten sich an: Mikroelektroden (Spitzendurchmesser mm). optische Methode Bestimmung des Membranpotentials aus der Verteilung von membranpermeablen Ionen zwischen Zelläußerem und -innerem Riesen Neuronen Potentialdifferenz Messung zwischen einer in axialer Richtung im Axonplasma und einer im Außenmedium liegenden Elektrode 8
9 3.9 K) Diffusionspotential Das Membranpotential (Diffusionspotential) berechnet sich nach der NERNST Gleichung wie folgt: ψ RT zf ln a a a i Für die Aktivitäten gelte im ersten Fall folgendes: a a 5 mm a i 133 mm Durch Einsetzen der verschiedenen Konstanten bei einer Raumtemperatur T für den ersten Fall: K folgt ψ * V Das innere Medium ist also positiver als das äußere und somit positiv gepolt. Für den zweiten Fall, bei einer im Außenmedium vorherrschenden Aktivität a i K Ionen, gilt für die Potentialdifferenz: ψ V 140 mm der Hier liegen die Polaritäten also genau umgekehrt zum ersten Fall, das äußere Medium ist positiver gegenüber dem Innenmedium und damit positiv gepolt DONNAN Potential Das DONNAN Potential kann in Zweiphasensystemen auftreten, in denen es neben austauschbaren Ladungsträgern auch solche Ladungsträger gibt, die die Phasengrenze nicht durchdringen können. 9
Versuch 5. Kinetik der Kaliumaufnahme durch Getreidewurzeln
 Versuch Kinetik der Kaliumaufnahme durch Getreidewurzeln Till Biskup Matrikelnummer: 67. Juni Aufgaben. Geben Sie die Kaliumkonzentration an, die am Ende der ersten Meßserie im Medium festgestellt wurde.
Versuch Kinetik der Kaliumaufnahme durch Getreidewurzeln Till Biskup Matrikelnummer: 67. Juni Aufgaben. Geben Sie die Kaliumkonzentration an, die am Ende der ersten Meßserie im Medium festgestellt wurde.
Der ph-wert ist als der negative dekadische Logarithmus der Wasserstoffionenkonzentration
 Einleitung Pufferlösungen Eine Pufferlösung enthält hohe Konzentrationen einer schwachen Säure und ihrer konjugierten Base, z.b. Essigsäure und Acetat. Für eine Lösung, die eine schwache Säure und ihre
Einleitung Pufferlösungen Eine Pufferlösung enthält hohe Konzentrationen einer schwachen Säure und ihrer konjugierten Base, z.b. Essigsäure und Acetat. Für eine Lösung, die eine schwache Säure und ihre
Versuch 6 Elektrophorese
 Versuch 6 Elektrophorese Till Biskup Matrikelnummer: 55567 2. Mai 2000 Einführung Ziel des Versuches ist es, die Zusammenhänge zwischen der elektristatischen Struktur auf Zelloberflächen und ihrem elektrokinetischen
Versuch 6 Elektrophorese Till Biskup Matrikelnummer: 55567 2. Mai 2000 Einführung Ziel des Versuches ist es, die Zusammenhänge zwischen der elektristatischen Struktur auf Zelloberflächen und ihrem elektrokinetischen
E3: Potentiometrische Titration
 Theoretische Grundlagen Als potentiometrische Titration bezeichnet man ein Analyseverfahren, bei dem durch Messung der Gleichgewichtsspannung einer galvanischen Kette auf die Menge des zu titrierenden
Theoretische Grundlagen Als potentiometrische Titration bezeichnet man ein Analyseverfahren, bei dem durch Messung der Gleichgewichtsspannung einer galvanischen Kette auf die Menge des zu titrierenden
Protokoll zu. Versuch 17: Elektrochemische Zellen
 Physikalisch-Chemisches Praktikum 1 26.04.2004 Daniel Meyer / Abdullah Atamer Protokoll zu Versuch 17: Elektrochemische Zellen 1. Versuchsziel Es sollen die EMK verschiedener Zellen mit Elektroden 1. Art
Physikalisch-Chemisches Praktikum 1 26.04.2004 Daniel Meyer / Abdullah Atamer Protokoll zu Versuch 17: Elektrochemische Zellen 1. Versuchsziel Es sollen die EMK verschiedener Zellen mit Elektroden 1. Art
Elektrochemisches Gleichgewicht
 Elektrochemisches Gleichgewicht - Me 2 - Me Me 2 - Me 2 - Me 2 Oxidation: Me Me z z e - Reduktion: Me z z e - Me ANODE Me 2 Me 2 Me 2 Me 2 Me Oxidation: Me Me z z e - Reduktion: Me z z e - Me KATHODE Instrumentelle
Elektrochemisches Gleichgewicht - Me 2 - Me Me 2 - Me 2 - Me 2 Oxidation: Me Me z z e - Reduktion: Me z z e - Me ANODE Me 2 Me 2 Me 2 Me 2 Me Oxidation: Me Me z z e - Reduktion: Me z z e - Me KATHODE Instrumentelle
Physikalische Chemie II (für Biol./Pharm. Wiss.) FS Lösung 7. Musterlösung zum Übungsblatt 7 vom
 Physikalische Chemie II (für Biol./Pharm. Wiss.) S 207 Lösung 7 Musterlösung zum Übungsblatt 7 vom 0.04.207 Diffusionspotential. Zu dieser Teilaufgabe vgl. Adam, Läuger, Stark, S. 326/327 und Skript I.3.3.
Physikalische Chemie II (für Biol./Pharm. Wiss.) S 207 Lösung 7 Musterlösung zum Übungsblatt 7 vom 0.04.207 Diffusionspotential. Zu dieser Teilaufgabe vgl. Adam, Läuger, Stark, S. 326/327 und Skript I.3.3.
Grundlagen: Galvanische Zellen:
 E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
23. Mai 2000 Physikalisch-Chemisches Praktikum Versuch Nr. 10
 23. Mai 2000 Physikalisch-Chemisches Praktikum Versuch Nr. 10 Thema: ph-gleichgewichte von Pufferlösungen Aufgabenstellung: Untersuchung der Puffereigenschaften von Essigsäure-(HAc)-Natriumacetat-(NaAc)-Gemischen
23. Mai 2000 Physikalisch-Chemisches Praktikum Versuch Nr. 10 Thema: ph-gleichgewichte von Pufferlösungen Aufgabenstellung: Untersuchung der Puffereigenschaften von Essigsäure-(HAc)-Natriumacetat-(NaAc)-Gemischen
Versuchsprotokoll Grundpraktikum Analytische Chemie WS 09/10. V2/2: Bestimmung von Fluorid mit einer ionenselektiven Elektrode
 Versuchsprotokoll Grundpraktikum Analytische Chemie WS 09/10 V2/2: Bestimmung von Fluorid mit einer ionenselektiven Elektrode Versuchsdurchführung: 18.01.2010 Protokollabgabe: 22.02.2010 durchgeführt von:
Versuchsprotokoll Grundpraktikum Analytische Chemie WS 09/10 V2/2: Bestimmung von Fluorid mit einer ionenselektiven Elektrode Versuchsdurchführung: 18.01.2010 Protokollabgabe: 22.02.2010 durchgeführt von:
Oekolab FUHRMANN GmbH Gesellschaft für Abwassertechnik und Umweltanalytik
 ÖKOLAB Oekolab FUHRMANN GmbH Gesellschaft für Abwassertechnik und Umweltanalytik Der PH-Wert Der ph-wert ist der negative dekadische Logarithmus der H 3 O + -Ionen-Konzentration: ph = -log c H3O + (also
ÖKOLAB Oekolab FUHRMANN GmbH Gesellschaft für Abwassertechnik und Umweltanalytik Der PH-Wert Der ph-wert ist der negative dekadische Logarithmus der H 3 O + -Ionen-Konzentration: ph = -log c H3O + (also
Seminar zum Quantitativen Anorganischen Praktikum WS 2011/12
 Seminar zum Quantitativen Anorganischen Praktikum WS 211/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 9.1.212, 8-1 Uhr, HS III Allgemeine Einführung in die Quantitative
Seminar zum Quantitativen Anorganischen Praktikum WS 211/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 9.1.212, 8-1 Uhr, HS III Allgemeine Einführung in die Quantitative
Messung der Leitfähigkeit wässriger Elektrolytlösungen
 Versuch Nr. 10: Messung der Leitfähigkeit wässriger Elektrolytlösungen 1. Ziel des Versuchs In diesem Versuch sollen die Leitfähigkeiten von verschiedenen Elektrolyten in verschiedenen Konzentrationen
Versuch Nr. 10: Messung der Leitfähigkeit wässriger Elektrolytlösungen 1. Ziel des Versuchs In diesem Versuch sollen die Leitfähigkeiten von verschiedenen Elektrolyten in verschiedenen Konzentrationen
Die spezifische Leitfähigkeit κ ist umgekehrt proportional zum Widerstand R:
 Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 205/206 Prof. Dr. Eckhard Bartsch / M. Werner M.Sc. Aufgabenblatt 3 vom 3..5 Aufgabe 3 (L) Leitfähigkeiten
Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 205/206 Prof. Dr. Eckhard Bartsch / M. Werner M.Sc. Aufgabenblatt 3 vom 3..5 Aufgabe 3 (L) Leitfähigkeiten
Praxis & Theorie der ph-messtechnik. sauer neutral alkalisch ph Milch
 1. Der ph-wert sauer neutral alkalisch ph 1 2 3 4 5 6 7 8 9 10 11 12 13 14 Milch Dest. Wasser Cola-Getränk Obstessig Bier Orangensaft Kaffee ph-werte von einigen Lebensmitteln In geringem Masse unterliegt
1. Der ph-wert sauer neutral alkalisch ph 1 2 3 4 5 6 7 8 9 10 11 12 13 14 Milch Dest. Wasser Cola-Getränk Obstessig Bier Orangensaft Kaffee ph-werte von einigen Lebensmitteln In geringem Masse unterliegt
Physikalische Chemie Praktikum. Elektrolyte: Dissoziationskonstante von Essigsäure λ von NaCl ist zu ermitteln
 Hochschule Emden/Leer Physikalische Chemie Praktikum Vers. Nr. 16 April 2017 Elektrolyte: Dissoziationskonstante von Essigsäure λ von NaCl ist zu ermitteln In diesem Versuch soll die Dissoziationskonstante
Hochschule Emden/Leer Physikalische Chemie Praktikum Vers. Nr. 16 April 2017 Elektrolyte: Dissoziationskonstante von Essigsäure λ von NaCl ist zu ermitteln In diesem Versuch soll die Dissoziationskonstante
Kapitel 2.2 Kardiopulmonale Homöostase. Kohlendioxid
 Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Base-Reaktionen. 1. Säure-Base. Base-Chemie. 1. Einleitung Seminar für Staatsexamenskandidaten
 Seminar für Staatsexamenskandidaten Säure-Base Base-Chemie 05.12.2007 Winter-Semester 2007/8 1 1. 2. 3. 4. 5. 1. Säure-Base Base-Reaktionen 1. Einleitung 2. Säure-Konstante und Säurestärke 3. ph-wert Wert-Berechnung
Seminar für Staatsexamenskandidaten Säure-Base Base-Chemie 05.12.2007 Winter-Semester 2007/8 1 1. 2. 3. 4. 5. 1. Säure-Base Base-Reaktionen 1. Einleitung 2. Säure-Konstante und Säurestärke 3. ph-wert Wert-Berechnung
Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung
 Versuchsprotokoll: Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung Gruppe 10 29.06.2013 Patrik Wolfram TId:20 Alina Heidbüchel TId:19 1 Inhaltsverzeichnis 1 Einleitung... 3 2 Theorie...
Versuchsprotokoll: Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung Gruppe 10 29.06.2013 Patrik Wolfram TId:20 Alina Heidbüchel TId:19 1 Inhaltsverzeichnis 1 Einleitung... 3 2 Theorie...
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Übung ph / pion. 1. Einleitung. Hauptseite Potenziometrie, Theorie. 1. Einleitung. 1. Potenziometrie, Theorie 2. ph-messung
 Übung ph / pion Hauptseite 1. Einleitung 1. Potenziometrie, Theorie 2. phmessung 1. phmessung mit Wasserstoffelektroden 2. ph Messung mit der Glaselektrode 3. Ionenselektive Messung 4. RedoxPotenziale
Übung ph / pion Hauptseite 1. Einleitung 1. Potenziometrie, Theorie 2. phmessung 1. phmessung mit Wasserstoffelektroden 2. ph Messung mit der Glaselektrode 3. Ionenselektive Messung 4. RedoxPotenziale
Chemisches Potential und Nernstgleichung Carsten Stick
 Chemisches Potential und Nernstgleichung Carsten Stick Definition der mechanischen Arbeit: Kraft mal Weg W = F! ds W = Arbeit oder Energie; F = Kraft; s = Weg Diese Definition lässt sich auch auf die Kompression
Chemisches Potential und Nernstgleichung Carsten Stick Definition der mechanischen Arbeit: Kraft mal Weg W = F! ds W = Arbeit oder Energie; F = Kraft; s = Weg Diese Definition lässt sich auch auf die Kompression
Versuchsprotokoll E11 Potentiometrische ph-messungen mit der Wasserstoffelektrode und der Glaselektrode
 Dieses Werk steht unter der Creative-Commons-Lizenz CC BY-NC 3.0 1 Physikalische Chemie I Versuchsprotokoll E11 Potentiometrische ph-messungen mit der Wasserstoffelektrode und der Glaselektrode Inhaltsverzeichnis
Dieses Werk steht unter der Creative-Commons-Lizenz CC BY-NC 3.0 1 Physikalische Chemie I Versuchsprotokoll E11 Potentiometrische ph-messungen mit der Wasserstoffelektrode und der Glaselektrode Inhaltsverzeichnis
Praktikum Physikalische Chemie I 30. Januar Aktivierungsenergie. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
8.+9. Tag: Säuren und Basen (II) / Redoxreaktionen (II)
 8.+9. Tag: Säuren und Basen (II) / Redoxreaktionen (II) 1 8.+9. Tag: Säuren und Basen (II) / Redoxreaktionen (II) 1. Säuren und Basen II : Puffersysteme Zuweilen benötigt man Lösungen, die einen definierten
8.+9. Tag: Säuren und Basen (II) / Redoxreaktionen (II) 1 8.+9. Tag: Säuren und Basen (II) / Redoxreaktionen (II) 1. Säuren und Basen II : Puffersysteme Zuweilen benötigt man Lösungen, die einen definierten
Elektrolytische Leitfähigkeit
 Elektrolytische Leitfähigkeit 1 Elektrolytische Leitfähigkeit Gegenstand dieses Versuches ist der Zusammenhang der elektrolytischen Leitfähigkeit starker und schwacher Elektrolyten mit deren Konzentration.
Elektrolytische Leitfähigkeit 1 Elektrolytische Leitfähigkeit Gegenstand dieses Versuches ist der Zusammenhang der elektrolytischen Leitfähigkeit starker und schwacher Elektrolyten mit deren Konzentration.
Kurstag 3. Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers
 Kurstag 3 Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Kurstag 3 Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
4 Flaschen mit Stammlösung (0,001 M HCl, 0,001 M NaCl, 0,1 M Essigsäure, 0,001 M Natriumacetat), demineralisiertes Wasser.
 Juni 29, 2017 Physikalisch-Chemisches Praktikum Versuch Nr. 9 Thema: Aufgabenstellung: Material: Substanzen: Ablauf: 1: 2: 3: 4: 5: 6: 7: 8: Ladungstransport in Elektrolytlösungen Ermittlung der Dissoziationskonstanten
Juni 29, 2017 Physikalisch-Chemisches Praktikum Versuch Nr. 9 Thema: Aufgabenstellung: Material: Substanzen: Ablauf: 1: 2: 3: 4: 5: 6: 7: 8: Ladungstransport in Elektrolytlösungen Ermittlung der Dissoziationskonstanten
Elektrizität. = C J m. Das Coulomb Potential φ ist dabei:
 Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Lösung 7. Allgemeine Chemie I Herbstsemester Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf.
 Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Versuchsprotokoll: Konduktometrische Titration und Potentiometrische Titration
 Versuchsprotokoll: Konduktometrische Titration und Potentiometrische Titration Patrik Wolfram TId: 0 Alina Heidbüchel TId: 9 Gruppe 0 05.05.3 Inhaltsverzeichnis. Konduktometrische Titration...3. Einleitung...3.
Versuchsprotokoll: Konduktometrische Titration und Potentiometrische Titration Patrik Wolfram TId: 0 Alina Heidbüchel TId: 9 Gruppe 0 05.05.3 Inhaltsverzeichnis. Konduktometrische Titration...3. Einleitung...3.
Einige Grundbegriffe der Elektrostatik. Elementarladung: e = C
 Einige Grundbegriffe der Elektrostatik Es gibt + und - Ladungen ziehen sich an Einheit der Ladung 1C Elementarladung: e = 1.6.10-19 C 1 Abb 14.7 Biologische Physik 2 Parallel- und Serienschaltung von Kondensatoren/Widerständen
Einige Grundbegriffe der Elektrostatik Es gibt + und - Ladungen ziehen sich an Einheit der Ladung 1C Elementarladung: e = 1.6.10-19 C 1 Abb 14.7 Biologische Physik 2 Parallel- und Serienschaltung von Kondensatoren/Widerständen
CHEMIE KAPITEL 4 SÄURE-BASE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
Übung 6 Vorlesung Bio-Engineering Sommersemester Nervenzellen: Kapitel 4. 1
 Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 21. 04. 08-16:30
Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 21. 04. 08-16:30
Aufbau der Zellmembran Zusammensetzung
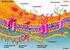 Membranphysiologie Die Zelle Aufbau der Zellmembran Zusammensetzung Der Anteil an Proteinen, Lipiden und Kohlehydraten variiert in biologischen Membranen sehr stark: Membran Anteil an der Trockenmasse
Membranphysiologie Die Zelle Aufbau der Zellmembran Zusammensetzung Der Anteil an Proteinen, Lipiden und Kohlehydraten variiert in biologischen Membranen sehr stark: Membran Anteil an der Trockenmasse
SS Thomas Schrader. der Universität Duisburg-Essen. (Teil 8: Redoxprozesse, Elektrochemie)
 Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Prof. Dr. Stefan Schuster Lehrstuhl für Tierphysiologie
 Prof. Dr. Stefan Schuster Lehrstuhl für Tierphysiologie Tierphysiologie = Wie Tiere funktionieren Welche Anpassungen. Leistungen, Moleküle etc sie einsetzen um zu leben und möglichst am Leben zu beiben
Prof. Dr. Stefan Schuster Lehrstuhl für Tierphysiologie Tierphysiologie = Wie Tiere funktionieren Welche Anpassungen. Leistungen, Moleküle etc sie einsetzen um zu leben und möglichst am Leben zu beiben
E5: Faraday-Konstante
 E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
Was ist Elektrochemie?
 Was ist Elektrochemie? Eine elektrochemische Reaktion erfüllt folgende vier Eigenschaften: Sie findet an Phasengrenzen statt. Die einzelnen Phasen sind unterschiedlich geladen. (unterschiedliche elektrische
Was ist Elektrochemie? Eine elektrochemische Reaktion erfüllt folgende vier Eigenschaften: Sie findet an Phasengrenzen statt. Die einzelnen Phasen sind unterschiedlich geladen. (unterschiedliche elektrische
Ruhemebranpotenzial. den 17 November Dr. Emőke Bódis
 Ruhemebranpotenzial den 17 November 2016 Dr. Emőke Bódis Prüfungsfrage Die Struktur und die Eigenschaften der Zellmembran. Das Ruhemembranpotenzial. Bernstein Kalium Hypothese, Nernst- Gleichung, Donnan-
Ruhemebranpotenzial den 17 November 2016 Dr. Emőke Bódis Prüfungsfrage Die Struktur und die Eigenschaften der Zellmembran. Das Ruhemembranpotenzial. Bernstein Kalium Hypothese, Nernst- Gleichung, Donnan-
Gefahrenstoffe. 2 Bechergläser (230 ml), Bürette, Magnetrührer, Trichter, Rührschwein, Pipette, Stativ, Muffe, ph-meter
 1.1 V1 Titration von Cola In diesem Versuch wird die in Cola enthaltene Phosphorsäure mittels Säure-Base-Titration titriert und bestimmt. Ebenfalls wird mit den erhaltenen Werten gerechnet um das chemische
1.1 V1 Titration von Cola In diesem Versuch wird die in Cola enthaltene Phosphorsäure mittels Säure-Base-Titration titriert und bestimmt. Ebenfalls wird mit den erhaltenen Werten gerechnet um das chemische
ph-messung mit Glaselektrode: Bestimmung der Dissoziationskonstanten schwacher Säuren durch Titrationskurven
 Übungen in physikalischer Chemie für Studierende der Pharmazie Versuch Nr.: 11 Version 2016 Kurzbezeichnung: ph-messung ph-messung mit Glaselektrode: Bestimmung der Dissoziationskonstanten schwacher Säuren
Übungen in physikalischer Chemie für Studierende der Pharmazie Versuch Nr.: 11 Version 2016 Kurzbezeichnung: ph-messung ph-messung mit Glaselektrode: Bestimmung der Dissoziationskonstanten schwacher Säuren
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease.
 A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
Übung Vor-Ort Parameter / Elektroden (1)
 Übung Vor-Ort Parameter / Elektroden (1) 14.04.2009 Filtration / Probenstabilisierung Gegeben ist eine Oberflächenwasser-Probe versetzt mit einer definierten Menge Multi- Element-Standard. Für Gruppe 1,
Übung Vor-Ort Parameter / Elektroden (1) 14.04.2009 Filtration / Probenstabilisierung Gegeben ist eine Oberflächenwasser-Probe versetzt mit einer definierten Menge Multi- Element-Standard. Für Gruppe 1,
Physikalische Chemie
 Physikalische Chemie Prüfungstag 03.02.2017 Bitte beachten Sie Erlaubt sind 4 Seiten Zusammenfassung plus ein Periodensystem. Erlaubt ist ein Taschenrechner. Alle Hilfsmittel, die nicht explizit erlaubt
Physikalische Chemie Prüfungstag 03.02.2017 Bitte beachten Sie Erlaubt sind 4 Seiten Zusammenfassung plus ein Periodensystem. Erlaubt ist ein Taschenrechner. Alle Hilfsmittel, die nicht explizit erlaubt
Die spezifische Leitfähigkeit κ ist umgekehrt proportional zum Widerstand R:
 Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 206/207 Prof. Dr. Eckhard Bartsch / M. Werner M.Sc. Aufgabenblatt 3 vom..6 Aufgabe 3 (L) Leitfähigkeiten
Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 206/207 Prof. Dr. Eckhard Bartsch / M. Werner M.Sc. Aufgabenblatt 3 vom..6 Aufgabe 3 (L) Leitfähigkeiten
Physik 4 Praktikum Auswertung Hall-Effekt
 Physik 4 Praktikum Auswertung Hall-Effekt Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Elektrischer Strom in Halbleitern..... 2 2.2. Hall-Effekt......... 3 3. Durchführung.........
Physik 4 Praktikum Auswertung Hall-Effekt Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Elektrischer Strom in Halbleitern..... 2 2.2. Hall-Effekt......... 3 3. Durchführung.........
Praktikumsprotokoll Physikalisch-Chemisches Anfängerpraktikum
 Tobias Schabel Datum des Praktikumstags: 16.11.2005 Matthias Ernst Protokoll-Datum: 22.11.2005 Gruppe A-11 7. Versuch: EM - Messung elektromotorischer Kräfte Assistent: G. Heusel Aufgabenstellung 1. Die
Tobias Schabel Datum des Praktikumstags: 16.11.2005 Matthias Ernst Protokoll-Datum: 22.11.2005 Gruppe A-11 7. Versuch: EM - Messung elektromotorischer Kräfte Assistent: G. Heusel Aufgabenstellung 1. Die
Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13
 Kantonsschule Kreuzlingen, Klaus Hensler Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13 Grundregeln für stöchiometrische Berechnungen Wenn es um Reaktionen geht zuerst die chem. Gleichung aufstellen
Kantonsschule Kreuzlingen, Klaus Hensler Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13 Grundregeln für stöchiometrische Berechnungen Wenn es um Reaktionen geht zuerst die chem. Gleichung aufstellen
Säure-Base-Titrationen
 Martin Raiber Chemie Protokoll Nr.3 19.2.2006 Säure-Base-Titrationen 1. Titration von Salzsäure mit Natronlauge Chemikalien: Salzsäure (100ml; c(hcl)=0,1 mol/l) Natronlauge (c(naoh)=1 mol/l) Bromthymolblau
Martin Raiber Chemie Protokoll Nr.3 19.2.2006 Säure-Base-Titrationen 1. Titration von Salzsäure mit Natronlauge Chemikalien: Salzsäure (100ml; c(hcl)=0,1 mol/l) Natronlauge (c(naoh)=1 mol/l) Bromthymolblau
Membranpotential bei Neuronen
 Membranpotential bei Neuronen J. Almer 1 Ludwig-Thoma-Gymnasium 9. Juli 2012 J. Almer (Ludwig-Thoma-Gymnasium ) 9. Juli 2012 1 / 17 Gliederung 1 Aufbau der Neuronmembran 2 Ruhepotential bei Neuronen Diffusion
Membranpotential bei Neuronen J. Almer 1 Ludwig-Thoma-Gymnasium 9. Juli 2012 J. Almer (Ludwig-Thoma-Gymnasium ) 9. Juli 2012 1 / 17 Gliederung 1 Aufbau der Neuronmembran 2 Ruhepotential bei Neuronen Diffusion
Säuren und Basen. Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17.
 Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
E3 Aktivitätskoeffizient
 Physikalisch-Chemische Praktika E3 Aktivitätskoeffizient Stichworte zur Vorbereitung: Den Kontext der folgenden Stichworte sollten Sie zur Vorbesprechung und während der Durchführung des Praktikumstermins
Physikalisch-Chemische Praktika E3 Aktivitätskoeffizient Stichworte zur Vorbereitung: Den Kontext der folgenden Stichworte sollten Sie zur Vorbesprechung und während der Durchführung des Praktikumstermins
Fragenkatalog zu BIOPHYSIK I: Teil 2
 Fragenkatalog zu BIOPHYSIK I: Teil 2 1. Was besagt das Lösungsmodell des Membrantransports? Leiten Sie einen mathematischen Ausdruck für die Membranpermeabilität her, der dieses Modell widerspiegelt! 2.
Fragenkatalog zu BIOPHYSIK I: Teil 2 1. Was besagt das Lösungsmodell des Membrantransports? Leiten Sie einen mathematischen Ausdruck für die Membranpermeabilität her, der dieses Modell widerspiegelt! 2.
AnC I Protokoll: 2.2 Potenziometrische Titration von Essigsäure mit NaOH-Lösung! SS Analytische Chemie I. Versuchsprotokoll
 Analytische Chemie I Versuchsprotokoll 2.2 Potenziometrische Titration von Essigsäure mit NaOH-Lösung 1.! Theoretischer Hintergrund Die Potenziometrische Bestimmung wird mit einem ph-meter durchgeführt.
Analytische Chemie I Versuchsprotokoll 2.2 Potenziometrische Titration von Essigsäure mit NaOH-Lösung 1.! Theoretischer Hintergrund Die Potenziometrische Bestimmung wird mit einem ph-meter durchgeführt.
Laborübungen aus Physikalischer Chemie Karl-Franzens-Universität Graz. Potentiometrie
 Potentiometrie Labor: Heinrichstraße 8, 4. OG Werner Dececco, Gerhard Kellner, Anton Huber 1 Ziele des Versuchs In diesem Versuch soll die Abhängigkeit des Dissoziationsverhaltens von Essigsäure bei vier
Potentiometrie Labor: Heinrichstraße 8, 4. OG Werner Dececco, Gerhard Kellner, Anton Huber 1 Ziele des Versuchs In diesem Versuch soll die Abhängigkeit des Dissoziationsverhaltens von Essigsäure bei vier
Standardelektrodenpotentiale und mittlere Aktivitätskoeffizienten
 Versuch PCA E 1 Standardelektrodenpotentiale und mittlere Aktivitätskoeffizienten Aufgabenstellung 1. Durch Messung der Zellspannung der galvanischen Zelle Ag/AgCl/HCl/H 2 /Pt sind zu bestimmen: a) das
Versuch PCA E 1 Standardelektrodenpotentiale und mittlere Aktivitätskoeffizienten Aufgabenstellung 1. Durch Messung der Zellspannung der galvanischen Zelle Ag/AgCl/HCl/H 2 /Pt sind zu bestimmen: a) das
ELEKTROCHEMIE. Elektrischer Strom: Fluß von elektrischer Ladung. elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie.
 ELEKTROCHEMIE Elektrischer Strom: Fluß von elektrischer Ladung Elektrische Leitung: metallische (Elektronen) elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie Galvanische Zellen Elektrolyse Die
ELEKTROCHEMIE Elektrischer Strom: Fluß von elektrischer Ladung Elektrische Leitung: metallische (Elektronen) elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie Galvanische Zellen Elektrolyse Die
Ungefähre Zusammensetzung des Blutes und des Blutplasmas. Die häufigsten Bestandteile des Blutplasmas (Mittelwerte)
 Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
Potentiometrie. Karl-Franzens-Universität Graz WS 2016/17. Treffpunkt: Heinrichstraße 28, 4. OG, Raum 408
 Potentiometrie Treffpunkt: Heinrichstraße 8, 4. OG, Raum 408 Betreuer: Werner De Cecco, Raum 40 (4. OG), Tel: 380 5468 Gerhard Kellner, Raum 317 (3. OG), Tel: 380 5416, e-mail: gerhard.kellner@uni-graz.at
Potentiometrie Treffpunkt: Heinrichstraße 8, 4. OG, Raum 408 Betreuer: Werner De Cecco, Raum 40 (4. OG), Tel: 380 5468 Gerhard Kellner, Raum 317 (3. OG), Tel: 380 5416, e-mail: gerhard.kellner@uni-graz.at
Membranen und Potentiale
 Membranen und Potentiale 1. Einleitung 2. Zellmembran 3. Ionenkanäle 4. Ruhepotential 5. Aktionspotential 6. Methode: Patch-Clamp-Technik Quelle: Thompson Kap. 3, (Pinel Kap. 3) 2. ZELLMEMBRAN Abbildung
Membranen und Potentiale 1. Einleitung 2. Zellmembran 3. Ionenkanäle 4. Ruhepotential 5. Aktionspotential 6. Methode: Patch-Clamp-Technik Quelle: Thompson Kap. 3, (Pinel Kap. 3) 2. ZELLMEMBRAN Abbildung
Protokoll. Basismodul Chemie I, Praktikum: Säure-Base Gleichgewichte
 Protokoll Basismodul Chemie I, Praktikum: Säure-Base Gleichgewichte Veranstalter: Dr. Ulrich Neuert Jörg Mönnich () Betreuer: Carolin, Christian Versuchstag: Freitag, 04.03.2005 Schwache Säuren und Basen;
Protokoll Basismodul Chemie I, Praktikum: Säure-Base Gleichgewichte Veranstalter: Dr. Ulrich Neuert Jörg Mönnich () Betreuer: Carolin, Christian Versuchstag: Freitag, 04.03.2005 Schwache Säuren und Basen;
Bestimmung des Spannungskoeffizienten eines Gases
 Bestimmung des Spannungskoeffizienten eines Gases Einleitung Bei diesem Experiment wollen wir den Spannungskoeffizienten α eines Gases möglichst genau bestimmen und in Folge mit dem Spannungskoeffizienten
Bestimmung des Spannungskoeffizienten eines Gases Einleitung Bei diesem Experiment wollen wir den Spannungskoeffizienten α eines Gases möglichst genau bestimmen und in Folge mit dem Spannungskoeffizienten
Säure-Base Titrationen
 Chemie Praktikum Säure-Base Titrationen WS 2006/2007 Verfasser: Lorenz Germann, Lukas Bischoff Versuchsteilnehmer: Lorenz Germann, Lukas Bischoff Datum: 29.11.2006 Assistent: Lera Tomasic E-mail: lukas-bischoff@student.ethz.ch
Chemie Praktikum Säure-Base Titrationen WS 2006/2007 Verfasser: Lorenz Germann, Lukas Bischoff Versuchsteilnehmer: Lorenz Germann, Lukas Bischoff Datum: 29.11.2006 Assistent: Lera Tomasic E-mail: lukas-bischoff@student.ethz.ch
Zusammenfassung vom
 Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Versuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten -
 1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
lg k ph Profil Versuchsprotokoll Versuch Flüssig D2 1. Stichworte
 Paul Elsinghorst, Jürgen Gäb, Carina Mönig, Iris Korte Versuchsprotokoll Versuch Flüssig D2 lg k ph Profil 1. Stichworte Reaktionskinetik, Reaktionsordnung, Reaktionsmolekularität Stabilität von wässrigen
Paul Elsinghorst, Jürgen Gäb, Carina Mönig, Iris Korte Versuchsprotokoll Versuch Flüssig D2 lg k ph Profil 1. Stichworte Reaktionskinetik, Reaktionsordnung, Reaktionsmolekularität Stabilität von wässrigen
Die ph-abhängigkeit des Redoxpotentials
 Die ph-abhängigkeit des Redoxpotentials Vortrag von Volker Engel im Rahmen der "Übungen im Vortragen mit Demonstrationen-AC" WS 99/00 Einstieg: Mit einem ph-messgerät wird der ph-wert von Leitungswasser
Die ph-abhängigkeit des Redoxpotentials Vortrag von Volker Engel im Rahmen der "Übungen im Vortragen mit Demonstrationen-AC" WS 99/00 Einstieg: Mit einem ph-messgerät wird der ph-wert von Leitungswasser
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
P2-55: Franck-Hertz-Versuch
 Physikalisches Anfängerpraktikum (P2) P2-55: Franck-Hertz-Versuch Auswertung Matthias Faulhaber Karlsruhe, den 16.12.2009 Durchführung: 16.12.2009 1 Franck-Hertz-Versuch mit Quecksilber-Röhre 1.1 Aufbau
Physikalisches Anfängerpraktikum (P2) P2-55: Franck-Hertz-Versuch Auswertung Matthias Faulhaber Karlsruhe, den 16.12.2009 Durchführung: 16.12.2009 1 Franck-Hertz-Versuch mit Quecksilber-Röhre 1.1 Aufbau
Praktikum - Physikalische Chemie I 14. Januar Reaktion 2. Ordnung. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum - Physikalische Chemie I 14. Januar 2016 Reaktion 2. Ordnung Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 Aufgabenstellung Die Reaktionsgeschwindigkeit von der Hydrolyse von Essigsäureacetatester
Praktikum - Physikalische Chemie I 14. Januar 2016 Reaktion 2. Ordnung Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 Aufgabenstellung Die Reaktionsgeschwindigkeit von der Hydrolyse von Essigsäureacetatester
Praktikumsprotokoll Physikalisch-Chemisches Anfängerpraktikum
 Praktikumsprotokoll Physikalisch-Chemisches Anfängerpraktikum Tobias Schabel Datum des Praktikumstags: 02.12.2005 Matthias Ernst Protokoll-Datum: 12/20/2005 Gruppe A-11 11. Versuch: Schmelzdiagramm Assistent:
Praktikumsprotokoll Physikalisch-Chemisches Anfängerpraktikum Tobias Schabel Datum des Praktikumstags: 02.12.2005 Matthias Ernst Protokoll-Datum: 12/20/2005 Gruppe A-11 11. Versuch: Schmelzdiagramm Assistent:
HA + B A - + HB + Säuren und Basen. Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor!
 Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
Aufgabe 1: Geben Sie die korrespondierenden Basen zu folgenden Verbindungen an: a) H 3 PO 4 b) H 2 PO 4
 Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Chemische Gleichgewichte, Säuren und
 Wiederholung der letzten Vorlesungsstunde: Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Thema heute: Chemische Gleichgewichte, Säuren
Wiederholung der letzten Vorlesungsstunde: Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Thema heute: Chemische Gleichgewichte, Säuren
2. Teilklausur zum Chemischen Grundpraktikum im WS 2014/15 vom
 2. Teilklausur zum Chemischen Grundpraktikum im WS 2014/15 vom 21.01.2015 A1 A2 A3 F4 R5 E6 Note 8 12 5 9 8 8 50 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung Schreiben Sie
2. Teilklausur zum Chemischen Grundpraktikum im WS 2014/15 vom 21.01.2015 A1 A2 A3 F4 R5 E6 Note 8 12 5 9 8 8 50 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung Schreiben Sie
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Martin Raiber Chemie Protokoll Nr Gruppe 2 (Schrankseite) Untersuchung von Glycin
 Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
Physikalisches Anfängerpraktikum Teil 2 Versuch PII 22: Lichtstreuung Auswertung
 Physikalisches Anfängerpraktikum Teil 2 Versuch PII 22: Lichtstreuung Auswertung Gruppe Mi-14: Marc A. Donges , 1060028 Tanja Pfister, 14846 05 07 12 1 1 Versuchsaufbau Der Versuch wurde
Physikalisches Anfängerpraktikum Teil 2 Versuch PII 22: Lichtstreuung Auswertung Gruppe Mi-14: Marc A. Donges , 1060028 Tanja Pfister, 14846 05 07 12 1 1 Versuchsaufbau Der Versuch wurde
Gefahrenstoffe H:
 V1 Verseifungsgeschwindigkeit eines Esters In diesem Versuch wird die Reaktionsgeschwindigkeit quantitativ ermittelt. Da dies anhand einer Verseifung eines Esters geschieht, sollten die Schülerinnen und
V1 Verseifungsgeschwindigkeit eines Esters In diesem Versuch wird die Reaktionsgeschwindigkeit quantitativ ermittelt. Da dies anhand einer Verseifung eines Esters geschieht, sollten die Schülerinnen und
ε 0 = Normalpotential Potentiometrie
 Potentiometrie Unter dem Name Potentiometrie werden diejenige analytische Methoden zusammengefasst, die auf der Messung des Elektrodenpotentials zurückzuführen sind (siehe dazu auch Mortimer, Kapitel 21,
Potentiometrie Unter dem Name Potentiometrie werden diejenige analytische Methoden zusammengefasst, die auf der Messung des Elektrodenpotentials zurückzuführen sind (siehe dazu auch Mortimer, Kapitel 21,
STELLUNGNAHMEN (SCHRIFTLICH) BIS AN DAS ON.
 ENTWURF ÖNORM M 6201 Ausgabe: 2006-07-01 Auch Normengruppen C und U2 Ersatz für ÖNORM DIN 19260 und ÖNORM DIN 19261 ICS 01.040.13 01.040.71 13.060.45 71.040.40 ph-messung Begriffe ph-measurement Terms
ENTWURF ÖNORM M 6201 Ausgabe: 2006-07-01 Auch Normengruppen C und U2 Ersatz für ÖNORM DIN 19260 und ÖNORM DIN 19261 ICS 01.040.13 01.040.71 13.060.45 71.040.40 ph-messung Begriffe ph-measurement Terms
Übung Vor-Ort Parameter / Elektroden (2)
 Übung Vor-Ort Parameter / Elektroden (2) 07.11.2006 Filtration / Probenstabilisierung Gegeben ist eine Oberflächenwasser-Probe versetzt mit unterschiedlichen Arsen- Konzentrationen (As(III) + As(V) je
Übung Vor-Ort Parameter / Elektroden (2) 07.11.2006 Filtration / Probenstabilisierung Gegeben ist eine Oberflächenwasser-Probe versetzt mit unterschiedlichen Arsen- Konzentrationen (As(III) + As(V) je
Fehlerrechnung. Bei physikalisch-technischen Messungen können systematische und zufällige Fehler auftreten.
 Seite 1 / 6 H.C. iehuus Fehlerrechnung Bei physikalisch-technischen Messungen können systematische und zufällige Fehler auftreten. Systematische Fehler erzeugen systematische Effekte. Falsch kalibrierte
Seite 1 / 6 H.C. iehuus Fehlerrechnung Bei physikalisch-technischen Messungen können systematische und zufällige Fehler auftreten. Systematische Fehler erzeugen systematische Effekte. Falsch kalibrierte
Wintersemester 2017 Seminar Stöchiometrie
 Wintersemester 2017 Seminar Stöchiometrie Themenüberblick Kurze Wiederholung der wichtigsten Formeln Neue Themen zur Abschlussklausur: 1. Elektrolytische Dissoziation 2. ph-wert Berechnung 3. Puffer Wiederholung
Wintersemester 2017 Seminar Stöchiometrie Themenüberblick Kurze Wiederholung der wichtigsten Formeln Neue Themen zur Abschlussklausur: 1. Elektrolytische Dissoziation 2. ph-wert Berechnung 3. Puffer Wiederholung
Elektrolythaushalt + Säure-Basen-Haushalt
 Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte im Blut: Natrium 135-145 mmol/l Kalium
Elektrolythaushalt + Säure-Basen-Haushalt Überblick Elektrolythaushalt Natrium Kalium Calcium Magnesium Phosphat Säure-Basen-Haushalt Der Elektrolythaushalt Normwerte im Blut: Natrium 135-145 mmol/l Kalium
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
Abb. 5.10: Funktion und Tangentialebene im Punkt ( ) ( ) ( ) 3.) Die Zahlenwerte und in Gleichung (Def. 5.11) berechnen sich durch ( ) ( )
 Abb. 5.0: Funktion und Tangentialebene im Punkt Aus der totalen Differenzierbarkeit folgt sowohl die partielle Differenzierbarkeit als auch die Stetigkeit von : Satz 5.2: Folgerungen der totalen Differenzierbarkeit
Abb. 5.0: Funktion und Tangentialebene im Punkt Aus der totalen Differenzierbarkeit folgt sowohl die partielle Differenzierbarkeit als auch die Stetigkeit von : Satz 5.2: Folgerungen der totalen Differenzierbarkeit
Endlich eine praxistaugliche Wasserstoffelektrode
 Endlich eine praxistaugliche Wasserstoffelektrode Dr. Tanja Kurzenknabe, Gaskatel GmbH Kassel Denise Böhm, Didaktik der Chemie, Universität Würzburg 12.04.2014, Kassel Entstehung von Potentialen - Selbstverkupferung
Endlich eine praxistaugliche Wasserstoffelektrode Dr. Tanja Kurzenknabe, Gaskatel GmbH Kassel Denise Böhm, Didaktik der Chemie, Universität Würzburg 12.04.2014, Kassel Entstehung von Potentialen - Selbstverkupferung
6.2.6 Ohmsches Gesetz ******
 6..6 ****** Motivation Das Ohmsche Gesetz wird mithilfe von verschiedenen Anordnungen von leitenden Drähten untersucht. Experiment 6 7 8 9 0 Abbildung : Versuchsaufbau. Die Ziffern bezeichnen die zehn
6..6 ****** Motivation Das Ohmsche Gesetz wird mithilfe von verschiedenen Anordnungen von leitenden Drähten untersucht. Experiment 6 7 8 9 0 Abbildung : Versuchsaufbau. Die Ziffern bezeichnen die zehn
Geräteversuche. Seminar zum Grundpraktikum in Analytischer Chemie
 Geräteversuche Seminar zum Grundpraktikum in Analytischer Chemie Folie Nr. 1 V 2/5 - Atomabsorptionsspektroskopie Durchführung Versuch AAS Bestimmung von Mangan in wässrigen Lösungen Messkolben auffüllen
Geräteversuche Seminar zum Grundpraktikum in Analytischer Chemie Folie Nr. 1 V 2/5 - Atomabsorptionsspektroskopie Durchführung Versuch AAS Bestimmung von Mangan in wässrigen Lösungen Messkolben auffüllen
Auswertung: Franck-Hertz-Versuch
 Auswertung: Franck-Hertz-Versuch Christine Dörflinger und Frederik Mayer, Gruppe Do-9 10. Mai 2012 1 Inhaltsverzeichnis 1 Erste Anregung von Quecksilber 3 1.1 Aufbauen der Schaltung der Quecksilber-Franck-Hertz-Röhre................
Auswertung: Franck-Hertz-Versuch Christine Dörflinger und Frederik Mayer, Gruppe Do-9 10. Mai 2012 1 Inhaltsverzeichnis 1 Erste Anregung von Quecksilber 3 1.1 Aufbauen der Schaltung der Quecksilber-Franck-Hertz-Röhre................
Standardadditionsverfahren (Eichzusatzverfahren)
 Standardadditionsverfahren (Eichzusatzverfahren) C3CL 1. Eine Farbstofflösung besitzt bei einer Messung in einem Fotometer (Schichtdicke und Wellenlänge unbekannt) die Absorbanz von A= 0,393. Berechnen
Standardadditionsverfahren (Eichzusatzverfahren) C3CL 1. Eine Farbstofflösung besitzt bei einer Messung in einem Fotometer (Schichtdicke und Wellenlänge unbekannt) die Absorbanz von A= 0,393. Berechnen
Versuch 17: Kennlinie der Vakuum-Diode
 Versuch 17: Kennlinie der Vakuum-Diode Inhaltsverzeichnis 1 Einleitung 3 2 Theorie 3 2.1 Prinzip der Vakuumdiode.......................... 3 2.2 Anlaufstrom.................................. 3 2.3 Raumladungsgebiet..............................
Versuch 17: Kennlinie der Vakuum-Diode Inhaltsverzeichnis 1 Einleitung 3 2 Theorie 3 2.1 Prinzip der Vakuumdiode.......................... 3 2.2 Anlaufstrom.................................. 3 2.3 Raumladungsgebiet..............................
[H3O+] [A-] [M+] - [Y-] >> [HA] [OH-] [Y - ] = Menge an M + (Base) welche zur Neutralisation der starkesäure gebraucht wurde!
![[H3O+] [A-] [M+] - [Y-] >> [HA] [OH-] [Y - ] = Menge an M + (Base) welche zur Neutralisation der starkesäure gebraucht wurde! [H3O+] [A-] [M+] - [Y-] >> [HA] [OH-] [Y - ] = Menge an M + (Base) welche zur Neutralisation der starkesäure gebraucht wurde!](/thumbs/55/37326984.jpg) Analytik 4.29 Einige wichtige Punkte der Titrationskurve: A: Beginn der Titration. Da starke Säure zur Essigsäure gegeben wurde ist f < 1. B,E: f = 0; Die starke Säure wurde titriert. Essigsäure in einer
Analytik 4.29 Einige wichtige Punkte der Titrationskurve: A: Beginn der Titration. Da starke Säure zur Essigsäure gegeben wurde ist f < 1. B,E: f = 0; Die starke Säure wurde titriert. Essigsäure in einer
Versuch 5: Zersetzungsspannung
 Gruppe : Christina Sauermann und Johannes Martin 1 Versuch 5: Zersetzungsspannung 1 Darstellung der theoretischen Hintergründe Wird an die beiden Elektroden einer galvanischen Zelle eine Gleichspannung
Gruppe : Christina Sauermann und Johannes Martin 1 Versuch 5: Zersetzungsspannung 1 Darstellung der theoretischen Hintergründe Wird an die beiden Elektroden einer galvanischen Zelle eine Gleichspannung
