BIOCHEMIE des Stoffwechsels ( )
|
|
|
- Martha Egger
- vor 9 Jahren
- Abrufe
Transkript
1 BIEMIE des Stoffwechsels ( ) 4. Einheit Glycolyse (1)
2 Wie werden nun Moleküle in der lebenden Zelle synthetisiert und abgebaut? Wie funktioniert der Intermediärstoffwechsel? Der Intermediärstoffwechsel hat zwei Aufgaben: A. Energiegewinnung für die Synthese von Makromolekülen und anderen energieabhängigen Prozessen. B. Versorgung dieser Prozesse mit den notwendigen Ausgangsstoffen: Aminosäuren (Protein-Biosynthese), Fettsäuren (Lipid-Biosynthese), Nucleosidtriphosphate (Nucleinsäure-Synthese) und Zucker (Polysaccharid- Synthese) Der Bedarf an Energie und Ausgangsstoffen variiert bei den verschiedenen biologischen Prozessen beträchtlich. Lebewesen halten ein Fließgleichgewicht aufrecht. Die Konzentration an Schlüsselmetaboliten ist innerhalb verschiedener Zellkompartimente bemerkenswert stabil (omöostase).
3 Die Bedürfnisse der verschiedenen Lebensformen sind zwar ähnlich. Sie benötigen Energie (ATP), Reduktionsäquivalente (z.b. NADP) und Bausteine ( Kohlenstoff-Quellen ) für Biosynthesen. Die Anforderungen erfüllen die verschiedenen Lebewesen aber auf sehr unterschiedliche Weise. Prinzipiell unterscheidet man (A) AUTTRPE RGANISMEN: Sie nutzen ihre anorganische Umwelt ohne Rückgriff auf Verbindungen, die von anderen rganismen stammen. Sie bauen ihre Kohlenstoffverbindungen aus 2 oder arbonat auf. hemoautotrophe rganismen gewinnen ATP und Reduktionsäquivalente aus der xidation anorganischer Materialen wie Wasserstoff ( 2 ) oder reduzierten Schwefel- ( 2 S) oder Stickstoffverbindungen (N 4+, N 2- ) oder Metall-Ionen (Fe 2+, Mn 2+ ). Dazu gehören nitrifizierende Bakterien und Wasserstoff-, Schwefel- oder Eisenbakterien. Photoautotrophe rganismen
4 A) AUTTRPE RGANISMEN hemoautotrophe rganismen Photoautotrophe rganismen erhalten ihr ATP aus einer Phosphorylierung durch photochemisch getriebenen (cyclischen) Elektronentransport. xygene photoautotrophe rganismen (Pflanzen, yanobakterien) nutzen die Energie des Sonnenlichts um aus Wasser ( 2 ) Elektronen zu entziehen und setzen bei diesem Prozeß molekularen Sauerstoff frei. Andere photoautotrophe rganismen entziehen die Elektronen aus 2 S oder anderen anorganischen Verbindungen (anoxygene phototrophe Bakterien). Immer ist Sonnenlicht die Energiequelle, wodurch diese rganismen unabhängig von allen Kohlenstoff- (außer 2 ) und Elektronenquellen sind (außer 2 oder 2 S usw.)
5 (B) ETERTRPE RGANISMEN sind abhängig von vorhandenen organischen Verbindungen für alle primären Erfordernisse. Die heterotrophe Zelle lebt auf Kosten von Verbindungen, die von anderen Zellen gebildet werden; sie ist zu keinem NETTEINBAU von Kohlendioxid in organische Verbindungen in der Lage. Als Kohlenstoffquelle dienen organische Verbindungen der Nahrung. hemoheterotrophe rganismen (Mensch, Tiere, viele Mikroorganismen und nicht photosynthetisch aktives pflanzliches Gewebe). Sowohl ATP als auch NADP werden durch xidation von organischen Verbindungen gewonnen. Photoheterotrophe rganismen können ATP photochemisch regenerieren, aber sie können photochemisch keine Elektronen auf NADP + übertragen. NADP wird durch xidation von organischen Verbindungen gewonnen.
6 rganismen- Quelle Quelle Quelle Beispiele Typ von ATP des NADP des Kohlenstoff EM- xidation v. xidation v. 2 Wasserstoff, AUTTRP anorganischen anorganischen Schwefel, Verbindungen Verbindungen Eisen und denitrifizierende Bakterien PT- Sonnenlicht 2, 2 S 2 öhere AUTTRP Pflanzen, yanobakt., Schwefelpurpurbakt. PT- Sonnenlicht xidation v. rganische Nicht- ETERTRP organischen Verbindungen Schwefel- Verbindungen purpurbakt. EM- xidation v. xidation v. rganische Mensch, ETER- organischen organischen Verbindungen höhere Tiere, TRP Verbindungen Verbindungen nicht-photosynthet. Pflanzenzellen
7 Nahrungsstoffe ADP ATP 2 Kataboler Stoffwechsel Abbau NADP + NADP Anaboler Stoffwechsel Biosynthese 2 Ausgangsstoffe Stoffwechsel eines aerob-chemoheterotrophen rganismus (z.b. Mensch) Erhaltung- und Wachstum
8 Tierische Zelle
9 Kompartimentierung/Stoffwechselfunktion tierischer rganellen Kompartiment Mitochondrium ytosol Lysosomen Funktion itronensäure-yclus, oxidative Phosphorylierung, Fettsäureoxidation, Aminosäureabbau Glycolyse, Pentosephosphatweg, Fettsäurebiosynthese, viele Reaktionen der Gluconeogenese, Glycogenstoffwechsel Enzymatische Verdauung von Zellkomponenten und aufgenommenen Stoffen
10 Zellkern Golgi-Apparat Rauhes Endoplasmatisches Retikulum Glattes Endoplasmatisches Retikulum Peroxisomen (bei Pflanzen Glyoxisomen) DNA-Replikation und Transkription, RNA-Processing Posttranslationale Modifikation von Membran- und sekretorischen Proteinen; Bildung von Plasmamembranen und sekretorischen Vesikeln Synthese von membrangebundenen und sekretorischen Proteinen Lipid- und Steroidbiosynthese Aminosäure-Abbau und Fettsäure-xidation (bei Pflanzen Reaktionen des Glyoxylatzyklus)
11 istorische Perspektive Louis Pasteur: Die enzymatische Umsetzung von Glucose zu Ethanol wird durch Mikroorganismen verursacht ( ). Eduard Buchner: Umsetzung erfolgt auch in zellfreien Extrakten (1897). Louis Pasteur Arthur arden und William Young: Im Jahre 1905 beobachteten A. ARDEN und W. YUNG, dass der Glucoseabbau zum Erliegen kommt, sofern nicht ausreichende Mengen an anorganischem Phosphat angeboten werden. Es wird letztlich dazu benötigt, Zucker zu phosphorylieren. Sie isolierten ein exosebisphosphat, das später als Fructose-1,6-bisphosphat identifiziert wurde, und zeigten, dass es sich dabei um ein Zwischenprodukt des Glucoseabbaus handelt.
12 Arthur arden und William Young: Ein zellfreier Extrakt kann durch Dialyse in zwei Fraktionen zerlegt werden: Nicht dialysierbare, wärmelabile Fraktion ( Zymase, später Enzyme genannt) und dialysierbare, wärmestabile Fraktion ( ozymase, später oenzyme oder ofaktoren genannt) (1910). 1940: Der gesamte Stoffwechselweg der Glycolyse (griech.:, glykos, süß; lysis, Auflösung) ist aufgeklärt. Gustav Embden, tto Meyerhof, Jacob Parnas (EMBDEN- MEYERF-PARNAS-WEG), arl ori, Gerti ori, arl Neuberg, Robert Robinson und tto Warburg. Die Reaktionsfolge der Umsetzung von Glucose in Pyruvat (= Glycolyse oder Fructose-1,6-bisphosphat-Weg) ist in allen Lebewesen sehr ähnlich. Der Prozeß ist evolutionsgeschichtlich sehr alt und wahrscheinlich in anaerober Umgebung entstanden. Keiner der Reaktionsschritte benötigt Sauerstoff.
13 Glycolyse ist ein prinzipiell anaerober Vorgang (keiner der 10 Reaktionsschritte ist auf die Anwesenheit von 2 angewiesen) P.A.L 1,0 P.A.L = present atmospheric level of 2 0,1 0,01 Prokaryoten Berkner-Marshall-Punkt Eukaryoten Pasteur-Punkt 0,001 Milliarden Jahre
14
15 Sämtliche glycolytischen Enzyme sind im ytosol lokalisiert. Alle sind lösliche Enzyme. Die Zwischenprodukte gelangen durch freie Diffusion zum Folgeenzym. efezellen
16 Glucose + 2 NAD ADP + 2 P i 2 NAD + 2 Pyruvat + 2 ATP hemische Strategie: 1. Addition von Phosphorylgruppen an Glucose 2. hemische Umwandlung der phosphorylierten Zwischenprodukte in Verbindungen mit hohen Gruppenübertragungspotentialen 3. hemische Kopplung der ydrolyse von Intermediaten mit hohem Phosphorylierungspotential an die ATP- Synthese (Substratkettenphosphorylierung)
17 Glucose + 2 NAD ADP + 2 P i 2 NAD + 2 Pyruvat + 2 ATP Reaktionen: Reaktion 1-5: Reaktion 6-10: Vorbereitende Phase. Überführung von Glucose in zwei Moleküle Glycerinaldehyd- 3-Phosphat. Investition von Energie (Verbrauch von 2 ATP-Molekülen pro Glucose) Überführung der 2 Glycerinaldehyd-3- Phosphat-Moleküle in Pyruvat (Bildung von 4 ATP Molekülen pro Glucose). Umwandlung von Glucose ( 6 -Körper) in zwei Pyruvat ( 3 -Körper) mit niedrigerer Freier Enthalpie. Nettogewinn von 2 ATP pro Glucose
18 GLUSE 2 ADP + 2 P i 2 NAD + Fructose-1,6-bisphosphat 2 ATP 2 NAD 2 Pyruvat Anaerobe homolactische Fermentation Aerobe xidation (Mitochondrien) Anaerobe alkoholische Gärung
19 2 Pyruvat Anaerobe homolactische Fermentation 2 NAD 2 NAD + 2 Acetyl-oA Anaerobe alkohol. Gärung itronensäure- yclus 2 NAD NAD 2 NAD + 2 Lactat xidative Phosphorylierung Ethanol 2 NAD
20 Regeneration des NAD + NAD + ist das auptoxidationsmittel der Glycolyse. Das gebildete NAD muss kontinuierlich reoxidiert werden. 3 Wege: 1. Muskel: Regeneration von NAD + unter anaeroben Bedingungen. Reduktion von Pyruvat zu Lactat durch NAD. MLATISE GÄRUNG 2. efe: Decarboxylierung von Pyruvat zu Acetaldehyd unter anaeroben Bedingungen. Reduktion von Acetaldehyd zu Ethanol durch NAD. ALKLISE GÄRUNG 3. Mitochondrien: Unter aeroben Bedingungen erfolgt die xidation von NAD in der Atmungskette unter Bildung von 2,5 bis 3 ATP pro NAD XIDATIVE PSPRYLIERUNG
21 Inhaltsverzeichnis Glycolyse 1. Glucosetransport 2. Abfolge der chemischen Umwandlungen der Glucose in Pyruvat (10 Reaktionen) 3. Mechanismen der einzelnen Reaktionen 4. Thermodynamik und Regulation 5. Anaerobe homolactische Fermentation und anaerobe alkoholische Gärung 6. Einschleusen von Galactose, Mannose, Fructose und Glycerin in die Glykolyse
22 Inhaltsverzeichnis Glycolyse 1. Glucosetransport Warum ist Glucose ein wichtiger und weit verbreiteter Brennstoff? In Säugern ist Glucose der einzige Brennstoff für das Gehirn (abgesehen vom ungerzustand) und von Erythrocyten. Gründe? Glucose kann unter präbiotischen Bedingungen aus Formaldehyd entstehen. ohe Stabilität: alle ydroxylgruppen in der Ringkonformation der -D-Glucose liegen äquatorial. Glucose hat geringe Tendenz Proteine zu glycosylieren und reagiert nicht mit Aminogruppen von Proteinen, da Ringbildung dominiert.
23 Die meisten eukaryotischen Zellen nehmen D- Glucose schnell, L-Glucose jedoch überhaupt nicht auf (hohe Spezifität biologischer Transportsysteme). Der Glucosetransport über die Plasmamembran wird durch erleichterte Diffusion mit einem speziellen Transportsystem katalysiert. Bei erleichterter Diffusion folgt der Nettofluss prinzipiell dem Konzentrationsgradienten. Muskelzellen übernehmen Glucose dennoch ständig aus dem Blut, weil die von der Zelle aufgenommene Glucose in einer schnellen Stoffwechselreaktion (1. Reaktion der Glycolyse) sofort in nicht mehr permeables Glucose-6-Phosphat (G6P) umgewandelt wird. Dadurch wird erreicht, dass 1. die geladene Form in der Zelle bleibt (Membran impermeabel für G6P) und die 2. intrazelluläre Konzentration von Glucose gering ist und dadurch die Diffusion in die Zelle begünstigt wird
24 Allgemein gilt, dass bei einem ungeladenen Stoff die Änderung der Freien Enthalpie bei der Bewegung dieses Moleküls vom Kompartiment 1, indem es in der Konzentration c 1 vorliegt, in ein Kompartiment mit der Konzentration c 2 folgendermaßen ist: G 1 2 = RTln (c 2 /c 1 ) = 2,3RTlog(c 2 /c 1 ) Der Nettofluss endet, wenn c 2 = c 1. D-Glucose Extrazellulär ytoplasma D-Glucose (ungeladen) ATP ADP Glucose-6-Phosphat (geladen)
25
26 Die thermodynamisch begünstigte Bewegung von Glucose durch die Plasmamembran tierischer Zellen wird durch mehrere Glucosetransportproteine vermittelt. Bezeichnung der Mitglieder dieser Proteinfamilie mit GLUT1, GLUT2, GLUT3, GLUT4 und GLUT5..GLUT10 (Isoformen mit funktioneller Spezialisierung). Typisches Strukturmotif: Integrale Membranproteine mit zwölf Transmembransegmenten ( -elices). Transport des Zuckermolelüls durch Konformationsänderung innerhalb des Transportproteins. Noch keine 3-D-Struktur bekannt. Die verschiedenen Mitglieder unterscheiden sich hinsichtlich ihrer Lokalisation (Gewebe, rgan), der Kinetik des Glucose-Transports (K M ), der Regulation, und des Expressionsmusters.
27 Muckler et al. (1985) Science 229, 941 Asn45 Modell eines GLUT-Proteins aus Säugetieren + 3 N - Glucosetransporter gehören zur major facilitator-(mf-)superfamilie: Vorkommen in unterschiedlichsten rganismen, z.b. auch E. coli
28 Typischer Serumglucosespiegel: 4-8 mmol/l Dünndarm: Resorption von Glucose aus dem Darm durch Symport: Na + -Glucose Symporter. Pumpt Glucose aus dem Dünndarm in die Darmepithelzellen. GLUT5: Expression in Dünndarm und Niere. Entläßt Glucose aus den Darmepithelzellen in den Blutstrom durch erleichterte Diffusion. Auch Fructosetransporter. GLUT1 und GLUT3 werden in Erythrocyten, Gehirn und Plazenta exprimiert und stellen in diesen rganen die Grundversorgung mit Glucose sicher. Transportieren ständig Glucose mit mehr oder weniger konstanter Geschwindigkeit. K M -Wert: 1 mmol/l. Transport durch erleichterte Diffusion. GLUT4: Expression in Skelettmuskel, Fettzellen und erz. K M -Wert: 5 mmol/l. Durch Insulin wird die Expression und Einbau von GLUT4-Transportern in der Plasmamembran begünstigt. Insulin fördert also die Aufnahme von Glucose in Muskel und Fettgewebe.
29 GLUT4 vermittelt Eintritt von Glucose in Fett- und Muskelzellen. K M -Wert: 5 mmol/l. Durch Insulin wird die Expression von GLUT4- Transportern in der Plasmamembran begünstigt. Insulin fördert also die Aufnahme von Glucose in Muskel und Fettgewebe. Insulin, ein Polypeptidhormon GLUT2 ist in Leber und pankreatischen -Zellen lokalisiert. K M -Wert: mmol/l. Die Eintrittsgeschwindigkeit von Glucose in diese Gewebe ist daher zum Blutglucosespiegel proportional. Die Bauspeicheldrüse ist daher in der Lage, den Glucosespiegel zu messen und die Geschwindigkeit der Insulinsekretion entsprechend anzupassen. Die Leber nimmt Glucose nur in Zeiten des Überflusses auf. Bei niedrigem Glucose- Spiegel gelangt Glucose bevorzugt ins Gehirn und andere Gewebe!
30 Diese Tabelle soll nur die Komplexität bezüglich Verteilung und Funktionalität von Isoformen von Proteinen in höheren rganismen unterstreichen.
31 Inhaltsverzeichnis Glycolyse 1. Glucosetransport 2. Abfolge der chemischen Umwandlungen der Glucose in Pyruvat (10 Reaktionen)
32 Reaktionen und Thermodynamik der Glycolyse Reaktion Enzym G K eq G kj/mol 25 kj/mol -D-Glucose + ATP 4- Glucose-6-Phosphat + ADP exokinase -16, ,9 Glucose-6-Phosphat Glucosephosphat Fructose-6-Phosphat Isomerase +1,67 0,51-2,92 Fructose-6-Phosphat + ATP 4- Phosphofructo- Fructose-1,6-Bisphosphat + ADP kinase -14, ,8 Fructose-1,6-bisphosphat Dihydroxyacetonphosphat + Glycerinaldehyd-3-P Aldolase +23,9 6, ,23
33 Reaktion Enzym G K eq G kj/mol kj/mol Dihydroxyacetonphosphat Triosephosphat- Glycerinaldehyd-3-P Isomerase 7,56 0,0472 2,41 Glycerinaldehyd-3-P + P i + Glycerinaldehyd-3-P- NAD + 1,3- Bisphosphoglycerat Dehydrogenase + NAD ,3 0,0786-1,29 1,3-Bisphosphoglycerat + ADP 3 Phosphoglycerat- - 3-Phosphoglycerat + ATP 4- Kinase -18, ,1 2-Phosphoglycerat Phosphoenolpyruvat + 2 Enolase +1,8 0,483 +1,1 3-Phosphoglycerat Phosphoglycerat- 2-Phosphoglycerat Mutase +4,4 0,169 +0,83 Phosphoenolpyruvat + ADP Pyruvat- Pyruvat + ATP 4- kinase -31,7 3, Pyruvat + NAD + + Lactat- Lactat + NAD + Dehydrogenase -25,2 2, ,8
34 Typische Konzentrationen von Intermediaten der Glycolyse in Erythrocyten Metabolit mm Glucose-6-phosphat 0,083 Fructose-6-phosphat 0,014 Fructose-1,6-bisphosphat 0,031 Dihydroxyacetonphosphat 0,14 Glycerinaldehyd-3-phosphat 0,019 1,3-Bisphosphoglycerat 0,001 2,3-Bisphosphoglycerat 4,0 3-Phosphoglycerat 0,12 2-Phosphoglycerat 0,030 Phosphoenolpyruvat 0,023 Pyruvat 0,051 Lactat 2,9 ATP 1,85 ADP 0,14 P i 1,0
35 Energetik der Umwandlung von Glucose in Lactat: G = -183,6 kj/mol Es findet keine Netto-xidation oder -Reduktion bei der Umwandlung von Glucose in Lactat statt (d.h. xidations- und Reduktionsreaktionen kompensieren sich). Bindungen lagern sich um, jedoch werden Elektronen weder gewonnen noch gehen sie verloren. Nur ein Teil der Energie, die in Glucose steckt, wird in Form von 2 ATP gewonnen: 2 ADP + 2 P i 2 ATP G = kj/mol = 61 kj/mol Glycolyse = Kopplung der Reaktionen: Glucose + 2 ADP + 2 P i 2 Lactat + 2 ATP G = -183, = -122,6 kj/mol (33% Wirkungsgrad; Realität: 50%)
36 Inhaltsverzeichnis Glycolyse 1. Glucosetransport 2. Abfolge der chemischen Umwandlungen der Glucose in Pyruvat (10 Reaktionen) 3. Mechanismen der einzelnen Reaktionen
37 Glycolyse 1. Reaktion: exokinase, Glucokinase Glucose + ATP Glucose-6-Phosphat + ADP + + Enzyme: D-exose-6-Phosphotransferase (E ) exokinase Glucokinase ofaktoren: Magnesiumionen (Mg 2+ ) Glucose-6-Phosphat Glucose-6-Phosphat
38 -D-Glucose + ATP 4- -D-Glucose-6-Phosphat + ADP Phosphorylierung von Glucose: ydrolyse von ATP: + 13,8 kj/mol - 30,5 kj/mol Realität (Erythrocyten): G = -16,7 kj/mol (K eq = 850) Standardbedingungen (Konzentrationen = 1 mol/l) [Glu] = 5 mm, [ATP] = 1,85 mm, [G-6-P] = 0,083 mm, [ADP] = 0,14 mm. G = G + RT ln {[G-6-P][ADP]/[Glu][ATP]} = G = - 16,7 kj/mol + (8,314 J/mol.K)(310K) ln {[0,083][0,14] /[5,0][1,85]} G = -33,9 kj/mol
39 D-Glucose wird also im ytoplasma phosphoryliert, wobei die Phosphorylgruppe aus ATP stammt. Enzyme, die Phosphorylgruppen übertragen heißen Kinasen. Im enzymatischen Namen scheint auch das Akzeptormolekül auf. Im Menschen sind zwei Enzyme für die Umwandlung von Glucose in Glucose-6- Phosphat zuständig: exokinase: Überträgt Phosphorylgruppe auf exosen, ist also unspezifisch hinsichtlich des Akzeptors. Substrate sind D-Glucose, D-Mannose und D-Fructose. K M (Glucose) = 0,1 mm; Vorkommen: ubiquitär; verschiedene gewebsspezifische Isoenzyme mit unterschiedl. kinetischen Eigenschaften. umane exokinase ist Monomer mit etwa 100 kda. Regulation: Allosterische emmung durch Glucose-6-Phosphat (G6P) (Produkthemmung)
40 Glucokinase: Überträgt Phosphorylgruppe spezifisch nur auf D-Glucose. K M (Glucose) = 10 mm; Vorkommen: nur in der Leber umane Glucokinase ist Monomer mit etwa 50 kda. Glucokinase wird im Gegensatz zur exokinase nicht durch das Reaktionsprodukt G6P inhibiert. Seine Expression wird jedoch durch Insulin induziert. Glucokinase ist an der Regulation des Blutglucose-Spiegels beteiligt. Die Aufgabe der Glucokinase besteht darin, Glucose-6-Phosphat für die Synthese von Glycogen (Glucose-Speicherform) in der Leber zu liefern. Der hohe K M -Wert der Glucokinase garantiert die Glucose-Grundversorgung des Gehirns und der Muskulatur.
41
42 PDB-code
43 Programme zur Visualisierung: RASML PDB-VIEWER:
44 PDB-ode: 1K Recombinant uman exokinase Type I omplexed With Glucose and Phosphate Authors: A. E. Aleshin, R. B. onzatko Exp. Method: X-ray Diffraction lassification: Phosphotransferase E Number: Source: omo sapiens Primary itation: J. Mol. Biol. (1998) 282, pp. 345
45 Phosphorylgruppenübertragung Angriff eines Nucleophils (Y) am elektrophilen Phosphoratom einer tetraedischen Phosphorylgruppe Y X P X P Y Trigonal bipyramidales Zwischenprodukt Eliminierung der Abgangsgruppe unter Inversion der Konfiguration P Y X
46 - 2 N P N N 2 P P - - N N - ATP, Adenosintriphosphat
47 Beispiel für enzymatische Phosphorylgruppenübertragung: Glykolyseenzym exokinase 17 P 16 -ADP P Inversion der Konfiguration 16 Glucose 16 -ADP P Glucose Trigonal bipyramidales Zwischenprodukt
48 exokinase und Glucokinase sind nur aktiv, wenn Mg 2+ -Ionen (oder andere zweiwertige Ionen wie z.b. Mn 2+ ) vorhanden sind. Gilt für alle Kinasen. Das divalente Metallion bildet einen Komplex mit dem ATP und erleichtert dadurch den nucleophilen Angriff durch Abschirmung der negativ geladenen Gruppen. Nichtkomplexiertes ATP hemmt die exokinase! N 2 Elektrophiles Phosphoratom N N N N P P P 2 Mg 2+
49 Frage: Warum überträgt die Kinase die Phosphorylgruppe so spezifisch auf Glucose und nicht auf Wasser (unter Bildung von ADP und P i ; ATPase-Aktivität)? Realität: Wasserkonzentration: 55 mol/l. Wasser klein genug für Bindungsstelle der Kinase Phosphorylgruppenübertragung des ATP auf Wasser ist stärker exergonisch als Übertragung auf Glucose. Die exokinase katalysiert die Übertragung auf Glucose mal schneller als auf Wasser Ursache: Reaktionsmechanismus: Random-Bi-Bi- Mechanismus mit tiefgreifender Konformationsänderung
50 exokinase (Mensch) Spalt: Aktives Zentrum Binden von Glucose: tiefgreifende Konformationsänderung. Die beiden Lappen bewegen sich bis zu 8 Å aufeinander zu und umschließen das Substrat Glucose (induced fit).
51 exokinase exokinase- Glucosekomplex Glucose Katalyse durch Annäherungseffekte. Binden von Glucose bewirkt Schließung der Enzymlappen und bringt die 5-ydroxymethylgruppe der D-Glucose in unmittelbare Nachbarschaft von bereits gebundenem ATP-Mg 2+. Substratinduzierte Konformationsänderung des Enzyms. Ausschluß von Wasser: Reduktion der Polarität des aktiven Zentrums, nucleophiler Reaktionsprozeß wird beschleunigt.
52 Beweis des Reaktionsmechanismus: Reaktion mit Pseudosubstrat -D-Xylose. Die -D-Xylose unterscheidet sich von der D-Glucose durch das Fehlen der 5-ydroxymethylgruppe. exokinase bindet -D-Xylose; es wird die idente Konformationsänderung durchgeführt (induced fit), jedoch überwiegt die ATPase-Aktivität der exokinase. Ursache: In der fehlenden 5-ydroxymethylgruppen-Position ist Platz für ein Wassermolekül, das nun als Akzeptor der Phosphorylgruppe fungiert. D-Xylose Induced fit durch Xylose
53 Glucose xidativer Pentose- phosphat- Weg Glucose-6-Phosphat Fructose-6-Phosphat Glycolyse Glycogen- Biosynthese Pyruvat
54 Glycolyse 2. Reaktion: Glucosephosphat-Isomerase Glucose-6-Phosphat Fructose-6-Phosphat Enzym: Isomerase (E x) Glucosephosphat-Isomerase (Phosphoglucoisomerase) Dimer, 2 61 kda (Kaninchenmuskel) Glucose-6-Phosphat Fructose-6-Phosphat
55 Glucose-6-Phosphat Fructose-6-Phosphat Mechanismus: p-abhängigkeit: Ringöffnung, Isomerisierung, Ringschluß Glockenförmige p-abhängigkeit der Katalysegeschwindigkeit (Maximum um p 8). Beteiligung von Aminosäuren mit pk a = 6.7 und 9.3 (inweis auf istidinund Lysinrest im aktiven Zentrum)
56 Glucosephosphat-Isomerase B B R Aldose R cis-endiolat-zwischenprodukt B B R R Ketose
57 3 P 2 B + B
58 3 P 2 B + Ringöffnung B
59 3 P 2 B Base (istidin) spaltet das saure Proton vom (2) ab. B + - Austausch mit dem Medium cis-endiolat-intermediat
60 B 3 P 2 Proton wird an (1) gebunden B
61 B + Ringschluß + 3 P 2 Reaktion absolut stereospezifisch B
62 Nichtenzymatische, durch Basen katalysierte Isomerisierung von Glucose, Fructose und Mannose: Glucose cis-endiolat Mannose
63 Glucose Mannose 2 2 cis-endiolat- Intermediat Fructose
64 Glycolyse 3. Reaktion: Phosphofructokinase Fructose-6-Phosphat + ATP Fructose-1,6-bisphosphat + ADP + + Enzym: Phosphotransferase Phosphofructokinase (E ) Tetramer 4 78 kda (Kaninchenmuskel) Fructose-6-Phosphat Fructose-1,6-bisphosphat
65 Fructose-6-Phosphat Fructose-1,6-bisphosphat PFK, Mg 2+ Mechanismus: ATP ADP + + Wie bei der exokinase-reaktion. Nucleophiler Angriff der (1)- -Gruppe von Fructose-6-Phosphat am elektrophilen -Phosphoratom des Mg 2+ -ATP-Komplexes. Katalyse durch Annäherungseffekte. Substratinduzierte Konformationsänderung des Enzyms (induced fit).
66 - P P 2 P - PFK, Mg ADP ATP + Fructose-6-P Fructose-1,6-bisphosphat + ADP + + Gekoppelte Reaktion: Fructose-6-P + P i Fructose-1,6-bisphosphat G = 16,3 KJ/mol ydrolyse von ATP Gekoppelte Reaktion G = - 30,5 kj/mol G = - 14,2 kj/mol
67 Glycolyse 4. Reaktion: Aldolase Fructose-1,6-bisphosphat Glycerinaldehyd-3-P + Dihydroxyacetonphosphat Enzym: Lyase Aldolase (E ) Tetramer 4 40 kda (Kaninchenmuskel) Fructose-1,6-bisphosphat Dihydroxyacetonphosphat, Glycerinaldehyd-3-P
68 Fructose-1,6-bisphosphat Aldolase Glycerinaldehyd-3-Phosphat Dihydroxyacetonphosphat
69 R 2 R 1 R 1 R 4 Aldolase Aldolase (Tetramer) Aldolkondensation ist die Verknüpfung von zwei arbonylverbindungen (z.b. Aldehyd mit Keton) zu einem Aldol (= -ydroxycarbonylverbindung). R 2 R 1 R 1 R 4
70 2 P P 3 2- Fructose-1,6- bisphosphat-aldolase 2-2 P P 3 K eq = 0,0001; G = +23,9 kj/mol Erythrocyt: G = -0,23 kj/mol
71 R R' B B R' R R' R Resonanzstabilisiertes arbanion (Enolat) R R' R' R R' R B Keton 2. Keton (elektrophiles Zentrum)
72 Nach der Art des Reaktionsmechanismus werden 2 Klassen von Aldolasen unterschieden: Klasse-I-Aldolasen: Bildung einer Schiff schen Base zwischen einem Lysinrest im aktiven Zentrum und der arbonylgruppe des Substrates. Inhibierung durch NaB 4, aber nicht durch EDTA (kein divalentes Kation im aktiven Zentrum). Pflanzen, Tiere, Mensch. Klasse-II-Aldolasen: Metalloproteine: meist Zn 2+ im aktiven Zentrum. Durch EDTA inhibierbar. Nicht durch NaB 4 inhibierbar. Pilze, Bakterien
73 G3P FBP Klasse-II-Aldolasen: Pilze, Bakterien 2-2 P P 3 E Zn 2+ - Zn 2+ E Stabilisierung des Enolat-Zwischenproduktes durch die Lewis-Säure Zn 2+ unter gleichzeitiger Polarisierung der arbonylgruppe
74 Klasse-I-Aldolasen: Mensch Lysin 2 N 2 ( 2 ) 3 - S 2 ystein N N istidin
75 Klasse-I-Aldolasen: Mensch 2 P 3 2- Lysin 2 N 2 ( 2 ) 3 FBP Binden des Substrates Reaktion der FBP- arbonylgruppe mit der -Aminogruppe des Lys 2-2 P 3 N N istidin - S 2 ystein
76 Klasse-I-Aldolasen: Mensch 2 N P Bildung einer protonierten Schiff- Base Substrat kovalent gebunden 2-2 P 3 N N - S 2
77 Klasse-I-Aldolasen: Mensch Enamin- Intermediat Aldolspaltung, dann Protonierung 2 N N R P S 2 Glycerinaldehyd- 3-phosphat N
78 Klasse-I-Aldolasen: Mensch 2 P 3 2- N pror 2 2 pros Tautomerisierung S 2 Iminium-Kation (protonierte Schiff- Base): ydrolyselabil N N
79 Klasse-I-Aldolasen: Mensch Lysin 2 N 2 ( 2 ) 3 ydrolyse der Schiff-Base - S 2 ystein 2 Dihydroxyacetonphosphat N N istidin
80 Beweis des Reaktionsmechanismus: Inaktivierung des Enzyms durch NaB 4 nur in Gegenwart von F-1,6-BP. Transfer eines ydrid- Ions ( - ) zum Imin- Kohlenstoff unter Ausbildung des ydrolyse-stabilen sekundären Amins. Beweis durch radioaktive Markierung (*) und anschließender Protein-ydrolyse. P i 2 * N 2 P Enzym NaB 4 -Reduktion ydrolyse 2 - * N N N 6 - -Glyceryllysin
81 Aldolasereaktion ist hoch stereoselektiv: es entsteht aus DA und GAP nur ein Produkt (FBP) Nichtenzymatisch: 4 Produkte, abhängig davon, ob der pro-roder pro-s-wasserstoff am (3) des DAP abgespalten wird und das gebildete arbanion GAP auf der re- oder der si-seite angreift. D-Fructose-1,6- Bisphosphat 2 P P 3 2 P P 3 D-Tagatose -1,6-Bisphosphat D-Psicose-1,6- Bisphosphat 2 P P 3 2 P P 3 D-Sorbose-1,6- Bisphosphat
82 Glycolyse 5. Reaktion: Triosephosphat-Isomerase Dihydroxyacetonphosphat Glycerinaldehyd-3-P Enzym: Isomerase Triosephosphat-Isomerase (E.. E ) Dimer 2 27 kda (ühnermuskel) Dihydroxyacetonphosphat Glycerinaldehyd-3-P
83 (1), (2) und (3) der Glucose werden äquivalent zu (4), (5) und (6). DAP 2 P 3 2- Triosephosphat- Isomerase K eq = [GAP]/[DAP] = 4,73 x 10-2 Gleichgewicht: [DAP] >> [GAP] Jedoch wird GAP bei der anschließenden Reaktion der Glycolyse verbraucht, sodass trotzdem permanent Dihydroxyacetonphosphat (DAP) in GAP umgewandelt wird. 2-2 P 3 Glycerinaldehyd- 3-phosphat, GAP
84 PDB-ode 7tim Typische 3D- Struktur der Triose- Isomerase: TIM-barrel
85 PDB-ode 7tim Triosephosphat-Isomerase (TIM) ist ein perfektes Enzym: Die Geschwindigkeir der bimolekularen Assoziation des Enzyms mit dem Substrat ist diffusionskontrolliert! Aufgrund seiner Struktur ist TIM ein / -Barrel- Protein Viele Proteine (mit oft ganz anderen katalytischen Eigenschaften) haben diese Struktur: oft als TIM-Barrel bezeichnet: Acht parallele Faltblätter werden durch acht -elices verbunden. Das Faßinnere ist hydrophob, am Fassboden sitzen die für die jeweilige enzymatische Aktivität notwendigen Reste.
86 Substrate Triosephosphatisomerase aus efe (Dimer) -Faltblätter: gelb; -elices: orange Fassstruktur (TIM-barrel) aus 8 - Faltblätter/ -elices
87 Glu165 is95 Lys12 Substrat Konservierte Reste des aktiven Zentrums
88 Blick durch den Substratkanal hne Loops Mit Loops
89 Enzymkinetik der Triose-Isomerase: Glockenförmige p- Abhängigkeit mit pk a -Werten von 6,5 und 9,5. Was ist die Natur der sauren Gruppe (pk a = 6,5)? Markierung durch Affinitätsreagenzien (Bromhydroxyacetonphosphat oder Glycidolphosphat): Inaktivierung von TIM durch Ausbildung von Estern mit Glutaminsäure. Freie Glutaminsäure (wässriges Medium): pk a = 4,1 Aktives Zentrum (hydrophober Faßboden ): pk a = 6,5!! 2 P P Br Bromhydroxyacetonphosphat 2 Glycidolphosphat
90 Reaktionsmechanismus über Endiolat-Zwischenprodukt? Beweis durch Pseudosubstrate (meist Inhibitoren), die eine hohe Affinität zur Geometrie des Übergangszustandes haben. Phosphoglycohydroxamat bindet 155mal besser an TIM als GAP oder DAP) N P 3 Phosphoglycohydroxamat P 3 Postuliertes Endiolat- Zwischenprodukt der Isomerase-Reaktion
91 Reaktionsmechanismus Glu DAP - B Enzym 2 P 3 2- Glu B Enzym p-abhängigkeit: glockenförmige Kurve: pk a -Werte bei p 6,5 (Glu) und 9,5 (is) (vgl. Glucose-Phosphat- Isomerase) Glu - 2 P P 3 2- Endiol- Intermediat GAP
92 Pseudosubstrat PGP (2- Phosphoglycolat) P 3 2- Glu165: Abstraktion von + von (1) u. Donor für (2) is195: Säure: Protonierung von = von (2) Base: Abstraktion von + von an (1) des Endiolat- ZWP.
93 Induced fit nach Substratbindung: Deckel verschließt Fass Freies Enzym Enzym-Substratkomplex Kanal Deckel
94 Glycolyse 6. Reaktion: Glycerinaldehyd-3- phosphat-dehydrogenase Glycerinaldehyd-3-P + NAD + + P i 1,3-Bisphosphoglycerat + NAD + + Enzym: xidoreductase Glycerinaldehyd-3-phosphat-Dehydrogenase (E ) Tetramer 4 37 kda (Kaninchenmuskel) Glycerinaldehyd-3-P 1,3-Bisphosphoglycerat
BIOCHEMIE des Stoffwechsels ( )
 IEMIE des Stoffwechsels (772.113) 4. Einheit Glycolyse (1) Wie werden nun Moleküle in der lebenden Zelle synthetisiert und abgebaut? Wie funktioniert der Intermediärstoffwechsel? Der Intermediärstoffwechsel
IEMIE des Stoffwechsels (772.113) 4. Einheit Glycolyse (1) Wie werden nun Moleküle in der lebenden Zelle synthetisiert und abgebaut? Wie funktioniert der Intermediärstoffwechsel? Der Intermediärstoffwechsel
Grundzüge des Energiestoffwechsels I
 Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
9. Abbau der Glukose zum Pyruvat
 9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Pentosephosphat-Weg: alternativer Abbau von Glucose. Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet.
 Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Z11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
Die Wege des Kohlenstoffes
 Die Wege des Kohlenstoffes 1. Licht vs. Dunkelreaktionen Lichtgetriebene Reaktionen o Dunkle -Reaktionen laufen nicht im Dunklen ab reduzieren CO 2-Zucker für Pflanzen zum Wachsen und für uns zum Nutzen
Die Wege des Kohlenstoffes 1. Licht vs. Dunkelreaktionen Lichtgetriebene Reaktionen o Dunkle -Reaktionen laufen nicht im Dunklen ab reduzieren CO 2-Zucker für Pflanzen zum Wachsen und für uns zum Nutzen
Kohlenhydrate C n. O) n (H 2. z.b. C 6 O 6 O) 6 H 12 : C 6. Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Monosaccharide
 Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Inhaltsverzeichnis - Kapitel
 Inhaltsverzeichnis - Kapitel 1. Einleitung: Die Chemie des Lebens 2. Kohlenhydrate 3. Lipide und Membranen 4. Nukleinsäuren 5. Aminosäuren und Proteine 6. Enzyme und Katalyse 7. Vitamine & Kofaktoren 8.
Inhaltsverzeichnis - Kapitel 1. Einleitung: Die Chemie des Lebens 2. Kohlenhydrate 3. Lipide und Membranen 4. Nukleinsäuren 5. Aminosäuren und Proteine 6. Enzyme und Katalyse 7. Vitamine & Kofaktoren 8.
Z 11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
Grundlagen der Physiologie
 Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Asmaa Mebrad Caroline Mühlmann Gluconeogenese
 Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Schrittweise Oxidation und Decarboxylierung von Glucose-6-phosphat zu Ribulose-5- phosphat
 1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O O 2 6 CO H 2 O G kj
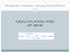 Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Hauptwege des Stoffwechsels
 Hauptwege des Stoffwechsels Auf- und Abbau der Stoffgruppen Kohlenhydrate 1 Enzyme Hauptklassen 1 2 3 4 5 6 Biochemie 08/2 Enzyme 1. Erhöhung der Reaktionsgeschwindigkeit ΔΔG kat = ΔG unkat - ΔG kat Erniedrigung
Hauptwege des Stoffwechsels Auf- und Abbau der Stoffgruppen Kohlenhydrate 1 Enzyme Hauptklassen 1 2 3 4 5 6 Biochemie 08/2 Enzyme 1. Erhöhung der Reaktionsgeschwindigkeit ΔΔG kat = ΔG unkat - ΔG kat Erniedrigung
BIOCHEMIE des Stoffwechsels ( )
 BIEMIE des Stoffwechsels (772.113) 5. Einheit Glycolyse (2) Glycolyse 6. Reaktion: Glycerinaldehyd-3- phosphat-dehydrogenase Glycerinaldehyd-3-P + NAD + + P i 1,3-Bisphosphoglycerat + NAD + + Enzym: xidoreductase
BIEMIE des Stoffwechsels (772.113) 5. Einheit Glycolyse (2) Glycolyse 6. Reaktion: Glycerinaldehyd-3- phosphat-dehydrogenase Glycerinaldehyd-3-P + NAD + + P i 1,3-Bisphosphoglycerat + NAD + + Enzym: xidoreductase
KOHLENHYDRATE PYRUVAT-DEHYDROGENASE
 PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Citratzyklus. Citratzyklus
 Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Mucosazelle. Mucosazelle
 Saccharase, Lactase Mucosazelle Mucosazelle Na-abhängiger Na-abhängiger Glucosetransporter (SGLT; (SGLT; aktiv): aktiv): nur nur in in Mucosazellen Mucosazellen (luminal) (luminal) und und Zellen Zellen
Saccharase, Lactase Mucosazelle Mucosazelle Na-abhängiger Na-abhängiger Glucosetransporter (SGLT; (SGLT; aktiv): aktiv): nur nur in in Mucosazellen Mucosazellen (luminal) (luminal) und und Zellen Zellen
Die Glycolyse (Glucose Katabolismus)
 Die Glycolyse (Glucose Katabolismus) 1. Übersicht über die Glykolyse 2. Reaktionschritte der Glykolyse 3. Gärung: Der anaerobe Weg des Pyruvats 4. Kontrolle der Glykolyse 5. Stoffwechsel von anderen Hexosen
Die Glycolyse (Glucose Katabolismus) 1. Übersicht über die Glykolyse 2. Reaktionschritte der Glykolyse 3. Gärung: Der anaerobe Weg des Pyruvats 4. Kontrolle der Glykolyse 5. Stoffwechsel von anderen Hexosen
Biochemie II. im Wintersemester 2009/2010. Joachim Wegener. Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg
 Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt.
 Übung und Lösung zur Übung Aminosäuren 1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt. 2. Das Tripeptid Glutathion ( -Glu-Cys-Gly)
Übung und Lösung zur Übung Aminosäuren 1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt. 2. Das Tripeptid Glutathion ( -Glu-Cys-Gly)
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Präsentation STOFFWECHSEL STOFFWECHSEL. Fettstoffwechsel im Sport. Biologische Oxidation Zitratzyklus und Atmungskette
 STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
Inhaltsverzeichnis. I Stoffwechsel. 1 Vom Organismus zum Molekül Aminosäuren Peptide und Proteine Enzyme...
 XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
Stoffwechsel. Metabolismus (3)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
KOHLENHYDRATE. Die Glykolyse
 Die Glykolyse Hexokinase Glucose Kostet 1ATP Mg 2+ Glucose-6-P Die Glucokinase kann durch Insulin induziert werden in : 1) Den Fettzellen 2) Den ß-Zellen des Pankreas 3) Der Nierenrinde 4) Der Leber Die
Die Glykolyse Hexokinase Glucose Kostet 1ATP Mg 2+ Glucose-6-P Die Glucokinase kann durch Insulin induziert werden in : 1) Den Fettzellen 2) Den ß-Zellen des Pankreas 3) Der Nierenrinde 4) Der Leber Die
Was bisher geschah 1
 Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Der Stoffwechsel: Konzepte und Grundmuster
 Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
1 Vom Organismus zum Molekül... 3
 I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
BIOCHEMIE DER ERNÄHRUNG II Oxidation von Lipiden. Gastrointestinaltrakt. Fettsäureoxidation zu Acetyl-CoA
 xidation von Lipiden ß-xidation: Fettsäureoxidation zu Acetyl-oA BIEMIE DER ERNÄRUNG II 07.05.2012 wichtigste Fettsäurequelle in Nahrung: Triacylglyceride Import freier Fettsäuren ins ytosol oder Erzeugung
xidation von Lipiden ß-xidation: Fettsäureoxidation zu Acetyl-oA BIEMIE DER ERNÄRUNG II 07.05.2012 wichtigste Fettsäurequelle in Nahrung: Triacylglyceride Import freier Fettsäuren ins ytosol oder Erzeugung
BIOCHEMIE des Stoffwechsels. (3 Std., )
 BIEMIE des Stoffwechsels (3 Std., 772.113) 1. Einheit Reaktionsmechanismen Stryer Biochemie J. M. Berg, J. L. Tymoczko, L. Stryer 6. Auflage (2007) Spektrum der Wissenschaft, ELSEVIER Die Lebewesen der
BIEMIE des Stoffwechsels (3 Std., 772.113) 1. Einheit Reaktionsmechanismen Stryer Biochemie J. M. Berg, J. L. Tymoczko, L. Stryer 6. Auflage (2007) Spektrum der Wissenschaft, ELSEVIER Die Lebewesen der
Oxidative Phosphorylierung
 BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!!
 Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Kontrolle der Genexpression auf mrna-ebene. Abb. aus Stryer (5th Ed.)
 Kontrolle der Genexpression auf mrna-ebene Abb. aus Stryer (5th Ed.) RNA interference (RNAi) sirna (small interfering RNA) mirna (micro RNA) Abb. aus Stryer (5th Ed.) Transcriptional silencing Inhibition
Kontrolle der Genexpression auf mrna-ebene Abb. aus Stryer (5th Ed.) RNA interference (RNAi) sirna (small interfering RNA) mirna (micro RNA) Abb. aus Stryer (5th Ed.) Transcriptional silencing Inhibition
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Zellulärer Abbau von Proteinen in Aminosäuren:! Proteine werden in Zellen durch Proteasom-Komplexe in! einzelne Aminosäuren abgebaut.!
 Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Klausur zur Vorlesung Biochemie I im WS 1993/1994. am 18. Februar Nachklausur zur Vorlesung Biochemie I im WS 1993/1994. am 30. Mai 1994.
 Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Einführung in die Biochemie Glykolyse
 Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Pentosephosphatzyklus. Synonym: Hexosemonophosphatweg
 Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Der Stoffwechsel. Wir zeigen dir wie er funktioniert.
 Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Praktikumsreferat Biochemie
 Praktikumsreferat Biochemie Thema: Glycolyse und Gluconeogenese 1. Glycolyse im Überblick Die Glycolyse (gr.: glykys = süß, lysis = auflösen) beschreibt den Abbau von Glucose zu Pyruvat (aerobe Glycolyse
Praktikumsreferat Biochemie Thema: Glycolyse und Gluconeogenese 1. Glycolyse im Überblick Die Glycolyse (gr.: glykys = süß, lysis = auflösen) beschreibt den Abbau von Glucose zu Pyruvat (aerobe Glycolyse
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8,
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8,
Tyrosinkinase- Rezeptoren
 Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
Basiswissen Ernährungslehre
 Basiswissen Ernährungslehre Hauptnährstoffgruppen und bioaktive Substanzen Ergänze folgende Übersicht zu den natürlichen Bestandteilen der Nahrung Natürliche Bestandteile der Nahrung Nährstoffe Funktionsgruppen
Basiswissen Ernährungslehre Hauptnährstoffgruppen und bioaktive Substanzen Ergänze folgende Übersicht zu den natürlichen Bestandteilen der Nahrung Natürliche Bestandteile der Nahrung Nährstoffe Funktionsgruppen
Bioenergetik. Technische Universität Ilmenau, FG Nanotechnologie. Zentrum für Mikro- und Nanotechnologien
 Bioenergetik Quellen: 1. Physiologie des Menschen (mit Pathophysiologie) R.F. Schmidt, F. Lang, G. Thews, 29. Auflage Springer Medizin Verlag Heidelberg (2005), ISBN 3-540-21882-3. 2. www.cg.bnv bamberg.de/t3/fileadmin/images/fachbereiche/biologie/dateien/kh-abbau.ppt
Bioenergetik Quellen: 1. Physiologie des Menschen (mit Pathophysiologie) R.F. Schmidt, F. Lang, G. Thews, 29. Auflage Springer Medizin Verlag Heidelberg (2005), ISBN 3-540-21882-3. 2. www.cg.bnv bamberg.de/t3/fileadmin/images/fachbereiche/biologie/dateien/kh-abbau.ppt
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Kohlenhydrate Aminosäuren Peptide
 Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik
 Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
ENZYME. Teil 1: Grundlagen und Substratbestimmungen
 ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
1. Die Bildung von Methan durch Mikroorganismen erfolgt (2 Punkte)
 Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
2. Klausur. 1. Aufgabe
 1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Bei der abschließenden
1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Bei der abschließenden
Klausur zur Vorlesung Biochemie I im WS 2004/05
 Klausur zur Vorlesung Biochemie I im W 2004/05 am 9.03.2005 von 0.00 -.30 Uhr Gebäude 42, örsaal 5 Lösungen in rot Punkte in grün Aufgabe : Formulieren ie die repetitiven chritte in der -xidation von Fettsäuren
Klausur zur Vorlesung Biochemie I im W 2004/05 am 9.03.2005 von 0.00 -.30 Uhr Gebäude 42, örsaal 5 Lösungen in rot Punkte in grün Aufgabe : Formulieren ie die repetitiven chritte in der -xidation von Fettsäuren
I. Zellatmung. =Abbau von Kohlenhydraten unter Sauerstoffverbrauch (aerob) KH + O 2 --> CO 2 + H 2 O + Energie
 KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat
 Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Klausur zur Vorlesung Biochemie I im WS 2002/03 Lösungen
 Klausur zur Vorlesung Biochemie I im W 00/03 Lösungen am 17.0.003 von 14.15 15.45 Uhr Gebäude 4, aum 115 (insgesamt 100 Punkte, mindestens 40 erforderlich) Bitte amen (in Druckbuchstaben), Matrikelnummer
Klausur zur Vorlesung Biochemie I im W 00/03 Lösungen am 17.0.003 von 14.15 15.45 Uhr Gebäude 4, aum 115 (insgesamt 100 Punkte, mindestens 40 erforderlich) Bitte amen (in Druckbuchstaben), Matrikelnummer
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Wichtig für die Resorption von Glucose. Wird im Abschnitt Verdauung/ Resorption besprochen.
 6. Stoffwechsel der Kohlenhydrate: 6.1. Glycolyse: Glucose 2 * Pyruvat Glucose+ 2 NAD + + 2 P i + 2 ADP 2* (Pyruvat + NADH + H + +ATP +H 2 O ) Glycos: süß, lysis: Spaltung Ubiquitärer Stoffwechselweg:
6. Stoffwechsel der Kohlenhydrate: 6.1. Glycolyse: Glucose 2 * Pyruvat Glucose+ 2 NAD + + 2 P i + 2 ADP 2* (Pyruvat + NADH + H + +ATP +H 2 O ) Glycos: süß, lysis: Spaltung Ubiquitärer Stoffwechselweg:
Energiegewinnung aus Nahrungsbestandteilen
 Energiegewinnung aus Nahrungsbestandteilen Fett Kohlenhydrate PROTEIN Fettsäuren und Glycerol Glucose und andere Zucker Acetyl CoA Aminosäuren Stadium I Stadium II ATP ADP CoA O 2 Oxidative Phosphorylierung
Energiegewinnung aus Nahrungsbestandteilen Fett Kohlenhydrate PROTEIN Fettsäuren und Glycerol Glucose und andere Zucker Acetyl CoA Aminosäuren Stadium I Stadium II ATP ADP CoA O 2 Oxidative Phosphorylierung
Zellen verwandeln Zucker in Energie
 Zellen verwandeln Zucker in Energie Kohlenhydrate sind äusserst wichtige Brennstofflieferanten. Pflanzen können Zucker selber herstellen (vgl. autotrophe Organismen); Tiere hingegen müssen Zucker (und
Zellen verwandeln Zucker in Energie Kohlenhydrate sind äusserst wichtige Brennstofflieferanten. Pflanzen können Zucker selber herstellen (vgl. autotrophe Organismen); Tiere hingegen müssen Zucker (und
Versuchsprotokoll: Leitenzyme
 Versuchsprotokoll: Leitenzyme Aufschluss von Lebergewebe / Fraktionierte Zentrifugation / Aufschluss von Mitochondrien / Nachweis von Leitenzymen im Cytosol und 1.1. Einleitung Für die Trennung der Organellen
Versuchsprotokoll: Leitenzyme Aufschluss von Lebergewebe / Fraktionierte Zentrifugation / Aufschluss von Mitochondrien / Nachweis von Leitenzymen im Cytosol und 1.1. Einleitung Für die Trennung der Organellen
Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten.
 Glukose hilft uns, auch bei intensiven Belastungen zu überleben. Wieso? Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten. In diesem Artikel geht es nicht nur um den Abbau
Glukose hilft uns, auch bei intensiven Belastungen zu überleben. Wieso? Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten. In diesem Artikel geht es nicht nur um den Abbau
1 Biomoleküle. und ihre Wechselwirkungen. 1.1 Die Entstehung des Lebens. Die Entstehung des Lebens
 1 Biomoleküle und ihre Wechselwirkungen Das Leben ist im Wasser entstanden, und Wasser ist der quantitativ wichtigste Bestandteil aller Lebewesen. Wasser ist das Lösungsmittel, in welchem die chemischen
1 Biomoleküle und ihre Wechselwirkungen Das Leben ist im Wasser entstanden, und Wasser ist der quantitativ wichtigste Bestandteil aller Lebewesen. Wasser ist das Lösungsmittel, in welchem die chemischen
Praktikum Biochemie B.Sc. Water Science WS Enzymregulation. Marinja Niggemann, Denise Schäfer
 Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Primärstoffwechsel. Prof. Dr. Albert Duschl
 Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Kapitel 5: 1. Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D.
 Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Pentosephosphat. hosphatweg
 Pentosephosphat hosphatweg Wie aus dem Namen abzuleiten ist, werden C5-Zucker, einschließlich Ribose, aus Glucose synthetisiert. Das oxidierende Agens ist hierbei NADP + ; es wird zu NADP reduziert, das
Pentosephosphat hosphatweg Wie aus dem Namen abzuleiten ist, werden C5-Zucker, einschließlich Ribose, aus Glucose synthetisiert. Das oxidierende Agens ist hierbei NADP + ; es wird zu NADP reduziert, das
Glycolyse und Gluconeogenese
 Glycolyse und Gluconeogenese Arbeiten, deren Beginn sich auf die Zeit um 1905 datieren lässt, führten dazu, dass in den 1940er Jahren alle Schritte der Glycolyse bekannt waren. Durchsicht der aktuellen
Glycolyse und Gluconeogenese Arbeiten, deren Beginn sich auf die Zeit um 1905 datieren lässt, führten dazu, dass in den 1940er Jahren alle Schritte der Glycolyse bekannt waren. Durchsicht der aktuellen
Angelika Stöcklinger. Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate
 Angelika Stöcklinger Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate Kohlenhydrate und das Immunsystem z.b. Mannosen Bindungspartner für Lektine Mannose Aufnahme von Pathogenen Dendritische Zelle
Angelika Stöcklinger Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate Kohlenhydrate und das Immunsystem z.b. Mannosen Bindungspartner für Lektine Mannose Aufnahme von Pathogenen Dendritische Zelle
Stoffwechsel. Die Chemie des Lebens ist in Stoffwechselwegen organisiert
 Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
STOFFTRANSPORT DURCH BIOMEM- BRANEN
 DIE BIOMEMBRAN Vorkommen Plasmalemma Grenzt Cytoplasma nach außen ab Tonoplast Grenzt Vakuole vom Cytoplasma ab Zellkernmembran Mitochondrienmembran Plastidenmembran ER Kompartimente Durch Zellmembran
DIE BIOMEMBRAN Vorkommen Plasmalemma Grenzt Cytoplasma nach außen ab Tonoplast Grenzt Vakuole vom Cytoplasma ab Zellkernmembran Mitochondrienmembran Plastidenmembran ER Kompartimente Durch Zellmembran
Glucose-Aufnahme und Stoffwechsel
 Glucose-Aufnahme und Stoffwechsel Biochemie Inhalt Transportvorgänge Glucoseaufnahme Blutglucose, Glucosetransporter und Insulin Diabetes mellitus Glucosestoffwechsel 1 Transportvorgänge Passive Transportvorgänge:
Glucose-Aufnahme und Stoffwechsel Biochemie Inhalt Transportvorgänge Glucoseaufnahme Blutglucose, Glucosetransporter und Insulin Diabetes mellitus Glucosestoffwechsel 1 Transportvorgänge Passive Transportvorgänge:
Organische Chemie für Mediziner WS 2016/2017. Übungsblatt 3: Ausgewählte Substanzklassen
 1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
Funktion von Proteinen:
 Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Versuch 6. Leitenzyme
 Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann [email protected] X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann [email protected] X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, [email protected] Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, [email protected] Dr. Martin Kahms
Grundlagen der Physiologie
 Grundlagen der Physiologie Bioenergetik www.icbm.de/pmbio Energieformen Von Lebewesen verwertete Energieformen o Energie ist etwas, das Arbeit ermöglicht. o Lebewesen nutzen nur zwei Formen: -- Licht --
Grundlagen der Physiologie Bioenergetik www.icbm.de/pmbio Energieformen Von Lebewesen verwertete Energieformen o Energie ist etwas, das Arbeit ermöglicht. o Lebewesen nutzen nur zwei Formen: -- Licht --
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Mechanismen der ATP Synthese in Mitochondrien
 Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Die Zelle. Membranen: Struktur und Funktion
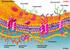 Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Membranen. U. Albrecht
 Membranen Struktur einer Plasmamembran Moleküle gegeneinander beweglich -> flüssiger Charakter Fluidität abhängig von 1) Lipidzusammensetzung (gesättigt/ungesättigt) 2) Umgebungstemperatur Biologische
Membranen Struktur einer Plasmamembran Moleküle gegeneinander beweglich -> flüssiger Charakter Fluidität abhängig von 1) Lipidzusammensetzung (gesättigt/ungesättigt) 2) Umgebungstemperatur Biologische
